Comment déterminer la concentration en ions chlorure dans des solutions de traitement du fer avec des bandelettes réactives Quantab – Notes de l’Institut canadien de conservation (ICC) 4/4
- Introduction
- Procédure : comment utiliser les bandelettes réactives Quantab
- Aspects scientifiques des bandelettes réactives Quantab
- Remerciements
- Fournisseurs
- Références
Introduction
Lorsqu’un objet en fer rouille, il se recouvre d’oxydes de fer qui le protègent partiellement. Cette couche de protection est toutefois altérée par les ions chlorure, ce qui accélère fortement la corrosion. Les ions chlorure posent un grave problème pour les objets archéologiques en fer, en particulier ceux qui ont été récupérés en milieu marin, et ils doivent être éliminés pour assurer la préservation de ces objets. La procédure généralement utilisée pour éliminer les ions chlorure consiste à faire tremper l’objet dans un bain alcalin. Un test simple de dépistage des ions chlorure doit alors être effectué pour vérifier si la solution du bain alcalin doit être changée ou si le traitement est terminé.
Un test au nitrate d’argent, décrit dans la Note de l’ICC 4/5 Comment déterminer la concentration en ions chlorure dans des solutions de traitement du fer à l’aide de nitrate d’argent, peut révéler la présence d’ions chlorure dans la solution de traitement et fournir une indication approximative de la concentration en ions chlorure sur une plage limitée. Les bandelettes réactives Quantab pour le chlorure permettent d’effectuer une mesure plus précise de la concentration sur une plage plus étendue. Ces bandelettes réactives comportent une étroite colonne imprégnée de dichromate d’argent. Lorsque la bandelette est trempée dans la solution, le liquide pénètre par un petit orifice, dans le bas de la colonne, et remonte dans celle-ci par capillarité. Les ions chlorure réagissent avec le dichromate d’argent en produisant une zone blanche de chlorure d’argent dans la colonne. La hauteur de la zone blanche peut alors être convertie en concentration d’ions chlorure à l’aide de l’information d’étalonnage fournie avec les bandelettes. Les bandelettes sont offertes en deux plages de concentrations : 30 à 600 mg/L (30 à 600 parties par million [ppm]) et 300 à 6 000 mg/L (300 à 6 000 ppm). Pour en apprendre davantage sur cette réaction, consulter la section Aspects scientifiques des bandelettes réactives Quantab.La présente Note de l’ICC décrit la procédure à suivre pour vérifier la concentration en ions chlorure dans des solutions de traitement à l’aide des bandelettes réactives Quantab pour le chlorure. La première étape consiste à faire un essai avec des solutions dont la concentration en ions chlorure est connue pour apprendre à utiliser les bandelettes réactives et confirmer que celles-ci fonctionnement correctement. Le test peut ensuite être effectué avec les solutions de traitement visées ou d’autres solutions dont la concentration d’ions chlorure est inconnue. Il n’est pas nécessaire d’effectuer ces essais dans un laboratoire équipé d’un système de ventilation, sauf si de l’acide nitrique doit être utilisé pour ajuster l’acidité de la solution. Le cas échéant, consulter la fiche signalétique de sécurité (FSS) de l’acide nitrique avant de l’utiliser afin de connaître l’information de santé et sécurité qui s’y rapporte.
Procédure : comment utiliser les bandelettes réactives Quantab
Équipement et matériel requis pour effectuer un test avec les bandelettes Quantab
- Solutions ayant des concentrations en ions chlorure connues et inconnues
- Les solutions dont la concentration en ions chlorure est connue doivent être achetées ou préparées avec des concentrations qui se situent dans la plage des bandelettes Quantab, soit 30 à 600 ppm pour la plage inférieure et 300 à 6 000 ppm pour la plage supérieure. La procédure utilisée pour préparer des solutions d’ions chlorure à 30 ppm, à 300 ppm et à 3 000 ppm est décrite dans la Note de l’ICC 4/5 Comment déterminer la concentration en ions chlorure dans des solutions de traitement du fer à l’aide de nitrate d’argent.
- Les solutions dont la concentration en ions chlorure est inconnue peuvent être, notamment, une solution de dessalement ou toute autre solution devant être testée.
- Éprouvettes en verre (par exemple, une éprouvette d’un diamètre extérieur de 16 mm et d’une longueur de 125 mm contient environ 20 mL)
- Support pour éprouvettes
- Bandelettes réactives Quantab pour le chlorure, plage inférieure ou supérieure (consulter la section Fournisseurs pour savoir comment se procurer ces bandelettes)
- Pincettes (pour sortir les bandelettes réactives Quantab de leur bouteille
- Pipettes (Pasteur ou en plastique) ou compte-gouttes
- Cylindre gradué (10 mL)
- Fiole jaugée (100 mL)
- Solution d’acide nitrique (HNO3) dilué, par exemple 5 % (v/v) (facultatif); la procédure pour préparer la solution est décrite à la section Préparer la solution
- Bouteille d’entreposage en verre (125 mL) pour la solution d’acide nitrique (facultatif)
- Papiers indicateurs de pH (facultatif)
- Papier filtre (facultatif)
- Entonnoir (facultatif)
Procédure pour effectuer un test avec les bandelettes Quantab
Toujours utiliser l’acide nitrique avec prudence et, au moment de le manipuler, porter un équipement de protection individuelle tel que des gants, des lunettes de sécurité et des vêtements de protection. Travailler dans un endroit équipé d’un système de ventilation, surtout si de l’acide nitrique concentré est utilisé. Pour obtenir des renseignements supplémentaires sur la préparation de solutions chimiques, consulter Odegaard et al. (2005) et Skoog et al. (2014)
Préparer la solution
Au besoin, préparer une solution d’acide nitrique à 5 % (v/v).
- Travailler sous une hotte.
- Remplir partiellement une fiole jaugée de 100 mL avec de l’eau distillée.
- Mesurer 5 mL d’acide nitrique concentré (à 68-70 % de HNO3 en poids) dans un cylindre gradué de 10 mL.
- Transférer l’acide nitrique dans la fiole jaugée (important : toujours ajouter l’acide concentré à l’eau, et non l’inverse).
- Mélanger en tournant.
- Ajouter de l’eau distillée dans la fiole jaugée jusqu’à la marque de 100 mL.
- Transvider dans une bouteille d’entreposage en verre et étiqueter la bouteille.
- La solution obtenue contient environ 0,8 M HNO3.
Tester les solutions à l’aide des bandelettes Quantab
- Si une solution contient des particules en suspension, filtrer d’abord la solution à l’aide d’un entonnoir et d’un papier filtre pour empêcher que des particules bloquent l’ouverture à la base de la bandelette.
- Dans un cylindre gradué de 10 mL, mettre, à l’aide d’une pipette ou d’un compte-gouttes, 2 mL d’une solution dont la concentration en ions chlorure est connue.
- Transférer la solution du cylindre gradué dans une éprouvette propre.
- Insérer une bandelette Quantab dans l’éprouvette et laisser tremper le bas de la bandelette dans le liquide.
- Laisser le liquide s’infiltrer dans la colonne jusqu’à ce que la bande horizontale au haut de la bandelette passe du jaune au noir; cela indique que le test est terminé.
- Noter l’heure à laquelle la bande horizontale devient noire.
- Attendre au moins 2 minutes (mais pas plus de 30 minutes), puis retirer la bandelette Quantab de l’éprouvette.
- Repérer le point le plus haut de la zone blanche, là où la colonne devient entièrement brune, et noter sa position sur l’échelle numérotée de la bandelette Quantab en arrondissant à l’échelon le plus près (intervalles de 0,2 unité).
- Consulter le tableau de conversion fourni sur le contenant des bandelettes Quantab. Convertir le résultat obtenu sur l’échelle de la bandelette Quantab en concentration d’ions chlorure (en parties par million). Comme les tableaux de conversion varient d’un lot à l’autre, il faut s’assurer d’utiliser le bon contenant au moment de convertir une mesure.
- Répéter les étapes 1 à 9 avec les autres solutions dont la concentration en ions chlorure est connue ou inconnue.
- Dans le cas des solutions dont la concentration en ions chlorure est inconnue, vérifier le pH avec un papier indicateur en utilisant un échantillon de solution distinct. Si le pH est supérieur à 10, la solution doit être neutralisée avec de l’acide nitrique 5 % (v/v), de la façon décrite dans la section Modification des solutions fortement alcalines.
- Si la bandelette Quantab doit être conservée pour référence ultérieure, éliminer l’excès de liquide en pressant la bandelette entre les doigts sur toute sa longueur de façon à en extraire le plus de liquide possible, puis la laisser sécher. Les bandelettes Quantab ne sont pas réutilisables.
Résultats du test
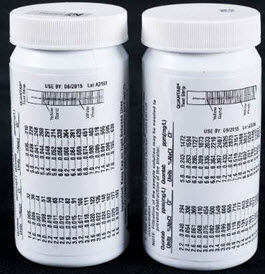
Les deux types de bandelettes Quantab pour le chlorure fabriquées par Hach sont présentés à la figure 1. Les bandelettes Quantab sont vendues pré-étalonnées, et un tableau de conversion est fourni sur leur contenant (figure 2).

©Gouvernement du Canada, Institut canadien de conservation. ICC 120260‐0376
Figure 1 : Les bandelettes réactives Quantab pour le chlorure, fabriquées par Hach, sont offertes dans deux plages. La bouteille et la bandelette de gauche sont un exemple de la plage inférieure et celles de droite sont un exemple de la plage supérieure.
© Gouvernement du Canada, Institut canadien de conservation. ICC 120260-0377
Figure 2 : Tableaux de conversion Quantab figurant au dos des bouteilles. L’échelle est unique à chaque lot de bandelettes.
La figure 3 montre un exemple de bandelette Quantab de la plage supérieure dans une éprouvette contenant 2 mL de solution, au début du test.

© Gouvernement du Canada, Institut canadien de conservation. ICC 120260-0378
Figure 3 : Bande Quantab de la plage supérieure dans une éprouvette contenant 2 mL de solution, au début du test.
Lorsque la colonne est saturée, la bande horizontale hydrosensible située dans le haut de la bandelette vire du jaune au noir, ce qui signifie que le test est terminé (figures 4a et 4b).

©Gouvernement du Canada, Institut canadien de conservation. ICC 120260-0381
Figure 4a : Détail d’une bandelette Quantab avant son exposition à une solution d’essai. La bande horizontale conçue pour indiquer la fin du test est jaune.

©Gouvernement du Canada, Institut canadien de conservation. ICC 120260-0383
Figure 4b : Détail d’une bandelette Quantab après un test de détection des ions chlorure. La bande horizontale conçue pour indiquer la fin du test est maintenant noire.
Une fois le test terminé, la concentration en ions chlorure peut être déterminée en notant la position de la pointe de la zone blanche, comme le montrent la figure 5 (plage inférieure) et la figure 6 (plage supérieure). Cette mesure est utilisée pour déterminer la concentration en ions chlorure d’après le tableau d’étalonnage fourni au dos de la bouteille. Bien que la valeur mesurée dans la solution de 15 ppm, montrée à la figure 5, se situe en deçà de la plage supérieure du tableau, la bandelette indique que des ions chlorure sont présents dans la solution.

©Gouvernement du Canada, Institut canadien de conservation. ICC 120260-0384
Figure 5 : Trois exemples de bandelettes Quantab de la plage inférieure dans des solutions contenant respectivement (de gauche à droite) 15 ppm, 35,5 ppm et 100 ppm d’ions chlorure.

©Gouvernement du Canada, Institut canadien de conservation. ICC 120260-0384
Figure 6 : Deux exemples de bandelettes Quantab de la plage supérieure dans des solutions contenant respectivement (de gauche à droite) 1 000 ppm et 3 545 ppm d’ions chlorure.
Renseignements supplémentaires
Exactitude des bandelettes réactives Quantab
Le fabricant teste chaque lot de bandelettes Quantab et garantit une exactitude de ± 10 % pour la concentration en ions chlorure (Hach, 2014).Cela signifie que, si la concentration mesurée est de 200 ppm d’ions chlorure, la concentration réelle peut varier de 180 à 220 ppm.
Interférences
Il pourrait être nécessaire de filtrer l’échantillon s’il contient des solides en suspension. Les solides en suspension peuvent obstruer l’ouverture qui se trouve à la base de la bandelette. Si cela se produit, la bande horizontale qui indique la fin du test, au haut de la colonne, ne deviendra jamais noire. Il est préférable d’utiliser des papiers filtres sans cendre, car ils ne contiennent que des traces d’ions chlorure. Il ne faut jamais utiliser du papier filtre qui contient des ions chlorure provenant d’un procédé de blanchissage. Pour vérifier si le papier filtre contient des ions chlorure, découper un morceau du papier et le placer dans une éprouvette avec une petite quantité d’eau, puis effectuer un test à l’aide des bandelettes réactives Quantab pour le chlorure.
Les autres ions qui peuvent interférer avec ce test et fausser les résultats sont ceux qui forment aussi un précipité avec le nitrate d’argent, par exemple les iodures et les bromures. Les ions nitrite et nitrate n’ont aucun effet sur le test. Il est possible que la réaction entre le dichromate d’argent et les ions chlorure ne fonctionne pas avec les acides forts et les bases fortes (Hach, 2014).
Le mode d’emploi qui figure sur le contenant de bandelettes Quantab indique de ne jamais plonger la bandelette dans le liquide au point où la bande jaune qui noircit à l’achèvement du test se retrouve immergée. Toutefois, puisque les directives de la présente procédure prescrivent d’effectuer le test dans une éprouvette contenant 2 mL de liquide, ce problème ne se pose pas.
Entreposage des bandelettes réactives Quantab
Les bandelettes Quantab doivent être conservées dans leur contenant d’origine. Le couvercle doit être fermé hermétiquement afin de les protéger contre la lumière et l’humidité. Chaque bouteille contient une petite quantité d’agent desséchant pour garder les bandelettes sèches. Les bouteilles doivent être entreposées à une température inférieure à 30 °C. Les bandelettes Quantab doivent être utilisées avant la date de péremption indiquée sur leur contenant. Celles dont la date de péremption est dépassée peuvent réagir plus lentement et produire des couleurs moins contrastées.
Modification des solutions fortement alcalines
Le fabricant (Hach) indique que les bandelettes réactives Quantab pour le chlorure ne doivent pas être utilisées dans une solution dont le pH est supérieur à 10. À pH élevé, l’hydroxyde d’argent et l’oxyde d’argent peuvent précipiter et éliminer les ions argent qui autrement précipiteraient sous forme de chlorure d’argent. Le pH d’une solution de traitement alcaline type composée d’hydroxyde de sodium à 1 % (p/v) (0,25 M) est d’environ 13,4. Les échantillons de solution de traitement doivent donc être neutralisés pour atteindre un pH inférieur à 10 avant d’être soumis à un essai avec les bandelettes. Les consignes qui suivent expliquent la façon de procéder.
Utiliser un échantillon de 2 mL de solution de traitement. Vérifier le pH à l’aide d’un papier indicateur. Ajouter de l’acide nitrique à 5 % (v/v) jusqu’à ce que le pH soit presque à 7. Il faut environ 0,4 mL d’acide nitrique à 5 % (v/v) pour neutraliser 2 mL d’hydroxyde de sodium à 1 % (p/v).
Si l’on ajoute un volume d’acide nitrique (par exemple, -0,4 mL) au volume initial (par exemple, -2 mL), la concentration en ions chlorure de l’échantillon de base se calcule à partir de la concentration de l’échantillon dilué à l’aide de la formule suivante :
cinitiale = cmesurée × (vintial + vajouté) / vinitial
où cinitiale est la concentration en ions chlorure de l’échantillon initial, cmesurée la concentration en ions chlorure de l’échantillon dilué, vinitial le volume initial de l’échantillon et vajouté le volume d’acide nitrique ajouté.
Avec la quantité estimative d’acide nitrique indiquée ci-dessus, soit 0,4 mL, alors
(vintial + vajouté) / vinitial
devient
(2 + 0,4)/2 = 1,2
donc
cinitiale = 1,2 cmesurée
Pour obtenir une valeur plus juste de la concentration initiale en ions chlorure, prendre en note le volume d’acide nitrique ajouté ou mesurer le volume final de la solution neutralisée.
Autres méthodes de mesure des ions chlorure
Il existe d’autres façons de mesurer la concentration en ions chlorure dans une solution aqueuse. L’une d’elles, simple mais moins précise, consiste à effectuer un test avec du nitrate d’argent, de la façon décrite dans la Note de l’ICC 4/5 Comment déterminer la concentration en ions chlorure dans les solutions de traitement du fer à l’aide de nitrate d’argent. Cette Note de l’ICC contient également des renseignements supplémentaires au sujet des sels présents dans les objets, notamment leurs sources et les dommages qu’ils peuvent causer, et de la surveillance du dessalement par la conductivité. Une analyse semi-quantitative peut être effectuée à l’aide des bandelettes réactives EM Quant pour les chlorures (Odegaard et al., 2011). Une autre méthode plus précise consiste à effectuer un titrage avec du nitrate d’argent (Selwyn, 2001). D’autres méthodes sont mentionnées et examinées par Wang et al. (2008) et Rimmer et al. (2012).
Aspects scientifiques des bandelettes réactives Quantab
La réaction entre les bandelettes réactives Quantab et les ions chlorure
Les bandelettes réactives Quantab pour le chlorure sont composées d’une mince languette en plastique sur laquelle est apposée une colonne capillaire imprégnée de dichromate d’argent de couleur brune (Ag2Cr2O7) (Hach, 2014). Lorsque la partie inférieure de la bandelette réactive Quantab est placée dans une solution aqueuse, le liquide pénètre par un petit orifice situé au bas de la bandelette et monte dans la colonne par capillarité.
Le dichromate d’argent est légèrement soluble dans l’eau, alors que le chlorure d’argent (AgCl) est insoluble dans l’eau. Les ions chlorure (Cl-) présents dans la solution réagissent avec les ions argent (Ag+) du dichromate d’argent, ce qui produit un précipité de chlorure d’argent. À mesure que les ions argent sont éliminés de la solution, le dichromate d’argent se dissout pour les remplacer, jusqu’à ce que tout le dichromate d’argent ait été dissous et que tous les ions argent aient été précipités sous forme de chlorure d’argent. La couleur de la colonne passe du brun au blanc là où le chlorure d’argent est précipité. La réaction globale, c’est-à-dire la substitution des ions chlorure de la solution par les ions dichromate (Cr2O72-) du solide, est exprimée comme suit :
2Cl- (aqueux) + Ag2Cr2O7 (solide brun) → 2AgCl (solide blanc) + Cr2O72- (aqueux)
Définition de « partie par million (ppm) »
La concentration en ions chlorure est souvent exprimée en parties par million (ppm). La partie par million est une unité de concentration définie comme étant le poids d’un soluté (ion ou composé ajouté) divisé par le poids de la solution (après l’ajout de l’ion ou du composé) multiplié par un million (106). Pour les solutions aqueuses diluées, on suppose généralement que l’ajout d’ions ne modifie pas la densité de l’eau; ainsi, la densité de la solution est la même que celle de l’eau pure à la température ambiante (environ 1 g/mL) (Skoog et al., 2014, p. 72). Partant de ce principe, la définition de « partie par million » est simplifiée de la façon suivante :
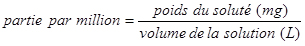
Ici, le soluté est l’ion chlorure, ce qui signifie qu’une solution de 1 ppm d’ions chlorure contient 1 milligramme (mg) d’ions chlorure par litre (L) de solution.
Remerciements
Merci tout spécialement à Catherine Machado, à Lucy ‘t Hart et à Meaghan Whalley, anciennes stagiaires à l’ICC, d’avoir contribué à l’élaboration de la présente Note.
Fournisseurs
Remarque : Les renseignements qui suivent visent uniquement à informer le lecteur. Le fait qu’une entreprise figure dans la présente liste ne signifie pas pour autant qu’elle est approuvée par l’Institut canadien de conservation.
Bandelettes réactives Quantab pour le chlorure
Les bandelettes Quantab sont fabriquées par Hach et distribuées par des fournisseurs de produits chimiques tels que Fisher Scientific.
- Hach (en anglais seulement)
- Fisher Scientific
Solutions étalons de chlorure
Trois solutions étalons de chlorure de marque Orion (0,1 M, 1 000 ppm, 100 ppm) sont fabriquées par Thermo Scientific. Quatorze solutions étalons de chlorure différentes (entre 1 ppm et 100 000 ppm) sont fabriquées par Ricca Chemical. Ces produits sont distribués par des fournisseurs de produits chimiques tels que Fisher Scientific.
- Thermo Scientific (en anglais seulement)
- Ricca Chemical (en anglais seulement)
- Fisher Scientific
Références
Hach, communication personnelle, 4 décembre 2014.
ODEGAARD, N., S. CARROLL et W. S. ZIMMT. Material Characterization Tests for Objects of Art and Archaeology, 2e éd., Londres (Royaume-Uni), Archetype Publications, 2005.
ODEGAARD, N., P. HILL, B. SANTARELLI et W. ZIMM. « Detecting and Identifying Salts During the Desalination Process with Spot Test Papers », WAAC (Western Association for Art Conservation) Newsletter, vol. 33 (2011), p. 14-17.
RIMMER, M., D. WATKINSON et Q. WANG. « The Efficiency of Chloride Extraction from Archaeological Iron Objects using Deoxygenated Alkaline Solutions », Studies in Conservation, vol. 57 (2012), p. 29-41.
SELWYN, L. Détermination de la concentration des ions chlorure en solutions aqueuses par titrage potentiométrique, Rapport de recherche no 2 de l’ICC, Ottawa (Ontario), ICC, 2001.
SKOOG, D. A., D. M. WEST, F. J. HOLLER et S. R. CROUCH. Chimie analytique, 3e éd., traduction de C. Buess-Herman et J. Dauchot, Bruxelles (Belgique), De Boeck, 2015.
WANG, Q., S. DOVE, F. SHEARMAN et M. SMIRNIOU. « Evaluation of Methods of Chloride Ion Concentration Determination and Effectiveness of Desalination Treatments using Sodium Hydroxide and Alkaline Sulphite Solutions », The Conservator, vol. 31 (2008), p. 67-74.
Rédigé par Lyndsie Selwyn
© Gouvernement du Canada, Institut canadien de conservation, 2016
ISSN 1928-5272