Bureau de liaison pour la Loi sur les aliments et drogues : Rapport sur les activités Avril 2015 à mars 2016

Télécharger le rapport au complet
(Format PDF, 400 Ko, 20 pages)
Organisation : Santé Canada
Type : Rapport
Date publiée : Avril 2015 - Mars 2016
Message du sous-ministre
À titre d’organisme de réglementation, Santé Canada joue un rôle important dans la protection de la santé et de la sécurité des Canadiens et des Canadiennes et s’engage à offrir un niveau accru de transparence et d’ouverture dans l’intérêt du public et pour favoriser la responsabilisation et renforcer la confiance à l’égard de ses décisions réglementaires.
En vertu de la Loi sur les aliments et drogues, nos responsabilités en matière de réglementation nécessitent un processus décisionnel rapide et complexe fondé sur des données scientifiques et des règlements rigoureux. Le Bureau de liaison pour la Loi sur les aliments et drogues (BLLAD) fait partie intégrante d’un processus de réglementation ouvert, transparent et compréhensible.
Le mandat du Bureau est d’offrir des services qui favorisent la communication respectueuse et positive entre Santé Canada et les parties externes en prêtant attention à notre façon d’administrer la Loi sur les aliments et drogues. Il s’agit d’un organisme neutre capable de résoudre les différends et d’améliorer les expériences en matière de service à la clientèle.
En harmonie avec son point de vue unique neutre et impartial, le BLLAD formule une rétroaction sur les préoccupations ou les améliorations que les intervenants ont constatées au chapitre du processus de réglementation. Comme le souligne le présent rapport annuel, le Bureau a entrepris des changements importants en vue d’accroître l’impartialité, la transparence et l’ouverture dans le processus de révision des décisions sur les médicaments d’ordonnance. Le rapport fait également état de la rétroaction des intervenants recueillie d’avril 2015 à mars 2016, ainsi que les engagements du Bureau concernant des améliorations à venir.
Simon Kennedy
Résumé des réalisations
- Lancement d’un nouveau processus de révision des décisions relatif aux examens de médicaments d’ordonnance
- Gestion de 135 cas de plainte et de demande de renseignements
- Élaboration et lancement de deux nouveaux ateliers sur le perfectionnement des compétences
- Tenue de 14 séances de formation
Révision en cours d’exercice
Lancement d’un nouveau processus de révision des décisions
Le processus de révision des décisions est un mécanisme de recours à Santé Canada pour les entreprises qui sont en désaccord avec une décision prise pendant le processus d’examen de médicaments. Le BLLAD a reçu le mandat de renforcer l’impartialité et la transparence du processus de révision des décisions. Ce mandat donne suite aux plaintes formulées par certains intervenants selon lesquelles la direction responsable de prendre la décision était aussi celle qui menait le processus de révision de la décision.
Le BLLAD est situé dans les bureaux de la Direction générale des communications et des affaires publiques de Santé Canada et, par conséquent, n’a aucun lien de dépendance avec les secteurs de réglementation responsables des examens de médicament. Le BLLAD a dirigé la restructuration et a commencé à gérer le processus tel qu’il est présenté dans la Ligne directrice : Révision des décisions sur les présentations de drogues pour usage humain. Le nouveau processus est entré en vigueur en avril 2015. Le BLLAD est dorénavant responsable de convoquer un groupe d’experts et d’organiser la réunion pour résoudre l’opposition. Nous pouvons organiser un processus interne en faisant appel aux experts de Santé Canada qui n’ont pas pris part à l’examen de la présentation ou entrer en contact avec des experts externes, si une expertise ou une perspective de l’extérieur est nécessaire. Le processus entraîne la formulation d’une recommandation à l’intention du directeur général responsable de l’examen du médicament.
Au cours de l’exercice 2015-2016, le BLLAD a reçu sept demandes de révision de décision. Un cas a été jugé non admissible, puisque la demande a été présentée après le délai de 30 jours. Voici une fragmentation des résultats. Le terme « innovateur » renvoie aux entreprises qui déposent une présentation de drogue nouvelle, alors que « générique » renvoie aux entreprises qui fabriquent une version générique d’un médicament de marque.
| Examen interne | Banc de révision | |||
|---|---|---|---|---|
| Décision d’origine maintenue | Décision d’origine modifiée et acheminée aux fins de révision | Décision d’origine maintenue | Décision d’origine modifiée et acheminée aux fins de révision | |
| Innovateur | s.o | s.o | 2 | 1 |
| Générique | 2 | 1 | s.o | s.o |
| Total | 2 | 1 | 2 | 1 |
Évaluation et rétroaction sur les changements
Dans le cadre de son engagement à l’égard de l’amélioration continue, le BLLAD a demandé à tous les participants au processus de révision des décisions de formuler une rétroaction. Les questionnaires d’évaluation ont été envoyés immédiatement après la réunion sur les révisions de décisions avant que la décision finale soit émise. Quinze réponses ont été reçues. Le tableau ci-dessous présente une partie de la rétroaction reçue (les réponses possibles étaient 1 = Fortement en désaccord, 2 = En désaccord, 3 = D’accord, 4 = Fortement d’accord).
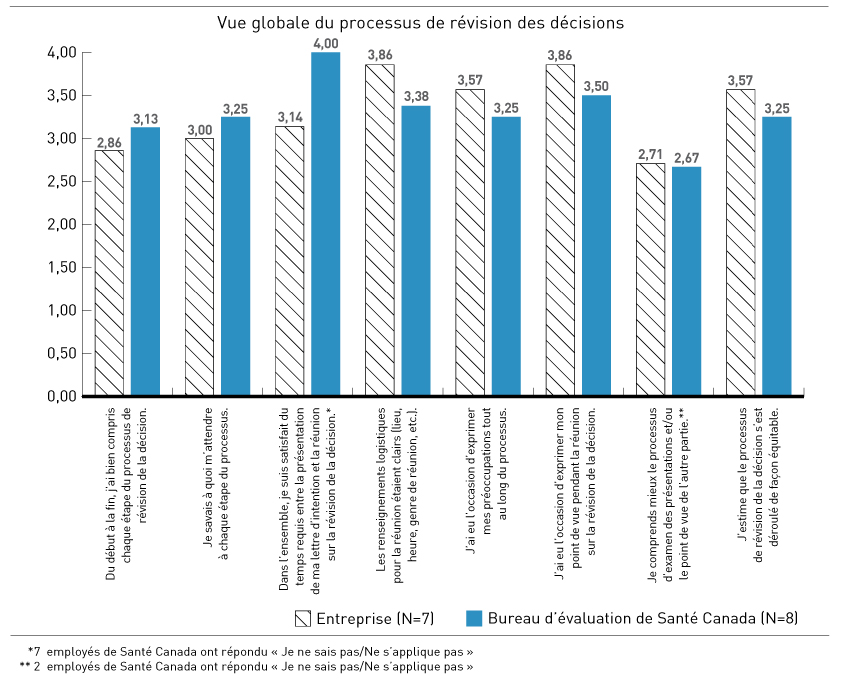
Figure 2 - Description textuel
Diagramme à barres verticales détaillant le résumé des réponses au questionnaire sur le processus de révision des décisions. Les réponses sont divisées en deux groupes : celles de l'entreprise et celles du bureau d'évaluation de Santé Canada. Sept représentants de l'entreprise et huit représentants de Santé Canada ont complété le questionnaire.
Le niveau de satisfaction varie entre zéro et quatre (quatre étant le niveau le plus élevé de satisfaction). Pour la première question 'Du début à la fin, j'ai bien compris chaque étape du processus de révision de la décision', le niveau de satisfaction de l'entreprise était 2.86 et celle de Santé Canada était 3.13.
Pour la deuxième question 'Je savais à quoi m'attendre à chaque étape du processus', le niveau de satisfaction de l'entreprise était 3.00 et celle de Santé Canada était 3.25.
Pour la troisième question 'Dans l'ensemble, je suis satisfait du temps requis entre la présentation de ma lettre d'intention et la réunion sur la révision de la décision', le niveau de satisfaction de l'entreprise était 3.14 et celle de Santé Canada était 4.00. A noter, 7 employés de Santé Canada ont répondu 'Je ne sais pas/Ne s'applique pas' à cette question.
Pour la quatrième question 'Les renseignements logistiques pour la réunion étaient clairs (lieu, heure, genre de réunion, etc.)', le niveau de satisfaction de l'entreprise était 3.86 et celle de Santé Canada était 3.38.
Pour la cinquième question 'J'ai eu l'occasion d'exprimer mes préoccupations tout au long du processus', le niveau de satisfaction de l'entreprise était 3.57 et celle de Santé Canada était 3.25.
Pour la sixième question 'J'ai eu l'occasion d'exprimer mon point de vue pendant la réunion sur la révision de la décision', le niveau de satisfaction de l'entreprise était 3.86 et celle de Santé Canada était 3.50.
Pour la septième question 'Je comprends mieux le processus d'examens des présentations et/ou le point de vue de l'autre partie', le niveau de satisfaction de l'entreprise était 3.14 et celle de Santé Canada était 4.00. A noter, sept employés de Santé Canada ont répondu 'Je ne sais pas/Ne s'applique pas' à cette question.
Pour la huitième question 'J'estime que le processus de révision de la décision s'est déroulé de façon équitable', le niveau de satisfaction de l'entreprise était 3.57 et celle de Santé Canada était 3.25.
* 7 employés de Santé Canada ont répondu « Je ne sais pas/Ne s’applique pas »
** 2 employés de Santé Canada ont répondu « Je ne sais pas/Ne s’applique pas »
Selon la rétroaction et l’expérience propre du BLLAD au cours de la dernière année, d’autres améliorations seront apportées au processus de révision des décisions afin qu’il comprenne ce qui suit :
- une feuille « foire aux questions » pour les participants;
- un code de conduite pour la réunion;
- une orientation à l’intention des membres du banc de révision sur la façon de gérer la réunion de révision de la décision;
- une assistance préparatoire pour les entreprises et les employés qui ont besoin de renseignements supplémentaires;
- des rapports normalisés aux fins de clarté et d’uniformité;
- des formulaires à jour.
Le BLLAD applique les leçons retenues dans le cadre de la restructuration du processus de révision des décisions sur les médicaments à d’autres processus semblables sous le régime de la Loi sur les aliments et drogues. En avril 2016, le Bureau a commencé à travailler sur la restructuration du processus pour les produits de santé naturels et sans ordonnance. Dans le cadre de nos efforts visant à améliorer le processus, nous consulterons et mobiliserons les intervenants intéressés, tant à l’intérieur qu’à l’extérieur du Ministère.
Gestion des cas
La gestion de cas en bref
- 135 cas gérés
- 63 Gestion des enjeux (plaintes), représentant 47 % de tous les cas
- 72 Recherche d’information (demandes de renseignements), représentant 53 % de tous les cas
En parallèle avec le lancement du nouveau processus de révision des décisions, le personnel du BLLAD a géré 135 cas en 2015-2016. Nous classons nos cas de façon globale dans les catégories « Gestion des enjeux » et « Recherche d’information ». Les cas de gestion des enjeux ont habituellement trait à une plainte. Notre expertise en règlement de différends s’applique tout à fait à la résolution précoce des conflits au niveau le moins élevé possible. Néanmoins, des intervenants nous ont mentionné que notre aide pour la navigation dans l’environnement de réglementation et la structure ministérielle complexe était très utile. Nous avons incorporé quelques études de cas à la fin du présent rapport pour expliquer notre façon de contribuer à résoudre les plaintes et à répondre aux demandes de renseignements.
Au cours de la période visant le présent rapport, nous avons constaté une augmentation de 35 % par rapport à l’année précédente (voir la figure 1). Nous attribuons cette augmentation de cas à nos efforts de sensibilisation ciblée du public et des employés de Santé Canada qui peuvent bénéficier de nos services. Nous avons renforcé notre présence Web, tenu des séances de sensibilisation avec des associations et du personnel de l’industrie et transmis de l’information par voie électronique aux personnes inscrites dans le Registre d’intervenants du Ministère. Les activités de consultation et de mobilisation que nous avons tenues dans le cadre de la restructuration du processus de révision des décisions sur les médicaments ont également aidé à accroître la visibilité du Bureau.
Une tendance déterminée antérieurement s’est poursuivie au cours des trois dernières années : un plus grand nombre d’entreprises communiquent avec le Bureau. Quatre-vingt-six (86) cas sont liés à des entreprises et des associations de l’industrie, soit 64 % de tous les cas. Nos services sont également offerts aux particuliers, y compris les patients et les consommateurs qui ont des questions ou des plaintes à formuler au sujet du processus de réglementation. Vingt-cinq particuliers ont communiqué avec nous.
Commentaires reçus
Les thèmes suivants saisissent les principales tendances qui ont été signalées par des intervenants au cours de la dernière année.
Rétroaction positive
Mobilisation dans l’ensemble des secteurs
Une séance de mobilisation unique en son genre avec un groupe diversifié d’intervenants s’est tenue en juin 2015. Il a réuni, entre autres, des membres des associations de l’industrie, des intervenants en soins de santé, des patients et des groupes de consommateurs, ainsi que des défenseurs d’une alimentation et d’un mode de vie sains. Les invités ont eu l’occasion d’entendre des fonctionnaires du Ministère et d’interagir les uns les autres sur la façon d’obtenir de meilleurs résultats pour les Canadiens au chapitre des aliments et des produits de soins de santé. Les fonctionnaires du Ministère ont fourni des renseignements sur les défis et les priorités en matière de réglementation et ont invité les participants à formuler une rétroaction sur la façon de mettre à jour et de renouveler le plan stratégique visant à régler ces questions. Les participants ayant des intérêts apparemment opposés ont eu la possibilité de discuter entre eux et avec le Ministère relativement à ces questions. Le BLLAD a entendu plusieurs participants mentionner qu’ils appréciaient la séance et espéraient que ce genre de dialogue allait se poursuivre ultérieurement.
Demandes d’amélioration de la part des intervenants
Volonté croissante d’établir un cadre pour les produits de santé destinés aux consommateurs
Le BLLAD continue de recevoir des plaintes de la part d’entreprises au sujet de l’approche actuelle en matière de réglementation des produits de santé destinés aux consommateurs. Les intervenants de l’industrie continuent de réclamer un nouveau cadre harmonisé qui correspond à l’approche de réglementation des médicaments en vente libre, des produits de santé naturels, des cosmétiques et des désinfectants.
Conformément à l’approche actuelle, selon leur classification par le Ministère, des niveaux d’attention différents sont accordés à des produits dont le profil de risque est semblable. Par exemple, il se peut qu’un baume pour les lèvres revendiquant un facteur de protection solaire (FPS) soit réglementé en tant que médicament ou produit de santé naturel, selon les ingrédients actifs et les allégations pour l’étiquetage. Cependant, si l’allégation de FPS est retirée, le produit peut être réglementé en tant que cosmétique. Un baume pour les lèvres réglementé comme un médicament doit faire l’objet d’un processus beaucoup plus coûteux, long et rigoureux, même si son profil de risque est semblable à celui d’un produit de santé naturel ou d’un cosmétique. Les intervenants de l’industrie accueillent favorablement tout suivi ou toute mesure visant à mettre en œuvre des changements au cadre pour les produits de santé destinés aux consommateurs à la suite de la rétroaction qu’ils ont fournie dans le cadre de la consultation qui s’est tenue de novembre 2014 à février 2015. Trente et une réponses ont été reçues, principalement de l’industrie. Elles expriment l’espoir qu’une nouvelle réglementation et des changements opérationnels soient adoptés bientôt afin de simplifier la façon de réglementer les produits de santé destinés aux consommateurs. Elles indiquaient que les améliorations permettraient d’attirer un nombre accru de fabricants sur le marché canadien et favoriseraient le lancement de produits novateurs pour les consommateurs.
En 2016, Santé Canada a mené d’autres activités en vue d’obtenir une rétroaction sur le cadre de réglementation des « soins personnels » de la part d’un groupe d’intervenants encore plus diversifié, y compris des consommateurs et des patients.
Catégorie réservée à un usage professionnel ou programme d’accès spécial pour les produits de santé naturels
Les praticiens de la médecine traditionnelle et de la santé naturelle soulignent qu’aucun cadre de réglementation n’est en place pour une catégorie de produits de santé naturels qui nécessitent la surveillance d’un pratitien de la santé pour qu’un consommateur ou un patient y ait accès. En vertu du Règlement sur les produits de santé naturels en vigueur actuellement, une fois qu’un produit respecte les normes d’innocuité et d’efficacité, les consommateurs peuvent l’acheter directement. Les praticiens de la médecine traditionnelle et de la santé demandent l’établissement d’une catégorie « réservé à un usage professionnel » pour les produits de santé naturels afin de pouvoir utiliser ces médicaments de source naturelle comme une solution de rechange aux médicaments d’ordonnance afin de soigner des états qui nécessitent une surveillance par un professionnel qualifié. Étant donné qu’à l’heure actuelle, aucune catégorie « réservé à un usage professionnel » n’est établie, les praticiens dans ce domaine demandent l’accès à ces médicaments naturels par l’intermédiaire du Programme d’accès spécial de Santé Canada actuellement en place.
Processus de recours limités pour les mesures de conformité et d’application de la loi
Les parties réglementées savent que les activités de conformité et d’application de la loi de Santé Canada sont essentielles à la protection des médicaments et des produits de santé naturels vendus aux Canadiens, ainsi qu’à l’intégrité des marques canadiennes. Cependant, il arrive que le Ministère et ses parties réglementées ne soient pas d’accord en ce qui concerne le type d’activité de conformité et d’application justifié. Il peut y avoir des désaccords quant aux résultats d’inspection d’une installation de fabrication ou sur un produit en particulier, qu’il soit fabriqué ou importé au Canada. Au cours de la période visée par le présent rapport, le BLLAD a ouvert 14 dossiers pour lesquels les intervenants demandaient un mécanisme de recours relativement à différentes mesures de conformité et d’application de la loi.
Les processus mis en place pour le traitement des désaccords en matière de conformité et d’application de la loi sont limités. Lorsqu’une « possibilité d’être entendu » ou un processus de révision est offert, comme dans le cas d’un refus ou de la suspension potentielle d’une licence d’établissement pharmaceutique, il est difficile de trouver l’information et de comprendre le processus.
L’approche adoptée par le BLLAD pour gérer tous les genres de plaintes en matière de conformité et d’application de la loi vise à instaurer une meilleure communication entre la partie réglementée et le Ministère. Nous aidons les intervenants à expliquer leur point de vue afin de favoriser la compréhension. Nous aidons aussi à faire en sorte que le Ministère transmette clairement la raison de sa décision et explique les lois et règlements à l’appui de façon compréhensible. Toutefois, il arrive que la partie réglementée ne soit pas d’accord avec les mesures prises par le personnel opérationnel, estimant qu’une erreur a peut-être été commise.
Ces différends peuvent nécessiter beaucoup de temps et de ressources de la part de toutes les parties concernées. Les intervenants ont demandé l’établissement d’un processus de recours administratif clairement défini et équitable du point de vue procédurale pour le règlement des différends touchant la conformité et l’application de la loi.
Mise en œuvre de documents d’orientation provisoires
Dans le but de suivre le rythme dans un environnement scientifique et de réglementation en constante évolution, Santé Canada doit sans cesse examiner et mettre à jour ses divers documents d’orientation. Des intervenants ont mentionné que, parfois, Santé Canada met en œuvre des processus d’orientation provisoires avant que le Ministère ait communiqué aux intervenants externes que la nouvelle orientation a été mise au point. Cela entraîne une confusion, un manque de prévisibilité et des retards. Les intervenants souhaitent être informés avant la mise en œuvre d’un nouveau document d’orientation. De plus, le cas échéant (aucune question d’innocuité importante et immédiate n’est en jeu), ils souhaitent se voir accorder une période de transition raisonnable pour se conformer aux nouvelles exigences.
Le BLLAD en action : Études de cas
| Enjeu | Notre bureau reçoit une demande du personnel de Santé Canada pour obtenir de l’aide au chapitre de la gestion des plaintes de la part d’un citoyen qui a continué à écrire et à appeler malgré les efforts pour tenir compte de ses préoccupations. La plainte du citoyen concerne le fait qu’il a souffert d’un grave problème de santé, mais que ses médecins traitants l’ont mal diagnostiqué. Il a précisé qu’il avait besoin d’un médicament dont la vente était interdite au Canada. Ses médecins n’étaient pas disposés à appuyer sa demande concernant ce médicament dans le cadre du Programme d’accès spécial de Santé Canada. |
|---|---|
| Intervention | Le personnel du BLLAD a examiné à fond la correspondance entre le citoyen et le Ministère. Il était clair qu’il s’agissait d’une situation complexe comportant des allégations de négligence des médecins formulées par le citoyen qui remettait en question les pratiques de l’hôpital et se plaignait du manque d’accès au médicament. Le BLLAD a discuté avec le citoyen afin de déterminer les enjeux précis qui le préoccupaient. Le Bureau a clarifié l’ensemble des questions ainsi que les processus de plainte adéquats pour chacune de ces questions qui nécessitaient la participation de plusieurs administrations. Le rôle et la portée des responsabilités de Santé Canada en matière de réglementation ont également été expliqués dans un langage clair et facile à comprendre. |
| Résultat | Le citoyen a écrit au BLLAD pour remercier le personnel de ses efforts et des explications reçues. Il a précisé avoir apprécié l’écoute du personnel. Quelque mois plus tard, le BLLAD a assuré un suivi auprès de Santé Canada et a constaté que l’envoi de lettres et les appels téléphoniques avaient cessé. |
| Enjeu | Au cours des dernières années, les régulateurs du monde entier ont constaté que de plus en plus de personnes développent une sensibilité de la peau en présence des agents de conservation méthylisothiazolinone et méthylchloroisothiazolinone – MI/MC. Santé Canada a ajouté ces substances à la Liste critique des ingrédients de cosmétiques au mois de décembre 2015, interdisant leur usage dans les produits sans rinçage tels que les lotions pour le corps. Cependant, de nombreuses entreprises croient qu’elles n’ont pas reçu de préavis suffisant pour modifier la formule de leurs produits. |
|---|---|
| Intervention | Le BLLAD a reçu plusieurs plaintes de petites et grandes entreprises en ce qui concerne l’approche de Santé Canada. Elles souhaitaient obtenir une période de transition afin de trouver de nouveaux agents de conservation pour les produits sans rinçage. Elles ont cru que les exigences actuelles en matière d’étiquetage donneraient les renseignements suffisants aux consommateurs pour prendre des décisions éclairées concernant l’achat des produits alors qu’ils sont en cours de reformulation. L’Europe avait accordé une telle période de transition à l’industrie. La Food and Drugs Administration des É.-U. a choisi de publier des avertissements à l’intention du public, sans interdire l’utilisation des ingrédients. |
| Résultat | Le BLLAD a aidé l’industrie à communiquer avec les cadres supérieurs du Ministère. Au moyen de la base de données des « rappels et avis de sécurité » pour communiquer les risques aux Canadiens, le Ministère a publié un avis public à l’intention des consommateurs. Santé Canada a reporté l’ordonnance d’arrêt réglementaire de la vente pour accorder une courte période de transition à l’industrie afin qu’elle modifie la formule des produits sans rinçage. |
| Enjeu | Un propriétaire d’une petite entreprise importait divers produits de soins personnels communément utilisés par son groupe culturel pendant de nombreuses années. Il a eu toute une surprise lorsqu’un jour, les agents des services frontaliers, à la demande de Santé Canada, ont refusé l’entrée au pays de leurs produits et les ont saisis. Comme bon nombre d’exploitants de petite entreprise, cette personne ne connaissait pas bien les lois et les règlements applicables et cela mit son entreprise en péril. Il allait devoir éponger d’importantes pertes financières. Il était très frustré et il a communiqué avec le BLLAD, puisque les agents de conformité et d’application de la loi ont rejeté sa demande visant une rencontre. |
|---|---|
| Intervention | Le BLLAD a communiqué avec les agents de conformité et d’application de la loi pour obtenir leur point de vue. À leur avis, la question était simple : les produits ne respectaient pas la réglementation et, par conséquent, ne pouvaient pas être importés. Ils estimaient avoir précisé ces informations assez clairement dans leur correspondance écrite. Le BLLAD a expliqué qu’une rencontre serait bénéfique pour cette personne, étant donné les différences culturelles et linguistiques et la complexité de la réglementation. Les agents de conformité et d’application de la loi ont accepté de le rencontrer. |
| Résultat | Le résultat n’a pas changé et les produits non conformes n’ont pas traversé la frontière, mais le propriétaire d’entreprise a bénéficié d’une rencontre instructive et utile. Il était reconnaissant du temps que les agents lui ont consacré en vue de démystifier la réglementation. Fort de ces connaissances, il pouvait dorénavant prendre les mesures nécessaires pour se conformer et continuer à exploiter son entreprise sans craindre d’autres perturbations. |
| Enjeu | Un employé de Santé Canada a communiqué avec le BLLAD pour qu’on l’aide à résoudre un conflit avec une entreprise. L’entreprise avait fait parvenir une présentation à une direction en particulier en croyant que la direction était responsable de ce produit. Le personnel d’examen a classifié le produit différemment et a transféré la présentation à une autre direction. Le personnel n’a pas clairement informé l’entreprise du transfert et de l’augmentation substantielle des frais connexes. Les examinateurs de la deuxième direction ont rejeté la présentation à l’étape de l’examen préliminaire. C’est à ce moment que le personnel a informé l’entreprise du transfert et de l’augmentation des frais. L’entreprise s’est opposée à la reclassification et à l’augmentation des frais. |
|---|---|
| Intervention | Le BLLAD a posé des questions sur le processus décisionnel qui a entraîné le changement de direction. Nous avons examiné avec soin ce que le personnel a communiqué à l’entreprise avant le transfert du dossier. Le personnel a convenu que la raison du transfert n’avait pas été expliquée clairement. L’entreprise n’avait pas eu l’occasion de répondre à la reclassification ou de retirer sa présentation. Le BLLAD a longuement discuté avec les deux directions afin de trouver des options pour régler la question rapidement et de façon équitable. |
| Résultat | Le BLLAD a été en mesure d’aider Santé Canada à traiter des préoccupations de l’entreprise et à éviter que la question soit inutilement renvoyée à l’échelon supérieur. Nous avons facilité les discussions avec le personnel des deux directions afin d’établir un consensus et de déterminer la façon de procéder. Le personnel a été en mesure de régler la question avec l’entreprise afin qu’elle n’assume que les frais initiaux auxquels elle s’attendait et qu’elle puisse prendre une décision éclairée à savoir si elle souhaite aller de l’avant avec sa présentation. |
Statistiques relatives aux cas
Ceux qui ont communiqué avec nous
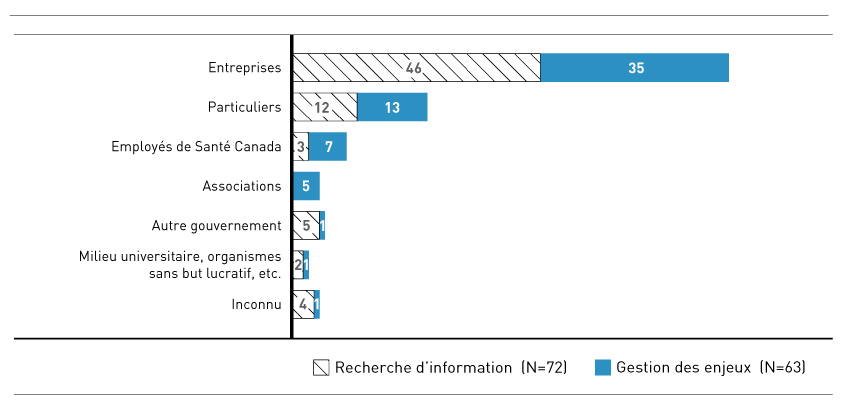
Figure 3 - Description textuel
Diagramme à barres horizontales expliquant le type d'intervenants qui ont communiqué avec le BLLAD. Le diagramme est réparti en fonction des dossiers de recherche d'information et de gestion des enjeux.
Vous trouverez ci-après la liste des contacts pour les 72 cas de recherche d'information : Particuliers: 12; Entreprises : 46; Employés de Santé Canada : 3; Universités, organismes sans but lucratif, professionnels de la santé, etc. : 2; Autre gouvernement : 5; Associations : 0; Inconnus : 4.
Vous trouverez ci-après la liste des contacts pour les 63 cas de gestion des enjeux : Particuliers : 13; Entreprises : 35; Employés de Santé Canada : 7; Universités, organismes sans but lucratif, professionnels de la santé, etc. : 1; Autre gouvernement : 1; Associations : 5; Inconnus : 1.
Répartition en thèmes
Nous avons réparti l’analyse des cas sous les quatre thèmes suivants :
- Problèmes de communication (Par exemple, des demandes de renseignements, des appels non retournés, une correspondance incohérente ou une correspondance qui ne répond pas aux préoccupations des intervenants.)
- Questions de politique (Par exemple, un désaccord à propos de l’interprétation ou de l’application des règlements, des politiques ou des lois, par exemple la classification d’un produit, l’évaluation des risques, la cohérence de la politique.)
- Questions de procédure (Par exemple, l’insatisfaction liée aux processus utilisés dans la prise de décisions réglementaires, comme la rapidité d’exécution, l’ouverture, la transparence, la prévisibilité, l’avis préalable des changements à l’établissement des règles.)
- Problèmes interpersonnels (Par exemple, la manière dont le personnel traite l’intervenant ou les demandes du personnel pour obtenir de l’aide lorsque la communication est difficile avec des intervenants.)
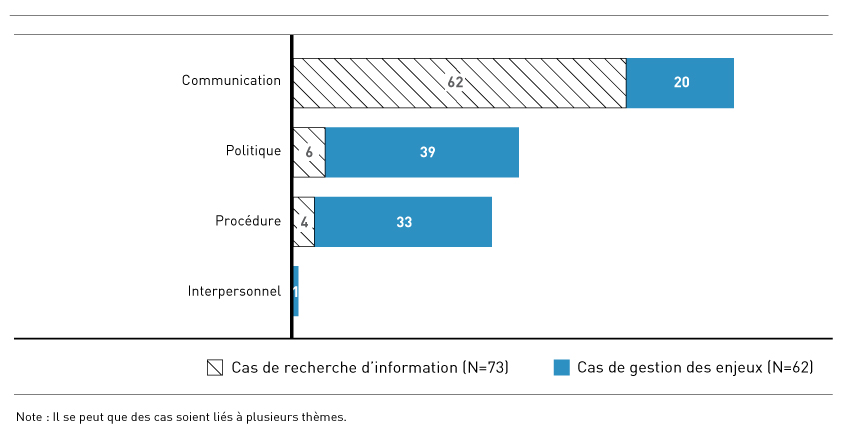
Figure 4 - Description textuel
Diagramme à barres horizontales expliquant le type d'intervenants qui ont communiqué avec le BLLAD. Le diagramme est réparti en fonction des dossiers de recherche d'information et de gestion des enjeux.
Vous trouverez ci-après la liste des contacts pour les 72 cas de recherche d'information : Particuliers: 12; Entreprises : 46; Employés de Santé Canada : 3; Universités, organismes sans but lucratif, professionnels de la santé, etc. : 2; Autre gouvernement : 5; Associations : 0; Inconnus : 4.
Vous trouverez ci-après la liste des contacts pour les 63 cas de gestion des enjeux : Particuliers : 13; Entreprises : 35; Employés de Santé Canada : 7; Universités, organismes sans but lucratif, professionnels de la santé, etc. : 1; Autre gouvernement : 1; Associations : 5; Inconnus : 1.
Directions impliquées dans nos cas
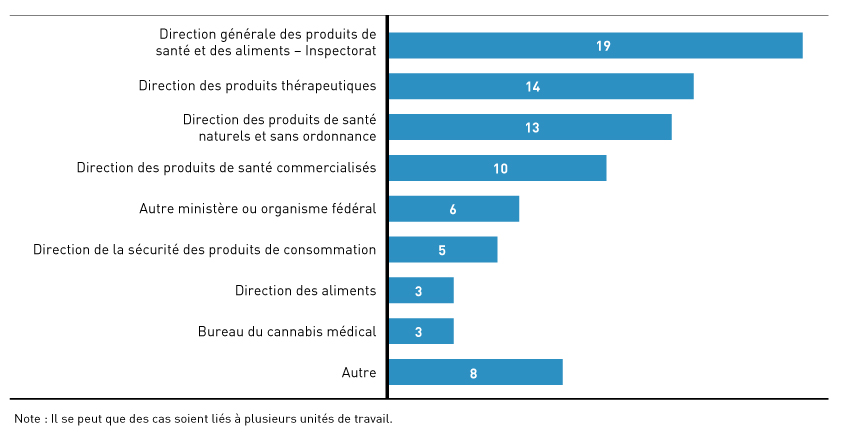
Figure 5 - Description textuel
Diagramme à barres horizontales expliquant les directions concernées par le règlement de nos 62 cas de gestions d'enjeux. Note : Il se peut que des cas soient liés à plusieurs unités de travail.
Inspectorat de la Direction générale des produits de santé et des aliments : 19; Direction des produits thérapeutiques : 14; Direction des produits de santé naturels et sans ordonnance : 13; Direction des produits de santé commercialisés : 10; Autre ministère ou organisme fédéral : 6; Direction de la sécurité des produits de consommation : 5; Direction des aliments : 3; Bureau de cannabis médical : 3; Autre : 8.

Figure 6 - Description textuel
Diagramme à barres horizontales indiquant les organismes auxquels le Bureau de liaison pour la Loi sur les aliments et drogues a renvoyé les intervenants pour les 73 cas de recherche d'information. Note : Il se peut que des cas soient liés à plusieurs unités de travail.
Inspectorat de la Direction générale des produits de santé et des aliments : 17; Direction des produits de santé naturels et sans ordonnance : 15; Direction des produits thérapeutiques : 14; Autres ministères ou gouvernements : 7; Direction des produits de santé commercialisés : 5; Direction des aliments : 5; Direction de la sécurité des produits de consommation : 4; Bureau des substances contrôlées : 4; Bureau du cannabis médical : 2; Autre : 3.
Origine géographique des cas
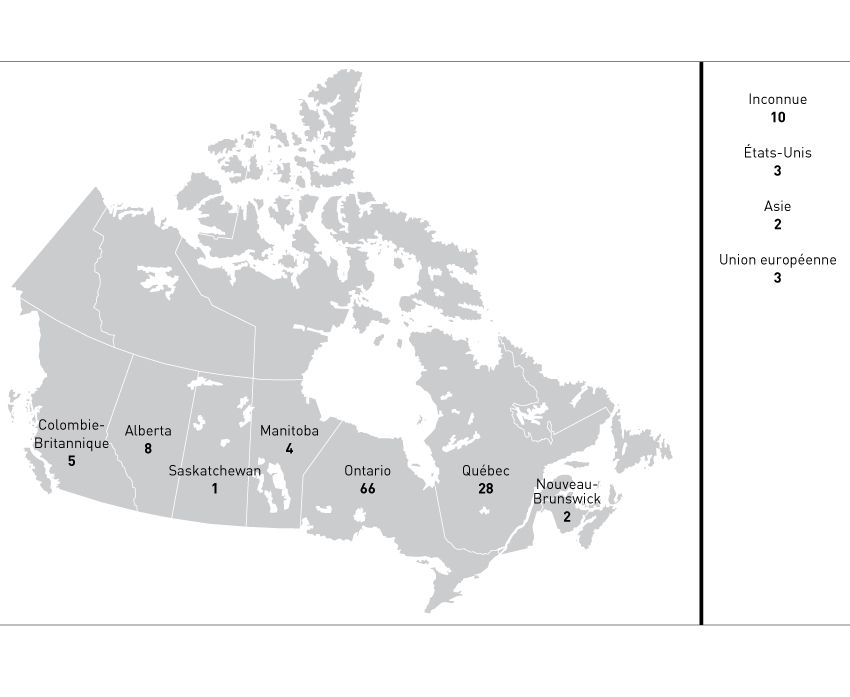
Figure 7 - Description textuel
Carte du Canada indiquant l'origine géographique des dossiers ouverts par le Bureau de liaison pour la Loi sur les aliments et drogues.
Ontario : 66; Québec : 28; Alberta : 8; Colombie-Britannique : 5; Manitoba : 4; Nouveau-Brunswick : 2; Saskatchewan : 1; les autres provinces et territoires : 0; États-Unis : 3; Union européenne : 3; Asie : 2; Inconnu: 10.
Perfectionnement des compétences
La formation en bref
- Tenue de 10 séances intitulées « Pour tirer le maximum des communications difficiles avec les intervenants » auxquelles un total de 186 personnes ont participé.
- Lancement de deux nouveaux mini-ateliers donnés quatre fois à un total de 56 participants.
Le BLLAD continue d’assumer un rôle important à Santé Canada pour perfectionner les compétences du personnel dans le domaine de la gestion des relations avec les intervenants dans un système de réglementation complexe et en constante évolution. Notre cours de deux jours intitulé « Pour tirer le maximum des communications difficiles avec les intervenants » est toujours très populaire. À l’occasion, nous offrons des places à des employés d’autres ministères fédéraux par l’intermédiaire de la Communauté des régulateurs fédéraux afin de permettre aux participants de différentes organisations d’échanger leurs connaissances et pratiques exemplaires.
En 2015-2016, nous avons lancé deux ateliers interactifs d’une demi-journée. Intitulés « À l’écoute des questions importantes » et « Reconnaître nos expériences », ils ont pour but d’approfondir la réflexion et de mettre au point l’approche visant le règlement des différends avec les intervenants. Ils peuvent se tenir pendant des journées de réflexion des employés ou des réunions d’équipe, ou servir de formation de mise à niveau à la suite de notre formation de deux jours.
Les prochaines étapes
Santé Canada a misé sur la position neutre et impartiale du BLLAD, rendant le Bureau responsable de la gestion du processus de révision des présentations de médicaments. Au cours de la prochaine année, le BLLAD mettra en pratique les leçons retenues dans le cadre de la restructuration du processus de révision des décisions pour les produits de santé naturels et sans ordonnance. Nous mènerons une consultation externe avant le lancement d’un nouveau processus. Le Bureau continuera d’assumer son rôle qui vise à favoriser le traitement des plaintes et des demandes de renseignements des intervenants externes, ainsi que d’agir à titre d’intermédiaire auprès du personnel de Santé Canada afin de régler ces questions de façon efficace et équitable.