Page 3 : Recommandations pour la qualité de l'eau potable au Canada : document technique – le chlorite et le chlorate
Le chlorite et le chlorate dans l'eau potableNote de bas de page 1
Partie II. Science et considérations techniques
4.0 Identité, utilisation et sources dans l'environnement
Le chlorite (ClO2-) et le chlorate (ClO3-) sont des anions qui peuvent former des sels (p. ex. avec le sodium). Le dioxyde de chlore (ClO2) est un gaz dont la couleur va de verdâtre à jaune rougeâtre à la température et à la pression ambiantes (Gates, 1989; Lewis, 1993). En raison de sa nature volatile et réactive, le dioxyde de chlore doit être produit sur place, et sa durée de conservation est très limitée. Le tableau 1 donne les principales propriétés du chlorite de sodium, du chlorate de sodium et du dioxyde de chlore.
| Propriétés/valeurs | Chlorite (sodium) | Chlorate (sodium) | Dioxyde de chlore |
|---|---|---|---|
| Forme | Cristal blanc/poudre cristalline blanche | Cristaux ou granules blancs ou incolores | Gaz verdâtre à jaune rougeâtre à la température et à la pression ambiantes |
| Point de fusion | Se décompose à > 180 °C | 248 °C | -59,6 °C |
| Point d'ébullition | S.O. (Se décompose à > 180°C) | Se décompose à > 265 °C | 10,9 °C |
| Densité | 2,47 à 25 °C | 2,49 à 25 °C | 1,64 à 0 °C |
| Pression de vapeur | ne s'applique pas | ne s'applique pas | 142,13 kPa (1066 mm Hg) à 20 °C |
| Solubilité | 405 g/L à 20 °C Très soluble (se dissocie en ions sodium et chlorite) |
960 - 1000 g/L Très soluble (se dissocie en des ions sodium et chlorite) |
3,01 g/L à 25 °C Grande solubilité |
| Coefficient de partage octanol-eau (log Koe) | -7.18 | -7.18 | -3.22 |
|
Notes de bas de page du Tableau 1
|
|||
Dans les usines municipales de traitement de l'eau, on utilise le dioxyde de chlore pour désinfecter l'eau ou pour en contrôler le goût, l'odeur et la couleur. Il s'agit d'un puissant oxydant (pouvoir oxydant comparativement à celui du chlore : 0,94) dans l'eau et on l'utilise pour contrôler le goût et les odeurs dans l'eau potable et comme substitut du chlore pour désinfecter. Le dioxyde de chlore est normalement utilisé comme désinfectant primaire, mais certains services publics ont été capables de maintenir une concentration résiduelle de dioxyde de chlore dans leur réseau de distribution afin de préserver la qualité de l'eau (Volk et coll., 2002). La désinfection au moyen du dioxyde de chlore requiert un temps de contact moins long et une dose moins élevée que la désinfection au chlore, pour une réduction égale du nombre de coliformes (Aieta et coll., 1980). Le seuil critique pour que le goût et l'odeur du dioxyde de chlore soient perceptibles est de 0,4 mg/L (NRC des États-Unis, 1987).
Le dioxyde de chlore est également utilisé dans le traitement des eaux industrielles et des eaux grises et l'épuration des eaux usées, dans les usines de pâtes (traitement des boues et machines à papier), dans la transformation des aliments et dans l'industrie textile. Il sert d'agent de blanchiment pour la cellulose, la pâte de bois, les gras et les huiles, les textiles et la cire d'abeille. On l'utilise comme désinfectant et agent de stérilisation pour les pièces et l'équipement (NRC des États-Unis, 1987; U.S. EPA, 2000; Budavari et coll., 2001; ATSDR, 2004).
Le chlorite de sodium est utilisé pour la production sur place de dioxyde de chlore. Il a aussi été utilisé comme agent de blanchiment dans la production de papier, de textiles et de pailles, la fabrication de cires, de laques et vernis, dans la composition de désinfectants, pour la stérilisation, et dans l'attaque chimique de cartes de circuit imprimé (U.S. EPA, 2000; ATSDR, 2004; OMS, 2004).
Le chlorate de sodium est utilisé dans la fabrication des teintures, des allumettes et des explosifs, la tannerie et la finition du cuir, et dans la formulation d'herbicides et de défoliants (OMS, 2004).
4.1 Comportement dans les réseaux de distribution de l'eau
Des études ont montré qu'approximativement 70 % du dioxyde de chlore introduit dans l'eau forme du chlorite, tandis que 10 % environ forme du chlorate (Volk et coll., 2002). Bien que le dioxyde de chlore soit un gaz instable qui se décompose rapidement dans l'air, il est très soluble dans l'eau (ATSDR, 2004). Les solutions aqueuses de dioxyde de chlore seul ne subiront pas une grande hydrolyse si le pH est maintenu entre 2-10 (ATSDR, 2004). Dans une solution alcaline, un mélange d'ions chlorite et chlorate se forme assez rapidement (Cotton et coll., 1999).
En présence d'une lumière solaire intense et à des concentrations élevées, le dioxyde de chlore ne réagit pas avec l'eau ni avec l'ammoniac, mais oxyde l'ion bromure en hypobromure et en bromate. Le dioxyde de chlore ne réagit généralement pas avec les amines primaires, mais il réagit lentement avec les amines secondaires et tertiaires pour produire des amines aliphatiques secondaires sans formation de N-oxydes (White, 1992). L'ATSDR (2004) a en outre rapporté que le dioxyde de chlore « exempt de chlore » ne forme pas de trihalométhanes (THM) dans sa réaction avec les acides humiques et fulviques; toutefois, d'autres composés organochlorés peuvent se former. Il faut cependant noter que la désinfection secondaire à l'aide du chlore entraînera la formation d'une petite quantité de sous-produits de désinfection chlorés (SPDC).
Les ions chlorite et chlorate subissent une altération sous l'effet des bactéries dans des conditions anaérobiques. La dégradation anaérobique est un processus important dans les eaux souterraines anoxiques. Par contre, on n'a trouvé aucune information quantitative sur le taux de biodégradation des ions chlorate ou chlorite dans l'environnement. Il semble toutefois que le taux de dégradation des ions chlorate soit rapide dans des conditions anaérobiques dans les installations de traitement des eaux usées (Logan, 1998).
5.0 Exposition
L'eau potable est la principale voie d'exposition environnementale au chlorite et au chlorate. Les ions chlorite et chlorate sont des sous-produits de désinfection qui se retrouvent souvent dans l'eau potable lorsque le dioxyde de chlore est utilisé dans le procédé de traitement. C'est la technique de production du dioxyde de chlore et, à un degré moindre, le réglage du générateur qui déterminent les types et la quantité des impuretés, comme les ions chlorite, chlorate et perchlorate (ClO4-), que l'on retrouve dans le dioxyde de chlore obtenu (Gordon, 2001). Les ions chlorate peuvent également se former pendant la décomposition photolytique du dioxyde de chlore et du chlorite présents dans l'eau, sous l'effet de la lumière du soleil ou d'un éclairage fluorescent (Griese et coll., 1992).
Au Canada, très peu d'usines de traitement utilisent du dioxyde de chlore. Le Québec est l'une des rares provinces où on l'utilise. Les concentrations de dioxyde de chlore, d'ions chlorite et d'ions chlorate ont été mesurées dans huit réseaux du Québec (Aranda-Rodriguez et coll., 2004; Santé Canada, 2005) au cours de l'hiver et de l'été 2003. Des échantillons ont été recueillis à la sortie des usines de traitement et à trois différents points des réseaux de distribution (D1, D2 et D3). Le tableau 2 donne l'étendue et la moyenne des concentrations pour tous les emplacements :
| Produit chimique | Saison | Étendue des concentrations observées, en mg/L (moyenne) | |||
|---|---|---|---|---|---|
| T | D1 | D2 | D3 | ||
| Dioxyde de chlore | Hiver | 0,01-0,53 (0,22) |
<0,01-0,21 (0,09) |
<0,01-0,22 (0,09) |
<0,01-0,06 (0,03) |
| Été | <0,01 - 0,63 (0,32) |
non analysé | non analysé | non analysé | |
| Ion chlorite | Hiver | <0,03-0,87 (0,36) |
<0,03-0,85 (0,36) |
<0,03-0,77 (0,34) |
<0,03-0,69 (0,29) |
| Été | <0,03-1,62 (0,48) |
<0,03-1,56 (0,45) |
<0,03-1,58 (0,44) |
<0,033-1,25 (0,39) |
|
| Ion chlorate | Hiver | <0,03-0,31 (0,13) |
<0,03-0,32 (0,13) |
<0,03-0,29 (0,12) |
<0,03-0,31 (0,13) |
| Été | 0,08-0,59 (0,21) |
0,12-0,61 (0,22) |
0,11-0,59 (0,22) |
0,15-0,58 (0,22) |
|
|
Notes de bas de page du Tableau 2
|
|||||
Le dioxyde de chlore, le chlorite et le chlorate peuvent se retrouver dans les produits alimentaires en raison de leur emploi dans la transformation de la farine et de leur utilisation comme agent de décoloration des caroténoïdes et d'autres pigments naturels (dioxyde de chlore), comme agent de blanchiment dans la préparation d'amidon modifié d'usage alimentaire (chlorite de sodium), comme additif indirect dans les produits de papier et de carton servant à emballer les produits alimentaires (chlorite de sodium) et comme défoliant, dessiccant et fongicide en agriculture (chlorate de sodium) (U.S. EPA, 1983; CMA, 1989; FDA des États-Unis, 1990).
Bien que la formation de chlorate soit habituellement associée à l'utilisation de dioxyde de chlore, le traitement de l'eau potable à l'aide d'hypochlorite de sodium (NaOCl) ou d'hypochlorite de calcium (Ca(OCl)2) peut également accroître la concentration de chlorate dans l'eau prête au débit. L'entreposage de longue durée des solutions d'hypochlorite peut aussi entraîner sa décomposition et la formation de chlorate. La formation d'ions chlorate dans une solution d'hypochlorite dépend des conditions d'entreposage comme le pH, la température, la durée de l'entreposage, la présence de rayons ultraviolets, la concentration de la solution et la présence de métaux de transition. Les formes solides d'hypochlorite ne font pas l'objet d'une telle décomposition (Gordon et coll., 1995).
Les ions chlorate et chlorite sont très solubles dans l'eau et on sait qu'on en trouve dans l'eau potable désinfectée avec du dioxyde de chlore. Si on se fie aux propriétés physiques et chimiques des ions chlorate et chlorite, et compte tenu de l'absence de données sur leur présence dans les aliments, l'air, le sol et les produits de consommation, on croit que le chlorate et le chlorite ne sont pas présents en quantité significative dans l'environnement, outre dans l'eau potable. On présume donc que l'eau potable constitue la principale source d'exposition au chlorate et au chlorite pour la population, et on a déterminé qu'un facteur d'allocation de 80 % était le plus approprié pour évaluer le risque que représente l'eau potable.
6.0 Méthodes d'analyse
L'analyse du chlorite, du chlorate et du dioxyde de chlore dans l'eau se fait généralement au moyen de techniques spectrophotométriques ou colorimétriques, électrochimiques et chromatographiques. Les principales méthodes d'analyse du chlorite et du chlorate dans l'eau sont résumées à l'annexe A. Lorsque c'est possible, les limites de détection de la méthode, les limites de quantification, les interférences possibles et les remarques pertinentes au sujet de l'application, dont les interférences, sont aussi indiquées. Toutefois, on renvoie les utilisateurs à la description complète de la méthode pour avoir des renseignements détaillés sur les interférences précises et la portée de l'application des méthodes.
6.1 Chlorite - Méthodes approuvées par la U.S. EPA
L'Environmental Protection Agency des États-Unis (U.S. EPA) approuve les trois méthodes suivantes pour déterminer la quantité de chlorite dans l'eau potable : 1) la méthode EPA 300.0, Revision 2.1 (U.S. EPA, 1999b), 2) la méthode EPA 300.1, Revision 1.0 (U.S. EPA, 1998), et 3) la méthode normalisée 4500-ClO2 E (APHA et coll., 1998).
Dans la méthode EPA 300.0, Revision 2.1, méthode chromatographique, un petit volume d'échantillon est introduit dans un appareil de chromatographie par échange d'ions. Les anions d'intérêt sont séparés et mesurés à l'aide d'un système constitué d'une colonne de garde, d'une colonne analytique, d'un suppresseur et d'un détecteur conductimétrique ou d'un détecteur UV/visible. La méthode EPA 300.1, Revision 1.0 propose la même procédure que la méthode EPA 300.0, sauf que la colonne analytique y est de qualité supérieure, ce qui offre une sensibilité d'analyse accrue.
La méthode normalisée 4500-ClO2 E est une méthode ampérométrique de dosage du dioxyde de chlore, du chlore, du chlorite et du chlorate dans l'eau, qui se fait par l'intermédiaire de titrages successifs à différents pH avec de l'oxyde de phénylarsine ou du thiosulfate de sodium comme titrant. L'utilisation de bromure de potassium comme réducteur à une étape du titrage permet de réduire au minimum l'oxydation, par l'oxygène à pH faible, de l'iodure en iode, tandis que l'addition de cristaux d'iodure de potassium permet d'empêcher la réduction de l'iodate en iode. Aux faibles pH nécessaires pour la détermination des quantités de chlorite et de chlorate, cette méthode est sensible aux interférences du manganèse, du cuivre et des nitrites. La méthode ampérométrique est utile quand on veut connaître les différentes fractions (chlore, dioxyde de chlore, chlorite et chlorate) présentes dans un échantillon d'eau. On l'utilise généralement pour les analyses quotidiennes effectuées dans les services publics; elle exige toutefois un équipement spécialisé et des compétences poussées en analyse. Il faut savoir que le calcul final de la concentration de chlorite est sujet à de grandes erreurs cumulatives avec cette méthode. (Gates, 1998).
6.2 Chlorate - Méthodes approuvées par la U.S. EPA
La U.S. EPA approuve deux méthodes pour déterminer la quantité de chlorate dans l'eau potable : 1) la méthode EPA 300.0, Revision 2.1 (U.S. EPA, 1999b) et 2) la méthode EPA 300.1, Revision 1.0 (U.S. EPA, 1998). Ces méthodes sont brièvement décrites à la section 6.1.
6.3 Dioxyde de chlore - Méthodes approuvées par la U.S. EPA
La U.S. EPA approuve les trois méthodes suivantes pour déterminer la quantité de dioxyde de chlore dans l'eau potable : 1) la méthode normalisée 4500-ClO2 C (APHA et coll., 2005), 2) la méthode normalisée 4500-ClO2 D (APHA et coll., 1998) et 3) la méthode normalisée 4500-ClO2 E (APHA et coll., 2005). On peut utiliser cette méthode pour la surveillance quotidienne de la dose de dioxyde de chlore à l'usine de traitement.
La méthode normalisée 4500-ClO2 C est une méthode ampérométrique approuvée pour le dosage du dioxyde de chlore, mais elle peut aussi servir à déterminer le dosage du chlorite, du chlore et des chloramines dans l'eau. L'analyse se fait par l'intermédiaire de titrages successifs à différents pH avec de l'oxyde de phénylarsine comme titrant. Cette méthode est sensible aux interférences de l'iodure, du bromure, du ferricyanure, du chromate, du bichromate et des ions ferreux.
La méthode normalisée 4500-ClO2 D est une extension de la méthode colorimétrique N,N-diethyl-p-phenylenediamine (DPD) qui sert à déterminer le dosage de chlore libre. Lorsqu'on l'utilise pour déterminer la quantité de dioxyde de chlore, le chlore libre est supprimé par l'ajout de glycine avant l'ajout du réactif DPD.
La méthode normalisée4500-ClO2 E est décrite à la section 6.1; on peut l'utiliser pour la surveillance quotidienne de la dose de dioxyde de chlore à l'usine de traitement.
6.4 Autres méthodes
La U.S. EPA propose aussi trois autres méthodes pour déterminer le dosage du chlorite et/ou du chlorate dans l'eau potable, méthodes qui n'ont pas encore été approuvées : 1) la méthode EPA 317.0, Revision 2.0 (U.S. EPA, 2001a), 2) la méthode EPA 326.0, Revision 1.0 (U.S. EPA, 2002) et 3) la méthode EPA 327.0, Revision 1.0 (U.S. EPA, 2003b).
Les méthodes EPA 317.0, Revision 2.0 et 317.0, Revision 1.0 sont des techniques chromatographiques de rechange qui permettent de déterminer le dosage de chlorite et de chlorate en utilisant un système de réaction post-colonne pour accroître la spécificité et la sensibilité de la méthode.
La méthode EPA 327.0, Revision 1.0 (U.S. EPA, 2003b) est une méthode spectrophotométrique UV/visible qui sert à mesurer le dioxyde de chlore et le chlorite présents dans l'eau potable. Elle fait appel à l'utilisation de l'indicateur coloré vert de Lissamine B. Il s'agit d'une autre méthode simple pour déterminer les concentrations de chlorite habituellement retrouvées dans l'eau des usines de traitement. On ajoute le réactif vert de Lissamine B/peroxydase de raifort à l'échantillon d'eau : la peroxydase de raifort aide à catalyser la transformation du chlorite en dioxyde de chlore. Le dioxyde de chlore oxyde ensuite le colorant vert de Lissamine B et en réduit l'absorbance, laquelle est proportionnelle à la concentration originale de chlorite. On mesure cette absorbance au moyen d'un spectrophotomètre à 633 nm.
La technique d'analyse par injection dans un flux peut également être utilisée pour la détection du dioxyde de chlore, du chlorite et du chlorate dans l'eau potable (Novatek, 1991). Cette méthode est toutefois sujette à l'interférence des chloramines et d'autres oxydants présents dans l'eau potable. Elle peut être automatisée et procurer un mode de surveillance en ligne. Wang et coll. (2001) ont modifié la méthode pour analyser de faibles concentrations de dioxyde de chlore en présence de chlore et autres anions. La limite de détection de la méthode est de 20 µg/L.
Parmi les autres méthodes mises au point pour analyser le dioxyde de chlore, citons les nécessaires d'analyse DPD. Ces nécessaires d'analyse sont fondés sur la méthode colorimétrique de la méthode normalisée 4500-ClO2 G et servent généralement pour déterminer sur le terrain la quantité de dioxyde de chlore résiduel. Ces méthodes s'appliquent à des concentrations supérieures à 0,1 mg/L de dioxyde de chlore. Elles sont sujettes à l'interférence du manganèse et autres oxydants chlorés.
Une méthode utilisant le C.I. mordant violet 5 (ACVK) (Masschelein 1989) pour déterminer le dosage de dioxyde de chlore est fondée sur l'oxydation et la décoloration subséquente de l'ACVK (violet d'alizarine 3R, indice de coloration 6170) à 548 nm, et fait appel à un spectrophotomètre.
La méthode de titrage iodométrique (méthode APHA 4500-ClO2 B) permet d'obtenir une mesure très précise du dioxyde de chlore (APHA et coll. 2005). Toutefois, elle ne permet pas la spéciation des diverses espèces de chlore; par conséquent, la méthode est plus utile pour les solutions de dioxyde de chlore standard (APHA et coll. 2005).
7.0 Techniques de traitement
7.1 Traitement à l'échelle municipale
Jusqu'à 70 % du dioxyde de chlore ajouté peut former ultérieurement du chlorite (Volk et coll., 2002). Comme le chlorite réagit avec le chlore libre pour former l'ion chlorate, très difficile à supprimer (Gallagher et coll., 1994; U.S. EPA, 1999a), deux stratégies sont recommandées pour réduire au minimum la formation initiale de chlorite : 1) le contrôle des procédés de traitement afin de réduire la quantité de désinfectant requise; et 2) le contrôle des procédés de production de dioxyde de chlore de manière à ce que le produit soit le plus pur possible. Actuellement, les générateurs de dioxyde de chlore que l'on trouve sur le marché peuvent être classifiés d'une façon générale comme des systèmes à base de chlorite ou de chlorate, ou comme des systèmes électrochimiques.
7.1.1 Chlorite
Il existe actuellement quatre techniques de traitement visant à contrôler la concentration de l'ion chlorite dans l'eau potable à l'échelle municipale : 1) réglage du générateur de dioxyde de chlore; 2) utilisation de charbon actif; 3) utilisation de réducteurs à base de fer; et 4) utilisation de réducteurs à base de soufre. Ces techniques sont décrites ci-dessous.
- Réglage du générateur de dioxyde de chlore. La conception et le rendement du générateur de dioxyde de chlore ont un impact considérable sur la quantité d'ions chlorite formée durant la production de dioxyde de chlore. La précision de l'opération (« réglage »), l'entretien adéquat du générateur et la technique employée avec l'appareil influent grandement sur l'efficacité de la production de dioxyde de chlore de même que sur le taux de production de chlorite et d'autres sous-produits indésirables, comme le chlorate, le peroxyde d'hydrogène et le perchlorate, et sur leur introduction dans l'eau avec la dose de dioxyde de chlore. La production sur place de dioxyde de chlore peut être difficile sur le plan technique pour l'opérateur. Des fuites mineures peuvent entraîner la formation de matière cristalline blanche dangereuse qui peut s'enflammer si elle entre en contact avec de puissants réducteurs ou si elle est soumise à des étincelles, à la flamme, à la friction ou à la compression. Tout déversement doit être immédiatement lavé à grande eau (Gates, 1998).
Un générateur convenablement réglé se caractérise par un dioxyde de chlore d'une pureté élevée, et donc par une présence réduite des contaminants qui peuvent pénétrer le réseau de distribution et accroître la concentration totale de chlorate et de chlorite (Gordon, 2001). Il importe de bien équilibrer et contrôler les générateurs de ClO2 pour éviter la formation et la pénétration d'impuretés comme les ions chlorate, les ions perchlorate et le chlore (Gordon, 2001). - Charbon actif. Le charbon actif permet d'éliminer les ions chlorite par un processus d'adsorption et de réduction chimique. On signale des problèmes de fuites précoces avec les filtres à charbon actif granulé (CAG), lorsque tous les sites d'adsorption ont été comblés, peutêtre par des composés organiques concurrents comme des matières organiques naturelles, et qu'il ne reste que le mécanisme de réduction qui soit fonctionnel. Le rendement des filtres à CAG pour l'élimination du chlorite est également compliqué par l'oxydation du chlorite en chlorate, qui peut survenir en présence de chlore libre dans l'eau d'alimentation. Une courte durée de vie du lit de drainage, des coûts d'exploitation élevés et la possibilité de formation de chlorate rendent l'utilisation du CAG peu pratique pour l'élimination de chlorite à l'échelle municipale (Dixon et Lee, 1991).
- Agents réducteurs à base de fer. Le fer ferreux (Fe2+) réduit chimiquement l'ion chlorite, diminuant ainsi sa concentration dans l'eau. L'ion chlorate ne se forme que si le pH diminue à moins de 5, ce qui peut survenir aux points d'application des réducteurs acides, comme le chlorure ferreux(II). L'utilisation adéquate de ces réducteurs, le mélange rapide et/ou l'ajustement du pH à 7 (neutre) peuvent aider à éviter la formation de microrégions à faible pH et la formation subséquente de chlorate (Griese et coll., 1992). Lorsque le pH dépasse 7, le chlorite réagit avec le fer ferreux pour former de l'hydroxyde ferrique insoluble, lequel peut aider à clarifier l'eau lorsqu'il est utilisé conjointement avec la filtration pour capter les solides (Iatrou et Knocke, 1992). Toutefois, si le pH dépasse 9, les taux élevés d'oxygène dissous et de carbone organique dissous bloquent l'efficacité du fer ferreux; il faut alors des doses plus importantes de composés ferreux pour obtenir une élimination adéquate du chlorite. L'utilisation de doses de fer ferreux de 3,5-4,0 mg/mg de chlorite permet l'élimination efficace de l'ion chlorite (Hurst et Knocke, 1997). Tout chlorite résiduel réagira avec le chlore pour former du chlorate, et doit donc être éliminé avant la désinfection secondaire au chlore. Le fer ferreux, si on l'utilise pour supprimer le chlorite et qu'on en utilise plus qu'il n'est nécessaire, peut nuire à l'efficacité de la désinfection secondaire (U.S. EPA, 2001b). Le fer ferreux utilisé pour réduire le chlorite peut donner lieu à des niveaux de fer dans l'eau traitée qui excèdent la recommandation esthétique de 0,3 mg/L.
- Agents réducteurs à base de soufre. Les substances à base de soufre comme le sulfite, le métabisulfite et le thiosulfate réduisent le dioxyde de chlore et l'ion chlorite; elles permettent donc de réduire la concentration de ces composés dans l'eau. Bien que des études en banc d'essai aient démontré que le thiosulfate est efficace pour réduire le dioxyde de chlore et le chlorite, et que ces réactions de réduction ne génèrent pas de chlorate comme sous-produit, elles requièrent un temps de contact assez long et sont fonction du pH, ce qui limite leur efficacité à l'échelle municipale (Griese et coll., 1991). En présence d'oxygène dissous, le sulfite et le métabisulfite réduisent le chlorite en ion chlorure et en ion chlorate; comme ce dernier est indésirable, l'utilisation du sulfite et du métabisulfite n'est pas recommandée pour éliminer le chlorite dans l'eau potable.
7.1.2 Chlorate
Le dioxyde de chlore et les ions chlorite réagiront avec le chlore libre pour former des ions chlorates. Une fois les ions chlorate présents dans l'eau, ils sont très persistants et très difficiles à supprimer (Gallagher et coll., 1994; U.S. EPA, 1999a). Du chlorate peut également se former pendant la génération du dioxyde de chlore. Il n'existe à l'heure actuelle aucun traitement pratique et économique pour éliminer l'ion chlorate, une fois qu'il a été formé dans l'eau potable. Jusqu'à 35 % du chlorate retrouvé dans un réseau de distribution peut être attribué au rendement (réglage) du générateur de dioxyde de chlore. Si l'ion chlorite est présent dans l'eau et n'est pas éliminé, il réagira avec le chlore libre introduit dans l'eau pour produire des ions chlorate et chlorure. Pour limiter la formation de ce sous-produit persistant, il est important de réduire au minimum sa production dans le processus de génération de dioxyde de chlore et d'éliminer les ions chlorite avant de procéder à la postchloration (Gallagher et coll., 1994).
Les conditions d'entreposage, comme le pH, la température, la durée d'entreposage, la présence de lumière ultraviolette, la concentration de la solution et la présence de métaux de transition, influent sur la formation d'ions chlorate dans les solutions d'hypochlorite (Gordon et coll., 1995). Les solutions d'hypochlorite doivent :
- contenir moins de 1500 mg de chlorate/L;
- avoir un pH supérieur à 12;
- être utilisées dans un délai relativement court après la livraison (dans les trois mois);
- être entreposées dans des endroits frais et sec où la température ne dépasse pas 30 °C, à l'abri de la lumière du soleil;
- contenir moins de 0,08 mg/L de métaux de transition (AWWA, 2004).
Les fabricants peuvent produire des agents de blanchiment ayant une concentration initiale de chlorate plus faible; les services publics devraient préciser qu'ils veulent des solutions d'hypochlorite dans lesquelles la concentration de chlorate est la plus faible possible, pour garantir le respect des normes en matière de chlorate dans l'eau traitée.
7.2 Traitement à l'échelle résidentielle
En général, il n'est pas recommandé d'utiliser des dispositifs pour traiter davantage l'eau provenant des usines de traitement municipales. Comme le dioxyde de chlore n'est pas utilisé pour désinfecter des systèmes individuels d'eau potable, il est peu probable de retrouver du chlorite ou du chlorate dans les sources d'eau souterraines ou les eaux de surface individuelles. Certains appareils de traitement à l'échelle résidentielle peuvent éliminer le chlorite, mais à l'heure actuelle, aucun n'est certifié à cette fin.
Santé Canada ne recommande pas de marques particulières de dispositifs de traitement de l'eau potable, mais conseille vivement aux consommateurs de n'utiliser que les dispositifs certifiés par un organisme de certification accrédité comme étant conformes aux normes appropriées du NSF International (NSF) et de l'American National Standards Institute (ANSI). Ces normes visent à protéger l'eau potable en aidant à garantir l'innocuité des matériaux et l'efficacité des produits qui entrent en contact avec l'eau potable. Les organismes de certification garantissent qu'un produit ou service est conforme aux normes en vigueur. Au Canada, le Conseil canadien des normes (CCN) a accrédité un certain nombre d'organismes qu'il autorise ainsi à certifier les dispositifs de traitement de l'eau potable qui satisfont aux normes susmentionnées du NSF et de l'ANSI :
- Canadian Standards Association International;
- NSF International;
- Water Quality Association;
- Underwriters Laboratories Inc.;
- Quality Auditing Institute and
- International Association of Plumbing & Mechanical Officials.
(Une liste à jour des organismes de certification accrédités peut être obtenue auprès du CCN).
7.2.1 Chlorite
Lorsque l'on considère la technique de traitement de l'eau au point d'entrée ou aux points d'utilisation à l'échelle résidentielle, les options pour éliminer le chlorite se limitent à l'adsorption au moyen d'un filtre de CAG. Cependant, à l'heure actuelle, aucun dispositif de traitement de l'eau potable n'est certifié pour éliminer spécifiquement l'ion chlorite. Le NSF a élaboré plusieurs normes pour les dispositifs de traitement de l'eau à l'échelle résidentielle conçus pour réduire la concentration de divers types de contaminants dans l'eau potable. À l'heure actuelle, cependant, aucune des normes du NSF ne porte sur le chlorite.
Des recherches sont actuellement en cours dans les secteurs public et privé pour vérifier et adopter des méthodes efficaces pour réduire la concentration du chlorite dans l'eau potable. Comme les produits faisant appel à la technique de l'adsorption (filtres à charbon actif) perdent de leur efficacité avec l'usage, il faut les remplacer après un certain temps. Les consommateurs doivent vérifier la longévité prévue du matériel d'adsorption de leur dispositif de traitement selon les recommandations du fabricant et en faire l'entretien en conséquence, car les études montrent que les fuites surviennent plus tôt pour les chlorites que pour les autres composés chlorés.
7.2.2 Chlorate
À l'heure actuelle, il n'existe aucune technique connue à l'échelle résidentielle pour éliminer l'ion chlorate de l'eau du robinet une fois qu'il a été formé (Gallagher et coll., 1994).
8.0 Cinétique et métabolisme
8.1 Absorption et métabolisme
L'ion chlorite, l'ion chlorate et le dioxyde de chlore sont rapidement absorbés dans le tube digestif chez le rat. Aucun organe en particulier ne semble concentrer sélectivement la dose à la suite d'une exposition à des ions chlorite ou chlorate, ou au dioxyde de chlore (Abdel-Rahman, 1985). Chez le singe, après l'ingestion, le dioxyde de chlore a rapidement été converti en ion chlorure et, dans une moindre mesure, en chlorite et en chlorate (Abdel-Rahman et coll., 1982a; Bercz et coll., 1982). Chez le rat, il a été transformé principalement en chlorure, une petite quantité demeurant sous forme de chlorite inchangé.
Chez le rat, après l'administration de dioxyde de chlore par voie orale, les concentrations dans le plasma ont culminé après 1 heure. La demi-vie plasmatique était de 44 heures (NRC des États-Unis, 1982).
8.2 Distribution
La distribution des ions chlorite et chlorate marqués au 36Cl, à raison de 10 mg/L et 5 mg/L de solution respectivement, a été étudiée chez des rats après une administration par voie orale. Les quantités observées dans divers liquides et tissus (en tant que pourcentage de la dose initiale) après 72 heures étaient les suivantes pour l'ion chlorite : 0,55 % dans le plasma; 0,63 % dans les globules concentrés; 0,64 % dans le sang entier; et un total d'environ 3 % dans les reins, les poumons, l'estomac, le duodénum, l'iléon, le foie, la rate, la moelle osseuse, les testicules, la peau et la carcasse. Les concentrations les plus élevées (0,4 % chacune) ont été retrouvées dans les testicules, la peau, l'estomac et les poumons. Le chlorate était distribué comme suit dans les tissus : 0,68 % dans le plasma; 0,23 % dans les globules concentrés; 0,57 % dans le sang entier; et un total de 3,6 % dans les reins, les poumons, l'estomac, le duodénum, l'iléon, le foie, la rate, la moelle osseuse, les testicules, la peau et la carcasse. Les concentrations les plus élevées (0,4 % chacune) ont été retrouvées dans les reins, les poumons, l'estomac, les testicules et la peau (Abdel-Rahman et coll., 1982a).
8.3 Excrétion
Après 72 heures, les rats avaient excrété dans l'urine 30 % de la dose orale de dioxyde de chlore marqué au 36Cl. Environ 27 % du chlore marqué était sous forme de chlorure et 3 % sous forme d'ion chlorite. Un autre 9 % a été excrété dans les matières fécales. Pour ce qui est du chlorite marqué administré aux rats par voie orale, 40 % a été excrété dans l'urine sous forme de chlorure après 72 heures. Aucun ion chlorate n'a été observé après l'ingestion de dioxyde de chlore ou de chlorite. Lorsque l'ion chlorate marqué a été administré aux rats par voie orale, environ 38 % du matériel marqué a été excrété dans l'urine, dont 20 % sous forme de chlorure, 4 % sous forme d'ion chlorite et 13 % sous forme d'ion chlorate. Les auteurs ont conclu qu'une fois ces substances ingérées, elles sont rapidement dégradées en chlorure dans l'organisme. Par conséquent, l'exposition chronique à ces substances par l'eau potable n'est pas considérée comme préoccupante sur le plan de la toxicité (Abdel-Rahman et coll., 1980b, 1984a, 1984b). L'excrétion du chlorite, du chlorate et du dioxyde de chlore se fait principalement dans l'urine, de plus petites quantités étant excrétées dans les matières fécales (Abdel-Rahman et coll., 1982a, 1985).
9.0 Effets sur la santé
9.1 Effets chez les êtres humains
9.1.1 Toxicité aiguë et à court terme
Étant donné que le chlorate est utilisé comme herbicide, un grand nombre de cas d'intoxication à cette substance ont été signalés (NRC des États-Unis, 1987). Les symptômes comprennent entre autres les suivants : méthémoglobinémie, anurie, douleurs abdominales et insuffisance rénale. On estime que la dose orale létale pour l'humain adulte est aussi faible que 20 g de chlorate de sodium ou de 230 mg de chlorate/kg p.c. (NRC des États-Unis, 1982).
Six doses différentes de dioxyde de chlore (0,1, 1, 5, 10, 18 et 24 mg/L), d'ion chlorite (0,01, 0,1, 0,5, 1,0, 1,8 et 2,4 mg/L) et d'ion chlorate (0,01, 0,1, 0,5, 1,0, 1,8 et 2,4 mg/L) incorporées à l'eau potable ont été administrées à 10 hommes volontaires (Lubbers et al., 1981). Chacun d'eux a ingéré 1000 mL d'eau répartis en deux portions. Cette étude comportait six séquences de trois jours. Un suivi des paramètres chimiques du sérum, de la numération globulaire et de l'analyse d'urine a été effectué. Une variation liée au traitement a été observée en ce qui concerne la valeur moyenne du taux sérique d'acide urique du groupe exposé au dioxyde de chlore, mais selon les auteurs, elle n'a pas eu d'effet physiologique nocif. La dose de dioxyde de chlore la plus élevée à avoir été testée, soit 24 mg/L (environ 0,34 mg/kg p.c. par jour), peut être définie comme la dose sans effet nocif observé (NOAEL). Chez les sujets exposés au chlorite, on a noté un changement des taux sériques moyens d'azote uréique, de créatinine et du rapport azote uréique/créatinine. Chez les sujets exposés au chlorate, on a observé de très légers changements des taux moyens de bilirubine sérique, de fer et de méthémoglobine. Dans les deux cas, les auteurs ont conclu que les variations n'avaient pas d'effets physiologiques néfastes. On a établi la NOAEL à 2,4 mg/L (0,034 mg/kg p.c. par jour) pour l'ion chlorite et l'ion chlorate (Lubbers et coll., 1981).
Les mêmes hommes volontaires ont bu 0,5 L d'eau contenant 5 mg/L de dioxyde de chlore chaque jour pendant environ 12 semaines. Ils ont ensuite été observés pendant huit semaines. Les paramètres sériques, la numération globulaire et l'analyse d'urine sont demeurés normaux, à l'exception d'une légère variation du taux sanguin d'azote uréique. Les auteurs ont conclu que l'effet physiologique ou toxicologique de ce changement était incertain. Cette exposition, équivalente à 0,036 mg/kg p.c par jour., peut être considérée comme la NOAEL (Lubbers et coll., 1981).
Dans une étude prospective menée sur 197 personnes, on a exposé une partie de la population d'un village rural à de l'eau traitée au dioxyde de chlore (contenant entre 0,25 et 1,1 mg/L de dioxyde de chlore et entre 0,45 et 0,91 mg/L de chlore libre) pendant 12 semaines. On n'a observé aucun changement significatif des paramètres hématologiques, de la créatinine sérique et de la bilirubine totale chez ces personnes (CMA, 1989).
9.1.2 Effets sur la reproduction
Durant les années 1988 et 1989, on a mené une étude transversale sur 548 naissances à l'hôpital Galliera de Gênes et 128 naissances à l'hôpital Chiavari de Chiavari (Italie). Les mères des bébés habitaient dans l'une ou l'autre des deux villes (Kanitz et al., 1996). À Gênes, les femmes ont été exposées à de l'eau filtrée désinfectée au dioxyde de chlore (eau de réservoir, de surface et de puits provenant de la rivière Brugneto) et/ou au chlore (réservoir du Val Noci). Les femmes habitant à Chiavari ont utilisé de l'eau de puits non traitée. On a noté la source de l'eau, le type de désinfectant, le revenu familial, l'âge de la mère, si elle fumait ou non, sa consommation d'alcool, son niveau de scolarité et les données relatives au bébé (faible poids à la naissance, naissance avant terme, longueur du corps, circonférence de la tête et présence ou absence d'ictère néonatal). La probabilité d'être atteints d'un ictère néonatal était presque deux fois plus élevée (rapport de cotes de 1,7; 95 %, intervalle de confiance de 1,1 à 3,1) chez les bébés dont la mère avait utilisé de l'eau de surface désinfectée au dioxyde de chlore que chez ceux dont la mère avait utilisé de l'eau de puits non traitée. L'eau de surface traitée au chlore n'a pas produit d'effets similaires. On a relié le fait de mettre au monde un bébé dont la tête et le corps sont plus petits à l'utilisation d'eau de surface désinfectée au chlore ou au dioxyde de chlore. Les risques de mettre au monde un bébé de faible poids (#2 500 g) étaient aussi augmentés dans les cas où la mère avait bu de l'eau désinfectée au chlore ou au dioxyde de chlore, mais l'augmentation n'était pas significative sur le plan statistique. Quoique faibles, les risques d'accouchement avant terme (#37 semaines) liés à la consommation d'eau désinfectée au chlore ou au dioxyde de chlore étaient augmentés, mais l'augmentation n'était pas significative. Cette étude suggère l'existence possible de risques associés à la consommation d'eau de surface désinfectée au chlore ou au dioxyde de chlore, mais les résultats doivent être interprétés avec beaucoup de prudence. En effet, on n'a recueilli aucune donnée sur la quantité d'eau consommée par les mères (y compris la quantité d'eau embouteillée consommée) ni sur leurs habitudes alimentaires, et la distribution de l'âge des mères n'a pas été prise en considération. En outre, les données relatives aux naissances ne sont peut-être pas complètes, et il pourrait y avoir entre les deux populations d'autres différences que le réseau d'eau potable étudié. Dans cette étude, on a comparé l'exposition aux sources d'eau de surface et d'eau souterraine, mais sans présenter de données quant à d'éventuelles différences qualitatives entre ces eaux. On ne peut tirer aucune conclusion à partir de cette étude, puisque certains des effets notés n'étaient pas significatifs sur le plan statistique et qu'on y a aussi décelé de nombreux biais (Kanitz et coll., 1996).
9.2 Effets chez les animaux de laboratoire et effets in vitro
9.2.1 Toxicité aiguë
Un résumé des études disponibles portant sur la toxicité aiguë du chlorite de sodium, du chlorate de sodium et du dioxyde de chlore est fourni au tableau 3.
| Composé | DL50 orale (mg/kg p.c) | Clinical observations | |||
|---|---|---|---|---|---|
| Rat | Souris | Lapin | Caille | ||
| Chlorite de sodium | 105-165Tableau 3 note de bas de page 1,Tableau 3 note de bas de page 2 | 350Tableau 3 note de bas de page 1 | non disponible | 300Tableau 3 note de bas de page 1 | non disponible |
| Chlorate de sodium | 1200Tableau 3 note de bas de page 3 | 3600Tableau 3 note de bas de page 1 | 7200Tableau 3 note de bas de page 1 | 6100Tableau 3 note de bas de page 1 | non disponible |
| Dioxyde de chlore | 292Tableau 3 note de bas de page 4 | non disponible | non disponible | non disponible | Somnolence et stimulation respiratoire |
|
Notes de bas de page du Tableau 3
|
|||||
Des effets aiguës ont aussi été observés une heure après que des chiens aient ingéré entre 0,5 et 2 g de chlorate de sodium/kg p.c., les chiens ont vomi et le taux de méthémoglobine dans leur sang a augmenté. De l'ion chlorate a été observé dans le sang et l'urine de ces animaux. Les chiens ayant reçu la plus forte dose (entre 1 et 2 g/kg p.c.) ont souffert de tachycardie et de dépression. Ils sont également devenus cyanosés et sont morts entre 12 et 24 heures après l'administration de la substance (Sheahan et coll., 1971).
9.2.2 Exposition de courte durée
9.2.2.1 Chlorite
Dans une étude plus récente, des doses de 0, 10, 25 ou 80 mg de chlorite de sodium/kg p.c. par jour (équivalant à 0, 7,4, 18,6 ou 59,7 mg de chlorite/kg p.c. par jour) ont été administrées quotidiennement par gavage à des rats Crl: CD (SD) BR mâles et femelles (15 rats de chaque sexe par groupe) pendant 13 semaines. La plus forte dose a entraîné la mort d'un certain nombre de rats (Harrington et coll., 1995). Elle a également donné lieu à des changements morphologiques dans les érythrocytes et à des diminutions importantes du taux d'hémoglobine. On a observé une diminution non significative du nombre d'érythrocytes à une dose de 10 mg/kg p.c. par jour chez les rats mâles, et des diminutions plus importantes à la dose de 80 mg/kg p.c. par jour. Aux doses de 25 mg/kg p.c. par jour et plus, le nombre d'érythrocytes a diminué de façon importante chez les femelles. Comme on pouvait s'y attendre en cas d'hémolyse, le poids de la rate a augmenté. Aux doses de 25 et de 80 mg/kg p.c. par jour, le poids des glandes surrénales a augmenté chez les femelles, tandis que chez les mâles, des changements statistiquement significatifs n'ont été observés qu'avec la dose de 80 mg/kg p.c. par jour. L'examen histopathologique des tissus à l'autopsie a révélé une hyperplasie de l'épithélium malpighien, une hyperkératose, de l'ulcération, une inflammation chronique et un oedème dans l'estomac chez 7 des 15 mâles et 8 des 15 femelles qui avaient reçu la dose de 80 mg/kg p.c. par jour. Cet effet a été observé chez seulement 2 des 15 animaux ayant reçu la dose de 25 mg/kg p.c. par jour, tandis qu'il était complètement absent à la dose de 10 mg/kg p.c. par jour. Dans cette étude, la NOAEL était de 7,4 mg de chlorite/kg p.c. par jour, compte tenu des lésions à l'estomac et de l'augmentation du poids de la rate et des glandes surrénales (Harrington et coll., 1995).
Dans une étude sur les dommages oxydatifs causés aux érythrocytes, les rats ont été exposés à l'ion chlorite ajouté à leur eau potable à raison de 0, 1, 5, 10, 25 ou 50 mg/kg p.c. par jour pendant 30 à 90 jours. Les paramètres hématologiques ont été surveillés. Les trois doses les plus élevées ont causé une anémie transitoire. Après 90 jours, la concentration de glutathion dans les érythrocytes des animaux recevant 10 mg/kg p.c. par jour était de 40 % inférieure à celle observée chez les animaux du groupe témoin, et d'au moins 20 % inférieure chez les rats recevant 5 mg/kg p.c. par jour. La NOAEL était de 1 mg/kg p.c. par jour (Heffernan et coll., 1979). Cette étude a permis d'obtenir des renseignements utiles sur la toxicité du chlorite, mais elle ne convient pas comme fondement pour l'élaboration d'une recommandation en matière d'eau potable : les effets observés étaient transitoires et n'apparaissaient qu'à deux doses.
Des souris A/J et C57L/J ont été exposées au chlorite de sodium ajouté à leur eau potable à raison de 0,15, 1,5 ou 15 mg/kg p.c. par jour environ, pendant 30 jours. À la dose de 15 mg/kg p.c. par jour, on a observé des augmentations de la glucose-6-phosphate déshydrogénase, du volume globulaire moyen et de la fragilité osmotique; cependant, aucune augmentation n'a été constatée à de plus faibles doses. Il y avait une différence importante entre les souches en ce qui concerne la glucose-6-phosphate déshydrogénase et la fragilité osmotique (Moore et Calabrese, 1982). Pour cette étude, la NOAEL était de 1,5 mg/kg p.c. par jour, compte tenu de la variation des paramètres sanguins.
Des singes verts d'Afrique (cinq mâles et cinq femelles) ont servi à l'étude des effets thyroïdiens du chlorite administré pendant 30 à 60 jours en tant que chlorite de sodium à raison de 0, 25, 50, 100, 200 and 400 mg/L (équivalent à 0, 4, 7,5, 15, 30 ou 58,4 mg/kg p.c. par jour) (NRC des États-Unis, 1987; Bercz, 1992). Le chlorite n'a pas causé de baisse de l'activité thyroïdienne. Il a entraîné un stress oxydatif lié à la dose, qui s'est traduit par une diminution du taux d'hémoglobine et du nombre d'érythrocytes ainsi que par une augmentation du taux de méthémoglobine, ce qui est interprété comme étant un stress oxydatif sur l'hématopoïèse. Il y a eu une augmentation statistiquement significative, liée à la dose, du taux d'alanine aminotransaminase, mais les auteurs indiquent que les variations n'étaient pas importantes sur le plan clinique. Les paramètres sanguins qui avaient montré des variations pendant l'étude sont revenus à la normale avant la fin de la période d'administration du chlorite, indiquant une fois encore que le chlorite n'avait entraîné que des variations bénignes sur le plan clinique. On n'a pu établir dans cette étude ni la NOAEL ni la LOAEL. Cependant, d'après une analyse réalisée par l'EPA des États-Unis (2000), les données n'ont pas été présentées d'une façon qui permette de déterminer les doses seuils pour l'apparition de ces effets.
Dans une autre étude, on a administré à des rats mâles et des poulets Leghorn blancs du chlorite dans l'eau potable à raison de 0, 4,28, 42,8 et 428 mg/kg p.c. par jour environ (poulets), et de 0, 3,42, 34,2 et 342 mg/kg p.c. par jour (rats) pendant 4 mois. On a observé chez les deux espèces et pour tous les groupes une diminution de la fragilité osmotique des érythrocytes et un effet sur leur morphologie (Abdel-Rahman et coll., 1980a)
9.2.2.2 Chlorate
On n'a observé aucun signe de toxicité, à l'exception d'une légère anémie à la dose la plus élevée, chez des rats auxquels on avait administré par voie orale (gavage) du chlorate de sodium à raison de 0, 10, 100 ou 1000 mg/kg p.c. par jour pendant 13 semaines (Bio/Dynamics, Inc., 1987b).
Des chiens Beagle (quatre chiens de chaque sexe par dose) ont reçu, par gavage, du chlorate de sodium à raison de 0, 10, 60 ou 360 mg/kg p.c. par jour pendant trois mois. Les variations sur le plan hématologique se sont limitées à une légère élévation du taux de méthémoglobine chez les animaux ayant reçu une dose élevée; mais comme cette élévation se situait dans les limites normales, on a estimé qu'elle n'était pas liée au traitement. Aucun autre effet n'a été observé. La NOAEL était de 360 mg/kg p.c. par jour chez les chiens (Bio/Dynamics, Inc., 1987a).
Des rats Sprague-Dawley (14 animaux de chaque sexe par dose) ont été exposés par gavage au chlorate de sodium à raison de 0, 10, 100 ou 1000 mg/kg p.c. par jour pendant une période ne dépassant pas trois mois. À la dose la plus élevée, les variations hématologiques indicatives d'une anémie comprenaient une diminution du nombre d'érythrocytes, du taux d'hémoglobine et du volume érythrocytaire (hématocrite). Aucun autre effet n'a été observé. La NOAEL était de 100 mg/kg p.c. par jour (Bio/Dynamics, Inc., 1987b).
Dans une étude qui s'est déroulée sur une période de 90 jours, du chlorate a été ajouté à l'eau potable de rats Sprague-Dawley à raison de 0, 30, 100 ou 510 mg/kg p.c. par jour chez les mâles et de 0, 42, 164 ou 800 mg/kg p.c. par jour chez les femelles. Chez les deux sexes, le gain pondéral a été nettement freiné à la dose la plus élevée. En général, cet effet est allé de pair avec une réduction du poids des organes (sauf pour le cerveau et les testicules). On a observé une certaine diminution du taux d'hémoglobine, de l'hématocrite et du nombre d'érythrocytes à cette même dose. Aux doses modérées ainsi qu'aux doses élevées, des lésions de l'hypophyse (vacuolisation dans le cytoplasme des cellules du lobe antérieur) et une déplétion de la colloïde de la glande thyroïde ont été constatées chez les deux sexes. La NOAEL était de 30 mg/kg p.c. par jour (McCauley et coll., 1995).
Des singes verts d'Afrique (cinq mâles et cinq femelles) ont servi à l'étude des effets thyroïdiens du chlorate administré en tant que chlorate de sodium à raison de 0, 25, 50, 100, 200 ou 400 mg/L (0, 4, 7,5, 15, 30 ou 58,4 mg/kg p.c. par jour) pendant 30 à 60 jours (Bercz, 1992; PISC, 2000). Le chlorate n'a pas entraîné de baisse de l'activité thyroïdienne. Contrairement au chlorite, il n'a pas causé de stress oxydatif lié à la dose. On n'a pu établir dans cette étude ni la NOAEL ni la LOAEL.
Dans une autre étude, des rats mâles et des poulets Leghorn blancs ont reçu du chlorate ajouté à leur eau potable à raison de 4,28, 42,8 et 428 mg/kg p.c. par jour (poulets) et de 3,42, 34,2 et 342 mg/kg p.c. par jour (rats) pendant 4 mois. On a observé chez les deux espèces et pour tous les groupes une diminution de la fragilité osmotique des érythrocytes et un effet sur leur morphologie (Abdel-Rahman et coll., 1980a).
9.2.2.3 Dioxyde de chlore
De l'eau potable contenant du dioxyde de chlore à raison de 0, 1,5 ou 15 mg/kg p.c. par jour a été donnée à des souris (10 animaux par dose) pendant 30 jours sans qu'il n'y ait eu d'effet apparent sur les paramètres sanguins. La NOAEL était de 15 mg/kg p.c. par jour (Moore et Calabrese, 1982).
Douze singes verts d'Afrique ont été exposés à de l'eau contenant du dioxyde de chlore à raison de 0, 30, 100 ou 200 mg/L (0, 3,5, 9,5 ou 11 mg/kg p.c. par jour) selon un protocole à dose croissante (Bercz, 1992). Chacune des doses a été administrée pendant une période de 30 à 60 jours, sauf pour le groupe d'exposition élevée qui a été arrêté après 1 semaine à cause de signes de déshydratation et d'un excès d'espèces azotées dans le sang suite à une insuffisance rénale. On a observé une légère baisse de l'activité thyroïdienne (diminution du taux de thyroxine) chez les singes qui avaient reçu 100 mg/L. Aucun autre effet n'a été constaté (Bercz et coll., 1982). Une étude réalisée dans le cadre du Programme international sur la sécurité des substances chimiques (PISC, 2002) a révélé que les deux concentrations les plus élevées équivalaient à environ 9 mg/kg p.c. par jour, en raison d'une baisse de l'appétibilité ayant entraîné une réduction du volume d'eau ingéré. La baisse de l'activité thyroïdienne ne concordait pas avec les quelques données disponibles. Dans l'ensemble, à la concentration de 200 mg/L, il était clair qu'il y a eu irritation de la cavité buccale, ce qui a causé des problèmes d'appétibilité. À la concentration de 100 mg/L (équivalant à environ 9 mg/kg p.c. par jour) ou moins, on n'a constaté aucun effet précis chez ces primates pendant une période d'exposition de 8 semaines (PISC, 2002).
Dans une étude d'une durée de 8 semaines, six singes ont reçu de l'eau potable contenant du dioxyde de chlore à raison de 4,6 mg/kg p.c. par jour. Le taux de thyroxine a diminué au bout de 4 semaines de ce traitement, mais il est remonté après les 4 semaines suivantes. Dans le cadre de la même étude, de l'eau potable renfermant du dioxyde de chlore a été administrée à des rats mâles (12 rats par dose) à raison de 0, 10 ou 20 mg/kg p.c. par jour. On a observé une diminution du taux de thyroxine liée à la dose après 8 semaines de ce traitement; il n'y a pas eu de remontée. La NOAEL dans cette étude était de 10 mg/kg p.c. par jour (Harrington et coll., 1986). D'après PISC (2002), il n'y a aucun profil constant en ce qui a trait aux effets sur la thyroïde.
Des rats Sprague-Dawley (10 rats de chaque sexe par dose) ont reçu du dioxyde de chlore administré dans l'eau potable pendant 90 jours à raison de 0, 2, 4, 6 ou 12 mg/kg p.c. par jour pour les mâles et de 0, 2, 5, 8 ou 15 mg/kg p.c. par jour pour les femelles. La consommation d'eau a diminué chez les deux sexes aux trois doses les plus élevées, probablement en raison de l'appétibilité réduite de l'eau. On a constaté une diminution de la consommation d'aliments chez les mâles recevant la dose la plus élevée. L'hyperplasie des cellules caliciformes s'est accrue de façon significative dans les cornets nasaux des femelles qui recevaient la dose de 8 ou de 15 mg/kg p.c. par jour, et dans ceux des mâles de tous les groupes traités. On a observé une inflammation de la fosse nasale chez les mâles recevant la dose de 2 mg/kg p.c. par jour, et chez les deux sexes aux doses plus élevées. Cependant, les auteurs ont signalé que ces lésions étaient probablement dues à une inhalation des vapeurs de dioxyde de chlore s'échappant de l'ouverture du tube de la bouteille d'eau potable ou au dégagement de vapeurs après que l'animal eut bu, plutôt qu'à l'ingestion même de l'eau potable. Les auteurs ont déterminé que la dose la plus faible (2 mg/kg p.c. par jour) correspondait à la LOAEL (Daniel et coll., 1990).
Dans une autre étude, on a administré à des rats mâles et des poulets Leghorn blancs du dioxyde de chlore dans l'eau potable à raison d'environ 0, 4,28, 42,8 et 428 mg/kg p.c. par jour (poulets) et de 0, 3,42, 34,2 et 342 mg/kg p.c. par jour (rats) pendant 4 mois. On a observé chez les deux espèces et pour tous les groupes traités une diminution de la fragilité osmotique des érythrocytes et un effet sur leur morphologie (Abdel-Rahman et coll., 1980a).
9.2.3 Exposition de longue durée et cancérogénicité
Une étude d'un an a été effectuée chez le rat pour examiner les effets du dioxyde de chlore et de ses métabolites sur la formation de chloroforme, l'incorporation de la H-thymidine dans les organes et l'activité des enzymes microsomales hépatiques. Des rats Sprague-Dawley mâles ont reçu de l'eau bidistillée contenant du dioxyde de chlore à une concentration de 0, 1, 10 ou 100 mg/L (correspondant à 0, 0,1, 1 et 10 mg/kg p.c. par jour), du chlorite à une concentration de 1 ou 10 mg/L (correspondant à 0,1 et 1 mg/kg p.c. par jour) ou du chlorate à une concentration de 1 ou 10 mg/L (correspondant à 0,1 et 1 mg/kg p.c. par jour) pendant un an. Le taux de chloroforme sanguin a diminué dans le groupe des animaux ayant reçu du dioxyde de chlore pendant une période de 2, 10 et 12 mois. Par ailleurs, dans le groupe des animaux ayant reçu du chlorite et celui ayant reçu du chlorate, on a constaté des diminutions comparables du taux de chloroforme sanguin après un an de traitement. Cependant, aucune quantité significative de chloroforme n'a été observée dans le foie, les reins, la rate, les testicules et le cerveau des animaux des groupes traités au cours de la même période (Suh et coll., 1984).
Des rats Sprague-Dawley (quatre mâles par groupe) ont reçu des concentrations différentes de dioxyde de chlore (0, 1, 10, 100 ou 1000 mg/L), d'ion chlorite (10 ou 100 mg/L) ou d'ion chlorate (10 ou 100 mg/L) dans de l'eau bidistillée, à raison de 20 heures par jour, 7 jours par semaine, pendant un an (Abdel-Rahman et coll., 1984a). Les animaux du groupe témoin ont reçu de l'eau bidistillée uniquement. On a administré, par voie intrapéritonéale, de la méthyl-1',3'-3H-thymidine à raison de 0,5 µCi/g p.c. aux rats ayant reçu 10 et 100 mg /L de dioxyde de chlore, 10 et 100 mg/L de chlorite et 10 mg/L de chlorate dans leur eau potable quotidienne. On a prélevé des noyaux de cellules du foie, des reins, des testicules et de la muqueuse de l'intestin grêle pour déterminer le degré d'incorporation de la thymidine. On a observé, chez tous les groupes traités, une diminution de la fragilité osmotique des érythrocytes. Après 2 mois de traitement, le taux de glutathion sanguin a diminué de façon significative chez tous les animaux traités, sauf chez ceux ayant reçu 100 mg/L de dioxyde de chlore. Après 4 mois, le taux de glutathion n'a diminué que chez les animaux ayant reçu 1 et 10 mg/L de dioxyde de chlore de même que chez ceux ayant reçu 100 mg /L de chlorite. Après 9 mois, on a observé que le taux de glutathion avait diminué chez les animaux ayant reçu du chlorite et ceux ayant reçu du chlorate, tandis qu'il avait augmenté de façon significative chez ceux ayant reçu 100 mg/L de dioxyde de chlore. On a constaté des changements dans le compartiment des cellules sanguines après 7 mois de traitement, mais pas avant. Le nombre d'érythrocytes a augmenté de façon significative dans le groupe ayant reçu 100 mg/L de dioxyde de chlore, tandis qu'il a diminué dans le groupe ayant reçu 10 mg/L de chlorate. L'hématocrite a augmenté dans les groupes ayant reçu 100 et 1000 mg/L de dioxyde de chlore et diminué dans celui ayant reçu 10 mg/L de chlorate. La teneur corpusculaire moyenne en hémoglobine a augmenté dans le groupe ayant reçu 10 mg/L de dioxyde de chlore et dans les groupes ayant reçu 10 et 100 mg/L de chlorite. Après 9 mois, le nombre d'érythrocytes, l'hématocrite et le taux d'hémoglobine avaient diminué chez tous les animaux traités. Chez le rat, les trois substances ont inhibé l'incorporation de 3H-thymidine dans le noyau des cellules des testicules, tandis que le chlorite a inhibé son incorporation dans le foie, et le dioxyde de chlore (100 mg/L), son incorporation dans les reins. L'incorporation de 3H-thymidine dans le noyau des cellules de l'intestin grêle a augmenté aux doses de 10 et 100 mg/L de dioxyde de chlore et de 10 mg/L de chlorite. Les trois substances ont entraîné une perte pondérale chez le rat dans tous les groupes après 10 et 11 mois de traitement (Abdel-Rahman et coll., 1984a).
9.2.3.1 Chlorite
Les effets du chlorite de sodium dans l'eau potable à des concentrations de 0, 1, 2, 4, 8, 100 ou 1000 mg/L (équivalent à des doses de 0, 0,09, 0,18, 0,35, 0,7, 9,3 ou 81 mg/kg p.c. par jour) sur la survie et les lésions pathologiques observées à l'autopsie de rats albinos (sept rats de chaque sexe par dose) ont été observés dans le cadre d'une étude qui s'est déroulée sur une période de deux ans. Aucune dose n'a eu d'effet significatif sur la durée de vie des animaux. Aucun effet n'a été observé chez les animaux exposés au chlorite à raison de 0,7 mg/kg p.c. par jour ou moins. Chez les animaux exposés à des doses de 9,3 ou 81 mg/kg p.c. par jour, on a constaté des lésions rénales liées au traitement; l'auteur a conclu à un effet non spécifique du sel (Haag, 1949). Dans une revue effectuée par TERA (1998), des effets nocifs sur les reins ont été observés à des doses de 8,3 ou plus, toutefois les auteurs indiquent que ceux-ci ne sont pas spécifiques, et que en se basant sur les effets observés sur le rein, on a établi la NOAEL à 0,7 mg/kg p.c. par jour. Selon la revue de TERA (1998), l'utilité de cette étude est limitée, parce que le nombre d'animaux examinés par groupe était insuffisant et que l'autopsie n'a été pratiquée que sur un petit nombre d'animaux. De plus, l'auteur n'a pas évalué adéquatement les paramètres plus sensibles.
Dans une étude sur la cancérogénicité dans le cadre de laquelle on a administré du chlorite de sodium à des souris B6C3F1 (50 souris de chaque sexe par dose) à des concentrations de 0, 250 ou 500 mg/L (équivalant à des doses d'ion chlorite de 0, 36 ou 71 mg/kg p.c. par jour) dans l'eau potable pendant 80 semaines, on n'a constaté aucune augmentation significative du nombre de tumeurs par rapport au groupe témoin, à une dose d'ion chlorite de 36 mg/kg p.c. par jour. Bien qu'on ait constaté chez les souris mâles exposées au chlorite une augmentation de l'incidence de tumeurs dans les poumons et le foie, celle-ci se situait dans les limites des valeurs observées chez les souris du groupe témoin. Dans le cas des tumeurs hépatiques, les augmentations ne présentaient pas de tendance dose-réponse typique, et des augmentations significatives n'ont été observées que dans le cas de tumeurs bénignes (Kurokawa et coll., 1986). Cette étude n'a pas porté sur toute la durée de vie des animaux et n'est pas considérée conforme aux lignes directrices de l'Organisation de coopération et de développement économiques (OCDE).
On a administré à des rats Sprague-Dawley (quatre mâles par groupe) de l'ion chlorite dans l'eau potable à raison de 0, 1 ou 10 mg/kg p.c. par jour pendant 12 mois (7 jours par semaine), la dose étant calculée à partir des valeurs de référence de 0,523 kg pour le poids corporel et de 0,062 L/jour pour le volume quotidien d'eau potable ingérée (Couri et Abdel-Rahman, 1980; Abdel-Rahman et coll., 1984b). On a observé des diminutions significatives du gain pondéral à la dose de 10 mg/kg p.c. par jour, quel que soit le moment de vérification; le gain pondéral a également diminué aux 10e et 11e mois de traitement dans le groupe ayant reçu la dose de 1 mg/kg p.c. par jour. Aucun changement n'a été constaté au niveau du nombre d'érythrocytes, de l'hématocrite ou du taux d'hémoglobine. La teneur corpusculaire moyenne en hémoglobine a augmenté aux deux doses de 1 et 10 mg/kg p.c. par jour après 7 mois d'exposition au chlorite, mais pas après 9 mois de traitement. La fragilité osmotique a diminué de façon significative aux deux doses après 7 et 9 mois de traitement. La synthèse d'ADN (mesurée par le taux d'incorporation de la 3H-thymidine) a diminué aux doses de 1 et 10 mg/kg p.c. par jour dans le foie et les testicules, ainsi qu'à la dose de 10 mg/kg p.c. par jour dans la muqueuse intestinale, et elle a augmenté à la dose de 1 mg/kg p.c. par jour dans la muqueuse intestinale. L'activité de la glutathion réductase dans le sang a augmenté de façon significative aux doses de 1 et 10 mg/kg p.c. par jour après 6 mois d'exposition, et diminué à la dose de 1 mg/kg p.c. par jour après 12 mois. L'activité de la glutathion peroxydase dans le sang n'a pas varié après 6 mois de traitement, mais a diminué dans les deux groupes après 12 mois. On a observé des diminutions significatives du taux de glutathion sanguin dans les deux groupes. L'activité de la catalase dans le sang a diminué après 6 mois de traitement aux doses de 1 et 10 mg/kg p.c. par jour, et augmenté après 12 mois de traitement à la dose de 1 mg/kg p.c. par jour. L'absence d'un profil dose-réponse constant, le petit nombre d'animaux et la faible ampleur des effets ont compliqué l'interprétation des résultats (Couri et Abdel-Rahman, 1980; Abdel-Rahman et coll., 1984b).
9.2.3.2 Chlorate
Il n'existe aucune étude sur le pouvoir cancérogène du chlorate administré seul. On a évalué le chlorate de sodium et le chlorate de potassium comme agents promoteurs de tumeurs rénales chez des rats F344 dont les tumeurs avaient été induites avec de la N-éthyl-N-hydroxyéthyl-nitrosamine. Le chlorate de sodium (mais pas le chlorate de potassium) a causé une augmentation du nombre de tumeurs rénales, mais l'effet n'était pas statistiquement significatif en raison du petit nombre d'animaux utilisé (Kurokawa et coll., 1986).
On a administré à des rats Sprague-Dawley (quatre mâles par groupe) de l'ion chlorate dans l'eau potable à raison de 0, 1 ou 10 mg/kg p.c. par jour pendant 12 mois (7 jours par semaine), la dose étant calculée à partir des valeurs de référence de 0,523 kg pour le poids corporel et de 0,062 L/jour pour le volume d'eau potable ingérée. Après 6 mois de traitement, la glutathion peroxydase a augmenté dans le sang uniquement à la dose de 10 mg/kg p.c. par jour. On a constaté une diminution de l'activité de la catalase à la dose de 10 mg/kg p.c. par jour. Après 6 et 12 mois de traitement, on a observé une augmentation significative du taux de glutathion sanguin aux deux doses évaluées comparativement au groupe témoin (Couri et Abdel-Rahman, 1980).
9.2.3.3 Dioxyde de chlore
On a administré à des rats Sprague-Dawley (quatre mâles par groupe) du dioxyde de chlore dans l'eau potable à raison de 0, 0,1, 1, 10 ou 100 mg/kg p.c. par jour pendant 12 mois (7 jours par semaine), la dose étant calculée à partir des valeurs de référence de 0,523 kg pour le poids corporel et de 0,062 L/jour pour le volume d'eau potable ingérée. Après 12 mois de traitement, le taux érythrocytaire de glutathion réductase chez les rats traités était semblable à celui du groupe témoin; par contre, le taux érythrocytaire de glutathion peroxydase a augmenté de façon significative aux doses de 10 et 100 mg/kg p.c. par jour. La teneur en glutathion des érythrocytes a diminué de façon significative après 6 mois de traitement aux doses de 0,1, 1 et 10 mg/kg p.c. par jour, et après 12 mois à la dose de 100 mg/kg p.c. par jour. Le taux de catalase des érythrocytes a augmenté après 6 et 12 mois de traitement dans le groupe ayant reçu la dose de 100 mg/kg p.c. par jour et diminué après 6 mois de traitement dans le groupe ayant reçu les doses de 0,1 et 1 mg/kg p.c. par jour (Couri et Abdel-Rahman, 1980).
On a également administré à des souris suisses du dioxyde de chlore dans l'eau potable à raison de 0, 0,18, 1,8, 18 ou 180 mg/kg p.c. par jour pendant 12 mois (7 jours par semaine). Après 12 mois de traitement, le taux de glutathion peroxydase a diminué à la dose de 18 mg/kg p.c. par jour et augmenté à celle de 180 mg/kg p.c. par jour, et le taux de glutathion a diminué aux doses de 1,8 et 18 mg/kg p.c. par jour. Le taux de catalase a augmenté aux doses de 1,8, 18 et 180 mg/kg p.c. par jour après 12 mois de traitement. L'absence de constance dans la relation entre la dose et l'ampleur des variations liées au glutathion rend l'interprétation des résultats de cette étude particulièrement difficile. De plus, on ne sait pas si ces effets sont significatifs sur le plan biologique. Par conséquent, on n'a pu déterminer ni la NOAEL ni la LOAEL (Couri et Abdel-Rahman, 1980).
On a administré à des poulets Leghorn blancs mâles (quatre par groupe) pendant 10 mois (7 jours par semaine) du dioxyde de chlore dans l'eau potable à des concentrations de 0, 10, 100 ou 1000 mg/L. On a observé une augmentation de 70 % de l'activité de la glutathion réductase à toutes les concentrations. L'activité de la glutathion peroxydase a diminué de façon significative à la concentration la plus élevée; cependant, dans le même groupe, l'activité de la catalase a augmenté. L'activité de la glutathion peroxydase a varié à l'inverse de la concentration de dioxyde de chlore dans l'eau potable (Couri et Abdel-Rahman, 1980).
On a administré à des rats (sept rats de chaque sexe par dose) du dioxyde de chlore dans l'eau potable pour obtenir une concentration de 0, 0,5, 1, 5, 10 ou 100 mg/L (équivalant à des doses de 0, 0,07, 0,13, 0,7, 1,3 et 13 mg/kg p.c. par jour) pendant 2 ans. À la dose la plus élevée, le taux de survie a considérablement diminué chez les deux sexes, et la longévité moyenne a été réduite comparativement à celle des animaux du groupe témoin. On n'a observé aucune corrélation entre le traitement et les résultats histopathologiques (Haag, 1949). On a établi la NOAEL à 1,3 mg/kg p.c. par jour, mais selon TERA (1998), cette étude de 1949 comporte d'importantes lacunes.
9.2.4 Mutagénicité/génotoxicité
9.2.4.1 Chlorite
Le chlorite de sodium a entraîné une augmentation du nombre de révertants chez la souche Salmonella typhimurium TA100 tant en présence qu'en l'absence d'une activation métabolique (Ishidate et coll., 1984). On n'a observé aucune anomalie chromosomique ni avec le test du micronoyau ni avec l'essai cytogénétique réalisés sur des cellules de moelle osseuse de souris après l'administration de chlorite par gavage (Meier et coll., 1985).
On a obtenu un résultat positif à un test du micronoyau réalisé sur des cellules de la moelle osseuse de souris ddY mâles après une injection intrapéritonéale unique de chlorite de sodium à raison de 0, 7,5, 15, 30 ou 60 mg/kg p.c. On a observé une réponse positive sur le plan statistique aux doses de 15 et 30 mg/kg p.c. seulement : 0,38 % et 1,05 % (dans l'ordre) comparativement à 0,18 % pour le groupe témoin (Hayashi et coll., 1988).
9.2.4.2 Chlorate
On sait depuis longtemps que le chlorate permet de sélectionner les mutants d'Aspergillus nidulans déficients en nitrate réductase (Cove, 1976). Cependant, on a aussi démontré l'effet mutagène du chlorate chez Chlamydomonas reinhardtii et Rhodobacter capsulatus. Le chlorate n'a pas induit de mutations chez la souche Salmonella typhimurium BA-13. Pour distinguer entre les cellules ayant véritablement subi une mutation à l'égard de la nitrate réductase et celles faisant simplement l'objet d'une sélection, on a incubé les cellules dans un milieu de culture ne contenant pas d'azote; l'absence d'azote empêche la division cellulaire pendant la période de traitement. Dans le cas de C. reinhardtii, on a constaté des augmentations significatives du nombre de cellules mutantes à des concentrations de 4-5 mmol/L et plus (Prieto et Fernandez, 1993).
On n'a observé aucune anomalie chromosomique ni avec le test du micronoyau ni avec l'essai cytogénétique réalisés sur des cellules de moelle osseuse de souris après l'administration de chlorate par gavage (Ishidate et coll., 1984).
9.2.4.3 Dioxyde de chlore
Dans des conditions in vitro, le dioxyde de chlore a un pouvoir mutagène chez la souche Salmonella typhimurium TA100 en l'absence d'un système d'activation métabolique (S9) (Ishidate et coll., 1984). Chez des souris mâles à qui l'on avait administré du dioxyde de chlore par gavage, on n'a observé aucune anomalie de la tête des spermatozoïdes (Meier et coll., 1985). Dans un essai cytogénétique réalisé in vitro sans activation métabolique (-S9), des cellules ovariennes de hamster chinois (CHO) ont été traitées avec du dioxyde de chlore à 0,2 % dans une solution saline tamponnée au phosphate contenant les concentrations suivantes de dioxyde de chlore : 0, 2,5, 5, 10, 15, 30 ou 60 µg/mL. On a répété l'expérience avec des concentrations de 0, 6, 13, 25, 50 ou 75 µg/mL et une activation métabolique (+S9). Dans la première expérience (sans activation métabolique), on a observé une cytotoxicité à la concentration de 60 µg/mL et une absence de cellules mitotiques à la concentration de 30 µg/mL. Aux concentrations de 2,5-15 µg/mL, on a constaté des augmentations statistiquement significatives liées à la dose du nombre de cellules en métaphase présentant des anomalies chromosomiques. Dans la seconde expérience (avec activation métabolique), on a constaté une cytotoxicité et une absence de cellules mitotiques à la concentration de 75 µg/mL. On a décelé une augmentation statistiquement significative du nombre de cellules en métaphase présentant des anomalies chromosomiques à la concentration de 50 µg/mL (Ivett et Myhr, 1986). Dans une épreuve de mutation directe sur des lymphomes de souris (avec des cellules L5178Y TK+/-), on a traité les cellules avec du dioxyde de chlore à une concentration variant de 0 à 65 µg/mL dans une solution saline tamponnée au phosphate avec et sans activation métabolique (S9). Sans S9, on a observé une toxicité marquée à la concentration la plus élevée, soit 37 µg/mL. La croissance relative aux concentrations de 15 et 24 µg/mL était de 13-18 %. On a aussi constaté une augmentation de la fréquence des mutants liée à la dose. Avec S9, on a constaté une toxicité marquée à la concentration la plus élevée, soit 65 µg/mL, et une augmentation de la fréquence des mutants liée à la dose, indiquant un résultat positif avec et sans activation métabolique dans ce système d'essai (Cifone et Myhr, 1986).
Dans des études in vivo, on n'a observé aucune anomalie chromosomique ni avec le test du micronoyau ni avec l'essai cytogénétique réalisés sur des cellules de moelle osseuse de souris après l'administration de dioxyde de chlore par gavage (Meier et coll., 1985). On a administré à des souris CD-1 (cinq de chaque sexe) une injection intrapéritonéale unique de dioxyde de chlore à raison de 0, 2, 5 ou 15 mg/kg p.c. dans le cadre d'un essai cytogénétique sur des cellules de la moelle osseuse. On a analysé les cellules de moelle osseuse en vue de déceler des anomalies chromosomiques après 6, 24 et 48 heures. On n'a obtenu aucun effet précis sur l'indice mitotique, mais deux souris mâles ayant reçu une dose d'environ 15 mg/kg p.c. sont mortes, et on a remarqué d'autres signes de toxicité à la dose la plus élevée. Par comparaison avec le groupe témoin, il n'y a eu aucune augmentation de la fréquence des anomalies chromosomiques chez les animaux traités, quel que soit le moment du sacrifice (Ivett et Myhr, 1984). Des groupes de cinq souris ICR mâles ont reçu une injection intrapéritonéale unique d'environ 0, 9, 21, 28 ou 39 mg/kg p.c. de dioxyde de chlore aqueux. Après une injection sous-cutanée de bromodésoxyuridine et 26 heures après l'administration de dioxyde de chlore, on a évalué le taux d'échange de chromatides soeurs dans environ 25 cellules de moelle osseuse en métaphase de chaque animal. Tous les animaux manifestaient de l'hyperactivité après l'administration de dioxyde de chlore. Dans l'ensemble, il n'y a pas eu d'augmentation significative du taux d'échange de chromatides soeurs dans aucun des groupes ayant reçu du dioxyde de chlore (Ivett et Myhr, 1984).
Dans un test de létalité dominante dans le cadre duquel on a administré à des rats jusqu'à 20 mg de dioxyde de chlore aqueux/kg p.c. par voie intrapéritonéale, on n'a observé aucun effet mutagène sur les cellules germinales des mâles (Moore et Myhr, 1984).
9.2.5 Toxicité pour la reproduction et le développement
9.2.5.1 Chlorite
Dans une série de trois expériences, on a administré à des rats mâles (12 rats par dose) du chlorite de sodium dans l'eau potable pendant 66-76 jours, à des concentrations de chlorite de 0, 0,075, 0,75, 7,5 ou 27 mg/kg p.c. par jour. Aucune anomalie liée à la substance n'a été observée à l'examen histopathologique de l'appareil reproducteur. Aux deux doses les plus élevées, on a constaté chez les spermatozoïdes des anomalies morphologiques et une diminution de la motilité, mais aucun effet sur les spermatozoïdes n'a été observé à la dose de 0,75 mg/kg p.c. par jour, dose qu'on peut établir comme la NOAEL (Carlton et coll., 1987).
Dans une autre partie de la même étude, on a accouplé des rats mâles avec des femelles ayant reçu du chlorite à raison de 0, 0,075, 0,75 ou 7,5 mg/kg p.c. par jour. Les mâles ont été exposés au chlorite pendant 56 jours et les femelles pendant une période commençant 14 jours avant l'accouplement et se terminant à la fin de la période d'accouplement de 10 jours. Les femelles ont également été exposées au chlorite pendant toute la gestation et la période de lactation jusqu'au sevrage des petits, 21 jours après la naissance. On n'a constaté aucun effet nocif sur le taux de conception, le nombre de petits par portée, le premier jour d'ouverture des yeux ou le jour de l'ouverture vaginale. On a observé des diminutions de la concentration sanguine de triiodothyronine et de thyroxine chez les petits, mâles et femelles, de 21 jours et de 40 jours exposés à 7,5 mg/kg p.c. par jour. On a établi la NOAEL à 0,75 mg/kg p.c. par jour, d'après les effets sur la reproduction (Carlton et coll., 1987).
La CMA (1996) et Gill et coll. (2000) ont effectué une étude portant sur deux générations, dans laquelle des rats Sprague-Dawley (30 rats de chaque sexe par dose) ont reçu de l'eau potable contenant du chlorite de sodium à une concentration de 0, 35, 70 ou 300 mg/L pendant 10 semaines, puis ils ont été appariés pour l'accouplement. Les mâles ont été exposés au chlorite de sodium pendant toute la période d'accouplement, puis ils ont été sacrifiés. Les femelles ont été exposées au chlorite de sodium pendant les périodes d'accouplement, de gestation et de lactation, jusqu'à l'autopsie réalisée après le sevrage des petits. On a choisi, pour constituer la génération F1, 25 mâles et femelles de chacune des 25 portées sevrées en premier dans un groupe traité. On a soumis les petits de la F1 au même régime de traitement que leurs parents. À l'âge d'environ 14 semaines, les petits ont été accouplés pour engendrer la génération F2a. En raison du nombre réduit de portées de la génération F1-F2a ayant reçu une dose de 70 mg/L , les rats F1 ont été accouplés de nouveau après le sevrage des petits de la génération F2a pour produire la génération F2b. Les doses de chlorite correspondantes, telles que calculées par la EPA et raportées dans la revue de TERA (1998), pour les animaux de la F0 étaient de 0, 3,0, 5,6 ou 20,0 mg/kg p.c. par jour pour les mâles, et de 0, 3,8, 7,5 ou 28,6 mg/kg p.c. par jour, pour les femelles. Pour les animaux de la F1, les doses étaient de 0, 2,9, 5,9 ou 22,7 mg/kg p.c. par jour pour les mâles, et de 0, 3,8, 7,9 ou 28,6 mg/kg p.c. par jour pour les femelles. On a observé des diminutions dans le volume d'eau ingérée, la quantité de nourriture consommée et le gain pondéral chez les animaux des deux sexes de toutes les générations à divers moments au cours de l'expérience, principalement aux doses de 70 et 300 mg/L; on a attribué ces effets à un manque d'appétibilité de l'eau. À une concentration de 300 mg/L, on a constaté une réduction du taux de survie chez les petits, un plus faible poids corporel à la naissance et pendant toute la période de lactation chez les animaux des générations F1 et F2, un plus faible poids du thymus et de la rate dans les deux générations, une diminution de l'incidence des petits à manifester un réflexe de redressement normal, des retards dans le développement sexuel des mâles et des femelles des générations F1 et F2, et des valeurs plus basses des paramètres érythrocytaires chez les animaux de la F1. On a décelé des réductions significatives du poids du foie (en valeurs absolue et relative) chez les femelles de la F0 de même que chez les mâles et les femelles de la F1, une réduction du poids absolu du cerveau chez les animaux des générations F1 et F2 ainsi qu'une diminution de la réponse maximale de sursaut à un stimulus sonore au jour 24 après la naissance, mais pas au jour 60 après la naissance dans les groupes ayant reçu des doses de 70 et 300 mg/L. On a constaté de légères variations dans les paramètres érythrocytaires chez les animaux de la génération F1 exposés à des concentrations de 35 et 70 mg/L, mais ces variations semblent se situer à l'intérieur des limites normales, d'après les données de référence. Dans cette étude, la NOAEL était de 35 mg/L (2,9 mg/kg p.c. par jour) et la LOAEL, de 70 mg/L (5,9 mg/kg p.c. par jour), d'après la baisse de l'amplitude du sursaut à un stimulus sonore, la diminution du poids absolu du cerveau chez les animaux des générations F1 et F2 et les variations du poids du foie chez les animaux des deux générations.
Deux groupes de souris A/J femelles ont été traitées avec du chlorite de sodium dans l'eau potable à des doses de 0 et 100 ppm (équivalent à 0 et 22 mg/kg p.c. par jour - selon la U.S. EPA, 2000) du jour 1 de la gestation et pendant toute la lactation; 21 femelles du groupe témoin et 12 exposée ont eu des portées. Les taux de conception étaient de 56% pour le groupe témoin et de 39% pour les souris traitées. Les poids corporels des petits au sevrage étaient réduits (14% sous ceux du groupe témoin) chez les souris traitées (Moore et Calabrese, 1982), établissant une LOAEL de 22 mg/kg p.c. par jour (la seule dose utilisée) (U.S. EPA, 2000).
On a examiné des foetus provenant de rates Sprague-Dawley exposées à l'ion chlorite dans l'eau potable à une concentration de 1 ou 10 mg/L pendant une période commençant 2,5 mois avant l'accouplement et se terminant à la fin de la gestation. On a observé une augmentation de l'incidence des anomalies aux deux concentrations; cependant, comme les groupes traités étaient restreints (6-9 femelles par groupe), on a estimé que les effets n'étaient pas statistiquement significatifs (Suh et coll., 1983).
On a administré à des lapins blancs de Nouvelle-Zélande (16 lapins par groupe) de l'ion chlorite dans l'eau potable à des concentrations de 0, 10, 26 ou 40 mg/kg p.c. par jour, du jour 7 au jour 19 de la gestation, pour étudier la toxicité de ce composé sur le développement. On a fait l'autopsie des animaux au jour 28. On a constaté une baisse de la consommation de nourriture aux deux doses les plus élevées, et une diminution de l'ingestion d'eau à toutes les doses, et plus particulièrement aux deux doses les plus élevées. La moyenne des poids foetaux était également légèrement plus faible aux deux doses les plus élevées, avec une incidence légèrement plus élevée de l'ossification incomplète de certains os. Aucune augmentation des anomalies liée à la dose n'a été établie. De légères anomalies du squelette ont été observées à mesure qu'on augmentait la concentration de chlorite dans l'eau et que diminuait la consommation de nourriture par les mères (Harrington et coll., 1995).
Des groupes de rats femelles Sprague-Dawley (12 femelles par groupe) ont été exposés pendant 9 semaines à de l'eau potable renfermant du chlorite à raison de 0, 3 ou 6 mg/kg p.c. par jour, le traitement débutant 10 jours avant l'accouplement avec des mâles non exposés et se poursuivant jusqu'à ce que les petits soient sacrifiés, 35-42 jours après la conception. Du jour 31 au jour 42 après la conception, on a évalué le développement de l'activité exploratoire des petits de six portées dans chaque groupe traité. On a observé une diminution constante et significative du comportement exploratoire chez les petits dont la mère a été exposée à une dose de 6 mg/kg p.c. par jour aux jours 36-39 après la conception, mais pas au jour 40. L'activité exploratoire était comparable entre les groupes traités et le groupe témoin après le 39e jour suivant la conception. On a établi la NOAEL à 3 mg/kg p.c. par jour et la LOAEL à 6 mg/kg p.c. par jour, d'après les effets du chlorite sur le comportement (Mobley et coll., 1990).
9.2.5.2 Chlorate
Il n'existe aucune étude portant sur la toxicité du chlorate sur le plan de la reproduction ou de l'embryogenèse. On a administré à des rates CD en gestation du chlorate de sodium par gavage à raison de 0, 10, 100 ou 1000 mg/kg p.c. par jour, du jour 6 au jour 15 de la gestation. Il n'y a eu aucun décès parmi les mères ayant reçu du chlorate ni aucun effet lié au traitement sur le gain pondéral de la mère, sa consommation de nourriture, les observations cliniques, le nombre d'implantations ou les observations macroscopiques à l'autopsie chez ces femelles. L'examen des foetus au jour 20 n'a révélé aucun effet sur le poids des foetus ou sur la proportion des sexes, et aucune anomalie externe, des viscères ou du squelette n'a été décelée. Dans cette étude, on a établi la NOAEL à 1000 mg/kg p.c. par jour chez le rat d'après les effets sur le développement (Bio/Dynamics, Inc., 1987c).
9.2.5.3 Dioxyde de chlore
On a effectué une étude portant sur une génération dans le cadre de laquelle on a administré à des rats Long-Evans mâles (12 mâles par groupe) du dioxyde de chlore par gavage à raison de 0, 2,5, 5 ou 10 mg/kg p.c. par jour pendant 56 jours, avant et pendant la période d'accouplement avec des femelles (24 femelles par groupe) ayant reçu du dioxyde de chlore pendant 14 jours avant l'accouplement et tout au long de la gestation. Les données sur la fertilité n'étaient pas significativement différentes d'un groupe à l'autre. On n'a constaté aucun modification liée à la dose des paramètres relatifs aux spermatozoïdes (c'est-à-dire, concentration, motilité, mouvement vers l'avant ou morphologie). Les taux d'hormones thyroïdiennes ont changé de façon significative, mais pas de manière constante. La seule différence significative consistait en une diminution du poids vaginal chez les rejetons femelles dont les mères avaient reçu la dose de 10 mg/kg p.c. par jour. On a établi la NOAEL à 5 mg/kg p.c. par jour d'après ce changement (Carlton et coll., 1991).
On a évalué le potentiel neurotoxique du dioxyde de chlore sur le développement au cours d'une étude dans laquelle cette substance a été administrée par intubation orale à des rejetons mâles et femelles de rats Sprague-Dawley à raison de 14 mg/kg p.c. par jour pendant les jours 1 à 20 après la naissance. La prolifération des cellules du cerveau antérieur a diminué au jour 35 après la naissance, et il y a eu des diminutions du poids et de la teneur en protéines du cerveau antérieur aux jours 21 et 35 après la naissance. La prolifération cellulaire dans le cervelet et le bulbe olfactif était comparable à celle des groupes témoins (non traités), comme l'étaient la migration et l'agrégation des neurones dans le cortex cérébral. L'examen histopathologique du cerveau antérieur, du cervelet et du tronc cérébral n'a pas révélé de lésion ou de changement dans ces tissus. Dans cette étude, on a établi la LOAEL à 14 mg/kg p.c. par jour, la seule dose évaluée (Toth et coll., 1990).
Des rats femelles Sprague-Dawley ont reçu du dioxyde de chlore dans leur eau potable à raison d'environ 0, 0,07, 0,7 ou 7 mg/kg p.c. par jour (Suh et coll., 1983). Après environ 10 semaines de ce traitement, on a accouplé les femelles avec des mâles non exposés au dioxyde de chlore et on a continué à leur administrer du dioxyde de chlore pendant toute leur gestation. Au jour 20 de la gestation, on a sacrifié les mères, retiré et pesé leur utérus et examiné leurs foetus; chez la moitié des foetus, on a recherché des anomalies du squelette et chez l'autre moitié, des anomalies des viscères. On n'a constaté aucun signe clinique de toxicité et aucune mortalité liée à l'exposition au dioxyde de chlore chez les mères. On a relevé une réduction légère, mais statistiquement significative, du gain pondéral chez les mères exposées aux doses de 0,7 et 7 mg/kg p.c. par jour pendant la gestation (une réduction d'environ 14 % par comparaison avec le groupe témoin). On a observé une légère réduction du nombre moyen d'implantations par mère aux deux doses les plus élevées, la réduction étant statistiquement significative à la dose de 7 mg/kg p.c. par jour (10,3 implantations par femelle exposée à la substance contre 12,3 pour le groupe témoin), avec une variation semblable dans le nombre de foetus vivants. Il est possible que cette variation soit liée à la toxicité de ces deux doses pour les mères, puisqu'il y a une légère réduction du gain pondéral chez les mères. La fréquence de portées comprenant des foetus anormaux n'a pas varié avec le traitement : 5/6, 4/6, 6/6 et 7/8 chez les animaux ayant reçu 0, 0,07, 0,7 et 7 mg/kg p.c. par jour, dans l'ordre (Suh et coll., 1983).
On a administré à des rats Sprague-Dawley femelles (13-16 femelles par dose) de l'eau potable contenant du dioxyde de chlore à raison de 0, 1, 3 ou 14 mg/kg p.c. par jour sur une période commençant 2 semaines avant l'accouplement, se poursuivant pendant la gestation et se terminant à la fin de la période de lactation, c'est-à-dire au moment du sevrage des petits, 21 jours après la naissance. On n'a observé aucun effet significatif sur le poids corporel des mères ou des petits à toutes les doses évaluées. On a constaté, au moment du sevrage, une baisse significative du taux sérique de thyroxine et une augmentation du taux sérique de triiodothyronine chez les petits de mères ayant reçu, pendant la gestation, 14 mg/kg p.c. par jour de dioxyde de chlore; ces effets ne se sont pas manifestés chez les mères. Les activités neurocomportementales d'exploration et de locomotion ont diminué chez les petits nés de mères exposées à la dose de 14 mg/kg p.c. par jour, mais pas chez les petits dont la mère a été exposée à la dose de 3 mg/kg p.c. par jour, que l'on a considérée comme la NOAEL (Orme et coll., 1985).
Dans une étude d'accompagnement, on a exposé directement (par gavage) de jeunes rats Sprague-Dawley à du dioxyde de chlore à raison de 14 mg/kg p.c. par jour du jour 5 au jour 20 après la naissance. On a observé une diminution du taux sérique de thyroxine, un retard légèrement plus important et plus uniforme dans le développement sur le plan de l'exploration et de la locomotion, ainsi qu'une diminution du gain pondéral des petits. La diminution du taux sérique de triiodothyronine n'était pas statistiquement significative. On a établi la LOAEL à 14 mg/kg p.c. par jour (la seule dose évaluée), d'après les effets sur le développement des petits et la diminution des taux d'hormones thyroïdiennes (Orme et coll., 1985).
Le nombre de cellules a diminué de façon significative dans le cervelet des petits âgés de 21 jours nés de rates Sprague-Dawley ayant reçu, pendant la gestation et la période de lactation, de l'eau contenant du dioxyde de chlore à raison d'environ 14 mg/kg p.c. par jour. Chez un groupe de 12 petits auxquels on a administré du dioxyde de chlore directement par gavage (14 mg/kg p.c. par jour), on a constaté un nombre réduit de cellules dans le cervelet et le cerveau antérieur au jour 11 après la naissance et une diminution de l'activité volontaire dans une roue d'exercice aux jours 50-60 après la naissance, malgré le fait que le traitement au dioxyde de chlore était terminé depuis le jour 20 après la naissance. Ces données semblent indiquer que le dioxyde de chlore peut influer sur le développement du cerveau des rats nouveau-nés. Dans cette étude, on a établi la LOAEL à 14 mg/kg p.c. par jour (seule dose évaluée) (Taylor et Pfohl, 1985).
10.0 Classification et évaluation
10.1 Chlorite
D'après les données disponibles, on a rangé le chlorite dans le groupe VIA (données insuffisantes pour l'évaluation de la cancérogénicité chez l'humain) (Santé Canada, 1994), ce qui concorde avec les conclusions du CIRC (1991) - Groupe 3, inclassable quant à sa cancérogénicité pour l'humain - et de la U.S. EPA (2005) - inclassable quant à sa cancérogénicité pour l'humain en raison de l'insuffisance de données chez l'humain et l'animal. (U.S. EPA, 1996)
Des études de toxicité subchronique sur des animaux (chats, souris, rats et singes) indiquent que le chlorite et le chlorate causent des changements sur le plan hématologique (fragilité osmotique, stress oxydatif, augmentation du volume globulaire moyen), des lésions à l'estomac et une augmentation du poids de la rate et des glandes surrénales (Heffernan et coll., 1979; Bercz et coll., 1982; Moore et Calabrese, 1982; Bio/Dynamics, Inc., 1987b; Harrington et coll., 1995; McCauley et coll., 1995).
On n'a trouvé aucune étude sur le potentiel cancérogène du chlorite dans la documentation. L'étude de toxicité chronique du chlorite réalisée chez la souris (Kurokawa et coll., 1986) n'ayant pas porté sur la durée de vie entière des animaux, elle n'a pas été considérée adéquate selon les lignes directrices de l'OCDE. Bien que des effets sur le plan hématologique aient été observés dans l'étude effectuée sur le rat (Couri et Abdel-Rahman, 1980; Abdel-Rahman et coll., 1984b), on n'a pas trouvé de relation constante entre la dose et l'effet; le nombre restreint d'animaux et la faible ampleur des effets compliquent l'interprétation des résultats. On a observé de légers changements des paramètres sanguins dans l'étude portant sur deux générations utilisée pour établir la recommandation (CMA, 1996; Gill et al., 2000; TERA, 1998), ce qui concorde avec les effets observés dans les études de toxicité subchronique chez le rat.
Les paramètres neurocomportementaux (baisse de l'amplitude du sursaut au stimulus sonore, diminution du poids du cerveau et de l'activité exploratoire) sont les plus susceptibles d'être touchés par une exposition au chlorite par voie orale (Mobley et coll., 1990; CMA, 1996; Gill et al., 2000). La LOAEL établie pour le chlorite dans l'étude de Mobley et coll. (1990) sur la toxicité de ce composé pour le développement est d'environ 6 mg/kg p.c. par jour. Mobley et coll. (1990) ont également constaté des diminutions importantes dans l'activité exploratoire à la dose de 3 mg/kg p.c. par jour, mais la différence entre l'activité à cette dose et celle du groupe témoin était faible. Néanmoins, la NOAEL du chlorite établie d'après les effets neurocomportementaux mis en évidence dans cette étude est de 3 mg/kg p.c. par jour. Dans l'étude sur deux générations effectuée par CMA (1996), une NOAEL similaire de 2,9 mg/kg p.c. par jour avait été identifiée basée sur la baisse de l'amplitude du sursaut, la diminution du poids absolu du cerveau dans les générations F1 et F2 et des changements dans le poids du foie chez deux générations. Ces deux études susmentionnées ont été réalisées en utilisant l'eau potable comme voie d'exposition, ce qui les rend pertinentes pour la présente évaluation.
L'étude de la CMA (1996) a été choisie pour un certain nombre de raisons. Elle a été réalisée avec un nombre suffisant d'animaux des deux sexes et des doses multiples, de même qu'elle a révélé un éventail d'effets sur de nombreux paramètres. L'effet de la substance est significatif sur le plan de la toxicologie, et le rat est une espèce largement utilisée pour illustrer les effets en matière de reproduction et de développement chez l'humain. Dans cette étude, les rats mâles étaient également exposés au chlorite de sodium pendant la période d'accouplement. Par conséquent, cette étude a permis de procéder à une évaluation plus complète des effets nocifs, ce qui la rend plus apte à être choisie comme étude déterminante pour l'élaboration d'une recommandation. Il existe suffisamment de données pour estimer l'apport quotidien tolérable (AQT) pour le chlorite, d'après cette étude portant sur deux générations où on a établi la NOAEL à 2,9 mg/kg p.c. par jour (CMA, 1996; TERA, 1998). L'AQT a été calculé d'après cette étude comme suit :
L'AQT pour le chlorite
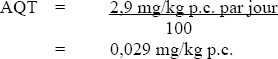
Équivalent textuel de l'équation utilisée pour calculer l'apport quotidien tolérable (AQT) pour le chlorite
L'apport quotidien tolérable pour le chlorite est de 0,029 milligrammes par kilogramme de poids corporel par jour. Cette valeur est calculée en divisant la NOAEL de 2,9 milligrammes par kilogramme de poids corporel par jour par le facteur d'incertitude de 100.
où
- 2,9 mg/kg p.c. par jour est la NOAEL déterminée d'après la baisse de l'amplitude du sursaut, la diminution du poids absolu du cerveau et la variation du poids du foie dans une étude portant sur deux générations de rats;
- 100 est le facteur d'incertitude (×10 pour les variations entre les espèces; ×10 pour les variations à l'intérieur d'une même espèce).
Cet AQT concorde avec les résultats obtenus dans des études portant sur des sujets humains volontaires.
Parce que le chlorite est classé dans le groupe VIA, on calcule la CMA pour le chlorite dans l'eau potable à partir de l'AQT comme suit :
La CMA pour le chlorite dans l'eau potable
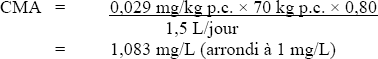
Équivalent textuel de l'équation utilisée pour calculer la concentration maximale acceptable (CMA) pour le chlorite
La concentration maximale acceptable pour le chlorite est de 1,083 milligrammes par litre (arrondie à 1 mg/L). Cette valeur est obtenue en multipliant l'apport quotidien tolérable de 0,029 milligrammes par kilogramme de poids corporel par jour par 70 kilogrammes, soit le poids moyen d'un adulte, puis par 0,8, soit la proportion de l'apport quotidien attribuable à l'eau potable. Le résultat de ces multiplications est ensuite divisé par 1,5 L/jour, qui est la consommation journalière moyenne d'eau potable pour un adulte.
où :
- 0,029 mg/kg p.c. est l'AQT, tel que calculé plus haut;
- 70 kg p.c. est le poids corporel moyen d'un adulte;
- 0,80 est la proportion de la dose quotidienne totale attribuée à l'eau potable (l'eau potable étant la principale source d'exposition);
- 1,5 L/jour est la consommation quotidienne moyenne d'eau potable pour un adulte.
10.2 Chlorate
Il n'existe aucune donnée pour l'évaluation du potentiel cancérogène du chlorate; c'est pourquoi le chlorate a été rangé dans le groupe VIB -- aucune donnée disponible pour l'évaluation de la cancérogénicité pour l'humain (Santé Canada, 1994). Le CIRC n'a pas évalué la cancérogénicité du chlorate. Les études portant sur la toxicité chronique et la cancérogénicité ainsi que celles portant sur le développement et la reproduction n'ont pas fourni suffisamment d'information pour établir une recommandation pour le chlorate.
L'exposition à une dose de chlorate de 0,036 mg/kg p.c. par jour pendant 12 semaines n'a pas causé d'effets nocifs chez les sujets humains volontaires (Lubbers et coll., 1981). Bien que la base de données du chlorate soit moins exhaustive que celle du chlorite, il existe une étude bien menée de 90 jours chez le rat dans laquelle on a établi la NOAEL à 30 mg/kg p.c. par jour, d'après une déplétion de la colloïde de la glande thyroïde observée à la dose élevée suivante de 100 mg/kg p.c. par jour (McCauley et coll., 1995).
On peut donc calculer l'AQT pour le chlorate comme suit :
L'AQT pour le chlorate
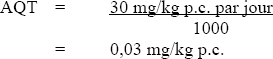
Équivalent textuel de l'équation utilisée pour calculer l'apport quotidien tolérable (AQT) pour le chlorate
L'apport quotidien tolérable pour le chlorate est de 0,03 milligrammes par kilogramme de poids corporel par jour. Cette valeur est calculée en divisant la NOAEL de 30 milligrammes par kilogramme de poids corporel par jour par le facteur d'incertitude de 1000.où :
- 30 mg/kg p.c. par jour est la NOAEL établie d'après la déplétion de la colloïde de la glande thyroïde dans une étude de 90 jours sur le rat;
- 1000 est le facteur d'incertitude (×10 pour les variations entre les espèces; ×10 pour les variations à l'intérieur d'une même espèce; ×10 pour tenir compte de la courte durée de l'étude).
Cet AQT concorde avec les résultats d'études réalisées avec des sujets humains volontaires.
Parce que le chlorate est classé dans le groupe VIB, on calcule la CMA pour le chlorate dans l'eau potable à partir de l'AQT comme suit :
La CMA pour le chlorate dans l'eau potable
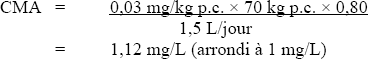
Équivalent textuel de l'équation utilisée pour calculer la concentration maximale acceptable (CMA) pour le chlorate
La concentration maximale acceptable pour le chlorate est de 1,12 milligrammes par litre (arrondi à 1 mg/L). Cette valeur est obtenue en multipliant l'apport quotidien tolérable de 0,03 milligrammes par kilogramme de poids corporel par jour par 70 kilogrammes, soit le poids moyen d'un adulte, puis par 0,8, soit la proportion de l'apport quotidien attribuable à l'eau potable. Le résultat de ces multiplications est ensuite divisé par 1,5 L/jour, qui est la consommation journalière moyenne d'eau potable pour un adulte.
où :
- 0,03 mg/kg p.c. est l'AQT, tel que calculé plus haut;
- 70 kg p.c. est le poids corporel moyen d'un adulte;
- 0,80 est la proportion de la dose quotidienne totale attribuée à l'eau potable (l'eau potable étant la principale source d'exposition);
- 1,5 L/jour représente la consommation quotidienne moyenne d'eau potable pour un adulte.
10.3 Dioxyde de chlore
On a montré que le dioxyde de chlore perturbait le développement neurocomportemental et neurologique chez les rats exposés à cette substance pendant la période périnatale. On a également observé une baisse significative des taux d'hormones thyroïdiennes dans les études portant sur des rats et des singes exposés au dioxyde de chlore par l'intermédiaire de l'eau potable. Cependant, on n'a pas proposé de CMA pour le dioxyde de chlore en raison de sa réduction rapide en chlorite (et, dans une moindre mesure, en chlorate). De même, la CMA pour le chlorite est considérée comme une protection appropriée contre la toxicité potentielle du dioxyde de chlore; la NOAEL de 2,9 mg/kg p.c. par jour utilisée pour calculer la DJA pour le chlorite est semblable aux plus faibles NOAEL observées pour ce qui est des effets du dioxyde de chlore sur le développement neurocomportemental et neurologique ainsi que sur les taux d'hormones thyroïdiennes.
L'OMS n'a pas établi de recommandation pour le dioxyde de chlore dans l'eau potable parce que celui-ci se décompose rapidement dans l'eau et parce que la recommandation provisoire pour le chlorite est protectrice de la toxicité potentielle du dioxyde de chlore. La U.S. EPA a établi un résidu maximal de désinfectant (Maximum Residual Disinfectant Level -MRDL), en se basant sur une évaluation du poids de la preuve qui inclut l'information sur le chlorite et ses effets nocifs sur la reproduction et le développement.
La concentration-seuil pour la perception du goût et de l'odeur du dioxyde de chlore est de 0,4 mg/L (NRC des États-Unis, 1987), valeur moins élevée que les CMA calculées pour le chlorite et le chlorate.
11.0 Justification
Le chlorite, le chlorate et le dioxyde de chlore peuvent se trouver dans l'eau potable traitée à l'aide de dioxyde de chlore comme désinfectant primaire au lieu de chlore, lequel est beaucoup plus utilisé. On peut également trouver du chlorate dans l'eau potable traitée avec des solutions d'hypochlorite (comme source de chlore) mal entreposées, utilisées de façon inadéquate, ou qui ne satisfont pas aux normes de qualité. Ces deux méthodes de désinfection sont très efficaces pour éliminer les maladies transmises par l'eau; cependant, toutes deux peuvent entraîner la formation de sous-produits dangereux. Ceux-ci doivent être réduits au minimum sans pour autant que ne soit compromise l'efficacité de la désinfection de l'eau.
Comme le dioxyde de chlore n'est utilisé que dans un nombre très restreint d'usines d'épuration des eaux au Canada, on s'attend à ce que le risque d'exposition au dioxyde de chlore, au chlorite et au chlorate ne soit pas significatif pour le Canadien moyen. Bien que plus de Canadiens pourraient être exposés à ces substances par l'utilisation de solutions d'hypochlorite, la qualité de ces solutions de même qu'un entreposage et une utilisation convenables de celles-ci peuvent grandement contribuer à éliminer toute exposition potentielle. Il n'existe aucune indication expérimentale selon laquelle le chlorite, le chlorate et le dioxyde de chlore seraient cancérogènes pour l'humain. Cependant, d'autres effets sur la santé observés au cours d'études expérimentales et épidémiologiques rigoureuses justifient l'établissement de recommandations pour le chlorite et le chlorate. Malgré les effets neurologiques et hormonaux constatés chez des animaux de laboratoire, on n'a pas jugé nécessaire de proposer de recommandation pour le dioxyde de chlore en raison de l'hydrolyse rapide de cette substance en chlorite, qui rend improbable une exposition humaine à cette substance par l'intermédiaire de l'eau potable. Il a été déterminé que les résultats d'études sur le chlorite pouvaient être considérés représentatifs des effets potentiels sur la santé reliés à l'exposition au dioxyde de chlore, et qu'il n'était donc pas nécessaire l'élaborer une recommandation spécifique pour ce composé. Une dose maximale appliquée a plutôt été recommandée, qui vise à assurer que les consommateurs ne soient pas exposées à des concentrations de dioxyde de chlore ou de ses sousproduits qui pourraient poser des risques sur la santé.
Dans le cadre du processus continuel de révision des recommandations, Santé Canada va continuer de surveiller la recherche effectuée dans ce domaine et de recommander tout changement jugé nécessaire à ce document technique.
11.1 Chlorite
Dans une des études effectuées, la diminution du poids du cerveau, la diminution de la réaction à un bruit fort et la variation du poids du foie dans les deux premières générations de descendants de rats Sprague-Dawley ont été considérées comme des effets significatifs de l'exposition au chlorite. Cette étude a été utilisée pour calculer l'AQT de 0,029 mg/kg p.c. et ses résultats concordent avec ceux d'études portant sur des sujets humains volontaires. La CMA de 1 mg/L peut facilement être mesurée dans l'eau potable à l'aide de plusieurs méthodes d'analyse de la U.S.EPA. Bien qu'il soit possible d'éliminer le chlorite de l'eau potable en la traitant par des méthodes faisant intervenir par exemple du charbon actif ou des agents réducteurs à base de soufre et de fer, l'approche recommandée consiste à réduire la production de chlorite dans le processus de désinfection en augmentant l'efficacité du générateur de dioxyde de chlore. On estime pouvoir atteindre des concentrations de chlorite inférieures à la CMA de 1 mg/L à l'aide de ces stratégies.
11.2 Chlorate
Dans une étude portant sur des rats Sprague-Dawley, une exposition subchronique au chlorate a été liée à un poids corporel et des poids d'organes plus faibles, ainsi qu'à des anomalies sanguines, de l'hypophyse et de la glande thyroïde. L'AQT calculé pour le chlorate à partir de cette étude, soit 0,03 mg/kg p.c., était très proche de celle du chlorite, et les résultats obtenus concordent avec ceux des études portant sur des sujets humains volontaires. La CMA de 1 mg/L peut facilement être mesurée dans l'eau potable à l'aide de plusieurs méthodes d'analyse de la U.S. EPA, dont des variantes des méthodes utilisées pour la détection du chlorite. Cependant, contrairement au cas du chlorite, il n'existe aucun traitement connu pouvant réduire l'ion chlorate une fois qu'il a été formé dans l'eau potable. Lorsque des solutions d'hypochlorote sont utilisées dans le traitement, il faut prendre les précautions nécessaires pour éviter la formation de chlorate. Qui plus est, le chlorite en excès peut réagir pour produire plus de chlorate. Il est donc important d'entretenir soigneusement le générateur de dioxyde de chlore pour qu'il fonctionne aussi efficacement que possible afin de réduire la formation de chlorite et de chlorate. Le chlorite en excès doit être éliminé avant la désinfection secondaire au chlore afin d'éviter la formation de chlorate dans le réseau de distribution. On estime que cette méthode peut permettre d'atteindre la CMA de 1 mg/L de chlorate.
12.0 Bibliographie
- Abdel-Rahman, M.S. 1985. Pharmacokinetics of chlorine obtained from chlorine dioxide, chlorine, chloramine and chloride. Dans : Water chlorination. Vol. 5. Chemistry, environmental impact and health effects. Sous la direction de R.L. Jolley. Lewis Publishers, Chelsea, MI. p. 281-293.
- Abdel-Rahman, M., Couri, D. et Bull, R.J. 1980. Kinetics of ClO2 and effects of ClO2, ClO2- and ClO3- in drinking water on blood glutathione and hemolysis in rat and chickens. J. Environ. Pathol. Toxicol., 3: 431-449.
- Abdel-Rahman, M.S., Couri, D. et Bull, R.J. 1982a. Metabolism and pharmacokinetics of alternate drinking water disinfectants. Environ. Health Perspect., 46: 19-23.
- Abdel-Rahman, M.S., Gerges, S.E. et Alliger, H. 1982b. Toxicity of alcide. J. Appl. Toxicol., 2(3): 160-164 [cité dans RTECS, 2000a].
- Abdel-Rahman, M.S., Couri, D. et Bull, R.J. 1984a. Toxicity of chlorine dioxide in drinking water. J. Am. Coll. Toxicol., 3(4): 277-284.
- Abdel-Rahman, M.S., Couri, D. et Bull, R.J. 1984b. The kinetics of chlorite and chlorate in the rat. J. Am. Coll. Toxicol., 3(4): 261-267.
- Abdel-Rahman, M.S., Couri, D. et Bull, R.J. 1985. The kinetics of chlorite and chlorate in rats. J. Environ. Pathol. Toxicol. Oncol., 6(1): 97-103.
- Aieta, E.M., Berg, J.D., Robert, P.V. et Cooper, R.C. 1980. Comparison of chlorine dioxide and chlorine in wastewater disinfection. J. Am. Water Pollut. Control Fed., 52(4): 810-822.
- APHA (American Public Health Association), American Water Works Association and Water Environment Federation. 1998. Standard methods for the examination of water and wastewater. 20e édition. American Public Health Association, Washington, DC.
- APHA (American Public Health Association), American Water Works Association and Water Environment Federation. 2005. Standard methods for the examination of water and wastewater. 21e édition. American Public Health Association, Washington, DC.
- Aranda-Rodriguez, R., Benoit, F.M., Lebel, G.L., Koudjonou, B. and Jay, B. 2004. Disinfection by-products in drinking water from systems using chlorine dioxide disinfectant. Dans : Proceedings of the 11th National Drinking Water Conference and 2nd Policy Forum. Calgary, Alberta, Canada. 4-7 avril.
- ATSDR (Agency for Toxic Substances and Disease Registry). 2004. Toxicological profile for chlorine dioxide and chlorite. September 2004. PB/2004/1007332. Agency for Toxic Substances and Disease Registry, Public Health Service, U.S. Department of Health and Human Services, Atlanta. GA.
- AWWA (American Water Works Association). 2004. AWWA standard hypochlorites. American Water Works Association, Denver, CO (ANSI/AWWA B300-4).
- Bercz, J.P., Jones, L., Garner, L., Murray, D., Ludwig, D. et Boston, J. 1982. Subchronic toxicity of chlorine dioxide and related compounds in drinking water in the non-human primate. Environ. Health Perspect., 46: 47-55.
- Bio/Dynamics, Inc. 1987a. A subchronic (3-month) oral toxicity study in the dog via gavage administration with sodium chlorate. Bio/Dynamics, Inc., East Millstone, NJ (Rapport no 86-3114; préparé pour Sodium Chlorate Task Force, Oklahoma City, OK) [cité dans OMS, 1996; 2004].
- Bio/Dynamics, Inc. 1987b. A subchronic (3-month) oral toxicity study of sodium chlorate in the rat via gavage. Bio/Dynamics, Inc., East Millstone, NJ (Rapport no 86-3112; préparé pour Sodium Chlorate Task Force, Oklahoma City, OK) [cité dans OMS, 1996; 2004].
- Bio/Dynamics, Inc. 1987c. A teratogenicity study in rats with sodium chlorate. Bio/Dynamics, Inc., East Millstone, NJ (Rapport no 86-3117; préparé pour Sodium Chlorate Task Force, Oklahoma City, OK) [cité dans OMS, 1996; 2004].
- Budavari, S. (dir.). 2001. The Merck index -- Encyclopedia of chemicals, drugs and biologicals. 13e édition. Merck and Co., Whitehouse Station, NJ.
- Carlton, B.D., Habash, D.L., Basaran, A.H., George, E.L. et Smith, M.K. 1987. Sodium chlorite administration in Long-Evans rats: reproductive and endocrine effects. Environ. Res., 42: 238-245.
- Carlton, B.D., Basaran, A.H., Mezza, L.E., George, E.L. et Smith, E.K. 1991. Reproductive effects in Long-Evans rats exposed to chlorine dioxide. Environ. Res., 56: 170-177.
- Cifone, M. et Myhr, B. 1986. Mutagenicity evaluation of chlorine dioxide in the mouse lymphoma forward mutation assay. Litton Bionetics Inc., Kensington, MD (Rapport no 20989) [cité dans PISC, 2002].
- CIRC (Centre international de recherche sur le cancer). 1991. Chlorinated drinking-water; chlorination by-products; some other halogenated compounds; cobalt and cobalt compounds. IARC Monogr. Eval. Carcinogen. Risks Hum., 52: 45-359.
- CMA (Chemical Manufacturers Association). 1989. A review of the uses, chemistry and health effects of chlorine dioxide and the chlorite ion. Chemical Manufacturers Association, Washington, DC [cité dans OMS, 1996; 2004].
- CMA (Chemical Manufacturers Association). 1996. Sodium chlorite: drinking water rat two-generation reproductive toxicity study. Chemical Manufacturers Association, Washington, DC (Quintiles Report CMA/17/96) [cité dans OMS, 1996; 2004].
- Cotton, F.A., Wilkinson, G.., Murillo, C.A. et Bochmann, M. 1999. Advanced inorganic chemistry. 6e édition. John Wiley & Sons, New York, p. 560-561.
- Couri, D. et Abdel-Rahman, M.S. 1980. Effect of chlorine dioxide and metabolites on glutathione dependent system in rat, mouse and chicken blood. J. Environ. Pathol. Toxicol., 3: 451-460.
- Cove, D.J. 1976. Chlorate toxicity in Aspergillus nidulans: Studies of mutants altered in nitrate assimilation. Mol. Gen. Genet., 146: 147-159.
- Daniel, F.B., Condie, L., Robinson, M., Stober, J., York, R., Olson, G. et Wang, S. 1990. Comparative subchronic toxicity studies of three disinfectants. J. Am. Water Works Assoc., 82: 61-69.
- Dixon, K. et Lee, R.G. 1991. The effect of sulfur-based reducing agents and GAC filtration on chlorine dioxide byproducts. J. Am. Water Works Assoc., 83: 48-55.
- FDA (Food and Drug Administration) des États-Unis. 1990. Food and drugs. Vol. 21. Parts 170-179. Office of the Federal Register, Washington, DC.
- Gallagher, D.L., Hoehn, R.C. et Dietrich, A.M. 1994. Sources, occurrence, and control of chlorine dioxide byproduct residuals in drinking water. American Water Works Association Research Foundation, Denver, CO.
- Gates, D.J. 1989. Improvements in chlorine dioxide use: A two-step method for determining residual oxidants in the presence of other chlorine species in finished water. Dans : Advances in water analysis and treatment: Proceedings of the American Water Works Association Water Quality Technology Conference, 13-17 novembre, 1988, St. Louis, MO. American Water Works Association, Denver, CO. p. 689-703.
- Gates, D.J. 1998. Analysis Methods. Dans : The chlorine dioxide handbook. American Water Works Association, Denver, CO. p. 130-131.
- Gill, M.W., Swanson, M.S., Murphy, S.R. et Bailey, G.P.. 2000. Two-generation reproduction and developmental neurotoxicity study with sodium chlorite in the rat. Journal of Applied Toxicology 20: 291-303.
- Gordon, G. 2001. Is all chlorine dioxide created equal? J. Am. Water Works Assoc., 93: 163-173.
- Gordon, G., Adam, L. et Bubnis, B. 1995. Minimizing chlorate formation in drinking water when hypochlorite ion is the chlorinating agent. American Water Works Association Research Foundation, Denver, CO.
- Griese, M.H., Hauser, K.A., Berkemeier, M. et Gordon, G. 1991. Using reducing agents to eliminate chlorine dioxide and chlorite ion residuals in drinking water. J. Am. Water Works Assoc., 83: 56-61.
- Griese, M.H., Kaczur, J.J. et Gordon, G. 1992. Combining methods for the reduction of oxychlorine residuals in drinking water. J. Am. Water Works Assoc., 84: 69-77.
- Haag, H.B. 1949. The effect on rats of chronic administration of sodium chlorite and chlorine dioxide in the drinking water. Rapport du Medical College of Virginia à Mathieson Alkali Works [cité dans OMS, 1996; 2004; TERA, 1998].
- Haller, J.F. et Northgraves, W.W. 1955. Chlorine dioxide and safety. TAPPI, 38: 199-202.
- Harrington, R.M., Shertzer, H.G. et Bercz, J.P. 1986. Effects of chlorine dioxide on thyroid function in the African green monkey and the rat. J. Toxicol. Environ. Health, 19: 235-242.
- Harrington, R.M., Romano, R.R. et Irvine, L. 1995. Developmental toxicity of sodium chlorite in the rabbit. J. Am. Coll. Toxicol., 14: 108-118.
- Hayashi, M., Kishi, M., Sofuni, T. et Ishidate, M., Jr. 1988. Micronucleus tests in mice on 39 food additives and 8 miscellaneous chemicals. Food Chem. Toxicol., 26(6): 487-500.
- Heffernan, W.P., Guion, C. et Bull, R.J. 1979. Oxidative damage to the erythrocyte induced by sodium chlorite, in vivo. J. Environ. Pathol. Toxicol., 2: 1487-1499.
- Hurst, G.H. et Knocke, W.R. 1997. Evaluating ferrous iron for chlorite ion removal. J. Am. Water Works Assoc., 89: 98-105.
- Iatrou, A. et Knocke, W.R. 1992. Removing chlorite by the addition of ferrous iron. J. Am. Water Works Assoc., 84: 63-68.
- Ishidate, M., Sofuni, T., Yoshikawa, K., Hayashi, M., Nohmi, T., Sawada, M. et Matsuoka, A. 1984. Primary mutagenicity screening of food additives currently used in Japan. Food Chem. Toxicol., 22: 623-636.
- Ivett, J. et Myhr, B. 1984. Mutagenicity evaluation of chlorine dioxide in the mouse bone marrow cytogenetic assay. Litton Bionetics Inc., Kensington, MD (Rapport no 22202) [cité dans PISC, 2002].
- Ivett, J. et Myhr, B. 1986. Mutagenicity evaluation of chlorine dioxide in an in vitro cytogenetic assay. Litton Bionetics Inc., Kensington, MD (Rapport no 20990) [cité dans PISC, 2002].
- Kanitz, S., Franco, Y., Patrone, V., Caltabellotta, M., Raffo, E., Riggi, C., Timitilli, D. et Ravera, G. 1996. Association between drinking water disinfection and somatic parameters at birth. Environ. Health Perspect., 104(5): 516-520.
- Kurokawa, Y., Takayama, S., Konishi, Y., Hiasa, Y., Asahina, S., Takahashi, M., Maekawa, A. et Hayashi, Y. 1986. Long-term in vivo carcinogenicity tests of potassium bromate, sodium hypochlorite and sodium chlorite conducted in Japan. Environ. Health Perspect., 69: 221-235.
- Lewis, R.J. 2001. Hawley's condensed chemical dictionary. 12e édition. Van Nostrand Reinhold, New York, NY.
- Lubbers, J.R., Chauhan, S. et Bianchine, J.R. 1981. Controlled clinical evaluation of chlorine dioxide, chlorite and chlorate in man. Fundam. Appl. Toxicol., 1: 334-338.
- Masschelein W.J. (1989). Determination of residual ozone or chlorine dioxide in water with ACVK -- an updated version. Ozone Sci. Eng. 11: 209-215.
- McCauley, P.T., Robinson, M., Daniel, F.B. et Olson, G.R. 1995. The effects of subchronic chlorate exposure in Sprague-Dawley rats. Drug Chem. Toxicol., 18: 185-199.
- Meier, J.R., Bull, R., Stober, J. et Cimino, M. 1985. Evaluation of chemicals used for drinking water disinfection for production of chromosomal damage and sperm-head abnormalities in mice. Environ. Mutagen., 7: 201-211.
- Mobley, S.A., Taylor, D.H., Laurie, R.D. et Pfohl, R.J. 1990. Chlorine dioxide depresses T3 uptake and delays development of locomotor activity in young rats. Dans : Water chlorination: Chemistry, environmental impact and health effects. Vol. 6. Sous la direction de R.L. Jolley, L.W. Condie et J.D. Johnson. Lewis Publishers, Ann Arbor, MI. p. 347-360.
- Moore, G.S. et Calabrese, E.J. 1982. Toxicological effects of chlorite in the mouse. Environ. Health Perspect., 46: 31-37.
- Moore, M. et Myhr, B. 1984. Evaluation of chlorine dioxide in the mouse dominant lethal assay. Litton Bionetics Inc., Kensington, MD (Rapport no 22203) [cité dans PISC, 2002].
- Musil, J., Knotek, Z. et Chalupa, J. 1964. Toxicologic aspects of chlorine dioxide application for the treatment of water containing phenols. Technol. Water, 8: 327-346.
- Novatek. 1991. Removal of chlorine dioxide by-products from drinking water. Rapport préparé par Novatek, Oxford, OH, pour l'Environmental Protection Agency des États-Unis, contrat 68D00033, avril.
- NRC (National Research Council) des États-Unis. 1980. Drinking water and health. Vol. 2. National Academy Press, Washington, DC.
- NRC (National Research Council) des États-Unis. 1982. Drinking water and health. Vol. 4. National Academy Press, Washington, DC.
- NRC (National Research Council) des États-Unis. 1987. Drinking water and health. Vol. 7. National Academy Press, Washington, DC.
- OMS (Organisation mondiale de la santé). 1996. Directives de qualité pour l'eau de boisson. 2e édition. Vol. 2. Critères d'hygiène et documentation à l'appui. Organisation mondiale de la santé, Genève.
- OMS (Organisation mondiale de la santé). 2004. Chlorite and Chlorate in Drinking-water. Background document for development of WHO Guidelines for Drinking-water Quality. World Health Organization, Geneva, Switzerland (WHO/SDE/WSH/03.04/38).
- Orme, J., Taylor, D., Laurie, R. et Bull, R. 1985. Effects of chlorine dioxide on thyroid function in neonatal rats. J. Toxicol. Environ. Health, 15: 315-322.
- PISC (Programme international sur la sécurité des substances chimiques). 2000. Disinfectants and disinfection byproducts. Environmental Health Criteria 216. Organisation mondiale de la santé, Genève.
- PISC (Programme international sur la sécurité des substances chimiques). 2002. Chlorine dioxide (gas). Organisation mondiale de la santé, Genève (Concise International Chemical Assessment Document 37).
- Prieto, R. et Fernandez, E. 1993. Toxicity and mutagenesis by chlorate are independent of nitrate reductase in Chlamydomonas reinhardtii. Mol. Gen. Genet., 237: 429-438.
- RTECS (Registry of Toxic Effects of Chemical Substances). 2006c. Sodium chlorite. RTECS Number VZ4800000. CAS # 7758-19-2. Created by Canadian Centre for Occupational Health and Safety, Hamilton, Ontario. Dernière mise à jour février 2006.
- RTECS (Registry of Toxic Effects of Chemical Substances). 2006a. Chlorine dioxide. RTECS Number F03000000. CAS # 10049-04-4. Created by Canadian Centre for Occupational Health and Safety, Hamilton, Ontario. Dernière mise à jour février 2006.
- RTECS (Registry of Toxic Effects of Chemical Substances). 2006b. Chloric acid, sodium salt. CAS # 7775-09-9 RTECS # FO0525000. Created by Canadian Centre for Occupational Health and Safety, Hamilton, Ontario. Dernière mise à jour février 2006.
- Santé Canada. 1994. Loi canadienne sur la protection de l'environnement -- L'évaluation du risque à la santé humaine des substances d'intérêt prioritaire. Annexe B : Critères de classification des substances cancérogènes. Direction de l'hygiène du milieu, Santé Canada (Ottawa).
- Santé Canada. 2005. Canadian drinking water from systems using chlorine dioxide disinfectant: A survey of 8 systems. Rapport préparé par R. Aranda-Rodriguez, Division de la recherche en chimie, Direction générale de la santé environnementale et de la sécurité des consommateurs, Santé Canada, Ottawa, Ontario.
- Sheahan, B.J., Pugh, D.M. et Winstanley, E.W. 1971. Experimental sodium chlorate poisoning in dogs. Res. Vet. Sci., 12: 387-389.
- Simpson, G.D., Kuykendall, C., Miller, J. et Averett, B. 1995. Biocides: The safe and effective use of chlorine dioxide. Ind. Water Treatment, 27(5): 48-54.
- Suh, D.H., Abdel-Rahman, M.S. et Bull, R.J. 1983. Effect of chlorine dioxide and its metabolites in drinking water on fetal development in rats. J. Appl. Toxicol., 3: 75-79.
- Suh, D.H., Abdel-Rahman, M.S. et Bull, R.J. 1984. Biochemical interactions of chlorine dioxide and its metabolites in rats. Arch. Environ. Contam. Toxicol., 13: 163-169.
- Taylor, D.H. et Pfohl, R.J. 1985. Effects of chlorine dioxide on the neurobehavioral development of rats. Dans : Water chlorination. Vol. 5. Chemistry, environmental impact and health effects. Sous la direction de R.L. Jolley. Lewis Publishers, Chelsea, MI. p. 355-364.
- TERA (Toxicology Excellence for Risk Assessment). 1998. Health risk assessment/characterization of the drinking water disinfection by-products chlorine dioxide and chlorite. Toxicology Excellence for Risk Assessment, Cincinnati, OH (Rapport 8W-0766-NTLX).
- Toth, G.P., Long, R., Mills, T. et Smith, M. 1990. Effects of chlorine dioxide on the developing rat brain. J. Toxicol. Environ. Health, 31: 29-44.
- U.S. EPA. 1983. Sodium chlorate: exemption from the requirement of a tolerance. Fed. Regist., 48: 19028.
- U.S. EPA. 1995. 40 CFR, Chapter I, Part 136, Appendix B: Definition and procedure for the determination of the method detection limit -- Revision 1.11. Environmental Protection Agency des États-Unis, Washington, DC.
- U.S. EPA. 1996. Proposed guidelines for carcinogen risk assessment. Fed. Regist., 61(79): 17959-18011.
- U.S. EPA. 1998. EPA Method 300.1. Determination of inorganic anions in drinking water by ion chromatography. Revision 1.0. Environmental Protection Agency des États-Unis, Washington, DC (EPA/600/R-98/118).
- U.S. EPA. 1999a. Alternative disinfectants and oxidants guidance manual. Office of Water, Environmental Protection Agency des États-Unis, Washington, DC, avril (EPA 815-R-99-014).
- U.S. EPA. 1999b. EPA Method 300.0, Revision 2.2. Determination of inorganic anions by ion chromatography. Environmental Protection Agency des États-Unis, Washington, DC, octobre (EPA-821-R-99-015).
- U.S. EPA. 2000. Toxicological review of chlorine dioxide and chlorite, in support of summary information on the Integrated Risk Information System (IRIS). Environmental Protection Agency des États-Unis, Washington, DC, septembre (EPA/636/R-00/007).
- U.S. EPA. 2001a. Method 317.0. Determination of inorganic oxyhalide disinfection by-products in drinking water using ion chromatography with the addition of a postcolumn reagent for trace bromate analysis. Revision 2.0. Environmental Protection Agency des États-Unis, Washington, DC, juillet (EPA 815-B-01-001).
- U.S. EPA. 2001b. Controlling disinfection by-products and microbial contaminants in drinking water. Environmental Protection Agency des États-Unis, Washington, DC, décembre (EPA/600/R-01/110).
- U.S. EPA. 2002. Method 326.0. Determination of inorganic oxyhalide disinfection by-products in drinking water using ion chromatography incorporating the addition of a suppressor acidified postcolumn reagent for trace bromate analysis. Revision 1.0. Environmental Protection Agency des États-Unis, Washington, DC, juin.
- U.S. EPA. 2003a. Stakeholder discussion on the reassessment of PQL's. Environmental Protection Agency des États-Unis, Washington, DC, 19 juin.
- U.S. EPA. 2003b. Method 327.0. Determination of chlorine dioxide and chlorite ion in drinking water using Lissamine Green B and horseradish peroxidase with detection by visible spectrophotometry. Revision 1.0. Technical Support Center, Office of Ground Water and Drinking Water, Environmental Protection Agency des États-Unis, Cincinnati, OH (EPA 815-B-03-001).
- U.S. EPA (United States Environmental Protection Agency). 2005. Chlorite (sodium salt) (CASRN 7758-19-2) Integrated Risk Information System (IRIS). Last revision 6/22/2005. National Center for Environmental Assessment, U.S. EPA, Washington, DC.
- Volk, C.J., Hofmann, R., Chauret, C., Gagnon, G.A., Ranger, G. et Andrews, R.C. 2002. Implementation of chlorine dioxide disinfection: Effects of the treatment change on drinking water quality in a full-scale distribution system. J. Environ. Eng. Sci., 1: 323-330.
- Wang G., Chen H. and Yuan L. (2001) New method for the flow injection spectrophotometric determination of low concentration chlorine dioxide in water using methylene blue. Anal. Let. 34(14): 2485-2492.
- White, G.C. 1992. The handbook of chlorination and alternative disinfectants. 3e édition. Van Nostrand Reinhold, New York, NY.