Dosage de l’acide sorbique dans le tabac entier : T-313
1 Portée
1.1
La présente méthode sert à doser l'acide sorbique ajouté au tabac entier comme agent antimicrobien, à l'aide d'un système de chromatographie en phase liquide haute performance (CLHP) en phase inversée muni d'un détecteur ultraviolet (détecteur UV). Elle est conçue pour l'analyse de routine et n'exige pas la préparation d'un dérivé.
Remarque : cette méthode ne permet pas de distinguer l'acide sorbique ajouté de l'acide sorbique présent naturellement (le cas échéant) dans le tabac entier.
2 Normes applicables
2.1
Méthode officielle T-115 de Santé Canada, Dosage du goudron, de l'eau, de la nicotine et du monoxyde de carbone dans la fumée principale de tabac, 2016.
2.2
Méthode officielle T-402 de Santé Canada. Préparation de cigarettes, de bâtonnets de tabac, de tabac à cigarette, de cigares, de petits cigares, de kreteks, de bidis, de tabac en feuille, de tabac à pipe ou de tabac sans fumée aux fins d'essais, 2016.
2.3
Organisation internationale de normalisation, ISO 8243, Cigarettes – Échantillonnage, 2013.
2.4
Organisation internationale de normalisation, ISO 15592-1, Tabac à rouler et objets confectionnés à partir de ce type de tabac – Méthodes d'échantillonnage, de conditionnement et d'analyse – Partie 1 : Échantillonnage, 2001.
2.5
AOAC INTERNATIONAL, méthode officielle 971.11, Fatty Acids (Volatile) in Eggs; Gas Chromatographic Method, Official Methods of Analysis of AOAC INTERNATIONAL, 20ème édition, 2016.
3 Définitions
3.1
Pour une définition des termes utilisés dans le présent document, se reporter à la méthode T-301.
4 Résumé de la méthode
4.1
Le tabac entier est extrait avec 25 mL d'eau chaude dans un agitateur à ultrasons.
4.2
La solution d'extraction est refroidie, filtrée avec un filtre pour seringue, puis le filtrat est récupéré dans un flacon ambré pour échantillonneur automatique et analysé par CLHP en phase inversée.
4.3
La phase mobile est surveillée grâce à un détecteur UV et l'acide sorbique trouvé dans le tabac entier est dosé par comparaison avec des étalons externes.
Avertissement : L'analyse et l'évaluation de certains produits à l'aide de cette méthode peuvent nécessiter l'utilisation de substances et/ou d'équipement potentiellement dangereux. Le présent document n'entend pas répondre à tous les aspects concernant la sécurité de son utilisation. Avant d'utiliser cette méthode normalisée, toute personne a la responsabilité de consulter les autorités compétentes et de prendre des mesures de protection de la santé et des mesures de sécurité qui tiennent compte de tous les règlements en vigueur.
5 Appareillage et équipement
5.1
Fiole jaugée de 2000 mL.
5.2
Fioles jaugées ambrés de 10 et 100 mL.
5.3
Éprouvette graduée de 50 mL, en verre.
5.4
Tubes à culture de 200 × 25 mm, avec bouchons à vis.
5.5
Bouchons en polypropylène, blancs, sans garniture.
5.6
Micropipettes de 25 et 200 µL ou l'équivalent.
5.7
Pipettes Pasteur jetables en verre.
5.8
Distributeur, 10 - 50 mL ou l'équivalent.
5.9
Filtre pour seringue.
5.10
Seringues jetables.
5.11
Flacons pour échantillonneur automatique avec bouchons filetés et septums recouverts de téflon.
5.12
Poires en caoutchouc.
5.13
Parafilm®.
5.14
Mélangeur Robot Coupe RS1-2V ou l'équivalent.
5.15
Mélangeur vortex.
5.16
Balance analytique précise au moins à quatre décimales.
5.17
pH-mètre.
5.18
Sonicateur.
5.19
Système de chromatographie liquide haute performance, avec détecteur UV, comprenant :
5.19.1
Colonne RP 18e ou l'équivalent.
5.19.2
Colonne de garde jetable.
6 Réactifs et matériel
6.1
Tous les réactifs doivent être, au minimum, de qualité réactif pour analyses.
Remarque : lorsque cela était possible, le numéro de registre des Chemical Abstracts [numéro CAS] a été ajouté entre crochets à la suite de chaque réactif.
6.2
Méthanol [67-56-1] distillé dans du verre.
6.3
Acide phosphorique [7664-38-2] pureté de 85 %.
6.4
Orthophosphate monopotassique [7778-77-0], pureté > 99 %.
6.5
Sorbate de potassium [590-00-1], pureté de 99 %.
6.6
Eau de type I, tel que stipulé dans le tableau 1 de la méthode D1193 de l'ASTM, Processes for Reagent Water Production, Note A.
7 Préparation de la verrerie
7.1
Nettoyer et sécher la verrerie de manière à s'assurer qu'il n'y ait aucune contamination.
8 Préparation des étalons
8.1
Étalons primaires de sorbate
8.1.1
Peser 134 mg de sorbate de potassium dans une fiole jaugée de 100 mL.
8.1.2
Convertir le sorbate de potassium en acide sorbique en multipliant le poids du sorbate de potassium par le poids moléculaire de l'acide sorbique (112,14) et en divisant par le poids moléculaire du sorbate de potassium (150,22).
Remarque : 112,14/150,22 = 0,7465; donc 134 mg de sorbate de potassium est équivalent à 134 × 0,7465 = 100 mg d'acide sorbique
8.1.3
Compléter avec de l'eau de type I.
8.2
Étalons de travail d'acide sorbique
8.2.1
Prélever des volumes appropriés (de 0,01 à 1,0 mL) de solution étalon primaire de sorbate de potassium et diluer jusqu'à 10 mL avec de l'eau de type 1, pour obtenir des étalons de travail dont la concentration approximative d'acide sorbique se situe dans l'intervalle de 0,2 à 100 ppm.
Étalons de travail d'acide sorbique
| Étalon no |
Volume (mL) de solution primaire d'acide sorbique |
Volume final (mL) |
Acide sorbique [µg/mL] (ppm) |
|---|---|---|---|
| 0 | 0 | 10 | 0,0 |
| 1 | 0,01 | 10 | 1,0 |
| 2 | 0,050 | 10 | 5,0 |
| 3 | 0,100 | 10 | 10,0 |
| 4 | 0,250 | 10 | 25,0 |
| 5 | 0,5 | 10 | 50,0 |
| 6 | 1,0 | 10 | 100,0 |
Remarque : la concentration d'acide sorbique varie selon la concentration exacte de la solution étalon primaire préparée.
Remarque : il peut être nécessaire de préparer d'autres étalons pour couvrir l'intervalle de réponses prévues avec les échantillons.
8.2.2
Transvaser dans des flacons ambrés pour échantillonneur automatique. Rincer d'abord les flacons, puis les remplir de manière à réduire le plus possible l'espace libre au-dessus du liquide.
8.2.3
Conserver à 4 ° C, à l'abri de la lumière, jusqu'au moment de l'analyse.
8.2.4
Préparer de nouvelles solutions étalons de travail d'acide sorbique tous les cinq jours.
9 Échantillonnage
9.1
L'échantillonnage des cigarettes aux fins des tests doit être effectué conformément à la norme ISO 8243.
9.2
L'échantillonnage des kreteks, des petits cigares, des bidis, des bâtonnets de tabac aux fins des tests doit être effectué conformément à la norme ISO 8243, mais modifié en remplaçant le terme cigarettes par kreteks, petits cigares, bidis ou bâtonnets de tabac, pour lesquels le terme carton est équivalent à 200 unités.
9.3
L'échantillonnage des cigares aux fins des tests doit être effectué conformément à la norme ISO 8243, mais modifié en remplaçant le terme cigarettes par cigares, pour lesquels 200 unités de cigarettes est équivalent à 200 grammes de cigare.
9.4
L'échantillonnage du tabac à cigarette aux fins des tests doit être effectué conformément à la norme ISO 15592-1
9.5
L'échantillonnage des feuilles de tabac, du tabac à pipe et du tabac sans fumée aux fins des tests doit être effectué conformément à la norme ISO 15592-1, mais modifié en remplaçant le terme tabac à rouler par le terme feuilles de tabac, tabac à pipe ou tabac sans fumée.
10 Préparation des produits du tabac
10.1
L'échantillonnage des produits du tabac à analyser doit être effectué conformément à la méthode T-402.
11 Préparation des échantillons
11.1
Peser avec précision 0,5 g de tabac finement broyé dans un tube à culture en verre.
11.2
Ajouter 25 mL d'eau de type I chaude (50 ° C) et traiter dans le sonicateur pendant 30 minutes à 50 ° C.
Remarque : le temps et l'efficacité d'extraction dépendent du type de tube, du type de sonicateur et de la quantité traitée.
11.3
Laisser refroidir l'échantillon.
11.4
Bien mélanger, puis à l'aide d'un filtre jetable pour seringue fixé à une seringue jetable, filtrer une portion dans un flacon ambre pour échantillonneur automatique. Boucher et conserver à 4 ° C à l'abri de la lumière jusqu'au moment de l'analyse.
12 Analyse des échantillons
12.1
Conditions chromatographiques (analyse par CLHP en phase inversée)
- Température de la colonne : 30 ° C
- Phase mobile réactifs:
- Solvant A : méthanol, filtrer et dégazer (par barbotage d'hélium ultrapur)
- Solvant B : préparer 2 L d'une solution d'isopropanol à 1 %, ajuster le pH à 2,3 avec de l'acide phosphorique, filtrer et dégazer (par barbotage d'hélium ultrapur)
- Lavage de l'échantillon : solvant A
- Phase mobile : gradient – isocratique
- Débit : 1,0 mL/minute
- Longueur d'onde UV : 259 nm
| Temps (minutes) | Composition | ||
|---|---|---|---|
| A (%) |
B (%) |
C (%) |
|
| 0,0 | 35 | 65 | 0 |
| 20,0 | 35 | 65 | 0 |
| Fin de l'analyse | 35 | 65 | 0 |
Temps d'équilibrage : 5 minutes
Remarque : il sera peut-être nécessaire de régler le gradient, selon les paramètres de l'instrument et de la colonne, et la résolution du pic de l'analyte.
12.2
Charger les flacons d'échantillon dans l'échantillonneur automatique.
12.3
13 Calculs
13.1
Courbe d'étalonnage
13.1.1
Injecter 20 µL de chaque solution étalon de travail dans le CLHP. Le chromatogramme doit être semblable à celui illustré à la figure 2 de l'annexe 1.
13.1.2
Préparer une courbe d'étalonnage en rapportant la surface des pics obtenus en fonction de la concentration des étalons.
13.1.3
Déterminer le facteur de réponse à partir de la courbe d'étalonnage.
13.2
Dosage des échantillons
13.2.1
Déterminer la quantité d'acide sorbique dans les échantillons par la méthode des étalons externes.
13.2.2
Identifier les pics par comparaison des temps de rétention avec ceux des étalons, et par dopage des échantillons.
13.3
Détermination de la teneur en acide sorbique, en µg/g

Figure 13-3 : Équivalent textuel
Acide sorbique [µg/g] =
Aire sous le pic
divisé par
Facteur de réponse
×
mL de solution
divisé par
Poids de tabac
13.3.1
Calculer la teneur en acide sorbique automatiquement en entrant le multiplicateur approprié (volume total de dilution de l'échantillon original, en mL) et le diviseur approprié (poids de l'échantillon original, en g); on obtient ainsi automatiquement la teneur en µg/g.
13.3.2
Pour convertir cette teneur en pourcentage (%), diviser le résultat en µg/g par 10 000.
13.3.3
Tous les résultats sont exprimés pour le tabac « tel que reçu ». On peut les exprimer en « matière sèche » en utilisant la valeur appropriée pour la teneur en humidité.
14 Contrôle de la qualité
14.1
14.2
Paramètres de contrôle typiques
Remarque : si les mesures de contrôle dépassent les limites de tolérance des valeurs prévues, il faut procéder à une étude appropriée et prendre les mesures qui s'imposent.
14.2.1
Blanc de réactifs (BR)
Chaque série d'analyse doit comprendre un blanc de réactifs (BR) afin de détecter toute contamination pouvant s'être produite lors de la préparation et de l'analyse des échantillons. Le BR est constitué de tous les réactifs utilisés pour exécuter l'analyse des échantillons, manipulés avec tout le matériel employé à cette fin. Le BR est analysé comme s'il s'agissait d'un échantillon.
14.2.2
Blanc fortifié (BF)
Chaque série d'analyse doit comprendre un blanc fortifié (BF) afin de détecter toute perte d'analytes pouvant s'être produite lors de la préparation et de l'analyse des échantillons. Le BF est constitué de tous les réactifs utilisés pour exécuter l'analyse des échantillons, manipulés avec tout le matériel employé à cette fin, et doit avoir été fortifié par l'addition d'une quantité connue d'au moins un des analytes d'intérêt. Le degré de fortification doit refléter l'intervalle de résultats caractéristiques de l'échantillon. Le BF est analysé comme s'il s'agissait d'un échantillon.
14.2.3
Matrice fortifiée (MF)
Chaque série d'analyse doit comprendre une matrice fortifiée (MF) afin de détecter toute interférence provenant de la matrice. Lors de la préparation et/ou de l'analyse des échantillons, diviser un échantillon et fortifier une des portions avec une quantité connue d'au moins un des analytes d'intérêt. Le degré de fortification doit refléter l'intervalle de résultats caractéristiques de l'échantillon. La MF est analysée comme s'il s'agissait d'un échantillon.
14.2.4
Échantillon de contrôle
Pour évaluer la performance globale d'une méthode d'analyse, procéder à l'analyse d'un échantillon de contrôle. En utilisant des méthodes statistiques appropriées, comparer les résultats ainsi obtenus aux « valeurs prévues » obtenues dans le laboratoire ou, en l'absence de tels résultats, aux valeurs publiées dans la littérature. Le laboratoire obtiendra ainsi des données sur l'exactitude et la précision de la méthode d'analyse.
14.2.5
Échantillon-étalon
Pour évaluer la stabilité du système d'analyse, analyser un étalon comme s'il s'agissait d'un échantillon. En utilisant des méthodes statistiques appropriées, comparer les résultats ainsi obtenus aux concentrations prévues.
14.3
Taux de récupération et niveaux de contamination
14.3.1
La valeur du BR est habituellement de 0,1 ± 0,5 μg/g d'acide sorbique.
14.3.2
Les taux de récupération du BF et de la MF se situent habituellement dans l'intervalle de 85 - 105 %.
14.4
Limite de détection (LD) et limite de quantification (LQ)
14.4.1
Limite de détection (LD)
La limite de détection (LD) est égale à trois fois l'écart-type des résultats obtenus en analysant l'étalon le moins concentré au moins 10 fois sur une période de plusieurs jours.
14.4.1.1
La valeur type de la LD, déterminée par analyse, est habituellement de 75 µg/g.
14.4.2
Limite de quantification (LQ)
La limite de quantification (LQ) est égale à 10 fois l'écart-type des résultats obtenus en analysant l'étalon le moins concentré au moins 10 fois sur une période de plusieurs jours.
14.4.2.1
La valeur de la LQ, déterminée par analyse, est habituellement de 250 µg/g.
14.5
Stabilité des réactifs et des solutions
14.5.1
Préparer de nouvelles solutions étalons primaires à partir de sorbate de potassium chaque semaine.
14.5.2
Préparer de nouveaux étalons de travail et de nouvelles solutions d'extraction chaque semaine.
14.5.3
Analyser tous les échantillons dans les 48 heures; les conserver à l'obscurité au réfrigérateur pour réduire toute perte potentielle d'acide sorbique par croissance microbienne.
15 Références
15.1
Rosa, N.; Caughill, C. W. H. 1984. Effect of Aqueous Ethanol, Sample Particle Size, and Temperature on Extractability of Soluble Acids from Tobacco. Tobacco Science. 1: 24-25.
15.2
ASTM International, Méthode ASTM D1193-06(2011), Standard Specifications for Reagent Water.
Annexe 1
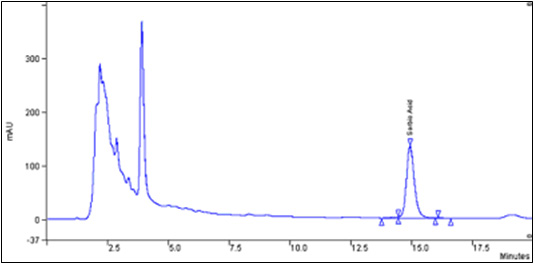
Figure 1. Chromatogramme typique obtenu lors de l'analyse par CLHP de l'acide sorbique dans un échantillon de tabac : Équivalent textuel
La figure suivante présente un exemple de chromatogramme typique d'un échantillon de tabac analysé par chromatographie en phase liquide à haute performance (CLHP) pour l'acide sorbique. L'intensité de l'absorbance en milliunités d'absorbance est tracée en fonction du temps (en minutes).

Figure 2. Chromatogramme typique obtenu lors de l'analyse par CLHP d'un étalon d'acide sorbique : Équivalent textuel
La figure suivante présente a un exemple de chromatogramme CLHP typique d'un cycle avec un étalon d'acide sorbique. L'intensité de l'absorbance en milliunités d'absorbance est tracée en fonction du temps (en minutes).