Dosage des nitrates dans le tabac entier : T-308
1 Portée
1.1
La présente méthode s'applique au dosage des nitrates dans le tabac entier au moyen d'un système d'analyse colorimétrique automatique continu.
1.2
Cette méthode ne permet pas de différencier les nitrates des nitrites présents dans le tabac, car tous les nitrates sont transformés en nitrites lors de l'analyse.
2 Normes applicables
2.1
Méthode officielle T-402 de Santé Canada. Préparation de cigarettes, de bâtonnets de tabac, de tabac à cigarette, de cigares, de petits cigares, de kreteks, de bidis, de tabac en feuille, de tabac à pipe ou de tabac sans fumée aux fins d'essais, 2016.
2.2
Méthode officielle T-115 de Santé Canada, Dosage du goudron, de l'eau, de la nicotine et du monoxyde de carbone dans la fumée principale de tabac, 2016.
2.3
Organisation internationale de normalisation, ISO 8243, Cigarettes - Échantillonnage, 2013.
2.4
Organisation internationale de normalisation, ISO 15592-1, Tabac à rouler et objets confectionnés à partir de ce type de tabac - Méthodes d'échantillonnage, de conditionnement et d'analyse - Partie 1 : Échantillonnage, 2001.
2.5
AOAC INTERNATIONAL, méthode officielle 968.07, Nitrogen (Nitrate and Nitrite) in Animal Feed, Colorimetric Method, Official Methods of Analysis of AOAC INTERNATIONAL, 20ème édition, 2016.
3 Définitions
3.1
Pour les définitions et les termes utilisés dans le présent document, se reporter à la méthode officielle T-301.
4 Résumé de la méthode
4.1
Le tabac entier broyé est extrait avec de l'acide acétique, puis l'extrait est filtré.
4.2
L'extrait est ensuite analysé à l'aide d'un colorimètre automatique à débit continu, dans lequel l'échantillon subit une dialyse en ligne afin d'éliminer les interférences.
4.3
Les ions nitrates sont réduits par réaction avec de l'hydrazine en présence de cuivre.
4.4
On fait réagir le nitrite ainsi formé avec du sulfanilamide, en milieu acide, pour obtenir un composé diazoïque qui, lorsqu'il est mélangé avec de la N-(napth-1-yl)éthylènediamine, forme un complexe de couleur rouge.
4.5
On surveille l'éluant au moyen d'un colorimètre à une seule voie. La teneur en nitrate est dosée par comparaison avec une courbe d'étalonnage externe.
4.6
L'analyse doit être effectuée dans les 24 heures suivant l'extraction.
Avertissement : L'analyse et l'évaluation de certains produits à l'aide de cette méthode d'essai peuvent nécessiter l'utilisation de substances et/ou d'équipement potentiellement dangereux. Le présent document n'entend pas répondre à tous les aspects concernant la sécurité de son utilisation. Avant d'utiliser cette méthode d'essai, toute personne a la responsabilité de consulter les autorités compétentes et de prendre des mesures de protection de la santé et des mesures de sécurité qui tiennent compte de tous les règlements en vigueur.
5 Appareillage et équipement
5.1
Broyeur de marque Robot Coupe, modèle RSI 2V, ou l'équivalent.
5.2
Balance pour analyses, précise à au moins quatre décimales.
5.3
Erlenmeyers de 125 mL en polyméthylpentène (PMP), à bouchon à vis, ou l'équivalent.
5.4
Agitateur oscillant, ou l'équivalent.
5.5
Seringue jetable de 5 mL.
5.6
Filtre-seringue de 0,45 µm en PVDF ou l'équivalent.
5.7
Analyseur automatique en continu (ou l'équivalent) comprenant :
5.7.1
Échantillonneur automatique.
5.7.2
Pompe péristaltique.
5.7.3
Manifold pour nitrates conçu pour l'analyseur automatique utilisé (voir la figure 1).
5.7.4
Colorimètre à une seule voie à circulation de 15 mm, muni d'un filtre à 550 nm.
5.8
Fioles jaugées de 100 mL avec rodage conique en verre.
5.9
Éprouvettes graduées de 50 mL.
5.10
Entonnoir-filtre en verre.
5.11
Agitateur magnétique.
5.12
Pipette automatique de 1000 µL, à volume réglable, ou l'équivalent (pour la préparation des étalons).
5.13
Flacons à échantillons pour l'analyseur automatique.
5.14
Fioles jaugées de 1 L.
6 Réactifs et matériel
6.1
Tous les réactifs doivent être, au minimum, de qualité réactif pour analyses.
Remarque : lorsque cela était possible, le numéro de registre des Chemical Abstracts [numéro CAS] a été ajouté entre crochets à la suite de chaque réactif.
6.2
Acide acétique - [64-19-7], qualité CLHP.
6.3
Brij-35 - [9002-92-0], 30 % p/v dans l'eau.
6.4
Sulfate cuivrique pentahydraté - [7758-99-8].
6.5
Sulfate d'hydrazine - [10034-93-2].
6.6
Acide chlorhydrique - [7647-01-0].
6.7
Méthanol - [67-56-1].
6.8
Dichlorhydrate de N-(napth-1-yl)éthylènediamine - [1465-25-4].
6.9
Acide orthophosphorique - [7664-38-2], à 98 %.
6.10
Nitrate de potassium - [7757-79-1].
6.11
Acétate de sodium anhydre - [127-09-3].
6.12
Hydroxyde de sodium - [1310-73-2].
6.13
Nitrite de sodium - [7632-00-0].
6.14
Sulfanilamide - [63-74-1].
6.15
Triton X-100 - [92046-34-9].
6.16
Eau de type I, tel que stipulé dans le tableau 1 de la méthode D1193 de l'ASTM, Processes for Reagent Water Production, Note A.
7 Préparation de la verrerie
7.1
Nettoyer et sécher la verrerie de manière à s'assurer qu'il n'y ait aucune contamination.
8 Préparation des solutions
Remarque : il se peut que les grands volumes de solution décrits dans ces préparations ne soient pas nécessaires si les volumes d'échantillons à analyser sont petits. Il est cependant important que les solutions préparées aient la bonne concentration.
8.1
Solution à 50 % de Triton X-100
8.1.1
Mélanger 50 mL de Triton X-100 avec 50 mL de méthanol. Transvaser dans une bouteille d'entreposage.
8.2
Réactif colorimétrique
8.2.1
Mettre 700 mL d'eau de type I dans une fiole jaugée de 1 L.
8.2.2
Ajouter 100 mL d'acide phosphorique concentré.
8.2.3
Dissoudre 40 g de sulfanilamide dans cette solution. Au besoin, chauffer pour que le produit se dissolve complètement.
8.2.4
Ajouter 2,0 g de dichlorhydrate de N-(napth-1-yl)éthylènediamine.
8.2.5
Laisser le mélange revenir à la température ambiante, ajouter 0,5 mL de Brij-35 et compléter avec de l'eau de type I.
8.2.6
Conserver dans une bouteille ambre à 4 °C. La solution est stable un mois.
8.3
Solution de sulfate de cuivre
8.3.1
Solution mère de sulfate cuivrique.
8.3.1.1
Dissoudre 1,25 g de sulfate cuivrique dans de l'eau de type I et diluer à 500 mL.
8.3.2
Verser 4,0 mL de la solution mère de sulfate cuivrique dans une fiole jaugée de 1 L contenant de l'eau de type I.
8.3.3
Ajouter 0,5 mL de Brij-35 et compléter avec de l'eau de type I.
8.4
Solution de sulfate d'hydrazine
8.4.1
Solution mère de sulfate d'hydrazine.
8.4.1.1
Dissoudre 25,0 g de sulfate d'hydrazine dans 800 mL d'eau de type I. Diluer à 1 L. Cette solution est stable pendant 6 mois si elle est conservée dans une bouteille ambre hermétique.
8.4.2
Dans une fiole jaugée de 1 L, mettre environ 900 mL d'eau de type I, puis y ajouter 36 mL de solution mère de sulfate d'hydrazine.
8.4.3
Ajouter 0,5 mL de Brij-35 et compléter avec de l'eau de type I.
8.4.4
Conserver dans une bouteille ambre. Cette solution est stable un mois.
8.5
Solution d'hydroxyde de sodium 0,2 N
8.5.1
Dissoudre 8,0 g d'hydroxyde de sodium dans environ 800 mL d'eau de type I.
8.5.2
Ajouter 0,5 mL de Brij-35, refroidir la solution et compléter à 1 L avec de l'eau de type I.
8.6
Tampon acétate (pH = 3,7)
8.6.1
Dissoudre 16,4 g d'acétate de sodium anhydre dans environ 300 mL d'eau de type I.
8.6.2
Ajouter 100 mL d'acide acétique, 1 mL de solution de Triton X-100 à 50 % et diluer à 1 L avec de l'eau de type I.
8.7
Solution pour la dialyse
8.7.1
Diluer 1 mL de Brij-35 à 1000 mL avec de l'eau de type I.
8.8
Solution pour l'extraction du tabac (acide acétique à 5 %)
8.8.1
Diluer 50 mL d'acide acétique glacial à 1000 mL avec de l'eau de type I.
8.9
Acide chlorhydrique 1,0 N
8.9.1
Dans une fiole jaugée de 1 L, mettre environ 800 mL d'eau de type I, puis verser avec précaution 83 mL d'acide chlorhydrique. Bien mélanger.
8.9.2
Laisser refroidir, puis diluer à 1000 mL avec de l'eau de type I.
8.9.3
Cette solution sert au nettoyage des conduites à sulfate de cuivre de l'analyseur automatique afin d'empêcher l'accumulation de cuivre d'un projet ou d'une série d'analyses à l'autre.
9 Préparations des étalons
9.1
Solution mère étalon de nitrate de potassium (2000 ppm d'azote)
9.1.1
Dissoudre 14,442 g de nitrate de potassium anhydre dans environ 800 mL de solution d'extraction à 5 % d'acide acétique (dans une fiole jaugée de 1 L).
9.1.2
Compléter avec la solution d'extraction à 5 % d'acide acétique.
9.2
Étalons de travail de nitrate de potassium
9.2.1
Prélever des volumes appropriés (de 0,20 à 3,0 mL) de solution mère étalon de nitrate de potassium et les diluer à 100 mL avec de la solution d'extraction, afin d'obtenir des étalons de travail ayant des concentrations d'azote (sous forme de nitrates) se situant dans les intervalles détaillés ci-dessous :
| Étalon no |
Volume (mL) de solution mère étalon de KNO3 | Volume final en mL |
Azote [ppm] |
|---|---|---|---|
| 0 | 0 | 100 | 0,0 |
| 1 | 0,2 | 100 | 4 |
| 2 | 0,5 | 100 | 10 |
| 3 | 1,0 | 100 | 20 |
| 4 | 2,0 | 100 | 40 |
| 5 | 3,0 | 100 | 60 |
Remarque : il peut être nécessaire de préparer d'autres étalons pour couvrir l'intervalle de réponses prévues avec les échantillons.
9.2.2
Préparer des solutions d'étalonnage fraîches tous les cinq jours.
9.3
Solution mère de nitrite de sodium (2000 ppm)
9.3.1
Dissoudre 9,852 g de nitrite de sodium anhydre dans environ 800 mL de solution d'extraction à 5 % d'acide acétique (dans une fiole jaugée de 1 L).
9.3.2
Compléter avec de la solution d'extraction à 5 % d'acide acétique.
9.4
Étalons de nitrite de sodium
9.4.1
Prélever 2,0 mL de solution mère de nitrite et les diluer à 100 mL avec la solution d'extraction afin d'obtenir un étalon à 40 ppm d'azote (sous forme de nitrite).
9.4.2
Utiliser immédiatement pour vérifier l'efficacité de réduction.
9.4.3
Préparer un étalon de nitrite frais suivant les besoins.
10 Échantillonnage
10.1
L'échantillonnage des cigarettes aux fins de tests doit être effectué conformément à la norme ISO 8243.
10.2
L'échantillonnage des kreteks, des petits cigares, des bidis, des bâtonnets de tabac aux fins des tests doit être effectué conformément à la norme ISO 8243, mais modifié en remplaçant le terme cigarettes par kreteks, petits cigares, bidis ou bâtonnets de tabac, pour lesquels le terme carton est équivalent à 200 unités.
10.3
L'échantillonnage des cigares aux fins des tests doit être effectué conformément à la norme ISO 8243, mais modifié en remplaçant le terme cigarettes par cigares, pour lesquels 200 unités de cigarettes est équivalent à 200 grammes de cigare.
10.4
L'échantillonnage du tabac à cigarette aux fins des tests doit être effectué conformément à la norme ISO 15592-1
10.5
L'échantillonnage des feuilles de tabac, du tabac à pipe et du tabac sans fumée aux fins des tests doit être effectué conformément à la norme ISO 15592-1, mais modifié en remplaçant le terme tabac à rouler par le terme feuilles de tabac, tabac à pipe ou tabac sans fumée.
11 Préparation des produits du tabac
11.1
Préparation de l'échantillon à analyser
11.1.1
Les produits du tabac à analyser doivent être préparés conformément à la méthode T-402.
11.1.2
Analyser les échantillons « tel que reçu » et, au besoin, effectuer une correction pour obtenir des résultats « en matière sèche », en mesurant la teneur en humidité du produit homogénéisé.
12 Préparation des échantillons
12.1
Extraction du tabac entier
12.1.1
Peser 0,5 g de l'échantillon à analyser dans un erlenmeyer en PMP de 125 mL, avec bouchon.
12.1.2
Ajouter 50 mL d'acide acétique à 5 % dans la fiole jaugée et la boucher.
12.1.3
Fixer le flacon sur l'agitateur oscillant et agiter pendant 15 minutes.
12.1.4
À l'aide d'un filtre-seringue relié à une seringue jetable de 5 mL, filtrer l'extrait de tabac entier directement dans un contenant pour échantillonneur automatique, correctement étiqueté.
13 Analyse des échantillons
13.1
Appareil d'analyse
13.1.1
Dispositif d'analyse en continu.
Remarque : ce dispositif est spécifique au système Technicon AutoAnalyzer. L'utilisation d'un système d'un autre fabricant peut nécessiter des débits et/ou des composants différents. Voir la figure 1.
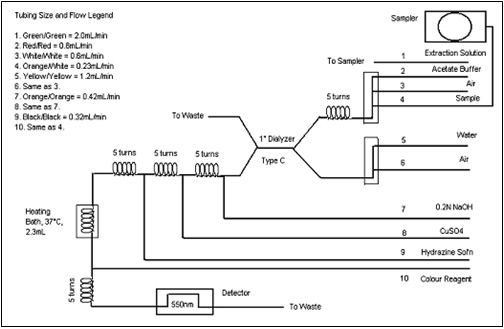
Figure 1 : diagramme typique du Technicon AutoAnalyzer : Équivalent textuel
La figure suivante est un organigramme schématique de l'autoanalyseur Technicon, qui intègre un détecteur et un bain chauffant connectés à la gauche du dialyseur primaire et un échantillonneur à la droite du dialyseur.
Taille des tubes et débits
- Vert/vert = 2,0 mL/minute
- Rouge/rouge = 0,8 mL/minute
- Blanc/blanc = 0,6 mL/minute
- Orange/blanc = 0,23 mL/minute
- Jaune/jaune = 1,2 mL/minute
- Comme en 3
- Orange/orange = 0,42 mL/minute
- Comme en 7
- Noir/noir = 0,32 mL/minute
- Comme en 4
- Solution d'extraction
- Tampon d'acétate
- Air
- Échantillon
- Eau
- Air
- NaOH 0,2N
- CuSO4
- Sol. d'hydrazine
- Réactif colométrique
13.1.2
Vérification de l'efficacité de réduction
L'efficacité de réduction de chaque solution de travail d'hydrazine doit être vérifiée. Faire cette vérification avec l'étalon à 40 ppm de nitrate et l'étalon de nitrite. Si la concentration apparente d'azote sous forme de nitrates (réponse) est bien plus faible que la concentration d'azote sous forme de nitrites, ajuster la solution de travail d'hydrazine en ajoutant des volumes de 1 mL de solution mère d'hydrazine, jusqu'à ce que les deux étalons donnent la même réponse.
13.1.3
Analyse en débit continu
13.1.3.1
Utiliser l'échantillonneur automatique de manière normale.
Exemple : avec une vitesse d'échantillonnage de 20 échantillons par heure et un rapport volume d'échantillon/volume de rinçage de 2 :1.
Remarque : les paramètres de fonctionnement peuvent varier en fonction de l'analyseur automatique utilisé.
13.1.4
Laisser assez de temps au système pour atteindre l'équilibre lorsqu'on pompe les liquides.
13.1.5
Charger les contenants d'échantillon sur l'échantillonneur automatique de manière à ce que les étalons soient les premiers analysés. Corriger ensuite la ligne de base.
13.1.6
Analyser les échantillons de nouveau, uniquement si la réponse obtenue est hors limite ou s'il y a eu un problème en cours d'analyse.
13.1.7
Faire la dialyse en ligne des échantillons.
13.1.8
Intercaler à intervalles réguliers des contenants d'échantillonnage ne contenant que la solution d'extraction à 5 % d'acide acétique pour permettre la correction de la ligne de base.
13.1.9
Se servir également de la solution d'extraction à 5 % d'acide acétique comme solution de rinçage.
14 Calculs
14.1
Courbe d'étalonnage
Préparer une courbe d'étalonnage de l'azote en rapportant la concentration de l'étalon en fonction de la hauteur du pic obtenu, puis calculer le facteur de réponse (FR).
14.2
Dosage des échantillons
Doser l'azote (sous forme de nitrates) présent dans les échantillons grâce à la méthode de l'étalon externe, en multipliant la hauteur du pic obtenu par le facteur de réponse (FR).
Azotenitrates (µg/mL) = Hauteuréch. × FR
14.3
Calcul de la teneur en azote (µg/g) sous forme de nitrates
Calculer automatiquement la teneur en azote (sous forme de nitrates) en µg/g, en utilisant le multiplicateur (volume total de dilution de l'échantillon d'origine (50 mL)) et le diviseur (poids initial de l'échantillon (0,5 g)) appropriés :

Figure 14.3 : Équivalent textuel
Azotenitrates (µg/g) = ppm d'azotenitrates (µg/mL) × 50 (mL)
divisé par
0,5 g d'échantillon
14.4
La teneur en azote (sous forme de nitrates) en mg/g est calculée ainsi :
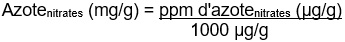
Figure 14.4 : Équivalent textuel
Azotenitrates (mg/g) = ppm d'azotenitrates (µg/g)
divisé par
1000 µg/g
14.5
Tous les résultats sont exprimés pour le tabac « tel que reçu ». Ils peuvent aussi être exprimés « en matière sèche » en utilisant le degré d'humidité déterminé.
14.6
Tous les résultats peuvent être rapportés sous forme de nitrates (mg/g) ou de nitrates (µg/g) en multipliant les résultats correspondants obtenus pour l'azote par 4,43 (le rapport de la masse de l'ion nitrate sur celle de l'azote). Les résultats peuvent aussi être exprimés en pourcentage (Nitrates (%)).
Nitrates (µg/g) = Azotenitrates (µg/g) × 4,43
Nitrates (mg/g) = Azotenitrates (mg/g) × 4,43

Figure 14.6 : Équivalent textuel
Nitrates (%) = Nitrates (µg/g) / 1 000 000 µg/g × 100
Nitrates (%) = Nitrates (µg/g) / 10 000
15 Contrôle de la qualité
15.1
Paramètres de contrôle typiques
Remarque : si les mesures de contrôle dépassent les limites de tolérance des valeurs prévues, il faut procéder à une étude appropriée et prendre les mesures qui s'imposent.
15.1.1
Blanc de réactifs (BR)
Chaque série d'analyse doit comprendre un blanc de réactifs (BR) afin de détecter toute contamination pouvant s'être produite lors de la préparation et de l'analyse des échantillons. Le BR est constitué de tous les réactifs utilisés pour exécuter l'analyse des échantillons, manipulés avec tout le matériel employé à cette fin. Le BR est analysé comme s'il s'agissait d'un échantillon.
15.1.2
Blanc fortifié (BF)
Chaque série d'analyse doit comprendre un blanc fortifié (BF) afin de détecter toute perte d'analytes pouvant s'être produite lors de la préparation et de l'analyse des échantillons. Le BF est constitué de tous les réactifs utilisés pour exécuter l'analyse des échantillons, manipulés avec tout le matériel employé à cette fin, et doit avoir été fortifié par l'ajout d'une quantité connue d'au moins un des analytes d'intérêt. Le degré de fortification doit refléter l'intervalle de résultats caractéristiques de l'échantillon. Le BF est analysé comme s'il s'agissait d'un échantillon.
15.1.3
Matrice fortifiée (MF)
Chaque série d'analyse doit comprendre une matrice fortifiée (MF) afin de détecter toute interférence provenant de la matrice. Lors de la préparation des échantillons et/ou pendant l'exécution des analyses, diviser un échantillon et fortifier une des portions avec une quantité connue d'au moins un des analytes d'intérêt. Le degré de fortification doit refléter l'intervalle de résultats caractéristiques de l'échantillon. La MF est analysée comme s'il s'agissait d'un échantillon.
15.1.4
Échantillon de contrôle
Afin d'évaluer la performance globale d'une méthode d'analyse, procéder à l'analyse d'un échantillon de contrôle. En utilisant des méthodes statistiques appropriées, comparer les résultats ainsi obtenus aux « valeurs prévues » obtenues dans le laboratoire ou, en l'absence de tels résultats, aux valeurs publiées dans la littérature. Le laboratoire obtiendra des données sur l'exactitude et la précision de la méthode d'analyse.
15.1.5
Échantillon-étalon
Pour évaluer la stabilité du système d'analyse, analyser un étalon comme s'il s'agissait d'un échantillon. En utilisant des méthodes statistiques appropriées, comparer les résultats obtenus aux concentrations prévues.
15.2
Taux de récupération et niveaux de contamination
15.2.1
Le BR typique donne une valeur de 0,01 ± 0,02 mg/g.
15.2.2
Le taux de récupération d'un BF typique se situe dans l'intervalle de 85 à 115 %.
15.2.3
Le taux de récupération d'une MF typique se situe dans l'intervalle de 90 à 120 %.
15.3
Limite de détection (LD) et limite de quantification (LQ)
15.3.1
La limite de détection (LD) est égale à trois fois l'écart-type des résultats obtenus en analysant l'étalon de plus faible concentration, au moins 10 fois pendant une période de plusieurs jours.
14.3.1.1
La valeur typique de la LD est de 0,15 mg/g de nitrate.
15.3.2
La limite de quantification (LQ) est égale à 10 fois l'écart-type des résultats obtenus en analysant l'étalon de plus faible concentration, au moins 10 fois pendant une période de plusieurs jours.
14.3.2.1
La valeur typique de la LQ est de 0,51 mg/g de nitrate.
15.4
Stabilité des réactifs
15.4.1
La solution mère de sulfate d'hydrazine est stable jusqu'à six mois dans une bouteille ambre très bien scellée, conservée à la température ambiante.
15.4.2
La solution de travail de sulfate d'hydrazine est stable jusqu'à un mois à la température ambiante.
15.4.3
Préparer la solution mère et les étalons de travail de nitrite de sodium quotidiennement, à cause de leur instabilité.
15.4.4
La solution de réactif colorimétrique au sulfanilamide est stable jusqu'à un mois si elle est conservée à 4 °C dans une bouteille ambre.
15.4.5
Préparer des solutions mères étalons de nitrate fraîches toutes les semaines.
15.4.6
Préparer des étalons de travail de nitrate et des solutions d'extraction fraîches toutes les semaines.
15.4.7
Analyser tous les échantillons dans les 48 heures, si les extraits sont conservés à la noirceur à 4 °C.
16 Références
16.1
Bran & Leubbe Inc., Technicon Industrial System Corp. Nitrate in Tobacco Extracts, Méthode industrielle no 838-87T, 1025 Busch Parkway, Buffalo Grove, Illinois, USA 60090 - 4516. Août 1987.
16.2
ASTM International, Méthode ASTM D1193-06(2011), Standard Specifications for Reagent Water.