Ligne directrice canadienne sur la biosécurité Évaluation des risques associés à l’agent pathogène

Télécharger le format de rechange
(Format PDF, 1.34 Mo, 52 pages)
Organisation : Agence de la santé publique du Canada
Date publiée : Avril 2018
Table des matières
- Préface
- Abréviations et sigles
- Chapitre 1 - Introduction
- Chapitre 2 - Principes de l'évaluation des risques associés à l'agent pathogène
- Chapitre 3 - Étapes d'une évaluation des risques associés à l'agent pathogène
- Chapitre 4 - Glossaire
- Chapitre 5 - Références et sources
Préface
Au Canada, les installations où sont manipulés et entreposés des agents pathogènes humains ou des toxines de groupe de risque 2, 3 et 4 sont réglementées par l’Agence de la santé publique du Canada (ASPC) en vertu de la Loi sur les agents pathogènes humains et les toxines (LAPHT) et du Règlement sur les agents pathogènes humains et les toxines (RAPHT). L’importation d’agents zoopathogènes, d’animaux infectés, de produits d’animaux, de sous-produits d’animaux (p. ex. des tissus ou du sérum), ou d’autres substances qui pourraient être porteuses d’un agent zoopathogène ou d’une partie de celui-ci (p. ex. une toxine) est réglementée par l’ASPC ou l’Agence canadienne d’inspection des aliments (ACIA) en vertu de la Loi sur la santé des animaux (LSA) et du Règlement sur la santé des animaux (RSA).
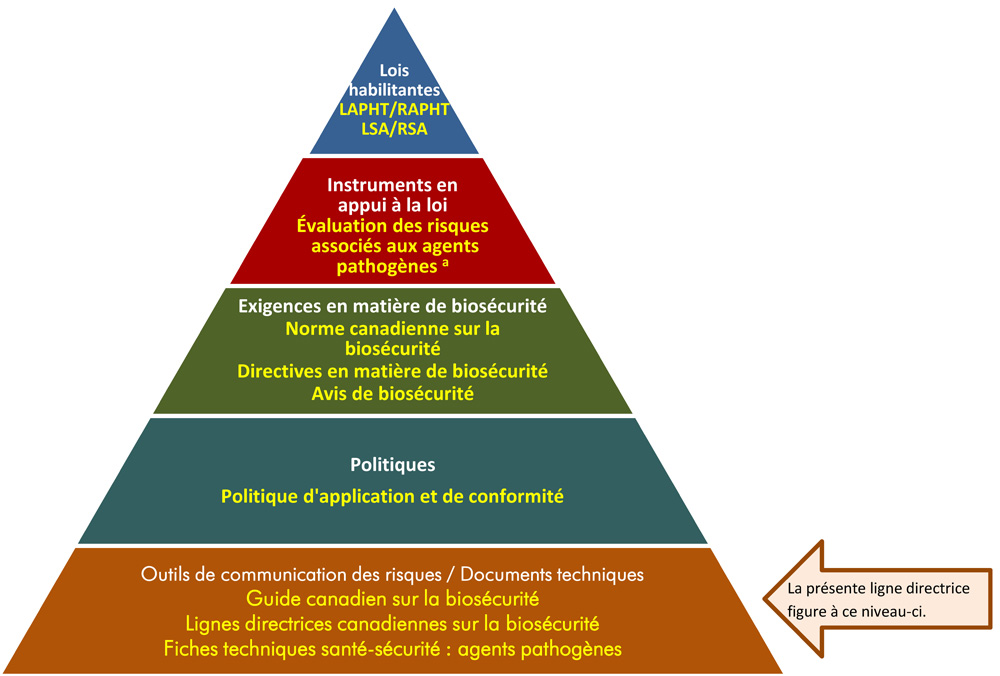
La figure suivante illustre la hiérarchie des documents qu’utilise l’ASPC pour surveiller les activités de biosécurité et de biosûreté. Chaque niveau de la pyramide correspond à un type de document. Les documents sont placés en ordre de priorité du haut de la pyramide vers le bas. La législation et les règlements se trouvent au sommet de la pyramide, car ce sont ces documents qui transmettent l’autorité légale à l’ASPC. Le matériel d’orientation et les éléments techniques se trouvent au bas de la pyramide, car ils sont uniquement destinés à résumer les recommandations et les informations scientifiques.
Figure 1 : La hiérarchie des documents en matière de biosécurité et de biosûreté de l’Agence de la santé publique du Canada
Équivalent textuel
Figure sous la forme d'une pyramide représentant la hiérarchie des documents utilisés par l'ASPC pour superviser les opérations de biosécurité et de biosûreté. Chacun des cinq niveaux de la pyramide correspond à un type de document, dont l'ordre de préséance augmente du bas vers le haut.
Au sommet, se trouve la législation habilitante, c'est-à-dire la LAPHT, le RAPHT, la LSA et RSA, qui transmet les autorités légales à l'ASPC. En-dessous des lois et des règlements figurent les Instrument à l'appui de la législation, et ceux-ci sont les évaluations des risques liés aux agents pathogènes. La prochaine étape est intitulée les Exigences en matière de biosécurité, notamment la Norme canadienne sur la biosécurité, les Directives en matière de biosécurité et les Avis de biosécurité. Le deuxième niveau du bas est Documents de politique, soit la Politique de conformité et d'application de la loi. Le matériel d'orientation et les pièces techniques trouvés au bas de la pyramide, sous l'en-tête des Outils de communication des risques et documents techniques, visent seulement à résumer les recommandations et les informations scientifiques. Il s'agit notamment du Guide canadien sur la biosécurité, des Lignes directrices canadiennes sur la biosécurité et des Fiches techniques santé-sécurité : agents pathogènes.
a) Les évaluations des risques associés à l’agent pathogène déterminent le groupe de risque de l’agent. Cette ligne directrice offre des directives exhaustives sur la façon d’effectuer une évaluation des risques associés à l’agent pathogène.
La ligne directrice des Évaluations des risques associés à l’agent pathogène a été élaborée par l’ASPC et l’ACIA dans le cadre d’une série de publications électroniques qui s’étendent sur les concepts liés à la biosécurité et la biosûreté présentés dans l’édition actuelle du Guide canadien sur la biosécurité (GCB), soit le document complémentaire à la Norme canadienne sur la biosécurité (NCB). Elle présente la méthodologie recommandée pour l’évaluation des risques associés aux agents pathogènes humains, aux agents zoopathogènes, aux toxines ou à toute autre matière infectieuse réglementée. Cette ligne directrice vise à aider les parties réglementées à satisfaire aux exigences énoncées dans la NCB, mais les informations qu’elle contient ne devraient pas être interprétées comme des exigences. Les parties réglementées peuvent choisir d’adopter différentes approches pour répondre aux exigences de la NCB.
Cette ligne directrice est un document en constante évolution et fait continuellement l’objet d’améliorations. L’ASPC et l’ACIA accueillent avec intérêt les commentaires, les clarifications et les suggestions visant l’amélioration des versions subséquentes de ce document. Veuillez envoyer toute information ou suggestion, accompagnées de références, le cas échéant, à l’adresse suivante :
Adresse courriel de l’ASPC : PHAC.pathogens-pathogenes.ASPC@canada.ca
Abréviations et sigles
- ABCSE
- Agent biologique à cote de sécurité élevée
- ACIA
- Agence canadienne d'inspection des aliments
- ASPC
- Agence de la santé publique du Canada
- ELR
- Évaluation locale des risques
- GCB
- Guide canadien sur la biosécurité
- GR
- Groupe de risque (c.-à-d. GR1, GR2, GR3, GR4)
- LAPHT
- Loi sur les agents pathogènes humains et les toxines
- LSA
- Loi sur la santé des animaux
- NCB
- Normes canadiennes sur la biosécurité
- RAPHT
- Règlement sur les agents pathogènes humains et les toxines
- RSA
- Règlement sur la santé des animaux
Chapitre 1 - Introduction
Les termes en caractères gras sont définis dans le glossaire du chapitre 4.
1.1 Portée
Les agents pathogènes sont classés par groupe de risque selon leurs caractéristiques inhérentes. Les agents pathogènes humains des groupes de risque 2 (GR2), GR3 et GR4 sont réglementés en vertu de la Loi sur les agents pathogènes humains et les toxines (LAPHT) et du Règlement sur les agents pathogènes humains et les toxines (RAPHT)Note de bas de page 1Note de bas de page 2. Tous les agents zoopathogènes sont réglementés en vertu de la Loi sur la santé des animaux (LSA) et du Règlement sur la santé des animaux (RSA)Note de bas de page 3Note de bas de page 4. Le groupe de risque aide à déterminer les exigences opérationnelles, les exigences minimales en matière de confinement physique et les exigences relatives aux vérifications et aux essais de performance applicables. Cependant, il peut y avoir des exigences supplémentaires ou différentes selon les activités spécifiques planifiées et, dans certains cas, en fonction des caractéristiques uniques de l’agent pathogène.
Les exigences opérationnelles, les exigences physiques en matière de confinement et les exigences relatives aux essais de vérification et de performance applicables pour les zones de confinement réglementées sont énoncées dans la Norme canadienne sur la biosécurité (NCB)Note de bas de page 5. Le Guide canadien sur la biosécurité (GCB) fournit des directives sur la manière de satisfaire aux exigencesNote de bas de page 6.
1.2 Aperçu
La ligne directrice de l’Évaluation des risques associés à l’agent pathogène offre des directives exhaustives sur la façon d’effectuer une évaluation des risques associés à l’agent pathogène sur des agents pathogènes n’ayant pas été caractérisés ou pouvant avoir été modifiés, afin de déterminer la probabilité et les conséquences d’exposition à l’agent pathogène ou de la libération de ce dernier. Cette ligne directrice est destinée à être utilisée conjointement avec la NCB, le GCB et le Modèle d’évaluation des risques associés à l’agent pathogène disponible sur le site Web du Gouvernement du CanadaNote de bas de page 7.
L’information présentée dans ce document n’existe qu’à titre indicatif et ne devrait pas être interprétée comme des exigences. Les parties réglementées peuvent choisir d’adopter d’autres approches pour satisfaire aux exigences énoncées dans la NCB.
Le processus d’évaluation des risques associés à l’agent pathogène sert à documenter les risques inhérents associés avec un agent pathogène et orientera l’élaboration des stratégies d’atténuation des risques. Le résultat final d’une évaluation des risques associés à l’agent pathogène dévoilera le groupe de risque de l’agent pathogène pour les humains et les animaux. Les renseignements recueillis lors de l’évaluation des risques associés à l’agent pathogène aideront à établir le niveau de confinement approprié pour les travaux impliquant l’agent pathogène en question et contribueront à l’élaboration d’évaluations locales des risques (ELR). C’est dans les ELR que les risques inhérents de l’agent pathogène sont évalués dans le contexte des activités entreprises.
1.3 Analyse des risques et évaluation des risques
Le but de la méthodologie d’évaluation des risques présentée dans ce document est d’identifier les facteurs de risque critiques permettant de déterminer le groupe de risque de l’agent pathogène, d’identifier les questions clés à répondre pour pleinement évaluer chaque facteur de risque, et de réduire la variabilité entre les opérateurs et dans une même évaluation. Une méthodologie rigoureuse permet d’assurer qu’une approche normalisée est utilisée pour que le résultat obtenu (c.-à-d. le groupe de risque) soit uniforme, peu importe la personne effectuant l’évaluation. L’évaluation des risques peut être très subjective, particulièrement lorsque les données sont limitées ou de nature variable. Bien que différents experts puissent tirer de différentes conclusions de l’analyse des mêmes données, l’expertise technique demeure la base de tout processus d’évaluation des risques.
1.3.1 Danger
Un danger est un élément, ou sa caractéristique, pouvant causer du tort aux humains ou à d’autres êtres vivants. Dans une évaluation des risques associés à l’agent pathogène, le danger est un microorganisme, une protéine ou un acide nucléique présentant le potentiel de causer du mal ou des effets néfastes sur la santé des humains ou des animaux (p. ex. infection, maladie, mort).
1.3.2 Risque
Le risque est une fonction de la probabilité qu’un événement indésirable survienne (p. ex. exposition à un agent pathogène) et la gravité des conséquences de cet événement (p. ex. infection, maladie, mort). Il doit y avoir une probabilité qu’un événement indésirable survienne et des conséquences pour qu’il existe un risque. S’il manque un des deux, il n’y a pas de risque.
1.3.3 Les principes de base de l’évaluation des risques
L’évaluation des risques est un mécanisme servant à déterminer la probabilité qu’un danger puisse causer du tort et le degré de ce tort. Les évaluations des risques sont fondées sur la science, les politiques et le jugement d’experts, et elles peuvent évoluer parallèlement à la progression du niveau de compréhension scientifique.
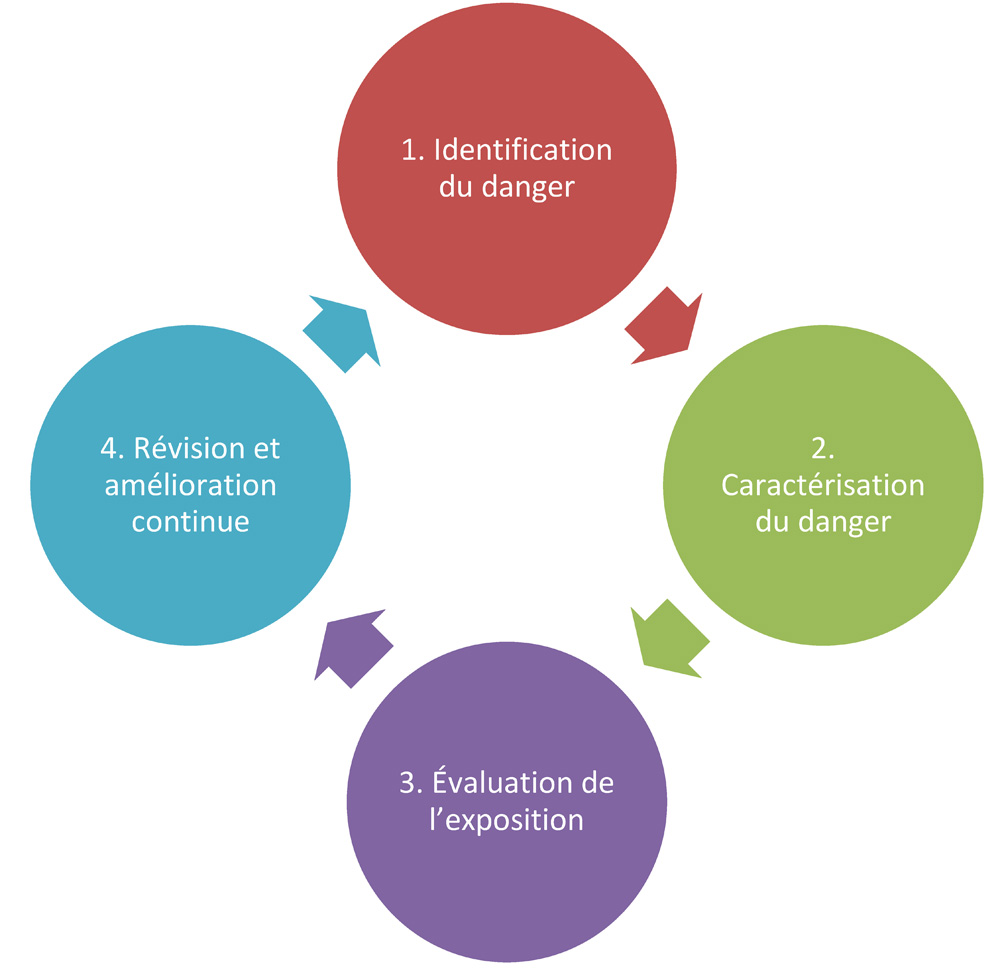
Dans un contexte de biosécurité, c’est souvent un agent pathogène qui constitue le danger. L’évaluation des risques vise à caractériser la probabilité qu’une exposition cause la maladie ainsi que la gravité de cette dernière. L’évaluation peut tenir compte des activités menées, des caractéristiques de l’agent pathogène et de la prévalence de l’agent pathogène dans l’environnement ou la communauté. L’évaluation des risques est un processus itératif comprenant quatre étapes : (1) l’identification du danger, (2) la caractérisation du danger, (3) l’évaluation de l’exposition et (4) la révision et l’amélioration continue (figure 1-1).
Figure 1-1 : Modèle de base d’évaluation des risques. Le modèle de base d’évaluation des risques comprend quatre étapes itératives : l’identification du danger, la caractérisation du danger, l’évaluation de l’exposition et l’amélioration continue.
Équivalent textuel
Figure illustrant la relation entre les quatre étapes itératives d'un modèle de base d'évaluation des risques, en commençant par l'identification du danger suivie de la caractérisation du danger suivie de l’évaluation de l'exposition suivie de l’amélioration continue qui complète le cycle se reliant à l’identification du danger.
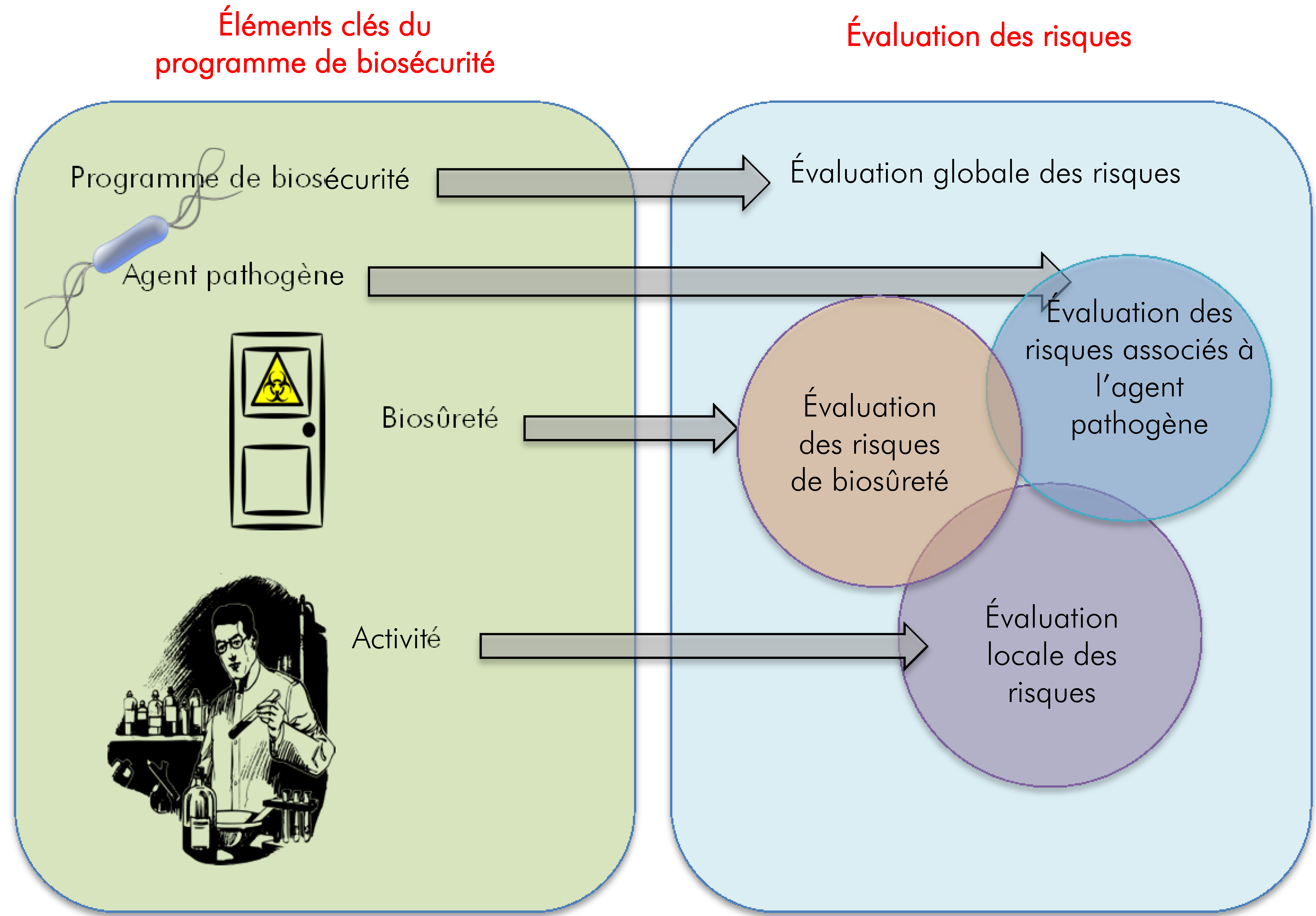
Plusieurs types d’évaluation des risques sont effectués pour appuyer le programme de biosécurité dans une organisation. La plus générale est l’évaluation globale des risques, qui couvre la gestion des risques et les stratégies d’atténuation qui s’appliquent au programme de biosécurité dans son ensemble. L’évaluation des risques associés à l’agent pathogène détermine le risque inhérent de l’agent pathogène, exprimé en termes de groupe de risque, ce qui aide à déterminer les exigences minimales en matière de confinement, qui sont énoncées dans la NCB. L’ELR tient compte non seulement des agents pathogènes ou des toxines utilisés, mais aussi des activités menées dans l’installation afin de déterminer si les stratégies d’atténuation en place sont suffisantes et appropriées. L’évaluation des risques de biosûreté élargit ces évaluations en tenant compte des risques liés à la perte, au vol, au mésusage, au détournement ou à la libération intentionnelle non autorisée d’agents pathogènes, de toxines ou d’autres ressources connexes. Ces évaluations des risques sont étroitement liées les unes aux autres, mais elles tiennent compte de différents aspects du risque. La figure 1-2 illustre la relation entre les éléments clés du programme de biosécurité et les types d’évaluation des risques correspondants.
Figure 1-2 : La relation entre les éléments clés du programme de biosécurité et les types d’évaluations des risques correspondants.
Équivalent textuel
Figure illustrant la relation entre les risques associés aux éléments clés du programme de biosécurité et les types d'évaluation des risques correspondants. Ceux-ci sont le programme de biosécurité lié à l'évaluation globale des risques; l’agent pathogène lié à l'évaluation des risques associés à l’agent pathogènes; la biosécurité liée à l'évaluation des risques de biosécurité; et l'activité liée à l'évaluation locale des risques. La figure présente également un chevauchement entre l'évaluation des risques associés à l’agent pathogène, l'évaluation des risques de biosécurité et l'évaluation locale des risques montrant qu'il y a aussi un lien entre ceux-ci. En outre, ces trois éléments font tous partie de l'évaluation globale des risques.
1.3.4 Groupes de risque
Les groupes de risque varient des agents pathogènes de GR1, qui posent un risque faible à l’individu et à la communauté, aux agents pathogènes de GR4, qui posent un risque élevé à l’individu et à la communauté (voir le tableau 1-1). Le groupe de risque est un élément essentiel à la détermination de la façon dont un agent pathogène doit être manipulé dans l’installation. Tous les agents pathogènes peuvent être classés dans des groupes de risque en fonction des résultats de l’évaluation des risques associés à l’agent pathogène. L’évaluation caractérise les risques associés à l’agent pathogène par l’examen approfondi de quatre facteurs de risque :
- la pathogénicité;
- la transmissibilité;
- les mesures de prévention et les mesures de traitement;
- l’effet sur la population animale (c.-à-d. gamme d’hôtes, aire de répartition naturelle et répercussions économiques).
La plupart des agents pathogènes se classeront clairement dans l’un des quatre groupes de risque. Le facteur de risque le plus important est la pathogénicité (c.-à-d. la capacité d’un agent pathogène à causer la maladie). Si un organisme est incapable de causer la maladie chez les humains ou les animaux, il est sans importance qu’il soit résistant aux traitements médicaux actuels. Les autres facteurs de risque sont importants à la compréhension du risque pour la communauté. Ils sont aussi particulièrement importants à la différenciation des agents pathogènes de GR3 et de GR4. Plus de renseignements sur les groupes de risque et les facteurs de risque sont disponibles au chapitre 4 du GCB.
| Groupe de risque | Risque pour l’individu | Risque pour la communauté | Exemple |
|---|---|---|---|
| GR1 | Aucun ou faible | Faible | Bactérie commensale |
| GR2 | Modéré | Faible | Escherichia coli pathogène |
| GR3 | Élevé | Faible | Bacillus anthracis |
| GR4 | Élevé | Élevé | Virus Ebola |
1.4 Comment utiliser la ligne directrice Évaluation des risques associés à l'agent pathogène
Au début de ce document figure une liste détaillée des abréviations et des sigles utilisés dans cette ligne directrice. Chaque terme ou nom est écrit au long à sa première apparition dans la ligne directrice, suivi immédiatement de son abréviation ou sigle entre parenthèses. Après cette définition initiale, l’abréviation ou le sigle est utilisé exclusivement dans tout le reste du document. Un glossaire complet des définitions des termes techniques est présenté au chapitre 4 de ce document. Les termes définis dans le glossaire apparaissent en caractères gras à leur première apparition dans la ligne directrice. Une liste de références et d’autres ressources est présentée au chapitre 5.
Chapitre 2 - Principes de l'évaluation des risques associés à l'agent pathogène
L’évaluation des risques associés à l’agent pathogène examine attentivement les facteurs de risque particuliers qui reflètent les caractéristiques inhérentes contribuant au risque que pose un agent pathogène aux humains et aux animaux. Le résultat d’une évaluation des risques associés à l’agent pathogène dévoile le groupe de risque, qui servira à déterminer les exigences physiques minimales en matière de confinement, les exigences opérationnelles et les exigences relatives aux essais de vérification et de performance pour la manipulation et l’entreposage sécuritaires de l’agent pathogène. Afin d’assurer l’intégrité de l’évaluation des risques associés à l’agent pathogène, il est essentiel d’établir et de communiquer les lacunes en matière de connaissances ainsi que toute hypothèse ayant été utilisée dans l’évaluation. De plus, toutes décisions et tous facteurs pris en compte lors de la prise de décisions doivent être documentés afin de maintenir la transparence dans le processus de l’évaluation des risques associés à l’agent pathogène.
2.1 L'évaluation quantitative des risques versus l'évaluation qualitative des risques
L’évaluation quantitative des risques implique d’attribuer des valeurs numériques fixes aux probabilités et aux conséquences. Elle a des exigences élevées par rapport aux données ainsi qu’une compréhension approfondie de la façon dont les probabilités et les conséquences se rapportent au risque global. Une approche quantitative est souvent utilisée pour répondre aux questions concernant, par exemple, le niveau sécuritaire d’exposition à un produit chimique ou la dose sécuritaire d’un médicament à l’intérieur d’une certaine marge d’erreur.
L’évaluation qualitative des risques utilise un langage descriptif ou des échelles d’intervalle pour évaluer les probabilités et les conséquences, et elle peut appliquer une relation de style mathématique ou matricielle pour déterminer le risque global. Ce type d’évaluation est utile pour trier les risques pour déterminer s’ils nécessitent une analyse plus approfondie ou pour catégoriser les risques dans des groupes distincts (p. ex. dans des groupes de risque). Contrairement aux évaluations quantitatives, les évaluations qualitatives peuvent être effectuées même lorsqu’il y a d’importantes lacunes dans les données. Les évaluations des risques associés à l’agent pathogène sont habituellement qualitatives puisqu’elles s’appuient typiquement sur des documents publiés, où l’information peut être variable ou même contradictoire et où il y a souvent d’importantes lacunes dans les données. En outre, une approche qualitative est appropriée puisque les résultats de l’évaluation des risques associés à l’agent pathogène sont une des quatre valeurs distinctes du groupe de risque (c.-à-d. GR1 à GR4).
2.2 Risque acceptable
L’absence de risque est généralement reconnue comme étant un but irréalisable et, par conséquent, plusieurs modèles d’évaluation des risques intègrent le concept du risque acceptable, aussi appelé « tolérance au risque ». Le risque acceptable est relié à la volonté d’une personne, d’une organisation ou de l’ensemble de la société d’accepter ou d’éviter un risque, et elle peut varier selon les circonstances. Le risque acceptable est établi en comparant les conséquences néfastes possibles aux facteurs qui déterminent si les individus ou les groupes au sein d’une société sont disposés à être soumis au risque. Par exemple, un risque peut être considéré comme « acceptable » s’il est compensé par un avantage considérable ou si le coût de réduction du risque est excessif comparé à l’avantage. En contraste, un risque peut être considéré comme « inacceptable » si les risques l’emportent sur l’avantage ou si le risque est excessivement élevé.
L’Agence de la santé publique du Canada (ASPC) a incorporé le concept du risque acceptable à la méthodologie d’évaluation des risques associés à l’agent pathogène, y compris dans les critères d’évaluation de chaque facteur de risque, et l’arbre décisionnel sur la façon dont ces critères déterminent le groupe de risqueNote de bas de page 7. En plus de déterminer le groupe de risque de l’agent pathogène, l’ASPC tient compte des facteurs spécifiques au scénario au cas par cas. Par exemple, lors d’une éclosion, l’ASPC peut délivrer un avis de biosécurité autorisant que certaines activités présentant un risque moindre soient menées selon de plus faibles exigences en matière de confinement, même si le groupe de risque ne change pas (p. ex. des activités de diagnostic impliquant un agent pathogène de GR3 peuvent être effectuées au NC2 avec des exigences supplémentaires spécifiques). Ceci pourrait permettre un diagnostic plus rapide, ce qui pourrait être avantageux pour les interventions globales en matière de santé publique ou animale.
2.3 Évaluation des risques fondée sur des données probantes
Autant que possible, les évaluations des risques associés à l’agent pathogène s’appuient sur une évaluation rigoureuse d’informations empiriques et actuelles. L’évaluation des risques associés à l’agent pathogène vise à maximiser l’objectivité par l’utilisation de données raisonnablement disponibles, l’adoption d’une méthodologie établie et l’application systématique et défendable du jugement d’experts. Les informations quantitatives devraient être utilisées lorsqu’elles sont disponibles et les informations qualitatives devraient être tirées de sources de confiance et évaluées par les pairs, telles que des journaux scientifiques réputés (p. ex. ayant un indice de citation élevé dans le domaine) et d’autres juridictions ou experts nationaux ou internationaux. Toute évaluation des risques associés à l’agent pathogène doit inclure une référence complète des sources utilisées, soit un élément fondamental pour démontrer l’intégrité scientifique de l’évaluation.
2.3.1 Qualité des données
La quantité et la qualité de l’information disponible sur l’agent pathogène influenceront la confiance dans les décisions prises durant l’évaluation des risques associés à l’agent pathogène. Les données de qualité supérieure comprennent l’information tirée d’essais cliniques et d’études normalisées (p. ex. éléments probants des examens systématiques d'essais cliniques randomisés et de méta-analyses). Les données de qualité inférieure comprennent les opinions d’experts et les articles sans références, telles que des sources Web ou des communications indépendantes. Les évaluations des risques devraient être révisées régulièrement lorsque de nouvelles informations deviennent disponibles, particulièrement si la qualité des données est inférieure. Une attribution adéquate des sources (c.-à-d. des références) viendra en aide au moment d’évaluer la qualité et la suffisance des données utilisées dans l’évaluation des risques.
Selon les types de sources de données utilisées et la suffisance de l’information disponible pour effectuer l’évaluation des risques associés à l’agent pathogène, la qualité des données (c.-à-d. le niveau de crédibilité de l’information) peut être estimée comme étant :
- Élevée : suffisante pour une analyse exhaustive de tous les éléments de l’évaluation des risques.
- Modérée : suffisante pour une analyse exhaustive de plusieurs éléments de l’évaluation des risques; quelques lacunes dans les données; quelques hypothèses avancées.
- Faible : insuffisante pour une évaluation des risques exhaustive; importante lacune dans les données; beaucoup d’hypothèses avancées.
2.4 Incertitudes et hypothèses
Au cours de l’évaluation des risques associés à l’agent pathogène, la présence d’incertitudes exigera inévitablement que des hypothèses soient avancées. Les évaluations des risques associés à l’agent pathogène devraient inclure un clair aperçu des lacunes en connaissances, des incertitudes et des hypothèses avancées afin de combler ces lacunes.
2.5 Principe de précaution
L’application du principe de précaution dans la prise de décisions fondées sur la science aux fins de protection de la santé humaine ou animale signifie simplement qu’un manque de certitude scientifique ne peut pas justifier un retard dans la prise de décision s’il existe un risque pouvant causer des dommages graves ou irréversiblesNote de bas de page 8.
En termes d’évaluation des risques associés à l’agent pathogène, l’application du principe de précaution signifie qu’une décision par rapport au groupe de risque doit toujours être prise, même lorsqu’il y a très peu ou pas d’information pour supporter une évaluation complète de tous les facteurs de risque. Concrètement, l’utilisation de données de substitution ou de preuves indirectes pour supporter les conclusions pourrait être nécessaire. De plus, une bonne compréhension de sa propre tolérance au risque peut avoir une incidence sur l’application du principe de précaution, car une tolérance au risque inférieure peut exiger des contrôles plus rigoureux.
Chapitre 3 - Étapes d'une évaluation des risques associés à l'agent pathogène
Toutes les évaluations de risque suivent essentiellement la même approche systématique qui inclue les quatre étapes suivantes, mises à jour pour refléter l’évaluation des risques associés à l’agent pathogène :
Identification du danger :
Identifier le microorganisme, la protéine ou l’acide nucléique capable de causer des effets néfastes sur la santé humaine ou animale. Ceci peut inclure le contexte historique, les caractéristiques physiques, la structure du génome, la taxonomie et d’autres caractéristiques d’identification.
Caractérisation du danger :
Une évaluation qualitative ou quantitative de la nature des effets néfastes sur la santé humaine ou animale associés au microorganisme, à la protéine ou à l’acide nucléique. Les agents infectieux peuvent être classés dans des groupes de risque bien définis.
Évaluation de l’exposition :
Une évaluation qualitative ou quantitative de la probabilité d’exposition à la substance infectieuse lors de sa manipulation directe, y compris l’évaluation de la relation dose-réponse lorsque c’est possible. Pour les évaluations des risques associés à l’agent pathogène, l’évaluation de l’exposition est directement liée aux zones de confinement (p. ex. laboratoire, salle animalière et box). Elle examine la relation entre les conséquences et la probabilité d’exposition, qui sont fondamentaux pour déterminer les exigences de confinement appropriées.
Révision et amélioration continue :
L’évaluation des risques associés à l’agent pathogène devrait être révisée régulièrement afin de déterminer les nouvelles informations concernant l’agent pathogène ou les mesures d’atténuation pouvant avoir une incidence sur le résultat de l’évaluation (p. ex. un nouvel hôte, l’évolution d’un agent pathogène, la disponibilité d’un nouveau traitement). Elle devrait aussi être révisée lorsque l’agent pathogène est modifié (p. ex. par manipulation génétique) afin de déterminer l’effet de la modification.
3.1 Identification du danger
Dans une évaluation des risques associés à l’agent pathogène, le danger est l’agent biologique faisant l’objet de l’enquête. L’évaluation débute avec la taxonomie de l’agent pathogène et son nom reconnu, qui peuvent être utiles pour déterminer s’il y a des exigences légales particulières associées à son utilisation. Par exemple, le travail impliquant des agents pathogènes zoonotiques qui causent aussi des maladies animales exotiques exige l’approbation de l’ASPC et de l’Agence canadienne d’inspection des aliments (ACIA).
Une brève description de l’agent pathogène devrait souligner les caractéristiques physiques pouvant être pertinentes à l’interprétation de l’évaluation des risques ou du risque général. Les facteurs possiblement pertinents incluent les suivants :
Informations générales
- La taxonomie et une brève description des sous-groupes, de la nomenclature précédente et des changements
- Le contexte historique
- La taille, la forme et la structure
- Les conditions de croissance idéales
- La structure du génome/les informations sur le génome
- Les modifications (p. ex. technologie « gene drive » et CRISPR)
Bactéries
- La motilité
- La sporulation
- La production de toxines
- Le besoin en oxygène
- La coloration de Gram, coloration par fuchsine acide
- L’activité enzymatique
Virus
- Le génome d’ARN ou d’ADN
- Le simple brin ou double brin
- La polarité positive ou la polarité négative
- Autres classifications (p. ex. arbovirus)
Autres (p. ex. champignons, prions, parasites)
- Le cycle vital
- La reproduction
- La morphologie
- La croissance et la physiologie
- La production de toxines
Les agents pathogènes reconstruits, conçus ou modifiés peuvent être évalués en comparant l’agent pathogène nouvellement créé à l’agent pathogène de type sauvage ou à un variant précédemment évalué. De cette façon, les diverses modifications peuvent être liées aux effets anticipés sur les différents facteurs de risque (p. ex. pathogénicité, transmissibilité). L’évaluation d’un organisme conçu ou modifié devrait tenir compte des risques que posent l’agent pathogène de type sauvage, des risques de la matière insérée et des risques combinés du produit.
3.1.1 Considérations relatives à la biosûreté
La biosûreté fait référence aux mesures de sécurité conçues pour prévenir l’accès non autorisé aux agents pathogènes, aux toxines et à d’autres ressources connexes (p. ex. personnel, équipement, matières non infectieuses et animaux) ou la perte, le vol, l’utilisation à mauvais escient ou la libération non autorisée de ceux-ci. Certains agents pathogènes et certaines toxines présentent un risque accru en matière de biosûreté en raison de la possibilité qu’ils soient utilisés comme arme biologique. Au Canada, ceux-ci sont qualifiés d’agents biologiques à cote de sécurité élevée (ABCSE). Les ABCSE sont identifiés en tant qu’agents pathogènes et toxines « précisés » à l’article 10 du RAPHTNote de bas de page 2. Cependant, même si l’agent pathogène n’est pas un ABCSE, il conviendrait de le signaler s’il apparaît sur d’autres listes d’agents biologiques susceptibles de provoquer des inquiétudes en matière de biosécurité. Ces listes incluent les Listes communes du Groupe Australie et la Select Agents and Toxins List (Liste des agents pathogènes et des toxines réglementées) des États-UnisNote de bas de page 9Note de bas de page 10.
3.2 Caractérisation du danger
La caractérisation du danger implique une analyse des quatre facteurs de risque clés étant les éléments déterminants essentiels du groupe de risque. Les facteurs de risque énumèrent de façon détaillée les caractéristiques inhérentes de l’agent pathogène contribuant au risque à l’individu ou à la communauté. Ces facteurs peuvent varier entre les humains et les animaux. Par exemple, bien que l’existence d’un vaccin efficace puisse freiner considérablement le risque à la population humaine, la vaccination systématique n’est pas courante pour les animaux et ainsi, elle ne représente pas un facteur de risque principal chez les animaux. Le tableau 3-1 donne un aperçu des facteurs de risque individuels.
| Facteur de risque | Humains | Animaux |
|---|---|---|
| Pathogénicité | Risque pour l’individu | Risque pour l’animal |
| Mesures de prévention et de traitement des expositions | Risque pour la communauté | Facteur non applicable pour les animaux |
| Transmissibilité | Risque pour la communauté | Risque pour la communauté |
| Répercussions sur la population animale (c.-à-d. gamme d’hôtes, aire de répartition naturelle et répercussions économiques) | Facteur non applicable pour les humains | Risque pour la communauté |
Chaque facteur de risque est évalué selon les réponses à une série de questions et la documentation des données complémentaires et des références connexes. Voilà les indicateurs des facteurs de risque. Par exemple, les indicateurs de la pathogénicité sont : (1) si l’agent pathogène peut causer une infection; (2) si l’agent pathogène peut causer une maladie aiguë; (3) si l’agent pathogène peut causer des séquelles sérieuses ou la mort; et (4) s’il y a des populations particulières à risque. Ces questions indicatrices soutiennent l’évaluation globale du facteur de risque (p. ex. pathogénicité faible, modérée ou élevée). Dans le Modèle d’évaluation des risques associés à l’agent pathogène disponible en ligne, les questions sur les indicateurs sont dans des encadrés blancs et la cote de facteur de risque est dans un encadré bleuNote de bas de page 7. Les cotes de facteur de risque sont utilisées conjointement avec l’arbre décisionnel pour déterminer le groupe de risque.
3.2.1 Pathogénicité
Le niveau de risque associé à la pathogénicité est le facteur déterminant de groupe de risque le plus important. Dans le cadre de l’évaluation des risques associés à l’agent pathogène, la pathogénicité désigne la proportion des personnes et des animaux exposés connaissant un taux de morbidité ou de mortalité important. La pathogénicité est composée de deux éléments distincts : (1) l’infectiosité, ou la proportion des personnes et des animaux exposés développant une infection, avec ou sans maladie, et (2) la virulence, ou la proportion des personnes et des animaux connaissant un taux de morbidité ou de mortalité important. Une partie de la terminologie couramment utilisée pour indiquer la pathogénicité est décrite ci-après.
Lors de l’évaluation des indicateurs de pathogénicité chez les animaux, il est important de tenir compte du ou des hôtes animaux naturels (plutôt qu’expérimentaux) ou de l’hôte chez qui l’agent pathogène est couramment trouvé. L’information sur les infections chez des hôtes inhabituels et, à un moindre degré, chez des hôtes infectés de manière expérimentale devrait être révisée de façon critique afin de déterminer si elle représente ce qu’il pourrait se passer dans la nature. La section 3 du Modèle d’évaluation des risques associés à l’agent pathogène illustre la façon dont les indicateurs de facteur de risque de la pathogénicité et la cote de facteur de risque sont tabulésNote de bas de page 7.
3.2.1.1 Infection
Une infection désigne la situation où un organisme (p. ex. une bactérie) croît et assure sa survie à l’intérieur d’un autre organisme (p. ex. un humain). L’infection pourrait être associée à des signes de maladie ou non. Par exemple, le taux d’infection pour les bactéries commensales est extrêmement élevé, mais la plupart de ces bactéries sont complètement inoffensives pour leurs hôtes. L’exposition à l’organisme, ainsi que la capacité de l’organisme à causer une infection et à provoquer une maladie par la suite, sont des considérations essentielles dans l’évaluation de la pathogénicité. Par exemple, quelques cas de maladie d’une bactérie commensale ubiquitaire (c.-à-d. taux d’exposition élevé, taux d’infection faible) pourraient être une preuve de faible pathogénicité, alors que quelques cas de maladie pour un agent pathogène très rare (c.-à-d. taux d’exposition faible, taux d’infection faible) pourraient être une preuve de pathogénicité modérée ou élevée.
3.2.1.2 Mortalité
La mortalité signifie simplement la mort. Le taux de mortalité constitue le nombre de décès dans une population donnée lors d’une période déterminée (=décès/population/temps). Afin de pleinement évaluer un taux de mortalité, il est important de tenir compte de l’incidence (=nouveaux cas/population/temps), la prévalence (=cas/population/temps), le taux d’attaque (=infecté/exposé), le taux de décès (=décès/infectés) et le taux de mortalité propre à une population (p. ex. une population jeune ou vieille, de femmes enceintes, de personnes âgées, gravement malade ou immunodéprimée). Le taux de mortalité propre à une population est appelé taux de mortalité clinique (p. ex. les décès dans une population de cas donné, comme les personnes et les animaux présentant une affectation concomitante) et dans certains cas, la mortalité est exclusivement associée aux populations à risque, telles que celles gravement malades ou immunodéprimées.
3.2.1.3 Morbidité
La morbidité signifie être atteint d’une maladie. Bon nombre des termes employés pour comprendre la mortalité peuvent aussi être utilisés pour évaluer la morbidité. L’évaluation des risques associés à l’agent pathogène sépare les signes de maladie en deux catégories : (1) aigu (effets immédiats ou à court terme), et (2) chronique (séquelles ou effets à long terme).
Effet aigu
L’effet immédiat réfère aux conditions aiguës ou aux signes et symptômes de maladie survenant à court terme (p. ex. en quelques jours ou semaines). Un effet immédiat faible représente des signes de maladie minimaux. Les personnes et les animaux affectés présentent des symptômes, mais ces derniers ne nuisent pas aux capacités normales de l’hôte et peuvent s’estomper d’eux-mêmes (p. ex. toux, mal de gorge, légère fièvre). Un effet immédiat modéré représente des signes évidents de maladie. Les personnes et les animaux affectés sont capables de fonctionner, mais de façon limitée (p. ex. peuvent devoir être alités ou s’absenter du travail). Un effet immédiat élevé représente des signes de maladie importants. Les personnes et les animaux affectés ne sont pas capables de fonctionner (p. ex. peuvent devoir être hospitalisés, s’absenter du travail pour des périodes prolongées; ou, dans les cas extrêmes, une aide mécanique peut être nécessaire ou la mort peut être imminente). Dans certains cas, l’effet immédiat est exclusivement associé aux populations à risque, telles que celles gravement malades ou immunodéprimées.
Effet chronique
Les effets à long terme représentent les signes et les symptômes de maladie persistant ou survenant à long terme (p. ex. pendant des mois ou des années). Les effets faibles à long terme représentent des signes ou des symptômes bénins à long terme qui ne nuisent pas aux capacités normales des hôtes (p. ex. feux sauvages, petites cicatrices). Les effets modérés à long terme représentent des signes et des symptômes qui nuisent aux capacités normales de l’hôte (p. ex. un certain degré d’immobilité, graves migraines, perte de mémoire). Les effets élevés à long terme représentent des signes ou des symptômes à long terme qui rendent l’hôte incapable de fonctionner normalement (p. ex. dommages irréversibles aux reins ou au foie, perte d’un des cinq sens, cancer). Dans certains cas, les effets à long terme sont exclusivement associés à des populations à risque, telles que celles gravement malades ou immunodéprimées.
3.2.1.4 Cote de facteur de risque
La cote de facteur de risque pour la pathogénicité est fondée sur la gravité de la maladie chez l’hôte. « Nul » désigne des agents biologiques ayant été déterminés comme non-pathogènes. Dans ce cas, aucun autre facteur de risque n’a besoin d’être évalué et le résultat de l’évaluation des risques sera GR1. « Faible » désigne des agents pathogènes opportunistes ayant rarement été associés à des maladies chez des personnes ou des animaux en bonne santé à la suite de circonstances exceptionnelles (p. ex. l’introduction d’une bactérie intestinale commensale dans la circulation sanguine à la suite d’une blessure pénétrante). « Faible » peut aussi désigner des agents pathogènes causant des maladies exclusivement chez les humains ou les animaux gravement malades ou immunodéprimés. « Modéré » désigne des agents pathogènes capables de causer des maladies graves, mais étant peu susceptibles de le faire, alors qu’« élevé » désigne des agents pathogènes étant susceptibles de causer des maladies graves.
3.2.1.5 Évaluer la pathogénicité à l’aide de données de substitution
Puisque la pathogénicité est l’élément déterminant de groupe de risque le plus important, elle doit être estimée en utilisant des données de substitution s’il n’y a pas suffisamment d’information pour l’évaluer. Cela peut inclure des preuves provenant d’animaux ou d’agents pathogènes apparentés sur le plan génétique et des preuves indirectes fondées sur l’exposition. Lorsqu’il n’est pas clair si un agent biologique est non-pathogène ou s’il n’a simplement pas eu la possibilité de causer une maladie chez les hôtes susceptibles, deux scénarios peuvent se présenter :
- Un microorganisme est identifié dans un environnement où les humains ou les animaux sont très susceptibles d’avoir été exposés (p. ex. des champignons trouvés sur des plantes consommées par les humains et les animaux);
- Un microorganisme est identifié dans un environnement où son exposition à un humain ou à un animal est peu probable (p. ex. des souches d’agents pathogènes adaptées en laboratoire exclusivement utilisées en confinement ou des isolats environnementaux de régions isolées).
Dans le premier cas, l’absence de cas de maladie conjuguée à l’exposition probable peut être utilisée en tant que preuve indirecte de non-pathogénicité. Dans le deuxième cas, la possibilité que le microorganisme puisse causer la maladie, mais que les hôtes susceptibles n’aient jamais été exposés, ne peut pas être rejetée et la pathogénicité ne peut pas être estimée « faible ». Lorsque la pathogénicité est estimée plutôt qu’évaluée, il est critique d’également souligner les incertitudes et les hypothèses avancées. Cela facilitera les révisions routinières lorsque de nouvelles informations deviendront disponibles.
3.2.2 Mesures de prévention et de traitement en matière d’exposition
L’accès à des traitements préventifs et thérapeutiques efficaces peut réduire les risques que pose un agent pathogène à l’individu et à la communauté. Les mesures de prévention constituent des interventions médicales pratiquées avant que l’exposition ait lieu afin de prévenir ou d’amoindrir les effets d’infection et de maladie (p. ex. prophylaxie ou vaccins préventifs). Les mesures de traitement constituent des interventions médicales pratiquées après l’exposition afin de prévenir l’infection ou d’amoindrir les effets d’infection ou de maladie (p. ex. prophylaxie post-exposition, traitement thérapeutique). Ce facteur de risque est surtout pertinent pour évaluer le risque pour la communauté humaine, car les interventions médicales de grande envergure pour prévenir ou traiter la maladie infectieuse ne sont pas fréquentes pour la population animale. Même s’il n’y a pas de cote de facteur de risque pour la protection de la population animale, les informations sur la disponibilité de mesures de prévention et de traitement efficaces devraient être prises en note et pourraient être précieuses pour l’ELR. La section 4 du Modèle d’évaluation des risques associés à l’agent pathogène illustre la façon dont les mesures sont classifiées afin d’évaluer la protection de la communautéNote de bas de page 7.
3.2.2.1 Immunité collective
La plupart des interventions médicales varient en efficacité et en disponibilité, laissant ainsi la communauté seulement partiellement protégée. En théorie, si la mesure préventive était complètement efficace et appliquée universellement, le risque général pour la population serait considérablement réduit ou même éliminé. Afin de déterminer si la communauté serait complètement protégée si l’agent pathogène était introduit dans la population, le concept du seuil d’immunité collective peut être appliqué.
Une mesure préventive complètement efficace serait presque efficace à 100 % dans la prévention de l’infection chez les personnes immunisées auparavant (c.-à-d. vaccinées), même si de multiples immunisations étaient nécessaires afin d’atteindre ce niveau de protection. Une mesure préventive appliquée universellement serait administrée au moins au pourcentage de la population nécessaire pour atteindre l’immunité collective. Voir l’exemple de la polio dans l’encadré suivant.Note de bas de page 11
Le concept du seuil d’immunité collective, par lequel une population peut être protégée selon le nombre d’individus immunisés, peut être calculé en tant que niveau critique de vaccination (Vc), oùNote de bas de page 12 :
Vc = (1-1/R0)/E, où R0 est le taux de reproduction de base, et E est l’efficacité du vaccin contre la transmission. Le taux de reproduction de base est le nombre total de cas secondaires générés par un individu infectieux typique lorsque le reste de la population est susceptible (c.-à-d. au début d’une nouvelle éclosion).
L’exemple de la polio
Un exemple d’agent pathogène qui pourrait être considéré comme « complètement évitable » est le virus poliomyélite (ou la polio). En 2013, le taux de vaccination contre la polio au Canada était de 91 % chez les enfants en âge de recevoir les quatre doses de vaccin recommandéesNote de bas de page 11. L’efficacité (E) du vaccin est de 95 % après trois doses et de 100 % après quatre doses. Le taux de reproduction de base (R0) est estimé à entre 4 et 7.
Voici un calcul prudent de l’immunité collective :
Vc = (1 - 1/7)/0,95
= 0,90 ou 90 %
L’immunité collective est de 90 %. Puisque 91 % de la population ont été vaccinée, l’immunité collective est accomplie.
Puisque les taux de vaccination varient au fil du temps, l’affaiblissement de l’immunité collective peut exiger que ce facteur de risque soit réévalué périodiquement afin de déterminer si le virus de la polio satisfait toujours à ces critères.
3.2.3 Transmissibilité
La transmissibilité est le facteur de risque à la communauté le plus important. Elle n’a pas seulement des effets sur le groupe de risque du microorganisme, mais aussi sur plusieurs exigences physiques et opérationnelles requises pour sa manipulation dans l’installation. Cela implique d’examiner les voies d’infection, ou la façon dont l’agent pathogène s’introduit dans l’hôte (p. ex. par inhalation, ingestion, injection, exposition des muqueuses), afin de déterminer la probabilité de la transmission directe ou indirecte. La possibilité que l’agent pathogène puisse se transmettre des humains aux animaux est aussi évaluée, même si la transmission d’un humain à l’autre et d’un animal à l’autre auront probablement l’effet le plus important sur le risque pour la communauté humaine ou animale, respectivement.
La voie principale par laquelle l’agent pathogène se transmet naturellement d’un individu à l’autre est appelée la « voie privilégiée ». Dans l’évaluation des risques associés à l’agent pathogène, une seule voie d’infection « privilégiée » devrait être sélectionnée, mais un agent pathogène peut avoir plusieurs autres voies « possibles ». La facilité de transmission par les différentes voies d’infection doit être analysée en combinaison afin de déterminer la probabilité que l’agent se transmette d’un hôte à l’autre par la transmission directe ou indirecte. Par exemple, si la seule voie d’infection (c.-à-d. privilégiée) est l’injection, le risque pour la communauté serait vraisemblablement faible. Cependant, le risque pour la communauté pourrait être plus important s’il était possible pour l’agent pathogène d’être aussi transmis par vecteurs ou par inhalation. Ce facteur de risque réfère seulement à la transmission d’un humain à l’autre ou d’un animal à l’autre, et non aux transmissions entre humains et animaux ou provenant de sources environnementales. Les zoonoses et les infections provenant de sources environnementales devraient être notées et considérées lors de la détermination des mesures de confinement efficaces, mais ne devraient pas être incluses dans les résultats de facteurs de risque de transmissibilité.
Les agents pathogènes nouveaux et émergents peuvent poser des risques uniques à la communauté ainsi qu’à la préparation et l’intervention en cas de pandémie. Par exemple, un agent pathogène émergent facilement transmissible avec un potentiel pandémique pourrait avoir une incidence importante sur la préparation et l’intervention en cas de pandémie. Si ces agents pathogènes étaient libérés dans la communauté, on s’attendrait à un nombre élevé de cas, un lourd fardeau imposé aux soins de santé et des coûts importants associés aux interventions médicales et aux effets sur la santé. Cet indicateur doit être revu régulièrement, particulièrement si l’agent pathogène s’établissait dans la population, puisque les risques précédents ou présents durant les premières phases de l’éclosion d’un agent pathogène émergent sont considérablement différents de ceux associés à un agent pathogène établi comme démontré dans l’exemple suivantNote de bas de page 13.
L’exemple de l’influenza
Le virus de la grippe A/H1N1 de 2009 a eu un effet immédiat et important sur la santé humaine et sur l’économie lorsqu’il est apparu pour la première fois. Il s’est rapidement propagé depuis son point d’origine, causant une pandémie mondiale et coûtant des milliards de dollars en intervention en matière de santé. Même si le nouveau virus entraînait généralement des symptômes semblables à ceux de la grippe saisonnière, les groupes d’âge inférieur avaient tendance à présenter des symptômes plus sévèresNote de bas de page 13. Par conséquent, le virus a été évalué initialement comme un agent pathogène de GR3. Une fois que cette souche s’était établie dans la population et que la souche pandémique avait été incorporée dans les campagnes de vaccination de la grippe saisonnière autour du monde, l’effet a diminué et la grippe A/H1N1 (2009) a été réévaluée en tant qu’agent pathogène de GR2.
Il convient d’informer l’ASPC ou l’ACIA de tout agent pathogène émergent n’ayant pas déjà été évalué par l’une de ces deux agences, car d’autres communications pourraient s’avérer nécessaires. Si un agent pathogène émergent est identifié, mais ne figure pas sur la liste du Portail de biosûreté, l’ASPC peut en être informée par courriel à l’adresse : PHAC.pathogens-pathogenes.ASPC@canada.ca
3.2.4 Effet sur la population animale (c.-à-d. gamme d’hôtes, aires de répartition naturelle et répercussions économiques)
Introduire un agent pathogène dans la population animale pourrait avoir un effet important sur la santé animale et l’économie. La gamme d’hôtes, l’aire de répartition naturelle et les répercussions économiques sont des indicateurs portant sur les répercussions de la libération d’un agent pathogène dans la population animale.
3.2.4.1 Gamme d’hôtes
La gamme d’hôtes est le nombre et la variété d’hôtes qu’un agent pathogène peut infecter. Seuls les hôtes naturels devraient être inclus dans le dénombrement des espèces. Les facteurs élargissant la gamme d’hôtes incluent des stratégies de transmission augmentant le contact avec de nouveaux hôtes (p. ex. vecteurs), une grande variabilité génétique et une réplication rapide. Un agent pathogène restreint à plusieurs espèces hôtes étroitement apparentées peut ne pas être aussi adaptable qu’un agent pathogène capable d’infecter des espèces de multiples familles ou d’ordres taxonomiques lointainement apparentés. Un agent pathogène capable d’infecter des espèces hôtes lointainement apparentées exigera des mécanismes divers pour entrer dans l’hôte et produire un effet pathogène, alors qu’un agent pathogène avec un niveau élevé de spécificité d’hôte peut avoir des mécanismes d’infection très particuliers. Francisella tularensis, par exemple, est considéré comme ayant une des plus larges gammes d’hôtes chez les agents pathogènes bactériens, et est retrouvé chez plus de 300 espèces, y compris les mammifères, les invertébrés, les oiseaux et les amphibiensNote de bas de page 14. Plusieurs virus sont capables d’infecter des espèces hôtes de plusieurs ordres, et ce fait est étroitement lié avec l’utilisation de vecteurs comme mode de transmissionNote de bas de page 15. Inversement, les virus principalement transmis par contact étroit sont plus susceptibles d’être limités à quelques espèces spécifiques chez lesquelles ce type de contact peut se produire.
3.2.4.2 Aire de répartition naturelle
L’aire de répartition naturelle d’un agent pathogène est importante pour déterminer l’effet sur la communauté animale si l’agent était libéré de son confinement. La libération d’un agent pathogène qui ne se trouve pas au Canada et dont ses espèces hôtes y sont présentes poserait un risque considérablement plus grand à la population qu’un agent pathogène déjà présent au Canada.
L’aire de répartition naturelle, ou l’endémicité, tient compte du fait qu’un agent pathogène soit déjà en circulation (c.-à-d. transmission naturelle) ou non dans un pays, une région ou une population humaine ou animale en particulier. La population affectée présentera habituellement un certain niveau de résistance ou d’immunité aux agents pathogènes endémiques. Si un agent pathogène non endémique entrait dans une région ou une population où il ne s’était pas établi, il aurait le potentiel de pénétrer une nouvelle population hôte (c.-à-d. naïve) et poserait un risque sérieux si le nouvel hôte offrait des conditions favorables à la reproduction et la transmission de l’agent pathogène.
Les agents pathogènes endémiques peuvent aussi, bien sûr, causer des éclosions graves dans les élevages. Ils peuvent être transmis par divers modes; ainsi, il est important de caractériser la fréquence de contact et les méthodes par lesquelles ils peuvent être transmis (p. ex. par contact direct entre animaux vivants, ou indirect par véhicules de transport, ramasseurs de cadavres d’animaux, vétérinaires et techniciens animaux) afin de déterminer le niveau de risque associé avec la libération de l’agent pathogèneNote de bas de page 16.
De plus, un changement dans un environnement favorable pour un agent pathogène endémique (p. ex. qui lui permet d’élargir sa gamme d’hôtes ou sa pathogénicité) peut conduire à l’émergence de nouvelles maladies infectieuses résultant d’un changement dans les paramètres immunitaires, écologiques ou comportementaux de l’hôte ou de l’agent pathogèneNote de bas de page 17.
3.2.4.3 Répercussions économiques
Au Canada, l’infection de certaines populations animales entraînerait de plus graves conséquences économiques. L’ACIA a classé les animaux selon leur valeur économique pour le Canada comme suit :
- Industries où le bétail a la plus grande valeur : bovine, équine, porcine, avicole, des crustacés et des poissons à nageoires sauvages ou en élevage.
- Industries où le bétail a une valeur moyenne : des petits ruminants (p. ex. ovin et caprin), apicole, des mollusques et d’autres ruminants en élevage (p. ex. cervidés, bisons).
- Industries où le bétail a la plus petite valeur et animaux autres que le bétail : des lagomorphes (p. ex. lapins), des animaux de compagnie (p. ex. chiens, chats), des reptiles, des amphibiens, des rongeurs et des primates.
Remarque : Les maladies d’importance considérable pour la santé animale ou l’économie canadienne sont habituellement des maladies animales exotiques ou à déclaration obligatoire (c.-à-d. l’infection par un agent zoopathogène non indigène), et peuvent être sous l’autorité de l’ACIA.
3.2.5 Classification par groupe de risque
Le groupe de risque global de l’organisme peut être déterminé en utilisant les évaluations des facteurs de risque présentés ci-haut (c.-à-d. la pathogénicité, les mesures de prévention et de traitement, transmissibilité, l’effet sur la population animale) et les arbres décisionnels de groupe de risque pour les humains et les animaux dans la section 8 du Modèle d'évaluation des risques associés à l'agent pathogèneNote de bas de page 7.
3.3 Évaluation de l'exposition
Dans le contexte de la biosécurité, l’évaluation de l’exposition prendra lieu : (1) lors de l’établissement des exigences physiques et opérationnelles en matière de confinement, qui sont énoncées dans la NCB; et (2) lors des ELR. Les deux visent à prévenir l’exposition de ceux qui travaillent avec des agents pathogènes et la libération d’agents pathogènes de la zone de confinement.
3.3.1 L’évaluation classique de l’exposition
L’évaluation classique des risques pour la santé implique habituellement une évaluation de l’exposition au niveau de la population et elle peut impliquer une modélisation dose-réponse, un suivi de données, des modèles et des estimations ou des données sur la persistance et l’accumulation d’une substance. Ces types d’évaluation d’exposition sont instrumentaux dans plusieurs évaluations des risques pour la santé, surtout lorsqu’il faut déterminer le niveau d’exposition « sécuritaire » à une substance particulière. Dans le cas de l’évaluation des risques associés à l’agent pathogène, les relations classiques entre l’exposition et l’intervention n’existent normalement pas pour les raisons suivantes :
- Le niveau d’exposition « sécuritaire » à un agent pathogène est à un niveau de moins que la dose infectieuse. Souvent, la dose infectieuse d’un agent pathogène n’est pas connue, et, pour les agents pathogènes, l’effet de l’exposition est généralement « tout ou rien ». L’infection a lieu ou non, tout simplement.
- La dernière étape de l’évaluation des risques associés à l’agent pathogène est l’identification du groupe de risque, ce qui aidera à déterminer les exigences minimales en matière de confinement pour la manipulation et l’entreposage sécuritaires de l’agent pathogène. Ceci limite l’utilisation d’une analyse de dose-réponse, puisque le but de l’évaluation des risques associés à l’agent pathogène est de prévenir l’exposition dans la zone de confinement en fonction des risques que pose l’agent pathogène, en adoptant des contrôles physiques et opérationnels spécifiques.
- Même s’il existe une série de lignes directrices d’essais harmonisées pour évaluer les effets toxiques de produits chimiques (p. ex. ceux provenant de l’Organization for Economic Cooperation and Development et de l’Office of Pollution Prevention and Toxics), il n’y a généralement pas suffisamment d’études normalisées sur les effets pathogènes d’organismes. Il existe peu de lignes directrices harmonisées pour évaluer les agents pathogènes, et celles qui existent sont incapables de capturer l’ensemble des effets pathogènes potentiels.
3.3.2 Incorporer les concepts d’exposition dans le processus d’évaluation des risques
L’évaluation de l’exposition se fait non seulement lorsque les exigences physiques et opérationnelles minimales en matière de confinement sont établies, mais aussi lorsque les ELR sont effectuées. Le groupe de risque d’un agent pathogène aide à déterminer le niveau de confinement auquel il doit être manipulé; cependant, l’ELR est essentielle pour mieux définir et atténuer les risques spécifiques à l’activité. De cette façon, l’évaluation de l’exposition à un agent pathogène influence le niveau de confinement et les exigences connexes énoncées dans la NCB, ainsi que les ELR effectuées dans l’installation.
Dans certains cas, l’ASPC ou l’ACIA peuvent réduire de façon proactive les exigences en matière de confinement pour un agent pathogène particulier. Par exemple, un agent pathogène capable de causer des maladies graves chez l’humain et qui répond à la définition d’un agent pathogène de GR3, mais qui est faiblement transmissible ou qui n’est pas transmissible dans l’air peut être manipulé de manière sécuritaire avec des exigences physiques réduites en matière de confinement, mais avec des exigences opérationnelles supplémentaires. L’ASPC a élaboré des directives en matière de biosécurité pour des agents pathogènes particuliers afin de définir ces exceptions et toutes les exigences supplémentaires en matière de biosécurité. Une partie réglementée qui détermine par une ELR que certaines activités impliquant un agent pathogène peuvent être effectuées de façon sécuritaire à un niveau de confinement inférieur doit attendre l’approbation de l’ASPC ou de l’ACIA avant d’apporter la modification.
La majorité des exigences opérationnelles et certaines exigences physiques en matière de confinement dans la NCB dépendent des activités effectuées ou de la nature des agents pathogènes utilisés (c.-à-d. en fonction d’une ELR). De cette manière, des scénarios d’exposition particuliers nécessitant l’utilisation de contrôles physiques ou opérationnels pour prévenir l’exposition et la libération peuvent être considérés (p. ex. l’utilisation d’une enceinte de sécurité biologique [ESB] lors du travail avec des agents pathogènes transmissibles par voie aérienne ou pour des procédures pouvant générer des aérosols infectieux).
Les activités menées dans des zones de confinement peuvent être divisées approximativement entre activités in vivo, qui représentent le plus grand risque, et activités in vitro; chacune de ces activités présente des risques différents, comme le risque supplémentaire de morsures, de griffures et d’excrétion d’agents pathogènes lors du travail impliquant des animaux. Les activités in vitro peuvent être davantage subdivisées en activités à culture et en activités sans culture (p. ex. l’extraction d’ADN). Les activités in vitro sans culture posent un risque plus faible et sont les plus susceptibles d’être permises d’être réalisées avec des exigences réduites en matière de confinement.
Si les exigences physiques en matière de confinement pour une partie ou l’ensemble des activités impliquant un agent pathogène venaient à être réduites ou modifiées, l’information serait communiquée sous la forme d’une directive en matière de biosécurité ou d’un avis de biosécurité, disponibles sur le site Web du Gouvernement du CanadaNote de bas de page 18.
L’exemple du virus de l’immunodéficience humain (VIH)
Le VIH est capable de causer des maladies graves et, ultimement, mortelles chez l’humain. Il est classifié en tant qu’agent pathogène humain de GR3. Le VIH est un agent pathogène à diffusion hématogène pouvant être transmis par l’exposition des muqueuses lors de contacts intimes. Il n’est pas aéroporté et il ne peut pas survivre très longtemps hors de l’hôte. Le scénario d’exposition le plus plausible pour le VIH dans une installation est par exposition percutanée accidentelle (p. ex. blessure par piqûre d’aiguille). Étant donné que les mesures physiques et d’ingénierie supplémentaires pour le niveau de confinement 3 (NC3) n’offrent pas de protection accrue contre le VIH, une directive en matière de biosécurité a été élaborée pour souligner la façon dont le VIH peut être manipulé au NC2 de manière sécuritaireNote de bas de page 18.
3.4 Autres considérations
3.4.1 Classification internationale
Il est recommandé, pour une évaluation des risques associés à l’agent pathogène, d’évaluer la façon dont le résultat s’aligne au paysage international. Même s’il y a une certaine variabilité dans les évaluations du groupe de risque des agents pathogènes par les organes directeurs internationaux, les groupes de risque sont généralement les mêmes. Si l’identification du groupe de risque diffère considérablement du paysage international, il pourrait être opportun de revoir l’évaluation pour en déterminer la raison. Dans plusieurs cas, la désignation du groupe de risque peut refléter la juridiction locale dans laquelle l’évaluation est effectuée. Par exemple, un pays où un agent pathogène particulier n’est pas endémique pourrait prescrire un groupe de risque plus élevé qu’un pays où l’agent est endémique. De même, si le vecteur pour un agent pathogène particulier n’est pas présent au Canada ou ne peut pas y survivre, le risque peut être plus faible que dans d’autres pays ayant un climat plus favorable.
3.5 Révision et amélioration continue
Bien qu’il n’y ait aucune période de temps spécifique assignée pour la révision de l’évaluation des risques associés à l’agent pathogène, il est fortement recommandé que cette dernière soit révisée régulièrement, puisqu’elle constitue un processus en évolution continue.
L’évaluation des risques associés à l’agent pathogène doit être révisée et mise à jour lorsque :
- de nouvelles données sont disponibles;
- l’agent pathogène ou la communauté a changé (p. ex. atténuation naturelle, atténuation par manipulation en laboratoire, immunité collective, vaccination, modification génétique);
- les conditions d’utilisation ont changé (p. ex. nouveau modèle animal, première utilisation d’une souche de laboratoire sur un animal);
- un nouveau vecteur apparaît dans une région;
- une maladie devient rare ou disparaît.
Chacun de ces scénarios a le potentiel de changer le groupe de risque, les exigences en matière de confinement, l’ELR ou tous les trois.
Chapitre 4 - Glossaire
La liste suivante renferme les termes employés dans cette ligne directrice accompagnés de leur définition tirée du GCB. Il est important de souligner que, bien que certaines des définitions fournies dans le glossaire soient universellement reconnues, beaucoup d’entre elles ont été établies expressément pour le GCB et la NCB. Par conséquent, certaines définitions pourraient ne pas s’appliquer aux installations qui échappent à la portée du GCB et de la NCB. Une liste exhaustive des termes et leurs définitions est offerte dans le glossaire du GCB.
- Agent pathogène
- Microorganisme, acide nucléique ou protéine ayant la capacité de causer une maladie ou une infection chez l’humain ou l’animal. Des exemples d’agents pathogènes humains figurent aux annexes 2 à 4 et à la partie 2 de l’annexe 5 de la Loi sur les agents pathogènes humains et les toxines, mais ils ne constituent pas une liste exhaustive; des exemples d’agents zoopathogènes peuvent être trouvés sur le site Web de l’Agence canadienne d’inspection des aliments.
- Agent zoopathogène
- Agent qui cause des maladies chez les animaux, qu’il soit issu de la biotechnologie ou non. Dans le Guide canadien sur la biosécurité, le terme « agent zoopathogène » ne réfère qu’à un agent qui cause des maladies chez les animaux terrestres, y compris chez les oiseaux et les amphibiens; toutefois, ce terme ne s’applique pas aux agents qui causent des maladies chez les animaux aquatiques ou les invertébrés.
- Agent zoopathogène non indigène
- Agent pathogène qui provoque une maladie animale figurant sur la liste « Maladies, infections et infestations de la Liste de l’OIE » (révisée régulièrement) de l’Organisation mondiale de la santé animale et qui est considéré comme allogène au Canada (c.-à-d. que cet agent causant des maladies animales exotiques ne se retrouve pas au pays). Ces agents pathogènes peuvent être dévastateurs en ce qui concerne la santé de la population animale canadienne.
- Aire de répartition naturelle
- L’aire géographique dans laquelle un agent pathogène est normalement présent.
- Biosécurité
- Ensemble des principes, des technologies et des pratiques liés au confinement mis en œuvre pour prévenir l’exposition involontaire à des matières infectieuses et à des toxines, ou leur libération accidentelle.
- Biosûreté
- Ensemble des mesures visant à prévenir la perte, le vol, le mésusage, le détournement ou la libération intentionnelle d’agents pathogènes, de toxines ou d’autres ressources liés à l’installation (p. ex. le personnel, l’équipement, les matières non infectieuses, les animaux).
- Communauté
- Englobe à la fois la population humaine (c.-à-d. le public) et la population animale.
- Confinement
- Ensemble de paramètres de conception physique et de pratiques opérationnelles visant à protéger le personnel, le milieu de travail immédiat et la communauté contre toute exposition à des matières biologiques. Dans le même contexte, on utilise aussi le terme « bioconfinement ».
- Danger
- Toute source (chose ou situation) ayant le potentiel de causer du dommage, du mal ou des effets néfastes pour les personnes ou d’autres êtres vivants. Dans une évaluation des risques associés à l’agent pathogène, le danger est un microorganisme, une protéine ou un acide nucléique pouvant produire une infection et mener à la maladie chez les humains ou les animaux.
- Endémique
- Trouvé régulièrement dans une région géographique définie ou dans une population humaine ou animale particulière.
- Évaluation des risques associés à l’agent pathogène
- Détermination du groupe de risque et des exigences liées au confinement physique et aux pratiques opérationnelles nécessaires pour manipuler de façon sécuritaire les matières infectieuses ou les toxines concernées.
- Évaluation des risques de biosûreté
- Évaluation des risques qui consiste à répertorier et à classer par ordre de priorité les agents pathogènes, les toxines, les matières infectieuses et les autres ressources (p. ex. l’équipement, les animaux, les renseignements) présents dans une installation, à définir les menaces et les risques associés à ces matières, ainsi qu’à déterminer les stratégies d’atténuation appropriées afin de prévenir le vol, le mésusage, le détournement ou la libération intentionnelle de ces matières.
- Évaluation globale des risques
- Évaluation générale qui soutient le programme de biosécurité dans son ensemble et qui peut englober plusieurs zones de confinement au sein d’un établissement ou d’une organisation. Les stratégies d’atténuation et de gestion des risques tiennent compte du type de programme de biosécurité nécessaire pour prévenir l’exposition du personnel aux agents pathogènes et aux toxines ainsi que la libération de ceux-ci.
- Évaluation locale des risques (ELR)
- Évaluation propre à un endroit en particulier réalisée pour repérer les dangers associés aux activités menées ainsi qu’aux matières infectieuses ou aux toxines utilisées. Cette évaluation permet d’élaborer des stratégies d’atténuation des risques et des stratégies de gestion des risques sur lesquelles on se fondera pour apporter des modifications relativement au confinement physique et aux pratiques opérationnelles dans l’installation concernée.
- Exigence opérationnelle
- Mesure ou procédure administrative appliquée dans une zone de confinement pour protéger le personnel, l’environnement et, ultimement, la communauté contre les matières infectieuses et les toxines, comme on l’énonce au chapitre 4 de la Norme canadienne sur la biosécurité.
- Exigences physiques en matière de confinement
- Mesures d’ingénierie et exigences relatives à la conception de l’installation visant à créer une barrière physique pour protéger le personnel, l’environnement et, ultimement, la communauté contre les agents pathogènes et les toxines, comme on l’énonce au chapitre 3 de la Norme canadienne sur la biosécurité.
- Exposition
- Contact ou proximité étroite avec des matières infectieuses ou des toxines pouvant respectivement causer une infection ou une intoxication. Les voies d’exposition sont l’inhalation, l’ingestion, l’inoculation et l’absorption.
- Facteur de risque
- Une caractéristique d’un agent pathogène liée au risque qu’il pose aux individus ou au public. Quatre facteurs de risque clés sont pris en considération au cours de l’évaluation des risques associés à l’agent pathogène.
- Gamme d’hôtes
- Une mesure du nombre et de la variété d’hôtes qu’un agent pathogène peut infecter.
- Groupe de risque (GR)
- Groupe dans lequel les matières biologiques sont classées en fonction de leurs caractéristiques inhérentes, comme la pathogénicité, la virulence, le risque de propagation et l’existence d’un traitement prophylactique ou thérapeutique efficace. Le groupe de risque énonce le risque pour la santé du personnel et du public ainsi que la santé des animaux et des populations animales.
- Hôte
- Organisme abritant, étant infecté par ou nourrissant un autre organisme. Ceux-ci peuvent inclure l’hôte définitif (primaire), l’hôte intermédiaire (secondaire), l’hôte réservoir et l’hôte final.
- Installation
- Structure, bâtiment ou aire définie à l’intérieur d’une structure ou d’un bâtiment dans lesquels sont manipulées ou entreposées des matières infectieuses ou des toxines. Il peut s’agir d’un laboratoire de recherche, d’un laboratoire de diagnostic, d’une aire de production à grande échelle ou d’une zone où l’on héberge des animaux. Ce terme désigne également une succession de pièces ou un bâtiment contenant plusieurs de ces aires.
- Immunité collective
- La réduction dans le risque d’infection chez les personnes susceptibles dans une population engendré par la proportion d’individus immunisés.
- Laboratoire
- Installation même ou aire située à l’intérieur d’une installation dans laquelle on manipule des matières biologiques à des fins scientifiques ou médicales.
- Libération
- Rejet de matières infectieuses ou de toxines hors du système de confinement.
- Maladie
- Trouble structural ou fonctionnel touchant un humain ou un animal vivant, ou une partie du corps de ceux-ci. Les maladies sont causées par une infection ou une intoxication et se manifestent généralement par des signes et des symptômes caractéristiques.
- Mesures de prévention
- Interventions médicales pratiquées avant que l’exposition ne se produise dans le but de prévenir l'infection ou d’amoindrir l’effet de l’infection ou de la maladie (p. ex. prophylaxie préexposition ou vaccination).
- Mesures post-exposition
- Interventions médicales pratiquées après l’exposition dans le but de prévenir l'infection ou de réduire l’effet de l’infection ou de la maladie (p. ex. prophylaxie post-exposition, traitements thérapeutiques).
- Mode de transmission
- Le moyen par lequel un agent infectieux se déplace vers un hôte (c.-à-d. contact direct, contact indirect, simple contact, microgouttelettes aérosolisées, transmises par l’air, injection, transmission vectorielle, et inhalation).
- Niveau de confinement (NC)
- Exigences minimales liées au confinement physique et aux pratiques opérationnelles visant la manipulation sécuritaire de matières infectieuses et de toxines dans les laboratoires, les zones de production à grande échelle et les environnements de travail avec des animaux. Il existe quatre niveaux de confinement, allant du niveau de base (niveau de confinement 1 [NC1]) au niveau le plus élevé (niveau de confinement 4 [NC4]).
- Pathogénicité
- Capacité d’un agent pathogène de causer une maladie chez un hôte humain ou animal.
- Répercussions économiques
- Le coût financier de la libération d’un agent pathogène ou d’une toxine d’une zone de confinement et inclut, sans s’y limiter, les coûts associés à la perte de cultures vivrières et de bétail, et les répercussions économiques en lien avec les restrictions commerciales.
- Risque
- La fonction de la probabilité qu’un événement indésirable survienne (p. ex. exposition à un agent pathogène) et la gravité des conséquences de cet événement (p. ex. infection, maladie, mort).
- Toxine (microbienne)
- Substance toxique produite par un microorganisme, ou dérivée de celui-ci, qui peut avoir des effets graves sur la santé humaine ou animale. Les toxines sont énumérées à l’annexe 1 et à la partie 1 de l’annexe 5 de la Loi sur les agents pathogènes humains et les toxines.
- Vecteur
- Organisme servant de véhicule pour transporter et transmettre un agent infectieux d’un hôte à l’autre, et étant nécessaire à une partie du cycle de croissance de l’agent infectieux. Plus couramment, les vecteurs sont des arthropodes ou des petits mammifères.
- Voie d’infection
- La voie par laquelle une matière infectieuse s’introduit dans un hôte. Tout en s’en distinguant, la voie d’infection est liée au mode de transmission, qui est le moyen par lequel un agent pathogène se déplace vers l’hôte.
- Zone de confinement
- Espace physique qui répond aux exigences liées à un niveau de confinement donné. Il peut s’agir d’une salle unique (p. ex. laboratoire de niveau de confinement 2 [NC2]), d’une série de salles situées dans un même endroit (p. ex. plusieurs espaces de travail en laboratoire de NC2 non adjacents, mais verrouillables) ou d’une série de salles adjacentes (p. ex. salles de niveau de confinement 3 [NC3] comprenant des aires réservées au travail en laboratoire et des salles animalières ou des box séparés). La zone de confinement peut comprendre des zones réservées au soutien, notamment des sas équipés de douches, de vestiaires « propres » et de vestiaires « sales », le cas échéant.
- Zoonose
- Maladie transmissible entre des humains et des animaux vivants. Les zoonoses comprennent les anthropozoonoses (c.-à-d. les maladies transmises des animaux aux humains) et les zooanthroponoses, aussi appelées zoonoses inversées (c.-à-d. les maladies transmises des humains aux animaux).
Chapitre 5 - Références et sources
Notes de bas de page
- Note de bas de page 1
Loi sur les agents pathogènes humains et les toxines (L. C. 2009, ch. 24). (2015).
- Note de bas de page 2
Règlement sur les agents pathogènes humains et les toxines (DORS/2015-44). (2015).
- Note de bas de page 3
Loi sur la santé des animaux (L. C. 1990, ch. 21). (2015).
- Note de bas de page 4
Règlement sur la santé des animaux (C.R.C., ch. 296). (2015).
- Note de bas de page 5
Gouvernement du Canada. (2015). Norme canadienne sur la biosécurité, 2e éd., Ottawa, ON, Canada : Gouvernement du Canada.
- Note de bas de page 6
Gouvernement du Canada. (2016). Guide canadien sur la biosécurité, 2e éd., Ottawa, ON, Canada : Gouvernement du Canada.
- Note de bas de page 7
Gouvernement du Canada. Modèle d'évaluation des risques associés à l'agent pathogène. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/biosecurite-biosurete-laboratoire/fiches-techniques-sante-securite-agents-pathogenes-evaluation-risques/modele-evaluation-risques-agent-pathogene.html
- Note de bas de page 8
Gouvernement du Canada. (2003) Cadre d'application de la précaution dans un processus décisionnel scientifique en gestion du risque. Consulté le 10 août 2017 à l'adresse http://www.pco-bcp.gc.ca/index.asp?lang=fra&page=information&sub=publications&doc=precaution/precaution-fra.htm
- Note de bas de page 9
Groupe Australie. List of Human and Animal Pathogens and Toxins for Export Control. Consulté le 10 août 2017 à l'adresse
http://www.australiagroup.net/en/human_animal_pathogens.html- Note de bas de page 10
Federal Select Agents Program des États-Unis. Select Agents and Toxins List. Consulté le 10 août 2017 à l'adresse
https://www.selectagents.gov/SelectAgentsandToxinsList.html- Note de bas de page 11
Gouvernement du Canada. (2016). Couverture vaccinale des enfants canadiens : points saillants de l'Enquête nationale sur la couverture vaccinale des enfants de 2013 (ENCVE). Consulté le 31 octobre 2017 à l'adresse https://www.canada.ca/fr/sante-publique/services/publications/vie-saine/couverture-vaccinale-enfants-canadiens-points-saillants-enquete-nationale-couverture-vaccinale-enfants-2013.html
- Note de bas de page 12
Fine, P., Eames K., et Heymann, D.L. (2011) « Herd Immunity» : A Rough Guide. Clinical Infectious Diseases », 52 (7):911–916.
- Note de bas de page 13
Van Kerkhove, M., Vandemaele, K., Shinde, V., Jaramillo-Gutierrez, G., Koukounari, A. et al. (2011). Risk factors for severe outcomes following 2009 Influenza A (H1N1) infection: A Global Pooled Analysis. PLOS Medicine, 8(7). Consulté le 24 octobre 2017 à l'adresse http://www.who.int/influenza/surveillance_monitoring/Risk_factors_H1N1.pdf
- Note de bas de page 14
Peterson, J.M., et Molins, C.R. (2010). Subpopulations of Francisella tularensis ssp. Tularensis and holarctica: identification and associated epidemiology, Future Microbiology, 5 (4):649-61.
- Note de bas de page 15
Pederson, A.B., Altizer, S., Poss, M., Cunningham, A.A., et Nunn, C.L. (2005) Patterns of host specificity and transmission among parasites of wild primates, International Journal of Parasitology, 35(6):647-57.
- Note de bas de page 16
Sternberg Lewerin, S., Osterberg, J., Alenius, S., Elvander, M., Traven, T. et coll. (2015). Risk assessment as a tool for improving external biosecurity at farm level, BMC Veterinary Research, 11:171.
- Note de bas de page 17
Rachowicz, L.J., Hero, J.M., Alford, R. A., Taylor, J.W., Morgan, J.A.T., et coll. (2005). The novel and endemic pathogen hypotheses: Competing explanations for the origin of emerging infectious diseases of wildlife, Conservation Biology, 19(5):1441-1448.
- Note de bas de page 18
Gouvernement du Canada. Directives, avis et avis spéciaux en matière de biosécurité. Disponible à l'adresse https://www.canada.ca/fr/sante-publique/services/biosecurite-biosurete-laboratoire/directives-avis-avis-speciaux-matiere-biosecurite.html