Effets secondaires suivant l’immunisation (ESSI) Rapport du troisième trimestre de 2016 (1er juillet – 30 septembre)
Résumé de l’évaluation de l’innocuité pour le troisième trimestre :
- Aucun signal préoccupant concernant l’innocuité des vaccins n’a été observé au cours du troisième trimestre (T3) de 2016.
- Ce rapport présente les 532 déclarations d'ESSI reçues périodiquement des autorités de la santé publique fédéral, provinciales et territoriales durant le troisième trimestre.
Contexte
Les vaccins sont étroitement surveillés au Canada à toutes les phases du « cycle de vie » du produit vaccinal, depuis sa découverte jusqu’à l’autorisation de mise en marché (avant commercialisation) et au-delà, à mesure que les gens commencent à les utiliser (après commercialisation). De nombreux intervenants participent à diverses activités liées à l’évaluation et la surveillance de l’innocuité des vaccins, y compris le gouvernement fédéral, les autorités de santé publique provinciales, territoriales et locales, les fournisseurs de soins de santé, l’industrie des vaccins et le public. Les programmes d’immunisation provinciaux et territoriaux effectuent le suivi des ESSI et les déclarent à l’Agence de la santé publique du Canada (l’Agence). L’Agence assure une surveillance de l’innocuité après la mise en marché par l’intermédiaire du Système Canadien de Surveillance des Effets Secondaires Suivant l’Immunisation (SCSESSI). Les signaux préoccupants des vaccins sont surveillés et adressés par l’intermédiaire du Groupe de travail sur la vaccinovigilance (GTVV).
Un effet secondaire suivant l’immunisation (ESSI) est défini comme étant tout événement médical fâcheux qui se produit à la suite de l’administration d’un vaccin et qui n’a pas nécessairement de lien causal avec celui-ci. Un effet secondaire suivant l’immunisation peut donc correspondre à un signe défavorable ou non intentionnel, à un résultat de laboratoire anormal, à un symptôme ou à une maladie. Selon la définition de l’Organisation mondiale de la Santé (OMS), les ESSI graves sont les effets secondaires qui menacent le pronostic vital, entraînent l’hospitalisation, le prolongement de l’hospitalisation, une invalidité permanente ou marquée, une malformation congénitale ou la mort. Les ESSI ne répondant pas à la définition d’effet grave sont classifiées comme non graves.
L’OMS définit un signal préoccupant concernant l’innocuité des vaccins comme un élément d’information (provenant d’une ou de plusieurs sources) qui indique l’existence d’un nouveau lien de causalité potentiel ou d’un nouvel aspect d’un lien de causalité connu, entre une vaccination et un effet secondaire précédemment inconnu ou insuffisamment documenté, susceptible de nuire à la santé. Des études épidémiologiques sont généralement nécessaires à l’évaluation du lien de causalité entre le vaccin et le signe de préoccupation. L’objectif principal de la surveillance après commercialisation des vaccins est de déceler les préoccupations concernant leur innocuité. Ces préoccupations comprennent une possible augmentation de la gravité ou de la fréquence des ESSI attendus, ou encore, la survenue d’un ou de plusieurs événements inattendus (c.-à-d. un effet secondaire suivant l’immunisation qui ne correspond pas aux renseignements ou à l’étiquette sur le produit canadien). Cela permet aux vaccinateurs et aux fournisseurs de programme de vaccination de santé publique de prendre des mesures dans le domaine de la santé publique :
- au niveau de la personne (p. ex. une enquête plus poussée afin de confirmer un diagnostic et de déterminer les causes possibles, une consultation en vue d’écarter la possibilité d’une allergie à un ou à plusieurs composantes du vaccin, ou une décision d’administrer ou non des doses subséquentes du vaccin), ou
- au niveau du programme de vaccination (p. ex. une enquête menée sur un ensemble d’effets secondaires, un examen des procédures pour s’assurer que les exigences relatives à l’entreposage des vaccins ont été rigoureusement suivies, ou encore un changement de politique permettant d’adopter un vaccin moins réactogène).
L’Agence partage aussi les données sur les ESSI avec la Direction générale des produits de santé et des aliments de Santé Canada, l’organisme de réglementation national pour les vaccins au Canada. Des mesures officielles liées aux vaccins commercialisés au Canada peuvent ainsi être prises, au besoin. Il peut s’agir de diffuser des communications aux vaccinateurs ou au public par rapport à la préoccupation en matière d’innocuité ou d’exiger de l’information ou une enquête supplémentaire de la part du distributeur du vaccin, ou encore d’apporter des changements à l’étiquette du produit.
L’Agence publie systématiquement les résultats des rapports de surveillance de l’innocuité des vaccins résumant les données du SCSESSI. Les rapports trimestriels présentent un sommaire de toutes les déclarations d'ESSI reçues par l’Agence de janvier à mars (premier trimestre), d’avril à juin (deuxième trimestre), de juillet à septembre (troisième trimestre) et d’octobre à décembre (quatrième trimestre), indépendamment de la date à laquelle le vaccin a été administré.
Afin de donner une idée générale de la variabilité des ESSI déclarés d’une année à l’autre, les données de chaque trimestre sont comparées avec une moyenne des données trimestrielles des quatre années précédentes; en d’autres termes, les données de ce trimestre, le deuxième trimestre, sont comparées avec la moyenne des données du deuxième trimestre des quatre années précédentes. Toutefois, étant donné que ces données reflètent les déclarations reçues au cours du trimestre en question et ne reflètent pas nécessairement la date à laquelle le vaccin a été administré, elles peuvent faire l’objet d’écarts importants selon le moment et la façon dont les déclarations sont reçues, traitées et envoyées par les autorités provinciales et territoriales de santé publique, ainsi que le nombre et le type de populations ayant reçu le vaccin dans un trimestre donné. Par conséquent, il est difficile de comparer et d’interpréter les données présentées. Le rapport fournit un aperçu des données qui met en évidence les déclarations d'ESSI graves et non graves reçues à des fins descriptives.
Remarques sur l’interprétation : Les déclarations d'ESSI à l’Agence représentent un soupçon, une opinion ou une observation par le déclarant plutôt qu’une affirmation ou une preuve que le vaccin a pu causer l’événement. D’autres limitations sur les données des déclarations d'ESSI comprennent une sous-déclaration potentielle, un manque de certitude quant à la validité du diagnostic d’un événement signalé, un manque de renseignements en ce qui concerne d’autres causes potentielles et d’autres biais de déclaration. Ces biais sont atténués par l’Agence par l’utilisation d’un formulaire de déclaration de MCI accompagné d’un guide d’utilisation, la codification médicale normalisée du Dictionnaire médical international des activités de réglementation (MedDRA), un suivi auprès des autorités provinciales et territoriales pour l’exhaustivité des données, des taux élevés de déclaration et l’inclusion d’une composante de surveillance pédiatrique active dans le SCSESSI.
Résultats mis en évidence pour le troisième trimestre de 2016
Les données présentées dans ce rapport trimestriel (T3) comprennent les déclarations d'ESSI reçues périodiquement entre le 1er juillet et le 30 septembre 2016. Des comparaisons sont faites par rapport au nombre moyen de déclarations reçues au cours du même trimestre lors des quatre années précédentes (de 2012 à 2015). Les données analysées ont été extraites de la base de données du SCSESSI le 20 mars 2017 par l’Agence. Depuis le milieu de l’année 2013, des problèmes techniques provenant d’une juridiction ont entraînés une diminution importante des déclarations d'ESSI. Toutes les déclarations sont traitées et codées à l’aide du MedDRA, source de terminologie médicale normalisée qui soutient la saisie, la récupération, l’évaluation et la présentation des données cliniques, et codée selon la raison principale au moyen d’un examen détaillé des dossiers médicaux de chaque déclaration. Par conséquent, si plus d’un effet secondaire est décrit, celui déterminé par l’examen comme étant celui ayant entraîné la déclaration est codé comme le principal ESSI. En outre, toutes les déclarations décrivant un effet secondaire grave ont été examinées et, sauf indication contraire dans le présent rapport, il a été établi que la plupart de ces effets secondaires étaient prévisibles (en fonction des effets indésirables connus associés au vaccin), explicables par d’autres raisons non liés à la vaccination, ou qu’ils faisaient actuellement l’objet d’un suivi ou qu’ils feraient l’objet d’une enquête future.
Nombre de déclarations d'ESSI et d'ESSI graves
Au cours du troisième trimestre de 2016, l’Agence a reçu un total de 532 déclarations d'ESSI; au cours du troisième trimestre de 2012, 2013, 2014 et 2015, l’Agence a reçu en moyenne 503 (plage : 400-668) déclarations [figure 1].
Au total, 44 déclarations d'ESSI reçues par l’Agence au cours du troisième trimestre de 2016 ont été classifiées comme étant graves (8 % de l’ensemble des déclarations d'ESSI). Au cours du troisième trimestre de 2012, 2013, 2014 et 2015, l’Agence a reçu en moyenne 43 (plage : 34-50) déclarations d'ESSI graves (de 7 à 10 % de toutes les déclarations d'ESSI).
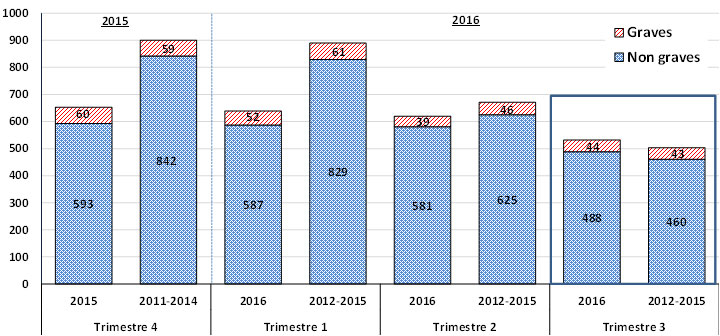
Équivalent textuel
Il s'agit d'un graphique en barres empilées. Les barres représentent le nombre total de déclarations d'effets secondaires suivant l'immunisation (ESSI) reçues chaque trimestre (T); le premier trimestre (T1) comprend les mois de janvier, février et mars, le deuxième trimestre (T2) inclut les mois d'avril, mai et juin, le troisième trimestre (T3) comprend les mois de juillet, août et septembre et le quatrième trimestre (T4) inclut les mois d'octobre, novembre et décembre. L'axe des y sur le côté gauche du graphique présente le nombre total de déclarations reçues pour chaque trimestre, qui est compris entre 0 et 1000. L'axe des x correspond au trimestre et va du premier trimestre au quatrième trimestre. Deux périodes sont représentées sur le graphique. Le premier ensemble de barres représente le nombre total de déclarations reçues durant chaque trimestre de 2015 pour T3 et T4 et 2016 pour T1 et T2, non graves en bleu et graves en rouge: non graves: 366 durant le T3, 593 durant le T4, 587 durant le T1 et 581 durant le T2; graves: 34 durant le T3, 60 durant le T4, 52 durant le T1 et 39 durant le T2. Le deuxième ensemble de barres représente la moyenne du nombre total de déclarations pour chaque trimestre de 2011 à 2014 pour T3 et T4 et 2012 à 2015 pour T1 et T2, non graves en bleu et graves en rouge: non graves: 566 durant le T3, 842 durant le T4, 829 durant le T1 et 625 durant le T2; graves: 51 durant le T3, 59 durant le T4, 61 durant le T1 et 46 durant le T2.
Fréquence des déclarations d’effets secondaires graves et non graves suivant la vaccination, par groupe d’âge
Le tableau 1 présente le nombre de déclarations d'ESSI graves et non graves par groupe d’âge au cours du T3 de 2016, sans changement significatif comparativement à la moyenne de 2012 à 2015.
| Groupe d'âge | Déclarations d'ESSI graves | Déclarations d'ESSI non graves | ||
|---|---|---|---|---|
| 2016 | Moyenne 2012-2015 | 2016 | Moyenne 2012-2015 | |
| de 0 à <1 an | 20 | 16 | 100 | 83 |
| de 1 à <2 ans | 12 | 16 | 92 | 77 |
| de 2 à <7 ans | 5 | 3 | 33 | 58 |
| de 7 à <18 ans | 4 | 5 | 70 | 71 |
| de 18 à <65 ans | 3 | 3 | 136 | 132 |
| 65+ ans | 0 | 1 | 54 | 32 |
| Inconnu | 0 | 0 | 3 | 9 |
| Total | 44 | 43 | 488 | 460 |
ESSI par ordre d’importance
La figure 2 présente les principaux types d'ESSI (graves et non graves) déclarés au cours du T3 de 2016. La majorité des ESSI rapportés sont des réactions au site de vaccination.
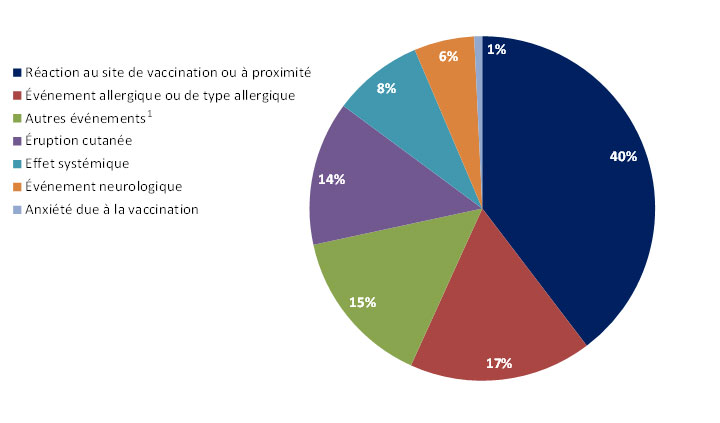
Équivalent textuel
Il s'agit d'un diagramme circulaire présentant les principales raisons d'effectuer une déclaration d'effet secondaire suivant la vaccination durant le troisième trimestre de 2016. En ordre décroissant de fréquence, les principales raisons sont: réaction au site de vaccination ou à proximité (40%), éruption cutanée (17%), autres événements (15%), événement allergique ou de type allergique (14%), effet systémique (8%), événement neurologique (6%), paresthésie/anesthésie, intussusception, arthrite, épisode hypotonique-hyporéactif, thrombocytopénia, pleurs persistents, ou parotidite (---%), et anxiété due à la vaccination (1%).
Les principaux types d'ESSI déclarés par niveau de gravité pour le troisième trimestre de 2016 sont présentés au tableau 2 et comparés à la moyenne de 2012-2015. Au cours du troisième trimestre de 2016, comme pour les quatre dernières années, les réactions au site de vaccination ou à proximité, les éruptions cutanées, et les événements allergiques ou de type allergique ont été les ESSI non graves les plus souvent signalés, et les événements neurologiques (le plus souvent des convulsions déclenchées par une fièvre) et les effets systémiques (événements qui touchent de nombreux systèmes de l’organisme, souvent accompagnés de fièvre), ont été les ESSI graves les plus souvent signalés. Le nombre d‘événements allergiques ou de type allergique a augmenté en 2016 en raison d'un changement dans la classification des cas graves à la mi-2015. Tous les cas d’anaphylaxie sont maintenant considérés potentiellement mortels et donc codé comme graves, même s’ils n'ont pas entraîné l'hospitalisation, prolongement de l'hospitalisation ou décès.
| Principaux ESSI déclarés | Déclarations d'ESSI graves | Déclarations d'ESSI non graves | ||
|---|---|---|---|---|
| 2016 | Moyenne 2012-15 | 2016 | Moyenne 2012-15 | |
| Réaction au site de vaccination ou à proximité | 2 | 3 | 209 | 174 |
| Èruption cutanée | 1 | 0 | 90 | 99 |
| Èvénement allergique ou de type allergique | 8 | 1 | 64 | 44 |
| Effet systémique | 10 | 11 | 35 | 59 |
| Èvénement neurologique | 13 | 180 | 17 | 14 |
| Anxiété due à la vaccination | 0 | 0 | 4 | 4 |
| Erreur de vaccination | 0 | 0 | 0 | 5 |
| Autre événementsTableau note 1 | 10 | 10 | 69 | 62 |
| Total | 44 | 43 | 488 | 460 |
Vaccins administrés mentionnés dans les déclarations d'ESSI
Le tableau 3 énumère les vaccins administrés les plus couramment mentionnés dans les déclarations d'ESSI reçues au troisième trimestre de 2016. La majorité des ESSI (graves et non graves) ont été signalés suite à l'administration du vaccins contre le pneumocoque, vaccins de série DCaT pour les nourrissons, la rougeole, la rubéole, les oreillons et la varicelle (RROV et RRO+V), et les vaccins contre la méningocoque, ce qui correspond avec le volume élevé de vaccinations prévus chez les enfants et souvent donné en conjonction avec d'autre. Outre les vaccins de série DCaT pour les nourrissons, nous avons reçu moins de déclarations graves pour ces vaccins en 2016 par rapport à la moyenne de 2012-2015.
| Vaccins administrés | Déclarations d'ESSI graves | Déclarations d'ESSI non graves | ||
|---|---|---|---|---|
| 2016 | Moyenne 2012-2015 | 2016 | Moyenne 2012-2015 | |
| 1. Dose de rappel du vaccin DCaT | 1 | 1 | 5 | 22 |
| 2. Vaccins de série DCat pour les nourrissons | 19 | 17 | 138 | 101 |
| 3. Hépatite B | 3 | 2 | 37 | 34 |
| 4. Virus du papillome humain (VPH) | 3 | 1 | 31 | 25 |
| 5. Grippe | 5 | 3 | 20 | 31 |
| 6. Rougeole, rubéole, oreillons, varicelle (RROV et RRO + V) | 16 | 21 | 133 | 129 |
| 7. Méningocoque | 11 | 18 | 97 | 88 |
| 8. Autre vaccins | 0 | 1 | 30 | 23 |
| 9. Pneumocoque | 23 | 25 | 176 | 126 |
| 10. Rotavirus | 12 | 8 | 52 | 33 |
| 11. Dose de rappel du vaccin dcaT | 4 | 1 | 86 | 73 |
| 12. Vaccins pour les voyageurs | 0 | 2 | 35 | 54 |
| 13. Virus varcicelle-zona | 0 | 1 | 27 | 25 |
- Table 3 - Note 1
-
- Les totaux sont supérieurs au nombre total des déclarations d'ESSI puisqu’une déclaration d'ESSI peut comprendre plus d’un vaccin. Comprend ce qui suit : 1) DCaT-IVP, DCaT; 2) DCaT-VPI-Hib, DCaT-HB-VPI-Hib; 3) HB, HB-H, HB-dial, HB-sTm; 4) VPH, VPH-2, VPH-4, VPH-9; 5) Inf, Inf-n.s.a, H1N1-09; 6) RRO, RROV, Var; 7) Men, Men-C, Men-C-ACYW-135, Men-C-C, Men-B, Men-P, Men-P-AC, Men-P-ACYW-135; 8) Rag, Td, Hib, BCG, TBEV, DTP, IPV, M; 9) Pneu, Pneu-C, Pneu-C-7, Pneu-C-10, Pneu-C-13, Pneu-P, Pneu-P-23; 10) Rot-1, Rot-5, Rota; 11) dcaT, dcaT-VPI, Td-VPI; 12) Chol-Ecol-O, HA, HA-Typh-I, HAHB, Typh-I, Typh-O, FJ, JE; 13) Zona
- DCaT-HB-VPI-Hib – Anatoxines diphtérique et tétanique combinées, coqueluche acellulaire, hépatite B (recombinant), polio inactivé et vaccin conjugué et adsorbé contre Haemophilus influenzae de type b
- DCaT-Hib – Anatoxines diphtériques et tétaniques, coqueluche acellulaire, Haemophilus influenzae de type b.
- DCaT-VPI – Composantes des vaccins anticoquelucheux et anatoxines diphtériques et tétaniques adsorbées combinées au vaccin antipoliomyélitique inactivé
- DCaT-VPI-Hib – Anatoxines diphtérique et tétanique et vaccin anticoquelucheux acellulaire adsorbé combinés avec un vaccin antipoliomyélitique inactivé et un vaccin conjugué contre l’Haemophilus de type b
Résumé
Le rapport du troisième trimestre de 2016 est fondé sur les déclarations d’effets secondaires suivant l’immunisation transmises à l’Agence par les autorités fédérales, provinciales, et territoriales de santé publique et le système de surveillance active dans les hôpitaux pédiatriques. L’évaluation détaillée des déclarations et des tendances de déclaration, effectuée en collaboration avec les centres de liaison provinciaux et territoriaux pour l’innocuité des vaccins du GTVV et à Santé Canada, ne présente pas de signal préoccupant concernant l’innocuité des vaccins. Les tableaux et les figures de ce rapport fournissent un aperçu des données fournies et examinées par l'Agence.