
 Téléchargez cet article en format PDF
Téléchargez cet article en format PDFPublié par : L'Agence de la santé publique du Canada
Numéro : Volume 47-4 : COVID-19 : un an aprés
Date de publication : avril 2021
ISSN : 1719-3109
Soumettre un article
À propos du RMTC
Naviguer
Volume 47-4, avril 2021 : COVID-19 : un an aprés
Éclosion
Une éclosion du virus de l'hépatite C attribuée à l'utilisation de flacons à doses multiples dans une clinique de coloscopie de la région de Waterloo, en Ontario
Arianne Folkema1, Hsiu-Li Wang1,2, Kristy Wright1, M Mustafa Hirji2,3, Anton Andonov4, Kathryn Bromley1, Chad Ludwig1, Amy MacArthur1
Affiliations
1 Region of Waterloo Public Health and Emergency Services, Waterloo, ON
2 Department of Health Research Methods, Evidence and Impact, Université McMaster, Hamilton, ON
3 Niagara Region Public Health & Emergency Services, Thorold, ON
4 Laboratoire national de microbiologie, Agence de la santé publique du Canada, Winnipeg, MB
Correspondance
Citation proposée
Folkema A, Wang HL, Wright K, Hirji MM, Andonov A, Bromley K, Ludwig C, MacArthur A. Une éclosion du virus de l’hépatite C attribuée à l’utilisation de flacons à doses multiples dans une clinique de coloscopie de la région de Waterloo, en Ontario. Relevé des maladies transmissibles au Canada 2021;47(4):245–53. https://doi.org/10.14745/ccdr.v47i04a07f
Mots-clés : VHC, prévention et contrôle des infections, contamination, épidémie, établissements de soins de santé externes
Résumé
Contexte : La transmission du virus de l’hépatite C (VHC) a été épidémiologiquement liée aux établissements de santé, en particulier aux établissements de soins externes, tels que les cliniques d’endoscopie et d’hémodialyse. Celles-ci ont été largement attribuées à des manquements concernant la prévention et le contrôle des infections.
Objectif : Décrire les mesures de santé publique face à une épidémie du VHC détectée parmi les patients d’une clinique de coloscopie en Ontario, et souligner les risques liés à l’utilisation de flacons à doses multiples et la nécessité d’améliorer les pratiques de prévention et le contrôle des infections dans les établissements de soins externes.
Méthodes : Le dépistage du VHC a été effectué chez les patients et le personnel qui ont fréquenté la clinique ou y ont travaillé en même temps que l’intervention du cas indexé. Les échantillons de sang des cas positifs ont été soumis à un séquençage viral. Des inspections de la clinique ont permis d’évaluer les pratiques de prévention et le contrôle des infections, et un examen des dossiers a été effectué pour cerner les mécanismes plausibles de transmission.
Résultat : Au total, 38 % des patients qui ont subi des interventions à la clinique le même jour que le cas indexé a reçu un résultat positif pour le VHC. Le séquençage génétique a montré un haut degré de similarité dans la séquence génétique du VHC parmi les échantillons positifs pour le VHC. L’examen des dossiers et l’inspection des cliniques ont permis de désigner l’utilisation de flacons à doses multiples de médicaments d’anesthésie chez plusieurs patients comme mécanisme plausible de transmission.
Conclusion : Les travailleurs de la santé, en particulier ceux qui se trouvent dans des établissements d’intervention ou chirurgicaux externes, devraient être vigilants et s’en tenir aux pratiques exemplaires de prévention et le contrôle des infections, notamment celles liées à l’utilisation de flacons à doses multiples, afin de prévenir la transmission d’infections hématogènes dans les établissements de soins de santé.
Introduction
Environ 246 000 Canadiens présentaient une infection chronique par le virus de l’hépatite C (VHC) en 2011Note de bas de page 1.
Le VHC est un virus transmissible par le sang, et les modes d’infection les plus courants sont l’utilisation d’accessoires destinés à la consommation de drogue contaminé par du sang infecté, l’utilisation de services corporels (e.g. le tatouage) utilisant des outils ou des pratiques de travail non hygiéniques, ou le partage d’articles de soins personnelsNote de bas de page 2.
Les poussées épidémiques du VHC ont été épidémiologiquement liées aux établissements de soins de santé au Canada et ailleurs, en particulier aux établissements chirurgicaux ou d’intervention externes comme les cliniques d’endoscopie et d’hémodialyse Note de bas de page 3Note de bas de page 4Note de bas de page 5Note de bas de page 6Note de bas de page 7Note de bas de page 8Note de bas de page 9Note de bas de page 10Note de bas de page 11Note de bas de page 12Note de bas de page 13Note de bas de page 14Note de bas de page 15Note de bas de page 16. La transmission dans ces lieux a été attribuée à la réutilisation de seringues, à la contamination de flacons de médicaments utilisés sur plusieurs patients, à l’entreposage et à la préparation de médicaments, de solutions intraveineuses et d’injections dans un environnement contaminé, et à d’autres manquements en matière de prévention et de contrôle des infections qui ont entraîné la contamination de médicaments injectables ou de solutions de rinçage utilisés sur plusieurs patientsNote de bas de page 3Note de bas de page 4Note de bas de page 5Note de bas de page 6Note de bas de page 7Note de bas de page 8Note de bas de page 9Note de bas de page 10Note de bas de page 11Note de bas de page 12Note de bas de page 13Note de bas de page 14Note de bas de page 15Note de bas de page 16.
Le but de ce rapport est de :
- Décrire les mesures de santé publique dans le cadre de cette éclosion du VHC dans une clinique de coloscopie
- Souligner le risque lié à l’utilisation de flacons à doses multiples
- Montrer la nécessité d’une amélioration continue des pratiques dans les établissements de soins externes
Contexte
En vertu de la Loi sur la protection et la promotion de la santé, le VHC est une maladie à déclaration obligatoire et les services de santé publique de l’Ontario doivent enquêter sur tous les nouveaux diagnostics du VHC qui surviennent dans leur juridictionNote de bas de page 17Note de bas de page 18.
Les Services de santé publique et d’urgence de la région de Waterloo (ci-après dénommés Santé publique), dans le sud de l’Ontario, coordonnent les activités de santé publique pour sa population urbaine et rurale d’environ 550 000 habitants. Dans le cadre de son enquête sur les maladies à déclaration obligatoire, Santé publique assure le suivi de tous les cas de VHC afin d’établir les sources possibles d’infection et de prendre des mesures pour en empêcher la propagationNote de bas de page 18.
Méthodes
Détection de l’éclosion
En octobre 2014, lors d’un suivi de routine auprès d’un individu qui avait récemment reçu un diagnostic de VHC et qui avait auparavant obtenu un résultat négatif au VHC lors de dépistages sanguins répétés dans le cadre du don du sang, Santé publique a établi que le seul facteur de risque de cet individu était une intervention dans une clinique de coloscopie le 24 décembre 2013. Tous les autres cas de VHC signalés dans la région de Waterloo depuis le 1er janvier 2010 (année d’ouverture de la clinique) ont ensuite été examinés pour déterminer si la coloscopie avait été établie comme facteur de risque dans d’autres cas.
L’examen a permis d’identifier une deuxième personne qui avait été signalée à Santé publique plus tôt en 2014 et qui avait également subi une intervention le même jour dans la même clinique. Bien que cette personne soit née dans un pays endémique, elle ne présentait aucun autre facteur de risque évident. Étant donné que les deux cas présentaient un facteur de risque commun et étaient liés par le temps et le lieu, une éclosion a été soupçonnée et une enquête plus approfondie a été menée. Des échantillons de sang des deux cas identifiés de VHC ont été obtenus et envoyés au Laboratoire national de microbiologie de l’Agence de la santé publique du Canada, à Winnipeg pour le génotypage et le séquençage.
Enquête
Santé publique a utilisé le document intitulé Viral hepatitis: Healthcare Investigation Guide et des documents tirés d’une enquête précédente sur les soins de santé des Centers for Disease Control and Prevention (CDC) connexes en tant qu’orientation, aux fins d’une approche systématique de l’enquête et des mesures de santé publique à cette épidémieNote de bas de page 19Note de bas de page 20.
Les listes de patients des 23 et 24 décembre 2013 ont été obtenues auprès de la clinique de coloscopie et la base de données provinciale des maladies à déclaration obligatoire a été consultée pour déterminer si d’autres cas de VHC déclarés dans la province avaient subi des interventions à la clinique depuis sa création le 14 octobre 2010. Le dépistage des patients n’a pas été effectué durant l’intervalle de deux jours avant et après les 23 et 24 décembre 2013, car la clinique était fermée les 21 et 22 décembre (un samedi et un dimanche), et les 25 et 26 décembre (jours fériés).
Conformément au protocole de laboratoire de Santé publique Ontario pour le dépistage du VHC, les patients ont d’abord été soumis à un dépistage des anticorps contre le VHC à l’aide du dosage des anticorps anti-hépatite C; ceux qui présentaient des anticorps anti-hépatite C ont ensuite subi un test supplémentaire de dépistage des anticorps anti-VHC pour confirmationNote de bas de page 21. Tous les patients ayant obtenu des résultats positifs lors des tests de confirmation ont ensuite dû soumettre de nouveaux échantillons en vue de tests moléculaires pour l’ARN de l’acide ribonucléique du VHC et le génotypage.
Santé publique a effectué une recherche sur le site Web de l’Ordre des médecins et chirurgiens de l’Ontario (OMCO) pour confirmer que tous les médecins travaillant à la clinique les 23 et 24 décembre 2013 étaient titulaires d’un permis professionnel valide et pour déterminer si des manquements antérieurs aux mesures de prévention et le contrôle des infections avaient été signalés.
Le personnel de Santé publique a communiqué avec tous les patients qui ont subi des interventions à la clinique les 23 et 24 décembre 2013 et leur a conseillé de se soumettre à un dépistage du VHC. Des cliniques de dépistage en journée et en début de soirée ont été proposées localement. Pour les patients qui résidaient en dehors de la juridiction du service de santé, Santé publique a facilité le suivi avec les médecins de leur région. Des échantillons de sang ont été soumis au Laboratoire national de microbiologie de Winnipeg pour le dépistage du VHC et les échantillons positifs ont été soumis à un séquençage génétique.
Un cas a été défini en tant qu’individu ayant une infection par le VHC confirmée en laboratoire (tests des anticorps et de l’ARN du VHC) et ayant subi une intervention à la clinique le 23 ou le 24 décembre qui pourrait être associée à la transmission de la maladie (coloscopie, œsophagogastroduodénoscopie/gastroscopie, surveillance du glucose et administration de médicaments par voie intraveineuse).
Entre le 17 novembre 2014 et le 21 avril 2015, Santé publique a effectué de multiples inspections de la clinique afin d’évaluer et de suivre les pratiques de prévention et le contrôle des infections. L’inspection a été guidée par un outil d’évaluation complet sur la base du document Infection Prevention and Control for Clinical Office Practice du Comité consultatif provincial des maladies infectieuses (CCPMI)Note de bas de page 22. Les inspections ont été complétées par de longs entretiens avec le personnel afin de comprendre leurs processus et les mesures de prévention et le contrôle des infections. L’inspection finale a été menée conjointement avec l’OMCO, qui exerce une surveillance réglementaire sur les cliniques communautaires de coloscopie (en Ontario, les services de santé publique n’enquêtent sur les établissements de soins externes qu’en cas de soupçon de manquement au contrôle des infections)Note de bas de page 23.
Les inspections comportaient l’observation d’interventions à haut risque, notamment la préparation et l’entreposage des médicaments, l’utilisation de flacons à doses multiples, les pratiques de retraitement des endoscopes, le nettoyage et la désinfection des surfaces et des appareils, l’utilisation de matériel et d’équipements tels que les gels médicaux, les rinçages de solution saline intraveineuse et les glucomètres, ainsi qu’un examen des politiques et procédures de la clinique en matière de prévention et le contrôle des infections. Plusieurs coloscopies ont été observées directement pour évaluer les mesures de prévention et le contrôle des infections, y compris l’administration de l’anesthésie.
Un examen approfondi de tous les dossiers des patients qui se sont rendus à la clinique pour des interventions les 23 et 24 décembre 2013 a également été effectué afin d’établir des schémas qui pourraient indiquer des voies de transmission potentielles. L’examen du dossier comprenait l’heure de la visite, la salle d’intervention utilisée, le numéro de série de l’endoscope, l’utilisation du glucomètre, la dose d’anesthésique (propofol) reçue, les autres médicaments reçus, ainsi que le chirurgien traitant, l’anesthésiste et le personnel infirmier.
Résultats
Au total, 40 personnes ont subi des interventions à la clinique les 23 et 24 décembre 2013. Santé publique a réussi à identifier 39 des 40 patients et 11 des 13 membres du personnel (tableau 1); un patient et deux membres du personnel n’ont pu être contactés. Parmi les 26 patients qui ont fréquenté la clinique et les neuf membres du personnel qui y travaillaient le 23 décembre, tous ont obtenu un résultat négatif pour le VHC. Parmi les patients qui se sont présentés à la clinique le 24 décembre, 5 sur 13 (38 %) ont reçu un résultat positif pour le VHC (tableau 2).
| Date | Total | VHC positif | VHC négatif | Non identifiésTableau 1 footnote a |
|---|---|---|---|---|
| Patients | ||||
| 2013-12-23 | 27 | 0 | 26 | 1 |
| 2013-12-24 | 13 | 5 | 8 | 0 |
| Personnel | ||||
| 2013-12-23 seulement | 8 | 0 | 6 | 2 |
| 2013-12-24 seulement | 2 | 0 | 2 | 0 |
| 2013-12-23 et 2013-12-24 | 3 | 0 | 3 | 0 |
| Total | 53 | 5 | 45 | 3 |
| Caractéristiques | Nombre de cas | |
|---|---|---|
| Sexe | Homme | 4 |
| Femme | 1 | |
| Groupe d'âge, années | 0–19 | 0 |
| 20–49 | 1 | |
| 50–69 | 3 | |
| 70 et plus | 1 | |
| Facteurs de risqueTableau 2 footnote a | Né dans un pays endémique | 1 |
| Intervention médicale/chirurgicale antérieure (plus de 20 ans auparavant) | 2 | |
| Intervention à la clinique de coloscopie le 24 décembre 2020 | 5 | |
Aucun des employés qui ont travaillé le 24 décembre n’a reçu de résultat positif. L’examen de tous les cas connus de VHC en Ontario depuis la création de la clinique en octobre 2010 n’a pas permis d’identifier d’autres cas de VHC liés à cette clinique. La recherche sur le site Web de l’OMCO a indiqué que tous les médecins travaillant à la clinique au moment de l’éclosion étaient titulaires d’un permis valide.
L’analyse phylogénétique menée par le Laboratoire national de microbiologie sur la base des séquences partielles des gènes du noyau (C), de l’enveloppe (E1) et des gènes non structuraux (NS5B) du VHC a clairement indiqué que les souches du VHC provenant des cinq patients de l’éclosion étaient génétiquement étroitement liées (figure 1), ce qui correspond à un groupe de transmission. Les cinq cas se sont regroupés dans un groupe monophylétique sur la base des séquences du gène E1. Une analyse plus détaillée sur la base du séquençage de nouvelle génération a révélé que la population de quasi-espèces de VHC des cinq patients se regroupait clairement sur une seule branche avec une probabilité de 99 % (figure 2). La distance génétique moyenne au sein des cinq cas impliqués dans la quasi-espèce de l’éclosion était de 0,036 alors que la distance génétique entre ce groupe et des éclosions similaires ainsi que des cas ontariens non apparentés et des souches de VHC de la GenBank était significativement plus élevée (p < 0,001).
Figure 1 : Analyse phylogénétique du séquençage populationnel de Sanger des régions subgénomiques du VHC E1/NS5B chez cinq patients dans le cadre d’une enquête sur une éclosionNote de bas de page a
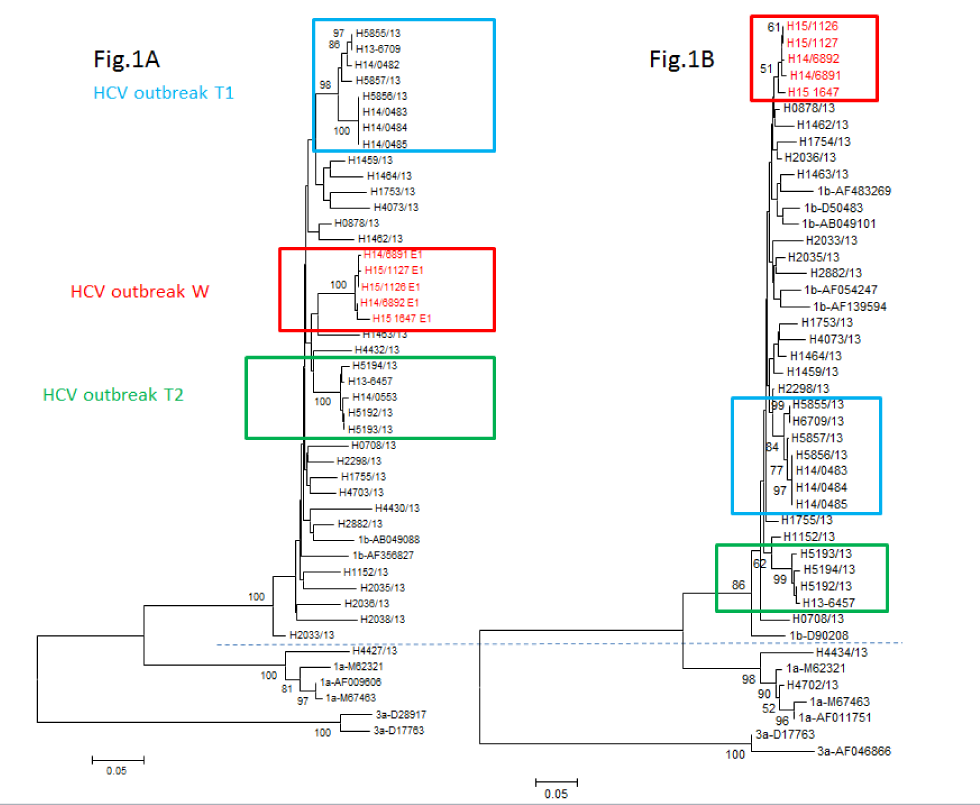
Description textuelle : Figure 1
Analyse phylogénétique du séquençage populationnel de Sanger des régions subgénomiques du VHC E1/NS5B chez cinq patients dans le cadre d'une enquête sur une flambée épidémique. L'arbre de voisinage a été créé en utilisant le modèle à deux paramètres de Kimura dans MEGA v.6. Les séquences de ce foyer (W) et de deux autres foyers similaires dans des cliniques d'endoscopie de Toronto (T1 et T2) figurent respectivement dans les cases rouge, verte et bleue. Les séquences du VHC sans lien épidémiologique avec la province de l'Ontario recueillies la même année (2013) ainsi que certaines séquences choisies au hasard dans GenBank sont en noir. Le dendrogramme de la figure 1A est basé sur la région E1 et celui de la figure 1B est fondé sur la région NS5B. Il convient de remarquer que l'analyse phylogénétique fondée sur la région NS5B ne présente pas un soutien bootstrap aussi fort que celui observé pour la région E1. En comparaison, les mesures bootstrap pour les deux autres foyers similaires T1 et T2 sont restées robustes pour E1 et NS5B, bien qu'elles aient quelque peu chuté de 98 à 84 pour T1.
Figure 2 : Analyse phylogénétique des quasi-espèces du VHC HVR-1 dans les échantillons de cinq patients impliqués dans un événement de transmission dans cette éclosion (éclosion W)Note de bas de page a
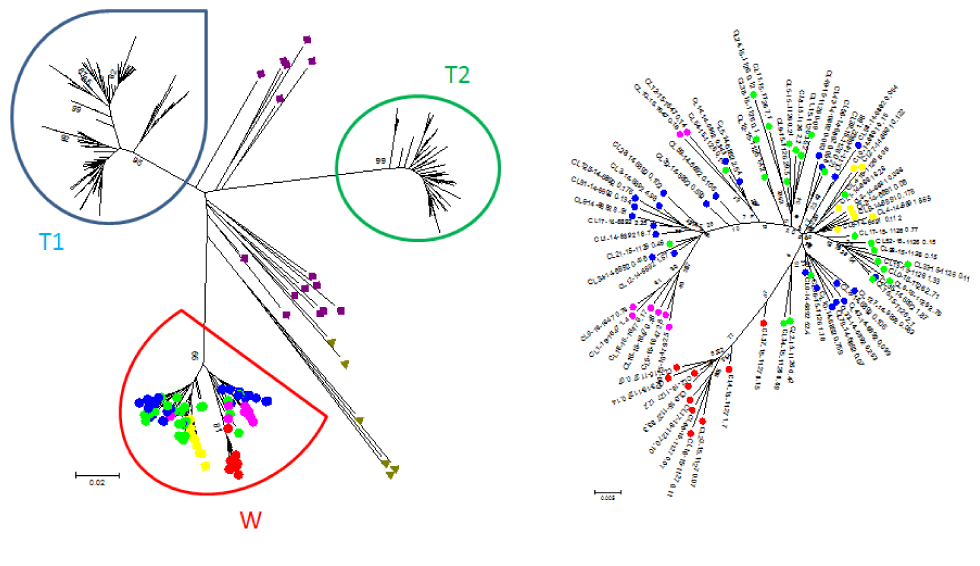
Description textuelle : Figure 2
Analyse phylogénétique des quasi-espèces HVR-1 du VHC dans les échantillons de cinq patients impliqués dans un événement de transmission dans le foyer W. Les séquences de la population de quasi-espèces de génotype 1b du VHC dérivées de trois flambées épidémiques différentes (T1, T2 et W), les séquences de souches de VHC non apparentées provenant de l'Ontario et de GenBank (triangles verts) et des souches de VHC sélectionnées au hasard dans Genbank (carrés violets) sont présentées sur le côté gauche de la figure. Les valeurs bootstrap sont indiquées au bas des nœuds. Les séquences appartenant aux cinq cas du foyer W sont codées en couleur et agrandies dans le coin droit de la figure. Chaque point de couleur (nœud) représente un seul variant du VHC. Quasi-espèces du patient n°6 (source de transmission) vert; patient n°7 rouge; patient n°8 rose; patient n°10 bleu; patient n°13 jaune. Il convient de remarquer que les séquences consensus des souches de VHC non apparentées provenant de l'Ontario et de la GenBank, ainsi que les quasi-espèces provenant de deux autres épidémies de VHC T1 et T2 occupent un espace séquentiel entièrement différent.
Les inspections de la clinique et les entretiens avec le personnel n’ont pas permis de déceler de préoccupations ou de lacunes en ce qui concerne l’utilisation, le nettoyage ou le retraitement des endoscopes. Le contrôle de la glycémie n’a pas été effectué sur les cinq patients atteints du VHC, ce qui exclut l’utilisation d’un glucomètre partagé comme source potentielle d’infection. Sur les 13 patients qui ont reçu un rinçage au sérum physiologique intraveineux, seuls cinq ont reçu un résultat positif pour le VHC, ce qui diminue la probabilité que le sac de sérum physiologique intraveineux utilisé pendant toute la journée soit une source potentielle d’infection.
L’examen des dossiers des patients ayant fréquenté la clinique le 24 décembre a montré qu’une seule salle d’intervention a été utilisée. Tous les patients qui se sont rendus à la clinique ce jour-là ont eu le même chirurgien, le même anesthésiste et les mêmes infirmières pendant leur intervention. Les 11 premiers patients ont eu la même infirmière avant l’intervention, tandis que les deux derniers patients ont eu une infirmière différente avant l’intervention. Des endoscopes différents ont été utilisés lors des interventions pour les cinq patients qui ont reçu un résultat positif pour le VHC.
Tous les patients infectés par le VHC se sont vu administrer le médicament anesthésique, le propofol, en utilisant des flacons de médicaments à doses multiples chez plusieurs patients, et c’est le seul mécanisme plausible de transmission du VHC établi. Sur la base de la quantité de propofol administrée à chaque patient selon leurs dossiers médicaux, une carte des médicaments administrés aux patients a été élaborée pour présenter la distribution hypothétique des flacons de 100 mL de propofol contaminés parallèlement à la distribution des cas de VHC à la clinique le 24 décembre 2013 (tableau 3). Étant donné que tous les patients ayant subi une intervention se sont également vu administrer du propofol au cours de leur intervention, un modèle a été établi dans l’occurrence de la positivité au VHC et l’utilisation du propofol.
| Numéro du patient | Heure de début de l'intervention | Type d'intervention | Résultat de laboratoire pour le VHC | Médicament administré | Dose totale administrée (mg)Tableau 3 footnote a |
Volume total administré (mL)Tableau 3 footnote b | Numéro de flacon hypothétique | Utilisation hypothétique de flacons de propofol (100 mL par flacon) |
|---|---|---|---|---|---|---|---|---|
| 1 | 08:54 | Coloscopie | Négatif | Propofol | 250 | 25 | Flacon #1 | Les 100 mL du premier flacon de propofol (flacon #1) ont été utilisés pour les cinq premiers patients. |
| 2 | 09:16 | Coloscopie | Négatif | Propofol | 150 | 15 | ||
| 3 | 09:54 | Endoscopie | Négatif | Propofol | 200 | 20 | ||
| 4 | 10:08 | Coloscopie | Négatif | Propofol | 200 | 20 | ||
| 5 | 10:42 | Coloscopie | Négatif | Propofol | 200 | 20 | ||
| 6 | 11:10 | Endoscopie/ coloscopie |
Positif | Propofol | 250 | 25 | Flacon #2 | Le deuxième flacon de propofol (flacon #2) a été contaminé par le sang du patient #6 atteint du VHC et a ensuite été utilisé sur les patients #7, #8 et #10. |
| 7 | 11:54 | Coloscopie | Positif | Propofol | 200 | 20 | ||
| 8 | 12:25 | Coloscopie | Positif | Propofol | 200 | 20 | ||
| 9 | s.o. | Début de l'IV seulement | Négatif | Aucun | Aucun | Aucun | ||
| 10 | 13:40 | Coloscopie | Positif | Propofol | 200 | 20 | ||
| 11 | 14:10 | Coloscopie | Négatif | Propofol | 200 | 20 | Flacon #3 | Les 15 derniers mL du flacon #2 ont été mélangés à 5 mL de propofol provenant d'un troisième flacon (flacon #3) pour fabriquer 20 mL de propofol pour le patient #11, contaminant ainsi le flacon #3, mais diluant la quantité de contamination. Cette dilution pourrait expliquer pourquoi un seul des trois patients ayant reçu du propofol provenant du flacon #3 a reçu un résultat positif pour le VHC. |
| 12 | 14:35 | Endoscopie/ coloscopie |
Négatif | Propofol | 250 | 25 | ||
| 13 | 15:11 | Coloscopie | Positif | Propofol | 200 | 20 | ||
Comme le montre le tableau 3, on suppose que les 100 mL du premier flacon de propofol (flacon #1) ont été utilisés pour les cinq premiers patients, dont aucun n’a reçu de résultat positif pour le VHC. Ensuite, le flacon de propofol #2 a été contaminé par le sang du patient #6 qui avait une infection au VHC préexistante non diagnostiquée. Ce même flacon a ensuite été utilisé pour les patients #7, #8 et #10. Enfin, les 15 mL de propofol restants dans le flacon #2 ont été mélangés avec 5 mL de propofol provenant d’un troisième flacon pour fabriquer 20 mL de propofol pour le patient #11, contaminant ainsi le flacon #3 mais diluant la quantité de contamination. Cette dilution pourrait expliquer pourquoi un seul des trois patients ayant reçu du propofol provenant du flacon n°3 a reçu un résultat positif pour le VHC.
Étant donné que le flacon de propofol utilisé pour chaque patient n’était pas indiqué dans les dossiers des patients, cette interprétation a fait l’objet d’une hypothèse fondée sur le type de flacons utilisés par les cliniques, les doses administrées aux patients consignées dans leurs dossiers et la découverte, lors des inspections et des entretiens, que des flacons à doses multiples ont été utilisés pour plusieurs patients.
Discussion
Les résultats de l’enquête sur l’éclosion soutiennent l’hypothèse d’une transmission du VHC d’un patient infecté par le VHC non diagnostiqué auparavant à quatre personnes non infectées. Les résultats de laboratoire ont démontré que les cinq cas de VHC avaient des virus génétiquement apparentés, ce qui indique une forte probabilité de transmission à partir d’une source commune. L’enquête a établi une association entre l’administration de propofol à partir de flacons à doses multiples et les patients qui ont reçu un résultat positif pour le VHC.
La contamination de flacons à doses multiples a été associée à d’autres cas de transmission d’infections transmissibles par le sang dans des cliniques de coloscopie, entre autresNote de bas de page 4Note de bas de page 8Note de bas de page 12Note de bas de page 24Note de bas de page 25. Il existe un risque de transmission d’agents pathogènes transmissibles par le sang lorsque des dispositifs (e.g. des glucomètres) et des médicaments (e.g. des flacons à doses multiples, des poches de solution saline) sont partagés entre les patients, même en l’absence de sang visible sur les objets Note de bas de page 6Note de bas de page 25Note de bas de page 26Note de bas de page 27Note de bas de page 28.
Les établissements de soins externes peuvent être plus vulnérables aux défaillances de la lutte contre les infections que les hôpitaux, car les ressources et la surveillance spécifiques des mesures de prévention et le contrôle des infections ont été moins solides dans ces millieuxNote de bas de page 29Note de bas de page 30. Les établissements de soins externes ne disposent généralement pas de spécialistes de la lutte contre les infections sur place, de conseils sur les politiques et les procédures adaptées à leur cadre de pratique, d’exigences en matière de vérification des pratiques du personnel, ni, dans de nombreuses régions, d’une procédure claire pour signaler et enquêter sur les manquements à la lutte contre les infectionsNote de bas de page 29.
De plus, les établissements non hospitaliers peuvent avoir des salles d’intervention plus petites, ce qui peut donner plus d’occasions aux fluides corporels des patients de contaminer les surfaces, les fournitures et les équipements à proximitéNote de bas de page 23Note de bas de page 31. En 2014, les salles d’opération des hôpitaux canadiens avaient une superficie minimale de 400 pieds carrés; en comparaison, les salles d’intervention non hospitalières n’ont pas de taille minimale fixe et exigent seulement que l’espace permette au médecin et au personnel d’assistance de se déplacer autour de la table d’intervention en ayant accès au patient sans contaminationNote de bas de page 23Note de bas de page 31.
Au moment de l’éclosion, les établissements de soins externes n’étaient inspectés qu’une fois tous les cinq ans, ce qui a entraîné des pratiques obsolètes, une diminution du respect des normes de pratique au fil du temps et/ou une incapacité à reconnaître les erreurs critiques dans la pratique pendant de longues périodesNote de bas de page 23Note de bas de page 32Note de bas de page 33.
Le dépistage des agents pathogènes à diffusion hématogène chez les clients avant les interventions médicales invasives n’est pas une pratique courante. Les procédures de prévention et le contrôle des infections ont été mis en place pour prévenir la transmission des agents pathogènes à diffusion hématogène. Cependant, les chercheurs estiment que 44 % des Canadiens infectés par le VHC ne sont pas diagnostiqués en raison de la nature asymptomatique et de la lenteur de la progression de l’infectionNote de bas de page 34. En outre, pour un sous-groupe de personnes nées entre 1945 et 1975 (« Baby-boomers »), jusqu’à 70 % des personnes qui sont porteuses du virus ne sont pas conscientes de leur état d’infectionNote de bas de page 34. Dans ses lignes directrices actualisées, l’Association canadienne pour l’étude du foie a souligné que les prestataires de soins de santé devraient proposer le test de dépistage du VHC aux personnes présentant un risque d’infection, notamment les enfants de l’après-guerreNote de bas de page 35. Ces lignes directrices actualisées pour le dépistage pourraient aider à sensibiliser au statut de positif pour le VHC avant les interventions médicales et contribuer à la prévention des agents pathogènes transmissibles par le sang dans tous les milieux.
Les défis de la réponse à l’éclosion
Les approches de Santé publique et des organismes de réglementation n’étaient pas nécessairement cohérentes et devaient être harmonisées. De plus, la connaissance des pratiques exemplaires de prévention et de contrôle des infections varie selon les groupes de professionnels de la santé. L’enquête concernant les mesures de prévention et le contrôle des infections devait également être menée tout en permettant à la clinique de continuer à fonctionner et en fournissant des interventions aux clients pendant l’enquête.
Enfin, au moment de l’éclosion, bien que les cas aient été identifiés par le biais d’un dépistage des patients, tous les cas n’étaient pas éligibles pour un traitement. Heureusement, des modifications ont depuis été apportées au Programme de médicaments de l’Ontario afin de couvrir le coût des médicaments pour tous les patients infectés par le VHC.
Conclusion
Cette enquête sur l’éclosion a permis de sensibiliser davantage les autorités locales et provinciales à la sécurité des injections de médicamentsNote de bas de page 23. Le 30 avril 2015, Santé publique Ontario a publié des directives actualisées sur l’utilisation des flacons à doses multiples. L’OMCO a adopté le guide des pratiques exemplaires de Santé publique Ontario comme norme pour les mesures de prévention et le contrôle des infections dans les établissements de soins externesNote de bas de page 22. Les lignes directrices actualisées font référence à la préférence écrasante pour les flacons de médicaments à usage unique et indiquent que les flacons à doses multiples devraient être réservés à des patients uniques. Les lignes directrices indiquent également que la sécurité des patients doit être privilégiée par rapport au coût lors du choix entre les flacons de médiation à doses multiples et à usage unique.
Depuis cette éclosion de 2013, d’autres éclosions liées à des manquements aux mesures de prévention et le contrôle des infections dans des établissements de soins externes sont survenues au CanadaNote de bas de page 15Note de bas de page 16. Les enquêtes de santé publique sur les plaintes relatives aux mesures de prévention et le contrôle des infections sont également en hausse en Ontario, y compris dans les milieux où travaillent des professionnels de la santé réglementésNote de bas de page 36. Compte tenu des pressions constantes exercées sur la prestation des soins de santé au Canada et dans le monde, le nombre d’interventions qui se déroulent dans des établissements de soins externes pourrait augmenter, ce qui entraînerait un risque accru d’éclosions si les mesures de prévention et le contrôle des infections ne sont pas optimales. Un examen attentif des ressources, du soutien et des réglementations en matière de prévention et le contrôle des infections est nécessaire lors d’une telle expansion des établissements de soins externes.
Déclaration des auteurs
- A. F. — Rédaction–projet initial, rédaction–révision et édition
- H. W. — Supervision de la gestion des éclosions et des interventions en matière de santé publique, rédaction–révision et édition
- K. W. — Supervision de la gestion des éclosions et des interventions en matière de santé publique, rédaction–révision et édition
- M. H. — Investigation, rédaction–révision et édition
- A. A. — Séquençage viral et interprétation, rédaction–révision et édition
- K. B. — Rédaction–révision et édition
- C. L. — Investigation, rédaction–révision et édition
- A. M. — Rédaction–révision et édition
Intérêts concurrents
Aucun.
Remerciements
Nous remercions Santé publique Ontario et le Laboratoire national de microbiologie de l’Agence de la santé publique du Canada pour leur expertise et leurs conseils au cours de l’enquête. Nous tenons également à remercier B. M. Hutchison et les équipes de santé sexuelle et de réduction des risques et de lutte contre les maladies infectieuses et la tuberculose de la Region of Waterloo Public Health pour leur contribution à l’enquête sur cette éclosion.
Financement
Ce travail a été soutenu par le ministère de la Santé de l’Ontario et la Région de Waterloo.
Références
- Note de bas de page 1
-
Trubnikov M, Yan P, Archibald C. Estimation de la prévalence de l'infection par le virus de l'hépatite C au Canada, 2011. Relevé des maladies transmissibles au Canada 2014;40(19):442-50. https://doi.org/10.14745/ccdr.v40i19a02f
- Note de bas de page 2
-
Gouvernement du Canada. Hépatite C. Ottawa (ON) : Gouvernement du Canada; 2016-03-10 (accédé 2021-03-21). https://www.canada.ca/fr/sante-publique/services/maladies/hepatite-c.html
- Note de bas de page 3
-
Germain JM, Carbonne A, Thiers V, Gros H, Chastan S, Bouvet E, Astagneau P. Patient-to-patient transmission of hepatitis C virus through the use of multidose vials during general anesthesia. Infect Control Hosp Epidemiol 2005;26(9):789-92. https://doi.org/10.1086/502618
- Note de bas de page 4
-
Fischer GE, Schaefer MK, Labus BJ, Sands L, Rowley P, Azzam IA, Armour P, Khudyakov YE, Lin Y, Xia G, Patel PR, Perz JF, Holmberg SD. Hepatitis C virus infections from unsafe injection practices at an endoscopy clinic in Las Vegas, Nevada, 2007-2008. Clin Infect Dis 2010;51(3):267-73. https://doi.org/10.1086/653937
- Note de bas de page 5
-
Centers for Disease Control and Prevention (CDC). Acute hepatitis C virus infections attributed to unsafe injection practices at an endoscopy clinic--Nevada, 2007. MMWR Morb Mortal Wkly Rep 2008;57(19):513-7.
- Note de bas de page 6
-
Centers for Disease Control and Prevention. Healthcare-associated hepatitis B and C outbreaks (≥ 2 cases) reported to the Centers for Disease Control and Prevention 2008-2019. Atlanta (GA): CDC; 2015 (accédé 2016-03-21). http://www.cdc.gov/hepatitis/outbreaks/healthcarehepoutbreaktable.htm
- Note de bas de page 7
-
Heikens E, Hetem DJ, Jousma-Rutjes JP, Nijhuis W, Boland GJ, Hommes NH, Thang OH, Schuurman R. Hepatitis C virus transmission in a Dutch haemodialysis unit: detailed outbreak investigation using NS5A gene sequencing. J Hosp Infect 2019;101(3):333-8. https://doi.org/10.1016/j.jhin.2018.11.015
- Note de bas de page 8
-
Chung YS, Choi JY, Han MG, Park KR, Park SJ, Lee H, Jee Y, Kang C. A large healthcare-associated outbreak of hepatitis C virus genotype 1a in a clinic in Korea. J Clin Virol 2018;106:53-7. https://doi.org/10.1016/j.jcv.2018.07.006
- Note de bas de page 9
-
Coyle JR, Goerge E, Kacynski K, Rodgers R, Raines P, Vail LS, Lowhim S. Hepatitis C virus infections associated with unsafe injection practices at a pain management clinic, Michigan, 2014-2015. Pain Med 2017;18(2):322-9. https://doi.org/10.1093/pm/pnw157
- Note de bas de page 10
-
Nguyen DB, Gutowski J, Ghiselli M, Cheng T, Bel Hamdounia S, Suryaprasad A, Xu F, Moulton-Meissner H, Hayden T, Forbi JC, Xia GL, Arduino MJ, Patel A, Patel PR. A large outbreak of hepatitis C virus infections in a hemodialysis clinic. Infect Control Hosp Epidemiol 2016;37(2):125-33. https://doi.org/10.1017/ice.2015.247
- Note de bas de page 11
-
Perz JF, Thompson ND, Schaefer MK, Patel PR. US outbreak investigations highlight the need for safe injection practices and basic infection control. Clin Liver Dis 2010;14(1):137-51. https://doi.org/10.1016/j.cld.2009.11.004
- Note de bas de page 12
-
Macedo de Oliveira A, White KL, Leschinsky DP, Beecham BD, Vogt TM, Moolenaar RL, Perz JF, Safranek TJ. An outbreak of hepatitis C virus infections among outpatients at a hematology/oncology clinic. Ann Intern Med 2005;142(11):898-902. https://doi.org/10.7326/0003-4819-142-11-200506070-00007
- Note de bas de page 13
-
Thompson ND, Perz JF, Moorman AC, Holmberg SD. Nonhospital health care-associated hepatitis B and C virus transmission: united States, 1998-2008. Ann Intern Med 2009;150(1):33-9. https://doi.org/10.7326/0003-4819-150-1-200901060-00007
- Note de bas de page 14
-
Savey A, Simon F, Izopet J, Lepoutre A, Fabry J, Desenclos JC. A large nosocomial outbreak of hepatitis C virus infections at a hemodialysis center. Infect Control Hosp Epidemiol 2005;26(9):752-60. https://doi.org/10.1086/502613
- Note de bas de page 15
-
Toronto Public Health. HCV Outbreak Investigation - North Scarborough Endoscopy Clinic Final Report. Toronto (ON): Toronto Public Health; 2014.
- Note de bas de page 16
-
Toronto Public Health. HCV outbreak investigation - Ontario Endoscopy Clinic Final Report. Toronto (ON): Toronto Public Health; 2015.
- Note de bas de page 17
-
Gouvernement de l'Ontario. Protection et la promotion de la santé (Loi sur la), L.R.O. 1990, chap. H.7. 2015:1-59. Toronto (ON) : Gouvernement de l'Ontario; 2020 (accédé 2019-12-24). https://www.ontario.ca/fr/lois/loi/90h07
- Note de bas de page 18
-
Ontario Ministry of Health and Long-Term Care. Ontario Public Health Standards: Requirements for programs, services, and accountability (Standards). Toronto (ON): Government of Ontario; 2018.
- Note de bas de page 19
-
Centers for Disease Control and Prevention. Viral hepatitis: Healthcare investigation guide. Atlanta (GA): CDC; 2015 (accédé 2019-12-21). http://www.cdc.gov/hepatitis/Outbreaks/HealthcareInvestigationGuide.htm
- Note de bas de page 20
-
Bornschlegel K, Dentinger C, Layton M, Balter S, France AM; Centers for Disease Control and Prevention (CDC). Investigation of viral hepatitis infections possibly associated with health-care delivery--New York City, 2008-2011. MMWR Morb Mortal Wkly Rep 2012;61(19):333-8.
- Note de bas de page 21
-
Ontario Agency for Health Protection and Promotion (Public Health Ontario). Labstract: Hepatitis C virus (HCV) RNA and genotype testing and interpretation. Toronto (ON): Public Health Ontario; 2008 (modifié 2019-12; accédé 2020-11-07). https://www.publichealthontario.ca/-/media/documents/lab/lab-sd-033-hep-c-rna-testing-update.pdf?la=en
- Note de bas de page 22
-
Comité consultatif provincial des maladies infectieuses. Prévention et contrôle des infections pour la pratique en cabinet et en clinique. Toronto (ON) : Santé Public Ontario; 2013 (accédé 2019-12-24). https://www.publichealthontario.ca/-/media/documents/b/2013/bp-clinical-office-practice.pdf?la=fr
- Note de bas de page 23
-
College of Physicians and Surgeons of Ontario. Out-of-Hospital Premises Inspection Program (OPHPIP) Program Standards. Toronto (ON): CPSO; 2013 (modifié 2017-10). https://www.cpso.on.ca/admin/CPSO/media/Documents/physician/your-practice/quality-in-practice/clinic-inspections-special-programs/ohpip-standards.pdf
- Note de bas de page 24
-
Greeley RD, Semple S, Thompson ND, High P, Rudowski E, Handschur E, Guo-Liang X, Ganova-Raeva L, Crawford J, Robertson C, Tan C, Montana B. Hepatitis B outbreak associated with a hematology-oncology office practice in New Jersey, 2009. Am J Infect Control 2011;39(8):663-70. https://doi.org/10.1016/j.ajic.2010.11.011
- Note de bas de page 25
-
County of Los Angeles Public Health. 2010 Pain Clinic Hepatitis Investigation Report - OB 201016. Los Angeles (CA): County of Los Angeles Public Health; 2011. http://publichealth.lacounty.gov/acd/docs/HepInfo/Final Report Hepatitis Investigation at Pain Clinic.pdf.PDF
- Note de bas de page 26
-
Comstock RD, Mallonee S, Fox JL, Moolenaar RL, Vogt TM, Perz JF, Bell BP, Crutcher JM. A large nosocomial outbreak of hepatitis C and hepatitis B among patients receiving pain remediation treatments. Infect Control Hosp Epidemiol 2004;25(7):576-83. https://doi.org/10.1086/502442
- Note de bas de page 27
-
Centers for Disease Control and Prevention (CDC). Notes from the field: deaths from acute hepatitis B virus infection associated with assisted blood glucose monitoring in an assisted-living facility--North Carolina, August-October 2010. MMWR Morb Mortal Wkly Rep 2011;60(6):182.
- Note de bas de page 28
-
Centers for Disease Control and Prevention (CDC). Hepatitis C virus transmission at an outpatient hemodialysis unit--New York, 2001-2008. MMWR Morb Mortal Wkly Rep 2009;58(8):189-94. https://doi.org/10.1097/01.NEP.0000350585.46820.f0
- Note de bas de page 29
-
Williams IT, Perz JF, Bell BP. Viral hepatitis transmission in ambulatory health care settings. Clin Infect Dis 2004;38(11):1592-8. https://doi.org/10.1086/420935
- Note de bas de page 30
-
Schaefer MK, Jhung M, Dahl M, Schillie S, Simpson C, Llata E, Link-Gelles R, Sinkowitz-Cochran R, Patel P, Bolyard E, Sehulster L, Srinivasan A, Perz JF. Infection control assessment of ambulatory surgical centers. JAMA 2010;303(22):2273-9. https://doi.org/10.1001/jama.2010.744
- Note de bas de page 31
-
Facility Guidelines Institute. Guidelines for design and construction of hospitals and outpatient facilities. Chicago (IL): American Hospital Association; 2014.
- Note de bas de page 32
-
Gouvernement de l'Ontario. Excellence des soins pour tous (Loi de 2010 sur l'), L.O. 2010, chap. 14; 2014. Toronto (ON) : Gouvernement de l'Ontario; 2020 (accédé 2019-12-21). https://www.ontario.ca/fr/lois/loi/10e14
- Note de bas de page 33
-
Gouvernement de l'Ontario. Règlements de l'Ont. 490/09 : substances désignées; 2013:21. https://www.ontario.ca/fr/lois/reglement/090490#
- Note de bas de page 34
-
Rotermann M, Langlois K, Andonov A, Trubnikov M. Seroprevalence of hepatitis B and C virus infections: results from the 2007 to 2009 and 2009 to 2011 Canadian Health Measures Survey. Health Rep 2013;24(11):3-13.
- Note de bas de page 35
-
Shah H, Bilodeau M, Burak KW, Cooper C, Klein M, Ramji A, Smyth D, Feld JJ; Canadian Association for the Study of the Liver. The management of chronic hepatitis C: 2018 guideline update from the Canadian Association for the Study of the Liver. CMAJ 2018;190(22):E677-87. https://doi.org/10.1503/cmaj.170453
- Note de bas de page 36
-
Cadieux G, Brown C, Sachdeva H. Enquête des plaintes relatives aux pratiques de prévention et de contrôle des infections par la santé publique en Ontario, de 2015 à 2018. Relevé des maladies transmissibles au Canada 2019;45(11):318-25. https://doi.org/10.14745/ccdr.v45i11a03f

Cette œuvre est mise à disposition selon les termes de la Licence Creative Commons Attribution 4.0 International