Mise en œuvre du traitement antiviral nirmatrelvir/ritonavir contre la COVID-19 au Canada en 2022

 Téléchargez cet article en format PDF (211 ko)
Téléchargez cet article en format PDF (211 ko)Publié par : L'Agence de la santé publique du Canada
Numéro : RMTC : Volume 51-8, août 2025 : Thérapie antivirale
Date de publication : août 2025
ISSN : 1719-3109
Soumettre un article
À propos du RMTC
Naviguer
Volume 51-8, août 2025 : Thérapie antivirale
Étude qualitative
Mise en œuvre du traitement antiviral nirmatrelvir/ritonavir (PaxlovidTM) contre la COVID-19 au Canada en 2022 : une analyse qualitative des principaux facteurs favorables et défis
Aklile Workneh1, Camilia Thieba1, Nadine Sicard2
Affiliations
1 Agence de la santé publique du Canada, Ottawa, ON
2 Agence de la santé publique du Canada, Montréal, QC
Correspondance
Citation proposée
Workneh A, Thieba C, Sicard N. Mise en œuvre du traitement antiviral nirmatrelvir/ritonavir (PaxlovidTM) contre la COVID-19 au Canada en 2022 : une analyse qualitative des principaux facteurs favorables et défis. Relevé des maladies transmissibles au Canada 2025;51(8):329−38. https://doi.org/10.14745/ccdr.v51i08a03f
Mots-clés : COVID-19, traitement, nirmatrelvir/ritonavir, mise en œuvre, Canada
Résumé
Contexte : L'utilisation du traitement antiviral nirmatrelvir/ritonavir (PaxlovidTM, N/R) contre la COVID-19 a été approuvée au Canada en janvier 2022, avec le gouvernement du Canada assumant un rôle en matière d'approvisionnement et les provinces, les territoires et les ministères fédéraux mettant en œuvre son utilisation au sein de leurs systèmes de santé respectifs. L'objectif de la présente analyse est de décrire la manière dont le N/R a été mis en œuvre dans les différentes administrations au cours des six premiers mois après sa mise à disposition et d'identifier les pratiques de mise en œuvre prometteuses.
Méthodes : Quatorze discussions semi-structurées en petits groupes ont été menées avec des représentants d'administrations impliqués dans la mise en œuvre du N/R. Une analyse descriptive des critères d'admissibilité et du modèle d'organisation des services a été effectuée. Une analyse thématique utilisant le Cadre consolidé pour la recherche sur la mise en œuvre et une analyse par grappes de codes ont ensuite été entreprises sur NVivo 12 afin d'identifier les thèmes principaux.
Résultats : Dans l'ensemble, les critères d'admissibilité étaient semblables d'une administration à l'autre et trois types de modèles d'organisation des services ont été identifiés. Dix thèmes principaux sont apparus comme des facteurs favorables et huit comme des défis pour la mise en œuvre. Le partenariat, la collaboration, la communication et la flexibilité figurent parmi les facteurs favorables identifiés, tandis que la complexité de l'intervention, c.-à-d. les interactions médicamenteuses), la perception par les prescripteurs de manque de données probantes confirmant l'efficacité et les limites de ressources ont été identifiés comme les principales difficultés de mise en œuvre.
Conclusion : Bien que la mise en œuvre du N/R ait varié d'une administration à l'autre, la communication et la collaboration, ainsi que la disponibilité de tests rapides pour dépister la COVID-19, sont apparues comme des facteurs favorables clés. Les interactions médicamenteuses, les pressions sur les ressources et le manque de données probantes ont été quelques-uns des principaux défis à relever. Dans l'ensemble, ces facteurs favorables et ces défis étaient semblables d'une administration à l'autre et peuvent informer les futurs plans de mise en œuvre de produits thérapeutiques pour la préparation aux pandémies.
Introduction
Le nirmatrelvir/ritonavir (PaxlovidTM, N/R) est un antiviral oral destiné au traitement du SRAS-CoV-2 chez les adultes présentant des symptômes légers ou modérés et un risque élevé de maladie sévère ou de décès. Le 17 janvier 2022, Santé Canada a autorisé son utilisation à la suite de la publication des résultats intermédiaires de l'essai EPIC-HR (Evaluation of Protease Inhibition for COVID-19 in High-Risk Patients) de phase 2/3, en double aveugle et contrôlée par placebo, démontrant une réduction des hospitalisations et de la mortalité toutes causes confondues liées à la COVID-19 Note de bas de page 1Note de bas de page 2. Le N/R a été le premier antiviral oral approuvé pour le traitement de la COVID-19 au Canada. Le gouvernement du Canada a assumé l'approvisionnement, les administrations étant chargées d'offrir le traitement à leurs populations. Compte tenu du contexte sans précédent de la pandémie de COVID-19, qui évoluait rapidement, et de son nouveau rôle pour l'approvisionnement, l'Agence de la santé publique du Canada (l'Agence) a élaboré un cadre d'évaluation en collaboration avec les intervenants des différentes administrations. L'une des composantes du cadre visait à répondre aux questions sur les pratiques exemplaires à la lumière de l'expérience limitée avec cette nouvelle option thérapeutique et à éclairer la mise en œuvre, sur laquelle cette étude se concentre. L'évaluation de la mise en œuvre visait à décrire la manière dont le déploiement du N/R s'est déroulé au Canada et à identifier les facteurs favorables et les défis associés à sa mise en œuvre.
Objectifs de l'évaluation
L'objectif principal de la présente évaluation était de répondre aux questions suivantes :
- Comment le N/R a-t-il été administré au Canada ?
- Quelles sont les stratégies les plus prometteuses pour administrer des produits thérapeutiques en milieu ambulatoire ?
Méthodes
Adoptant une méthodologie qualitative, la présente étude a utilisé des discussions de groupe semi-structurées comme principale méthode de collecte de données. S'inspirant du cadre de Donabedian Note de bas de page 3, du Cadre consolidé pour la recherche sur la mise en œuvre (CFIR) Note de bas de page 4, du cadre Reach, Effectiveness, Adoption, Implementation, and Maintenance (RE-AIM) Note de bas de page 5 et des modèles théoriques des sciences du comportement Note de bas de page 6Note de bas de page 7, un questionnaire structuré a guidé les discussions, couvrant des sujets clés tels que l'admissibilité, l'organisation des services, la communication, la formation et les processus d'approvisionnement.
Les participants ont été identifiés et recrutés au sein de divers groupes de travail fédéraux, provinciaux et territoriaux (FTP) à l'aide d'une technique d'échantillonnage boule de neige, garantissant ainsi une représentation diversifiée comprenant des gestionnaires et des professionnels de la santé œuvrant dans la planification de l'offre des produits thérapeutiques contre la COVID-19. Au total, 12 provinces et territoires et deux ministères fédéraux ont participé.
Les entretiens ont duré une heure et chaque séance a été enregistrée, transcrite et résumée. Ces résumés, validés par les participants, ont servi de base aux analyses descriptives et thématiques guidées par le CFIR. L'approche a principalement suivi une méthode déductive en adéquation avec les domaines et les concepts du CFIR, tout en restant ouverte à des ajouts inductifs au schéma de codage si nécessaire. Tous les facteurs du CFIR ont été inclus dans le schéma de codage déductif initial. Chaque passage codé s'est vu attribuer un sentiment indiquant la direction du facteur déterminant (c.-à-d., obstacle ou facteur favorable). Les passages détaillant les critères d'admissibilité et les modèles d'organisation des services des administrations participantes n'ont pas été codés, mais résumés.
Le CFIR est un cadre théorique élaboré pour explorer systématiquement les facteurs complexes qui influencent la mise en œuvre réussie des innovations dans divers contextes organisationnels. Les cinq domaines du CFIR examinent des éléments essentiels, notamment les caractéristiques de l'intervention, les contextes organisationnels externes et internes, les caractéristiques individuelles et le processus de mise en œuvre. Dans ces domaines, il existe 39 concepts et sous-concepts du CFIR, qui représentent les facteurs fondés sur des données probantes les plus susceptibles d'avoir un impact sur la mise en œuvre des interventions. Le CFIR a été utilisé pour coder les données et organiser les thèmes émergents après la collecte des données. Pour l'analyse, l'administration responsable de la mise en œuvre a été l'unité de référence. Le N/R a été codé comme étant l'innovation; les organismes de santé provinciaux, territoriaux et fédéraux ont été codés comme étant le contexte interne; et le gouvernement fédéral et toute autre institution externe comme étant le contexte externe.
Le processus d'analyse des données a comporté un codage initial dans NVivo 12 Note de bas de page 8 à l'aide du CFIR. Ensuite, une analyse par grappes a été effectuée pour découvrir des tendances parmi les éléments codés sur la base de leur cooccurrence (coefficient de Pearson) et, enfin, de requêtes de codage matriciel pour les concepts qui ont été codés comme étant positifs (facteur favorable) ou négatifs (défi). Une analyse thématique, inspirée par Guest et Mclelan Note de bas de page 9, a été effectuée pour identifier des thèmes généraux lorsque de nombreux thèmes pertinents émergeaient de l'ensemble de données. Les résultats ont été synthétisés grâce à un processus en plusieurs étapes commençant par l'identification de thèmes généraux se dégageant de l'analyse par grappes. L'analyse des sentiments a été utilisée pour distinguer les facteurs favorables et les obstacles, et des thèmes majeurs et mineurs ont été élaborés sur la base de la reconnaissance de tendances dans les données. L'analyse comprenait une triangulation, la vérification entre membres et la fiabilité entre observateurs afin de renforcer la crédibilité et la transférabilité des conclusions. Des cycles itératifs d'analyse et d'affinage ont favorisé une compréhension nuancée du processus complexe de mise en œuvre.
Approbation éthique
La politique de l'Agence en matière d'activités de recherche a été respectée et il n'a pas été nécessaire de consulter le Comité d'éthique de la recherche puisque l'évaluation de la mise en œuvre s'inscrit dans les pratiques habituelles de l'Agence en matière d'évaluation de ses programmes. Des consultations ont eu lieu avec la Division de la gestion de la protection des renseignements personnels afin de s'assurer que tout renseignement personnel susceptible d'être divulgué au cours de l'évaluation soit traité conformément à la règlementation fédérale et aux politiques ministérielles.
Résultats
Les entretiens ont permis d'identifier deux phases principales dans le déploiement du N/R : la première, au début du déploiement, lorsque l'offre de N/R était limitée, et la seconde, caractérisée par une offre accrue et stable. Ces phases ont eu un impact direct sur les processus décisionnels et l'accès des Canadiens au N/R.
Critères d'admissibilité
Au début du déploiement, les administrations ont fondé leurs critères d'admissibilité au traitement avec le N/R sur les recommandations de l'Agence et de l'Agence canadienne des médicaments et des technologies de la santé (ACMTS) Note de bas de page 10, sur les résultats de l'essai EPIC-HR Note de bas de page 2, sur la monographie du produit Note de bas de page 11 et sur les conseils de comités consultatifs d'experts. Compte tenu de l'offre limitée et du court délai entre l'autorisation du médicament et sa distribution, l'utilisation de celui-ci a été accordée en priorité aux personnes présentant le risque le plus élevé de conséquences graves, notamment les personnes âgées, sous-vaccinées ou non vaccinées, les populations Autochtones et les personnes atteintes d'immunosuppression, de facteurs de risque spécifiques ou de comorbidités (c.-à-d., IMC ≥ 30, diabète, maladies pulmonaires et cardiovasculaires). Ces critères variaient d'une administration à l'autre en ce qui concerne les limites d'âge pour l'admissibilité de concert avec le statut vaccinal et les comorbidités, le nombre de comorbidités nécessaires pour être admissible (d'une à trois) et les comorbidités incluses (c.-à-d., le tabagisme, l'hypertension, l'insuffisance rénale chronique).
Avec l'augmentation de l'offre, la plupart des administrations ont élargi leurs critères d'admissibilité, certaines d'entre elles passant de critères définis à des recommandations à l'intention des prescripteurs. Parmi les modifications apportées, citons l'abaissement des limites d'âge, l'inclusion des personnes vaccinées, le raffinement de la définition du statut vaccinal (p. ex., les doses de rappel) et les listes de comorbidités. Les facteurs à l'origine de ces changements sont l'augmentation de l'offre, les nouveaux résultats de recherche (soit les résultats de l'essai EPIC-SR Note de bas de page 12), les preuves d'une réduction de l'efficacité des anticorps monoclonaux neutralisants (soit le sotrovimab) contre les nouveaux variants préoccupants et l'évolution des études épidémiologiques propres aux administrations respectives.
Modèles d'organisation des services
Les modèles d'organisation des services varient d'une administration à l'autre en raison des différences d'infrastructure du système de santé, ce qui a donné lieu à trois modèles principaux : centralisé, décentralisé et mixte, qui combine les deux (voir la figure 1). Au départ, la plupart des administrations se sont appuyées sur un modèle centralisé, ce qui a permis de mieux contrôler la distribution, et qui a été influencée par l'offre limitée, les considérations logistiques et le peu de preuves à l'appui d'une utilisation élargie. Cependant, avec l'augmentation de l'offre, beaucoup sont passées à un modèle décentralisé ou mixte.
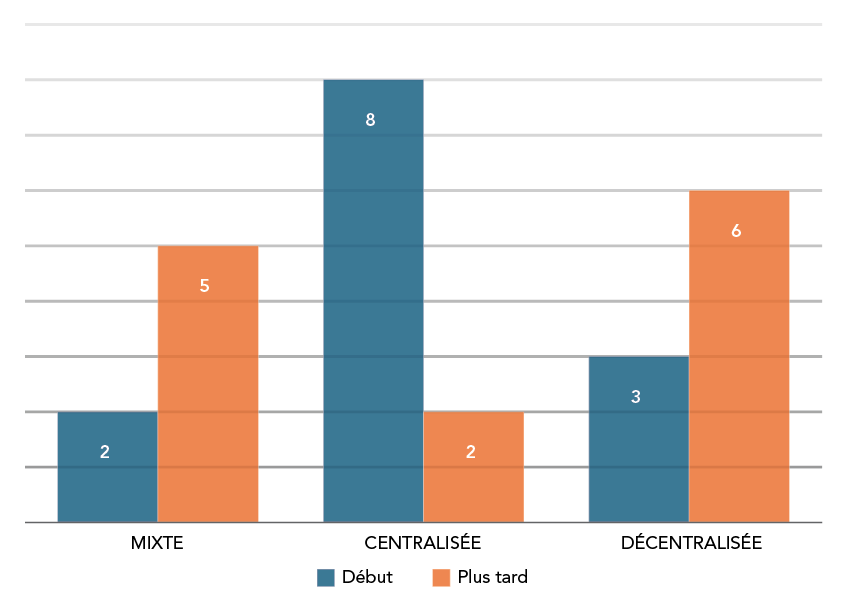
Figure 1 : Équivalent textuel
Il s'agit d'un graphique à barres montrant la répartition des modèles d'organisation des services au début de la mise en œuvre par rapport au moment de l'évaluation. Au début de la mise en œuvre, il existait deux modèles d'organisation des services mixtes, huit modèles centralisés et trois modèles décentralisés. Au moment de l'évaluation, il existait cinq modèles d'organisation des services mixtes, deux modèles centralisés et six modèles décentralisés.
Notes de bas de page figure 1
Répartition des modèles d'organisation des services au début du déploiement par rapport à ultérieurement (données pour 13 administrations). Au début de la mise en œuvre du nirmatrelvir/ritonavir (N/R), huit administrations participantes ont utilisé un modèle de prestation centralisé, caractérisé par des points d'accès désignés ou des prescripteurs désignés pour le N/R. Après le déploiement initial, deux administrations sont passées à un modèle décentralisé et quatre à un modèle mixte (en conservant le modèle centralisé pour les patients non affiliés ou les patients qui n'ont pas pu accéder à leurs prestataires de soins de santé en temps voulu, tout en utilisant un modèle décentralisé pour la plupart des autres patients). Trois administrations ont utilisé un modèle décentralisé dès le début et ont maintenu cette approche. Deux administrations ont utilisé un modèle mixte au départ, et l'une d'entre elles a opté pour un modèle de prestation décentralisé par la suite
Les prescripteurs autorisés varient en fonction de la règlementation en vigueur au sein de l'administration, les médecins, les infirmières praticiennes ou les pharmaciens étant autorisés à prescrire du N/R. Plusieurs administrations ont modifié leur règlementation afin d'élargir le cercle des prestataires de soins de santé désignés autorisés à prescrire et à administrer l'antiviral. Au moment de la collecte des données, cinq administrations autorisaient les pharmaciens à le prescrire, tandis qu'une administration autorisait les infirmières communautaires à le prescrire dans le cadre d'un rôle élargi (ces chiffres ont augmenté depuis). L'augmentation du nombre de points d'accès et de prescripteurs autorisés a été soulignée comme ayant augmenté la prescription et l'accès au N/R dans certaines administrations.
Analyse thématique
L'analyse des relations entre les codes et de leur fréquence de cooccurrence a permis de dégager sept thèmes essentiels, qui définissent les principaux facteurs de la mise en œuvre du N/R au Canada (tableau 1). L'examen des obstacles et des facteurs favorables de la mise en œuvre du N/R au Canada a mis en évidence plusieurs facteurs clés communs dans l'ensemble des administrations. Ils sont résumés dans le tableau 2, organisés par domaine du CFIR.
| Numéro du thème | Description |
|---|---|
| Thème 1 | Disponibilité de l'offre, système de soutien et réceptivité |
| Thème 2 | Identifier les besoins et communiquer les disponibilités |
| Thème 3 | Efforts coordonnés pour l'utilisation efficiente des tests et de l'administration |
| Thème 4 | Alignement général et détermination à mettre en œuvre l'intervention |
| Thème 5 | Synergie organisationnelle/structurelle pour faciliter la mise en œuvre de l'intervention |
| Thème 6 | Adaptabilité des processus/systèmes de mise en œuvre |
| Thème 7 | Efforts concertés et mobilisation des intervenants pour donner la priorité aux populations à haut risque (en s'appuyant sur les systèmes préexistants) |
| Domaine du CFIR plus concepts | Facteurs favorables Sous-thèmes |
Défis Sous-thèmes |
|---|---|---|
| Caractéristique : Domaine de l'individu | Motivation des patients et des prestataires à utiliser le produit (anecdotique) Citation 1 : Les prescripteurs étaient heureux d'avoir accès au PaxlovidTM, en particulier lors de l'éclosion qui s'est produite à XX de janvier à mars 2022. Capacité du prestataire à administrer (évaluation clinique et prescrire) le produit |
Perception d'un manque de bienfaits de l'intervention Citation 1 : Dans l'ensemble, la réaction et la perception des professionnels de la santé à l'égard de PaxlovidTM et des thérapies contre la COVID-19 variaient entre le souhait que tout le monde puisse y avoir accès et les préoccupations liées au manque de données probantes. |
| Rôles : Domaine de l'individu | Systèmes en place pour donner la priorité aux populations à haut risque – considérations d'équité Citation 1 : XX a donné la priorité aux communautés des Premières Nations (PN) dans les critères d'admissibilité en réduisant l'âge requis pour recevoir PaxlovidTM et en veillant à ce qu'il y ait des points d'accès près des communautés. Citation 2 : Le parcours XX est recommandé pour les cas complexes ou les patients orphelins qui n'ont pas accès à un professionnel de la santé ou qui n'ont pas accès à leur fournisseur de soins primaires. Citation 3 : Le XX a joué un rôle important dans la mise en œuvre de l'accès rapide à PaxlovidTM dans les établissements de soins de longue durée. |
s.o. |
| Mise en œuvre : Domaine du processus | Flexibilité de l'intervention et des processus de mise en œuvre pour s'adapter au contexte et aux besoins Citation 1 : […]. Le soutien [des organisations de santé publique] était important pour offrir l'accès aux populations vulnérables. En outre, […] la possibilité d'accéder à PaxlovidTM par le biais de la télésanté, augmentant ainsi la portée et l'utilisation. Développement d'outils de dépistage et de déclaration pour soutenir l'administration Citation 1 : La diffusion de séances de formation, des ensembles de modèles d'ordonnances et du protocole a facilité le déploiement. Les mises à jour des orientations ont été rapides, tout comme les approbations. Le Bureau de la santé publique a partagé des informations sur les mises à jour relatives à la COVID; des canaux ont été créés sur Teams pour publier des notes de service et des documents provenant des différentes tables et comités. Disponibilité de modalités de tests autres que PCR pour l'admissibilité au N/R (tests antigéniques rapides, ID NOW, Lucera) Citation 1 : En outre, les TAG ont été un outil important puisqu'ils sont disponibles à domicile et facilement accessibles. Il a été considérablement plus facile d'utiliser des [traitements] contre la COVID-19 en éliminant les obstacles potentiels à l'accès. Pratiques de collaboration multilatérale Citation 1 : La collaboration avec des médecins régionaux de santé publique a été déterminante pour la mise en œuvre. La collaboration avec des responsables de pharmacies a permis d'identifier les lacunes dans la distribution du PaxlovidTM. Le déploiement a permis de créer de nouveaux partenariats avec des centres afin d'élargir la portée et de travailler en collaboration pour combler les lacunes, le cas échéant, dans l'organisation des services de PaxlovidTM. Citation 2 : L'excellente collaboration entre les pharmaciens, les médecins et les infirmières a été essentielle pour la réussite du déploiement. Un comité consultatif médical composé d'intervenants clés (pharmaciens, médecins et infirmières) a été mis en place et de nombreuses discussions ont eu lieu afin de ne pas épuiser rapidement les stocks de PaxlovidTM. |
Processus d'administration (du dépistage à la distribution) Citation 1 : Un réseau de distribution a été nécessaire pour permettre l'accès à PaxlovidTM dans des communautés et des installations pouvant se trouver à plus de deux ou trois heures de route, avec un système de messagerie et des services de taxi pour s'assurer que le traitement commence dans les 24 heures. Citation 2 : Il y a eu quelques difficultés au départ, car il a fallu adapter le processus de commande pour passer de traitements injectables contre la COVID-19 acquis directement par l'hôpital à des traitements oraux, tels que PaxlovidTM, qui pouvaient être distribués et utilisés en dehors de l'hôpital. Test PCR Citation 1 : De plus, l'échéancier et la rapidité des résultats des tests ont représenté un obstacle à l'accès puisque certains patients ne se sentaient pas suffisamment malades pour envisager un test ou étaient testés plus de cinq jours après l'apparition des symptômes, par exemple, et au moment où ils cherchaient à se faire soigner, ils n'étaient plus admissibles au PaxlovidTM. Citation 2 : Des difficultés ont été rencontrées pour faire en sorte que les patients soient testés et identifiés dans le délai de cinq jours. Des problèmes de capacité des laboratoires ont entraîné des retards dans les tests PCR. |
| Domaine du contexte interne | Exploitation des canaux préexistants pour la diffusion d'informations aux professionnels de la santé Citation 1 : Il y a également eu des communications ciblées au sein des réseaux. En effet, les réseaux tels que [les associations de professionnels de la santé] ont diffusé des communications sur PaxlovidTM en interne par le biais de leurs bulletins respectifs pour atteindre les divisions de médecine familiale et les IP. Citation 2 : En outre, XX et la possibilité d'accéder à PaxlovidTM par le biais de la télésanté, augmentant ainsi la portée et l'utilisation. XX a pu tirer parti des voies de communication préexistantes pour diffuser des informations sur PaxlovidTM auprès de la communauté, et le MH a également présenté des communications claires. Élaboration de documents de formation et d'orientation pour les prescripteurs Citation 1 : […] Des programmes de formation pour les médecins ont également été organisés par le biais de présentations (en anglais et en français pour les médecins et les pharmaciens), car le modèle d'organisation des services prenait de l'ampleur. Citation 2 : Les documents d'orientation et les directives supplémentaires sur la prescription aux patients souffrant d'une insuffisance rénale grave, créés par le réseau de santé rénale XX, ont également été utiles. Avec le temps, les prescripteurs se sont familiarisés avec PaxlovidTM et l'utilisation a augmenté. Création de nouvelles infrastructures renforcées par des voies préexistantes pour faciliter la mise en œuvre (p. ex., technologies de l'information, processus de travail)/Exploitation d'infrastructures préexistantes (technologies de l'information ou systèmes) Citation 1 : Ce réseau a été mis en place au début de la pandémie et supervise toutes les approbations de recommandations thérapeutiques; les processus de mise en œuvre sont également discutés au sein du réseau, ce qui a permis une évaluation continue du processus et des interventions rapides en cas de problèmes de mise en œuvre. Cette approche collaborative a été essentielle pour le déploiement. Citation 2 : La possibilité de modifier les règlements pour permettre aux pharmaciens de prescrire a joué un rôle déterminant dans le déploiement. |
L'indisponibilité des infrastructures informatiques et de travail préexistantes pour répondre aux besoins de la mise en œuvre (p. ex., stockage, flux de travail) Citation 1 : L'un des principaux défis du déploiement à XX a été le manque de ressources, en particulier pendant le pic d'infections par la COVID-19, qui a coïncidé avec le début du déploiement. Compte tenu de la capacité limitée, il a été difficile de respecter le délai de cinq jours pour les prescriptions, et certains patients ont appelé parce qu'ils n'allaient pas respecter le délai de traitement. Les prestataires faisaient des heures supplémentaires pour s'assurer que les patients recevaient leur ordonnance, ce qui a également entraîné de la fatigue chez les prestataires. Au départ, il n'était pas possible d'assurer le suivi des patients; aujourd'hui, les infirmières sont en mesure d'assurer un suivi à partir du deuxième et du sixième jour. Citation 2 : XX a dû s'appuyer sur ses infrastructures de pharmacie d'hôpital pour livrer les stocks aux pharmacies communautaires, ce qui a mis à rude épreuve des ressources qui ne sont pas organisées pour mener à bien de telles activités. Citation 3 : Le principal obstacle au stockage de PaxlovidTM a été l'espace de stockage, certaines pharmacies communautaires ne disposant pas de l'espace nécessaire pour stocker des volumes importants compte tenu du faible taux d'utilisation. |
| Domaine de l'innovation | s.o. | Perception d'un niveau de preuve insuffisant quant à l'efficacité du traitement Citation 1 : […] les avantages de PaxlovidTM ont été démontrés par un seul essai mené auprès d'une population en particulier. Citation 2 : Les données probantes sur PaxlovidTM étant limitées, la prise de décisions concernant l'admissibilité et l'accès a été difficile au début du déploiement. Interactions médicamenteuses (autres produits avec moins d'interactions médicamenteuses/plus faciles à gérer) Citation 1 : La réaction des professionnels de la santé a été partagée, certains ayant participé à la mise en œuvre ou demandé l'accès à PaxlovidTM avant sa mise à disposition, tandis que d'autres ont exprimé leur appréhension à prescrire PaxlovidTM en raison de la complexité des interactions médicamenteuses et du manque de soutien. Citation 2 : Au départ, l'adoption de PaxlovidTM par les prescripteurs a été lente, avec une certaine hésitation en raison de la complexité et des interactions médicamenteuses. |
| Domaine du contexte externe | Pratiques de collaboration plurigouvernementale et pluridisciplinaire Citation 1 : La volonté du conseil des pharmaciens de modifier la loi pour permettre aux pharmaciens de prescrire le traitement contre la COVID-19 a amélioré l'accès des patients et a joué un rôle important dans le déploiement, d'autant plus qu'une partie de la population n'a pas accès à un professionnel de la santé. Le lancement dans les pharmacies communautaires, associé à l'accès aux trousses de dépistage, a également joué un rôle important dans l'augmentation de l'accès à PaxlovidTM dans le délai de cinq jours. Approvisionnement fédéral et disponibilité de l'intervention Citation 1 : Dans l'ensemble, XX apprécie le rôle joué par le gouvernement fédéral dans l'approvisionnement et l'accès accéléré à PaxlovidTM. Un soutien et des conseils ont été apportés tout au long du processus, et le stock attribué est utilisé. Citation 2 : XX reconnaît qu'il est important que l'Agence prenne l'initiative de l'approvisionnement, car il n'aurait pas été possible d'approvisionner sa population autrement, compte tenu des pénuries à l'échelle mondiale. L'approvisionnement était essentiel pour assurer l'accès à leur population. En outre, les groupes de travail ont favorisé la collaboration et la transparence; les enjeux ont été discutés au fur et à mesure qu'ils se présentaient, ce qui a facilité le déploiement. |
Le contexte mondial de pénurie de l'offre restreint la communication et la capacité de mise en œuvre Citation 1 : En outre, compte tenu de l'offre limitée au début, la planification du déploiement et la garantie de l'accès à PaxlovidTM sans épuiser les stocks ont constitué un défi pour XX. Citation 2 : De même, lorsque l'accès a été élargi pour la première fois, certains patients ne savaient pas que PaxlovidTM était accessible par l'intermédiaire de leurs fournisseurs et pharmacies habituels; une communication accrue a été nécessaire pour sensibiliser les patients. Délai de mise en œuvre court Citation 1 : […] l'urgence de l'autorisation n'a pas suivi les processus habituels pour les essais cliniques et les protocoles de données probantes. Les avantages ont été évalués à l'aide d'un seul essai clinique et PaxlovidTM a été approuvé et distribué très rapidement. |
La capacité d'adaptation à un contexte en évolution rapide et la collaboration entre les intervenants sont apparues comme des facteurs favorables cruciaux, évidents dans les domaines de l'individu (caractéristiques et rôles), du processus de mise en œuvre et des contextes interne et externe du CFIR. La disponibilité de recommandations, produits par l'ACMTS Note de bas de page 10, l'Agence et les comités consultatifs d'experts, au début de la mise en œuvre, ainsi que leur adaptation au contexte de l'administration (c.-à-d., priorisation des groupes en quête d'équité et des populations à haut risque) pour la création d'outils de dépistage et de déclaration ont permis de rationaliser le processus, facilitant ainsi le classement par priorité, l'évaluation et, dans certains cas, le suivi efficaces des patients. La collaboration plurigouvernementale et pluridisciplinaire a facilité l'élaboration de processus améliorés, aidés par des systèmes préexistants de diffusion de l'information, d'accès aux outils de test et de dépistage, et de délivrance de médicaments en temps opportun. La formation complète, l'apprentissage continu et les documents d'orientation destinés aux prescripteurs ont largement contribué au succès de l'intervention, diffusée par le biais de divers canaux préexistants et nouveaux, tels que les associations de professionnels de la santé, les établissements universitaires, et même par le biais de messages informels sur une application courante de messagerie interne. La disponibilité et l'admissibilité d'autres modalités de test (c.-à-d., les tests antigéniques rapides et les tests moléculaires rapides au point d'intervention) ont contribué à simplifier le déploiement dans les phases ultérieures, ainsi qu'à garantir l'accès au N/R dans les communautés éloignées et rurales dans la fenêtre d'admissibilité de cinq jours. Il a été signalé que les politiques élargissant l'autorité des pharmaciens et des infirmières communautaires pour prescrire et administrer le N/R augmentaient l'utilisation. Enfin, les considérations d'équité ont guidé la mise en œuvre des composantes et activités visant à donner la priorité aux populations à haut risque (p. ex., les résidents des établissements de soins de longue durée, les populations autochtones et les personnes racialisées et marginalisées).
Les éléments contribuant aux obstacles à la mise en œuvre de la N/R au Canada ont été principalement observés dans les domaines de l'individu (caractéristique), du processus de mise en œuvre, de l'innovation et des contextes internes et externes du CFIR. L'absence perçue d'avantages et la complexité de la prescription du médicament, attribuée à un manque de données probantes et à de nombreuses interactions médicamenteuses, ont influencé les attitudes à l'égard de son adoption. Le court laps de temps entre l'autorisation et la distribution et les contraintes dans l'offre au niveau mondial dans le contexte d'une pandémie ont posé des défis aux infrastructures des services de santé, en particulier pour la mise en place des processus administratifs, des technologies de l'information et des infrastructures de travail nécessaires à l'identification en temps voulu des patients admissibles et des meilleurs candidats, ainsi qu'à la fourniture en temps voulu du traitement. La mise en place de systèmes permettant d'identifier les cas positifs grâce aux tests PCR a présenté des défis au départ, mais s'est améliorée avec la généralisation des tests antigéniques rapides. En ce qui concerne l'approvisionnement, certaines administrations ont exprimé le besoin de permettre une capacité de stockage centralisée et une distribution fédérale des produits thérapeutiques, ainsi que d'élargir les processus de coordination FPT en cas de pandémie afin d'inclure des discussions cliniques. La contrainte de l'offre mondiale a également influencé les stratégies de communication et les modèles d'organisation des services dans un premier temps, jusqu'à ce que l'offre canadienne se stabilise. Les limitations infrastructurelles et les ressources humaines insuffisantes, y compris des prestataires de soins de santé, ont également eu un impact sur le déploiement de la N/R au Canada. Sur la base des conclusions de l'analyse thématique, une trajectoire des patients pour accéder au N/R au Canada ainsi que des stratégies possibles pour faciliter le processus ont été dégagés (voir la figure 2).

Figure 2 : Équivalent textuel
Figure montrant la trajectoire des patients pour accéder au nirmatrelvir/ritonavir (N/R) et ses dimensions, y compris les stratégies possibles. 1) L'approvisionnement : l'offre mondiale et nationale, les attributions, le système de distribution et le coût (le coût n'a pas été évalué); les stratégies possibles sont un stockage centralisé et une planification à long terme; 2) L'apparition de symptômes de la COVID-19 (non évaluée) : les comportements liés à la santé, les connaissances, attitudes et comportements (CAC) liés à la COVID-19; les stratégies possibles sont des communications accrues, une mobilisation communautaire, des études sur les CAC et des stratégies basées sur les perceptions documentées; 3) Les tests de la COVID-19 : la perception du risque et les comportements liés à la santé (non évalué), les critères de test et l'accessibilité des tests; les stratégies possibles sont un testage facilité et une disponibilité continue; 4) L'évaluation pour N/R et l'ordonnance : Les critères d'admissibilité (approvisionnement, données probantes, demande), la fenêtre de cinq jours, les interactions médicamenteuses, le modèle d'organisation des services, les ressources des systèmes de santé et l'accessibilité (l'accessibilité a été partiellement explorée), les stratégies possibles sont des essais de plateforme adaptative, une consolidation des formations, des outils efficaces, une stabilisation des ressources et une simplification des modèles d'organisation des services; 5) Distribution du N/R : le modèle d'organisation des services, les ressources des systèmes de santé et l'accessibilité (l'accessibilité a été partiellement explorée), les stratégies possibles comprennent des données sur les lacunes en accessibilité, des études sur les CAC, des stratégies pour supporter l'adhérence et des mesures pour accroître l'accessibilité; et 6) L'administration du N/R (non évaluée) : la perception du risque et les effets indésirables. Les dimensions de l'accessibilité qui ont été partiellement explorées et les stratégies possibles entre parenthèses comprennent : l'abord facile/accessibilité (p. ex., la complexité du langage et la distance), l'acceptabilité (p. ex., la sécurité culturelle), la disponibilité et l'accommodement (p. ex., les temps d'attente, les services aux 24 h, l'abordabilité (p. ex., sans coût) et le caractère approprié du traitement.
Notes de bas de page figure 2
Abréviations : CAC, connaissances, attitudes et comportements; IM, interactions médicamenteuses; N/R, nirmatrelvir/ritonavir
- Note de bas de page a
-
Le texte orange indique les dimensions qui n'ont pas été explorées dans la présente évaluation; le texte bleu indique les dimensions qui ont été partiellement explorées dans la présente évaluation Note de bas de page 7
Discussion
Cette étude qualitative visait à examiner la mise en œuvre de la N/R au cours des six premiers mois suivant son approbation au Canada pendant la pandémie de COVID-19. L'objectif était d'identifier les principaux facteurs favorables et défis rencontrés au cours de ce processus de mise en œuvre et d'en tirer des leçons applicables à la mise en œuvre de futurs traitements ambulatoires afin d'améliorer la préparation aux pandémies dans le contexte canadien. Bien que les critères d'admissibilité et les modèles d'organisation des services aient varié d'une administration à l'autre en raison des différences en matière d'infrastructures des systèmes de santé, les conclusions de cette évaluation ont souligné l'importance de la communication, du partenariat et de la collaboration, ainsi que de la flexibilité et de l'adaptabilité des politiques et des processus de mise en œuvre pour garantir un accès équitable aux traitements contre la COVID-19. En effet, les administrations ont partagé leurs connaissances et leurs ressources, que ce soit avec des documents d'orientation ou des protocoles de test et de dépistage, afin de faciliter le déploiement du N/R. Le contexte dans lequel le N/R a été mis en œuvre, le court délai de mise en œuvre dans un contexte de pénurie mondiale, ainsi que des éléments directement liés au produit thérapeutique (c.-à-d., la complexité des produits thérapeutiques en raison des nombreuses interactions médicamenteuses et du manque perçu de données probantes, et la courte fenêtre d'admissibilité), ainsi que les limitations en matière d'infrastructures et de main-d'œuvre, ont posé des défis à sa mise en œuvre.
Notre analyse a permis de dégager dix thèmes liés aux facteurs favorables et huit thèmes liés aux défis (voir le tableau 2). Bien que les facteurs affectant l'adoption et les obstacles varient d'une administration à l'autre en fonction de la structure du système de santé, des caractéristiques de la population et de la capacité d'analyse des données, des stratégies ont été proposées en synthétisant les idées des participants et en tenant compte des défis et des approches réussies, afin de lever certains des obstacles mis en évidence dans la présente étude (figure 2). Ces stratégies s'appliquent également à l'ensemble de la chaîne d'approvisionnement en N/R, de l'achat à la délivrance ou à l'administration aux patients. La capacité du système de santé a eu une incidence notable sur le déploiement du N/R, la capacité des soins primaires étant un facteur critique soulevé par les participants à l'évaluation. Bien que certains défis soient systémiques et complexes, des stratégies réalisables pourraient inclure la consolidation de la formation des prestataires, la simplification des parcours des patients et la garantie d'un accès continu aux tests rapides pour les patients admissibles au traitement. Il est essentiel de gérer les barrières d'accès associés aux coûts (pour les patients) en proposant des tests et des traitements gratuits, d'autant plus que les effets de la COVID-19 ne sont pas uniformément répartis au sein des populations canadiennes Note de bas de page 13. Bien qu'il faille s'attendre à des variations dans la mise en œuvre, compte tenu de la grande diversité de la population et des défis uniques présents dans les administrations. En outre, les leçons apprises de la mise en œuvre du N/R peuvent contribuer à orienter les futurs efforts de mise en œuvre de produits thérapeutiques et à éclairer la planification fédérale en cours pour renforcer la préparation du Canada aux menaces pour la santé publique, alors que le Canada met à jour son plan de préparation aux pandémies Note de bas de page 14. Elles peuvent contribuer à la planification logistique de la mise en œuvre des produits thérapeutiques (p. ex., les tests, le stockage et la surveillance de la distribution et de la délivrance), ainsi qu'à la facilitation de la collaboration FPT et autochtone au cours des processus décisionnels afin de garantir un accès et une distribution équitables des produits thérapeutiques dans les situations d'urgence sanitaire à venir.
Limites
Le niveau de participation a été élevé, la quasi-totalité des administrations ayant participé à l'évaluation. Les participants aux séances de discussion étaient variés et comprenaient des personnes qui contribuaient à différentes capacités (c.-à-d., des professionnels de la santé et des gestionnaires de soins de santé). Ainsi, des expériences vécues partout au pays ont été prises en compte, ce qui a permis de mieux comprendre les processus de mise en œuvre du N/R. L'évaluation présente toutefois des limites potentielles : les perspectives des patients et des autres composantes locales ou régionales du système de soins de santé n'ont pas été explorées, et les informations obtenues provenaient des expériences des participants. La dynamique potentielle entre les participants ne peut être exclue puisque les séances de discussion se sont déroulées en groupes pour chaque administration. En outre, bien qu'il ait été indiqué que les résultats de l'évaluation seraient anonymisés et que les données acquises seraient traitées de manière à garantir la confidentialité des participants, le risque de biais de désirabilité subsiste, car les séances de discussion ont été animées par des employés de l'Agence. Il existe également un risque de biais de rappel de la part des personnes interrogées, étant donné que l'évaluation a porté sur les expériences vécues au cours des six premiers mois de la mise en œuvre. En outre, si le CFIR permet de mieux comprendre les processus de mise en œuvre, la complexité et la portée de ses 39 concepts peuvent limiter sa généralisabilité et la cohérence de son application; ces limites ont été atténuées en définissant la portée des paramètres pour faciliter la reproductibilité.
Conclusion
Il a été décrit précédemment que les comportements des patients en matière de demande de soins de santé étaient influencés par leurs connaissances, leurs attitudes et leurs croyances Note de bas de page 6Note de bas de page 7, ainsi que par l'accessibilité des services de diagnostic (tests) et de traitement. Bien que cette évaluation n'ait pas porté sur les connaissances, les attitudes et les comportements des patients et des prestataires, des travaux futurs dans ce domaine permettraient d'éclairer davantage les efforts de mise en œuvre de produits thérapeutiques et de comprendre et de relever certains des défis identifiés dans la présente étude.
L'évaluation a porté sur la manière dont le N/R a été administré au Canada au cours des six premiers mois de la mise en œuvre, identifiant des points de pression et les considérations à prendre en compte pour les étapes initiales du déploiement d'un produit thérapeutique. Bien que les administrations aient depuis modifié leurs programmes de N/R, les leçons apprises restent précieuses pour le futur déploiement d'un produit thérapeutique dans le contexte d'une menace pour la santé publique.
Déclaration des auteurs
- A. W. — Gestion de projet, conceptualisation, méthodologie, animation de séances de discussion, analyse de données, interprétation, rédaction de la version originale, rédaction–révision et édition
- C. T. — Conceptualisation, méthodologie, animation de séances de discussion, analyse de données, interprétation, rédaction de la version originale, rédaction–révision et édition
- N. S. — Supervision, conceptualisation, méthodologie, animation de séances de discussion, interprétation de données, rédaction–révision et édition
Contributeurs
Des représentants de 14 administrations qui ont contribué au projet d'évaluation de la mise en œuvre.
Intérêts concurrents
N. S. avait déjà eu certaines interactions avec certains des participants à la présente étude dans le cadre d'autres activités de l'Agence de la santé publique du Canada.
Identifiants ORCID
- Aklile Workneh — 0009-0009-7098-6622
- Camilia Thieba — 0000-0002-7444-630X
Remerciements
Nous tenons à remercier tous les représentants des provinces, des territoires et des ministères fédéraux participants, dont les contributions et la collaboration ont rendu ce projet possible.
Financement
Ce travail a été soutenu par l'Agence de la santé publique du Canada. Aucun fonds supplémentaire n'a été accordé à l'Agence de la santé publique du Canada pour effectuer la présente évaluation, pas plus que l'Agence de la santé publique du Canada n'a accordé de fonds aux administrations participantes. Tous les travaux d'évaluation ont été effectués avec les ressources existantes.
Références
- Notes de bas de page 1
-
Santé Canada. Santé Canada homologue PaxlovidTM pour les patients atteints d'une forme légère ou modérée de COVID-19 qui présentent un risque élevé d'évolution vers une forme grave de la maladie. Ottawa, ON : SC; 2022. [Consulté le 16 janv. 2024]. https://www.canada.ca/fr/sante-canada/nouvelles/2022/01/sante-canada-homologue-paxlovidtm-pour-les-patients-atteints-dune-forme-legere-ou-moderee-de-covid-19-qui-presentent-un-risque-eleve-devolution-ver.html
- Notes de bas de page 2
-
Hammond J, Leister-Tebbe H, Gardner A, Abreu P, Bao W, Wisemandle W, Baniecki M, Hendrick VM, Damle B, Simón-Campos A, Pypstra R, Rusnak JM; EPIC-HR Investigators. Oral Nirmatrelvir for High-Risk, Nonhospitalized Adults with Covid-19. N Engl J Med 2022;386(15):1397–408. https://doi.org/10.1056/NEJMoa2118542
- Notes de bas de page 3
-
Donabedian A. Evaluating the quality of medical care. Milbank Q 2005;83(4):691–729. https://doi.org/10.1111/j.1468-0009.2005.00397.x
- Notes de bas de page 4
-
Damschroder LJ, Aron DC, Keith RE, Kirsh SR, Alexander JA, Lowery JC. Fostering implementation of health services research findings into practice: a consolidated framework for advancing implementation science. Implement Sci 2009;4:50. https://doi.org/10.1186/1748-5908-4-50
- Notes de bas de page 5
-
RE-AIM. What is RE-AIM? – RE-AIM. [Consulté le 1er juin 2022]. https://re-aim.org/learn/what-is-re-aim/
- Notes de bas de page 6
-
Glanz K, Bishop DB. The role of behavioral science theory in development and implementation of public health interventions. Annu Rev Public Health 2010;31:399–418. https://doi.org/10.1146/annurev.publhealth.012809.103604
- Notes de bas de page 7
-
Levesque JF, Harris MF, Russell G. Patient-centred access to health care: conceptualising access at the interface of health systems and populations. Int J Equity Health 2013;12(1):18. https://doi.org/10.1186/1475-9276-12-18
- Notes de bas de page 8
-
International QS. (1999) NVivo Qualitative Data Analysis Software NVIVO 12. https://qsrinternational.com/nvivo/nvivo-products/
- Notes de bas de page 9
-
Guest G, McLellan E. Distinguishing the trees from the forest: applying cluster analysis to thematic qualitative data. Field Methods 2003;15(2):186–201. https://doi.org/10.1177/1525822X03015002005
- Notes de bas de page 10
-
Agence des médicaments du Canada et technologies de la santé et systèmes. Le nirmatrelvir et le ritonavir (Paxlovid) dans le traitement de la COVID-19 légère ou modérée. Ottawa, ON : AMCTSS; 2022. https://www.cda-amc.ca/fr/le-nirmatrelvir-et-le-ritonavir-paxlovid-dans-le-traitement-de-la-covid-19-legere-ou-moderee
- Notes de bas de page 11
-
Pfizer Canada UCL. PAXLOVIDTM (nirmatrelvir tablets; ritonavir tablets). Product Monograph. 2022. https://covid-vaccine.canada.ca/info/pdf/paxlovid-pm-en.pdf
- Notes de bas de page 12
-
Pfizer. Pfizer Reports Additional Data on PaxlovidTM Supporting Upcoming New Drug Application Submission to U.S. FDA | Pfizer. 2022. [Consulté le 9 sept. 2024]. https://www.pfizer.com/news/press-release/press-release-detail/pfizer-reports-additional-data-paxlovidtm-supporting
- Notes de bas de page 13
-
Agence de santé publique du Canada. Du risque à la résilience : Une approche axée sur l'équité concernant la COVID-19. Rapport de l'administratrice en chef de la santé publique du Canada sur l'état de la santé publique au Canada. Ottawa, ON : ASPC; 2020. [Consulté le 18 nov. 2022]. https://www.canada.ca/fr/sante-publique/organisation/publications/rapports-etat-sante-publique-canada-administrateur-chef-sante-publique/du-risque-resilience-approche-equite-covid-19.html
- Notes de bas de page 14
-
Agence de santé publique du Canada. À propos du nouveau plan de préparation en cas de pandémie au Canada. Ottawa, ON : ASPC; 2025. [Consulté le 30 juillet 2025]. https://www.canada.ca/fr/sante-publique/services/mesures-interventions-urgence/propos-nouveau-plan-preparation-pandemie.html

Cette œuvre est mise à disposition selon les termes de la Licence Creative Commons Attribution 4.0 International