Lignes directrices relatives à l’intervention et à la gestion d’un événement ou d’une éclosion de poliovirus au Canada
Télécharger en format PDF
(1,108 Ko, 54 pages)
Organisation : Agence de la santé publique du Canada
Date publiée : septembre 2024
Cat. : HP40-343/2023F-PDF
ISBN : 978-0-660-49136-3
Pub. : 230129
Mise à jour : septembre 2024
Table des matières
- Acronymes
- Buts et objectifs
- 1. Introduction
- 2. Définition d'un événement ou d'une éclosion de poliovirus
- 3. Importance d'une détection, d'une notification et d'une enquête rapides
- 4. Rôles et responsabilités des autorités fédérales, provinciales et territoriales
- 5. Classification des cas
- 6. Détection
- 7. Notification
- 8. Enquête
- 9. Gestion des cas et des contacts
- 10. Évaluation des risques
- 11. Intervention de la santé publique en cas d'événement ou d'éclosion de poliovirus au Canada
- Remerciements
- Ressources
- Annexes
- Annexe A : Principales étapes initiales et exigences en matière de notification
- Annexe B : Gestion de la santé publique d'un événement lié à l'installation impliquant le poliovirus
- Annexe C : Protocoles de laboratoire
- Annexe D : Signalements en vertu du RSI
- Annexe E : Évaluation initiale des risques de l'IMEP
- Références sélectionnées
Acronymes
- PFA
- Paralysie flasque aiguë
- VPOb
- Vaccin antipoliomyélitique oral bivalent
- RMTC
- Relevé des maladies transmissibles au Canada
- CDC
- Centers for Disease Control and Prevention des États-Unis
- SCP
- Société canadienne de pédiatrie
- PCSP
- Programme canadien de surveillance pédiatrique
- RCRSP
- Réseau canadien de renseignements sur la santé publique
- PAM
- Plan d'action mondial (pour le confinement du poliovirus)
- IMEP
- Initiative mondiale pour l'éradication de la poliomyélite
- LAPHT
- Loi sur les agents pathogènes humains et les toxines
- RSI
- Règlement sanitaire international (2005)
- VPI
- Vaccin antipoliomyélitique inactivé
- ANC
- Autorité nationale de confinement (du poliovirus)
- CCNI
- Comité consultatif national de l'immunisation
- nVPO
- Nouveau vaccin antipoliomyélitique oral
- LNM
- Laboratoire national de microbiologie
- VPO
- Vaccin antipoliomyélitique oral
- USPPI
- Urgence de santé publique de portée internationale
- OPS
- Organisation panaméricaine de la santé
- ASPC
- Agence de la santé publique du Canada
- MPI
- Matière potentiellement infectée (par la polio)
- PT
- Provinces et territoires ou provincial/territorial
- TIP
- Trouble d'immunodéficience primaire
- PON
- Procédures opérationnelles normalisées
- PPAV
- Poliomyélite paralytique associée à la vaccination
- PVDVc
- Poliovirus circulant dérivé d'une souche vaccinale
- PVDV
- Poliovirus dérivé d'une souche vaccinale
- OMS
- Organisation mondiale de la Santé
- PVS
- Poliovirus sauvage
Buts et objectifs
Les Lignes directrices relatives à l'intervention et à la gestion d'un événement ou d'une éclosion de poliovirus au Canada fournissent des pratiques exemplaires pour aider à se préparer au poliovirus, à le détecter et à le contrôler, et définissent les rôles et les responsabilités pour une intervention coordonnée à travers le pays. Les objectifs des mesures décrites dans les lignes directrices sont les suivants :
- Améliorer la détection rapide et précoce, la notification et les enquêtes pour appuyer la mise en œuvre en temps opportun des contrôles de santé publique afin de limiter la propagation et de soutenir l'éradication mondiale de la poliomyélite.
- Réduire l'impact du poliovirus sur la santé des Canadiens.
- Veiller à ce que les interventions en santé publique soient fondées sur les pratiques exemplaires, les données scientifiques et les avis d'experts.
1. Introduction
1.1 Polio
La poliomyélite (polio) est une maladie virale très contagieuse qui peut s'attaquer au système nerveux central et endommager les cellules nerveuses qui activent les muscles. La plupart des personnes infectées ne présentent pas de symptômes, toutefois certaines personnes deviennent symptomatiques et une faible proportion des infections entraîne de graves symptômes tels que la paralysie. Dans les pays où la couverture vaccinale des enfants est faible, les infections par le poliovirus sont plus fréquentes chez les enfants de moins de 5 ans; toutefois, toute personne qui n'est pas immunisée contre le poliovirus, peu importe son âge, peut être infectée. Le poliovirus se transmet essentiellement par voie oro-fécale, en particulier dans les régions où l'assainissement est déficient (c'est-à-dire où le virus excrété peut contaminer les aliments ou l'eau, ou se propager directement d'une personne à l'autre). La propagation par voie respiratoire est également possible, mais elle est moins fréquente.
Depuis 2014, le directeur général de l'Organisation mondiale de la Santé (OMS) considère la propagation internationale du poliovirus comme une urgence de santé publique de portée internationale (USPPI). L'USPPI a introduit des recommandations temporaires pour réduire la propagation internationale afin de soutenir l'éradication de la poliomyélite et de prévenir la réintroduction du poliovirus dans les régions qui ont atteint l'élimination Note de bas de page 1.
Il existe trois sérotypes de poliovirus sauvage (PVS) – type 1, type 2 et type 3. Grâce aux efforts de l'Initiative mondiale pour l'éradication de la poliomyélite (IMEP), le PVS de type 2 a été déclaré éradiqué en septembre 2015, le dernier cas ayant été détecté en Inde en 1999 Note de bas de page 2. Le PVS de type 3 a été déclaré éradiqué en octobre 2019, le dernier cas ayant été détecté au Nigeria en 2012 Note de bas de page 3. En septembre 2024, le PVS de type 1 était toujours endémique au Pakistan et en Afghanistan.
Il n'existe aucun médicament particulier contre la polio et les soins sont de nature palliative. Cependant, on peut prévenir la maladie par la vaccination. Deux types de vaccins contre la poliomyélite sont utilisés dans le monde : le vaccin antipoliomyélitique inactivé (VPI) et le vaccin antipoliomyélitique oral (VPO). Le VPI (ou le vaccin Salk) consiste en des souches inactivées (tuées) de poliovirus pour les sérotypes 1, 2 et 3 qui ne sont pas capables de se reproduire et qui sont administrées par injection. Le VPI n'induit pas l'immunité dans l'intestin et, par conséquent, si une personne vaccinée contre le VPI est exposée au poliovirus, elle peut quand même transmettre le poliovirus en rejetant le virus dans ses selles. Le VPO (ou le vaccin Sabin) contient un virus vivant affaibli administré par voie orale. Il se reproduit dans l'intestin pour stimuler une réponse immunitaire protectrice et interrompt efficacement la transmission du virus. Le VPI et le VPO sont sûrs, très efficaces pour prévenir la maladie paralytique et ont joué un rôle essentiel dans les efforts mondiaux d'éradication. Au Canada, seul le VPI est utilisé depuis 1995-1996.
Après l'administration du VPO, le virus du vaccin est excrété dans les selles et peut se transmettre d'une personne à l'autre par voie fécale-orale. Par conséquent, on peut trouver des virus vaccinaux Sabin ou de type Sabin dans des échantillons d'eaux usées environnementaux dans les régions où le VPO est utilisé ou dans une région où se rend une personne ayant récemment reçu le VPO.
Outre le poliovirus sauvage, le poliovirus dérivé d'une souche vaccinale (PVDV) est une autre forme de poliovirus présente à l'échelle mondiale. Le PVDV peut se développer dans les communautés où la couverture vaccinale est faible lorsque le virus vivant du VPO mute en se propageant d'une personne sous-vaccinée à une autre sur une longue période (environ 12 à 18 mois) ou, dans de rares cas, en se reproduisant pendant une période prolongée chez un hôte immunodéprimé. De cette façon, les souches du VPO peuvent perdre leurs propriétés atténuées (affaiblies) et revenir à une forme virulente, ce qui donne un PVDV qui se comporte de la même façon que le virus de type sauvage et peut être tout aussi pathogène et transmissible. Par définition, une souche sera classée PVDV si la région génomique de la capside virale (VP1) est > 1 % divergent (ce qui signifie > = 10 changements nucléotidiques) de la souche du sérotype 1 et 3 du VPO ou > 0,6 % divergent (ce qui signifie > = 6 changements nucléotidiques) de la souche du VPO du sérotype 2. Une souche virale qui est < 1 % (type 1 ou 3) ou < 0,6 % (type 2) divergent de la souche vaccinale est classée de type Sabin ou de type vaccin Note de bas de page 4.
Lorsqu'il y a des signes de transmission de personne à personne du PVDV dans une communauté, on définit les PVDV comme des PVDV circulants ou PVDVc. Les personnes qui sont entièrement immunisées contre la poliomyélite (soit avec le VPI ou le VPO) seront protégées contre la paralysie causée par le poliovirus de type sauvage et le PVDV.
La poliomyélite paralytique associée à la vaccination (PPAV) est différente du poliovirus dérivé d'une souche vaccinale (PVDV). La PPAV est un événement indésirable rare découlant de la vaccination par le VPO lorsque l'un des virus atténués ou affaiblis du VPO cause la poliomyélite paralytique chez une personne qui a reçu le VPO ou ses contacts étroits. Au Canada, le VPI est utilisé exclusivement pour la vaccination et ne comporte aucun risque de PPAV. Toutes les provinces et tous les territoires (PT) financent publiquement le VPI dans le cadre des programmes de vaccination systémique Note de bas de page 5.
L'OMS recommande que tous les enfants soient vaccinés contre la poliomyélite. Comme le PVS de type 2 a été éradiqué en 2015 et que la plupart des PVDVc détectés dans le monde sont de type 2, la composante de type 2 du VPO a été supprimée en faveur d'un VPO bivalent (types 1 et 3) en 2016 Note de bas de page 6. En avril 2019, tous les pays qui continuent d'utiliser le VPOb ont intégré au moins une dose de VPI dans les programmes de vaccination systémique Note de bas de page 7. L'OMS fournit des recommandations sur le calendrier de vaccination pour les pays qui utilisent une combinaison de VPI et de VPO dans des exposés de principes sur les vaccins contre la poliomyélite Note de bas de page 8.
En date de novembre 2020, l'OMS a autorisé l'utilisation d'urgence d'un nouveau vaccin, le nouveau VPO de type 2 (nVPO2), dans certaines situations, pour répondre aux éclosions de PVDVc2 Note de bas de page 9. Le nVPO2 est une version modifiée du VPO2 monovalent qui offre une protection comparable, mais qui est plus stable sur le plan génétique et moins susceptible d'être associée à l'émergence du PVDV Note de bas de page 10. Étant donné que le nVPO2 est utilisé dans le cadre de la Liste des utilisations d'urgence de l'OMS, les pays doivent satisfaire à des critères précis avant de l'utiliser, et son efficacité et sa sécurité sont étroitement surveillées, y compris l'évaluation de sa capacité à revenir à une forme plus virulente qui se comporte comme le poliovirus de type sauvage Note de bas de page 11. Le nVPO2 fait l'objet d'une évaluation pour l'homologation complète du vaccin et de nouveaux VPO ciblant les types 1 et 3 sont également en cours d'élaboration Note de bas de page 12.
1.2 Contexte canadien
Depuis 1924, la poliomyélite fait partie des maladies à déclaration obligatoire à l'échelle nationale et est incluse dans le Système canadien de surveillance des maladies à déclaration obligatoire (SCSMDO). De plus, pour veiller à ce que le Canada maintienne son statut de pays exempt de poliomyélite conformément à l'OMS, l'Agence de la santé publique du Canada (ASPC), en collaboration avec la Société canadienne de pédiatrie (SCP), effectue la surveillance de la paralysie flasque aiguë (PFA) chez les enfants de moins de 15 ans. La PFA est un résultat possible d'une infection par le poliovirus qui implique l'apparition aiguë d'une paralysie dans un ou plusieurs membres, mais qui peut également être causée par un certain nombre d'autres virus, ainsi que d'autres causes. En cherchant activement des cas de PFA au Canada et en écartant la poliomyélite, le Canada est en mesure de fournir des preuves continues que le pays demeure exempt de poliomyélite. Le Canada signale les cas de PFA à l'Organisation panaméricaine de la santé (OPS) deux fois par année. Le rendement de la surveillance de la PFA est évalué en fonction de trois indicateurs clés établis par l'OMS :
- Détecter au moins un cas de FPA non poliomyélitique par an pour 100 000 personnes âgées de moins de 15 ans.
- Tous les cas de PFA devraient faire l'objet d'une enquête clinique et virologique complète, au moins 80 % des cas de PFA ayant fait l'objet d'un prélèvement « adéquat » de selles.
- Au moins 80 % des cas de PFA devraient faire l'objet d'un examen de suivi 60 jours après l'apparition de la paralysie.
Le Canada, et de nombreux autres pays qui ont réussi à éliminer la poliomyélite, ne respectent pas toujours les principaux indicateurs de surveillance de la FPA pour des raisons comme la disponibilité de diagnostics rapides qui confirment un diagnostic alternatif, le signalement rétrospectif des cas de FPA, et le manque de connaissances cliniques sur les exigences en matière de tests sur les selles Note de bas de page 13. Bien que la surveillance de la PFA au Canada ne soit pas conforme aux indicateurs de l'OMS, le Système canadien de surveillance de la PFA continue d'être un système de surveillance sensible et actif pour l'enquête rapide et appropriée des cas de PFA afin de détecter la poliomyélite.
Aucun cas endémique de poliovirus sauvage n'a été découvert au Canada depuis 1979 et le Canada a été certifié exempt de poliomyélite par l'OMS en 1994Note de bas de page 14. Les cas de poliovirus sauvage signalés au Canada depuis lors ont été associés à des importations en provenance de pays où le virus circulait encore. Le Canada n'a pas détecté de poliovirus sauvage depuis 1996. Depuis 2004, quatre cas de poliovirus ressemblant à celui de Sabin ont été détectés dans des cas non paralytiques, et un cas probable de PPAV a été signalé au Canada, qui ont tous été importés d'endroits à l'extérieur du Canada où le VPO a été utiliséNote de bas de page 15. Tant que l'éradication de la poliomyélite n'aura pas été réalisée à l'échelle mondiale et que le VPO ne sera plus utilisé, il subsistera un faible risque d'importation de poliovirus (de type sauvage, Sabin ou de type Sabin, ou poliovirus dérivé d'une souche vaccinale) au Canada.
En vertu de la résolution de la 71e Assemblée mondiale de la santé (2018), le Canada a pris des engagements internationaux en matière de confinement biologique du poliovirus. La 4e édition du Plan d'action mondial de l'OMS pour le confinement du poliovirus identifie les violations du confinement liées aux installations (comme un laboratoire ou une installation de production de vaccins) comme un risque majeur de réapparition de la poliomyélite dans un monde post-éradication Note de bas de page 16. Au Canada, les poliovirus éradiqués ne sont conservés que dans des installations certifiées essentielles pour la protection contre les poliovirus, qui sont contrôlées par l'Autorité nationale de confinement (ANC) au sein du Centre de la biosûreté de l'ASPC.
Le risque de poliomyélite au Canada est minime en raison des pratiques exemplaires en matière de biosécurité, d'un bon assainissement et d'une couverture vaccinale élevée. Une couverture élevée du VPI prévient la paralysie en cas de circulation du virus. La couverture vaccinale contre la polio est élevée au Canada, cependant, il y a encore des communautés au Canada qui ont une faible couverture vaccinale.
1.3 Élaboration des lignes directrices
Les lignes directrices élaborées pour être utilisées lors d'un événement ou d'une éclosion de poliovirus au Canada s'appuient sur les documents suivants : Protocole pour l'investigation des cas de PFA et des cas soupçonnés de poliomyélite paralytique (article du RMTC de 1998) et PON de l'IMEP : Riposte à un Évènement Ou à une Flambée de Poliomyélite (version 4, mars 2022).
Les lignes directrices doivent être utilisées conjointement avec le Plan d'intervention fédéral-provincial-territorial en matière de santé publique dans les cas d'incidents biologiques.
2. Définition d'un événement ou d'une éclosion de poliovirus
Les lignes directrices décrivent la réponse et la gestion d'un événement ou d'une éclosion de poliovirus (poliovirus de type sauvage [PVS], poliovirus dérivé d'une souche vaccinale [PVDV], ou Sabin ou de type Sabin). Un événement de poliovirus vise à capturer les détections de poliovirus provenant de sources humaines, environnementales (eaux usées) ou liées aux installations qui n'indiquent pas la circulation locale. Une éclosion de poliovirus est une détection qui suggère une transmission à l'échelle communautaire.
Les définitions ci-dessous sont adaptées du document PON de l'IMEP : Riposte à un Évènement Ou à une Flambée de Poliomyélite (version 4, mars 2022).
Les critères permettant de confirmer une poliomyélite paralytique ou une infection par le poliovirus non paralytique chez une personne sont décrits ci-dessous à la section 5 : Classification des cas.
Un événement de poliovirus est défini comme suit :
- Détection chez une personne :
- Détection d'une poliomyélite paralytique confirmée (de type sauvage ou PVDV/PVDVc) chez une personne ayant des antécédents de voyage dans une région où le poliovirus circule dans les 35 jours précédant le début de la paralysie, et aucune preuve de transmission locale au Canada; ou
- Détection d'une infection par le poliovirus non paralytique confirmée en laboratoire avec des antécédents de voyage dans une région où le poliovirus circule dans les six semaines précédant la détection du poliovirusRéférence a chez la personne, et aucune preuve de transmission par la communauté locale au Canada; ou
- Poliomyélite paralytique associée à la vaccination (PPAV) :
- PPAV chez un bénéficiaire d'un VPO qui a reçu le VPO dans les 7 à 35 jours précédant le début de la paralysie; ou
- PPAV en contact étroit avec un destinataire de VPO, lorsque l'exposition au contact étroit s'est produite pendant la période de communication du destinataire de VPO (dans les six semaines suivant la réception du VPO).
- Détection environnementale :
- Détection unique dans l'environnement (eaux usées) confirmée en laboratoire (par le Laboratoire national de microbiologie [LNM] du Canada) du PVS, du PVDV ou Sabin ou de type Sabin; ou
- Détections multiples dans l'environnement (eaux usées) confirmées par le LNM de Sabin ou de type Sabin 1 et 3; ou
- Détections multiples dans l'environnement (eaux usées) confirmées par le LNM si elles ne répondent pas aux critères d'une éclosion ci-dessous (par exemple, les détections proviennent d'un site dans les deux mois et aucune preuve de réplication virale continue).
- Liées à l'installationRéférence b : Exposition confirmée au poliovirus spécifique à un type, déversement ou brèche dans un laboratoire ou une installation de production de vaccins qui traite le poliovirus.
Une éclosion de poliovirus est définie comme suit :
- Détection d'une infection confirmée de poliovirus (paralytique ou non paralytique) chez une personne (à moins d'être définie comme un « événement impliquant le poliovirus » ci-dessus); ou
- Deux détections distinctes confirmées par le LNM dans l'environnement (PVS, PVDV, les virus Sabin / de type Sabin 2), où « distinctes » signifie que les échantillons ont été prélevés sur deux sites différents sans chevauchement des zones de captage ou à partir du même site, mais à au moins deux mois d'intervalle; ou
- Tout PVDVc nouvellement détectéRéférence c, que ce soit dans un échantillon humain ou environnemental, c'est-à-dire lorsqu'un PVDV isolé dans des selles humaines ou dans l'environnement peut être immédiatement génétiquement lié à un autre PVDV dans la communauté, confirmant ainsi la circulation dans les zones de détection.
3. Importance d'une détection, d'une notification et d'une enquête rapides
L'identification rapide du poliovirus est essentielle pour identifier la transmission possible. La détection précoce et les enquêtes subséquentes appuient la mise en œuvre rapide de mesures de santé publique visant à limiter la propagation des poliovirus et à maintenir le statut d'élimination atteint par le Canada en 1994. Le Canada doit procéder à une identification et à une enquête précoce pour aviser ses partenaires internationaux afin de faciliter le partage des connaissances et la coopération internationale en matière de santé publique. À ce titre, tous les niveaux du système de santé publique jouent un rôle dans la détection rapide, la notification et l'enquête d'un événement ou d'une éclosion de poliovirus.
4. Rôles et responsabilités des autorités fédérales, provinciales et territoriales
Vous trouverez ci-dessous un aperçu des rôles et des responsabilités de l'ASPC, des autorités de santé publique provinciales et territoriales, locales et régionaux, ainsi que du rôle des laboratoires à tous les niveaux lors d'une intervention de santé publique en cas d'événement ou d'éclosion de poliovirus. Si la gravité, la portée ou l'importance exigent une intervention fédérale, provinciale ou territoriale coordonnée, veuillez consulter l'annexe C du Plan d'intervention fédéral-provincial-territorial en matière de santé publique dans les cas d'incidents biologiques pour voir une liste des rôles et responsabilités du portefeuille fédéral de la santé et des PTs, et examiner la possibilité d'activer les centres des opérations concernés.
4.1 ASPC
Les rôles de l'ASPC dans un événement ou une éclosion de poliovirus, en collaboration avec le Laboratoire national de microbiologie (LNM) de l'ASPC (dont les rôles précis sont décrits ci-dessous), consistent notamment à fournir des lignes directrices et des conseils d'experts, à coordonner la collaboration et la communication interprovinciales/territoriales et internationales, ainsi qu'à élaborer et à coordonner les évaluations des risques de l'ASPC. L'ASPC peut également jouer un rôle de soutien en coordonnant les comités d'enquête sur les éclosions avec les provinces et les territoires dans le cas d'éclosions relevant de plusieurs administrations, ou d'éclosions ou d'événements qui exigent une coordination et une collaboration nationale. L'ASPC fournira un soutien aux enquêtes à la demande d'une province ou d'un territoire. Dans son rôle de point focal du Règlement sanitaire international (RSI) pour le Canada, l'ASPC est également responsable d'aviser l'OMS des incidents qui peuvent constituer une urgence de santé publique de portée internationale (USPPI). L'ASPC, en collaboration avec les PTs touchés, communiquera des renseignements opportuns sur les incidents à d'autres régions du Canada. En outre, l'Autorité nationale de confinement (ANC) du poliovirus du Canada est chargée de tenir à jour l'inventaire national des poliovirus, et de vérifier et d'inspecter les installations essentielles à la lutte contre la polio dans le cadre de la 4e édition du Plan d'action mondial de l'OMS et de la Loi sur les agents pathogènes humains et les toxines (LAPHT) du Canada. Le Comité consultatif national de l'immunisation (CCNI) et le Secrétariat du CCNI de l'ASPC fournissent des conseils sur l'utilisation des vaccins contre la poliomyélite dans les situations où l'on prévoit un risque accru d'exposition au poliovirus.
4.2 Provincial/territorial et local/régional
Les PTs et les administrations locales et régionales sont responsables des diagnostics de première ligne, de la collecte d'échantillons de cas soupçonnés et de la fourniture de services de santé publique et de soins de santé, y compris des programmes de vaccination, aux personnes relevant de leur administration. Les autorités locales de santé publique sont responsables d'entreprendre des enquêtes après la détection du poliovirus ainsi que de la gestion des cas et des contacts, et de veiller à ce que les pratiques appropriées de prévention et de contrôle des infections soient suivies, le cas échéant. Les PTs et les autorités sanitaires locales devraient fournir des renseignements recueillis dans le cadre d'une enquête de santé publique et partager leur expertise avec l'ASPC, afin d'appuyer une intervention concertée associée à un événement ou à une éclosion de poliovirus. Les PTs doivent également collaborer avec l'ASPC pour partager des renseignements opportuns sur les événements avec d'autres régions du Canada et des partenaires internationaux. Les autorités de la santé et de la santé publique devraient également veiller à ce que des procédures appropriées soient en place pour recueillir des renseignements épidémiologiques et cliniques pertinents qui accompagnent les spécimens de cas soupçonnés de poliomyélite, et que les spécimens soient transportés au laboratoire d'analyse de manière sécuritaire et efficace.
4.3 Laboratoire
Le LNM est le seul laboratoire de référence régional de l'OMS pour le poliovirus au Canada et est une installation essentielle à la lutte contre la polio désignée assujettie à la norme et au régime de certification du confinement de la 4e édition du Plan d'action mondial de l'OMS. Le laboratoire de poliovirus du LNM effectue l'isolement des virus et la caractérisation moléculaire par le séquençage du génome et est autorisé pour les activités contrôlées avec les poliovirus en vertu de la LAPHT et du Règlement sur les agents pathogènes humains et les toxines.
Par conséquent, tous les échantillons dont le dépistage est positif pour le poliovirus (s'ils ont été testés) ou les échantillons prélevés d'une poliomyélite soupçonnée ou d'un cas soupçonné de PFA doivent être envoyés au LNM aux fins d'isolement du poliovirus et de caractérisation moléculaire. Les échantillons sont habituellement renvoyés au LNM par le laboratoire de santé publique provincial ou territorial. Toutefois, ils peuvent aussi être envoyés directement au LNM à partir d'un hôpital ou d'un laboratoire communautaire. Si l'envoi se fait directement, les centres sont encouragés à signaler le cas présumé de poliomyélite ou de PFA aux autorités de santé publique locales ou provinciales/territoriales afin d'assurer le respect des lignes directrices des PTs en matière de déclaration des maladies et des conditions à déclaration obligatoire. En raison de la présence possible d'un poliovirus, le LNM manipulera davantage les échantillons, comme le recommande le Plan d'action mondial de l'OMS pour le confinement du poliovirus.
5. Classification des cas
Au moment de l'élaboration des lignes directrices, la définition nationale de cas de poliovirus était en cours de révision. Par conséquent, les lignes directrices font référence à la classification des cas adaptée pour confirmer les cas dans le tableau 1. Pour obtenir des renseignements sur l'identification des cas suspects, consultez la section 8.1.1 : Indice de soupçon de poliomyélite en attente de confirmation en laboratoire.
| Classification des cas | Cas confirmé |
|---|---|
| Poliomyélite paralytique |
|
| Infection par le poliovirus non paralytique |
|
|
|
6. Détection
Tous les échantillons soupçonnés de contenir du poliovirus prélevés par les laboratoires provinciaux, territoriaux et de traitement des eaux usées doivent être envoyés au LNM aux fins d'analyse afin de déterminer la présence de poliovirus. En raison de la présence possible d'un poliovirus, les échantillons respiratoires, fécaux et des eaux usées concentrées et leurs dérivés qui ont été prélevés à un moment et à un endroit où le poliovirus était en circulation, y compris les échantillons qui sont entreposés dans des conditions qui maintiennent la viabilité du virusRéférence d sont considérés comme des matières potentiellement infectées (MPI) du poliovirus. Lors de l'utilisation et de l'entreposage des MPI, des mesures d'atténuation des risques doivent être prises pour prévenir les événements liés à l'installation, comme indiqué dans le document d'orientation sur les MPI de l'OMS (2e édition). Consultez l'annexe C pour plus de détails sur les exigences en matière de MPI.
Pour tous les cas compatibles avec la définition de cas de PFA et tous les cas soupçonnés de poliomyélite, comme indiqué dans la section 8.1.1 : Indice de soupçon de poliomyélite en attente de confirmation en laboratoire, assurez-vous de collecter au moins deux échantillons de selles (prises à un intervalle d'au moins 24 heures et au moins 2 grammes par échantillon) dans les 14 jours suivant l'apparition des symptômes pour les études virales (bien qu'il soit possible de prélever des échantillons jusqu'à 6 semaines après l'apparition s'il n'est pas possible de les prélever plus tôt). En plus de l'analyse des selles, d'autres tests diagnostiques et enquêtes devraient être effectués, le cas échéant, pour aider à détecter les infections de poliovirus ou d'autres conditions qui peuvent présenter des symptômes semblables. Cela peut comprendre ce qui suit :
- Prélèvement d'échantillons respiratoires (prélevés par deux écouvillons oropharyngés ou nasopharyngés) ou de liquide céphalorachidien
- Examens neurologiques, y compris les études de conduction nerveuse ou l'électromyographie, l'imagerie par résonance magnétique (IRM) ou la tomodensitométrie (TDM)
Les selles (deux échantillons prélevés à un intervalle d'au moins 24 heures) constituent l'échantillon clinique requis pour l'enquête en laboratoire et le diagnostic des infections de poliovirus. On préfère un échantillon de selles à un écouvillon rectal parce que le diagnostic de poliovirus est plus fiable. Les échantillons de selles doivent être placés dans un contenant stérile étanche, congelé à ≤-20°C jusqu'à ce qu'ils soient envoyés pour analyse et expédiés congelés sur de la glace sèche. Aucun support spécial n'est requis. Pour obtenir des renseignements sur les spécimens, les prélèvements et d'autres détails de laboratoire pour les échantillons cliniques, veuillez consulter la page Détection et caractérisation moléculaire du LNM. Pour obtenir plus de détails sur les protocoles de laboratoire, consultez l'annexe C.
Pour les échantillons des eaux usées environnementales soupçonnées de contenir du poliovirus, les échantillons doivent être empaqueté par le laboratoire de collecte et envoyés au LNM, conformément aux directives décrites dans le document. Pour obtenir plus de détails sur la soumission d'échantillons d'eaux usées pour des essais en laboratoire, consultez
7. Notification
7.1 Déclarations dans une province ou un territoire
Tout événement ou toute éclosion de poliovirus (tel que défini à la section 2 : Définition d'un événement ou d'une éclosion de poliovirus) doit être signalé immédiatement à l'autorité de santé publique locale ou régionale et aux autorités et laboratoires de santé publique provinciales ou territoriales. Les autorités sanitaires devraient également être avisées des cas en attente d'une confirmation de laboratoire avec suspicion de poliomyélite, comme indiqué à la section 8.1.1 : Indice de soupçon de poliomyélite en attente de confirmation en laboratoire.
Les cas compatibles avec la définition de cas de FPA doivent être signalés à l'autorité locale de santé publique, si la législation l'exige dans l'administration.
7.2 Déclarations entre les autorités PTs et l'ASPC
La poliomyélite est une maladie à déclaration obligatoire au Canada. De plus, pour favoriser la conformité au Règlement sanitaire international (RSI), toutes les PTs doivent aviser les autorités de l'ASPC (courriel : vpd-mev@phac-aspc.gc.ca et hpoc-cops@phac-aspc.gc.ca) dans les 24 heures suivant la détection par les provinces et les territoires du poliovirus pour tout événement ou éclosion de poliovirus, (tel que défini à la section 2 : Définition d'un événement ou d'une éclosion de poliovirus).
Lorsque vous signalez un cas à l'ASPC, indiquez si le cas respecte la classification indiquée à la section 5 : Classification des cas. En plus des cas confirmés, envisagez de signaler à l'ASPC les cas faisant l'objet d'une enquête qui sont compatibles avec la liste des caractéristiques cliniques et qui ont un indice de suspicion plus élevé pour la poliomyélite, comme il est indiqué à la section 8.1.1 : Indice de soupçon de poliomyélite en attente de confirmation en laboratoire.
Dans le cas d'une détection environnementale confirmée ou d'un événement lié à l'installation, il y a des obligations de notification supplémentaires. Les responsables locaux et PT de la santé publique et l'ASPC doivent être avisés de tous les échantillons environnementaux qui contiennent du poliovirus confirmé par le LNM dans les 24 heures. En cas d'événement lié à une installation mettant en cause le poliovirus, l'installation essentielle à la lutte contre la polio réglementée par la LAPHT doit aviser le Centre de la biosécurité par l'entremise du Portail vers la biosûreté sécurisé (Notification d'événement en laboratoire Canada) conformément au paragraphe 12(1) et 13 de la LAPHT.
Une alerte de santé publique du Réseau canadien de renseignements sur la santé publique (RCRSP) devrait être envisagée pour permettre la notification ou la diffusion de l'information en temps opportun entre les intervenants locaux/régionaux, provinciaux et territoriaux et nationaux en santé publique. L'ASPC et le LNM peuvent collaborer avec les autorités locales, régionales et provinciales et territoriales pour émettre une alerte, au besoin.
7.3 Déclarations de l'ASPC à l'OMS
Le jour « 0 » pour la déclaration internationale (à l'OMS) est défini comme le jour où le LNM confirme un résultat positif en laboratoire pour le poliovirus par séquençage génétique (PVDV, PVS, Sabin ou de type Sabin) à partir d'échantillons des eaux usées humaines ou environnementales.
En vertu du RSI, le Canada a l'obligation de signaler, au moyen d'une notification en vertu de l'article 6, tous les incidents qui peuvent constituer une urgence de santé publique de portée internationale sur son territoire Note de bas de page 17. Les équipes techniques pertinentes de l'ASPC ont 48 heures pour effectuer une évaluation à l'aide de l'annexe 2 du RSI « Instrument de décision permettant d'évaluer et de notifier les événements qui peuvent constituer une urgence de santé publique de portée internationale » (annexe D), en travaillant en collaboration avec la province ou le territoire déclarant et le point focal national RSI.
Si, en utilisant l'instrument de décision, il est déterminé que l'incident répond aux critères de l'article 6 (Notification) ou de l'article 7 (Communication d'informations en cas d'événements inattendus ou inhabituels), le Canada doit en aviser l'OMS dans les 24 heures suivant l'évaluation. La déclaration d'un incident en vertu de l'article 6 ou de l'article 7 nécessite une description de l'incident ainsi que les détails disponibles et l'évaluation écrite à l'aide de l'annexe 2 du RSI. Le siège de l'OMS informera les partenaires concernés de l'Initiative mondiale pour l'éradication de la poliomyélite (IMEP).
Comme l'indiquent les définitions de cas du RSI pour les maladies nécessitant une notification, toutes les détections de poliomyélite paralytique dues à un poliovirus de type sauvage nécessitent une notification immédiate en vertu de l'article 6 dans toutes les circonstances. L'ASPC doit envoyer la notification au bureau régional respectif de l'OMS dans les 24 heures suivant le séquençage par le LNM d'un poliovirus à déclaration obligatoire (jour 0) par l'intermédiaire du point focal national RSI (hpoc-cops@phac-aspc.gc.ca et une copie conforme à ihr-rsi@phac-aspc.gc.ca). Il convient de noter que dans ces cas, il n'y a pas de période de 48 heures pour effectuer l'évaluation de l'annexe 2 du RSI.
En plus des cas confirmés en laboratoire de poliomyélite paralytique causée par un poliovirus sauvage, l'isolement des éléments suivants doit généralement être signalé à l'OMS Note de bas de page 18 en tant qu'article 6 ou 7, tel que déterminé par les autorités de la santé publique qui effectuent l'évaluation à l'aide de l'annexe 2 du RSI :
- Isolement du poliovirus sauvage d'un cas d'infection par le poliovirus non paralytique
- Isolement du poliovirus sauvage d'une source non humaine (détection environnementale)
- Isolement du poliovirus dérivé d'une souche vaccinale (types 1, 2, 3) à partir de sources humaines ou non humaines
- Isolement de Sabin ou de type Sabin 2 à partir de sources humaines ou non humaines si elles ont été détectées dans une zone où le VPO2 de Sabin n'a pas été utilisé au cours des quatre mois précédents
En ce qui concerne les événements liés au poliovirus qui ne répondent pas aux critères de notification de l'article 6 ou de l'article 7, d'autres exigences de déclaration et de partage de l'information à l'OMS et à d'autres points focaux nationaux RSI peuvent toujours s'appliquer en vertu du Règlement pour soutenir la transparence et la réponse de la santé publique.
Remarque : La notification à l'OPS/OMS peut mener à la publication d'un Bulletin d'information sur les flambées épidémiques ou d'une alerte épidémiologique sur les sites Web publics de l'OPS/OMS, selon le cas, en fonction du type de virus, de l'évaluation des risques et de l'état de l'éclosion, ainsi que sur le site d'information sur les événements de l'OMS, qui n'est accessible qu'aux points focaux nationaux RSI. De plus, selon les exigences en matière de partage des données de l'IMEP et du Réseau mondial de laboratoires pour la poliomyélite, le Canada a la responsabilité de partager la géolocalisation d'un échantillon de poliovirus ou d'un cas de poliovirus positif. Les données de localisation seront publiées sur un site sécurisé à la disposition des points focaux nationaux RSI et aux membres de l'IMEP.
Si une éclosion est déclarée, consultez les recommandations temporaires émises par le directeur général de l'OMS sur l'avis du comité d'urgence du RSI concernant la propagation internationale du poliovirus. Visitez le site Web de l'Organisation mondiale de la Santé pour consulter les déclarations antérieures du RSI.
L'annexe A contient des chiffres qui illustrent les étapes initiales clés et les exigences de notification pour la détection de la poliomyélite.
8. Enquête
8.1 Enquête sur un cas
8.1.1 Indice de soupçon de poliomyélite en attente de confirmation en laboratoire
Si un cas de PFA est en attente de confirmation de laboratoire et qu'il a un lien épidémiologique avec un cas confirmé de poliomyélite en laboratoire, passez à la section 8.1.2 : Caractéristiques épidémiologiques du poliovirus pertinentes pour l'enquête et la gestion des cas et des contacts, car cela correspond à la classification de cas pour la poliomyélite paralytique confirmée.
Pour les autres cas en attente des résultats de laboratoire des cas présentant une PFA, voici les facteurs de risque élevés qui soulèvent l'indice de soupçon concernant le poliovirus et justifieraient de gérer le cas de PFA comme un cas de poliomyélite :
- Si la personne atteinte de PFA a reçu le VPO au cours des 35 jours précédents
- Si la personne atteinte de PFA a été exposée à une personne qui a reçu un VPO au cours des six semaines précédant l'exposition
- Si la personne atteinte de PFA était un contact d'une personne faisant l'objet d'une enquête pour paralysie ou poliomyélite
La gestion de ces cas à risque élevé en attente de confirmation en laboratoire comprend ce qui suit :
- Isoler et gérer le cas, conformément aux considérations du tableau 3
- Envisager d'entreprendre l'identification et la gestion des contacts, conformément aux considérations des tableaux 2, 4 et 5
D'autres facteurs peuvent également accroître les soupçons qu'une personne atteinte de poliomyélite peut justifier une gestion précoce de la santé publique :
- Voyage récent dans une région où sévit le poliovirus
- Contact avec un voyageur récent en provenance d'une région où sévit le poliovirus
- Provient d'une communauté comptant une importante population non immunisée ou a visité une communauté où le poliovirus circulait
- Non vaccinés ou sous-vaccinés contre le poliovirus
La gestion de ces cas en attente de confirmation en laboratoire pourrait inclure les considérations relatives à la gestion des cas et des contacts dans les tableaux 2 à 5.
Si la présence de poliovirus est confirmée, des lignes directrices sur la gestion sont fournies à la Section 8.1.3 : Enquête sur une infection par le poliovirus (avec ou sans paralysie).
8.1.2 Caractéristiques épidémiologiques du poliovirus pertinentes pour l'enquête et la gestion des cas et des contacts
Période de contagiosité
Le poliovirus peut être identifié à partir des sécrétions de la gorge dès 36 heures après l'exposition et à partir des selles dès 72 heures après l'exposition. Le virus persiste dans la gorge pendant environ une semaine et dans les selles pendant trois à six semaines. Les cas sont les plus infectieux dans les jours précédant et suivant l'apparition des premiers symptômes (qui peuvent être des symptômes non spécifiques).
Période d'incubation
La période d'incubation est de 3 à 6 jours pour l'apparition de symptômes non spécifiques. Chez les patients qui deviennent paralysés, cela se produit dans les 7 à 21 jours suivant l'exposition (peut varier jusqu'à 35 jours).
Postulats pour ce document
La transmissibilité commence très rapidement après l'acquisition du poliovirus, de sorte que dans certaines circonstances pour ce document, la transmissibilité sera considérée comme commençant au moment de l'acquisition du virus. Par conséquent, pour les personnes atteintes de poliomyélite paralytique, 35 jours (5 semaines) avant l'apparition de la paralysie est la limite extérieure du temps d'acquisition et approximativement le début de la période de transmissibilité. Pour les personnes atteintes du poliovirus non paralytique et dont le poliovirus a été détecté dans leurs selles, six semaines avant le moment de la détection dans les selles est la limite extérieure du temps d'acquisition et approximativement le début de la période de transmissibilité. Par souci de simplicité, six semaines seront utilisées dans certaines circonstances comme maximum pour la période d'incubation et le début de la période de transmissibilité pour les personnes ayant une infection confirmée du poliovirus (avec ou sans paralysie) à certains endroits dans le présent document. Les circonstances d'un cas ou d'un contact particulier pourraient limiter davantage ces périodes, telle que la date précise du retour du voyage.
Veuillez noter que, dans certains cas, la période d'incubation ou la période de transmissibilité peuvent être plus longues. À titre d'exemple, les personnes atteintes d'une immunodéficience primaire peuvent excréter le poliovirus pendant des périodes prolongées, ce qui prolonge la période de transmissibilité et signifie que la période d'acquisition peut être considérablement plus tôt que 6 semaines.
Dans les sections du présent document qui suivent, le terme « détection » désigne soit la date d'apparition de la paralysie, soit la date du prélèvement de l'échantillon de selles qui a été positif pour le poliovirus (pour les personnes atteintes d'une infection par le poliovirus non paralytique).
8.1.3 Enquête sur une infection par le poliovirus (avec ou sans paralysie)
Si le poliovirus est détecté, les autorités de la santé publique devraient entreprendre une enquête dans les 24 heures suivant la détection par la PT ou le LNM (n'attendez pas le séquençage ou la classification finale du virus par le LNM). Les renseignements recueillis dans le cadre des enquêtes seront importants pour éclairer les évaluations des risques et les obligations internationales en matière de notification à l'OMS. Les PTs et les responsables locaux/régionaux collaboreront pour mener des enquêtes, avec l'aide de l'ASPC, le cas échéant.
En l'absence d'un formulaire d'enquête de cas dans l'administration correspondante, l'ASPC recommande d'utiliser le formulaire d'enquête sur le cas de poliomyélite de l'OPS (toutes les sections sauf la section VII) comme guide pour éclairer les enquêtes de santé publique. Les exigences minimales de données suivantes devraient être recueillies et incluses dans l'enquête pour chaque cas :
- Date de naissance et sexe
- Statut vaccinal contre la poliomyélite, y compris le nombre total de doses de VPO ou de VPI reçues, ainsi que la ou les dates d'administration
- Exposition à une personne qui a reçu le VPO, où l'exposition a eu lieu pendant la période transmissible (jusqu'à six semaines après la réception du VPO)
- Antécédents de voyage à destination, de voyage en provenance, ou de résidence d'un autre pays portant un risque d'exposition au poliovirus ou au VPO dans les six semaines précédant le début de la paralysie ou le prélèvement d'un échantillon positif de selles (pour ceux pas atteints de poliomyélite paralytique); détails des antécédents de voyage, y compris les dates et les lieux de voyage
- Exposition à une personne ayant des antécédents de voyage ou étant résidant dans un autre pays portant un risque d'exposition au poliovirus ou au VPO, où l'exposition a eu lieu pendant la période potentiellement transmissible (jusqu'à six semaines après le retour du voyageur) et que le début de la paralysie ou le prélèvement d'un échantillon positif de selles (pour les personnes qui n'ont pas de poliomyélite paralytique) a eu lieu dans les six semaines qui ont suivi; les détails des antécédents de voyage, y compris les dates et les lieux des voyages
- Résumé de la présentation clinique, évolution de la maladie et diagnostic final (s'il est connu)
- Résultats des tests sur les selles (s'ils ne sont pas disponibles pour les tests, ils devraient également être indiqués dans le rapport)
- Les résultats d'autres tests ou examens appropriés (y compris les écouvillons oropharyngé ou nasopharyngé, le liquide céphalorachidien, les études de conduction nerveuse ou EMG, IRM ou TDM), s'ils sont disponibles (indiquer également si les tests n'ont pas été effectués)
- Antécédents médicaux pertinents, y compris l'état immunodéprimé ou les antécédents neurologiques anormaux
- Si c'est un membre d'un groupe ou d'une communauté connue pour être sous ou non vacciné.
- Résultat final obtenu 60 jours après l'apparition de la maladie
Les éléments de données suivants doivent être recueillis pour éclairer la gestion des cas et des contacts :
- Renseignements sur la façon de joindre le cas (téléphone, courriel, message texte, adresse)
- Profession, ou fréquentation d'une école ou d'une garderie
- Liste et renseignements sur la façon de joindre les membres du ménage et les contacts étroits, y compris si le cas vit dans un logement de groupe (tels que les dortoirs, des refuges, des centres de détention, des foyers de groupe, des foyers pour immigrants/réfugiés) et d'autres contacts décrits au tableau 2, selon le cas
- Préparation des repas pour les autres pendant la période de transmissibilité, avec noms, dates et renseignements sur la façon de les joindre
- Sources possibles d'exposition pendant la période d'incubation, si la source d'acquisition n'est pas claire (comme les magasins d'alimentation, les aliments importés consommés, les restaurants, les repas préparés par d'autres, les salles de bains utilisées)
8.1.4 Suivi des contacts
Le suivi des contacts étroits est important pour identifier une source potentielle d'infection si elle n'est pas immédiatement apparente (source d'acquisition) et aussi pour déterminer les personnes qui pourraient avoir été infectées par le cas (risque de transmission) afin de prévenir une propagation ultérieure. Certains contacts peuvent nécessiter des exclusions (voir la section 9.2 : Gestion des contacts) et doivent donc être identifiés sans délai. Le suivi des contacts pour l'acquisition n'est requis que si la source n'est pas évidente et que les sources possibles d'acquisition sont toujours à l'étude (ceci ne serait pas nécessaire si le cas avait une source évidente d'acquisition, tel qu'un voyage récent dans un pays où la transmission du poliovirus se produit ou une exposition liée à l'établissement). Les contacts potentiels sont décrits dans le tableau 2.
Tableau 2 : Contacts potentiels d'un cas infecté par le poliovirus et risque possible d'acquisition ou de transmission.
Les contacts à risque élevé comprennent les contacts du ménage et ceux qui ont passé la nuit dans le même ménage que le cas; les contacts sexuels; les contacts dans les milieux de vie de groupe qui ont partagé une salle de bain avec le cas ou qui ont eu des interactions étroites avec le cas (par exemple, dortoirs, refuges, centres de détention, foyers de groupe, foyers pour immigrants/réfugiés); les enfants et le personnel de garderie qui ont fréquenté la garderie avec le cas; et ceux qui ont été en contact avec les matières fécales du cas (à l'exclusion des fournisseurs de soins de santé qui ont utilisé des pratiques appropriées de prévention et de contrôle des infections). Les autres contacts sont généralement considérés comme à faible risque. Le risque de transmission d'un contact dépend du moment et de la nature de l'exposition au cas et n'est pas influencé par le statut vaccinal du contact, puisque les personnes vaccinées contre le VPI peuvent risquent toujours d'être infectées et de transmettre l'infection.
| Contact potentiel ou source d'exposition (généralement indiqué du risque de transmission le plus élevé au plus faible) | Déterminer la source d'acquisition (uniquement si une source d'acquisition n'est pas apparente) | Déterminer le risque de transmission | Niveau de risque de transmission |
|---|---|---|---|
| Ménage et autres contacts étroits, y compris ceux qui ont passé la nuit dans le même ménage que le cas, les contacts sexuels et les contacts dans des milieux de vie de groupe qui partageaient une salle de bain avec le cas ou qui ont eu des interactions étroites avec le cas (comme les dortoirs, les refuges, les centres de détention, les foyers de groupe, les foyers pour immigrants/réfugiés), s'il y a lieu | Si l'exposition a eu lieu pendant la période d'incubation du cas (peut comprendre jusqu'à 6 semaines avant la détection) | Si l'exposition a eu lieu pendant que le cas était transmissible (peut comprendre jusqu'à six semaines avant la détection jusqu'à ce que le cas soit reconnu et que des mesures de prévention et de contrôle des infections appropriées aient été prises) | Contact à risque élevé – Voir le tableau 4 pour les considérations de gestion |
| Contacts avec la garderie : y compris le personnel et les enfants du groupe ou de la classe et les groupes ou les classes qui ont eu des interactions régulières avec le cas ou qui ont partagé régulièrement une salle de bain avec le groupe ou la classe du cas à la garderie | Si l'exposition a eu lieu pendant la période d'incubation du cas (peut comprendre jusqu'à 6 semaines avant la détection) | Si l'exposition a eu lieu pendant que le cas était transmissible (peut comprendre jusqu'à six semaines avant la détection jusqu'à ce que le cas soit reconnu et exclu de la garderie) | Contact à risque élevé – Voir le tableau 4 pour les considérations de gestion |
| Contact connu avec des matières fécales (y compris le changement de couches et l'aide à la toilette) Consultez la dernière ligne pour les travailleurs de la santé et de laboratoire qui manipulent des échantillons du cas | Si l'exposition a eu lieu pendant la période d'incubation du cas (peut comprendre jusqu'à 6 semaines avant la détection) | Si l'exposition a eu lieu pendant que le cas était transmissible (peut comprendre jusqu'à six semaines avant la détection jusqu'à ce que le cas soit reconnu et que des mesures de prévention et de contrôle des infections appropriées aient été prises) | Contact à risque élevé – Voir le tableau 4 pour les considérations de gestion |
| Exposition aux toilettes (tel que l'utilisation d'une salle de bain commune dans un lieu de travail) | Si l'exposition a eu lieu pendant la période d'incubation du cas (peut comprendre jusqu'à 6 semaines avant la détection) | Ceux qui partageaient fréquemment des toilettes avec le cas si l'exposition s'est produit pendant que le cas était transmissible (cela pourrait inclure jusqu'à six semaines avant la détection jusqu'à ce que la toilette soit adéquatement nettoyée, désinfectée et ne soit pas réutilisée par le cas) | Contact à risque généralement moins élevé – Voir le tableau 5 pour les considérations de gestion |
| Exposition à ou manipulation des aliments | Magasins d'alimentation, aliments importés consommés, restaurants, repas préparés par d'autres pendant la période d'incubation du cas (peut comprendre jusqu'à six semaines avant la détection) | Si le cas a préparé de la nourriture pour d'autres personnes pendant qu'il était contagieux (peut inclure jusqu'à six semaines avant la détection jusqu'à ce que les mesures appropriées de prévention et de contrôle de l'infection soient mis en place, particulièrement si l'aliment n'a pas été cuit après avoir été manipulé par le cas) |
Contact à risque généralement moins élevé – Voir le tableau 5 pour les considérations de gestion |
| Les travailleurs de la santé qui ont soigné le cas et les travailleurs de laboratoire qui ont manipulé les échantillons du cas | S. O. | Si l'exposition a eu lieu alors que le cas était contagieux (peut inclure jusqu'à 6 semaines avant la détection) | Contact à risque généralement moins élevé – Voir le tableau 5 pour les considérations de gestion. S'il est déterminé que le travailleur de la santé n'a pas utilisé d'équipement de protection individuelleNote de bas de page * adéquat ou de pratiques de prévention et de contrôle des infections en plus d'avoir un contact étroit avec le cas ou un contact avec les matières fécales du cas, il pourrait être considéré comme présentant un risque plus élevé – Voir le tableau 4 pour les considérations de gestion Si l'on détermine que le travailleur de la santé ou de laboratoire a utilisé de l'équipement de protection individuelleNote de bas de page * adéquat et des pratiques de prévention et de contrôle des infections, on pourrait considérer qu'il ne s'agit pas d'un contact. |
|
|||
Les données minimales suivantes doivent être recueillies auprès des membres du ménage ou d'autres contacts à risque élevé. La collecte d'une partie ou de la totalité de ces renseignements sur les contacts à faible risque peut également être pertinente selon les circonstances :
- Renseignements sur la façon de joindre le contact (téléphone, courriel, message texte, adresse)
- Date de naissance et sexe
- Statut vaccinal contre la poliomyélite, y compris le nombre total de doses de VPO ou de VPI reçues, ainsi que la ou les dates d'administration
- Antécédents de voyage dans les 12 semaines précédant l'apparition de la maladie chez le cas et les détails des antécédents, y compris les dates et les emplacements si les sources d'acquisition ne sont pas claires et que le contact pourrait être une source d'acquisition possible
- Si le contact présente des symptômes, y compris des détails sur les symptômes et leur apparition
- Si le contact est membre d'un groupe ou d'une communauté connue pour être sous ou non vacciné.
- Antécédents médicaux pertinents, y compris l'état immunodéprimé ou les antécédents neurologiques anormaux
- Profession, ou fréquentation d'une école ou d'une garderie
- Milieux de vie de groupe (par exemple, dortoirs, refuges, centres de détention, foyers de groupe, foyers pour immigrants/réfugiés)
- S'il ne s'agit pas d'un contact avec le ménage, déterminez les dates, les heures et les lieux d'exposition au cas dans les six semaines précédant la détection du cas et jusqu'à ce que les mesures de prévention et de contrôle des infections appropriées aient été utilisées. Indiquez si et quand le contact a préparé de la nourriture pour le cas (si la source d'acquisition du cas n'est pas évidente) ou si et quand le cas a préparé de la nourriture pour le contact
- Pour les travailleurs de la santé qui ont fourni des soins au cas et les travailleurs de laboratoire qui ont manipulé des échantillons du cas pendant que le cas était contagieux, déterminez les dates et les types d'exposition et, le cas échéant, l'équipement de protection individuelle (voir * la remarque ci-dessus dans le tableau 2 pour de plus amples renseignements), et les pratiques de prévention et de contrôle des infections qui ont été utilisées
En plus de l'enquête sur les cas et les contacts, la collecte de renseignements sur la population locale, comme la couverture vaccinale et les caractéristiques sociodémographiques des personnes non vaccinées et sous-vaccinées dans la région, peut être justifiée pour éclairer les évaluations des risques afin d'évaluer le potentiel de transmission.
8.2 Enquête sur la détection à partir de l'échantillonnage des eaux usées environnementales
Si un poliovirus préoccupant (PVS, PVDV ou Sabin ou de type Sabin 2) est confirmé dans un échantillon d'eaux usées environnementales par le LNM, les autorités sanitaires locales et régionaux devraient entreprendre une enquête dans les 24 heures suivant la confirmation. Les meilleurs efforts doivent être faits pour recueillir les renseignements suivants propres à la zone de collecte du site d'échantillonnage et aux sites avoisinants :
- Caractéristiques de la population (par exemple, taille de la population incluse dans la zone de collecte, démographie de la population touchée, couverture vaccinale contre la poliomyélite, présence de groupes non vaccinés et sous-vaccinés, acceptation du vaccin)
- Mouvement de la population (par exemple, migration et habitudes de voyage, liens culturels ou de voyage avec d'autres zones touchées)
- Description de la zone de collecte (par exemple, emplacement, liens avec d'autres sites, réseau d'égout fermé ou convergent, densité des logements)
- Institutions pertinentes (par exemple, établissements de santé, écoles, installation essentielles à la lutte contre la polio tel qu'un fabricant ou un laboratoire de vaccin contre le poliovirus, centres de transport comme les aéroports, foyers pour les nouveaux arrivants)
- Calendrier de collecte, nombre et fréquence des échantillons prélevés, opportunité et exhaustivité de la collecte
D'autres éléments de données à prendre en considération sont décrits dans lesPON de l'IMEP : Riposte à un Évènement Ou à une Flambée de Poliomyélite (version 4, mars 2022) – chapitre 3
8.3 Enquête sur un événement lié à une installation impliquant le poliovirus
L'installation essentielle à la lutte contre la polio effectue des enquêtes sur les événements liés à une installation contenant le poliovirus, et l'ANC fournirait des lignes directrices sur le confinement et superviserait l'enquête sur les causes fondamentales menant à un événement. Les recommandations relatives au suivi des contacts qui figurent à la Section 8.1.4 : Suivi des contacts et les autres mesures de suivi en santé publique, peuvent tout de même être nécessaires et, par conséquent, les autorités sanitaires locales, régionales et provinciales et territoriales doivent être avisées conformément à la Section 7.1 :Déclarations dans une province ou un territoire.
9. Gestion des cas et des contacts
La détection d'un cas de poliomyélite ou d'une infection par le poliovirus non paralytique au Canada est probablement très rare. Toutefois, en cas de détection d'un cas, des précautions immédiates en matière de santé publique devraient être prises pour prévenir la transmission. La transmission du poliovirus peut mettre en danger les personnes non vaccinées ou sous-vaccinées au Canada et pourrait mettre en danger le statut du Canada en tant que pays exempt de poliomyélite. Par conséquent, les recommandations ci-dessous concernant la gestion des cas et des contacts sont de nature restrictive afin de réduire au minimum le risque de transmission. Les recommandations de gestion visent à appuyer la prise de décisions par les PTs et ne visent pas à remplacer les lignes directrices ou les protocoles existants dans une administration.
9.1 Gestion des cas
Recommandations générales :
- Avisez l'autorité de santé publique locale de tous les cas soupçonnés de poliomyélite, comme il est indiqué à la section 8.1.1 : Indice de soupçon de poliomyélite en attente de confirmation en laboratoire.
- Enquêtez sur tous les cas afin de maintenir le statut du Canada en tant que pays exempt de la poliomyélite, de déterminer la source de l'infection et de prévenir d'autres cas. Les renseignements qui devraient être collecté sur le cas sont décrits ci-dessus à la section 8.1.3 : Enquête sur une infection par le poliovirus (avec ou sans paralysie).
- Suivez toutes les mesures appropriées de prévention et de contrôle des infections. L'hospitalisation est recommandée dans les cas où cela est indiqué sur le plan clinique. Dans le cas des patients hospitalisés, il faut les admettre dans une chambre individuelle avec des pratiques de routine et des précautions de contact. Les cas qui ne nécessitent pas d'hospitalisation peuvent être isolés à domicile au moyen de mesures appropriées de prévention et de contrôle des infections. Un aperçu des recommandations et des considérations possibles en matière de gestion de cas est présenté au tableau 3.
- Manipulez les sécrétions, les matières fécales et les articles contaminés en suivant les pratiques habituelles et en prenant des précautions de contact. Dans les régions où il existe un système moderne d'évacuation des eaux usées, les matières fécales et l'urine peuvent être rejetées directement dans les égouts. Recueillez et incinérez les déchets si les égouts sanitaires ne sont pas reliés à un système municipal de gestion des eaux usées.
- Signalez les cas compatibles avec la définition de cas de PFA au Programme canadien de surveillance pédiatrique (PCSP) à l'aide du questionnaire sur les cas du PCSP, en plus de la l'autorité de santé publique locale si la législation l'exige dans l'administration.
- Pour les cas qui répondent à la définition de cas de PFA, effectuez une évaluation de suivi du résultat de la paralysie 60 jours après le début de la paralysie. Un rapport de suivi doit être présenté lorsque l'information est disponible.
- Remarque : Le rapport initial ne devrait pas être retardé en raison de renseignements incomplets; toutefois, tous les renseignements pertinents sur le cas devraient être envoyés dans un rapport de suivi dès qu'ils sont disponibles.
Tableau 3 : Aperçu des recommandations et des considérations relatives à la gestion de cas de poliomyélite possible (avec ou sans paralysie).
Remarques :
Ce qui suit s'applique aux cas confirmés. Certains aspects peuvent également s'appliquer aux cas suspects en attente des résultats de laboratoire, selon le niveau de soupçon que le cas est atteint de poliomyélite (p. ex. si le cas a une paralysie et a reçu un VPO au cours des 35 jours précédents ou s'il est membre d'une communauté où éclosion de poliovirus est en cours).
Certaines des recommandations ou considérations possibles suivantes sont pertinentes jusqu'à ce que le cas ne soit plus jugé infectieux (marqué d'un *). Un cas peut être considéré comme n'étant plus infectieux sur la base de trois échantillons de selles négatifs consécutifs prélevés à des intervalles d'au moins 24 heures. Tous les tests d'échantillons de selles doivent être analysés par le LNM. Le délai pour l'isolement du poliovirus en culture cellulaire au LNM est de 14 jours (voir l'annexe C pour plus de détails).
Le poliovirus présent dans les selles disparaît généralement en 3 à 6 semaines chez une personne immunocompétente. Pour les cas où l'infection n'est pas éliminée au cours de cette période, comme les personnes atteintes d'un trouble immunodéficitaire primaire, la gestion de la santé publique et le dépistage des selles seront déterminés au cas par cas en consultation avec des spécialistes de la santé publique et des maladies infectieuses. D'autres recommandations se trouvent dans les Lignes directrices sur la mise en œuvre de la surveillance du poliovirus chez les patients atteints de déficit immunitaire primaire (DIP) de l'IMEP. Les recommandations et les considérations ci-dessous reflètent également qu'il peut y avoir des cas non reconnus dans le ménage, car les enquêtes sur les contacts peuvent encore être en cours.
| Facteur | Recommandations et considérations |
|---|---|
| Isolement et prévention et contrôle des infections dans les établissements de soins de santéNote de bas de page * |
|
| Isolement et prévention et contrôle des infections à domicileNote de bas de page * |
|
| Tests de sellesNote de bas de page * |
|
| Préparation des alimentsNote de bas de page * |
|
| ExclusionsNote de bas de page * |
|
| VisiteursNote de bas de page * |
|
| Gestion clinique |
|
| Suivi |
|
| Vaccination |
|
|
|
9.2 Gestion des contacts
Recommandations générales :
- Un guide sur l'identification des contacts se trouve au tableau 2 et les renseignements à obtenir auprès des contacts sont décrits ci-dessus à la section 8.1.4 : Recherche des contacts.
- Un résumé des recommandations et des considérations relatives à la gestion des contacts est présenté au tableau 4 pour les contacts du ménage, et les autres contacts étroits et à risque élevé et au tableau 5 pour les contacts à faible risque.
Tableau 4 : Recommandations et considérations relatives à la gestion des contacts à risque élevé pour le poliovirus
S'appliquent aux personnes suivantes : Le ménage et les autres contacts étroits ou à risque élevé, y compris ceux qui ont passé la nuit dans le même ménage que le cas; les contacts sexuels; les contacts dans les milieux de vie de groupe qui ont partagé une salle de bain avec le cas ou qui ont eu des interactions étroites avec le cas (par exemple, dortoirs, refuges, centres de détention, foyers de groupe, foyers pour immigrants/réfugiés); les enfants qui ont fréquenté la garderie avec le cas et les travailleurs de la garderie; et ceux qui ont été en contact avec les matières fécales du cas (à l'exclusion des fournisseurs de soins de santé qui ont utilisé des pratiques appropriées de prévention et de contrôle des infections).
Remarques :
Certaines des recommandations ou considérations suivantes sont pertinentes jusqu'à ce qu'il soit déterminé que le contact n'est pas infecté (marqué d'un *), en fonction de deux échantillons de selles négatifs consécutifs prélevés à un intervalle d'au moins 48 heures, la première au moins quatre jours après la dernière exposition du contact au cas avant que les mesures de prévention et de contrôle des infections ne soient mises en œuvre. Il convient de noter qu'il s'agit d'une procédure différente pour l'analyse des échantillons de selles par rapport au processus décrit dans le tableau 3 pour un cas de poliomyélite. Tous les tests d'échantillons de selles doivent être analysés par le LNM. Le délai pour l'isolement du poliovirus en culture cellulaire au LNM est de 14 jours (voir l'annexe C pour plus de détails).
| Facteur | Recommandations/considérations |
| Prévention des infections à domicileNote de bas de page * |
|
| Tests de sellesNote de bas de page * |
|
| Préparation des alimentsNote de bas de page * |
|
| ExclusionsNote de bas de page * |
|
| VisiteursNote de bas de page * |
|
| Suivi |
|
| Vaccination |
Remarque : La vaccination est recommandée pour protéger une personne contre une exposition continue et non comme immunoprophylaxie post-exposition pour les contacts. |
|
|
Tableau 5 : Recommandations et considérations relatives à la gestion des contacts à faible risque pour le poliovirus
S'appliquent aux personnes suivantes : Ceux qui ont partagé des toilettes avec le cas; ceux qui ont mangé de la nourriture préparée par le cas; les travailleurs de la santé qui se sont occupés du cas ou les travailleurs de laboratoire qui ont manipulé les échantillons du cas (à moins qu'ils ne soient classés comme présentant un risque plus élevé ou aucun risque, voir le tableau 2).
Remarques :
Si les contacts ont partagé des toilettes avec le cas, ont mangé de la nourriture préparée par le cas, ou si les travailleurs de la santé qui se sont occupés du cas ou les travailleurs de laboratoire qui manipulent des échantillons provenant du cas sont considérés, sur la base d'une évaluation des risques, comme présentant un risque plus élevé de contracter le poliovirus du fait de leur exposition au cas, ils doivent suivre les recommandations du tableau 4, sinon ils doivent suivre les recommandations du tableau 5. Les travailleurs de la santé ou de laboratoire qui ont utilisé un équipement de protection individuelle adéquat et des pratiques de prévention et de contrôle des infections pourraient ne pas être considérés comme des contacts.
Pour obtenir des renseignements sur l'équipement de protection individuelle adéquat pour le poliovirus, veuillez consulter les Pratiques de base et précautions additionnelles visant à prévenir la transmission des infections dans les milieux de soins (2016) – page 95 de l'ASPC.
| Facteur | Recommandations/considérations |
|---|---|
| Prévention et contrôle des infections |
|
| Analyses des selles |
|
| Suivi |
|
| Vaccination |
|
D'autres mesures de contrôle possibles pour la gestion d'une personne exposée au poliovirus à la suite d'un événement lié à l'installation sont présentées à l'annexe B.
10. Évaluation des risques
Évaluation initiale des risques de l'IMEP : Envisagez d'utiliser l'outil d'évaluation des risques de l'IMEP (annexe E du présent document et annexe 1 des PON de l'IMEP) aux premières étapes de l'enquête sur les détections du PVS, du PVDV et de Sabin ou de type Sabin 2. L'évaluation initiale des risques peut servir de guide pour déterminer le type et le niveau de l'intervention, y compris un examen des risques virologiques et des caractéristiques épidémiologiques, et pour déterminer le risque de transmission supplémentaire dans la zone de l'événement ou de l'éclosion et à l'échelle internationale. L'évaluation peut être effectuée par des experts en la matière à l'ASPC et les PTs touchés.
Un aperçu de l'instrument de risque de l'IMEP est présenté dans les PON de l'IMEP : Riposte à un Évènement Ou à une Flambée de Poliomyélite (version 4, mars 2022) – chapitre 4
Évaluation rapide des risques : Une évaluation rapide des risques exhaustive est un outil important pour décrire le risque pour les Canadiens et évaluer les lacunes dans les connaissances à l'aide d'un cadre et d'une méthode normalisés. S'il y a lieu, en fonction des renseignements établis, l'évaluation rapide des risques serait menée par l'ASPC, avec la contribution de la PT chargé(e) de l'enquête. Ce processus est conforme à la phase d'évaluation initiale (3,2) du Plan d'intervention fédéral-provincial-territorial en matière de santé publique dans les cas d'incidents biologiques.
11. Intervention de la santé publique en cas d'événement ou d'éclosion de poliovirus au Canada
Les autorités de la santé publique au Canada gèrent les interventions en cas d'événements de santé publique de diverses façons, comme les activités de surveillance et de suivi, les mesures de santé publique et l'exploitation des réseaux de laboratoires. Les autorités de gestion des urgences facilitent et appuient la coordination des interventions en cas d'événements de santé publique, par exemple en fournissant des conseils et un soutien logistique, et en utilisant des plateformes et des outils comme les centres des opérations d'urgence pour la planification et la coordination des activités d'intervention intégrées. Le Plan d'intervention fédéral-provincial-territorial en matière de santé publique dans les cas d'incidents biologiques décrit la façon dont les deux programmes fonctionneront ensemble en utilisant la structure de gouvernance et le concept des opérations du plan, et que les activités d'intervention et la coordination requise varieront selon les objectifs d'intervention de l'événement.
Les activités suivantes doivent être envisagées en réponse à un événement ou à une éclosion de poliovirus.
11.1 Surveillance accrue des cas
L'objectif des activités de surveillance accrue des cas est d'accroître la probabilité de détecter les cas et d'améliorer la qualité des rapports. En cas de détection d'un cas de PVS ou de PVDV, ou d'une détection environnementale au Canada, des améliorations aux réseaux de surveillance actifs existants sont justifiées pour assurer la sensibilité.
Voici d'autres considérations :
- Communications accrues aux professionnels de la santé à tous les niveaux au sujet de la situation actuelle et de l'importance de :
- Détecter les cas présentant des symptômes compatibles avec la PFA (à tous les âges)
- Surveiller les symptômes non spécifiques chez les personnes exposées au poliovirus
- Prélever des échantillons de selles dans les 14 jours suivant l'apparition des symptômes et envoyer au laboratoire pour tous les cas de PFA, ainsi que lorsqu'il y a suspicion de poliovirus
- Signaler à la santé publique locale des cas soupçonnés de poliovirus et des cas confirmés de PFA
- Élargissement de la surveillance de la PFA pour qu'elle soit déclarée obligatoirement par les PTs dans toutes les administrations
- Inclusion des adolescents et des adultes dans les signalements de la PFA (la zone géographique sera éclairée par l'enquête initiale)
11.2 Élargissement de l'échantillonnage des eaux usées environnementales
Dans le cas d'une détection d'un cas de PVS/PVDV ou environnementale au Canada ou de détections internationales présentant un risque d'importation au Canada, l'élargissement de l'échantillonnage stratégique des eaux usées de l'environnement (comme l'augmentation du nombre de sites échantillonnés ou l'augmentation de la fréquence de l'échantillonnage) peut être justifié pour compléter la surveillance de la PFA. Il est important de noter que les analyses des eaux usées pour le poliovirus sont différentes de celles pour d'autres agents pathogènes comme la COVID-19. Les analyses des eaux usées pour le poliovirus ne sont pas couramment ou largement recommandées, et il existe des exigences strictes en matière de sécurité en laboratoire. Pour s'assurer que des plans de santé publique sont en place pour confirmer, interpréter et assurer le suivi des détections environnementales, les décisions de mettre en œuvre ou d'élargir l'échantillonnage des eaux usées environnementales dans une région sont la responsabilité conjointe des intervenants locaux, provinciaux et territoriaux et fédéraux. Si l'on s'entend sur l'échantillonnage des eaux usées dans une région, tous les échantillons doivent être envoyés au LNM pour analyse.
Si un cas est identifié, la zone de résidence du cas et d'autres zones de captage (selon les liens épidémiologiques identifiés) pourraient être prises en compte pour l'échantillonnage environnemental afin d'évaluer la portée géographique des détections, la transmission communautaire et la durée de la circulation du poliovirus. La détermination des zones à risque les plus élevées devrait être fondée sur l'emplacement des populations considérées comme à risque et sur les caractéristiques comportementales qui représentent un risque potentiel de transmission, notamment :
- Lacunes connues ou présumées de l'immunité de la population, comme des cohortes d'âge précises qui n'ont pas été vaccinées et des groupes qui ne sont pas vaccinés ou qui sont sous-vaccinés pour des motifs religieux, philosophiques ou autres
- Liens connus ou soupçonnés avec des zones où circulent des poliovirus
- Régions comptant une importante population mobile (par exemple, déplacement quotidien de la population pour le travail, migrants, nomades, réfugiés, établissements informels, travailleurs invités sans-papiers)
- Faible couverture de la vaccination systématique contre le poliovirus (< 90 %)
La fréquence d'échantillonnage recommandée est toutes les deux semaines, mais la fréquence minimale est mensuelle. L'échantillonnage prendra fin lorsqu'il n'y aura plus de PVS/PVDV isolés au cours d'une période de six mois.
Pour de plus amples renseignements sur l'amélioration de la surveillance environnementale, veuillez consulter la PON de l'IMEP pour la surveillance environnementale de la poliomyélite à la suite d'une enquête sur un événement ou une éclosion de poliovirus (version 15, décembre 2020).
11.3 Échantillonnage communautaire des selles
Dans certains cas, on peut tenir compte de l'échantillonnage communautaire des selles avec consentement lorsqu'on tente de déterminer une source possible ou l'étendue de la transmission. Cela peut être approprié dans les groupes fermés, comme les garderies, les milieux de vie collectifs ou les communautés religieuses qui ne sont pas vaccinées ou qui sont sous-vaccinées. L'échantillonnage d'échantillons de selles ou de couches prélevés régulièrement dans les bureaux de soins de santé, les établissements de soins de santé ou les garderies pourrait être envisagé, avec le consentement des parents ou des tuteurs.
11.4 Vaccination
L'évaluation de la couverture vaccinale et les campagnes de vaccination ciblées contre le VPI sont justifiées dans les populations à risque élevé, comme les communautés situées près de l'événement détecté ou celles dont on sait ou soupçonne qu'elles ne sont pas vaccinées ou qu'elles sont sous-vaccinées. Étant donné que la mise en œuvre des programmes d'immunisation relève de la responsabilité des provinces et des territoires, les activités de vaccination seront dirigées par les autorités sanitaires provinciales et territoriales respectives et appuyées par l'ASPC au besoin. Le Comité consultatif national de l'immunisation (CCNI) peut également participer à la formulation de recommandations précises en matière de vaccination, et le Comité canadien de l'immunisation (CCI) peut participer à des discussions sur les programmes et les opérations. S'il y a lieu, la mobilisation de membres de la communauté de confiance, comme des chefs religieux, peut être incluse dans les efforts de la campagne de vaccination.
L'étendue des activités de vaccination contre le VPI dépend de l'événement ou de l'éclosion et est déterminée en fonction des facteurs liés au cas ou aux contacts, de l'évaluation rapide des risques et en consultation avec la santé publique et d'autres partenaires, le cas échéant. D'autres activités de vaccination pourraient être organisées :
- Vaccins de rattrapage pour les personnes non vaccinées ou sous-vaccinées
- Vaccination avec un seul vaccin de rappel pour adultes à vie contenant un vaccin contenant le VPI pour les adultes à risque élevé s'ils n'en ont pas déjà eu un avant ou après l'âge de 18 ans (comme les contacts étroits, les travailleurs de la santé, les adultes à risque d'exposition)
- Vaccination durant les éclosions dans certains groupes (par exemple, tous les enfants de moins de 5 ans, peu importe leur statut vaccinal).
Si les PTs ont besoin de produits de vaccination supplémentaires, l'ASPC peut participer à la coordination de l'approvisionnement. Les partenaires fédéraux et provinciaux et territoriaux devront faire preuve de vigilance dans la diffusion des communications publiques pour s'assurer que les vaccins sont à jour, conformément aux Programmes de vaccination systématique et de rattrapage des provinces et des territoires au Canada. Des recommandations sur les programmes de vaccination systémique, les doses de rappel et la vaccination des voyageurs sont disponibles dans le document Vaccin contre la poliomyélite : Guide canadien d'immunisation.
11.5 Communication
Une communication uniforme, claire et coordonnée est importante à la suite d'un événement ou d'une éclosion de poliovirus afin d'appuyer les activités d'intervention, d'informer les Canadiens des risques et des mesures à prendre pour protéger leur santé, accroître la vaccination et soutenir une surveillance robuste grâce à la notification rapide de la PFA et du poliovirus.
Pendant un événement ou une éclosion, il est important d'élaborer des stratégies et des ressources de communication pour :
- Conseiller aux professionnels de la santé de considérer la poliomyélite chez les patients présentant des symptômes semblables à ceux de la poliomyélite (pour les symptômes cliniques de la poliomyélite, voir le document Vaccin contre la poliomyélite : Guide canadien d'immunisation), surtout si le patient n'est pas vacciné ou s'il est sous-vacciné ou s'il a récemment voyagé ou résidé dans un pays où la poliomyélite est toujours présente ou il a été exposé à une personne qui s'est rendue dans ces régions ou qui a été potentiellement exposée dans le cadre d'un événement local ou d'une éclosion.
- Conseiller aux professionnels de la santé de s'assurer que leurs patients sont à jour dans leur vaccination contre la polio, conformément aux recommandations du Guide canadien d'immunisation.
- Accroître la sensibilisation aux risques de la polio pour les enfants, les familles et les communautés.
- Renforcer la confiance de la communauté à l'égard de la vaccination et encourager la vaccination.
Considérations relatives à la communication :
- Coordonnez et harmonisez les approches de communication et les messages entre les autorités FPT, le cas échéant.
- Mobilisez et exploitez les intervenants pour aider à atteindre les publics cibles, le cas échéant.
- Ayez recours à des approches ciblées et à la traduction dans les communautés marginalisées et éloignées, au besoin.
- Faites preuve d'ouverture, de transparence et de rapidité avec des renseignements et des messages qui fournissent des conseils, reconnaissent les incertitudes et expliquent les prochaines étapes.
- En plus des médias traditionnels et des médias sociaux, tirez parti des plateformes de communication existantes, comme les réseaux professionnels, les alertes de santé publique du RCRSP et les cliniques sur la fièvre jaune et la santé de voyage.
11.6 Évaluation de la surveillance et évaluation à la suite d'une enquête
Suite à l'enquête initiale sur tout événement ou éclosion de poliovirus, il est essentiel d'évaluer et d'améliorer la surveillance de l'AFP et du poliovirus.
Le système canadien actuel de surveillance de la paralysie flasque aiguë devrait être évalué et amélioré, au besoin, afin d'accroître la capacité de gestion des données pour veiller à ce que toutes les bases de données et les analyses soient à jour, d'assurer l'harmonisation des données avec le laboratoire, et de collaborer avec les professionnels de la santé pour accroître la conformité des cas aux enquêtes cliniques et virologiques complètes et au suivi des cas.
Conformément aux recommandations de l'IMEP, procédez aux évaluations suivantes de la réponse aux éclosions :
- Première évaluation dans les 3 à 4 mois suivant la notification du laboratoire.
- Évaluations trimestrielles de suivi pendant la durée de l'éclosion.
- Évaluation finale après au moins 6 mois sans détection de poliovirus.
- Examens documentaires supplémentaires en cas d'éclosion prolongées, le cas échéant.
Pour de plus amples renseignements sur la surveillance à la suite d'une enquête, veuillez consulter la PON de l'IMEP : Riposte à un Évènement Ou à une Flambée de Poliomyélite (version 4, mars 2022) – chapitre 7
Remerciements
L'Agence de la santé publique du Canada tient à exprimer sa sincère gratitude à toutes les personnes et à tous les organismes qui ont contribué à l'élaboration des Lignes directrices relatives à l'intervention et à la gestion d'un événement ou d'une éclosion de poliovirus. Les efforts de collaboration des centres de l'Agence et des partenaires externes ont été inestimables pour façonner le cadre solide et complet.
Nous remercions les groupes suivants pour leurs précieuses contributions et leur expertise :
- Comité canadien d'immunisation
- Partenaires provinciaux et territoriaux
- Comité consultatif spécial / Réseau pancanadien de santé publique
- Centre de la biosécurité, Agence de la santé publique du Canada
- Centre de santé des frontières et des voyages, Agence de la santé publique du Canada
- Direction générale des communications et des affaires publiques, Santé Canada/Agence de la santé publique du Canada
- Centre de mesures et d'interventions d'urgence, Agence de la santé publique du Canada
- Centre de préparation à l'immunisation, Agence de la santé publique du Canada
- Centre de l'immunisation et des maladies respiratoires infectieuses (CIMRI), Agence de la santé publique du Canada
- Centre de surveillance de l'immunisation, Agence de la santé publique du Canada
- Laboratoire national de microbiologie, Agence de la santé publique du Canada
Ressources
Biosécurité
- Loi sur les agents pathogènes humains et les toxines du Canada
- Stratégie de l'IMEP pour le confinement mondial du poliovirus
- Assemblée mondiale de la santé. WHA 71,16 Poliomyélite ‒ confinement des poliovirus
- Système de certification du confinement de l'OMS
- Plan d'action mondial de l'OMS pour le confinement du poliovirus
- Plan d'action mondial de l'OMS pour la surveillance de la poliomyélite 2022-2024
- Directives de l'OMS visant à réduire au minimum les risques pour les installations qui recueillent, manipulent ou entreposent des matières potentiellement infectieuses pour les poliovirus (2e édition, 2021)
- Gestion en santé publique de l'exposition à des poliovirus vivants associée aux établissements de l'OMS
Définitions de cas
- Définitions de cas relatives aux 4 maladies devant être notifiées à l'OMS en toutes circonstances en vertu du RSI (2005)
- CDC Infection à poliovirus non paralytique définition de cas
- Définition de cas de PFA du PCSP
- Définition du cas de poliomyélite du gouvernement du Canada
Questionnaires sur les cas
- Questionnaire sur les cas de PFA
- Manuel de l'utilisateur sur la PFA
- Formulaire d'enquête sur les cas de polio de l'OPS
Procédures de laboratoire
- Détection et caractérisation moléculaire du LNM (pour soumettre des échantillons cliniques au laboratoire)
- Détection moléculaire du SARS-CoV-2 dans les eaux usées du LNM (procédure de soumission d'échantillons environnementaux au laboratoire)
- Requête de détection du LNM
Rapports
- Alerte du RCRSP
- Protocole de paralysie flasque aiguë du PCSP
- Bulletins d'information de l'OMS sur les flambées épidémiques
- Lignes directrices de l'OMS pour l'utilisation de l'annexe 2
- Règlement sanitaire international (2005) (RSI)
- Énoncés du Comité d'urgence du RSI sur la poliomyélite
PON et références
- PON canadienne (RMTC 1998)
- Vaccin contre la poliomyélite : Guide canadien d'immunisation
- Programmes de vaccination systématique et de rattrapage des provinces et des territoires au Canada
- Indicateurs de surveillance de la PFA de l'IMEP
- Classification et notification des poliovirus dérivés d'une souche vaccinale (PVDV) de l'IMPE
- PON de l'IMEP : Riposte à un Évènement Ou à une Flambée de Poliomyélite (version 4, mars 2022)
- PNE de l'IMEP pour la surveillance environnementale de la poliomyélite à la suite d'une enquête sur une éclosion de poliovirus
- PON de l'IMEP : Lignes directrices sur la mise en œuvre de la surveillance du poliovirus chez les patients atteints de déficit immunitaire primaire (DIP)
- Plan d'intervention fédéral-provincial-territorial en matière de santé publique dans les cas d'incidents biologiques
- Mise à jour épidémiologique de l'OPS. Détection du poliovirus circulant dérivé d'une souche vaccinale de type 2 (PVDVc2) aux États-Unis : Considérations pour la région des Amériques
- Pratiques de base et précautions additionnelles visant à prévenir la transmission des infections dans les milieux de soins
- Désinfectants pour surfaces contre les agents pathogènes viraux émergents
Annexes
Annexe A : Principales étapes initiales et exigences en matière de notification
Les principales étapes initiales et exigences de notification qui suivront sont illustrées dans le cas d'un cas de poliomyélite ou d'une infection par le poliovirus non paralytique (figure 1), d'un échantillon positif d'eaux usées de l'environnement (figure 2) ou d'un événement lié à l'installation impliquant un poliovirus (figure 3).
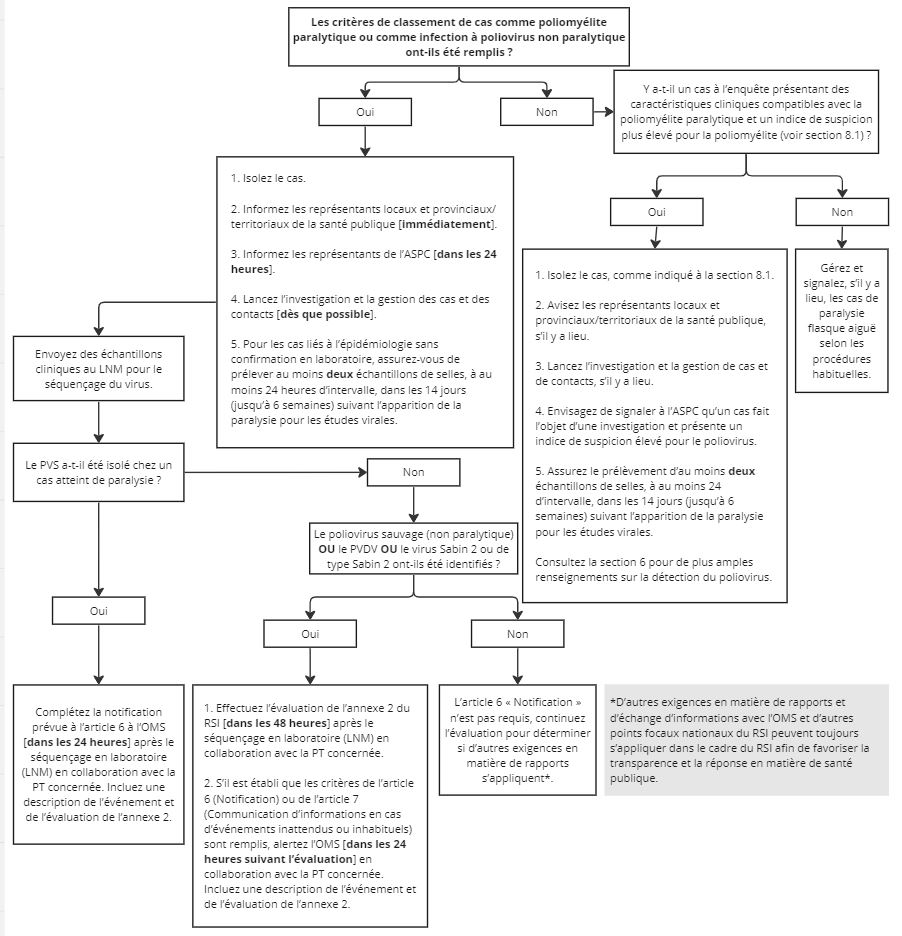
Figure 1 - Équivalent textuel
Le graphique est un organigramme illustrant les principales étapes initiales et les exigences en matière de notification de la poliomyélite paralytique ou de l'infection à poliovirus non paralytique chez une personne.
La première étape consiste à déterminer si les critères permettant de classer le cas comme poliomyélite paralytique ou comme infection à poliovirus non paralytique sont remplis.
Si la réponse est « oui », les prochaines étapes seraient les suivantes :
- Isolez le cas.
- Avisez les représentants locaux et provinciaux/territoriaux de la santé publique [immédiatement].
- Avisez les représentants de l'ASPC dans les 24 heures.
- Lancez dès que possible une investigation et une gestion de cas et de contacts.
- Pour les cas liés à l'épidémiologie sans confirmation en laboratoire, assurez-vous de prélever au moins deux échantillons de selles, à au moins 24 heures d'intervalle, dans les 14 jours (jusqu'à 6 semaines) suivant l'apparition de la paralysie pour les études virales.
- La prochaine étape consiste à envoyer des échantillons cliniques au LNM pour le séquençage du virus afin de détecter si le PVS a été isolé d'un cas avec une paralysie.
- Si oui, complétez la notification prévue à l'article 6 à l'OMS (dans les 24 heures) après le séquençage en laboratoire (LNM), en collaboration avec la PT concernée, et incluez une description de l'événement et l'évaluation de l'annexe 2.
- Si non, le PVS (non paralytique), le PVDV OU le virus Sabin 2 ou de type Sabin 2 ont-ils été identifié ?
- Si oui, effectuez l'évaluation de l'annexe 2 du RSI [dans les 48 heures] après le séquençage en laboratoire (LNM) en collaboration avec la PT concernée. Ensuite, s'il est établi que les critères de l'article 6 (Notification) ou de l'article 7 (Communication d'informations en cas d'événements inattendus ou inhabituels) sont remplis, alertez l'OMS [dans les 24 heures suivant l'évaluation] en collaboration avec la PT concernée et incluez une description de l'événement et une évaluation de l'annexe 2.
- Si ce n'est pas le cas, la notification au titre de l'article 6 n'est pas nécessaire, poursuivez l'évaluation pour déterminer si d'autres exigences en matière de rapports s'appliquent dans le cadre du RSI afin de favoriser la transparence et la réponse en matière de santé publique.
Si la réponse est « non » et que les critères pour classer le cas comme poliomyélite paralytique ou poliomyélite non paralytique n'ont pas été remplis, il faut alors déterminer s'il existe un cas à l'étude présentant des caractéristiques cliniques compatibles avec la poliomyélite paralytique et un indice de suspicion plus élevé pour la poliomyélite (plus de détails à la section 8.1).
Si la réponse est « oui », suivez les étapes ci-dessous :
- Isolez le cas comme indiqué à la section 8.1.
- Avisez les représentants locaux et provinciaux/territoriaux de la santé publique, s'il y a lieu.
- Lancez l'investigation et la gestion de cas et de contacts, s'il y a lieu.
- Envisagez de signaler à l'ASPC qu'un cas fait l'objet d'une investigation et présente un indice de suspicion élevé pour le poliovirus, et veillez à prélever au moins deux échantillons de selles, à au moins 24 heures d'intervalle, dans les 14 jours (jusqu'à 6 semaines) suivant l'apparition de la paralysie, pour des études virales.
- La section 6 contient des renseignements supplémentaires concernant la détection du poliovirus.
S'il n'y a pas de cas à l'étude avec des caractéristiques cliniques compatibles avec la poliomyélite paralytique et un indice de suspicion plus élevé pour la poliomyélite, le cas échéant, gérer et signaler les cas de paralysie flasque aiguë selon les procédures habituelles.
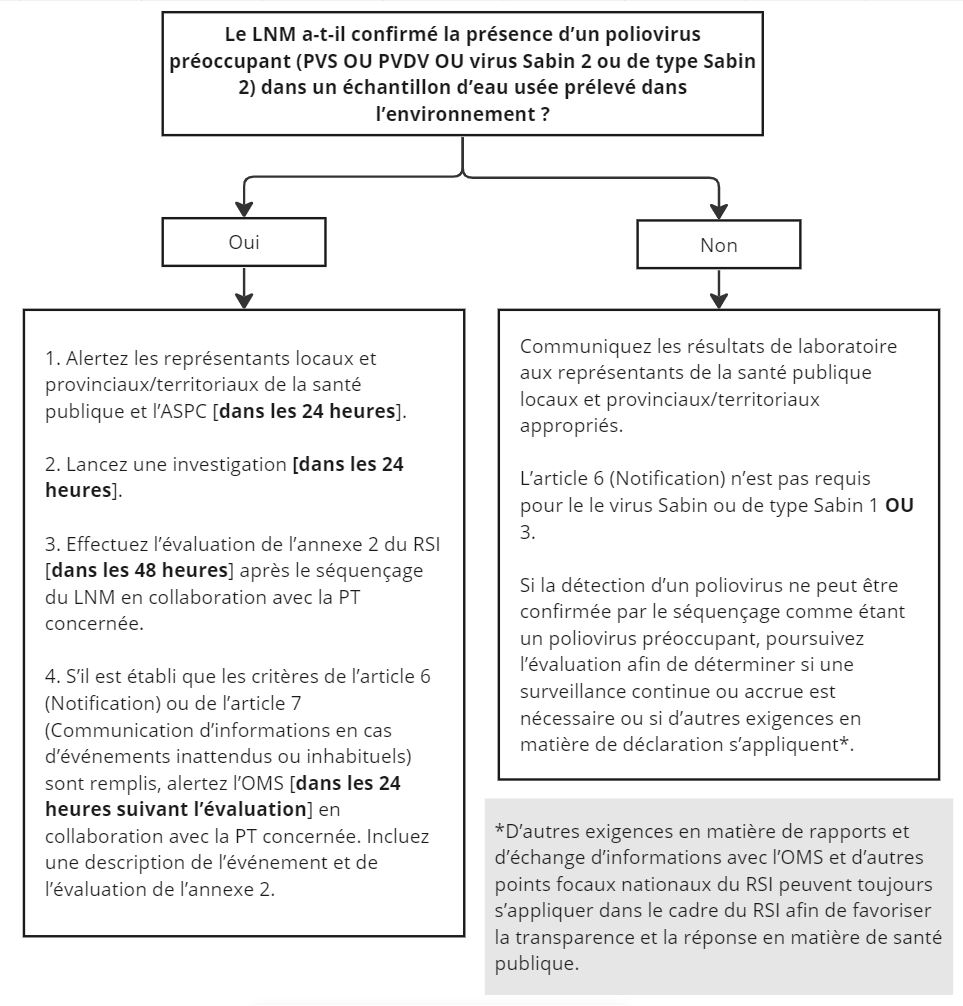
Figure 2 - Équivalent textuel
Le graphique est un organigramme illustrant les principales étapes initiales et les exigences de notification pour la détection du poliovirus à partir d'un prélèvement d'eau usée dans l'environnement.
La première étape consiste à déterminer si le LNM a confirmé la présence d'un poliovirus préoccupant (PVS OU PVDV OU virus Sabin 2 ou de type Sabin 2) dans un échantillon d'eau usée prélevé dans l'environnement.
Si la réponse est oui, les prochaines étapes seraient les suivantes :
- Alertez les représentants locaux et provinciaux/territoriaux de la santé publique et l'ASPC dans les 24 heures.
- Lancez une investigation dans les 24 heures.
- Effectuer l'évaluation de l'annexe 2 du RSI dans les 48 heures après le séquençage du LNM en collaboration avec la PT concernée.
- S'il est établi que les critères de l'article 6 (Notification) ou de l'article 7 (Communication d'informations en cas d'événements inattendus ou inhabituels) sont remplis, alertez l'OMS dans les 24 heures suivant l'évaluation en collaboration avec la PT concernée. Incluez une description de l'événement et de l'évaluation de l'annexe 2.
Si la réponse est non et qu'un poliovirus préoccupant n'a pas été confirmé, les résultats du laboratoire seront communiqués aux représentants de la santé publique locaux, provinciaux et territoriaux appropriés.
L'article 6 (Notification) n'est pas requis pour le virus Sabin ou de type Sabin 1 ou 3.
Si la détection d'un poliovirus ne peut être confirmée par le séquençage comme étant un poliovirus préoccupant, poursuivez l'évaluation afin de déterminer si une surveillance continue ou accrue est nécessaire ou si d'autres exigences en matière de rapports s'appliquent dans le cadre du RSI afin de favoriser la transparence et la réponse en matière de santé publique.

Figure 3 - Équivalent textuel
Le graphique est un organigramme illustrant les principales étapes initiales et les exigences en matière de notification pour un événement lié à l'installation impliquant le poliovirus.
Il est à noter que si une personne ou une source environnementale est détectée à tout moment, il faut suivre le processus illustré à la figure 1 ou à la figure 2, respectivement.
La première étape consiste à déterminer s'il y a eu un événement lié à une installation impliquant le poliovirus.
Si la réponse est non, aucun rapport n'est requis.
Si la réponse est oui, les prochaines étapes seraient les suivantes :
- Alertez sans délai les représentants provinciaux/territoriaux de la santé publique appropriés, l'ASPC, le LNM et le Centre de la biosûreté.
- Effectuez une investigation de l'événement dans les 24 heures.
Une fois les étapes ci-dessus terminées, suivez les étapes suivantes :
- Effectuez l'évaluation de l'annexe 2 du RSI dans les 48 heures à la suite d'un événement lié à l'installation, en collaboration avec la PT concernée.
- S'il est établi que les critères de l'article 6 (Notification) ou de l'article 7 (Communication d'informations en cas d'événements inattendus ou inhabituels) sont remplis, alertez l'OMS dans les 24 heures suivant l'évaluation en collaboration avec la PT concernée et incluez une description de l'événement et une évaluation de l'annexe 2.
Si les critères de l'article 6 ou de l'article 7 ne sont pas remplis, poursuivez l'évaluation pour déterminer si d'autres exigences en matière de rapports s'appliquent dans le cadre du RSI afin de favoriser la transparence et la réponse en matière de santé publique.
Annexe B : Gestion de la santé publique d'un événement lié à l'installation impliquant le poliovirus
Évaluation des risques pour la santé publique d'une exposition au poliovirus liée à l'installation
| Risque pour la santé publique | Événement d'exposition au poliovirus |
|---|---|
| Risque très élevé |
|
| Risque élevé |
|
| Faible risque |
|
| Risque minimal |
|
Remarque 1 : Lorsqu'une brèche implique plusieurs poliovirus, évaluez le risque pour le virus qui présente le plus grand risque pour la santé publique.
Remarque 2 : Lorsque vous évaluez le risque pour la santé publique, tenez compte des antécédents et du profil de vaccination des personnes exposées ayant des contacts étroits ou de la communauté locale.
Surveillance de l'excrétion virale après l'exposition dans un événement lié à l'établissement : calendrier de prélèvement et d'échantillonnage des échantillons.
Prélevez des échantillons de milieu de transport universel et de selles (2 à 8 g) les jours 3/4 et 7/8 après l'exposition. Si le ou les échantillons se sont révélés négatifs pour le poliovirus par RT-PCR, l'exposition probable n'a pas entraîné l'excrétion mesurable du virus. Il est possible de mettre fin à l'isolement de la personne.
Si des échantillons obtiennent un résultat positif au test de dépistage du poliovirus, continuez de prélever des échantillons de selles tous les jours jusqu'à ce que trois échantillons consécutifs prélevés à 24 heures d'intervalle obtiennent un résultat négatif.
Mesures de contrôle possibles pour la gestion d'une personne potentiellement exposée dans un événement lié à l'installation par le type de matériel contenant le poliovirus
| Activité | Sabin / de type Sabin 1 et 3 | Sabin / de type Sabin 2 (avec une couverture du VPI de > 90 % et un accès à des eaux usées gérées en toute sécurité) |
PVS/PVDV (tout type) Sabin / de type Sabin 2 – (< 90 % de couverture du VPI et moindre accès à des eaux usées gérées en toute sécurité) |
|---|---|---|---|
| Isolement | Aucun | Au domicile | Au domicile, bonne conformité |
| Durée de l'isolement | S. O. | Au moins 7 jours à domicile si tous les tests sont négatifs | Au moins 7 jours à domicile si tous les tests sont négatifs |
| Gestion des selles | Eaux usées générales; désinfection des toilettes après utilisation | Eaux usées générales. Toilettes dédiées (à usage personnel) si possible. | Eaux usées générales. Toilettes dédiées (à usage personnel) ou Recueillir et incinérer si les toilettes ne sont pas raccordées à un système municipal de gestion des eaux usées |
| Nettoyage/ désinfection | Désinfectant contenant de l'eau de Javel à usage domestique et du peroxyde d'hydrogène accéléré (PHA) à 0,5 % (p. ex. PREempt RTU) | Désinfectant contenant de l'eau de Javel à usage domestique et du PHA à 0,5 % (p. ex. PREempt RTU) | Désinfectant contenant de l'eau de Javel à usage domestique et du PHA à 0,5 % (p. ex. PREempt RTU) |
| Manipulation des aliments (pour les autres personnes) | Non autorisé | Non autorisé | Non autorisé |
| Contacts étroits/visiteurs | Devrait se limiter aux personnes qui ont des antécédents prouvés de vaccination et qui sont en bonne santé en général (c.-à-d. qui ne sont pas immunodéprimées); devrait être informé sur le lavage des mains approprié. | Devrait se limiter aux personnes qui ont des antécédents prouvés de vaccination et qui sont en bonne santé en général (c.-à-d. qui ne sont pas immunodéprimées); devrait être informé sur le lavage des mains approprié. | Devrait se limiter aux personnes qui ont des antécédents prouvés de vaccination et qui sont en bonne santé en général (c.-à-d. qui ne sont pas immunodéprimées); devrait être informé sur le lavage des mains approprié. |
Pour obtenir d'autres recommandations de mesures de contrôle fondées sur le risque pour la santé publique posé par l'exposition, voir Gestion en santé publique de l'exposition à des poliovirus vivants associée aux établissements de l'OMS
Législation canadienne pertinente : Loi sur les agents pathogènes humains et les toxines
- En vertu paragraphe 12(1) de la LAPHT : « Obligation d'aviser le ministre : Rejet involontaire 12 (1) Le titulaire de permis qui a des motifs de croire que des agents pathogènes humains ou des toxines ont été involontairement rejetés de l'établissement dans le cadre d'activités par ailleurs autorisées par le permis en avise le ministre et communique à celui-ci, sans délai, les renseignements visés au paragraphe (3) relevant de lui ».
- Dans le cas d'un événement de bioconfinement de poliovirus impliquant une maladie humaine : « Obligation d'aviser le ministre : Maladie (13) Le titulaire de permis qui a des motifs de croire qu'un événement mettant en cause des agents pathogènes humains ou des toxines qui sont en sa possession a causé ou peut avoir causé une maladie chez une personne en avise le ministre et communique à celui-ci, sans délai, les renseignements ci-après relevant de lui : a) une description de l'événement; b) le nom des agents pathogènes humains ou des toxines en cause; et c) ceux exigés par le ministre relativement à l'événement ».
Annexe C : Protocoles de laboratoire
Protocole de collecte d'échantillons cliniques
Pour les diagnostics, assurez-vous de prélever au moins deux échantillons de selles (prélevés à au moins 24 heures d'intervalle et à au moins 2 grammes par échantillon) dans les 14 jours suivant l'apparition des symptômes pour les études virales.
Les selles (deux échantillons prélevés à au moins 24 heures d'intervalle) constituent l'échantillon clinique requis pour l'enquête en laboratoire et le diagnostic des infections de poliovirus. Les selles prélevées dans les couches sont des échantillons acceptables. On préfère un échantillon de selles à un écouvillon rectal parce que le diagnostic de poliovirus est plus fiable.
Un cas peut être considéré comme n'étant plus infectieux sur la base de trois échantillons de selles négatifs consécutifs prélevés à au moins 24 heures d'intervalle.
On peut déterminer qu'un contact à risque élevé soumis à un échantillonnage des selles n'est pas infecté, en se fondant sur deux échantillons de selles négatives consécutives prélevées à au moins 48 heures d'intervalle, la première ayant été prélevée au moins quatre jours après la dernière exposition du contact au cas avant que les mesures de prévention et de contrôle des infections ne soient mises en œuvre.
| Volume minimum requis | 2-8 g |
|---|---|
| Délai d'exécution | Le délai total d'exécution de l'algorithme complet de dépistage de la poliomyélite est de 28 jours civils :
|
| Collecte, stockage et conservation des échantillons avant l'expédition | Au moins deux spécimens de selles prélevés à au moins 24 heures d'intervalle, idéalement dans les 14 jours suivant l'apparition de la maladie Les échantillons peuvent être prélevés jusqu'à six semaines après le début s'il n'est pas possible de les prélever plus tôt Placer dans un récipient stérile et étanche Conserver les échantillons à l'état congelé (≤ -20 o C) Ne pas ajouter de milieu de transport |
| Instructions d'expédition | Le LNM n'accepte pas les envois de routine les week-ends et les jours fériés. Veillez à ce que les colis arrivent du lundi au vendredi. Expédiez les spécimens congelés sur glace sèche conformément aux réglementations du Règlement sur le transport des marchandises dangereuses. |
- Requête de détection du poliovirus du LNM
- Détection et caractérisation moléculaire du LNM (pour soumettre des échantillons cliniques au laboratoire)
| Collecte, stockage et conservation des échantillons avant l'expédition | Il faut envoyer 500 mL d'échantillons composites ou instantanés à l'Unité de surveillance des eaux usées du LNM de l'ASPC. Idéalement, les échantillons devraient être conservés à 4 oC pendant le prélèvement et l'entreposage. L'impact des agents de conservation communs pour l'eau et les eaux usées n'a pas été évalué, et les auteurs sont déconseillés d'envoyer des échantillons conservés. Veuillez communiquer avec le LNM (NMLWastewater.NMLWastewater@phac-aspc.gc.ca) avant de planifier l'envoi d'échantillons au LNM pour la recherche du poliovirus dans les eaux usées. |
|---|---|
| Instructions d'expédition | Le LNM n'accepte pas les expéditions systémiques les week-ends et les jours fériés. Veillez à ce que les colis arrivent du lundi au vendredi. Veuillez consulter le Protocole d'emballage des échantillons d'eaux usées en vue de leur expédition. Chaque expédition est accompagnée d'un modèle de formulaire de requête disponible en ligne.
Détails essentiels :
|
Travailler et stocker du matériel potentiellement infectieux (poliovirus)
Lors de l'utilisation et de l'entreposage des MPI, des mesures d'atténuation des risques doivent être prises pour prévenir les événements liés à l'installation, comme indiqué dans le document d'orientation sur les MPI de l'OMS (2e édition). Ces exigences sont les suivantes :
- Vérification de la vaccination contre la polio du personnel manipulant le virus. Si la vaccination ne peut être vérifiée, ils doivent recevoir un seul vaccin à vie pour adultes contenant du VPI. Protocoles de biosécurité améliorés - cela comprend le stockage du MPI dans des congélateurs verrouillés, séparés de l'inventaire général, avec accès limité au personnel formé. En outre, des inventaires détaillés doivent être tenus à jour et communiqués au Centre de biosécurité de l'ASPC en tant qu'autorité nationale de confinement (ANC) du Canada pour le poliovirus. For additional information, containment questions can be directed to Canada's NAC at polio@phac-aspc.gc.ca; utilisez la ligne d'objet « Eaux usées de confinement du poliovirus ».
- Remarque : Bien que les eaux usées et les concentrés ne présentent pas de risque immédiat pour le personnel vacciné (la concentration du virus est inférieure à la dose infectieuse), les lignes directrices visent à s'assurer que l'installation identifie ces matières afin qu'aucune activité à risque élevé activités à haut risque (comme l'inoculation dans des cellules permissives contre la polio) sont effectuées par inadvertance.
- Les évaluations détaillées des risques biologiques, qui éclaireront les pratiques exemplaires en matière de biosécurité (comme les mesures visant à réduire l'exposition aux aérosols, les désinfectants et l'ÉPI supplémentaire à utiliser) doivent être versées au dossier.
- Si la présence d'un poliovirus éradiqué (type 2), ou de tout type ou d'un PVDV/PVS, est confirmée, cette matière est assujettie aux exigences de confinement complet. Pour les laboratoires qui ne sont pas officiellement désignés par l'ANC comme installation essentielle à la lutte contre la polio, le MPI doit être détruit ou désactivé au moyen de procédures validées. On peut communiquer avec l'ACN canadienne pour obtenir des conseils sur le confinement et l'élimination de MPI à polio@phac-aspc.gc.ca.
- Si l'installation souhaite conserver ce matériel, les options sont les suivantes :
- Transférez le MPI à une installation essentielle à la lutte contre le polio certifiée (le LNM);
- Présentez une demande à l'ANC pour devenir une installation essentielle à la lutte contre le polio certifiée pour répondre aux exigences en matière de biosûreté et de biosécurité décrites dans le Plan d'action mondial pour le confinement du poliovirus (GAPIV) et la Stratégie pour le confinement du poliovirus.
Annexe D : Signalements en vertu du RSI
Invites de description d'événement
Insérez la description de l'événement, si possible en incluant :
- le nombre de cas et de décès
- la définition des cas
- les résultats de laboratoire
- la source et le type de risque
- les conditions affectant la propagation de la maladie
- les mesures de santé publique prises
Remarque : Si ces renseignements ne sont pas encore disponibles au moment du signalement il faut les fournir à l'OPS et à l'OMS dès que possible dans un rapport de suivi ou de mise à jour.

Figure 4 - Équivalent textuel
Le graphique est un organigramme illustrant les points de décision pour l'évaluation et la notification des événements susceptibles de constituer une urgence de santé publique de portée internationale.
Les événements détectés par les systèmes de surveillance nationaux relèvent de l'une des trois catégories suivantes :
La première catégorie concerne les cas de certaines maladies qui sont inhabituelles ou inattendues et qui peuvent avoir d'importantes répercussions pour la santé publique, et qui doivent donc être notifiées conformément aux définitions de cas de l'OMS. Ces maladies sont la variole, la poliomyélite due à un poliovirus de type sauvage, la grippe humaine causée par un nouveau sous-type ou le syndrome respiratoire aigu sévère (SRAS). L'illustration précise que la liste des maladies ne doit être utilisée qu'aux fins du présent règlement.
- Si l'événement est un cas de l'une des maladies identifiées, il doit être notifié à l'OMS en vertu du Règlement sanitaire international.
La deuxième catégorie d'événements concerne tout événement d'avoir une ampleur internationale pour la santé publique, y compris les événements dont les causes ou l'origine sont inconnues et ceux impliquant des événements ou des maladies autres que ceux mentionnés dans la première catégorie ou la troisième catégorie, entraîne l'utilisation de l'algorithme.
La troisième catégorie concerne les événements impliquant la présence des maladies ci-après entraîne toujours l'utilisation de l'algorithme, car il a été démontré qu'elles pouvaient avoir d'importantes répercussions sur la santé publique et étaient susceptibles de se propager rapidement au plan international. Les maladies répertoriées sont le choléra, la peste pulmonaire, la fièvre jaune, les fièvres hémorragiques virales (Ebola, Lassa, Marburg), la fièvre à West Nile et d'autres maladies ayant une ampleur nationale ou régionale particulière, par exemple dengue, fièvre de la vallée du Rift et méningococcies.
Pour les deuxième et troisième catégories d'événements, l'utilisateur est invité à évaluer l'événement à l'aide de quatre questions :
- Les répercussions de l'événement sur la santé publique sont-elles graves?
- L'événement est-il inhabituel ou inattendu?
- Y a-t-il un risque important de propagation internationale?
- Y a-t-il un risque important de restrictions aux voyages internationaux et au commerce international?
En cas de réponse affirmative à au moins deux de ces questions, le diagramme indique que l'événement doit être notifié à l'OMS en vertu du Règlement sanitaire international. En cas de réponse affirmative à moins de deux questions, le diagramme indique qu'il n'est pas nécessaire de notifier l'événement à ce stade et qu'il convient de réévaluer la situation lorsqu'on dispose d'informations supplémentaires.
Source : Annexe 2 du Règlement sanitaire international (2005) (RSI)
Remarque : La décision pour chaque invite, ainsi qu'une justification, devront être consignées et soumises dans le cadre de l'évaluation.
Annexe E : Évaluation initiale des risques de l'IMEP
| Catégorie de risque | Risque élevé | Faible risque | Remarques |
|---|---|---|---|
| VIROLOGIE | |||
| PVDVc | Automatiquement défini comme situation à risque élevé | - | - |
| Facteurs virologiques | |||
| Écart génétique par rapport au virus du vaccin d'origine (changements nucléotidiques) | Significatif | Mineur | Demander l'évaluation d'un virologue expert |
| Lien, le cas échéant, avec les isolations passées | Lié | Non lié | |
| Caractérisation ou interprétation du virologue | Oui | Non | |
| Co-circulation avec le PVS | Oui | Non | |
| Détection d'autres PVDV (non liés) dans la région | Oui | Non | |
| Source humaine | |||
| Co-isolation avec d'autres virus Sabin ou entérovirus | Oui | Non | |
| Preuve d'une immunodéficience primaire | Non | Oui | |
| Science de l'environnement | |||
| Nombre d'isolats de virus | Élevé | Moyen/faible | |
| Diversité génétique (nombre de groupes génétiques) | |||
| CONTEXTE | |||
| Caractéristiques des cas | |||
| Membre d'une population « à haut risque » connue ou mal desservie (bidonville, minorité, réfugié, mobile, déplacé, etc.) | Oui | Non | Examen et discussion par des experts techniques, aux niveaux nationaux, régional et mondial |
| 0 dose ou « sous » vacciné | Oui | Non | |
| Âgés de plus de 5 ans | Oui | Non | |
| Données de couverture | |||
| Couverture de la vaccination de routine (VPI si disponible – sinon diphtérie-tétanos-coqueluche) dans le niveau 1 de l'administration infectée | Faible | Bien/élevé | L'immunité de la population pour les poliovirus de type 2 devrait tenir compte du temps écoulé depuis le changement et l'utilisation du VPI pour estimer la population naïve de type 2 |
| Qualité des précédents (>5 % d'enfants manqués par les données sur la GI, >80 % de LQAS réussis) | Faible | Passable/bien | |
| Catégorie de risque | Risque élevé | Faible risque | Remarques |
| Qualité de la surveillance | |||
| Qualité de la surveillance (facteurs comme des indicateurs de FPA inférieurs aux normes, surveillance de l'environnement peu fréquents ou absents, virus orphelin) dans le niveau 1 de l'administration infectée | Évident | Passable/bien | - |
| Autre détection récente du poliovirus | Oui | Non | - |
| Contexte du niveau 1 de l'administration | |||
| Grandes régions densément peuplées | Oui | Non | - |
| Populations à haut risque connues (mobiles, réfugiées, commerçants, pèlerins, personnes déplacées) | Oui | Non | - |
| Zone peu sûre ou inaccessible affectant la surveillance ou la vaccination | Oui | Non | - |
| Tout type d'événement sentinelle indiquant un risque plus élevé de propagation rapide | Oui | Non | - |
| Preuve d'une rupture de confinement | Oui | Non | - |
| Recherche du VOTP/mVPO2/nVPO2 dans un balayage de la chaîne de distribution des vaccins | Oui | Non | - |
| Conditions environnementales associées à des niveaux élevés de transmission fécale-orale | Eau et assainissement insuffisants | Eau et assainissement passables/bons | - |
| Diffusion internationale | |||
| Liens avec la frontière internationale | |||
| Liaison de transport contiguë ou directe avec la frontière internationale (en particulier si l'autre zone est connue comme présentant un risque élevé) | Oui | Non | Enquête locale sur le cas ou basée sur les données disponibles Examen et discussion par les experts techniques de l'IMEP, en consultation avec les niveaux nationaux et régionaux |
| Liens entre le site ou la personne ayant un poliovirus et d'autres pays (comme les marchés, les voies de transport) | Oui | Non | |
| Antécédents de voyage d'un cas de poliovirus ou d'un ménage (comme un réfugié, un nomade, un pèlerinage, un apatride) vers le pays voisin (ou tout autre pays) | Oui | Non | |
| Antécédents de transmission de la poliomyélite et d'éclosions entre les pays | Oui | Non | |
| Mobilité/migration de la population | |||
| Points de service communs entre la zone infectée et les zones avoisinantes, comme les marchés, les sites de pèlerinage, les sites de commerce communs, etc. | Oui | Non | - |
| Preuves de niveaux élevés de migration (à partir des données de séquençage, des données disponibles sur les téléphones cellulaires, des modèles de migration antérieurs, etc.) | Oui | Non | - |
| Contexte des régions avoisinantes | |||
| Preuve de lacunes en matière de surveillance ou d'autres facteurs de risque élevé dans les régions avoisinantes susceptibles d'être importées des régions touchées | Oui | Non | - |
| Immunité de la population dans les pays ou régions avoisinantes | Faible | Bien/élevé | - |
| Conflit | Présent | Aucun | - |
Source : PON de l'IMEP : Riposte à un Évènement Ou à une Flambée de Poliomyélite
Références sélectionnées
- Note de bas de page 1
-
Organisation mondiale de la Santé. Énoncés du Comité d'urgence du RSI sur la poliomyélite. 2023; disponible à l'adresse : https://www.who.int/groups/poliovirus-ihr-emergency-committee
- Note de bas de page 2
-
Initiative mondiale pour l'éradication de la poliomyélite. Global eradication of wild poliovirus type 2 declared. 2015; disponible à l'adresse https://polioeradication.org/news-post/global-eradication-of-wild-poliovirus-type-2-declared
- Note de bas de page 3
-
Initiative mondiale pour l'éradication de la poliomyélite. Two out of three wild poliovirus strains eradicated. 2019; disponible à l'adresse https://polioeradication.org/news-post/two-out-of-three-wild-poliovirus-strains-eradicated/
- Note de bas de page 4
-
Initiative mondiale pour l'éradication de la poliomyélite. Classification et notification des poliovirus dérivés d'une souche vaccinale (PVDV). 2016; disponible à l'adresse https://polioeradication.org/wp-content/uploads/2016/09/Reporting-and-Classification-of-VDPVs_Aug2016_FR.pdf
- Note de bas de page 5
-
Agence de la santé publique du Canada. Programmes de vaccination systématique et de rattrapage des provinces et des territoires pour les nourrissons et les enfants au Canada. 2023; disponible à l'adresse : https://www.canada.ca/fr/sante-publique/services/renseignements-immunisation-provinces-et-territoires/programmes-vaccination-systematique-provinces-territoires-nourrissons-enfants.html
- Note de bas de page 6
-
Initiative mondiale pour l'éradication de la poliomyélite. OPV Cessation. 2023; disponible à l'adresse : https://polioeradication.org/polio-today/preparing-for-a-polio-free-world/opv-cessation/#:~:text=The%20switch,with%20significant%20public%20health%20benefitsalertalert
- Note de bas de page 7
-
Initiative mondiale pour l'éradication de la poliomyélite. Inactivated polio vaccine now introduced worldwide. 2019; disponible à l'adresse https://polioeradication.org/news-post/inactivated-polio-vaccine-now-introduced-worldwide/
- Note de bas de page 8
-
Organisation mondiale de la Santé. Polio vaccines: WHO position paper - June 2022. Wkly Epidemiol Rec 24 juin 2022;25(97):277-300
- Note de bas de page 9
-
Organisation mondiale de la Santé. First ever vaccine listed under WHO emergency use. 2020; disponible à l'adresse : https://www.who.int/news/item/13-11-2020-first-ever-vaccine-listed-under-who-emergency-use
- Note de bas de page 10
-
Initiative mondiale pour l'éradication de la poliomyélite. nOPV2. 2023; disponible à l'adresse : https://polioeradication.org/nopv2
- Note de bas de page 11
-
Initiative mondiale pour l'éradication de la poliomyélite. Preparing for nOPV2 Use: An overview on requirements for countries. 2022; disponible à l'adresse : https://polioeradication.org/wp-content/uploads/2022/06/nOPV2-requirements-overview-for-countries-.pdf
- Note de bas de page 12
-
Macklin GR, Peak C, Eisenhawer M, Kurji F, Mach O, Konz J, et al. Enabling accelerated vaccine roll-out for Public Health Emergencies of International Concern (PHEICs): Novel Oral Polio Vaccine type 2 (nOPV2) experience. Vaccine 6 avril 2023;41:A122-A127
- Note de bas de page 13
-
Desai S, Smith T, Thorley BR, Grenier D, Dickson N, Altpeter E, et al. Performance of acute flaccid paralysis surveillance compared with World Health Organization standards. J Paediatr Child Health 14 juillet 2014;51(2):209-214
- Note de bas de page 14
-
Agence de la santé publique du Canada. Polio : Pour les professionnels de la santé. 2023; disponible à l'adresse : https://www.canada.ca/fr/sante-publique/services/maladies/poliomyelite-polio/professionels.html
- Note de bas de page 15
-
Booth TF, Grudeski E, McDermid A, Rotondo J. La phase finale de l'éradication de la poliomyélite : Pourquoi l'immunisation et la surveillance continue sont essentielles Relevé des maladies transmissibles au Canada 15 octobre 2015;41:233
- Note de bas de page 16
-
Organisation mondiale de la Santé. WHO Global Action Plan for Poliovirus Containment (GAPIV). 2022; https://polioeradication.org/wp-content/uploads/2022/07/WHO-Global-Action-Plan-for-Poliovirus-Containment-GAPIV.pdf
- Note de bas de page 17
-
Organisation mondiale de la Santé. Règlement sanitaire international (2005), 3e éd. 2016; disponible à l'adresse : https://apps.who.int/iris/handle/10665/246187
- Note de bas de page 18
-
Organisation mondiale de la Santé. Définitions de cas relatives aux 4 maladies devant être notifiées en toutes circonstances en vertu du Règlement sanitaire international. 2005; disponible à l'adresse : https://cdn.who.int/media/docs/default-source/documents/emergencies/case-definitions-ihr-four-diseases7f1ee707-3d13-4581-a1af-d5f44f86423a.pdf?sfvrsn=9c68df20_1&download=true
Références
- Référence a
-
Détection signifie la date du prélèvement de l'échantillon de selles qui a été positif pour le poliovirus chez les personnes qui ont une infection par le poliovirus non paralytique.
- Référence b
-
Voir l'annexe B pour plus de détails sur les incidents liés aux installations. Pour de plus amples renseignements sur les incidents de poliovirus liés à la fabrication de laboratoires et de vaccins, voir Gestion en santé publique de l'exposition à des poliovirus vivants associée aux établissements.
- Référence c
-
Les critères de classification du PVDVc figurent à la page 3 du document « Classification et notification des poliovirus dérivés d'une souche vaccinale (PVDV) » de l'IMEP.
- Référence d
-
Le poliovirus présent dans les échantillons cliniques et environnementaux survit indéfiniment dans le congélateur de laboratoire (≤ -20 o C) et pendant de nombreux mois dans le réfrigérateur.
