Les équivalents de biosurveillance comme outil d’évaluation des données de biosurveillance à l’échelle de la population : Perspective de Santé Canada

Télécharger le rapport complet (Format PDF, 641 ko, 40 pages)
Organisation : Santé Canada
Cat.: H129-66/2016F-PDF
ISBN: 978-0-660-06289-1
Publiée : décembre 2016
Préparé par le sous-Groupe de travail sur les équivalents de biosurveillance du Groupe de travail sur l'évaluation des risques scientifiques (GTERS)
- Annie St-Amand, Bureau de la surveillance des produits chimiquesNote de bas de page 1, Direction des sciences de la santé environnementale et de la radioprotection (DSSER), Direction générale de la santé environnementale et de la sécurité des consommateurs (DGSESC)
- Kristin Macey, Bureau de l'évaluation des risques pour les substances existantes, Direction de la sécurité des milieux, DGSESC
- Andy Nong, Bureau de la science et de la recherche en santé environnementale, DSSER, DGSESC
- Mark Feeley, Bureau d'innocuité des produits chimiques, Direction des aliments, Direction générale des produits de santé et des aliments
- Kim Irwin, Agence de réglementation de la lutte antiparasitaire, Santé Canada
- Victoria Honeyman, Agence de réglementation de la lutte antiparasitaire, Santé Canada
- Michelle Deveau, Bureau de la qualité de l'eau et de l'air, Direction de la sécurité des milieux, DGSESC
Examinateurs :
- Stephanie Wille, Bureau de l'évaluation des risques pour les substances existantes, Direction de la sécurité des milieux, DGSESC
- Meredith Curren, Bureau de la surveillance des produits chimiquesNote de bas de page 1, DSSER, DGSESC
- Gurusankar Saravanabhavan, Bureau de la surveillance des produits chimiquesNote de bas de page 1, DSSER, DGSESC
- Kate Werry, Bureau de la surveillance des produits chimiquesNote de bas de page 1, DSSER, DGSESC
- Nellie Roest, Bureau de la surveillance des produits chimiquesNote de bas de page 1, DSSER, DGSESC
- Doug Haines, Bureau de la surveillance des produits chimiquesNote de bas de page 1, DSSER, DGSESC
Remerciements :
- Bette Meek, Centre McLaughlin d'évaluation du risque pour la santé des populations, Université d'Ottawa. Le présent document s'appuie sur des éléments tirés d'un rapport non publié de B. Meek (2012).
- Lesa Aylward et Sean Hays, Summit Toxicology. Le présent document s'appuie sur des éléments tirés d'un rapport non publié d'Aylward et Hays (2012).
- Stephanie Wille, Santé Canada. Le présent document s'appuie sur des éléments tirés d'un rapport interne non publié de Willie et al. (29 juin 2011).
- Janine Murray, Santé Canada.
- Monique D'Amour, Santé Canada.
Décembre 2015
Table des matières
- Remerciements :
- Résumé
- 1. Introduction
- 2. Objectif et portée
- 3. Renseignements généraux
- 4. Méthodes
- 5. Élaboration et processus d'examen par les pairs
- 6. Application des EB
- 7. Avantages and Limites
- 8. Perspective internationale
- 9. Références
- Annexe A – Résumé des EB calculés
- Annexe B – Examens externes par les pairs
Résumé
Au Canada, on dispose de plus en plus de données de biosurveillance en population générale. Ces données fournissent des concentrations de référence de contaminants environnementaux chez les Canadiens et peuvent guider l'établissement de priorités quant à l'évaluation et à la gestion des expositions aux substances chimiques. En raison de l'absence de valeurs guides permettant d'interpréter les données de biosurveillance pour la plupart des contaminants de l'environnement, ces données sont normalement présentées sans comparaison à des facteurs de risque. Il est donc difficile de déterminer si les niveaux d'exposition mesurés chez les Canadiens peuvent entraîner des risques pour la santé. Un outil utile pour l'interprétation des données de biosurveillance est l'équivalent de biosurveillance (EB). Par définition, un EB est la concentration mesurée d'un biomarqueur (p. ex. une substance chimique présente dans le sang ou l'urine) qui correspond à une valeur guide de protection de la santé établie pour la population générale (p. ex. dose journalière admissible, dose chronique de référence). Les EB ont été principalement mis au point comme outils d'évaluation pour interpréter les données de biosurveillance dans un contexte de risque pour la santé de la population et, par conséquent, pourraient avoir des applications potentielles pour Santé Canada. Plus particulièrement, une comparaison directe des EB avec les résultats d'études de biosurveillance effectuées auprès de la population canadienne pourrait aider les décideurs à déterminer si les expositions actuelles s'approchent des niveaux tolérables pour la population générale ou les dépassent. Cet exercice peut contribuer à établir des priorités en matière d'évaluation et de gestion des risques liés aux contaminants de l'environnement par Santé Canada.
1. Introduction
La biosurveillance consiste à mesurer une substance chimique, ou ses produits de réaction, dans les tissus ou les liquides humains, le plus souvent dans le sang, l'urine et le lait maternel. Conformément à des initiatives menées dans d'autres pays, la biosurveillance de la population générale au Canada est réalisée dans le cadre de l'Enquête canadienne sur les mesures de santé (ECMS) et d'autres études telles que l'Étude mère-enfant sur les composés chimiques de l'environnement (étude MIREC), l'Initiative de biosurveillance des Premières Nations et le Programme de lutte contre les contaminants dans le Nord. Outre l'établissement de niveaux de référence des contaminants de l'environnement chez les Canadiens, un des objectifs énoncés dans l'ECMS est d'aider à déterminer les substances chimiques d'intérêt prioritaire qui pourraient nécessiter l'adoption d'autres mesures pour protéger la santé publique.
Au cours des prochaines années, l'accessibilité des résultats de biosurveillance augmentera pour une vaste gamme de substances chimiques. Il est donc opportun d'examiner la manière dont Santé Canada peut utiliser ces données de biosurveillance pour aider à déterminer les substances chimiques d'intérêt prioritaire qui pourraient nécessiter l'adoption d'autres mesures. Pour quelques substances, notamment le plomb et le mercure, des études épidémiologiques exigeantes en temps et en ressources ont permis d'établir une relation quantitative directe entre les mesures de biomarqueurs et les effets sur la santé. Toutefois, une corrélation définitive entre les effets sur la santé et l'exposition d'une population à des niveaux relativement faibles d'un contaminant de l'environnement (mesuré par biosurveillance) est peu probable pour la plupart des substances chimiques. Par conséquent, il faut envisager d'autres approches pour mettre les données de biosurveillance dans un contexte de risque pour la santé. Il peut s'agir d'approches descriptives (p. ex. comparaisons avec d'autres ensembles de données de biosurveillance) ou d'approches fondées sur le risque qui décrivent le niveau de risque associé à un résultat de biosurveillance donné (National Research Council [NRC], 2006).
L'approche des équivalents de biosurveillance permettrait d'identifier les expositions potentiellement importantes (NRC, 2007).
2. Objectif et portée
L'objectif précis du présent rapport est de décrire l'utilité des EB comme outil d'évaluation pour interpréter les données de biosurveillance tirées de l'ECMS et d'autres initiatives de Santé Canada en matière de biosurveillance.
Dans le présent rapport, les méthodes de dérivation des EB sont décrites en fonction de leur application possible dans les programmes de Santé Canada. Au départ, des renseignements généraux sur les EB sont présentés, ainsi qu'une description des objectifs et de la nature des conseils en vue de l'élaboration des EB. La pertinence et l'application possible sont ensuite examinées et suivies d'une analyse sur le contexte international actuel, notamment les précédents relatifs à l'utilisation d'EB pour interpréter les données de biosurveillance. Enfin, des recommandations formulées par le groupe de travail sont présentées.
3. Renseignements généraux
Un équivalent de biosurveillance (EB) est défini comme étant la concentration d'une substance chimique dans un milieu biologique (p. ex. sang, urine, lait maternel) qui correspond à une valeur guide d'exposition chronique ayant été calculée au moyen de données pharmacocinétiques (Hays et al., 2008a). L'EB peut être utilisé comme outil d'évaluation pour interpréter les données de biosurveillance en population dans un contexte de risque pour la santé (p. ex. Aylward et al., 2001a; Kirman et al., 2012).
L'évaluation (ou la sélection) est définie comme [traduction] « l'application d'outils ou de procédures simples qui peuvent être utilisés rapidement pour délimiter les populations susceptibles de présenter, dans une certaine mesure, un risque accru pour la santé de celles qui ne présentent pas ce genre de risque » (Hays et al., 2007). La définition indique en outre que, selon les résultats, les procédures d'évaluation exigent qu'un suivi de confirmation détaillé soit effectué avant qu'on ne puisse tirer des conclusions définitives.
Les EB sont surtout censés servir de valeurs préliminaires à l'intention des professionnels de l'environnement et de la santé pour les aider à évaluer les données de biosurveillance en population générale ou dans une population en particulier. Selon Hays et al. (2007), les EB [traduction] « ne doivent pas servir à évaluer les données de biosurveillance provenant d'individus ni à établir un diagnostic. »
Les valeurs préliminaires sont utilisées depuis un certain temps dans l'évaluation d'expositions professionnelles. Les valeurs de référence fondées sur la biosurveillance comme les indices biologiques d'exposition (IBE) élaborés par l'American Conference of Governmental Industrial Hygienists (ACGIH) représentent normalement la concentration d'un analyte dans un milieu biologique qui correspond à une valeur guide d'exposition (p. ex. la valeur limite d'exposition).
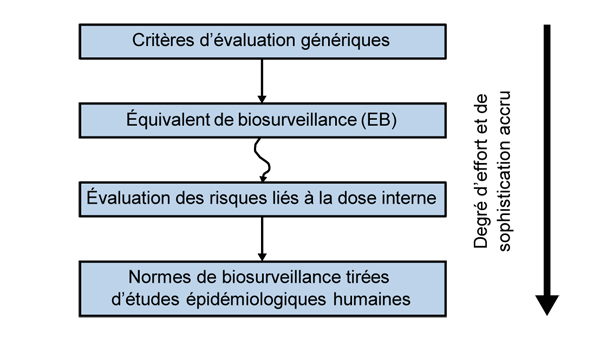
Sur un continuum d'approches de plus en plus fondées sur des données, les EB sont considérés comme étant moins fiables qu'une évaluation exhaustive des risques liés à la dose interne, laquelle est considérée comme moins fiable que les valeurs fondées sur des études épidémiologiques comprenant la biosurveillance (p. ex. la présence de plomb dans le sang) (Hays et al., 2008a) (figure 1). L'EB s'appuie sur des valeurs guides d'exposition et les données pharmacocinétiques disponibles chez l'animal ou l'humain. Une évaluation des risques liés à la dose interne permet d'établir un lien quantitatif entre le point de départ (PDD) toxicologique chez l'animal et une mesure de la dose critique (la concentration dans les tissus de la forme chimique active entraînant la toxicité) qu'on transpose ensuite chez l'humain. Les normes de biosurveillance provenant d'études épidémiologiques humaines sont fondées sur une compréhension quantitative de la relation entre les niveaux de biosurveillance chez l'humain et une réponse biologique/toxicologique observée (p. ex. le plomb et le mercure).
Figure 1. Approches de plus en plus fondées sur des données pour interpréter les données de biosurveillance (adaptation de Hays et al., 2008a)
Équivalent textuel
Ce diagramme illustre les diverses approches pour interpréter les données de biosurveillance dans un continuum, de haut en bas. En raison du degré d’effort et de sophistication accru requis tout au long du continuum, ces approches doivent englober les éléments suivants : (1) Critères d’évaluation génériques; (2) Équivalent de biosurveillance (EB); (3) Évaluation des risques liés à la dose interne; (4) Normes de biosurveillance tirées d’études épidémiologiques humaines.
4. Méthodes
4.1 Étapes de calcul
La mise au point des EB comporte quatre étapes :
- Étape 1 – Déterminer la dose pertinente et déterminer l'analyte cible
- Étape 2 – Évaluer les données et les modèles pharmacocinétiques disponibles
- Étape 3 – Calculer la concentration du biomarqueur au PDD équivalent chez l'humain (EBPDD et l'EB)
- Étape 4 – Évaluer la variabilité et l'incertitude des données et du calcul
Ces étapes s'appliquent au calcul de la plupart des EB; certaines exceptions se sont toutefois produites.
4.1.1 Étape 1 – Déterminer la dose pertinente et déterminer l'analyte cible (biomarqueurs)
La première étape du calcul d'un EB est la recherche d'une dose d'exposition produisant un effet qui peut provenir d'une dose de référence existante ou d'un point de départ de toxicité pertinent chez l'animal ou l'humain.
Les analytes ou les biomarqueurs cibles pertinents sont tirés des études de biosurveillance et des programmes de surveillance de la santé humaine. Les avantages et les inconvénients des analytes cibles sont caractérisés. À titre d'exemple, les concentrations de la substance chimique d'origine présente dans le sang ou l'urine sont cotées en fonction de leur capacité à bien décrire l'exposition de la substance chimique liée à sa toxicité ou à son mode d'action.
4.1.2 Étape 2 – Évaluer les données et les modèles pharmacocinétiques disponibles
La deuxième étape consiste à évaluer les données pharmacocinétiques et à examiner la possibilité de calculer une valeur tissulaire cible qui corresponde au PDD ou au niveau d'exposition pertinent. Les relations pharmacocinétiques peuvent être aussi simples qu'un ratio entre l'exposition et une dose interne et aussi complexes qu'un modèle physiologique décrivant des processus biologiques complexes. Comme les valeurs guides sont généralement représentatives d'une exposition chronique, des relations pharmacocinétiques simples à l'état d'équilibre sont souvent appliquées pour calculer une mesure de la dose interne. Diverses applications et approches pharmacocinétiques pour le calcul des EB sont décrites en détail plus loin.
4.1.3 Étape 3 – Calculer l'EBPDD et l'EB
La troisième étape consiste à calculer une valeur d'EBPDD en appliquant le facteur d'incertitude pour convertir le PDD chez l'animal en l'équivalent chez l'humain. Cette étape n'est pas requise dans le cas des EB calculés selon les données sur l'humain. La valeur d'EB est ensuite calculée selon la combinaison des données ou modèles PDD et pharmacocinétiques. Le niveau de confiance de la valeur d'EB estimée dépendra de l'incertitude entourant les données PDD et pharmacocinétiques de différentes espèces. Les facteurs d'incertitude peuvent s'appliquer; en outre, ils correspondent généralement à ceux utilisés pour calculer la valeur guide d'exposition qui sous-tend l'EB. Dans certains cas toutefois, l'utilisation de données pharmacocinétiques propres à une substance chimique peut remplacer la partie pharmacocinétique du facteur d'incertitude inter-espèces ou intra-espèce (p. ex. le toluène).
4.1.4 Étape 4 – Évaluer la variabilité et l'incertitude des données et du calcul
La quatrième étape consiste à évaluer la variabilité et l'incertitude de toutes les données (données pharmacocinétiques, mode d'action, étude toxicologique, etc.) Ce processus permet d'établir une classification qualitative du niveau de confiance dans l'EB calculé, soit faible, moyen ou élevé.
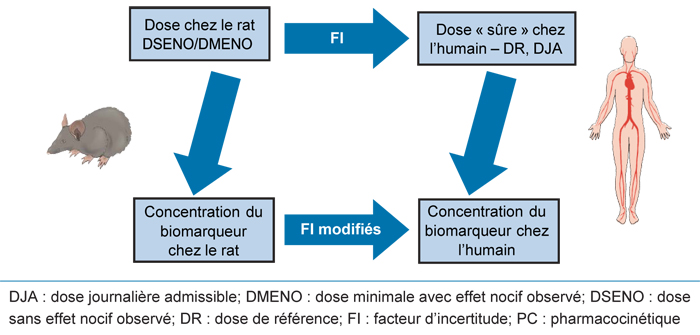
En résumé, les EB reposent sur des considérations semblables à celles des valeurs guides liées à la santé humaine, mais peuvent parfois inclure des renseignements supplémentaires sur les données pharmacocinétiques, tant chez l'animal que chez l'humain (figure 2).
Figure 2. Approche du parallélogramme – équivalents de biosurveillance (adaptation de Hays et al., 2009)
Équivalent textuel
Ce diagramme illustre le processus de calcul des concentrations de biomarqueurs, intégrant des données pharmacocinétiques chez l’animal et l’humain.
La première méthode englobe les étapes ci-après : (1) Détermination de la dose sans effet nocif observé et de la dose minimale avec effet nocif observé (DSENO/DMENO); (2) Détermination de la dose « sûre » pour l’humain (p. ex. dose journalière admissible et dose de référence) en tenant compte de facteurs d’incertitude; (3) Détermination de la concentration du biomarqueur chez l’humain en tenant compte des données pharmacocinétiques pour l’humain.
La deuxième méthode englobe les étapes ci-après : (1) Détermination de la dose sans effet nocif observé et de la dose minimale avec effet nocif observé (DSENO/DMENO); (2) Détermination de la concentration du biomarqueur chez le rat en tenant compte des données pharmacocinétiques pour l’animal; (3) Détermination de la concentration du biomarqueur chez l’humain en tenant compte de facteurs d’incertitude modifiés.
4.2 Composantes nécessaires
La mise au point des EB dépend de la disponibilité de trois composantes clés :
- Composante 1 – Valeur guide d'exposition appropriée
- Composante 2 – Analyte cible pertinent (biomarqueur)
- Composante 3 – Données pharmacocinétiques
Les composantes requises sont décrites dans les sections ci-après.
4.2.1 Composante 1 – Valeur guide d'exposition appropriée
Pour mettre au point des EB, des doses admissibles ou des doses de référence appropriées, conçues pour protéger la population générale, y compris les souspopulations sensibles dans des conditions d'exposition chronique, sont nécessaires. Ces valeurs comprennent notamment des doses de référence (DR) et des concentrations de référence, des niveaux de risque minimaux et des doses journalières admissibles (DJA) établis par Santé Canada, l'Environmental Protection Agency (EPA) des États-Unis, l'Agency for Toxic Substances and Disease Registry (ATSDR) des États-Unis ou l'Organisation mondiale de la Santé (OMS) (Hays et al., 2009). La préférence est accordée aux valeurs guides d'exposition fondées sur des évaluations toxicologiques récentes, qui sont davantage susceptibles de tenir compte de toutes les données pertinentes. Le choix de valeurs guides appropriées liées à la santé humaine tient également compte de la situation géographique et de la population.
Il est également possible de calculer un EB à partir d'un PDD provisoire tiré d'une évaluation n'ayant pas mené à une valeur guide. Un tel calcul ne répond pas à la définition classique d'un EB, mais peut s'appliquer puisque les valeurs guides reposent sur un PDD qui indique un seuil de toxicité comprenant une incertitude sur la valeur (p. ex. différences entre les espèces, variabilité interindividuelle dans une population). Un PDD, ou toute forme d'exposition à une dose induisant un effet, n'est pas différent et peut être modifié pour s'appliquer à un calcul d'EB (Hays et al., 2014). Les modifications du processus de calcul découlant d'une valeur guide pourraient inclure d'autres facteurs comme l'extrapolation d'une espèce à l'autre ou la conversion d'une dose minimale avec effet nocif observé (DMENO) à une dose sans effet nocif observé (DSENO).
4.2.2 Composante 2 – Analyte cible pertinent (biomarqueur)
Les facteurs à prendre en considération pour le choix de l'analyte cible pertinent qui servira au calcul de l'EB sont principalement axés sur les données et reposent sur le biomarqueur mesuré dans les études de biosurveillance. Les EB ne sont pas toujours fondés sur la fraction toxique du composé. Les phtalates en sont un exemple. Même si la mesure de la substance mère dans le sang est plus étroitement liée à la toxicité, l'EB est fondé sur les métabolites urinaires, qui sont le plus souvent mesurés dans les études de biosurveillance. Le choix de biomarqueurs dans les études de biosurveillance et les programmes de surveillance de la santé tient compte entre autres de la disponibilité des méthodes d'analyse, de la spécificité du biomarqueur, de la pertinence relative à la toxicité ou à l'exposition, de la stabilité, du caractère invasif des procédures de prélèvement et de la facilité d'interprétation (Hays et al., 2008a).
4.2.3 Composante 3 – Données pharmacocinétiques
Le calcul des valeurs d'EB requiert des données pharmacocinétiques propres à la substance chimique qui établissent un lien entre la concentration du biomarqueur aux niveaux d'exposition externe du composé d'origine ou aux concentrations internes dans les tissus cibles associées à des effets critiques qui sous-tendent l'évaluation des risques. Ainsi, la nature des données pharmacocinétiques requises varie. Pour de nombreuses substances chimiques, il existe une abondance de données pharmacocinétiques chez les animaux ou les humains. Pour d'autres, ces données sont rares. Le calcul des valeurs d'EB exige un jugement explicite pour compenser les lacunes, tenir compte de la variabilité dans les données pharmacocinétiques et formuler des hypothèses sur l'exposition à l'état d'équilibre. Les hypothèses concernant les propriétés pharmacocinétiques de la substance chimique requises pour calculer l'EB et la confiance en la base de données de pharmacocinétique sont caractérisées par souci de transparence.
4.3 Approches de calcul des EB
Les méthodes de calcul des EB sont classées en trois approches conceptuelles de base. Elles varient de l'approche la moins fondée sur des données (bilan urinaire) à l'approche la plus fondée sur des données (extrapolation de la dose interne) :
- Approche du bilan urinaire
- Approche des concentrations sanguines à l'état d'équilibre
- Approche de l'extrapolation de la dose interne
Les différentes approches de calcul sont décrites dans les sections qui suivent, et un résumé est présenté dans le tableau 1.
Dans ces exemples, les PDD chez l'animal servent à calculer les valeurs d'EB. Il est toutefois possible d'utiliser différentes formes d'exposition à la dose comme PDD pour l'humain; une dose journalière recommandée peut même être utilisée pour calculer un EB provisoire (Hays et al., 2014). Puisque les valeurs guides établies par les agences de santé sont généralement des limites d'exposition à une dose pour un critère d'effet précis, toute forme de dose peut être utilisée comme valeur comparable pour établir un EB provisoire. Cela est important pour les substances chimiques pour lesquelles il n'existe pas de valeurs guides définies ou pour lesquelles il y a peu de données pour faire appel à un PDD. Par ailleurs, il est possible de calculer des EB provisoires pour divers paramètres concernant la même substance chimique et de les évaluer à différents degrés de préoccupation. Cette interprétation ouverte de l'EB provisoire est un outil puissant pour évaluer l'exposition à des substances chimiques sans restreindre l'évaluation à des valeurs guides connues.
4.3.1 Approche du bilan urinaire
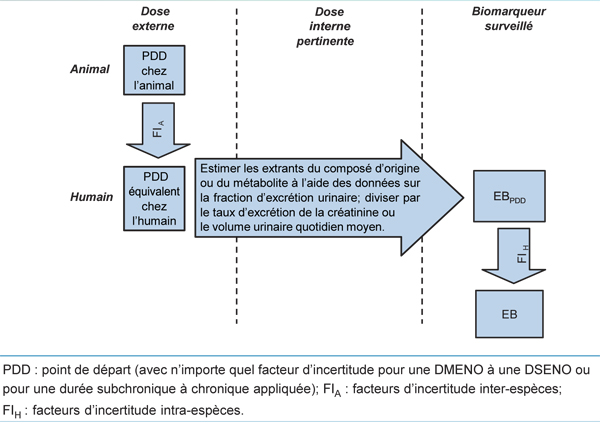
On prédit le taux d'excrétion urinaire à l'état d'équilibre du composé d'origine ou d'un ou de plusieurs métabolites précis d'après des données chez l'humain sur la pharmacocinétique de la substance chimique d'intérêt (figure 3). Les valeurs d'EB calculées de cette façon fournissent des renseignements directement fondés sur des doses internes pertinentes sur le plan toxicologique et, par conséquent, il n'y a aucune incidence sur le réexamen des facteurs concernant les différences inter-espèces et la variabilité humaine intégrées aux doses admissibles ou aux doses de référence sur lesquelles l'EB est basé.
Figure 3. Calcul des valeurs d'EB dans l'urine en fonction du bilan urinaire (adaptation d'Angerer et al., 2011)
Équivalent textuel
Ce diagramme illustre le processus permettant de calculer les valeurs d’EB dans l’urine en fonction du bilan urinaire. Les boîtes de textes s’affichent sous les trois colonnes ci-après, de gauche à droite : Dose externe, Dose interne pertinente et Biomarqueur surveillé.
Dans la colonne Dose externe, les trois étapes ci-dessous sont décrites comme suit, de haut en bas : (1) Point de départ chez l’animal; (2) Facteurs d’incertitude inter-espèces; (3) Point de départ équivalent chez l’humain.
À partir de ce point, une flèche portant la mention « Estimer les extrants du composé d’origine ou du métabolite à l’aide des données sur la fraction d’excrétion urinaire; diviser par le taux d’excrétion de la créatinine ou le volume urinaire quotidien moyen » traverse la colonne du centre (dose interne pertinente).
Cette même flèche passe dans la colonne Biomarqueur surveillé et pointe sur trois étapes, décrites de haut en bas : (1) EB au point de départ; (2) Facteurs d’incertitude inter-espèces; (3) EB.
4.3.2 Approche des concentrations sanguines à l'état d'équilibre
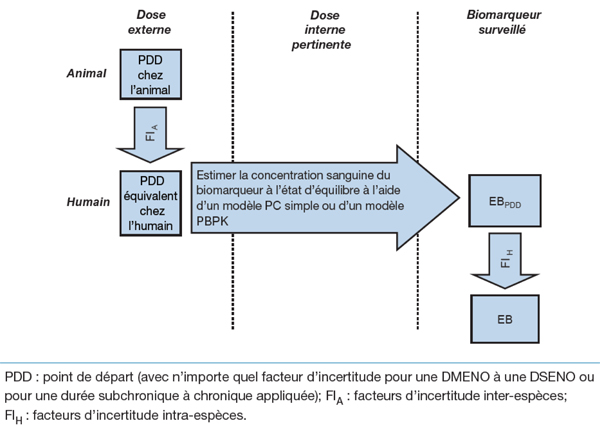
Cette approche prévoit l'estimation de concentrations sanguines, sériques ou plasmatiques à l'état d'équilibre chez l'humain qui correspondent au niveau d'exposition tolérable à l'aide d'une relation pharmacocinétique simple (figure 4). Tout comme l'approche du bilan urinaire, des données sur les corrélations entre l'exposition et les concentrations de la substance chimique ou du métabolite dans le sang (p. ex. concentration corrélative du benzène dans l'air et le sang) sont appliquées pour calculer les estimations à l'état d'équilibre.
Figure 4. Calcul des valeurs d'EB dans le sang en fonction d'un modèle pharmacocinétique simple ou d'un modèle pharmacocinétique (PC) fondée sur la physiologie (modèle PBPK) pour l'humain (adaptation d'Angerer et al., 2011)
Équivalent textuel
Ce diagramme illustre le processus permettant de calculer les valeurs d’EB dans le sang en fonction d’un modèle PC simple ou d’un modèle PBPK pour l’humain. Les boîtes de textes s’affichent sous les trois colonnes ci-après, de gauche à droite : Dose externe, Dose interne pertinente et Biomarqueur surveillé.
Dans la colonne Dose externe, les trois étapes ci-dessous sont décrites comme suit, de haut en bas : (1) Point de départ chez l’animal; (2) Facteurs d’incertitude inter-espèces; (3) Point de départ équivalent chez l’humain.
À partir de ce point, une flèche portant la mention « Estimer la concentration sanguine du biomarqueur à l’état d’équilibre à l’aide d’un modèle PC simple ou d’un modèle PBPK » traverse la colonne du centre (dose interne pertinente).
Cette même flèche passe dans la colonne Biomarqueur surveillé et pointe sur trois étapes, décrites de haut en bas : (1) EB au point de départ; (2) Facteurs d’incertitude inter-espèces; (3) EB.
4.3.3 Approche de l'extrapolation de la dose interne
Dans cette approche, le PDD provient d'une étude de toxicité réalisée sur des animaux, et il existe suffisamment de données pharmacocinétiques ou de données de concentration tissulaire tirées de l'étude critique sur laquelle le PDD est fondé ou d'études complémentaires sur les mêmes espèces animales. Par ailleurs, un modèle pharmacocinétique ou un modèle pharmacocinétique fondée sur la physiologie (modèle PBPK) est accessible pour les espèces présentant un intérêt. Il est possible de calculer la valeur d'EB en reconstruisant l'extrapolation de l'animal à l'humain en fonction des concentrations de la dose interne et du biomarqueur afin d'estimer une valeur (habituellement une valeur sanguine, sérique ou plasmatique) correspondant à l'évaluation des risques liés à la dose externe. Il peut s'agir de données pharmacocinétiques recueillies auprès de l'animal de laboratoire ou de l'humain, et les composantes pharmacocinétiques des facteurs d'incertitude inter-espèces ou intra-espèces peuvent être réexaminés (figure 5).
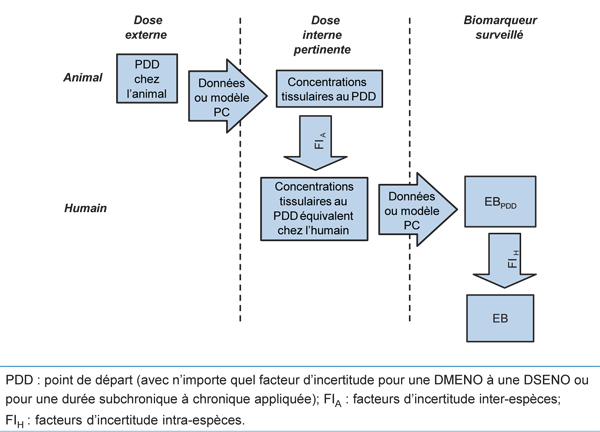
Figure 5. Calcul des valeurs d'EB pour des biomarqueurs sanguins en fonction de la dose interne si le biomarqueur est distinct de la dose tissulaire cible pertinent sur le plan toxicologique (adaptation d'Angerer et al., 2011)
Équivalent textuel
Ce diagramme illustre le processus permettant de calculer les valeurs d’EB pour des biomarqueurs sanguins en fonction de la dose interne si le biomarqueur est distinct de la dose tissulaire cible pertinente sur le plan toxicologique.
Les boîtes de textes s’affichent sous les trois colonnes ci-après, de gauche à droite : Dose externe, Dose interne pertinente et Biomarqueur surveillé.
Dans la colonne Dose externe, la première boîte de texte affiche « Point de départ chez l’animal ». À partir de cette boîte de texte, une flèche indiquant « Données ou modèle PC » traverse la colonne du centre (Dose interne pertinente). À partir de ce point, les trois étapes ci-dessous sont décrites comme suit, de haut en bas : (1) Concentrations tissulaires au PDD; (2) Facteurs d’incertitude inter-espèces; (3) Concentrations tissulaires au point de départ équivalent chez l’humain. À partir de ce point, une deuxième flèche indiquant « Données ou modèle PC » pointe sur la dernière colonne (Biomarqueur surveillé), où sont décrites les trois étapes suivantes, de haut en bas : (1) EB au point de départ; (2) Facteurs d’incertitude inter-espèces; (3) EB.
Il est question de cas particulier lorsqu'on s'attend à ce que les concentrations sanguines ou plasmatiques du biomarqueur soient directement et étroitement liées à la concentration tissulaire cible (figure 6). Dans ce cas, les concentrations du biomarqueur dans le sang mesurées chez les animaux de laboratoire peuvent être extrapolées directement en fonction de la dose interne aux concentrations du biomarqueur chez l'humain. Lorsqu'une dose interne pertinente est utilisée comme base pour l'extrapolation inter-espèces, l'application d'un facteur d'incertitude interespèces pour établir des différences pharmacocinétiques entre les espèces n'est pas forcément nécessaire.
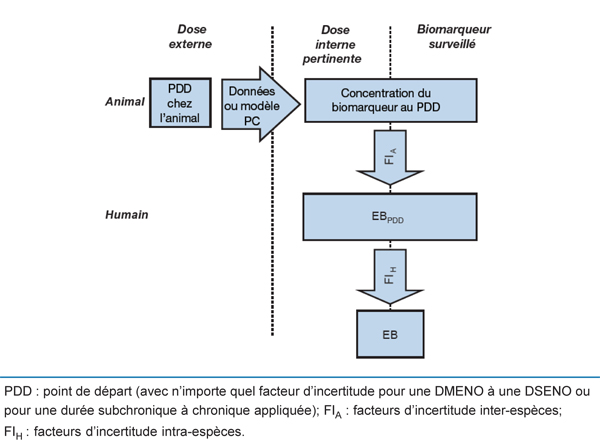
Figure 6. Calcul des valeurs d'EB pour des biomarqueurs sanguins en fonction de la dose interne si le biomarqueur est directement lié ou équivalent à la dose tissulaire cible pertinente sur le plan toxicologique
Équivalent textuel
Ce diagramme illustre le processus permettant de calculer les valeurs d’EB pour des biomarqueurs sanguins en fonction de la dose interne si le biomarqueur est directement lié ou équivalent à la dose tissulaire cible pertinente sur le plan toxicologique.
Les boîtes de textes s’affichent sous les trois colonnes ci-après, de gauche à droite : Dose externe, Dose interne pertinente et Biomarqueur surveillé.
Dans la colonne Dose externe, la première boîte de texte affiche « Point de départ chez l’animal ». À partir de cette boîte de texte, une flèche indiquant « Données ou modèle PC » pointe vers la partie de droite. De là, les cinq étapes ci-dessous sont décrites, de haut en bas, à mi-chemin entre les deux dernières colonnes (Dose interne pertinente et Biomarqueur surveillé) : (1) Concentration du biomarqueur au PDD; (2) Facteurs d’incertitude inter-espèces; (3) EB au point de départ; (4) Facteurs d’incertitude intra-espèces; (5) EB.
Le tableau 1 présente un résumé de la nature des renseignements requis pour l'élaboration de divers types d'EB ainsi que des exemples connexes.
| Approche de calcul (de la moins fondée à la plus fondée sur des données) | Éléments de données | Substances chimiques (référence) |
|---|---|---|
| Calcul des valeurs d'EB dans l'urine en fonction du bilan urinaire (figure 3) | Données chez l'humain sur la pharmacocinétique de la substance chimique d'intérêt | Triclosan (Krishnan et al., 2010a) |
| Conversion directe du niveau d'exposition tolérable à la concentration du biomarqueur dans le sang (figure 4) | Modèle pharmacocinétique simple ou modèle PBPK chez l'humain, ou données établissant une corrélation entre la substance chimique dans le sang et l'exposition externe (dose orale ou concentration dans l'air) | 38 composés organiques volatils (Aylward et al., 2010c); acide 2,4dichlorophénoxyacétique dans le plasma (Aylward et Hays, 2008) |
| Reconstruction de l'évaluation des risques en fonction de la dose interne – concentration tissulaire (figure 5) | Compréhension de la dosimétrie (c.-à-d. la concentration dans le tissu cible) | Cadmium (Hays et al., 2008b) |
| Données ou modèle servant à estimer la dosimétrie pertinente au PDD chez les espèces ou dans l'étude qui sous-tend le calcul de la dose admissible | Acrylamide (Hays et Aylward, 2008) | |
| Données ou modèle établissant un lien entre la dosimétrie et la concentration du biomarqueur dans le sang | Trihalométhanes (Aylward et al., 2008a) | |
| Reconstruction de l'évaluation des risques en fonction de la dose interne – concentration du biomarqueur (figure 6) | Compréhension de la mesure de la dose pertinente (c.-à-d. la concentration tissulaire moyenne dans le tissu sensible) | Hexachlorobenzène (Aylward et al., 2010a) |
| Compréhension de la relation entre la concentration sanguine et la concentration tissulaire cible | Toluène (Aylward et al., 2008b) |
5. Élaboration et processus d'examen par les pairs
5.1 Élaboration du concept de l'EB
Le concept de l'EB comme outil d'interprétation des données de biosurveillance de la population générale a été créé et proposé par Hays et al. (2007). Le projet pilote sur les EB est le résultat d'un effort de collaboration visant à élaborer une première série de lignes directrices pour calculer des EB, mettre en œuvre le concept et appliquer l'approche à certaines études de cas concernant des substances chimiques. Le projet pilote a été mené par Summit Toxicology et commandité par une gamme d'organismes gouvernementaux (dont Santé Canada) et d'associations industrielles. Un groupe d'experts du domaine de la pharmacocinétique, de l'évaluation des risques, de l'éthique médicale et de la communication relatives aux risques provenant d'horizons divers (gouvernement, milieu universitaire et industrie) a participé à l'atelier d'experts sur les équivalents de biosurveillance qui a eu lieu en juin 2007. Les participants avaient pour tâche d'examiner les problèmes techniques et de communication relevés dans le calcul des EB. Un des objectifs de la rencontre était d'élaborer et de publier des lignes directrices pour le calcul et la communication des EB (Hays et al., 2008a; Lakind et al., 2008). À la suite de l'atelier, on a calculé et publié des EB pour cinq substances : l'acrylamide, l'acide 2,4-dichloroacétique (2,4D), le cadmium, les trihalométhanes et le toluène (Hays et Aylward, 2008; Aylward et Hays, 2008; Hays et al., 2008b; Aylward et al., 2008a; Aylward et al., 2008b). Ces EB étaient fondés sur des valeurs guides d'exposition existantes établies par plusieurs organismes de réglementation, notamment Santé Canada, l'EPA des États-Unis et l'OMS.
Dans le cadre d'un contrat de trois ans (2008–2011) signé avec Santé Canada, Summit Toxicology a élaboré des EB pour 13 autres substances chimiques. À Santé Canada, une équipe composée notamment d'évaluateurs de risques provenant de la DGSPA, de la DGSESC et de l'ARLA ont participé à la déclaration et à la sélection de substances chimiques et à l'examen de l'établissement des EB. Parmi les critères de déclaration se trouvaient des substances chimiques qui ont été mesurées et détectées dans le cadre de l'ECMS et qui disposaient de valeurs guides d'exposition établies par Santé Canada (doses journalières admissibles, doses journalières acceptables ou coefficients de cancérogénicité). La plupart des substances chimiques répondaient à ces critères, notamment la cyfluthrine (métabolite 4-F-3-PBA), le phtalate de di(2éthylhexyle) (DEHP), le phtalate de diéthyle (DEP), le phtalate de benzyle et de butyle (BBP), le phtalate de dibutyle (DBP), l'hexachlorobenzène, le triclosan, le bisphénol A (BPA), l'arsenic, le dichlorodiphényltrichloroéthane (DDT) (et son métabolite, le dichlorodiphényldichloroéthylène [DDE]), la deltaméthrine (métabolite cis-DBCA), le polybromodiphényléther 99 (PBDE 99) et le phtalate de diisononyle (DINP). Ces calculs d'EB ont été publiés dans la revue Regulatory Toxicology and Pharmacology (Aylward et al., 2009a; Aylward et al., 2009b; Aylward et al., 2010b; Aylward et al., 2011; Hays et al., 2009; Hays et al., 2010; Hays et al., 2011; Kirman et al., 2011; Krishnan et al., 2010a; Krishnan et al., 2010b; Krishnan et al., 2011).
Les EB établis pour de nombreuses autres substances, notamment les dioxines, les composés organiques volatils (COV) et l'uranium, ont été publiés ou sont en cours d'élaboration. Environ 80 valeurs D'EB comprenant plus de 100 analytes sont maintenant publiées. L'annexe A présente une liste des substances pour lesquelles des EB ont été établis et pour lesquelles les données de l'ECMS sont ou seront accessibles dans les cycles 1 à 6.
Dans les manuscrits publiés, on a comparé les valeurs d'EB aux données de biosurveillance tirées de l'ECMS (St-Amand et al., 2014) et de la National Health and Nutrition Examination Survey (NHANES) des États-Unis (Aylward et al., 2013). Plusieurs autres publications ont permis de comparer des données de biosurveillance aux valeurs d'EB, notamment des concentrations de 2,4D dans différentes cohortes de biosurveillance (Aylward et al., 2010c), des COV dans le sang tirés de l'étude NHANES (Kirman et al., 2012) et des concentrations sanguines de HBCD dans diverses populations (Aylward et Hays, 2011).
5.2 Processus d'examen par les pairs
Le concept des EB a été proposé par Hays et al. (2007) comme outil d'évaluation des données de biosurveillance pour la population générale. Il s'agit du prolongement d'outils similaires déjà utilisés dans le secteur professionnel (p. ex. les indices biologiques d'exposition de l'ACGIH).
En juin 2007, un atelier d'experts sur les équivalents de biosurveillance s'est tenu en présence d'un éventail d'experts internationaux du domaine de la pharmacocinétique, de l'évaluation des risques, de la médecine du travail et de la communication relative aux risques en vue d'élaborer des lignes directrices pour le calcul et la communication des EB (Hays et al., 2008a; LaKind et al., 2008). La plupart des EB calculés par Santé Canada ont été soumis à deux rondes d'examen indépendant par des pairs.
Le premier examen par les pairs a été entrepris pour répondre aux questions suivantes :
- Les EB respectent-ils les principes des lignes directrices relatives au calcul des équivalents de biosurveillance (Guidelines for the Derivation of Biomonitoring Equivalents) énoncés dans Hays et al. (2008a)?
- Les documents de communication relatifs aux EB respectent-ils les principes des lignes directrices sur la communication des EB (Guidelines for communication of BEs) énoncés dans LaKind et al. (2008)?
- Est-ce que la modélisation propre à une substance chimique sur laquelle repose chaque EB correspond aux meilleurs données et pratiques possibles ou est fondée sur celles-ci?
Ces examens par les pairs ont été réalisés par des experts choisis de manière indépendante, dont au moins une personne faisant partie du comité qui a élaboré les lignes directrices relatives au calcul et à la communication des EB et une autre qui est un expert reconnu du profil pharmacocinétique de la substance chimique d'intérêt. La deuxième ronde d'examen indépendant par les pairs a été effectuée par la revue dans laquelle chaque manuscrit d'EB est publié.
Les EBNote de bas de page 2 mis au point pour soutenir les évaluations de Santé Canada ont également fait l'objet d'un examen par les pairs fondé sur l'indépendance, la transparence, une expertise appropriée et un processus rigoureux. Ces principes et pratiques évoluent à la lumière de l'expérience acquise dans la gestion des commentaires des pairs sur divers aspects d'un vaste programme de réglementation de Santé Canada (c.-à-d. les substances existantes) en consultation avec d'importants partenaires du domaine. Pour ces EB, on a demandé aux examinateurs de dresser une liste de questions dans le cadre de l'examen (annexe B).
Au fur et à mesure de leur mise au point, les EB continuent de faire l'objet d'un examen interne par les pairs de Santé Canada avant d'être examinés par les pairs de la revue.
6. Application des EB
Outils d'évaluation pour l'interprétation des données de biosurveillance dans un context de risque
Les EB conjugués aux données de biosurveillance offrent un outil d'évaluation qui aide à déterminer si les expositions actuelles à des contaminants de l'environnement s'approchent des niveaux tolérables pour la population générale ou les dépassent (figure 7). Cet outil peut contribuer à établir des priorités en matière d'évaluation et de gestion des risques liés aux contaminants de l'environnement par Santé Canada.
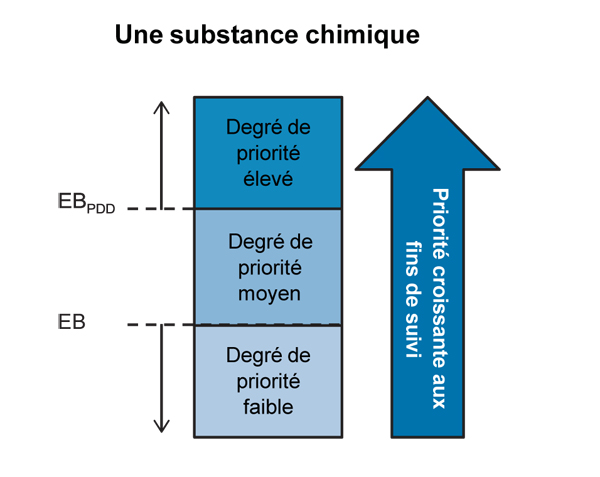
Figure 7. Scénario de priorisation pour l'interprétation de données de biosurveillance fondées sur des valeurs d'EB (adaptation de LaKind et al., 2008)
Équivalent textuel
Ce diagramme illustre le scénario de priorisation pour l’interprétation de données de biosurveillance fondées sur des valeurs d’EB pour une seule substance chimique. Les boîtes Degré de priorité élevé, Degré de priorité moyen et Degré de priorité faibe sont illustrées de haut en bas. L’EB se trouve au point de jonction entre les boîtes Degré de priorité moyen et Degré de priorité faible, et l’EBPDD, au point de jonction entre les boîtes Degré de priorité élevé et Degré de priorité moyen. Une flèche pointant vers le haut et portant la mention « Priorité croissante aux fins de suivi » figure à droite de ces boîtes, établissant la priorité de la plus faible à la plus élevée.
Outre la comparaison directe des données de biosurveillance aux valeurs d'EB, d'autres approches peuvent être utilisées pour comparer ces données. Dans le cadre d'une évaluation des risques classique, les estimations des niveaux d'exposition exprimés en mg/kg-d ou en mg/m3 sont comparées aux niveaux d'exposition tolérables comme la dose de référence ou la dose journalière admissible. Cette comparaison peut consister en un calcul d'un quotient de danger (QD), défini comme étant le ratio de la dose estimée à la valeur guide d'exposition. Selon ce cadre, les valeurs de QD inférieures à 1 indiquent que les expositions estimées ne dépassent pas la dose admissible. Dans les cas où les valeurs de QD approchent ou dépassent 1, les expositions mesurées s'approchent des doses admissibles ou les dépassent et il faut envisager d'autres mesures, notamment une amélioration de l'évaluation, de l'atténuation ou de la gestion des risques.
Il est possible de recourir à des approches similaires pour comparer les données de biosurveillance aux valeurs d'EB. Un exercice d'évaluation peut être effectué dans l'ensemble des substances chimiques mesurées dans le cadre de l'ECMS. Un classement relatif des quotients de danger (QD) peut indiquer quelles substances doivent être considérées comme une priorité en vue d'une évaluation approfondie ou lesquelles ont besoin de recherche supplémentaire (St-Amand et al., 2014).
Le QD peut correspondre au rapport entre la concentration de biomarqueurs provenant de la moyenne géométrique au 95e percentile et la valeur d'EB propre à une substance chimique. Il est également possible de l'exprimer à l'inverse, c'est-à-dire le rapport entre une valeur d'EB et les concentrations de biomarqueurs provenant de la moyenne géométrique au 95e percentile.
Les valeurs d'EB peuvent servir à évaluer des données de biosurveillance dans un contexte de risque pour la santé pour aider à évaluer quelles substances chimiques sont présentes à des concentrations relativement faibles par rapport aux valeurs d'EB (valeurs de QD plus faibles). Cette approche est analogue à la façon dont les valeurs guides d'exposition sous-jacentes (notamment les lignes directrices sur l'apport alimentaire admissible, les recommandations relatives à l'eau potable ou les recommandations pour la qualité des sols) sont utilisées pour évaluer les estimations externes des expositions. L'interprétation du dépassement d'un EB est également similaire à l'interprétation du dépassement d'une valeur guide d'exposition. Le dépassement d'une valeur guide d'exposition réduit la marge de sécurité intégrée à la recommandation, mais n'entraîne pas forcément un risque appréciable pour la santé des Canadiens. Les EB constituent un outil d'évaluation et non un niveau d'intervention.
À l'issue de la comparaison des données de biosurveillance aux EB, les dépassements devraient donner lieu à une enquête approfondie par le Ministère en vue de déterminer si une substance chimique donnée doit faire l'objet, en priorité, d'une évaluation ou d'une gestion des risques approfondie. Les mesures à prendre pourraient inclure une révision des publications, des analyses de données approfondies ou l'élaboration de valeurs guides fondées sur les tissus.
7. Avantages and Limites
7.1 Avantages des EB comme outil d'évaluation
Les EB se veulent un outil d'évaluation qui permet de mettre en contexte des données de biosurveillance dans un cadre de risque pour la santé. Ils permettent de comparer les concentrations de biomarqueurs observées dans le sang ou l'urine des humains aux recommandations en matière de santé visant les doses jugées « sûres » ou « acceptables ». Ils fournissent de l'information qui permet de prioriser les substances en matière d'évaluation et de gestion des risques. Par contre, leur recours n'empêche pas la mise au point ni l'utilisation d'autres outils complémentaires pour interpréter des données de biosurveillance.
Les EB tirent parti des évaluations de risque existantes par le recours à des PDD toxicologiques et à des facteurs d'incertitude préalablement déterminés, misant ainsi sur des travaux déjà réalisés. Si une évaluation des risques est mise à jour (par exemple, si on cerne un critère d'effet différent), il est relativement facile de mettre à jour un EB. Pour de nombreuses substances chimiques pour lesquelles des EB ont été mis au point, plusieurs valeurs de référence ont été examinées en parallèle, ce qui a mené à un EB pour chacune de ces valeurs. Contrairement aux approches pour lesquelles des estimations classiques d'exposition sont utilisées pour calculer des concentrations tissulaires prévues ou pour lesquelles un ensemble de données de biosurveillance est utilisé pour estimer la dose, un EB représente une valeur de référence unique qu'on peut comparer à de multiples ensembles de données de biosurveillance. On évite ainsi de répéter le processus de calcul et d'analyse pour chaque scénario d'exposition ou chaque ensemble de données de biosurveillance.
L'approche des EB a été mise au point avec la participation d'un groupe d'experts dans divers domaines, qui ont discuté de nombreux aspects de l'établissement des EB dans le cadre de l'atelier tenu en 2007 (Hays et al., 2008a). Chacun des EB calculés jusqu'à maintenant a fait l'objet d'un examen par les pairs avant d'être publié dans des revues scientifiques. Les EB mis au point dans le cadre du contrat de Santé Canada ont aussi été examinés par les pairs dans le contexte du respect des lignes directrices relatives au calcul des EB. Le processus d'établissement des EB est donc fondé sur des données scientifiques, il est rigoureux et a l'appui du milieu scientifique.
7.2 Les limites des EB comme outil d'évaluation
Les EB s'appliquent uniquement à l'échelle de la population et non à l'échelle des individus. Ils seront pertinents pour la population dans laquelle le ou les analytes ont été recueillis, et il faut considérer avec prudence l'utilisation d'un EB comme outil d'évaluation pour d'autres populations. Par exemple, en raison du peu de données recueillies auprès de jeunes enfants de moins de 6 ans dans l'ECMS (en ce qui concerne les propriétés cinétiques, les volumes d'urine et l'excrétion de la créatinine), les analytes urinaires n'ont pu être mesurés chez les enfants de 3 à 5 ans; les EB pour ces substances chimiques ne peuvent donc s'appliquer à cette souspopulation. Les EB ne sont pas censés être utilisés comme critères de diagnostic pour l'évaluation du risque d'effets nocifs pour la santé. Ils représentent plutôt une valeur préliminaire des mesures de la biosurveillance qui est basée sur une valeur de référence déterminée au préalable. Comme les EB sont liés à des valeurs de référence existantes, toutes les hypothèses et les incertitudes associées à la valeur de référence sous-jacente s'appliquent également à l'EB. L'EB correspond au critère d'effet toxicologique choisi pour le calcul de la valeur de référence; même si des critères d'effet toxicologique plus pertinents ou plus sensibles sont déterminés après le calcul de la valeur de référence, ils ne sont pas intégrés au calcul de l'EB. De même, comme les doses de référence, les doses journalières admissibles et d'autres critères peuvent s'appliquer à une seule substance, à partir d'une seule voie d'exposition, l'EB associé représente également une concentration propre à la substance, sans égard à l'exposition globale ou cumulative (c.-à-d. de multiples substances chimiques comportant des voies ou des modes d'action de toxicité similaires).
Par définition, la mise au point d'un EB pour une substance chimique en particulier exige qu'une ligne directrice en matière d'exposition comme une dose journalière admissible ou une dose de référence établie par un organisme de réglementation existe pour cette substance chimique. Malheureusement, pour de nombreuses substances d'intérêt dans les études de biosurveillance, dont l'ECMS, de telles lignes directrices n'existent pas. Si on ne tient compte que des substances assujetties aux lignes directrices de Santé Canada en matière d'exposition, le nombre d'EB possibles est réduit davantage. Dans certains cas, un EB fondé sur une valeur guide établie par une compétence autre que Santé Canada peut être approprié; toutefois, cette situation devrait être évaluée au cas par cas avant que le Ministère n'utilise cette donnée comme outil d'évaluation. En outre, de nombreux programmes d'évaluation préliminaire à Santé Canada établissent des concentrations associées à un effet critique pour l'évaluation des risques, mais aucune dose journalière admissible n'est établie. Des mécanismes permettant d'intégrer ces concentrations associées à un effet critique à des EB provisoires ont été étudiés (Aylward et Hays, 2011; Hays et al., 2014), et l'interprétation des données de biosurveillance pour des substances chimiques ne disposant pas de valeurs guides établies en fonction d'une marge d'exposition (EBPDD [ou PDD chez l'animal]/concentration du biomarqueur) a été décrite (Becker et al., 2012).
Les EB comportent deux sources fondamentales d'incertitude : la connaissance de la pharmacocinétique propre à une substance chimique et les caractéristiques du biomarqueur comme mesure ou représentant de l'exposition externe d'intérêt.
7.2.1 Incertitudes pharmacocinétiques
La disponibilité et la fiabilité des données pharmacocinétiques limitent la mise au point d'un EB. Sans une certaine connaissance de la relation entre la dose externe, la dose interne et le mode d'action de la toxicité, il est impossible d'établir un EB avec certitude. Même s'il existe suffisamment de données pour calculer les EB de contaminants de l'environnement bien connus (p. ex. polluants organiques persistants, ignifugeants, pesticides), pour d'autres contaminants émergents, il se peut qu'il y ait peu de données sur la pharmacocinétique et le mode d'action de la toxicité. Même dans le cas des substances chimiques pour lesquelles la pharmacocinétique et le mode d'action de la toxicité sont relativement bien comprises, il subsiste une incertitude quant à la valeur d'EB, et cette incertitude doit être reconnue et caractérisée lorsqu'on applique l'EB comme examen préalable.
Le calcul des valeurs d'EB fait appel à un jugement explicite en ce qui concerne la confiance dans la base de données de pharmacocinétique et la classification qualitative de la confiance dans l'EB, soit faible, moyenne ou élevée. Étant donné que l'interprétation des données de biosurveillance chez l'humain à l'aide de ces EB se veut un exercice de présélection pour aider à prioriser les substances chimiques en vue d'une évaluation approfondie, le fait que les données pharmacocinétiques utilisées pour établir des EB présentent une certaine incertitude ne les empêche pas d'être utiles. Si un composé présentant un faible niveau de confiance dans les approches pharmacocinétiques comporte un QD élevé, certains secteurs de programme devraient enquêter davantage.
7.2.2 Fiabilité des biomarqueurs
Pour qu'un EB soit utile en tant qu'outil d'évaluation, les méthodes d'analyse et les biomarqueurs utilisés dans l'étude de biosurveillance doivent être comparables à ceux pris en compte dans le calcul des EB. À titre d'exemple, si un EB est fondée sur un métabolite conjugué, la méthode doit être en mesure de séparer les formes libres et conjuguées de ce métabolite et de consigner les résultats séparément; de même, si l'EB fait référence à plusieurs métabolites ou formes différenciées, la méthode doit permettre de quantifier chacune de ces substances et de consigner les résultats séparément.
Pour diverses raisons (y compris l'échantillonnage non invasif, la disponibilité de biomarqueurs, la demi-vie plasmatique courte), bon nombre d'EB ont été établis jusqu'à maintenant sur la base de métabolites urinaires. Ces EB comportent leur propre lot de problèmes et de limites, dont plusieurs sont décrits en détail dans la publication sur le calcul de l'EB pour le DEHP (Aylward et al., 2009b). Par exemple, dans le cas de métabolites ayant une demi-vie urinaire courte, les échantillons ponctuels (comme dans l'ECMS) ne reflètent pas nécessairement une exposition continue et pourraient surreprésenter ou sous-représenter l'exposition réelle « à l'état d'équilibre ». Ainsi, sans connaissance du moment et du degré d'exposition, l'utilité de l'EB est limitée. Par conséquent, pour ces EB, les comparaisons ne devraient être faites qu'avec des mesures de tendance centrale (c.-à-d. la moyenne géométrique), plutôt qu'avec les queues de la distribution de la population.
Un autre problème lié à la fiabilité des biomarqueurs est la spécificité du biomarqueur. Dans la plupart des cas, les analytes inclus dans l'ECMS et d'autres programmes nationaux de biosurveillance sont propres à l'exposition à une substance chimique en particulier. Il existe toutefois quelques exceptions. Dans le domaine des pesticides, des analytes urinaires qui sont des métabolites du composé d'origine peuvent découler, dans certains cas, d'une exposition directe à ce métabolite présent dans les aliments ou l'environnement comme produit de dégradation dans l'environnement du composé d'origine. Le 3,5,6-trichloro-2-pyridinol (TCPy), par exemple, est un métabolite spécifique et le produit de dégradation dans l'environnement du chlorpyrifos. Le TCPy urinaire a d'abord été interprété comme un marqueur précis de l'exposition au chlorpyrifos. Toutefois, des analyses d'aliments et de milieux naturels démontrent que la plus grande partie du TCPy urinaire chez l'humain dans la population générale découle probablement d'une exposition directe au TCPy, qui est relativement non toxique. Des données semblent indiquer que le TCPy est absorbé et excrété dans l'urine humaine sans transformation (Morgan et al., 2011; Timchalk et al., 2007). Ainsi, les concentrations de TCPy dans l'urine ne sont pas nécessairement significatives comme marqueur de l'exposition au chlorpyrifos. Il est important de tenir compte de la solidité du biomarqueur comme mesure de l'exposition au composé d'origine lors d'une évaluation détaillée des données de biosurveillance.
En général, le calcul des valeurs d'EB fondées sur des doses journalières admissibles repose sur l'hypothèse qu'un équilibre entre la dose et la concentration/excrétion (c.-à-d. l'état d'équilibre) a été atteint dans la matrice biologique. À cet égard, les valeurs d'EB sont des estimations qui correspondent aux valeurs théoriques de dose chronique admissible qui sous-tendent le calcul, plutôt qu'une tentative d'estimer les doses réelles ou de prédire les concentrations de biomarqueurs découlant des conditions d'exposition réelles, qui sont susceptibles d'être variables et intermittentes. Dans le monde réel, l'exposition à des substances chimiques n'est pas continue; il est probable qu'elle varie au cours d'une journée et d'une journée à l'autre. Un tel écart entre les hypothèses utilisées dans l'établissement des valeurs d'EB et les profils d'exposition dans le monde réel se traduit par la nécessité de faire preuve de prudence lors de l'interprétation des données de biosurveillance.
7.3 Questions liées aux communications
Grâce aux données provenant des cycle 1 (2007–2009), cycle 2 (2009–2011) et cycle 3 (2012–2013) de l'ECMS publiées entre 2010 et 2015 et aux données provenant des cycles 4 à 6 (2014–2019) qui suivront, Santé Canada pourrait se concentrer sur l'identification et la mise en œuvre d'outils pour mettre en contexte les données de l'ECMS en ce qui concerne le risque pour la santé. Les EB ne représentent pas un point décisif entre des concentrations « sûres » et « dangereuses », ne doivent pas être utilisés comme niveaux d'intervention ou d'action, et ne doivent pas servir à établir des comparaisons avec des concentrations de biosurveillance à l'échelle des individus; les EB sont plutôt conçus pour être utilisés comme valeurs préliminaires, pour permettre de comprendre comment l'exposition dans la population générale se compare à une ligne directrice d'exposition fondée sur la santé.
Lorsqu'on utilise les EB comme outil d'évaluation, il faut inclure les incertitudes et la confiance associées à l'EB et aux données de biosurveillance.
Les EB peuvent être utilisés dans d'autres contextes (p. ex. évaluation de risques) et il incombe à l'auteur de définir les EB et leurs limites dans le contexte où ils seront utilisés.
8. Perspective internationale
Les EB ne sont pas un concept nouveau, mais leur calcul dans le contexte des contaminants de la santé environnementale a été élaboré pour la première fois dans les années 2000. Même si peu d'organismes de réglementation les utilisent maintenant, on s'y intéresse de plus en plus. Il existe un potentiel de collaboration internationale dans ce domaine, et Santé Canada pourrait y jouer un rôle important puisque peu de pays possèdent un programme de biosurveillance aussi vaste comme l'ECMS et autant d'expérience pour établir et appliquer des EB.
La Commission allemande de biosurveillance humaine a défini des valeurs de biosurveillance humaines (human biomonitoring values ou valeurs HBM) [en anglais] pour le cadmium, le mercure, le thallium, le pentachlorophénol, les métabolites du DEHP, les biphényles polychlorés (BPC) et le BPA [en anglais]. Il existe deux types de valeurs HBM : la valeur HBM-I, considérée comme une valeur de vérification, et la HBM-II, qui est un niveau d'action. Pour toutes les substances, sauf le DEHP et le BPA, les valeurs HBM ont été déterminées selon des études adéquates sur les effets pour la santé humaine. En théorie, les valeurs HBM-I et les EB sont identiques. Les valeurs de biomarqueurs inférieures aux HBM-I sont considérées comme des concentrations en-dessous desquelles il n'y aurait pas de risque d'effets nocifs pour la santé et elles correspondent donc à la définition de la valeur d'EB et aux définitions de doses journalières. Toutefois, les valeurs HBM-II de la Commission allemande de biosurveillance humaine sont explicitement définies du point de vue de l'interprétation des données de biosurveillance individuelles et représentent des concentrations qui, si elles sont dépassées, seraient susceptibles de causer des effets nocifs pour la santé qui doivent être considérées comme pertinentes pour la personne touchée, et qui sont par conséquent plus similaires aux lignes directrices de Santé Canada relatives à la concentration de mercure dans le sang. La Commission envisage d'utiliser les EB comme valeurs HBM-I pour d'autres substances (Angerer et al., 2011).
Dans l'ensemble, l'analyse par les Centers for Disease Control and Prevention (CDC) des résultats de biosurveillance provenant de l'enquête NHANES est axée sur l'approche descriptive, qui crée des valeurs de référence au 95e percentile (CDC, 2009). En général, le message des CDC sur les données de biosurveillance, c'est que la mesure d'une substance chimique dans le sang ou l'urine ne signifie pas que cette substance cause la maladie. Des avancées réalisées dans les méthodes d'analyse permettent de mesurer de faibles concentrations de substances chimiques présentes dans l'environnement chez les personnes, mais des études distinctes portant sur des concentrations d'exposition et des effets sur la santé qui varient sont nécessaires pour déterminer si ces concentrations dans le sang ou dans l'urine provoquent des maladies. Pour la plupart des substances chimiques de l'environnement (autres que le plomb), il faut poursuivre les recherches pour évaluer les risques pour la santé provenant de différentes concentrations sanguines ou urinaires (CDC, 2009). Les CDC n'ont pas officiellement approuvé l'utilisation d'EB comme outil d'évaluation des données de biosurveillance.
On a communiqué avec les cadres supérieurs des bureaux de programmes au sein de l'EPA des États-Unis pour savoir dans quelle mesure les EB ou les considérations sur lesquelles ils reposent sont actuellement intégrés à la prise de décision visant à établir des priorités pour l'évaluation des risques. Ces bureaux comprennent l'Office of Pollution Prevention and Toxics, l'Office of Pesticide Programs et l'Office of Water. Essentiellement, la plupart des programmes adoptent les concepts et les principes sur lesquels sont basés les EB (c.-à-d. réduire l'incertitude par l'intégration, dans la mesure du possible, d'approches de plus en plus fondées sur des données qui intègrent des renseignements toxicocinétiques et toxicodynamiques), mais il reste encore à approuver officiellement ou à utiliser les EB en tant que tels dans leurs programmes (Meek, 2012).
En Europe, le règlement REACH (pour Registration, Evaluation, Authorisation and Restriction of Chemical substances – enregistrement, évaluation, autorisation et restriction des substances chimiques) est un règlement de l'Union européenne qui est entré en vigueur en 2007. Ce règlement porte sur la production et l'utilisation de substances chimiques, ainsi que sur les répercussions possibles sur la santé humaine et l'environnement. REACH exige la caractérisation des risques que présentent les substances chimiques par leur exposition dans l'environnement. Au moins deux publications rédigées par l'industrie examinent la façon dont les EB pourraient s'appliquer pour interpréter les données de biosurveillance en vue de caractériser le risque pour la santé aux termes du règlement REACH (Boogaard et al. 2012, Boogaard et al. 2011).
En France, l'Agence nationale de sécurité sanitaire de l'alimentation, de l'environnement et du travail (ANSES) examine aussi divers moyens pour interpréter les données de biosurveillance comme les résultats d'enquêtes de biosurveillance en cours effectuées au pays (ANSES 2014).
9. Références
- Angerer J, Aylward LL, Hays SM, Heinzow B, and Wilhelm M. (2011). Human biomonitoring assessment values: Approaches and data requirements. International Journal of Hygiene and Environmental Health, 214(5), 348–360.
- ANSES (alimentation, environnement, travail). (2014). Orientations de l'Anses dans le domaine de la santé environnment pour 2014. Accessible à l'adresse : www.anses.fr/fr/system/files/ANSES-Ft-OrientStrat2014-SantEnv.pdf.
- Arnold SM, Morriss A, Velovitch J, Juberg D, Burns CJ, Bartels M, Aggarwal M, Poet T, Hays S, and Price P. (2015). Derivation of human biomonitoring guidance values for chlorpyrifos using a physiologically based pharmacokinetic and pharmacodynamic model of cholinesterase inhibition. Regulatory Toxicology and Pharmacology, 71(2), 235–243.
- Aylward LL, and Hays SM. (2008). Biomonitoring equivalents (BE) dossier for 2,4-dichlorophenoxyacetic acid (2,4-D) (CAS no. 94–75–7). Regulatory Toxicology and Pharmacology, 51(3 SUPPL.), S37–S48.
- Aylward LL, LaKind JS, and Hays SM. (2008a). Biomonitoring equivalents (BE) dossier for trihalomethanes. Regulatory Toxicology and Pharmacology, 51(3 SUPPL.), S68–S77.
- Aylward LL, Barton HA, and Hays SM. (2008b). Biomonitoring equivalents (BE) dossier for toluene (CAS no. 108–88–3). Regulatory Toxicology and Pharmacology, 51(3 SUPPL.), S27–S36.
- Aylward LL, LaKind JS, and Hays SM. (2008c). Derivation of biomonitoring equivalent (BE) values for 2,3,7,8-tetrachlorodibenzo-p-dioxin (TCDD) and related compounds: A screening tool for interpretation of biomonitoring data in a risk assessment context. Journal of Toxicology and Environmental Health—Part A: Current Issues, 71(22), 1499–1508.
- Aylward LL, Hays SM, Gagné M, and Krishnan K. (2009a). Derivation of biomonitoring equivalents for di(2-ethylhexyl) phthalate (CAS no. 117–81–7). Regulatory Toxicology and Pharmacology, 55(3), 249–258.
- Aylward LL, Hays SM, Gagné M, and Krishnan K. (2009b). Derivation of biomonitoring equivalents for di-n-butyl phthalate (DBP), benzylbutyl phthalate (BzBP), and diethyl phthalate (DEP). Regulatory Toxicology and Pharmacology, 55(3), 259–267.
- Aylward LL, Kirman CR, Blount BC, and Hays SM. (2010a). Chemical-specific screening criteria for interpretation of biomonitoring data for volatile organic compounds (VOCs)—application of steady-state PBPK model solutions. Regulatory Toxicology and Pharmacology, 58(1), 33–44.
- Aylward LL, Hays SM, Gagné M, Nong A, and Krishnan K. (2010b). Biomonitoring equivalents for hexachlorobenzene. Regulatory Toxicology and Pharmacology, 58(1), 25–32.
- Aylward LL, Morgan MK, Arbuckle TE, Barr DB, Burns CJ, Alexander BH, and Hays SM. (2010c). Biomonitoring data for 2,4-dichlorophenoxyacetic acid in the United States and Canada: Interpretation in a public health risk assessment context using biomonitoring equivalents. Environmental Health Perspectives, 118(2), 177–181.
- Aylward LL, and Hays SM. (2011). Biomonitoring-based risk assessment for hexabromocyclododecane (HBCD). International Journal of Hygiene and Environmental Health, 214(3), 179–187.
- Aylward LL, Krishnan K, Kirman CR, Nong A, and Hays SM. (2011). Biomonitoring equivalents for deltamethrin. Regulatory Toxicology and Pharmacology, 60(2), 189–199.
- Aylward LL, and Hays SM. (2012). Interpretation of Biomonitoring Data from the Canadian Health Measure Survey in a risk Assessment context: Use of biomonitoring Equivalents. Rapport préparé conformément au numéro de contrat 4500278933 de Santé Canada.
- Aylward LL, Kirman CR, Schoeny R, Portier CJ, and Hays SM. (2013). Evaluation of biomonitoring data from the CDC national exposure report in a risk assessment context: Perspectives across chemicals. Environmental Health Perspectives, 121(3), 287–294.
- Aylward LL, Hays SM, Vezina A, Deveau M, St-Amand A, and Nong A. (2015). Biomonitoring equivalents for interpretation of urinary fluoride. Regulatory Toxicology and Pharmacology, 72(1), 158–167.
- Becker RA, Hays SM, Robison S, and Aylward LL. (2012). Development of screening tools for the interpretation of chemical biomonitoring data. Journal of Toxicology, 2012, ID de l'article 941082.
- Boogaard PJ, Hays SM, and Aylward LL. (2011). Human biomonitoring as a pragmatic tool to support health risk management of chemicals—examples under the EU REACH programme. Regulatory Toxicology and Pharmacology, 59(1), 125–132.
- Boogaard PJ, Aylward LL, and Hays SM. (2012). Application of human biomonitoring (HBM) of chemical exposure in the characterisation of health risks under REACH. International Journal of Hygiene and Environmental Health, 215(2), 238–241.
- CDC (Centers for Disease Control and Prevention). 2009. Fourth National Report on Human Exposure to Environmental Chemicals. Atlanta (GA).
- Hays SM, Becker RA, Leung HW, Aylward LL, and Pyatt DW. (2007). Biomonitoring equivalents: A screening approach for interpreting biomonitoring results from a public health risk perspective. Regulatory Toxicology and Pharmacology, 47(1), 96–109.
- Hays SM, and Aylward LL. (2008). Biomonitoring equivalents (BE) dossier for acrylamide (AA) (CAS no. 79–06–1). Regulatory Toxicology and Pharmacology, 51(3 SUPPL.), S57–S67.
- Hays SM, Aylward LL, LaKind JS, Bartels MJ, Barton HA, Boogaard PJ, Brunk C, DiZio S, Dourson M, Goldstein DA, Lipscomb J, Kilpatrick ME, Krewski D, Krishnan K, Nordberg M, Okino M, Tan Y-M, Viau C, and Yager JW. (2008a). Guidelines for the derivation of biomonitoring equivalents: Report from the biomonitoring equivalents expert workshop. Regulatory Toxicology and Pharmacology, 51(3 SUPPL.), S4–S15.
- Hays SM, Nordberg M, Yager JW, and Aylward LL. (2008b). Biomonitoring equivalents (BE) dossier for cadmium (Cd) (CAS no. 7440–43–9). Regulatory Toxicology and Pharmacology, 51(3 SUPPL.), S49–S56.
- Hays SM, Aylward LL, Gagné M, and Krishnan K. (2009). Derivation of biomonitoring equivalents for cyfluthrin. Regulatory Toxicology and Pharmacology, 55(3), 268–275.
- Hays SM, Aylward LL, Gagné M, Nong A, and Krishnan K. (2010). Biomonitoring equivalents for inorganic arsenic. Regulatory Toxicology and Pharmacology, 58(1), 1–9.
- Hays SM, Aylward LL, Kirman CR, Krishnan K, and Nong A. (2011). Biomonitoring equivalents for di-isononyl phthalate (DINP). Regulatory Toxicology and Pharmacology, 60(2), 181–188.
- Hays SM, Pyatt DW, Kirman CR, and Aylward LL. (2012). Biomonitoring equivalents for benzene. Regulatory Toxicology and Pharmacology, 62(1), 62–73.
- Hays SM, Macey K, Nong A, and Aylward LL. (2014). Biomonitoring equivalents for selenium. Regulatory Toxicology and Pharmacology, 70(1), 333–339.
- HBM (Human Biomonitoring) Commission. (2011). Stoffmonographie Thallium-Referenz- und Human-Biomonitoring-(HBM)- Werte für Thallium im Urin. Bundesgesundheitsbl. Gesundheitsforsch. Gesundheitsschutz 54, 516–524. (Tel que cite dans Schulz et al., 2012)
- Kirman CR, Aylward LL, Hays SM, Krishnan K, and Nong A. (2011). Biomonitoring equivalents for DDT/DDE. Regulatory Toxicology and Pharmacology, 60(2), 172–180.
- Kirman CR, Aylward LL, Blount BC, Pyatt DW, and Hays SM. (2012). Evaluation of NHANES biomonitoring data for volatile organic chemicals in blood: Application of chemical-specific screening criteria. Journal of Exposure Science and Environmental Epidemiology, 22(1), 24–34.
- Krishnan K, Gagné M, Nong A, Aylward LL, and Hays SM. (2010a). Biomonitoring equivalents for triclosan. Regulatory Toxicology and Pharmacology, 58(1), 10–17.
- Krishnan K, Gagné M, Nong A, Aylward LL, and Hays SM. (2010b). Biomonitoring equivalents for bisphenol A (BPA). Regulatory Toxicology and Pharmacology, 58(1), 18–24.
- Krishnan K, Adamou T, Aylward LL, Hays SM, Kirman CR, and Nong A. (2011). Biomonitoring equivalents for 2,2',4,4',5-pentabromodiphenylether (PBDE-99). Regulatory Toxicology and Pharmacology, 60(2), 165–171.
- LaKind JS, Aylward LL, Brunk C, DiZio S, Dourson M, Goldstein DA, Kilpatrick ME, Krewski D, Bartels MJ, Barton HA, Boogaard PJ, Lipscomb J, Krishnan K, Nordberg M, Okino M, Tan Y-M, Viau C, Yager JW, and Hays SM. (2008). Guidelines for the communication of biomonitoring equivalents: Report from the biomonitoring equivalents expert workshop. Regulatory Toxicology and Pharmacology, 51(3 SUPPL.), S16–S26.
- Meek B. (2012). Centre McLaughlin d'évaluation du risque pour la santé des populations, Université d'Ottawa / McLaughlin Centre for Population Health Risk Assessment, University of Ottawa. Le 30 mars, 2012. Relevance of Biomonitoring Equivalents to Health Canada Chemical Risk Assessment Programs Rapport préparé conformément au numéro de contrat 4500279187 de Santé Canada.
- Morgan, M.K., Sheldon, L.S., Jones, P.A., Croghan, C.W., Chuang, J.C., and Wilson, N.K. (2011). The reliability of using urinary biomarkers to estimate children's exposures to chlorpyrifos and diazinon. Journal of Exposure Science and Environmental Epidemiology, 21(3), 280–290.
- NRC (National Research Council). (2006). Human Biomonitoring for Environmental Chemicals. Washington, DC: National Academies Press.
- NRC (National Research Council). (2007). Toxicity Testing in the 21st Century: A Vision and a Strategy. Washington, DC: National Academies Press.
- Schulz C, and Butte W. (2007). Revised reference value for pentachlorophenol in morning urine. International Journal of Hygiene and Environmental Health, 210(6), 741–744.
- Schulz C, Wilhelm M, Heudorf U, and Kolossa-Gehring M. (2012). Réimpression du document intitulé “Update of the reference and HBM values derived by the German Human Biomonitoring Commission”. International Journal of Hygiene and Environmental Health, 215(2), 150–158.
- St-Amand A, Werry K, Aylward LL, Hays SM, and Nong A. (2014). Screening of population level biomonitoring data from the Canadian health measures survey in a risk-based context. Toxicology Letters, 231(2), 126–134.
- Timchalk C, Busby A, Campbell JA, Needham LL, and Barr DB. (2007). Comparative pharmacokinetics of the organophosphorus insecticide chlorpyrifos and its major metabolites diethylphosphate, diethylthiophosphate and 3,5,6-trichloro-2-pyridinol in the rat. Toxicology, 237(1–3), 145–157.
Annexe A – Résumé des EB calculés
| Substance chimique | Référence |
|---|---|
| Acrylamide | |
| Acrylamide | Hays et Aylward, 2008 |
| Chlorophénols | |
| Pentachlorophénol | Schulz et Butte, 2007 |
| Dioxines et furanes | |
| EQT des dioxines | Aylward et al., 2008c |
| Phénols dans l'environnement | |
| Bisphénol ANote de bas de page 1Note de bas de page 2 | Krishnan et al., 2010b |
| TriclosanNote de bas de page 2 | Krishnan et al., 2010a |
| Ignifugeants | |
| HexabromocyclododécaneNote de bas de page 1Note de bas de page 3 | Aylward et Hays, 2011 |
| PBDE-99Note de bas de page 2 | Krishnan et al., 2011 |
| Métaux et éléments à l'état de trace | |
| ArsenicNote de bas de page 1Note de bas de page 2 | Hays et al., 2010 |
| AntimoineNote de bas de page 2 | En cours d'élaboration |
| BoreNote de bas de page 2 | En cours d'élaboration |
| FluorureNote de bas de page 1Note de bas de page 2 | Aylward et al., 2015 |
| ManganèseNote de bas de page 2 | En cours d'élaboration |
| NickelNote de bas de page 2 | En cours d'élaboration |
| SéléniumNote de bas de page 2 | Hays et al., 2014 |
| Thallium | HBM 2011 |
| UraniumNote de bas de page 2 | En cours d'élaboration |
| Cadmium | Hays et al., 2008b |
| Composés organochlorés | |
| DDT/DDENote de bas de page 1Note de bas de page 2 | Kirman et al., 2011 |
| HexachlorobenzèneNote de bas de page 1Note de bas de page 2 | Aylward et al., 2010b |
| Pesticides | |
| CyfluthrineNote de bas de page 1Note de bas de page 2 | Hays et al., 2009 |
| Deltaméthrine | Aylward et al., 2011 |
| Acide 3-phénoxybenzoïqueNote de bas de page 2Note de bas de page 3 | En cours d'élaboration |
| Chlorpyrifos | Arnold et al., 2015 |
| Malathion | En cours d'élaboration |
| Acide 2,4dichlorophénoxyacétique (2,4-D) | Aylward et Hays, 2008 |
| Phtalates | |
| Phtalate de di(2éthylhexyle)Note de bas de page 1Note de bas de page 2 | Aylward et al., 2009b |
| Phtalate de diisononyleNote de bas de page 1Note de bas de page 2 | Hays et al., 2011 |
| Phtalate de dibutyleNote de bas de page 1Note de bas de page 2 | Aylward et al., 2009a |
| Phtalate de diéthyleNote de bas de page 1Note de bas de page 2 | Aylward et al., 2009a |
| Phtalate de benzyle et de butyleNote de bas de page 1Note de bas de page 2 | Aylward et al., 2009a |
| Phtalate de diisobutyleNote de bas de page 2 | En cours d'élaboration |
| Phtalate de diisodécyleNote de bas de page 2Note de bas de page 3 | En cours d'élaboration |
| Phtalate de dicyclohexyleNote de bas de page 2Note de bas de page 3 | En cours d'élaboration |
| Composés organiques volatils (COV) | |
| Benzène | Hays et al., 2012 |
| Toluène | Aylward et al., 2008b |
| Trihalométhanes : chloroforme, bromoforme, bromodichlorométhane, dibromochlorométhane | Aylward et al., 2008a |
| Autres COV | Aylward et al., 2010c |
Remarque :
|
|
| Présente dans l'environnement | Cycle de l'ECMS | |||
|---|---|---|---|---|
| 1 (2007–2009) |
2 (2009–2011) |
3 et 4 (2012–2015) |
5 et 6 (2016–2019) |
|
| Acrylamide | ||||
| Acrylamide | Aucune donnée disponible | Aucune donnée disponible | ■ | ■ |
| Dioxines et furanes | ||||
| Dioxines et furanes | ■ | Aucune donnée disponible | ■ | ■ |
| Phénols dans l'environnement | ||||
| Bisphénol A | ■ | ■ | ■ | ■ |
| Triclosan | Aucune donnée disponible | ■ | ■ | Aucune donnée disponible |
| Ignifugeants | ||||
| HexabromocyclododécaneNote de bas de page 1 | ■ | Aucune donnée disponible | ■ | ■ |
| PBDE-99 | ■ | Aucune donnée disponible | ■ | ■ |
| Métaux et éléments à l'état de trace | ||||
| Antimoine | * | * | Aucune donnée disponible | Aucune donnée disponible |
| Arsenic, inorganique (différencié) | Aucune donnée disponible | ■ | ■ | ■ |
| Bore | Aucune donnée disponible | Aucune donnée disponible | Aucune donnée disponible | * |
| Cadmium | ■ | ■ | ■ | ■ |
| Fluorure | Aucune donnée disponible | ■ | ■ | Aucune donnée disponible |
| Manganèse | * | * | Aucune donnée disponible | Aucune donnée disponible |
| Nickel | * | * | Aucune donnée disponible | Aucune donnée disponible |
| Sélénium | * | * | Aucune donnée disponible | * |
| Thallium | Aucune donnée disponible | * | Aucune donnée disponible | Aucune donnée disponible |
| Uranium | * | * | Aucune donnée disponible | Aucune donnée disponible |
| Composés organochlorés | ||||
| DDT | ■ | Aucune donnée disponible | Aucune donnée disponible | Aucune donnée disponible |
| Hexachlorobenzène | ■ | Aucune donnée disponible | ■ | ■ |
| Pesticides | ||||
| Chlorpyrifos | Aucune donnée disponible | Aucune donnée disponible | ■ | Aucune donnée disponible |
| Cyfluthrine | ■ | ■ | Aucune donnée disponible | ■ |
| 2,4-D | ■ | ■ | Aucune donnée disponible | Aucune donnée disponible |
| Deltaméthrine | ■ | ■ | Aucune donnée disponible | ■ |
| Malathion | Aucune donnée disponible | Aucune donnée disponible | * | Aucune donnée disponible |
| Acide 3-phénoxybenzoïqueNote de bas de page 1 | * | * | Aucune donnée disponible | ■ |
| Phtalates | ||||
| Phtalate de benzyle et de butyle | ■ | ■ | Aucune donnée disponible | ■ |
| Phtalate de dibutyle | ■ | ■ | Aucune donnée disponible | ■ |
| Phtalate de dicyclohexyleNote de bas de page 1 | * | * | Aucune donnée disponible | ■ |
| Phtalate de di(2-éthylhexyle) | ■ | ■ | Aucune donnée disponible | ■ |
| Phtalate de diéthyle | ■ | ■ | Aucune donnée disponible | ■ |
| Phtalate de diisobutyle | Aucune donnée disponible | ■ | Aucune donnée disponible | ■ |
| Phtalate de diisononyle | ■ | * | Aucune donnée disponible | ■ |
| COV | ||||
| Benzène | Aucune donnée disponible | Aucune donnée disponible | ■ | ■ |
| Bromodichlorométhane | Aucune donnée disponible | Aucune donnée disponible | ■ | ■ |
| Bromoforme | Aucune donnée disponible | Aucune donnée disponible | ■ | ■ |
| Chloroforme | Aucune donnée disponible | Aucune donnée disponible | ■ | ■ |
| Dibromochlorométhane | Aucune donnée disponible | Aucune donnée disponible | ■ | ■ |
| Éthylbenzène | Aucune donnée disponible | Aucune donnée disponible | ■ | ■ |
| Styrène | Aucune donnée disponible | Aucune donnée disponible | ■ | ■ |
| Tétrachloroéthène | Aucune donnée disponible | Aucune donnée disponible | ■ | ■ |
| Toluène | Aucune donnée disponible | Aucune donnée disponible | ■ | ■ |
| Trichloroéthène | Aucune donnée disponible | Aucune donnée disponible | ■ | ■ |
| Xylènes, mélangés | Aucune donnée disponible | Aucune donnée disponible | ■ | ■ |
■ – valeurs d'EB publiées * – valeurs en cours d'élaboration |
||||
Annexe B – Examens externes par les pairs
On a demandé aux examinateurs de dresser une liste de questions concernant un sous-ensemble des EB élaborés pour Santé Canada, soit les phtalates, la cyfluthrine, l'arsenic inorganique, l'hexachlorobenzène, le BPA, le DDT, le triclosan, la deltaméthrine et le PBDE-99.
- A-t-on relevé tous les renseignements essentiels pertinents pour l'établissement de l'EB? Par exemple, a-t-on relevé et examiné toutes les valeurs guides/de référence pertinentes comme fondement possible pour des EB? Si la réponse est non, veuillez fournir un exemplaire de la référence ou du document omis.
- Les renseignements essentiels présentés sont-ils suffisamment détaillés pour appuyer une caractérisation adéquate du fondement pour l'EB (p. ex. pertinence de l'analyte cible pour la toxicité selon le mode d'action?) Discute-t-on suffisamment et de façon critique des aspects concernant les renseignements à l'appui et l'approche de calcul des EB? Si non, que faudrait-il ajouter?
- Connaissez-vous les limites des renseignements essentiels qui servent de fondement aux EB qui n'ont pas été présentés?
- L'établissement des EB est-il conforme aux principes énoncés dans Hays et al. (2008a) et fondé sur les meilleurs pratiques possibles? Les conclusions sont-elles valables selon les renseignements examinés ou présentés? Par exemple :
- A-t-on choisi le bon analyte cible? Veuillez répondre à la question en tenant compte des éléments suivants (voir Hays et al., 2008a) :
- spécificité
- pertinence pour la toxicité (selon la compréhension du mode d'action);
- stabilité;
- acceptabilité;
- facilité d'interprétation;
- justesse des données pharmacocinétiques.
- A-t-on choisi la bonne méthode de calcul des EB (comme on le souligne dans les figures 3, 4 et 6 des travaux de Hays et al., 2008a)?
- Est-ce que l'inclusion ou le remplacement de facteurs d'incertitude par défaut pour les différences inter-espèces et la variabilité des propriétés toxicologiques chez l'humain correspond aux valeurs guides présentées au tableau 1 tiré de Hays et al. (2008a)?
- A-t-on choisi le bon analyte cible? Veuillez répondre à la question en tenant compte des éléments suivants (voir Hays et al., 2008a) :
- Le facteur d'incertitude ou le degré de confiance des diverses composantes et les EB qui en découlent sont-ils suffisamment pris en compte et présentés?
- Est-ce que des modifications apportées à la présentation amélioreraient la compréhension? Veuillez proposer des changements précis.
- Note de bas de page 1
-
Maintenant la Division de la surveillance des produits chimiques, Bureau de la science et de la recherche en santé environnementale, DSSER, DGSESC
- Note de bas de page 2
-
Les composés particuliers traités de cette façon étaient les phtalates, la cyfluthrine, l'arsenic inorganique, l'HCB, le BPA, le DDT, le triclosan, la deltaméthrine et le PBDE-99.