Recommandations à jour sur l’utilisation des vaccins contre le zona

Télécharger le format de rechange
(Format PDF, 1.42 Mo, 84 pages)
Organisation : Agence de la santé publique du Canada
Publiée : 2018-08-30
Sujets connexes
Une déclaration d'un comité consultatif (DCC)
Comité consultatif national de l'immunisation (CCNI)
Table des matières
- Préambule
- Sommaire de l'information contenue dans la présente déclaration du CCNI
- I. Introduction
- II. Méthodologie
- III. Épidémiologie
- IV. Vaccin
- V. Économie
- VI. Recommandations
- VII. Priorités en matière de recherche
- VIII. Enjeux en matière de surveillance
- Tableaux
- Liste des abréviations
- Remerciements
- Annexes
- Références
Préambule
Le Comité consultatif national de l'immunisation (CCNI) donne à l'Agence de la santé publique du Canada (ASPC) des conseils continus et à jour liés à l'immunisation dans le domaine de la médecine, des sciences et de la santé publique.
En plus de la prise en compte du fardeau associé aux maladies et des caractéristiques vaccinales, l'ASPC a élargi le mandat du CCNI pour lui permettre d'inclure l'étude systématique des facteurs liés aux programmes dans la formulation de ses recommandations axées sur des données probantes. Cette initiative devrait aider le CCNI à prendre des décisions en temps opportun en ce qui a trait aux programmes de vaccination financés publiquement à échelle provinciale et territoriale.
Les nouveaux facteurs que le CCNI devra examiner de façon systématique sont les suivants : économie, équité, éthique, acceptabilité et faisabilité. Au cours des années à venir, le CCNI s'emploiera à peaufiner ses approches méthodologiques dans le but de tenir compte de ces facteurs. Ce ne seront pas toutes ses déclarations qui exigeront une analyse appronfondie de l'ensemble des facteurs programmatiques. Mais au fur et à mesure de la mise en œuvre de son mandat élargi, le CCNI produira des déclarations choisies qui incluront divers degrés d'analyses visant les programmes de santé publique.
L'ASPC confirme que les conseils et les recommandations figurant dans la présente déclaration reposent sur les connaissances scientifiques les plus récentes et diffuse ce document à des fins d'information. Les vaccinateurs doivent également connaître le contenu de la monographie de produit applicable. Les recommandations d'utilisation et les autres renseignements qui figurent dans le présent document peuvent différer du contenu de la monographie de produit rédigée par le fabricant du vaccin au Canada. Les fabricants ont fait homologuer les vaccins et ont démontré leur innocuité et leur efficacité lorsqu'ils sont utilisés conformément à la monographie de produit uniquement. Les membres du CCNI et les agents de liaison doivent se conformer à la politique de l'ASPC régissant les conflits d'intérêts, notamment déclarer chaque année les conflits d'intérêts possibles.
Sommaire de l'information contenue dans la présente déclaration du CCNI
Les faits saillants suivants font ressortir l'information importante pour les vaccinateurs. Veuillez consulter le reste de la Déclaration pour obtenir plus de précisions.
Quoi
Maladie de l'herpès zoster
- Une infection primaire par le virus varicelle-zona (VVZ) cause la varicelle, tandis qu'une infection réactivée entraîne l'herpès zoster (zona). Le zona se caractérise par une douleur neuropathique et une éruption dermatologique vésiculaire.
- La réactivation du VVZ se produit lorsque la réponse immunitaire cellulaire est réduite en raison du vieillissement ou d'une immunosuppression. Le zona est le plus souvent observé chez les adultes plus âgés (avec une incidence considérablement plus élevée chez les 50 ans et plus) et les personnes immunodéprimées.
- La névralgie post-zostérienne (NPZ) peut s'avérer débilitante et représente la complication la plus courante du zona. De façon similaire à l'incidence du zona et au taux d'hospitalisation connexe, le risque de développer la NPZ parmi les cas de zona augmente considérablement avec l'âge.
Vaccins contre le zona
- Deux vaccins contre le zona sont actuellement autorisés pour utilisation au Canada chez les individus immunocompétents de 50 ans et plus. L'utilisation d'un vaccin à virus vivant atténué, ZostavaxMD II (vaccin à virus vivant contre le zona [VVVCZ]), est autorisée depuis 2008. L'utilisation d'un vaccin à sous-unités recombinant, ShingrixMD (vaccin recombinant contre le zona, [VRZ]), a été autorisée en octobre 2017. Les deux vaccins se sont avérés sûrs et immunogènes, en plus de réduire l'incidence du zona et de la NPZ.
- L'efficacité du vaccin (EV) contre le zona diminue en fonction de l'âge et au fil du temps avec le VVVCZ, tandis que l'EV du VRZ demeure élevée et semble diminuer plus lentement que l'EV du VVVCZ, et ce, chez tous les groupes d'âge.
- L'EV du VRZ dans les incidents de zona et de NPZ observés au cours des 3 années suivant l'immunisation semble être deux fois plus importante que celle du VVVCZ.
- L'EV du VRZ dans les incidents de zona observés au cours des 4 années suivant l'immunisation demeure la même dans l'ensemble, sans diminution considérable constatée au fil du temps; en comparaison, un important déclin de la protection a été observé au cours de l'année suivant l'immunisation avec le VVVCZ.
- Les différences observées dans l'EV contre les incidents de zona ne sont pas importantes à travers les différents groupes d'âge durant les quatre années suivant le VRZ; en comparaison, le VVVCZ est considérablement moins efficace chez les adultes de plus de 70 ans par rapport aux adultes de 50 à 59 ans.
- En raison de l'adjuvant présent dans le VRZ, lequel entraîne une importante réponse immunitaire dans les cellules pour compenser le déclin immunitaire naturel associé au vieillissement, ce vaccin s'avère plus réactogène que le VVVCZ.
- Les deux vaccins sont rentables chez les adultes de 50 ans et plus par rapport à l'absence de vaccination, en particulier chez les adultes de 65 à 79 ans. Le VRZ est plus rentable que le VVVCZ.
Qui
Le CCNI présente les recommandations ci-après relativement au processus décisionnel au niveau des programmes de santé publique et au niveau individuel. (Bien que dans cette déclaration, les recommandations sont essentiellement les mêmes pour les deux niveaux du processus décisionnel, la justification et le contexte sont quelque peu différents.)
Pour ce qui est du processus décisionnel au niveau des programmes de santé publiqueNote de bas de page *, le CCNI recommande ce qui suit :
- On devrait offrir le VRZ aux populations de 50 ans et plus qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI, données probantes de catégorie A)
- On devrait offrir le VRZ aux populations de 50 ans et plus qui ont par le passé reçu le VVVCZ et qui ne présentent pas de contre-indications. (Fortement recommandé par le CCNI, données probantes de catégorie A)
- On peut envisager la revaccination par l'administration de deux doses du VRZ au moins un an après l'administration du VVVCZ (Recommandation discrétionnaire du CCNI, données probantes de catégorie I)
- On devrait offrir le VRZ aux populations de 50 ans et plus qui ontdes antécédents de zona et qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI, données probantes de catégorie B)
- On peut envisager la vaccination par l'administration de deux doses du VRZ au moins un an après le dernierépisode de zona (Recommandation discrétionnaire du CCNI, données probantes de catégorie I)
- On peut envisager l'administration du VVVCZ aux personnes immunocompétentes de 50 ans et plus qui ne présentent pas de contre-indication lorsque le VRZ est contre-indiqué, s'il est impossible à obtenir ou lorqu'il est trop cher. (Recommandation discrétionnaire du CCNI, données probantes de catégorie A)
- On peut envisager l'administration du VRZ (et non le VVVCZ) aux personnes immunodéprimées de 50 ans et plus, selon une évaluation individuelle. (Recommandation discrétionnaire du CCNI, données probantes de catégorie I). Le CCNI surveillera les résultats des essais en cours chez les personnes immunodéprimées et réévaluera ses recommandations lorsqu'ils seront disponibles.
- Note de bas de page *
-
Pour ce qui est du processus décisionnel au niveau des programmes de santé publique, le CCNI reconnaît qu'il existe des différences dans le contexte opérationnel à travers le Canada; il suggère donc que les provinces et les territoires qui le désirent se réfèrent au Tableau 10 des options de gestion pour prendre en considération les différences entre les groupes d'âge (p. ex., en ce qui concerne l'épidémiologie et le rapport coût-efficacité [RCE]) si l'établissement de l'ordre de priorité des programmes d'immunisation ciblés est requis pour la mise en œuvre.
Pour ce qui est du processus décisionnel au niveau individuelNote de bas de page **, le CCNI recommande ce qui suit :
- On devrait offrir le VRZ aux personnes de 50 ans et plus qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI, données probantes de catégorie A)
- On devrait offrir le VRZ aux personnes de 50 ans et plus qui ont par le passé reçu le VVVCZ et qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI, données probantes de catégorie A)
- On peut envisager la revaccination par l'administration de deux doses du VRZ au moins un an après l'administration du VVVCZ (Recommandation discrétionnaire du CCNI, données probantes de catégorie I)
- On devrait offrir le VRZ aux personnes de 50 ans et plus qui ont des antécédents de zona et qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI, données probantes de catégorie B)
- On peut envisager l'administration de deux doses du VRZ au moins un an après le dernier épisode de zona (Recommandation discrétionnaire du CCNI, données probantes de catégorie I)
- On peut envisager l'administration du VVVCZ aux personnes immunocompétentes de 50 ans et plus qui ne présentent pas de contre-indication lorsque le VRZ est contre-indiqué non disponibleou inaccessible. (Recommandation discrétionnaire du CCNI, données probantes de catégorie A)
- On peut envisager l'administration du VRZ (et non le VVVCZ) aux personnes immunodéprimées de 50 ans et plus, selon une évaluation individuelle des avantages par rapport aux risques. (Recommandation discrétionnaire du du CCNI, données probantes de catégorie I). Le CCNI assurera le suivi des résultats pour les essais en cours chez les personnes immunodéprimées et réévaluera ses recommandations au fur et à mesure de l'évolution des données probantes.
- Note de bas de page **
-
Pour ce qui est du processus décisionnel au niveau individuel concernant les vaccins contre le zona qui ne sont peut-être pas actuellement offerts dans le cadre des programmes d'immunisation de la santé publique, le CCNI suggère que les personnes et les cliniciens passent en revue les points de décision décrits dans le Tableau 9 des options de gestion.
Comment
VRZ
- Le VRZ est administré par voie intramusculaire en deux doses prévues à 2 et 6 mois d'intervalle. Afin d'améliorer l'adhérence à la 2e dose (p. ex., au moyen de l'administration simultanée avec un autre vaccin), on peut envisager l'administration à 0 et 12 mois selon les données probantes appuyant un profil de sûreté acceptable et une solide réponse immunitaire anti-gE.
- Le VRZ est contre-indiqué chez les personnes démontrant une hypersensibilité connue à tout composant vaccinal. On ne possède que des données limitées sur les personnes immunodéprimées et aucune donnée chez les femmes enceintes ou qui allaitent; par conséquent, le VRZ devrait être utilisé avec précaution pour ces groupes à l'heure actuelle.
- En général, les vaccins inactivés peuvent être administrés de manière concomitante pendant ou à tout moment avant ou après tout autre vaccin inactivé ou vaccin à virus vivant offrant une protection contre une maladie différente. Pour les injections parentérales concomitantes, il faut utiliser différents points d'injection ainsi que des aiguilles et des seringues distinctes. Le VRZ peut être administré au même moment que le vaccin sans adjuvant contre la grippe saisonnière. Les études sur l'administration concomitante du vaccin antipneumococcique 23-valent polysaccharidique (Pneu-P-23) et de BoostrixMD (tétanos, faible concentration de diphtérie et vaccin anticoquelucheux acellulaire; dcaT) se poursuivent. Les études sur l'administration concomitante du vaccin avec adjuvant contre la grippe saisonnière (FluadMD) n'ont pas encore été menées.
VVVCZ
- Le VVVCZ est administré par voie sous-cutanée en une seule dose.
- Le VVVCZ est un vaccin à virus vivant et est donc contre-indiqué pour les personnes enceintes ou immunodéprimées. Il est également contre-indiqué chez les personnes démontrant une hypersensibilité connue à tout composant vaccinal. La décision d'administrer ce vaccin chez les femmes qui allaitent doit être fait avec précaution.
- En général, les vaccins à virus vivant administrés par voie parentérale peuvent être utilisés de manière concomitante avec d'autres vaccins. Pour les injections parentérales concomitantes, il faut utiliser différents endroits ainsi que des aiguilles et des seringues distinctes. S'ils ne sont pas administrés de manière concomitante, un minimum de 4 semaines d'intervalle doit être maintenu entre deux vaccins parentéraux à virus vivant. Le VVVCZ peut être administré en même temps que le Pneu-P-23 car n'y a aucune réduction de l'efficacité ni augmentation des événements indésirables (EI), Aucune préoccupation en matière de sûreté ni interférence avec les réponses immunitaires n'a été relevée suivant l'administration concurrente d'un vaccin inactivé contre la grippe.
Pourquoi
- Le zona est douloureux et peut entraîner de graves complications, y compris des douleurs névralgiques persistantes.
- L'incidence et la gravité du zona et de ses complications augmentent avec l'âge.
- Près d'un Canadien sur trois développera une forme de zona au cours de sa vie.
- Les vaccins sont sûrs, immunogènes, efficaces et rentables pour prévenir le zona et la NPZ.
I. Introduction
I.1 Objectif de la présente déclaration
La nécessité d'une déclaration à jour du Comité consultatif national de l'immunisation (CCNI) sur l'utilisation des vaccins contre l'herpès zoster (zona) découle de données probantes relatives à l'autorisation d'un nouveau vaccin à sous-unités, recombinant contre le zona (VRZ), ShingrixMD, lequel est recommandé pour prévenir le zona chez les personnes de 50 ans et plus. La présente déclaration vise avant tout à examiner les données probantes actuelles et à élaborer des lignes directrices sur l'utilisation de ShingrixMD, en plus de déterminer si l'on devrait offrir le vaccin à virus vivant contre le zona (VVVCZ) précédemment autorisé, ZostavaxMD II et/ou le VRZ récemment apprové aux Canadiens de 50 ans et plus :
- au niveau de la population, dans le cadre de programmes d'immunisation financés publiquement;
- au niveau individuel, aux personnes souhaitant prévenir le zona ou par les cliniciens qui souhaitent conseiller à certains patients de se protéger du zona au moyen de vaccins qui ne sont peut-être pas actuellement offerts dans le cadre des programmes d'immunisation de la santé publique.
Les questions précises examinées à l'appui de l'objectif comprennent les suivantes :
- Le VRZ (par rapport à un placebo et au VVVCZ) est-il immunogène, efficace, sûr et rentable?
- À quels groupes d'âge devrait-on offrir les vaccins contre le zona?
- Quels sont les mérites relatifs du VRZ par rapport au VVVCZ?
- Le VRZ devrait-il être offert à ceux qui ont précédemment reçu le VVVCZ? Si on l'offre, quel devrait être l'intervalle entre les doses?
- Devrait-on offrir le VRZ à ceux qui ont des antécédents de zona? Si on décide de l'offrir, quel devrait être l'intervalle entre l'épisode de zona et la vaccination?
Le CCNI examinera les données probantes sur les vaccins contre le zona chez les personnes immunodéprimées dans une autre déclaration du comité consultatif. Des études sur l'immunogénicité, l'innocuité et l'efficacité du VRZ chez divers groupes de personnes immunodéprimées de18 ans et plus étaient toujours en cours au moment des délibérations du CCNI. Bien que l'utilisation du VRZ ne soit pas contre-indiquée chez les personnes immunodéprimées, aucune indication n'a été diffusée sur l'utilisation du VRZ chez les personnes de moins de 50 ans au Canada, et on ne dispose que de données probantes limitées chez les personnes immunodéprimées à l'heure actuelle. Des données probantes préliminaires non examinées par des pairs et présentés dans les résumés de certaines conférences sur le VRZ dans certains groupes de personnes immunodéprimées suggèrent qu'il n'y a aucune préoccupation importante concernant l'innocuité ou l'immunogénicité du vaccin. Le CCNI continuera d'examiner les données probantes au fur et à mesure de leur évolution et réévaluera ses recommandations.
I.2 Aperçu des recommandations reposant sur les données probantes concernant l'utilisation des vaccins contre le zona dans la présente déclaration
Selon les données probantes examinées et résumées dans la présente déclaration de son comité consultatif, le CCNI fera les recommandations suivantes relativement à l'utilisation du VVVCZ recommandé par le passé et du VRZ récemment autorisé au niveau de la population (Tableau 1) et au niveau individuel (Tableau 2). (Bien que dans cette déclaration les recommandations sont essentiellement les mêmes pour les deux niveaux du processus décisionnel, la justification et le contexte sont quelque peu différents.)
(Veuillez noter :
- Une forte recommandation s'applique à la majeure partie de la population et devrait être suivie, à moins que l'on puisse justifier de manière claire et convaincante l'adoption d'une autre approche.
- Dans certains cas, on peut envisager d'offrir une recommandation discrétionnaire pour des populations spécifiques et certaines personnes en particulier. D'autres approches peuvent s'avérer acceptables.
Veuillez consulter le Tableau 11 pour obtenir une explication plus détaillée de la force des recommandations du CCNI et de la catégorie de l'ensemble des données probantes.)
| Recommandation du CCNI (Force de la recommandation) |
Cote de qualité des données probantes à l'appui de la recommandation |
|---|---|
| VRZ | |
| 1. Le CCNI recommande d'offrir le VRZ aux populations de 50 ans et plus qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI) |
Le CCNI conclut qu'il existe de bonnes données probantes pour recommander une immunisation. (Données probantes de catégorie A) |
| 2. Le CCNI recommande d'offrir le VRZ aux populations de 50 ans et plus qui ont déjà reçu le VVVCZ et qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI) |
Le CCNI conclut qu'il existe de bonnes données probantes pour recommander une immunisation. (Données probantes de catégorie A) |
| 2a. Chez les adultes de 50 ans et plus qui ont déjà reçu le VVVCZ, le CCNI recommande d'envisager une revaccination par deux doses du VRZ au moins un an après l'administration du VVVCZ. (Recommandation discrétionnaire du CCNI; selon l'opinion d'experts.) |
Le CCNI conclut que les données probantes sont insuffisantes pour formuler une recommendation sur l'intervalle entre l'administration du VVVCZ et celle du VRZ. (Données probantes de catégorie I) |
| 3. Le CCNI recommande d'offrir le VRZ aux populations de 50 ans et plus qui ont des antécédents de zona et qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI) |
Le CCNI conclut qu'il existe desdonnées probantes passables pour recommander une immunisation. (Données probantes de catégorie B) |
| 3a. Le CCNI recommande pour les adultes de 50 ans et plus ayant déjà contracté le zona d'attendre au moins un an après leur épisode pour une vaccination par deux doses du VRZ. (Recommandation discrétionnaire du CCNI; selon l'opinion d'experts.) |
Le CCNI conclut que les données probantes sont insuffisantes pour recommander un intervalle entre un épisode antérieur de zona et l'administration du VRZ. (Données probantes de catégorie I) |
| VVVCZ | |
| 4. Le CCNI recommande d'envisager, l'administration du VVVCZ aux populations de 50 ans et plus qui sont immunocompétentes et qui ne présentent pas de contre-indication, dans les cas où le VRZ est contre-indiqué, s'il est n'est pas disponible. (Recommandation discrétionnaire du CCNI.) |
Le CCNI conclut qu'il existe de bonnes données probantes pour recommander une immunisation. (Données probantes de catégorie A) |
| VRZ par rapport au VVVCZ pour les personnes immunodéprimées | |
| 5. Le CCNI recommande d'envisager, au cas par cas, l'administration du VRZ (et non le VVVCZ) chez les adultes immunodéprimées de 50 ans et plus. (Recommandation discrétionnaire du CCNI, selon l'opinion l'experts.) Le CCNI examinera les données probantes au fur et à mesure de leur évolution et réévaluera ses recommandations. |
Le CCNI conclut que les données probantes sont insuffisantes actuellement pour recommander une immunisation. (Preuve de catégorie I.) |
|
|
| Recommandation du CCNI (Force de la recommandation) |
Cote de qualité de la données probantes à l'appui de la recommandation |
|---|---|
| VRZ | |
| 1. Le CCNI recommande d'offrir le VRZ aux personnes de 50 ans et plus qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI) |
Le CCNI conclut qu'il existe de bonnes données probantes sont bonnes pour recommander une immunisation. (Données probantes de catégorie A) |
| 2. Le CCNI recommande que le VRZ soit offert aux personnes de 50 ans et plus qui ont déjà reçu le VVVCZ et qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI) |
Le CCNI conclut qu'il existe de bonnes données probantes pour recommander une immunisation. (Données probantes de catégorie A) |
| 2a. Le CCNI recommande pour les adultes de 50 ans et plus qui ont déjà reçu le VVVCZ d'attendre un intervalle d'au moins un an avant une revaccination par deux doses du VRZ. (Recommandation discrétionnaire du CCNI; selon l'opinion d'experts.) |
Le CCNI conclut que les données probantes sont insuffisantes pour recommander un intervalle entre l'administration du VVVCZ et du VRZ. (Données probantes de catégorie I) |
| 3. Le CCNI recommande que le VRZ soit offert aux personnes de 50 ans et plus ayant des antécédents de zona et qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI) | Le CCNI conclut qu'il existe des données probanets passables pour recommander une immunisation. (Données probantes de catégorie B) |
| 3a. Le CCNI recommande pour les adultes de 50 ans et plus ayant des antécédents de zona d'attendre un intervalle d'au moins un an avant une vaccination par deux doses du VRZ. (Recommandation discrétionnaire du CCNI; selon l'opinion d'experts.). | Le CCNI conclut que les données probantes sont insuffisantes pour recommander un intervalle entre un épisode antérieur de zona et l'administration du VRZ. (Données probantes de catégorie I) |
| VVVCZ | |
| 4. Le CCNI recommande d'envisager l'administration du VVVCZ aux les personnes immunocompétentes de 50 ans et plus qui ne présentent pas de contre-indication, lorsque le VRZ est contre-indiqué ou s'il n'est pas disponible. (Recommandation discrétionnaire du CCNI.) | Le CCNI conclut qu'il existe de bonnes données probantes pour recommander une immunisation. (Données probantes de catégorie A) |
| VRZ par rapport au VVVCZ pour les personnes immunodéprimées | |
| 5. Le CCNI recommande d'envisager, au cas par car, l'administration du le VRZ (et non le VVVCZ) chez les personnes immunodéprimées de 50 ans et plus, selon une évaluation individuelle des avantages par rapport aux risques. (Recommandation discrétionnaire du CCNI, selon l'opinion l'experts.) Le CCNI examinera les données probantes au fur et à mesure de leur évolution et réévaluera ses recommandations. | Le CCNI conclut que les données probantes sont actuellement insuffisantes pour recommander une immunisation. (Données probantes de catégorie I) |
|
|
Aucune étude sur le VRZ n'a été menée auprès des personnes ayant des antécédents de zona ophtalmique (ZO)Note de bas de page 1 .
I.3 Renseignements généraux sur les vaccins contre le zona, les programmes d'immunisation et les recommandations au Canada
Au Canada, un VVVCZ en vue d'une utilisation chez les personnes de 60 ans et plus a été autorisé initialement par la Direction des produits biologiques et thérapies génétiques de Santé Canada en août 2008, et a été autorisé en mai 2011 pour une utilisation chez les personnes de 50 ans et plus. En 2008, seul un produit stable au congélateur (ZostavaxMD) était disponible; toutefois, en 2011, un produit stable au réfrigérateur (ZostavaxMD II) l'a remplacé.
En 2010, le CCNI a publié une déclaration du comité consultatif recommandant le seul vaccin disponible à ce moment (VVVCZ) pour la prévention du zona et de ses complications chez les personnes de 60 ans et plus, qui ne présentent pas de contre-indication (p. ex., personne immunodéprimée). Cette recommation était basée sur des données probantes que le comité jugeait être de bonne qualité.. En 2014, le CCNI a publié une mise à jour de la déclaration du comité consultatif recommandant que l'on puisse utiliser le vaccin chez les patients de 50 à 59 ans en se fondant sur de bonnes données probantes. (Cette recommandation n'a pas changé depuis la déclaration précédente, mais la catégorie de données probantes a été mise à niveau, puisque l'on a ensuite démontré que le vaccin était sûr et efficace pour ce groupe d'âge. Toutefois, puisque la durée de la protection du vaccin était inconnue au-delà des cinq premières années, on ne savait pas avec certitude si la vaccination à un âge plus jeune offrirait une protection continue aux âges plus avancés lorsque l'incidence du zona est la plus élevée.) Dans les recommandations de 2014, le CCNI est également arrivé à la conclusion qu'il n'y avait pas assez de données probantes pour recommander ou rejeter l'administration du vaccin contre le zona chez les personnes ayant été atteintes de ZO par le passé. Bien que la causalité ait été difficile à déterminer, des cas de ZO ont été signalés après l'administration du vaccin contre le zona.
Les recommandations du CCNI dans les déclarations du comité consultatif de 2010 et de 2014 sur le vaccin contre le zona dont l'utilisation a été autorisée au Canada à l'époque (VVVCZ) sont résumées dans le Tableau 3.
| Scénarios populationnels | Recommandations du CCNI de 2010 | Recommandations du CCNI de 2014 |
|---|---|---|
| 60 ans et plus | Recommandé (données probantes de catégorie A) | Recommandé (données probantes de catégorie A) |
| De 50 à 59 ans | Peut être utilisé (données probantes de catégorie B) | Peut être utilisé (données probantes de catégorie A) |
| Épisode précédent de zona | Non recommandé (données probantes de catégorie I) | Peut être administré (catégorie B) au moins un an après (opinion d'experts) – 2014 |
| Épisode précédent de ZO | Non recommandé (données probantes de catégorie I) | |
| Antécédents consignés de varicelle ou infection antérieure par la varicelle | Recommandé (données probantes de catégorie A) | |
| Personne immunodéprimée | ||
| – VIH, après une greffe d'organe ou une transplantation de cellules souches hématopoïétiques, ou chez les personnes recevant une dose élevée de corticostéroïdes, une chimiothérapie ou des médicaments affaiblissant le système immunitaire. | Non recommandé (données probantes de catégorie I) | |
| – Faible dose de médicaments immunodépresseurs ou d'anti-TNF, au cas par cas | Peut être administré (données probantes de catégorie B) | |
| Co-administration | ||
| – Avec vaccin antigrippal trivalent inactivé (VTI) | À un différent point d'injection, recommandé (données probantes de catégorie A) | |
| – Avec Pneumo-23 | Avec au moins 4 semaines d'intervalle, recommandé (données probantes de catégorie B) | Utilisé de manière concomitante à un différent point d'injection (données probantes de catégorie A) |
En mai 2014, le Comité canadien d'immunisation a recommandé d'offrir le VVVCZ de manière systématique aux adultes immunocompétents de 60 à 65 ans et plus qui ne présentent pas de contre-indication. Cette recommandation considérait l'épidémiologie du virus varicelle-zona, les caractéristiques du vaccin contre le zona, une analyse des modèles et de l'économie de la maladie ainsi que la faisabilité et l'acceptation des programmes d'immunisation contre le zona Note de bas de page 2 .
Le vaccin à virus vivant atténué contre le zona était disponible à l'achat privé; toutefois, jusqu'à tout récemment, aucun programme d'immunisation financé publiquement n'était offert au Canada. En septembre 2016, l'Ontario a été le premier gouvernement à offrir le vaccin contre le zona dans le cadre d'un programme financé publiquement à des personnes de 65 à 70 ans.
En octobre 2017, l'utilisation du VRZ contenant la glycoprotéine E du VVZ et le système adjuvant AS01B a été autorisée au Canada.
Le zona n'est pas une maladie à déclaration obligatoire au Canada, et aucun objectif national n'est présentement établi pour réduire la maladie ou établir des cibles concernant la couverture vaccinale contre cette maladie évitable par la vaccination.
I.4 Renseignements généraux sur les vaccins contre le zona, programmes d'immunisation et recommandations à l'échelle mondiale
L'utilisation du VVVCZ a été autorisée pour prévenir le zona aux États-Unis (É.-U.) en 2006 et a été recommandée par l'Advisory Committee on Immunization Practices (ACIP) en 2008 chez les adultes immunocompétents de 60 ans et plusNote de bas de page 3 .
En 2006, l'Agence européenne des médicaments (EMA) a émis une autorisation de commercialisation en ce qui concerne le VVVCZ aux fins de vaccination systématique chez les personnes de 60 ans et plusNote de bas de page 4 , et a étendu sa recommandation de sorte à englober les personnes de 50 ans et plus en 2007 Note de bas de page 5 . À partir de 2013, le National Health Service (NHS)Note de bas de page 6 britannique a commencé à offrir le VVVCZ aux personnes de 70 à 79 ans.
Actuellement, l'utilisation du nouveau VRZ est autorisée au Canada, aux É.-U, en Europe et au Japon. Le 25 octobre 2017, l'ACIP a recommandé de favoriser l'utilisation du VRZ par rapport au VVVCZ chez les adultes immunocompétents de 50 ans et plus, y compris ceux qui avaient précédemment reçu le VVVCZ. L'ACIP n'a toujours pas formulé de recommandation particulière concernant l'utilisation du VRZ chez les personnes immunodéprimées. Le VVVCZ demeure un vaccin recommandé pour prévenir le zona chez les adultes immunocompétents de 60 ans et plus aux É.-U. Note de bas de page 7 .
II. Méthodologie
En bref, voici les étapes générales de la préparation d'une déclaration du comité consultatif du CCNI :
- La synthèse des connaissances (collecte et résumé d'études individuelles, détermination du niveau [c.-à-d. conception de l'étude] et qualité des données probantes – résumés dans les tableaux sommaires des données probantes en annexe).
- La synthèse de l'ensemble de données probantes sur les avantages et les effets néfastes et considérant la qualité des données probantes et l'ampleur des effets observés.
- La transposition des données probantes en une recommandation.
De plus amples renseignements sur la méthodologie normalisée du CCNI reposant sur les données probantes sont disponibles.
Dans le cadre de cette déclaration du comité consultatif, le CCNI a examiné les principales questions lors de l'examen des données probantes, comme l'a proposé le groupe de travail sur le zona (GTZ), y compris les facteurs tels que le fardeau associé à la maladie à prévenir et les populations cibles; l'innocuité, l'immunogénicité ainsi que les efficacités potentielle et réelle des vaccins contre le zona; les calendriers de vaccination, l'économie et les autres aspects de la stratégie globale d'immunisation. Dans le cadre de la présente déclaration, des stratégies distinctes ont été adoptées afin de rassembler les données probantes sur les caractéristiques du vaccin, le fardeau associé à la maladie et les facteurs programmatiques liés aux vaccins contre le zona, lesquels ont ensuite été intégrés à un résumé global des connaissances par des employés techniques de l'ASPC (SI, MT, OB, KE, MD, SDB) et le contractant JH embauché dans le cadre d'un contrat sous la supervision du GTZ.
- Afin d'évaluer le fardeau associé à la maladie, les principaux documents ont été résumés par le MD dans la section de l'épidémiologie et ont été complémentés par les figures du MB reposant sur les données administratives tirées de plusieurs administrations canadiennes. Il n'y a actuellement aucun programme de surveillance en place au Canada permettant de surveiller les incidences de zona, de NPZ ou du zona ophtalmique.
- Afin d'évaluer l'efficacité et l'innocuité du vaccin, une collaboration a été entreprise entre l'ASPC et le Réseau sur l'innocuité et l'efficacité des médicaments (RIEM) des Instituts de recherche en santé du Canada (IRSC). Au sein du RIEM, le Groupe des méthodes et des applications de comparaisons indirectes (GMACI) a mené un examen systématique des études publiées et non publiées sur l'innocuité et l'efficacité du VVVCZ et du VRZ.
- Le GTZ a fourni une rétroaction et des directives sur les critères d'admissibilité des études, ainsi qu'ils sont définis par le cadre de la Population, des Interventions, des Comparateurs, des Résultats et des Études (PICOS) (P – adultes de 50 ans et plus, I – vaccins contre le zona, C – simulacre [ou vaccin placebo], aucun traitement ou un autre vaccin contre le zona, O – efficacité et innocuité du vaccin et qualité de vie, S – essais cliniques randomisés (ECR) et études non randomisées) ainsi que la stratégie de recherche documentaire. Cette stratégie, élaborée par un bibliothécaire (EC), a été examinée par un pair bibliothécaire (JM) à l'aide de la liste de vérification de l'examen des stratégies de recherche électronique par les pairs (PRESS). MEDLINE, EMBASE et la Bibliothèque Cochrane ont été consultées du début jusqu'au 19 janvier 2017 et ont été complémentées d'une recherche documentaire grise (c.-à-d. documents difficiles à trouver ou non publiés).
- Les citations récupérées ont fait l'objet d'une sélection indépendante aux fins d'admissibilité par les pairs des membres de l'équipe du GMACI (WZ, RC, PK, VN, MG, RW et JPS) après l'achèvement d'un exercice de calibration de l'équipe, de sorte à établir une entente entre les évaluateurs. L'admissibilité de chaque article complet et pertinent a été évaluée à l'aide d'un processus semblable. Une fois une liste des études répondant aux critères d'admissibilité (c.-à-d. l'efficacité de l'enquête présentée dans les études ainsi que l'efficacité ou l'innocuité des vaccins VVVCZ ou VRZ chez les adultes de 50 ans et plus) dressée par le GMACI, les données de chaque article admissible ont été résumées et évaluées de manière indépendante afin de déterminer le risque de biais par deux membres de l'équipe du GMACI (WZ, RC, PK, VN, MG, RW et JPS).
- Ce risque a été évalué à l'aide de l'outil d'évaluation des risques de biais de la Collaboration Cochrane visant les essais contrôlés randomisés, de l'échelle d'évaluation de la qualité de Newcastle-Ottawa pour les études de cohorte et les études cas/témoins ainsi que de l'outil d'évaluation des risques de biais de l'ouvrage « Effective Practice and Organisation of Care » pour les essais contrôlés non randomisés. On a également évalué les études selon la méthodologie normalisée du CCNI aux fins d'intégration aux tableaux des données probantes.
- En plus des études choisies et évaluées par le GMACI, le GTZ a ajouté 11 études supplémentaires sur l'innocuité et l'efficacité initialement exclues par l'équipe du GMACI conformément aux critères liés au cadre du PICOS en raison de l'absence d'un groupe de comparaison. La qualité de ces études supplémentaires a été évaluée à l'aide de la méthodologie normalisée du CCNI, et ces mêmes études ont été déclassées, le cas échéant, en raison de l'absence de groupes de comparaison. Toutes les études incluses sur l'efficacité et l'innocuité ont été extraites en tableaux des données probantes et ont été résumées dans un sommaire narratif par les employés techniques à l'ASPC (SDB, OB et MT).
- Afin d'évaluer l'immunogénicité des vaccins contre le zona, l'ASPC a demandé un examen documentaire dans le cadre d'un contrat, sous la supervision du GTZ du CCNI, y compris des tableaux sommaires indiquant la qualité des données probantes selon la hiérarchie méthodologique du CCNI (Tableaux 12 et 13), conformément à la méthodologie normalisée du CCNI. La stratégie de recherche a été élaborée en collaboration avec un bibliothécaire de Santé Canada (LG), et des recherches ont eu lieu le 5 juin 2017, pour ensuite être mises à jour le 10 octobre 2017 selon la question de recherche suivante : P – adultes de 50 ans et plus, I – vaccins contre le zona, C – simulacre (ou vaccin placebo), aucun traitement, un autre vaccin contre le zona ou aucun comparateur, O – immunité humorale ou immunité à médiation cellulaire (IMC).
- Afin d'évaluer le rapport coût-efficacité de différentes stratégies de vaccination contre le zona, une analyse économique a été effectuée par MD, ZZ, CS, PDW, VG, RA, EB et MB sous la supervision et l'orientation du GTZ. Les résultats obtenus ont été présentés à ce dernier le 12 janvier 2018, et ces éléments probants ont été résumés dans un sommaire narratif par KE, responsable technique à l'ASPC. Des méthodes précises pour cette analyse économique sont disponibles dans la section sur l'économie de la présente déclaration.
À la suite d'un examen de l'ensemble des données probantes résumées, des recommandations proposées sur l'utilisation des vaccins ont été formulées. Le président du groupe de travail et les responsables techniques de l'ASPC ont présenté les données probantes et proposé des recommandations au CCNI le 7 février 2018. Suivant l'examen approfondi des données probantes et des consultations tenues à la réunion du CCNI du 7 février 2018, le comité a voté sur les recommandations précises formulées. La description des facteurs pertinents, la justification des décisions précises et les lacunes en matière de connaissances sont présentées dans le texte.
Les résultats sont présentés pour la « population générale » en ce qui a trait à l'analyse de l'innocuité, de l'efficacité et de l'immunogénicité des vaccins. Il convient toutefois de noter que les études appuyant ces sections peuvent comprendre des sujets immunocompétents et immunodéprimés, mais que plusieurs études n'ont pas suffisamment stratifié les données pour pouvoir mener des analyses distinctes.
Les études visant précisément les groupes immunodéprimés ne se retrouvent pas dans la synthèse narrative de l'ensemble des données probantes. Bien que ces études n'aient pas été exclues des examens documentaires et se retrouvent dans les tableaux des données probantes, elles n'ont pas été analysées explicitement dans la présente déclaration, puisque le CCNI a déterminé que des recommandations propres aux populations immunodéprimées seront formulées à une date ultérieure, lorsque plus de données probantes seront disponibles. Plusieurs essais cliniques sur le VRZ sont actuellement menés auprès de divers groupes immunodéprimés, y compris les personnes atteintes d'une tumeur solide, ou ayant reçu une greffe d'organe solide ou de cellules souches hématopoïétiques. Le CCNI continuera de surveiller les données probantes au fur et à mesure de leur évolution et fera une autre synthèse des connaissances pour ce groupe. Le CCNI formulera également des recommandations à partir des prochaines études, en plus des études particulières mentionnées dans les présents examens documentaires.
III. Épidémiologie
III.1 Description de la maladie
L'herpès zoster, ou le zona, est une éruption vésiculaire douloureuse touchant généralement un seul dermatome. Le zona se développe en raison de la réactivation du virus varicelle-zona (VVZ) latent dans les ganglions de la racine dorsale à la suite d'une primo-infection par la varicelle lorsque les composants immunitaires propres au VVZ s'affaiblissent (plus généralement en raison de l'âge ou chez une personne immunodéprimée). Bien qu'elles soient moins contagieuses que les personnes atteintes de la varicelle primaire, celles souffrant d'un cas aigu de zona peuvent transmettre le VVZ à d'autres personnes susceptibles, la transmission ayant principalement lieu par contact direct avec des lésions vésiculairesNote de bas de page 8 Note de bas de page 9 Note de bas de page 10 .
Jusqu'à 40 % des personnes atteintes d'un cas aigu de zona ont rapporté au moins une complication attribuable à la maladieNote de bas de page 11 Note de bas de page 12 Note de bas de page 13 . Les complications courantes sont potentiellement graves et comprennent la NPZ, une douleur prolongée et souvent débilitante affectant près de 20% des personnes affectées par le VVZ,Note de bas de page 14 Note de bas de page 15 Note de bas de page 16 et le ZO, où une réactivation du VVZ se produit dans la division ophtalmique du nerf trijumeau chez 10 à 15 % des cas Note de bas de page 17 , laquelle peut entraîner d'importantes douleurs chroniques, des cicatrices au visage ou une perte de vision. Les complications moins courantes, mais tout aussi graves, du zona comprennent des infections du système nerveux central, une paralysie des nerfs, y compris le syndrome Ramsay-Hunt, des maladies neuromusculaires dont le syndrome Guillain-Barré, une pneumonie, une hépatite et des infections bactériennes secondairesNote de bas de page 18 Note de bas de page 19 Note de bas de page 20 .
En général, les complications associées au zona sont plus courantes et plus graves chez les personnes plus âgées ou immunodépriméesNote de bas de page 14 Note de bas de page 17 Note de bas de page 21 . Les enfants sans comorbidité sont moins à risque de subir des complications découlant du zonaNote de bas de page 22 Note de bas de page 23 .
III.2 Répartition de la maladie
En l'absence d'une vaccination contre le zona, on estime que près d'un Canadien sur trois a développé un cas de zona au cours de sa vieNote de bas de page 24 , et près de 130 000 cas de zona, 17 000 cas de NPZ et 20 décès attribuables au zona surviennent chaque année au CanadaNote de bas de page 11 . L'âge est le principal facteur de risque du développement du zona, l'incidence du zona augmentant considérablement en fonction de l'âge chez les personnes de 50 ans et plusNote de bas de page 17 Note de bas de page 25 Note de bas de page 26 Note de bas de page 27 Note de bas de page 28 Note de bas de page 29 . Cette incidence varie également en fonction du sexe, les femmes courant environ 1,3 plus de risques de contracter la maladie par rapport aux hommesNote de bas de page 30 .
L'âge est également le facteur de risque prédominant pour le développement de la NPZ parmi les cas de zona, chaque période de 10 ans étant associée à une augmentation moyenne de 1,2 à 3,1 du risque relatif de développer la NPZNote de bas de page 31 . Le risque de NPZ est particulièrement élevé chez les personnes de 50 ans et plus, ce risque variant de 4 à 15 % parmi les cas de zona de 50 à 59 ans, de 7 à 26 % parmi les cas de 60 à 69 ans et de 14 à 29 % parmi les cas de zona de 70 ans et plus, selon les études de cohorte prospectivesNote de bas de page 17 . Une preuve de lien entre le risque de NPZ et le sexe s'avère conflictuelle, puisqu'un récent examen systématique offre des conclusions différentes et une hétérogénéité considérable entre les étudesNote de bas de page 31 . Contrairement à la NPZ, le risque de ZO ne varie pas en fonction de l'âgeNote de bas de page 17 .
En général, les facteurs de risque liés à l'incidence, aux complications et à la gravité du ZO sont largement inconnus; toutefois, on a proposé l'hypothèse qu'ils soient peut-être liés à la virulence de l'infection ou à la réponse immunitaire de l'hôteNote de bas de page 32 .
Le zona n'est pas actuellement une maladie à declaration obligatoire au Canada; par conséquent, les estimations provinciales de son incidence ont grandement été déduites à partir de données administratives. Les bases de ces données comportent des limitations inhérentes pour déterminer l'incidence du zona, telles que l'inclusion des données se limitant aux cas de zona vus par un médecin et le rôle important des codes administratifs de facturation dans la désignation des visites médicales liées au zona. Par conséquent, ces études peuvent manquer ou mal catégoriser certains cas de zona. Malgré ces limitations, ces études demeurent utiles, en particulier dans la détermination et l'examen des tendances sous-jacentes de la maladie associée au zona, tant et autant que les pratiques relatives aux codes administratifs ne changent pas au fil du tempsNote de bas de page 33 .
À ce jour, les tendances observées dans l'incidence du zona et les taux d'utilisation médicale ont été examinées à partir des données administratives obtenues auprès de l'Alberta, de la Colombie-Britannique, du Manitoba, de l'Ontario et du QuébecNote de bas de page 24 Note de bas de page 26 Note de bas de page 27 Note de bas de page 28 Note de bas de page 29 Note de bas de page 34 Note de bas de page 35 Note de bas de page 36 . En général, les résultats étaient semblables : des taux d'incidence bruts et standardisés de 3 à 5 cas par 1 000 années-personnes ont été observés chez les personnes ayant reçu des services médicaux pour le zonaNote de bas de page 24 Note de bas de page 26 Note de bas de page 27 Note de bas de page 28 Note de bas de page 29 Note de bas de page 34 Note de bas de page 35 . L'incidence du zona était fortement associée à l'âge, un nombre d'occurrences minimal et maximal de la maladie ayant été systématiquement observées chez les groupes plus jeunes et plus âgés, respectivementNote de bas de page 24 Note de bas de page 26 Note de bas de page 27 Note de bas de page 28 Note de bas de page 29 Note de bas de page 34 (Figure 1). Comme pour les estimations mondiales de l'incidence du zonaNote de bas de page 17 Note de bas de page 25 , le nombre de cas chez les Canadiens a considérablement augmenté chez les personnes de 50 ans et plus. On observe une hausse de zona variant de 4 à 6 cas par 1 000 années-personnes parmi les adultes de 50 ans, de 6 à 9 cas par 1 000 années-personnes parmi les adultes de 60 ans, de 7 à 11 cas par 1 000 années-personnes parmi les adultes de 70 ans et de 8 à 13 cas par 1 000 années-personnes parmi les adultes de 80 ans et plus (Figure 1). Les femmes courent également un plus grand risque de contracter le zona, et ce, dans toutes les tranches d'âgeNote de bas de page 26 Note de bas de page 27 Note de bas de page 28 Note de bas de page 29 . Approximativement 2 à 4 % des cas de zona au Canada ont été hospitalisésNote de bas de page 26 Note de bas de page 27 .
Tout comme pour l'incidence de la maladie, les taux d'hospitalisation étaient fortement associés à l'âge, et les taux les plus élevés étaient observés chez les personnes de 65 ans et plusNote de bas de page 24 Note de bas de page 26 Note de bas de page 29 Note de bas de page 34 Note de bas de page 36 (Figure 2). De façon similaire, des données internationales issues d'études publiées sur les cas de zona révèlent une forte corrélation entre l'âge et le risque de NPZ, en particulier chez les personnes de 65 ans et plus (Figure 3).
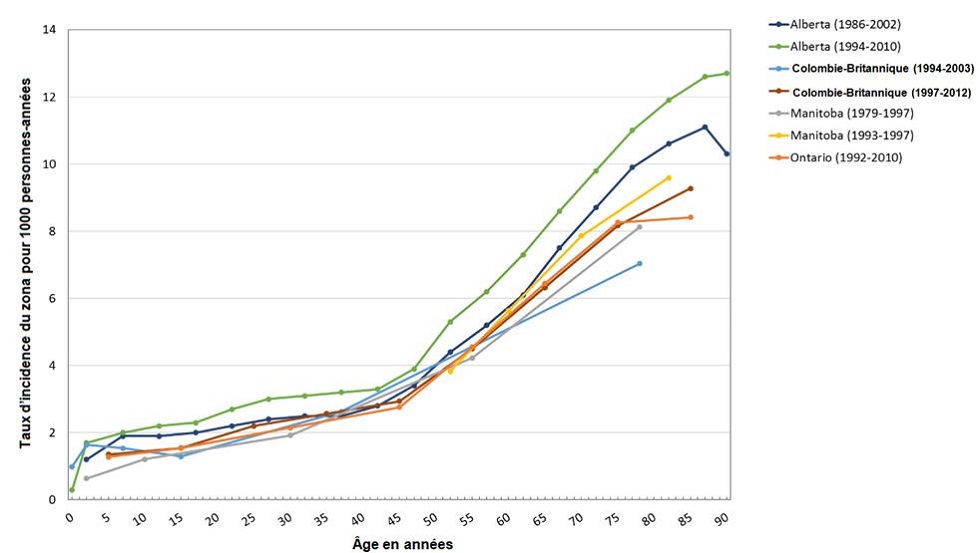
Figure 1 - Équivalent du texte
La figure 1 démontre le taux d'incidence du zona pour 1 000 années-personnes (axe vertical) par rapport à l'âge de la population en années (axe horizontal). Les points de données sont basés sur des études des provinces et territoires du Canada. Parmi les études où les taux sont observés pour un intervalle d'âges, l'âge est déterminé en fonction de l'âge médian de la catégorie d'âge. Pour les catégories d'âge qui comprennent une tranche d'âge non discrète (c'est-à-dire des âges inférieurs ou supérieurs à un âge donné), les âges minimum et maximum de la catégorie sont présumés être 0 et 90 ans, respectivement.
Les résultats de l'étude sont tracés dans des couleurs individuelles distinctes, en distinguant la province, le territoire et / ou l'intervalle de temps à partir duquel les données ont été obtenues. Les provinces et les intervalles de temps à partir desquels les données publiées étaient disponibles étaient l'Alberta (1986-2002, bleu foncé), l'Alberta (1994-2010, vert); Colombie-Britannique (1994-2003, bleu clair); Colombie-Britannique (1997-2012, marron); Manitoba (1979-1997, gris); Manitoba (1999-1997, jaune) et l'Ontario (1992-2010, orange).
Tous les tracés de données provinciales sont entrelacés, suivant la même tendance des âges ≤10 aux âges ≥ 75 ans, lorsque les études commencent à montrer plus d'écart. Une étude de l'Alberta (1994-2010) présentant une tendance démontrant une incidence plus élevée (d'environ 1 à 3 années-personnes) que la moyenne. La tendance générale est une lente augmentation de l'incidence du zona de zéro à environ 3 cas pour 1 000 années-personnes de 0 à 45 ans. À l'âge de 45 ans, les pentes de tous les tracés semblent augmenter, démontrant une hausse de l'incidence du zona de ~7 cas par 1 000 années-personnes (minimum - Colombie-Britannique 1994-2003) et ~13 cas par 1 000 années-personnes (maximum - Alberta 1994-2010) à l'âge ≥ 75 ans.
Veuillez noter que les taux rapportés pour une tranche d'âge sont établis selon l'âge moyen de cette tranche. Pour les catégories d'âge comprenant une tranche d'âge non discrète (c.-à-d. les personnes plus jeunes ou plus vieilles que l'âge désigné), les âges minimums ou maximums de la catégorie sont présumés à 0 et 90 ans, respectivement.
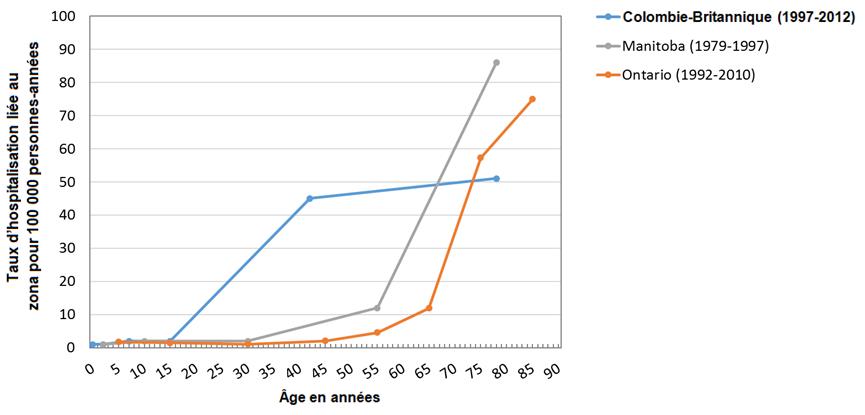
Figure 2 - Équivalent du texte
La figure 2 démontre le taux d'hospitalisation dû au zona pour 100 000 personnes-années (axe vertical) par rapport à l'âge de la population en années (axe horizontal). Les points de données sont basés sur des études des provinces et territoires du Canada. Parmi les études où les taux sont observés pour un intervalle d'âges, l'âge est déterminé en fonction de l'âge médian de la catégorie d'âge. Pour les catégories d'âge qui comprennent une tranche d'âge non discrète (c'est-à-dire des âges inférieurs ou supérieurs à un âge donné), les âges minimum et maximum de la catégorie sont présumés être 0 et 90 ans, respectivement.
Les résultats de l'étude sont tracés dans des couleurs individuelles distinctes, en distinguant la province, le territoire et / ou l'intervalle de temps à partir duquel les données ont été obtenues. Les provinces et les intervalles de temps pour lesquels des données publiées étaient disponibles étaient la Colombie-Britannique (1994-2003, bleu), le Manitoba (1979-1997, gris) et l'Ontario (1992-2010, orange).
Les courbes du Manitoba et de l'Ontario présentent des tendances similaires, soit un taux d'hospitalisation dû au zona inférieur à 10 pour 100 000 personnes-années pour une population de moins de 45 ans, ainsi qu'une augmentation très significative de la pente à partir de 55 ans (Manitoba) et 65 ans (Ontario), atteignant des valeurs maximales de ~87 hospitalisation dues au zona par 100 000 années-personnes à l'âge de 75 ans (Manitoba) et à ~75 par 100 000 années-personnes à l'âge de 85 ans (Ontario). Le tracé restant (Colombie-Britannique) présente des hospitalisations dues au zona de près de zéro pour 100 000 personnes-années parmi la population âgée de moins de 15 ans, une augmentation marquée jusqu'à ~45 pour 100 000 personnes-années autour des 45 ans; et le taux le plus bas parmi les ≥ 80, soit ~51 hospitalisations dues au zona par 100 000 personnes-années.
Veuillez noter que les taux rapportés pour une tranche d'âge sont établis selon l'âge moyen de cette tranche. Pour les catégories d'âge comprenant une tranche d'âge non discrète (c.-à-d. les personnes plus jeunes ou plus vieilles que l'âge désigné), les âges minimums ou maximums de la catégorie sont présumés à 0 et 90 ans, respectivement.
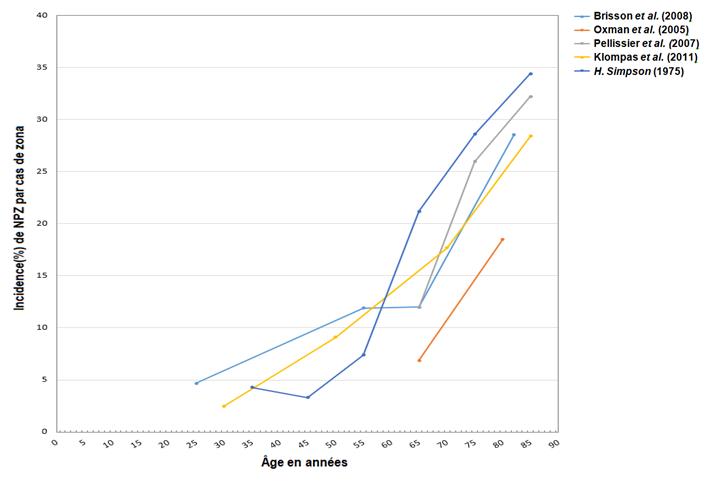
Figure 3 - Équivalent du texte
La figure 3 démontre le pourcentage d'incidence de NPZ par cas de zona (axe vertical) par rapport à l'âge de la population en années (axe horizontal) parmi les études publiées. Dans toutes les études, les taux ont été rapportés pour une gamme d'âges. L'âge a donc été tracé en fonction de l'âge médian de la catégorie d'âge observée. Pour les catégories d'âge qui comprenaient une tranche d'âge non discrète (c'est-à-dire des âges inférieurs ou supérieurs à un âge donné), les âges minimum et maximum de la catégorie étaient présumés être 0 et 90 ans, respectivement.
Les résultats de l'étude sont tirés de données provenant d'études publiées, y compris une gamme de conceptions d'études et de méthodologies différentes. Les études comprennent: un ECR (Oxman et al, 2005 - orange), deux modèles de cohortes analytiques (Brisson et al, 2008 - bleu clair, Pellissier et al, 2007 - gris) et deux études de cohorte rétrospectives (H-Simpson, 1975 - bleu foncé, Klompas et al, 2011 - jaune).
Toutes les études démontrent une tendance à la hausse similaire du pourcentage d'incidence de NPZ par cas de zona avec l'âge. Les valeurs les plus faibles observées chez les cohortes plus jeunes (25-45 ans) et les valeurs les plus basses observées chez une cohorte d'âge plus avancée sont montrées par la courbe d'Oxman et al (2005), avec un pourcentage de d'incidence de NPZ par cas de zona de ~7% autour des 65 ans et de ~18% autour des 80 ans. Le reste des études présente un risque d'incidence de NPZ plus élevé par cas de zona avec l'âge avancé : le deuxième plus faible taux de NPZ par cas de zona étant ~12% et le plus élevé étant de ~23% dans la tranche d'âge 60-65 ans, atteignant jusqu'à ~27% (le plus bas, Klompas et al 2011) à ~34% (le plus haut, H-Simpson 1975) dans la tranche d'âge ≥ 80 ans.
Veuillez noter que ces données sont dérivées d'études publiées, y compris un éventail varié de plans d'étude et de méthodologies. Les plans d'études comportent un ECRNote de bas de page 37 , deux modèles analytiques de cohorteNote de bas de page 11 Note de bas de page 38 et deux études rétrospectives de cohorteNote de bas de page 13 Note de bas de page 39 .
Toutes les études ont rapporté des taux pour différentes tranches d'âge; par conséquent, l'âge est établi selon l'âge moyen de la tranche. Pour les catégories d'âge comprenant une tranche d'âge non discrète (c.-à-d. les personnes plus jeunes et plus vieilles que l'âge désigné), les âges minimum ou maximum de la catégorie sont présumés à 0 et 90 ans, respectivement.
Plusieurs études provinciales ont examiné les tendances dans les taux de zona relativement à l'adoption du vaccin contre la varicelle à l'enfanceNote de bas de page 26 Note de bas de page 27 Note de bas de page 29 Note de bas de page 35 Note de bas de page 36 en réponse à une hypothèse stipulant que la vaccination primaire contre la varicelle pourrait réduire le renforcement naturel de l'immunité contre le VVZ en circulation et entraîner un plus grand risque de réactivation du VVZNote de bas de page 40 Note de bas de page 41 .
Bien que l'on ait observé une hausse de l'incidence du zona ou des taux de visites cliniques par rapport à la période d'étude dans quatre études provinciales sur cinq, deux d'entre ellesNote de bas de page 29 Note de bas de page 35 ont révélé une incidence accrue du zona associée à l'homologation du vaccin contre le zona, mais non à la mise en œuvre de la vaccination contre la varicelle. Selon ces conclusions, les auteurs ont émis l'hypothèse que l'augmentation de l'incidence du zona puisse être attribuable à une classification erronée des visites liées à la vaccination contre le zona comme étant plutôt associées à une maladie relative au zona. Dans les deux autres études ayant déclaré une augmentation des taux de zonaNote de bas de page 27 Note de bas de page 36 , on a également observé une augmentation des taux au cours de la période antérieure au vaccin, rendant difficile de déterminer avec certitude le véritable lien entre le zona et la vaccination primaire contre la varicelle. Selon la dernière étude, le risque de contracter le zona pendant la période suivant le programme de vaccination contre la varicelle financé publiquement n'était pas statistiquement différent de la période où les vaccins contre la varicelle n'étaient pas financés publiquement, après ajustement des facteurs confondants potentielsNote de bas de page 26 . Des tendances variables dans l'incidence du zona ont été rapportées dans les études précédant et suivant la mise en œuvre des programmes de vaccination primaire contre la varicelle aux É.-U. et ailleursNote de bas de page 17 Note de bas de page 42 Note de bas de page 43 . Par conséquent, le lien entre les programmes de vaccination primaire contre la varicelle et l'incidence du zona demeure flouNote de bas de page 44 .
Puisque les souches primaires de vaccins contre la varicelle peuvent se réactiver et entraîner le zona, un examen des taux de zona auprès des enfants vaccinés est également d'intérêt pour la période suivant la vaccination contre la varicelle. Des études de l'Alberta, de la Colombie-Britannique, de l'Ontario et du Québec ont révélé une diminution des taux de zona pendant la période postérieure relative à la période précédant la vaccination chez les enfants de moins de 10 ans admissibles au vaccin contre la varicelleNote de bas de page 26 Note de bas de page 27 Note de bas de page 29 Note de bas de page 36 . Ces données concordaient avec les résultats des autres études, lesquelles indiquaient un risque plus faible de zona chez les enfants ayant reçu le vaccin contre la varicelle par rapport aux enfants non vaccinésNote de bas de page 45 Note de bas de page 46 Note de bas de page 47 Note de bas de page 48 .
Le risque de zona chez les enfants qui ont reçu le vaccin contre la varicelle est un domaine d'intérêt continu, en particulier à mesure que les enfants vaccinés atteindront la tranche d'âge traditionnellement associée à un risque plus élevé de zonaNote de bas de page 8 Note de bas de page 49 .
III.3 Groupes à risque élevé
En raison d'affections sous-jacentes ou d'agents immunodépresseurs, les personnes immunodéprimées courent un plus grand risque de développer le zonaNote de bas de page 26 Note de bas de page 30 Note de bas de page 50 et peuvent être plus à même d'avoir une maladie et des complications atypiques et plus gravesNote de bas de page 51 Note de bas de page 52 Note de bas de page 53 Note de bas de page 54 Note de bas de page 55 .
Un récent examen systématique et une méta-analyse ont examiné le risque d'occurrence du zona chez les personnes atteintes de maladies auto-immunes, y compris la polyarthrite rhumatoïde, le lupus érythémateux disséminé et la maladie inflammatoire chronique de l'intestin, et ont révélé un risque de 1,4 à 2,1 supérieur (variable selon la maladie) chez les personnes atteintes de ces maladies par rapport aux personnes sans comorbiditéNote de bas de page 17 Note de bas de page 30 . Un autre examen systématique et une méta-analyse ont estimé un risque de 1,2 à 2,2 plus élevé d'occurrence du zona chez les personnes utilisant un médicament immunodépresseur, tel qu'un modificateur de la réponse biologique ne ciblant pas le facteur de nécrose tumorale, un médicament antirhumatismal non biologique modificateur de la maladie ou des corticostéroïdes (dont le risque varie selon le médicament) par rapport aux personnes utilisant un placebo ou n'utilisant aucun médicamentNote de bas de page 50 .
Les personnes immunodéprimées peuvent également courir un plus grand risque de développer la NPZ que la population générale, des taux plus élevés de NPZ étant observés chez les personnes gravement immunodéprimées, atteintes du diabète de type II ou du lupus érythémateux disséminéNote de bas de page 31 . Les taux de NPZ durant plus de 6 mois étaient également plus élevés chez les personnes atteintes de maladies qui toucheraient l'IMC chez l'hôte par rapport à la population générale, dans une étude sur la base de données administrative des É.-U.Note de bas de page 55 .
III.4 Sommaire de la couverture de l'immunisation contre le zona au Canada
À l'heure actuelle, la couverture du vaccin contre le zona n'est pas examinée dans le cadre d'enquêtes nationales au Canada. Une étude récente de l'Alberta estime toutefois que la couverture provinciale de ce vaccin était d'environ 8 % chez les personnes de 60 ans et plus pendant les 4 années suivant l'homologation du vaccin contre le zona et ce, en l'absence d'un programme de financement public pour ce vaccinNote de bas de page 56 . Compte tenu de son programme public de vaccination contre le zona, la couverture provinciale de ce vaccin est probablement plus importante en Ontario; toutefois, aucune donnée sur la couverture n'est disponible à l'heure actuelle (correspondance avec l'auteur).
IV. Vaccin
IV.1 Préparations dont l'utilisation est autorisée au Canada
Deux vaccins contre le zona sont actuellement autorisés pour utilisation au Canada chez les personnes immunocompétentes de 50 ans et plus. Un vaccin à virus vivant atténué sans adjuvant, stable au congélateur, ZostavaxMD, a été autorisé en 2008, mais un nouveau produit stable au réfrigérateur, ZostavaxMD II, l'a remplacé en 2011. Un vaccin recombinant à sous-unités et avec adjuvants, ShingrixMD, a récemment été autorisé en octobre 2017.
Le VVVCZ est fondé sur la souche atténuée du virus de la varicelle Oka/Merck, laquelle est également utilisée dans la production de vaccins contre la varicelleNote de bas de page 57 . Bien que le vaccin contre le zona contienne les mêmes composantes que celui contre la varicelle VarivaxMD (Merck), il comprend une concentration de virus au moins 14 fois supérieure (≥ 19 400 unités formatrices de plaques par dose).
Le VRZ combine un antigène (glycoprotéine à surface recombinante lyophilisée du virus varicelle-zona E, VVZ gE) et un système adjuvant (ASO1B). Ce système adjuvant est composé de liposomes contenant deux immunostimulants (monophosphoryl lipide 3-O-désacétylé-4' A [MPL]) et le Quillaja saponaria Molina, fraction 21 (QS-21)Note de bas de page 58 , et a été conçu de sorte à améliorer la réponse immunitaire humorale ainsi qu'à induire une réponse immunitaire cellulaire élevée afin d'aider à contrer le déclin naturel du système immunitaire associé à l'âge (immunosénescence). Des systèmes adjuvants semblables (combinaisons de molécules immunostimulantes améliorant la protection par rapport aux sels d'aluminium) sont présents dans deux vaccins homologués au Canada (ASO3 dans le vaccin prépandémique ArepanrixMD H5N1; ASO4 dans le vaccin contre le virus du papillome humain, CervarixMD)Note de bas de page 59 , ainsi que des vaccins faisant actuellement l'objet d'essais cliniques. Le VRZ est le premier vaccin autorisé au Canada qui comprend le système adjuvant ASO1B, lequel est également examiné dans les vaccins candidats contre la malaria.
Les caractéristiques des vaccins contre le zona dont l'utilisation est actuellement autorisée au Canada sont résumées dans le Tableau 4.
| Produit | ZostavaxMDIINote a | ShingrixMDNote b |
|---|---|---|
| Fabricant | Merck Canada Inc | GlaxoSmithKline Inc |
| Date d'autorisation au Canada | 2008 (ZostavaxMD) – n'est plus disponible au Canada 2011 (ZostavaxMDII) |
Octobre 2017 |
| Type de vaccin | Vivant atténué | Sous-unité recombinante |
| Composition | Ingrédient actif : souche Oka/ MERCK du VVZ élaborée à partir de passages en séries dans la culture de tissu. Autres ingrédients : 31,16 mg de saccharose; 15,58 mg de gélatine de porc hydrolysée; 3,99 mg de chlorure de sodium; 0,62 mg de L-glutamate monosodique; 0,57 mg d'hydrogénophosphate de disodium; 0,10 mg de phosphate de potassium monobasique; 0,10 mg de chlorure de potassium; composantes résiduelles de cellules MRC-5, y compris l'ADN et les protéines, ainsi que la néomycine à l'état de trace et le sérum embryonnaire de veau. |
Recombinant de la glycoprotéine E du VVZ (protéine retrouvée dans le VVZ) 50 mcg. Adjuvant : ASO1B (à base de liposomes) contient 50 mcg d'extrait de plante Quillaja saponaria Molina, fraction 21 (QS-21) + 50 mcg de monophosphoryl lipide 3-O-désacétylé-4' A (MPL) de la Salmonella minnesota avec 1 mg de dioléoyl phosphatidylcholine |
| Administration | Une dose | Deux doses, à un intervalle de 2 à 6 mois (Le CCNI suggère d'envisager un calendrier d' administration à 0 et 12 mois afin d'améliorer l'adhérence à la 2e dose (p. ex. au moyen de l'administration simultanée avec un autre vaccin) selon un profil d'innocuité acceptable et une solide réponse immunitaire anti-gE pour ce calendrier. bien qu'elle n'ait pas été non-inférieure à ceux d'une administration à 0 et 2 mois Note c |
| Voie d'administration | Sous-cutanée | Intramusculaire |
| Indications | Prévention du zona chez les personnes ≥ 50 ans | Prévention du zona chez les personnes ≥ 50 ans |
| Contre-indications | – Antécédents d'hypersensibilité à tout composant du vaccin, y compris la gélatine et la néomycine |
– Hypersensibilité connue à la substance active ou à tout composant du vaccin |
| Précautions | Allaitement |
– Grossesse (aucune donnée sur les humains) |
| Exigences liées au stockage | ZostavaxMDII : stable au réfrigérateur (ZostavaxMD - n'est plus disponible au Canada : stable au congélateur) |
Stable au réfrigérateur |
|
||
IV.2 Efficacités potentielle et réelle
IV.2.1 Efficacités potentielle et réelle du VVVCZ dans la population générale
Quatorze études ont évalué les efficacités potentielle (EV) et réelle du VVVZ à dose unique et l'efficacité au sein de la population générale. Parmi ces études, 3 étaient considérées comme de bonne qualité et 11, de qualité passable (voir les tableaux sommaires des données probantes, Annexe A).
L'EV du VVVCZ dans la prévention du zona chez les adultes de 50 à 59 ans a été rapportée dans un important ECR visant plus de 22 000 personnesNote de bas de page 61 . Après 1,5 an suivant l'immunisation, l'EV était estimée à 69,8 % (intervalle de confiance [IC] de 95 % : de 54,1 % à 80,6 %). L'efficacité réelle réduite du vaccin au cours de l'année suivant l'immunisation (50,34 % [IC de 95 % : de 36,01 % à 51,55 %]) dans ce groupe d'âge a été rapportée à la suite d'une analyse des données d'observationNote de bas de page 62 .
Bien que des effets de protection comparables contre les occurrences de zona aient été rapportés chez les adultes de 60 à 69 ans, un déclin dans l'efficacité réelle des vaccins a, dans l'ensemble, été observé avec l'âge. Dans le plus important essai clinique ayant évalué la protection offerte par le vaccin chez les adultes de 60 ans et plus, l'EV sur une période de 3 ans était la plus élevée chez les adultes de moins de 70 ans (63,9 % [IC de 95 % : de 55,5 % à 79,9 %] par rapport à 37,6 % [IC de 95 % : de 25 % à 48,1 %]) chez les adultes de 70 ans et plusNote de bas de page 37 Note de bas de page 63 (efficacité globale du vaccin dans les essais : 51,3 % [IC de 95 % : de 44,2 % à 57,6 %]). Bien qu'il soit possible que l'échantillonnage de la population issu de l'étude d'EV pour la prévention du zona (en collaboration avec le ministère des Anciens Combattants) ne permette pas une représentation complète de la population générale, les estimations concordaient avec les études d'observation dans lesquelles l'efficacité réelle sur 3 ans variait de 48 % (IC de 95 % : de 39 % à 56 %) à 55 % (IC de 95 % : de 52 % à 58 %)Note de bas de page 62 Note de bas de page 64 Note de bas de page 65 Note de bas de page 66 Note de bas de page 67 Note de bas de page 68 pour les adultes de plus de 60 ans, et de 33 % (IC de 95 % : de 32 % à 35 %) à 49,8 % (IC de 95 % : de 46,6 % à 52,8 %) chez les adultes de 70 ans et plus. En plus du déclin de la population observé avec l'âge, les études examinées ont également révélé un déclin continu dans l'efficacité réelle au fil du temps, avec une protection minimale ou inexistante au-delà de la période de 6 ans suivant l'immunisationNote de bas de page 61 Note de bas de page 66 .
L'immunisation par le VVVCZ s'est également avérée une mesure de protection contre la NPZ et le zona récurrent. Dans les essais cliniques, l'efficacité réelle de 3 ans contre la NPZ a démontré un taux de 65,7 % (IC de 95 % : de 20,4 % à 86,7 %) chez les adultes de 60 à 69 ans, et de 66,8 % (IC de 95 % : de 43,3 % à 81,3 %) chez les adultes de 70 ans et plusNote de bas de page 37 Note de bas de page 63 .
Ces estimations étaient semblables à celles rapportées dans les études d'observationNote de bas de page 68 Note de bas de page 70 .
Chez les personnes précédemment atteintes du zona, la protection pendant la période d'immunisation de 3 ans a seulement été observée chez les adultes de moins de 70 ans (61 % [IC de 95 % : de -3,45 % à 95 %]), mais non chez ceux de 70 ans et plus (-0,05 % [IC de 95 % : de -1,09 % à 70 %Note de bas de page 69 ]).
IV.2.2 Efficacités potentielle et réelle du VRZ dans la population générale
Les estimations d'EV du VRZ (deux doses) étaient disponibles à partir de deux essais cliniques pivots menés auprès de 28 000 adultes de plus de 50 ans. Les deux essais sont considérés comme des études de bonne qualitéNote de bas de page 71 Note de bas de page 72 (voir les tableaux sommaires des données probantes). Parmi les adultes de 50 à 59 ans, l'efficacité estimée sur la période de 3 ans était de 96,6 % (IC de 95 % : de 89,6 % à 99,3 %) pour les incidences du zona et de 100 % (IC de 95 % : de 40,8 % à 100 %) pour la NPZ. Chez les adultes de 60 à 69 ans, l'efficacité rapportée était de 97,4 % (IC de 95 % : de 90,1 % à 99,7 %). Chez les adultes de 70 ans et plus, nous avons estimé à partir des données regroupées des deux études que l'efficacité des vaccins contre le zona était de 91,3 % (IC de 95 % : de 86,8 % à 94,5 %). Bien qu'une efficacité réduite ait été observée dans ce groupe d'âge au cours de la période de 4 ans suivant l'immunisation, les différences entre la première année (97,6 % [IC de 95 % : de 90,9 % à 99,8 %]) et la quatrième année (84,7 % [IC de 95 % : de 69 % à 93,4 %]) ne se sont pas révélées statistiquement significatives. Dans l'ensemble, l'efficacité du vaccin contre la NPZ était de 91,2 % (IC de 95 % : de 75,9 % à 97,7 %) chez les adultes de 50 ans et plus et de 88,8 % (IC de 95 % : de 68,7 % à 97,1 %) chez les adultes de 70 ans et plus.
IV.3 Immunogénicité
Traditionnellement, les études sur les vaccins contre le zona ont utilisé des anticorps anti-VVZ afin d'évaluer l'immunité humorale, ainsi que divers essais cellulaires pour évaluer l'IMC. Plus récemment, pour évaluer l'immunité humorale, des essais pivots sur le VRZ ont précisément mesuré les anticorps anti-gE en plus des anticorps anti-VVZ. Certaines études ont seulement rapporté des anticorps anti-gE. Aucune équivalence entre les réponses anticorps anti-VVZ et anti-gE suivant la vaccination ou l'infection n'a été établie dans les documents, mais les données aux dossiers des fabricants indiquent une bonne corrélation entre les anticorps anti-gE et anti-VVZ.
Aucun corrélat sérologique de protection humorale ou cellulaire n'est actuellement établi pour la protection contre le zona ou la NPZ pour les patients qui ont été atteints d'une infection primaire par le VVZ ou ceux qui ont été vaccinés par le passéNote de bas de page 73 Note de bas de page 74 . Par conséquent, toutes les études évaluant l'immunogénicité des vaccins contre le zona doivent être interprétées avec prudence. Il semblerait que les cellules CD4+ et CD8+ jouent un rôle central dans la prévention de la réactivation du VVZNote de bas de page 71 Note de bas de page 75 , et une seule étudeNote de bas de page 76 a suggéré que l'IMC (telle que mesurée par les cellules T produisant des interférons gamma) au moment de l'apparition du zona était associée à la gravité moindre de la maladie et à la probabilité réduite de la NPZ, tandis que ce n'était pas le cas pour l'immunité humorale (telle que mesurée par les anticorps anti-VVZ)Note de bas de page 77 .
De nombreuses études examinées sur l'immunogénicité ne comprenaient pas de groupes de contrôle où les patients n'avaient pas reçu de vaccin, et la qualité globale des données probantes de la plupart des études était passable ou faible (voir le Tableau sommaire des données probantes, Annexe B).
IV.3.1 Immunogénicité du VVVCZ dans la population générale
Toutes les études examinées utilisaient le VVVCZ (il n'y avait aucun autre vaccin à virus vivant dans ce groupe de la population). De façon générale, les études ont évalué l'immunité humorale à partir des niveaux d'anticorps anti-VVZ, et bon nombre d'entre elles ont également évalué l'IMC à l'aide des cellules formant des taches à interférons gamma propres au VVZ avec la technique ELISPOT ou des essais sur la fréquence des cellules répondantes mesurant les comptes par minute d'intégration d'H3-thymidine dans les cellules sanguines mononucléaires périphériques stimulées par le VVZ. Le VVVCZ s'est avéré immunogénique (c.-à-d. que l'on a observé d'importantes augmentations dans les niveaux d'anticorps ou de cellules) dans toutes les études.
La durée du suivi variait de 4 semaines à 3 ans (à l'exception des études examinant les cas ayant reçu un vaccin de rappel). En général, l'immunité mesurée en fonction des niveaux d'anticorps et du nombre de cellules T était maximale à 6 semaines, avant de redescendre par la suite. Une étudeNote de bas de page 76 jugée de bonne qualité suggérait que l'IMC (telle que mesurée par les cellules T positives à interférons gamma) au moment de l'apparition du zona était associée à la gravité moindre de la maladie et à la probabilité réduite de la NPZ, tandis que ce n'était pas le cas pour l'immunité humorale (telle que mesurée par les anticorps anti-VVZ). Une autre étude jugée de bonne qualité suggérait une corrélation entre la hausse de la concentration d'anticorps jusqu'à 6 semaines après la vaccination et l'efficacité du vaccin, tandis que les niveaux d'anticorps après 6 semaines ne l'étaient pasNote de bas de page 77 .
Les réponses immunitaires au VVVCZ semblaient décliner avec l'âge. Une étudeNote de bas de page 78 jugée de bonne qualité suggérait que la réponse humorale chez les personnes de 50 à 59 ans était légèrement plus importante que chez le groupe des 60 ans et plus. Une autre étude de qualité passable suggérait que la réponse à l'IMC était supérieure chez les personnes de 60 à 69 ans par rapport à ceux de plus de 70 ans.
En ce qui concerne le mécanisme d'administrationNote de bas de page 79 , une étude de qualité passable suggérait que l'administration intradermique du VVVCZ était associée à une augmentation supérieure et plus persistante dans l'immunité humorale que l'administration sous-cutanée traditionnelle. Une autre étude de qualité passable n'a révélé aucune différence entre l'administration intramusculaire et sous-cutanéeNote de bas de page 80 . En ce qui a trait au nombre de doses requises, deux étudesNote de bas de page 81 Note de bas de page 82 suggéraient qu'il n'y avait aucune différence dans l'immunogénicité entre les administrations d'une ou deux doses de VVVCZ. Pour ce qui est des doses de rappel, une étude de qualité passable et une autre de faible qualité ont évalué l'effet d'une dose de rappel chez les personnes de plus de 70 ans par rapport à celles vaccinées pour la première fois. Pour les personnes recevant les vaccins de rappel, il semblait y avoir une réponse plus importante à l'IMC, mais aucune différence dans la réponse humoraleNote de bas de page 83 Note de bas de page 84 .
IV.3.2 Immunogénicité du VRZ dans a population générale
Les études examinées sur l'immunogénicité du VRZ ont généralement toutes évalué l'immunité humorale à l'aide des niveaux d'anticorps anti-gE, et nombre d'entre elles ont également évalué l'IMC, généralement par les cellules T CD4+ avec au moins deux marqueurs d'activation (y compris l'expression des interférons gamma, des IL-12, des TNF alpha ou des ligands de CD40). Le VRZ s'est révélé immunogénique dans toutes les études.
En ce qui concerne la durée de la protection, une étude dont seulement le résumé était disponible au moment des délibérations du CCNI a révélé que les mesures de l'immunité à médiation humorale et cellulaire demeuraient supérieures par rapport au niveau de référence 9 ans après la vaccination, les niveaux d'anti-gE et de cellules T atteignant un plateau entre 4 et 9 ans après la vaccinationNote de bas de page 85. Une autre étude jugée de faible qualité a révélé que, bien que l'immunité à médiation humorale et cellulaire ait atteint un plateau à 3 mois, les niveaux d'anti-gE et de cellules T CD4+ étaient plus élevés que le niveau de référence 72 mois après la vaccinationNote de bas de page 86 .
Les niveaux d'immunité ne semblaient pas varier en fonction de l'âge. Une étude non-publiée au moment des délibérations du CCNI et jugée de faible qualité a révélé des niveaux semblables d'IMC et d'immunité humorale chez les personnes de 50 à 59 ans, de 60 à 69 ans et de 70 ans et plusNote de bas de page 105 . Parmi les sujets ayant des antécédents de zona, on a découvert que le vaccin à sous-unités générait une solide réponse humorale semblable chez tous les groupes d'âge de plus de 50 ans dans une autre étude jugée de faible qualitéNote de bas de page 87 . Cette étude présentait des limitations empêchant l'évaluation définitive d'un épisode antérieur de zona.
Le résumé d'une étude (qui a depuis été publiée) suggérait qu'une vaccination antérieure au moyen d'un vaccin à virus vivant administré au moins 5 ans auparavant ne semblait pas changer les mesures de référence de l'immunité à médiation humorale ou cellulaire, tandis que le VRZ menait à une réponse semblable chez les patients qu'ils aient reçu ou non le VVVCZ par le passéNote de bas de page 88 . De même, une étude jugée de faible qualité a démontré que parmi les patients ayant des antécédents de zona, le VRZ a entraîné une solide réponse immunitaire humorale semblable pour tous les groupes d'âge de plus de 50 ansNote de bas de page 87 .
IV.3.3 Comparaisons directes entre le VVVCZ et le VRZ
Seule une étude de Weinberg et al. a offert une comparaison directe de l'immunogénicité entre les vaccins à virus vivant et les vaccins à sous-unités, et est à l'heure actuelle seulement disponible sous la forme de résumé dont on n'a pu évaluer la qualitéNote de bas de page 89 .
Cette étude suggère une réponse plus importante des lymphocytes T mémoires CD4+ et CD8+ chez les personnes recevant le VRZ par rapport à celles recevant le vaccin à virus vivant. Ces résultats suggèrent que le VRZ est plus immunogénique que le vaccin à virus vivant.
IV.4 Administration et calendrier des vaccins
IV.4.1 Administration et calendrier du VVVCZ
Le VVVCZ est administré par injection sous-cutanée, de préférence dans la région deltoïdienne. Il doit être reconstitué immédiatement après avoir été sorti du réfrigérateur. Veuillez consulter la monographie du produit pour obtenir les détails de la reconstitution du vaccin avant de l'administrer.
Les personnes devraient recevoir une seule dose composée de la totalité du contenu du flacon reconstitué (environ 0,65 ml).
Le besoin d'administrer une dose de rappel après la vaccination primaire n'a pas été établi.
IV.4.2 Administration et calendrier du VRZ
Le VRZ est administré par injection intramusculaire, de préférence dans le muscle deltoïde. Le vaccin est offert sous la forme d'un flacon de glycoprotéine à surface recombinante lyophilisée du virus varicelle-zona E (VVZ gE), lequel est reconstitué au moment de l'utilisation avec le flacon accompagnateur de suspension adjuvante AS01B. Veuillez consulter la monographie du produit pour obtenir les détails de la reconstitution du vaccin avant de l'administrer.
L'administration primaire du vaccin consiste en une série de deux doses (0,5 mL par dose), la deuxième étant administrée entre 2 et 6 mois après la première. L'administration de deux doses du VRZ à 2 mois d'intervalle s'est avérée une solution immunogénique et efficace contre le zona. Les études sur l'immunogénicité qui ont examiné d'autres calendriers de dosage ont démontré qu'une administration à 0 et 6 mois étaient non-inférieures à celle à 0 et 2 mois. Toutefois, la non-infériorité d'une administration à 0 et 12 mois n'a pas été démontrée. La petite étude de 346 participants a révélé que l'administration de deux doses du VRZ a entraîné de solides réponses immunitaires anti-gE chez les adultes de 50 ans et plus avec des administrations à 0 et 2 mois, 6 et 12 mois, sans aucune préoccupation en matière d'innocuité relevée pour l'une des trois administrations. Les réponses immunitaires au VRZ administré aux mois 0 et 6 n'étaient pas inférieures à celles associées à une administration à 0 et 2 mois. La non-infériorité relative aux réponses immunitaires humorales anti-gE n'a pas été démontrée un mois après la deuxième dose pour l'administration à 0 et 12 mois. Cela peut être attribuable au faible nombre de participants affichant des niveaux d'anticorps anti-gE considérablement plus faibles après la vaccination et non observés dans les autres groupes. Les investigateurs n'ont pas pu offrir d'explication pour les faibles niveaux d'anticorps anti-gE suivant la vaccination de ces neuf participants dans l'administration à 0 et 12 mois.
Bien que l'intervalle recommandé entre les deux doses du VRZ soit de 2 et 6 mois, un intervalle minimal entre les doses (en dessous duquel la deuxième dose est établie comme invalide et devrait être répétée) d'un mois (4 semaines) devrait être maintenu. Les premiers résultats des études chez les personnes immunodéprimées pour lesquelles un intervalle d'un mois a été utilisé entre les doses du VRZ suggèrent qu'il n'y a aucune donnée préoccupante en matière d'innocuité, d'immunogénicité ou d'efficacité du vaccinNote de bas de page 61 . Si un intervalle plus long que 6 ou 12 mois s'est écoulé après la première dose, il n'est pas nécessaire de refaire la série vaccinale; toutefois, les personnes peuvent demeurer à risque du zona pendant l'intervalle plus long que celui qui est recommandé entre la première et la deuxième dose.
Le besoin d'administrer une dose de rappel après l'administration de la vaccination primaire n'a pas été établi.
IV.5 Tests sérologiques
Les tests sérologiques avant ou après l'administration du vaccin contre le zona ne sont pas recommandés. Aucun corrélat sérologique de protection n'est accepté pour mesurer les anticorps humoraux ou l'IMC contre la varicelle ou le zona. La vaccination contre le zona sur des personnes en santé susceptibles de contracter le VVZ n'est associée à aucun risque connu en ce qui concerne l'innocuité. Si, dans de rares circonstances, une personne de 50 ans et plus est jugée susceptible de contracter le VVZ, deux doses de vaccin univalent contre la varicelle devraient être administrées en lieu et place du vaccin contre le zonaNote de bas de page 90 .
La protection immunitaire contre le zona ne peut pas être testée facilement; par conséquent, il n'y a pas d'indication pour la mesure des concentrations d'anticorps suivant l'immunisation.
IV.6 Exigences liées au stockage
IV.6.1 Exigences liées au stockage du VVVCZ
Pendant son expédition, le VVVCZ doit demeurer à une température entre -50 °C et +8 °C afin de s'assurer d'en maintenir l'efficacité. Le VVVCZ doit être stocké dans un réfrigérateur à une température de +2 °C à + 8 °C ou inférieure jusqu'à sa reconstitution avant l'injection. Le diluant devrait être stocké séparément à la température de la pièce (de +20 °C à +25 °C) ou au réfrigérateur (de +2 °C à + 8 °C). Avant d'être reconstitué, il doit être protégé de la lumière. Après sa reconstitution, le vaccin ne doit pas être congelé. Tout vaccin reconstitué non utilisé dans les 30 minutes devra être jetéNote de bas de page 57 .
IV.6.2 Exigences liées au stockage du VRZ
Le flacon de gE lyophilisé et le flacon de solution adjuvante doivent tous deux être stockés dans un réfrigérateur, à une température de +2 °C à + 8 °C dans l'emballage original (afin de les protéger de la lumière). Aucun flacon ne doit être congelé. Après sa reconstitution, le vaccin doit être utilisé sur-le-champ. Si cela n'est pas possible, il doit être stocké dans un réfrigérateur à une température de +2 °C à + 8 °C. Tout vaccin reconstitué non utilisé dans une période de 6 heures devra être jetéNote de bas de page 58 .
IV.7 Administration simultanée avec d'autres vaccins
L'administration simultanée des vaccins peut s'avérer bénéfique en réduisant le nombre requis de visites des patients et en augmentant l'adhésionaux vaccins recommandés.
IV.7.1 Administration simultanée du VVVCZ avec d'autres vaccins
En général, les vaccins à virus vivant administrés par voie parentérale peuvent être utilisés de manière concomitante avec d'autres vaccinsNote de bas de page 91 . Pour les injections parentérales concomitantes, il faut utiliser différents points d'injection ainsi que des aiguilles et des seringues distinctesNote de bas de page 91 . S'ils ne sont pas administrés de manière concomitante, un minimum de 4 semaines d'intervalle doit être maintenu entre deux vaccins.
En 2014, le CCNI a recommandé qu'il est possible d'administrer le vaccin antipneumococcique 23-valent polysaccharidique (Pneu-P-23) de manière concomitante avec le VVVCZ à un différent point d'injection, selon de bonnes données probantes tirées d'une étude ne démontrant aucune augmentation des cas de zona chez les personnes ayant reçu les vaccins de manière concomitante par rapport à une administration séquentielleNote de bas de page 69 .
L'administration concomitante du VVVCZ avec un vaccin quadrivalent contre la grippe s'est avérée tout aussi efficace selon les critères préétablis (ratio de titre moyen géométrique des anticorps [TMG] de 0,87) pour l'administration non concomitante et a entraîné une hausse de ratio des moyennes géométriques d'anticorps anti-VVZ de 1,9Note de bas de page 92 .
Parmi les personnes ayant reçu le VVVCZ avec un vaccin inactivé contre la grippe ou Pneu-P-23, l'administration concomitante n'a entraîné aucune augmentation des EI par rapport à l'administration individuelle des vaccins.
IV.7.2 Administration simultanée du VRZ avec d'autres vaccins
En général, les vaccins inactivés peuvent être administrés de manière concomitante pendant ou à tout moment avant ou après tout autre vaccin inactivé ou vaccin à virus vivant offrant une protection contre une maladie différente. Pour les injections parentérales concomitantes, il faut utiliser différents endroits ainsi que des aiguilles et des seringues distinctesNote de bas de page 93 Note de bas de page 94 .
Une étude sur l'administration concomitante du VRZ avec le vaccin quadrivalent contre la grippe n'a révélé aucune donnée préoccupante en matière d'innocuité ou d'interférence avec les réponses immunitaires de l'un des vaccins Note de bas de page 94 . L'administration concomitante des vaccins s'est avérée tout aussi efficace (le contrôle du rapport de TMG pour l'administration concomitante était de 1,08) pour le VRZ et le vaccin contre l'influenza, tels que mesurés par les ratios de TMG un mois après la vaccination.
Les études sur l'administration simultanée du Pneu-P-23 et de BoostrixMD (tétanos, faible concentration de diphtérie et vaccin anticoquelucheux acellulaire) se poursuivent. L'innocuité et l'efficacité de l'administration concomitante ou selon d'autres intervalles de deux vaccins avec adjuvants (p. ex., le VRZ et le vaccin avec adjuvant contre la grippe FluadMD) n'ont pas été évaluées.
IV.8 Événements indésirables
IV.8.1 Événements indésirables du VVVCZ dans la population générale
Au total, 21 études ont rapporté l'innocuité à court et à long terme du vaccin suivant l'administration du VVVCZ à différentes concentrations. De ces études, 11 étaient de bonne qualité; 8, de qualité passable et 2, de faible qualité (voir les tableaux sommaires des données probantes, Annexe C).
Chez les adultes de moins de 60 ansNote de bas de page 61 Note de bas de page 95 , les EI les plus souvent rapportés consistaient en une réaction au point d'injection, dont la majorité (>95 %) était jugée légers ou modérés. Dans l'essai clinique pivot au cours duquel plus de 11 000 adultes de 50 à 59 ans ont reçu le VVVCZ, un EI au point d'injection a été rapporté par 63,9 % des personnes ayant reçu le vaccin (différence de risque de 49,5 % [IC de 95 % : de 48,4 % à 50 %] par rapport au placebo). Dans ce même essai, des EI systémiques (EIS) liés au vaccin observés pendant les 42 jours suivant l'immunisation ont été rapportés chez 6,7 % des personnes (risque accru de 2 % [IC de 95 % : de 1,4 % à 2,6 %] d'EIS par rapport au placebo). Chez les personnes de moins de 60 ans, seul un EI lié au vaccin a été rapporté dans les études examinées.
Comparativement aux adultes de moins de 60 ansNote de bas de page 63 Note de bas de page 79 Note de bas de page 80 Note de bas de page 82 Note de bas de page 95 Note de bas de page 96 Note de bas de page 97 Note de bas de page 98 Note de bas de page 99 Note de bas de page 100 , ceux de 60 ans et plus ont généralement rapporté moins d'EI au point d'injection. L'intensité de la majeure partie (>95 %) de ces événements était considérée comme légère ou modérée, et sa durée était de moins de 2 jours. Dans les études d'observation, l'érythème, la douleur, la sensibilité au toucher et les enflures étaient les symptômes les plus courants rapportés par un quart ou un tiers des personnes. Dans un essai clinique pivot évaluant l'innocuité des vaccins chez plus de 3 300 adultes de plus de 60 ans, des EI au point d'injection étaient rapportés par 56,6 % des participants de 60 à 69 ans (différence de risque de 37,7 % [de 34,6 % à 40,6 %] par rapport au placebo), et 39,2 % des participants de 70 ans et plus (différence de risque de 25,4 % [de 22,5 % à 28,4 %] par rapport au placebo).
Chez les adultes de 60 ans et plus, des EIS liés aux vaccins apparaissant au cours des 42 jours suivant l'immunisation ont été rapportés par moins de 8 % des personnes. Dans un essai clinique pivot évaluant l'innocuité des vaccins chez plus de 3 300 adultes, des événements systémiques associés au vaccin ont été rapportés par 6,3 % des participants (différence de risque de 1,4 % [IC de 95 % : de 0,3 % à 2,5 %] par rapport au placebo). Les EI graves (EIGs) associés au vaccin ont rarement été rapportés par ce groupe d'âge, celui-ci n'ayant indiqué qu'une hausse du taux de réactions allergiques observées chez les personnes à qui l'on a administré le VVVCZ. Aucune augmentation dans les EIGs associés au vaccin (p. ex., mesure de l'augmentation des taux d'hospitalisation et d'admission au service d'urgence) n'a été rapportée dans les études d'observation examinéesNote de bas de page 46 Note de bas de page 69 Note de bas de page 101 Note de bas de page 102 . Les études qui ont évalué l'innocuité de l'administration du VVVCZ chez les personnes de plus de 60 ans ayant par le passé contracté le zonaNote de bas de page 83 Note de bas de page 103 Note de bas de page 104 ont indiqué des taux semblables d'EI à ceux rapportés par les personnes non précédemment immunisées par le VVVCZ.
IV.8.2 Événements indésirables associés au VRZ dans la population générale
L'innocuité du VRZ a fait l'objet d'une enquête dans sept études randomiséesNote de bas de page 71 Note de bas de page 72 Note de bas de page 86 Note de bas de page 105 Note de bas de page 106 Note de bas de page 107 Note de bas de page 108 .
Les deux études majeures consistaient en deux essais pivots dans le cadre desquels plus de 14 000 adultes de plus de 50 ans ont reçu deux doses du VRZ. Parmi les études mentionnées dans la recherche documentaire, quatre étaient de bonne qualité et trois, jugées de qualité passable (voir les tableaux sommaires des données probantes, Annexe C).
Des EI au point d'injection étaient couramment rapportés par les participants, dont environ 80 % ont indiqué une douleur et environ 30 %, une rougeur. Dans un essai pivot évaluant l'innocuité du vaccin chez plus de 15 400 adultes de 50 ans et plus, des réactions de catégorie 3 au point d'injection (des EI suffisamment graves pour empêcher de mener des activités normales) ont été rapportées par 9,5 % (IC de 96 % : de 8,7 % à 10,4 %) des personnes ayant reçu le vaccin par rapport au 0,4 % (IC de 95 % : de 0,2 % à 0,6 %) des personnes ayant reçu un placebo. Parmi les adultes de 70 ans et plus, des EI de catégorie 3 au point d'injection ont été rapportés par 8,5 % (IC de 95 % : de 6,2 % à 11,3 %) des personnes ayant reçu le vaccin et par 0,2 % (IC de 95 % : de 0 % à 1,1 %) des personnes ayant reçu un placebo. Une douleur a généralement été rapportée plus souvent par les participants de moins de 70 ans par rapport à ceux de 70 ans et plus. La durée médiane des EI rapportés au point d'injection était de 2 à 3 jours.
Les EIS les plus souvent rapportés dans les essais cliniques étaient une fatigue et une myalgie (rapportées par jusqu'à la moitié des personnes ayant reçu le vaccin) ainsi que des céphalées (rapportés par jusqu'à 40 % des personnes ayant reçu le vaccin). Dans un essai pivot ayant évalué l'innocuité des vaccins chez plus de 15 400 adultes de plus de 50 ans, des réactions systémiques de catégorie 3 ont été rapportées par 11,4 % (IC de 95 % : de 10,5 % à 12,4 %) des personnes ayant reçu le vaccin par rapport à 2,4 % (IC de 95 % : de 2 % à 2,9 %) des personnes ayant reçu un placebo. Parmi les adultes de 70 ans et plus, des EIS de catégorie 3 ont été rapportés par 6 % (IC de 95 % : de 4,1 % à 8,4 %) des personnes ayant reçu le vaccin et par 2 % (IC de 95 % : de 1 % à 3,6 %) des personnes ayant reçu un placebo. Les événements systémiques comprenant des réactions de catégorie 3 étaient plus souvent signalés après l'administration de la deuxième dose du VRZ. La durée médiane des EIS rapportés était de 1 à 2 jours.
Dans l'ensemble, les taux d'EIGs observés dans les études examinées étaient semblables entre l'intervention et les groupes de contrôle, puisqu'aucun EIG n'était considéré comme étant lié aux vaccins par les enquêteurs de l'étude selon la plausibilité et le temps écoulé depuis la vaccination. Les taux d'EIGs rapportés et de maladies d'origine immunologique liés au vaccin étaient semblables pour le vaccin et le groupe du placebo, et ce, jusqu'à 9 ans après l'immunisation.
IV.9 Contre-indications et précautions
IV.9.1 Contre-indications et précautions en ce qui concerne le VVVCZ
Le VVVCZ est contre-indiqué chez les personnes ayant des antécédents d'hypersensibilité à tout composant du vaccin, y compris la gélatine, ou une réaction anaphylactique ou anaphylactoïde à la néomycine (présente à l'état de trace dans le vaccin).
Puisqu'il s'agit d'un vaccin à virus vivant pouvant entraîner une maladie disséminée chez les personnes immunodéprimées ou immunodéficientes, le VVVCZ est contre-indiqué chez les personnes atteintes d'un état d'immunodéficience primaire ou acquise, mais n'est toutefois pas contre-indiqué chez les personnes recevant des corticostéroïdes topiques ou inhalés, de faibles doses de corticostéroïdes systémiques ou des corticostéroïdes dans le cadre d'une thérapie de remplacement (p. ex., pour une insuffisance surrénale). Il est contre-indiqué chez les personnes atteintes de tuberculose active non traitée.
Le VVVCZ est contre-indiqué durant la grossesse, et toute grossesse devrait être évitée durant les 3 mois suivant l'administration du vaccin. Bien qu'aucune étude n'ait été menée auprès de cette population, une infection naturelle par le VVZ est une source connue d'effets nocifs pour le fœtus dans certains cas.
Il faut faire preuve de précaution lorsque le VVVCZ est administré aux femmes qui allaitent, puisqu'on ne sait pas si le VVZ est sécrété dans le lait maternel. En présence d'une fièvre de plus de 38,5 °C, il faut envisager de reporter la vaccinationNote de bas de page 57 .
IV.9.2 Contre-indications et précautions en ce qui concerne le VRZ
Le VRZ est contre-indiqué chez les personnes atteintes d'une hypersensibilité à tout composant du vaccin.
Ce vaccin devrait être utilisé avec précaution chez les femmes enceintes (puisque nous n'avons aucune donnée sur son utilisation dans cette population) ou qui allaitent (puisque les effets sur les nouveau-nés allaités par les femmes ayant reçu le vaccin n'ont pas été étudiés). L'innocuité et l'efficacité du vaccin chez les personnes de moins de 18 ans n'ont pas été étudiées, et on ne possède que des données limitées sur son utilisation chez les personnes immunodéprimées de 50 ans et plusNote de bas de page 58.
V. Économie
V.1 Description du modèle économique
Afin d'estimer le RCE de la vaccination contre le zona, une analyse coût-utilité (ACU) a été adaptée des recherches de Brisson et al. (2008)Note de bas de page 11 pour comparer les résultats cliniques et économiques de différentes options de vaccination.
Dans l'étude en question, les auteurs ont comparé le VVVCZ à l'absence de vaccination dans une cohorte traversant les différentes phases du zona. Le modèle a été élargi de sorte à comprendre le VRZ. Par conséquent, cette ACU: 1) a évalué le RCE de la vaccination contre le zona au moyen d'un ou des deux vaccins (VVVCZ et VRZ) par rapport à l'absence de vaccination et 2) a comparé le RCE entre le VVVCZ et le VRZ. En bref, le modèle suit une cohorte de personnes traversant les différentes phases du zona. Comme le démontre la Figure 4, différentes phases du zona sont représentées par les boîtes et flêches indiquant les étapes de transition de la maladie. A priori, les individus sont assumés non-atteint, mais susceptible de developer le zona. Une probabilité d'engendrer la NPZ est ensuite appliquée à la proportion d'individus ayant développé le zona. Le décès est également associé à chaque état de santé. Les cas de zona et de NPZ sont catégorisés en fonction de la gravité de la douleur : aucune douleur, une douleur faible ou modérée et une douleur importante. Ce modèle compare l'incidence du zona et de la NPZ entre les cohortes de personnes vaccinées et non vaccinées.
La perspective de l'étude est celle du système de soins de santé, lequel comprend tous les coûts médicaux directs pour le traitement de la maladie. Quant à la perspective sociétale, qui prend en compte les coûts extérieurs à ceux du système de soins de santé, comme la productivité perdue, elle n'a pas été retenue, puisque ces coûts sortent du cadre des programmes de vaccination et du système de soins de santé. Le scénario de référence suppose une vaccination des personnes de 65 ans. D'autres analyses ont également examiné la vaccination des personnes âgées de 50 à 85 ans. La cohorte est modélisée tout au long de la vie, avec un taux d'escompte des coûts et des avantages de 3%.
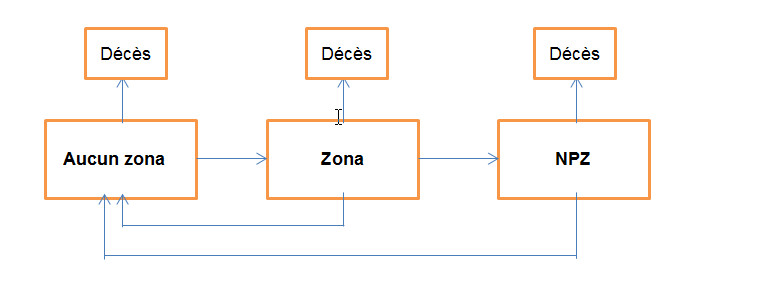
Figure 4 - Équivalent du texte
La figure 4 démontre différents états (boîtes oranges) associées au zona. Les boîtes représentent les phases Aucun zona, avec zona, avec NPZ et décès. La transition d'une phase de la maladie vers une autre est démontrée par des flèches. À la phase Aucun zona, les flèches démontrent que la maladie peut engendrer une transition vers le zona, la NPZ ou le décès. À la phase de Zona, les flèches démontrent que la maladie peut engendrer une transition vers la NPZ, le décès ou un retour à l'état Aucun zona. À la phase de NPZ, les flèches démontrent que la maladie peut engendrer une transition vers le décès ou un retour à l'état Aucun zona. Le retour à Aucun zona arrive subséquemment au traitement de la maladie.
V.2 Paramètres du modèle : épidémiologie, caractéristiques des vaccins et économie
Les paramètres du modèle peuvent être catégorisés par les données sur l'épidémiologie, les caractéristiques des vaccins et l'économie (Tableau 5). Les caractéristiques des vaccins sur l'efficacité pour le VRZ et le VVVCZ reposaient sur des essais cliniquesNote de bas de page 61 Note de bas de page 63 Note de bas de page 71 Note de bas de page 72 . Les données épidémiologiques sur les incidences du zona et d'une hospitalisation connexe axées sur l'âge proviennent de bases de données administratives du QuébecNote de bas de page 109 Note de bas de page 110 et d'une revue de la littérature. Les articles repérés dans cette revue proviennent de l'OntarioNote de bas de page 29 , de la Colombie-BritanniqueNote de bas de page 26 et de l'AlbertaNote de bas de page 27 .
L'étude en question a examiné les valeurs minimales et maximales de ces sources de données, et le scénario de référence retenu est la moyenne de ces valeurs. D'autres données sur la durée du séjour, des consultations par cas et de NPZ par cas tirent leur origine de la littératureNote de bas de page 11 Note de bas de page 24 Note de bas de page 63 Note de bas de page 111 , de MedEchoNote de bas de page 110 et de la Régie de l'assurance maladie du Québec (RAMQ)Note de bas de page 109 .
Les données économiques sur les coûts, provenant de la littérature, ont été ajustées à la valeur du dollar canadien de 2015. Des coefficients de pondération d'utilité correspondant aux divers états de santé ont été utilisés dans l'estimation des années de vie ajustées par la qualité (AVAQ). Ces données ont été compilées à partir de l'étude MASTER (Monitoring and Assessing Shingles Through Education and Research)Note de bas de page 112 et de celles de Brisson et alNote de bas de page 11 .
| Paramètres | Source de données |
|---|---|
| Utilisation de la ressource liée à l'épidémiologie et aux soins de santé | |
| Incidence du zona | RAMQ 2001-2015, Brisson et al. 2008, Tanuseputro et al. 2011, Marra et al. 2016, Russell et al. 2014. |
| Hospitalisations | MedEcho 2001-2015, Brisson 2008, Tanuseputro et al. 2011, Brisson et al. 2001 |
| Consultations (par cas) | RAMQ 2001-2015, Brisson et al. 2008, Najafzadeh et al. 2009 |
| Durée du séjour (journées) | MedEcho 2001-2015, Brisson et al. 2001, Najafzadeh et al. 2009 |
| Taux de létalité | Brisson et al. 2008 |
| Risque de NPZ (par cas) | Oxman et al. 2005, Brisson et al. 2008 |
| Caractéristiques du vaccin | |
| Shingrix®(VRZ) | |
| ZOE-50 | Lal et al 2015 |
| ZOE-70 | Cunningham et al 2016 |
| Zostavax®(VVVCZ) | |
| SPS | Oxman et al. 2005 |
| STPS | Schmader et al. 2012 |
| Économie | |
| Coûts unitaires (ajustés selon la valeur du dollar canadien de 2015) | |
| Consultations d'un médecin généraliste concernant le zona | Friesen et al. 2017Note a, Najafzadeh et al. 2009, Brisson et al. 2008 |
| Hospitalisations associées au zona | Friesen et al. 2017Note a, Najafzadeh et al. 2009, Brisson et al. 2008 |
| Traitement pour un épisode de zona | Friesen et al. 2017Note a, Najafzadeh et al. 2009, Brisson et al. 2008 |
| Traitement pour un épisode de NPZ | Friesen et al. 2017Note a, Najafzadeh et al. 2009, Brisson et al. 2008 |
| Coéfficients de pondération d'utilité (estimations des AVAQ) | Brisson et al. 2008, Drolet et al. 2010 |
|
|
V.2.1 Paramètres du modèle : caractéristiques du vaccin
Les caractéristiques du vaccin ont été définies par l'EV et le taux de déclin. L'EV tient compte de la proportion de personnes protégées suivant l'immunisation et leur niveau de protection. Le taux de déclin est le taux auquel la protection conférée par le vaccin diminue au fil du temps. Les valeurs des paramètres d'EV propres aux deux vaccins ont été estimées en ajustant l'incidence annuelle du zona selon l'âge prédit par le modèle avec les valeurs observées dans les données tirées des ECR pour le groupe de personnes vaccinées à l'aide de six fonctions différentes pour mesurer le déclin de l'efficacité au fil du temps (linéaire, exponentiel-1, à la puissance, exponentiel, logarithmique et à la puissance-1). Cette méthode, fondée sur les études de modélisation antérieuresNote de bas de page 11 Note de bas de page 113, permet d'estimer l'efficacité à court terme des vaccins et le déclin de leur efficacité grâce aux essais cliniques, et permet également d'examiner les incertitudes quant à l'efficacité à long terme des deux vaccins. La Figure 5 illustre les résultats de calibration de l'efficacité vaccinale prédite par rapport aux données des ECR (efficacité contre le zona selon l'âge, efficacité contre le zona selon les années écoulées depuis la vaccination, efficacité contre la NPZ selon l'âge).
Les valeurs des paramètres d'EV propres à l'âge ont été utilisées dans ce modèle. À chaque âge, l'EV était supérieure pour le VRZ par rapport au VVVCZ. Pour le VVVCZ, l'EV contre la NPZ a été estimée supérieure à l'EV contre le zona pour les personnes de plus de 70 ans (comme le démontre Brisson et al. 2008). Pour le VRZ, les essais n'ont pas indiqué de différence significative dans l'EV contre le zona et la NPZ, et le modèle a présumé que tant l'EV initiale que l'efficacité déclinante étaient semblables pour les indicateurs de résultat du zona et de la NPZ. Le scénario de référence suppose la pleine conformité de l'administration d'une série de deux doses du VRZ.
Figure 5 : EV ajustée selon les données tirées des essais cliniques vaccinaux
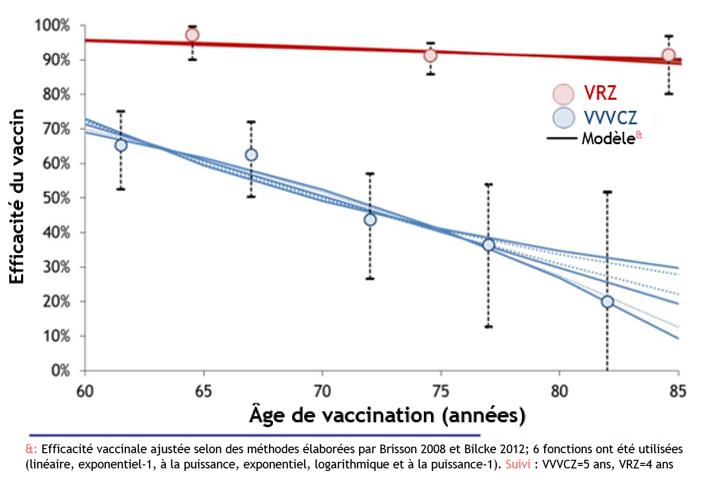
Figure 5A - Équivalent du texte
La Figure 5A démontre des graphes linéaires de l'efficacité vaccinale en fonction de l'âge.
L'axe horizontal représente l'âge à la vaccination à partir de 60 à 85 ans, en incréments de 5 années. L'axe vertical représente l'efficacité vaccinale en pourcentage de 0% à 100% en incréments de 10%.
Les lignes rouges associées au VRZ et les lignes bleues associées au VVVCZ démontrent l'efficacité vaccinale estimée. Le VRZ et le VVVCZ ont chacun 6 lignes basées sur six différentes estimations d'efficacité vaccinale.
Des boutons rouges et bleus associées à des intervalles de confiance représentant les efficacités vaccinales des essais cliniques pour tous les âges longent les estimées linéaires du VRZ et du VVVCZ afin de corroborer leur précision.
L'efficacité vaccinale du VRZ est similaire pour les six estimations linéaires. À l'âge de 60 ans, l'efficacité vaccinales est supérieure à 95% et décline à près de 90% à l'âge de 85 ans.
L'efficacité vaccinale des six lignes associées au VVVCZ sont similaires mais le taux de déclin diffère après l'âge de 75 ans. L'efficacité vaccinale est près de 70% à l'âge de 60 ans et décline jusqu'à près de 10% à 30% à l'âge de 85 ans.
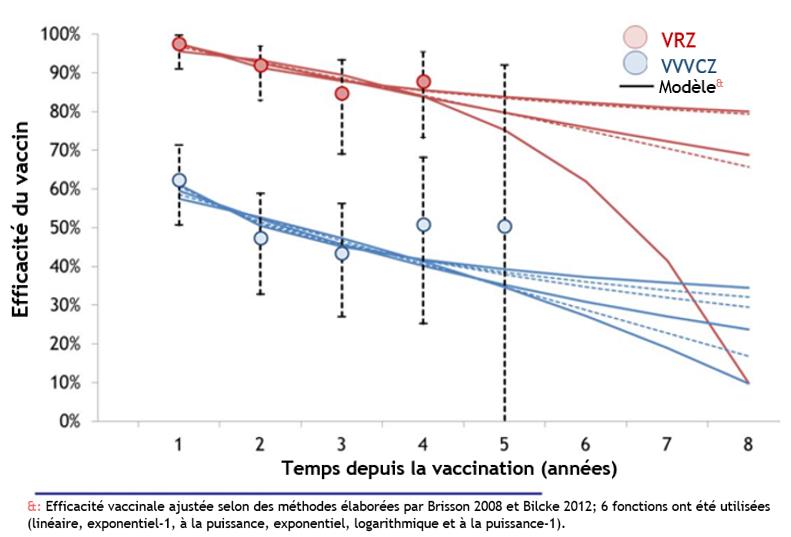
Figure 5B - Équivalent du texte
La Figure 5B démontre des graphes linéaires de l'efficacité vaccinale en fonction du temps depuis la vaccination.
L'axe horizontal représente le temps depuis la vaccination de la première à la huitième année en incréments annuel. L'axe vertical représente l'efficacité vaccinale en pourcentage de 0% à 100% en incréments de 10%.
Les lignes rouges associées au VRZ et les lignes bleues associées au VVVCZ démontrent l'efficacité vaccinale estimée. Le VRZ et le VVVCZ ont chacun 6 lignes basées sur six différentes estimations d'efficacité vaccinale.
Des boutons rouges et bleus associées à des intervalles de confiance représentant les efficacités vaccinales des essais cliniques de la première à la quatrième année depuis la vaccination longent les estimées linéaires du VRZ et du VVVCZ afin de corroborer leur précision. L'efficacité vaccinale du VRZ est similaire pour les six estimées linéaires entre les années 1-4, se maintenant aux alentours de 90%. Après la quatrième année, cinq des six estimées linéaires restent similaires, démontrant une efficacité vaccinale entre 70% et 85% après 8 années. Considérablement, la sixième estimée linéaire démontre un déclin jusqu'à une efficacité vaccinale de 10% huit années après la vaccination.
L'efficacité vaccinale du VVVCZ est similaire pour les six estimées linéaires mais se différencie après la marque des 5-ans. L'efficacité vaccinale diminue des environs de 60% jusqu'à 40% pendant les 5 premières années, après lesquelles les estimées atteignent un maximum près de 40% et un minimum près des 10% à la marque des 8 années, le restant des estimées restant séparées entre ces valeurs.
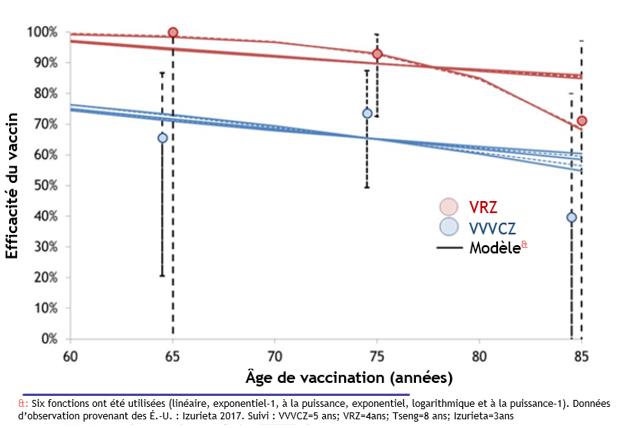
Figure 5C - Équivalent du texte
La Figure 5C démontre des graphes linéaires de l'efficacité vaccinale contre la NPZ en fonction de l'âge à la vaccination.
L'axe horizontal représente l'âge à la vaccination à partir de 60 à 85 ans, en incréments de 5 années. L'axe vertical représente l'efficacité vaccinale en pourcentage de 0% à 100% en incréments de 10%.
Les lignes rouges associées au VRZ et les lignes bleues associées au VVVCZ démontrent l'efficacité vaccinale estimée. Le VRZ et le VVVCZ ont chacun 6 lignes basées sur six différentes estimations d'efficacité vaccinale.
Des boutons rouges et bleus associées à des intervalles de confiance représentant les efficacités vaccinales des essais cliniques pour tous les âges longent les estimées linéaires du VRZ et du VVVCZ afin de corroborer leur précision.
L'efficacité vaccinale du VRZ est similaire pour les six estimations linéaires, démontrant une efficacité de 90% à presque 100% pour les âges de 60 à 80 ans. À l'âge de 80 ans, l'efficacité vaccinale aux alentours de 90% reste constante pour 4 des 6 estimées linéaires, tandis que deux estimées linéaires démontrent une diminution de l'efficacité atteignant près de 75% à l'âge de 85 ans. L'efficacité vaccinale du VVVCZ est similaire pour les six estimées linéaires, démontrant une diminution lente mais constante à partir d'environ 75% à l'âge de 60 ans jusqu'à près de 65% à l'âge de 85 ans.
V.2.2 Paramètres du modèle : estimations de l'utilisation des ressources épidémiologiques et liées aux soins de santé
Les paramètres pour l'utilisation de la ressource liée à l'épidémiologie et aux soins de santé sont présentés dans le Tableau 6. Pour tous les paramètres, ceux de Brisson et al. 2008 ont été examinés et mis à jour au moyen de revues de la littérature et d'analyses spécifiques sur les sources de données disponibles. Les paramètres concernant l'incidence du zona, les consultations médicales, hospitalisations et décès connexes ont été actualisés au moyen d'une revue systématique de la littérature et de l'analyse des bases de données administratives du Québec (RAMQ et banque de données Med-Echo sur les hospitalisations). Les paramètres du Tableau 6 représentent les valeurs minimales et maximales qui ont été trouvées dans la littérature et qui proviennent également de l'analyse des bases de données administratives non publiées du Québec. Le scénario de référence représente la moyenne des valeurs minimales et maximales. La NPZ a été définie comme une douleur cliniquement significative persistant pendant plus de 90 jours suivant l'apparition de l'éruption cutanée. La proportion des cas de zona développant la NPZ découle des valeurs minimales et maximales de Brisson et al. 2008, lesquelles reposent sur les données provenant de l'étude Shingles Prevention StudyNote de bas de page 63 et d'Edmunds et al. 2001Note de bas de page 114 . Les valeurs concernant le taux de létalité sont fondées sur des études provenant de l'Angleterre et du Pays de Galles, étant donné l'absence de données canadiennes sur le taux de mortalité attribuable au zona.
| Groupe d'âge | Valeur de référence | Min. | Max. | Source de données |
|---|---|---|---|---|
| Incidence du zona (pour 1 000 années-personnes) | ||||
| 50 à 54 ans | 3,8 | 3,5 | 4,2 | RAMQ 2001-2015 Brisson et al. 2008 Tanuseputro et al. 2011 Russell et al. 2014 Marra et al. 2016 |
| 55 à 64 ans | 6,0 | 5,1 | 6,9 | |
| 65 à 74 ans | 8,6 | 7,3 | 10,0 | |
| 75+ ans | 9,9 | 8,0 | 11,8 | |
| Taux d'hospitalisations (par cas) | ||||
| 50 à 54 ans | 1,1% | 0,5% | 1,6% | MedEcho 2001-2015 Brisson et al. 2008 Tanuseputro et al. 2011 Brisson et al. 2001 |
| 55 à 64 ans | 1,6% | 0,7% | 2,5% | |
| 65 à 74 ans | 3,3% | 1,5% | 5,1% | |
| 75+ ans | 9,9% | 4,1% | 15,6% | |
| Consultations (par cas) | ||||
| 50 à 54 ans | 1,7 | 1,0 | 2,4 | MedEcho 2001-2015 |
| 55 à 64 ans | 2,0 | 1,0 | 2,9 | |
| 65 à 74 ans | 2,3 | 1,0 | 3,5 | |
| 75+ ans | 2,6 | 1,0 | 4,2 | |
| Durée du séjour (jours) | ||||
| 50 à 54 ans | 9,3 | 5,9 | 12,7 | MedEcho 2001-2015 Brisson et al. 2001 Najafzadeh et al. 2009 |
| 55 à 64 ans | 11,1 | 6,2 | 15,9 | |
| 65 à 74 ans | 12,6 | 8,3 | 16,9 | |
| 75+ ans | 18,0 | 12,4 | 23,6 | |
| Taux de létalité | ||||
| 50 à 54 ans | 0,000% | 0,000% | 0,002% | Brisson et al. 2008 |
| 55 à 64 ans | 0,000% | 0,000% | 0,002% | |
| 65 à 74 ans | 0,012% | 0,012% | 0,083% | |
| 75+ ans | 0,076% | 0,040% | 0,083% | |
| Risque de NPZ (par cas) | ||||
| 50 à 54 ans | 9,4% | 6,9% | 11,9% | Oxman et al. 2005 Brisson et al. 2008 |
| 55 à 64 ans | 9,4% | 6,9% | 11,9% | |
| 65 à 74 ans | 26,0% | 18,5% | 33,4% | |
| 75+ ans | 27,7% | 22,0% | 33,4% | |
V.2.3 Paramètres du modèle : économie
Les valeurs des paramètres des données économiques du modèle étaient catégorisées selon les renseignements sur l'établissement des coûts et les estimations des AVAQ dérivées des coéfficients de pondération d'utilité (Tableau 7 et 8). Les coûts représentaient les dépenses associées aux soins de santé utilisés pour traiter le zona calculées à partir de la moyenne des coûts tirés des sources de données recueillies et corrigées en fonction de l'indice des prix à la consommation de 2015. Cela comprend les consultations auprès des médecins généralistes, les hospitalisations ainsi que les coûts des ordonnances et du traitement de la NPZ calculés à partir des données de la littérature (Tableau 7). Les coûts des vaccins représentaient à la fois le prix et les coûts administratifs. Ces coûts tenaient compte de l'incertitude des prix pour le VRZ et le VVVCZ dans le cadre des programmes financés publiquement ainsi que de la variabilité des coûts pour administrer un vaccin dans l'ensemble des provinces et des territoires. Au Canada, les prix annoncés au public sont les « prix courants » ou les prix de détail, lesquels sont tous deux généralement plus élevés que les prix négociés pour les programmes de vaccination provinciaux et territoriaux dans le cadre d'un programme d'achat en masse ou de contrats individuels conclus avec les administrations. Étant donné l'incertitude et la confidentialité des prix négociés ainsi que la variabilité des coûts administratifs, le scénario de référence a plutôt examiné les coûts des vaccins de 140 $ et 200 $ (prix et administration). Les coéfficients de pondération d'utilité ont été utilisés dans l'estimation des AVAQ. Ces pondérations varient de 0 à 1, 0 représentant un décès et 1 une pleine santé (ou l'absence de handicap). Les pondérations établies entre les valeurs maximales et minimales représentent la morbidité à diverses capacités fonctionnelles en matière de santé. Les AVAQ perdues par cas (qu'il s'agisse du zona ou de la NPZ) constituent la différence dans les coéfficients de pondération d'utilité avec et sans maladie au fil du temps. Les données sur le coéfficient de pondération d'utilité ont été obtenues à partir de l'étude MASTERNote de bas de page 112 et de Brisson et al. 2008Note de bas de page 11 . Le scénario de référence représente la moyenne des valeurs minimales et maximales (Tableau 8).
| Paramètres | Coûts ($ CAN en 2015) | Source de données | ||
|---|---|---|---|---|
| Scénario de référence | Min. | Max. | ||
| Hospitalizations | 876 $ | 473$ | 1 419$ | Friesen et al. 2017Note a Najafzadeh et al. 2009 Brisson et al. 2008 |
| Consultations | 27 $ | 23$ | 108$ | Friesen et al. 2017Note a Najafzadeh et al. 2009 Brisson et al. 2008 |
| Traitement par épisode de zona | 129 $ | 52$ | 244$ | Friesen et al. 2017Note a Najafzadeh et al. 2009 Brisson et al. 2008 |
| Traitement par épisode de NPZ | 1 515 $ | 924$ | 2 591$ | Friesen et al. 2017Note a Najafzadeh et al. 2009 Brisson et al. 2008 |
Min : Valeurs minimales définies dans la littérature; Max : Valeurs maximales définies dans la littérature; scénario de référence : valeurs tirées de Friesen et al. 2017
|
||||
| Groupe d'âge | AVAQ perdues (valeurs utilitaires) | Source de données | ||
|---|---|---|---|---|
| Scénario de référence | Min. | Max. | ||
| Zona | ||||
| 50 à 59 ans | 0,009 | 0,006 | 0,012 | Brisson et al 2008 Drolet et al 2010 |
| 60 à 69 ans | 0,010 | 0,006 | 0,013 | |
| 70+ ans | 0,010 | 0,007 | 0,014 | |
| NPZ | ||||
| 50 à 59 ans | 0,041 | 0,032 | 0,052 | Brisson et al 2008 Drolet et al 2010 |
| 60 à 69 ans | 0,192 | 0,103 | 0,290 | |
| 70+ ans | 0,234 | 0,191 | 0,290 | |
Min : Valeurs minimales définies dans la littérature; Max : Valeurs maximales définies dans la littérature; scénario de référence : valeurs tirées de Friesen et al. 2017 |
||||
V.3 Résultats
Toutes les estimations du modèle ont été fondées sur 30 000 simulations et présentent des valeurs médianes et des intervalles d'incertitude (II) de 90 % ainsi que les 5e et 95e percentiles de la distribution des résultats de simulation. Pour obtenir ces estimations, une distribution triangulaire de probabilité a eté attribué à chaque paramètre, et des combinaisons de ces valeurs de paramètre ont été tirées au moyen de la méthode d'échantillonnage par hypercube latin. Les valeurs minimales et maximales de la distribution triangulaire représentent les valeurs minimales et maximales déterminées à partir de la littérature, et les valeurs médianes constituent les valeurs pour le scénario de référence qui se trouve dans les Tableaux 6, 7 et 8.
V.3.1 Résultats : Rapport coût-efficacité
Les résultats du scénario de référence ont tenu compte des personnes de 65 ans (Figure 6). Le VRZ offre un rapport coût-efficacité différentiel (RCED) médian variant de la réalisation d'économies à 6 356 $ par AVAQ pour différents coûts liés aux vaccins (100 $-200 $). Le VVVCZ comporte un RCED médian plus élevé variant de 7 673 $ à 37 249 $ par AVAQ et s'avère donc moins rentable que le VRZ.
La Figure 7 présente les résultats pour tous les groupes d'âge selon les différents coûts pour les vaccins. En comparaison à l'utilisation du VVVCZ, le VRZ s'avère moins coûteux par AVAQ pour tous les groupes d'âge et les différents coûts pour les vaccins et, par conséquent, est plus rentable que le VVVCZ. Pour le groupe d'âge 65-79 ans, le VRZ est le plus rentable par rapport aux autres groupes d'âge en raison du fardeau plus élevé de la maladie associé à l'âge (augmentation du risque des hospitalisations et de la NPZ pour les cas de zona) et de la probabilité que le vaccin soit efficace pendant les années au cours desquelles le fardeau de la maladie est plus élevé (à moins que l'EV décline plus rapidement que prévu).
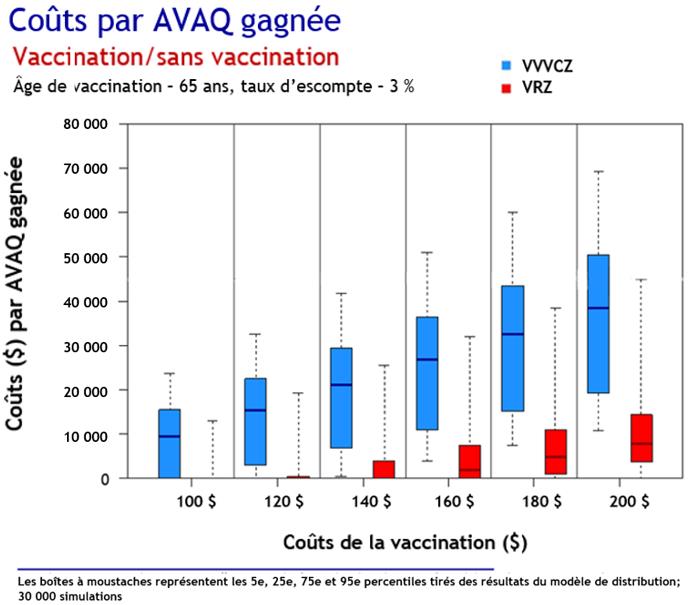
Figure 6 - Équivalent du texte
| Âge à la vaccination/ Coût du vaccin | VVVCZ Percentiles prédits par modèle |
VRZ Percentiles prédits par modèle |
||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 5e | 25e | Médiane | 75e | 95e | 5e | 25e | Médiane | 75e | 95e | |
| 65 ans | ||||||||||
| 100 $ | EC | EC | 7 673 | 14 224 | 22 710 | EC | EC | EC | EC | 11 778 |
| 120 $ | EC | 1 688 | 13 647 | 21 334 | 31 929 | EC | EC | EC | EC | 18 187 |
| 140 $ | EC | 5 828 | 19 576 | 28 434 | 41 349 | EC | EC | EC | 2 922 | 24 715 |
| 160 $ | 1 064 | 9 960 | 24 486 | 35 614 | 50 822 | EC | EC | 488 | 6 359 | 31 295 |
| 180 $ | 4 686 | 14 139 | 31 345 | 42 810 | 60 345 | EC | EC | 3 414 | 9 874 | 37 839 |
| 200 $ | 8 235 | 18 344 | 37 249 | 49 994 | 70 059 | EC | 1 507 | 6 356 | 13 433 | 44 382 |
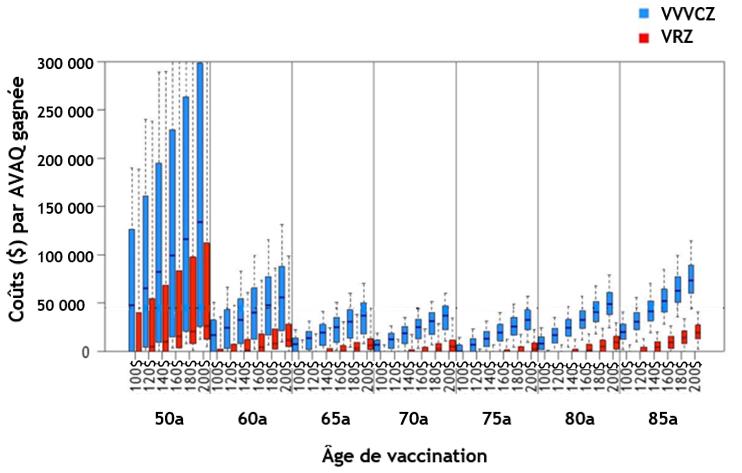
Figure 7 - Équivalent du texte
| Âge à la vaccination/ Coût du vaccin | VVVCZ Percentiles prédits par modèle |
VRZ Percentiles prédits par modèle |
||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 5e | 25e | Médiane | 75e | 95e | 5e | 25e | Médiane | 75e | 95e | |
| 50 ans | ||||||||||
| 100 $ | EC | EC | 48 218 | 126 144 | 190 174 | EC | EC | EC | 40 129 | 188168 |
| 120 $ | EC | 4 595 | 65 295 | 160 411 | 239 776 | EC | EC | 5 018 | 54 585 | 238517 |
| 140 $ | EC | 9 938 | 82 335 | 194 883 | 289 253 | EC | 288 | 10 391 | 68 986 | 289570 |
| 160 $ | 3 777 | 15 269 | 99 362 | 229 146 | 339 041 | EC | 4 266 | 15 704 | 83 534 | 339960 |
| 180 $ | 7 995 | 20 713 | 116 389 | 263 419 | 388 706 | 1 320 | 8 214 | 21 128 | 97 972 | 390442 |
| 200 $ | 12 200 | 26 172 | 133 416 | 297 892 | 438 704 | 5 067 | 12 164 | 26 651 | 112450 |
441319 |
| 60 ans | ||||||||||
| 100 $ | EC | EC | 16 723 | 32 160 | 50 672 | EC | EC | EC | 2 673 | 35 736 |
| 120 $ | EC | 3 348 | 24 494 | 43 291 | 66 795 | EC | EC | EC | 7 667 | 48 432 |
| 140 $ | EC | 7 844 | 32 343 | 54 540 | 83 021 | EC | EC | 1 401 | 12 826 | 61 003 |
| 160 $ | 2 621 | 12 440 | 40 077 | 65 819 | 99 318 | EC | EC | 4 888 | 17 876 | 73 565 |
| 180 $ | 6 458 | 17 052 | 47 905 | 76 965 | 115 451 | EC | 2 353 | 8 431 | 22 972 | 86 128 |
| 200 $ | 10 151 | 21 691 | 55 856 | 88 191 | 131 697 | EC | 5 398 | 11 995 | 28 126 | 98 793 |
| 65 ans | ||||||||||
| 100 $ | EC | EC | 7 673 | 14 224 | 22 710 | EC | EC | EC | EC | 11 788 |
| 120 $ | EC | 1 688 | 13 647 | 21 334 | 31 920 | EC | EC | EC | EC | 18 187 |
| 140 $ | EC | 5 828 | 19 576 | 28 434 | 41 349 | EC | EC | EC | 2 922 | 24 715 |
| 160 $ | 1 064 | 9 960 | 25 486 | 35 614 | 50 822 | EC | EC | 488 | 6 359 | 31 295 |
| 180 $ | 4 686 | 14 139 | 31 345 | 42 810 | 60 345 | EC | EC | 3 414 | 9 874 | 37 839 |
| 200 $ | 8 235 | 18 344 | 37 249 | 49 994 | 70 059 | EC | 1 507 | 6 356 | 13 433 | 44 382 |
| 70 ans | ||||||||||
| 100 $ | EC | EC | 6 489 | 11 977 | 18 662 | EC | EC | EC | EC | 6 578 |
| 120 $ | EC | 3 517 | 12 759 | 19 026 | 26 835 | EC | EC | EC | EC | 12 122 |
| 140 $ | EC | 8 287 | 19 014 | 26 071 | 35 096 | EC | EC | EC | 1 531 | 17 638 |
| 160 $ | 2 884 | 12 982 | 25 241 | 33 217 | 43 540 | EC | EC | EC | 4 794 | 23 262 |
| 180 $ | 6 983 | 17 770 | 31 446 | 40 397 | 51 967 | EC | EC | 2 322 | 8 142 | 28 963 |
| 200 $ | 11 097 | 22 509 | 37 651 | 47 589 | 60 467 | EC | 498 | 5 345 | 11 513 | 34 667 |
| 75 ans | ||||||||||
| 100 $ | EC | EC | 217 | 6 431 | 14 717 | EC | EC | EC | EC | EC |
| 120 $ | EC | EC | 6 649 | 13 531 | 22 971 | EC | EC | EC | EC | 2 327 |
| 140 $ | EC | 5 272 | 13 078 | 20 750 | 31 439 | EC | EC | EC | EC | 7 122 |
| 160 $ | EC | 11 006 | 19 604 | 28 101 | 40 086 | EC | EC | EC | 1 436 | 12 127 |
| 180 $ | 4 492 | 16 696 | 26 148 | 35 515 | 48 764 | EC | EC | EC | 5 109 | 17 214 |
| 200 $ | 9 457 | 22 290 | 32 659 | 42971 | 57 628 | EC | EC | 2 260 | 8 805 | 22 435 |
| 80 ans | ||||||||||
| 100 $ | EC | 1 440 | 8 414 | 14 995 | 24 843 | EC | EC | EC | EC | 1 238 |
| 120 $ | EC | 8 904 | 16 492 | 24 060 | 35 479 | EC | EC | EC | EC | 6 616 |
| 140 $ | 4 739 | 16 314 | 24 594 | 33 231 | 46 389 | EC | EC | EC | 2 807 | 12 147 |
| 160 $ | 11 471 | 23 585 | 32 758 | 42 483 | 57 379 | EC | EC | 1 175 | 7 203 | 17 856 |
| 180 $ | 18 038 | 30 791 | 40 952 | 51 828 | 68 355 | EC | EC | 5 253 | 11 661 | 23 675 |
| 200 $ | 24 461 | 38 023 | 49 162 | 61 164 | 79 723 | EC | 2 717 | 9 281 | 16 146 | 29 630 |
| 85 ans | ||||||||||
| 100 $ | 1 538 | 12 753 | 20 428 | 28 498 | 41 271 | EC | EC | EC | EC | 6 854 |
| 120 $ | 10 580 | 22 376 | 31 013 | 40 526 | 55 661 | EC | EC | EC | 4 826 | 13 360 |
| 140 $ | 19 343 | 31 855 | 41 575 | 52 584 | 70 095 | EC | EC | 4 392 | 10 394 | 20 133 |
| 160 $ | 27 814 | 41 316 | 52 256 | 64 758 | 84 823 | EC | 3 158 | 9 522 | 16 053 | 26 970 |
| 180 $ | 36 051 | 50 716 | 62 889 | 77 032 | 99 751 | EC | 8 061 | 14 643 | 21 784 | 34 035 |
| 200 $ | 44 151 | 60 056 | 73 533 | 89 362 | 114 693 | 2 694 | 12 894 | 19 800 | 27 617 | 41 170 |
EC = Épargne de coûts |
||||||||||
V.3.2 Résultats : Épidémiologie
Le nombre nécessaire à la vaccination (NNV) – soit le nombre de personnes qui devraient être vaccinées pour éviter un seul cas de zona, de NPZ, de ZO et d'hospitalisation – a été calculé comme suit : nombre de personnes vaccinées divisé par nombre d'événements prévenus. Moins de vaccinations avec le VRZ se sont avérées nécessaires par rapport à celles avec le VVVCZ, et ce, dans tous les groupes d'âge. La Figure 8 indique le NNV nécessaire pour réduire un cas de zona, de NPZ, de ZO et d'hospitalisation. À différents âges, le NNV s'est révélé relativement stable pour le VRZ, indépendamment des résultats. Le VVVCZ requiert plus de vaccinations pour pouvoir prévenir un cas de zona, de NPZ et de ZO chez les personnes plus âgées. Pour les hospitalisations, le VVVCZ requiert relativement plus de vaccinations chez les personnes de 50 à 65 ans et celles de 80 ans et plus par rapport au groupe des 70 à 75 ans.
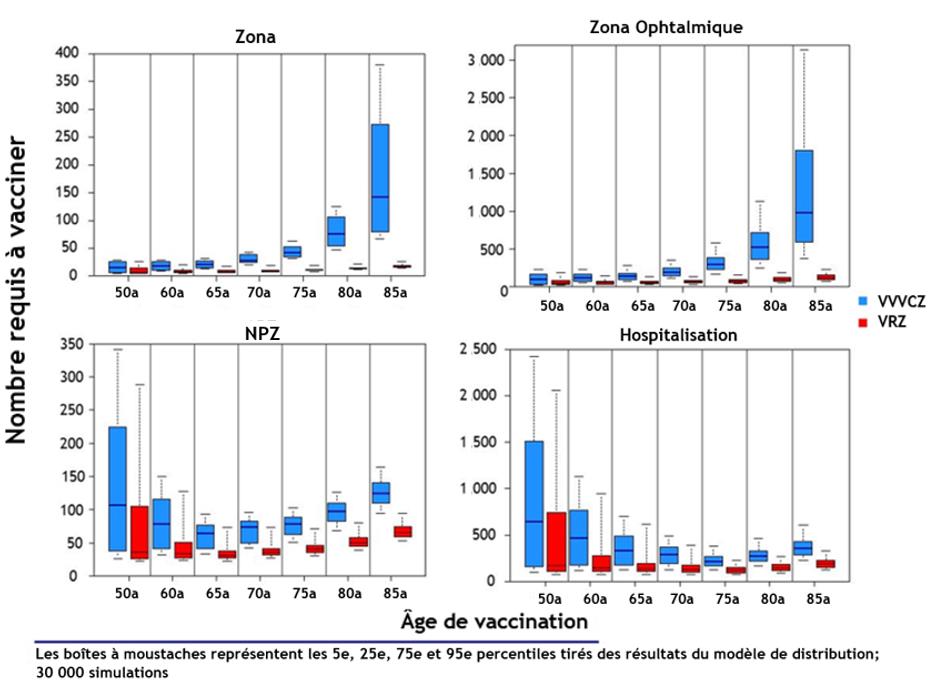
Figure 8 - Équivalent du texte
| Âge à la vaccination | VVVCZ Percentiles prédits par modèle |
VRZ Percentiles prédits par modèle |
||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 5e | 25e | Médiane | 75e | 95e | 5e | 25e | Médiane | 75e | 95e | |
| 50 ans | ||||||||||
| Zona | 6 | 6 | 15 | 26 | 28 | 5 | 5 | 7 | 14 | 26 |
| NPZ | 26 | 37 | 106 | 225 | 341 | 22 | 26 | 36 | 105 | 288 |
| Hospitalisation | 103 | 162 | 638 | 1511 | 2419 | 84 | 108 | 171 | 742 | 2061 |
| Zona Ophtalmique | 34 | 43 | 103 | 173 | 230 | 29 | 36 | 49 | 9626 | 193 |
| 60 ans | ||||||||||
| Zona | 9 | 10 | 18 | 26 | 28 | 6 | 7 | 8 | 11 | 21 |
| NPZ | 31 | 41 | 78 | 116 | 150 | 23 | 27 | 33 | 51 | 128 |
| Hospitalisation | 119 | 178 | 463 | 771 | 1136 | 84 | 111 | 149 | 275 | 947 |
| Zona Ophtalmique | 56 | 74 | 122 | 168 | 229 | 34 | 43 | 54 | 76 | 150 |
| 65 ans | ||||||||||
| Zona | 13 | 14 | 21 | 28 | 31 | 6 | 7 | 8 | 10 | 18 |
| NPZ | 33 | 41 | 64 | 77 | 93 | 23 | 27 | 31 | 38 | 73 |
| Hospitalisation | 124 | 179 | 335 | 491 | 700 | 82 | 107 | 137 | 191 | 613 |
| Zona Ophtalmique | 76 | 102 | 138 | 185 | 285 | 37 | 46 | 57 | 75 | 138 |
| 70 ans | ||||||||||
| Zona | 21 | 24 | 28 | 39 | 43 | 7 | 9 | 9 | 11 | 19 |
| NPZ | 42 | 50 | 73 | 83 | 96 | 27 | 31 | 35 | 40 | 73 |
| Hospitalisation | 133 | 191 | 289 | 374 | 494 | 83 | 106 | 130 | 173 | 385 |
| Zona Ophtalmique | 123 | 157 | 196 | 251 | 362 | 43 | 54 | 65 | 85 | 139 |
| 75 ans | ||||||||||
| Zona | 32 | 35 | 42 | 53 | 63 | 9 | 10 | 11 | 12 | 19 |
| NPZ | 51 | 62 | 78 | 89 | 102 | 31 | 36 | 40 | 46 | 71 |
| Hospitalisation | 126 | 172 | 215 | 267 | 378 | 75 | 95 | 116 | 152 | 226 |
| Zona Ophtalmique | 171 | 230 | 295 | 386 | 586 | 48 | 61 | 77 | 103 | 161 |
| 80 ans | ||||||||||
| Zona | 47 | 54 | 75 | 106 | 125 | 11 | 13 | 14 | 15 | 22 |
| NPZ | 68 | 82 | 97 | 109 | 126 | 40 | 45 | 50 | 57 | 80 |
| Hospitalisation | 169 | 221 | 269 | 333 | 466 | 95 | 119 | 145 | 184 | 267 |
| Zona Ophtalmique | 257 | 365 | 523 | 721 | 1136 | 60 | 77 | 96 | 125 | 190 |
| 85 ans | ||||||||||
| Zona | 67 | 80 | 142 | 273 | 380 | 15 | 17 | 18 | 20 | 25 |
| NPZ | 94 | 110 | 124 | 140 | 164 | 52 | 59 | 66 | 74 | 94 |
| Hospitalisation | 229 | 290 | 351 | 421 | 604 | 125 | 156 | 188 | 234 | 328 |
| Zona Ophtalmique | 377 | 590 | 983 | 1801 | 3133 | 79 | 101 | 124 | 159 | 237 |
V.3.3 Résultats : Analyse de la sensibilité
Des analyses de la sensibilité univariée ont été effectuées pour les paramètres clés du modèle (p. ex., pourcentage des cas de zona provoquant la NPZ, AVAQ ainsi perdues). À cette fin, on a attribué une valeur clé aux valeurs minimale et maximale du modèle et on a fait varier tous les autres paramètres au moyen d'une méthode de distribution triangulaire des probabilités. Ce procédé a été répété pour tous les paramètres clés. Cela a été réalisé selon des coûts différents pour les vaccins (prix et administration) de 140 $ et de 200 $ pour les deux vaccins.
Paramètres épidémiologiques
Les paramètres clés qui variaient dans les analyses de sensibilité univariée sont les suivants : pourcentage des cas de zona provoquant la NPZ, AVAQ ainsi perdues, incidence du zona, hospitalisation et pourcentage de tous les événements éprouvés par les personnes immunocompétentes (Figures 9, 10, 11 et 12). Un fardeau de la maladie plus faible sur les valeurs minimales a entraîné le plus faible RCE (coûts plus élevés par AVAQ), par rapport au scénario de référence, puisqu'il y a moins de cas à prévenir.
D'autre part, les valeurs maximales pour les paramètres ont démontré un plus lourd fardeau de la maladie, ce qui veut dire davantage de cas prévenus et par conséquent un meilleur RCE (coût moindre par AVAQ). Cependant, l'ordre de grandeur des RCED, y compris les conclusions, n'était pas très différent du RCED du scénario de référence pour les deux vaccins. Toutefois, pour le VVVCZ, à 200 $ (prix et administration) (ce qui est supérieur au prix du détail et au prix négocié qui pourrait lui être inférieur), le RCED était de près de 50 000 $ (scénario de référence de près de 37 000 $) lorsque les valeurs minimales (fardeau moindre) étaient utilisées pour les paramètres épidémiologiques clés, exception faite des hospitalisations.
Paramètres économiques
Les paramètres économiques clés qui variaient dans les analyses sont les suivants : coût du traitement pour un épisode de NPZ, hospitalisation, consultations, traitement du zona par épisode et taux de rabais (Figure 13, 14, 15 et 16). Les valeurs minimale et maximale pour chaque paramètre ont donné un RCED médian stable par rapport au scénario de référence pour le VVVCZ et le VRZ et n'ont pas influé sur les conclusions.
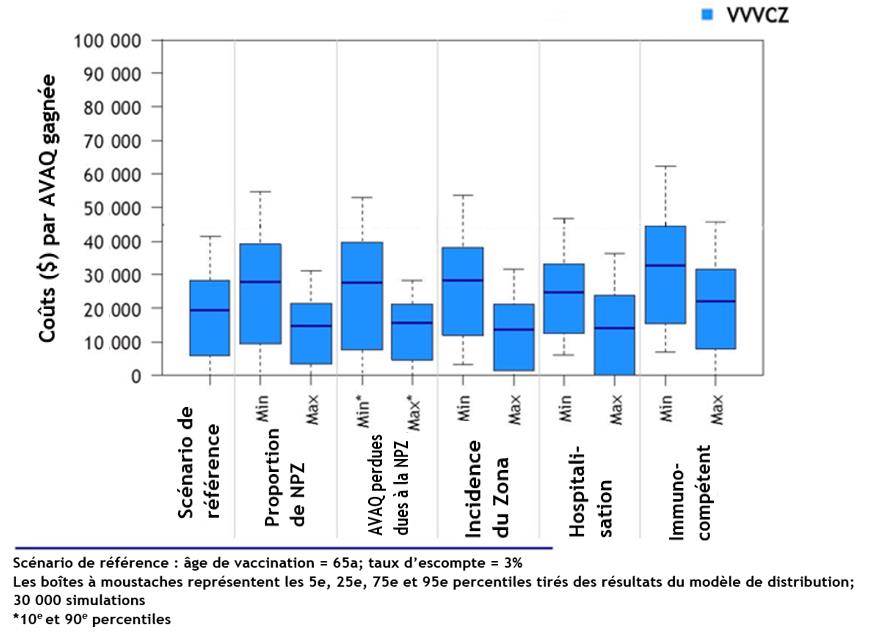
Figure 9 - Équivalent du texte
| Paramètre modifié | VVVCZ Percentiles prédits par modèle |
||||
|---|---|---|---|---|---|
| 5e | 25e | Médiane | 75e | 95e | |
| Scénario de base | EC | 5828 | 19576 | 28 434 | 41 349 |
| Proportion NPZ min | EC | 9486 | 27840 | 39 188 | 54 900 |
| Proportion NPZ max | EC | 3509 | 14760 | 21 436 | 31 088 |
| AVAQs perdues NPZ min | EC | 7591 | 27518 | 39 594 | 52 996 |
| AVAQs perdues NPZ max | EC | 4625 | 15656 | 21 406 | 28 413 |
| Incidence zona min | 3218 | 11871 | 28217 | 38 193 | 53 451 |
| Incidence zona max | EC | 1346 | 13697 | 21 196 | 31 535 |
| Hospitalisations min | 6207 | 12380 | 24725 | 33 084 | 46 842 |
| Hospitalisations max | EC | EC | 14320 | 23 787 | 36 491 |
| Immunocompétent min | 6873 | 15610 | 32836 | 44 548 | 62 448 |
| Immunocompétent max | EC | 7827 | 22135 | 31 635 | 45 684 |
EC : Épargne de coûts; NPZ : Névralgie Post-Zostérienne |
|||||
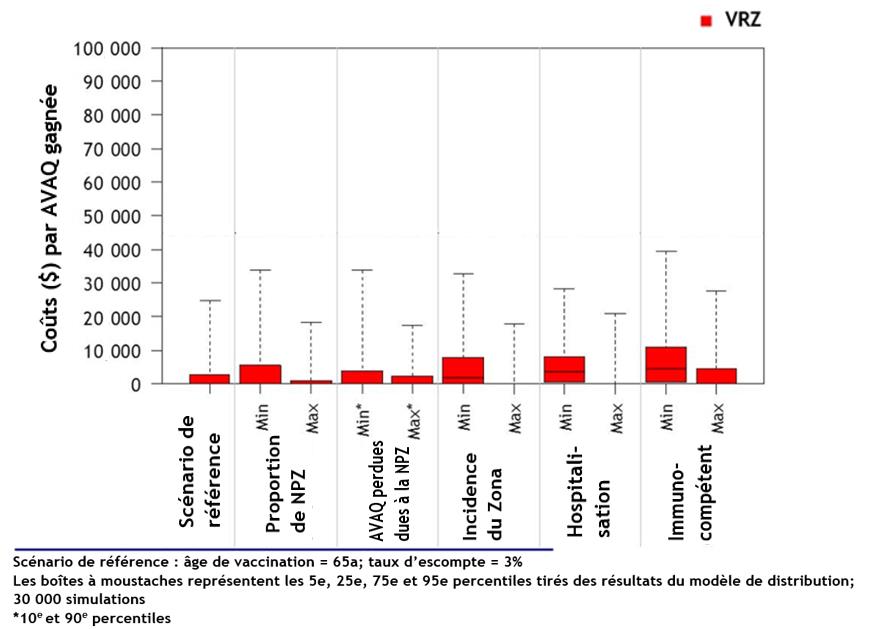
Figure 10 - Équivalent du texte
| Paramètre modifié | VRZ Percentiles prédits par modèle |
||||
|---|---|---|---|---|---|
| 5e | 25e | Médiane | 75e | 95e | |
| Scénario de base | EC | EC | EC | 2 922 | 24 715 |
| Traitement/Épisode NPZ min | EC | EC | EC | 5 673 | 33 889 |
| Traitement/Épisode NPZ max | EC | EC | EC | 1 166 | 18 191 |
| Hospitalisations min | EC | EC | EC | 3 933 | 33 849 |
| Hospitalisations max | EC | EC | EC | 2 359 | 17 604 |
| Consultations min | EC | EC | 1835 | 7 831 | 32 990 |
| Consultations max | EC | EC | EC | EC | 17 994 |
| Traitement/Épisode zona min | EC | 752 | 3671 | 8 287 | 28 213 |
| Traitement/Épisode zona max | EC | EC | EC | EC | 21 080 |
| Taux d'escompte 0% | EC | 564 | 4716 | 11 010 | 39 464 |
| Taux d'escompte 5% | EC | EC | EC | 4 543 | 27 629 |
EC : Épargne de coûts; NPZ : Névralgie Post-Zostérienne |
|||||
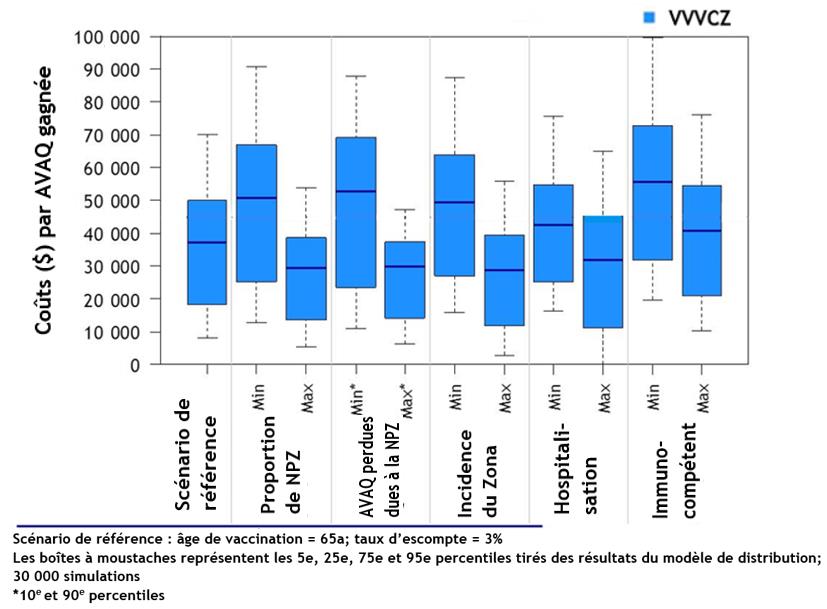
Figure 11 - Équivalent du texte
| Paramètre modifié | VVVCZ Percentiles prédits par modèle |
||||
|---|---|---|---|---|---|
| 5e | 25e | Médiane | 75e | 95e | |
| Scénario de base | 8235 | 18344 | 37249 | 49994 | 70059 |
| Proportion NPZ min | 12597 | 25247 | 50803 | 66789 | 90787 |
| Proportion NPZ max | 5364 | 13608 | 29242 | 38783 | 53821 |
| AVAQs perdues NPZ min | 10892 | 23615 | 52727 | 69056 | 87860 |
| AVAQs perdues NPZ max | 6527 | 14250 | 29869 | 37398 | 47227 |
| Incidence zona min | 15987 | 27073 | 49431 | 63973 | 87371 |
| Incidence zona max | 2915 | 11854 | 28962 | 39538 | 55750 |
| Hospitalisations min | 16308 | 25248 | 42407 | 54724 | 75753 |
| Hospitalisations max | 218 | 11174 | 31893 | 45208 | 64856 |
| Immunocompétent min | 19877 | 31785 | 55579 | 72709 | 99659 |
| Immunocompétent max | 10555 | 20949 | 40773 | 54485 | 75968 |
EC : Épargne de coûts; NPZ : Névralgie Post-Zostérienne |
|||||
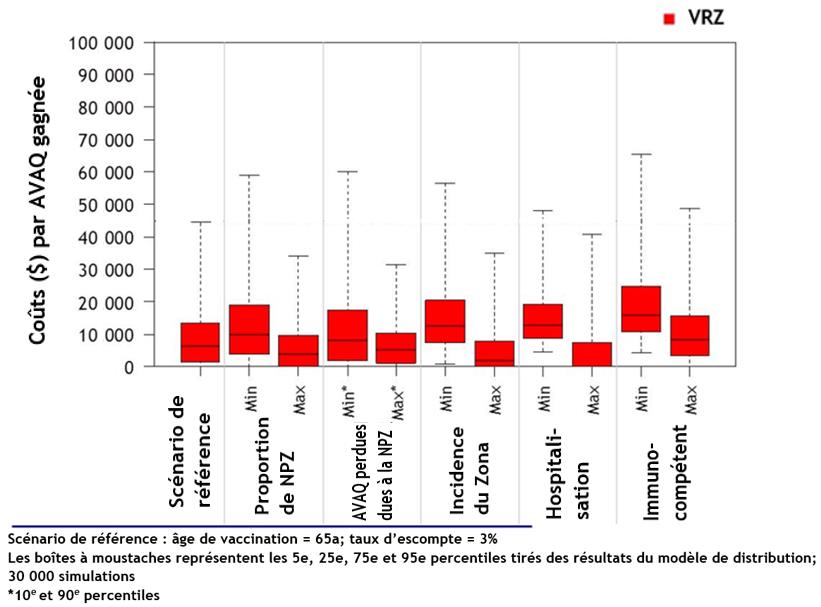
Figure 12 - Équivalent du texte
| Paramètre modifié | VRZ Percentiles prédits par modèle |
||||
|---|---|---|---|---|---|
| 5e | 25e | Médiane | 75e | 95e | |
| Scénario de base | EC | 1507 | 6356 | 13433 | 44382 |
| Traitement/Épisode NPZ min | EC | 3909 | 9990 | 18902 | 59157 |
| Traitement/Épisode NPZ max | EC | EC | 3945 | 9643 | 34022 |
| Hospitalisations min | EC | 1985 | 8183 | 17458 | 60081 |
| Hospitalisations max | EC | 1187 | 5066 | 10460 | 31386 |
| Consultations min | 933 | 7384 | 12525 | 20625 | 56469 |
| Consultations max | EC | EC | 1786 | 7999 | 34829 |
| Traitement/Épisode zona min | 4535 | 8761 | 12631 | 19245 | 48011 |
| Traitement/Épisode zona max | EC | EC | EC | 7469 | 40679 |
| Taux d'escompte 0% | 4473 | 10703 | 15969 | 24885 | 65366 |
| Taux d'escompte 5% | EC | 3438 | 8350 | 15653 | 48629 |
EC : Épargne de coûts; NPZ : Névralgie Post-Zostérienne |
|||||
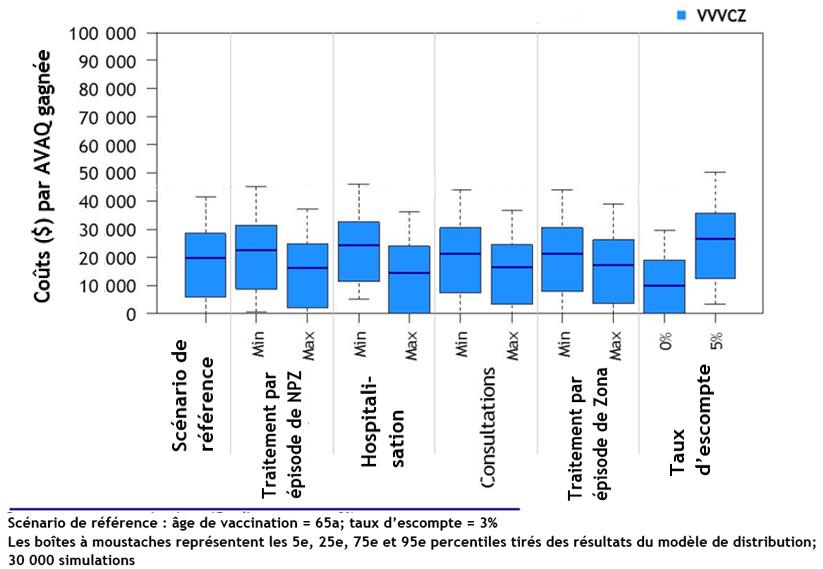
Figure 13 - Équivalent du texte
| Paramètre modifié | VVVCZ Percentiles prédits par modèle |
||||
|---|---|---|---|---|---|
| 5e | 25e | Médiane | 75e | 95e | |
| Scénario de base | EC | 5828 | 19576 | 28434 | 41349 |
| Traitement/Épisode NPZ min | 450 | 8695 | 22420 | 31447 | 45143 |
| Traitement/Épisode NPZ max | EC | 2180 | 16166 | 24674 | 37176 |
| Hospitalisations min | 5135 | 11257 | 24081 | 32450 | 45865 |
| Hospitalisations max | EC | EC | 14572 | 23994 | 36329 |
| Consultations min | EC | 7228 | 21417 | 30385 | 44082 |
| Consultations max | EC | 3262 | 16340 | 24622 | 36548 |
| Traitement/Épisode zona min | EC | 7744 | 21383 | 30461 | 43845 |
| Traitement/Épisode zona max | EC | 3662 | 17478 | 26170 | 38812 |
| Taux d'escompte 0% | EC | EC | 9830 | 19036 | 29650 |
| Taux d'escompte 5% | 3356 | 12449 | 26593 | 35586 | 50347 |
EC : Épargne de coûts; NPZ : Névralgie Post-Zostérienne |
|||||
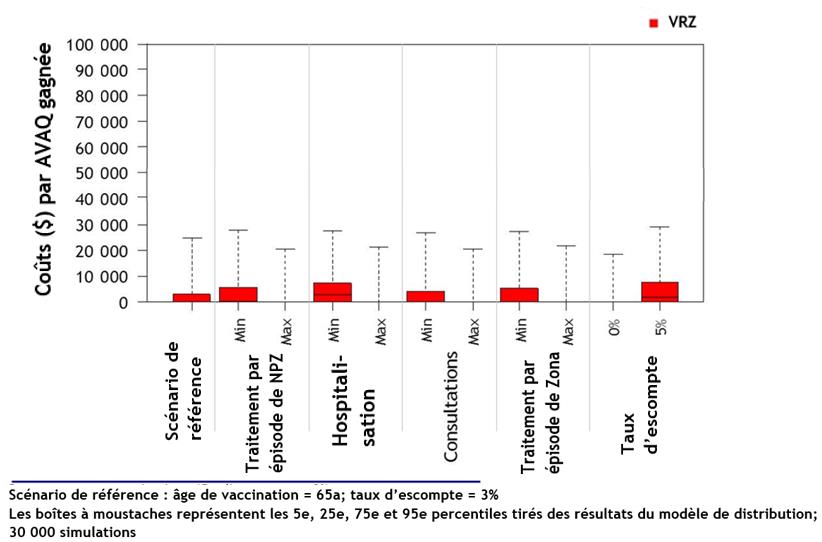
Figure 14 - Équivalent du texte
| Paramètre modifié | VRZ Percentiles prédits par modèle |
||||
|---|---|---|---|---|---|
| 5e | 25e | Médiane | 75e | 95e | |
| Scénario de base | EC | EC | EC | 2922 | 24715 |
| Traitement/Épisode NPZ min | EC | EC | 276 | 5657 | 27801 |
| Traitement/Épisode NPZ max | EC | EC | EC | EC | 20600 |
| Hospitalisations min | EC | EC | 2656 | 7348 | 27565 |
| Hospitalisations max | EC | EC | EC | EC | 21331 |
| Consultations min | EC | EC | EC | 4289 | 26717 |
| Consultations max | EC | EC | EC | 192 | 20543 |
| Traitement/Épisode zona min | EC | EC | EC | 5322 | 27488 |
| Traitement/Épisode zona max | EC | EC | EC | 105 | 21583 |
| Taux d'escompte 0% | EC | EC | EC | EC | 18384 |
| Taux d'escompte 5% | EC | EC | 1843 | 7551 | 29093 |
EC : Épargne de coûts; NPZ : Névralgie Post-Zostérienne |
|||||
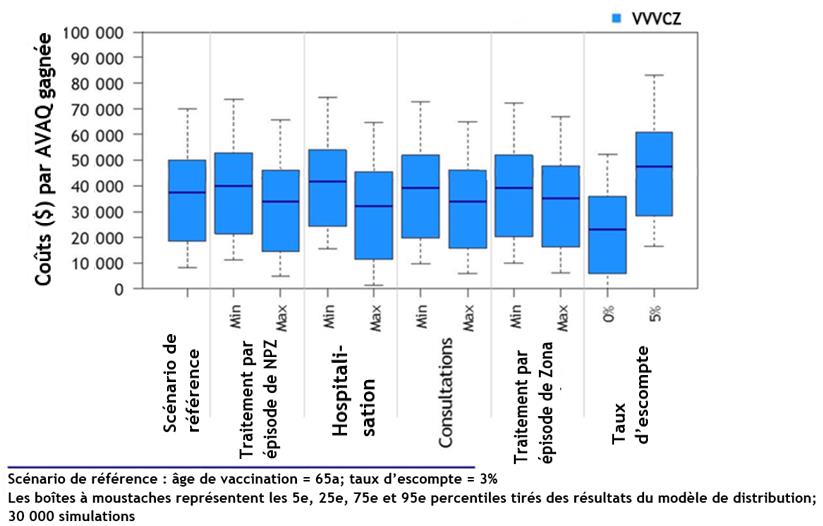
Figure 15 - Équivalent du texte
| Paramètre modifié | VVVCZ Percentiles prédits par modèle |
||||
|---|---|---|---|---|---|
| 5e | 25e | Médiane | 75e | 95e | |
| Scénario de base | 8235 | 18344 | 37249 | 49994 | 70059 |
| Traitement/Épisode NPZ min | 11065 | 21263 | 40092 | 53000 | 73737 |
| Traitement/Épisode NPZ max | 4850 | 14530 | 33893 | 46110 | 65627 |
| Hospitalisations min | 15269 | 24124 | 41754 | 54103 | 74649 |
| Hospitalisations max | 1182 | 11199 | 32165 | 45385 | 64497 |
| Consultations min | 9506 | 19601 | 39027 | 51930 | 72707 |
| Consultations max | 5882 | 15627 | 33903 | 46144 | 65000 |
| Traitement/Épisode zona min | 9986 | 20303 | 39014 | 52045 | 72402 |
| Traitement/Épisode zona max | 6210 | 16056 | 35141 | 47641 | 66898 |
| Taux d'escompte 0% | EC | 5898 | 23111 | 35918 | 52175 |
| Taux d'escompte 5% | 16370 | 28123 | 47368 | 60865 | 83201 |
EC : Épargne de coûts; NPZ : Névralgie Post-Zostérienne |
|||||
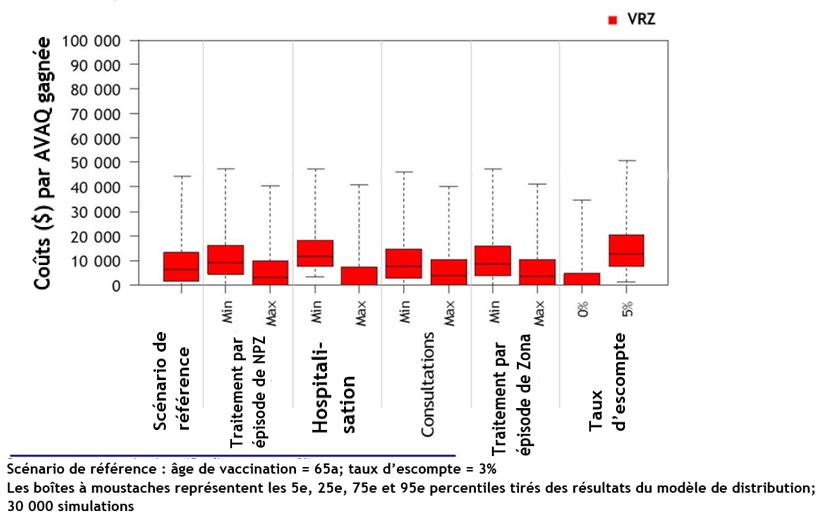
Figure 16 - Équivalent du texte
| Paramètre modifié | VRZ Percentiles prédits par modèle |
||||
|---|---|---|---|---|---|
| 5e | 25e | Médiane | 75e | 95e | |
| Scénario de base | EC | 1507 | 6356 | 13433 | 44382 |
| Traitement/Épisode NPZ min | EC | 4324 | 9088 | 16285 | 47551 |
| Traitement/Épisode NPZ max | EC | EC | 2887 | 9756 | 40539 |
| Hospitalisations min | 3401 | 7687 | 11653 | 18246 | 47322 |
| Hospitalisations max | EC | EC | EC | 7437 | 40807 |
| Consultations min | EC | 2822 | 7670 | 14870 | 46550 |
| Consultations max | EC | EC | 3773 | 10539 | 40173 |
| Traitement/Épisode zona min | EC | 3930 | 8719 | 15900 | 47400 |
| Traitement/Épisode zona max | EC | EC | 3553 | 10461 | 41206 |
| Taux d'escompte 0% | EC | EC | EC | 4605 | 34648 |
| Taux d'escompte 5% | 1289 | 7694 | 12754 | 20575 | 51280 |
EC : Épargne de coûts; NPZ : Névralgie Post-Zostérienne |
|||||
V.4 Limites de l'étude
Le modèle utilisait les données sur les coûts des soins de santé associés au zona et à la NPZ, lesquelles sont incomplètes pour le Canada. Bien que le Canada ait démontré une fluctuation de ses coûts en soins de santé, menant ainsi à des paramètres de coûts incertains, l'analyse de la sensibilité n'a révélé aucune incidence majeure de ces coûts sur les conclusions du modèle. Les résultats de référence supposaient une conformité totale des deux doses du VRZ, conformément aux essais cliniques; toutefois, les réalités observées suivant la mise en marché du vaccin ne semblent pas indiquer un taux de conformité si élevé pour les deux doses. L'étude ne tenait pas compte des répercussions potentielles de la vaccination contre la varicelle sur l'incidence du zona. On a suggéré qu'en réduisant l'incidence de la varicelle primaire au moyen de la vaccination contre la varicelle, une vaccination universelle contre la varicelle mènerait à une augmentation de court à moyen terme de l'incidence du zona chez les groupes d'âge n'ayant pas reçu le vaccin contre la varicelleNote de bas de page 11 Note de bas de page 112. Si tel est le cas, les résultats de cette étude seront prudents et sous-estimeront le RCE d'une vaccination contre le zonaNote de bas de page 11 .
VI. Recommandations
Suivant l'examen des données probantes disponibles résumées ci-dessus et dans le tableau des options de gestion ci-dessous (Tableau 9) comparant les vaccins contre le zona actuellement utilisés au Canada, le CCNI a formulé les recommandations suivantes en ce qui a trait au processus décisionnel au niveau de la santé publique et au niveau individuel. (Bien que dans cette déclaration les recommandations soient essentiellement les mêmes pour les deux niveaux, la justification et le contexte sont quelque peu différents.)
Veuillez noter :
- Une solide recommandation s'applique à la majeure partie de la population et devrait être suivie, à moins que l'on ne puisse justifier de manière claire et convaincante l'adoption d'une autre approche.
- Une recommandation discrétionnaire peut être envisagée dans certains cas pour certaines personnes ou populations. D'autres approches peuvent s'avérer acceptables.
Voir le Tableau 11 pour obtenir une explication plus détaillée de la force des recommandations du CCNI et de la catégorie de l'ensemble des données probantes.
Le CCNI continuera de surveiller les développements scientifiques liés aux vaccins contre le zona, y compris les études liées aux populations immunodéprimées, et mettra à jour ses recommandations à mesure que les données probantes évolueront.
VI.1 Recommandations relatives au processus décisionnel à l'échelle des programmes de santé publique
(C.-à-d. les provinces et territoires prenant des décisions concernant les programmes d'immunisation financés publiquement)
Au moment d'examiner ces recommandations et dans le cadre de la mise en œuvre du programme financé publiquement, les provinces et territoires peuvent tenir compte d'autres facteurs opérationnels locaux (p. ex., programmes d'immunisation actuels, ressources disponibles). En reconnaissant le fait qu'il existe des différences dans les contextes opérationnels à l'échelle nationale, les compétences provinciales et territoriales voudront peut-être se référer au Tableau 10 options de gestion présenté ci-dessous pour obtenir un sommaire des mérites relatifs aux cohortes des différents groupes d'âge de personnes vaccinées (p. ex., en ce qui concerne l'épidémiologie et le RCE) si l'établissement de l'ordre de priorité des programmes d'immunisation ciblés est requis pour la mise en œuvre.
VRZ : Recommandations relatives au processus décisionnel au niveau du programme de santé publique
1. Le CCNI recommande d'offrir le vaccin recombinant contre le zona aux populations de 50 ans et plus qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI)
Résumé des données probantes et justification :
- L'âge est le principal facteur de risque du développement du zona, de la NPZ et d'une hospitalisation connexe. On a observé une importante hausse de l'incidence du zona et du risque de NPZ dans un cas de zona chez les 50 ans et plus. Les taux les plus élevés d'hospitalisation connexe sont observés chez les personnes de 65 ans et plus.
- La protection contre le zona diminue en fonction de l'âge et, au fil du temps, avec l'administration du VVVCZ, tandis que l'EV du VRZ récemment autorisé demeure élevée et semble diminuer plus lentement que l'EV du VVVCZ dans tous les groupes d'âge.
- L'EV du VRZ dans l'ensemble des incidents de zona et de NPZ observés au cours des 3 années suivant l'immunisation semble être deux fois plus importante que celle du VVVCZ.
- L'EV du VRZ dans les incidents de zona observés au cours des 4 années suivant l'immunisation demeure la même, sans diminution considérable constatée au fil du temps; en comparaison, un important déclin de la protection a été observé au cours de l'année suivant l'immunisation avec le VVVCZ.
- Les différences observées au cours des 4 années suivant l'EV du VRZ pour les incidents de zona ne sont pas importantes entre les différents groupes d'âge; en comparaison, le VVVCZ est considérablement moins efficace chez les adultes de plus de 70 ans par rapport aux adultes de 50 à 59 ans.
- Les deux vaccins sont sûrs pour personnes immunocompétentes. En raison de l'adjuvant dans le VRZ, lequel entraîne une importante réponse d'immunité cellulaire et contribue à atténuer le déclin immunitaire naturel associé au vieillissement, ce vaccin s'avère plus réactogène que le VVVCZ. Les réactions locales et systémiques de catégorie 3 (c.-à-d. suffisamment graves pour empêcher les activités régulières) ont été plus souvent rapportées suivant l'administration du VRZ que du VVVCZ, mais ces réactions sont transitoires (d'une durée de 2 à 3 jours).
- Le VVVCZ et le VRZ sont tous deux immunogéniques (bien qu'aucun corrélat sérologique de protection n'ait été établi et qu'il faille interpréter les résultats de l'étude avec prudence). Pour le VVVCZ, la réponse immunitaire semble plus solide chez les personnes de 50 à 59 ans que les groupes plus âgés, mais demeure la même dans tous les groupes d'âge de plus de 50 ans avec le VRZ. L'immunogénicité a été démontrée jusqu'à 9 ans suivant la vaccination avec le VRZ comparativement à 3 ans après la vaccination avec le VVVCZ.
- Le VVVCZ et le VRZ offrent tous deux un bon RCE par rapport à la non-vaccination (déterminé dans le cadre d'une ACU), et présentent un meilleur RCE (coût le plus bas/AVAQ) chez les personnes de 65 à 79 ans. Le VRZ s'est avéré plus rentable que le VVVCZ, et ce, même en tenant compte de la réactogénicité possible du VRZ et de la non-conformité quant à la deuxième dose du vaccin.
- Du point de vue de la mise en œuvre du programme, des ressources seront requises pour mettre en œuvre une administration de deux doses (à 0, 2 à 6 mois) du VRZ (par rapport à une administration d'une seule dose de VVVCZ) et offrir des services de consultation sur la réactogénicité du VRZ. Les responsables des programmes de santé publique peuvent envisager d'adopter une administration à 0 et 12 mois si cela améliore la couverture de la deuxième dose par l'administration simultanée avec d'autres vaccins chez les adultes. Même si dans une étude de petite tailleNote de bas de page 60
- cette administration n'a pas répondu au critère de non-infériorité par rapport à une administration à 0 et 2 mois (contrairement à l'administration à 0 et 6 mois), elle a offert un profil d'innocuité acceptable et une réponse immunitaire anti-gE solide.
Le CCNI a tenu compte des divers facteurs liés aux vaccins contre le zona dont l'utilisation est actuellement autorisée au Canada (décrits dans le Tableau 9 des options de gestion). Le VVVCZ et le VRZ sont tous deux sûrs, immunogènes et efficaces pour prévenir le zona et la NPZ. Finalement, le CCNI estime qu'étant donné l'efficacité supérieure du VRZ chez les adultes de 50 ans et plus, le déclin minimal de la protection et le RCE lié à l'immunisation, il y a tout lieu de formuler une recommandation au niveau du programme de santé publique consistant à vacciner la population de 50 ans et plus. Ce groupe court un plus grand risque de contracter le zona et la NPZ et continuera probablement d'être protégé par le VRZ chez les personnes plus âgées au fur et à mesure que le risque de zona et de NPZ continuera de croître. Du point de vue du programme de santé publique, le VRZ s'est révélé plus rentable que le VVVCZ. Les programmes nécessiteront des stratégies (p. ex., éducation et rappels) afin d'assurer la l'adhésion au schéma posologique en deux doses du VRZ (puisque l'EV et la durée de la protection sont incertaines après seulement une dose) et d'offrir des services de consultations sur la réactogénicité du vaccin à court terme. Si, en raison des contraintes opérationnelles, l'ordre de priorité des programmes d'immunisation ciblés est requis pour la mise en œuvre, les compétences provinciales et territoriales voudront peut-être se référer au Tableau 10 des options de gestion présenté ci-dessous pour obtenir un sommaire des mérites relatifs aux cohortes des différents groupes d'âge de personnes vaccinées (p. ex., en ce qui concerne l'épidémiologie et le RCE).
2. Le CCNI recommande d'offrir le vaccin recombinant contre le zona aux populations de 50 ans et plus qui ont déjà reçu le vaccin à virus vivant contre le zona et qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI)
2a. Chez les adultes de 50 ans et plus qui ont déjà reçu le VVVCZ le CCNI recommande d'envisager une revaccination par deux doses du VRZ au moins un an après l'administration du VVVCZ. (Recommandation discrétionnaire du CCNI)
Résumé des données probantes et justification :
- Pour les raisons décrites ci-dessus, y compris une preuve convaincante d'EV supérieure en ce qui concerne le VRZ dans tous les groupes d'âge (en particulier chez les groupes de personnes plus âgées) et le déclin minimal de la protection après l'administration du VRZ par rapport au VVVCZ (ce qui est particulièrement important étant donné l'incidence accrue du zona et de NPZ avec l'âge), le CCNI a conclu que les personnes ayant déjà reçu le VVVCZ bénéficieraient d'une meilleure protection si elles recevaient le VRZ.
- L'EV pour le VVVCZ diminue après la première année suivant l'immunisation.
- À l'heure actuelle, peu de données probantes appuient les intervalles minimaux et recommandés entre l'administration du VVVCZ et du VRZ. Une étude récemment publiée concernant les adultes de 65 ans et plus qui ont reçu le VRZ a révélé une immunogénicité et une réactogénicité comparables chez les personnes ayant reçu le VVVCZ au moins 5 ans avant par rapport à celles n'ayant jamais reçu le VVVCZ. Aucune préoccupation liée à l'innocuité du vaccin n'a été soulevée au cours du premier mois après l'administration des deux doses du VRZ. Des intervalles plus courts entre les deux vaccins n'ont pas fait l'objet d'études.
- En général, les vaccins inactivés peuvent être administrés de manière concomitante pendant ou à tout moment avant ou après tout autre vaccin à virus vivant offrant une protection contre une maladie différente. Il n'y a aucune ligne directrice sur les intervalles entre l'administration d'un vaccin inactivé et d'un vaccin à virus vivant protégeant contre la même maladieNote de bas de page 91.
- L'intervalle minimal démontré comme sécuritaire et efficace entre les doses du VRZ est de 2 mois; aucune donnée semblable n'existe concernant les intervalles minimaux entre l'administration du VVVCZ et du VRZ.
Les personnes ayant précédemment reçu le VVVCZ acquerront une protection supplémentaire après les deux doses du VRZ, étant donné l'EV plus élevée et durable dans tous les groupes d'âge. Une innocuité, une réactogénicité et une immunogénicité comparables ont été démontrées entre les personnes ayant précédemment reçu le VVVCZ et ceux ne l'ayant pas reçu. Pour les personnes qui ont reçu le VVVCZ, l'examen de l'intervalle entre son administration et celle du VRZ dépendra de l'âge de l'administration du VVVCZ (puisque l'EV diminue avec l'âge) et du temps écoulé depuis l'administration du VVVCZ (puisque l'efficacité diminue après la première année). Selon les données probantes limitées ci-dessus, le CCNI suggère une revaccination par l'administration de deux doses du VRZ au moins une année après l'administration du VVVCZ en raison du déclin rapide de l'efficacité de ce dernier après la période d'un an suivant l'immunisation. Bien que la seule étude publiée à ce jour examine l'immunisation effectuée avec le VRZ à la suite du VVVCZ utilisé à au moins 5 ans d'intervalle, il n'y a aucune raison de croire qu'un intervalle plus court serait nuisible.
3.Le CCNI recommande d'offrir le VRZ aux personnes de 50 ans et plus qui ont des antécédents de zona qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI)
3a. Le CCNI recommande pour les populations de 50 ans et plus ayant déjà contracté le zona d'attendre au moins un an après leur épisode pour une vaccination par deux doses du VRZ. (Recommandation discrétionnaire du CCNI)
Résumé des données probantes et justification :
- Dans sa déclaration du comité consultatif de 2014, le CCNI a recommandé que l'on administre le VVVCZ aux personnes ayant des antécédents de zona (selon les données probantes de catégorie B), au moins un an après un épisode (selon l'opinion d'expert). Veuillez consulter la déclaration de 2014 pour obtenir un résumé de ces données probantes.
- Comme le CCNI l'a résumé dans sa déclaration de 2014 sur le zona, les épisodes récurrents ont été confirmés chez les personnes immunocompétentes, et certaines études suggèrent que le risque de zona chez les personnes ayant des antécédents est comparable à celui de personnes sans antécédents. Par conséquent, cette population continue d'être à risque pour le zona et profitera probablement de la protection offerte par le vaccinNote de bas de page 60.
- Des antécédents rapportés d'occurrence du zona peuvent être incorrects, puisqu'il n'existe aucune évaluation en laboratoire permettant de confirmer un diagnostic.
- Il n'y a actuellement qu'une seule étude (jugée de faible qualité) examinant l'immunogénicité et l'innocuité du VRZ chez les patients ayant des antécédents de zona. Dans cette étude, les réponses immunitaires au VRZ et son profil d'innocuité chez les adultes de 50 ans et plus avec des antécédents de zona consignés à leurs dossiers par des médecins concordaient avec les observations faites chez les personnes de 50 ans et plus sans antécédents consignés. Aucune comparaison officielle en fonction du temps écoulé depuis l'épisode de zona antérieur n'a été effectuée dans cette étude.
- Dans ses recomandations de 2014, le CCNI a conclu que les données probantes étaient insuffisantes pour recommander ou rejeter l'administration du vaccin contre le zona chez les personnes ayant des antécédents de ZO. Quoique la causalité soit difficile à déterminer, des cas de ZO ont été rapportés à la suite de l'administration du VVVCZ.
Comme dans sa recommandation de 2014 sur le VVVCZ, le CCNI recommande une immunisation par le VRZ chez les personnes ayant connu un épisode de zona. Celles ayant connu un tel épisode courent toujours un risque de contracter le virus, les antécédents de zona n'étant pas fiables; par conséquent, la vaccination par le VRZ chez les personnes ayant déclaré des antécédents de zona pourrait être bénéfique. En outre, l'une des études n'a démontré aucune différence dans l'innocuité ou l'immunogénicité du VRZ chez les personnes ayant de tels antécédents. En l'absence de données probantes appuyant un intervalle approprié, le CCNI maintient sa suggestion d'attendre au moins un an après un épisode avant d'administrer le vaccin contre le zona. Aucune étude sur le VRZ chez les personnes ayant des antécédents de ZO n'a été effectuée.
VVVCZ : Recommandations relatives au processus décisionnel au niveau du programme de santé publique.
4. Le CCNI recommande d'envisager l'administration du VVVCZ aux populations immunocompétentes de 50 ans et plus qui ne présentent pas de contre-indication, lorsque le VRZ est contre-indiqué ou s'il n'est pas disponible. (Recommandation discrétionnaire du CCNI)
Résumé des données probantes et justification :
- Le CCNI est arrivé à la conclusion (comme dans les déclarations précédentes du comité consultatif sur le zona) que de bonnes données probantes appuient une immunisation par le VVVCZ chez les adultes de 60 ans et plus (données probantes de catégorie A). Toutefois, la recommandation sur l'utilisation de ce vaccin chez les personnes immunocompétentes de 60 ans et plus est maintenant « discrétionnaire » en raison des données probantes comparatives sur l'efficacité supérieure, la durée accrue de la protection et le RCE relatif du VRZ récemment autorisé (résumés ci-dessus et dans le Tableau 9 des options de gestion).
- Bien que le VVVCZ soit sûr et efficace chez les personnes de 50 à 59 ans et ait été précédemment recommandé de manière discrétionnaire par le CCNI pour ce groupe d'âge, le déclin de la protection du vaccin signifie qu'il n'offrira peut-être pas une protection optimale continue chez les personnes plus âgées, chez qui le risque de zona et de NPZ est plus important. Avec l'arrivée du VRZ récemment autorisé ainsi que son efficacité et sa durée de protection accrues dans ce groupe d'âge, le CCNI recommande maintenant fortement d'utiliser ce vaccin chez les personnes de 50 à 59 ans ainsi que chez les adultes de 60 ans et plus qui ne présentent pas de contre-indication.
- On peut continuer d'envisager l'administration du VVVCZ aux sujets chez qui le VRZ est contre-indiqué (phénomène également connu comme une hypersensibilité à l'un des composants du vaccin) ou si le VRZ n'est pas disponible. Le VVVCZ est autorisé au Canada depuis 2008, et son utilisation s'est révélée sûre, immunogénique et efficace.
Les autres recommandations concernant l'utilisation du VVVCZ dans la déclaration du CCNI de 2014 sur l'utilisation du vaccin contre le zona (Recommandations nos 3 à 5 et 9 concernant l'administration du VVVCZ chez les personnes ayant connu un épisode antérieur de zona ou de ZO, une dose de rappel, une administration concomitante avec le Pneu-P-23) sont toujours pertinentes, et sont disponibles sur la mise à jour sur l'utilisation du vaccin contre la zona.
VRZ par rapport au VVVCZ pour les personnes immunodéprimées : Recommandations relatives au processus décisionnel au niveau du programme de santé publique
5. Le CCNI recommande que d' envisager au cas par cas l'administration du VRZ (non le VVVCZ) pour les personnes immunodéprimées de 50 ans et plus. (Recommandation discrétionnaire du CCNI)
Résumé des données probantes et justification :
- Les personnes immunodéprimées en raison d'affections sous-jacentes ou d'agents immunodépresseurs courent un plus grand risque de développer le zona et peuvent être plus à même de contracter une maladie et des complications atypiques ou plus graves.
- Bien que les personnes immunodéprimées ne devraient pas généralement recevoir de vaccins vivants en raison du risque de maladie causé par les souches de vaccin, le CCNI a précédemment recommandé d'utiliser le VVVCZ chez les sujets recevant une faible dose de thérapie immunosuppressive ou d'agents biologiques anti-TNF, selon le cas. La recommandation a été offerte en l'absence d'un vaccin inactivé et en supposant que les personnes étaient déjà immunisées contre le virus varicelle-zona.
- Chez les personnes immunodéprimées, puisque les antigènes du vaccin ne peuvent se répliquer, le CCNI recommande généralement d'utiliser des vaccins inactivés en lieu et place d'autres vaccins à virus vivant.
- L'ampleur et la durée de l'immunité offerte par le vaccin sont souvent réduites chez les personnes immunodéprimées.
- En général, les experts en immunodéficience recommandent des vaccins tels que le VRZ aux patients immunodéprimés, même si leur efficacité chez ce groupe est incertaine. Cette observation repose sur l'hypothèse que le vaccin ne sera pas nuisible et pourrait s'avérer bénéfique, sans oublier que les sujets immunodéprimés ne sont pas homogènes et y réagiront souvent d'une façon ou d'une autre.
- Le VVVCZ est contre-indiqué chez les personnes immunodéprimées. Bien que nous ne disposions actuellement que de données limitées ayant fait l'objet d'un examen par les pairs et appuyant précisément l'utilisation du VRZ chez les personnes immunodéprimées, le VRZ n'est pas contre-indiqué chez ce groupe.
Contrairement au VVVCZ, le VRZ n'est pas contre-indiqué chez les personnes immunodéprimées. Compte tenu du fardeau de la maladie associé au zona chez les sujets immunodéprimés et les directives générales sur l'utilisation de vaccins inactivés par rapport aux vaccins à virus vivant atténués dans ce groupe (résumées ci-dessus), le CCNI estime que les avantages d'envisager l'administration du VRZ (plutôt que le VVVCZ) chez ces personnes sont plus importants que les risques potentiels à l'heure actuelle.
Le CCNI surveillera les données probantes au fur et à mesure de leur évolution et réévaluera ses recommandations au niveau individuel et du programme de santé publique concernant les personnes et les groupes immunodéprimés dès que les données probantes des essais continus (dans différents groupes de personnes immunodéprimées de 18 ans et plus impliquant des calendriers différents de 2 et 3 doses) seront disponibles.
VI.2 Recommandations pour le processus décisionnel à l'échelle individuelle
(C.-à-d. les personnes souhaitant prévenir le zona ou les cliniciens qui souhaitent conseiller à certains patients de se protéger du zona au moyen de vaccins qui ne sont peut-être pas actuellement offerts dans le cadre des programmes d'immunisation de santé publique.)
VRZ : Recommandations relatives au processus décisionnel au niveau individuel
1. Le CCNI recommande d'offrir le VRZ aux personnes de 50 ans et plus qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI)
Résumé des données probantes et justification :
(Voir les points présentés à la Recommandation no 1 ci-dessus concernant le processus décisionnel au niveau du programme de santé publique.)
Finalement, le CCNI estime que l'efficacité supérieure du VRZ chez les adultes de 50 ans et plus ainsi que le déclin minimal de la protection appuient une recommandation au niveau individuel consistant à vacciner les personnes de 50 ans et plus, qui courent un plus grand risque de contracter le zona et la NPZ et continueront probablement d'être protégées par le VRZ lorsqu'elles seront plus âgées alors que le risque de zona et de NPZ continue de croître. D'un point de vue individuel, les personnes souhaitant prévenir le zona ou les cliniciens conseillant les patients devraient passer en revue les points de décision décrits dans le Tableau 9 des options de gestion au moment de prendre une décision, en plus de tenir compte du coût individuel du VRZ par rapport au VVVCZ. Les personnes devraient se préparer à suivre une administration de deux doses pour le VRZ (puisqu'on ne connaît pas l'EV et la durée de la protection après seulement une dose) et comprendre qu'il est possible qu'elles subissent une plus grande réactogénicité à court terme en raison du VRZ. Le Tableau 10 des options de gestion décrit les mérites relatifs à la vaccination avec le VRZ à différents âges, principalement du point de vue du système de soins de santé.
2. Le CCNI recommande que le VRZ soit offert aux personnes de 50 ans et plus qui ont déjà reçu le VVVCZ et qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI)
2a. Le CCNI recommande pour les adultes de 50 ans et plus qui ont déjà reçu le VVVCZ d'attendre un intervalle d'au moins un an avant une revaccination par deux doses du VRZ. (Recommandation discrétionnaire du CCNI)
Résumé des données probantes et justification :
(Voir les points présentés aux Recommandations nos 2 et 2a ci-dessus concernant le processus décisionnel au niveau du programme de santé publique.)
Les personnes ayant déjà reçu le VVVCZ acquerront une protection supplémentaire après les deux doses du VRZ, étant donné l'EV plus élevée et durable dans tous les groupes d'âge. Une innocuité, une réactogénicité et une immunogénicité comparables ont été démontrées entre les personnes ayant déjà reçu le VVVCZ et ceux ne l'ayant pas reçu. Pour les personnes qui ont déjà reçu le VVVCZ, l'examen de l'intervalle entre son administration et celle du VRZ dépendra de l'âge de vaccination par le VVVCZ (puisque l'EV diminue avec l'âge) et du temps écoulé depuis l'administration du VVVCZ (puisque l'efficacité diminue après la première année). Selon les données probantes limitées résumées ci-dessus, le CCNI suggère la revaccination par l'administration de deux doses du VRZ au moins une année après l'administration du VVVCZ, en raison du déclin rapide de l'efficacité de ce dernier après la première année. Bien que la seule étude publiée à ce jour examine l'immunisation effectuée avec le VRZ à la suite du VVVCZ utilisé à un intervalle d'au moins 5 ans, il n'y a aucune raison de croire qu'un intervalle plus court serait nuisible.
3.Le CCNI recommande que le VRZ soit offert aux personnes de 50 ans et plus ayant des antécédents de zona et qui ne présentent pas de contre-indication. (Fortement recommandé par le CCNI)
3a. Le CCNI recommande pour les adultes de 50 ans et plus ayant des antécédants de zona d'attendre un intervalle d'au moins un an avant unevaccination par deux doses du VRZ. (Recommandation discrétionnaire du CCNI)
Résumé des données probantes et justification :
(Voir les points présentés aux Recommandations nos 3 et 3a ci-dessus concernant le processus décisionnel au niveau du programme de santé publique.)
La vaccination contre le zona demeure bénéfique pour les personnes ayant rapporté des antécédents de zona, puisqu'elles courent un risque de contracter de nouveau la maladie. En outre, l'une des études n'a démontré aucune différence dans l'innocuité ou l'immunogénicité du VRZ chez les personnes ayant des antécédents de zona. En l'absence de données probantes appuyant un intervalle approprié, le CCNI maintient sa suggestion consistant à attendre au moins un an après l'épisode de zona avant d'administrer le vaccin contre le zona.
VVVCZ : Recommandations relatives au processus décisionnel au niveau individuel
4. Le CCNI recommande d'envisager l'administration du VVVCZ aux personnes immunocompétentes de 50 ans et plus qui ne présentent pas de contre-indication, lorsque le VRZ est contre-indiqué ou s'il n'est pas disponible. (Recommandation discrétionnaire du CCNI)
Résumé des données probantes et justification :
(Voir les points présentés à la Recommandation no 4 ci-dessus concernant le processus décisionnel au niveau du programme de santé publique.)
On peut envisager l'administration du VVVCZ aux sujets pour qui le VRZ est contre-indiqué ou non disponible, ou aux personnes qui préfèrent ce vaccin au VRZ après avoir examiné les points de décision décrits dans le Tableau 9 des options de gestion (p. ex., les personnes qui ne termineront pas l'administration des deux doses du VRZ ou pour qui le VRZ est trop coûteux). Le VVVCZ est autorisé au Canada depuis 2008, et son utilisation s'est révélée sûre, immunogénique et efficace. Toutefois, selon les données probantes comparatives sur l'efficacité et la durée de protection supérieures contre le zona avec le VRZ récemment autorisé, en particulier chez les groupes de personnes plus âgées pour qui le risque d'être atteintes du zona ou de la NPZ est supérieur, la recommandation du CCNI en ce qui concerne le VVVCZ est « discrétionnaire » (voir le Tableau 11 pour une description de la force des recommandations du CCNI).
Les autres recommandations sur l'utilisation du VVVCZ présentées dans la déclaration de 2014 du CCNI concernant l'utilisation du vaccin contre le zona (Recommandations nos 3 à 5 et 9 sur l'administration du VVVCZ chez les personnes ayant connu un épisode antérieur de zona ou de ZO, une dose de rappel, une administration concomitante du Pneu-P-23) sont toujours pertinentes et sont disponibles sur la mise à jour sur l'utilisation du vaccin contre la zona.
VRZ par rapport au VVVCZ pour les personnes immunodéprimées : Recommandations relatives au processus décisionnel au niveau individuel
5.Le CCNI recommande d'envisager au cas par cas l'administration du VRZ (et non le VVVCZ) chez les personnes immunodéprimées de 50 ans et plus selon une évaluation individuelle des avantages par rapport aux risques. (Recommandation discrétionnaire du CCNI)
(Voir les points de la Recommandation no 5 ci-dessus concernant le processus décisionnel au niveau du programme de santé publique.)
Le VVVCZ est contre-indiqué chez les personnes immunodéprimées, mais le VRZ ne l'est pas. Selon le fardeau de la maladie associée au zona chez les sujets immunodéprimés et les directives générales sur l'utilisation de vaccins inactivés par rapport aux vaccins à virus vivant chez les personnes immunodéprimées (résumées ci-dessus), le CCNI estime que les avantages d'envisager l'administration du VRZ (par rapport au VVVCZ) chez les personnes immunodéprimées au cas par cas sont plus importants que les risques à l'heure actuelle.
Le CCNI surveillera les données probantes au fur et à mesure de leur évolution et réévaluera ses recommandations au niveau individuel et au niveau du programme de santé publique concernant les personnes et les groupes immunodéprimés dès que les données probantes des essais continus (dans différents groupes de personnes immunodéprimées de 18 ans et plus impliquant des calendriers différents de 2 et 3 doses) seront disponibles.
VI.3 Options de gestion
L'utilisation de deux vaccins est maintenant autorisée au Canada pour prévenir le zona chez les personnes de 50 ans et plus. Le choix de l'option du vaccin préférable dépend des principaux facteurs associés à chacun et d'une comparaison des mérites relatifs respectifs, tels qu'ils sont résumés dans le Tableau 9 ci-dessous.
| Options VVVCZ par rapport au VRZ |
Facteurs à prendre en compte | Points de décision |
|---|---|---|
| 1. VVVCZ | Efficacité contre le zona (EV [IC de 95 %])
Efficacité contre la NPZ (EV [IC de 95 %])
– EV contre le zona : 51 % chez ≥60 ans; diminue avec l'âge suivant l'administration du vaccin. Durée de la protection contre le zona Efficacité contre le zona [IC de 95 %] Immunogénicité Innocuité Économie Faisabilité et acceptabilité |
– L'utilisation du VVVCZ est autorisée au Canada et ailleurs (p. ex., É.-U., Europe et R.-U.) depuis plus de 10 ans, et les recommandations du CCNI sur son utilisation sont en place depuis 2010. L'utilisation du VRZ a récemment été autorisée au Canada et aux É.-U., soit en octobre 2017. Épidémiologie Efficacité Durée de la protection Inconnus Immunogénicité Inconnus Innocuité Inconnus Économie Faisabilité et acceptabilité Inconnus |
| 2. VRZ | Efficacité contre le zona (EV [IC de 95 %])
Efficacité contre la NPZ (EV [IC de 95 %])
Durée de la protection contre le zona Immunogénicité Innocuité (Les données suivantes reposent sur deux ECR importants en phase 3 et d'autres études plus petites.)Note fNote g – Lors des essais cliniques, les réactions à la dose 1 n'ont pas fortement prédites les réactions à la dose 2. Rentabilité – Réactogénicité plus élevée que le VVVCZ |
|
|
||