Annexes de l'évaluation préalable
Groupe de substances azoïques aromatiques et à base de benzidine
Certains pigments monoazoïques
Environnement et Changement climatique Canada
Santé Canada
Mai 2016
Table des matières
- Annexe A : Identité chimique, structures, formules et poids moléculaires des 33 pigments monoazoïques, organisés par sousensemble
- Annexe B : Propriétés physiques et chimiques expérimentales (à une température ambiante selon la situation) des pigments monoazoïques et de leurs analogues
- Annexe C : Données expérimentales sur la biodégradation des pigments monoazoïques et de leurs analogues
- Annexe D : Données expérimentales sur la toxicité aquatique des 33 pigments monoazoïques et de leurs analogues
- Annexe E : Calculs de l'exposition écologique pour les pigments monoazoïques
- Annexe F : Estimations de l’exposition liée à l’utilisation de cosmétiques
- Annexe G : Estimations de l’exposition liée à l’utilisation de pigments monoazoïques dans les peintures.
- Annexe H. Estimation de l’exposition à court terme aux pigments monoazoïques dans l’encre de tatouage permanente (adulte)
- Annexe I : Calculs des doses repères pour le PR3, le PO5, le PR4 et le PR53:1
- Annexe J : Pigments monoazoïques avec effets préoccupants
- Retour à l'évaluation préalable
Annexe A : Identité chimique, structures, formules et poids moléculaires des 33 pigments monoazoïques, organisés par sousensemble
| Sous-ensemble | N° Chemical Abstracts Service (CAS) | Nom dans la LIS (anglais) | Nom dans le C.I. (Numéro dans le C.I.) |
Identificateur de la substance | Structure chimique, formule moléculaire (poids moléculaire) |
|---|---|---|---|---|---|
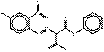
| Pigments jaunes monoazoïques | 2512-29-0 | 2-(4-Méthyl-2-nitrophénylazo)-3-oxo-N-phénylbutyramide | Pigment Yellow 1 (C.I. 11680) |
PY1 |
C17H16N4O4 |
| Pigments jaunes monoazoïques | 6486-23-3 | 2-[(4-Chloro-2-nitrophényl)azo]-N-(2-chlorophényl)-3-oxobutyramide | Pigment Yellow 3 (C.I. 11710) |
PY3 |
C16H12Cl2N4O4 |
| Pigments jaunes monoazoïques | 13515-40-7 | 2-[(4-Chloro-2-nitrophényl)azo]-N-(2-méthoxyphényl)-3-oxobutyramide | Pigment Yellow 73 (C.I. 11738) |
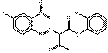
PY73 | 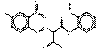 C17H15ClN4O5 (391 g/mol) |
| Pigments de βnaphtol | 2425-85-6 | 1-(4-Méthyl-2-nitrophénylazo)-2-naphtol | Pigment Red 3 (C.I. 12120) |
PR3 | C17H13N3O3 (307 g/mol) |
| Pigments de βnaphtol | 2814-77-9 | 1-(2-Chloro-4-nitrophénylazo)napht-2-ol | Pigment Red 4 (C.I. 12085) |
PR4 | 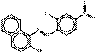 C16H10ClN3O3 (328 g/mol) |
| Pigments de βnaphtol | 6410-13-5 | 2-Naphtalénol, 1-[(4-chloro-2-nitrophenyl)azo]- | Pigment Red 6 (C.I. 12090) |
PR6 | C16H10ClN3O3 (328 g/mol) |
| Pigments de βnaphtol | 6410-09-9 | 1-[(2-Nitrophényl)azo]-2-naphtol | Pigment Orange 2 (C.I. 12060) |
PO2 | C16H11N3O3 (293 g/mol) |
| Pigments de βnaphtol | 3468-63-1 | 1-(2,4-dinitrophénylazo)napht-2-ol | Pigment Orange 5 (C.I. 12075) |
PO5 | 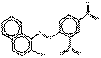 C16H10N4O5 (338 g/mol) |
| Pigments de βnaphtol | 49744-28-7 | 1-(4-Méthoxy-2-nitrophénylazo)napht-2-ol | Non disponible | NONPA | C17H13N3O4 (323 g/mol) |
| Pigments de β-naphtol laqués | 1103-38-4 | Bis{2-[(2-hydroxynaphtyl)azo]naphtalènesulfonate} de baryum | Pigment Red 49:1 (C.I. 15630:1) |
PR49:1 | 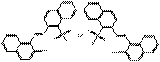 C40H26N4O8S2Ba (892 g/mol) |
| Pigments de β-naphtol laqués | 6372-81-2 | Bis[2-[(2-hydroxy-1-naphtyl)azo]benzoate] de baryum | Pigment Red 50:1 (C.I. 15500:1) |
PR50:1 | 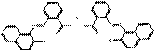 C34H22N4O6Ba (720 g/mol) |
| Pigments de β-naphtol laqués | 5160-02-1 | Bis{2-chloro-5-[(2-hydroxy-1-naphtyl)azo]toluène-4-sulfonate} de baryum | Pigment Red 53:1 (C.I. 15585:1) |
PR53:1 | 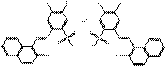 C34H24Cl2N4O8S2Ba (889 g/mol) |
| Pigments de naphtol AS | 6410-41-9 | N-(5-Chloro-2,4-diméthoxyphényl)-4-({5-[(diéthylamino)sulfonyl]-2 méthoxyphényl}azo)-3 hydroxynaphtalène-2-carboxamide | Pigment Red 5 (C.I. 12490) |
PR5 | 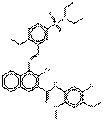 C30H31ClN4O7S (627 g/mol) |
| Pigments de naphtol AS | 6535-46-2 | 3-Hydroxy-N-(o-tolyl)-4-[(2,4,5-trichlorophényl)azo]naphtalène-2-carboxamide | Pigment Red 112 (C.I. 12370) |
PR112 | 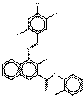 C24H16Cl3N3O2 (485 g/mol) |
| Pigments de naphtol AS | 2786-76-7 | 4-{[4-(Aminocarbonyl)phényl]azo}-N-(2-éthoxyphényl)-3-hydroxynaphtalène-2-carboxamide | Pigment Red 170 (C.I. 12475) |
PR170 | 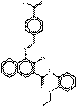 C26H22N4O4 (455 g/mol) |
| Pigments de naphtol AS | 59487-23-9 | 4-[[5-[[[4-(Aminocarbonyl)phényl]amino]carbonyl]-2-méthoxyphényl]azo]-N-(5-chloro-2,4-diméthoxyphényl)-3-hydroxynaphtalène-2-carboxamide | Pigment Red 187 (C.I. 12486) |
PR187 | 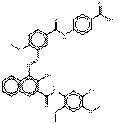 C34H28ClN5O7 (654 g/mol) |
| Pigments de naphtol AS | 36968-27-1 | 4-{[4-(Aminocarbonyl)phényl]azo}-3-hydroxy-N-(2-méthoxyphényl)naphtalène-2-carboxamide | Pigment Red 266 (C.I. 12474) |
PR266 | 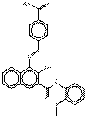 C25H20N4O4 (441 g/mol) |
| Pigments de naphtol AS | 16403-84-2 | N-[4-(Acétylamino)phényl]-4-[[5-(aminocarbonyl)-2-chlorophényl]azo]-3-hydroxynaphtalène-2-carboxamide | Pigment Red 268 (C.I. 12316) |
PR268 | 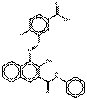 C25H20N4O3 (425 g/mol) |
| Pigments de naphtol AS | 12236-64-5 | N-[4-(Acétylamino)phényl]-4-{[5-(aminocarbonyl)-2-chlorophényl]azo}-3-hydroxynaphtalène-2-carboxamide | Pigment Orange 38 (C.I. 12367) |
PO38 | 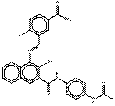 C26H20ClN5O4 (502 g/mol) |
| Pigments de naphtol AS | 94199-57-2 | N-(2-Éthoxyphényl)-3-hydroxy-4-[(2-nitrophényl)azo]naphtalène-2-carboxamide | Non disponible | NAPNPA | 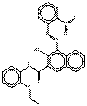 C25H20N4O5 (457 g/mol) |
| Pigments de naphtol AS | 85005-63-6 | 4-[(2,4-Dinitrophényl)azo]-3-hydroxy-N-phénylnaphtalène-2-carboxamide | Non disponible | NANPAP | 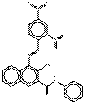 C23H15N5O6 (457 g/mol) |
| Pigments de naphtol AS | 13824-00-5 | N-(p-Anisyl)-3-hydroxy-N-4-[(4-méthylphényl)azo]naphtalène-2-carboxamide | Non disponible | NAPMPA | 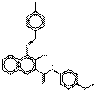 C25H21N3O3 (412 g/mol) |
| Pigments de naphtol AS | 17947-32-9 | N-(p-Anisyl)-3-hydroxy-4-(phénylazo)naphtalène-2-carboxamide | Non disponible | NAPPA | 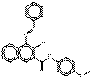 C24H19N3O3 (397 g/mol) |
| Pigments de BONA laqués | 7023-61-2 | 4-[(5-Chloro-4-méthyl-2-sulfonatophényl)azo]-3-hydroxy-2-naphtoate de calcium | Pigment Red 48:2 (C.I. 15865:2) |
PR48:2 | 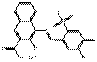 C18H11ClN2O6SCa (459 g/mol) |
| Pigments de BONA laqués | 71832-83-2 | 4-[(5-Chloro-4-méthyl-2-sulfonatophényl)azo]-3-hydroxy-2-naphtoate de magnésium | Pigment Red 48:5 (C.I. 15865:5) |
PR48:5 | 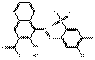 C18H11ClN2O6SMg (443 g/mol) |
| Pigments de BONA laqués | 17852-99-2 | 4-[(4-Chloro-5-méthyl-2-sulfonatophényl)azo]-3-hydroxy-2-naphtoate de calcium | Pigment Red 52:1 (C.I. 15860:1) |
PR52:1 | 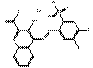 C18H11ClN2O6SCa (459 g/mol) |
| Pigments de BONA laqués | 6417-83-0 | 3-Hydroxy-4-[(1-sulfonato-2-naphtyl)azo]-2-naphtoate de calcium | Pigment Red 63:1 (C.I. 15880:1) |
PR63:1 | 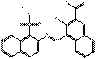 C21H12N2O6SCa (461 g/mol) |
| Pigments de benzimidazolone | 12236-62-3 | 2-[(4-Chloro-2-nitrophényl)azo]-N-(2,3-dihydro-2-oxo-1H-benzimidazol-5-yl)-3-oxobutyramide | Pigment Orange 36 (C.I. 11780) |
PO36 | 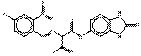 C17H13ClN6O5 (417 g/mol) |
| Pigments de naphtol AS laqués | 43035-18-3 | Bis[4-[[3-[[2-hydroxy-3-[[(4-méthoxyphényl)amino]carbonyl]-1-naphtyl]azo]-4-méthylbenzoyl]amino]benzènesulfonate] de calcium (2:1) | Pigment Red 247:1 (C.I. 15915) |
PR247:1 | 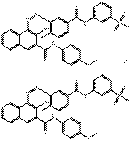 C64H50N8O14S2Ca (1259 g/mol) |
| Pigments de pyrazoloquinazolone | 74336-60-0 | 1-[(5,7-dichloro-1,9-dihydro-2-méthyl-9-oxopyrazolo [5, 1-b]quinazolin-3-yl)azo]anthraquinone | Pigment Red 251 (C.I. 12925) |
PR251 | 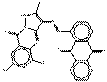 C25H13Cl2N5O3 (502 g/mol) |
| Pigments de BONA laqués - individuels | 12238-31-2 | Pigment Red 52:2 | Pigment Red 52:2 (C.I. 15860:2) |
PR52:2 | 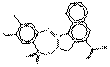 C18H11ClMnN2O6S (474 g/mol) |
| Pigments jaunes monoazoïques (individuels) |
6407-74-5 | 4-[(2-Chlorophényl)azo]-2,4-dihydro-5-méthyl-2-phényl-3H-pyrazol-3-one | Pigment Yellow 60 (C.I. 12705) |
PY60 | C16H13ClN4O (313 g/mol) |
| Autres pigments (individuels) | 83249-60-9 | 2-[(2-Hydroxy-6-sulfonato-1-naphtyl)azo]naphtalènesulfonate de calcium | Non disponible | NSNAC | 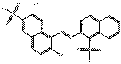 C20H12N2O7S2Ca (497 g/mol) |
Annexe B : Propriétés physiques et chimiques expérimentales (à une température ambiante selon la situation) des pigments monoazoïques et de leurs analogues
| Sous-ensemble | Substance | Propriété (acronyme) | Valeur | Référence |
|---|---|---|---|---|
| Pigments jaunes monoazoïques | PY1 | Température de décomposition (TD), ºC | 249 | Étude présentée, 2012a |
| Pigments jaunes monoazoïques | PY1 | Hydrosolubilité (HS, Se), µg/L | 0,23 | Étude présentée, 2012j |
| Pigments jaunes monoazoïques | PY1 | Hydrosolubilité (HS; Se), µg/L | inférieur(e) à 20 | Étude présentée, 2012c |
| Pigments jaunes monoazoïques | PY1 | Solubilité dans le n-octanol (Soct), µg/L | 9 530 | Étude présentée, 2012k |
| Pigments jaunes monoazoïques | PY1 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 4,62 | Étude présentée, 2012j, k |
| Pigments jaunes monoazoïques | PY1 | Le logarithme du quotient du partage carbone organique-eau coefficient (Koc), sans dimension | 5,5 | Étude présentée, 2012q |
| Pigments jaunes monoazoïques | PY3 | Hydrosolubilité (HS, Se), µg/L | 7,5 | Étude présentée, 2012m |
| Pigments jaunes monoazoïques | PY3 | Solubilité dans le n-octanol (Soct), µg/L | 5 960 | Étude présentée, 2012m |
| Pigments jaunes monoazoïques | PY3 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 2,90 | Étude présentée, 2012l |
| Pigments jaunes monoazoïques | PY74* | Point de fusion (PF) (°C) | Pas de point de fusion (effet endothermique dans une plage de températures allant de 260 à 290 °C directement suivie par une décomposition exothermique spontanée dans une plage de températures allant de 290 à 390 °C) | ECHA, 2012 |
| Pigments jaunes monoazoïques | PY74* | Température de décomposition (TD), ºC | 290 | ECHA, 2012 |
| Pigments jaunes monoazoïques | PY74* | Distribution granulométrique : diamètre médian massique (D50), µm | 1,96 | ECHA, 2012 |
| Pigments jaunes monoazoïques | PY74* | Densité, g/cm3 | 1,43 | ECHA, 2012 |
| Pigments jaunes monoazoïques | PY74* | Hydrosolubilité (HS, Se), µg/L | 7,6 | ECHA, 2012 |
| Pigments jaunes monoazoïques | PY74* | Solubilité dans le n-octanol (Soct), µg/L | 740 | ECHA, 2012 |
| Pigments jaunes monoazoïques | PY74* | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 2,0 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:2 | Point de fusion (PF) (°C) | Pas de point de fusion (évaporation et décomposition avant la fusion) | ECHA, 2012 |
| Pigments de BONA laqués | PR48:2 | Température de décomposition (TD), ºC | 350 °C | ECHA, 2012 |
| Pigments de BONA laqués | PR48:2 | Distribution granulométrique : diamètre médian massique (D50), µm | 2,15; 6,61; 10,44 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:2 | Hydrosolubilité (HS, Se), µg/L | 250-280 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:2 | Solubilité dans le n-octanol (Soct), µg/L | 43-52 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:2 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | –0,75 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:1* | Point de fusion (PF) (°C) | Pas de point de fusion : évaporation (75-165 °C) et décomposition (à partir de 370 °C) avant la fusion | ECHA, 2012 |
| Pigments de BONA laqués | PR48:1* | Température de décomposition (TD), ºC | 370 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:1* | Distribution granulométrique : diamètre médian massique (D50), µm | 17,05 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:1* | Densité, g/cm3 | 1,20 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:1* | Hydrosolubilité (HS, Se), µg/L | inférieur(e) à 25 µg/L | ECHA, 2012 |
| Pigments de BONA laqués | PR48:1* | Solubilité dans le n-octanol (Soct), µg/L | 31-33 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:1* | Solubilité dans d'autres solvants | Soluble dans le N,N-diméthylformamide, le diméthylsulfoxyde, le N-méthyl-pyrrolidine, le méthanol; insoluble dans l'acétone, le 1,4-dioxane, l'acétonitrile, et l'éthanol | ECHA, 2012 |
| Pigments de BONA laqués | PR48:1* | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | supérieur(e) à 0,11 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:3* | Point de fusion (PF) (°C) | Pas de point de fusion (évaporation et décomposition avant la fusion) | ECHA, 2012 |
| Pigments de BONA laqués | PR48:3* | Température de décomposition (TD), ºC | 350 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:3* | Distribution granulométrique : diamètre médian massique (D50), µm | 10,06 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:3* | Hydrosolubilité (HS, Se), µg/L | 100-120 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:3* | Solubilité dans le n-octanol (Soct), µg/L | 60-70 | ECHA, 2012 |
| Pigments de BONA laqués | PR48:3* | Solubilité dans d'autres solvants | Soluble dans le N,N-diméthylformamide, le diméthylsulfoxyde, le N-méthyl-pyrrolidine, le m/thanol; insoluble dans l'acétone, le 1,4-dioxane, l'acétonitrile, et l'éthanol | ECHA, 2012 |
| Pigments de BONA laqués | PR48:3* | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | - 0,23 |
ECHA, 2012 |
| Pigments de BONA laqués | PR57:1* | Point de fusion (PF) (°C) | Pas de point de fusion (évaporation et décomposition avant la fusion) | ECHA, 2012 |
| Pigments de BONA laqués | PR57:1* | Point de fusion (PF) (°C) | 357,5 | CPMA, 2006b |
| Pigments de BONA laqués | PR57:1* | Température de décomposition (TD), ºC | 310 | ECHA, 2012 |
| Pigments de BONA laqués | PR57:1* | Distribution granulométrique : diamètre médian massique (D50), µm | 1,69; 4,08 | ECHA, 2012 |
| Pigments de BONA laqués | PR57:1* | Hydrosolubilité (HS, Se), µg/L | 500-580; 1 200-1 300 | ECHA, 2012 |
| Pigments de BONA laqués | PR57:1* | Hydrosolubilité (HS, Se), µg/L | 8 900 | MITI, 1992 |
| Pigments de BONA laqués | PR57:1* | Solubilité dans le n-octanol (Soct), µg/L | 4 600-4 900; 5 100-6 000 | ECHA, 2012 |
| Pigments de BONA laqués | PR57:1* | Solubilité dans d'autres solvants | Soluble dans le N,N-diméthylformamide, le diméthylsulfoxyde, le Nméthyl-pyrrolidine, le m/thanol; insoluble dans l'acétone, le 1,4-dioxane, l'acétonitrile, et l'éthanol | ECHA, 2012 |
| Pigments de BONA laqués | PR57:1* | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 0,65; 0,94 | ECHA, 2012 |
| Pigments de βnaphtol | PR3 | Point de fusion (PF) (°C) | 276 | Øllgaard et al., 1998 |
| Pigments de βnaphtol | PR3 | Point de fusion (PF) (°C) | 270-272 | Green, 1990 |
| Pigments de βnaphtol | PR3 | Dimension moyenne des particules, µm | 0,26-0,37 | Clariant, 2007 |
| Pigments de βnaphtol | PR3 | Dimension moyenne des particules, µm | 0,26-0,53 | NPIRI, 2000 |
| Pigments de βnaphtol | PR3 | Densité, g/cm3 | 1,37-1,50 | Stubbs, 1973 |
| Pigments de βnaphtol | PR3 | Solubilité dans le n-octanol (Soct), µg/L | 17 900 | Étude présentée, 2007f |
| Pigments de βnaphtol | PR3 | Solubilité dans le n-octanol (Soct), µg/L | 17 000 | Anliker et Moser, 1987 |
| Pigments de βnaphtol | PR3 | Hydrosolubilité (HS, Se), µg/L | 3,3 | Étude présentée, 2007hg |
| Pigments de β-naphtol | PR3 | Hydrosolubilité (HS, Se), µg/L | 800 | Stubbs, 1973; Green, 1990 |
| Pigments de βnaphtol | PR3 | Solubilité dans d'autres solvants | Soluble dans l'éthanol (0,7 g/L), l'éther méthylique de l'éthylèneglycol (0,9 g/L), l'acétone, le benzène; très soluble dans les essences minérales, les hydrocarbures et les plastifiants | Stubbs, 1973; Green, 1990 |
| Pigments de βnaphtol | PR3 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 3,73 | Étude présentée, 2007f, g |
| Pigments de βnaphtol | PR4 | Point de fusion (PF) (°C) | 276 | NPIRI, 2000 |
| Pigments de βnaphtol | PR4 | Dimension moyenne des particules, µm | 0,27 | Clariant, 2007 |
| Pigments de βnaphtol | PR4 | Dimension moyenne des particules, µm | 0,24 | NPIRI, 2000 |
| Pigments de βnaphtol | PR4 | Hydrosolubilité (HS, Se), µg/L | 3,3 | Étude présentée, 2007h. |
| Pigments de βnaphtol | PR4 | Solubilité dans le n-octanol (Soct), µg/L | 9 400 | Étude présentée, 2007i |
| Pigments de βnaphtol | PR4 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 3,45 | Étude présentée, 2007h, i |
| Pigments de βnaphtol | PO2 | Point de fusion (PF) (°C) | 212 | NPIRI, 2000 |
| Pigments de βnaphtol | PO5 | Point de fusion (PF) (°C) | 302 | NPIRI, 2000 |
| Pigments de βnaphtol | PO5 | Dimension moyenne des particules, µm | 0,29 | Clariant, 2007 |
| Pigments de βnaphtol | PO5 | Dimension moyenne des particules, µm | 0,32-0,37 | NPIRI, 2000 |
| Pigments de βnaphtol | PO5 | Hydrosolubilité (HS, Se), µg/L | 6,8 | Étude présentée, 2007j |
| Pigments de βnaphtol | PO5 | Solubilité dans le n-octanol (Soct), µg/L | 1 760 | Étude présentée, 2007j |
| Pigments de βnaphtol | PO5 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 2,41 | Étude présentée, 2007j |
| Pigments de naphtol AS | PR5 | Point de fusion (PF) (°C) | 306 | NPIRI, 2000 |
| Pigments de naphtol AS | PR5 | Dimension moyenne des particules, µm | 0,1 | NPIRI, 2000 |
| Pigments de naphtol AS | PR5 | Densité, g/cm3 | 1,40-1,44 | NPIRI, 2000 |
| Pigments de naphtol AS | PR5 | Hydrosolubilité (HS, Se), µg/L | 7,8 | Étude présentée, 2007k |
| Pigments de naphtol AS | PR5 | Solubilité dans le n-octanol (Soct), µg/L | 133 | Étude présentée, 2007l |
| Pigments de naphtol AS | PR5 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 1,23 | Étude présentée, 2007k, l |
| Pigments de naphtol AS | PR112 | Point de fusion (PF) (°C) | Pas de point de fusion (effet endothermique dans une plage de températures allant de 260 à 270 °C directement suivie par une décomposition exothermique spontanée dans une plage de températures allant de 270 à 290 °C) | ECHA, 2012 |
| Pigments de naphtol AS | PR112 | Température de décomposition (TD), ºC | 270 | ECHA, 2012 |
| Pigments de naphtol AS | PR112 | Distribution granulométrique : diamètre médian massique (D50), µm | 4,56 | ECHA, 2012 |
| Pigments de naphtol AS | PR112 | Densité, g/cm3 | 1,48 | ECHA, 2012 |
| Pigments de naphtol AS | PR112 | Hydrosolubilité (HS, Se), µg/L | 9,8 | ECHA, 2012 |
| Pigments de naphtol AS | PR112 | Solubilité dans le n-octanol (Soct), µg/L | 3 310 | ECHA, 2012 |
| Pigments de naphtol AS | PR112 | Solubilité dans le n-octanol (Soct), µg/L | 7 800 | Anliker et Moser, 1987 |
| Pigments de naphtol AS | PR112 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 2,53 | ECHA, 2012 |
| Pigments de naphtol AS | PR266 | Hydrosolubilité (HS, Se), µg/L | 3,0 | Étude présentée, 2012n |
| Pigments de naphtol AS | PR266 | Solubilité dans le n-octanol (Soct), µg/L | 160 | Étude présentée, 2012m |
| Pigments de naphtol AS | PR266 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 1,73 | Étude présentée, 2012m |
| Pigments de naphtol AS | PR187 | Dimension moyenne des particules, µm | 0,11 | Clariant, 2007 |
| Pigments de naphtol AS | PR187 | Hydrosolubilité (HS, Se), µg/L | 8,9 | Étude présentée, 2012m |
| Pigments de naphtol AS | PR187 | Solubilité dans le n-octanol (Soct), µg/L | 22,1 | Étude présentée, 2012m |
| Pigments de naphtol AS | PR187 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 0,4 | Étude présentée, 2012m |
| Pigments de naphtol AS | PO38 | Dimension moyenne des particules, µm | 0,17 | Clariant, 2007 |
| Pigments de naphtol AS | PO38 | Densité, g/cm3 | 1,46 | Clariant, 2007 |
| Pigments de naphtol AS | PO38 | Hydrosolubilité (HS, Se), µg/L | 24,9 | Étude présentée, 2007m |
| Pigments de naphtol AS | PO38 | Solubilité dans le n-octanol (Soct), µg/L | 155 | Étude présentée, 2007m |
| Pigments de naphtol AS | PO38 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 0,79 | Étude présentée, 2007m |
| Pigments de naphtol AS | PR2* | Hydrosolubilité (HS, Se), µg/L | 5,4 | Étude présentée, 2007p |
| Pigments de naphtol AS | PR2* | Solubilité dans le n-octanol (Soct), µg/L | 8 630 | Étude présentée, 2007p |
| Pigments de naphtol AS | PR2* | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 3,2 | Étude présentée, 2007p) |
| Pigments de naphtol AS | PR146* | Dimension moyenne des particules, µm | 0,11 | NPIRI, 2000 |
| Pigments de naphtol AS | PR146* | Hydrosolubilité (HS, Se), µg/L | 8,7 | Étude présentée, 2007q |
| Pigments de naphtol AS | PR146* | Solubilité dans le n-octanol (Soct), µg/L | 100 | Étude présentée, 2007q |
| Pigments de naphtol AS | PR146* | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 1,1 | Étude présentée, 2007q |
| Pigments de naphtol AS | PR253* | Hydrosolubilité (HS, Se), µg/L | 8 | Étude présentée, 2007m |
| Pigments de naphtol AS | PR253* | Solubilité dans le n-octanol (Soct), µg/L | 202 | Étude présentée, 2007m |
| Pigments de naphtol AS | PR253* | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 1,40 | Étude présentée, 2007m |
| Pigments de β-naphtol laqués | PR53:1 | Point de fusion (PF) (°C) | supérieur(e) à 330 | Commission européenne, ©2000a |
| Pigments de β-naphtol laqués | PR53:1 | Point de fusion (PF) (°C) | 330 | CPMA, 2006a |
| Pigments de β-naphtol laqués | PR53:1 | Point de fusion (PF) (°C) | Fusion sous décomposition à 330 °C | OCDE, 1999a,b |
| Pigments de β-naphtol laqués | PR53:1 | Température de décomposition (TD), ºC | 343-345 | NTP, 1982 |
| Pigments de β-naphtol laqués | PR53:1 | Densité, g/cm3 | 1,5 | Commission européenne, ©2000a |
| Pigments de β-naphtol laqués | PR53:1 | Hydrosolubilité (HS, Se), µg/L | 1 300; 3 400 | Commission européenne, ©2000a |
| Pigments de β-naphtol laqués | PR53:1 | Hydrosolubilité (HS, Se), µg/L | 2 000 | OCDE, 1999a,b |
| Pigments de β-naphtol laqués | PR53:1 | Hydrosolubilité (HS, Se), µg/L | 2 200 | Commission européenne, ©2000a |
| Pigments de β-naphtol laqués | PR53:1 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | –0,26 | OCDE, 1999a,b |
| Pigments de benzimidazolone (individuels) | PO36 | Hydrosolubilité (HS, Se), µg/L | 14 | Étude présentée, 2012p |
| Pigments de benzimidazolone (individuels) | PO36 | Hydrosolubilité (HS, Se), µg/L | inférieur(e) à 20,6 | Étude présentée, 2012o |
| Pigments de benzimidazolone (individuels) | PO36 | Solubilité dans le n-octanol (Soct), µg/L | 86,1 | Étude présentée, 2012n |
| Pigments de benzimidazolone (individuels) | PO36 | Solubilité dans le n-octanol (Soct), µg/L | supérieur(e) à 137 | Étude présentée, 2012o |
| Pigments de benzimidazolone (individuels) | PO36 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 0,8 | Étude présentée, 2012n, o |
| Pigments de naphtol AS laqués (individuels) | PR247:1 | Dimension moyenne des particules, µm | 0,18 | Clariant, 2007 |
| Pigments de naphtol AS laqués (individuels) | PR247:1 | Hydrosolubilité (HS, Se), µg/L | 112 | Étude présentée, 2007m |
| Pigments de naphtol AS laqués (individuels) | PR247:1 | Solubilité dans le n-octanol (Soct), µg/L | 178 | Étude présentée, 2007m |
| Pigments de naphtol AS laqués (individuels) | PR247:1 | Le logarithme du quotient des concentrations molaires d'un soluté dans l'octanol et l'eau [calculé comme log (Soct/Se), sans dimension] | 0,2 | Étude présentée, 2007m |
Abréviations :
DMF, N,N-diméthylformamide;
DMSO, diméthylsulfoxyde;
NMP, N-méthyl-pyrrolidine
Annexe C : Données expérimentales sur la biodégradation des pigments monoazoïques et de leurs analogues
| Sous-ensemble (substance) | Valeur de la biodégradation (%) | Durée de l'essai (en jours) |
Détails | Référence |
|---|---|---|---|---|
| Pigments jaunes monoazoïques (PY1) | 14 | 28 | Biodégradabilité intrinsèque; purité = 99,7 % | Étude présentée, 2012a |
| Pigments de BONA laqués (PR48:2) | 0 | 28 | Biodégradation rapide | ECHA, 2012 |
| Pigments de BONA laqués (PR57:1*) | 0 | 28 | Biodégradabilité rapide; analyse par chromatographie liquide à haute performance (CLHP) | MITI, 1992 |
| Pigments de BONA laqués (PR57:1*) | 9; 12,9 | 28 | Biodégradabilité rapide; analyse de la demande biochimique d'oxygène | MITI, 1992 |
| Pigments de βnaphtol laqués (PR53:1) | 0 | 14 | Biodégradation rapide | MITI, 1992 |
| Pigments de βnaphtol laqués (PR53:1) | 33 | 21 | Biodégradabilité; 33 % éliminés après 21 jours; dans le test Zahn-Wellens, 10 % d'élimination en raison de l'absorption sur les boues | Commission européenne, ©2000 |
Annexe D : Données expérimentales sur la toxicité aquatique des 33 pigments monoazoïques et de leurs analogues
| Substance (sous-ensemble) |
Type d'essai (durée) | Organisme | Paramètre et valeur | Détails | Référence |
|---|---|---|---|---|---|
| (PY1) pigments jaunes monoazoïques | Toxicité aiguë (96 h) |
Dard-perche (Brachydanio rerio) | CL0 = 1 mg/L; CL50 supérieur(e) à 1 mg/L | Semi-statique. Ligne directrice de l'OCDE 203 Solution saturée (1 mg/L; pureté : 99,7 %). Particules non dissoutes retirées par membrane filtrante (0,45 µm) Concentrations mesurées inférieur(e) à LQ |
Étude présentée, 2012b |
| (PY1) pigments jaunes monoazoïques | Toxicité chronique (21 jours) |
Puce d'eau (Daphnia magna) | CSEO = 1 mg/L | Semi-statique. Ligne directrice de l'OCDE 211 (reproduction) Solution saturée (1 mg/L; pureté : 99,7 %). Particules non dissoutes retirées par membrane filtrante (0,45 µm) Effets : taux de reproduction, apparence de la première couvée; nombre de couvées; juvéniles morts nés et œufs avortés; mortalité des adultes; poids corporel et taille Aucune signification biologique ou statistique entre le groupe témoin et le groupe soumis à 1 mg/L Concentrations mesurées inférieur(e) à LQ |
Étude présentée, 2012c |
| (PY1) pigments jaunes monoazoïques | Toxicité chronique (72 h) |
Algues (Desmodesmus subspicatus) | CSEO = 1 mg/L | Statique. Ligne directrice de l'OCDE 201 Solution saturée (1 mg/L; pureté : 99,7 %). Particules non dissoutes retirées par membrane filtrante (0,45 µm) Effets : taux de croissance et rendement Aucune signification biologique ou statistique entre le groupe témoin et le groupe soumis à 1 mg/L Concentrations mesurées inférieur(e) à LQ |
Étude présentée, 2012d |
| (PY3) pigments jaunes monoazoïques | Toxicité aiguë (48 h) |
Puce d'eau (Daphnia magna) | Aucun effet à 100 mg/L; | Statique. Ligne directrice de l'OCDE 202. HS inférieur(e) à 1 mg/L déclaré Solution saturée (100 mg/L; pureté : 99,8 %). Particules non dissoutes retirées par membrane filtrante (0,45 µm) Aucune signification biologique ou statistique dans l'immobilisation entre le groupe témoin et le groupe soumis à 100 mg/L |
Étude présentée, 2012e |
| PO36 (pigments de benzimidazolone) | Toxicité aiguë (96 h) |
Dard-perche (Brachydanio rerio) | CL0 = 1 mg/L; CL50 supérieur(e) à 1 mg/L | Semi-statique. Ligne directrice de l'OCDE 203. Solution saturée (1 mg/L; pureté : 99,5 %). Particules non dissoutes retirées par membrane filtrante (0,45 µm) Concentrations mesurées inférieur(e) à LQ |
Étude présentée, 2012f |
| PO36 (pigments de benzimidazolone) | Toxicité chronique (21 jours) |
Puce d'eau (Daphnia magna) | CSEO = 1 mg/L | Semi-statique. Ligne directrice de l'OCDE 211. Solution saturée (1 mg/L; pureté : 99,5 %). Particules non dissoutes retirées par membrane filtrante (0,45 µm) Effets : taux de reproduction, apparence de la première couvée; nombre de couvées; mortalité; poids corporel et taille, autre. Aucune signification biologique ou statistique entre le groupe témoin et le groupe soumis à 1 mg/L Concentrations mesurées inférieur(e) à LQ |
Étude présentée, 2012g |
| PR53:1 (pigments de β-naphtol laqués) | Toxicité aiguë (96 h) |
Dard-perche (Brachydanio rerio) | CL50 supérieur(e) à 500 mg/L | Statique. Des groupes de 10 poissons ont été exposés à cinq concentrations nominales (17,1-180 mg/L), contrôle du diméthylsulfoxyde (DMSO) (0,5 mg/L) et contrôle de l'eau en laboratoire | CPMA, 2006a |
| PR53:1 (pigments de β-naphtol laqués) | Toxicité aiguë (48 h) |
Medaka (Oryzias latipes) | CL50 supérieur(e) à 500 mg/L | Système semi-statique. | CPMA, 2006a |
| PR53:1 (pigments de β-naphtol laqués) | Toxicité aiguë (48 h) |
Medaka (Oryzias latipes) | CL50 supérieur(e) à 420 mg/L | Système semi-statique. | MITI, 1992 |
| PR53:1 (pigments de β-naphtol laqués) | Toxicité aiguë (48 h) |
Puce d'eau (Daphnia magna) | CE0 supérieur(e) à 2,2 mg/L | Solution saturée de la substance d'essai (pureté : 98,1 %) | Commission européenne, ©2000a |
| PR53:1 (pigments de β-naphtol laqués) | Toxicité aiguë (48 h) |
Puce d'eau (Daphnia magna) | CE0 supérieur(e) à 3,8 mg/L | Solution saturée de la substance d'essai (pureté : 98,1 %) | Commission européenne, ©2000a |
| PR3 (pigments de β-naphtol) | Toxicité aiguë (48 h) |
Puce d'eau (Daphnia magna) | CE0 = 0,9 mg/L | Statique. 20 daphnies; solution saturée (brassage de la solution mère pendant 24 h et suppression des particules non dissoutes par centrifugation) et un contrôle. Le COD était de 0,6 mg/L au début et à la fin de l'essai, valeur étant estimée à 0,9 mg/L de la concentration de pigment. Aucun effet biologique important (immobilisation) à saturation. |
Étude présentée, 2007 |
| PO5 (pigments de β-naphtol) | Toxicité aiguë (48 h) |
Puce d'eau (Daphnia magna) | CE0 = 1,6 mg/L | Statique. Saturation atteinte en brassant la solution mère pendant 24 h et en supprimant les particules non dissoutes par filtration sur membrane de 0,45 μm. Le COD a été mesuré et été déterminé comme correspondant à une concentration de 1,6 mg/L de pigment. Aucun effet biologique important (immobilisation) à saturation. | Étude présentée, 2007o |
| PR112 (pigments de naphtol AS) | Toxicité chronique (21 jours) |
Puce d'eau (Daphnia magna) | CSEO = 1 mg/L | Semi-statique. Ligne directrice de l'OCDE 211. Solution saturée : 1 mg/L (brassage à 20 tr/min pendant 48 h; particules non dissoutes retirées par membrane filtrante, 0,45 µm) Charge : solution saturée comme concentration limite Effets : mortalité des adultes (quotidienne); nombre de juvéniles (quotidien); juvéniles morts nés et œufs avortés (quotidien); taux intrinsèque de croissance naturelle (fin de l'essai); croissance - longueur totale et poids sec (fin de l'essai) Aucun effet biologiquement ou statistiquement significatif à 1 mg/L |
ECHA, 2012 |
| PR112 (pigments de naphtol AS) | Toxicité chronique (72 h) |
Algues (Desmodesmus subspicatus) | CSEO = 1 mg/L (inhibition liée au taux; inhibition du rendement) | Statique. Ligne directrice de l'OCDE 201 Solution saturée (dispersion de 1 mg/L; brassée à 20 tr/min pendant 48 h; membrane filtrante, 0,45 µm; aucune concentration mesurée) Charge différentielle : solution saturée comme concentration limite Effets : inhibition liée au taux; inhibition du rendement. Aucune inhibition après 72 h à la solution saturée (1 mg/L). |
ECHA, 2012 |
| PR2* (pigments de naphtol AS) | Toxicité aiguë (48 heures); statique | Puce d'eau (Daphnia magna) | CE50 supérieur(e) à 100 mg/L | Daphnies exposées à une solution saturée de 100 mg/L (brassage à 20 tr/min pendant 24 h; particules non dissoutes retirées par membrane filtrante, 0,45 µm) Aucune concentration mesurée Aucun effet biologique important (immobilisation) observé à saturation. |
Étude présentée, 2007a |
| PR253* (pigments de naphtol AS) | Toxicité aiguë (96 h) |
Carpe commune (Cyprinus carpio) | CL50 = 172 mg/L | Statique. Six concentrations d'essai (non mesurées) Aucune réaction toxique relevée jusqu'à une concentration de 90 mg/L. |
Étude présentée, 2007a |
| PR253* (pigments de naphtol AS) | Toxicité aiguë (24 h) |
Puce d'eau (Daphnia magna) | CE50 = 990,7 mg/L | Statique. Sept concentrations d'essai (non mesurées). 10 % d'immobilisation observée jusqu'à une concentration de 500 mg/L. | |
| PR146* (pigments de naphtol AS) | Toxicité aiguë (48 h) |
Puce d'eau (Daphnia magna) | CE50 supérieur(e) à 100 mg/L | Statique. Daphnies exposées à une solution saturée de 100 mg/L (brassage à 20 tr/min pendant 24 h; particules non dissoutes retirées par membrane filtrante, 0,45 µm) Aucune concentration mesurée Aucun effet biologique important (immobilisation) observé à saturation. |
Présentation de projet, 2007d |
| PR57:1* (pigments de BONA laqués) | Toxicité aiguë (96 h) |
Medaka (Oryzias latipes) | CL50 = 33 mg/L | Semi-statique. Des groupes de 10 poissons ont été exposés à cinq concentrations nominales (7,1-180 mg/L), contrôle du diméthylsulfoxyde (DMSO) (0,5 mg/L) et contrôle de l'eau en laboratoire Pureté du pigment : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité aiguë (72 h) |
Medaka (Oryzias latipes) | CL50 = 44 mg/L | Semi-statique. Des groupes de 10 poissons ont été exposés à cinq concentrations nominales (7,1–180 mg/L), contrôle du diméthylsulfoxyde (DMSO) (0,5 mg/L) et contrôle de l’eau en laboratoire Pureté du pigment : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité aiguë (48 h) |
Medaka (Oryzias latipes) | CL50 = 98 mg/L | Semi-statique. Des groupes de 10 poissons ont été exposés à cinq concentrations nominales (7,1–180 mg/L), contrôle du diméthylsulfoxyde (DMSO) (0,5 mg/L) et contrôle de l’eau en laboratoire Pureté du pigment : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité aiguë (24 h) |
Medaka (Oryzias latipes) | CL50 = 170 mg/L | Semi-statique. Des groupes de 10 poissons ont été exposés à cinq concentrations nominales (7,1–180 mg/L), contrôle du diméthylsulfoxyde (DMSO) (0,5 mg/L) et contrôle de l’eau en laboratoire Pureté du pigment : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité aiguë (48 h) |
Medaka (Oryzias latipes) | CL50 = 50 mg/L | Système à écoulement continu | MITI, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité aiguë (24 h) |
Puce d'eau (Daphnia magna) | CE50 = 280 mg/L | Statique. Ligne directrice de l'OCDE 202. Cinq concentrations nominales (90-940 mg/L; pureté : 87 %), contrôle du diméthylsulfoxyde (DMSO) à HCO-40 = 9:1 (100 mg/L) et contrôle de l'eau en laboratoire | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité chronique (72 h) |
Algues (Selenastrum capricornutum) | CSEO = 5,8 mg/L | Statique. Effets : biomasse CE50 calculée à partir de 13 concentrations nominales (1-1 000 mg/L) et du contrôle Pureté du pigment : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité chronique (72 h) |
Algues Selenastrum capricornutum | CL50 = 190 mg/L | Statique. Effets : biomasse CE50 calculée à partir de 13 concentrations nominales (1–1 000 mg/L) et du contrôle. Pureté du pigment : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité aiguë (24 h) |
Puce d'eau (Daphnia magna) | CL50 = 210 mg/L | Semi-statique. Effets : mortalité Daphnies exposées à cinq concentrations nominales (3-300 mg/L), contrôle du diméthylsulfoxyde (DMSO) à HCO-40 = 9:1 (100 mg/L) et contrôle de l'eau en laboratoire Pureté du pigment : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité aiguë (48 h) |
Puce d'eau (Daphnia magna) | CL50 = 43 mg/L | Semi-statique. Effets : mortalité Daphnies exposées à cinq concentrations nominales (3–300 mg/L), contrôle du diméthylsulfoxyde (DMSO) à HCO-40 = 9:1 (100 mg/L) et contrôle de l’eau en laboratoire Pureté du pigment : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité aiguë (96 h) |
Puce d'eau (Daphnia magna) | CL50 = 18 mg/L | Semi-statique. Effets : mortalité Daphnies exposées à cinq concentrations nominales (3–300 mg/L), contrôle du diméthylsulfoxyde (DMSO) à HCO-40 = 9:1 (100 mg/L) et contrôle de l’eau en laboratoire Pureté du pigment : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité aiguë (7 jours) |
Puce d'eau (Daphnia magna) | CL50 = 13 mg/L | Semi-statique. Effets : mortalité Daphnies exposées à cinq concentrations nominales (3–300 mg/L), contrôle du diméthylsulfoxyde (DMSO) à HCO-40 = 9:1 (100 mg/L) et contrôle de l’eau en laboratoire Pureté du pigment : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité chronique (14 jours) |
Puce d'eau (Daphnia magna) | CL50 = 10 mg/L | Semi-statique. Effets : mortalité Daphnies exposées à cinq concentrations nominales (3–300 mg/L), contrôle du diméthylsulfoxyde (DMSO) à HCO-40 = 9:1 (100 mg/L) et contrôle de l’eau en laboratoire Pureté du pigment : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité chronique (21 jours) |
Puce d'eau (Daphnia magna) | CL50 = 9,7 mg/L | Semi-statique. Effets : mortalité Daphnies exposées à cinq concentrations nominales (3–300 mg/L), contrôle du diméthylsulfoxyde (DMSO) à HCO-40 = 9:1 (100 mg/L) et contrôle de l’eau en laboratoire Pureté du pigment : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité chronique (14 jours) |
Puce d'eau (Daphnia magna) | CE50 = 4,4 mg/L | Semi-statique. Effets : reproduction Daphnies exposées à cinq concentrations nominales (3-300 mg/L), contrôle du diméthylsulfoxyde (DMSO) à HCO-40 = 9:1 (100 mg/L) et contrôle de l'eau en laboratoire Pureté : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité chronique (21 jours) |
Cladocère (Daphnia magna) | CE50 = 9,1 mg/L | Semi-statique. Effets : reproduction Daphnies exposées à cinq concentrations nominales (3–300 mg/L), contrôle du diméthylsulfoxyde (DMSO) à HCO-40 = 9:1 (100 mg/L) et contrôle de l’eau en laboratoire Pureté : 87 % | EA Japan, 1992 |
| PR57:1* (pigments de BONA laqués) | Toxicité chronique (21 jours) |
Cladocère (Daphnia magna) | CSEO = 3 mg/L | Semi-statique. Effets : reproduction Daphnies exposées à cinq concentrations nominales (3–300 mg/L), contrôle du diméthylsulfoxyde (DMSO) à HCO-40 = 9:1 (100 mg/L) et contrôle de l’eau en laboratoire Pureté : 87 % | EA Japan, 1992 |
Annexe E : Calculs de l'exposition écologique pour les pigments monoazoïques
A5.1 Calculs de l'exposition aquatique liée à la fabrication de pigment
Une importante installation de fabrication de pigments au Canada a été choisie pour estimer le niveau d'exposition aquatique aux pigments monoazoïques. L'estimation a été calculée comme suit :
La production quotidienne de pigments monoazoïques était un paramètre essentiel pour les calculs de l'exposition aquatique, mais elle était inconnue. Ce paramètre a été estimé sur la base de la quantité totale de pigments organiques fabriqués (déclarée) au Canada, soit 3 000 000 kg/an (Linak et al., 2011), et du nombre de jours de production, soit 300 jours/an, calculé pour la quantité fabriquée de 3 000 000 kg/an selon le document d'orientation sur l'évaluation des risques de la Commission européenne (Commission européenne, 2003) :
Production quotidienne de pigments monoazoïques :
= Quantité annuelle de pigments organiques fabriqués/Jours de production par année
= 3 000 000 kg/an/300 jours/an
= 10 000 kg/jour
Environnement Canada a mené un certain nombre de visites à des installations de fabrication de pigments en 2010 (Environnement Canada 2010) et a appris que l'équipement de production de pigments était régulièrement nettoyé avec de l'eau. Les eaux usées générées étaient ensuite traitées pour l’enlèvement des matières solides par un système de traitement des eaux usées sur place avant d’être rejetées dans le réseau d’égouts. Environnement Canada a également mené différentes visites à d'autres types d'installations, comme une installation de formulation de peinture au latex (Environnement Canada, 2013a), une installation de fabrication de revêtements en poudre (Environnement Canada, 2013b), une installation de fabrication de cosmétiques (Environnement Canada et Santé Canada, 2010) et à une installation de nettoyage de camion-citerne (Environnement Canada, 2009b). Toutes ces visites, y compris des installations de fabrication de pigments, ont montré que les produits perdus dans les eaux usées lors du nettoyage de l'équipement variaient grandement, mais ne dépassaient pas 10 % de la production totale ou du volume de retenue de l'équipement. Cette valeur de 10 % a été utilisée comme estimation prudente pour le plus fort facteur d'émission dans les eaux usées découlant du nettoyage de l'équipement de production des pigments.
Facteur d'émission dans les eaux usées découlant du nettoyage de l'équipement = 10 %
Les déversements quotidiens dans les eaux usées de pigments monoazoïques ont ensuite été estimés en multipliant la production quotidienne par le facteur d'émission.
Déversements quotidiens des pigments monoazoïques dans les eaux usées
= Production quotidienne de pigments monoazoïques × Facteur d'émission dans les eaux usées découlant du nettoyage de l'équipement
= 10 000 kg/jour × 10 %
= 1 000 kg/jour
On a déclaré que le traitement primaire des eaux usées sur place permettait d'éliminer 90 % des pigments avec une hydrosolubilité inférieure à 1 mg/L (OCDE, 2009, p. 58). Étant donné que tous les pigments monoazoïques ont une solubilité dans l'eau inférieure à 1 mg/L et que le traitement des eaux usées par l'installation sur place devrait afficher une efficacité d'élimination primaire ou équivalente, selon les visites des installations de fabrication des pigments (Environnement Canada, 2010), le taux d'élimination de 90 % a été utilisé pour le traitement des eaux usées sur place.
Traitement et élimination des eaux usées sur place = 90 %
Les rejets quotidiens de pigments monoazoïques dans le réseau d'égouts ont ensuite été estimés :
Déversements quotidiens de pigments monoazoïques dans le réseau d'égouts
= Déversements quotidiens de pigments monoazoïques dans les eaux usées × (1 - Traitement et élimination des eaux usées sur place)
= 1 000 kg/jour × (1 - 0,9)
= 100 kg/année
Les eaux usées traitées rejetées par l’installation ont ensuite été traitées par un système de traitement des eaux usées hors site. Ce système avait un débit de 334 900 000 L/jour. La concentration de pigments monoazoïques dans les eaux brutes est estimée en divisant les émissions quotidiennes dans le réseau d'égouts par le débit :
Concentration de pigments monoazoïques dans les eaux brutes
= Déversements quotidiens de pigments monoazoïques dans le réseau d’égouts / Débit du système de traitement des eaux usées hors site
= 100 kg/jour / 334 900 000 L/jour
= 298,6 × 10−9 kg/L
= 298,6 μg/L
L’élimination des pigments monoazoïques par le système de traitement des eaux usées hors site a été estimée à l’aide de modèles. Le système était du type secondaire, et son taux d'élimination a été estimé par le modèle ASTreat (2006) dans une plage allant de 0,5 à 49,2 %, sur la base de la plage de log Koe allant de -0,75 à 4,62 pour les pigments monoazoïques. Dans cette estimation, compte tenu du manque de données sur la biodégradation, on a considéré les pigments monoazoïques comme des substances non volatiles, en supposant qu'ils ne se biodégradent pas. Par conséquent, le taux d'élimination estimé était un résultat de la sorption des boues, uniquement. La valeur de l'extrémité inférieure de cette plage a été utilisée pour calculer une CEE aquatique prudente.
Traitement et élimination des eaux usées hors site = 0,5 %
La concentration de pigments monoazoïques dans les effluents a ensuite été calculée :
Concentration de pigments monoazoïques dans les effluents
= Concentration des pigments monoazoïques dans les eaux brutes × (1 − Traitement et élimination des eaux usées hors site)
= 298,6 μg/L × (1 - 0,005)
= 297 μg/L
Les eaux réceptrices du système de traitement des eaux usées hors site étaient un lac de grande taille, et on a présumé que le facteur de dilution au point de rejet était de 10. Ainsi, la concentration des pigments monoazoïques dans les eaux réceptrices près du point de rejet, ou la CEE aquatique, ont été estimées :
CEE aquatique
= Concentration des pigments monoazoïques dans les effluents / Facteur de dilution dans les eaux réceptrices
= 297 μg/L / 10
= 29,7 μg/L
La CEE pour la fabrication des pigments est présentée au tableau 14.
A5.2 Calculs de l'exposition aquatique pour la formulation des peintures et des revêtements
Soixante-quinze installations de formulation de peintures et de revêtements ont été identifiées par les utilisateurs industriels de pigments monoazoïques dans le cadre d'enquêtes menées en vertu de l'article 71 de la LCPE (1999 (Canada 2006, 2007, 2008, 2011), et huit d'entre elles ont été déterminées comme étant les utilisateurs les plus importants. En moyenne, huit installations ont utilisé 5 000 à 10 000 kg/an par pigment pour un ou plusieurs pigments monoazoïques. Ces huit installations ont donc été choisies pour déterminer le niveau d'exposition aquatique pour le secteur de formulation des peintures et des revêtements. Moins de cinq de ces autres installations ont initialement été définies comme des utilisateurs importants en fonction d'enquêtes menées en vertu de l'article 71 de la LCPE (1999) mentionnées ci-dessus, mais des questions de suivi ont montré que chacune de ces installations utilisait moins de 5 000 kg/an tous pigments monoazoïques combinés (courriels de l'installation adressés à Environnement Canada en 2013, source non citée).
Des pigments peuvent être libérés dans le milieu aquatique par l'intermédiaire du traitement des eaux usées lorsque l'équipement de formulation est nettoyé avec de l'eau. Le nettoyage est prévu pour les peintures et les revêtements à base d'eau. Les calculs de l'exposition présentés ci-dessous ont donc été basés sur des données liées aux peintures et aux revêtements à base d'eau.
On a déterminé que la taille d'un lot de production de peinture/revêtement variait de 1 000 à 19 000 kg, selon une analyse des données de l'industrie (Environnement Canada, 2012). Étant donné que la quantité rejetée à partir du nettoyage de l'équipement est proportionnelle à la taille du lot, la plus grande taille de lot (19 000 kg) a été utilisée pour calculer une CEE prudente.
Taille de lot maximale = 19 000 kg
La quantité de résidus perdus lors du nettoyage de l'équipement a également été obtenue à partir d'une analyse des données de l'industrie. Cette quantité, généralement exprimée comme un pourcentage d'une taille de lot et indiquée comme un facteur d'émission dans les eaux usées, était de 0,3 % (Environnement Canada, 2012) et elle a été utilisée pour le scénario de formulation de peintures et de revêtements.
Facteur d'émission dans les eaux usées : 0,3 %
La teneur en pigments des peintures et des revêtements à base d'eau variait de 15 % à 45 % sur la base d'un certain nombre de visites d'installations de formulation de peintures et de revêtements (Crechem Technologies, 2003), et de 2 % à 30 % sur la base d'une plus récente visite de site (Environnement Canada, 2013c). La plus forte teneur en pigments (45 %) a été choisie comme le scénario de la pire éventualité.
Teneur en pigments des peintures/revêtements = 45 %
Une analyse des données de l'industrie a montré que le nettoyage de l'équipement de formulation des revêtements était effectué en un jour (Environnement Canada, 2012). La quantité maximale de pigments rejetée dans des eaux usées brutes sur place a ensuite été estimée :
Quantité quotidienne maximale de pigments rejetée dans les eaux usées brutes sur place
= Taille de lot maximale × Teneur maximale de pigments dans les peintures/revêtements × Facteur d'émission dans les eaux usées
= 19 000 kg × 45 % × 0,3 % = 25,7 kg/jour
Des visites d'installations de formulation de peintures et de revêtements ont indiqué que le traitement des eaux usées sur place pour l'élimination des matières solides était courant pour les installations de grande taille (Crechem Technologies, 2003). Les visites de sites ont également indiqué que les eaux usées traitées sur place étaient ensuite traitées à nouveau par un système de traitement des eaux usées hors site avant de finir en milieu aquatique. On a donc pris en compte le traitement des eaux usées sur place et hors site dans les calculs de l'exposition.
Les pigments affichant une hydrosolubilité inférieure à 1 mg/L devraient être éliminés à 90 % par l'intermédiaire de boues primaires (OCDE, 2009). Étant donné que tous les pigments monoazoïques ont une solubilité dans l'eau inférieure à 1 mg/L et que les systèmes de traitement des eaux usées sur place devraient avoir au moins une efficacité d'élimination primaire ou équivalente, l'efficacité d'élimination devrait être de 90 % pour le traitement des eaux usées sur place.
Traitement et élimination des eaux usées sur place = 90 %
La quantité maximale de pigments rejetée dans le réseau d'égouts après le traitement des eaux usées sur place a ensuite été estimée :
Quantité maximale de pigments rejetée dans le réseau d'égouts
= Quantité quotidienne maximale de pigments rejetés dans des eaux usées brutes sur place × (1 - Traitement et élimination des eaux usées sur place)
= 25,7 kg/jour × (1 - 0,9)
= 2,57 kg/jour
Les calculs présentés ci-dessous dépendent de l'emplacement de l'installation concernée. Pour une installation au site C-2, le débit des eaux usées d’un système de traitement des eaux usées hors site était de 14 700 000 L/jour. La concentration de pigments dans les eaux brutes a ensuite été estimée :
Concentration de pigments dans les eaux brutes
= Quantité maximale de pigments rejetée dans le réseau d'égouts / Débit du système de traitement des eaux usées municipales hors site
= 2,57 kg/jour / 14 700 000 L/jour
= 1,75 × 10−7 kg/L = 175 μg/L
L’efficacité d’élimination des systèmes de traitement des eaux usées hors site aux huit installations de peintures et de revêtements a été estimée à l’aide de modèles. Les systèmes de traitement utilisés sur ces sites étaient tous secondaires, et leur efficacité d’élimination a été estimée à l’aide du modèle d’ASTreat (2006). Compte tenu du manque de données sur la biodégradation, on a considéré les pigments monoazoïques comme des substances non volatiles, en supposant qu'ils ne biodégradent au cours du traitement des eaux usées. Par conséquent, l'efficacité de l'élimination a été estimée uniquement en fonction de la sorption des boues. Ces estimations variaient de 0,5 à 49,2 % pour les systèmes secondaires, sur la base de la plage de log Koe allant de -0,75 à 4.62. La valeur inférieure de cette plage a été utilisée pour calculer des CEE aquatiques prudentes.
Traitement et élimination des eaux usées hors site = 0,5 %
Pour le site C-2, la concentration de pigments dans les effluents a été estimée :
Concentration de pigments dans les effluents
= Concentration des pigments dans les eaux brutes × (1 − Traitement et élimination des eaux usées hors site)
= 175 μg/L × (1 - 0,005) = 174 μg/L
La CEE aquatique a été estimée en divisant la concentration dans les eaux résiduaires par un facteur de dilution approprié dans l'eau réceptrice. Étant donné que la CEE aquatique est évaluée près du point de déversement, le facteur dilution dans les eaux réceptrices sélectionné doit également être applicable à cette exigence. Le plein potentiel de dilution d'une rivière, sur la base de son débit au 10e percentile, est considéré comme approprié si le facteur de dilution se situe entre un et dix. Sinon, la dilution est présumée à dix pour les grandes rivières et les eaux calmes. Les eaux réceptrices pour le système de traitement des eaux usées au site C-2 sont une rivière avec un débit au 10e percentile de 98 120 000 L/jour. Par conséquent, le facteur de dilution a été calculé comme suit :
Facteur de dilution dans les eaux réceptrices = Débit au 10e percentile / Débit du système de traitement des eaux usées municipales hors site
= 98 120 000 L/jour / 14 700 000 L/jour
= 6,7
Le facteur de dilution a été utilisé dans le calcul de la CEE aquatique pour le site C-2 :
CEE aquatique =
= Concentration de pigments dans les effluents / Facteur de dilution dans les eaux réceptrices
= 174 μg/L / 6,7 = 25,9 μg/L
Les CEE aquatiques pour les huit installations de formulation de peintures et de revêtements sont résumées au tableau 14.
A5.3 Calculs de l'exposition aquatique liée aux activités de désencrage
Dix-sept installations ont été définies comme menant des activités de désencrage du papier par trois sources, notamment le répertoire de Pulp and Paper Canada (2013), le répertoire de Lock-wood Post (2011) et la plateforme FisherSolveMC (2013). Parmi ces 17 installations, on disposait de renseignements suffisants sur 13 permettant d'effectuer des calculs de l'exposition aquatique. On a jugé que ces 13 installations représentaient bien l'ensemble du secteur canadien du désencrage.
La CEE aquatique a été estimée pour chacune des 13 installations. Ces installations ont généré et traité leurs eaux usées respectives sur le site, puis les ont déversées directement dans des eaux réceptrices. La CEE aquatique a été estimée pour chaque installation en fonction de la quantité de pigments monoazoïques entrant dans l'installation, du facteur d'émission dans les eaux usées, du volume d'eaux usées, de l'efficacité d'élimination sur place de l'usine de traitement des eaux usées, et de la dilution dans les eaux réceptrices.
Une explication détaillée des calculs de la CEE aquatique pour les pigments monoazoïques est fournie ci-dessus en prenant le site D-1 comme exemple.
Au Canada, la quantité de papier recyclé était de 4 170 000 tonnes ou représentait 69 % des déchets de papier générés en 2010, selon le Conseil des produits de pâtes et papiers (courriel de Marketing Strategy and Sustainability Consulting, Kitchener, Ontario, adressé à la Division des évaluations écologiques d'Environnement Canada en 2012, source non citée). Ces chiffres se sont traduits par 6 043 000 tonnes de déchets de papier générés en 2010 au Canada :
Quantité de déchets de papiers générée : = 4 170 000 tonnes / 69 % = 6 043 000 tonnes/an
La teneur moyenne des produits de papier imprimé en pigments monoazoïques peut donc être estimée en divisant la quantité totale de pigments monoazoïques utilisée par la quantité de déchets de papier générée. La quantité totale de pigments monoazoïques utilisée pour l'impression variait de 10 000 à 100 000 kg/an selon des enquêtes menées en vertu de la LCPE (1999) (Canada, 2006, 2007, 2008, 2011). La valeur de l'extrémité supérieure de cette plage a été utilisée pour calculer une teneur moyenne prudente en pigments monoazoïques dans les déchets de papier.
Teneur moyenne en pigments dans le papier : (100 000 kg/an) / 6 043 000 tonnes/an = 0,0165 kg/tonne
Cette teneur moyenne a été utilisée pour estimer la quantité de pigments pénétrant dans une installation de désencrage en fonction de sa capacité de désencrage. Par exemple, la capacité de désencrage de l'installation au site D-1 était de 71 375 tonnes/an (plateforme FisherSolveMC, 2013). L'apport annuel des pigments dans l'installation a ensuite été estimé :
Apport annuel de pigments : 0,0165 kg/tonne × 71 375 tonnes/an = 1 178 kg/an
L'installation au site D-1 fonctionne 350 jours/an sur une base continue (plateforme FisherSolveMC, 2013). L'apport annuel des pigments dans l'installation au site D-1 a ensuite été estimé :
Apport quotidien de pigments : (1 178 kg/an) / 350 jours/an = 3,37 kg/jour
Une recherche documentaire a été menée pour déterminer les facteurs d'émission dans les eaux usées découlant des opérations de désencrage. Peu de données ont été trouvées. On a ensuite communiqué avec une association industrielle qui a fourni une estimation de 20 % pour la proportion de pigments entrant dans les eaux usées par le désencrage (discussions téléphoniques entre un expert en pâtes et papiers d'une association industrielle et Environnement Canada en 2013, source non citée). Cette estimation a été utilisée dans des calculs ultérieurs.
Facteur d'émission dans les eaux usées : 20 %
La quantité quotidienne de pigments monoazoïques rejetée dans les eaux usées brutes à l'installation du site D-1 est estimée d'après le facteur d'émission dans les eaux usées de 20 % et l'apport quotidien de pigments monoazoïques dans l'installation :
Émissions quotidiennes de pigments dans les eaux usées brutes : 3,37 kg/jour × 20 % = 0,67 kg/jour
La concentration de pigments monoazoïques dans les eaux usées brutes a été estimée en divisant les émissions quotidiennes dans les eaux usées par le débit quotidien d'eaux usées généré. Pour le site D-1, le débit quotidien d'eaux usées généré était de 40 000 000 L/jour (plateforme FisherSolveMC, 2013). La concentration de pigments monoazoïques dans les eaux usées brutes a ensuite été calculée :
Concentration de pigments dans les eaux usées brutes = (0,67 kg/jour × 109 µg/kg) / 40 000 000 L/jour = 16,8 μg/L
où 109 μg/kg est un facteur de conversion.
Les pigments affichant une hydrosolubilité inférieure à 1 mg/L devraient être éliminés à 90 % par l'intermédiaire de boues primaires (OCDE, 2009). Étant donné que tous les pigments monoazoïques ont une solubilité dans l'eau inférieure à 1 mg/L et que les eaux usées générées par des installations de désencrage au Canada font l'objet d'un traitement secondaire, la réduction de la concentration de pigments monoazoïques sera au moins supérieure à 90 % par le traitement des eaux usées.
Pour l'installation au site D-1, la concentration maximale de pigments monoazoïques dans les eaux usées traitées est estimée :
Concentration maximale de pigments dans les eaux usées traitées :
= 16,8 μg/L × (1 - 0,9) = 1,7 μg/L
Les eaux réceptrices pour l'installation du site D-1 est une rivière avec un débit au 10e percentile de 950 400 000 L/jour. La pleine capacité de dilution des eaux réceptrices a été estimée comme étant le rapport entre le débit au 10e percentile et le volume quotidien d'eaux usées, notamment :
Pleine capacité de dilution des eaux réceptrices = (950 400 000 L/jour) / 40 000 000 L/jour = 24
Dans l'estimation de la concentration d'un produit chimique dans les eaux réceptrices, un facteur de dilution approprié doit être utilisé afin de bien caractériser la concentration près du point de rejet. Aux fins de la présente évaluation des risques, une capacité de dilution de dix fois a été choisie pour tenir compte de la dilution limitée près du point de rejet lorsque la pleine capacité de dilution est supérieure à 10. Pour l'installation du site D-1, la concentration de pigments monoazoïques dans les eaux réceptrices près du point de rejet ou la CEE aquatique ont donc été estimées :
CEE aquatique = 1,7 µg/L / 10 = 0,17 μg/L
Les CEE aquatiques pour tous les sites de désencrage sont résumées au tableau 14.
A5.4 Calculs de l'exposition dans les sédiments
Une méthode du partage eau-sédiment à l'équilibre décrite par l'Agence européenne des produits chimiques (ECHA, 2010) a été utilisée pour estimer la concentration de pigments monoazoïques dans les sédiments. Cette approche présume que la concentration dans les sédiments benthiques est en équilibre avec la concentration dans l'eau sus-jacente. Lors du partage à l'équilibre, la CEE dans les sédiments benthiques peut être en corrélation, de façon linéaire, avec la concentration dans la phase aqueuse de l'eau sus-jacente, comme suit :
CEE dans les sédiments = KseCe
où :
- K se :
- coefficient de partage sédiments-eau (L/kg)
- C e :
- concentration du produit chimique en phase aqueuse (mg/L)
Le coefficient de partage sédiments-eau (Kse, L/kg) peut être estimé à partir de la fraction de carbone organique (CO) des sédiments (Fco, kg CO/kg), de la capacité de sorption du carbone organique dans les sédiments (Aco, L/kg CO) et du coefficient de partage octanol-eau (Koe, sans dimension) (Gobas, 2010) :
Kse = FcoAcoKoe
Une valeur de CEE dans les sédiments peut alors être estimée à partir de l'équation :
CEE dans les sédiments = FcoAcoKoeCe
La concentration en phase aqueuse (Ce, mg/L) peut être estimée à partir de la CEE aquatique (mg/L). Il existe trois phases distinctes dans la colonne d'eau : aqueuse, sédiments sous forme de particules en suspension et sédiments dissolus en suspension (Gobas, 2007). Par conséquent, la concentration totale dans la colonne d'eau ou la CEE aquatique (mg/L) peut être exprimée sous forme de somme des concentrations dans la phase aqueuse (Ce, mg/L), dans les sédiments sous forme de particules en suspension (Cps, mg/L) et de sédiments dissolus en suspension (Csd, mg/L) :
CEE aquatique = Ce + Cps + Csd
Lorsque la phase de sorption d'une substance est une phase de carbone organique dans les sédiments sous forme de particules en suspension et de sédiments dissolus en suspension, l'équation ci-dessus peut être convertie de façon à exprimer le ratio de CEE aquatique (mg/L) afin d'obtenir la concentration en phase aqueuse (Ce, mg/L) (Gobas, 2007) :
CEE aquatique/Ce = 1 + (XspFpcoApco + XsdFdcoAdco)Koe
où :
- A pco :
- capacité de sorption de particules de CO par rapport à l'octanol (L/kg CO)
- A cod :
- capacité de sorption de CO dissolu par rapport à l'octanol (L/kg CO)
- F cop :
- fraction de CO dans les sédiments sous forme de particules en suspension (kg CO/kg)
- F cod :
- fraction de CO par rapport aux sédiments dissolus en suspension (kg CO/kg)
- K oe :
- coefficient de partage octanol-eau (sans dimension)
- X sp :
- contenu en sédiments sous forme de particules en suspension dans la colonne d'eau (kg/L)
- X sd :
- contenu de sédiments dissolus en suspension dans la colonne d'eau (kg/L)
Au Canada, le niveau moyen de matières particulaires en suspension dans la colonne d'eau (Xsp) est de 47 mg/L (Environnement Canada, 2013d). Cette valeur a été utilisée pour obtenir la CEE dans les sédiments aux sites évalués :
Xsp = 47 mg/L = 4,7 × 10−5 kg/L
Selon Gobas (2010), la fraction de CO dans les matières particulaires en suspension variait de 0,1 à 0,2 CO/kg de sédiments. Les valeurs inférieures de cette plage ont été utilisées pour calculer la CEE de façon prudente dans les sédiments.
Fcop = 0,1 kg CO/kg
Karickhoff (1981) a proposé une valeur de 0,41 L/kg CO pour la fraction de carbone organique des sédiments sur la base d'un ensemble de 17 échantillons de sédiments et de sol et de différents composés organiques non polaires et hydrophobes. Cette valeur a été utilisée comme capacité de sorption des particules de CO (Acop).
Acop = 0,41 L/kg CO
Au Canada, la teneur en CO dissous dans la colonne d'eau était en moyenne de 2,7 mg CO/L (Environnement Canada, 2013d). Cette valeur a été utilisée pour obtenir la CEE dans les sédiments aux sites évalués : Il est à noter que la teneur en CO équivaut au produit du contenu de sédiments dissous en suspension (Xsd, mg/L) et de sa fraction de CO (Fcod, kg CO/kg) :
XsdFcod = 2,7 mg CO/L = 2,7 × 10−6 kg CO/L
Gobas (2007) a fourni une estimation de 0,08 L/kg CO pour la capacité de sorption du CO dissous (Acod) Cette estimation a été utilisée.
Acod = 0,08 L/kg CO
Le coefficient de partage octanol-eau (Koe) montre une influence importante sur la CEE dans les sédiments. Selon les deux équations suivantes (décrites précédemment) :
CEE dans les sédiments = FcoAcoKoeCe
CEE aquatique/Ce = 1 + (XpsFcopAcop + XsdFcodAcod)Koe
la dépendance de la CEE dans les sédiments sur le Koe est calculée comme suit :
CEE aquatique = CEE aquatique × FcoAco/(1/Koe + XpsFcopAcop + XdsFcodAcod)
Cette dépendance révèle que la CEE dans les sédiments est proche de 0 pour les substances hydrosolubles avec un faible Koe, et d'une concentration constante maximale pour les substances hautement hydrophobes avec un Koe élevé. Autrement dit, la CEE dans les sédiments augmente en fonction du Koe. Les valeurs de log Koe pour les pigments monoazoïques variaient de -0,75 à 4,62. La valeur de l'extrémité supérieure de cette plage a été utilisée pour calculer des CEE prudentes dans les sédiments.
log Koe = 4,62 ou Koe = 41 687
Le rapport de la CEE aquatique à la concentration en phase aqueuse (Ce) a été calculé :
CEE aquatique/Ce = 1 + (XpsFcopAcop + XsdFcodAcod)Koe
= 1 + (4,7 × 10−5 kg/L × 0,1 kg CO/kg × 0,41 L/kg CO + 2,7 × 10−6 kg CO/L × 0,08 L/kg CO) × 41 687
= 1 + 2,14 × 10−6 × 41 687
= 1 + 0,089 = 1,089
À titre d'exemple, la CEE aquatique au site C-2 pour la formulation de peintures et de revêtements a été estimée à 25,9 µg/L. La concentration en phase aqueuse (Ce) au site a ensuite été calculée à partir du rapport CEE aquatique-Ce :
Ce = CEE aquatique/1,089 = 25,9 µg/L/1,089 = 23,8 µg/L
Gobas (2010) a suggéré une valeur par défaut de 0,01 à 0,03 CO/kg pour la fraction de CO dans les sédiments benthiques de rivières. La valeur de l'extrémité supérieure de cette plage a été choisie comme norme pour les CEE calculées.
Fco = 0,03 kg CO/kg
Pour les matières particulaires en suspension et les sédiments, la capacité de sorption du CO des sédiments benthiques a été relevée à 0,41 L/kg CO, sur la base des travaux de Karickhoff (1981).
Aco = 0,41 L/kg CO
La CEE dans les sédiments au site C-2 a ensuite été estimée à partir des valeurs ci-dessus :
CEE dans les sédiments = FcoAcoKoeCe
= 0,03 kg CO/kg × 0,41 L/kg CO × 41 687 × 23,8 µg/L
= 512,8 L/kg × 23,8 µg/L
= 12 205 µg/kg
= 12,2 mg/kg
Les CEE dans les sédiments pour tous les sites ont été estimées en suivant la méthode ci-dessus et sont résumées au tableau 14.
A5.5 Calculs de l'exposition dans le sol
Le secteur du désencrage a été sélectionné pour calculer une estimation prudente de la concentration des pigments monoazoïques dans le sol. Parmi les principaux secteurs de rejets (fabrication de pigments, formulation de peintures et de revêtements, et désencrage) pris en compte pour les calculs de l'exposition, le secteur du désencrage est la plus importante source de rejets dans les boues. Lorsque ces boues sont transformées en biosolides, puis épandues sur le sol, la quantité entière de pigments monoazoïques retirée du désencrage peut finir dans le sol, tandis que les deux autres secteurs n’émettent qu’un petit pourcentage de rejets dans le sol par l’intermédiaire des biosolides générés par des systèmes de traitement des eaux usées hors site. Le secteur du désencrage devrait donc émettre les plus fortes concentrations de pigments monoazoïques dans le sol.
La concentration de pigments monoazoïques dans le sol a été estimée dans le cadre d'un scénario prudent. Dans ce scénario, on a supposé que des biosolides contenant des pigments générés par le secteur du désencrage étaient épandus sur des terres agricoles au taux moyen de 28 tonnes humides/ha, tel qu'il a été déclaré à Québec (Hébert et Chaker, 2011), sur un nombre important d'années (10 ans). On a aussi présumé que les pigments s'étaient accumulés dans le sol et ne subissaient pas de dégradation, de volatilisation, de ruissellement du sol ou de pertes par lessivage. Les calculs détaillés sont présentés ci-après.
La quantité totale annuelle de pigments monoazoïques utilisée pour l'impression variait de 10 000 à 100 000 kg/an selon des enquêtes menées en vertu de la LCPE (1999) (Canada, 2006, 2007, 2008, 2011). La valeur de l'extrémité supérieure de cette plage a été utilisée pour établir une estimation prudente de l'exposition dans le sol.
Quantité totale annuelle de pigments monoazoïques : 100 000 kg/an
D'après le Conseil des produits de pâtes et papiers (courriel de Marketing Strategy and Sustainability Consulting, Kitchener, Ontario, adressé à la Division des évaluations écologiques d'Environnement Canada en 2012, source non citée), le taux de recyclage de papier était de 69 % au Canada en 2010. Sur la base de ce taux, la quantité de pigments monoazoïques dans le papier recyclé a été estimée :
Quantité de pigments dans du papier recyclé : 100 000 kg/an × 69 % = 69 000 kg/an
À titre d'estimation prudente, on a supposé que la quantité totale de pigments monoazoïques dans le papier recyclé finissait dans les boues d'usines de désencrage.
Quantité de pigments dans les boues : 69 000 kg/an
Des usines de papier journal menant des opérations de désencrage ont déclaré un taux moyen de production de boues de 835 tonnes anhydres/jour, selon une étude par contrat demandée par Environnement Canada (2009a). Ce taux quotidien se traduit par un taux annuel de 292 250 tonnes/an, en supposant que les usines de papier journal fonctionnent 350 jours/an.
Production annuelle de boues par les usines de désencrage = 292 250 tonnes/an
La concentration de pigments monoazoïques dans les boues issues d'usines de désencrage a été estimée en divisant la quantité de pigments dans les boues par la quantité de boues :
Concentration de pigments dans les boues = (69 000 kg/an) / 292 250 tonnes/an = 0,236 kg/tonne = 236 mg/kg
Le taux d'épandage de boues d'usines de pâtes et papiers au Québec a été utilisé. Le taux moyen déclaré était de 28 tonnes humides/ha (Hébert et Chaker, 2011). En supposant un taux moyen de biosolides de 40 % (Environnement Canada, 2009a), on obtient un taux moyen d'épandage sur le sol d'environ 11 tonnes anhydres/ha. Étant donné que 1 ha = 10 000 m2, le taux annuel d'épandage sur le sol annuel serait :
Taux annuel d'épandage sur le sol = 11 tonnes/ha par an = 1,1 kg/m2 par an
L'Agence européenne des produits chimiques (ECHA, 2010) a proposé d'utiliser une période de dix années consécutives comme durée d'accumulation dans l'évaluation de l'exposition dans le sol provenant de l'épandage de biosolides. La quantité de pigments monoazoïques reçue par mètre carré de sol modifié au cours de cette période de dix ans serait :
Quantité de pigments par mètre carré de sol
= Taux annuel d'épandage sur le sol × 10 ans × Concentration de pigments dans les boues
= 1,1 kg/m2 par an × 10 ans × 236 mg/kg
= 2 596 mg/m2
L'Agence européenne des produits chimiques (ECHA, 2010) a également proposé d'utiliser 20 cm (c.-à-d., 0,2 m) comme profondeur de labourage pour déterminer une couche de mélange. À l'aide d'une densité du sol sec de 1 200 kg//m3 (Williams, 1999), la masse de la couche supérieure de 20 cm du sol par mètre carré a été estimée :
Masse de la couche de sol de labourage par mètre carré = 1 200 kg/m3 × 1 m2 × 0,2 m = 240 kg/m2
La CEE dans le sol est calculée en divisant la quantité de pigments lors de l'épandage sur dix ans par la masse de la couche de sol de labourage par mètre carré :
CEE dans le sol = (2 596 mg/m2) / 240 kg/m2 = 10,8 mg/kg
Annexe F : Estimations de l’exposition liée à l’utilisation de cosmétiques
| Substance | Scénario pour le produit (adulte, sauf indication contraire) | Plage de concentration (% p/p) | Par exposition1Note de bas de page Annexe F Tableau 1 [a] (µg/kg p.c.) | Exposition quotidienne [a] (µg/kg p.c. par jour) |
|---|---|---|---|---|
| PY1 | Crème, lotion et hydratant pour le corps | 1-3 | 37-112 | 41-123 |
| PY1 | Maquillage pour le visage | 0,3-1 | 1,4-4,6 | 1,7-5,6 |
| PY1 | Fragrance/parfum en vaporisateur | inférieur(e) à 0,1 | inférieur(e) à 0,3 | 0-0,48 |
| PY1 | Savon liquide (pour la douche) | inférieur(e) à 1 | inférieur(e) à 0,24 | 0-0,24 |
| PY1 | Revitalisant capillaire | inférieur(e) à 0,1 | inférieur(e) à 0,12 | 0-0,12 |
| PY1 | Crème à raser pour homme (visage) | inférieur(e) à 0,1 | inférieur(e) à 0,06 | 0-0,06 |
| PY1 | Savon en pain (pour les mains) | inférieur(e) à 0,1 | inférieur(e) à 0,01 | inférieur(e) à 0,01 |
| PY1 | Produits pour le bain (huile) | 1-3 | inférieur(e) à 0,06 | s.o. |
| PY1 | Vernis à ongles | 3-10 | 1,3-4,3 | s.o. |
| PY1 | Sels de bain | inférieur(e) à 3 | inférieur(e) à 0,09 | s.o. |
| PY3 | Masque de beauté/maquillage pour le visage | 0,3-1 | 5,1-16,9 | 1,5-4,9 |
| PY3 | Fragrance/parfum en vaporisateur | inférieur(e) à 0,1 | inférieur(e) à 0,3 | 0-0,5 |
| PY3 | Savon liquide (pour la douche) | inférieur(e) à 1 | inférieur(e) à 0,24 | 0-0,24 |
| PY3 | Revitalisant capillaire | inférieur(e) à 0,1 | inférieur(e) à 0,12 | 0-0,12 |
| PY3 | Crème à raser pour homme (visage) | inférieur(e) à 0,1 | inférieur(e) à 0,06 | 0-0,06 |
| PY3 | Vernis à ongles | inférieur(e) à 0,1 | inférieur(e) à 0,06 | s.o. |
| PY3 | Sels de bain | inférieur(e) à 0,1 | inférieur(e) à 0,003 | s.o. |
| PY73 | Vernis à ongles | inférieur(e) à 0,1 | inférieur(e) à 0,042 | s.o. |
| PR4 | Masque de beauté/maquillage pour le visage | inférieur(e) à 1 | inférieur(e) à 16,9 | 0-4,9 |
| PR4 | Crème, lotion et hydratant pour le corps | inférieur(e) à 0,1 | inférieur(e) à 3,72 | 0-4,08 |
| PR4 | Maquillage pour le visage (fard à joues) | 3-10 | 0,9-3 | 1,08-3,72 |
| PR4 | Produit anti-rides (ancienne utilisation) | 0,3-1 | 3,1-10,1 | 5,5-18,3 |
| PR4 | Crayon pour les yeux | 3-10 | 0,06-0,12 | 0-0,06 |
| PR4 | Fard à paupières | 1-3 | 0,06-0,2 | 0,12-0,3 |
| PR4 | Savon liquide (pour la douche) | inférieur(e) à 1 | inférieur(e) à 0,2 | 0-0,2 |
| PR4 | Revitalisant capillaire | inférieur(e) à 0,1 | inférieur(e) à 0,12 | 0-0,12 |
| PR4 | Produits pour le bain (huile) | 1-3 | inférieur(e) à 0,06 | s.o. |
| PR4 | Vernis à ongles | inférieur(e) à 30 | inférieur(e) à 12,7 | s.o. |
| PR4 | Huile essentielle : massage | inférieur(e) à 0,1 | inférieur(e) à 6,8 | s.o. |
| PR4 | Sels de bain | 0,1-3 | inférieur(e) à 0,09 | s.o. |
| PR4 | Crème dépilatoire | inférieur(e) à 0,1 | inférieur(e) à 0,5 | s.o. |
| PR49:1 | Colorant capillaire - sans vaporisateur/lavable; semi-permanent | 0,3-1 | 0,5-1,5 | s.o. |
| PR53:1 | Fard à cils | inférieur(e) à 0,1 | inférieur(e) à 0,01 | inférieur(e) à 0,01 |
| PR53:1 | Colorant capillaire - sans vaporisateur/lavable; semi-permanent | 0,3-1 | 1,5-4,9 | 0,2-0,7 |
| PR112 | Fard à paupières | 0,1-0,3 | 0,003-0,02 | 0,01-0,03 |
| PR112 | Savon liquide (pour la douche) | inférieur(e) à 0,1 | inférieur(e) à 0,02 | inférieur(e) à 0,02 |
| PR112 | Vernis à ongles | inférieur(e) à 0,1 | inférieur(e) à 0,04 | s.o. |
| PR63:1 | Vernis à ongles | 10-30 | 0,71-2,12 | s.o. |
| Scénario pour le produit | Facteurs d'expositionNote de bas de page Annexe F Tableau 2 [a] |
|---|---|
| Crème, lotion et hydratant pour le corps | Fréquence d'exposition : 1,1/jour (Loretz et al., 2005) Quantité de produit : 4,4 g/application (Loretz et al., 2005) Facteur de rétention global : 1 (Cadby et al. 2002; Wormuth et al., 2005; CSPC, 2006; NICNAS, 2009; SDA, 2010a, b) Surface exposée : 16 925 cm2 |
| Préparations pour le bain (huile, sels) | Fréquence d'exposition = 0,285/jour Quantité de produit : 25 g/application Facteur de rétention global : 2,08 × 10−7 (facteur de dilution de RIVM, 2006a; le facteur de rétention présumé après le rinçage est de 0,001, sur la base d'un jugement scientifique |
| Laque pour cheveux | Fréquence d'exposition : 1,51/jour (Loretz et al., 2006) Quantité de produit : 3,64 g/application (Loretz et al., 2006) Facteur de rétention global : 0,09 |
| Savon liquide (pour la douche) | Fréquence d'exposition = 0,901/jour Quantité de produit : 8,7 g/application Facteur de rétention global : 0,0033 (SDA, 2010a) |
| Gel capillaire | Fréquence d'exposition : 0,586/jour Quantité de produit : 1,9 g/application Facteur de rétention global : 0,1 (CSPC, 2006) |
| Revitalisant capillaire | Fréquence d'exposition : 1,1/jour (Loretz et al., 2008) Quantité de produit : 13,1 g/application (Loretz et al., 2008) Facteur de rétention global : 0,01 (Wormuth et al. 2005; CSPC, 2006; SDA, 2010b) |
| Parfum en vaporisateur | Fréquence d'exposition : 1,7/jour (Loretz et al., 2006) Quantité de produit : 0,33 g/application (Loretz et al., 2006) Facteur de rétention global : 1 (Wormuth et al. 2005; SDA, 2010a, b) |
| Savon en pain (pour les mains) | Fréquence d'exposition : 6/jour Quantité de produit : 2,4 g/application Facteur de rétention global : 0,0033 (Cadby et al. 2002; RIVM, 2006a; SDA, 2010a) |
| Colorant capillaire | Fréquence d'exposition : 0,02/jour (communication personnelle : tableaux de données compilés par Statistique Canada - Cycle 1 de l'Enquête canadienne sur les mesures de la santé (ECMS) sur l'utilisation de produits d'hygiène utilisés par les Canadiens (2007-2009) à l'intention du Bureau d'évaluation du risque des substances existantes, mars 2012, source non citée) Quantité de produit : 100 g/application |
| Colorant capillaire en aérosol - temporaire (enfant) | Poids du corps d'un enfant (5 à 11 ans) : 31 kg (Santé Canada, 1998) Fréquence d'exposition : 0,016/jour (c.-à-d. 6 fois/an) |
| Vernis à ongles | Fréquence d'exposition : 0,43 fois/an Quantité de produit sur la peau : 0,05 g/application (adulte) |
| Maquillage pour le visage (y compris fard à joues) | Fréquence d'exposition : 1,24/jour (Loretz, 2006) Quantité de produit : 0,54 g/application (Loretz, 2006) Quantité de produit (fard à joues) : 0,54 g/application (Loretz, 2006) × 160 cm2 (RIVM, 2006a) / 637 cm2 (Santé Canada, 1998) = 0,14 g/application |
| Crème à raser pour homme (visage) | Fréquence d'exposition : 1/jour (Commission européenne, 2003) Quantité de produit : 4 g/application (SDA, 2010a) |
| Masque de beauté/maquillage pour le visage | Fréquence d'exposition : 2 fois/semaine Quantité de produit : 20 g/application |
| Fard à cils | Fréquence d'exposition : 0,67/jour (Wu et al., 2010) Quantité de produit : 0,025 g/application |
| Fard à paupières | Fréquence d'exposition : 1,2/jour (Loretz et al., 2010) Quantité de produit : 0,009 g/application (Loretz et al., 2010) |
| Crayon pour les yeux | Fréquence d'exposition : 0,68/jour (Wu et al., 2010) Quantité de produit : 0,005 g/application (CTFA, 2010a) |
| Produit anti-rides | Fréquence d'exposition : 1,80/jour (Loretz et al., 2005) Quantité de produit : 1,2 g/application (Loretz et al., 2005) Crème, lotion et hydratant pour le corps utilisés |
| Crème dépilatoire | Fréquence d'exposition : 0,0466 g/jour Quantité de produit : 5,5 g/application Facteur de rétention global : 0,1 (USEPA, 2011) |
| Substance | Scénario pour le produit (adulte, sauf indication contraire) | Plage de concentration ( % p/p) | Par exposition (µg/kg p.c.) | Absorption quotidienne (µg/kg p.c. par jour) |
|---|---|---|---|---|
| PY1 | Fragrance/parfum en vaporisateurNote de bas de page Annexe F Tableau 3 [a] | inférieur(e) à 0,1 | inférieur(e) à 0,1 | S.O. |
| PY3 | Fragrance/parfum en vaporisateur[a] | inférieur(e) à 0,1 | inférieur(e) à 0,1 | S.O. |
| PR4 | Rouge à lèvres | inférieur(e) à 3 | inférieur(e) à 4,2 | inférieur(e) à 10,2 |
| PR53:1 | Rouge à lèvres/baume pour les lèvres | inférieur(e) à 0,3 | inférieur(e) à 0,4 | inférieur(e) à1,0 |
| PR53:1 | Rouge à lèvres/baume pour les lèvres (tout-petit) | inférieur(e) à 0,3 | inférieur(e) à 1,9 | inférieur(e) à 1,1 |
| PR112 | Rouge à lèvres/baume pour les lèvres | 0,1–0,3 | 0,1–0,4 | 0,3–1,0 |
| PR112 | Rouge à lèvres/baume pour les lèvres (tout-petit) | 0,1–0,3 | 0,6–1,9 | 0,4–1,1 |
| Substance | Scénario pour le produit (adulte, sauf indication contraire) | Plage de concentration ( % p/p) | Par exposition (µg/kg p.c.) | Absorption quotidienne (µg/kg p.c. par jour) |
|---|---|---|---|---|
| PY1 | Fragrance/parfum en vaporisateur | inférieur(e) à 0,1 | inférieur(e) à 0,2 | inférieur(e) à 0,1 |
| PY3 | Fragrance/parfum en vaporisateur | inférieur(e) à 0,1 | inférieur(e) à 0,2 | inférieur(e) à 0,1 |
| Produit | Voies d'exposition | Facteurs d'exposition |
|---|---|---|
| Rouge à lèvres | Voie orale | Fréquence d’exposition : 2,4/jour (Loretz et al., 2005) Quantité de produit : 0,01 g/application (Loretz et al., 2005) Facteur de rétention global : 1 (SCCP, 2006; SDA, 2010a, b) Poids du corps d’un adulte : 70,9 kg (Santé Canada, 1998) Concentrations : diverses, telles qu’énoncées dans le tableau A6-3 (communication personnelle, courriels de la Direction de la sécurité des produits de consommation [Santé Canada] adressés au Bureau de l’évaluation des risques des substances existantes [Santé Canada], 2011-2014, source non citée) |
| Fragrance/ parfum en vaporisateur | Exposition par inhalation et par voie orale non respirable | Version 4.1 du modèle ConsExpo : « Exposition, modèle d'aérosol » Fréquence d'exposition : 1,7/jour (Loretz et al., 2006) Quantité de produit : 0,33 g/application (Loretz et al., 2006) Facteur de rétention global : 1 (Wormuth et al. 2005; SDA, 2010a, b) Poids du corps d'un adulte : 70,9 kg (Santé Canada, 1998) Concentrations : diverses, telles qu'énoncées dans les tableaux A-6-3 et A6-4 (courriels de la Direction de la sécurité des produits de consommation, Santé Canada, adressés au Bureau de l'évaluation des risques des substances existantes, Santé Canada, en 2011 et 2013, source non citée) Durée de la vaporisation : 0,08 min Durée d'exposition : 5 min Volume de la pièce : 10 m3 Hauteur de la pièce : 2,5 m Débit de ventilation : 2x/heure Volume du nuage : 0,0625 m3 Taux moyen de production massique : 0,1 g/s (RIVM, 2010) Fraction atmosphérique : 0,2 g/g Fraction massique non volatile : 0,05 g/g Densité de la fraction non volatile : 1,5 g/cm3 Moyenne de la distribution initiale des particules de diamètre (c.v.) : 2,7 µm (0,73) (RIVM, 2010) Diamètre minimum d'inhalation : 15 µm |
| Sous-ensemble des pigments monoazoïques | Substance | Utilisation potentielle d’encres de tatouage au Canada | Utilisation potentielle d’encres de tatouage en Europe |
|---|---|---|---|
| Pigments de βnaphtol | PR3 | Hauri (2010b) | |
| Pigments de βnaphtol | PR4 | Santé Canada (2011, 2013) Note de bas de page Annexe F Tableau 6 [a] |
Hauri (2010b) Hauri (2011b) NVWA (2008) |
| Pigments de βnaphtol | PO5 | Agence de protection de l’environnement du Danemark (2012) Hauri (2010c) |
|
| Pigments de βnaphtol laqués | PR49:1 | Hauri (2010c) | |
| Pigments de βnaphtol laqués | PR53:1 | Hauri (2010c) | |
| Pigments de BONA laqués | PR63:1 | Starbrite (2013) | Agence de protection de l’environnement du Danemark (2012) |
| Pigments jaunes monoazoïques | PY1 | Agence de protection de l’environnement du Danemark (2012) De Cuyper et D’hollander (2010) Hauri (2010b) Hauri (2011b) Høgsberg et al. (2010) NVWA (2008) |
|
| Pigments jaunes monoazoïques | PY3 | Santé Canada (2011, 2013)[a] SkinCandy (2013) |
Hauri (2011b) Høgsberg et al. (2010) NVWA (2008) |
| Pigments de naphtol AS | PR5 | Bäumler et al. (2000) Agence de protection de l’environnement du Danemark (2012) De Cuyper et D’hollander (2010) Hauri (2010b) Hauri (2011b) NVWA (2008) |
|
| Pigments de naphtol AS | PR112 | Santé Canada (2011, 2013) [a] |
Bäumler et al. (2000) Hauri (2010c) Hauri (2011b) Høgsberg et al. (2010) NVWA (2008) |
| Pigments de naphtol AS | PR170 | SkinCandy (2013) | Bäumler et al. (2000) Agence de protection de l’environnement du Danemark (2012) De Cuyper et D’hollander (2010) Hauri (2010c) Hauri (2011b) Høgsberg et al. (2010) NVWA (2008) |
| Pigments de benzimidazolone | PO36 | Hauri (2010b) |
Annexe G : Estimations de l’exposition liée à l’utilisation de pigments monoazoïques dans les peintures
| Sous-ensemble des pigments monoazoïques | Substance | Teneur maximale en pigment prévue (%)Note de bas de page Annexe G Tableau 1 [a] | Estimation de l’exposition par voie orale (mg/kg p.c. par événement) | Estimation de l’exposition par voie cutanée appliquée (mg/kg p.c. par événement)Note de bas de page Annexe G Tableau 1 [b] |
|---|---|---|---|---|
| Pigments de βnaphtol | PR4 | 1,75 | 0,452 | 0,12906 |
| Pigments de βnaphtol | PO5 | 0,57 | 0,147 | 0,04206 |
| Pigments de βnaphtol laqués | PR49:1 | 2 | 0,516 | 0,02458 |
| Pigments de BONA laqués | PR48:2 | 0,7 | 0,181 | 0,00860 |
| Pigments de BONA laqués | PR63:1 | 3 | 0,774 | 0,03687 |
| Pigments jaunes monoazoïques | PY1 | 0,8 | 0,206 | 0,05898 |
| Pigments jaunes monoazoïques | PY3 | 1.3 | 0,335 | 0,06959 |
| Pigments jaunes monoazoïques | PY73 | 1 | 0,258 | 0,07374 |
| Pigments de naphtol AS | PR5 | 5 | 1,290 | 0,36870 |
| Pigments de naphtol AS | PR112 | 1,1 | 0,284 | 0,08112 |
| Pigments de naphtol AS | PR170 | 1,3 | 0,335 | 0,09588 |
| Pigments de naphtol AS | PO38 | 3 | 0,774 | 0,03687 |
| Substance | Teneur maximale en pigment prévue (%)Note de bas de page Annexe G Tableau 2 [a] | Estimation de l'exposition par voie cutanée appliquée (mg/kg p.c. par événement)Note de bas de page Annexe G Tableau 2 [b] |
|---|---|---|
| PY3, PY73, PR112 | 15 | 0,813 |
| PR49:1, PR53:1, PR63:1 | 15 | 0,135 |
| PY1 | 0,3–1,0 | 0,016 – 0,054 |
| PR4 | 0,1–1,0 | 005 – 0,054 |
| Scénario pour le produit | Facteurs d'expositionNote de bas de page Annexe G Tableau 3 [a] |
|---|---|
| Peinture au doigt | Exposition par voie orale (utilisation du scénario pour la craie) C : charge = 400 mg/événement (RIVM, 2008) FM : fraction massique = variable, voir tableau G-1. P.C. : Poids corporel (tout-petit) = 15,5 kg Estimation de l’exposition par voie orale (par événement) = (C × FM) ÷ PC Exposition par voie cutanée (adaptée de LGC, 2000): C : charge = 1 905 mg/événement basé sur la charge ajustée à la surface sur une main d’adulte FM : fraction massique = variable, voir tableau G-1. Estimation de l'exposition par voie cutanée (par événement) = (C × FM) ÷ PC |
| Peinture faciale (enfant) | Exposition par voie cutanée C : charge = 1 400 mg/application (RIVM, 2006a) FM : fraction massique = variable, voir tableau G-2. P.C. : Poids corporel (tout-petit) = 15,5 kg Estimation de l’exposition par voie cutanée (par événement) = (C × FM) ÷ PC |
| Sous-ensemble des pigments monoazoïques | Substance | Clariant, 2011Note de bas de page Annexe G Tableau 4 [a] | Hansen, 2008 | Hauri, 2009b | Mont Marte, 2009a, 2009b |
|---|---|---|---|---|---|
| bêta-naphtol | PR3 | aquarelle et gouache, crayon, craie | peinture d’affiches | ||
| bêta-naphtol | PR4 | peinture à l’huile, aquarelle et gouache, craie | |||
| bêta-naphtol | PO5 | aquarelle et gouache, peinture acrylique, pastel à la cire, craie | |||
| pigment de bêta-naphtol laqué | PR53:1 | crayon, craie | pâte à modeler | ||
| BONA | PR63:1 | peinture acrylique, peinture aquarelle | |||
| monoazoïque jaune | PY1 | peinture à l’huile, aquarelle et gouache, peinture acrylique, crayon, pastel à la cire, craie | pâte à modeler | peinture acrylique, peinture aquarelle | |
| monoazoïque jaune | PY3 | peinture à l’huile, aquarelle et gouache, peinture acrylique, crayon, pastel à la cire, craie | peinture acrylique, peinture aquarelle | ||
| naphtol AS | PR5 | peinture à l’huile, aquarelle et gouache, peinture acrylique, crayon, craie | pâte à modeler | ||
| naphtol AS | PR112 | peinture à l’huile, aquarelle et gouache, peinture acrylique, crayon, pastel à la cire, craie | pâte à modeler | ||
| naphtol AS | PR170 | peinture à l’huile, aquarelle et gouache, peinture acrylique, crayon | |||
| autres | PO36 | peinture à l’huile, aquarelle et gouache, crayon, pastel à la cire |
| Substance | Teneur maximale en pigment prévue (%)Note de bas de page Annexe G Tableau 5 [a] | Peinture d’un mur à l’aide d’un pulvérisateur sans air compriméNote de bas de page Annexe G Tableau 5 [b] (mg/kg p.c. par événement) |
Ponçage de la peintureb (mg/kg p.c. par événement) |
|---|---|---|---|
| Pigments de β-naphtol PR3, PR4, PO5, NONPA; pigments de β-naphtol laqués PR49:1, PR53:1; pigments de BONA laqués PR48:2, PR52:1, PR52:2, PR63:1; pigments jaunes monoazoïques PY1, PY3, PY73 pigments de naphtol AS PR5, PR112, PR170, PR266; autre pigment PO36 |
5 | 0,000367 | 0,00055 |
Annexe H : Estimation de l’exposition à court terme aux pigments monoazoïques dans l’encre de tatouage permanente (adulte)
Les facteurs d’exposition ont été calculés à partir d’une étude qui examinait la perte de pigment de tatouage monoazoïque de la peau de souris in vivo due à la diffusion biologique et à la décomposition photochimique (Engel et al., 2009). Tandis que cette étude portait spécifiquement sur le Pigment Red 22 (PR22), une approche générique a été adoptée comme approche prudente pour estimer l’exposition aux pigments azoïques dans l’encre de tatouage. Dans Engel et al. (2009), 19 souris femelles SKH-1 rasées, divisées en quatre groupes, ont été tatouées sur leur zone dorsale avec du PR22. L’exposition à une lumière ambiante normale pendant 32 jours après 10 jours de récupération suivant l’injection initiale (total de 42 jours) a entraîné une réduction de 32 % du PR22 dans la peau. Ce pourcentage de perte a été considéré comme étant principalement attribuable à la diffusion biologique du pigment de tatouage dans le système lymphatique. Un groupe séparé de souris exposé au rayonnement solaire simulé au lieu de la lumière ambiante normale a montré une réduction de 60 % dans la concentration initiale de pigment dans la peau. La fraction de Pigment Red 22 photodécomposée qui a entraîné la formation d’amines aromatiques est inconnue pour le rayonnement solaire simulé. Par conséquent, ce scénario d’exposition est axé sur les expositions systémiques du pigment intact seulement.
Scénario d’exposition (EPA du Danemark, 2012, sauf indication contraire)
Voie d’exposition : Injection dans le derme
Concentration moyenne dans la peau : 2,53 mg pigment/cm2 dans de la peau humaine ou de cochon ex vivo (Engel et al., 2008)
Concentration dans la peau dans la pire éventualité : 9,42 mg pigment/cm2
Zone de peau couverte par le tatouage moyen : 430 cm2
Zone de peau couverte par le tatouage (tout le dos) : 1 090 cm2
Quantité de pigment azoïque dans le tatouage potentiellement disponible pour l’absorption :
MO (moyen) : 1,09 g
TD (tout le dos) : 10,3 g
P.C. (poids corporel d’un adulte): 70,9 kg p.c. (Santé Canada, 1998)
FP: Fraction de pigment dans le derme qui est mobilisée dans le système lymphatique :32 % sur 42 jours (Engel et al., 2009)
Exposition au pigment = [(MO – TD) × FP] ÷ (P.C. × Durée de l’étude)
= [(1,09 – 10,3 g) × 0,32] ÷ [70,9 kg p.c. × 42 jours]
= 0,12–1,1 mg/kg p.c. par jour
Par conséquent, l’exposition quotidienne systémique à court terme aux pigments monoazoïques chez les personnes tatouées est estimée à 0,12 mg/kg p.c. par jour en moyenne, et à 1,1 mg/kg p.c. par jour à titre d’estimation prudente.
Annexe I : Calculs des doses repères pour le PR3, le PO5, le PR4 et le PR53:1
| Substance | Sexe/ espèce (souche) |
Emplacement de la tumeur | Type de tumeur | BMD10 (mg/kg p.c. par jour) | BMDL10 (mg/kg p.c. par jour) |
Référence |
|---|---|---|---|---|---|---|
| PR3 | RF (F344) | Foie | Adénome | 1096,05 | 910,83 | NTP, 1992 |
| PR4 | RF (Wistar) | Foie | Nodules néoplasiques et cholangiome total | 88,42 | 41,38 | Kupradinun et al. 2002 |
| PR53:1 | RM (F344) | Foie | Nodules néoplasiques | 70,64 | 44,09 | NTP, 1982 |
| Rats F344/N mâles | Incidence des tumeurs malignes 0 ppm |
Incidence des tumeurs malignes 6 000 ppm |
Incidence des tumeurs malignes 12 500 ppm |
Incidence des tumeurs malignes 25 000 ppm |
|---|---|---|---|---|
| Dose équivalente (mg/kg p.c. par jour) | 0 | 272 | 568 | 1 181 |
| Foyers éosinophiles du foie | 6/50 | 37/50 | 36/50 | 41/50 |
| Foyers de cellules mixtes du foie | 2/50 | 24/50 | 21/50 | 15/50Note de bas de page Annexe I Tableau 2A [a] |
| Dégénérescence kystique du foie | 9/50 | 36/50 | 40/50 | 36/50[a] |
| Angiectasie multifocale du foie | 3/50 | 20/50 | 21/50 | 29/50 |
| Rats F344/N femelles | Incidence des tumeurs malignes 0 ppm |
Incidence des tumeurs malignes 6 000 ppm |
Incidence des tumeurs malignes 12 500 ppm |
Incidence des tumeurs malignes 25 000 ppm |
|---|---|---|---|---|
| Dose équivalente (mg/kg p.c. par jour) | 0 | 321 | 682 | 1 389 |
| Adénome hépatique | 0/50 | 0/50 | 1/50 | 10/50 |
| Tumeurs/effets | Nom du modèle | Nbre de groupes | CIA | Valeur prédictive | SRI | BMR | BMD10 (mg/kg p.c. par jour) | BMDL10(mg/kgp.c. par jour) |
|---|---|---|---|---|---|---|---|---|
| Foyers éosinophiles du foie | LogLogistic | 4 | 209,11 | 0,096 | -0,131 | 0,1 | 22,30 | 15,40 |
| Foyers de cellules mixtes du foie | LogLogistic | 3 | 163,48 | 0,019 | -0,173 | 0,1 | 60,62 | 41,84 |
| Dégénérescence kystique du foie | LogLogistic | 3 | 160,74 | 0,607 | -0,02 | 0,1 | 17,66 | 11,25 |
| Angiectasie multifocale du foie | LogLogistic | 4 | 232,8 | 0,242 | -0,291 | 0,1 | 88,61 | 63,12 |
| Tumeurs/effets | Nom du modèle | Nbre de groupes | CIA | Valeur prédictive | SRI | BMR | BMD10 (mg/kg p.c. par jour) | BMDL10(mg/kgp.c. par jour) |
|---|---|---|---|---|---|---|---|---|
| Adénome hépatique | Cancer multistades | 4 | 62,18 | 0,978 | 0,125 | 0,1 | 1 096,05 | 910,828 |
| Incidence des tumeurs | 0 ppm | 1 000 ppm | 2 000 ppm |
|---|---|---|---|
| Dose équivalente pour des rats femelles (mg/kg p.c. par jour) (conversion de Santé Canada) | 0 | 50 | 100 |
| Nodules hépatiques et cholangiome total | 3/50 | 6/47 | 8/50 |
| Tumeurs | Nom du modèle | Nbre de groupes | CIA | Valeur prédictive | SRI | BMR | BMD10 (mg/kg p.c. par jour) | BMDL10 (mg/kg p.c. par jour) |
|---|---|---|---|---|---|---|---|---|
| Nodules hépatiques et cholangiome total | LogLogistic | 3 | 106,63 | 0,796 | -0,133 | 0,1 | 88,42 | 41,38 |
| Incidence des tumeurs | 0 ppm | 1 000 ppm | 3 000 ppm |
|---|---|---|---|
| Dose équivalente pour des rats mâles (mg/kg p.c. par jour) (conversion de Santé Canada) | 0 | 50 | 150 |
| Nodules néoplasiques hépatiques | 0/50 | 6/50 | 7/49 |
| Tumeurs | Nom du modèle | Nbre de groupes | CIA | Valeur prédictive | SRI | BMR | BMD10 (mg/kg p.c. par jour) | BMDL10 (mg/kg p.c. par jour) |
|---|---|---|---|---|---|---|---|---|
| Adénomes hépatiques | LogLogistic | 3 | 81,0622 | 0,3054 | 1,281 | 0,1 | 70,6374 | 44,0888 |
Abréviations :
CIA, critère d'information d'Akaike;
BMD10, dose repère pour une incidence accrue de 10 % des tumeurs de la glande de Harder chez les souris mâles;
BMDL10, limite inférieure de l'intervalle de confiance de la dose repère pour une incidence accrue de 10 % des tumeurs de la glande de Harder chez les souris mâles;
BMR, réaction de référence;
SRI, résidu d'intérêt proportionné
Annexe J : Pigments monoazoïques avec effets préoccupants
Certains pigments monoazoïques figurant dans la présente évaluation préalable ont des effets préoccupants en raison du potentiel de cancérogénicité. Les détails à l’appui de la cancérogénicité potentielle de ces substances sont décrits à la section 7.2 « Évaluation des effets sur la santé » (voir les paragraphes pertinents), et sont généralement basés sur un ou plusieurs des éléments de preuve suivants :
- Classifications établies par des organismes nationaux ou internationaux quant à la cancérogénicité (il peut s’agir d’une classification de groupe).
- Preuve de cancérogénicité selon les études sur les animaux ou l’épidémiologie humaine pour une substance donnée.
- Potentiel de libération d’une ou plusieurs amines aromatiques EU22 par clivage de la liaison azoïque.
- Données déduites à partir d’analogues des substances connexes pour lesquelles un ou plusieurs des éléments de preuve ci-dessus s’appliquent.
| Nom ou acronyme de la substance et n° CAS | Classification de la cancérogénicitéNote de bas de page Annexe J Tableau 1 [a] | Preuve de cancérogénicité selon les études sur les animaux ou l’épidémiologie humaine | Libération d’amines aromatiques EU22 par clivage de la liaison azoïque | Données déduites à partir d’analogues |
|---|---|---|---|---|
| PO5 3468-63-1 |
x (Hart et al., 1986; USFDA, 1986) |
|||
| PR4 2814-77-9 |
Données déduites à partir d’analogues pour le PR3Note de bas de page Annexe J Tableau 1 [b] et le PO5 (pigments de βnaphtol, voir la section 7.2.1) |
|||
| PO2 6410-09-9 |
Données déduites à partir d’analogues pour le PR3[b] et le PO5 (pigments de βnaphtol, voir la section 7.2.1) |
|||
| PR6 6410-13-5 |
Données déduites à partir d’analogues pour le PR3[b] et le PO5 (pigments de βnaphtol, voir la section 7.2.1) |
|||
| NONPA 49744-28-7 |
Données déduites à partir d’analogues pour le PR3[b] et le PO5 (pigments de β-naphtol, voir la section 7.2.1) |
|||
| PR53:1 5160-02-1 |
x (NTP, 1982) |