Évaluation préalable Groupe des anthraquinones
Titre officiel : Évaluation préalable
Groupe des anthraquinones
Numéros de registre du Chemical Abstracts Service
81-48-1
81-77-6
6408-72-6
14233-37-5
17418-58-5
72391-24-3
74499-36-8
Environnement et Changement climatique Canada
Santé Canada
Juillet 2021
Cat. no. : En84-228/2021F-PDF
ISBN : 978-0-660-38280-7
Sommaire
En vertu des articles 68 ou 74 de la Loi canadienne sur la protection de l’environnement, 1999 (LCPE), les ministres de l’Environnement et de la Santé ont réalisé une évaluation préalable portant sur sept des quinze substances formant le « groupe des anthraquinones » et qui sont appelées ainsi dans le Plan de gestion des produits chimiques. Ces sept substances ont été jugées prioritaires pour une évaluation, car elles satisfont aux critères de catégorisation du paragraphe 73(1) de la LCPE ou suscitent d’autres préoccupations pour la santé humaine. Il a été établi par d’autres approches que les huit substances restantes étaient peu préoccupantes, et les décisions relatives à ces substances sont fournies dans des rapports distinct Note de bas de page 1,Footnote 2 . Par conséquent, le présent rapport d’évaluation préalable porte sur les sept substances énumérées dans le tableau ci-dessous. Les sept substances évaluées dans la présente évaluation préalable seront ci-après appelées les substances du groupe des anthraquinones.
| NE CASa | Nom dans la Liste intérieure des substances | Nom commun |
|---|---|---|
| 81-48-1 | 1-Hydroxy-4-(p-toluidino)anthraquinone | Solvent Violet 13 |
| 81-77-6 | 6,15-Dihydroanthrazine-5,9,14,18-tétrone | Pigment Blue 60 |
| 6408-72-6 | 1,4-Diamino-2,3-diphénoxyanthraquinone | Solvent Violet 59 |
| 14233-37-5 | 1,4-Bis(isopropylamino)anthraquinone | Solvent Blue 36 |
| 17418-58-5 | 1-Amino-4-hydroxy-2-phénoxyanthraquinone | Disperse Red 60 |
| 72391-24-3 | α-(Chloroacétamido)[4-[[4-(cyclohexylamino)-9,10-dihydro-9,10-dioxo-1-anthryl]amino]phénoxy]xylènesulfonate de sodium | Acid Blue 239 |
| 74499-36-8b, c | 1,4-Diaminoanthraquinone, dérivés N,N’-mixtes 2-éthylhexyliques, méthyliques et pentyliques. | N.D. |
Abréviations : N.D., non déterminé
a Le numéro de registre du Chemical Abstracts Service (NE CAS) est la propriété de l’American Chemical Society. Toute utilisation ou redistribution est interdite sans l’autorisation écrite préalable de l’American Chemical Society, sauf en réponse à des besoins législatifs et aux fins des rapports destinés au gouvernement du Canada en vertu d’une loi ou d’une politique administrative.
b Cette substance ne figure pas dans le paragraphe 73(1) de la LCPE, mais elle est visée par la présente évaluation, car elle est considérée comme prioritaire en raison des préoccupations pour la santé humaine qu’elle suscite.
c La substance de ce NE CAS est un UVCB (substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques).
Les substances du groupe des anthraquinones sont utilisées comme colorants dans des produits de consommation, notamment les cosmétiques (p. ex. crèmes pour le corps, rouges à lèvres/baumes pour les lèvres, maquillage, produits capillaires et peinture faciale), du matériel d’emballage des aliments, des matériaux de bricolage et d’artisanat (p. ex. étampes), des jouets, des articles de bricolage (p. ex., lubrifiants pour usages spéciaux, revêtements en époxy) et des textiles. D’après les renseignements fournis lors d’une enquête réalisée aux termes de l’article 71 de la LCPE, les quantités suivantes ont été importées pendant l’année civile 2011 : entre 1000 et 10 000 kg pour le Solvent Violet 13, entre 10 000 et 100 000 kg pour le Pigment Blue 60, entre 1000 et 10 000 kg pour le Solvent Violet 59, moins de 100 kg pour le Solvent Blue 36, entre 100 et 1 000 kg pour le Disperse Red 60 et l’Acid Blue 239 chacun, et entre 1000 et 10 000 kg pour la substance de NE CAS 74499-36-8. Aucune quantité n’a été déclarée pour la production des substances de ce groupe en quantité supérieure au seuil de déclaration de 100 kg, pour l’année civile 2011.
Les risques pour l’environnement associés aux substances du groupe des anthraquinones ont été caractérisés à l’aide de la Classification du risque écologique (CRE) des substances organiques, laquelle est une méthode fondée sur le risque qui tient compte de plusieurs paramètres liés au danger et à l’exposition, et sur une pondération des multiples éléments de preuve. Les profils de danger reposent principalement sur des paramètres liés au mode d’action toxique, à la réactivité chimique, aux seuils de toxicité interne établis à partir du réseau trophique, à la biodisponibilité et à l’activité chimique et biologique. Parmi les paramètres pris en compte pour les profils d’exposition, il y a le taux d’émission potentielle, la persistance globale et le potentiel de transport à grande distance. Une matrice de risques est utilisée pour attribuer aux substances un potentiel de préoccupation faible, moyen ou élevé, fondé sur leurs profils de danger et d’exposition. D’après les résultats obtenus avec l’analyse de CRE, il est improbable que les substances du groupe des anthraquinones puissent avoir des effets nocifs sur l’environnement.
Compte tenu de tous les éléments de preuve contenus dans la présente évaluation préalable, le Solvent Violet 13, le Pigment Blue 60, le Solvent Violet 59, le Solvent Blue 36, le Disperse Red 60, l’Acid Blue 239 et la substance de NE CAS 74499‑36‑8 présentent un risque d’effets nocifs faible sur l’environnement. Il est conclu que le Solvent Violet 13, le Pigment Blue 60, le Solvent Violet 59, le Solvent Blue 36, le Disperse Red 60, l’Acid Blue 239 et la substance de NE CAS 74499-36-8 ne satisfont pas aux critères énoncés aux alinéas 64a) ou b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
Pour la population générale du Canada, la principale source d’exposition aux substances du groupe des anthraquinones provient de l’utilisation des produits de consommation qui renferment ces substances. Pour chaque substance, l’exposition a été estimée pour les utilisations présentant le plus grand potentiel d’exposition. La principale voie d’exposition est la voie cutanée, mais certaines utilisations donnent lieu à une exposition par voie orale ou par inhalation. Les estimations de l’exposition potentielle au Solvent Violet 13 ont été obtenues en tenant compte de données sur l’utilisation de cosmétiques. Les estimations de l’exposition potentielle au Pigment Blue 60 ont été obtenues en tenant compte de données sur l’utilisation de matériaux de bricolage (p. ex. étampes). Les estimations de l’exposition potentielle au Solvent Violet 59 ont été obtenues en tenant compte de données sur la mise à la bouche de jouets en plastique. Les estimations du potentiel d’exposition au Solvent Blue 36 ont été établies en tenant compte de données sur l’utilisation d’après‑shampoing et de lubrifiants pour usages spéciaux. Les estimations de l’exposition potentielle au Disperse Red 60 et à l’Acid Blue 239 ont été établies en tenant compte de données sur le contact avec des textiles. Les estimations de l’exposition potentielle à la substance de NE CAS 74499-36-8 ont été établies en tenant compte de données sur l’application de produits de revêtement en époxy.
Le Pigment Blue 60 a été évalué à l’étranger par l’intermédiaire du Comité mixte FAO/OMS (Organisation des Nations Unies pour l’alimentation et l’agriculture/Organisation mondiale de la santé) d’experts des additifs alimentaires (JECFA). Dans les études de laboratoire, le Pigment Blue 60 était une substance toxique pour la reproduction, mais n’était pas génotoxique ni cancérogène. Le Solvent Blue 36 a été considéré comme toxique pour le développement. Étant donné certaines limites dans les renseignements sur les effets sur la santé d’autres substances du groupe des anthraquinones, une méthode d’extrapolation à partir des données sur les effets sur la santé du Solvent Blue 36 et de l’anthraquinone ont éclairé la caractérisation des effets de ces substances. À partir de l’anthraquinone, les effets critiques non cancérogènes pour le Solvent Violet 13, le Solvent Violet 59 et le Disperse Red 60 comprennent la toxicité pour les reins, le foie, la rate et la moelle osseuse, et à partir du Solvent Blue 36, les effets critiques non cancérogènes pour l’Acid Blue 239 et la substance au CAS RN 74499-36-8 sont des effets sur le développement. En ce qui concerne les effets cancérigènes, toutes les substances du groupe des anthraquinones sauf le Pigment Blue 60, sont considérées comme possiblement cancérogènes, étant donné leur squelette structurel commun, l’anthraquinone. Les marges d’exposition entre les niveaux d’exposition de la population générale, découlant de l’utilisation quotidienne du Solvent Violet 13 dans certains cosmétiques (crème pour le corps, parfum en aérosol), et les niveaux associés à des effets non cancérogènes sont considérées comme potentiellement inappropriées pour que soient levées les incertitudes dans les bases de données sur les effets sur la santé et l’exposition. Les marges entre les niveaux d’exposition de la population générale découlant de l’utilisation quotidienne du Solvent Violet 13 dans certains cosmétiques (baume à lèvres, rouge à lèvres, crème pour le corps, colorant capillaire permanent, parfum en aérosol et peinture faciale) et les effets cancérogènes ont également été considérés comme possiblement inadéquates. Les marges d’exposition ont cependant été jugées adéquates pour les autres utilisations du Solvent Violet 13 et pour d’autres substances du groupe des anthraquinones.
À la lumière des renseignements contenus dans la présente évaluation préalable, il a été conclu que le Solvent Violet 13 satisfait au critère du paragraphe 64c) de la LCPE, car il pénètre ou peut pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaines.
À la lumière des renseignements contenus dans la présente évaluation préalable, il a été conclu que le Pigment Blue 60, le Solvent Violet 59, le Solvent Blue 36, le Disperse Red 60, l’Acid Blue 239 et la substance de NE CAS 74499‑36‑8 ne satisfont pas au critère énoncé au paragraphe 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Par conséquent, il a été conclu que le Solvent Violet 13 satisfait à au moins un des critères énoncés à l’article 64 de la LCPE. Il a été conclu que le Pigment Blue 60, le Solvent Violet 59, le Solvent Blue 36, le Disperse Red 60, l’Acid Blue 239 et la substance de NE CAS 74499-36-8 ne satisfont à aucun des critères énoncés à l’article 64 de la LCPE.
Il a été conclu que le Solvent Violet 13 satisfait au critère de persistance, mais non à celui de la bioaccumulation, critères qui sont énoncés dans le Règlement sur la persistance et la bioaccumulation pris en application de la LCPE.
1. Introduction
En vertu des articles 68 et 74 de la Loi canadienne sur la protection de l’environnement, 1999 (LCPE), les ministres de l’Environnement et de la Santé ont réalisé l’évaluation préalable de sept des quinze substances formant le groupe des anthraquinones dans le Plan de gestion des produits chimiques, afin de déterminer si ces substances présentent ou peuvent présenter un risque pour l’environnement ou la santé humaine. Ces sept substances ont été jugées prioritaires pour une évaluation, car elles satisfont aux critères de catégorisation du paragraphe 73(1) de la LCPE ou suscitent d’autres préoccupations pour la santé humaine (ECCC, SC [modifié en 2017]).
Les huit autres substances (énumérées dans le tableau 1-1, ci-dessous) ont été prises en compte dans le document sur l’approche scientifique intitulé « Classification du risque écologique des substances organiques (CRE) », et soit dans le document sur l’approche scientifique intitulé « Approche fondée sur le seuil de préoccupation toxicologique (SPT) » (Santé Canada, 2016), soit par l’intermédiaire de l’approche appliquée dans l’Examen préalable rapide des substances avec une exposition limitée pour la population générale (ECCC, SC, 2018a), et ont été jugées peu préoccupantes pour la santé humaine et l’environnement. Par conséquent, la suite du rapport n’en traite pas. Les conclusions pour ces huit substances sont présentées soit dans l’évaluation préalable des substances jugées peu préoccupantes compte tenu de l’évaluation préalable réalisée à l’aide de la Classification du risque écologique des substances organiques et de l’Approche fondée sur le seuil de préoccupation toxicologique (SPT) pour certaines substances (ECCC, SC, 2017 b) soit dans le rapport de l’Évaluation rapide de substances auxquelles l’exposition de la population générale est limitée (ECCC, SC, 2018a). Les sept substances évaluées dans la présente évaluation préalable seront ci‑après appelées substances du groupe des anthraquinones.
| NE CASa | Nom dans la Liste intérieure des substances | Approche utilisée pour l’évaluation de la substance | Références |
|---|---|---|---|
| 2379-79-5 | 2-(1-Aminoanthraquinon-2-yl)anthra[2,3-d]oxazole-5,10-dione | CRE/SPT | ECCC, SC, 2018b |
| 2475-45-8 | 1,4,5,8-Tétraaminoanthraquinone | CRE/Examen préalable rapide | ECCC, SC, 2018a |
| 4051-63-2 | 4,4’-Diamino(1,1’-bianthracène)-9,9’,10,10’-tétraone | CRE/Examen préalable rapide | ECCC, SC, 2018a |
| 13676-91-0 | 1,8-Bis(phénylthio)anthraquinone | CRE/Examen préalable rapide | ECCC, SC, 2018a |
| 15791-78-3 | 1,8-Dihydroxy-4-[[4-(2-hydroxyéthyl)phényl]amino]-5-nitroanthraquinone | CRE/SPT | ECCC, SC, 2018b |
| 19286-75-0 | 1-Anilino -4-hydroxyanthraquinone | CRE/Examen préalable rapide | ECCC, SC, 2018a |
| 19720-45-7 | 1,4-Bis[(2-méthylpropyl)amino]anthraquinone | CRE/SPT | ECCC, SC, 2018b |
| 28173-59-3 | Carbonate de 2-[(1-amino-9,10-dihydro-4-hydroxy-9,10-dioxo -2-anthryl)oxy]éthyle et de phényle | CRE/SPT | ECCC, SC, 2018b |
a Le numéro de registre du Chemical Abstracts Service (NE CAS) est la propriété de l’American Chemical Society. Toute utilisation ou redistribution est interdite sans l’autorisation écrite préalable de l’American Chemical Society, sauf en réponse à des besoins législatifs et aux fins des rapports destinés au gouvernement du Canada en vertu d’une loi ou d’une politique administrative.
Les risques pour l’environnement associés aux substances du groupe des anthraquinones ont été caractérisés par l’approche de CRE (ECCC, 2016a). La CRE décrit les dangers d’une substance à l’aide de paramètres clés, y compris le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne obtenus à partir du réseau trophique, la biodisponibilité, ainsi que l’activité chimique et biologique, et elle tient compte de l’exposition possible des organismes dans les milieux aquatique et terrestre, d’après des facteurs comme les taux d’émission potentiels, la persistance globale et le potentiel de transport à grande distance dans l’atmosphère. Les divers éléments de preuve sont combinés afin d’identifier les substances nécessitant une évaluation plus poussée de leur potentiel de causer des effets nocifs sur l’environnement ou dont la probabilité de causer des effets nocifs sur l’environnement est faible.
La présente évaluation préalable tient compte des renseignements sur les propriétés chimiques, le devenir dans l’environnement, les dangers, les utilisations et l’exposition, ainsi que des renseignements supplémentaires présentés par les parties intéressées. Des données pertinentes ont été recensées jusqu’en avril 2017 et la documentation ciblée a été fouillée jusqu’en octobre 2020. Des données supplémentaires ont été fournies par les intervenants jusqu’en juillet 2019. Les données empiriques obtenues d’études clés, ainsi que certains résultats de modélisations ont servi à dégager les conclusions proposées. Lorsqu’ils étaient disponibles et pertinents, les renseignements contenus dans les évaluations effectuées par d’autres instances ont été utilisés.
La présente évaluation préalable a été préparée par le personnel des programmes d’évaluation des risques selon la LCPE, travaillant à Santé Canada et à Environnement et Changement climatique Canada. Elle comprend des informations provenant d’autres programmes de ces ministères. Le document sur la CRE a fait l’objet d’un examen externe par des pairs et d’une consultation publique de 60 jours. La partie de la présente évaluation préalable portant sur l’environnement est fondée sur le document décrivant la Classification du risque écologique (publié le 30 juillet 2016), qui a fait l’objet d’une évaluation externe par des pairs ainsi qu’une période de commentaires du public de 60 jours. Des commentaires sur les parties techniques ayant trait à la santé humaine ont été reçus de la part de mesdames Theresa Lopez, Jennifer Flippin et Joan Garey, de Tetra Tech. De plus, l’ébauche de la présente évaluation préalable (publiée le 3 novembre 2018) a fait l’objet d’une période de commentaires publics de 60 jours. Même si des commentaires externes ont été pris en compte, Santé Canada et Environnement et Changement climatique Canada assument l’entière responsabilité du contenu final et des conclusions de la présente évaluation préalable.
La présente évaluation préalable est axée sur des renseignements essentiels pour déterminer si les substances satisfont aux critères énoncés à l’article 64 de la LCPE. Pour ce faire, les renseignements scientifiques ont été étudiés et intégrés à une méthode fondée sur le poids de la preuve et le principe de précaution Footnote 3 . Dans la présente évaluation préalable, les renseignements essentiels et les considérations à partir desquels les conclusions proposées ont été dégagées sont présentés.
2. Identité des substances
Le NE CAS, le nom sur la Liste intérieure des substances (LIS) et le nom commun de chaque substance et de chaque structure représentative du groupe des anthraquinones sont présentés au Tableau 2‑1.
| NE CAS | Nom sur la LIS (nom commun) | Structure chimique et formule moléculaire | Masse molécu-laire (g/mol) |
|---|---|---|---|
| 81-48-1 | 1-Hydroxy-4-(p-toluidino)anthraquinone (Solvent Violet 13; aussi appelé Disperse Blue 72) | 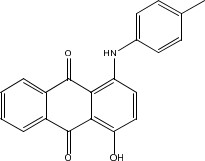 C21H15NO3 | 329,35 |
| 81-77-6 | 6,15-Dihydroanthrazine-5,9,14,18-tétrone (Pigment Blue 60) | ![Structure chimique représentative Pigment Blue 60, SMILES: c12c3c([nH]c4c5c(c(c6ccccc6c5=O)=O)ccc4[nH]3)ccc1c(c1ccccc1c2=O)=O](/content/dam/eccc/images/pded/anthraquinones/20210406-Table2.1.2.jpg) C28H14N2O4 | 442,43 |
| 6408-72-6 | 1,4-Diamino-2,3-diphénoxyanthraquinone (Solvent Violet 59; aussi appelé Disperse Violet 31 et Disperse Violet 26) |  C26H18N2O4 | 422,44 |
| 14233-37-5 | 1,4-Bis(isopropylamino)anthra-quinone (Solvent Blue 36) | 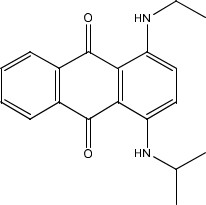 C20H22N2O2 C20H22N2O2 | 322,41 |
| 17418-58-5 | 1-Amino-4-hydroxy-2-phénoxyanthraquinone (Disperse Red 60) |  C20H13NO4 | 331,33 |
| 72391-24-3 | α-(Chloroacétamido)[4-[[4-(cyclohexylamino)-9,10-dihydro-9,10-dioxo-1-anthryl]amino]phénoxy]xy-lènesulfonate de sodium (Acid Blue 239) | 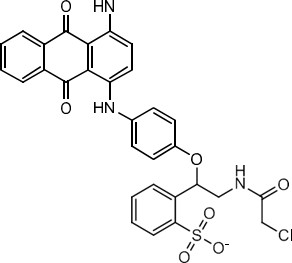 C36H34ClN3O7S.Na | 710,18 |
| 74499-36-8a | 1,4-Diaminoanthraquinone, dérivés N,N’-mixtes 2-éthylhexyliques, méthyliques et pentyliques(N.D.) | 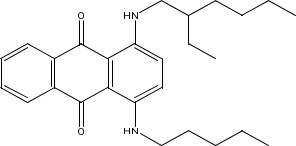 C27H36N2O2 | 420,60 |
Abréviations : N.D., non disponible
a La substance de ce NE CAS est un UVCB (substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques). La structure représentative et la formule moléculaire présentées ici appartiennent aux dérivés 2-éthylhexyliques et pentyliques.
2.1 Sélection d’analogues et utilisation des modèles QSAR
Une méthode d’extrapolation faisant appel à des données d’analogues et aux résultats des modèles de relations (quantitatives) structure-activité (QSAR), le cas échéant, a été utilisée pour éclairer l’évaluation relative à la santé humaine des substances du groupe des anthraquinones pour lesquelles les données sur certains effets critiques sont limitées. Des analogues ont été sélectionnés sur la base de structures et de propriétés similaires (propriétés physicochimiques et toxicocinétiques similaires) et la disponibilité de données empiriques pertinentes. Les précisions sur les données d’extrapolation choisies pour éclairer l’évaluation des effets des substances du groupe des anthraquinones sur la santé humaine sont données dans les sections pertinentes du présent rapport. L’un des analogues sélectionnés était l’anthraquinone, qui est le squelette structural commun des substances du groupe des anthraquinones et de leurs analogues. Il est présenté au tableau 2‑2 ci‑dessous. Le Solvent Blue 36, qui fait partie du groupe des anthraquinones, a également été utilisé pour éclairer le danger pour la santé humaine associé à l’Acid Blue 239 et à la substance au NE CAS 74499-36-8.
| NE CAS | Nom sur la LIS ou autre(nom commun) | Structure chimique et formule moléculaire | Masse moléculaire (g/mol) |
|---|---|---|---|
| 84-65-1 | Anthracène-9,10-dione (anthraquinone) | 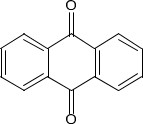 C14H8O2 | 208,22 |
3. Propriétés physiques et chimiques
Un résumé des propriétés physiques et chimiques des substances du groupe des anthraquinones est présenté au tableau 3-1. Les données expérimentales concernant les propriétés physiques et chimiques de ces substances sont limitées. Les valeurs modélisées s’appuient sur les données des modèles QSAR. D’autres propriétés physiques et chimiques sont présentées dans ECCC, 2016b (voir dans les références).
| Substance | Solubilité dans l’eau (mg/L) | log Koe | Pression de vapeur (Pa) | Principales références |
|---|---|---|---|---|
| Solvent Violet 13 | 0,001799 (estimation)a | 6,5 | 1,44 E-9 (estimation)b | BASF Corporation, 2015; EPI Suite, c2000-2012 |
| Pigment Blue 60 | « Non soluble »; 0,005 | 1 | « 0 »c | ECHA, 2017; Haynes, 2017 |
| Solvent Violet 59 | « Non soluble »; 0,053 | 5,19 | 1,34E-11 (estimation)b | Sijm et al., 1999; EPI Suite, c2000-2012; Brown, 1983 |
| Solvent Blue 36 | 0,004586 (estimation)a | 6,07 (estimation)d | 5,18E-7 (estimation)b | EPI Suite, c2000-2012 |
| Disperse Red 60 | 0,00064 | 1,77 | 9,53 E-10 (estimation)b | Yen et al., 1989; ECHA, c2007-2017; EPI Suite, c2000-2012 |
| Acid Blue 239 | 3,09 (estimation) | 0,96 (estimation) | 1E-19 (estimation) | ECCC, 2016b |
| N° CAS 74499-36-8 | 1,157E-6 (estimation)a | 9,58 (estimation)d | 9,71 E-10 (estimation)b | EPI Suite, c2000-2012 |
a La solubilité dans l’eau a été modélisée à l’aide du modèle WSKOW (EPI Suite, c2000-2012) et du log Koe expérimental de 6,5 comme intrant.
b La pression de vapeur a été modélisée à l’aide de la méthode de Grain modifiée (EPI Suite, c2000-2012).
c Étant donné l’absence de chiffre significatif, une valeur modélisée de 1,25 E-16 obtenue à l’aide de la méthode de Grain modifiée (EPI Suite, c2000-2012) a également été prise en compte.
d Le log Koe a été modélisé à l’aide du modèle KOWWIN (EPI Suite, c2000-2012).
4. Sources et utilisations
Toutes les substances du groupe des anthraquinones ont fait l’objet d’une enquête menée conformément à l’article 71 de la LCPE (Canada, 2012). Le tableau 4‑1 présente un résumé des quantités totales importées des substances du groupe des anthraquinones; aucune activité manufacturière supérieure au seuil de déclaration n’a été déclarée.
| Nom commun | Quantités totales importéesa (kg) |
|---|---|
| Solvent Violet 13 | 1000 – 10 000 |
| Pigment Blue 60 | 10 000 – 100 000 |
| Solvent Violet 59 | 1000 – 10 000 |
| Solvent Blue 36 | Moins de 100 |
| Disperse Red 60 | 100 – 1000 |
| Acid Blue 239 | 100 – 1000 |
| N° CAS 74499-36-8 | 1000 – 10 000 |
a Les valeurs représentent les quantités déclarées en réponse à une enquête menée en vertu de l’article 71 de la LCPE (Environnement Canada, 2013). Veuillez consulter les paramètres de l’enquête pour en connaître les inclusions et exclusions particulières (annexes 2 et 3).
Au Canada et dans le monde entier, les substances du groupe des anthraquinones servent de colorants et ont, de ce fait, plusieurs applications potentielles. Le tableau 4‑2 présente un résumé des principales utilisations des substances du groupe des anthraquinones, fondées sur les renseignements présentés en réponse à une enquête menée en vertu de l’article 71 de la LCPE (Environnement Canada, 2013). D’autres utilisations ont également été déclarées, mais ne sont pas indiquées ici, car elles sont considérées comme des renseignements commerciaux confidentiels.
| Substance | Utilisationsa |
|---|---|
| Solvent Violet 13 | Fabrication de chandelles |
| Pigment Blue 60 | Peintures et revêtements; automobile, aéronef et transport |
| Solvent Violet 59 | Jouets, équipement de terrain de jeu et de sport |
| Solvent Blue 36 | Entretien automobile; antigel et agent de déglaçage |
| Disperse Red 60 | Articles en tissus, en textile et en cuir |
| Acid Blue 239 | Articles en tissus, en textile et en cuir |
| N° CAS 74499-36-8 | Lubrifiants et graisses;combustibles et produits connexes, mélanges ou articles manufacturés |
a Renseignements non confidentiels sur les utilisations déclarées en réponse à une enquête menée en vertu de l’article 71 de la LCPE (Environnement Canada, 2013). Voir les enquêtes pour les inclusions et exclusions spécifiques (annexes 2 et 3).
Au Canada, le Solvent Violet 13, le Pigment Blue 60, du Solvent Violet 59 et le Disperse Red 60 a peuvent être utilisés comme composants dans les matériaux d’emballage des aliments. Le Solvent Violet 13 et la substance de NE CAS 74499-36-8 peuvent également être présents comme constituants d’additifs indirects utilisés dans les établissements de transformation alimentaire : le Solvent Violet 13 peut être utilisé comme constituant dans des désinfectants pour les mains qu’on rince à l’eau et qu’on utilise avant de manipuler la nourriture, et dans des nettoyants qu’on rince à l’eau, tandis que la substance de NE CAS 74499-36-8 peut être utilisée dans les lubrifiants synthétiques qui n’ont aucun contact avec la nourriture (communication personnelle, courriel de la Direction des aliments de Santé Canada, adressé au Bureau de l’évaluation des risques pour les substances existantes de Santé Canada, daté de 2016; sans référence).
D’après les avis présentés à Santé Canada en vertu du Règlement sur les cosmétiques, le Solvent Violet 13 et le Solvent Blue 36 sont présents dans les cosmétiques. Le Solvent Violet 13 est utilisé dans plusieurs cosmétiques, dont les crèmes pour le corps, les produits pour le bain, les rouges à lèvres/baumes pour les lèvres, le maquillage, les produits pour les ongles, les shampoings et après‑shampoings, les colorants capillaires permanents, les produits de coiffure, les parfums et les peintures faciales, tandis que le Solvent Blue 36 inscrit dans les avis est présent dans les après‑shampoings uniquement (communication personnelle, courriels de la Direction de la sécurité des produits de consommation et des produits dangereux et des produits dangereux de Santé Canada, adressés au Bureau d’évaluation du risque des substances existantes, Santé Canada datés de 2016 et 2019; sans référence).
Le Solvent Violet 13, qui a un rôle non médicinal et est destiné à un usage externe seulement en tant que colorant artificiel dans les produits de santé naturels, figure dans la Base de données d’ingrédients de produits de santé naturels (BDIPSN). Il figure également dans la Base de données des produits de santé naturels homologués (BDPSNH), étant présent en tant que tel, comme ingrédient non médicinal, dans un nombre limité de produits de santé naturels homologués à application topique, comme les produits pour le traitement de l’acné (p. ex. en gel ou en liquide), les nettoyants antiseptiques pour la peau (p. ex. en crème, en mousse, en gel, en liquide et en aérosol) et les produits antipelliculaires (p. ex. shampoings) (BDPSNH [modifié en 2016]); (BDPSNH [modifié en 2017]); communication personnelle, courriels de la Direction des produits de santé naturels et sans ordonnance [DPSNSO] adressés au Bureau d’évaluation du risque des substances existantes, datés de 2016‑2017; sans référence). Le Pigment Blue 60 est présent dans la Base de données sur les produits pharmaceutiques en tant qu’ingrédient non médicinal dans les désinfectants au Canada (communication personnelle, courriel de la Direction des produits thérapeutiques de Santé Canada adressé au Bureau d’évaluation du risque des substances existantes de Santé Canada, daté de 2016; sans référence). Cette utilisation est cependant limitée aux locaux destinés aux aliments, aux installations de soins de santé et/ou aux hôpitaux.
Le Solvent Violet 13 et le Pigment Blue 60 figurent sur la Liste des produits de formulation de l’Agence de réglementation de la lutte antiparasitaire (ARLA) de Santé Canada (communication personnelle, courriel de l’ARLA de Santé Canada adressé au Bureau d’évaluation du risque des substances existantes de Santé Canada, daté de 2016; sans référence). Aucune des substances du groupe des anthraquinones n’est parmi les ingrédients actifs homologués de pesticides au Canada (communication personnelle, courriel de l’ARLA de Santé Canada adressé au Bureau d’évaluation du risque des substances existantes de Santé Canada, daté de 2016; sans référence).
Aucune des substances du groupe des anthraquinones ne figure dans la Liste critique des ingrédients dont l’utilisation est restreinte ou interdite dans les cosmétiques ni n’est un additif alimentaire permis (Santé Canada [modifié en 2015a]; Santé Canada [modifié en 2015b]; communications personnelles, courriels de la Direction de la sécurité des produits de consommation et des produits dangereux et de la Direction des aliments de Santé Canada adressés au Bureau d’évaluation du risque des substances existantes de Santé Canada, datés de 2016; sans référence).
D’autres utilisations destinées aux consommateurs ont été trouvées au Canada pour certaines substances du groupe des anthraquinones dans des sources accessibles au public et sont énumérées au tableau 4-3.
| Substance | Utilisations | Références |
|---|---|---|
| Solvent Violet 13 | Shampoing pour animaux de compagnie | MSDS 2007a, 2015a |
| Pigment Blue 60 | Matériel de bricolage et d’artisanat (p. ex., étampes); peintures pour artistes | MSDS, 2009a,b,c, 2015b, 2018 |
| Solvent Blue 36 | Réparation d’enfoncements; lubrifiants pour usages spéciaux; gels pour bec de chalumeau | MSDS 2002, 2008, 2015c |
| N° CAS 74499-36-8 | Chandelles parfumées; nettoyants pour meubles; revêtements époxy | MSDS, 2007b,c,d, 2011b, 2015d |
Dans le monde entier, le Solvent Violet 13 est également un colorant utilisé dans les jouets qui ne sont pas en plastique (Danish EPA, 2015) et dans d’autres produits, notamment les textiles, le papier et les plastiques (ECHA c2007-2019a). Le Pigment Blue 60 a été trouvé dans les encres, les toners et les produits contenant du matériel à base de tissus, de textiles et de vêtements (p. ex. vêtements, matelas, rideaux, tapis et jouets en matière textile) (ECHA, 2017).
5. Devenir et comportement dans l’environnement
5.1 Persistance dans l’environnement
D’après les modèles utilisés par la méthode de CRE (ECCC, 2016b) le Solvent Violet 13, le Pigment Blue 60, le Solvent Violet 59, le Solvent Blue 36, le Disperse Red 60 et la substance au NE CAS 74499-36-8 devraient être persistantes dans l’eau, les sédiments et le sol. En outre, le Pigment Blue 60 devrait être persistant dans l’air. L’Acid Bleu 239 ne devrait pas persister dans l’eau, les sédiments, le sol ou l’air.
5.2 Potentiel de bioaccumulation
Pour ce groupe de substances, les facteurs de bioconcentration (FBC) prédictifs après correction pour métabolisme étaient tous faibles (ECCC 2016b). D’ailleurs, les diamètres transversaux modélisés pour ces substances étaient compris entre 1,3 et 2,4 nm (Catalogic 2014), ce qui indique que l’encombrement stérique au niveau des membranes cellulaires peut réduire l’absorption de ces substances à partir de l’eau, ainsi limitant, au bout du compte, la biodisponibilité et le potentiel de bioconcentration (Dimitrov et al. 2005).
Les FBC modélisés ont été jugés peu fiables, car les domaines de structure et/ou de propriété de ces substances se situent à l’extérieur des domaines des modèles (Environnement Canada, 2000). Par conséquent, des données empiriques de bioconcentration obtenues par extrapolation à partir d’analogues sélectionnés ont également été prises en compte. Les données empiriques d’extrapolation indiquent un faible potentiel de bioaccumulation du Solvent Violet 13. Le Disperse Blue 77 et le Solvent Blue 36 ont été identifiés comme des analogues du Solvent Violet 13 (boîte à outils QSAR de l’OCDE 2017). L’étude empirique des FBC pour le Disperse Blue 77 a produit des valeurs inférieures à 100. Un poids plus important a été attribué à cette étude, car elle est considérée comme fiable sur la base de l’évaluation du protocole expérimental (Hu et Shen 2008), et puisque du point de vue structurel, le Disperse Blue présente une similarité plus grande avec le Solvent Violet 13 qu’avec le Solvent Blue 36. Une pondération globale plus faible a été donnée au résumé de l’étude des FBC du Solvent Blue 36, qui a établi des FBC de 5300 à 5400 (J-CHECK c2010-), en raison du manque de détails suffisants pour évaluer sa fiabilité. D’ailleurs, une étude empirique de bioamplification pour le Solvent Blue 36 a déterminé un faible potentiel de bioamplification (Inoue et al. 2012).
6. Potentiel de causer des effets nocifs sur l’environnement
Les risques des substances du groupe des anthraquinones pour l’environnement ont été caractérisés à l’aide de la Classification du risque écologique des substances organiques (CRE) (ECCC, 2016a). La CRE est une approche fondée sur les risques qui tient compte de plusieurs paramètres liés au danger et à l’exposition et qui repose sur la pondération de plusieurs éléments de preuve. Les divers éléments de preuve sont combinés afin de distinguer les substances présentant une puissance plus ou moins élevée et un potentiel d’exposition plus ou moins élevé dans divers milieux. Cette approche réduit l’incertitude globale de la caractérisation des risques comparativement à une approche de caractérisation qui reposerait sur un seul paramètre dans un seul milieu (p. ex. la concentration létale médiane [CL50]). Puisque la substance de NE CAS 74499-36-8 est un UVCB et pourrait ne pas être bien représentée par une seule structure chimique, une méthode manuelle de classification, fondée sur le jugement, a été utilisée. Les paragraphes suivants résument l’approche, qui est décrite en détail dans ECCC (2016a).
Les données sur les propriétés physico-chimiques, le devenir (demi-vies chimiques dans divers milieux et biotes, coefficients de partage et bioconcentration dans les poissons), l’écotoxicité aiguë pour les poissons et les volumes de produits chimiques importés et fabriqués au Canada proviennent de diverses sources : la littérature scientifique, les bases de données empiriques disponibles (p. ex. boîte à outils QSAR de l’OCDE, 2014) et les réponses aux enquêtes réalisées en vertu de l’article 71 de la LCPE, ou ont été obtenues à partir de de modèles de relation (quantitative) structure-activité ([Q]SAR) ou de modèles du devenir du bilan massique ou de la bioaccumulation. Ces données ont été utilisées comme intrants dans d’autres modèles de bilan massique ou pour achever les profils d’exposition et de danger de la substance.
Les profils de danger reposent principalement sur des paramètres liés au mode d’action toxique, à la réactivité chimique, aux seuils de toxicité interne établis à partir du réseau trophique, à la biodisponibilité et à l’activité chimique et biologique. Les profils d’exposition sont également fondés sur de nombreux paramètres, dont les taux d’émission potentielle, la persistance globale et le potentiel de transport à grande distance. Les profils de danger et d’exposition ont été comparés aux critères de décision, permettant ainsi de classer les potentiels de danger et d’exposition de chaque substance organique comme faibles, moyens ou élevés. D’autres règles ont été appliquées (p. ex. cohérence de la classification, marge d’exposition) pour raffiner les classifications préliminaires du danger et de l’exposition. Cependant, dans le cas de la substance de NE CAS 74499-36-8, le danger et l’exposition pourraient ne pas constituer de profil en raison de l’absence de structure représentative pour estimer les propriétés nécessaires et de l’absence de données empiriques pour ces propriétés. Par conséquent, la classification manuelle du danger et de l’exposition a été réalisée au moyen de l’examen des constituants de l’UVCB et des données déclarées en réponse à une enquête menée en vertu de l’article 71 de la LCPE, et les décisions ont été fondées sur l’examen de substances similaires et l’application du jugement de spécialistes.
Une matrice de risques a été utilisée pour attribuer à chaque substance un risque potentiel faible, moyen ou élevé, fondé sur la classification de son danger et de son exposition. Les classifications du risque potentiel au moyen de la CRE ont été vérifiées à l’aide d’une approche en deux étapes. La première étape servait à ajuster les résultats de la classification du risque de moyen ou élevé à faible pour les substances présentant un faible taux d’émission estimé dans l’eau après le traitement des eaux usées, représentant un faible potentiel d’exposition. La deuxième étape servait à examiner les résultats de la classification du potentiel de risque faible selon des scénarios de risque relativement prudents, à l’échelle locale (c.-à-d. dans la zone à proximité immédiate du point de rejet) et conçus pour protéger l’environnement, afin de déterminer si la classification du risque potentiel devrait être accrue.
La CRE s’appuie sur une approche pondérée afin de réduire au minimum le potentiel de sous-classification et de surclassification des dangers, de l’exposition et des risques subséquents. Les approches équilibrées pour tenir compte des incertitudes sont décrites plus en détail dans le document ECCC 2016a (dans les références). Voici une description de deux des zones d’incertitude les plus importantes. Les erreurs dans les valeurs de toxicité aiguë empiriques et modélisées pourraient entraîner des modifications dans la classification du danger, en particulier en ce qui a trait aux paramètres reposant sur des valeurs de résidus dans les tissus (c.-à-d. mode d’action toxique), dont un grand nombre sont des valeurs estimées à l’aide de modèles QSAR (boîte à outils QSAR de l’OCDE 2014). Cependant, l’impact de cette erreur est atténué par le fait qu’une surestimation de la létalité médiane conduira à une valeur prudente (protectrice) pour les résidus dans les tissus, utilisée pour l’analyse des résidus corporels critiques (RCC). L’erreur dans la sous-estimation d’une toxicité aiguë sera atténuée par le recours à d’autres paramètres de danger, comme le profilage structural du mode d’action, la réactivité et/ou l’affinité de liaison à l’œstrogène. Les changements ou les erreurs dans les quantités chimiques pourraient entraîner des classifications différentes de l’exposition, car la classification de l’exposition et du risque dépend grandement du taux d’émission et des quantités utilisées. Les résultats de la CRE représentent donc l’exposition et le risque au Canada, fondés sur les estimations des quantités actuellement utilisées, et pourraient ne pas représenter les tendances futures.
Les données essentielles et les facteurs à considérer, utilisés pour élaborer les profils spécifiques des substances du groupe des anthraquinones, ainsi que les résultats de la classification du danger, de l’exposition et des risques figurent dans ECCC (2016 b).
Les classifications des sept substances du groupe des anthraquinones sur le plan du danger et de l’exposition sont résumées au tableau 6-1.
| Substance | Classification du danger selon la CRE | Classification de l’exposition selon la CRE | Classification des risques selon la CRE |
|---|---|---|---|
| Solvent Violet 13 | élevé | faible | faibles |
| Pigment Blue 60 | élevé | faible | modérés |
| Solvent Violet 59 | élevé | faible | faibles |
| Solvent Blue 36 | élevé | faible | faibles |
| Disperse Red 60 | élevé | faible | faibles |
| Acid Blue 239 | élevé | faible | faibles |
| N° CAS 74499-36-8 | élevé | faible | faibles |
Selon les données découlant de la CRE, le Solvent Violet 13, le Solvent Violet 59, le Solvent Blue 36, le Disperse Red 60, l’Acid Blue 239 et la substance au NE CAS 74499-36-8 ont un faible potentiel de danger. Le Solvent Violet 13, le Solvent Violet 59, le Solvent Blue 36, le Disperse Red 60, l’Acid Blue 239 et la substance au NE CAS 74499-36-8 ont été classés comme ayant un potentiel d’exposition élevé en raison de leur réactivité et leur potentiel d’effets nocifs sur les réseaux trophiques aquatiques et terrestre. En outre, des alertes structurales provenant de la boîte à outils de l’OCDE ont indiqué que le Solvent Violent 13 et le Disperse Red 60 sont des liants potentiels aux récepteurs endocriniens. La substance de NE CAS 74499-36-8 a également présenté un ratio d’écotoxicité élevé, ce qui indique une probabilité élevée de grande toxicité. Ces six substances ont été initialement classées comme ayant un potentiel de risques pour l’environnement moyen. Cependant, la classification du risque a diminué pour être portée à faible potentiel de risques pour l’environnement, après un ajustement de la classification des risques d’après les quantités utilisées à ce moment-là (voir la section 7.1.1 du document sur l’approche de la CRE dans ECCC, 2016a). Les effets potentiels et la façon dont ils peuvent se manifester dans l’environnement n’ont pas été étudiés plus en profondeur en raison de la faible exposition à ces substances. Étant donné les profils d’utilisation actuels, il est peu probable que ces substances suscitent des préoccupations relatives à l’environnement au Canada.
D’après les données prises en compte dans l’approche de CRE, le Pigment Blue 60 a été classé comme une substance ayant un faible potentiel d’exposition. Le potentiel de danger du Pigment Blue 60 a été classé élevé sur la base de l’adéquation entre la réactivité et le ratio d’écotoxicité élevé, les deux semblant indiquer une probabilité élevée de grande toxicité. De plus, le Pigment Blue 60 a été classé comme ayant un potentiel élevé de causer des effets nocifs dans les réseaux trophiques aquatiques. Le Pigment Blue 60 a été classé comme une substance ayant un potentiel modéré de risques pour l’environnement. Les effets potentiels et la façon dont ils peuvent se manifester dans l’environnement n’ont pas été étudiés plus en profondeur en raison de la faible exposition à cette substance. Compte tenu des profils d’emploi actuels, il est peu probable que ces substances suscitent des préoccupations pour l’environnement au Canada.
7. Potentiel de causer des effets nocifs sur la santé humaine
7.1 Évaluation de l’exposition
Les substances du groupe des anthraquinones n’ont pas été décelées ni mesurées dans aucun milieu de l’environnement au Canada ou ailleurs. Dans l’ensemble, étant donné les quantités commerciales limitées de ces substances au Canada, de leur très faible volatilité, de leur faible solubilité dans l’eau (sauf pour l’Acid Blue 239), de la dispersion de tout rejet potentiel et de l’élimination prévue par les unités de traitement des eaux, l’exposition par l’intermédiaire du milieu de l’environnement qui pourrait affecter la santé humaine de la population générale est considérée comme minime pour les substances de ce groupe.
Bien que les substances du groupe des anthraquinones n’aient pas été déclarées présentes dans la nourriture, un potentiel de contact direct par les aliments a été déterminé pour le Solvent Violet 13, le Pigment Blue 60, le Solvent Violet 59 et le Disperse Red 60 en raison de l’utilisation de ces substances dans la fabrication de matériel d’emballage des aliments au Canada (communication personnelle, courriel du Bureau de gestion du risque, Santé Canada, adressé au Bureau d’évaluation du risque des substances existantes, Santé Canada, daté du 17 février 2016; sans référence). Cependant, l’exposition à ces substances par le matériel d’emballage des aliments est considérée comme négligeable (communication personnelle, courriel de la Direction des aliments, Santé Canada, adressé au Bureau d’évaluation du risque des substances existantes, Santé Canada, daté du 24 avril 2017; sans référence).
Les expositions découlant de l’utilisation de produits de consommation ont été évaluées. Les estimations d’exposition pour les utilisations qui entraînent les niveaux d’exposition potentielle les plus élevés de chaque substance par la voie orale ou cutanée, appelées ci-après les scénarios sentinelles, sont présentées aux tableaux 7-1 et 7-2, respectivement. Les expositions potentielles ont été estimées à l’aide d’hypothèses prudentes et de valeurs par défaut. Voir l’annexe A pour des précisions sur les hypothèses, les valeurs par défaut et les algorithmes ou modèles utilisés pour estimer les expositions. L’exposition générale estimée pour chaque scénario est exprimée par utilisation et/ou par jour, selon la fréquence d’exposition et les effets critiques sur la santé (voir la section 7.3, Caractérisation des risques pour la santé humaine).
Pour la caractérisation des risques découlant des effets cancérogènes, les expositions générales quotidiennes estimées par groupe d’âge ont été utilisées sauf là où un ajustement pour la durée de la vie a été fait en guise d’approfondissement ou a été plus approprié au scénario (voir la section 7.3, Caractérisation des risques pour la santé humaine). Pour ces scénarios où un tel ajustement a été apporté, les doses quotidiennes moyennes à vie (DQMV) ont été calculées.
| Substance | Scénario pour le produit | Groupe d’âge | Exposition générale, par utilisation (mg/kg p.c.) | Exposition générale, par jour (mg/kg p.c./j) |
|---|---|---|---|---|
| Solvent Violet 13 | Baume pour les lèvres | Tout-petits | 0,0065 | 0,0038 |
| Solvent Violet 13 | Rouge à lèvres | Adultes | N.D. | 0,0034 |
| Solvent Violet 13 | Peinture faciale | Tout-petits | 0,53 | N.D. |
| Pigment Blue 60 | Matériel de bricolage et d’artisanat pour enfants (p. ex., étampes) | Tout-petits | 1,29 | 0,0645 |
| Solvent Violet 59 | Jouets en plastique, portés à la bouche | Tout-petits | 8,5E-06a | 3,4E-06a |
| Disperse Red 60 | Textiles, portés à la bouche | Nourrissons | 0,0027 b | 0,00027 b |
| Acid Blue 239 | Textiles, portés à la bouche | Nourrissons | 0,0027 b | 0,00027 b |
Abréviation : N.D., non déterminé
a Bien que l’action de porter un objet à la bouche soit considérée comme un geste quotidien, les estimations de l’exposition générale par utilisation et par jour correspondent à l’utilisation d’une concentration maximale et moyenne dans une simulation (voir annexe A).
b Bien que l’action de porter des textiles à la bouche soit considérée comme un geste quotidien, les estimations de l’exposition générale par utilisation et par jour correspondent à l’utilisation d’une fraction de migration initiale « aiguë » et de plus longue durée « chronique », respectivement (voir l’annexe A).
Pour estimer le risque de cancérogénicité potentielle du Solvent Violet 13 découlant d’une exposition par voie orale quotidienne (baume pour les lèvres appliqué sur les tout-petits et les enfants des groupes plus âgés, rouges à lèvres pour les adultes) ou d’une exposition par voie orale intermittente, par utilisation (peinture faciale appliquée sur les tout-petits), les DQMV de 0,00342 mg/kg p.c./j et de 0,00102 mg/kg p.c./j ont été calculées pour le Solvent Violet 13 utilisé dans le baume à lèvres ou le rouge à lèvres, et la peinture faciale, respectivement. Pour tous les autres scénarios d’exposition par voie orale, où les risques de cancérogénicité potentiels ont été estimés, les expositions générales quotidiennes par groupe d’âge ont été utilisées (voir la section 7.3, Caractérisation des risques pour la santé humaine).
Pour les expositions potentielles par voie cutanée estimées, l’approche du flux maximum (Jmax) (Williams et al., 2016) a été utilisée pour le Solvent Blue 36 et l’Acid Blue 239 pour la caractérisation plus poussée des expositions générales. Pour le Disperse Red 60, une fraction d’absorption par voie cutanée de 0,02 dans les zones de transpiration élevée a été utilisée comme hypothèse prudente dans l’estimation de l’exposition par les vêtements, conformément aux recommandations du groupe de travail sur les « textiles », au German Federal Institute for Risk Assessment (BfR, 2007). Cette recommandation est fondée sur des analyses d’études réalisées par l’Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers (ETAD, 1994, 1995) sur l’absorption cutanée de plusieurs colorants dispersés, dont le Disperse Red 60, en utilisant de la peau de porc et d’humain examinée après 55 heures. Bien que le plan expérimental de l’étude ne tienne pas compte des résidus de colorants liés à la peau à la fin des expériences, les données semblent indiquer une absorption cutanée relativement faible du Disperse Red 60 dans ces études.
Dans une étude d’absorption cutanée in vitro du Solvent Violet 13 faisant appel à de la peau humaine, l’absorption cumulative a été mesurée sur une période d’exposition de 24 heures dans des conditions où la zone est obstruée, pour deux préparations à l’essai (Charles River Laboratories, 2017). Une dose absorbable potentielle (qui comprend des mesures de la substance dans des bandes, 3 à 20, de la couche cornée de l’épiderme, de l’épiderme viable, du derme, du fluide récepteur et des eaux de rinçage de la chambre réceptrice) de 1,63 µg/cm2 a été mesurée en vue de la préparation d’un test sur une crème OilatumMD (contenant 1 % en poids de Solvent Violet 13 radiomarqué). Cette dose correspond à la dose moyenne potentiellement absorbable de 0,45 µ g/cm2 plus deux écarts‑types de 0,59 µ g/cm2 pour tenir compte de la variabilité élevée. Dans la même étude, une dose absorbable potentielle de 41,33 µ g/cm2 a été mesurée pour une préparation à l’essai consistant en de l’huile d’olive (contenant 10 % de Solvent Violet 13 radiomarqué, en poids). Cette dose correspond à la dose maximale potentiellement absorbable, car la dose moyenne plus deux écarts-types (pour tenir compte de la variabilité élevée) dépassent la dose maximale. Pour évaluer les expositions au Solvent Violet 13 par une crème pour le corps, la dose de 1,63 µ g/cm2 correspondant à la crème OilatumMD comme préparation à l’essai a été utilisée en raison de la similitude entre le type de produit et la préparation expérimentale. Pour tous les autres scénarios d’exposition cutanée, comme aucune préparation expérimentale n’avait de correspondance directe avec les types de produits, une fourchette de doses de 1,63 à 41,33 µ g/cm2 a été utilisée. L’absorption cutanée a été supposée, par prudence, équivalente à l’absorption par le tube digestif pour les autres substances du groupe.
Aucune donnée n’a été identifiée indiquant la présence de Solvent Violet 59 dans des produits disponibles pour les consommateurs qui pourrait causer une exposition cutanée à cette substance. Par conséquent, aucune exposition au Solvent Violet 59 par voie cutanée ne devrait se produire.
| Substance | Scénario pour le produit | Groupe d’âge | Exposition générale par utilisation (mg/kg p.c.)a | Exposition générale par jour (mg/kg p.c./j)a |
|---|---|---|---|---|
| Solvent Violet 13 | Crème pour le corps | Adultes | N.D. | 0,389 |
| Solvent Violet 13 | Parfum en aérosol | Adultes | N.D. | 0,00230 –0,0583 |
| Solvent Violet 13 | Colorant capillaire permanent | Adolescents | 0,0175 –0,444 | N.D. |
| Solvent Violet 13 | Peinture faciale | Tout-petits | 0,0457 –1,16 | N.D. |
| Pigment Blue 60 | Matériel de bricolage et d’artisanat (p. ex. étampes) | Tout-petits, Adolescentsb | 1,29, 0,337 | 0,0645, 0,0168 |
| Solvent Violet 59 | Colorant capillaire permanent | Adolescents | 0,0103 | N.D. |
| Solvent Blue 36 | Lubrifiant pour usages spéciaux | Adultes | 3,82E-05 | N.D. |
| Solvent Blue 36 | Après-shampoing | Adultes | N.D. | 1,84E-04 |
| Disperse Red 60 | Textiles, vêtements | Nourrissons | 0,00805c | 8,05E-04c |
| Disperse Red 60 | Textiles, vêtements | Adultes | 0,00513 c | 5,13E-04c |
| Acid Blue 239 | Textiles, vêtements | Nourrissons | 1,33E-05d | 1,33E-05d |
| Acid Blue 239 | Textiles, vêtements | Adultes | 8,49E-06d | 8,49E-06d |
| NE CAS 74499-36-8 | Revêtements époxy, application | Adultes | 0,0035 | N.D. |
Abréviation : N.D., non déterminé
a L’absorption cutanée du Pigment Blue 60 et de la substance de NE CAS 74499-36-8 a été supposée, par prudence, équivalente à l’absorption par le tube digestif. L’absorption cutanée supposée du Disperse Red 60 était de 2 %. L’absorption cutanée du Solvent Violet 13 a été estimée à 1,63 µg/cm2 ou à 1,63 à 41,33 µ g/cm2, selon le scénario. Les expositions cutanées au Solvent Blue 36, au Solvent Violet 59 et à l’Acid Blue 239 ont été estimées à l’aide de l’approche du flux maximum (voir l’annexe A).
b Bien que l’utilisation de ces produits par les adolescents puisse également entraîner une ingestion orale accidentelle, l’exposition cutanée estimée devrait être considérablement plus élevée que l’exposition orale potentielle pour ce groupe d’âge.
c Bien que l’action de porter des textiles soit considérée comme un geste quotidien, les estimations de l’exposition générale par utilisation et par jour correspondent à l’utilisation d’une fraction de migration initiale « aiguë » et de plus longue durée « chronique », respectivement (voir l’annexe A).
d À la différence du scénario appliqué au Disperse Red 60 ci-dessus, la distinction entre les scénarios d’exposition « aiguë » et « chronique » à l’Acid Blue 239 par le port de textiles n’est pas applicable à l’estimation de l’exposition cutanée étant donné l’utilisation de l’approche du flux maximum (voir l’annexe A).
Pour estimer le risque de cancer potentiel, les DQMV ont été calculées pour les expositions cutanées générales quotidiennes au Solvent Violet 13 présent dans plusieurs produits, au Solvent Violet 59 dans des colorants capillaires permanents, au Solvent Blue 36 dans des après-shampoings et au Disperse Red 60 et à l’Acid Blue 239 dans des textiles. Ces estimations d’exposition sont fournies au tableau 7‑3.
| Substance | Scénario de produits et groupe d’âge | DQMV (mg/kg p.c./j)a |
|---|---|---|
| Solvent Violet 13 | Crème pour le corps (enfants, adolescents, adultes) | 0,368 |
| Solvent Violet 13 | Parfum en aérosol (enfants, adolescents, adultes) | 0,00226 –0,0558 |
| Solvent Violet 13 | Colorant capillaire permanent (adolescents, adultes) | 2,4E-04 –0,00579 |
| Solvent Violet 13 | Peinture faciale (tout-petits, enfants, adolescents, adultes)b | 4,53E-04 –0,0115 |
| Solvent Violet 59 | Colorant capillaire permanent (adolescents, adultes) | 1,35E-04 |
| Solvent Blue 36 | Après-shampoing (tout-petits, enfants, adolescents, adultes) | 1,83E-04 |
| Disperse Red 60 | Textiles, vêtements (nourrissons, tout-petits, enfants, adolescents et adultes) | 5,45E-04 |
| Acid Blue 239 | Textiles, vêtements (nourrissons, tout-petits, enfants, adolescents et adultes) | 9,01E-06 |
Abréviation : DQMV, dose quotidienne moyenne à vie
a L’absorption cutanée supposée du Disperse Red 60 est de 2 %. L’absorption cutanée du Solvent Violet 13 a été estimée à 1,63 µg/cm2 ou à 1,63 à 41,33 µ g/cm2, selon le scénario. Les expositions cutanées au Solvent Blue 36, au Solvent Violet 59 et à l’Acid Blue 239 ont été estimées à l’aide de l’approche du flux maximum (voir l’annexe A).
b Bien que seulement les tout-petits ont été pris en compte dans le calcul de la DQMV pour les expositions par voie orale à la peinture faciale (en raison du potentiel de contact main-bouche), les enfants, les adolescents et les adultes ont également été pris en compte lors du calcul de la DQMV découlant d’expositions par voie cutanée (voir l’annexe A).
L’exposition quotidienne globale des nourrissons qui portent à leur bouche leur pyjama a également été calculée pour le Disperse Red 60 et l’Acid Blue 239 (0,00108 et 2,83 E-04 mg/kg p.c./j, respectivement). D’autres expositions globales potentielles (p. ex. expositions par voie orale et cutanée au Solvent Violet 13 dans la peinture faciale et co-expositions par l’utilisation de multiples cosmétiques contenant du Solvent Violet 13) ont été prises en compte, mais ne sont pas présentées en raison du caractère inadéquat potentiel des marges d’exposition (ME) de chaque estimation d’exposition par voie et par produit (voir la section 7.3, Caractérisation des risques pour la santé humaine).
L’exposition cutanée au Pigment Blue 60, par l’utilisation de peintures d’artiste (MSDS 2015b, 2018), et avec le Solvent Blue 36, par l’utilisation de produits de réparation d’enfoncements (MSDS, 2002) et de gels pour bec de chalumeau (MSDS, 2015c), ont également été pris en compte, mais tout contact de ce genre s’est révélé fortuit et inférieur aux autres estimations d’exposition par voie cutanée présentées ici.
L’exposition par inhalation a été examinée pour le Solvent Violet 13, par l’utilisation de parfums en aérosol; une exposition générale quotidienne de 1,72 E-05 mg/kg p.c./j a été estimée pour les adultes. L’exposition par inhalation aux autres substances du groupe des anthraquinones n’a pas été jugée préoccupante, en raison de leur volatilité très faible et de leur profil d’emploi (c.‑à‑d. produits non aérosols).
7.2 Évaluation des effets sur la santé
Les données d’effets sur la santé propres à un produit chimique étaient limitées pour les substances du groupe des anthraquinones. Des analogues potentiels ont été décelés à l’aide de la boîte à outils QSAR de l’OCDE (2014) et pris en compte en raison de leurs similitudes sur le plan des propriétés physiques et chimiques, de la métabolisation et de la structure. En utilisant une méthode d’extrapolation, les données sur les effets sur la santé provenant d’analogues ont été utilisées pour renseigner certains paramètres lorsque des données chimiques spécifiques sur les substances du groupe des anthraquinones n’étaient pas disponibles.
Les données d’effets sur la santé propres à un produit chimique pour chaque substance du groupe des anthraquinones seront présentées en premier, suivies par les effets sur la santé pour les produits chimiques sources (c.‑à‑d. analogues) utilisés dans les extrapolations et par un résumé des points de référence choisis pour la caractérisation des risques pour la santé humaine.
Solvent Violet 13
Dans une étude de toxicité orale à doses répétées sur 28 jours (ligne directrice 407 de l’OCDE), des rats Wistar (5/sexe/dose) ont reçu du Macrolex Violett B (contenant 97% de Solvent Violet 13) par gavage à des doses de 0, 250, 500 ou 1000 mg/kg pc/jour. Des changements statistiquement significatifs de certains paramètres hématologiques ont été observées chez les mâles et les femelles du groupe ayant reçu la dose la plus élevée (par exemple, augmentation des réticulocytes et diminution de l’hémoglobine corpusculaire moyenne (HCM), des érythrocytes, de l’hémoglobine, de l’hématocrite et des plaquettes), mais aucun changement histopathologique n’a été observé dans la rate ni la moelle osseuse. Il n’y a eu aucun effet sur le poids corporel ni le gain de poids corporel chez les mâles ni les femelles, quelle que soit la dose. L’examen histopathologique des tissus n’a révélé aucun changement lié à l’administration du produit chimique. Chez les femelles du groupe recevant 1000 mg/kg pc/jour, une diminution du poids des surrénales a été observé, mais à cette dose aucune diminution similaire n’a été constatée chez les mâles. En l’absence de tout changement histopathologique, les auteurs de l’étude ont déterminé que ces résultats ne représentaient pas d’effet indésirable causé par le traitement. Une dose sans effet nocif observé (DSENO) de 1000 mg/kg pc/jour, la plus forte dose testée, a été déterminée par les auteurs de l’étude (ECHA c2007-2019a).
Dans un test de dépistage de la toxicité pour la reproduction et le développement (ligne directrice 421 de l’OCDE), des rats Wistar (12/sexe/dose) ont reçu 0, 250, 500 ou 1000 mg/kg pc/jour de Macrolex Violett B (contenant 97 % de solvant Violet 13) par gavage pendant environ 6 semaines pour les mâles et jusqu’à 8 semaines pour les femelles, y compris une phase de 2 semaines avant l’accouplement, et pendant l’accouplement, la gestation et le début de la lactation pour les femelles. Aucun effet lié au traitement sur le poids corporel ni le poids de la thyroïde n’a été observé quel que soit le sexe. Aucun effet sur le poids des organes reproducteurs mâles n’a été observé, quelle que soit la dose. L’examen histopathologique des organes reproducteurs (testicules, épididymes et ovaires) des animaux témoins et des animaux recevant 1000 mg/kg pc/jour n’a révélé aucun effet lié au traitement. Un mâle recevant 1000 mg/kg pc/jour a présenté une masse sur l’épididyme droit et l’examen microscopique a révélé un léger granulome spermatique. Cependant, en l’absence de tout effet similaire dans ce groupe, les auteurs de l’étude ont jugé cette observation comme fortuite et non liée au traitement. L’évaluation de la thyroxine (T4) chez les mâles adultes et la progéniture à leur jour 13 n’a pas identifié d’effet lié au traitement, quelle que soit la dose. Il n’y a pas eu d’effet lié au traitement sur les cycles œstraux, les performances d’accouplement, la fertilité et la durée de gestation à des doses allant jusqu’à 1000 mg/kg pc/jour. Il n’y a pas eu d’effet sur le nombre d’implantations, la perte post-implantation, la taille de la portée et le rapport des sexes à la naissance, ni sur la survie ultérieure de la progéniture jusqu’au 13e jour de vie à des doses allant jusqu’à 1 000 mg/kg p.c./jour. Aucun effet lié au traitement n’a été observé chez la progéniture de la naissance jusqu’à l’arrêt au jour 13, quelle que soit la dose. Une DSENO de 1000 mg/kg pc/jour, la plus forte dose testée, pour les effets sur la reproduction et le développement a été établie par les auteurs de l’étude (ECHA c2007-2019a).
Le Solvent Violet 13 n’était pas mutagène dans un test de mutation inverse bactérien in vitro (c.-à-d. l’essai d’Ames) (Muzzal et Cook 1979). Il a également produit des résultats négatifs dans un test d’aberration chromosomique in vivo chez la souris (ECHA c2007-2019a). Le Solvent Violet 13 n’a pas manifesté d’effet cancérigène lorsque la peau de souris a été peinte avec 0,1 ml d’une solution à 1% (environ 4,7 mg/kg pc/jour) une fois par semaine pendant 18 mois (Carson 1984). Toutefois, cette étude est jugée limitée en raison de sa méthodologie (faible dose unique non exclue, régime de dosage hebdomadaire) et de ses incertitudes (une dose unique faible, non obstruée, de schéma posologique hebdomadaire) et des incertitudes (pureté, effet du vecteur, le sulfate de sodium à 0,1). Étant donné les données limitées sur les dangers spécifiques à la substance concernant les paramètres de toxicité chronique et de cancérogénicité, l’anthraquinone a été utilisé comme analogue pour éclairer cette partie de l’évaluation des dangers (comme décrit plus loin).
Pigment Blue 60
Le Pigment Blue 60 a été examiné par JECFA (1974) qui ont indiqué que la substance avait une toxicité aiguë par voie orale faible et n’est pas un sensibilisant cutané (Lu et Lavallée, 1964; Bär et Griepentrog, 1960). Aucun effet général n’a été observé chez le rat ayant reçu 50 mg/kg p.c./j pendant six mois, par l’alimentation (Umeda, 1956). Dans une étude de toxicité à doses répétées combinée avec le test de dépistage de la toxicité pour la reproduction et le développement (des lignes directrices no 422 de l’OCDE pour les essais), des rats (10/sexe/dose) ont reçu des doses de 0, 100, 300 ou 1000 mg/kg p.c./j par gavage pendant deux semaines, avant l’accouplement, pendant une durée totale d’environ cinq (mâles parents) à sept semaines (femelles traitées jusqu’au quatrième jour de lactation et petits traités jusqu’au quatrième jour postnatal) (Heucotech Ltd, 2013). À 1 000 mg/kg p.c./j, il y a eu la perte d’une portée entière chez une mère, une augmentation des pertes post-implantatoires, une diminution de la consommation maternelle de nourriture (diminution de 13 % pendant la gestation), une légère diminution du poids corporel des mères (pendant la gestation) et une diminution de la prise de poids corporel chez les mères (diminution de 20 % entre le jour de la conception et le septième jour de gestation), sans effet observé à 100 ou à 300 mg/kg p.c./j. Bien que dans d’anciennes archives on ait noté une autre mère du groupe témoin ayant perdu une portée entière et deux mères ayant perdu 93 % de leur portée, la perte d’une portée entière était inhabituelle, de sorte qu’elle n’a pas été indiquée, comme d’habitude. Il est admis que l’importance biologique des effets sur la reproduction n’était pas claire, étant donné que les effets ont été causés à la dose limite, qu’aucun effet n’a été observé chez les petits et que les deux effets sur la reproduction ont été influencés entièrement ou en grande partie par une mère. Cependant, puisque l’unique mère représentait 10 % du groupe échantillonné et que l’ampleur des pertes post‑implantatoires dépassait celles des sujets témoins de l’étude et des études antérieures, la DSENO pour la reproduction était de 300 mg/kg p.c./j (Heucotech Ltd, 2013). La DSENO parentale a été établie à 300 mg/kg p.c./j, d’après la diminution de la consommation maternelle de nourriture (statistiquement significative pendant la gestation) et la diminution de la prise de poids corporel chez les mères (statistiquement significative entre le jour de la conception et le septième jour de gestation) à la dose minimale avec effet nocif observé (DMENO) de 1000 mg/kg p.c./j (Heucotech Ltd, 2013).
À l’appui de la DSENO pour la reproduction de 300 mg/kg p.c./j, des rats (20 à 23/sexe/dose) ont reçu des doses de 0 à 500 mg/kg p.c./j par l’alimentation pendant six mois précédant l’accouplement et jusqu’à deux ans, sauf lors de la période de lactation, dans une étude de toxicité pour la reproduction combinée à une étude de cancérogénicité. Une diminution du poids corporel a été notée (30 g comparativement à 50 g chez les sujets témoins) après une exposition pendant le reste de la période de deux ans (Oettel et al.,1965). Malheureusement, les précisions fournies sur les études étant limitées concernant les paramètres de la reproduction ont réduit la confiance en ces études combinées sur la toxicité pour la reproduction et la cancérogénicité pour établir une DSENO pour la reproduction (Oettel et al.,1965).
La génotoxicité in vitro du Pigment Blue 60 était mixte. Avec ou sans activation métabolique, le Pigment Blue 60 n’a pas été génotoxique dans les tests d’Ames (ETAD, 1988) ni dans les essais d’aberration chromosomique, mais il a été génotoxique dans un test d’échange de chromatides sœurs (NTP [modifié en 2017]).
Invariablement, aucune tumeur ni toxicité générale n’a été observée après deux ans d’exposition, chez des rats, à des doses de 0, 50 ou 500 mg/kg p.c./j par voie alimentaire dans une étude sur la cancérogénicité (DFG, 1957) ou à une dose de 500 mg/kg p.c./j par voie alimentaire dans une étude combinée de toxicité pour la reproduction et de cancérogénicité (Oettel et al., 1965). Bien que la méthodologie de l’étude présente des limites, notamment dans le nombre d’animaux (jusqu’à 23/sexe/dose dans les études de cancérogénicité, le manque de précisions), les deux études limitées semblent indiquer que le Pigment Blue 60 n’était ni génotoxique ni cancérogène.
Solvent Blue 36
Dans une étude de toxicité à doses répétées combinée avec l’essai de dépistage de la toxicité pour la reproduction et le développement (Essai no 422 des lignes directrices de l’OCDE), des rats (12/sexe/dose) ont reçu par gavage des doses de 0, 12, 60 ou 300 mg/kg p.c./j pendant environ six ou sept semaines jusqu’au quatrième jour postnatal (MHLWJ, 2012). En outre, un groupe de rats non reproducteurs (5/sexe/dose) a reçu, par gavage, des doses de 0 ou de 300 mg/kg/j pendant six semaines et a également été examiné après une période de récupération de deux semaines. À la dose faible de 12 mg/kg p.c./j et aux doses supérieures, une diminution a été constatée dans la consommation de nourriture chez les mères en phase post-natale (de 16 % à 20 %) et dans la prise de poids corporel (13 % ou 60 %). À partir de la dose de 60 mg/kg p.c./j, les mâles de la génération parentale exposés pendant six semaines ont présenté une toxicité au foie (augmentation du poids absolu et du poids relatif du foie), tandis que les mères ont présenté une augmentation de la toxicité (y compris une diminution de 5 % du poids corporel, une diminution de 15 % du poids absolu et de 13 % du poids relatif de l’hypophyse, une diminution des globules blancs [leucocytes, neutrophiles, basophiles, monocytes] et une augmentation des concentrations des hormones thyroïdiennes [T3, T4, TSH]). À 300 mg/kg p.c./j, une augmentation de la toxicité a été constatée chez tous les adultes exposés pendant six semaines, notamment une augmentation des concentrations de l’alanine aminotransférase (ALT), une atrophie du thymus et une hypertrophie des cellules corticales des glandes surrénales chez les femelles non gestantes et gestantes, ainsi que d’autres signes de toxicité (infiltration de cellules inflammatoires dans la prostate et diminution des éosinophiles chez les mâles; hypertrophie du foie, augmentation du poids des glandes surrénales chez les femelles non gestantes; diminution de l’hématocrite et des concentrations d’azote uréique sérique, régénération tubulaire dans les reins, présence de microgranulomes dans le foie, hématopoïèse extramédullaire dans la rate chez les mères au cinquième jour de lactation). Puisque la diminution de la consommation d’aliments et la diminution de la prise de poids corporel à 12 mg/kg p.c./j n’ont correspondu à aucun changement dans le poids corporel chez les mères et qu’elles pouvaient être réversibles, ces diminutions n’ont pas été choisies comme DMENO parentale. La DSENO parentale était de 12 mg/kg p.c./j, déterminée d’après la DMENO de 60 mg/kg p.c./j à laquelle une augmentation du poids du foie et une hypertrophie du foie chez les mâles exposés pendant six semaines, ainsi qu’une diminution du poids corporel, de la prise de poids corporel et de la consommation de nourriture chez les mères.
À partir de 12 mg/kg p.c./j, on a noté une diminution du poids corporel (de 12 % à la dose de 12 mg/kg p.c./j, de 35 % à 36 % à celle de 60 mg/kg p.c./j) des petits des deux sexes par rapport aux sujets témoins, au quatrième jour postnatal. Bien que ces effets puissent avoir été secondaires aux effets sur les mères, nous avons retenu la concentration de 12 mg/kg p.c./j comme DMENO pour le développement pour le Solvent Blue 36 eu égard à la gravité accrue des effets à la dose de 60 mg/kg p.c./j, dose à laquelle une diminution du poids à la naissance des petits (diminution de 5 %, de 8 % [statistiquement significative] et de 13 % [statistiquement significative] aux doses faibles, intermédiaires et élevées, respectivement, chez les deux sexes), une diminution de la prise de poids corporel (diminution statistiquement significative de 90 % à 93 % par rapport aux sujets témoins chez les petits des deux sexes, du jour de la naissance au quatrième jour postnatal) et une diminution de la viabilité (moyenne), chez les petits au quatrième jour postnatal, de 86 %, 87 %, 30 % (statistiquement significative) et 0,6 % (statistiquement significative) chez les sujets témoins (dose nulle), à la dose faible, à la dose intermédiaire et à la dose élevée, respectivement. À 300 mg/kg p.c./j, des portées entières ont été perdues, à l’exception d’un petit mâle. L’altération de la couleur chez les petits au quatrième jour postnatal à toutes les doses (graisse bleue chez tous les petits, certains ayant la peau et le contenu gastro-intestinal bleus) n’a pas été jugée nocive, mais elle semble indiquer un transfert par le lait. Comme la dose la plus faible était de 12 mg/kg p.c./j, la DSENO pour le développement n’a pas été déterminée.
Le Solvent Blue 36 s’est révélé positif dans un test d’Ames (avec activation) in vitro et dans un test d’aberration chromosomique effectué sur des cellules pulmonaires V79 de hamsters chinois (MHLWJ, 2012).
Disperse Red 60
Des rats (20/sexe/dose) ayant reçu 0 ou 1000 mg/kg pc/jour de Disperse Red 60 par gavage pendant quatre semaines (une fois par jour, cinq jours par semaine) n’ont pas été affectés autrement que par une altération de la couleur de l’urine et des tissus (Leist, 1982). L’altération de la couleur des tissus est considérée comme une conséquence de l’absorption et non comme un effet nocif, et une DSENO à 1 000 mg/kg p.c./j a donc été déterminée.
Le profil de génotoxicité du Disperse Red 60 in vitro était mixte (test d’Ames négatif avec ou sans activation, test d’Ames positif avec ou sans activation, positif et négatif dans un essai sur cellules de lymphome murin à gène tk), mais le colorant n’était pas clastogène dans les tests d’aberration chromosomique et d’échange de chromatides sœurs (ECHA c2007-2019b; ETAD, 1988; Seifried et al., 2006; Crompton et Knowles, 1988; NTP [modifié en 2017]).
Solvent Violet 59
Dans une étude sur la toxicité à court terme avec doses répétées (ligne directrice 407 de l’OCDE), des rats Wistar (5/sexe/dose) ont reçu 0, 100, 300 ou 1000 mg/kg pc/jour de Macrolex Rotviolett R (contenant de 94 % à 100 % de Solvent Violet 59) par gavage pendant 28 jours consécutifs. Aucun changement du poids corporel ni d’organes lié au traitement n’a été observé, ni aucun changement hématologique lié au traitement. L’examen histopathologique des tissus n’a révélé aucun changement lié à l’administration de la substance. Une DSENO de 1000 mg/kg pc/jour, la plus forte dose testée, a été établie par les auteurs de l’étude (ECHA c2007-2019c).
Dans un essai de dépistage de la toxicité pour la reproduction et le développement (ligne directrice 421 de l’OCDE), des rats Wistar (12/sexe/dose) ont reçu 0, 100, 300 ou 1000 mg/kg p.c./jour de Macrolex Rotviolett R (contenant une concentration nominale de 91 % à 103 % de Solvent Violet 59) par gavage pendant environ 6 semaines pour les mâles et jusqu’à 8 semaines pour les femelles (notamment une phase de 2 semaines avant l’accouplement, la gestation et la lactation jusqu’au 13e jour). Aucun effet lié au traitement sur le poids corporel ni le poids de la thyroïde n’a été observé, quel que soit le sexe. Aucun effet sur le poids des organes reproducteurs mâles n’a été observé, quelle que soit la dose. À 300 mg/kg p.c./jour, deux mâles ont présenté des testicules flasques et de petite taille et des épididymes de petite taille, et ces deux mâles n’ont pas réussi à s’accoupler avec leurs partenaires femelles. En l’absence de résultats similaires à la dose élevée de 1000 mg/kg p.c./jour, l’auteur de l’étude a jugé ces résultats comme fortuits et sans rapport avec le traitement. L’analyse de la thyroxine (T4) chez les mâles adultes et la progéniture au jour 13 de l’âge n’a pas indiqué d’effets liés au traitement, quelle que soit la dose. Il n’y a pas eu d’effet lié au traitement sur les cycles œstraux, les performances d’accouplement, la fertilité ou la durée de la gestation à des doses allant jusqu’à 1000 mg/kg pc/jour. Il n’y a pas eu d’effet sur le nombre d’implantations, la perte post-implantation, la taille de la portée, le rapport des sexes à la naissance ou la survie ultérieure de la progéniture jusqu’au 13e jour de vie à des doses allant jusqu’à 1000 mg/kg pc/jour. Aucun effet lié au traitement n’a été observé chez la progéniture de la naissance jusqu’au jour 13, quelle que soit la dose. Une DSENO de 1000 mg/kg pc/jour, la plus forte dose testée, a été établie par les auteurs de l’étude pour les effets sur la reproduction et le développement (ECHA c2007-2019c).
Le Solvent Violet 59 a été mutagène in vitro, dans un test d’Ames modifié faisant appel aux souches YG1041 et YG1042 de Salmonella typhimurium (dérivées de TA 98 et 100, respectivement), avec et sans activation métabolique (Santé Canada, 2017).
Acid Blue 239 et substance au NE CAS 74499-36-8
Les renseignements sur les effets sur la santé étaient minimes pour les deux autres substances du groupe des anthraquinones. Le dossier d’inscription de l’Acid Blue par l’ECHA contient un test d’Ames qui ne révèle aucune preuve de mutagénicité avec et sans activation métabolique, bien que la pureté du matériau d’essai ne soit que de 65,6 % (ECHA c2007-2019d). Le NE CAS 74499-36-8 s’est révélé mutagène dans un test d’Ames modifié utilisant les souches YG 1040 et YG 1042 de Salmonella typhimurium (dérivées des TA 98 et 100, respectivement), avec et sans activation métabolique (Santé Canada 2017).
Sélection d’analogues et renseignements sur les effets sur la santé correspondants pour l’extrapolation aux substances du groupe des anthraquinones
Les points de référence d’expositions par utilisation de Solvent Violet 13, au Pigment Blue 60, au Solvent Violet 59 et au Solvent Blue 36 présentés dans le tableau 7-4 ont été tirés d’études spécifiques à la substance décrites plus haut dans cette section; il n’a pas été nécessaire de faire une extrapolation. Pour le Solvent Violet 13 et le Solvent Violet 59, les points de départ étaient basés sur les essais réalisés conformément à la ligne directrice 421 de l’OCDE, établissant des DSENOs de 1000 mg/kg pc/jour pour la reproduction et le développement (ECHA c2007-2019a, ECHA c2007-2019c). Les points de départ pour le Pigment Blue 60 et le Solvent Blue 36 étaient basés sur les études réalisées conformément à la ligne directrice 422 de l’OCDE avec une DSENO de toxicité reproductive/parentale de 300 mg/kg pc/jour (Heucotech Ltd 2013) et une DMENO de toxicité pour le développement de 12 mg/kg pc/jour (MHLWJ 2012), respectivement.
La toxicité systémique du Disperse Red 60 a été déterminée dans une étude de 4 semaines spécifique à la substance, et la DSENO de 1000 mg/kg pc/jour (Leist 1982) est identifiée dans le tableau 7-4 comme point de référence pour les expositions par utilisation. En ce qui concerne les effets sur la reproduction et le développement, une étude réalisée conformément à la ligne directrice 422 de l’OCDE a été identifiée dans le dossier d’inscription de cette substance par l’ECHA; elle était basée sur une comparaison avec un analogue (ECHA c2007-2019b), pour lequel aucun effet sur la reproduction ou le développement n’a été observé jusqu’à la plus forte dose testée de 1000 mg/kg pc/jour.
Les effets systémiques et les effets sur la reproduction et le développement de l’Acide Blue 239 et de la substance au numéro de CAS 74499-36-8 ont été déterminés par extrapolation d’une étude réalisée conformément à la ligne directrice 422 de l’OCDE décrite précédemment sur des rats ayant reçu du Solvant Blue 36 par gavage (MHLWJ 2012). Le point de référence pour les effets systémiques consistait en une DSENO parentale de 12 mg/kg pc/jour basée sur les effets indésirables identifiés avec 60 et 300 mg/kg pc/jour de Solvent Blue 36 (y compris une toxicité accrue du foie chez les deux sexes, une augmentation du poids et une hypertrophie des glandes surrénales, une atrophie du thymus et une diminution du poids de la rate et des ovaires chez les femelles). Concernant la toxicité du Solvent Blue 36 pour la reproduction et le développement, aucun effet sur la reproduction n’a été observé jusqu’à la plus forte dose testée de 300 mg/kg pc/jour, mais des effets sur le développement auraient survenus à la plus faible dose testée de 12 mg/kg pc/jour. Les points de départ tirés de cette étude consistaient en une DSENO parentale et une DMENO développementale de 12 mg/kg pc/jour. Ces valeurs ont été déterminées comme étant les paramètres les plus sensibles parmi les analogues potentiels considérés concernant les effets systémiques et le développement, la DMENO de 12 mg/kg pc/jour pour le développement étant la plus sensible.
Concernant les expositions quotidiennes (systémiques) aux autres substances du groupe des anthraquinones, les effets systémiques chroniques ont été déterminés par l’étude de cancérogénicité chronique de deux ans menée sur l’anthraquinone (NTP 2005), dans laquelle les effets observés comprennent une diminution du poids corporel et des effets sur les reins, le foie, la rate et la moelle osseuse chez les rats, ce qui a amené à une DSENO de 20 mg/kg pc/jour. Des détails supplémentaires sur cette étude sont fournis ci-dessous. Cette DMENO de 20 mg/kg pc/jour est présentée dans le tableau 7-4 comme le point de référence des expositions quotidiennes (systémiques) au Solvent Violet 13, au Solvent Violet 59 et au Disperse Red 60. Cependant, pour le Solvent Blue 36, l’Acid Blue 239 et la substance au NE CAS 74499-36-8, l’étude sur le Solvent Blue 36 réalisée conformément à la ligne directrice 422 de l’OCDE (MHLWJ 2012) a été utilisée pour établir le point de référence des expositions quotidiennes (systémiques) présentées dans le tableau 7-4. Les effets de toxicité pour le développement auraient été survenus à la plus faible dose testée de 12 mg/kg pc/jour, comme décrit précédemment, et la DMENO de 20 mg/kg pc/jour avec l’anthraquinone ne peut être atteinte sans dépasser la DMENO par utilisation de 12 mg/kg pc/jour.
Les prédictions de la génotoxicité in vitro de l’Acid Blue 239, obtenues à l’aide des modèles QSAR, ont donné des résultats mixtes : dans le modèle statistique Leadscope, la prédiction de génotoxicité de la substance s’est révélée positive (Leadscope Model Applier, 2016). Dans le modèle d’alertes structurales TIMES, la prédiction de génotoxicité était positive (TIMES, 2016); dans le modèle Derek Nexus expert fondé sur les connaissances, aucune alerte structurale n’a été trouvée (Derek Nexus, 2016). Les données de génotoxicité in vitro d’autres substances du groupe des anthraquinones étaient mixtes (RSI, 2017). Le Solvent Violet 13 n’était pas génotoxique in vitro (test d’Ames négatif) (Muzzal et Cook, 1979), le Pigment Blue 60 n’était pas génotoxique, en général (test d’Ames, essai sur cellules de lymphomes de souris, essais d’aberration chromosomique négatifs; test d’échange de chromatides sœurs positif) (ECHA c2007-2019b; ETAD 1988, NTP 2005), le Solvent Blue 36 n’était pas génotoxique (test d’Ames et essai d’aberration chromosomique positifs) (MHLWJ, 2012), et les résultats étaient équivoques pour la génotoxicité de Disperse Red 60 (résultats mixtes au test d’Ames et à l’essai sur cellules de lymphome de souris et résultats négatifs à l’essai d’aberration chromosomique et au test d’échange de chromatides sœurs) (ETAD, 1988; Seifried et al., 2006; Crompton et Knowles, 1988; NTP [modifié en 2017]) et le Solvent Violet 59 et la substance de NE CAS 74499-36-8 étaient génotoxiques (test d’Ames modifié positif) (Santé Canada, 2017). Les données disponibles semblent indiquer que l’Acid Blue 239 peut être génotoxique in vitro.
Bien qu’il y ait des résultats mixtes pour la génotoxicité in vitro et in vivo de l’anthraquinone (NE CAS 84-65-1), qui constitue le squelette structurel commun des substances du groupe des anthraquinones, les résultats positifs ont été attribués aux impuretés potentielles qui étaient mutagènes (p. ex. 9‑nitroanthracène) et qui ont été introduites lorsque l’anthraquinone était produite par oxydation de l’anthracène distillée provenant du goudron de houille (ECHA, 2015a; Alay, 2012). Il a également été noté que la mutagénicité potentielle due aux métabolites mutagènes ne peut être exclue (ECHA 2015b), mais sur la base d’une approche fondée sur le poids de la preuve, l’ECHA a déterminé que les tests in vitro et in vivo n’indiquent généralement aucun effet sur la fréquence des mutations (ECHA 2015a).
En ce qui concerne les analogues possibles, la cancérogénicité des substances du groupe des anthraquinones autres que le Pigment Blue 60 potentiellement cancérogènes (RSI, 2017). Le Pigment Blue 60 n’a pas été considéré comme un analogue potentiel pour ce paramètre par la boîte à outils QSAR de l’OCDE, en raison probablement de différences dans les alertes structurales entre le Pigment Blue 60 et les autres substances du groupe des anthraquinones. Six analogues potentiels, définis à l’aide de la boîte à outils de l’OCDE, ont augmenté les tumeurs dans le foie (NE CAS 82-28-0, 84-65-1, 117-10-2, 129-15-7 et 129-43-1) et dans la vessie (NE CAS 81-54-9) chez le rat et/ou la souris (NCI, 1978; NTP, 2005; Mori et al., 1985, 1986, 1990, 1991; Yoshimi et al., 1995; Tanaka et al., 1991; Bionetics Research Labs, 1968; Krishna Murthy et al., 1977; CPDB [modifié en 2007]). Les points de référence chroniques ont été assez variables, les DMENO variant de 20 mg/kg p.c./j (voir le Tableau 7-4) pour l’anthraquinone (NE CAS 84-65-1) à 500 mg/kg p.c./j (uniquement les doses testées de NE CAS 117-10-2, 81-54-9 et 129‑43‑1) chez le rat et de 39 mg/kg p.c./j (NE CAS 129-15-7) à 260 mg/kg p.c./j (NE CAS 117-10-2) chez la souris.
L’anthraquinone (NE CAS 84-65-1) était tumorigène chez le rat et la souris par la voie alimentaire et a été sélectionnée comme produit chimique source pour l’extrapolation du potentiel cancérogène et les effets généraux non cancérogènes de certaines substances du groupe des anthraquinones, puisqu’elle a la DMENO la plus faible à laquelle des tumeurs ou des effets généraux ont été observés et que la méthodologie de certaines études présentait des limites (p. ex., dose unique, posologie irrégulière, durée courte, pureté faible). Puisque l’anthraquinone augmente l’incidence des tumeurs aux reins chez le rat à la dose d’essai la plus faible de 20 mg/kg p.c./j, aucune DSENO n’a été déterminée pour cette substance. Cette DMENO a été considérée comme protectrice contre les tumeurs observées dans d’autres études de cancérogénicité par voie alimentaire réalisées avec des analogues, dont le 2-méthyl-1-nitroanthracène-9,10-dione (NE CAS 129-15-7) qui a induit la formation de fibromes sous‑cutanés chez des rats mâles à une DMENO (concentration minimale à l’essai) légèrement plus élevée de 30 mg/kg p.c./j lors d’une étude de toxicité par voie alimentaire de 78 semaines (NCI, 1978).
Le Centre international de recherche sur le cancer (CIRC, 2013) a classé l’anthraquinone dans le groupe 2B (données suffisantes chez l’animal, insuffisantes chez l’humain). Cette substance n’est pas considérée être un mutagène in vitro et in vivo, et classée comme cancérogène de la catégorie 1B du Système général harmonisé (SGH) par l’ECHA (UE, 2017; ECHA, 2015a). Dans une étude de cancérogénicité de deux ans menée par le National Toxicology Program (NTP) chez le rat et la souris avec de l’anthraquinone administrée par voie alimentaire, des rats F344/N (50/sexe/dose) ont reçu dans leur alimentation des doses de 0, 469, 938, 1 875 ou 3 750 ppm d’anthraquinone (équivalant à 0, 20/25, 45/50, 90/100, 180/200 mg/kg p.c./j, pour les mâles et les femelles, respectivement) (NTP, 2005). À une dose de 20/25 mg/kg p.c./j (mâles/femelles) et plus, les observations comprenaient une diminution du poids corporel (de 6 % chez les mâles, de 11 % chez les femelles), et des effets sur les reins (augmentation du poids absolu et du poids relatif, néphropathie, accumulation de gouttelettes hyalines, pigmentation, minéralisation dans la médulla rénale, hyperplasie épithéliale transitoire chez les deux sexes), le foie (augmentation du poids absolu et relatif chez les deux sexes), la rate (incidence de congestion, pigmentation, prolifération des cellules hématopoïétiques chez les deux sexes), la moelle osseuse (augmentation de l’hyperplasie, augmentation de l’atrophie chez les femelles) et augmentation des adénomes dans les tubules rénaux chez les deux sexes ainsi que des adénomes et des carcinomes combinés chez les femelles. Les incidences des adénomes dans les tubules rénaux étaient de 1/0, 3/4, 9/9, 5/7, 3/12 chez les mâles et les femelles sur l’ensemble de 50/sexe/dose (mais 49 femelles ont reçu la dose élevée), incidences toutes supérieures aux fourchettes de valeurs témoin historiques pour les deux sexes (de 0 % à 4 % chez les mâles, de 0 % à 2 % chez les femelles). Par comparaison avec les témoins, ces augmentations étaient statistiquement significatives chez les mâles ayant reçu 45 et 180 mg/kg p.c./j et chez les femelles ayant reçu 50 mg/kg p.c./j et plus. À 45/50 mg/kg p.c./j ou plus, une augmentation des effets sur la vessie (hyperplasie épithéliale transitoire, papillomes et/ou carcinomes) et sur le foie (adénomes hépatocellulaires chez les femelles, augmentation suspectée d’adénomes et de carcinomes combinés chez les mâles) a été constatée. Le NTP a conclu qu’il y avait des preuves de cancérogénicité chez le rat F344/N mâle par l’augmentation des incidences d’adénomes dans les tubules rénaux et de papillomes épithéliaux transitoires dans les reins et la vessie et que les néoplasmes hépatocellulaires peuvent être liés. Il existe une preuve nette de cancérogénicité chez le rat F344/N femelle en raison de l’augmentation des incidences des néoplasmes dans les tubules rénaux, des papillomes/carcinomes épithéliaux transitoires (combinés) de la vessie et des adénomes hépatocellulaires (NTP, 2005).
Les incidences respectives des adénomes et des carcinomes rénaux combinés chez le rat femelle aux doses de 0, 25, 50, 100 ou 200 mg/kg p.c./j ont été de 0, 6, 9, 8 et 14 sur 50 rats femelles, mais sur 49 rats femelles dans le groupe ayant reçu la dose la plus élevée (NTP, 2005). À l’aide de la version 2.6.0 du logiciel Benchmark Dose Software (BMDS) de l’EPA des États‑Unis et du modèle LogLogistic qui a la valeur du critère d’information d’Akaike la plus faible et qui manque d’avertissements dans le calcul de la dose seuil de référence (DSR), la dose de référence pour un risque supplémentaire de 10 % a été établie à 41 mg/kg p.c./j et la limite inférieure pour un risque supplémentaire de 10 % (DSR10), à 30,3 mg/kg p.c./j (communication personnelle, courriel de l’Unité de biostatistique de Santé Canada adressé au Bureau d’évaluation du risque des substances existantes de Santé Canada, daté du 12 avril 2017; sans référence).
Dans l’étude du NTP de deux ans (2005) réalisée avec l’administration de 0, 833, 2500 ou 7500 ppm (équivalant à 0, 90/80, 265/235, 825/745 mg/kg p.c./j chez les mâles et les femelles, respectivement) d’anthraquinone par voie alimentaire à des souris B6C3F1 (50/sexe/groupe de traitement, 60/sexe/groupe témoin), des effets ont été relevés à la dose d’essai la plus faible de 90/80 mg/kg p.c./j (mâle/femelle) et plus dans le foie (notamment une hypertrophie, des hépatoblastomes, des adénomes et des carcinomes) et à la glande thyroïde (hyperplasie des cellules folliculaires et augmentations suspectées des néoplasmes). Le NTP (2005) a déterminé qu’il s’agissait là d’une preuve sans équivoque de cancérogénicité chez les souris B6C3F1 mâles et femelles, en raison de l’augmentation de l’incidence des néoplasmes dans le foie, et a considéré que les néoplasmes de cellules folliculaires de la glande thyroïde pourraient être liés. Ce résultat diffère de celui d’une étude de cancérogénicité plus ancienne où aucune augmentation claire de l’incidence des tumeurs n’a été établie chez les souris B6C3F1 ou B6AKF1 ayant reçu 464 mg/kg p.c./j par gavage pendant quatre semaines, puis 157 mg/kg p.c./j par voie alimentaire pour une durée allant jusqu’à 18 mois (Bionetics Research Labs, 1968). L’écart ne peut être expliqué clairement, mais il pourrait être lié à la méthode puisque la pureté ou la stabilité de l’article à l’essai n’était pas claire, qu’il y avait moins d’animaux (18/sexe/lignée, dont 4/sexe/BC3F1 et 3 souris B6AKF1 femelles atteintes mortellement de pneumonie) et que l’étude était plus courte. Les tumeurs observées dans les études du NTP ne pouvaient être attribuées entièrement aux impuretés mutagènes de l’anthraquinone utilisée, qui renfermait 0,1 % de 9‑nitroanthracène (NTP, 2005; ECHA, 2015a).
Les points de référence de ces études de toxicité par voie orale ont été jugés applicables aux voies d’exposition cutanée et par inhalation, en l’absence de données appropriées sur le danger propres à l’exposition, quelle que soit la voie. Une étude d’exposition par inhalation, de l’organisme entier, d’une durée de quatre mois dans le cadre de laquelle un total de 96 rats ont été exposés à une dose de 0, 5,5 ou 12,2 mg/m3 d’anthraquinone pendant cinq ou six heures par jour, a été considérée comme une étude de référence, parce que les précisions étaient limitées. À 12 mg/m3, les rats ont connu une diminution de leur poids corporel, de leur hémoglobine, de leurs érythrocytes et une augmentation de la réticulocytopénie (Volodchenko et al., 1970).
Résumé des points de référence sélectionnés pour la caractérisation des risques pour la santé humaine
Les points de référence sélectionnés pour la caractérisation des risques pour la santé humaine pour chaque substance (voir la section 7.3, Caractérisation des risques pour la santé humaine) sont présentés dans le tableau 7-4. À moins qu’il existe des données empiriques sur les effets sur la santé propres à la substance chimique, les données sur les effets sur la santé utilisés provenaient d’une substance analogue.
| Substance | Exposition par utilisation | Exposition quotidienne (générale) |
|---|---|---|
| Solvent Violet 13 | Essai no 421 des lignes directrices de l’OCDE (rats, gavage); toxicité pour la reproduction et le développement DSENO de 1000 mg/kg p.c./j Sans effet à la plus haute dose d’essai | Tirée d’une étude de 2 ans sur la cancérogénicité chronique de l’anthraquinone (rats, alimentation) DSENO de 20 mg/kg pc/jour (diminution de la masse corporelle et effets sur les reins, le foie, la rate, la moelle osseuse) |
| Pigment Blue 60 | Essai no 422 des lignes directrices de l’OCDE (rats, gavage); DSENO de 300 mg/kg p.c./j et DMENO de 1000 mg/kg p.c./j pour la toxicité pour la reproduction et la toxicité parentale (pertes de portées, augmentation des pertes post‑implantatoires, diminution de consommation de nourriture et de gain de poids chez les mères) | Basé sur le point de référence par utilisation de la DSENO reproductive/parentale de 300 mg/kg p.c./jour |
| Solvent Violet 59 | Essai no 421 des lignes directrices de l’OCDE (rats, gavage); toxicité pour la reproduction et le développement DSENO de 1000 mg/kg p.c./j Sans effet à la plus haute dose d’essai | Tirée d’une étude de 2 ans sur la cancérogénicité chronique de l’anthraquinone (rats, alimentation) DSENO de 20 mg/kg pc/jour (diminution de la masse corporelle et effets sur les reins, le foie, la rate, la moelle osseuse) |
| Solvent Blue 36 | Essai no 422 des lignes directrices de l’OCDE (rats, gavage) DSENO toxicité parentale/pour la reproduction de 12 mg/kg p.c./j, DMENO de 60 mg/kg p.c./j (↑ poids du foie, hypertrophie du foie au 42e jour chez les mâles; ↓ p.c., prise de p.c., CA chez les mères au 4e JL)DMENO toxicité pour le développement de 12 mg/kg p.c./j (DEF) : ↓ p.c. chez les petits au 4e JPN | Basé sur le point de référence par utilisation de DMENO pour toxicité pour le développement de 12 mg/kg p.c./j. (DEF) |
| Disperse Red 60 | Étude de quatre semaines (rats, gavage) DSENO de 1 000 mg/kg p.c./j (DEE) | Basé sur une étude de cancérogénicité de deux ans sur l’anthraquinone (rats, voie alimentaire); DMENO de 20 mg/kg p.c./j (diminution de p.c. et effets sur reins, foie, rate, moelle osseuse) |
| Acid Blue 239 | Voir Solvent Blue 36 | Voir Solvent Blue 36 |
| NE CAS 74499-36-8 | Voir Solvent Blue 36 | Voir Solvent Blue 36 |
Abréviations : p.c. = poids corporel; CA = consommation alimentaire, DEE = dose d’essai la plus élevée; JPN = jour postnatal; DMENO = concentration minimale avec effet nocif observé; DEF = dose d’essai la plus faible; DSENO = concentration sans effet nocif observé; Essai no 422 des lignes directrices de l’OCDE : étude de toxicité à doses répétées combinée à l’essai de dépistage de la toxicité pour la reproduction et le développement.
Comme mentionné antérieurement, la DSR10 de 30,3 mg/kg p.c./j, fondée sur une augmentation des adénomes et des carcinomes rénaux chez les rats femelles auxquels de l’anthraquinone a été administrée, a été utilisée pour estimer le risque de cancer pour tous les scénarios d’exposition quotidienne par voie cutanée et par voie orale aux substances du groupe des anthraquinones, sauf le Pigment Blue 60. L’estimation du risque de cancer pour le Pigment Blue 60 a été jugée non requise, étant donné son profil de toxicité (p. ex., cancérogénicité négative jusqu’à 500 mg/kg p.c./j et génotoxicité négative).
7.3 Caractérisation des risques pour la santé humaine
Les tableaux 7-5 et 7-6 fournissent des estimations utiles de l’exposition par voie orale et par voie cutanée et des points de référence (PR) de danger pour les substances du groupe des anthraquinones, ainsi que les marges d’exposition (ME) résultantes, pour la détermination des risques.
| Scénario d’exposition | Exposition générale (mg/kg p.c. [/j]) | Concentration d’effet critique (mg/kg p.c [/j]) | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Baume pour les lèvres, tout-petits,par utilisation, Solvent Violet 13 | 0,0065 | DSENO, 1000 | Évaluation préliminaire de la toxicité pour la reproduction et le développement; aucun effet nocif à la plus forte dose testée | 150 000 |
| Baume pour les lèvres, tout-petits,quotidien, Solvent Violet 13 | 0,0038 | DMENO, 20 | Étude de 2 ans sur la cancérogénicité chronique, diminution du poids corporel et effets sur les reins, le foie, la rate et la moelle osseuse | 5263 |
| Peinture faciale, tout-petits, par utilisation, Solvent Violet 13 | 0,53 | DSENO, 1000 | Évaluation préliminaire de la toxicité pour la reproduction et le développement; aucun effet nocif à la plus forte dose testée | 1887 |
| Rouge à lèvres, adultes, par jour, Solvent Violet 13 | 0,0034 | DMENO, 20 | Étude de 2 ans sur la cancérogénicité chronique, diminution du poids corporel et effets sur les reins, le foie, la rate et la moelle osseuse | 5882 |
| Matériel de bricolage et d’artisanat (p. ex. tampons), tout-petits,par utilisation, Pigment Blue 60 | 1,29 | DSENO, 300 | Étude combinée à doses répétées et évaluation préliminaire de la toxicité pour la reproduction et le développement, diminution de la consommation de nourriture chez les mères et diminution du gain de poids corporel | 233 |
| Matériel de bricolage et d’artisanat (p. ex. tampons), tout‑petits, par jour, Pigment Blue 60 | 0,0645 | DSENO, 500 | Étude combinée à doses répétées et évaluation préliminaire de la toxicité pour la reproduction et le développement, diminution de la consommation de nourriture chez les mères et diminution du gain de poids corporel | 4651 |
| Jouets en plastique, portés à la bouche, tout-petitspar utilisation, Solvent Violet 59 | 3,4E-06 | DMENO, 12 | Étude de 2 ans sur la cancérogénicité chronique, diminution du poids corporel et effets sur les reins, le foie, la rate et la moelle osseuse | 5 900 000 |
| Textiles, portés à la bouche, nourrissons,par jour, Disperse Red 60 | 0,00027 | DMENO, 20 | Étude de 2 ans sur la cancérogénicité chronique, diminution du poids corporel et effets sur les reins, le foie, la rate et la moelle osseuse | 74 000 |
| Textiles, portés à la bouche, nourrissons,par utilisation, Acid Blue 239 | 0,0027 a | DMENO, 12 | Étude combinée à doses répétées et évaluation préliminaire de la toxicité pour la reproduction et le développement, diminution de la consommation de nourriture chez les mères et diminution du gain de poids corporel | 4444 |
Abréviations : DMENO = dose minimale avec effet nocif observé; CSENO = concentration sans effet nocif observe; DSENO = dose sans effet nocif observé.
a Bien que l’action de porter des textiles à la bouche survienne tous les jours, l’exposition générale par voie orale « par utilisation », estimée à partir de la fraction de migration « aiguë » initiale, a été utilisée pour protéger le paramètre du développement.
Compte tenu des paramètres prudents utilisés dans la modélisation des expositions aux produits, les ME obtenues pour les effets généraux non cancérogènes sont considérées comme appropriées pour réduire les incertitudes des bases de données sur les effets sur la santé et l’exposition pour les scénarios d’exposition par voie orale au Solvent Violet 13, au Pigment Blue 60, au Solvent Violet 59, au Disperse Red 60 et à l’Acid Blue 239.
| Scénario d’exposition | Exposition générale (mg/kg p.c. [/j]) | ME (d’après la DSR10)a |
|---|---|---|
| Baume pour les lèvres ou rouge à lèvres, DQMV (tout-petits, enfants, adolescents, adultes), Solvent Violet 13 | 0,00342 b | 8860 |
| Peinture faciale, DQMV (tout‑petits), Solvent Violet 13 | 0,00102 | 30 000 |
| Jouets en plastique, portés à la bouche, tout-petits, par jour, Solvent Violet 59 | 3,4E-06 | 9 000 000 |
| Textiles, portés à la bouche, nourrissons, par jour, Disperse Red 60 | 0,00027 | 100 000 |
| Textiles, portés à la bouche, nourrissons, par jour, Acid Blue 239 | 0,00027 | 100 000 |
Abréviation : DQMV, dose quotidienne moyenne à vie; ME = marge d’exposition.
a DSR10 de 30,3 mg/kg p.c./j déterminée à partir de l’augmentation de l’incidence des adénomes et des carcinomes rénaux chez les rats femelles (NTP, 2005).
b La DQMV représente l’utilisation du baume à lèvres par les tout-petits, les enfants, les adolescents et les adultes et protège contre l’utilisation d’un rouge à lèvres.
Le point de référence pour les risques de cancer liés à l’exposition quotidienne à des substances du groupe des anthraquinones ait été déterminé d’après un agent cancérogène non génotoxique, les ME pour les risques de cancer ont été jugées appropriées parce que le point de référence a été établi d’après une augmentation de 10 % des risques de formation de tumeurs rénales et non d’après un incident précurseur déclencheur d’un mode d’action seuil bien défini. Par conséquent, les ME des scénarios d’exposition par voie orale pour les effets cancérogènes ont été jugées appropriées pour réduire les incertitudes dans les bases de données sur les effets sur la santé et l’exposition pour le Solvent Violet 59, le Disperse Red 60 et l’Acid Blue 239, mais elles sont peut-être inappropriées pour le Solvent Violet 13 associé à l’utilisation de baume pour les lèvres ou de rouge à lèvres lorsqu’elles sont ajustées à une exposition à vie.
| Scénario d’exposition | Exposition générale (mg/kg p.c. [/j]) | Concentration d’effet critique (mg/kg p.c [/j]) | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Crème pour le corps, adultes, par jour, Solvent Violet 13 | 0,389 | DMENO, 20 | Étude de 2 ans sur la cancérogénicité chronique, diminution du poids corporel et effets sur les reins, le foie, la rate et la moelle osseuse | 51 |
| Colorant capillaire permanent, adolescents, par utilisation, Solvent Violet 13 | 0,0175 –0,444 | DSENO, 1000 | Évaluation préliminaire de la toxicité pour la reproduction et le développement, aucun effet nocif à la plus forte dose testée | 2252 – 57 143 |
| Parfum en aérosol, adultes,par jour, Solvent Violet 13 | 0,00230 –0,0583 | DMENO, 20 | Étude de 2 ans sur la cancérogénicité chronique, diminution du poids corporel et effets sur les reins, le foie, la rate et la moelle osseuse | 343 – 8696 |
| Peinture faciale, tout-petits, par utilisation, Solvent Violet 13 | 0,0457 –1,16 | DMENO, 1000 | Une évaluation préliminaire de la toxicité pour la reproduction et le développement, aucun effet nocif à la plus forte dose testée | 862 – 21 882 |
| Matériaux de bricolage et d’artisanat (p. ex., tampons) adolescents, par utilisation, Pigment Blue 60 | 1,29 | DSENO, 300 | Augmentation des pertes de portées entières, diminution de la consommation alimentaire chez les mères et diminution de la prise de poids corporel | 233 |
| Matériaux de bricolage et d’artisanat (p. ex. tampons), adolescents, par utilisation, Pigment Blue 60 | 0,337 | DSENO, 300 | Étude combinée à doses répétées et évaluation préliminaire de la toxicité pour la reproduction et le développement, perte accrue ou complète de la portée. | 890 |
| Matériaux de bricolage et d’artisanat (p. ex. tampons), tout-petits, par jour, Pigment Blue 60 | 0,0645 | DSENO, 300 | Étude combinée à doses répétées et évaluation préliminaire de la toxicité pour la reproduction et le développement, diminution de la consommation alimentaire chez les mères et diminution de la prise de poids corporel | 4651 |
| Matériaux de bricolage et d’artisanat (p. ex. tampons), adolescents, par utilisation, Pigment Blue 60 | 0,0168 | DSENO, 300 | Étude combinée à doses répétées et évaluation préliminaire de la toxicité pour la reproduction et le développement, perte accrue ou complète de la portée. | 18 000 |
| Lubrifiant pour usages spéciaux, adultes, par utilisation, Solvent Blue 36 | 3,82E-05 | DMENO, 12 | Étude combinée à doses répétées et évaluation préliminaire de la toxicité pour la reproduction et le développement, diminution du poids corporel chez les petits au 4e JPN | 310 000 |
| Après-shampoing, adulte, par jour, Solvent Blue 36 | 1,84E-04 | DMENO, 12 | Étude combinée à doses répétées et évaluation préliminaire de la toxicité pour la reproduction et le développement, diminution du poids corporel chez les petits au 4e JPN | 65 000 |
| Textiles, port de vêtements, nourrissons, par jour, Disperse Red 60 | 8,05E-04 | DMENO, 20 | Étude de 2 ans sur la cancérogénicité chronique, diminution du poids corporel et effets sur les reins, le foie, la rate et la moelle osseuse | 25 000 |
| Textiles, port de vêtements, adultes, par jour, Disperse Red 60 | 5,13E-04 | DMENO, 20 | Étude de 2 ans sur la cancérogénicité chronique, diminution du poids corporel et effets sur les reins, le foie, la rate et la moelle osseuse | 39 000 |
| Textiles, port de vêtements, nourrissons, par utilisation, Acid Blue 239 | 1,33E-05 | DMENO, 12 | Étude combinée à doses répétées et évaluation préliminaire de la toxicité pour la reproduction et le développement,diminution du poids corporel chez les petits au 4e JPN | 902 000 |
| Textiles, port de vêtements, adultes, par utilisation, Acid Blue 239 | 8,49E-06 | DMENO, 12 | Étude combinée à doses répétées et évaluation préliminaire de la toxicité pour la reproduction et le développement,diminution du poids corporel chez les petits au 4e JPN | 1 400 000 |
| Revêtement en époxy, application, adultes, par utilisation, NE CAS 74499‑36‑8 | 0,0035 | DMENO, 12 | Étude combinée à doses répétées et évaluation préliminaire de la toxicité pour la reproduction et le développement,diminution du poids corporel chez les petits au 4e JPN | 3429 |
Abréviations : DMENO = dose minimale avec effet nocif observé; CSENO = concentration sans effet nocif observe; DSENO = dose sans effet nocif observé
Compte tenu des paramètres prudents utilisés dans la modélisation de l’exposition aux produits, les ME résultantes pour les effets généraux autres que cancérogènes sont jugées appropriées pour tenir compte des incertitudes des bases de données sur les effets sur la santé et l’exposition au Solvent Violet 13 provenant de la teinture capillaire permanente et de la peinture pour le visage et pour les scénarios d’exposition par voie cutanée au Pigment Blue 60, au Solvent Violet 59, au Solvent Blue 36, au Disperse Red 60, à l’Acid Blue 239 et à la substance au NE CAS 74499-36-8. Cependant, les ME résultantes pour les effets systémiques autres que cancérogènes ne sont pas jugées appropriées pour tenir compte des incertitudes des scénarios d’exposition cutanée au Solvent Violet 13 provenant de la crème corporelle et du parfum en aérosol.
L’exposition quotidienne globale par voie orale et par voie cutanée de 0,00108 et 2,83E‑04 mg/kg p.c./j a été calculée pour le Disperse Red 60 et l’Acid Blue 239, respectivement, pour les nourrissons vêtus de leur pyjama et les nourrissons qui portent leur pyjama à la bouche. Ce calcul d’exposition a donné lieu à des ME de 18 000 et de 42 000, respectivement, pour les effets autres que cancérogènes, lorsque comparés avec les DMENO de 20 et de 12 mg/kg p.c./j, respectivement. Ces ME ont été jugées appropriées pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé.
| Scénario d’exposition | DQMV (mg/kg p.c [/j]) | ME (d’après la DSR10)a |
|---|---|---|
| Crème pour le corps (enfants, adolescents, adultes), Solvent Violet 13 | 0,368 | 82 |
| Colorant capillaire permanent (adolescents, adultes), Solvent Violet 13 | 2,4E-04 –0,00579 | 5 233 – 130 000 |
| Parfum en aérosol (enfants, adolescents, adultes), Solvent Violet 13 | 0,00226 –0,0558 | 543 – 13 000 |
| Peinture faciale (tout-petits, enfants, adolescents, adultes)b, Solvent Violet 13 | 4,53E-04 –0,0115 | 2 635 – 67 000 |
| Colorant capillaire permanent (adolescents, adultes), Solvent Violet 59 | 1,35E-04 | 220 000 |
| Après-shampoing (tout-petits, enfants, adolescents, adultes), Solvent Blue 36 | 1,83E-04 | 166 000 |
| Textiles, vêtements portés (nourrissons, tout-petits, enfants, adolescents, adultes), Disperse Red 60 | 5,45E-04 | 56 000 |
| Textiles, vêtements portés (nourrissons, tout-petits, enfants, adolescents, adultes), Acid Blue 239 | 9,01E-06 | 3 400 000 |
Abréviation : DQMV, dose quotidienne moyenne à vie; ME marge d’exposition
a DSR10 de 30,3 mg/kg p.c./j déterminée à partir de l’augmentation de l’incidence des adénomes et des carcinomes rénaux chez les rats femelles (NTP, 2005).
b Bien que seuls les tout-petits aient été pris en compte dans le calcul de la DQMV pour l’exposition par voie orale à la peinture faciale (en raison du potentiel de contact main-bouche), les enfants, les adolescents et les adultes ont également été pris en compte pour l’exposition par la voie cutanée lors du calcul de la DQMV (voir l’annexe A).
Bien que les risques associés au paramètre du cancer dans les scénarios d’exposition cutanée aient été jugés appropriés pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé concernant le Solvent Violet 59, le Solvent Blue 36, le Disperse Red 60 et l’Acid Blue 239, ils ont été inappropriés pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé concernant le Solvent Violet 13 dans des crèmes pour le corps, des colorants capillaires permanents, des parfums en aérosol et de la peinture faciale.
Les risques associés à l’inhalation pendant l’exposition quotidienne au Solvent Violet 13 présent dans du parfum en aérosol (1,72 E-05 mg/kg p.c./j) ont été jugés appropriés lorsque comparés à la DMENO de 20 mg/kg p.c./j, établie d’après une diminution du poids corporel et effets sur les reins, le foie, la rate et la moelle osseuse, et assortis à une ME de 1 200 000. La ME de 1 800 000 établie à l’aide d’une DSR10 de 30,3 mg/kg p.c./j pour les effets cancérogènes était également appropriée pour l’exposition quotidienne par inhalation au Solvent Violet 13 provenant de parfum en aérosol.
Étant donné les paramètres prudents utilisés dans la modélisation de l’exposition aux produits, les ME résultantes pour les effets généraux et les effets cancérogènes dans les scénarios d’exposition par inhalation sont jugées appropriées pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé relatives au Solvent Violet 13. Cependant, comme les ME associées aux effets cancérogènes et aux effets autres que cancérogènes, établies pour l’exposition générale par voie cutanée, ont été jugées potentiellement inappropriées pour le Solvent Violet 13 provenant de parfum en aérosol, les ME établies pour l’exposition globale par inhalation et par voie cutanée seraient aussi potentiellement inappropriées.
Même si l’exposition de la population générale au Solvent Violet 59, au Solvent Blue 36, au Disperse Red 60, à l’Acid Blue 239 et à la substance de NE CAS 74499-36-8 n’est pas préoccupante aux concentrations actuelles, ces substances sont considérées comme ayant des effets préoccupants sur la santé, en raison de la cancérogénicité potentielle de leur anthraquinone analogue. Par conséquent, il pourrait y avoir une préoccupation pour la santé humaine si l’exposition à ces substances venait à augmenter.
7.4 Incertitudes de l’évaluation des risques pour la santé humaine
Les principales sources d’incertitude sont présentées dans le tableau ci-dessous.
| Principales sources d’incertitude | Impact |
|---|---|
| L’exposition par voie orale au Pigment Blue 60 a été estimée à partir de l’ingestion fortuite de matériaux de bricolage (p. ex., tampons) par les tout-petits. La biodisponibilité de ce pigment par voie orale n’est pas connue. Pour assurer la protection de la santé humaine, l’hypothèse d’une absorption systémique après ingestion a été retenue. | + |
| Il a été supposé avec prudence que l’absorption cutanée est équivalente à l’absorption par le tube digestif en ce qui concerne le Pigment Blue 60 et le NE CAS 74499-36-8. | + |
| Il n’existe aucune étude de métabolisation pour les substances du groupe des anthraquinones, sauf par absorption cutanée, pour Disperse Red 60 et Solvent Violet 13. | +/- |
| Il n’existe aucune étude de génotoxicité in vivo pour les substances du groupe des anthraquinones. | +/- |
| Il n’existe aucune étude à doses répétées ou à exposition chronique menée sur des animaux exposés par voie orale, sauf pour le Pigment Blue 60 (à doses répétées, exposition chronique), le Solvent Blue 36 et le Disperse Red 60 (à doses répétées). | +/- |
| Il n’existe aucune étude animale à doses répétées ou à exposition chronique par inhalation pour le Solvent Violet 13. | +/- |
| Il n’existe aucune étude animale à doses répétées ou à exposition chronique par voie cutanée pour les substances du groupe des anthraquinones, mais il existe une étude limitée de peinture corporelle pour le Solvent Violet 13. | +/- |
+ = incertitude présentant un potentiel de causer une surestimation de l’exposition/des risques; - = incertitude présentant un potentiel de causer une sous-estimation de l’exposition/des risques; +/- = potentiel inconnu de causer une surestimation ou une sous-estimation des risques.
8. Conclusion
Compte tenu de tous les éléments de preuve contenus dans la présente évaluation préalable, le Solvent Violet 13, le Pigment Blue 60, le Solvent Violet 59, le Solvent Blue 36, le Disperse Red 60, l’Acid Blue 239 et la substance de NE CAS 74499‑36‑8 présentent un faible risque d’effets nocifs sur l’environnement. Il a été conclu que le Solvent Violet 13, le Pigment Blue 60, le Solvent Violet 59, le Solvent Blue 36, le Disperse Red 60, l’Acid Blue 239 et la substance de NE CAS 74499-36-8 ne satisfont pas aux critères énoncés aux alinéas 64a) et b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
À la lumière des renseignements présentés dans la présente évaluation préalable, il a été conclu que le Solvent Violet 13 satisfait aux critères du paragraphe 64c) de la LCPE, car il pénètre ou peut pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaines.
À la lumière des renseignements contenus dans la présente évaluation préalable, il a été conclu que le Pigment Blue 60, le Solvent Violet 59, le Solvent Blue 36, le Disperse Red 60, l’Acid Blue 239 et la substance de n° CAS 74499‑36‑8 ne satisfont pas au critère énoncé au paragraphe 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Par conséquent, il a été conclu que le Solvent Violet 13 satisfait à au moins un des critères énoncés à l’article 64 de la LCPE. Il a également été conclu que le Pigment Blue 60, le Solvent Violet 59, le Solvent Blue 36, le Disperse Red 60, l’Acid Blue 239 et la substance de NE CAS 74499-36-8 ne satisfont à aucun des critères énoncés à l’article 64 de la LCPE.
Il a été conclu que le Solvent Violet 13 satisfait au critère de la persistance, mais non à celui de la bioaccumulation, critères énoncés dans le Règlement sur la persistance et la bioaccumulation pris en application de la LCPE.
Références
Alay GM. 2012. Anthraquinone, genotoxicity and carcinogenicity potential of different manufacturing origins. Barcelona (ES): REACH Monitor SLNE. (disponible en anglais seulement)
Bär F, et F. Griepentrog. 1960. Die allergenwirkung von fremden stiffen in den lebensmitteln. Med U Ernähr. 1:9. [mentionné dans JECFA, 1974].
BASF Corporation. 2015. Notice in accordance with TSCA Section 8(e): Results of a log Pow measurement of 1-Hydroxy-4-(p-toluidino)anthraquinone (CAS No. 81-48-1). Lettre de A. Boucher, BASF Corp., adressée à TSCA, US EPA. (disponible en anglais seulement)
[BDIPSN] Base de données d’ingrédients de produits de santé naturels [base de données]. [modifiée le 10 janvier 2017]. Ottawa (Ont.) : Santé Canada. [consultée le 19 mai 2017]. [BDPSNH] Base de données des produits de santé naturels homologués [base de données]. [modifiée le 10 août 2016]. Ottawa (Ont.) : Santé Canada. [consultée le 9 janvier 2017].
[BfR] Bundesinstitut für Risikobewertung. 2007. Introduction to the problems surrounding garment textiles. Berlin (DE): German Federal Institute for Risk Assessment (BfR). BfR Information No. 018/2007, 1 June 2007. Disponible sur demande.
Bionetics Research Labs Inc. 1968. Evaluation of carcinogenic, teratogenic, & mutagenic activities of selected pesticides and industrial chemicals. Volume I: Carcinogenic study. Bethesda (MD): National Cancer Institute. Report No.: NCI-DCCP-CG-1973-1-1. (disponible en anglais seulement)
Bremmer HJ, Prudhomme de Lodder LCH, et JGM van Engelen. 2006. Cosmetics fact sheet. RIVM report 320104001/2006 [PDF]. (disponible en anglais seulement).
Bremmer HJ, et MP van Veen. 2002. Children’s toys fact sheet to assess the risk for the consumer. RIVM report 612810012/2002 [PDF]. (disponible en anglais seulement)
Brown D (ICI Group Environmental Laboratory, Brixham, UK). 1983. Environmental assessment of dyestuffs. Prepared for the Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers, Basel, Switzerland. ETAD ecological sub-committee project E3020. Submitted to Environment Canada, May 9, 2008.
Canada. 1999. Loi canadienne sur la protection de l’environnement, 1999. L.C. 1999, ch. 33. Gazette du Canada, partie III, vol. 22, no 3.
Canada, ministère de l’Environnement. 2012. Loi canadienne sur la protection de l’environnement, 1999 : Avis concernant certaines substances de la Liste intérieure. Gazette du Canada, partie I, vol. 146, no48, Supplément [PDF].
Carson ST. 1984. Skin painting studies in mice on 11 FD&C and D&C colors: FD&C Green No. 3, Red No. 2, Red No. 4, Yellow No. 6, and External D&C No. 7, D&C Orange No.4, Violet No. 2, Red No. 17, Red No. 34, and Yellow No. 7. J Toxicol. 3(3):309-331. (disponible en anglais seulement)
Charles River Laboratories. 2017. The in vitro percutaneous absorption of radiolabelled solvent violet 13 in two test preparations through human skin. Draft report. Elphinstone (UK) : Charles River Laboratories Edinburgh Ltd. 67 p. Report No. : 38617. Financé par le Bureau de la science et de la recherche en santé environnementale, Santé Canada, Ottawa (Ont.). [Accès restreint].
[CIRC] Centre international de recherche sur le cancer. 2013. Some chemicals present in industrial and consumer products, food and drinking-water: Anthraquinone. IARC Monogr. 101:41-70.(disponible ane anglais seulement)
[ConsExpo] Consumer Exposure Model [Internet]. 2006. Version 4.1. Bilthoven (NL): Rijksinstituut voor Volksgezondheid en Milieu [Institut national de la santé publique et de l’environnement].(disponible en anglais seulement)
[ConsExpo Web] Consumer Exposure Web Model. 2016. Bilthoven (NL): Rijksinstituut voor Volksgezondheid en Milieu [Institut national de la santé publique et de l’environnement]. (disponible en anglais seulement).
[CPDB] Carcinogenic Potency Database. [modifié le 3 octobre 2007]. (disponible en anglais seulement)
Crompton et Knowles Corp. 1988. Health and safety data for six primary aminoanthraquinones selected for reporting by the EPA with attachments and cover letter dated 020188. Submission to the US EPA TSCA. Document number 86880000132. Microfiche No.: OTS0514022. (disponible en anglais seulement)
Derek Nexus [toxicity prediction module]. 2016. Ver. 5.0.2. Leeds (UK): Lhasa Limited. (disponible en anglais seulement).
[DFG] Deutsche Forschungsgemeinschaft. 1957. Kommission zur Bearbeitung des Lebensmittelfarbstoffproblems. Mitteilung. 6. Toxikologische Daten von Farbstoffen und . für Lebensmittel in verschiedenen Ländern. Bonn (DE) : DFG. [mentionné dans JECFA 1974].
[ECCC] Environnement et changement climatique Canada. 2016a. Document sur l’approche scientifique : Classification du risque écologique des substances organiques. Ottawa (Ont.) : gouvernement du Canada..
[ECCC] Environnement et Changement climatique Canada. 2016b. Document complémentaire : Data used to create substance-specific hazard and exposure profiles and assign risk classifications in the Ecological Risk Classification of organic substances. Gatineau (Qc). Renseignements à l’appui du Document sur l’approche scientifique : Classification du risque écologique des substances organiques. Disponible sur demande à l’adresse : substances@ec.gc.ca. (disponible en anglais seulement)
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada; [modifié en 2017]; Catégorisation; Ottawa (ON), gouvernement du Canada [consulté le 25 avril 2017].
[ECCC, SC] Environnement et Changement climatique Canada,Santé Canada. 2018a. Évaluation préalable rapide des substances pour lesquelles l’exposition de la population générale est limitée. Ottawa (Ont.) : gouvernement du Canada.
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada. 2018b. Évaluation préalable substances jugées comme étant peu préoccupantes au moyen de l’approche de la Classification du risque écologique des substances organiques et de l’approche fondée sur le seuil de préoccupation toxicologique (SPT). Ottawa (Ont.): gouvernement du Canada.
[ECHA] European Chemical Agency. 2015a. Committee for Risk Assessment: RAC Opinion proposing harmonised classification and labelling at EU level of Anthraquinone. Helsinki (FI): ECHA. (disponible en anglais seulement)
[ECHA] European Chemical Agency. 2015b. CLH proposed report for anthraquinone (CAS No. 84-65-1). Helsinki (FI) : ECHA.
[ECHA] European Chemicals Agency. 2017. Brief profile : 6,15-dihydroanthrazine-5,9,14,18-tetrone; CAS RN 81-77-6. Helsinki (FI): ECHA. [mis à jour le 4 avril 2017; consulté le 18 avril 2017]. (disponible en anglais seulement).
[ECHA] European Chemicals Agency. c2007-2017. Base de données sur les substances enregistrées; résultats de recherche pour les substances des nos CAS 81-77-6 et 17418-58-5. Helsinki (FI) : ECHA. [mise à jour le 12 mai 2017; consultée le 14 juin 2017]. (disponible en anglais seulement) .
[ECHA] European Chemicals Agency. c2007-2019a. Base de données sur les substances enregistrées; résultats de recherche pour la substance de no CAS 81-48-1. Helsinki (FI): ECHA. [consulté le 30 mai 2019]. (disponible en anglais seulement).
[ECHA] European Chemicals Agency. c2007-2019b. Base de données sur les substances enregistrées; résultats de recherche pour la substance de no CAS 17418-58-5. Helsinki (FI): ECHA. [consulté le 19 oct 2019]. (disponible en anglais seulement).
[ECHA] European Chemicals Agency. c2007-2019c. Base de données sur les substances enregistrées; résultats de recherche pour la substance de no CAS 6408-72-6. Helsinki (FI): ECHA. [consulté le 30 mai 2019]. (disponible en anglais seulement).
[ECHA] European Chemicals Agency. c2007-2019d. Base de données sur les substances enregistrées; résultats de recherche pour l’Acid Blue 239. Helsinki (FI): ECHA. [consulté le 14 auôt 2019]. (disponible en anglais seulement).
[Environ] ENVIRON International Corporation. 2003. Voluntary Children’s Chemical Evaluation Program Pilot (VCCEPP)-Tier 1 assessment of the potential health risks to children associated with exposure to the commercial octabromodiphenyl ether product and appendices. Emerville (CA): ENVIRON International Corporation. (disponible en anglais seulement).
Environnement Canada (2000). Environmental categorization for persistence, bioaccumulation and inherent toxicity of substances on the Domestic Substances List using QSARs. Rapport final non publié. Gatineau (QC) : Environnement Canada, Division des substances existantes. En page couverture : Results of an international QSAR workshop hosted by the Chemicals Evaluation Division of Environment Canada, November 11-12, 1999, Philadelphia, Pennsylvania. Disponible sur demande. (disponible en anglais seulement).
Environnement Canada. 2013. Données de la Mise à jour de l’inventaire de la LIS recueillies en vertu de l’article 71 de la Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances de la Liste intérieure. Données préparées par Environnement Canada et Santé Canada, Programme des substances existantes.
[EPA du Danemark] Danish Environmental Protection Agency. 2008. Survey and health assessment of chemical substances in hobby products for children. Survey of chemical substances in consumer products, No 93. Copenhagen (Denmark): Danish Environmental Protection Agency. (disponible en anglais seulement)
[EPA du Danemark] Danish Environmental Protection Agency. 2015. CMR substances in toys – Market surveillance and risk assessment [PDF]. Copenhagen (Denmark): Danish Environmental Protection Agency. [consulté le 23 décembre 2015]. (disponible en anglais seulement)
[EPI Suite] Estimation Program Interface Suite for Microsoft Windows [estimation model]. c2000-2012. Ver. 4.11. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. (disponible en anglais seulement)
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 1983. Final report on extractability of dyestuffs from textiles. Basel (CH): ETAD. Project No. A 4007.
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 1988. Toxicological testing of major colorants. Basel (CH): ETAD. Project T 2015. OTS0000621. (disponible en anglais seulement)
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 1994. In vitro absorption of various dyes through human and pig epidermis. Basel (CH): ETAD. Project T 2030, Part 1. OTS0001293. (disponible en anglais seulement)
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 1995. In vitro absorption of two disperse dyes from synthetic perspiration and five formulations. Basel (CH): ETAD. Project T 2030, Part 2.
[EU] European Union. 2017. Commission Regulation (EU) 2017/776 of 4 May 2017 amending, for the purposes of its adaptation to technical and scientific progress, Regulation (EC) No 1272/2008 of the European Parliament and of the Council on classification, labelling and packaging of substances and mixtures. Off J Eur Union L 116:1–19. (disponible en anglais seulement)
Gulati DK, Witt K, Anderson B, Zeiger E, Shelby MD. 1989. Chromosome aberration and sister chromatid exchange tests in Chinese Hamster ovary cells in vitro III: Results with 27 chemicals. Environ Mol Mutagen. 13:133-193.
Haynes WM, editor. 2017. CRC Handbook of Chemistry and Physics: Physical constants of organic compounds. [Internet]. 97th ed. Boca Raton (FL): CRC Press/Taylor & Francis.
Heucotech Ltd. 2013. Notice in accordance with TSCA section 8(e) – toxicological results for 6,15-dihydroanthrazine-5,9,14,18-tetrone (CASRN 81-77-6). Lettre adressée à l’Environmental Protection Agency des États‑Unis, datée du 7 juin 2013. (disponible en anglais seulement)
Hu S, Shen G (Environmental Testing Laboratory, Shanghai Academy of Environmental Sciences, Shanghai, China). 2008. Bioconcentration test of C.I. Disperse Blue 77 in fish. Prepared for Dystar on behalf of Ecological and Toxicological Association of the Dyes and Organic Pigments Manufacturers (ETAD) Basel, Switzerland. Report No. S-071-2007. Présenté à Environnement Canada en avril 2008. (disponible en anglais seulement)
Inoue Y, Hashizume N, Yoshida T, Murakami H, Suzuki Y, Koga Y, Takeshige R, Kikushima E, Yakata N, Otsuka M. 2012. Comparison of bioconcentration and biomagnification factors for poorly water-soluble chemicals using Common Carp (Cyprinus carpio L.). Arch Environ Contam Toxicol. 63:241–248. (disponible en anglais seulement)
[JECFA] Joint FAO/WHO Expert Committee on Food Additives. 1974. Indanthrene Blue RS. Toxicological evaluation of certain veterinary drug residues in food. WHO Food Additives Series, No. 6. Préparé par Eighteenth Meeting of the Joint FAO/WHO Expert Committee on Food Additives. World Health Organization, Geneva (CH). (disponible en anglais seulement)
[J-CHECK] Japan CHEmicals Collaborative Knowledge Database [database]. c2010- . Tokyo (JP): National Institute of Technology and Evaluation (NITE). [consulté le 18 juin 2020]. (disponible en anglais seulement)
Krishna Murthy AS, Baker JR, Smith ER, et GG Wade. 1977. Development of hemangiosarcomas in B6C3F1 mice fed 2-methyl-1-nitroanthraquinone. Int J Cancer. 19(1):117-121.
Leadscope Model Applier [prediction module]. 2016. Ver. 2.1. Columbus (OH): Leadscope, Inc.. [Accès restreint]. (disponible en anglais seulement)
Leist KH. 1982. Subacute toxicity studies of selected organic colorants. Ecotoxicol Environ Saf. 6:457-463.
Loretz LG, Api AM, Babcock L, Barraj LM, Burdick J, Cater KC, Jarrett G, Mann S, Pan YHL, Re TA, et al. 2008. Exposure data for cosmetic products: Facial cleanser, hair conditioner, and eye shadow. Food Chem Toxicol 46: 1516-1524.
Loretz L, Api AM, Barraj L, Burdick J, Davis DA, Dressler W, Gilberti E, Jarrett G, Mann S, Pan YHL, et al. 2006. Exposure data for personal care products: Hairspray, spray perfume, liquid foundation, shampoo, body wash, and solid antiperspirant. Food Chem Toxicol 44: 2008-2018.
Loretz LG, Api AM, Barraj LM, Burdick J, Dressler WE, Gettings SD, Han Hsu H, Pan YHL, Re TA, Renskers KJ, et al. 2005. Exposure data for cosmetic products: lipstick, body lotion, and face cream. Food Chem Toxicol 43: 279-291.
Lu FC, et A Lavallée. 1964. The acute toxicity of some synthetic colours used in drugs and foods. Canad Pharm J. 97:30. [mentionné dans JECFA 1974].
[MHLWJ] Ministry of Health, Labour and Welfare of Japan. 2012. 1,4 bisu(isopropylamino)anthraquinone: Reverse mutation test using bacteria. Final Report. Tokyo (JP): MHLWJ Pharmaceutical Foods Division, Administration Division, & Chemical Substance Safety Division. [traduction].
Mori H, Sugie S, Niwa K, Takahashi M, et K Kawai. 1985. Induction of intestinal tumours in rats by chrysazin. Br J Cancer. 52:781-783.
Mori H, Sugie s, Niwa K, Yoshimi N, Tanaka T, et I Hirono. 1986. Carcinogenicity of chrysazin in large intestine and liver of mice. Gann. 77:871-876.
Mori H, Yoshimi N, Iwata H, Mori Y, Hara A, Tanaka T, et K Kawai. 1990. Carcinogenicity of naturally occurring 1-hydroxyanthraquinone in rats: induction of large bowel, liver and stomach neoplasms. Carcinogenesis 11(5):799-802.
Mori Y, Yoshimi N, Iwata H, Tanaka T, et H Mori. 1991. The synergistic effect of 1-hydroxyanthraquinone on methylazoxymethanol acetate-induced carcinogenesis in rats. Carcinogenesis 12(2):335-338. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2002. Pullmelt 7B. Appenzell (CH): Beulentechnik AG. [consulté le 10 janvier 2017]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2007a. No rinse natural cat shampoo. Dallas (TX): OUT! International Inc. [consulté le 26 janvier 2016]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2007b. 665098876496 (Lotus Blossom). Mayfield (KY): MVP Group International. [consulté le 26 janvier 2016]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2007c. 665098866503 (Fresh Cut Grass). Mayfield (KY): MVP Group International. [consulté le 26 janvier 2016]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2007d. 665098866480 (Ocean Spray). Mayfield (KY): MVP Group International. [consulté le 26 janvier 2016]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet [PDF]. 2008. Cam & lifter installation lube. Memphis (TN): Comp Cams. [consulté le 10 janvier 2017]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2009a. Ink (green color) in Christmas 6 pack stamper. Hong Kong (HK): G T Plus Limited. [consulté le 26 janvier 2016]. Disponibles sur demande. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2009b. Ink in 6pk Valentine stamper. Hong Kong (HK): G T Plus Limited. [consulté le 26 janvier 2016]. Disponibles sur demande. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet [PDF]. 2011. Furniture cleaner & restorer aerosol. Hickory (NC): RPM Wood Finishes Group, Inc. [consulté le 11 janvier 2017]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2015a. Groomer’s best puppy shampoo. Secaucus (NJ): Hartz Mtn. Corp. [consulté le 26 janvier 2016]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet [PDF]. 2015b. Utrecht studio series oil colors. Brooklyn (NY) : Utrecht Manufacturing. [consulté le 4 janvier 2016]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet [PDF]. 2015c. Nozzle gel. Oakville (ON): Techniweld Corporation. [consulté le 10 janvier 2017]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2015d. MCS 7000 Component A. Clifton (NJ): DriTac Flooring Products, LLC. [consulté le 11 janvier 2017]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet [PDF]. 2018. Series 13 – PRIMAcryl. Erkrath (DE): H. Schmincke & Co. GmbH & Co. KG. [consulté le 10 janvier 2017]. (disponible en anglais seulement)
Muzzal JM, et WL Cook. 1979. Mutagenicity of dyes used in cosmetics with the Salmonella/mammalian-microsome test. Mutat Res. 67:1-8. (disponible en anglais seulement)
[NCI] National Cancer Institute. 1978. Bioassay of 2-methyl-1-nitroanthraquinone for possible carcinogenicity (CAS No. 129-15-7). Bethesda (MD): NCI, Division of Cancer Cause and Prevention. Report No.: 29. (disponible en anglais seulement)
[NTP] National Toxicology Program. 2005. Toxicology and carcinogenesis studies of anthraquinone (CAS No. 84-65-1) in F344/N rats and B6C3F1 mice (feed studies). Research Triangle Park (NC): US Department of Health and Human Services, National Toxicology Program. Report No.: TR 494. (disponible en anglais seulement)
[NTP] National Toxicology Program. [modifié le 17 mai 2017]. Testing status of C.I. Disperse Red 60 –M88155. Research Triangle Park (NC): US Department of Health and Human Services, National Toxicology Program. [consulté le 18 mai 2017]. (disponible en anglais seulement)
Noguerol-Cal R, López-Vilariño JM, González-Rodríguez MV, et L Barral-Losada. 2011. Effect of several variables in the polymer toys additive migration to saliva. Talanta 85(4): 2080-2088. (disponible en anglais seulement)
Norris B, Smith S. 2002. Research into the mouthing behaviour of children up to 5 years old [PDF] [Internet]. Report commissioned by UK Department of Trade and Industry, London, UK.(disponible en anglais seulement)
OCDE – Boîte à outils QSAR [Outil de références croisées]. 2014. Paris (FR): Organisation de coopération et de développement économiques, Laboratory of Mathematical Chemistry.
OCDE – Boîte à outils QSAR [Outil de références croisées]. 2017. Paris (FR): Organisation de coopération et de développement économiques, Laboratory of Mathematical Chemistry
Oettel H, Frohberg H, Nothdurft H, et G Wilhelm. 1965. Testing some synthetic dyes for their suitability for food coloring. Arch Toxicol. 21:9-29. [mentionné dans JECFA, 1974]. (disponible en anglais seulement)
Recherche dans les étiquettes de pesticides [base de données]. [modifié le 25 janvier 2016]. Ottawa (Ont.) : Santé Canada. [consulté le 30 septembre 2015].
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [Institut national de la santé publique et de l’environnement (NL)]. 2006. Cosmetics fact sheet [PDF]: To assess the risks for the consumer: version mise à jour pour ConsExpo 4. Bilthoven (NL): RIVM. Report No. : 320104001/2006. (disponible en anglais seulement)
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [Institut national de la santé publique et de l’environnement (NL)]. 2007. Do-it-yourself products fact sheet [PDF]: To assess the risks for the consumer. Bilthoven (NL): RIVM. Report No.:320104007/2007. (disponible en anglais seulement)
Santé Canada. 1995. Enquête sur l’exposition des êtres humains aux contaminants dans le milieu : un guide pour les calculs de l’exposition. Ottawa (Ont.) : gouvernement du Canada.
Santé Canada. 1998. Exposure factors for assessing total daily intake of priority substances by the general population of Canada. Rapport non publié. Ottawa (Ont.) : gouvernement du Canada.
Santé Canada. [modifié le 7 octobre 2015]a. Liste des colorants autorisés. [Internet]. Ottawa (Ont.) : gouvernement du Canada. [mentionné en août 2016].
Santé Canada. [modifié le 14 décembre 2015]b. Liste critique des ingrédients de cosmétiques : Liste des ingrédients dont l’usage est interdit dans les cosmétiques. Ottawa (Ont.) : gouvernement du Canada. [consulté en août 2016].
Santé Canada. 2016. Document sur l’approche scientifique : Approche fondée sur le seuil de préoccupation toxicologique (SPT) pour certaines substances. Septembre 2016. 59 p. Ottawa (Ont.) : gouvernement du Canada.
Santé Canada. 2017. Assessment of mutagenicity for selected Chemicals Management Plan-directed needs compounds with the plate incorporation Ames mutagenicity assay. Ottawa (Ont.) : Santé Canada, Bureau de la science et de la recherche en santé environnementale. 33 p. Préparé pour le Bureau de l’évaluation des risques pour les substances existantes, Santé Canada.
[SCCS] Scientific Committee on Consumer Safety. 2012. The SCCS’s notes of guidance for the testing of cosmetic ingredients and their safety evaluation, 8th Revision [PDF]. [Internet]. Scientific Committee on Consumer Safety. [consulté le 23 février 2017]. (disponible en anglais seulement)
Seifried HE, Seifried RM, Clarke JJ, Junghans TB, et RHC San. 2006. A compilation of two decades of mutagenicity test results with the Ames Salmonella typhimurium and L5178Y mouse lymphoma cell mutation assays. Chem Res Toxicol. 19:627-644. (disponible en anglais seulement)
Sijm DTHM, Schüürmann G, de Vries PJ, et A Opperhuizen. 1999. Aqueous solubility, octanol solubility, and octanol/water partition coefficient of nine hydrophobic dyes. Environ Toxicol Chem. 18(6): 1109-1117. [mentionné dans Epi Suite, c2000-2012].
Statistique Canada. 2012. Enquête canadienne sur les mesures de la santé (ECMS) : cycle 1. Ottawa (Ont.) : Statistique Canada. Disponible sur demande.
Tanaka T, Kojima T, Yoshimi N, Sugie S, et H Mori. 1991. Inhibitory effect of the nonsteroidal anti-inflammatory drug, indomethacin on the naturally occurring carcinogen, 1-hydroxyanthraquinone in male ACI/N rats. Carcinogenesis 12:1949–1952. [mentionné dans CIRC, 2002]. (disponible en anglais seulement)
[TIMES] TIssue MEtabolism Simulator [prediction module]. 2016. Ver. 2.27.19. Bourgas (BG): University “Prof. Dr. Assen Zlatarov”, Laboratory of Mathematical Chemistry. (disponible en anglais seulement) [Accès restreint].
[UE] Union européenne. 2017. Règlement (UE) 2017/776 de la Commission du 4 mai 2017 modifiant, aux fins de son adaptation au progrès technique et scientifique, le règlement (CE) n° 1272/2008 du Parlement européen et du Conseil relatif à la classification, à l’étiquetage et à l’emballage des substances et des mélanges. J. off. dr. de l’Union. Eur. 116:1–19. (disponible en anglais seulement)
Umeda M. 1956. Experimental study of xanthene dyes as carcinogenic agents. Gann. 47:51. [mentionné dans JECFA 1974].
[US EPA] US Environmental Protection Agency. 2011. Age dependent Adjustment Factor (ADAF) application. Final Report. Washington (DC): US EPA, Office of Water Policy.
[US EPA] US Environmental Protection Agency. 2012. Standard operating procedures for residential exposure assessments [PDF]. Washington (DC): US EPA, Office of Chemical Safety and Pollution Prevention, Office of Pesticide Programs, Health Effects Division. (disponible en anglais seulement)
Versar Inc. 1986. Standard scenarios for estimating exposure to chemical substances during use of consumer products. Prepared for US EPA Office of Toxic Substances, Exposure Evaluation Division.
Volodchenko VA, Gudz ZA, Timchenko AN. 1970. Materialy k obosnovaniju predelno dopustimoj koncentraciji antrachinona v vozduche rabocej zony. Gig Tr Prof Zabol. 15(2):58-59. [mentionné dans ECHA 2015 b].
Williams FM, Rothe H, Barrett G, Chiodini A, Whyte J, Cronin MTD, Monteiro-Riviere NA, Plautz J, Roper C, Westerhout J, et al. 2016. Assessing the safety of cosmetic chemicals: consideration of a flux decision tree to predict dermally delivered systemic dose for comparison with oral TTC (Threshold of Toxicological Concern). Regul Toxicol Pharmacol 76:174-186. (disponible en anglais seulement)
Wu X, Bennett DH, Ritz B, Cassady DL, Lee K, et I Hertz-Picciotto. 2010. Usage pattern of personal care products in California households. Food Chem Toxicol 48:3109-3119.
Yen CC, Perenich TA, Baughman GL. 1989. Fate of dyes in aquatic systems II. Solubility and octanol/water partition coefficients of disperse dyes. Environ Toxicol Chem. 8(11):981-986. [mentionné dans EPI Suite, c2000-2012].
Yoshimi N, Ino N, Suzui M, Tanaka T, Nakashima S, Nakamura M, Nozawa Y, et H Mori. 1995. The mRNA overexpression of inflammatory enzymes, phospholipase A2 and cyclooxygenase, in the large bowel mucosa and neoplasms of F344 rats treated with naturally occurring carcinogen, 1-hydroxyanthraquinone. Cancer Lett. 97:75-82.
Zeiger E, Anderson B, Haworth S, Lawlor T, et K Mortelmans. 1988. Salmonella mutagenicity tests: IV. Results from the testing of 300 chemicals. Environ Mol Mutagen. 11(S12):1-158. [mentionné dans NTP 2005].
Zeilmaker MJ, Kroese ED, van Haperen P, van Veen MP, Bremmer HJ, van Kranen HJ, Wouters MFA, Janus JA. 1999. Cancer risk assessment of azo dyes and aromatic amines from garment and footwear. Bilthoven (NL): Rijksinstituut voor Volksgezondheid en Milieu [Institut national de la santé publique et de l’environnement]. RIVM Report No. : 601503014. (disponible en anglais seulement)
Zeilmaker MJ, van Kranen HJ, van Veen MP, et JA Janus. 2000. Cancer risk assessment of azo dyes and aromatic amines from tattoo bands, folders of paper, toys, bed clothes, watch straps and ink [internet]. Bilthoven (NL): Rijksinstituut voor Volksgezondheid en Milieu (RIVM) [Institut national de la santé publique et de l’environnement]. Report No. : 601503 019. (disponible en anglais seulement)
Annexe A. Exposition potentielle estimée aux substances du groupe des anthraquinones
Des scénarios d’exposition sentinelle ont été utilisés pour estimer l’exposition potentielle aux substances du groupe des anthraquinones; les hypothèses des scénarios sont résumées dans le tableau A-3. L’exposition a été estimée à l’aide du modèle ConsExpo, version 4.1, ou d’algorithmes du modèle (ConsExpo, 2006), sauf si indiqué autrement. Un facteur de rétention (FR) global de 1 a été utilisé, sauf si indiqué autrement.
L’exposition a été estimée pour différents groupes d’âge établis en fonction du poids corporel (p.c.) provenant des facteurs d’exposition de Santé Canada pour la population générale du Canada (Santé Canada, 1998) :
Nourrissons (nouveau-nés à 6 mois) : 7,5 kg
Tout-petits (0,5 à 4 ans) : 15,5 kg
Enfants (5 à 11 ans) : 31,0 kg
Adolescents (12 à 19 ans) : 59,4 kg
Adultes (20 ans) : 70,9 kg
Exposition au Solvent Violet 13 par voie cutanée
Les doses potentielles absorbables du Solvent Violet 13 de l’étude de Charles River (2017) ont été utilisées pour caractériser l’exposition générale dans chaque scénario d’exposition par voie cutanée. Voici les paramètres, les algorithmes et les facteurs à considérer qui ont été utilisés :
AV : superficie cutanée exposée
PAA : dose potentielle absorbable (pendant une exposition de 24 heures)
F : fréquence d’exposition
Conc. : concentration
FR : facteur de rétention
Exposition générale par utilisation = (AV × PAA)/p.c.
Pour la vérification du bilan massique :
Charge cutanée (totale) = conc. × qté de produit × FR × F
(où « F » est seulement incorporé si > 1)
Si l’exposition générale par utilisation était inférieure à la charge cutanée (totale), l’exposition générale par utilisation a été employée pour caractériser l’exposition générale, étant donné l’absence d’épuisement complet de la dose. Sinon, la charge cutanée (totale) a été utilisée (en raison de l’épuisement complet de la dose). Si « F » est supérieur à une fois par jour, l’exposition générale par utilisation peut être utilisée comme estimation de l’exposition générale quotidienne. Autrement dit, aucun ajustement ne serait nécessaire pour la fréquence d’exposition, quel que soit le nombre d’applications de produit sur une période de 24 heures, étant donné que « PAA » représente la quantité cumulative absorbée pendant 24 heures. Dans les scénarios où « F » est inférieur à une fois par jour et au besoin, la fréquence d’exposition a été intégrée pour (aussi) produire une estimation de l’exposition générale quotidienne.
| Scénario d’exposition sentinelle | Groupe d’âge | Charge cutanée (mg/cm2) | Dose absorbable potentielle (mg/cm2)b |
|---|---|---|---|
| Crème pour le corps | Enfants | 0,00260 | 0,00163 |
| Crème pour le corps | Adolescents | 0,00255 | 0,00163 |
| Crème pour le corps | Adultes | 0,00257 | 0,00163 |
| Parfum en aérosol | Enfants | 0,0330 | 0,00163 –0,04133 |
| Parfum en aérosol | Adolescents | 0,0561 | 0,00163 –0,04133 |
| Parfum en aérosol | Adultes | 0,0561 | 0,00163 –0,04133 |
| Colorant capillaire permanent | Adolescents | 0,157 | 0,00163 –0,04133 |
| Colorant capillaire permanent | Adultes | 0,157 | 0,00163 –0,04133 |
| Peinture faciale | Tout-petits | 0,0897 | 0,00163 –0,04133 |
| Peinture faciale | Enfants | 0,0893 | 0,00163 –0,04133 |
| Peinture faciale | Adolescents | 0,0893 | 0,00163 –0,04133 |
| Peinture faciale | Adultes | 0,0893 | 0,00163 –0,04133 |
a Voir les scénarios d’exposition dans le tableau A-3 pour la fréquence (F), si pertinent.
b Les différences entre les doses absorbables sont dues aux différences dans les formulations et les concentrations utilisées dans les préparations d’essai de l’étude. La dose potentielle absorbable présentée pour le scénario d’exposition à des crèmes pour le corps correspond à la formulation de la crème Oilatum, tandis que tous les autres scénarios d’exposition par voie cutanée sont réalisés avec un éventail de formulations de crème Oilatum et d’huile d’olive, car aucune des formulations expérimentales ne correspond directement aux types de produits.
Approche du flux maximum
Comme amélioration, l’approche du flux maximum (Jmax), telle qu’utilisée dans Williams et al. (2016), a été employée pour l’estimation de l’exposition par voie cutanée pour le Solvent Blue 36 et l’Acid Blue 239. Jmax représente la limite supérieure théorique du flux à l’état d’équilibre d’une substance donnée à travers la peau, quel que soit le véhicule (empêchant les effets potentiels de retardement ou de renforcement de la pénétration de certaines formulations). Il ne tient pas compte de la présence des résidus potentiellement absorbables liés à la peau après la fin de l’exposition. Cependant, il est prudent de l’utiliser conformément aux hypothèses voulant qu’une substance donnée soit présente à sa limite de solubilité dans le vecteur « en usage » d’un produit et que l’absorption soit entièrement à l’équilibre (c.‑à‑d., ignore l’absorption plus lente durant la phase de latence).
Les équations utilisées sont fournies ci-dessous et les valeurs de solubilité dans l’eau, de log Koe et de poids moléculaire (p.c.) sont tirées des tableaux 2-1 et 3-1 du présent rapport d’évaluation préalable. Le bilan massique a également été vérifié; cette équation varie légèrement selon le scénario d’exposition et est donc fournie dans le tableau A-3 ci-dessous.
Kp (équation de Potts et Guy, fondée sur un vecteur aqueux) :
log Kp (en cm/h) = -2,71 + (0,71)(log Koe) - (0,0061)(masse moléculaire, en g/mol)
Jmax :
Jmax (en mg/cm2/h) = Kp (en cm/h) × solubilité dans l’eau (en mg/cm3)
Quantité théorique maximale absorbée par jour (Qabs) :
Qabs (en mg) = Jmax (en mg/cm2/h) × superficie du contact cutané (en cm2) × durée de l’exposition (en h)
Exposition générale par voie cutanée = Qabs/p.c.
L’estimation de l’exposition générale par voie cutanée indiquée ci-dessus représente une estimation « par utilisation », où F était inférieure à une fois par jour et une estimation « par jour » où F est égal ou supérieur à une fois par jour. Dans les cas où « F » était inférieur à une fois par jour, la fréquence d’exposition a été intégrée au besoin pour produire (aussi) une estimation de l’exposition générale quotidienne. Comme Qabs représente la quantité maximale théorique absorbée pendant une période de 24 heures pour les scénarios sentinelles examinés pour le Solvent Blue 36 et l’Acid Blue 239, aucun ajustement pour le nombre d’applications de produit n’a été nécessaire pour produire les estimations d’exposition générale quotidienne lorsque « F » était supérieur à une fois par jour.
| Substance et scénario d’exposition sentinelle | Groupe(s) d’âge | Jmax (mg/cm2/h) | Qabs (mg) |
|---|---|---|---|
| Solvent Blue 36, lubrifiants pour usages spéciaux | Adultes | 5,00E-7 | 0,00273 |
| Solvent Blue 36, après-shampoing (rinçage) | Tout-petits | 5,00E-7 | 0,00521 |
| Solvent Blue 36, après-shampoing (rinçage) | Enfants | 5,00E-7 | 0,0101 |
| Solvent Blue 36, après-shampoing (rinçage) | Adolescents, adultes | 5,00E-7 | 0,0131 |
| Solvent Violet 59, colorant capillaire permanent | Adolescents, adultes | 1,13E-6 | 0,0173 |
| Acid Blue 239, textiles, vêtements portés | Nourrissons | 1,38E-9 | 9,99E-5 |
| Acid Blue 239, textiles, vêtements portés | Tout-petits | 1,38E-9 | 1,91E-4 |
| Acid Blue 239, textiles, vêtements portés | Enfants | 1,38E-9 | 3,20E-4 |
| Acid Blue 239, textiles, vêtements portés | Adolescents | 1,38E-9 | 5,36E-4 |
| Acid Blue 239, textiles, vêtements portés | Adultes | 1,38E-9 | 6,02E-4 |
a Voir les scénarios d’exposition dans le tableau A-3 pour la fréquence (F), si pertinent.
Dose quotidienne moyenne à vie (DQMV)
La DQMV a été calculée pour toutes les expositions par voie orale et par voie cutanée au Solvent Violet 13 en tant qu’amélioration et également pour certaines expositions cutanées au Solvent Blue 36, au Disperse Red 60 et à l’Acid Blue 239 afin de tenir compte de l’utilisation du produit par d’autres groupes d’âge. Voici les hypothèses et l’équation utilisées :
EGQ : exposition générale quotidienne
Longévité moyenne (LM) : 70 ans (US EPA, 2011)
Durée des groupes d’âge (DA) : 0,5 an pour les nourrissons (0 à 6 mois), 4,5 ans pour les tout-petits (7 mois à 4 ans), 7 ans pour les enfants (5 à 11 ans), 8 ans pour les adolescents (12 à 19 ans) et 50 ans pour les adultes (20 ans et plus) (Santé Canada, 1998)
DQMV = [(EGQnourrissons × DAnourrissons) + (EGQtout-petits × DAtout-petits) + (EGQenfants × DAenfants) + (EGQadolescents × DAadolescents) + (EGQadultes × DAadultes)] / [LM]
| Substance(s) | Scénario d’exposition sentinelle | Hypothèses |
|---|---|---|
| Solvent Violet 13 | Baume pour les lèvres ou rouge à lèvres (tout-petits, enfants, adolescents et adultes) | Conc. : ≤ 1 % (communication personnelle, courriel de la Direction de la sécurité des produits de consommation et des produits dangereux de Santé Canada adressé au Bureau d’évaluation du risque des substances existantes de Santé Canada, daté de 2016; sans référence)F : 0,59/jour (tout-petits) et 0,89/jour (enfants) (Wu et al., 2010); 2,4/jour pour les adolescents et les adultes (Loretz et al., 2005)Quantité de produit : 0,01 g/application, quel que soit le groupe d’âge (Loretz et al., 2005), 100 % ingérés, présumément |
| Solvent Violet 13 | Crème pour le corps (enfants, adolescents et adultes) | Conc. : ≤ 0,9 % (communication personnelle, courriel de la Direction de la sécurité des produits de consommation et des produits dangereux de Santé Canada adressé au Bureau d’évaluation du risque des substances existantes de Santé Canada, daté de 2016; sans référence)F : 1,1/jour (Loretz et al., 2005)Quantité de produit par application (moyenne) : 2,2 g pour les enfants, 3,8 g pour les adolescents et 4,4 pour les adultes (Loretz et al., 2005; en utilisant les facteurs d’ajustement de la superficie pour les enfants et les adolescents)AV : 8 390 cm2 pour les enfants, 14 740 cm2 pour les adolescents et 16 925 cm2 pour les adultes (Santé Canada, 1995)PAA : 1,63 µ g/cm2 (Charles River Laboratories 2017) |
| Solvent Violet 13 | Parfum en aérosol (enfants, adolescents et adultes) | Conc. : ≤ 1 % (communication personnelle, courriel de la Direction de la sécurité des produits de consommation et des produits dangereux de Santé Canada adressé au Bureau d’évaluation du risque des substances existantes de Santé Canada, daté de 2016; sans référence)F : 0,58/jour ou 17,4/mois pour les enfants (Wu et al., 2010); 1,7/jour pour les adolescents et les adultes (Loretz et al., 2006)Quantité de produit : 0,33 g/application pour tous les groupes d’âge (Loretz et al., 2006)AV : 100 cm2 pour tous les groupes d’âge (ConsExpo, 2006)PAA: 1,63 to 41,33 µg/cm2 (Charles River Laboratories 2017)Taux d’inhalation (adultes) : 16,2 m3/jour (Santé Canada, 1998) |
| Solvent Violet 13 | Colorant capillaire permanent (à laver) (adolescents et adultes) | Conc. : ≤ 1 % (communication personnelle, courriels de la Direction de la sécurité des produits de consommation et des produits dangereux de Santé Canada adressés au Bureau d’évaluation du risque des substances existantes de Santé Canada, datés du 1er février 2016; sans référence)F : 0,01/jour pour les adolescents et 0,02/jour ou 7,99/an pour les adultes (Statistique Canada, 2012)Pour les deux groupes d’âge :Quantité de produit : 100 g/application (RIVM, 2006)FR : 0,10 (SCCS 2012)AV : 638 cm2 (Santé Canada, 1995)PAA : 1,63 à 41,33 µ g/cm2 (Charles River Laboratories, 2017) |
| Solvent Violet 13 | Peinture faciale (tout-petits, enfants, adolescents et adultes) | Conc ≤ 3% (communication personnelle, courriels de Direction de la sécurité des produits de consommation et des produits dangereux de Santé Canada, adressés au Bureau de l’évaluation des risques pour les substances existantes de Santé Canada, daté 2019; sans référence)F : 0,03/jour ou 12/an pour les tout-petits, les enfants et les adolescents; 0,02/jour ou 6/an pour les adultes (Bremmer et al., 2006) Pour l’exposition par voie cutanée estimée :Quantité de produit par application : 1,3 g pour les tout-petits, 1,8 g pour les enfants et 1,9 g pour les adolescents et les adultes (Bremmer et al., 2006)AV : 435 cm2 pour les tout-petits, 605 cm2 pour les enfants et 638 cm2 pour les adolescents et les adultes (Santé Canada, 1995)PAA : 1,63 à 41,33 µ g/cm2 (Charles River Laboratories, 2017) L’exposition par voie orale à la peinture faciale (indirectement, par la main portée à la bouche) a également été estimée pour les tout-petits.Taux d’ingestion : 0,44 mg/min (Bremmer et van Veen, 2002)Duration : 480 min (Bremmer et van Veen, 2002) |
| Pigment Blue 60 | Matériel de bricolage et d’artisanat (p. ex., tampon), tout-petits et adolescents | Conc. : 40 % (MSDS, 2009a,b,c)Ligne d’encre quotidienne : 25 cm/jour (communication personnelle, courriels de l’Art and Creative Materials Institute adressés au Bureau d’évaluation du risque des substances existantes de Santé Canada, datés de 2009; sans référence)Taux de couverture de l’encre : 100 µg/cm (90e centile du niveau de couverture de l’encre d’instruments d’écriture; communication personnelle, courriels de l’Art and Creative Materials Institute adressés au Bureau d’évaluation du risque des substances existantes de Santé Canada, datés de 2016; sans référence)Quantité d’encre estimée par exposition : 50 mg (supposé, de façon prudente, être la même que pour un stylo-feutre; EPA du Danemark, 2008) Fraction absorbée : 1 (comme pire scénario) Exposition par voie orale/cutanée par utilisation = (conc. × quantité estimative d’encre par exposition × fraction absorbée)/p.c. Exposition par voie orale/cutanée quotidienne estimée= (ligne d’encre quotidienne x taux de couverture de l’encre x conc.)/(p.c.) |
| Solvent Violet 59 | Jouets en plastique, portés à la bouche (tout-petits) | Concentration de simulacre (conc.) : 0,004 mg/L (concentration moyenne utilisée pour l’exposition générale quotidienne)a; 0,01 mg/L (concentration maximale utilisée pour une exposition « par utilisation »)a (Noguerol-Cal et al., 2011)Flux de salivation (Vs) : 0,00022 L/min (Environ., 2003)Extraction fractionnée (FR; fraction sans unité) : 1Facteur d’absorption par voie orale (AFo; fraction sans unité) : 1F : 60 min/jour (Norris et Smith, 2002) Exposition par voie orale estimée = (conc. × Vs × FR × AFo × F)/ p.c.(adapté d’Environ., 2003) |
| Solvent Blue 36 | Lubrifiant pour usages spéciaux (adultes) | Conc. : 1 % (MSDS, 2008)Superficie de la zone de contact cutané : 227,5 cm2 (correspond au quart de la superficie de la main dans Santé Canada, 1995)Épaisseur du film sur la peau (t) : 15,88 E-03 cm (valeur pour l’épaisseur initiale du film d’huile minérale sur la peau après immersion) (Versar, 1986)Masse volumique du produit (DSY) : 1 g/cm3 (masse volumique de l’eau utilisée comme approximation grossière faute de masse volumique propre au produit)Durée de l’exposition : 24 h Pour la vérification du bilan massique : Charge cutanée = Conc. × T × DSY |
| Solvent Blue 36 | Après-shampoing (à rincer) (tout-petits, enfants, adolescents, adultes) | Conc. : =< 3 % (communication personnelle, courriel de la Direction de la sécurité des produits de consommation et des produits dangereux de Santé Canada adressé au Bureau d’évaluation du risque des substances existantes de Santé Canada, daté de 2016; sans référence)Superficie de la zone de contact cutané : 435 cm2 pour les tout-petits, 845 cm2 pour les enfants et 1 092,5 cm2 pour les adolescents et les adultes (Santé Canada, 1995)F : 0,44/jour pour les tout-petits (Wu et al., 2010), 0,49/jour pour les enfants (Wu et al., 2010) et 1,10/jour pour les adolescents et les adultes (Loretz et al., 2008)Quantité de produit : 8,9 g/application pour les tout-petits (d’après le coefficient d’ajustement de la superficie) et 13,1 g/application pour les enfants, les adolescents et les adultes (Loretz et al., 2008)Durée de l’exposition : 24 h/jourFR : 0,01 (SCCS, 2012) Pour la vérification du bilan massique : Charge cutanée (totale) = conc. × qté de produit × FR × F |
| Disperse Red 60, Acid Blue 239 | Textiles, porter des objets à la bouche (nourrisson) | Conc. : 1 % (BfR, 2007)F : 1/jourSuperficie (SA) de l’objet porté à la bouche : 20 cm2 (Zeilmaker et al., 2000)Masse surfacique (AW) de textile : 20 mg/cm2 (US EPA, 2012)cFraction de migration (MF) : 0,005 (aiguë); 0,0005 (chronique) (BfR, 2007)d Exposition par voie orale estimée = conc. × SA × AW × MF × F)/p.c. |
| Disperse Red 60 | Textiles, vêtements portés (nourrissons, tout-petits, enfants, adolescents et adultes) | Conc. : 1 % (BfR 2007)F : 1/jourSuperficie de la zone de contact cutané : 3 020 cm2 pour les nourrissons (pyjama); 5 780 cm2 pour les tout-petits, 9 660 cm2 pour les enfants, 16 200 cm2 pour les adolescents et 18 200 cm2 pour les adultes (vêtements personnels) (Santé Canada, 1995)Masse surfacique (AW) : 20 mg/cm2 (US EPA, 2012)bMF : 0,005 (aiguë); 0,0005 (chronique) (BfR, 2007)cCoefficient de contact cutané (SCF) : 1Absorption cutanée (DA) pour Disperse Red 60 : 2 % (zones de transpiration abondante) (Bfr, 2007) Exposition par voie cutanée estimée = (conc. × SA × AW × MF × F × SCF × DA)/p.c. |
| Acid Blue 239 | Textiles, vêtements portés (nourrissons, tout-petits, enfants, adolescents et adultes) | Superficie de la zone de contact cutanée : 3 020 cm2 pour les nourrissons (pyjama); 5 780 cm2 pour les tout-petits, 9 660 cm2 pour les enfants, 16 200 cm2 pour les adolescents et 18 200 cm2 pour les adultes (vêtements personnels) (Santé Canada, 1995)Durée de l’exposition : 24 h/jourMasse surfacique (AW) : 20 mg/cm2 (US EPA, 2012)bMF : 0,005 (aiguë); 0,0005 (chronique) (BfR, 2007)c Pour la vérification du bilan massique : Charge cutanée = Conc. × SA × AW × MF |
| N° CAS 74499-36-8 | Revêtement en époxy, application (adultes) | Conc. : 0,1 % (MSDS, 2015d) Quantité de produit : 0,25 g (RIVM, 2007)Exposition estimée à l’aide de ConsExpo Web (2016) |
Abréviations : AV, superficie de la peau exposée; PAA, dose absorbable potentielle (exposition de 24 heures); F, fréquence d’exposition; Conc., concentration; FR, facteur de rétention.
a Faute de données empiriques sur la migration propres au Solvent Violet 59, la concentration mesurée de Solvent Blue 35 (NE CAS 17354-14-2), une anthraquinone colorante, provenant de jouets de polymères commerciaux (n = 3) en contact avec un simulacre de salive (pH de 6,8; à température ambiante; durée de contact de 10 jours) a été utilisée comme donnée de substitution en raison de la similitude du type de produit, étant donné que les deux produits font partie de la même catégorie de produits chimiques et de la même catégorie d’application de colorant. Solvent Blue 35 devrait être un analogue prudent pour la migration, étant donné que sa masse moléculaire de 350,45 g/mol est inférieure à celui du Solvent Violet 59 (422,44 g/mol).
b La masse surfacique du textile correspond à celle du coton, laquelle est représentative de celle du textile dans le pire scénario par rapport à celle des tissus synthétiques (c.-à-d. 1 mg/cm2), et est considérée comme protectrice sur ce plan.
c La migration des colorants provenant de textiles varie considérablement selon le type de fibre, le type de teinture utilisée, la charge de teinture, la technologie utilisée pour teindre, l’intensité de la couleur et l’après-traitement. L’exposition aux teintures des textiles est en partie dictée par la quantité de teinture migrant du textile à la peau humaine (ETAD, 1983) ou du textile porté à la bouche. Le groupe de travail sur les « textiles » (BfR, 2007) utilise une fraction de migration initiale maximale de 0,005 pour estimer l’exposition aux teintures des vêtements neufs non lavés, et la fraction de migration chronique supposée est le dixième de la valeur mesurée pour la première migration pour représenter l’exposition avec les premiers lavages. Il est présumé que la fraction migrante due à la sueur est semblable à la fraction migrante due à la salive, ce qui concorde avec les observations du comportement de lessivage des colorants des textiles faites par Zeilmaker et al. (1999). Par conséquent, une fraction du colorant qui migre d’un textile de 0,0005 par jour a été formulée comme hypothèse pour l’estimation de l’exposition par voie cutanée et par voie orale de façon chronique.
