Évaluation préalable groupe des acides carboxyliques
Titre officiel : Évaluation préalable groupe des acides carboxyliques
Numéros d’enregistrement du Chemical Abstracts Service
79-09-4, 107-92-6, 112-05-0, 144-62-7
Environnement et Changement climatique Canada
Santé Canada
Mars 2019
No de cat. : En14-364/2019F-PDF
ISBN 978-0-660-29736-1
Sommaire
En vertu de l’article 74 de la Loi canadienne sur la protection de l’environnement 1999 (LCPE), la ministre de l’Environnement et la ministre de la Santé ont procédé à une évaluation préalable de quatre substances désignées collectivement sous le nom de groupe des acides carboxyliques. Les substances de ce groupe figurent parmi celles qui ont été désignées comme devant être évaluées en priorité, car elles satisfont aux critères de catégorisation au sens du paragraphe 73(1) de la Loi. Leur numéro d’enregistrement du Chemical Abstract ServiceNote de bas de page 1 (NE CAS), leur nom sur la Liste intérieure, et leur nom commun figurent au tableau ci-dessous.
| NE CAS | Nom dans la LI | Nom commun |
|---|---|---|
| 79-09-4 | Acide propionique | Acide propionique |
| 107-92-6 | Acide butyrique | Acide butyrique |
| 112-05-0 | Acide nonanoïque | Acide nonanoïque |
| 144-62-7 | Acide oxalique | Acide oxalique |
Entre 10 000 et 100 000 kg d’acide butyrique et d’acide oxalique, 28 925 kg d’acide nonanoïque et entre 1 000 000 et 10 000 000 kg d’acide propionique ont été déclarés avoir été importés en 2011. Selon les déclarations couvrant 2011 aucune de ces substances n’aurait été produite au Canada en des quantités dépassant le seuil de déclaration de 100 kg.
Plusieurs utilisations commerciales des substances du groupe des acides carboxyliques ont été signalées au Canada, notamment comme adjuvant de traitement, composant de matériaux plastiques ou caoutchouteux, substance industrielle intermédiaire, lubrifiant, solvant et composés non pesticides utilisés en agriculture.
Ces substances sont produites naturellement. Les acides propionique et butyrique sont endogènes chez l’humain et sont élaborés par la fermentation microbienne dans le tube digestif. Les acides propionique, butyrique et nonanoïque sont naturellement présents dans divers aliments et sont aussi utilisés comme agents aromatisants. L’acide propionique est aussi un additif alimentaire approuvé au Canada. Les acides propioniqueet oxalique sont aussi utilisés comme ingrédients dans la fabrication de divers matériaux d’emballage alimentaire. L’acide nonanoïque et l’acide oxalique sont des additifs accidentels dans les installations de transformation des aliments. L’acide oxylique est également naturellement présent dans divers aliments et a été identifié comme ingrédient dans certains produits nettoyant disponibles aux consommateurs au Canada.
Toutes les substances du groupe des acides carboxyliques sont des produits de formulation de pesticide homologués au Canada. Elles sont également toutes des ingrédients autorisés de produits de santé naturels. Les acides propionique, butyrique et oxalique ont été identifiés dans des produits de santé naturels. Certaines de ces substances sont également présentes dans des produits disponibles aux consommateurs, comme l’acide nonanoïque dans les produits de maquillage pour les yeux et les produits de nettoyage, et l’acide oxalique dans les produits de nettoyage.
Les risques des substances du groupe des acides carboxyliques pour l’environnement ont été caractérisés au moyen de l’approche de la Classification du risque écologique des substances organiques (CRE), approche basée sur les risques qui tient compte de plusieurs paramètres liés au risque et à l’exposition exerçant une pondération des éléments de preuve pour classer le risque. Les profils de danger sont principalement établis sur la base de paramètres liés au mode d’action toxique, à la réactivité chimique, à des seuils de toxicité interne dérivés du réseau trophique, à la biodisponibilité et à l’activité biologique et chimique. Parmi les paramètres pris en compte pour les profils d’exposition, citons le taux d’émission potentiel, la persistance globale et le potentiel de transport à grande distance. Une matrice de risque est utilisée pour que soit assigné aux substances un risque de préoccupation faible, moyen ou élevé, selon leur profil de danger et d’exposition. D’après les résultats de l’analyse de la CRE, il est peu probable que l’acide propionique, l’acide butyrique, l’acide nonanoïque et l’acide oxalique causent des effets nocifs pour l’environnement.
Compte tenu de tous les éléments de preuve contenus dans la présente évaluation préalable, le risque que l’acide propionique, l’acide butyrique, l’acide nonanoïque et l’acide oxalique nuisent à l’environnement est faible. Il a été conclu que l’acide propionique, l’acide butyrique, l’acide nonanoïque et l’acide oxalique ne satisfont à aucun des critères énoncés aux alinéas 64a) ou 64b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique ou qui constituent ou peuvent constituer un danger pour l’environnement essentiel pour la vie.
Sur le plan de la santé humaine, l’acide propionique a été étudié par l’Organisation de coopération et de développement économiques (OCDE 2007) et l’Autorité européenne de sécurité des aliments (EFSA 2014), l’acide butyrique par l’OCDE (OCDE 2003) et l’acide nonanoïque par l’Agence européenne des produits chimiques (ECHA 2013). La population générale pourrait être exposée aux acides propionique et butyrique à cause de leur présence naturelle dans l’environnement et les aliments, de leur emploi comme additif alimentaire ou comme aromatisant, et de leur utilisation dans des produits de santé naturels ou des produits homéopathiques. La population générale pourrait être exposée à l’acide nonanoïque à cause de sa présence naturelle dans l’environnement et les aliments, de son emploi comme aromatisant dans les aliments et de sa présence dans des produits de maquillage pour les yeux et des solutions désinfectantes liquides. Les informations des évaluations internationales susmentionnées indiquent que l’acide propionique, l’acide butyrique et l’acide nonanoïque sont des substances présentant un faible potentiel de danger et donc que les risques qu’elles posent à la santé humaine sont faibles.
L’exposition à l’acide oxalique peut découler de sa présence comme ingrédient dans des produits de nettoyage et sa présence naturelle dans les aliments. Les renseignements disponibles sur les effets sur la santé de l’acide oxalique indiquent de possibles effets sur le système reproducteur. Nous considérons que les marges d’exposition entre l’exposition estimée à l’acide oxalique et le seuil d’effets critiques observé en laboratoire sont adéquates pour compenser les incertitudes dans les bases de données sur l’exposition et sur les effets sur la santé.
À la lumière des renseignements présentés dans la présente évaluation préalable, il a été conclu que l’acide propionique, l’acide butyrique, l’acide nonanoïque et l’acide oxalique ne satisfont à aucun des critères énoncés à l’alinéa 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ni dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la santé ou la vie humaine.
Il a été conclu que l’acide propionique, l’acide butyrique, l’acide nonanoïque et l’acide oxalique ne satisfont à aucun des critères énoncés à l’article 64 de la Loi.
1. Introduction
Conformément à l’article 74 de la Loi canadienne sur la protection de l’environnement 1999 (la Loi), la ministre de l’Environnement et la ministre de la Santé ont réalisé une évaluation préalable de quatre substances désignées collectivement sous le nom de groupe des acides carboxyliques afin d’établir si celles-ci constituent ou pourraient constituer un risque pour l’environnement ou la santé humaine. Les substances du groupe ont été évaluées en priorité, car elles répondaient aux critères de catégorisation du paragraphe 73(1) de la Loi (ECCC et SC, modifié, 2017).
Les risques posés à l’environnement par les quatre substances du groupe des acides carboxyliques ont été caractérisés au moyen de la Classification des risques écologiques des substances organiques (CRE) (ECCC 2016a). La CRE décrit les risques posés par une substance en utilisant des paramètres clés parmi lesquels le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne dérivés du réseau alimentaire, la biodisponibilité et l’activité chimique et biologique. Elle tient compte de l’exposition possible des organismes dans des environnements terrestres ou aquatiques, basée sur des facteurs incluant les taux d’émission potentiels, la persistance globale et le potentiel de transport atmosphérique sur de grandes distances. Les divers éléments probants sont combinés afin de déterminer quelles substances nécessitent une évaluation plus poussée de leur potentiel d’effets nocifs sur l’environnement ou présentant une faible probabilité de tels effets.
Diverses organisations internationales ont étudié les substances du groupe des acides carboxyliques, notamment l’Organisation de coopération et de développement économiques (OCDE) dans le cadre du Programme d’évaluation coopérative des produits chimiques, l’Agence européenne des produits chimiques (ECHA) et l’Autorité européenne de sécurité des aliments (EFSA). Environnement et Changement climatique Canada et Santé Canada considèrent que ces évaluations sont fiables. Nous avons utilisé les données de ces évaluations pour éclairer la caractérisation des effets sur la santé de certaines des substances du groupe des acides carboxyliques.
La présente évaluation préalable tient compte des renseignements sur les propriétés chimiques des substances visées, de leur devenir environnemental, de leurs dangers, de leurs utilisations et l’exposition à celles-ci, ainsi que d’autres renseignements communiqués par des parties intéressées. Nous avons cherché des données pertinentes jusqu’en octobre 2016. Toutefois, des études ou des renseignements plus récents obtenus auprès de pairs à l’interne ou étrangers peuvent aussi être cités. Nous avons utilisé des données d’études cruciales et des résultats tirés de modèles pour arriver à nos conclusions.
La présente évaluation préalable a été rédigée par le personnel du Programme d’évaluation des risques de la Loi travaillant à Santé Canada et à Environnement et Changement climatique Canada. La partie du présent document portant sur l’environnement repose sur le document de CRE (publié le 30 juillet 2016) et a fait l’objet d’un examen externe et d’une consultation publique de 60 jours. Les parties du présent document portant sur la santé humaine ont fait l’objet d’un examen ou d’une consultation par des pairs externes. Nous avons reçu des commentaires sur les parties techniques portant sur la santé humaine de la part de Lynne Haber (département de la santé environnementale, collège de médecine, université de Cincinnati), Michael Jayjock (Jayjock & Associates LLC) et Raymond York (RG York & Associates LLC). De plus, l’ébauche de la présente évaluation préalable publiée le 30 décembre 2017 a été soumise à une consultation publique de 60 jours. Les commentaires de l’extérieur ont été pris en compte, toutefois Santé Canada et Environnement et Changement climatique Canada assument la responsabilité du contenu final et des résultats de l’évaluation préalable.
La présente évaluation préalable repose sur des renseignements critiques permettant de déterminer si les substances satisfont aux critères énoncés à l’article 64 de la Loi. Pour ce faire, les informations scientifiques ont été étudiées et intégrées à une approche basée sur le poids de la preuve et le principe de précautionNote de bas de page 2 . Dans la présente évaluation préalable, nous présentons les renseignements critiques et les considérations à partir desquels nous avons tiré la conclusion.
2. Identité des substances
Le tableau 2‑1 présente le numéro d’enregistrement du Chemical Abstracts ServiceNote de bas de page 3 (NE CAS), le nom sur la Liste intérieure (LI) et d’autres noms pour chaque substance du groupe des acides carboxyliques. On peut trouver d’autres noms chimiques en anglais (par ex., noms commerciaux) dans les National Chemical Inventories (NCI 2015).
| NECAS | Nom sur la LI (autres noms) | Structure chimique et formule moléculaire | Poids moléculaire (g/mol) |
|---|---|---|---|
| 79-09-4 | Acidepropionique (acidepropanoïque, acideéthylformique, acideméthylacétique) | 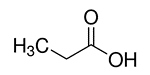 C3H6O2 C3H6O2 |
74,08 |
| 107-92-6 | Acidebutyrique (acidebutanoïque, acideéthylacétique, aciden-butanoïque) | 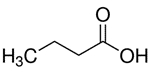 C4H8O2 C4H8O2 |
88,11 |
| 112-05-0 | Acidenonanoïque (acidepélargique, acidenonylique, acidepélargonique | 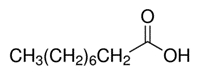 C9H18O2 C9H18O2 |
158,24 |
| 144-62-7 | Acide oxalique (acideéthanedioïque, sel d’oseille) | 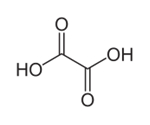 C2H2O4 C2H2O4 |
90,04 |
3. Propriétés physiques et chimiques
Le tableau 3‑1 donne un résumé des propriétés physiques et chimiques des substances du groupe des acides carboxyliques avec la gamme des valeurs trouvées pour chaque propriété. ECCC (2016b) énumère d’autres propriétés physiques et chimiques.
| Propriété | Acide propionique | Acide butyrique | Acide nonanoïque | Acide oxalique | Références principales |
|---|---|---|---|---|---|
| État physique | Liquide huileux incolore | Liquide huileux incolore | Liquide huileux incolore | Solide blanc | ChemIDplus 1993-a,b,c,d |
| Point de fusion (°C) | -20,7 | -5,7 | 12,3 | 189,5 | ChemIDplus 1993-a,b,c,d |
| Pression de vapeur (Pa) | 470 | 220 | 2,20 | 0,031 | ChemIDplus 1993-a,b,c,d |
| Constante de la loi de Henry (atm m3/mol) | 4,45 × 10-7 | 5,35 × 10-7 | 1,62 × 10-6 | 1,43 × 10-10 | ChemIDplus 1993-a,b,c,d |
| Hydrosolubilité (mg/L) | 1,0 × 106 | 60 000 | 284 | 220 000 | ChemIDplus 1993-a,b,c,d |
| log Koe (sans dimension) | 0,33 | 0,79 | 3,42 | -2,22* | ChemIDplus 1993-a,b,c,d |
| pKa1 (sans dimension) | 4,87 | 4,82 | 4,95 | 1,46 | HSDB 1993-a,b,c, Haynes 2016 |
| pKa2 (sans dimension) | s.o. | s.o. | s.o. | s.o. | Haynes 2016 |
Abréviations – Koe : coefficient de partition octanol-eau, pKa : constante d’acidité
* : la valeur publiée est une estimation
4. Sources et utilisations
L’acide propionique, l’acide butyrique et l’acide nonanoïque existent naturellement dans une grande variété d’aliments, notamment les fruits, les légumes, les produits laitiers, la viande, le café, les noix et les produits céréaliers; de même, l’acide butyrique et l’acide nonanoïque sont naturellement présents dans certaines huiles essentielles (Burdock 2009, HSDB 1983-a, b, c). La principale source alimentaire d’acide oxalique découle de sa présence naturelle dans les plantes et les produits végétaux, en particulier les graines et les plantes feuillues proches de l’épinard ou de la rhubarbe (Holmes et Kennedy 2000). Certaines substances peuvent aussi se retrouver dans les aliments à cause de leur utilisation comme agents aromatisants ou additifs dans les aliments, comme nous l’explicitons plus bas.
Les acides propionique et butyrique sont des acides gras volatils et ils sont produits par la fermentation métabolique de matières végétales dont la cellulose, les fibres, les amidons et les sucres (Bergman 1990). Ils sont produits par fermentation microbienne dans le tube digestif en grande proportion par les herbivores et chez l’humain, dans une moindre mesure (Bergman 1990). L’acide oxalique est produit par les mammifères comme le produit final de la métabolisation des acides aminés, de l’acide hydroxyacétique et de l’acide ascorbique (EMA 2003). L’oxydation photochimique d’autres hydrocarbures et oléfines cycliques dans l’atmosphère pourrait produire de l’acide oxalique dans l’air (Kawamura et Kaplan 1987). On a aussi signalé la présence de cette substance dans les gaz d’échappement des véhicules (Kawamura et Kaplan 1987).
L’emploi d’un composé à la structure similaire, l’acide oxalique dihydrate (NE CAS 6153-56-6), pourrait constituer une source d’exposition à l’acide oxalique. L’acide oxalique dihydrate est homologué comme ingrédient actif de pesticides au Canada et est réglementé en vertu de la Loi sur les produits antiparasitaires. Il est aussi présent au Canada dans des produits de nettoyage vendus au consommateur.
Toutes les substances du groupe ont été visées par les enquêtes menées conformément à l’avis émis en vertu de l’article 71 de la LCPE (ECCC 2013). Selon les déclarations, aucune de ces substances n’a été fabriquée au Canada en 2011. Le tableau 4‑1 donne un résumé des quantités des substances du groupe des acides carboxyliques fabriquées et importées en 2011.
| Substance | Importations totalesa (kg) |
|---|---|
| Acide propionique | 1 000 000 – 10 000 000 |
| Acide butyrique | 10 000 – 100 000 |
| Acide nonanoïque | 28 925 |
| Acide oxalique | 10 000 – 100 000 |
a Ces valeurs proviennent des quantités déclarées en réponse aux enquêtes réalisées en vertu de l’article 71 de la Loi (ECCC 2013). Consultez l’enquête pour les inclusions et exclusions particulières (annexes 2 et 3).
On utilise l’acide propionique au Canada comme formulant dans les produits antiparasitaires. L’utilisation de l’acide propionique et de ses sels de sodium et de calcium est autorisée dans les aliments en tant qu’additif, comme l’indique la Liste des agents de conservation autorisés. On l’emploie comme agent de conservation dans certains aliments comme les pains et certains types de fromages. On le retrouve aussi comme ingrédient dans la fabrication de matériaux d’emballage alimentaire, notamment dans les encres à l’extérieur des matériaux utilisés pour emballer les aliments et les revêtements de tuyauterie (communication personnelle de 2017, courriels de la Direction des aliments de Santé Canada au Bureau d’évaluation du risque des substances existantes de Santé Canada, sans référence).
En 2011, la production américaine d’acide propionique, d’acide butyrique et d’acide oxalique se situait entre 9 et 204 millions de kg (entre 20 et 450 millions de livres), respectivement (ChemView 2013-a,b,c). En 2011, on y avait synthétisé plus de 9 millions de kg (20 millions de livres) d’acide nonanoïque (Chemview 2013-a,b,c).
En Europe, l’acide propionique est aussi utilisé comme aromatisant ou additif dans les aliments (EU Food Flavouring Database [modifiée en 2016]; EU Food Additives Database [modifiée en 2018]) et, aux États-Unis, la substance est autorisée par le titre 21 CFR 184.1081 comme ingrédient alimentaire sans limitation autre que les bonnes pratiques de fabrication actuelles et elle est « généralement considérée sûre » (US FDA 2016a, FCC 2016). L’acide propionique figure à la Base de données d’ingrédients de produits de santé naturels (BDIPSN) avec un rôle médicinal et est classé comme substance de produit de santé naturel, visé par l’article 2 (extrait ou isolat) de l’annexe 1 du Règlement sur les produits de santé naturels (RPSN). Cet acide est aussi mentionné avec un rôle non médicinal comme rehausseur de saveur ou agent de conservation antimicrobien (BDIPSN 2018). Il figure dans la Base de données des produits de santé naturels homologués (BDPSNH), comme étant présent comme ingrédient non médicinal dans un produit de santé naturel (BDPSNH 2018). Au Canada, l’acide propionique a plusieurs utilisations commerciales, notamment comme adjuvant de traitement dans les peintures et les revêtements, les traitements à l’eau et les matériaux de plastique ou de caoutchouc (ECCC 2013).
Au Canada, on utilise l’acide butyrique comme formulant de produits antiparasitaires. Il figure dans la BDIPSN qui mentionne qu’il a un rôle médicinal. Il est classé parmi les substances de produits de santé naturels à l’article 2 (un isolat) de l’annexe 1 du Règlement sur les produits de santé naturels, avec un rôle non médicinal comme agent aromatisant, et substance homéopathique servant d’ingrédient médicinal dans les produits de santé naturels homologués comme médicaments homéopathiques (BDIPSN 2018). Il figure aussi dans les BDPSNH comme ingrédient médicinal et non médicinal d’un certain nombre de produits de santé naturels actuellement homologués, dont les médicaments homéopathiques (BDPSNH 2018). Selon des informations divulguées conformément à l’avis émis en vertu de l’article 71 de la LCPE, on trouve de l’acide butyrique dans des aliments et boissons au Canada où il est un ingrédient de produits aromatisants (ECCC 2017). Aux États-Unis, l’acide butyrique est utilisé dans les aliments comme agent aromatisant et est autorisé en vertu du titre 21 CFR 182.60 comme aromatisant synthétique « généralement reconnu sûr » (US FDA 2016b). En Europe, il est soumis à l’UE no 872/2012 en tant qu’aromatisant (UE 2012). Au Canada, les utilisations commerciales de l’acide butyrique comprennent les produits agricoles non pesticides (ECCC 2013). La plus grande partie de l’acide butyrique fabriqué aux États-Unis sert de substance intermédiaire dans la synthèse d’acétobutyrate de cellulose (OCDE 2003). Les feuilles d’acétobutyrate de cellulose sont diversement utilisées, notamment dans les thermoplastiques, les visières de protection, les lunettes de sécurité et les revêtements pour les automobiles (OCDE 2003). Ailleurs dans le monde, l’acide butyrique est notamment utilisé comme substance intermédiaire dans la production de produits pharmaceutiques, d’émulsifiants et de désinfectants, d’agents de tannage du cuir, de parfums d’ester de butyrate et des agents aromatisants des aliments (SRI 1999, Hawley 1981, Reimenshneider 1986 et Furia 1972, cités par OCDE 2003).
On utilise l’acide nonanoïque au Canada comme formulant dans les produits antiparasitaires et il aussi présent comme ingrédient dans les maquillages pour les yeux et une solution désinfectante liquide prête à l’emploi (communication personnelle, courriels de 2016, de l’Agence de réglementation de la lutte antiparasitaire au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence; communication personnelle, courriels de 2016 de la Direction des produits thérapeutiques à Santé Canada au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence). On a aussi déclaré l’acide nonanoïque comme ingrédient de désinfectants utilisés dans les installations de transformation des aliments (communication personnelle, courriels de 2017 de la Direction des Aliments de Santé Canada au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence). L’acide nonanoïque a différentes utilisations commerciales au Canada, notamment pour la synthèse de substances intermédiaires, de lubrifiants, d’additifs aux lubrifiants et de produits antiparasitaires (ECCC 2013). L’acide nonanoïque figure à la BDIPSN avec un rôle non médicinal comme exhausteur de goût, mais n’apparaît pas dans la BDPSNH comme étant présent dans les produits de santé naturels homologués (BDPSNH 2018, BDIPSN 2018). L’acide nonanoïque n’est pas un additif alimentaire au Canada, mais son usage est approuvé aux États-Unis et en Europe, ainsi que comme exhausteur de goût synthétique et on a signalé son usage alimentaire, notamment dans les boissons alcoolisées, les produits de boulangerie, les produits laitiers, les produits de viande et les collations (US FDA 2016c; EU Food Flavourings Database [modifiée en 2016], Burdock 2009). Dans le monde, il est présent dans les produits antiparasitaires (EPA 1998).
Au Canada, l’acide oxalique apparaît comme produit de formulation dans différents produits antiparasitaires (communication personnelle, courriels de 2016 de l’Agence de réglementation de la lutte antiparasitaire de Santé Canada au Bureau d’évaluation du risque des substances existantes de Santé Canada, sans référence). L’utilisation d’un composé structurellement similaire à l’acide oxalique α ─ soit l’acide oxalique dihydrate (NE CAS 6153-56-6) ─ pourrait constituer une source d’exposition à l’acide oxalique. Au Canada, l’acide oxalique dihydrate est inscrit comme ingrédient actif de pesticides et il est réglementé par la Loi sur les produits antiparasitaires. On le trouve aussi dans des produits de nettoyage au Canada. On a déclaré que l’acide oxalique était un ingrédient dans la fabrication d’un nombre réduit de matériaux d’emballage alimentaire; par exemple dans les encres utilisées sur la surface extérieure d’emballage alimentaire et de revêtement ou de garniture internes de boîtes de conserve (communication personnelle, courriels de 2017 de la Direction des aliments de santé Canada au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence). Il pourrait aussi être utilisé dans les nettoyants et les détergents à lessives d’installation de transformation des aliments (communication personnelle, courriels de 2016, de la Direction des aliments de Santé Canada au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence). On n’a pas déclaré l’acide oxalique comme additif alimentaire au Canada ou ailleurs. L’acide oxalique figure dans la BDIPSN comme ingrédient médical avec un rôle homéopathique dans les produits de santé naturels homologués comme médicaments homéopathiques. Selon la BDPSNH, il est présent dans un nombre réduit de produits de santé naturels, actuellement homologués comme médicaments homéopathiques (BDIPSN 2018, BDPSNH 2018). On a également déclaré sa présence dans des produits de nettoyage vendus aux consommateurs au Canada, nommément des vaporisateurs tout usage conçus pour traiter la rouille domestique, des solutions de nettoyage des coques de bateau pour éliminer les taches le long de la ligne de flottaison et un nettoyant pour la carène qui retire la ligne de salissure et les taches de rouille (FS 2014a, FS 2014b, FS 2015a, FS 2015b et FS 2015c). Au Canada, les utilisations industrielles de l’acide oxalique comprennent notamment ses utilisations comme solvant et inhibiteur de corrosion dans les produits de nettoyage du métal et des tissus dans les voitures, ainsi que son utilisation dans les peintures et les revêtements (ECCC 2013). À l’échelle mondiale, on utilise l’acide oxalique dans les produits de nettoyage et de lavage, de régulation du pH, de traitement de l’eau, et de traitement des surfaces métallique ou non métallique, comme produit chimique, dans les produits de revêtement et comme substance intermédiaire dans la synthèse d’autres produits chimiques (ECHA c2007-2016).
Le tableau 4‑2 ci-dessous donne un résumé de ces utilisations.
| Utilisation | Acide propionique | Acide butyrique | Acide nonanoïque | Acide oxalique |
|---|---|---|---|---|
| Additif alimentairea | O | N | N | N |
| Matériaux d’emballage alimentaire | O | N | O | O |
| Additif alimentaire indirectb | N | N | O | O |
| Ingrédient médicinal ou non médicinal dans des désinfectants, des produits pharmaceutiques à usage humain ou vétérinairec | N | N | O | N |
| Dans la Base de données sur les ingrédients des produits de santé naturelsd | O | O | O | O |
| Ingrédient médicinal ou non médicinal dans les produits de santé naturels homologués | O | O | N | O |
| Présent dans les cosmétiques, selon les déclarations présentées en vertu du Règlement sur les cosmétiquesf | N | N | O | N |
| Produit de formulation dans les produits antiparasitaires homologuésg | O | O | O | O |
Abréviations : O = Oui, cette utilisation a été déclarée pour cette substance; N = Non, cette utilisation n’a pas été déclarée pour cette substance.
a Communication personnelle, courriels de 2016 de la Direction des aliments de Santé Canada au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence.
b Communication personnelle, courriels de 2016 de la Direction des aliments de Santé Canada au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence.
c Communication personnelle, courriels de 2016 de la Direction des produits thérapeutiques de Santé Canada au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence.
d Communication personnelle, courriels de 2016 de la Direction des produits de santé naturels et sans ordonnance de Santé Canada au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence.
e Communication personnelle, courriels de 2016 de la Direction des produits de santé naturels et sans ordonnance de Santé Canada au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence.
f Communication personnelle, courriels de 2016 de la Direction de la sécurité des produits de consommation de Santé Canada au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence.
g Communication personnelle, courriels de 2016 de l’Agence de de réglementation de la lutte antiparasitaire au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence.
5. Potentiel de causer des effets nocifs pour l’environnement
5.1 Caractérisation des risques pour l’environnement
Nous avons caractérisé les substances du groupe des acides carboxyliques à l’aide de la méthode de Classification du risque écologique des substances organiques (CRE) (ECCC 2016a). La CRE est une méthode basée sur les risques qui tient compte de plusieurs paramètres liés au danger et à l’exposition basés sur la pondération de plusieurs éléments de preuve. Les divers éléments de preuve sont combinés pour distinguer les substances plus ou moins dangereuses et les potentiels d’exposition plus ou moins élevés dans divers milieux. Cette méthode réduit l’incertitude globale de la caractérisation des risques comparativement à une autre qui reposerait sur un seul paramètre dans un seul milieu (la CL50 par exemple). Nous résumons plus bas la méthode. On peut trouver un exposé détaillé dans ECCC (2016a).
Nous avons colligé les données sur les propriétés physico-chimiques, le devenir (demi-vie chimique dans divers milieux et biotes, le coefficient de partition, la bioconcentration dans les poissons), l’écotoxicité aiguë chez le poisson, et les volumes de ces produits importés ou fabriqués au Canada, à partir des publications scientifiques, des bases de données empiriques disponibles (par ex., la boîte à outils RQSA de l’OCDE) et des réponses aux enquêtes menées en vertu de l’article 71 de la Loi. Nous avons produit d’autres données à partir de la relation quantitative structure-activité (RQSA) ou les modèles du devenir du bilan massique ou de la bioaccumulation. Ces données ont été utilisées comme intrants dans d’autres modèles de bilan massique ou pour compléter les profils d’exposition et de danger de la substance.
Les profils de danger ont principalement été déterminés à partir de paramètres liés au mode d’action toxique, à la réactivité chimique, aux seuils de toxicité interne dérivés du réseau trophique, à la biodisponibilité et à l’activité biologique et chimique. Les profils d’exposition ont aussi été dérivés à partir de plusieurs paramètres dont le taux potentiel d’émission, la persistance globale et le potentiel de transport sur de grandes distances. Les profils de danger et d’exposition ont été comparés aux critères de décision afin de catégoriser les potentiels de risque et d’exposition de chaque substance comme faible, moyen ou élevé. Nous avons appliqué d’autres règles (ou constance du classement ou marge d’exposition par exemple) pour raffiner les classements préliminaires du risque et de l’exposition.
Nous avons utilisé une matrice de risques pour attribuer à chaque substance un risque potentiel faible, moyen ou élevé, en se fondant sur les profils de risque et d’exposition. Nous vérifions le classement du risque écologique potentiel donné par la CRE en suivant une approche en deux étapes. La première étape permet d’ajuster les résultats de la classification du risque de modéré ou élevé à faible pour les substances pour lesquelles le taux estimé d’émission dans l’eau après passage par une usine de traitement des eaux usées est faible, ce qui implique un faible potentiel d’exposition. Lors de la deuxième étape, nous avons examiné les profils faibles pour le potentiel de risque au moyen de scénarios de risque relativement prudents, à l’échelle locale (dans la zone à proximité du point de rejet), conçus pour protéger l’environnement pour déterminer si le classement du risque potentiel devrait être haussé.
La CRE utilise une approche pondérée visant à réduire la surestimation ou la sous-estimation possible du classement du danger, de l’exposition ou du risque subséquent. Le lecteur trouvera dans ECCC (2016a) une description détaillée des approches équilibrées pour traiter les incertitudes. Dans ce qui suit, nous décrivons deux des plus importants domaines d’incertitude. Les erreurs dans les valeurs de toxicité aiguë empiriques ou modélisées peuvent modifier les classements du danger, notamment les paramètres reposant sur les valeurs qui dépendent des résidus dans les tissus (le mode d’action toxique), dont plusieurs sont prédites par les modèles QSAR. L’incidence d’une telle erreur est toutefois atténuée par le fait que toute surestimation de la létalité médiane générera une valeur prudente (protectrice) de la valeur utilisée lors de l’analyse des résidus corporels critiques (RCC). De même, toute erreur de sous-estimation de la toxicité aiguë est atténuée par le recours à d’autres paramètres du danger, tels que l’établissement du profil structural du mode d’action, de la réactivité ou de l’affinité pour les récepteurs d’œstrogènes. Les modifications ou les erreurs de quantité de substances chimiques pourraient se traduire par des classifications différentes de l’exposition, les classifications du risque et de l’exposition étant fortement sensibles à la vitesse d’émission et à la quantité utilisée. Les résultats de la CRE reflètent donc l’exposition et le risque au Canada basés sur les quantités actuellement utilisées et pourraient ne pas refléter des tendances futures.
Le lecteur trouvera dans ECCC (2016b) les données critiques et les paramètres utilisés pour produire les profils des quatre substances du groupe des acides carboxyliques et les résultats du classement du danger, de l’exposition et du risque.
Le tableau 5‑1 résume les classements du danger, de l’exposition et du risque des quatre substances du groupe des acides carboxyliques
| Substance | Profil du danger | Profil de l’exposition | Classification du risque écologique |
|---|---|---|---|
| Acide propionique | faible | élevé | faible |
| Acide butyrique | faible | faible | faible |
| Acide nonanoïque | faible | faible | faible |
| Acide oxalique | faible | faible | faible |
D’après les renseignements examinés dans la classification du risque écologique, l’acide propionique présente un potentiel élevé d’exposition étant donné les quantités élevées déclarées et son potentiel de transport sur de grandes distances. Étant donné son faible potentiel de danger, l’acide propionique est catégorisé comme ayant un faible potentiel de risque pour l’environnement. Il est peu probable que l’acide propionique suscite des préoccupations pour l’environnement au Canada, étant donné son profil d’utilisation actuel.
Étant donné les potentiels faibles pour le danger et l’exposition selon les renseignements examinés dans le cadre de la CRE, l’acide butyrique, l’acide nonanoïque et l’acide oxalique sont catégorisés comme ayant un faible potentiel de constituer un risque pour l’environnement. Il est donc peu probable que ces substances suscitent des préoccupations pour l’environnement au Canada.
6. Potentiel de causer des effets nocifs pour la santé humaine
6.1 Acide propionique
6.1.1 Évaluation de l’exposition
Dans la présente sous-section, nous donnons des informations générales sur l’exposition à l’acide propionique. Puisque nous considérons que l’acide propionique possède un faible potentiel de danger (sous-section 6.1.2), nous n’avons pas calculé d’estimation quantitative de l’exposition de la population générale.
Nous n’avons pas répertorié de données canadiennes ou de données internationales récentes sur les concentrations d’acide propionique dans l’air intérieur, l’eau potable ou le sol.
La présence d’acide propionique dans l’air ambiant peut occasionner une exposition par inhalation. McGinn et coll. (2003) ont mesuré la concentration d’acide propionique dans l’air ambiant à proximité de trois installations d’élevage intensif de bétail dans le Sud albertain au Canada. Ils ont observé une baisse de la concentration d’acides volatiles gras totaux, dont l’acide propionique (qui peut être dégagé par le fumier), dans des échantillons prélevés à 100 et 200 m sous le vent depuis des parcs d’engraissement.
Puisqu’au Canada, l’acide propionique et ses sels de sodium et de calcium sont des additifs autorisés dans certains aliments, notamment dans le pain et certains types de fromages, on peut prévoir que des personnes seront exposées à cette substance par voie alimentaire. La teneur en acide propionique peut atteindre un maximum de 2000 ou 3000 ppm (2000 ou 3000 mg/kg) en fonction de la catégorie d’aliment auquel il peut être intégré (Santé Canada 2016). L’acide propionique est aussi utilisé dans la fabrication de certains matériaux d’emballage alimentaire qui ne touchent pas aux aliments. Nous ne prévoyons donc pas d’exposition alimentaire à l’acide propionique par son utilisation dans les matériaux d’emballage alimentaire (communication personnelle, courriels de 2017 de la Direction des aliments de Santé Canada au Bureau d’évaluation des risques des substances existantes de Santé Canada, sans référence).
L’exposition à l’acide propionique par voie orale peut aussi survenir du fait de sa présence comme ingrédient non médicinal dans un produit de santé naturel à base de glucosamine liquide (BDPSNH 2018).
6.1.2 Évaluation des effets sur la santé
L’OCDE (2007) et l’EFSA (2014) ont étudié l’acide propionique et nous avons utilisé leurs résultats pour éclairer la caractérisation de ses effets sur la santé. Nous avons réalisé une recherche dans les publications scientifiques pour la période s’étendant de janvier 2006 à octobre 2016 et n’avons répertorié aucune étude qui aurait pu entraîner une caractérisation des effets sur la santé différente de celle des évaluations de l’OCDE (2007) et de l’EFSA (2014).
L’acide propionique se trouve naturellement dans le corps humain. Il est un métabolite intermédiaire normal et constitue 4 % du total des acides gras normaux du plasma (OCDE 2007).
Toxicité à dose répétée
L’OCDE et EFSA ont toutes deux conclu que le seul effet nocif signalé de l’exposition à l’acide propionique avait été observé au point de contact et résultait de ses propriétés irritantes, et qu’aucune toxicité systémique n’avait été relevée lors d’études à doses répétées.
L’OCDE a recensé différentes études de toxicité à doses répétées. Dans l’une d’elles, des chiens mâles et femelles ont reçu des doses allant jusqu’à 3 % (environ 1800 mg/kg p.c./jour) d’acide propionique dans leur alimentation pendant 100 jours. On n’a détecté ni mortalité ni signe clinique de toxicité. Trois animaux ayant reçu de fortes doses ont montré des effets au point de contact qui incluaient l’hyperplasie épithéliale diffuse de la muqueuse œsophagienne. L’incidence des lésions de l’œsophage chez les animaux ayant reçu une forte dose était, après une période de récupération de six semaines, similaire à celle observée chez les témoins (BASF 1988, cité par OCDE 2007).
Lors d’une autre étude d’administration répétée d’une dose orale, des rats Sprague-Dawley mâles et femelles ont reçu une dose de 3300 mg/kg p.c./jour environ d’acide propionique en poudre pendant 91 jours. On n’a observé aucune mortalité. Les mâles du groupe ayant reçu de fortes doses ont montré une baisse de gain de poids corporel. On n’a observé aucun autre signe clinique de toxicité. On a toutefois observé des effets au point de contact, soit l’épithélium de la muqueuse du préestomac des rats du groupe ayant reçu une forte dose. Ces changements n’ont toutefois pas été observés après une période de récupération de six semaines (BASF AG 1971, cité par OCDE 2007).
D’autres études sur l’alimentation des rats s’étendant sur une période de 28 jours à toute leur vie ont été répertoriées. Ces études se sont uniquement intéressées aux effets sur le point de contact du préestomac. Le résultat de ces études a varié en fonction du type d’alimentation (en granule ou en poudre), mais était cohérent avec les effets au point de contact signalés par d’autres études.
Cancérogénicité
L’OCDE (2007) a répertorié une étude d’alimentation pendant toute la vie de rats mâles ayant reçu des doses d’acide propionique allant jusqu’à 4 % (environ 2700 mg/kg p.c./jour). Se fondant sur cette étude, l’OCDE a conclu que l’on ne pouvait prédire que l’acide propionique avait un potentiel cancérogène sur le point de contact (préestomac). Les changements observés lors de l’administration de fortes doses d’acide propionique résultent de l’irritation et de l’inflammation chroniques et de la réaction de réparation proliférative hyperplasique.
L’EFSA (2014) a également conclu que l’acide propionique n’était pas préoccupant du point de vue de la cancérogénicité.
Génotoxicité
Les essais in vitro et in vivo avec de l’acide propionique ont donné des résultats négatifs. L’OCDE (2007) et l’EFSA (2014) ont donc conclu que l’acide propionique n’était pas préoccupant du point de vue de la génotoxicité.
Toxicité pour la reproduction et le développement
Nous n’avons répertorié aucune étude sur la reproduction relative à la toxicité de l’acide propionique sur la reproduction et le développement. Toutefois, une étude d’alimentation durant 100 jours pendant laquelle des chiens reçurent jusqu’à 1800 mg/kg p.c./jour d’acide propionique n’a montré aucune preuve de toxicité pour les organes reproducteurs mâle ou femelle (OCDE 2007).
L’OCDE a aussi recensé une étude remontant à 1971 dans le cadre de laquelle des rats Sprague-Dawley mâles et femelles reçurent dans leur alimentation quotidienne jusqu’à 500 000 ppm d’acide propionique (ou 5 % de leur diète). Or, on n’a observé aucun effet sur les organes reproducteurs mâle ou femelle (OCDE 2007).
Aucune étude des effets de l’acide propionique sur le développement n’a été répertoriée. L’OCDE et l’EFSA ont toutefois considéré les résultats d’une étude sur le dipropanoate de calcium. L’étude a montré l’absence d’effet sur la taille ou la viabilité des portées ou de hausse d’anormalité fœtale chez les souris femelles ou les rates ayant reçu pendant leur gestation des doses de dipropanoate de calcium allant jusqu’à 300 mg/kg p.c./jour, et chez les hamsters femelles et les lapines ayant reçu des doses allant jusqu’à 400 mg/kg pc.c./jour (OCDE 2007, EFSA 2014).
6.1.3 Caractérisation des risques pour la santé humaine
Lors de sa 49e réunion (OMS 1998), le Comité mixte OAA/OMS d’experts sur les additifs alimentaires (JECFA) a évalué un groupe aromatisants formé d’alcools primaires, d’aldéhydes et d’acides saturés, aliphatiques, acycliques et linéaires, comprenant l’acide propionique. Il a conclu que l’on pouvait prédire qu’après leur ingestion, les substances de ce groupe d’aromatisants sont complètement métabolisées en produits endogènes, par les voies des acides gras et de l’acide tricarboxylique. Puisque les concentrations endogènes de métabolites de ces substances ne provoqueraient pas de perturbation dépassant l’intervalle physiologique normal, le JECFA a conclu que leur utilisation comme agent aromatisant ne serait pas préoccupante pour la santé. Lors de ses délibérations, le JECFA a aussi maintenu la cote « non limitée » pour la dose journalière admissible (DJA) que l’on avait antérieurement attribuée à l’acide propionique et ses sels de sodium, potassium et calcium pour son utilisation comme additif alimentaire.
En 2014, l’Autorité européenne de sécurité des aliments (EFSA) a réévalué la sécurité de l’acide propionique et de ses sels qui sont des additifs alimentaires homologués aux États-Unis. Le comité de l’EFSA a conclu que l’emploi de l’acide propionique et de ses sels comme additif alimentaire était la source principale d’exposition par voie alimentaire, mais que son emploi jusqu’aux concentrations maximales autorisées aux États-Unis (jusqu’à 3000 ppm) ne suscitait pas de préoccupation sur le plan de la sécurité. À l’instar du JECFA, l’EFSA a attribué la cote « non spécifiée » pour la dose journalière admissible des substances du groupe à l’acide propionique et ses sels.
L’OCDE (2007) et l’EFSA (2014) ont conclu qu’aucune toxicité systémique n’avait été observée chez les animaux après une exposition à l’acide propionique en doses répétées (les essais comportaient des doses aussi élevées que 3300 mg/kg p.c./jour). Ces deux organismes ont conclu que l’on ne pouvait pas prédire que l’acide propionique aurait un potentiel cancérogène ou génotoxique. Ils n’ont pas relevé d’observation lors d’études à doses répétées d’effets négatifs sur les organes reproducteurs ou le développement de diverses espèces. En outre, l’acide propionique existe naturellement dans le corps humain, comme métabolite intermédiaire normal et constitue jusqu’à 4 % des acides gras totaux normaux du plasma. Nous considérons donc que l’acide propionique a un faible potentiel de dangerosité.
Puisque l’on estime que l’acide propionique a un faible potentiel de dangerosité, nous considérons que l’estimation de l’exposition aux sources et des utilisations mentionnées dans la partie 4 n’est pas pertinente, et que le risque pour la santé humaine est faible.
6.2 Acide n-butyrique
6.2.1 Évaluation de l’exposition
Dans la présente section, nous donnons des renseignements généraux sur l’exposition à l’acide n‑butyrique. Comme nous considérons que l’acide n‑butyrique présente un faible potentiel de danger (section 6.2.2), nous n’avons pas estimé quantitativement l’exposition de la population générale.
La présence d’acide n‑butyrique dans l’air ambiant peut occasionner une exposition par inhalation. McGinn, Janzen et Coates (2003) ont mesuré des concentrations d’acide n‑butyrique ainsi que d’acide propionique (provenant du fumier) dans l’air ambiant à proximité des exploitations d’élevage intensif dans le sud de l’Alberta, au Canada. Ils ont détecté de l’acide n‑butyrique dans l’air extérieur avoisinant les parcs d’engraissement de bovins et ont remarqué que les concentrations totales des acides gras volatils diminuaient à mesure que l’on s’éloigne des installations.
Nous n’avons répertorié aucune donnée canadienne ou donnée récente d’autres pays sur les concentrations d’acide n‑butyrique dans l’air intérieur, l’eau potable ou le sol.
L’exposition par voie alimentaire à l’acide n‑butyrique peut être attribuable à son utilisation comme ingrédient ajoutant de la saveur dans les concentrés aromatisants au Canada (ECCC, 2017). En outre, l’exposition à l’acide n‑butyrique par voie orale peut aussi survenir en raison de sa présence comme ingrédient non médicinal dans un petit nombre de produits de santé naturels au Canada (BDPSNH, 2018).
6.2.2 Évaluation des effets sur la santé
L’OCDE a étudié l’acide n‑butyrique (2003), et nous nous sommes servis des résultats pour éclairer la caractérisation de ses effets sur la santé.
Nous avons effectué une recherche dans les études publiées entre janvier 2002 et octobre 2016, mais aucune étude n’a révélé d’effets sur la santé, différents de ceux de l’évaluation de l’OCDE (2003).
L’OCDE a évalué ensemble l’acide n‑butyrique et l’anhydride butyrique, car ces deux substances sont étroitement apparentées. L’anhydride s’hydrolyse rapidement en présence d’eau pour donner l’acide, et ces substances partagent un caractère toxique. L’OCDE a aussi utilisé les données sur le n‑butanol et l’acétate de butyle pour déterminer les dangers associés à une exposition générale à l’acide n‑butyrique, puisque l’acétate de butyle et le n‑butanol sont des précurseurs métaboliques de l’acide n‑butyrique.
L’acide n‑butyrique est produit métaboliquement au cours de la fermentation de matières végétales comme la cellulose, les fibres, l’amidon et les glucides. Les animaux herbivores en fabriquent de grandes quantités, mais aussi les humains, bien qu’en moindre quantité, au cours de la fermentation microbienne qui a lieu dans le tractus gastro-intestinal (Bergman, 1990, cité par OCDE, 2003).
Toxicité des doses répétées
L’OCDE a repéré plusieurs études menées avec des doses répétées. Dans une étude sur l’inhalation, des rats Sprague-Dawley mâles et femelles ont été exposés à des concentrations d’acétate de butyle de 0, 500, 1500 ou 3000 ppm (environ 0, 2376, 7128 ou 14256 mg/m3), à raison de 6 heures par jour, 5 jours par semaine pendant 13 semaines. Les effets généraux comprenaient une baisse du poids corporel et une diminution de la consommation de nourriture, une augmentation du poids des testicules, une augmentation du poids des glandes surrénales et des signes d’une nécrose localisée de l’épithélium olfactif, effets que l’on a observés à la dose moyenne et à la dose élevée. On a aussi constaté une narcose minime et des effets de sédation chez les rats du groupe ayant reçu la dose moyenne et chez ceux du groupe ayant reçu la dose élevée. En outre, on a relevé une diminution du poids de la rate et une augmentation du poids des poumons dans le groupe ayant reçu la dose élevée (David et. coll., 2001).
L’OCDE souligne qu’une dégénérescence de l’épithélium olfactif a été observée à la suite de l’exposition à des concentrations supérieures à 1500 ppm (7128 mg/m3). On estime qu’il s’agit là d’une lésion courante chez les rats exposés à des acétates d’alcool, lésion qui serait attribuable à la libération d’acide acétique par ces cellules à la suite de l’hydrolyse du lien ester. Comme les rats respirent strictement par le museau, la dose administrée à cette partie de l’organisme est plus grande chez les rats que chez l’humain. La pertinence de cette lésion pour la santé humaine est donc discutable.
Dans une étude antérieure réalisée par le même auteur et avec le même plan d’étude, les rats présentaient des effets sur le système nerveux central (activité réduite) au cours de l’exposition, mais ils se sont rétablis rapidement après que l’exposition ait cessé (David et. coll., 1998, cité par OCDE, 2003). L’OCDE a aussi répertorié une étude par voie orale d’une durée de 13 semaines menée chez le rat avec des doses de n‑butanol pouvant aller jusqu’à 500 mg/kg p.c./jour administrées par gavage, dans laquelle on a fait état d’une DSENO de 125 mg/kg/jour et d’une DNENO de 500 mg/kg p.c./jour, d’après l’ataxie transitoire post-dose et l’hypoactivité (Tox. Res. Lab., 1986, cité par OCDE, 2003). Comme ils étaient temporaires, ces effets n’ont donc pas été considérés comme étant de véritables effets nocifs.
Cancérogénicité
L’OCDE (2003) n’a relevé aucune donnée sur la cancérogénicité de la substance, et les publications depuis 2003 ne font état d’aucun effet cancérogène.
Génotoxicité
L’acide n‑butyrique n’était pas mutagène dans l’essai d’Ames avec ou sans activation métabolique. Par ailleurs, on n’a observé aucun effet mutagène sur les cellules de poumon de hamster chinois en culture. Dans un essai in vivo, on a exposé des souris NMRL mâles et femelles au n‑butanol par gavage à des concentrations pouvant atteindre 2000 mg/kg. Aucune lésion chromosomique et aucun signe d’altération de la distribution des chromosomes au cours de la mitose (aucun effet perturbateur sur le fuseau mitotique) n’ont été observés (OCDE, 2003).
Toxicité pour la reproduction et le développement
L’OCDE a repéré plusieurs études faisant état d’une toxicité pour la reproduction. Dans l’une de ces études, des rats femelles Sprague‑Dawley ont été exposées par inhalation à des concentrations de n‑butanol pouvant atteindre 6000 ppm (environ 18192 mg/m3) pendant 7 heures par jour, du jour 1 au jour 20 de la gestation. Aucun effet détectable sur le taux de gestation n’a été observé. Dans une autre étude menée par le même auteur, des rats mâles ont reçu de l’acétate de butyle par inhalation à des concentrations allant jusqu’à 3 000 ppm (environ 14256 mg/m3), pendant 6 heures par jour et durant 14 semaines. On n’a relevé aucun signe de toxicité dans les testicules (Nelson et. coll., 1989a, cité par OCDE, 2003).
L’OCDE (2003) a recensé deux études examinant les effets sur le développement du n‑butanol. Dans l’une des études, on a administré à des rates Sprague‑Dawley gravides du n‑butanol par inhalation à des concentrations de 0, 3500, 6000 ou 8000 ppm (environ 0, 10612, 18192, 24256 mg/m3) durant 7 heures par jour, du jour 1 au jour 19 de la gestation. On a noté des effets chez les mères, comme une consommation moindre de nourriture, dans les groupes ayant reçu 6000 et 8000 ppm, ainsi qu’une narcose et une mortalité uniquement dans le groupe ayant reçu 8000 ppm. Une légère diminution du poids des fœtus a été observée dans les groupes ayant reçu 6000 et 8000 ppm. La DSENO calculée par l’auteur d’après les effets sur les mères et les fœtus était de 3500 ppm (10612 mg/m3) (Nelson et. coll., 1989b, cité par OCDE, 2003). Dans une étude sur la neurotoxicité pour le développement, des rats mâles et femelles ont été exposés par inhalation à des concentrations de n‑butanol pouvant atteindre 6000 ppm (environ 18192 mg/m3). Les mâles ont été exposés pendant six semaines avant l’accouplement avec des femelles non exposées, et les femelles ont reçu la substance uniquement du jour 1 au jour 20 de la gestation durant trois semaines. L’auteur a déterminé que la DSENO associée à une neurotoxicité pour le développement était la dose la plus élevée étudiée (6000 ppm ou 18192 mg/m3) autant pour les rats mâles que les rats femelles (Nelson et. coll., 1989a, cité par OCDE, 2003).
Les résultats des études menées avec l’acétate de butyle chez le rat et le lapin ont aussi tenu lieu de données justificatives pour l’acide n‑butyrique. Aucun effet sur le développement n’a été constaté au cours de ces études (Hackett et. coll., 1982, cité par OCDE, 2003).
6.2.3 Caractérisation des risques pour la santé humaine
Le JECFA a évalué un groupe d’aromatisants, dont l’acide n‑butyrique (OMS 1998). Le comité a conclu qu’il était possible de prédire que les substances de ce groupe d’aromatisants (notamment l’acide n‑butyrique) subissent une métabolisation complète après ingestion pour donner des produits endogènes, par les voies métaboliques des acides gras et de l’acide tricarboxylique. Comme la concentration endogène des métabolites de ces substances ne donne pas lieu à des perturbations physiologiques, le JECFA a conclu que leur utilisation comme agent aromatisant dans les aliments ne soulève aucune préoccupation de sécurité.
D’après les données existantes sur les précurseurs de l’acide n‑butyrique (n‑butanol et acétate de butyle), on ne s’attend pas à ce que l’acide n‑butyrique ait un potentiel cancérogène ou génotoxique et entraîne des effets pour la reproduction ou le développement. Des effets généraux comme l’augmentation du poids des testicules et des glandes surrénales ont été observés chez des animaux d’expérience à la suite d’une exposition répétée par inhalation d’une durée de 13 semaines à l’acide n‑butyrique, mais uniquement aux doses élevées pouvant atteindre 7128 ou 14256 mg/m3 (environ 2210 ou 4420 mg/kg‑p.c./jour, respectivement), doses qui sont considérées non pertinentes compte tenu des niveaux d’exposition possibles pour l’humain, et du fait que l’inhalation ne devrait pas être la principale voie d’exposition à l’acide n‑butyrique étant donné son profil d’utilisation dans la population générale. En outre, dans une étude réalisée avec des doses répétées administrées par voie orale, on n’a constaté que des effets transitoires à la dose la plus élevée étudiée. C’est pourquoi l’acide n‑butyrique est considéré comme ayant un faible potentiel de danger.
Puisqu’on estime que le potentiel de danger de l’acide n‑butyrique est faible, nous avons jugé qu’il n’était pas nécessaire de calculer des estimations de l’exposition aux sources et découlant des usages mentionnés à la section 4, et que le risque pour la santé humaine est faible.
6.3 Acide nonanoïque
6.3.1 Évaluation de l’exposition
La présente section contient des renseignements généraux sur l’exposition à l’acide nonanoïque. Puisque nous considérons que l’acide nonanoïque possède un faible potentiel de danger (section 6.3.2), nous n’avons pas calculé d’estimations quantitatives de l’exposition de la population générale.
Il n’existe aucune donnée canadienne ni donnée récente d’autres pays sur la concentration de l’acide nonanoïque dans l’air ambiant, l’air intérieur ou l’eau potable, mais il est possible d’être exposé à cette substance par inhalation ou accidentellement par voie orale en raison de sa présence naturelle dans le sol et l’air ambiant (Rogge et coll., 1993; ECHA, 2013). Selon un rapport du Conseil national de recherche du Canada de 2011, l’acide nonanoïque est présent dans la poussière domestique. Les concentrations d’acide nonanoïque dans les échantillons de poussière se situaient entre 0,67 et 654,93 μg/g de poussière (n = 37), et la moyenne arithmétique était de 36,83 μg/g de poussière.
Bien qu’il n’y ait aucun renseignement définitif sur l’utilisation de l’acide nonanoïque comme aromatisant alimentaire au Canada, il est possible que la substance soit présente comme agent aromatisant dans des aliments vendus au Canada étant donné l’utilisation de cette substance comme agent aromatisant synthétique dans les aliments aux États‑Unis et en Europe, et qu’elle entraîne une exposition par voie alimentaire. Au Canada, cet acide est utilisé comme ingrédient dans des désinfectants utilisés dans les établissements de transformation des aliments. Toutefois, l’exposition alimentaire, le cas échéant, par cette utilisation devrait être négligeable (communication personnelle, courriels de la Direction des aliments de Santé Canada adressés au Bureau d’évaluation du risque des substances existantes de Santé Canada, janvier 2017; sans référence).
Puisque l’acide nonanoïque est un ingrédient de quelques cosmétiques et produits de consommation au Canada, cette présence pourrait entraîner une exposition par voie cutanée. On a signalé qu’un produit de maquillage non permanent et non huileux pour les yeux contenait de l’acide nonanoïque (communication personnelle, courriels de la Direction de la sécurité des produits de consommation de Santé Canada adressés au Bureau de l’évaluation des risques des substances existantes de Santé Canada, janvier 2016; sans référence). Selon les déclarations, la substance est aussi présente à de faibles concentrations dans une solution désinfectante prête à l’usage utilisée pour désinfecter et assainir des surfaces (FS, 2011; TDS, 2011; communication personnelle, courriels de la Direction des produits thérapeutiques de Santé Canada au Bureau de l’évaluation des risques des substances existantes de Santé Canada, mars 2016).
6.3.2 Évaluation des effets sur la santé
L’ECHA (2013) a étudié l’acide nonanoïque à l’échelle internationale, et nous avons utilisé les résultats de cet examen pour éclairer la caractérisation des effets de cet acide sur la santé. Nous avons réalisé une recension des écrits publiés entre janvier 2012 et octobre 2016, mais n’avons trouvé aucune étude faisant état d’effets sur la santé, différents de ceux de l’examen de l’ECHA (2013).
Toxicité des doses répétées
Plusieurs études sur la toxicité de doses répétées ont été répertoriées. Dans une étude menée par voie orale d’une durée de 28 jours, des rats Wistar mâles et femelles ont reçu par gavage des concentrations de 0, 50, 150 ou 1000 mg par kg p.c./jour d’acide nonanoïque dans le propylène glycol à 0, 1, 3 ou 20 %. On a observé une hyperplasie légère à marquée de l’épithélium squameux du préestomac dans le groupe ayant reçu la dose élevée uniquement. Les calculs ont donné une CSENO de 150 mg/kg p.c./jour. Toutefois, l’ECHA a indiqué que cet effet était vraisemblablement associé à une irritation locale plutôt qu’à une action générale de la substance (ECHA, 2013).
En outre, l’ECHA a relevé plusieurs études répétées faisant appel à des triglycérides à chaîne moyenne lui permettant d’étayer davantage sa conclusion selon laquelle il n’y a aucun effet toxicologique pertinent induit par les doses très élevées dans les études menées avec des doses répétées d’acide nonanoïque administrées par voie orale (ECHA, 2013). Selon l’ECHA, il n’était pas nécessaire d’effectuer d’autres études compte tenu des facteurs suivants : omniprésence de l’acide nonanoïque et d’autres acides gras similaires dans la nature, connaissance des voies métaboliques (catabolisme complet pour un apport énergétique ou une transformation en acides gras destinés au stockage), qui sont semblables pour tous les acides gras et absence d’effets généraux dans les études répétées existantes.
Cancérogénicité
L’acide nonanoïque a été l’objet d’un bioessai évaluant la cancérogénicité par voie cutanée chez la souris. On a appliqué de l’acide nonanoïque sur la peau rasée du dos de souris mâles C3H/HeJ à des doses de 25 ou 50 mg, à raison de deux fois par semaine durant 80 semaines. Les groupes témoins étaient les suivants : un groupe non traité, un groupe de témoins négatifs traités avec 50 mg d’huile minérale et un groupe de témoins positifs traités avec 0,05 % de benzo(α)pyrène dissous dans l’huile minérale. On n’a relevé aucun signe de tumeur cutanée macroscopique chez les souris traitées avec de l’acide nonanoïque et dans les deux groupes de témoins négatifs. Des lésions cutanées non néoplasiques ont été observées dans le groupe ayant reçu la substance, et ces lésions y étaient aussi nombreuses que dans les groupes de témoins négatifs (ECHA, 2013).
Aucune étude de cancérogénicité par voie orale n’a été recensée. Toutefois, l’ECHA (2013) souligne que l’hyperplasie de l’épithélium squameux du préestomac observée dans l’étude menée par gavage et d’une durée de 28 jours susmentionnée n’est pas jugée pertinente dans l’évaluation des risques de cancer chez l’humain. Cette conclusion est étayée par l’absence d’effets génotoxiques et par les connaissances dont nous disposons sur la cinétique et le métabolisme des acides gras (ECHA, 2013).
Génotoxicité
L’acide nonanoïque a donné un résultat négatif dans les essais de mutation sur bactéries, avec ou sans activation métabolique. Les essais de mutation génétique, d’aberration chromosomique et des micronoyaux chez la souris in vivo (ECHA, 2013) ont tous abouti à des résultats négatifs.
Toxicité pour la reproduction et le développement
Aucune étude sur la reproduction n’a été recensée pour l’acide nonanoïque. Cependant, les études réalisées avec des triglycérides à chaîne moyenne n’indiquent aucun effet sur la fertilité des rats ayant reçu jusqu’à 8000 mg/kg p.c./jour (ECHA, 2013).
Dans une étude sur la toxicité pour le développement, des rates CD gravides ont reçu des concentrations de 0 et de 1500 mg/kg p.c./jour d’acide nonanoïque dans l’huile de maïs, administrées par intubation orale, du jour 6 au jour 15 de la gestation. On n’a constaté aucun effet chez les mères ni pour le développement (ECHA, 2013).
6.3.3 Caractérisation des risques pour la santé humaine
Le JECFA (1997) a évalué un groupe d’aromatisants, dont l’acide nonanoïque. Le comité a conclu qu’on peut prédire que les substances de ce groupe d’aromatisants (notamment l’acide nonanoïque) subissent une métabolisation complète après ingestion pour donner des produits endogènes, par les voies métaboliques des acides gras et de l’acide tricarboxylique. Comme la concentration endogène des métabolites de ces substances ne donne pas lieu à des perturbations physiologiques, le JECFA a conclu que leur utilisation comme agent aromatisant dans les aliments ne soulève aucune préoccupation de sécurité.
Selon les conclusions de l’ECHA (2013), aucune toxicité générale n’a été observée chez les animaux d’expérience après l’exposition à des doses répétées pouvant atteindre 1000 mg/kg p.c./jour d’acide nonanoïque. On estime que la substance ne présente aucun potentiel cancérogène ou génotoxique. Aucune étude sur la reproduction n’a été recensée. Toutefois, des études réalisées avec des triglycérides à chaîne moyenne n’indiquent aucun effet sur la fertilité des rats ayant reçu jusqu’à 8000 mg/kg p.c./jour, et on n’a noté aucun signe d’effets sur le développement dans une étude chez le rat. L’ECHA (2013) a conclu que les connaissances sur les voies métaboliques des acides gras en général, soit le catabolisme complet à des fins d’approvisionnement énergétique ou de transformation en acides gras destinés au stockage, sont cohérentes avec la prévision selon laquelle il ne devrait y avoir aucun effet général observé dans les études répétées, même à doses très élevées. C’est pourquoi nous considérons que l’acide nonanoïque présente un faible potentiel de danger.
Puisqu’on estime que le potentiel de danger de l’acide nonanoïque est faible, nous avons jugé qu’il n’était pas nécessaire de calculer des estimations de l’exposition aux sources et découlant des usages mentionnés à la section 4, et que le risque pour la santé humaine est faible.
6.4 Acide oxalique
6.4.1 Évaluation de l’exposition
Milieux naturels et aliments
Nous n’avons recensé aucune donnée canadienne ou donnée récente d’autres pays sur la présence d’acide oxalique dans le sol, la poussière ou l’eau. Dans une étude sur l’acide oxalique et les émissions produites par les véhicules, Huang et Yu (2007) ont répertorié plusieurs concentrations d’acide oxalique en aérosol mesurées dans différents pays, et l’acide oxalique a été détecté dans les PM0,7-2,5 ou les particules totales en suspension. Les concentrations d’acide oxalique en aérosol variaient d’une valeur inférieure à 0,004 (Allemagne) à 0,78 μg/m3 (partie ouest de Los Angeles, États‑Unis).
Compte tenu des propriétés physicochimiques (solubilité élevée dans l’eau) et des utilisations de l’acide oxalique (produits de nettoyage vendus aux consommateurs), les rejets dans l’eau pourraient être une source d’exposition. Cependant, les concentrations potentielles dans l’eau devraient être faibles, car la substance se biodégrade facilement dans l’eau (ECHA, 2017).
À la lumière des données sur les concentrations d’acide oxalique dans les milieux naturels, l’exposition indirecte de la population générale à l’acide oxalique présent dans les milieux naturels au Canada devrait être minime.
Nous n’avons repéré aucune utilisation de l’acide oxalique comme additif ou aromatisant alimentaire, mais on a signalé la présence naturelle de cette substance dans divers aliments comme les noix, les fruits, les légumes, les céréales et les légumineuses (Tang et. coll., 2008), à des concentrations plus élevées que dans les graines et les plantes à feuilles apparentées à l’épinard et à la rhubarbe (Holmes et Kennedy, 2000). Chez les végétaux et les animaux, dans des conditions physiologiques, l’acide oxalique existe sous forme d’oxalate, qui est son anion. La teneur en oxalate des aliments varie considérablement, même pour un même aliment (Holmes et Kennedy, 2000), en raison de facteurs tels que la variété végétale, le développement de la plante, la saison et les conditions de croissance (Libert et Franceschi, 1987, cité par Holmes et Kennedy, 2000). Dans un rapport sur l’absorption d’oxalate, Taylor et Curhan (2007) ont mené une étude prospective sur trois cohortes d’envergure : la Health Professionals Follow-up Study (HPFS, n = 45 985 hommes) et la Nurses’ Health Studies (NHS) I (n = 92 872) et II (n = 101 824). Dans cette étude au cours de laquelle on a administré tous les quatre ans des questionnaires sur la fréquence de la consommation d’aliments durant 44 années (période de suivi), l’estimation de l’absorption moyenne d’oxalate chez les hommes (HPFS), chez les femmes âgées (NHS I) et chez les jeunes femmes (NHS II) était de 214, 185 et 183 mg/jour, respectivement.
Au Canada, l’acide oxalique est utilisé dans la fabrication de certaines matières d’emballage alimentaire (p. ex. encres appliquées à l’extérieur des emballages alimentaires et revêtements intérieurs de boîtes de conserve). Il peut aussi entrer dans la composition de nettoyants et de détergents à lessive employés dans les établissements de transformation d’aliments. La contribution de toutes ces utilisations devrait être négligeable par rapport à l’exposition naturelle découlant de la consommation d’aliments et des concentrations d’acide oxalique endogène (communication personnelle, courriels de la Direction des aliments de Santé Canada au Bureau de l’évaluation des risques des substances existantes de Santé Canada, 2016; sans référence).
Produits disponibles aux consommateurs
De l’acide oxalique a été décelé dans un détachant tout usage pour la rouille en vaporisation, destiné à éliminer les taches de rouille domestiques et dans un nettoyant abrasif en poudre (FS, 2015a; FS, 2015b). On a aussi déclaré sa présence dans des solutions nettoyantes pour la coque des bateaux visant à éliminer les taches causées par la ligne de flottaison ainsi que dans des nettoyants destinés à nettoyer le fond des bateaux pour éliminer l’écume et les taches de rouille (FS, 2014a; FS, 2014b; FS, 2015c).
L’estimation la plus élevée de l’exposition par voie cutanée à l’acide oxalique découlant de l’utilisation de produits de consommation est associée à l’utilisation de solutions de nettoyage pour coques de bateau. On a estimé l’exposition cutanée découlant de cette utilisation en présumant que toute la surface de la main serait exposée au produit (application de la solution à l’aide d’une éponge ou d’un linge). L’exposition par voie cutanée attribuable à cette utilisation a été estimée à 1,09 mg/kg p.c., pour une concentration d’acide oxalique de 8 % dans le produit (FS, 2014a). On n’a pas examiné l’exposition par inhalation découlant de cet usage, car le produit est généralement appliqué à l’extérieur. L’exposition par inhalation à l’acide oxalique associée à la vaporisation d’un nettoyant antirouille tout usage sur une surface à nettoyer (FS, 2015a) a été estimée à l’aide de ConsExpo Web (ConsExpo Web, 2016). En présumant que ce produit contient 10 % d’acide oxalique (FS, 2015c), on estime que l’exposition par inhalation est de 0,033 mg/m3, ce qui équivaut à une exposition générale de 0,00028 mg/kg p.c./jour. Le lecteur trouvera le détail du calcul lié à ces scénarios d’exposition à l’annexe A.
Les usages d’un composé ayant une structure semblable, soit l’acide oxalique dihydraté (NE CAS 6153‑56‑6), peuvent aussi occasionner une exposition à l’acide oxalique. Ce composé dihydraté est présent dans les produits de nettoyage vendus aux consommateurs, notamment des nettoyants pour terrasses, des produits de polissage et des nettoyants de cuvette. L’exposition à l’acide oxalique découlant de l’utilisation de produits contenant de l’acide oxalique dihydraté serait inférieure ou équivalente à celle découlant de l’utilisation des produits contenant de l’acide oxalique décrits précédemment.
6.4.2 Évaluation des effets sur la santé
Toxicité des doses répétées
Dans une étude par voie orale réalisée à long terme, des rats Osborne‑Mendel mâles et femelles ont reçu de l’acide oxalique à la concentration de 0, 0,1, 0,5, 0,8 ou 1,2 % dans leur alimentation durant deux ans. Aucun effet nocif important n’a été observé à la dose la plus élevée étudiée (Fitzhugh et Nelson, 1947).
On a signalé des effets nocifs de l’acide oxalique chez l’humain, par exemple la formation de calculs rénaux d’oxalate de calcium chez les personnes consommant beaucoup d’aliments riches en oxalate comme les épinards, la rhubarbe ou le persil, et peu de produits laitiers contenant du calcium (Hodgkinson et Zarembski, 1968).
Génotoxicité
L’acide oxalique a donné un résultat négatif à l’essai d’Ames (Rossman et. coll., 1991), et l’essai d’aberration chromosomique sur fibroblastes de poumon de hamster chinois (V79) (Ishidate Jr. et. coll., 1984). On n’a recensé aucune étude sur la génotoxicité in vivo.
Toxicité pour la reproduction et le développement
Le National Toxicology Program des États‑Unis (NTP US) a réalisé une étude sur les effets de l’acide oxalique sur la reproduction et la fertilité des souris. Les souris mâles et femelles ont été jumelées aléatoirement et exposées à l’acide oxalique présent dans l’eau potable à une concentration de 0, 0,05, 0,1 ou 0,2 % (environ 100, 200 ou 400 mg/kg p.c./jour). Les souris sont restées en couple pendant 98 jours, puis ont été séparées durant 21 jours, période au cours de laquelle les petits sont nés. Dans les groupes ayant reçu les doses de 0,05 et 0,1 %, on n’a observé aucun effet important (p > 0,05) sur le nombre de petits vivants par portée, le ratio des sexes et le poids moyen des petits vivants. Dans le groupe ayant reçu une concentration de 0,2 % d’acide oxalique dans l’eau potable, on a constaté une réduction importante (p < 0,05) du nombre de portées par couple fertile et une diminution du poids moyen des petits (corrigé en fonction de la taille de la portée).
On a effectué une évaluation plus approfondie de l’efficacité de la reproduction chez les petits du groupe témoin et du groupe ayant reçu la dose élevée. Le groupe A comprenait 20 couples témoins et le groupe B, 20 couples ayant reçu la dose élevée (0,2 %). Après une période de cohabitation de sept jours, les couples ont été séparés et les femelles ont donné naissance à leurs petits. Le nombre total de petits vivants et le nombre de petits femelles vivants issus de la deuxième génération de couples étaient considérablement plus faibles (p < 0,05) par rapport au groupe témoin correspondant.
La prostate des animaux adultes ayant reçu 0,2 % d’acide oxalique était plus petite, comme l’indique la diminution importante du poids absolu et du poids corrigé mesurés lors de la nécropsie. Pour les souris de la deuxième génération, le poids corrigé des reins des souris femelles et le poids absolu des reins des souris mâles avaient considérablement augmenté (p < 0,05).
D’après des études sur la morphologie des spermatozoïdes et la cytologie vaginale, le traitement prolongé par l’acide oxalique peut avoir des effets sur la fréquence relative des périodes de chaleur, comme l’indiquent les données sur la première génération de souris. Les spermatozoïdes anormaux étaient plus fréquents dans la deuxième génération de souris ayant reçu 0,2 % d’acide oxalique dans l’eau potable. Comme on a observé une augmentation du pourcentage de spermatozoïdes anormaux à la fois chez les animaux de la deuxième génération et les souris adultes traitées, il est possible que l’acide oxalique interfère avec la spermiogenèse. Le National Toxocology Program a conclu que l’administration d’acide oxalique dans l’eau potable à des concentrations pouvant atteindre 0,1 % n’a aucun effet sur la fertilité chez les souris CD‑1 adultes ou de deuxième génération (NTP, 1985). Par conséquent, on a établi une DSENO de 0,1 % d’acide oxalique dans l’eau potable (ou 200 mg/kg p.c./jour) d’après la fréquence des effets sur la reproduction attribuable à la concentration de 0,2 % d’acide oxalique.
Dans une étude sur le développement mené avec l’acide oxalique administré par voie orale, des lapins femelles ont reçu des concentrations de 0, 2,5, 12, 54 et 250 mg/kg p.c./jour par gavage, du jour 6 au jour 18 de la gestation. On n’a relevé aucun effet sur le développement à la dose la plus élevée étudiée (ECHA, c2007‑2017).
6.4.3 Caractérisation des risques pour la santé humaine
L’exposition de la population générale à l’acide oxalique devrait principalement se produire par voie alimentaire et découler de l’utilisation de nettoyants pour bateau et de produits antirouille domestiques en vaporisation. L’exposition à long terme à l’acide oxalique de la population générale devrait principalement survenir par l’alimentation, car la substance est naturellement présente dans certains aliments. Comme il existe des données sur la vaste gamme des concentrations de l’acide oxalique dans différents aliments et au sein de mêmes aliments, il n’a pas été nécessaire de calculer les marges d’exposition associées à sa présence naturelle dans les aliments.
La DSENO de 200 mg/kg/p.c./jour calculée dans l’étude sur les effets sur la reproduction était le critère d’effet le plus pertinent permettant de caractériser les risques pour la santé humaine associés à une exposition intermittente à l’acide oxalique présent dans des produits de consommation.
Le tableau 6‑1 présente les estimations d’exposition pertinentes, les doses critiques d’acide oxalique ainsi que les marges d’exposition résultantes.
| Scénario d’exposition | Estimation de l’exposition | Dose critique | Effet critique | Marge d’exposition |
|---|---|---|---|---|
| Exposition intermittente par voie cutanée découlant de l’utilisation d’un nettoyant pour bateau | 1,09 mg/kg p.c. (par application) | DSENO = 200 mg/kg p.c./jour (administration orale par l’eau potable, étude sur la reproduction et la fertilité) | Diminution du nombre total de petits vivants et du nombre de petits femelles vivants, augmentation du nombre de spermatozoïdes anormaux chez les deux générations de souris exposées à la dose suivante (400 mg/kg p.c./jour) | 183a |
| Exposition intermittente par inhalation découlant de l’emploi d’un antirouille tout usage en pulvérisateur | 0,00028 mg/kg p.c./jour (estimation de la concentration transformée en exposition générale) | DSENO = 200 mg/kg p.c./jour (administration orale par l’eau potable, étude sur la reproduction et la fertilité) | Diminution du nombre total de petits vivants et du nombre de petits femelles vivants, augmentation du nombre de spermatozoïdes anormaux chez les deux générations de souris exposées à la dose suivante (400 mg/kg p.c./jour) | 714 285 |
a En présumant que l’absorption par voie cutanée est équivalente à la biodisponibilité par voie orale.
La caractérisation des risques associés à l’acide oxalique est considérée comme prudente; la durée de l’étude sur la reproduction et la fertilité était beaucoup plus grande que la durée prévue des expositions intermittentes découlant de l’utilisation d’un nettoyant pour bateau et d’un antirouille tout usage en vaporisation contenant de l’acide oxalique. En outre, on a utilisé des valeurs par défaut prudentes, comme une absorption par voie cutanée de 100 % et le recours aux concentrations maximales signalées dans les fiches signalétiques, pour estimer l’exposition.
On a obtenu des marges d’exposition d’environ 183 et >710 000 après avoir comparé la DSENO de 200 mg/kg p.c./jour établie d’après les effets sur la reproduction observés chez la souris à la prochaine dose étudiée aux estimations de l’exposition découlant de l’utilisation d’un nettoyant pour bateau (1,09 mg/kg p.c.) et d’un antirouille tout usage en vaporisation (0,00028 mg/kg p.c./jour), respectivement. Ces marges ont été jugées adéquates pour tenir compte des incertitudes liées aux bases de données sur l’exposition et les effets sur la santé.
6.4.4 Incertitudes dans l’évaluation des risques pour la santé humaine
Les principales sources d’incertitude liées à la caractérisation des risques associés à l’acide oxalique sont présentées au tableau 6‑2 ci‑dessous.
| Principales sources d’incertitude | Incidence |
|---|---|
| En présumant une absorption par voie cutanée de 100 % lorsqu’on utilise un critère d’effet par voie orale pour caractériser le risque associé à l’exposition par voie cutanée à l’acide oxalique découlant de l’emploi de nettoyants pour bateau | + |
| Base de données limitée sur le danger de l’acide oxalique, absence d’études à court terme sur la substance administrée par voie cutanée et par inhalation | +/- |
+ = incertitude liée au risque de surestimer l’exposition ou le risque; +/- = risque non connu de surestimer ou de sous‑estimer le risque.
7. Conclusion
À la lumière de tous les éléments de preuve contenus dans la présente évaluation préalable, l’acide propionique, l’acide n‑butyrique, l’acide nonanoïque et l’acide oxalique posent un risque faible de causer des effets nocifs pour l’environnement. Il a été conclu que l’acide propionique, l’acide n‑butyrique, l’acide nonanoïque et l’acide oxalique ne satisfont pas aux critères énoncés à l’alinéa 64a) ou b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
D’après les renseignements contenus dans la présente évaluation préalable, il a été conclu que l’acide propionique, l’acide n‑butyrique, l’acide nonanoïque et l’acide oxalique ne satisfont pas au critère énoncé à l’alinéa 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Par conséquent, il a été conclu que l’acide propionique, l’acide n‑butyrique, l’acide nonanoïque et l’acide oxalique ne satisfont à aucun des critères énoncés à l’article 64 de la LCPE.
Références
[BDIPSN] Base de données sur les ingrédients des produits de santé naturels. [Base de données]. [modifié le 10 janvier 2017]. Ottawa (Ont.), Santé Canada. [Consultée le 15 janvier 2017].
[BDPP] Base de données sur les produits pharmaceutiques [base de données]. [Modifiée le 17 juillet 2015]. Ottawa (Ont.), Santé Canada. [mis à jour le 17 février 2017, consultée le 1er mars 2017].
[BDPSNH] Base de données des produits de santé naturels homologués [base de données]. [Modifiée le 10 août 2016]. Ottawa (Ontario), Santé Canada. [Consultée le 15 janvier 2017].
Bergman EN. 1990. « Energy contributions of volatile fatty acids from the gastrointestinal tract in various species ». Physiol Rev. vol. 70, no 2, p. 567-590.
Burdock GA. 2009. Fenaroli’s handbook of flavour ingredients. 6e éd. Boca Raton (Floride), CRC Press.
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999). L.C. 1999, ch.33. Gazette du Canada, partie III, vol. 22, no 3.
Canada, ministère de l’Environnement. 2012. « Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances de la Liste intérieure [PDF, 1.98 Mo] ». Gazette du Canada, partie I, vol. 146, no 48, supplément.
ChemIDplus 1993-a. [Base de données]. Bethesda (Maryland), US National Library of Medicine. Résultats de la recherche sur le no CAS 79-09-4. [Consultée le 15 septembre 2016]. (disponible seulement en anglais)
ChemIDplus 1993-b [base de données]. Bethesda (Maryland), US National Library of Medicine. Résultats de la recherche sur le no CAS 107-92-6. [Consultée le 15 septembre 2016]. (disponible seulement en anglais)
ChemIDplus 1993-c. [Base de données]. Bethesda (Maryland), US National Library of Medicine. Résultats de la recherche sur le no CAS 112-05-0. [Consultée le 15 septembre 2016]. (disponible seulement en anglais)
ChemIDplus 1993-d. [Base de données]. Bethesda (Maryland), US National Library of Medicine. Résultats de la recherche sur le no CAS 144-62-7. [Consultée le 15 septembre 2016]. (disponible seulement en anglais)
ChemView 2013-a. [Base de données]. Washington DC, US Environmental Protection Agency. Résultats de la recherche sur le no CAS 79-09-4. [Consultée le 1er décembre 2016]. (disponible seulement en anglais)
ChemView 2013-b [Base de données]. Washington DC, US Environmental Protection Agency. Résultats de la recherche sur le no CAS 107-92-6. [Consultée le 1er décembre 2016]. (disponible seulement en anglais)
ChemView 2013-c. [Base de données]. Washington DC, US Environmental Protection Agency. Résultats de la recherche sur le no CAS 144-62-7. [Consultée le 1er décembre 2016]. (disponible seulement en anglais)
[ConsExpo Web] Consumer Exposure Model. 2016. Version Internet. Bilthoven (Pays-Bas) Rijksinstituut voor Volksgezondheid en Milieu [Institut national de santé publique et d’environnement].
[CNRC] Conseil national de recherches du Canada. 2011. Data gathering on chemicals released to indoor air of residences from building materials and furnishings. Institut de recherches en construction du CNRC, rapport no B3332.2. Produit pour Santé Canada, Ottawa (Ontario).
David RM, Tyler TR, Ouellette T, Faber WD et Banton MI. 2001. « Evaluation of subchronic toxicity of n‑butyl acetate vapor ». Food Chem Toxicol., vol. 39, p. 877-886.
[ECCC] Environnement et Changement climatique Canada. 2013. Données de la Mise à jour de l’inventaire de la LIS recueillies en vertu du de l’article 71 de la Loi canadienne sur la protection de l’environnement de 1999 : Avis concernant certaines substances inanimées (chimiques) inscrites sur la Liste intérieure. Données préparées par Environnement Canada et Santé Canada, Programme des substances existantes.
[ECCC] Environnement et Changement climatique Canada. 2016a. Document sur l’approche scientifique : Classification du risque écologique des substances organiques.
[ECCC] Environnement et Changement climatique Canada. 2016b. Gatineau (Québec). Data used to create substance-specific hazard and exposure profiles and assign risk classifications in the Ecological Risk Classification of organic substances. Gatineau (Québec). Disponible auprès de substances@ec.gc.ca.
[ECCC] Environnement et Changement climatique Canada. 2017. Data collected from a targeted information gathering initiative for assessments under the Chemicals Management Plan (février 2017). Donnés préparées par Environnement et Changement climatique Canada, Santé Canada, Programme des substances existantes.
[ECCC] Environnement et Changement climatique Canada. 2017. Data submitted pursuant to the Canadian Environmental Protection Act, 1999, section 70. Données préparées par ECCC et Santé Canada, Programme des substances existantes.
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada. [Modifié le 12 mars 2017]. Catégorisation. Ottawa (ON): Governement of Canada. [consulté le 10 février 2017].
[ECHA] Agence européenne des produits chimiques. c2007-2016. Registered substances database. Résultats de la recherche sur le no CAS 144-62-7. Helsinki (Finlande): ECHA. [Mise à jour du 14 janvier 2016, consulté en décembre 2016]. (disponible en anglais seulement)
[ECHA] Agence européenne des produits chimiques, 2013 [PDF, 768 Ko]. Annex 1 Background document to the Opinion proposing harmonised classification and labelling at Community level of nonanoic acid. EC number: 203-931-2; CAS number: 112-05-0. Comité de l’évaluation des risques. (disponible en anglais seulement)
[ECHA] Agence européenne des produits chimiques. 2017. Brief Profile: Oxalic acid. Helsinki (Finlande), ECHA [mis à jour le 12 mai 2017, consulté le 15 mai 2017]. (disponible en anglais seulement)
[EFSA] Autorité européenne de sécurité des aliments. 2014. « Scientific opinion on the re-evaluation of propionic acid (E 280), sodium propionate (E281), calcium propionate (E 282) and potassium propionate (E 283) as food additives ». EFSA Journal. vol. 12, no 7, p. 3779.
[EMA] Agence européenne pour l’évaluation des médicaments. 2003 [PDF, 151 Ko]. Committee for veterinary medicinal products: oxalic acid summary report. Londres (Royaume-Uni): EMA. [Mis à jour le 1er décembre 2003, consulté le 1er mars 2017]. (disponible en anglais seulement)
[EPA] Environmental Protection Agency. 1998. EPA pesticide fact sheet. Pelargonic acid. Washington DC: Environmental Protection Agency, Biopesticides and Pollution Prevention Division. Disponible auprès de NTIS, Springfield (Virginie), 199823. Commandité par l’Office of Pesticide Program.
[EPI Suite] Estimation Program Interface Suite for Microsoft Windows [modèle d’estimation]. c2000-2012. Ver. 4.11. Washington DC: US Environmental Protection Agency, Office of Pollution Prevention and Toxics, Syracuse (New-York): Syracuse Research Corporation. (disponible en anglais seulement)
EU Food Flavourings Database [Base de données]. [Modifiée en 2016]. Brussels (BE): European Commission Directorate-General for Health and Consumers. [Consultée en 2015]. (disponible en anglais seulement)
EU Food Additives Database [Base de données]. [Modifiée en 2018]. Brussels (BE): European Commission Directorate-General for Health and Consumers. [Consultée en 2015]. (disponible en anglais seulement)
[EU] European Union. 2012. COMMISSION REGULATION (EU) No 872/2012 of 1 October 2012 adopting the list of flavouring substances provided for by Regulation (EC) No 2232/96 of the European Parliament and of the Council, introducing it in Annex I to Regulation (EC) No 1334/2008 of the European Parliament and of the Council and repealing Commission Regulation (EC) No 1565/2000 and Commission Decision 1999/217/EC. 161 pp. (disponible en anglais seulement)
[FCC] Food Chemical Codex. 2016. United States Pharmacopeial Convention. Rockville (Maryland). (disponible en anglais seulement)
Fitzhugh OG et Nelson AA. 1947. « The comparative chronic toxicities of fumaric, tartaric, oxalic and maleric acids ». J Am Pharm Assoc. vol. 36, no 7, p. 217-219.
[FS] Fiche signalétique. 2014a. Star brite Nettoyant de coque instantané. Fort Lauderdale (Floride), Star brite Inc. [Consultée le 15 décembre 2016].
[FS] Fiche signalétique. 2014b. Star brite Nettoyant anti rouille. Fort Lauderdale (Floride), Star brite Inc. [Consultée le 15 décembre 2016].
[FS] Fiche signalétique. 2015a. Iron OUT (liquid). [PDF, 151 Ko] Fort Wayne (Indiana), Iron Out dba Summit Brands. [Consultée le 15 décembre 2016].
[FS] Fiche signalétique. 2015b. Bar Keepers Friend Cleanser & Polish. [PDF, 490 Ko] Indianapolis (Indiana): SerVaas Laboratories Inc. [Consultée le 15 décembre 2016].
[FS] Fiche signalétique. 2015c. Nettoyant œuvres vives. Fort Lauderdale (Floride), Star Brite Inc. [Consultée le 15 décembre 2016].
Haynes W, directeur. 2016. CRC handbook of chemistry and physics, 97th ed. [Base de données]. Résultats de la recherche sur le no CAS 144-62-7. Boca Raton (Floride). Consulté le 15 septembre 2016.
Hodgkinson A et Zarembski PM. 1968. « Oxalic acid metabolism in man: a review ». Calcif Tissue Res. vol. 2, p. 115-132.
Holmes RP e, Kennedy M. 2000. « Estimation of the oxalate content of foods and daily oxalate intake ». Kidney Int. vol. 57, p. 1662-1667.
[HSDB] Hazardous Substances Data Bank [base de données]. 1983-a. Résultats de la recherche sur le no CAS 144-62-7. Bethesda (Maryland): National Library of medicine (US). [Mise à jour le 24 juin 2005, consultée le 1er décembre 2016]. (disponible en anglais seulement)
[HSDB] Hazardous Substances Data Bank [base de données]. 1983-b. Résultats de la recherche sur le no CAS 112-05-0. Bethesda (Maryland): National Library of medicine (US). [Mise à jour le 7 octobre 2008, consultée le 1er décembre 2016]. (disponible en anglais seulement)
[HSDB] Hazardous Substances Data Bank [base de données]. 1983-c. Résultats de la recherche sur le no CAS 107-92-6. Bethesda (Maryland): National Library of medicine (US). [Mise à jour le 20 décembre 2006; consultée le 1er décembre 2016]. (disponible en anglais seulement)
Huang XF et Yu JZ. 2007. « Is vehicle exhaust a significant primary source of oxalic acid in ambient aerosols? » Geophys Res Lett. vol. 34, p. 1-5.
Ishidate M Jr, Sofuni T, Yoshikawa K, Hayashi M, Nohmi T, Sawada M et Matsuoka A. 1984. « Primary mutagenicity screening of food additives ». Food Chem Toxicol. vol. 22, no 8, p. 623-636.
Kawamura K et Kaplan IR. 1987. « Motor exhaust emissions as a primary source of dicarboxylic acids in Los Angeles ambient air ». Environ Sci Technol. vol. 21, p. 105-110.
McGinn SM, Janzen HH et Coates T. 2003. « Atmospheric ammonia, volatile fatty acids, and other odorants near beef feedlots ». J Environ Qual. vol. 32, p. 1173-1182.
[MSDS] Material Safety Data Sheet. [PDF, 18 Ko] 2011. CleanCide. Kirkwood (MO): Wexford Labs Inc. [Consultée le 15 décembre 2016]. (disponible en anglais seulement)
Nelson BK, Brightwell WS, Robertson SK, Kahn A, Krieg EF Jr et Massari VJ. 1989a. « Behavioral teratology investigation of 1-butanol in rats ». Neurotoxicol Teratol. vol. 11, no 3, p. 313-315.
Nelson BK, Brightwell WS, Kahn A, Burg JR et Goad PT. 1989b. « Lack of selective developmental toxicity of three butanol isomers administered by inhalation to rats ». Fundam Appl Toxicol. vol. 12, no 3, p. 469-479.
[NTP] US National Toxicology Program. 1985. Oxalic acid: reproduction and fertility assessment in CD-1 mice when administered in drinking water. National Toxicology Program. National Institute of Environmental Health Science. NTP-85-322.
[OCDE] Organisation de coopération et de développement économiques. 2003. SIDS initial assessment report: n-butyric acid. CAS No. 107-92-6. [PDF, 150 Ko] Réunion d’évaluation initiale du SIDS, 27 au 30 mai 2003, Helsinki (Finlande). (disponible en anglais seulement)
[OCDE] Organisation de coopération et de développement économiques. 2007. SIDS initial assessment report: propionic acid. CAS No. 79-09-4. [PDF, 170 Ko] Réunion d’évaluation initiale du SIDS, 16 au 19 octobre 2007, Helsinki (Finlande). (disponible en anglais seulement)
[OMS] Organisation mondiale de la santé. 1998. Evaluation of certain food additives and contaminants. 49e réunion du comité expert conjoint OAA-OMS/WHO sur les additifs alimentaires. Genève (Suisse), Organisation mondiale de la santé. 104 p., rapport no 884.
Rogge WF, Mazurek MA, Hildemann LM, Cass GR. 1993. Quantification of urban organic aerosols at a molecular level: Identification, abundance and seasonal variation. Atmospheric Environment. 27(8):1309-1330.
Rossman TG, Molina M, Meyer L, Boone P, Klein CB, Wang Z, Li F, Lin WC et Kinney PL. 1991. « Performance of 133 compounds in the lambda prophage induction endpoint of the Microscreen assay and a comparison with S. typhimurium mutagenicity and rodent carcinogenicity assays ». Mutat Res. vol. 260, no 4, p. 349-367.
Santé Canada. [Modifiée le 14 décembre 2015]. Liste critique des ingrédients de cosmétiques : liste des ingrédients dont l’usage est interdit dans les cosmétiques. Ottawa (Ontario), gouvernement du Canada. [Consultée le 1er mars 2016].
Santé Canada. [Modifiée le 14 décembre 2016] Liste des agents de conservation autorisés (Listes des additifs alimentaires autorisés). Ottawa (Ont.), gouvernement du Canada. [Consultée le 1er février 2016].
Tang M, Larson-Meyer DE et Liebman M. 2008. « Effect of cinnamon and tumeric on urinary oxalate excretion, plasma lipids, and plasma glucose in healthy subjects ». Am J Clin Nutr. vol. 87, p. 1262-1267.
Taylor EN, Curhan GC. 2007. « Oxalate intake and the risk for nephrolithiasis ». J Am Soc Nephrol. vol. 18, no 7, p. 2198-2204.
[TDS] Technical Data Sheet. 2011. CleanCide. [PDF, 18 Ko] Kirkwood (Missouri): Wexford Labs Inc. [Consulté le 15 décembre 2016].
[TRL] Toxicity Research Laboratories Ltd. 1986. Rat oral subchronic toxicity study of normal butanol. Étude no 032-006. Muskegon (Michigan), TRL.
[US FDA] US Food and Drug Administration. 2016a. [Révisé le 1er avril 2016]. Code of Federal Regulations Title 21, Volume 3: Section 184.1081 Propionic acid. [En ligne] Consulté le 15 septembre 2016] (disponible en anglais seulement)
[US FDA] US Food and Drug Administration. 2016b. [Révisé le 1er avril 2016]. Code of Federal Regulations Title 21, Volume 3: Section 182.60 Synthetic flavoring substances and adjuvants. [En ligne] (disponible en anglais seulement)
[US FDA] US Food and Drug Administration. 2016c. [Révisé le 1er avril 2016]. Code of Federal Regulations Title 21, Volume 3: Section 172.515 Synthetic flavoring substances and adjuvants. [En ligne] (disponible en anglais seulement)
Versar. 1985. Methods of assessing exposure to chemical substances. Volume 7. Methods for assessing consumer exposure to chemical substances. Washington D.C.: U.S. Environmental Protection Agency. EPA 560/5-85-007.
Annexes
Annexe A. Estimation de l’exposition à l’acide oxalique
L’exposition à l’acide oxalique découlant de l’utilisation de produits de consommation a été estimée d’après un adulte ayant un poids présumé de 70,9 kg (Santé Canada, 1998) et de comportements d’utilisation courants. Pour obtenir les estimations, on s’est servi de ConsExpo Web (ConsExpo Web, 2016) ou d’algorithmes provenant du modèle (RIVM, 2007). Compte tenu de l’absence de données sur l’absorption par voie cutanée, on a présumé une absorption par voie cutanée de 100 %.
| Scénario d’exposition | Hypothèses |
|---|---|
| Nettoyant pour coque de bateau (cutané) | Épaisseur du film : 0,00213 cm (VERSAR, 1985) Superficie de la main : 455 cm2 (Santé Canada, 1998) Masse volumique du produit : 1,0 g/cm3 Concentration de la substance dans le produit : 8 % (FS, 2014a) |
| Antirouille tout usage à vaporiser (inhalation) | Modèle : ConsExpo – nettoyant pour salle de bain à vaporiser : vaporisation (RIVM, 2007) Durée de l’application : 1,5 min (RIVM, 2007) Durée de l’exposition : 25 min (RIVM, 2007) Volume de la pièce : 10 m3 (RIVM, 2007) Vitesse de renouvellement de l’air : 2,0 par heure (RIVM, 2007) Concentration de la substance dans le produit : 10 % (FS, 2015a) |
