Évaluation préalable groupe de certaines substances ignifuges organiques N,N′-Éthylènebis(3,4,5,6-tétrabromophtalimide) (EBTBP)
Titre officiel : Évaluation préalable groupe de certaines substances ignifuges organiques N,N′-Éthylènebis(3,4,5,6-tétrabromophtalimide) (EBTBP)
Numéro de registre du Chemical Abstracts Service 32588-76-4
Environnement et Changement climatique Canada
Santé Canada
Mai 2019
No de cat. : En14-367/2019F-PDF
ISBN 978-0-660-29861-0
Sommaire
Conformément à l'article 68 de la Loi canadienne sur la protection de l'environnement (1999) (Canada 1999), la ministre de l'Environnement et la ministre de la Santé ont procédé à une évaluation préalable du N,N′-éthylènebis(3,4,5,6-tétrabromophtalimide) [no CAS 32588-76-4], communément connu sous le nom d'éthylène bis(tétrabromophthalimide) et désigné par l'abréviation EBTBP. Cette substance fait partie du groupe de certaines substances ignifuges organiques, lequel est constitué de dix substances organiques ayant une fonction similaire, soit l’application à des matériaux en vue de retarder l'inflammation et la propagation du feu. L'EBTBP a été désigné comme substance prioritaire pour l'évaluation en raison des possibles préoccupations relatives à la santé humaine (liées au potentiel d'exposition).
L'EBTBP ne se trouve pas à l’état naturel dans l'environnement.
Les résultats d'une enquête menée auprès de l'industrie en 2011 ont indiqué que l'EBTBP n'était pas été fabriqué au Canada en 2011; toutefois, de 1 000 à 10 000 kg d'EBTBP pur, de 10 000 à 100 000 kg de formulation et de 100 000 à 1 000 000 kg d'EBTBP dans des articles manufacturés ont été importés au Canada.
L'EBTBP est utilisé au Canada uniquement en tant qu'ignifuge aux fins d'utilisation dans notamment les matériaux de plastique et de caoutchouc ainsi qu'au sein de l'industrie automobile. Cette substance est utilisée comme produit de substitution au décabromodiphényléther (décaBDE). À l'échelle internationale, l'EBTBP est utilisé comme produit ignifuge dans les plastiques, les caoutchoucs et les tissus. Cette substance sert aussi aux applications et aux composantes électroniques.
Des rejets dans l'environnement sont susceptibles de se produire en raison de la fabrication, du transport, de l'utilisation et de l'élimination de l'EBTBP ou des matériaux qui en sont composés.
On ne dispose que de peu de données physiques et chimiques mesurées sur l'EBTBP. L'EBTBP se caractérise par une hydrosolubilité modélisée faible et une pression de vapeur modélisée très faible, ainsi qu'une constante de la loi de Henry et des valeurs modélisées très élevées pour le coefficient de partage octanol-eau. Les propriétés physiques et chimiques modélisées indiquent que l'EBTBP devrait se répartir dans les sédiments et le sol, et se lier à la fraction organique de la matière particulaire. De plus, il est peu probable que l'EBTBP soit transporté à grande distance dans l'eau en raison de son hydrosolubilité limitée et de son coefficient de partage carbone organique-eau élevé. L'EBTBP se caractérise par une demi-vie modélisée en phase gazeuse plutôt courte (6,5 heures); cependant, on s'attend à ce que plus de 99 % des produits chimiques se répartissent dans la phase aérosol particulaire, où la dégradation dans l'air serait très limitée. Lorsqu'il est adsorbé aux aérosols atmosphériques, l'EBTBP devrait demeurer dans l’air suffisamment longtemps pour être transporté dans l’atmosphère à une grande distance à partir de ses sources d’émission.
Il existe un nombre limité de données empiriques sur la persistance, la bioaccumulation et l'écotoxicité de l'EBTBP. Il existe peu de données empiriques sur les structures analogues pour l'EBTBP. Toutefois, on a considéré des données expérimentales sur la persistance et l'écotoxicité du décabromodiphényléthane (DBDPE), son analogue le plus étroitement apparenté, à titre de données déduites à partir d'analogues pour ces critères d'effet, qui, quant à elles, s'appuient partiellement sur les données déduites à partir d'analogues pour le décaBDE, son analogue structurel.
D'après les données expérimentales modélisées et limitées sur la biodégradation, l'EBTBP ne devrait présenter qu'une biodégradation limitée. Dans l'ensemble, l'EBTBP peut persister dans l'eau, les sédiments, le sol et les aérosols atmosphériques, mais pas dans l'air.
D'après la seule étude de bioconcentration chez les poissons disponible, l'EBTBP présente un potentiel de bioconcentration faible à modéré. Toutefois, les résultats de ces données empiriques n'étaient pas fiables, puisque les concentrations dans cette étude étaient plus élevées que l'hydrosolubilité de l'EBTBP. Néanmoins, l'EBTBP affiche un coefficient de partage octanol-eau très élevé et une hydrosolubilité très faible, ce qui entraîne une biodisponibilité limitée, et ce, même à la suite d'une exposition alimentaire. Ainsi, on s'attend à ce que cette substance présente un faible potentiel de bioaccumulation dans les organismes.
L'EBTBP devrait être rejeté dans l'environnement canadien pendant les activités industrielles de traitement. Même si on peut trouver de l'EBTBP dans les produits commerciaux ou les produits disponibles aux consommateurs, les renseignements sur les rejets dans l'environnement par cette voie sont limités, et les rejets devraient être diffus et minimes par rapport aux rejets industriels. Des scénarios industriels basés sur les renseignements provenant des sites ont été élaborés aux fins d'estimation des rejets dans l'eau. On a déterminé les concentrations prévues dans les sédiments grâce à la méthode de partage à l'équilibre. L'exposition de l'EBTBP dans le sol a été estimée d'après un scénario d'application de biosolides.
Les analyses du quotient de risque, intégrant des estimations prudentes de l'exposition dans des données sur la toxicité, ont été effectuées pour les milieux sédimentaires et terrestres (sol). Les données empiriques limitées sur la toxicité disponible pour l'EBTBP indiquent un faible niveau de toxicité aiguë pour les organismes aquatiques et les mammifères (rongeurs). Puisque l'EBTBP affiche une faible biodisponibilité, une hydrosolubilité très faible et un coefficient de partage octanol-eau très élevé, il est peu probable qu'il présente des effets de toxicité aiguë chez les organismes aquatiques. Par conséquent, on n'a pas effectué d'analyse de risques pour les organismes aquatiques. Une méthode du partage eau-sédiment à l'équilibre a été utilisée pour estimer la concentration de l'EBTBP dans les sédiments benthiques. On a élaboré des scénarios d'exposition dans les sédiments dans le cadre d'une extension des scénarios de rejets industriels dans le milieu aquatique afin de déterminer les concentrations environnementales estimées (CEE) dans les sédiments lors du partage à l'équilibre. Des scénarios d'exposition dans le sol ont été élaborés dans le cadre d'une extension des scénarios dans le milieu aquatique, à l'aide des concentrations de biosolides et des taux de production basés sur des usines de traitement des eaux usées propres au site.
Bien que les données empiriques et modélisées sur la biodégradation laissent entendre que l'EBTBP est très stable dans l'eau, le sol et les sédiments, il est peu probable que cette substance soit hautement biodisponible ou qu'elle s'accumule fortement dans les organismes et ne devrait pas présenter de risque pour l'environnement d'après les expositions estimées actuelles.
Compte tenu de tous les éléments de preuve disponibles présentés dans cette évaluation préalable, le risque que l'EBTBP nuise à l'environnement est faible. Il est conclu que l'EBTBP ne répond pas aux critères énoncés à l'alinéa 64a) ou b) de la Loi canadienne sur la protection de l'environnement, car il ne pénètre pas dans l'environnement en une quantité, à une concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique, ou à mettre en danger l'environnement essentiel pour la vie.
On n'a relevé aucune classification des effets de l'EBTBP sur la santé d'organismes de réglementation nationaux ou internationaux. En outre, on n'a recensé aucune étude sur la toxicité chronique et la cancérogénicité liée à l'EBTBP. D'après les renseignements disponibles sur la génotoxicité, l'EBTBP n'est pas jugé génotoxique in vitro.
Aucun effet nocif n'a été observé chez les animaux de laboratoire exposés à l'EBTBP par voie orale, à la plus forte dose testée dans les études de la toxicité à court terme et subchronique. Dans des études sur la toxicité pour le développement, aucun effet sur la mère lié au traitement ni aucun effet sur le développement n'a été observé chez les animaux de laboratoire exposés à l'EBTBP par voie orale, jusqu'à la dose la plus élevée testée.
Lors des essais sur des animaux de laboratoire, les doses les plus élevées testées, sans effet lié au traitement, étaient de six ordres de grandeur plus élevés que les estimations de l'absorption d'EBTBP de la population générale du Canada dans les milieux naturels. Cette marge d'exposition est jugée adéquate pour rendre compte des incertitudes liées aux bases de données concernant les effets sur la santé et l'exposition.
À la lumière des renseignements contenus dans la présente évaluation préalable, il est conclu que l'EBTBP ne répond pas aux critères énoncés à l'alinéa 64c) de la Loi canadienne sur la protection de l'environnement, car il ne pénètre pas dans l'environnement en une quantité, à une concentration ou dans des conditions de nature à mettre en danger la vie et la santé humaine au Canada.
Conclusion générale
Il est conclu que l'EBTBP ne répond à aucun des critères énoncés à l'article 64 de la LCPE.
1. Introduction
Conformément aux articles 68 ou 74 de la Loi canadienne sur la protection de l’environnement, 1999, (Canada 1999) la ministre de l'Environnement et la ministre de la Santé procèdent à une évaluation préalable des substances afin de déterminer si elles présentent ou sont peuvent présenter un risque pour l'environnement ou la santé humaine.
L'Initiative des groupes de substances constitue un élément clé du Plan de gestion des produits chimiques (PGPC) du gouvernement du Canada. Le groupe de substances ignifuges organiques s'inscrit dans le cadre de l'Initiative des groupes de substances du PGPC du gouvernement du Canada. Ce groupe comprend dix substances qui ont été déclarées prioritaires en matière de mesure à prendre, car elles satisfaisaient aux critères de catégorisation en vertu de l'article 73 de la LCPE ou étaient considérées comme prioritaires en raison de préoccupations relatives à l'environnement ou à la santé humaine (ECCC et SC [modifié en 2017]). Toutes ces substances présentent une fonction similaire qui est l'application sur des matériaux en vue d'empêcher l'ignition et la propagation du feu. En outre, ces substances sont des substituts potentiels à d'autres produits ignifuges qui sont actuellement soumis à des contrôles réglementaires ou à un retrait progressif à l'échelle mondiale ou au Canada.
La présente évaluation préalable porte sur la substance N,N′-éthylènebis(3,4,5,6-tétrabromophtalimide) [no CAS 32588-76-4], communément connue sous le nom d'éthylène bis(tétrabromophthalimide) et désignée par l'abréviation EBTBP. L'évaluation de cette substance a été considérée comme prioritaire d'après d'autres préoccupations relatives à la santé humaine lors de la catégorisation visant la Liste intérieure des substances (LIS) aux termes du paragraphe 73(1) de la LCPE. Lors de la catégorisation, la substance répondait également aux critères de persistance, mais elle a donné un résultat incertain concernant la satisfaction des critères relatifs à la bioaccumulation et à la toxicité intrinsèque pour les organismes non humains.
La présente évaluation préalable tient compte des renseignements sur les propriétés chimiques, le devenir dans l'environnement, les dangers, les utilisations et l'exposition, ainsi que des renseignements supplémentaires soumis par les intervenants. Nous avons relevé des données pertinentes jusqu'en janvier 2017 pour les sections portant sur l'environnement ainsi que la santé humaine. Les données empiriques obtenues d'études clés, ainsi que certains résultats provenant de modèles, ont servi à formuler les conclusions. Lorsqu'ils étaient disponibles et pertinents, les renseignements contenus dans les évaluations effectuées par d'autres instances ont été utilisés.
Les parties de la présente évaluation préalable qui portent sur la santé humaine et l'écologie ont fait l'objet d'un examen externe par écrit par des pairs ou d'une consultation de ces derniers. M. Jon Arnot, Ph. D. (Arnot Research and Consulting Inc.), M. Adiran Covaci, Ph. D. (département de biologie de l'Université d'Anvers), Mme Laurence Deydier, Ph. D. (Agence européenne des produits chimiques) et Mme Marcia L. Hardy, Ph. D., conseillère principale en toxicité (Albemarle Corporation) ont fourni des commentaires sur les parties techniques concernant l'environnement. Michael Jayjock (LifeLine Group), Penny Fenner-Crisp, consultante indépendante et John Reichard (Toxicology Excellence for Risk Assessment [TERA]) ont fourni des commentaires sur les parties techniques concernant la santé humaine. Par ailleurs, l’ébauche de la présente évaluation préalable a été soumise à une période de consultation publique de 60 jours. Bien que les commentaires externes aient été pris en considération, Santé Canada et Environnement et Changement climatique Canada (ECCC) assument la responsabilité du contenu final et des résultats de l'évaluation préalable.
La présente évaluation préalable repose sur des données critiques permettant de déterminer si les substances satisfont aux critères énoncés à l’article 64 de la LCPE. À cette fin, nous avons examiné les renseignements scientifiques et suivi une approche basée sur une pondération des éléments de preuve et le principe de précautionNote de bas de page 1 . Cette évaluation préalable présente les principales données et considérations sur lesquelles repose la conclusion.
2. Identité des substances
La présente évaluation préalable porte sur la substance N,N′-éthylènebis(3,4,5,6-tétrabromophtalimide) [no CAS 32588-76-4], qui est également connue sous le nom d'éthylène bis(tétrabromophthalimide) (NCI, 2013). Aux fins de la présente évaluation, l'éthylène bis(tétrabromophthalimide) sera appelé par son acronyme EBTBP. L'identité de cette substance est présentée au tableau 2-1. Les autres noms de cette substance sont aussi disponibles (ECCC 2017a).
| No CAS | Structure chimique | Masse moléculaire | Formule chimique |
|---|---|---|---|
| 32588-76-4 | 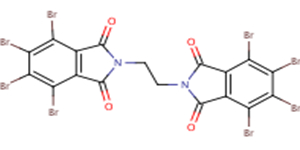 |
951,47 g/mol | C18H4Br8N2O4 |
2.1 Sélection des analogues et utilisation de modèles de relations quantitatives structure-activité (QSAR)
Les analogues structuraux qui comportent des données empiriques pertinentes peuvent être utilisés pour aider à évaluer ces substances qui manquent de données empiriques. Les analogues structuraux sont des produits chimiques qui ont une structure semblable les unes aux autres et qui, par conséquent, sont censés avoir des propriétés physiques et chimiques semblables, se comporter de manière comparable dans l'environnement et démontrer des toxicités similaires pour les organismes non humains (comme fonction de biodisponibilité et de réactivité chimique). Lorsqu'il existe des données expérimentales concernant une propriété donnée d'une substance analogue et que cet analogue présente une structure, une réactivité chimique et une biodisponibilité très similaires, ces données peuvent être utilisées telles quelles (en tant que données déduites à partir d'analogues) ou on peut les modifier afin d'obtenir une estimation de la valeur de cette propriété pour la substance faisant l'objet de l'évaluation. Si la structure présente des différences légèrement ou modérément marquées, il est possible d'apporter des modifications aux estimations sur la propriété afin de tenir compte de ces différences à l'aide de méthodes quantitatives (p. ex. méthode d'ajustement de la valeur expérimentale d'EPIsuite) ou de méthodes qualitatives (p. ex. utilisation de l'analogue comme référence à partir de laquelle on procède à l'extrapolation). Cependant, lorsqu'il existe des différences dans la réactivité (mode d'action particulier, par exemple), on effectue une analyse afin de déterminer si l'analogue structurel possède un potentiel convenable de déduction à partir d'analogues pour le paramètre biologique ou la propriété en question.
Dans la partie portant sur l'environnement de la présente évaluation, deux analogues présentant une structure chimique étroitement apparentée à celle de l'EBTBP (possédant deux noyaux aromatiques entièrement bromés, même s'ils ne sont pas composés du groupe caractéristique indoline-1,3-dione) ont été relevés à l'aide de la boîte à outils Relation quantitative structure-activité (QSAR) de l'Organisation de coopération et de développement économiques 2012 (tableau 2-2). Ces analogues sont le décabromodiphényléther (décaBDE; no CAS 1163-19-5) et le décabromodiphényléthane (DBDPE; no CAS 84852-53-9).
Compte tenu de la différence structurelle ayant trait au groupe caractéristique indoline-1,3-dione (groupe imide) de l'EBTBP par rapport au DBDPE et au décaBDE, ces substances ne sont pas considérées comme étant des analogues convenables pour l'EBTBP en ce qui concerne la persistance et la transformation. À cet égard, le groupe imide présente d'importantes incertitudes quant à la voie de transformation, et il est difficile de déterminer s'il serait analogue au décaBDE ou au DBDPE. Cependant, comme il est expliqué ci-dessous, le DBDPE et le décaBDE sont considérés comme étant des analogues convenables pour l'EBTBP d'après les données déduites concernant leurs propriétés physiques et chimiques et leur toxicité.
La boîte à outils QSAR de l'OCDE, version 3.0, indique que ces substances provoquent un mode d'action toxique du narcotique de surface de base et ne présentent aucune différence relative à la réactivité. Puisque les données empiriques sur les propriétés physiques et chimiques du decaDBE sont disponibles en plus grand nombre que celles sur le DBDPE, les données concernant le décaBDE sont donc prises en compte à titre de données possibles déduites à partir des analogues pour l'EBTBP (Environnement Canada, 2006a, 2010). Tout comme l'EBTBP, le DBDPE est utilisé en tant que produit ignifuge de remplacement au décaBDE. Étant donné que les applications du DBDPE sont similaires à celles de l'EBTBP, probablement en raison de la similitude de leurs propriétés, on a comparé les données sur le devenir environnemental du DBDPE avec celles de l'EBTBP. Les données sur la toxicité utilisées dans le cadre de l'évaluation du DBDPE sont également prises en compte lors de l'évaluation des effets sur l'environnement et des scénarios d'exposition de l'EBTBP.
| No CAS ou acronyme | Nom de la substance | Structure chimique | Données empiriques disponibles (critères d'effet) |
|---|---|---|---|
| EBTBP 32588-76-4 | Éthylène bis(tétrabromophthal-imide) | 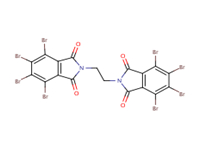 |
Biodégradation, facteur de bioconcentration (FBC), toxicité aquatique |
| décaBDE 1163-19-5 | Décabromodiphényléther | 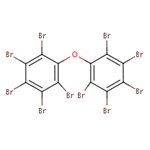 |
HS, PF, biodégradation, FBC |
| DBDPE 84852-53-9 | Décabromodiphényléthane | 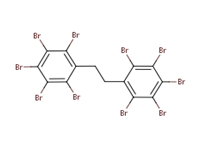 |
PV, HS, log Koe, données sur la toxicité dans les sédiments et le sol |
3. Propriétés physiques et chimiques
Quelques données sur les principales propriétés physiques et chimiques de l'EBTBP sont présentées au tableau 3-1 (ECCC 2017a).
Les données expérimentales sur les propriétés physiques et chimiques disponibles pour l'EBTBP sont limitées; par conséquent, on prendra en compte les données déduites à partir de renseignements empiriques pertinents sur son analogue, le décaBDE, ainsi que les résultats modélisés.
Pour effectuer des prévisions relatives au devenir dans l'environnement des composés organiques, il faut connaître leur propension à demeurer en phase aqueuse. L'EBTBP se retrouve à l'état solide à la température ambiante. Les ajustements du ratio de fugacité des liquides sous-refroidis pour les solides ont été effectués d'après un ratio de fugacité (F). Dans le cadre de la présente évaluation, on a déterminé le ratio F à l'aide du point de fusion de l'EBTBP (ECCC, 2017a). Le ratio de fugacité des liquides sous-refroidis a été appliqué à la solubilité dans l'octanol, à l'hydrosolubilité et à la pression de vapeur (ECCC, 2017a). Par la suite, on a vérifié les propriétés physiques et chimiques de l'EBTBP aux fins d'uniformité interne, et la variance relative de ces propriétés a été prise en compte dans le cadre du procédé d'ajustement par la méthode des moindres carrés d'après Schenker et al., (2005) (ECCC, 2017a). Ces propriétés physiques et chimiques découlant du modèle d'ajustement selon la méthode des moindres carrés ont ensuite servi de données d'entrée dans EPI Suite v4.1 afin de calculer la constante de la loi d'Henry et le coefficient de partage carbone organique-eau (Kco). Par conséquent, les données sur les propriétés physiques et chimiques utilisées dans le cadre de cette évaluation sont présentées au tableau 3-1.
L'EBTBP se présente sous la forme d'une poudre blanche ou jaune pâle la température ambiante (Albemarle, 2005, 1999a, b) et son point de fusion est élevé. L'EBTBP se caractérise par une hydrosolubilité, une pression de vapeur et une constante de la loi de Henry faibles (valeurs modélisées) ainsi qu'un coefficient de partage octanol-eau (Koe), un Koc et un coefficient de partage octanol-air (Koa) élevés (tableau 3-1; ECCC, 2017a).
| Propriété | Type | Valeur | Température | Référence |
|---|---|---|---|---|
| Forme physique | Valeurs expérimentales | Poudre blanche à jaune pâle | NP | Albermarle, 2005 |
| Point de fusion (°C) | Valeurs expérimentales | 445 | S.O. | EPI Suite, 2012 [MPBPVP, 2010] Correspondance de la structure de la base de données expérimentales : Saytex BT 93 |
| Point d'ébullition (°C) | Valeurs expérimentales | 827,9 (à 760 mm Hg) | S.O. | ChemNet, 1997 World of Chemicals, 2013 (données empiriques) |
| Pression de vapeur (Pa) | Valeurs estimées | (1,81 x 10-25) (liquide sous-refroidi, 2,59 x 10-21a) | N.P. | Geomeana; Calcul du ratio de fugacité des liquides sous-refroidis à l'aide du point de fusion et du modèle d'ajustement selon la méthode des moindres carrésa |
| Constante de la loi d'Henry (Pa•m3/mol) | Valeurs modélisées | 4,15 x 10-21 (4,21 x 10-16 atm•m3/mol) | N.P. | EPI Suite, 2012 [HENRYWIN, 2011]a |
| Log Koe (sans dimension) | Valeurs estimées | 8,90 | N.P. | Valeur moyenne des estimations et modèle d'ajustement selon la méthode des moindres carrésa |
| Log Kco (sans dimension) | Valeurs modélisées | 5,34 (Kco = 2,22x 105 L/kg) | N.P. | EPI Suite, 2012 [KOCWIN, 2010]a |
| Log Koa (sans dimension) | Valeurs modélisées | 27,52 (Koa = 3,29 x 1027) | N.P. | Modèle d'ajustement selon la méthode des moindres carrésa |
| Log Kae (sans dimension) | Valeurs modélisées | -18,62 (Kae = 2,40 x 10-19) | N.P. | Modèle d'ajustement selon la méthode des moindres carrésa |
| Hydrosolubilité (mg/L) | Valeurs modélisées | 2,88 x 10-7 (liquide sous-refroidi, 0,00413a) | N.P. | Geomeana; Calcul du ratio de fugacité des liquides sous-refroidis à l'aide du point de fusion et du modèle d'ajustement selon la méthode des moindres carrésa |
| pKa (sans dimension) | S.O. | S.O. | S.O. | S.O. |
Abréviations : log Koe, coefficient de partage octanol-eau;
log Kco, coefficient de partage carbone organique-eau;
log Koa, coefficient de partage octanol-air;
log Kae, coefficient de partage air-eau, sans dimension;
pKa, constante de dissociation acide;
S.O., sans objet. N.P., non précisé.
a ECCC 2017a
4. Sources
L'EBTBP n'est pas présent naturellement dans l'environnement. L'EBTBP est produit de façon commerciale en Arkansas, aux États-Unis (NIEHS, 1999) et au Connecticut, aux États‑Unis (Commission européenne, 2000b). Il semble que cette substance serait également fabriquée en Chine (Unibrom 2014). La plupart des rejets d'EBTBP dans l'environnement pourraient être attribuables aux processus industriels dans lesquels cette substance est utilisée.
On a signalé que 1 000 à 1 000 000 kg d'EBTBP ont été importés au Canada en 1986 (Environnement Canada, 1986). Des renseignements sur l'EBTBP présentés en 2000 en réponse à l'Avis concernant certaines substances inscrites sur la LIS (Canada, 2001), en vertu de l'article 71 de la LCPE, ont indiqué que cette substance n'était pas fabriquée au Canada; toutefois, entre 10 000 et 100 000 kg de cette substance y avaient été importés. Les renseignements fournis en 2013 en réponse à l'Avis concernant certaines substances ignifuges organiques (ECCC 2013 à 2014), en vertu de l'article 71 de la LCPE, ont indiqué que l'EBTBP n'était pas fabriqué au Canada en 2011, bien que des quantités variant entre 100 000 et 1 000 000 kg aient été importées au pays. L'EBTBP était importé au Canada en importante quantité dans les produits commerciaux ou ceux disponibles aux consommateurs (100 000 à 1 000 000 kg), en quantité moindre dans une formulation (10 000 à 100 000 kg) et en petite quantité sous forme de substance pure (1 000 à 10 000 kg) (ECCC 2013 à 2014).
Aux États-Unis, on a signalé que la production d'EBTBP était inférieure à 450 tonnes en 1990, et supérieure à 450 tonnes en 1986 et en 1994 (NIEHS, 1999). L'EBTBP a été inscrit à la liste de substances chimiques produites en grande quantité aux États-Unis en 1994. D'après le Inventory Update Reporting de l'Environnemental Protection Agency des États-Unis (US EPA, 2006), la quantité d'EBTBP fabriquée aux États-Unis chaque année variait entre 450 et 4 500 tonnes. En Europe, les quantités totales produites annuellement avaient été fixées précédemment à 5 250 tonnes (United Kingdom Environment Agency, 2003). En outre l'EBTBP est considéré comme étant une substance produite en grande quantité par l'OCDE (OCDE, 2011). L'EBTBP est utilisé dans les pays nordiques depuis 1999 (SPIN, 2006); toutefois, en raison de la confidentialité des renseignements, la quantité annuelle produite ou utilisée n'est pas disponible.
5. Utilisations
L'EBTBP est utilisé en tant qu'additif ignifuge dans les plastiques, les caoutchoucs et les textiles. On a déterminé que l'EBTBP présentait une température de flexion sous charge (température de fléchissement sous charge) plus élevée ainsi qu'une meilleure stabilité aux rayons ultraviolets que d'autres substances ignifuges (OCDE, 1995). Sa stabilité aux rayons ultraviolets et à la chaleur, de même que sa résistance à l'efflorescence, font de cette substance un produit ignifuge idéal (NIEHS, 1999). Plus précisément, l'EBTBP est utilisé comme additif ignifuge dans le polystyrène choc, le polyéthylène, le polypropylène, les polymères thermoplastiques, le polyamide, les terpolymères d'éthylène-propylène-diène (élastomères EPDM) et autres caoutchoucs synthétiques, le polycarbonate, les polymères d'éthylène, les résines d'ionomère, les résines époxydes et les traitements de textiles (Radloff et al. 1996, PISSC, 1997; Tice, 1999; Covaci et al., 2011). Les articles manufacturés qui pourraient contenir de l'EBTBP sont, notamment, les composants électriques et électroniques, comme les isolants pour fils et câbles, les interrupteurs et les connecteurs, les matériaux de construction, les produits d'entreposage et de distribution, les produits automobiles ainsi que les émulsions et les revêtements à base d'eau (PISSC, 1997; US EPA, 2014; Albemarle, 1999a, b; Albemarle, 2004; Covaci et al., 2011).
L'EBTBP est considéré comme étant un produit de remplacement pour le décaBDE, qui était utilisé en tant que substance ignifuge dans les produits électroniques (Kolic et al., 2009). Cela laisse entendre également que l'EBTBP est un produit de remplacement pour le décaBDE dans la production de polystyrène choc (US EPA, 2014).
Au Canada, des utilisations de l'EBTBP ont été déclarées en réponse à une enquête menée en vertu de l'article 71 de la LCPE (Canada, 2013). L'EBTBP est utilisé au Canada en tant qu'ignifuge aux fins d'utilisation dans les matériaux de plastique et de caoutchouc, dans l’électricité et l’électronique ainsi qu'au sein de l'industrie automobile (ECCC 2013 à 2014). On a signalé que moins de 10 000 kg d'EBTBP avait été importé sous forme de substance pure (ECCC 2013 à 2014). L'EBTBP est principalement utilisé dans les produits disponibles aux consommateurs comme étant ajouté aux plastiques qui composent les revêtements de fils et de câbles ainsi que les boîtiers électroniques. Les adhésifs thermofusibles dont se servent les consommateurs dans le cadre de leurs passe-temps pourraient également contenir de l'EBTBP (fiche signalétique, 2010).
L'EBTBP n'est pas répertorié comme un additif alimentaire approuvé dans les listes des additifs alimentaires autorisés, qui ont été incorporés par renvoi dans leurs autorisations de commercialisation respectives en vertu de la Loi sur les aliments et drogues (Santé Canada, [modifié en 2017]), et il n'a pas non plus été défini comme étant utilisé ou présent dans des formulations de matériaux d'emballage des aliments ou comme additif indirect (courriel de la Direction des aliments de Santé Canada au Bureau de gestion du risque de Santé Canada daté de 2013, source non citée). De plus, l'EBTBP n'est inscrit ni dans la base de données sur les produits pharmaceutiques (BDPP, [modifié en 2017]), ni dans la base de données sur les ingrédients non médicinaux interne de la Direction des produits thérapeutiques, ni dans la base de données sur les ingrédients des produits de santé naturels (BDIPSN, [modifié en 2017]), ni dans la base de données sur les produits de santé naturels homologués (BDPSNH, [modifié en 2016]) en tant qu'ingrédient médicinal ou non médicinal dans les produits pharmaceutiques finaux, les produits de santé naturels ou les médicaments vétérinaires (courriel de la Direction des produits thérapeutiques, de la Direction des produits de santé naturels et de la Direction des médicaments vétérinaires de Santé Canada adressé au Bureau de gestion du risque de Santé Canada de 2013, source non citée). Selon la notification soumise aux termes du Règlement sur les cosmétiques à Santé Canada, l'EBTBP ne devrait pas être utilisé dans les produits cosmétiques au Canada (communication personnelle, courriel de la Direction de la sécurité des produits de consommation [Santé Canada], adressés au Bureau de l'évaluation des risques des substances existantes [Santé Canada], daté de 2013, source non citée).
6. Rejets dans l'environnement
Les rejets anthropiques dans l'environnement dépendent de différentes pertes qui surviennent pendant la fabrication, l'utilisation industrielle, l'utilisation commerciale ou par les consommateurs, la durée de vie utile, et l'élimination de la substance.
Selon des renseignements présentés en vertu de l'article 71 (Canada, 2013), l'EBTBP est importé au Canada sous forme pure, en tant que composant de formulation et dans des articles manufacturés (Canada, 2013). Bien qu'elles ne soient pas précisément identifiées par des importateurs de l'EBTBP au Canada, les utilisations prises en compte pour cette substance dans le cadre de la présente évaluation devraient être semblables à celles du DBDPE, en raison des profils d'utilisation communs, seulement à des quantités moins élevées que celui-ci. Par conséquent, les scénarios d'exposition pour l'EBTBP ont été déterminés d'après ceux élaborés pour le DBDPE (voir l'évaluation sur le DBDPE; ECCC, SC, 2018). Les processus suivants ont servi de base à l'élaboration des scénarios d'exposition pour l'EBTBP au Canada : fabrication de textiles, confection de mélanges de caoutchouc, extrusion de plastique, moulage par injection plastique et revêtement de textiles (ECCC, 2017b).
On s'attend à ce que les rejets d'EBTBP dans l'environnement, similaires à ceux de DBDPE, surviennent au cours de la fabrication, de la formulation ou de l'utilisation industrielle dans ces secteurs. Les rejets dans l'environnement devraient, quant à eux, se produire par l'intermédiaire des eaux usées, avec certains rejets provenant de sites industriels et finissant directement dans l'eau. Des rejets dans le sol (c.-à-d. dans les terres agricoles) pourraient également se produire pendant l'épandage de biosolides. En ce qui concerne la migration à partir d'articles manufacturés, cette substance, sous forme d'additif ignifuge bromé mélangé avec un produit polymérique (plutôt qu'un produit ignifuge réactif chimiquement lié à produit polymérique), présente un risque de rejet de produits disponibles aux consommateurs dans l'environnement (Andersson et al., 2006; Guerra et al., 2011). Toutefois, les rejets dans l'environnement par cette voie devraient être minimes et diffus.
Les émissions atmosphériques peuvent donner lieu à des dépôts atmosphériques dans le sol et l'eau. Lorsqu'une substance est transférée accidentellement vers les terres, elle peut pénétrer dans les égouts ou les eaux de surface, ou être transférée par le vent ou la pluie vers le sol proche. Cependant, en raison de la faible volatilité de l'EBTBP, on s'attend à ce que la voie de transport atmosphérique des rejets soit très limitée. Enfin, les sites d'enfouissement qui n'accueillent ni ne traitent leurs lixiviats peuvent rejeter des substances dans le sol ou l'eau de surface, par l'entremise des lixiviats.
Cette information est utilisée pour développer davantage les scénarios de caractérisation de l'exposition afin d'estimer les concentrations environnementales qui en découlent.
7. Devenir et comportement dans l'environnement
La documentation disponible renferme peu de données sur les concentrations de l'EBTBP dans l'environnement canadien. Bien que l'EBTBP ait été importé au pays depuis un certain temps, aucun rapport n'indique que cette substance se retrouve dans l'environnement canadien.
Une seule concentration dans l'environnement est disponible au sein des autres territoires de compétence. On a détecté la présence d'EBTBP à une concentration de 0,035 mg/L dans l'un des trois échantillons répétés d'eaux d'infiltration qui ont été prélevés dans un point de rejet d'une usine de recyclage du métal dans la rivière Loselva, en Norvège (Nyholm et al., 2013).
7.1 Distribution dans l'environnement
On s'attend à ce que l'EBTBP soit rejeté principalement dans les eaux usées, où il devrait être retenu dans les biosolides. Le modèle de fugacité de niveau III (tableau 7-1), utilisant le modèle EQC mis à jour (version 1.0, 2012), a été appliqué en vue de décrire le devenir du DBDPE relativement à ces modes d'entrée possibles dans l'environnement.
| Rejet d'EBTBP dans chaque milieu | Air | Eau | Sol | Sédiments |
|---|---|---|---|---|
| 100 % dans l'air | 0,3 | 0,4 | 90,5 | 8,8 |
| 100 % dans l'eau | Négligeable | 4,6 | Négligeable | 95,4 |
| 100 % dans le sol | Négligeable | Négligeable | 99,8 | 0,2 |
a EQC, version 1.0, 2012.
b Les propriétés physiques et chimiques et les demi-vies (t1/2) de l'EBTBP dans les milieux naturels sont requises aux fins de modélisation et sont disponibles (ECCC, 2017a).
Les résultats du modèle de fugacité de niveau III (EQC, 2012; voir le tableau 7-1) indiquent que l'EBTBP résidera principalement dans la phase solide du milieu dans lequel il est rejeté ou il sera redéposé dans le sol.
Lorsque l'EBTBP est rejeté dans l'air, moins de 0,3 % de cette substance devrait s'y répartir. En phase gazeuse, l'EBTBP se dégrade rapidement à la suite d'une réaction avec des radicaux hydroxyles (t ½ inférieur ou égal à 1 jour) [voir le tableau 7-3] et il se répartira sous forme particulaire dans l'air (c.-à-d., log Koa de 27,52). Par conséquent, on ne s'attend pas à ce que l'EBTBP en phase gazeuse soit transporté dans l'air sur de grandes distances vers des régions éloignées. Les particules se déposent sur le sol et sur l'eau sous forme de dépôts humides et secs. De la quantité transférée de l'air au sol, la majorité (90,5 %) restera dans le sol, tandis qu'une plus petite partie peut être transportée sous forme de ruissellement de surface dans les systèmes aqueux; en outre, lorsqu'elle est combinée aux apports atmosphériques, elle représente environ 8,8 % de la fraction massique dans les sédiments.
Le modèle de dépistage de l'OCDE (LTRP POPs) peut être utilisé pour identifier les produits chimiques à fort potentiel de persistance et de transport à grande distance (Scheringer et al., 2009). La distance de parcours caractéristique (DTC) calculée pour l'EBTBP à l'aide du modèle de l'OCDE est de 2 860 km, ce qui indique que l'EBTBP a un fort potentiel de transport dans l'air (avec 100 % de la masse dans l'air répartie dans des particules et des aérosols), mais cette distance est inférieure à la limite (5 097 km, DTC des PCB 28) proposée pour les polluants mondiaux par Klasmeier et al., (2006). Le modèle calcule également une persistance globale (Pglob) de 547 jours ainsi que l'efficacité de transfert (ET), qui est le pourcentage du flux d'émissions dans l'air qui se déposent à la surface (eau ou sol) dans la région éloignée. L'ET calculée pour l'EBTBP était de 12,7 %, ce qui est supérieur à la limite de 2,248 % (PCB-28). L'efficacité du transfert élevée indique que l'EBTBP devrait se déposer dans une certaine mesure à la surface de la Terre dans des régions éloignées.
Quelques produits ignifuges organiques, comme certains polybromodiphényléthers (PBDE), sont ou seraient fort probablement transportés à grande distance dans l'air en association avec des particules fines en suspension (Harner et Shoeib, 2002; Muir et al., 2006). En règle générale, tandis que l'EBTBP (d'après les propriétés physiques et chimiques et les données de modélisation) ne devrait pas constituer une préoccupation importante vis-à-vis du transport à grande distance, si l'on examine la forte efficacité de transport prévue, le rôle du transport de la substance liée à des particules (aérosols) laisse croire que le transport à grande distance de l'EBTBP serait possible.
Les résultats du programme AEROWIN (version 1.00) et du modèle de dépistage (POPs) de l'OCDE semblent indiquer que la totalité de la fraction rejetée dans l'air sera associée à la phase particulaire, en grande partie en raison de la valeur élevée du log Koa estimée. De plus, la persistance globale de 547 jours, dans les aérosols (6,5 heures en phase gazeuse) estimée par le modèle de dépistage (POPs) de l'OCDE indique que la photodégradation de l'EBTBP pourrait être négligeable ou grandement diminuée. Toutefois, les estimations modélisées de la distance de parcours caractéristique (DTC), de la persistance globale et du rendement thermique pour cette substance ne sont pas fiables en raison des incertitudes associées aux principaux coefficients de partage modélisés (Koa, Koe, Kae) requis à titre d'intrants.
Lorsque l'EBTBP est rejeté dans les eaux de surface, la grande majorité (95 %) devrait s'adsorber fortement dans les matières solides en suspension puis se déposer éventuellement dans les sédiments. La volatilisation à partir de l'eau de surface dans l'air est très faible. Ainsi, la perte d'EBTBP dans les systèmes aqueux serait principalement attribuable à l'enfouissement dans les sédiments et à la biodégradation qui devrait être très lente (voir les tableaux 7-2 et 7-3).
Lorsque l'EBTBP est rejeté dans le sol, la plus grande partie de la fraction massique (99,9 %) devrait s'adsorber au sol en raison de la nature très hydrophobe de la substance. L'évaporation de la substance à partir du sol dans l'air n'est pas prévue, compte tenu de sa très faible pression de vapeur. En outre, l'EBTBP devrait être très stable dans le sol et résistant à la minéralisation (t ½ supérieur à 182 jours) [voir les tableaux 7-2 et 7-3]. Par conséquent, le processus de perte dans le sol sera entraîné principalement par l'enfouissement dans le sol ou le ruissellement de surface, comme il est mentionné ci-dessus.
7.2 Persistance dans l'environnement
D'après les rejets probables de l'EBTBP et ses caractéristiques de répartition, la persistance de cette substance dans l'environnement est la plus pertinente pour le sol et les sédiments, où la plus grande partie de la substance devrait se retrouver. Toutefois, en raison du transport potentiel de l'EBTBP en phase particulaire dans l'air et l'eau, tous les milieux sont analysés dans la présente section. Des données empiriques et modélisées ont été prises en compte dans le poids de la preuve pour la persistance de l'EBTBP. Des données ont également été comparées à des données de l'analogue DBDPE.
Les résultats des données de biodégradation empiriques et modélisées indiquent que la demi-vie dans l'eau prévue devrait se situer entre quelques mois à peut-être plus d'un an. En outre, l'EBTBP serait très stable dans le sol et les sédiments, et il est susceptible de présenter des expositions à long terme au sein de ces milieux.
Les tableaux 7-2 et 7-3 présentent des données de dégradation empiriques et modélisées pour l'EBTBP.
7.2.1 Données empiriques sur la persistance
Le tableau 7-2 présente les données empiriques sur la dégradation de l'EBTBP. La documentation disponible contient peu de données empiriques sur la persistance de l'EBTBP; par conséquent, les données sur la persistance du DBDPE sont également prises en compte à titre de données déduites à partir d'analogues de l'EBTPB (également présentées au tableau 7-2).
Une étude sur la biodégradation aérobie menée par le Chemical Biotesting Center au Japon a été rapportée par Albemarle Corporation (US EPA, 2004; US EPA, 2012). Un essai de biodégradation rapide conforme aux lignes directrices en vigueur (MITI) a été effectué au Japon en 1981. Lors de cette étude, des boues activées standard ont été inoculées avec 100 mg/L d'EBTBP puis intubées à une température de 25 ± 1 °C pendant une durée de contact de 14 jours. Au 28e jour, la valeur de la demande biochimique en oxygène (DBO) était de 0 %. Par conséquent, on a déterminé que l'EBTBP n'était pas facilement biodégradable lors de cette étude.
| Substance | Milieu | Processus du devenir | Valeur pourla dégradation | Paramètre et unités de la dégradation | Méthode | Référence |
|---|---|---|---|---|---|---|
| EBTBP | Boues activées standard | Essai de biodégradation rapide (biodégradation aérobie) | 0% | % dégradation par DBO ou UV après 28jours | Étude301C de l'OCDE (essai MITI modifié) | US EPA, 2004; US EPA, 2012 |
| DBDPE | Boues activées | Biodégradation | 2% | Biodégradation à 28jours, DBO/% | Étude301C de l'OCDE (essai MITI modifié) | CITI, 1991 |
| DBDPE | Milieu aqueux renfermant des sels minéraux | Biodégradation | 2,2% | Biodégradation à 90jours/% | Étude302D de l'OCDE (essai CONCAWE) | Schaefer et Carpenter, 2010 |
| DBDPE | Biosolides de la digestion anaérobie | Minéralisation biotique/ abiotique anaérobie | 0 (biotique) 0 (abiotique) | Minéralisation anaérobie de 63jours /% | Étude314c de l'OCDE (biosolides de digestion anaérobies) | Schaefer et Matthews, 2011 |
aDes sommaires de rigueur d'étude ont été menés pour l'EBTBP afin de déterminer la qualité de l'étude, et sont fournis en annexe (pour des études critiques) ou sont disponibles sur demande.
Dans l'ensemble, les données de biodégradation empiriques immédiates disponibles pour le DBDPE indiquent également un taux de biodégradation égal à ou proche de 0 % après 28 jours (US EPA, 2004; US EPA, 2014). Compte tenu des données sur la persistance disponibles pour l'EBTBP et le DBDPE, on peut conclure que l'EBTBP est résistant à la biodégradation. En outre, ces études n'ont démontré aucun élément probant concernant l'hydrolyse, et cela est corroboré par l'absence de groupements fonctionnels hydrolysables dans les molécules.
Deux produits de décomposition prévus de l'EBTBP, à des quantités de 0,1257 et de 0,1745 mol/1 mol d'origine sont identifiés par CATALOGIC, 2012. Toutefois, ces quantités sont jugées négligeables.
7.2.2 Modélisation de la persistance
Le tableau 7-3 résume les résultats des modèles de prévision QSAR disponibles sur la dégradation dans divers milieux naturels.
Une méthode du poids de la preuve reposant sur des QSAR a aussi été utilisée avec les modèles de dégradation indiqués dans le tableau 7-3. Étant donné l'importance écologique du sol et des sédiments et le fait que l'EBTBP devrait demeurer principalement dans ces milieux, il est jugé raisonnable et pertinent d'examiner la biodégradation dans le sol et les sédiments.
La probabilité de biodégradation n'a pu être obtenue grâce au modèle TOPKAT (2004), car les résultats se situent en dehors de l'intervalle de prévision optimal ou du domaine structurel du modèle. Par conséquent, ces résultats ne sont pas cités ici puisqu'ils ne sont pas considérés comme étant fiables. De plus, puisque le modèle CATALOGIC (2012) n'a pas reconnu 56 % des fragments de l'EBTBP, on juge que cette estimation est peu fiable. Toutefois, les modèles TOPKAT et CATALOGIC semblent indiquer des taux de minéralisation extrêmement lents à partir de la biodégradation, qui correspondent à ceux des données empiriques et d'autres modèles (tableau 7-3). Les données sur la persistance prévues (modélisées) tirées du sous-modèle 3 : enquête d'expert BIOWIN, du sous-modèle 5 : MITI, probabilité linéaire BIOWIN et du sous-modèle 6 : MITI, probabilité non linéaire BIOWIN semblent indiquer que l'EBTBP est très stable dans l'eau.
En résumé, les résultats des données de biodégradation empiriques et modélisées indiquent que la demi-vie dans l'eau prévue devrait se situer entre quelques mois à peut-être plus d'un an. Environnement Canada a adopté une procédure d'extrapolation des demi-vies d'après Boethling et al., (1995) en utilisant un ratio de 1:1:4 pour les demi-vies de biodégradation dans l'eau, le sol et les sédiments. Les résultats de cette méthode indiquent que l'EBTBP serait également très stable dans le sol et les sédiments et qu'il est susceptible de présenter des expositions à long terme au sein de ces milieux.
| Processus du devenir | Modèle et base du modèle | Résultat et prévision du modèle | Demi-vie extrapolée (jours) |
|---|---|---|---|
| Oxydation atmosphérique (air) | AOPWIN, 2010a,e | t1/2 = 0,271jour | ≤ 2 |
| Réaction avec l'ozone (air) | AOPWIN, 2010a | S.O.b | S.O. |
| Hydrolyse (eau) | HYDROWIN, 2010a | S.O.b | S.O. |
| Biodégradation primaire (aérobie) | BIOWIN, 2010a Sous-modèle 4: enquête d'expert (résultats qualitatifs) |
1,2469c «récalcitrant» | ≥ 182 |
| Biodégradation ultime (aérobie) | BIOWIN, 2010a Sous-modèle 3: enquête d'expert (résultats qualitatifs) |
0,0085c «récalcitrant» | ≥ 182 |
| Biodégradation ultime (aérobie) | BIOWIN, 2010a Sous-modèle5: Probabilité linéaire MITI |
-0,6854d «ne se biodégrade pas rapidement» | ≥ 182 |
| Biodégradation ultime (aérobie) | BIOWIN, 2010a Sous-modèle6: Probabilité non linéaire MITI |
0,0000d «ne se biodégrade pas rapidement» | ≥ 182 |
| Biodégradation ultime (aérobie) | TOPKAT, 2004 Probabilité |
0,000d «se biodégrade très lentement» | ≥ 182 |
| Biodégradation ultime (aérobie) | CATALOGIC, 2012 Pourcentage de la DBO (demande biochimique en oxygène) |
% DBO = 9,5 «se biodégrade très lentement» Demi-vie ultime: 6 mois et 13 jours | ≥ 182 |
a EPI Suite, version 4.1. (2012)
b Le modèle ne donne pas d'estimation pour ce type de structure.
c Le résultat s'exprime par une valeur numérique de 0 à 5.
d Le résultat s'exprime par un taux de probabilité.
e 8 760 heures plutôt que 6 mois et 13 jours (CATALOGIC, 2012). La prévision du modèle EPIWIN de 4 320 heures est choisie à titre d'intrant du modèle pour la demi-vie visée par la présente évaluation, pour une période de biodégradation de plus de 6 mois.
7.3 Produits de transformation potentiels
Il n'existe aucune donnée probante empirique concernant les dérivés potentiels de l'EBTBP. On pourrait émettre une hypothèse selon laquelle une transformation pourrait survenir en raison d'une débromation (p. ex. semblable au décaBDE) ou d'un clivage de noyaux suivi d'une débromation ou de toute autre voie inconnue. Cependant, l'EBTBP renferme un pont imide entre les deux noyaux, contrairement au DBDPE et au décaBDE. Cela semble démontrer une sensibilité à la biodégradation et au clivage de noyaux, contrairement à la voie de débromation prévue pour le DBDPE ou le décaBDE (ECCC, SC, 2018; Environnement Canada, 2010).
Les dérivés de biodégradation prévus de l'EBTBP, par clivage de noyaux à une quantité de 0,01635 mol/1 mol d'origine, entraînent éventuellement la formation d'un produit de dégradation, l'acide 4,5-dibromophtalique (C8H4Br2O4; no CAS 24063-28-3), à une quantité de 0,6595 mol/1 mol d'origine; ils sont identifiés par CATALOGIC, 2012. La modélisation des QSAR avait prévu que cet acide phtalique bromé possède un faible potentiel de bioaccumulation (FBA de 6,177 L/kg ph chez le poisson de niveau trophique intermédiaire) ainsi qu'une toxicité inhérente faible à modérée (toxicité chronique estimée de 16,261 mg/L chez la mysis effilée).
7.4 Bioaccumulation
Lors de la discussion sur le potentiel de bioaccumulation, on a examiné plusieurs paramètres potentiels, y compris les propriétés de la substance (c.-à-d. log Koe, log Koa, taille moléculaire et diamètres transversaux), ainsi que le facteur de bioconcentration (FBC), le facteur de bioamplification (FBM), le facteur d'amplification trophique (FAT) et le facteur de bioaccumulation (FBA). En outre, on étudie la dérivation ainsi que le rôle des constantes du taux de métabolisme dans le calcul du potentiel de bioaccumulation.
7.4.1 Propriétés physiques et chimiques
Compte tenu des valeurs modélisées de log Koe (8,9) et de log Koa (5,34) élevées, on s'attend à ce que l'EBTBP présente une forte propension à être adsorbé dans les solides tels que les sédiments/particules en suspension et le sol, ce qui entraîne la formation de résidus cutanés dans l'environnement. Il est possible que ce taux d'adsorption limite la biodisponibilité de cette substance, particulièrement pour les organismes aquatiques. En outre, en raison de la valeur de log Koe élevée, on s'attend à ce que l'EBTBP présente une faible efficacité de l'assimilation par le tractus gastro-intestinal (Kelly et al., 2004). Malgré certaines incertitudes quant aux coefficients de partage estimés, il est raisonnable de présumer que l'EBTBP est fortement hydrophobe et qu'il présente une valeur de log Koe élevée, d'après un examen de sa structure chimique (c.-à-d. aucun groupement fonctionnel solubilisant dans l'eau et présence de multiples atomes halogènes.
7.4.2 Bioaccumulation déterminée de manière empirique
7.4.2.1 Facteur de bioconcentration (FBC)
Une étude de bioconcentration à deux concentrations dans l'eau menée chez les poissons (tableau 7-4) a été rapportée par Albemarle Corporation (2004). L'étude a permis de conclure que l'EBTBP ne présentait aucun potentiel de bioconcentration chez les poissons (Cyprinus carpio) lors d'un essai de plus de huit semaines. À la concentration la plus élevée de l'essai, soit 2 mg/L, on a obtenu un FBC de 1,3 lorsque la Cyprinus carpio (carpe d'eau douce) était exposée à l’EBTBP pendant 56 jours à 25 °C. À la concentration la plus faible de l'essai, soit 0,2 mg/L, on a obtenu un FBC inférieur à 3,3 à la suite d'une exposition de la Cyprinus carpio. Cette étude a été réalisée conformément aux lignes directrices du MITI, et la pureté de la substance d'essai était supérieure ou égale à 99 %. Le HCO-40 a été utilisé pour disperser la matière d'essai dans l'eau. Toutefois, les concentrations du traitement dans le cadre de cet essai sont plus élevées que l'hydrosolubilité de l'EBTBP. Par conséquent, ces essais sont jugés peu fiables, ce qui rend l'interprétation des FBC calculés plus difficile. Bien que les données expérimentales sur le FBC disponibles pour l'EBTBP aient été testées à des concentrations supérieures à la limite d'hydrosolubilité de la substance (0,00413 mg/L), on peut raisonnablement conclure que les études ont démontré un niveau très faible de bioconcentration chez les poissons.
Bien que cette étude semble indiquer un faible potentiel de bioconcentration à partir de l'eau pour la substance, on s'attend à ce que le régime alimentaire et les solides constituent des voies d'exposition plus pertinentes chez les poissons, compte tenu de la nature hydrophobe de cette substance.
| Organisme d'essai | valeur à l'état stable (L/kg)a,b | Référence |
|---|---|---|
| Carpe d'eau douce Cyprinus carpio | < 0,3 à 1,3 (2 mg/L) | Albemarle Corporation, 2004 |
| Carpe d'eau douce Cyprinus carpio | < 3,3 (0,2 mg/L) | Albemarle Corporation, 2004 |
a Les valeurs entre parenthèses représentent les concentrations d'essai auxquelles les FBC ont été obtenus.
b Des sommaires de rigueur d'étude ont été menés afin de déterminer la qualité de l'étude, et sont fournis en annexe (pour des études critiques) ou sont disponibles sur demande.
Les données sur la taille moléculaire et les diamètres transversaux peuvent être utiles et sont couramment utilisées par des compétences internationales, comme l'Union européenne (ECHA, 2014), pour tirer des conclusions sur le potentiel de bioaccumulation suivant la méthode du poids de la preuve. De récentes études faisant le lien entre les données de FBC chez les poissons et les paramètres de taille moléculaire (Dimitrov et al., 2002 et 2005) laissent entendre que la probabilité qu'une molécule traverse la membrane cellulaire par diffusion passive diminue de façon importante à mesure qu'augmente le diamètre maximal (Dmax). La probabilité de diffusion passive diminue de façon notable lorsque le diamètre maximal est supérieur à environ 1,5 nm et diminue de façon encore plus significative dans le cas des molécules ayant un diamètre maximal supérieur à 1,7 nm. Sakuratani et al. (2008) ont également étudié l'effet du diamètre transversal sur la diffusion passive dans un ensemble d'essais de FBC d'environ 1 200 substances chimiques nouvelles et existantes. Ils ont observé que les substances qui ne présentent pas un potentiel de bioconcentration très élevé (FBC inférieur à 5 000) ont souvent un Dmax supérieur à 2,0 nm et un diamètre effectif (Deff) supérieur à 1,1 nm.
Comme l'ont évoqué Arnot et al. (2010), il existe des incertitudes quant aux seuils proposés par Dimitrov et al. (2002, 2005) et Sakuratani et al. (2008), étant donné que les études sur le FBC utilisées pour calculer ces seuils n'ont pas fait l'objet d'évaluations critiques. Arnot et al. (2010) ont souligné que la taille moléculaire a un effet sur la solubilité et la capacité de diffusion dans l'eau et dans les phases organiques (membranes), et que les plus grosses molécules peuvent avoir un taux d'absorption plus lent. Toutefois, ces mêmes contraintes liées aux cinétiques s'appliquent aux voies de diffusion de l'élimination chimique (c.-à-d. absorption lente = élimination lente). Un potentiel de bioaccumulation important peut donc s'appliquer aux substances qui sont soumises à un processus d'absorption lent, si elles sont biotransformées ou éliminées lentement par d'autres processus.
D'après l'analyse tridimensionnelle de 30 conformères de l'EBTBP calculés à l'aide du modèle de FBCmax avec des facteurs d'atténuation (Dimitrov et al., 2005), le diamètre maximal de l'EBTBP est compris entre 1,48 nm et 2,01 nm, tandis que le diamètre effectif est de 1,02 nm. Cela laisse supposer que l'EBTBP est plus susceptible de connaître un taux d'absorption réduit découlant d'effets stériques à la surface des branchies, ce qui permettrait aux processus d'élimination d'atténuer l'accumulation. Cela pourrait expliquer, en partie, les faibles valeurs empiriques observées pour le FBC.
7.4.2.2 Facteur de bioamplification (FBM)
Les valeurs du FBM décrivent le processus dans lequel la concentration d'un produit chimique dans un organisme atteint un niveau qui est supérieur à celui dans l'alimentation de l'organisme, en raison de l'absorption alimentaire (Gobas et Morrison, 2000). Au moment de la présente analyse, aucune étude expérimentale sur le FBM n'a été recensée dans la documentation disponible.
7.4.2.3 Facteur d'amplification trophique (FAT)
Le facteur d'amplification trophique (FAT) est une mesure du potentiel de bioamplification d'une substance au sein d'un réseau trophique étudié dans des conditions naturelles. Ce facteur est estimé en mettant en corrélation des concentrations de substance normalisées dans le biote à différents niveaux trophiques. Aucune valeur de FAT n'était disponible dans la documentation pour le EBTBP au moment de la présente analyse.
7.4.2.4 Facteur de bioaccumulation (FBA)
Les facteurs de bioaccumulation sont mesurés dans des conditions naturelles en tant que rapport entre les charges de substance chimique absorbées dans le corps entier découlant de toutes les expositions et les concentrations se trouvant dans l'eau ambiante. Le calcul du FBA est une mesure préconisée pour évaluer le potentiel de bioaccumulation des substances, car il intègre toutes les expositions à la substance chimique, y compris l'exposition alimentaire qui prédomine pour les substances présentant un log Koe supérieur à 4, environ (Arnot et Gobas, 2003a).
Aucune donnée empirique sur le FBA n'était disponible pour l'EBTBP.
7.4.3 Bioaccumulation modélisée
Arnot et Gobas (2006) ont évalué de façon critique les données de bioaccumulation accessibles (FBC et FBA) pour les poissons et d'autres organismes et ils ont créé une base de données empiriques de valeurs de FBC et de FBA de qualité que le Canada a utilisée pour la catégorisation de la LIS, et qu'il utilise actuellement pour les évaluations préalables en vertu du Plan de gestion des produits chimiques (Arnot et Gobas, 2003b). Dans la base de données d'Arnot et Gobas (2006) et la propre base de données d'Environnement Canada sur les FBC/FBA, la distribution empirique des données « acceptables » de FBC et de FBA des poissons montre qu'il n'existe pratiquement aucune valeur enregistrée pour la substance dont le log Koe est supérieur à environ 8,2 (c.-à-d. seulement un ou deux biphényles hautement halogénés). La mesure d'un log Koe supérieure à 8 et sa concordance avec d'autres propriétés deviennent de plus en plus incertaines en raison de la difficulté à mesurer précisément des propriétés de partitionnement pour des composés superhydrophobes. De plus, le peu d'essais sur le FBC réalisés au-delà de cette limite ont toujours utilisé un agent solubilisant, ce qui réduit la force d'inférence de l'essai. Enfin, la relation entre l'efficacité d'absorption alimentaire d'une substance et son log Koe a été étudiée par différents auteurs et résumée dans la publication de Kelly et al. (2004).
Kelly et al. (2004) ont démontré que l'absorption du produit chimique par voie orale chez des poissons (et d'autres espèces sauvages) diminue avec l'augmentation du log Koe à partir de 7 à 7,5 environ, car la diffusion de substances hydrophobes, telles que l'EBTBP, à travers une couche d'eau non agitée vers la membrane luminale (c.-à-d. tractus gastro-intestinal) d'un organisme limite les taux d'un log Koe très élevé et d'une hydrosolubilité très faible dans les couches d'eau. Même si Arnot et Gobas (2003a, 2004, 2006) déclarent que le domaine de log Koe du modèle varie de 1 à 9, on considère qu'il y a suffisamment de preuves empiriques sur le terrain (p. ex., FBA) pour appuyer les estimations modélisées dépassant le log Koe de 8,2. Ainsi, le log Koe de 8,90 pour l'EBTBP est considéré comme étant hors du domaine du modèle pour le bilan massique du modèle BCFBAF sur trois niveaux trophiques (Arnot et Gobas, 2003a) et du modèle QSAR de Dimitrov et al. (2005). Plus important encore, le manque de données empiriques sur le facteur de bioconcentration et le facteur de bioaccumulation pour des produits chimiques dont le log Koe est supérieur à 8,3 ne permet pas d'effectuer une analyse comparative de données de référence liées aux résultats prévus. Ainsi, l'EBTBP n'a pas été modélisé dans la présente évaluation.
En résumé, les données empiriques sur le potentiel de bioaccumulation de l'EBTBP sont limitées, et la valeur de log Koe élevée de l'EBTBP a empêché la modélisation BCF/BAF. Les propriétés physiques et chimiques de l'EBTBP semblent indiquer que cette substance présentera une biodisponibilité limitée dans l'environnement en raison de son log Koe élevé, de sa faible hydrosolubilité et de son potentiel élevé de formation de résidus liés. On a observé une faible bioconcentration même lorsque la biodisponibilité était accrue, comme lors des essais sur le FBC menés par le Japon. Néanmoins, le manque d'autres mesures de bioaccumulation effectuées sur le terrain (comme le FBM ou le FAT) et le manque de capacité de modélisation semblent indiquer qu'il existe toujours certaines incertitudes, particulièrement en ce qui a trait au potentiel de bioamplification. On considère que l'EBTPB présente un potentiel de bioconcentration et de bioamplification limité dans l'environnement, ce qui atténuera la charge corporelle de cette substance dans les organismes et diminuera son potentiel d'écotoxicité global.
7.5 Résumé du devenir dans l'environnement
L'EBTBP devrait être rejeté à partir de sources industrielles, principalement par des eaux usées. Une forte tendance d'adsorption en phase solide dans divers milieux (y compris des particules en suspension dans l'air) indique que cette substance chimique résidera dans des biosolides, des sédiments et des particules en suspension dans l'air et qu'elle sera transférée du sol à partir de dépôts secs et de l'épandage de biosolides sur des terres. L'exposition aux organismes vivant dans l'eau devrait être minime. La persistance intrinsèque élevée de l'EBTBP laisse entendre que des expositions à long terme peuvent être attendues dans les sédiments et le sol, avec un potentiel d'accumulation important dans les milieux environnants, découlant d'émissions continues. Le processus d'élimination de l'environnement devrait inclure l'enfouissement dans les sédiments et le sol. L'EBTBP devrait subir un transport à grande distance dans l'air et se déposer dans des milieux éloignés en raison du transport de particules, comme cela s'est produit avec d'autres produits ignifuges hydrophobes. Même avec une exposition à long terme à l'EBTBP dans des milieux terrestres et aquatiques, cette substance ne devrait pas être hautement biodisponible; ainsi, les niveaux de résidus dans les tissus des organismes et la migration dans les réseaux trophiques ne devraient pas être importants.
8. Potentiel d'effets nocifs sur l'environnement
8.1 Évaluation des effets sur l'environnement
Des données empiriques pour l'EBTBP et de l'analogue structurel DBDPE ont été prises en compte dans le poids de la preuve pour évaluer les effets écologies de l'EBTBP.
Les données empiriques limitées sur la toxicité, disponibles pour l'EBTBP indiquent un faible niveau de toxicité aiguë pour les organismes aquatiques et les mammifères (rongeurs). Compte tenu du manque de données empiriques sur les effets de l'EBTBP, les études portant sur le DBDPE ont également été prises en compte. L'ensemble de données disponibles sur la toxicité du DBDPE comprend les valeurs des critères d'effet pour les espèces aquatiques, terrestres ou vivant dans les sédiments. Dans l'ensemble, on s'attend à ce que l'EBTBP présente un faible degré de toxicité pour les organismes aquatiques en raison de son log Koe élevé (8,90) et de son hydrosolubilité très faible (2,88 x 10-7 mg/L), qui indiquent une faible biodisponibilité et une absorption alimentaire limitée pour cette substance.
Même si l'on a utilisé la modélisation grâce à ECOSAR (2012) pour l'EBTBP, les prévisions relatives à la toxicité aiguë et chronique n'ont pas été jugées fiables et ne sont pas présentées ici, car la valeur du log Koe de cette substance se trouve en dehors du champ d'application. Les limites proposées dans le modèle ECOSAR pour le champ d'application du log Koe à l'égard des prévisions relatives à la toxicité aiguë et à la toxicité chronique sont respectivement d'environ 5,0 et de 8,0.
Les résultats de la modélisation du devenir indiquent que les quantités négligeables d'EBTBP rejetées dans l'eau demeureront dans l'eau et, selon le milieu de rejet, la majeure partie se déposera dans les sédiments ou le sol. En ce qui concerne la fraction qui demeure dans l'eau (inférieur à 5 %), les valeurs modélisées élevées du log Koe et du log Koc ainsi que la très faible hydrosolubilité limiteront la biodisponibilité de la substance dans les organismes pélagiques. D'après les données limitées sur la toxicité aiguë (abordées dans la section « Études empiriques pour le milieu aquatique »), l'EBTBP ne devrait avoir aucun effet à la concentration de saturation dans l'eau. Pour ces raisons, les concentrations estimées sans effet (CESE) ont été calculées pour les sédiments et le sol, mais non pour l'eau.
8.1.1 Études empiriques pour le milieu aquatique
Albemarle a observé une toxicité à court terme (CL50) supérieure à 500 mg/L après 48 heures chez le médaka (Oryzias latipes), un poisson d'eau douce (Commission européenne, 2000a). L'étude a été réalisée conformément aux lignes directrices du MITI, et la pureté de l'EBTBP était supérieure ou égale à 99 %. On n’a constaté aucun effet à la concentration de saturation dans l'eau, et la concentration de traitement est plus élevée que la limite d'hydrosolubilité pour l'EBTBP par plusieurs ordres d'importance dans cette étude. Par conséquent, cette étude n'est pas jugée fiable et n'est donc pas prise en compte dans le cadre de la présente évaluation. On n'a trouvé aucune autre donnée empirique sur la toxicité pour les organismes aquatiques dans la documentation disponible. En ce qui a trait à son analogue, le DBDPE, on constate d'importantes incertitudes quant aux études empiriques sur la toxicité pour les organismes aquatiques disponibles. En outre, ces études étaient caractérisées par des concentrations de traitement supérieures à la limite d'hydrosolubilité du DBDPE, attribuables à l'utilisation d'agents solubilisants, ou les résultats n'indiquaient aucun effet à la concentration de saturation.
8.1.2 Études empiriques concernant d'autres milieux naturels
Il n'existe aucune autre donnée empirique sur la toxicité de l'EBTBP pouvant être prise en considération dans le cadre de la présente évaluation. L'ensemble de données disponibles sur la toxicité du DBDPE comprend les valeurs des critères d'effet pour les organismes benthiques et vivant dans le sol. D'après les résultats de l'essai de toxicité chronique dans les sédiments et le sol, le DBDPE, à des concentrations élevées dans le sol, a le potentiel d'entraîner des effets sur la reproduction des lombrics et d'avoir une incidence sur la survie et la croissance des plantes (Aufderheide, 2003; Hardy et al., 2011).
Des essais de toxicité sur des organismes vivant dans des sédiments ont été effectués pour l'analogue de l'EBTBP, le DBDPE, chez des chironomidés (Chironomus riparius) et des oligochètes (Lumbriculus variegates) (Krueger et al., 2003a, b; Hardy et al., 2012) (tableau 8-1). Les chironomidés (moucherons) ont été exposés au DBDPE dans des sédiments avec de l'eau sus-jacente pendant 28 jours dans des conditions statiques. Dans les essais sur les oligochètes, dix oligochètes par concentration d'essai ont été exposés au DBDPE pendant 28 jours dans des conditions de renouvellement continu. Dans les deux études, des effets potentiels ont été relevés, mais les paramètres n'ont pas montré d'effet important. Par conséquent, les valeurs de CE50 et les CSEO pour tous les paramètres mesurés étaient supérieures au plus fort niveau de concentration supérieure à 5 000 mg/kg pour les études sur les chironomidés et les oligochètes. Étant donné que les sédiments d'essai contenaient 1,8 % de carbone organique, la « solubilité » maximale (ECCC, 2017b) du DBDPE dans les sédiments était supérieure à 298 mg/kg de poids sec (ps). Ainsi, il se peut que la limite de solubilité dans les sédiments ait été dépassée dans les conditions de l'étude, bien qu'aucun effet nocif n'ait été observé dans les organismes d'essai. Par conséquent, une valeur critique de toxicité de 5 000 mg/kg est choisie pour l'EBTBP dans des sédiments, représentant le seul paramètre de toxicité de l'EBTBP disponible, bien que cette valeur ne soit liée à aucun effet observé à cette concentration.
| Organisme d'essai | Type d'essai | Paramètre | Valeur (mg/kg ps) | Référence |
|---|---|---|---|---|
| Moucheron (Chironomus riparius) | Toxicité prolongée dans les sédiments: survie, émergence et développement | CE50 après 28jours CMEO CSEO |
> 5000 > 5000 5000 |
Krueger et al., 2003a, Hardy et al., 2012 |
| Oligochète (Lumbriculus variegates) | Toxicité prolongée dans les sédiments: survie et croissance | CE50 après 28jours CMEO CSEO |
> 5000 > 5000 > 5000 |
Krueger et al., 2003b, Hardy et al., 2012 |
Abréviations : CE, concentration entraînant un effet; CMEO, concentration minimale avec effet observé; CSEO, concentration sans effet observé
Des essais de toxicité dans le sol pour l'analogue de l'EBTBP, le DBDPE, ont été effectués avec des eaux usées et des bactéries du sol, des lombrics et des plantes (Hardy et al., 2011) (tableau 8-2). Les effets du DBDPE sur l'émergence et la croissance de plantules terrestres ont été évalués par Hardy et al. (2011) dans une étude de 21 jours. Le maïs (Zea mays), l'oignon (Allium cepa) et l'ivraie vivace (Lolium perenne) représentaient les monocotylédones, tandis que le concombre (Cucumis sativa), le soya (Glycine max) et la tomate (Lycopersicon esculentum) représentaient les dicotylédones. Aucun effet nocif sur un paramètre n'a été signalé pour le maïs, l'ivraie vivace ou le soya, donnant des valeurs de CE25 supérieures à 6 250 mg/kg. La survie moyenne du groupe des concombres a été réduite de 18 % à la plus forte concentration (CSEO = 6 250, CSEO = 3 125 mg/kg). Des réductions de 22 % et de 24 % de la haute moyenne de plants d'oignons, et de 32 % et 30 % de leur poids ont été observées aux deux plus fortes concentrations (CMEO = 3 125, CSEO = 1 563 mg/kg). Des effets sur la hauteur et le poids de plants de tomates à la plus forte concentration du DBDPE ont entraîné des réductions de 37 % et 40 % comparativement aux témoins (CMEO = 6 250, CSEO = 3 125 mg/kg). Une CE25 de 2 440 mg/kg a été déclarée pour l'oignon.
| Organisme d'essai | Type d'essai | Paramètre | Valeur (mg/kg ps) | Référence |
|---|---|---|---|---|
| Lombrics (Eisenia fetida) | Essai de survie de 28 jours | CL50 | > 3720 | Aufderheide, 2003 |
| Lombrics (Eisenia fetida) | Essai de reproduction de 56 jours | CE10 CE50 CMEO CSEO |
1860 3180 3720 (reproduction réduite de 60%) 1910 |
Aufderheide, 2003 |
Plantes: monocotylédones Oignon (Allium cepa) |
21 jours Survie/reproduction | CMEO CSEO CE25 |
3091 (3125 – valeur nominale) 1722 (1563 – valeur nominale) 2440 (réduction de la hauteur de 22% et 24% à 3125; réduction du poids de 32% et 30% à 6250, respectivement) |
Porch et Krueger, 2005 |
Plantes: dicotylédones Tomate (Lycopersicon esculentum) |
21 jours Survie/reproduction | CMEO CSEO CE25 |
6076 (6250 – valeur nominale) 2677 (3125 – valeur nominale) 4990 (réduction de la hauteur de 37% et réduction du poids de 40% à 6250) |
Porch et Krueger, 2005 |
Abréviations : CL, concentration létale;
CE, concentration entraînant un effet;
CMEO, concentration minimale avec effet observé;
CSEO, concentration sans effet observé
Dans les études sur toxicité dans le sol, la plus faible concentration à laquelle un effet évident a été signalé est la valeur de CE10 pour la reproduction du lombric de 1 860 mg/kg de DBDPE dans le sol, et la CE25 pour la baisse du poids de plants d'oignons de 2 440 mg/kg (CSEO dans l'oignon = 1 563 mg/kg, mais de faibles valeurs de CE sont privilégiées par rapport à des valeurs de CSEO). Aux fins de la présente évaluation, la valeur de 2 440 mg/kg (CE25 pour la baisse du poids de plants d'oignons de 2 440 mg/kg) est choisie comme valeur critique de toxicité (VCT) pour l'EBTBP.
8.1.3 Calcul des concentrations estimées sans effet
La seule étude empirique disponible pour l'EBTBP a été effectuée en utilisant une valeur largement supérieure à la limite d'hydrosolubilité, remettant ainsi en cause l'utilité de ce résultat. De plus, les prévisions du modèle de toxicité pour les organismes aquatiques ne sont pas fiables et ne peuvent être utilisées pour calculer la CESE prévue. Cependant, compte tenu de la faible hydrosolubilité prévue de l'EBTBP (2,88 x 10-7 mg/L) et du log Koe élevé (8,90), on s'attend à ce que l'exposition par l'eau soit minimale et bien moins appropriée que l'exposition dans le sol et les sédiments. Pour cette raison, aucune CESE n'est déterminée pour l'EBTBP à l'égard des organismes pélagiques.
En ce qui concerne les sédiments, il existe peu de données énonçant clairement les concentrations avec effet chez les organismes pour l'analogue de l'EBTBP, le DBDPE. Des essais de toxicité sur des organismes vivant dans des sédiments ont été effectués pour le DBDPE chez des chironomidés (Chironomus riparius) et des oligochètes (Lumbriculus variegates) (Krueger et al., 2003a, b). Lors de ces deux études, des effets ont été observés seulement à des concentrations d'essai très élevées, c'est-à-dire largement supérieures à celles prévues dans l'environnement. Les valeurs de CE50 et les CSEO pour tous les paramètres mesurés étaient supérieures au plus fort niveau de concentration de traitement de 5 000 mg/kg ps pour les études sur les chironomidés et les oligochètes.
En utilisant les données sur l'analogue DBDPE, une VCT de 5 000 mg/kg est sélectionnée pour l'EBTBP dans les sédiments, même si cette valeur n'est liée à aucun effet observé à cette concentration. Lorsque cette valeur est ajustée à partir de la teneur en carbone organique d'essai (1,8 %) à une teneur en contenu en carbone organique standard dans les sédiments (4 %) (Webster et al., 2004), la VCT pour les organismes vivant dans les sédiments est de 11 100 mg/kg ps. Un facteur d'évaluation de 100 est appliqué pour prendre en compte de la transposition des conditions de laboratoire à celle du terrain, et des variations inter‑espèces et intra‑espèces de la sensibilité; la CESE qui en résulte pour les organismes vivant dans les sédiments est de 111 mg/kg ps. On reconnaît que cette valeur est déjà une valeur sans effets observés; toutefois, un facteur d'application plus élevé est également jugé approprié, étant donné que l'EBTBP pourrait être passablement plus biodisponible que le DBDPE.
D'après les critères d'effet découlant de diverses études sur la toxicité dans le sol du DBDPE (bactérie du sol, lombrics et six espèces de plantes) [Aufderheide, 2003; Hardy et al., 2011; Porch et al., 2005], la valeur de la CE25 après 21 jours pour la baisse du poids de plants d'oignons de 2 440 mg/kg est choisie comme VCT. Lorsque cette valeur est ajustée à partir de la teneur en carbone organique d'essai (2,7 %) à une teneur en contenu en carbone organique standard dans les sédiments (2 %), la VCT pour les organismes vivant dans le sol est de 1 807 mg/kg ps. Un facteur d'évaluation de 100 est appliqué pour tenir compte de la transposition des conditions de laboratoire à celles du terrin et des variations inter-espèces et intra-espèces relatives à la sensibilité; la CESE qui en résulte pour les organismes vivant dans le sol est de 18,07 mg/kg de sol sec.
8.2 Évaluation de l'exposition de l'environnement
Au Canada, on n'a recensé aucune concentration d'EBTBP dans l'eau. Par conséquent, les concentrations environnementales ont donc été évaluées sur la base des renseignements disponibles, y compris les estimations relatives aux quantités estimées de la substance, les estimations relatives aux taux de rejets industriels et les caractéristiques du milieu récepteur. Des concentrations environnementales ont été estimées pour des scénarios de rejets industriels, comme il est décrit dans les sections suivantes.
8.2.1 Scénarios d'exposition et concentrations environnementales estimées
8.2.1.1 Rejets industriels
Les scénarios de rejets industriels de l'EBTBP prennent en compte les renseignements disponibles concernant l'utilisation de l'EBTBP et du DBDPE (ECCC, 2015b). Puisque les profils d'utilisation et les applications de l'EBTBP et du DBDPE sont jugés très similaires, et étant donné le manque de renseignements sur les utilisations industrielles de l'EBTBP au Canada, on a évalué l'exposition à l'EBTBP dans l'environnement en fonction des données propres à l'EBTBP et au DBDPE. Bien que les utilisations de l'EBTBP et du DBDPE soient semblables, les quantités d'EBTBP utilisées sont bien moins élevées que celles de DBDPE.
8.2.1.2 Milieu aquatique
Une exposition aquatique à l'EBTBP devrait avoir lieu si la substance est rejetée durant les procédés de fabrication industrielle et de formulation, que ce soit directement ou vers une usine de traitement des eaux usées qui rejette ses effluents dans un plan d'eau de surface récepteur. La concentration de la substance dans les eaux réceptrices près du point de rejet de système d'assainissement est utilisée comme CEE afin de calculer les CEE dans les sédiments et le sol dans l'évaluation du risque que pose la substance pour ces milieux. On peut la calculer à l'aide de l'équation suivante (ECCC, 2015b) :
Ceau-ind = [1000 x Q x L x (1-R)] / [N x F x D]
où
Ceau-ind : concentration en milieu aquatique due aux rejets industriels, en mg/L
Q : quantité de substance totale utilisée chaque année sur un site industriel, en kg/an
L : pertes dans les eaux usées, fraction
R : taux d'élimination du système de traitement des eaux usées, fraction
N : nombre de jours de rejets annuels, en jour par an
F : débit de l'effluent du système d'assainissement des eaux usées, en m3 par jour
D : facteur de dilution dans l'eau réceptrice, sans dimension
Plusieurs scénarios de rejets industriels dans l'eau ont été élaborés pour tenir compte d'une large gamme d'activités industrielles potentielles au Canada. Ces scénarios incluent les formulateurs de mélanges de caoutchouc, les formulateurs de mélanges de matières plastiques, les moules à injection en plastique, les installations de fabrication de textile et d'extrusion de plastique, les installations d'enduction d'envers pour textiles (aux fins de l'évaluation écologique uniquement) et les installations qui utilisent cette substance pour des activités industrielles non précisées. Le tableau 8-3 présente la série de données d'entrée utilisée pour estimer les concentrations de la substance dans le milieu aquatique près des points de rejet industriel. D'après ces hypothèses, les scénarios industriels donnent des CEE prévues dans le milieu aquatique de 2,20 x 10-8 à 2,88 x 10-7 mg/L (ECCC, 2017b). Ces valeurs de CEE représentent les concentrations totales d'EBTBP dans le plan d'eau récepteur près du point de rejet à chaque site et, dans certains cas, ces concentrations ont dépassé la limite d'hydrosolubilité de l'EBTBP (c.-à.-d. limite d'EBTBP dissous) d'un à quatre ordres d'importance. Les plus fortes CEE découlent de scénarios industriels impliquant des rejets importants. Ces scénarios présentent également des incertitudes (p. ex., industries du textile, en général) et sont jugés plus prudents.
| Intrant | Valeur | Justification et référence |
|---|---|---|
| Quantité utilisée par site (kg) | 1000 à 100 000 | Enquête réalisée en vertu de l'article 71 (Canada, 2013) |
| Pertes dans les eaux usées (%) | 0,001 à 1 | OCDE, 2010 |
| Efficacité d'élimination du système de traitement des eaux usées (%) | 0, 57,3, ou 82,5 | Prévision obtenue à partir du modèle ASTreat 1.0 (2006) sans traitement, avec traitement primaire ou traitement secondaire |
| Nombre de jours de rejets annuels (jours par an)a | 250 à 350 | Données de l'Inventaire national des rejets de polluants ou hypothèse standard d'Environnement Canada |
| Débit de l'effluent du système d'assainissement des eaux usées, en m3 par jour | 2908 à 400 000 | Données du système de traitement des eaux usées propres au site |
| Facteur de dilution (-) | 1 à 10 | Débit du système de traitement des eaux usées propre au site/débit de l'environnement récepteur Lorsque le facteur de dilution était supérieur à 10, une valeur maximale par défaut de 10 a été utilisée. |
8.2.1.3 Sédiments
Une méthode du partage eau-sédiment à l'équilibre a été utilisée pour estimer la concentration de l'EBTBP dans les sédiments benthiques. Cette approche fait appel à un principe de répartition décrite par l'Agence européenne des produits chimiques (ECHA, 2010) et intègre deux autres méthodes de calcul supplémentaires. La première méthode consiste à estimer la concentration de la substance dans la phase aqueuse (réellement dissoute) de l'eau sus-jacente de sa concentration totale, selon des études menées par Gobas (2007 et 2010). La deuxième méthode consiste à estimer la concentration de la substance dans les sédiments benthiques à partir de sa concentration dans la phase aqueuse de l'eau sus-jacente et repose sur une hypothèse de partage à l'équilibre entre les sédiments benthiques et l'eau sus-jacente tel qu'il est décrit par le National Center for Environnemental Assessment de l'Environnemental Protection Agency des États-Unis (US EPA, 2003). À l'équilibre, la concentration environnementale estimée (CEE) dans les sédiments benthiques peut être en corrélation, de façon linéaire, avec la concentration dans la phase aqueuse de l'eau sus-jacente, comme suit : Des scénarios d'exposition des sédiments ont été élaborés dans le cadre d'une extension des scénarios de rejets industriels dans le milieu aquatique décrits ci-dessus pour déterminer l'équilibre des CEE dans les sédiments normalisées à une teneur en carbone organique de 4 % (une teneur en carbone organique typique dans les sédiments benthiques pour les rivières et les lacs). Les valeurs de CEE qui en découlent variaient de 0,00015 à 0,020 mg/kg ps.
8.2.1.4 Sol
Une méthode décrite par l'Agence européenne des produits chimiques (ECHA, 2010) a été utilisée afin de déterminer les CEE dans le sol découlant de l'épandage de biosolides. Cette méthode utilise les quantités de biosolides accumulés dans la couche supérieure de 20 cm du sol (profondeur de labourage) au cours d'une période de dix années consécutives. Selon une hypothèse sous-jacente de la méthode, il n'y avait aucune perte en raison de la dégradation, de la volatilisation, du lessivage ou du ruissellement au moment de la pénétration des substances dans les sols à la suite de l'épandage de biosolides. Cette hypothèse a permis d'obtenir des CEE dans le sol prudentes. Des scénarios d'exposition dans le sol ont été élaborés dans le cadre d'une extension des scénarios d'exposition dans le milieu aquatique décrits ci-dessus, à l'aide des concentrations de biosolides et des taux de production des systèmes de traitement des eaux usées propres au site. La concentration estimée dans les biosolides variait de 0,0030 à 73,44 mg/kg ps. Les CEE dans le sol ont été normalisées à 2 % de carbone organique, et les valeurs de CEE obtenues variaient de 1 x 10-4 à 2,54 mg/kg ps (annexe A).
8.2.1.5 Rejets commerciaux et par les consommateurs
Bien que l'EBTBP puisse se trouver dans des produits commerciaux ou disponibles aux consommateurs, les rejets de ces produits dans l'environnement devraient être minimes. L'utilisation d'EBTPB en tant qu'additif dans certains produits semble indiquer que des émissions diffuses peuvent découler de produits commerciaux ou de consommation et que, même s'il y a des incertitudes, le taux d'émission pourrait être faible. Même si des taux de rejets au cours de la durée de vie utile n'ont pas été observés pour l'EBTBP, une étude menée par Kemmlein et al. (2003) a permis de déterminer un taux d'émission dans l'air spécifique de 0,3 ng/m2/h pour le décaBDE (dans la formulation technique d'octabromodiphényléther) au cours d'un essai de 105 jours sur un boîtier de téléviseur (23 °C). De plus, bon nombre des produits fabriqués avec de l'EBTBP n'entrent pas souvent en contact avec l'eau (p. ex. produits électroniques, câblages et appareils). Le potentiel de rejet de la substance dans l'eau durant la durée de vie utile du produit est estimé à 0,05 % par année si le produit est destiné à un usage intérieur et de 0,16 % par année s'il est destiné à un usage extérieur (OCDE, 2009). Dans l'ensemble, les rejets issus des produits devraient être géographiquement dispersés et se propager pendant la durée de vie utile et la fin de vie utile de ces produits.
Par conséquent, le scénario de la pire éventualité en ce qui concerne le rejet diffus d'EBTBP partout au Canada (par les systèmes de traitement des eaux usées et le rejet diffus directement dans l'environnement) à l'aide du taux de rejet à l'intérieur de 0,05 % sur la durée de vie utile d'après les renseignements de l'OCDE (2009), a été estimé à 555 kg. Ce scénario comprend plusieurs hypothèses : les valeurs maximales provenant de chaque plage d'importation (1 000 000 kg pour les produits commerciaux ou de produits disponibles aux consommateurs; 100 000 kg pour la formulation; et 10 000 kg pour les substances pures); utilisation complète de l'EBTBP dans des produits, faible exposition dans l'eau sur la durée de vie utile et utilisation à l'intérieur. Ce résultat laisse entendre qu'un rejet important provenant de produits contenant de l'EBTBP est improbable. Le résultat du scénario est jugé très incertain.
8.3 Caractérisation des risques pour l'environnement
8.3.1 Analyse des quotients de risque
La démarche utilisée dans le cadre de cette évaluation écologique préalable visait à examiner les divers renseignements pertinents afin de tirer des conclusions fondées sur la méthode du poids de la preuve et le principe de prudence, conformément aux dispositions de la LCPE. Les éléments de preuve pris en compte comprenaient les résultats de calculs prudents du quotient de risque ainsi que des renseignements sur la persistance, la bioaccumulation, la toxicité intrinsèque ou l'écotoxicité, les sources et le devenir de la substance.
Une analyse du quotient de risque, intégrant des estimations prudentes de l'exposition à l'EBTBP aux renseignements concernant la toxicité de son analogue, le DBDPE, a été réalisée pour le sol et les sédiments afin de déterminer si la substance pourrait avoir des effets nocifs sur l'environnement canadien. On n'a pas mené d'analyse du quotient de risque pour le milieu aquatique pélagique en raison de la faible pertinence et de la nature peu fiable des données empiriques et prévues sur la toxicité.
Les scénarios industriels présentés ci-dessus ont donné des CEE de 2,20 x 10-8 à 2,88 x 10-7 mg/L (ECCC, 2017b) pour les eaux de surface. Ces valeurs de CEE représentent le niveau d'exposition dans les eaux réceptrices près du point de rejet. En utilisant des CEE en milieu aquatique pour déterminer les CEE à l'équilibre dans les sédiments, normalisées à 4 % de carbone organique, les valeurs de CEE obtenues variaient de 0,00015 à 0,020 mg/kg ps. Une CESE a été calculée à partir de valeurs de toxicité chronique chez des organismes vivant dans les sédiments pour le DBDPE, donnant ainsi une valeur de 111 mg/kg ps (voir la section « Évaluation des effets sur l'environnement »). Quotients de risque obtenus (CEE/CESE) = 1,3 x 10-6 à 0,00018 (tableau 8-4).
Selon une méthode CEE/CESE similaire, les CEE dans le sol, prévues découlant de l'épandage de biosolides (normalisées à 2 % de carbone organique) variaient de 1 x 10-4 à 2,54 mg/kg ps. La CESE pour les organismes vivant dans le sol est de 18,07 mg/kg de sol sec (voir la section « Évaluation des effets sur l'environnement »). Quotients de risque obtenus (CEE/CESE) = 5,8 x 10-6 à 0,14 (tableau 8-4). Par conséquent, il est peu probable que cette substance ait des effets nocifs sur les organismes vivant dans le sol pour ces scénarios.
| Milieu | Scénario | CESE | CEE | QR |
|---|---|---|---|---|
| Sédiments | Rejets industriels dans l'eau | 111 mg/kg ps | 0,00015 à 0,020mg/kg ps | 1,3 x 10-6 à 0,00018 |
| Sol | Épandage de biosolides sur le sol | 18,07 mg/kg ps | 1.0 x 10-4 à 2,54 mg/kg ps | 5,8 x 10-6 à 0,14 |
8.3.2 Examen des éléments de preuve et conclusion
L'EBTBP devrait être persistant dans l'eau, le sol et les sédiments, mais pas dans l'air (phase gazeuse). L'EBTBP devrait présenter un potentiel de bioaccumulation limité; toutefois, en raison du manque de données empiriques, on ne peut écarter la bioamplification dans les réseaux trophiques. Les quantités d’EBTBP importées au Canada ainsi que les données sur les utilisations indiquent un faible risque de rejet à grande échelle dans l’environnement au Canada. Une fois rejeté dans l'environnement, l'EBTBP se retrouvera principalement dans les sédiments et le sol, où il est susceptible de persister pendant de longues périodes. Il n'existe aucune donnée expérimentale sur la toxicité pour l'EBTBP, mis à part celle provenant d’une étude de toxicité en milieu aquatique menée à des concentrations supérieures à la solubilité de l’EBTBP dans l’eau, et les prévisions relatives à la toxicité aiguë et chronique ne sont pas fiables, car la valeur du log Koe de cette substance est très élevée (8,90) et se trouve donc en dehors du domaine de modélisation des modèles disponibles. Les données sur la toxicité du DBDPE pour les organismes vivant dans le sol et les sédiments sont utilisées à titre de données déduites à partir d'analogues pour l'EBTBP. Les résultats de l'analyse du quotient de risque indiquent que l'EBTBP présente des quotients de risque prévus très faibles pour les organismes vivant dans les sédiments (QR inférieur à 0,00018) et dans le sol (QR < 0,14). D'après ces études et le poids de la preuve (annexe A), l'EBTBP présente un potentiel de danger faible pour les organismes vivant dans le sol et les sédiments.
Ces renseignements indiquent que l'EBTBP ne peut pas entraîner d'effets nocifs sur l'environnement au Canada.
8.3.3 Incertitudes dans l'évaluation des risques pour l'environnement
Il existe des incertitudes liées au manque de données sur les concentrations de la substance dans l'environnement canadien, notamment dans les effluents des eaux usées ainsi que dans les biosolides, les sols, les sédiments et le biote associés. En outre, une certaine incertitude plane quant aux propriétés physiques et chimiques estimées. Bien que l'on ait utilisé la méthode de compensation des moindres carrés dans le cadre de la présente évaluation et que les valeurs d'entrée aient été ajustées de la meilleure manière possible, les propriétés physiques et chimiques présentent toujours des incertitudes, car la plupart des estimations et des valeurs des QSAR tirées d'autres modèles ont été utilisées à titre de données d'entrée pour la méthode d'ajustement des moindres carrés. Plus particulièrement, la correction pour le log Koe est de 194 %; le log Koe a donc sans doute été sous-estimé. Cependant, il n'existe aucun renseignement indiquant la mesure dans laquelle il pourrait avoir été sous-estimé. En général, le niveau de confiance à l'égard des propriétés physiques et chimiques de l'EBTBP est faible à modéré.
Toutefois, les estimations modélisées de la DTC, de la persistance globale et du rendement thermique pour cette substance ont besoin d’être analysées avec prudence en raison des incertitudes concernant les principaux coefficients de partage modélisés (Koa, Koe, Kae) requis à titre d'intrants. Les scénarios d'exposition pour l'utilisation dans l'analyse de risques ont été élaborés d'après la meilleure information disponible, et certaines données de référence sur le DBDPE ont été utilisées compte tenu des usages visiblement semblables. Néanmoins, ces scénarios caractérisent de façon prudente les risques potentiels associés aux rejets d'EBTBP dans l'environnement canadien.
Le rapport d'évaluation reconnaît qu'il n'existe aucune donnée sur la caractérisation des rejets potentiels provenant de produits commerciaux ou disponibles aux consommateurs pendant leur utilisation, ainsi que lors de leur élimination ou de leur recyclage à la fin de leur vie utile. La présente évaluation n'a pas tenu compte des rejets d'EBTBP dans l'environnement qui découlent de la lixiviation de produits ou de la dégradation de produits contenant de l'EBTBP dans les sites d'enfouissement, en raison du manque de données et puisque l'on s'attend à ce que les émissions pendant l'utilisation soient faibles. Au Canada, la plupart des sites d’enfouissement devraient recueillir et traiter le lixiviat, aucune donnée canadienne sur les lixiviats d'EBTBP dans les sites d'enfouissement n'a été recensée à ce jour, mais ces données pourraient être utiles pour interpréter les rejets en fin de vie utile. En général, le niveau de confiance à l'égard des scénarios d'exposition à l'EBTBP est modéré.
Même avec des hypothèses prudentes sur les importantes quantités d'EBTBP utilisées à des sites industriels, les quotients de risque étaient bien inférieurs à 1, ce qui indique peu de risque. Enfin, la présente évaluation reconnaît qu'il existe des lacunes liées à l'information sur la toxicité de l'EBTBP pour les espèces vivant dans le sol et les sédiments et les espèces sauvages. L'utilisation du DBDPE à titre d'analogue de l'EBTBP pour la toxicité dans les sédiments et le sol représente une source supplémentaire d'incertitude, car le DBDPE est moins biodisponible que l'EBTBP (le log Kco du DBDPE est supérieur à celui de l'EBTBP), et les données sur la toxicité présentées dans le cadre de la présente évaluation constituent la pire éventualité; par conséquent, les incertitudes relatives aux effets tendent à être extrêmement prudentes. Compte tenu du facteur d'évaluation élevé (100), on considère que l'analyse est suffisamment prudente pour caractériser de manière adéquate les effets potentiels qui pourraient être causés par l'utilisation de l'EBTBP. En général, le niveau de confiance à l'égard des résultats de toxicité pour l'EBTBP est modéré.
Enfin, il n'existe aucune donnée probante empirique attestant de la transformation de l'EBTBP dans l'environnement, ni aucune information caractérisant les voies de dégradation potentielles. Par conséquent, le niveau de confiance associé à l'analyse des dérivés hypothétiques de l'EBTBP est faible.
9. Potentiel d'effets nocifs sur la santé humaine
9.1 Évaluation de l'exposition
9.1.1 Milieux naturels et aliments
L'EBTBP est un additif ignifuge utilisé dans la fabrication de boîtiers électroniques, de revêtements de fils et de câbles et d'adhésifs au Canada. À titre d'additif ignifuge, l'EBTBP n'est pas considéré comme étant chimiquement lié à la matrice polymère qui le renferme; par conséquent, il pourrait être rejeté dans l'environnement au cours de la durée de vie utile d'un produit (Andersson et al,. 2006; Guerra et al., 2011).
Dans les études où l'EBTBP fait l'objet d'une surveillance, il n'est pas souvent détecté en raison des limitations des méthodes analytiques employées (Nyholm et al,. 2013). En raison de la faible valeur des estimations de la volatilité et de l’insolubilité dans l'eau, l'EBTBP devrait se répartir principalement dans la poussière et les sédiments lorsqu'il est rejeté; en outre, on s'attend à ce que sa concentration dans l'eau soit faible. La population générale des milieux naturels devrait donc être exposée à la substance principalement par la poussière ou le sol. La limite supérieure des estimations de l’absorption quotidiene d’EBTBP dans les milieux naturels par la population générale du Canada sont présentés à l’annexe B et varient de 0,0004 à 0,39 µg/kg de poids corporel par jour.
9.1.1.1 Air
On n'a recensé aucun rapport dans lequel la concentration d'EBTBP avait été calculée dans l'air ambiant ou l'air intérieur, que ce soit au Canada ou ailleurs.
9.1.1.2 Poussière
On n'a recensé aucune étude dans le cadre de laquelle la concentration d'EBTBP dans la poussière avait fait l'objet d'une surveillance au Canada. On peut s'attendre à déceler de l'EBTBP dans la poussière domestique, puisqu'il est utilisé dans la fabrication d'électroménagers. L'abrasion de revêtements de fils en plastique contenant de l'EBTBP pourrait libérer des rejets sous forme de poussière, représentant ainsi une source potentielle d'exposition par ingestion fortuite de poussière. Étant donné le manque de données sur la surveillance de la poussière pour l'EBTBP, les concentrations de poussière de produits ignifuges présentant des profils d'utilisation et des propriétés physiques et chimiques similaires (c.-à-d. le décaBDE et le DBDPE) ont été utilisées pour prévoir les concentrations de poussière de l'EBTBP. Le décaBDE (no CAS 1163-19-5) et le DBDPE (no CAS 84852-53-9) sont deux ignifugeants bromés qui entrent dans la composition des plastiques utilisés dans la fabrication de produits électroniques domestiques. Ces substances pourraient être rejetées dans le flux poussiéreux en raison de l'usure normale ou de l'abrasion des produits. En 2006, des échantillons de poussière ont été prélevés dans 19 résidences de Boston et ont ensuite été analysés pour déceler la présence de DBDPE. Dans cette étude, on a obtenu une moyenne géométrique de 153 ng/g ainsi qu'une concentration maximale de 11 070 ng/g (Stapleton et al., 2008). En 2012, de la poussière a été prélevée dans 30 résidences de Boston (Stapleton et al., 2014) en vue d’un dosage de l’EBTBP. Dans cette étude, on a obtenu une moyenne géométrique de 1 720 ng/g ainsi qu'une concentration maximale de 76 130 ng/g. En vue d'adopter une approche prudente à l'égard de l'EBTBP, on a utilisé les concentrations maximales de poussière domestique pour le décaBDE (BDE209) et le DBDPE (respectivement 76 130 ng/g et 11 070 ng/g) rapportées dans Stapleton et al. (2008, 2014) afin de représenter la plage d'exposition potentielle découlant de la poussière. À noter que cette concentration est supérieure à la concentration maximale estimée d'EBTBP dans le sol (2,54 mg/kg ps), qui découle de l'épandage de biosolides (voir la section 8.2.1.4).
9.1.1.3 Sol et sédiments
On n'a recensé aucune étude appropriée ou pertinente sur la surveillance de l'EBTBP dans le sol et les sédiments en Amérique du Nord. D'après ses propriétés physiques et chimiques, cette substance devrait se répartir dans le sol et les sédiments. En supposant que les biosolides provenant des systèmes de traitement des eaux usées sont épandus sur des terres agricoles, on a utilisé le modèle BASL4 pour prévoir une concentration dans le sol de 2,54 mg/kg (section 8.2.1.4). On a calculé la dose journalière totale en fonction de l'estimation de cette CEE.
9.1.1.4 Eau
Il n'existe aucun rapport sur l'échantillonnage de l'EBTBP dans l'eau ou les précipitations au Canada. Lors d'une étude norvégienne, on a décelé la présence d'EBTBP dans les eaux d'infiltration situées à l'extérieur d'une usine de recyclage du métal à une concentration de 35 ng/L (Nyholm et al., 2013). Des concentrations d'EBTBP ont été détectées dans un seul échantillon (limite de détection de la méthode de 6 ng/L). Les auteurs ont signalé des interférences analytiques lors de l'analyse des échantillons d'eau et ont pris pour hypothèse que la concentration d'EBTBP décelée dans l'eau pourrait être interprétée comme étant un faux positif (Nyholm et al., 2013).
En raison de l'insolubilité dans l'eau estimée (< 1 mg/L) de l'EBTBP et de sa forte propension à se répartir dans les solides (poussière ou sol), ainsi que des valeurs de CEE présentées à la section 8.2.1.2, il est peu probable qu'il soit présent dans l'eau à la concentration (35 ng/L) rapportée par Nyholm et al. (2013). Par conséquent, cette source d’exposition n'a pas été jugée pertinente pour calculer l'estimation de la dose journalière totale chez la population canadienne.
9.1.1.5 Aliments
Aucun rapport d'EBTBP dans des aliments n'a été recensé au Canada ni dans d'autres régions du globe.
9.1.2 Produits de consommation
L'EBTBP est une substance ignifuge qui est utilisée au Canada dans les matériaux de plastique et de caoutchouc qui composent les produits électriques et électroniques ainsi que les adhésifs au sein de l’industrie automobile (voir la section 5) [ECCC 2013-2014; fiche signalétique, 2010].
L'EBTBP n'est pas destiné à la vente au grand public; toutefois, il est ajouté à divers articles manufacturés, comme les isolants pour fils et câbles et l'équipement électronique, ce qui pourrait entraîner une exposition domestique potentielle.
Lorsque cette substance est utilisée dans des boîtiers d'équipement électronique (c.à-d. ordinateurs ou imprimantes) ou dans des isolants de câbles électriques, l'exposition à celle-ci devrait être minime. En raison du faible taux de pression de vapeur et de vaporisation, l'exposition par inhalation à cette substance est peu probable. L'hydrosolubilité négligeable de l'EBTBP réduit le potentiel de transfert cutané par l'intermédiaire de l'eau ou de la transpiration. En outre, on s'attend à ce que l'absorption cutanée par un contact physique avec les articles électroniques soit plutôt faible. L'abrasion des surfaces en plastique pourrait faire en sorte que l'EBTBP adhère aux particules de poussière se trouvant à proximité. L'absorption de poussière est abordée dans la section « Milieux naturels et aliments » (voir la section 9.1.1 ci-dessus).
Autour de la maison, les nourrissons et les enfants pourraient avoir accès à des articles électroniques et à des câbles électriques qu'ils pourraient porter à leur bouche. Lors d'une étude portant sur le comportement de mâchonnement des enfants, on a observé la mise en bouche accidentelle de nombreux produits, tels que les antennes de téléphones sans fil, les cordons électriques, les rallonges électriques et les télécommandes (Juberg et al., 2001). Cependant, on considère que comportement entraîne un niveau d'exposition plus faible que celui causé par le mâchonnement de jouets ou d'autres articles destinés aux enfants, compte tenu de la nature fortuite de l'exposition et de la faible hydrosolubilité de l'EBTBP.
L'EBTBP entre également dans la fabrication des adhésifs thermofusibles, qui sont utilisés dans les pistolets à colle. L'exposition potentielle à la substance pendant l'utilisation d'un pistolet à colle a été jugée peu élevée compte tenu de sa faible pression de vapeur. Le risque que le taux de volatilisation de l'EBTBP augmente en raison de la hausse de température lors de l'application de colle ne devrait pas entraîner une augmentation significative de la concentration dans l'air. L'exposition cutanée est peu probable, car le contact avec la peau est évité naturellement afin d'éviter les brûlures. D'après les renseignements actuels concernant le profil d'utilisation et les propriétés physiques et chimiques de l'EBTBP, le potentiel d'exposition de l'ensemble de la population canadienne à cette substance par des articles manufacturés est faible. Par conséquent, les estimations de l'exposition n'ont pas été calculées. Toute exposition par des articles manufacturés devrait être prise en compte dans les estimations de l’absorption d'EBTBP par le sol et la poussière (voir les sections 9.1.1.2 et 9.1.1.3).
9.2 Évaluation des effets sur la santé
On n'a relevé aucune classification des effets de l'EBTBP sur la santé d'organismes de réglementation nationaux ou internationaux. En outre, on n'a recensé aucune étude sur la toxicité chronique et la cancérogénicité liée à l'EBTBP. Les résultats des études sur la mutagénicité de l'EBTBP menées chez la Salmonella typhimurium (souches TA 98, TA 100, TA 1535, TA 1537, et TA 1538), l'Escherichia coli (souche WP2 uvrA) et la Saccharomyces cerevisiae étaient négatives lors d'essais avec ou sans activation métabolique à des concentrations allant de 0 à 5 000 μg/plate dans le DMSO (Cannon Laboratories Inc., 1978c; Chemical Inspection and Testing Institute, 1982; Zeiger et al., 1985; Albemarle Corporation, 2008). Les résultats d'un essai d'aberration chromosomique effectué chez des cellules ovariennes (CHO) de hamsters de Chine étaient également négatifs à des concentrations allant jusqu'à 750 μg/mL pendant 20 jours avec ou sans activation métabolique (Albemarle Corporation, 2008). Aucune étude in vivo n'a été relevée.
En l'absence d'études sur la toxicité chronique et la cancérogénicité de l'EBTBP, Santé Canada a mené une analyse quantitative des prévisions du modèle des QSAR pour la cancérogénicité. Les prévisions du modèle des QSAR ont appuyé les conclusions tirées des essais in vitro voulant que l'EBTBP ne soit pas génotoxique; cependant, elles se sont révélées non concluantes quant à son potentiel de cancérogénicité. Toutefois, il est peu probable que l'EBTBP soit considéré comme étant cancérogène en raison des résultats négatifs des études sur la génotoxicité, de l'absence d'effets nocifs chez les animaux de laboratoire à la dose d'essai la plus élevée (voir les études à doses répétées présentées ci-dessous) ainsi que de la solubilité limitée et de la taille moléculaire de l'EBTBP qui entraîneraient une absorption limitée.
On n'a observé aucun effet nocif chez les animaux de laboratoire ayant reçu de l'EBTBP dans leur régime alimentaire lors de plusieurs études à doses répétées.
Dans le cadre d'une étude subchronique, on a administré de l'EBTBP à des rats Sprague-Dawley mâles et femelles (15 animaux par sexe et par groupe), à des doses de 0, 0,01, 0,1 et 1 % de leur régime alimentaire pendant 90 jours; par la suite, on a nourri les rats avec des aliments du groupe témoin pendant 46 jours. On n'a constaté aucun changement lié à l'exposition à l'égard de l'hématologie, de la composition chimique du sérum et de l'analyse d'urine. En outre, on n'a noté aucune différence statistiquement significative par rapport aux poids moyens relatifs et absolus des organes (foie, reins, cœur et glande thyroïde) entre le groupe témoin et les groupes exposés. Aucun changement histologique lié à l'exposition ni aucune lésion dans les organes et les tissus n'ont été observés dans l'ensemble des groupes examinés à la fin de l'étude. La dose d'essai la plus élevée était de 1 % d'EBTBP dans le régime alimentaire, ce qui représentait 692 mg/kg p.c. par jour chez les mâles et 775 mg/kg p.c. par jour chez les femelles (Cannon Laboratories Inc., 1978b; Albemarle Corporation, 2004).Note de bas de page 2
On a relevé une étude à court terme lors de laquelle on a administré de l'EBTBP à des rats mâles Sprague-Dawley (SD) (10 animaux par groupe) à des doses de 0, 0,01, 0,1 et 1 % du régime alimentaire pendant 28 jours. Aucun signe clinique de toxicité n'a été observé. Le poids corporel moyen, les gains de poids corporel, la consommation de nourriture et le poids des organes (foie, cœur, rate, reins et testicules) n'ont pas été touchés par l'exposition à la substance. On n'a observé aucun changement lié à l'exposition à l'égard de l'hématologie et de la composition chimique du sérum, ni aucune modification macroscopique ou microscopique des tissus. La dose d'essai la plus élevée était de 1 % de la substance dans le régime alimentaire, ce qui représentait 1 267 mg/kg p.c. par jour (WARF Institute Inc., 1976; Albemarle Corporation, 2004).
Les effets de l'EBTBP sur le développement des rats et des lapins ont été étudiés. L'EBTBP a été administré à quatre groupes de rats femelles Sprague Dawley accouplés (25 animaux par groupe) par gavage dans de l'huile de maïs à des doses de 0, 100, 500 et 1 000 mg/kg p.c. par jour du 6e au 15e jour de gestation. Des animaux ont été observés chaque jour afin de détecter chez eux des signes de toxicité. Le poids corporel et la consommation de nourriture ont été calculés aux jours de gestation 0, 6, 9, 12, 16 et 20. Tous les rats femelles ont été sacrifiés au 20e jour de gestation et ont subi une césarienne. On a pesé les fœtus, déterminé leur sexe et les a examinés minutieusement afin de détecter toute anomalie externe, viscérale et squelettique. Au cours de l'étude, on n'a observé aucune mortalité maternelle ni aucun signe clinique de toxicité liée à l'exposition. Aucune différence liée à l'exposition n'a été notée chez les groupes par rapport au poids corporel des mères, à la consommation de nourriture et aux lésions morphopathologiques. Le taux de survie intra-utérin et le poids des fœtus étaient similaires parmi tous les groupes étudiés. La fréquence des effets sur le développement chez les groupes traités était comparable à celle du groupe témoin. Dans l'ensemble, on a déterminé que l'EBTBP n'était pas toxique pour les mères et n'avait aucun effet sur le développement des rates gravides lorsqu'il était administré par voie orale à des doses aussi élevées que 1 000 mg/kg p.c. par jour (Rodwell, 1988a; Albemarle Corporation, 2004).
Lors d'une autre étude sur la toxicité pour le développement, on a administré l'EBTBP à deux groupes de lapins blancs femelles néo-zélandais accouplés (20 animaux par groupe) par gavage dans de la carboxyméthylcellulose à des concentrations de 0 ou 1 000 mg/kg p.c. par jour du 7e au 19e jour de gestation. Des animaux ont été observés chaque jour afin de détecter chez eux des signes de toxicité. On a mesuré les poids corporels aux jours de gestation 0, 7, 10, 13, 19, 24 et 29. La consommation de nourriture était calculée chaque jour. Tous les lapins femelles ont été sacrifiés au 29e jour de gestation et ont subi une césarienne. On a pesé les fœtus, déterminé leur sexe et les a examinés minutieusement afin de détecter toute anomalie externe, viscérale et squelettique. Au cours de l'étude, on n'a observé aucune mortalité maternelle ni aucun avortement ou signe clinique de toxicité liée à l'exposition. Le poids corporel des mères, les gains de poids corporel, la consommation d'aliments, les constats d'autopsie et les paramètres de césarienne étaient comparables entre les deux groupes étudiés. Le taux de survie intra-utérin et le poids des fœtus n'ont pas été touchés par l'exposition à l'EBTBP. La fréquence des effets sur le développement chez le groupe de traitement était comparable à celle du groupe témoin. Par conséquent, on a déterminé que l'EBTBP n'était pas toxique pour les mères et n'avait aucun effet sur le développement des lapines gravides lorsqu'il était administré par voie orale à des concentrations aussi élevées que 1 000 mg/kg p.c. par jour (Rodwell, 1988b; Albemarle Corporation, 2004).
Les renseignements disponibles concernant la toxicocinétique de l'EBTBP sont limités. On a relevé une étude lors de laquelle on a administré de l'EBTBP marqué au carbone-14 (dose équivalente de 0,67 mg/kg p.c. par jour) à cinq rats femelles Sprague-Dawley par gavage dans de l'huile de maïs pendant 14 jours consécutifs. Environ 80 % de la dose totale a été récupérée dans les matières fécales (~ 65 %) et dans l'urine (~15 %) pendant les 14 jours de dosage. On a détecté une activité du carbone-14 négligeable dans l'air expiré. Tous les organes contenaient des résidus radioactifs. Après 14 jours, les concentrations les plus élevées étaient observées dans le foie et les reins. On a détecté un faible taux de radioactivité dans les muscles, les tissus adipeux et le cerveau. Trente jours après le traitement, les niveaux d'activité du carbone-14 ont continué de diminuer, les plus élevés étant observés dans les muscles (0,05 ppm) [Cannon, 1978a; Commission européenne, 2000a; Albemarle Corporation, 2004].
9.3 Caractérisation des risques pour la santé humaine
Aucune classification des effets sur la santé de l’EBTBP effectuée par des organismes de règlementation nationaux ou d’autres pays n’a été relevée. Aucune étude sur les effets de l’EBTBP à long terme et sur sa cancérogénicité n’a été recensée. D'après les renseignements disponibles sur la génotoxicité, l'EBTBP n'est pas jugé génotoxique in vitro.
Aucun effet nocif significatif sur le plan toxicologique n'a été observé chez les rats exposés à l'EBTBP par voie orale à des doses allant jusqu'à 692 et 1 267 mg/kg p.c. par jour, pendant respectivement 90 et 28 jours. Aucune étude de la toxicité pour la reproduction n'a été recensée. Dans les études portant sur la toxicité pour le développement, aucun effet sur la mère lié au traitement n'a été observé chez des rats ou des lapins exposés à l'EBTBP par voie orale, et aucun effet sur le développement n'a non plus été constaté chez la progéniture, à des doses allant jusqu'à 1 000 mg/kg p.c.; toutefois, les lapins n'ont pas reçu la dose pendant toute la durée de l'étude.
Les doses d'essai les plus élevées (respectivement de 692 et de 1 267 mg/kg p.c. par jour administrées par voie orale à des rats lors des études de 90 et de 28 jours), sans aucun effet lié au traitement, sont plus élevées de six ordres de grandeur que les estimations de l’absorption d’EBTBP pour l'ensemble de la population canadienne par ingestion de poussière et de sol (0,0004 à 0,39 µg/kg p.c. par jour). Cette marge d'exposition est jugée adéquate pour rendre compte des incertitudes liées aux bases de données concernant les effets sur la santé et l'exposition.
9.4 Incertitudes dans l'évaluation des risques pour la santé humaine
Dans l'ensemble, le degré de confiance à l'égard de la base de données sur l'exposition pour les milieux naturels est considéré comme étant faible, étant donné qu'on n'a recensé aucune donnée sur la concentration de l'EBTBP dans des milieux naturels et que ce problème pourrait être attribuable aux difficultés liées à la détection des méthodes d’analyse.
Il existe certaines incertitudes associées à l'estimation de l'exposition humaine à l'EBTBP par les milieux naturels, car celle-ci est basée sur les concentrations de poussière mesurées pour des produits ignifuges connexes. Bien que le DBDPE et le décaBDE présentent des profils d'utilisation et des propriétés physiques et chimiques similaires à ceux de l'EBTBP, il existe des incertitudes quant à l'utilisation de ces substances à titre de substituts pour le calcul de la concentration de poussière.
Le degré de confiance à l'égard de la base de données sur les effets sur la santé de l'EBTBP est considéré comme étant modéré, car on constate que les données sur la cancérogénicité et la toxicité pour la reproduction sont manquantes et que la base de données sur la toxicité à doses répétées par voie orale étaient limitées.
10. Conclusion
Compte tenu de tous les éléments de preuve contenus dans la présente évaluation préalable, il existe un risque faible d’effets nocifs de l’EBTBP sur les organismes et l’intégrité globale de l’environnement. Il est conclu que l'EBTBP ne répond pas aux critères énoncés à l'alinéa 64a) ou b) de la Loi canadienne sur la protection de l'environnement (1999), car il ne pénètre pas dans l'environnement en une quantité, à une concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l'environnement ou sur la diversité biologique, ou à mettre en danger l'environnement essentiel pour la vie.
Compte tenu de l'adéquation de la marge d’exposition entre les estimations de l’exposition de la population générale et de la plus forte dose d'essai sans effet nocif observé chez les animaux de laboratoire, il est conclu que l'EBTBP ne satisfait pas aux critères énoncés à l'alinéa 64c) de la LCPE, car il ne pénètre pas l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Il est conclu que l'EBTBP ne répond à aucun des critères énoncés à l'article 64 de la LCPE.
Références
[AEROWIN] AEROWIN Program for Windows [Estimation Model]. 2010. Version 1.00. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [consulté en janvier 2014] (disponible en anglais seulement)
Albemarle Corporation. 1999a. Product Sheet: Saytex BT-93 Flame Retardant. Baton Rouge (LA): Albemarle Corporation. (disponible en anglais seulement)
Albemarle Corporation. 1999b. Product Sheet: Saytex BT-93W Flame Retardant. Baton Rouge (LA): Albemarle Corporation. (disponible en anglais seulement)
Albemarle Corporation. 2004. HPV Data Summary and Test Plan for 1H-Isoindole-1,3(2H)-dione,2,2’-(1,2-ethanediyl)bis(4,5,6,7-tetrabromo- (a.k.a Ethylene bis tetrabromophthalimide) CAS No. 32588-76-4. Report no. 201-15090. Baton Rouge (LA): Albemarle Corporation. (disponible en anglais seulement)
Albemarle Corporation. 2005. Material Safety Data Sheet: Saytex BT-93W Flame Retardant. 2005. Baton Rouge (LA): Albemarle Corporation. (disponible en anglais seulement)
Albemarle Corporation. 2008. Summary: Chromosome aberration assay in Chinese hamster ovary cells [PDF]. US EPA High Production Volume (HPV) Challenge Program, Revised Summaries for 1H-Isoindole-1,3(2H) -dione, 2,2'-(1,2-ethanediyl) bis(4,5,6,7-tetrabromo-, 17-8-2008. (disponible en anglais seulement)
Andersson P, Oberg K, Orn U. 2006. Chemical characterization of brominated flame retardants and identification of structurally representative compounds. Environ Tox and Chem 25(5): 1275-1282. (disponible en anglais seulement)
[AOPWIN] Atmospheric Oxidation Program for Windows [Estimation Model]. 2010. Version 1.92a. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [consulté en janvier 2014]. (disponible en anglais seulement)
Arnot JA, Gobas FAPC. 2003a. A generic QSAR for assessing the bioaccumulation potential of organic chemicals in aquatic food webs. QSAR Comb Sci 22(3):337–345. (disponible en anglais seulement)
Arnot JA, Gobas FAPC. 2003b. Categorization of organic substances on the Domestic Substances List for bioaccumulation potential. Rapport destiné à Environnement Canada, Division des substances existantes. Juin 2003. Gatineau (QC): Environnement Canada. (disponible en anglais seulement)
Arnot JA, Gobas FAPC. 2004. A food web bioaccumulation model for organic chemicals in aquatic ecosystems. Environ Toxicol Chem 23(10): 2343–2355. (disponible en anglais seulement)
Arnot JA, Gobas FAPC. 2006. A review of bioconcentration factor (BCF) and bioaccumulation factor (BAF) assessments for organic chemicals in aquatic organisms. Environ Rev 14:257–297. (disponible en anglais seulement)
Arnot JA, Arnot MI, Mackay D, Couillard Y, MacDonald D, Bonnell M, Doyle P. 2010. Molecular size cutoff criteria for screening bioaccumulation potential: fact or fiction? Integr Environ Assess Manage 6(2):210–224. (disponible en anglais seulement)
ASTreat 1.0 (2006). Un programme informatique mis au point par Procter & Gamble pour obtenir des prédictions relatives à l’élimination par les stations de traitement des eaux usées, révisé et diffusé en 2006, obtenu du Dr Drew C. McAvoy, Procter & Gamble Company, boîte postale 538707, Cincinnati, OH 45253-8707, USA. Most conservative removal rate of the 4 STP models (STP-EX SimpleTreat 3.0 STP Model 2.1 ASTreat 1.0) (disponible en anglais seulement)
Aufderheide J. 2003. Effects of Saytex 8010 on the survival and reproduction of the earthworm, Eisenia fetida. ABC Laboratories, Columbia, Missouri (USA): Study number 47634. (disponible en anglais seulement)
[BCFBAF] Bioaccumulation Program for Windows [Estimation Model]2010. Version 3.10. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [consulté en janvier 2014]. (disponible en anglais seulement)
[BDIPSN] Base de données d'ingrédients de produits de santé naturels [base de données]. [modifié le 21 juin 2017]. Ottawa (Ont.) : Gouvernement du Canada. [consulté le 24 avril 2014].
[BDPP] Base de données sur les produits pharmaceutiques [base de données]. [modifié le 17 février2017]. Ottawa (Ont.) : Gouvernement du Canada. [consulté le 24 avril 2014].
[BDPSNH] Base de données des produits de santé naturels homologués [base de données]. [modifié le 10 août 2016]. Ottawa (Ont.) : Gouvernement du Canada. [consulté le 24 avril 2014 24].
[BIOWIN] Biodegradation Probability Program for Windows [Estimation Model]. 2010. Version 4.10. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. (disponible en anglais seulement)
Boethling RS, Howard PH, Beauman JA, Larosche ME. 1995. Factors for intermedia extrapolations in biodegradability assessment. Chemosphere 30(4):741−752. (disponible en anglais seulement)
Boîte à outils QSAR de l’OCDE. [Outil de lecture croisée]. 2012. Version 3.0. Paris (FR): Organisation de coopération et de développement économiques, Direction de l’environnement. (disponible en anglais seulement)
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999). L.C. 1999, ch. 33. Gazette du Canada, Partie III, vol. 22, no 3.
Canada 2000. Loi canadienne sur la protection de l'environnement (1999) : Règlement sur la persistance et la bioaccumulation [PDF]. C.P. 2000-348, 23 mars 2000, DORS/2000-107, Gazette du Canada, Partie II, vol. 134, no 7, p. 607-612. [consulté en août 2017]
Canada. 2001. CAS RN 32588-76-4 – Rapport préliminaire de l'article 71 de la Loi canadienne sur la protection de l'environnement (1999). Rapport inédit. Gatineau (Qc) : Environnement Canada, Division des évaluations écologiques.
Canada. 2013. Loi canadienne sur la protection de l'environnement (1999) : Avis concernant certaines substances ignifuges organiques. Gazette du Canada, Partie I, vol. 147, no 13, p. 613-633. 30 mars 2013. [consulté le 17 août 2017]
Cannon Laboratories, Inc. (1978a). Excretion and tissue distribution of 14C-RW-4-178B administered orally to rats. In: Ethyl Corporation (1990). Excretion and tissue distribution of 14C-RW-4-178B administered orally to rats with attachments and cover letter dated 030890. EPA/OTS 0522911: #86-900000347. Testing laboratory: Cannon Laboratories, Inc. Report date: 1978-05-23. (disponible en anglais seulement)
Cannon Laboratories, Inc. (1978b). 90-day feeding study in rats evaluating Cities Service compound RW-4-178B. In: Ethyl Corporation (1990). 90-day feeding evaluation study in rats with cover letter dated 030890. EPA/OTS 0522927: #86-900000363. Laboratoire d’analyse : Cannon Laboratories, Inc. Date du rapport : 1978-09-19. (disponible en anglais seulement)
Cannon Laboratories, Inc. (1978c). Mutagenicity evaluation of RW-4-178B (BT-93) in the Ames Salmonella/microsome plate test. In: Ethyl Corporation (1990). Mutagenicity evaluation of RW-4-178B (BT-93) in the Ames Salmonella/microsome plate test with cover letter dated 030890. EPA/OTS 0522926: #86-900000362. Laboratoire d’analyse : Cannon Laboratories, Inc. Date du rapport : 1978-03-09.CATALOGIC [Computer Model]. 2012. Version 5.11.6. Bourgas (BG): Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. (disponible en anglais seulement)
Chemical Inspection and Testing Institute. 1982. Mutagenicity evaluation of ethylene-1,2-bis(3,4,5,6-tetrabromophthalimide) in Ames Salmonella/microsome assay with cover letter dated 030890. Laboratoire d’analyse : Chemical Inspection and Testing Institute. Date du rapport : 1982-02-18. (disponible en anglais seulement)
ChemNet [base de donnée en ligne]. 1997. CAS search, CAS: 32588-76-4 [online database]. ChemNet. [consulté le 1er janvier 2012] (disponible en anglais seulement)
[CITI] Chemicals Inspection and Testing Institute. 1991. Test of biodegradability of Saytex-402 by microorganisms. Kurume Research Laboratories, Chemical Biotesting Center. Test number 11893. (disponible en anglais seulement)
Covaci A, Harrad S, Abdallah M, Ali N, Law R, Herzke D, de Wit C. 2011. Novel brominated flame retardants: a review of their analysis, environmental fate and behaviour. Envi Int. 37:532-556. (disponible en anglais seulement)
Dimitrov S, Dimitrova N,Walker J, Veith G, Mekenyan O. 2002. Predicting bioconcentration potential of highly hydrophobic chemicals. Effect of molecular size. Pure and Appl Chem. 74(10):1823–1830. (disponible en anglais seulement)
Dimitrov S, Dimitrova N, Parkerton T, Comber M, Bonnell M, Mekenyan O. 2005. Base-line model for identifying the bioaccumulation potential of chemicals. SAR QSAR Environ Res 16(6):531–554. (disponible en anglais seulement)
[ECHA] European Chemicals Agency. 2014. Guidance on information requirements and chemical safety assessment. Chapter R.11: PBT/vPvB assessment. Version 2.0, Novembre 2014, p. 53. Guidance for the implementation of REACH. Helsinki (FI): European Chemicals Agency. (disponible en anglais seulement)
[ECHA] European Chemicals Agency. 2012. Guidance on information requirements and chemical safety assessment. Chapter R.16:Environmental exposure estimation. Version 2.1, Octobre 2012. Guidance for the implementation of REACH. Helsinki (FI): European Chemicals Agency. (disponible en anglais seulement)
[ECOSAR] Ecological Structure Activity Relationships Class Program [Estimation Model]. 2012. Version 1.11. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [consulté en janvier 2014]. (disponible en anglais seulement)
Environment Canada. 1986. DSL main_Quantity and Use codes_07-06-07.xls. Gatineau (QC): Environment Canada, Ecological Assessment Division. (disponible en anglais seulement)
Environnement Canada. 2006a. Rapport d'évaluation écologique préalable des polybromodiphényléthers (PBDE) [PDF], LCPE, juin 2006. Environnement Canada, Division des évaluations écologiques. [consulté en juin 2006]
Environnement Canada. 2010. Rapport sur l’état des connaissances scientifiques écologiques concernant le décabromodiphényléther (décaBDE) – Bioaccumulation et transformation [Internet]. [consulté en août 2010]
[ECCC] Environnement et Changement climatique Canada. 2013-2014. Données pour le groupe de substances ignifuges organiques recueillies en vertu de l'article 71 de la Loi canadienne sur la protection de l'environnement (1999) : Avis concernant certaines substances ignifuges organiques. Données préparées par Environnement Canada, Santé Canada, Programme des substances existantes.
[ECCC 2017a] Environnement et Changement climatique Canada. 2017a. Supporting documentation: Summary tables of substance identity, physical chemical properties and environmental fate and behaviour for Ethylene bis(tetrabromophthalimide). Gatineau (Qc) : Environnement Canada. Information in support of the Screening Assessment for 1H-isoindole-1,3(2H)-dione, 2,2'-(1,2-ethanediyl)bis[4,5,6,7-tetrabromo-. Disponible sur demande à l’adresse : ec.substances.ec@canada.ca (disponible en anglais seulement)
[ECCC 2017b] Environnement et Changement climatique Canada. 2017b. Supporting documentation: Summary tables of ecological exposure information for Ethylene bis(tetrabromophthalimide). Gatineau (Qc) : Environnement Canada. Information in support of the Screening Assessment for 1H-isoindole-1,3(2H)-dione, 2,2'-(1,2-ethanediyl)bis[4,5,6,7-tetrabromo-. Disponible sur demande à l’adresse : ec.substances.ec@canada.ca (disponible en anglais seulement)
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada. [modifié le 12 mars 2017]. Catégorisation. Ottawa (Ont.) : Gouvernement du Canada. [consulté le 20 juin 2017].
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada. 2019. Évaluation préalable – Groupe de certaines substances ignifuges organiques – 1,1'-(Éthane-1,2-diyl)bis[pentabromobenzène] ou Décabromodiphényléthane (DBDPE). Ottawa (Ont.) : Environnement Canada, Santé Canada; Programme des substances existantes.
[EPI Suite] Estimation Programs Interface Suite for Microsoft Windows [Estimation Model]. 2000-2012. Version 4.1. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. (disponible en anglais seulement)
[EQC] Equilibrium Criterion Model [Estimation Model]. 2012. Version 1.00. Peterborough (ON): Trent University, Canadian Environmental Modelling Centre. (disponible en anglais seulement)
[EC] European Commission. 2000a. IUCLID Dataset, N,N’-ethylenebis(3,4,5,6-tetrabromophthalimide), CAS No. 32588-76-4 Year 2000 CD-ROM edition. [place unknown]: European Chemicals Agency, European Commission. [consulté le 18 août 2000] (disponible en anglais seulement)
[EC] European Commission. 2000b. IUCLID Dataset. N,N'-ethylenebis(3,4,5,6)-tetrabromophthalimide. European Commission Joint Research Centre, Institute for Health and Consumer Protection, European Chemical Substances Information System. Rapport. pp. 20. (disponible en anglais seulement)
Gobas FACP, Morrison HA. 2000. Bioconcentration and biomagnification in the aquatic environment. In Boethling RS, Mackay D, editors. Handbook of property estimation methods for chemicals, environmental and health sciences. Boca Raton (FL): CRC Press. p. 189–231. (disponible en anglais seulement)
Gobas F. 2007. Development and review of a generic water-sediment modelling framework for organic chemicals. Rédigé pour Environnement Canada, 26 mars 2007. (disponible en anglais seulement)
Gobas F. 2010. Comments on Approach to Sediment Approach. Rédigé pour Environnement Canada, 25 mars 2010. (disponible en anglais seulement)
Guerra P, Alaee M, Eljarrat E,Barcelo D. 2011. Introduction to Brominated Flame Retardants:Commercially Products, Applications, and Physicochemical Properties. In Eljarrat E, Barceló D. editors. 2011. Brominated Flame Retardants. Series: The Handbook of Environmental Chemistry. Volume 16. Heidelberg Berlin: Springer. 290 pp. (disponible en anglais seulement)
Hardy ML, Aufderheide J, Krueger HO, Mathews ME, Porch JR, Schaefer EC, Stenzel JI, Stedeford T. 2011. Terrestrial toxicity evaluation of decabromodiphenyl ethane on organisms from three trophic levels. Ecotox and Environ Safety 74:703-710. (disponible en anglais seulement)
Hardy ML, Krueger HO, Blankinship AS, Thomas S, Kendall TZ, Desjardins D. 2012. Studies and evaluation of the potential toxicity of decabromodiphenyl ethane to five aquatic and sediment organisms. Ecotox and Environ Safety 75:73-79. (disponible en anglais seulement)
Harner T, Shoeib M. 2002. Measurements of octanol-air partition coefficients (KoA) for polybrominated diphenyl ethers (PBDEs): Predicting partitioning in the environment. J Chem Eng Data 47:228-232. (disponible en anglais seulement)
[HENRYWIN] Henry’s Law Constant Program for Microsoft Windows [Estimation Model]. 2011. Version 3.20. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [consulté en janvier 2014]. (disponible en anglais seulement)
[HYDROWIN] Hydrolysis Rates Program for Microsoft Windows [Estimation Model]. 2010. Version 2.00. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [consulté en janvier 2014]. (disponible en anglais seulement)
[IPCS] International Programme on Chemical Safety. 1997. Flame Retardants: A General Introduction, Environmental Health Criteria 192. (disponible en anglais seulement)
International Research and Development Corporation. 1981. Acute inhalation (one hour) toxicity study in rats (14 days). Testing laboratory: IRDC. Report no.: 254-028. (disponible en anglais seulement)
Juberg D, Alfano K, Coughlin R, Thompson K. 2001. An observational study of object mouthing behaviour by young children. Pediatrics 107(1):135-142. (disponible en anglais seulement)
Kelly BC, Gobas FAPC, McLachlan MS. 2004. Intestinal absorption and biomagnification of organic contaminants in fish, wildlife and humans. Environ Toxicol Chem 23(10):2324–2336. (disponible en anglais seulement)
Kemmlein S, Hahn O, Jann O. 2003. Emissions of organophosphate and brominated flame retardants from selected consumer products and building materials. Atmos Environ 37: 5485–5493. (disponible en anglais seulement)
Klasmeier J, Matthies M, MacLeod M, Fenner K, Scheringer M, Stroebe M, Le Gall AC, McKone TE, van de Meent D, Wania F. 2006. Application of multimedia models for screening assessment of long-range transport potential and overall persistence. Environ Sci Technol 40:53–60. (disponible en anglais seulement)
[KOCWIN] Organic Carbon Partition Coefficient Program for Windows [Estimation Model]. 2010. Version 2.00. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [consulté en janvier 2014].
Kolic T, Shen L, MacPherson K, Fayez L, Gobran T, Helm P, Marvin C, Arsenault G, Reiner E. 2009. The analysis of halogenated flame retardants by GC-HRMS in environmental samples. J Chromatographic Science 47:83-91. (disponible en anglais seulement)
Krueger H, Thomas S, Kendall T. 2003a. S8010: A prolonged sediment toxicity test with Chironomus riparius using spiked sediment. Wildlife International, Ltd. Easton, Maryland (USA): Project number 471A-110. (disponible en anglais seulement)
Krueger H, Thomas S, Kendall T. 2003b. S8010: A prolonged sediment toxicity test with Lumbriculus variegatus using spiked sediment with a total of 2% organic carbon. Wildlife International, Ltd. Easton, Maryland (USA): Project number 471A-109. (disponible en anglais seulement)
[MPBPVP] Melting Point Boiling Point Program for Microsoft Windows [Estimation Model]. 2010. Version 1.43. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [consulté en janvier 2014]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2010. 3M Scotch-Weld hot melt adhesive [PDF]. (disponible en anglais seulement)
Muir DCG, Backus S, Derocher AE, Dietz R, Evans TJ, Gabrielsen GW, Nagy J, Norstrom RJ, Sonne C, Stirling I, Taylor MK and Lectcher RJ. 2006. Brominated Flame Retardants in polar Bears (Ursus maritimus) from Alaska, the Canadian Artic, East Greenland, and Svalbard. Environ. Sci. & Technol. 40(2):449-455. (disponible en anglais seulement)
[NCI] National Chemical Inventories [database on CD-ROM]. 2013. Issue 1. Columbus (OH): American Chemical Society. (disponible en anglais seulement)
[NIEHS] National Institute of Environmental Health Sciences. 1999. Ethylenebis(tetrabromophthalimide) [CASRN 32588-76-4] Review of Toxicological Literature. Research Triangle Park (North Carolina): Integrated Laboratory Systems. (disponible en anglais seulement)
Nyholm JR, Grabic R, Arp HP, Moskeland T, Andersson PL. 2013. Environmental occurrence of emerging and legacy brominated flame retardants near suspected sources in Norway. Science of the Total Environment 443:307-314. (disponible en anglais seulement)
[OCDE] Organisation de coopération et de développement économiques. 1995. OECD Environment Monograph Series No. 102. Risk Reduction Monograph No. 3 - Selected brominated flame retardants background and national experience with reducing risk [PDF]. (disponible en anglais seulement)
[OCDE] Organisation de coopération et de développement économiques. 2010. Emission scenario document on plastics additives [PDF]. Paris (FR): OECD, Environment Directorate. Series on Emission Scenario Documents No. 3. Report No. ENV/JM/MONO(2004)8/REV1, JT00166678. (disponible en anglais seulement)
[OCDE] Organisation de coopération et de développement économiques. 2011. OECD guidelines for testing of chemicals bioaccumulation in fish: Aqueous and dietary exposure. Ébauche V.10. Paris (FR): OCDE, Direction de l’environnement. (disponible en anglais seulement)
Porch JR and Krueger HO. 2005. S8010: A toxicity test to determine the effects of the test substance on seedling emergence of six species of plants. Wildlife International, Ltd. Easton, Maryland (USA): Project number 471-101A. (disponible en anglais seulement)
Radloff D, Spiess HW, Books JT, Dowling KC. 1996. Interaction Between Polybrominated Flame Retardants and High Impact Polystyrene. Journal of Applied Polymer Science 60: 715-720. (disponible en anglais seulement)
Rodwell DE. 1988a. Teratology study in rabbits with BT-93 (final report). Spring Life Sciences, Inc. Conducted for Ethyl Corporation. Study number: 3196.5. Date du rapport : 1988-12-16. (disponible en anglais seulement)
Rodwell DE. 1988b. Teratology study in rats with BT-93 (final report). Spring Life Sciences, Inc. Conducted for Ethyl Corporation. Study number: 3196.4. Date du rapport : 1988-12-16. (disponible en anglais seulement)
Santé Canada. [modifié le 3 mai 2017]. Listes des additifs alimentaires autorisés. Ottawa (Ont.) : Santé Canada, Direction des aliments. [consulté le 24 avril 2014].
Sakuratani Y, Noguchi Y, Kobayashi K, Yamada J, Nishihara T. 2008. Molecular size as a limiting characteristic for bioconcentration in fish. J Environ Biol 29(1):89–92. (disponible en anglais seulement)
Schaefer EC, Carpernter K. 2010. Saytex 8010 : An evaluation of Inherent Biodegradability using the CONCAWE Test. Wildlife International Ltd. Project No. 471E-104. Draft OECD Guideline 302D. Wildlife International Lt Maryland. 45pp. (disponible en anglais seulement)
Schaefer EC, Matthews ME. 2011. Saytex 8010 : Biodegradation in anaerobic digester sludge. Wildlife International Ltd. Project No. 471E-105. OECD Guideline 314C. Wildlife International Lt Maryland. 56pp. (disponible en anglais seulement)
Schenker U, MacLeod M, Scheringer M, Hungerbuhler K. 2005. Improving data quality for environmental fate models: A least-squares adjustment procedure for harmonizing physicochemical properties of organic compounds. Environ Sci Technol 39(21): 8434-8441. (disponible en anglais seulement)
Scheringer M, MacLeod M and Wegmann F. 2009. The OECD Pov and LRTP Screening Tool, Version 2.2, A manual for the OECD Pov and LRTP Screening Tool 2.2 that is a follow-up version of the software POPorNot 1.0 distributed at the OECD/UNEP Workshop on Application of Multimedia Models for Identification of Persistent Organic Pollutants. ETH Zurich, April 2009. Version 2.2 fixes a bug introduced by changes in Excel 2007. (disponible en anglais seulement)
[SPIN] Substances in Preparations in Nordic Countries [database]. 2006. Copenhagen (DK): Nordic Council of Ministers. (disponible en anglais seulement)
Stapleton HM, Allen JG, Kelly SM, Konstantinov A, Klosterhaus S, Watkins D, McClean MD, Webster TF. 2008. Alternate and new brominated flame retardants detected in U.S. house dust. Environ Sci Technol 42:6910-6916. (disponible en anglais seulement)
Stapleton HM, Misenheimer J, Hoffman K, Webster T. 2014. Flame retardant associations between children’s handwipes and house dust. Chemosphere 116:54-60. (disponible en anglais seulement)
Tice R. 1999. Ethylenebis (tetrabromopnthalimide) review of toxicological literature [PDF]. Rédigé pour le National Institute of Environmental Health Sciences. (disponible en anglais seulement)
[TOPKAT] Toxicity Prediction by Komputer Assisted Technology [prediction module]. 2004. Version 6.2. San Diego (CA): Accelrys Software Inc. (disponible en anglais seulement)
UNIBROM. 2014. Unibrom Corp. products: EcoFlame B-951 [internet]. [consulté le 26 mai 2014] (disponible en anglais seulement)
United Kingdom Environment Agency. 2003. Prioritisation of flame retardants for environmental risk assessment.Peter Fish Associates for United Kingdom Environment Agency. ISBN : 978-1-84432-956-4. (disponible en anglais seulement)
[US EPA] US Environmental Protection Agency. 2003. “Exposure and human health reassessment of 2,3,7,8-tetrachlorodibenzo-p-dioxin (TCDD) and related compounds, Part I: Estimating exposure to dioxin-like compounds, Volume 4: Site-specific assessment procedures, Chapter 4: Estimating exposure media concentrations,” EPA/600/P-00/001Cb, U.S. Environmental Protection Agency, National Center for Environmental Assessment, Washington, DC, December 2003. (disponible en anglais seulement)
[US EPA] US Environmental Protection Agency. 2004. High Production Volume (HPV) Track. Sponsor: Albemarle Corporation. CAS Number: 32588764. Phthalimide, N,N'-ethylenebis(tetrabromo-. (disponible en anglais seulement)
[US EPA] US Environmental Protection Agency. 2006. Inventory Update Reporting for CAS RN: 32588-76-4. [US EPA] US Environmental Protection Agency. 2014. An Alternative Assessment for the Flame retardant Decarbromodiphenyl Ether (DecaBDE) (final report) [PDF]. 901 pp. (disponible en anglais seulement)
WARF Institute, Inc. 1976. Rat - 28 day feeding study - study code T-626. Testing laboratory: WARF Institute, Inc. Study number: T-626. Report date: 1976-09-15. (disponible en anglais seulement)
Webster E, Mackay D, Di Guardo A, Kane D,and Woodfine D. 2004. Regional differences in chemical fate model outcome. Chemosphere 55:1361–1376. (disponible en anglais seulement)
Wilson R, Jones-Otazo H, Petrovic S, Mitchell I, Bonvalot Y, Williams D, Richardson GM. 2013. Revisiting dust and soil ingestion rates based on hand-to-mouth transfer. Human and Ecological Risk Assessment 19(1):158-188. (disponible en anglais seulement)
World of Chemicals [database]. 2013. CAS search, CAS: 32588-76-4. Ethylenebistetrabromophthalimide. Singapore: WOC Labs Pte. Limited. (disponible en anglais seulement)
Zeiger E, Haworth S, Mortelmans K, Speck W. 1985. Mutagenicity testing of di(2-ethylhexyl) phthalate and related chemicals in Salmonella. Environmental Mutagenesis 7: 213-232. Testing laboratory: SRI International. (disponible en anglais seulement)
Annexe A. Tableau du poids de la preuve pour la caractérisation des risques pour l'environnement
| Preuve | degré de confiancea | Pertinence dans l’évaluationb | Poids attribuéc |
|---|---|---|---|
| Propriétés phyiques et chimiques (hydrosolubilité et log Koe) | Faible à modérée | Élevé | Modéré |
| Persistance | Élevé | Modéré à élevé | Élevé |
| Bioaccumulation | Modéré | Élevé | Modéré à élevé |
| Analyse de l'exposition | Faible à modéré | Élevé | Modéré à élevé |
| Analyse des risques | Faible à modéré | Élevé | Modéré à élevé |
| Dérivés (produits de phototransformation et produits de biodégradation) | Faible | Faible | Faible |
a Le degré de confiance est déterminé en fonction de la qualité des données, leur variabilité, leur adéquation et les lacunes en cette matière.
b La pertinence renvoie à l’incidence de l’élément de preuve dans l’évaluation.
c Le poids est attribué à un élément de preuve selon la combinaison du degré de confiance qui lui est associé et sa pertinence dans l’évaluation.
Annexe B. Estimations de l'absorption quotidienne (ug/kg p.c. par jour) d'EBTBP par divers groupes d'âge au sein de la population générale du Canada
| Voie d'exposition | 0 à 6 moisa | 0,5 à 4 ansb | 5 à 11 ansc | 12 à 19 ansd | 20 à 59 anse | 60 ans et plusf |
|---|---|---|---|---|---|---|
| Poussièreg | 0,06 à 0,39 | 0,03 à 0,20 | 0,011 à 0,076 | 4,1E-04 à 2,82E-03 | 3,9E-04 à 2,7E-03 | 3,8E-04 à 2,6E-03 |
| Solh | 0,0E+00 | 4,6E-05 | 1,7E-03 | 6,0E-05 | 5,7E-05 | 5,3E-05 |
| Absorption totale | 3,9E-01 | 2,0E-01 | 7,8E-02 | 2,9E-03 | 2,7E-03 | 2,7E-03 |
a On présume que le nourrisson pèse 7,5 kg (Santé Canada, 1998) et ingère 38 et 0 mg de poussière et de sol par jour, respectivement (Wilson et al., 2013).
b On présume que le nourrisson pèse 15,5 kg (Santé Canada, 1998) et ingère 41 et 14 mg de poussière et de sol par jour, respectivement (Wilson et al., 2013).
c On présume que le nourrisson pèse 31 kg (Santé Canada, 1998) et ingère 31 et 21 mg de poussière et de sol par jour, respectivement (Wilson et al., 2013).
d On présume que le nourrisson pèse 59,4 kg (Santé Canada, 1998) et ingère 2,2 et 1,4 mg de poussière et de sol par jour, respectivement (Wilson et al., 2013).
e On présume que le nourrisson pèse 70,9 kg (Santé Canada, 1998) et ingère 2,5 et 1,6 mg de poussière et de sol par jour, respectivement (Wilson et al., 2013).
f On présume que le nourrisson pèse 72 kg (Santé Canada, 1998) et ingère 2,5 et 1,5 mg de poussière et de sol par jour, respectivement (Wilson et al., 2013).
g On n'a relevé aucune donnée canadienne pour l'EBTBP dans les études sur le sol ou la poussière. L'EBTBP n'a pas été mesuré dans le sol ni dans la poussière à aucun autre endroit. On utilise une plage de concentrations de poussière pour les produits ignifuges substituts, le décaBDE et le DBDPE, afin d'estimer l'exposition à l'EBTBP par la poussière. On a signalé une concentration maximale de 76 130 ng/g de décaBDE dans 30 résidences à Boston, au Massachusetts (Stapleton et al., 2014). Le DBDPE a également été détecté dans 20 résidences à Boston à une concentration maximale de 11 070 ng/g (Stapleton et al., 2008). Ces deux concentrations ont été choisies pour calculer une fourchette d'estimations d'absorption de l'EBTBP par la poussière.
h On n'a recensé aucune étude appropriée ou pertinente sur la surveillance de l'EBTBP dans le sol et les sédiments en Amérique du Nord. Par conséquent, on a choisi la CEE maximale prévue dans le sol de 2 540 µg/kg ps pour calculer les estimations d'absorption découlant de l'ingestion de sol.
