Petite chauve-souris brune, de la chauve-souris nordique et de la pipistrelle de l’Est : programme de rétablissement proposé 2015
Loi sur les espèces en péril
Série de Programmes de rétablissement

gauche Photo : © Jordi Segers, 2015; centre Photo : © Hugh Broders, 2015; droite Photo : © Hugh Broders, 2015
Table des matières
- Table des matières
- Préface
- Remerciements
- Sommaire
- Résumé du caractère réalisable du rétablissement
- 1. Évaluation des espèces par le COSEPAC
- 2. Information sur la situation de l’espèce
- 3. Information sur les espèces
- 4. Menaces
- 5. Objectifs en matière de population et de répartition
- 6. Stratégies et approches générales pour l’atteinte des objectifs
- 7. Habitat essentiel
- 8. Mesure des progrès
- 9. Énoncé sur les plans d’action
- 10. Références
- Annexe A : Effets sur l’environnement et sur les espèces non ciblées
- Annexe B : Autres besoins en matière d’études des menaces connues et présumées

Référence recommandée :
Environnement Canada. 2015. Programme de rétablissement de la petite chauve-souris brune (Myotis lucifugus), de la chauve-souris nordique (Myotis septentrionalis) et de la pipistrelle de l’Est (Perimyotis subflavus) au Canada [Proposition]. Série de Programmes de rétablissement de la Loi sur les espèces en péril. Environnement Canada, Ottawa. ix + 121 pp.
Pour télécharger le présent programme de rétablissement ou pour obtenir un complément d’information sur les espèces en péril, incluant les rapports de situation du Comité sur la situation des espèces en péril au Canada (COSEPAC), les descriptions de la résidence, les plans d’action et d’autres documents connexes sur le rétablissement, veuillez consulter le Registre public des espèces en péril.
Illustrations de la couverture : gauche : chauve-souris nordique, © Jordi Segers; centre : petite chauve-souris brune, © Hugh Broders; droite : pipistrelle de l’Est © Hugh Broders
Also available in English under the title
“Recovery Strategy for Little Brown Myotis (Myotis lucifugus), Northern Myotis (Myotis septentrionalis), and Tri-colored Bat (Perimyotis subflavus) in Canada [Proposed]”
Le contenu du présent document (à l’exception des illustrations) peut être utilisé sans permission, mais en prenant soin d’indiquer la source.
Préface
En vertu de l’Accord pour la protection des espèces en péril (1996), les gouvernements fédéral, provinciaux et territoriaux signataires ont convenu d’établir une législation et des programmes complémentaires qui assureront la protection efficace des espèces en péril partout au Canada. En vertu de la Loi sur les espèces en péril (L.C. 2002, ch. 29) (LEP), les ministres fédéraux compétents sont responsables de l’élaboration des programmes de rétablissement pour les espèces inscrites comme étant disparues du pays, en voie de disparition ou menacées et sont tenus de rendre compte des progrès réalisés dans les cinq ans suivant la publication du document final dans le Registre public des espèces en péril.
Le ministre de l’Environnement et ministre responsable de l’Agence Parcs Canada est le ministre compétent en vertu de la LEP de la petite chauve-souris brune, de la chauve-souris nordique et de la pipistrelle de l’Est, et a élaboré ce programme de rétablissement, conformément à l’article 37 de la LEP. Dans la mesure du possible, le programme de rétablissement a été préparé en collaboration avec les gouvernements de la Colombie-Britannique, de l’Alberta, de la Saskatchewan, du Manitoba, de l’Ontario, du Québec, du Nouveau-Brunswick, de l’Île-du-Prince-Édouard, de la Nouvelle-Écosse, de Terre-Neuve-et-Labrador, du Yukon et des Territoires du Nord-Ouest, ainsi que du Sahtu Renewable Resources Board et du Wek’èezhìi Renewable Resources Board.
La réussite du rétablissement des espèces dépendra de l’engagement et de la collaboration d’un grand nombre de parties concernées qui participeront à la mise en œuvre des directives formulées dans le présent programme. Cette réussite ne pourra reposer seulement sur Environnement Canada, sur l’Agence Parcs Canada ou sur toute autre compétence. Tous les Canadiens et les Canadiennes sont invités à appuyer le programme et à contribuer à sa mise en œuvre pour le bien de la petite chauve-souris brune, de la chauve-souris nordique, de la pipistrelle de l’Est et de l’ensemble de la société canadienne.
Le présent programme de rétablissement sera suivi d’un ou de plusieurs plans d’action qui présenteront de l’information sur les mesures de rétablissement qui doivent être prises par Environnement Canada, l’Agence Parcs Canada et d’autres compétences et/ou organisations participant à la conservation de l’espèce. La mise en œuvre du présent programme est assujettie aux crédits, aux priorités et aux contraintes budgétaires des compétences et organisations participantes.
Le programme de rétablissement établit l’orientation stratégique visant à arrêter ou à renverser le déclin de l’espèce, incluant la désignation de l’habitat essentiel dans la mesure du possible. Il fournit à la population canadienne de l’information pour aider à la prise de mesures visant la conservation de l’espèce. Lorsqu’un programme de rétablissement désigne de l’habitat essentiel, il peut y avoir des incidences réglementaires futures, selon l’endroit où se trouve l’habitat essentiel désigné. La LEP exige que l’habitat essentiel désigné se trouvant à l’intérieur d’aires protégées fédérales soit décrit dans la Gazette du Canada, après quoi les interdictions relatives à la destruction de cet habitat seront appliquées. En ce qui concerne l’habitat essentiel situé sur le territoire domanial à l’extérieur des aires protégées fédérales, le ministre de l’Environnement doit présenter un énoncé sur la protection juridique existante ou prendre un arrêté de manière à ce que les interdictions relatives à la destruction de l’habitat essentiel soient appliquées. En ce qui concerne l’habitat essentiel se trouvant sur le territoire non domanial, si le ministre de l’Environnement estime qu’une partie de l’habitat essentiel n’est pas protégée par les dispositions de la LEP, par les mesures prises aux termes de cette dernière ou par toute autre loi fédérale, et que cette partie de l’habitat essentiel n’est pas protégée efficacement par les lois provinciales ou territoriales, il doit, comme le prévoit la LEP, recommander au gouverneur en conseil de prendre un décret visant à étendre l’interdiction de détruire à cette partie de l’habitat essentiel. La décision de protéger l’habitat essentiel se trouvant sur le territoire non domanial et n’étant pas autrement protégé demeure à la discrétion du gouverneur en conseil.
Remerciements
Le présent programme de rétablissement a été préparé par Krista Baker, David Andrews, Kathy St. Laurent (Environnement Canada – Service canadien de la faune (EC SCF) – Région de l’Atlantique), Ryan Zimmerling et Sybil Feinman (EC SCF – Région de la capitale nationale).
Andrew Boyne (EC SCF – Région de l’Atlantique), Robert McLean, Manon Dubé, Carolyn Seburn, Veronica Aponte, Marc André Cyr (EC SCF – Région de la capitale nationale), Diana Ghikas, Donna Bigelow, Lynne Burns, Amy Ganton, Dawn Andrews (EC SCF – Région des Prairies et du Nord), Syd Cannings, Tanya Luszcz, Megan Harrison (EC SCF – Région du Pacifique et du Yukon), Sylvain Giguère, Pierre André Bernier (EC SCF – Région du Québec), Krista Holmes (EC SCF – Région de l’Ontario), Hugh Broders (Saint Mary’s University), Craig Willis (University of Winnipeg), Jordi Segers (Canadian Wildlife Health Cooperative), Derek Morningstar (Myotistar/Golder Associates), Juliet Craig (British Columbia Community Bat Project Network), Laura Kaupas (University of Calgary), Thomas Jung (ministère de l’Environnement du Yukon), Joanna Wilson, Ashley McLaren, Stephanie Behrens (gouvernement des Territoires du Nord-Ouest), Purnima Govindarajulu (ministère de l’Environnement de la Colombie-Britannique), Lisa Wilkinson (ministère de l’Environnement et des Parcs de l’Alberta), Daphne Murphy (ministère de l’Environnement de la Saskatchewan), Jay Fitzsimmons, Lesley Hale, Chris Risley, Brian Naylor, Jim Saunders, Vivian Brownell, Katie Paroschy, Sue Russell, Aileen Wheeldon, Todd Copeland, Peter Davis, Chuck McCridden, Megan Rasmussen, Valerie Vaillancourt, Laura Darbey, Bill Greaves, Christopher Martin, April Mitchell (ministère des Richesses naturelles et des Forêts de l’Ontario), Nathalie Desrosiers, Ariane Masse, Anouk Simard, Isabelle Gauthier (ministère des Forêts, de la Faune et des Parcs du Québec), Mary Sabine, Maureen Toner (ministère des Ressources naturelles du Nouveau-Brunswick), Garry Gregory (ministère des Communautés, des Terres et de l’Environnement de l’Île-du-Prince-Édouard), Mark Elderkin (ministère des Ressources naturelles de la Nouvelle-Écosse), Shelley Pardy, Bruce Rodrigues, Allysia Park, Sara McCarthy (ministère de l’Environnement et de la Conservation de Terre-Neuve-et-Labrador), Marie Josée Laberge, Pippa Shepherd (Agence Parcs Canada) et le personnel du ministère de la Défense nationale ont fourni leur expertise, un examen de la documentation et/ou des données durant la préparation du programme de rétablissement.
Sommaire
La petite chauve-souris brune (Myotis lucifugus), la chauve-souris nordique (Myotis septentrionalis) et la pipistrelle de l’Est (Perimyotis subflavus) sont des espèces insectivores de petite taille appartenant à la famille des Vespertilionidés. Les trois espèces ont été inscrites d’urgence en 2014 comme espèces en voie de disparition à l’annexe 1 de la Loi sur les espèces en péril (LEP) en raison de déclins spectaculaires et soudains dans l’est des aires de répartition de la petite chauve-souris brune et de la chauve-souris nordique, et dans l’ensemble de l’aire de répartition canadienne de la pipistrelle de l’Est. Ces déclins sont directement attribuables au syndrome du museau blanc (SMB).
La présence de la petite chauve-souris brune et de la chauve-souris nordique a été confirmée dans chaque province et chaque territoire du Canada, à l’exception du Nunavut. Environ 50 et 40 % de leurs aires de répartition mondiales respectives se trouvent au Canada. La présence de la pipistrelle de l’Est a été signalée en Ontario, au Québec, au Nouveau-Brunswick et en Nouvelle-Écosse, et on estime que 10 % de sa population mondiale se trouve au Canada.
Le SMB constitue la plus grande menace pesant sur la petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est. En raison de l’importance du SMB, le cas échéant, le présent programme de rétablissement établit les différences entre les zones touchées par le SMB et celles qui ne le sont pas encore (p. ex. objectifs en matière de population et de répartition, menaces et approches de rétablissement). Dans les régions qui sont déjà touchées par le SMB, l’importance des autres menaces pesant sur les trois espèces de chauves-souris est amplifiée, car la mortalité d’un petit nombre d’individus restants (en particulier d’adultes) pourrait avoir des incidences sur la survie et le rétablissement des populations locales, de même que sur le développement d’une résistance au champignon responsable du SMB. Les menaces autres que le SMB comprennent la perte et la dégradation de l’habitat (p. ex. destruction ou dégradation des hibernacles, des colonies de maternité et des aires d’alimentation), les perturbations ou les dommages (p. ex. les collisions et le barotraumatismenote1 associés aux éoliennes, les dommages intentionnels aux individus, le dérangement découlant d’activités scientifiques ou récréatives et les perturbations industrielles), la pollution et les changements climatiques.
On ignore si le rétablissement de la petite chauve-souris brune, de la chauve-souris nordique et de la pipistrelle de l’Est est réalisable au Canada. Suivant le principe de précaution, le présent programme de rétablissement a été élaboré, conformément au paragraphe 41(1) de la LEP.
Dans les régions touchées par le SMB, l’objectif à court terme (de 12 à 18 ans) en matière de population pour la petite chauve-souris brune et la chauve-souris nordique consiste à maintenir (et à accroître, dans la mesure du possible) la population par rapport à son niveau actuel (2015). Toujours dans les régions touchées par le SMB, l’objectif à long terme (plusieurs générations) en matière de population est une population autosuffisante, résiliente et redondante (voir la section 5 : Objectifs en matière de population et de répartition pour de plus amples détails et pour les définitions). Dans les régions qui ne sont pas encore touchées par le SMB, l’objectif en matière de population consiste à maintenir (et à accroître, dans la mesure du possible) la population par rapport à son niveau actuel. L’objectif en matière de répartition établi pour la petite chauve-souris brune et la chauve-souris nordique consiste à maintenir (ou à rétablir, le cas échéant) la zone d’occurrence antérieure à l’apparition du SMB.
L’objectif à court terme en matière de population pour la pipistrelle de l’Est consiste à maintenir (et à accroître, dans la mesure du possible) la population par rapport à son niveau actuel (2015) au cours des 10 prochaines années. L’objectif à long terme est une population autosuffisante, résiliente et redondante. L’objectif en matière de répartition consiste à rétablir (puis à maintenir) la zone d’occurrence antérieure à l’apparition du SMB.
Les stratégies générales visant à soutenir la survie et le rétablissement de la petite chauve-souris brune, de la chauve-souris nordique et de la pipistrelle de l’Est sont présentées à la section 6.2, intitulée Orientation stratégique pour le rétablissement. Les approches nécessaires pour l’atteinte des objectifs en matière de population et de répartition seront différentes dans les régions où le SMB a déjà causé des déclins spectaculaires par rapport aux régions qui n’ont pas encore été touchées par le SMB.
L’habitat essentiel des trois espèces est partiellement désigné dans le présent programme de rétablissement. Un calendrier des études est inclus pour obtenir les renseignements nécessaires à l’achèvement de la désignation de l’habitat essentiel.
Un ou plusieurs plans d’action visant la petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est seront publiés dans le Registre public des espèces en péril dans les trois années suivant la publication finale du présent programme de rétablissement.
Résumé du caractère réalisable du rétablissement
D’après les quatre critères suivants utilisés par le gouvernement du Canada, le caractère réalisable du rétablissement de la petite chauve-souris brune, de la chauve-souris nordique et de la pipistrelle de l’Est est inconnu. Conformément au principe de précaution, un programme de rétablissement a été élaboré en vertu du paragraphe 41(1) de la LEP, tel qu’il convient de faire lorsque le rétablissement est déterminé comme étant réalisable. Le présent programme de rétablissement aborde les lacunes dans les connaissances entourant le caractère réalisable du rétablissement. Le caractère réalisable du rétablissement de la pipistrelle de l’Est est évalué séparément car, contrairement à ce que l’on observe chez la petite chauve-souris brune et la chauve-souris nordique, le SMB s’étend à l’ensemble de l’aire de répartition canadienne de la pipistrelle de l’Est.
Petite chauve-souris brune et chauve-souris nordique
1. Des individus des espèces sauvages capables de se reproduire sont disponibles maintenant ou le seront dans un avenir prévisible pour maintenir les populations ou augmenter leur abondance.
Oui. Dans les provinces et les territoires où le SMB n’est pas présent, les deux espèces sont apparemment abondantes dans la majeure partie de leurs aires de répartition respectives. À l’heure actuelle, on pense qu’un nombre adéquat d’individus reproducteurs serait disponible dans les Prairies et l’Ouest canadien pour maintenir les espèces au Canada ou augmenter leur abondance. Le nombre d’individus restants dans la majeure partie de l’est du Canada et des États-Unis est très faible. Une immigration depuis des populations externes (c.-à-d. depuis les États-Unis) n’est donc pas considéré comme probable. Toutefois, des données préliminaires recueillies dans certaines parties de l’aire de répartition des espèces indiquent qu’une très faible proportion d’individus pourrait survivre au SMB.
2. De l’habitat convenable suffisant est disponible pour soutenir les espèces, ou pourrait être rendu disponible par des activités de gestion ou de remise en état de l’habitat.
Inconnu. Il y a probablement suffisamment d’habitat d’estivage (c.-à-d. aires de repos et d’alimentation), et d’autres superficies d’habitat pourraient être rendues disponibles par des activités de gestion ou de remise en état. Cependant, ce ne sont pas tous les sites qui sont connus. L’habitat d’hivernage convenable (c.-à-d. hibernacles) qui est exempt de spores causant le SMB est probablement suffisant dans les Prairies ainsi que dans l’ouest et le nord du Canada, mais a considérablement diminué dans de nombreuses régions de l’est du pays. Bien que les caractéristiques des hibernacles soient généralement connues dans l’est du Canada, l’emplacement de certains d’entre eux demeure inconnu. Dans les Prairies ainsi que dans l’ouest et le nord du pays, les caractéristiques de l’habitat et l’emplacement des hibernacles ne sont pas encore bien compris. À l’heure actuelle, il est impossible de repérer l’habitat d’hivernage disponible, mais actuellement inoccupé, qui pourrait s’avérer nécessaire au rétablissement de l’une ou l’autre des deux espèces.
3. Les principales menaces pesant sur les espèces ou sur leur habitat (y compris les menaces à l’extérieur du Canada) peuvent être évitées ou atténuées.
Inconnu. La principale menace pesant sur ces espèces est le SMB, causé par un champignon envahissant (Pseudogymnoascus destructans) dont les spores responsables du SMB sont introduites dans les hibernacles non infectés. Il pourrait être possible, par la sensibilisation du public et le respect des protocoles de manipulation et des pratiques de gestion bénéfiques (PGB), de limiter la propagation de la maladie par l’homme en évitant les activités qui peuvent favoriser la propagation des spores dans les hibernacles non infectés. Néanmoins, on prévoit que le SMB continuera de se propager au Canada par des contacts entre les chauves-souris. On ne sait pas si les obstacles naturels (p. ex. les Rocheuses) peuvent stopper ou ralentir la propagation de la maladie par les chauves-souris. Aucun traitement du SMB ayant fait l’objet d’essais à grande échelle n’existe, mais un programme de recherche intensive porte actuellement sur le traitement et les mesures d’atténuation possibles. De nouvelles recherches ont permis de découvrir des substances issues d’une bactérie et d’une levure qui inhibent la croissance du P. destructans en laboratoire. Cette recherche en est encore aux premiers stades d’élaboration, et l’efficacité de son application dans le domaine est inconnue.
4. Des techniques de rétablissement existent pour atteindre les objectifs en matière de population et de répartition ou leur élaboration peut être prévue dans un délai raisonnable.
Inconnu. Même si le SMB s’est principalement propagé au Canada par l’entremise des chauves-souris elles mêmes, la gestion et l’intendance de l’habitat visant à empêcher (ou à ralentir) la propagation par l’homme des spores causant le SMB pourraient constituer des techniques de rétablissement efficaces de ces espèces. Des traitements potentiels et des mesures d’atténuation du SMB font actuellement l’objet de recherches et d’essais. Des techniques de mise en valeur de l’habitat qui accroissent la disponibilité d’aires de repos optimales dans les régions où l’on sait que les chauves-souris élèvent leurs petits pourraient aider au rétablissement de ces espèces. De plus, le fait de limiter l’accès aux hibernacles et les activités perturbant ces derniers peut avoir des effets positifs sur la croissance de la population.
Pipistrelle de l’Est
1. Des individus de l’espèce sauvage capables de se reproduire sont disponibles maintenant ou le seront dans un avenir prévisible pour maintenir la population ou augmenter son abondance.
Oui. Dans l’est du Canada, où l’espèce et le SMB sont présents, la pipistrelle de l’Est continue à persister avec de très faibles niveaux de population. Des populations existent encore aux États-Unis, mais une immigration depuis des populations de l’extérieur n’est pas considérée comme probable. Il n’existe aucune estimation fiable de la population au Canada. Pour le moment, il y aurait peu d’individus capables de reproduction pour accroître l’abondance des populations.
2. De l’habitat convenable suffisant est disponible pour soutenir l’espèce, ou pourrait être rendu disponible par des activités de gestion ou de remise en état de l’habitat.
Inconnu. Il y a probablement suffisamment d’habitat d’estivage (aires de repos et d’alimentation), mais ce ne sont pas tous les sites qui sont connus. L’habitat d’hivernage convenable (c.-à-d. hibernacles) qui est exempt du champignon causant le SMB pourrait être inexistant parce que la totalité de l’aire de répartition canadienne de la pipistrelle de l’Est chevauche les zones touchées par le SMB. On ne connaît pas l’emplacement de tous les hibernacles de l’espèce. Il est actuellement impossible de repérer l’habitat disponible, mais actuellement inoccupé, qui pourrait s’avérer nécessaire au rétablissement de l’espèce.
3. Les principales menaces pesant sur l’espèce ou sur son habitat (y compris les menaces à l’extérieur du Canada) peuvent être évitées ou atténuées.
Inconnu. La principale menace pesant sur ces espèces est un champignon envahissant (Pseudogymnoascus destructans). Il n’existe aucun traitement du SMB ayant fait l’objet d’essais à grande échelle, mais un programme de recherche intensive porte actuellement sur le traitement et les mesures d’atténuation possibles. De nouvelles recherches ont permis de découvrir des substances issues d’une bactérie et d’une levure qui inhibent la croissance du P. destructans en laboratoire. Cette recherche en est encore aux premiers stades d’élaboration, et l’efficacité de son application dans le domaine est inconnue
4. Des techniques de rétablissement existent pour atteindre les objectifs en matière de population et de répartition ou leur élaboration peut être prévue dans un délai raisonnable.
Inconnu. Parce qu’il est présumé que le SMB couvre la totalité de l’aire de répartition canadienne de la pipistrelle de l’Est, il sera difficile de réaliser les recherches nécessaires à la mise au point d’un traitement du SMB à l’intérieur d’un délai raisonnable pour le rétablissement. On mène actuellement des recherches intensives à cet égard.
1. Évaluation des espèces par le COSEPACnote *
- Date de l’évaluation :
- Novembre 2013
- Nom commun (population) :
- Petite chauve-souris brune
- Nom scientifique :
- Myotis lucifugus
- Statut selon le COSEPAC :
- Espèce en voie de disparition
- Justification de la désignation :
- Environ 50 % de l’aire de répartition mondiale de cette petite chauve-souris se trouve au Canada. Les sous-populations dans la partie est de l’aire de répartition ont été dévastées par le syndrome du museau blanc, une maladie fongique causée par un pathogène introduit. Cette maladie a été détectée pour la première fois au Canada en 2010 et a causé jusqu’à maintenant un déclin général de 94 % des effectifs connus de chauves-souris Myotis hibernantes en Nouvelle-Écosse, au Nouveau-Brunswick, en Ontario et au Québec. L’aire de répartition actuelle du syndrome du museau blanc s’étend à un rythme moyen de 200 à 250 kilomètres par année. À ce rythme, l’ensemble de la population canadienne sera probablement affectée d’ici 12 à 18 ans. La propagation vers le nord ou vers l’ouest du pathogène ne semble pas être contenue, et les conditions favorables à sa croissance sont présentes dans toute l’aire de répartition restante.
- Présence au Canada :
- Yukon, Territoires du Nord-Ouest, Colombie-Britannique, Alberta, Saskatchewan, Manitoba, Ontario, Québec, Nouveau-Brunswick, Île-du-Prince-Édouard, Nouvelle-Écosse, Terre-Neuve-et-Labrador
- Historique du statut selon le COSEPAC :
- Espèce désignée « en voie de disparition » suivant une évaluation d’urgence le 3 février 2012. Réexamen et confirmation du statut en novembre 2013.
- Date de l’évaluation :
- Novembre 2013
- Nom commun (population) :
- Chauve-souris nordique
- Nom scientifique :
- Myotis septentrionalis
- Statut selon le COSEPAC :
- Espèce en voie de disparition
- Justification de la désignation :
- Environ 40 % de l’aire de répartition mondiale de cette chauve-souris nordique se trouve au Canada. Les sous-populations dans la partie est de l’aire de répartition ont été dévastées par le syndrome du museau blanc, une maladie fongique causée par un pathogène introduit. Cette maladie a été détectée pour la première fois au Canada en 2010 et a causé jusqu’à maintenant un déclin général de 94 % des effectifs connus de chauves-souris Myotis hibernantes dans les hibernacles en Nouvelle-Écosse, au Nouveau-Brunswick, en Ontario et au Québec, par comparaison aux dénombrements effectués avant l’apparition de la maladie. Les modèles prédisent une probabilité de disparition fonctionnelle de la petite chauve-souris brune de 99 % d’ici 2026 dans le nord-est des États-Unis. Étant donné des caractéristiques semblables du cycle vital, les prédictions s’appliquent probablement également à la présente espèce. En plus de sa tendance à être relativement peu abondante dans les hibernacles, certaines indications montrent que l’espèce connaît des déclins plus marqués que d’autres espèces depuis l’apparition du syndrome du museau blanc. L’aire de répartition actuelle du syndrome du museau blanc chevauche environ un tiers de l’aire de répartition de l’espèce et prend de l’expansion à un rythme moyen de 200 à 250 kilomètres par année. À ce rythme, l’ensemble de la population canadienne sera probablement affectée d’ici 12 à 18 ans. La propagation vers le nord ou vers l’ouest du pathogène ne semble pas être contenue, et les conditions favorables à sa croissance sont présentes dans toute l’aire de répartition restante.
- Présence au Canada :
- Yukon, Territoires du Nord-Ouest, Colombie-Britannique, Alberta, Saskatchewan, Manitoba, Ontario, Québec, Nouveau-Brunswick, Île-du-Prince-Édouard, Nouvelle-Écosse, Terre-Neuve-et-Labrador
- Historique du statut selon le COSEPAC :
- Espèce désignée « en voie de disparition » suivant une évaluation d'urgence le 3 février 2012. Réexamen et confirmation du statut en novembre 2013.
- Date de l’évaluation :
- Novembre 2013
- Nom commun (population) :
- Pipistrelle de l’Est
- Nom scientifique :
- Perimyotis subflavus
- Statut selon le COSEPAC :
- Espèce en voie de disparition
- Justification de la désignation :
- Cette chauve-souris est l’une des plus petites espèces de chauves-souris de l’est de l’Amérique du Nord. Environ 10 % de son aire de répartition mondiale se trouve au Canada, et elle est considérée comme étant rare dans la majeure partie de son aire de répartition canadienne. Des déclins de plus de 75 % causés par le syndrome du museau blanc ont été constatés dans les populations hibernantes connues au Québec et au Nouveau-Brunswick. Cette maladie fongique, causée par un pathogène envahissant, a été détectée pour la première fois au Canada en 2010 et a entraîné des déclins semblables chez la petite chauve-souris brune et la chauve-souris nordique dans l’est du Canada et dans le nord-est des États-Unis. La majeure partie de l’aire de répartition canadienne de l’espèce chevauche l’aire de répartition actuelle du syndrome du museau blanc, et d’autres déclins sont à prévoir suivant l’infection d’un nombre grandissant d’hibernacles.
- Présence au Canada :
- Ontario, Québec, Nouveau-Brunswick, Nouvelle-Écosse
- Historique du statut selon le COSEPAC :
- Espèce désignée « en voie de disparition » suivant une évaluation d'urgence le 3 février 2012. Réexamen et confirmation du statut en novembre 2013.
2. Information sur la situation de l’espèce
Environ 50 %, 40 % et 10 % des aires de répartition mondiales de la petite chauve-souris brune, de la chauve-souris nordique et de la pipistrelle de l’Est, respectivement, se trouvent au Canada (COSEWIC, 2013).
La petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est ont été inscrites comme espèces en voie de disparition au Canada à l’annexe 1 de la Loi sur les espèces en péril (LEP, ch. 29) en novembre 2014 par l’intermédiaire d’un décret d’inscription d’urgence. La petite chauve-souris brune et la chauve-souris nordique sont inscrites à la Liste des espèces en péril de l’Ontario comme espèces en voie de disparition depuis janvier 2013 (O. Reg. 230/08), en vertu de la Loi de 2007 sur les espèces en voie de disparition (LEVD) de l’Ontario (OMNRF, 2015). Les trois espèces sont aussi protégées en vertu de la Loi de 1997 sur la protection du poisson et de la faune de l’Ontario, à titre de mammifères spécialement protégés. Les trois espèces sont inscrites comme espèces en voie de disparition aux termes de la Loi sur les espèces en péril du Nouveau-Brunswick depuis juin 2013, et ont été ajoutées à la liste des animaux protégés en vertu de l’Endangered Species Act de la Nouvelle-Écosse en juillet 2013. La petite chauve-souris brune et la chauve-souris nordique sont inscrites comme espèces en voie de disparition aux termes de la Loi sur les espèces et les écosystèmes en voie de disparition du Manitoba depuis juin 2015.
Ces espèces ne sont pas visées par les lois provinciales et territoriales sur les espèces en péril du Yukon, de la Colombie-Britannique, des Territoires du Nord-Ouest, de l’Alberta, de la Saskatchewan, du Québec et de Terre-Neuve-et-Labrador, mais elles sont néanmoins protégées en vertu des lois sur les espèces sauvages de ces provinces et territoires. Au Québec, la pipistrelle de l’Est figure sur la Liste des espèces susceptibles d’être désignées menacées ou vulnérables, établie aux termes de la Loi sur les espèces menacées ou vulnérables (RLRQ, chap. E-12.01), mais cette dernière n’offre aucune protection supplémentaire à l’espèce. En Saskatchewan, le Wildlife Amendment Regulation (2013) a retiré tous les Chiroptères de la Saskatchewan de la liste des espèces sauvages non protégées, ce qui leur confère une protection contre la chasse non autorisée. Ces espèces ne sont pas visées ni protégées par la Wildlife Conservation Act de l’Île-du-Prince-Édouard. La présence de ces espèces n’a pas été confirmée au Nunavut, mais la couverture des relevés y est limitée.
Les cotes de conservation de NatureServe (2015) pour le Canada et les États-Unis sont présentées au tableau 1.
| Région | Petite chauve-souris brune | Chauve-souris nordique | Pipistrelle de l’Est | Présence du SMB (découvert en hiver) |
|---|---|---|---|---|
| Cote mondiale | G3G4 | G1G2 | G3G4 | - |
| États-Unis | N3 | N1N2 | N3N4 | Oui (2006-2007) |
| Canada | N3 | N2N3 | N2N3 | - |
| Terre Neuve | S4 | S2S3 | Sans objet | - |
| Labrador | S4 | SNR | Sans objet | - |
| Nouvelle-Écosse | S1 | S2 | S1 | Oui (2010-2011) |
| Île-du-Prince-Édouard | S1 | S1 | Sans objet | Oui (2012-2013) |
| Québec | S1 | S1 | S1 | Oui (2009-2010) |
| Nouveau-Brunswick | S1 | S1 | S1 | Oui (2010-2011) |
| Ontario | S4 | S3 | S3? | Oui (2009-2010) |
| Manitoba | S2N, S5B | S3S4N, S4B | Sans objet | - |
| Saskatchewan | S5B, S5N | S4B, SNRN | Sans objet | - |
| Alberta | S5 | S2S4 | Sans objet | - |
| Colombie-Britannique | S4 | S3S4 | Sans objet | - |
| Terre Neuve | S2 | S2 | Sans objet | - |
| Yukon | S1S3 | S1S2 | Sans objet | - |
- Types de cotes : G – cote de conservation mondiale; N – cote de conservation nationale; S – cote de conservation infranationale (provinciale ou territoriale).
- Définitions des cotes : 1 = gravement en péril; 2 = en péril; 3 = vulnérable; 4 = apparemment non en péril; 5 = non en péril; SNR = non classée; SU = non classable; B = population reproductrice; N = population non reproductrice.
3. Information sur les espèces
3.1. Description des espèces
Petite chauve-souris brune
La petite chauve-souris brune (entre 7 et 9 g) est une petite chauve-souris qui présente un pelage brun, des oreilles noires, des ailes noires et une membrane interfémorale noire (van Zyll de Jong, 1985). Son envergure est d’environ 22 à 27 cm. La femelle est légèrement plus grosse que le mâle (Harvey et al., 2011). Par comparaison à d’autres mammifères, la petite chauve-souris brune est longévive, et certains individus vivent plus de 30 ans (Davis et Hitchcock, 1995).
Chauve-souris nordique
La chauve-souris nordique est une petite chauve-souris (entre 5 et 8 g) de taille et de couleur semblables à celles de la petite chauve-souris brune, dont elle se distingue généralement par ses longues oreilles qui recouvrent le museau lorsqu’on les rabat, sa queue plus longue et une surface alaire plus grande (Caceres et Barclay, 2000; Harvey et al., 2011). La chauve-souris nordique se distingue aussi par son tragusnote2, qui est long et mince et dont l’extrémité est pointue (van Zyll de Jong, 1985). Les caractéristiques du cycle vital de la chauve-souris nordique sont semblables à celles de la petite chauve-souris brune; le record de longévité dans la nature est de 18,5 ans (Caceres et Barclay, 2000).
Pipistrelle de l’Est
La pipistrelle de l’Est a une coloration distincte : chaque poil est noir à la base, jaune au milieu et brun à l’extrémité, ce qui donne à la chauve-souris une couleur globale brun rougeâtre à brun jaunâtre (Harvey et al., 2011). Ses oreilles et son visage sont bruns, ses avant-bras sont rouge-orange ou rosâtres, et ses ailes et ses membranes alaires sont noirâtres (Fujita et Kunz, 1984; Naughton, 2012). La pipistrelle de l’Est est semblable en taille et en poids (entre 5 et 9 g) à la petite chauve-souris brune et à la chauve-souris nordique (Fujita et Kunz, 1984; van Zyll de Jong, 1985; Farrow et Broders, 2011).
3.2 Population et répartition
Répartition
Petite chauve-souris brune
La présence de la petite chauve-souris brune a été confirmée dans chaque province et territoire du Canada, à l’exception du Nunavut, où on ne dispose d’aucune preuve normalisée de l’existence de l’espèce (c’est-à-dire que des observations ont été signalées, mais non confirmées) (COSEWIC, 2013). De manière générale, la répartition canadienne de l’espèce s’étend à la forêt boréale, du sud de la limite des arbres, jusqu’à la frontière des États-Unis (van Zyll de Jong, 1985; Grindal et al., 2011; Burles et al., 2014) (figure 1).
La limite nord de l’aire de répartition de l’espèce est difficile à définir en raison des activités de relevés limitées et des difficultés logistiques connexes (p. ex. grande superficie, peu de routes – voir Jung et al., (2014) pour une explication approfondie). Peu de colonies de maternité ou d’hibernacles ont été trouvés dans la partie nord de l’aire de répartition (COSEWIC, 2013), mais Wilson et al., (2014) ont observé des femelles reproductrices et des colonies de maternité de petites chauves-souris brunes dans le sud-ouest et le centre-sud des Territoires du Nord-Ouest. L’espèce se trouve aussi au sud du 64° au Yukon (Slough et Jung, 2008). Des hibernacles ont été confirmés dans les Territoires du Nord-Ouest, mais aucun n’a été trouvé au Yukon (Slough et Jung, 2008; Wilson et al., 2014). On compte certaines mentions éparses au Nunavut et dans le nord des Territoires du Nord-Ouest (c.-à-d. au nord de l’aire de répartition définie à la figure 1), mais on ne sait pas si ces mentions représentent des individus reproducteurs résidents ou des observations extralimites note3(COSEWIC, 2013).
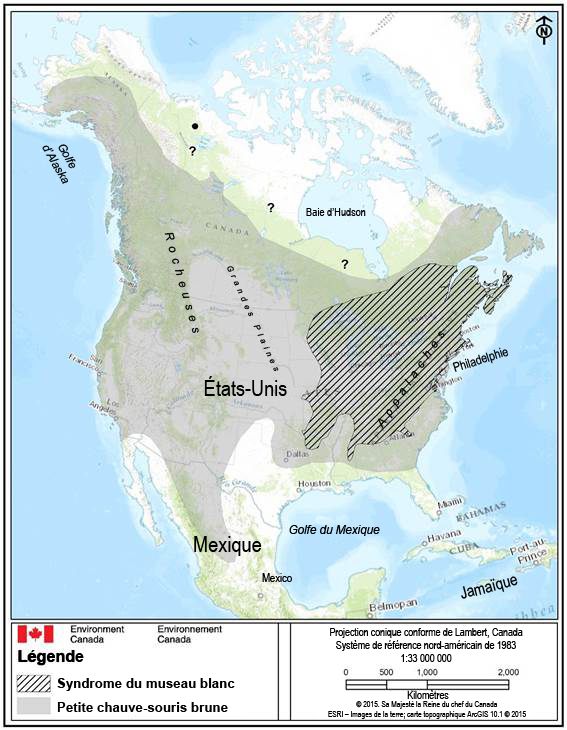
Description longue pour la figure 1
Carte illustrant l’aire de répartition approximative de la petite chauve-souris brune (Myotis lucifugus) en Amérique du Nord (zone en gris) et son chevauchement avec la zone touchée par le syndrome du museau blanc (Pseudogymnoascus destructans) (SMB) (zone hachurée) en mai 2015 (Naughton, 2012; COSEWIC, 2013; Wilson et al., 2014; CWHC, 2015; GNWT, 2015a). Les occurrences observées, mais non confirmées, de la petite chauve-souris brune dans les Territoires du Nord-Ouest et au Nunavut sont indiquées par un point d’interrogation (« ? »), alors que les observations extralimites (à l’extérieur de l’aire de répartition délimitée par la zone en gris) sont représentées par un point noir. L’occurrence de l’espèce est confirmée dans toutes les provinces et dans tous les territoires du Canada, sauf au Nunavut (présence non confirmée).
L’aire de répartition continentale de l’espèce est continue, et sa limite septentrionale s’étend depuis le centre de l’Alaska (point le plus au nord), et passe par le centre-nord du Yukon et le sud des Territoires du Nord-Ouest en suivant la limite des arbres de la forêt boréale, jusque dans les régions du nord de la Saskatchewan, du Manitoba, de l’Ontario, du Québec, et de Terre-Neuve-et-Labrador. La limite occidentale de l’aire de répartition s’étend de la côte de l’Alaska à l’extrémité la plus au nord de la péninsule de la Basse-Californie, au Mexique. La limite sud-ouest va de la péninsule de la Basse-Californie, le long de la frontière entre les États-Unis et le Mexique, au centre-nord du Mexique. La limite centre-sud de l’aire de répartition s’étend du nord du Texas aux portions septentrionales des États du Golfe, (Louisiane, Mississippi et frontières méridionales de l’Alabama et de la Géorgie). La limite orientale s’étend depuis le nord de Terre-Neuve-et-Labrador, et suit la côte atlantique, jusqu’au sud de la Géorgie, aux États-Unis. L’aire de répartition du SMB chevauche l’aire de répartition centre-est de l’espèce.
Chauve-souris nordique
La présence de la chauve-souris nordique a été confirmée dans chaque province et territoire du Canada, à l’exception du Nunavut (van Zyll de Jong, 1985; Brown et al., 2007; Henderson et al., 2009; Park et Broders, 2012; Broders et al., 2013, Reimer et Kaupas, 2013) (figure 2). La répartition canadienne de l’espèce comprend la forêt boréale au sud de la ligne des arbres, ainsi que les forêts montagnardes de l’ouest et les forêts mixtes de l’est. La chauve-souris nordique est pratiquement absente des Prairies canadiennes et, lorsqu’elle est observée à l’extérieur des régions forestières, on la trouve dans des forêts reliques ou dans des hibernacles (Turner, 1974).
Comme c’est le cas pour la petite chauve-souris brune, il est difficile d’établir la limite septentrionale de l’aire de répartition de la chauve-souris nordique en raison des activités de relevé limitées et des problèmes logistiques connexes (p. ex. grande superficie, peu de routes). Toutefois, la reproduction de la chauve-souris nordique a été confirmée au Yukon (Lausen et al., 2008) et dans les Territoires du Nord-Ouest (Wilson et al., 2014). Aucun site d’hibernation n’a été signalé au Yukon (Jung et al., 2006, Slough et Jung, 2007), mais il y en a probablement dans les Territoires du Nord-Ouest (Wilson et al., 2014).
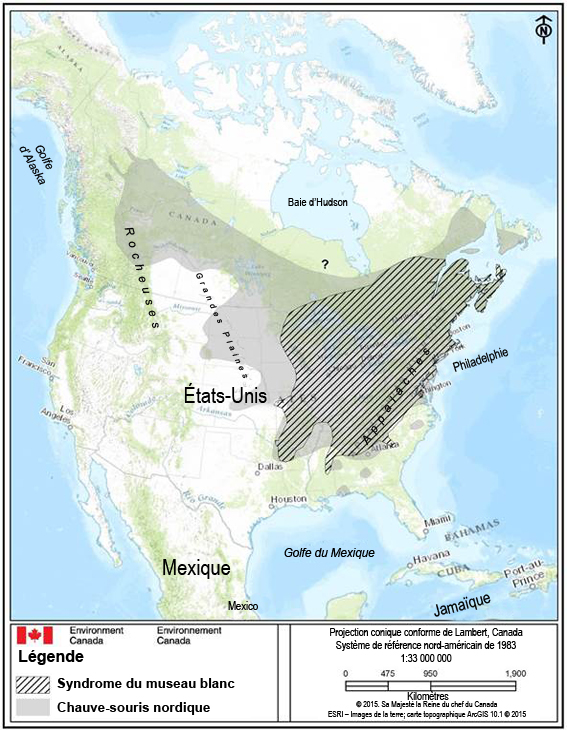
Description longue pour la figure 2
Carte illustrant l’aire de répartition approximative de la chauve-souris nordique (Myotis septentrionalis) en Amérique du Nord (zone en gris) et son chevauchement avec la zone touchée par le syndrome du museau blanc (Pseudogymnoascus destructans) (SMB) (zone hachurée) en mai 2015 (Naughton, 2012; COSEWIC, 2013; Wilson et al., 2014; CWHC, 2015; GNWT, 2015b). Les emplacements observés, mais non confirmés, fréquentés par la chauve-souris nordique en Ontario sont indiqués par un point d’interrogation (« ? »). L’occurrence de l’espèce est confirmée dans toutes les provinces et dans tous les territoires du Canada, sauf au Nunavut (présence non confirmée) (van Zyll de Jong, 1985; Brown et al., 2007; Henderson et al., 2009; Park et Broders, 2012; Broders et al., 2013; Reimer et Kaupas, 2013).
L’aire de répartition continentale de l’espèce est presque continue, et sa limite septentrionale s’étend depuis le sud-est du Yukon/sud-ouest des Territoires du Nord-Ouest jusque dans le centre-nord des Prairies canadiennes et de l’Ontario, et jusqu’au Québec, et à Terre-Neuve-et-Labrador. Le sud de l’aire de répartition de l’espèce couvre les États du centre-sud des États-Unis, mais l’espèce est généralement absente dans le Midwest et dans le centre des Prairies. D’ouest en est, l’aire de répartition de l’espèce suit la forêt boréale de l’Ouest canadien (Colombie-Britannique ), et passe par le centre-nord des provinces des Prairies canadiennes, le nord de l’Ontario et le centre-nord du Québec, pour atteindre le sud-est de Terre-Neuve. La limite orientale de l’aire de répartition de l’espèce va de l’intérieur de la Géorgie centrale et du nord-ouest de la Caroline du Sud, aux États-Unis, en suivant la côte atlantique, au sud-est de Terre-Neuve et au sud-est du Labrador. L’aire de répartition de l’espèce est également discontinue dans le sud-est des États-Unis (occurrences isolées en Alabama, en Floride, en Géorgie et dans le centre de la Caroline du Sud). Le chevauchement avec le syndrome du museau blanc couvre la portion est de l’aire de répartition nord-américaine de l’espèce.
Pipistrelle de l’Est
L’aire de répartition canadienne de la pipistrelle de l’Est englobe la Nouvelle-Écosse continentale, le sud du Nouveau-Brunswick, le Québec et l’Ontario (van Zyll de Jong, 1985; Fraser et al., 2012) (figure 3), mais certaines populations pourraient se trouver isolées à l’intérieur de cette aire (Broders et al., 2003). Des mentions de reproduction de la pipistrelle de l’Est ont été confirmées en Nouvelle-Écosse (Broders et al., 2003), mais pas au Nouveau-Brunswick (Broders et al., 2001). Bien que l’espèce ait été détectée en Ontario et au Québec en été (COSEWIC, 2013), il n’est pas clair si la reproduction y a été confirmée. La présence de l’espèce a été signalée dans des hibernacles dans toutes les provinces qui font partie de l’aire de répartition, quoique rarement et/ou en nombres relativement faibles (COSEWIC, 2013).
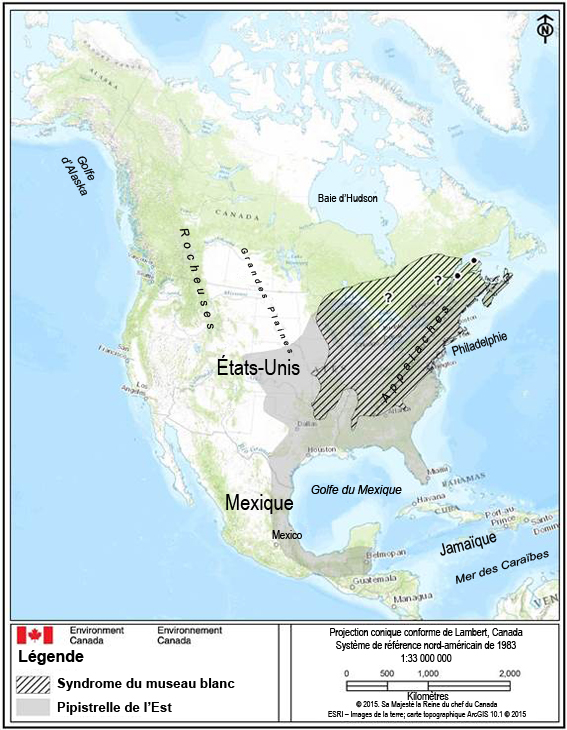
Description longue pour la figure 3
Carte illustrant l’aire de répartition approximative de la pipistrelle de l’Est (Perimyotis subflavus) en Amérique du Nord (zone en gris) et son chevauchement avec la zone touchée par le syndrome du museau blanc (Pseudogymnoascus destructans) (SMB) (zone hachurée) en mai 2015 (Naughton, 2012; COSEWIC, 2013; CWHC, 2015). Les occurrences observées, mais non confirmées, de pipistrelles de l’Est en Ontario et au Québec sont indiqués par un point d’interrogation (« ? »), alors que les observations extralimites (au nord) sont indiquées par des points noirs. L’occurrence de l’espèce au Canda se limite aux provinces du centre-est (Ontario, Québec, sud du Nouveau-Brunswick et Nouvelle-Écosse).
L’aire de répartition continentale de l’espèce est continue, mais elle est confinée au centre et à l’est des États-Unis et du Canada, et sa limite septentrionale suit les Grands Lacs et les Laurentides, au Canada. L’aire de répartition de l’espèce devient plus étroite/rétrécit depuis le sud des États du Golfe jusqu’au Mexique, où le sud de l’aire de répartition longe la côte ouest du Golfe du Mexique pour se rendre jusqu’au Guatemala. Le chevauchement de l’aire de répartition de l’espèce avec celle du syndrome du museau blanc couvre la portion nord-est de l’aire de répartition nord-américaine de l’espèce.
Population
Le présent programme de rétablissement définit deux périodes qui sont pertinentes aux fins d’analyse des populations de chauves-souris au Canada : la période précédant l’apparition du SMB au Canada (jusqu’à 2009 inclusivement) et la période suivant l’apparition du SMB au Canada (à partir de 2010). Il est cependant à noter que la taille des populations et l’abondance relative des trois espèces de chauves-souris au Canada avant l’apparition du SMB et après l’apparition du SMB (au Canada et en Amérique du Nord) sont inconnues; c’est pourquoi il est difficile d’obtenir des estimations précises des déclins propres à chaque espèce au sein des populations canadiennes.
Dans le nord-est des États-Unis, Langwig et al., (2012) ont estimé que, de manière générale, les populations de chauves-souris (toutes les espèces) augmentaient à un rythme moyen de 8 % par année avant l’apparition du SMB. Des analyses des tendances des populations fondées sur les données recueillies dans des hibernacles partout aux États-Unis avaient indiqué que ces trois espèces de chauves-souris, particulièrement, étaient relativement stables (c.-à-d. il avait été impossible de déceler une tendance positive ou négative) (Ellison et al., 2003; Frick et al., 2010a; Frick et al., 2010b). Il peut y avoir des variations considérables à l’intérieur d’une même année et d’une année à l’autre dans le nombre d’individus (et d’espèces) en hibernation dans un hibernacle (Trombulak et al., 2001); néanmoins, les données recueillies en hiver dans les hibernacles reflètent probablement bien la situation des populations des trois espèces (COSEWIC, 2013). En outre, les données des relevés estivaux corroborent les observations faites dans les hibernacles (COSEWIC, 2013; NatureServe, 2015).
Depuis l’apparition du SMB en Amérique du Nord en 2006, on a observé les déclins les plus soudains jamais enregistrés chez des espèces sauvages d’Amérique du Nord (Kunz et Tuttle, 2009). On estime qu’un million de chauves-souris (de diverses espèces) sont mortes dans le nord-est des États-Unis au cours des 3 années qui ont suivi l’apparition du SMB (Kunz et Tuttle, 2009), et qu’entre 5,7 et 6,7 millions de chauves-souris sont mortes dans les 6 années suivant son apparition (U.S. Fish and Wildlife Service, 2012). Au Canada, le nombre total de chauves-souris Myotis spp. relevé dans des hibernacles de la Nouvelle-Écosse, du Nouveau-Brunswick, de l’Ontario et du Québec a chuté d’environ 94 % entre 2010 et 2012 (COSEWIC, 2013). Au Québec, en Nouvelle-Écosse et au Nouveau-Brunswick, certains hibernacles ne comptent plus aucun individu de ces espèces (McAlpine et Vanderwolf, données inédites in COSEWIC, 2013; Mainguy et Desrosiers, 2011; H. Broders, comm. pers., 2015).
L’information est limitée en ce qui concerne la proportion des populations de chauves-souris qui se trouve dans l’est du Canada par rapport à l’ouest du Canada. Au Canada, 95 % des observations de chauves-souris Myotis spp. hibernantes proviennent de la Nouvelle-Écosse au Manitoba, tandis que peu d’entre elles ont été trouvées à l’ouest du Manitoba (COSEWIC, 2013). On a découvert moins d’hibernacles dans les provinces de l’ouest et les territoires du nord que dans l’est (sauf à Terre-Neuve-et-Labrador, où la présence de quelques hibernacles est connue). De plus, les hibernacles de l’est tendent à abriter plus d’individus par site (> 10 000) par rapport à ceux du nord et de l’ouest (< 1 000 par site) (Nagorsen et Brigham, 1993; Olson et al., 2011). Certains chercheurs avancent qu’une grande proportion de la population de la petite chauve-souris brune, avant l’apparition du SMB, vivait dans le nord-est des États-Unis (Kunz et Reichard, 2010). Des données génétiques indiquent également que les populations de l’est étaient plus grandes que celles de l’ouest (Wilder, 2014). Cependant, il est possible que les chauves-souris du nord et de l’ouest du Canada ne soient pas nécessairement moins abondantes, mais tendent plutôt à hiberner seules ou en plus petits nombres, ce qui compliquerait davantage l’obtention d’estimations précises des populations (c.-à-d. de nombreux sites abritant un faible nombre de chauves-souris dans le nord et l’ouest; peu de sites abritant un grand nombre d’individus dans l’est). Les comparaisons entre l’est et l’ouest sur le plan de l’abondance doivent être interprétées avec prudence, en raison des limites précédemment mentionnées en matière de relevés dans le nord, en plus des difficultés rencontrées dans l’ouest (c.-à-d. en Colombie-Britannique) pour différencier la petite chauve-souris brune de la chauve-souris de Yuma (Myotis yumanensis) (COSEWIC, 2013).
Petite chauve-souris brune
Avant l’apparition du SMB
Selon les données de nombreux relevés, la petite chauve-souris brune était probablement l’espèce de chauve-souris la plus commune dans la majeure partie du Canada, et elle le demeure dans bon nombre de régions qui ne sont pas touchées par le SMB (COSEWIC, 2013). La petite chauve-souris brune serait relativement commune à la limite septentrionale de son aire de répartition, quoique l’abondance soit difficile à estimer en raison des problèmes précédemment mentionnés en ce qui concerne le recensement des populations dans le nord (COSEWIC, 2013; Jung et al., 2014).
La taille de la population canadienne de la petite chauve-souris brune avant l’apparition du SMB n’est pas connue, mais la population excédait probablement 1 million d’individus (COSEWIC, 2013). Frick et al., (2010a) ont estimé que la population s’élevait à 6,5 millions d’individus dans le nord-est des États-Unis en 2006, ce qui appuie l’estimation d’un nombre d’individus supérieur à 1 million au Canada. NatureServe (2015) estime que la population mondiale s’établirait entre 100 000 et moins de 1 000 000 d’individus avant l’apparition du SMB. Les données sur les hibernacles connus sont incomplètes mais, avant l’apparition du SMB, certains hibernacles connus étaient utilisés par des milliers, voire des dizaines de milliers de chauves-souris dans le sud de l’Ontario, du Québec, de la Nouvelle-Écosse, du Nouveau-Brunswick et du Manitoba (Fenton, 1970; Scott et Hebda, 2004; Mainguy et Desrosiers, 2011).
Après l’apparition du SMB
NatureServe (2015) indique que la taille de la population mondiale actuelle est inconnue, mais dépasse encore probablement 100 000 individus. Les résultats de la modélisation montrent que la petite chauve-souris brune sera fonctionnellement disparuenote4 (c.-à-d. 1 % de la population avant l’apparition du SMB, ou 65 000 individus) dans le nord-est des États-Unis d’ici 2026 (Frick et al., 2010a). Toutefois, de nouvelles données indiquent que certains individus survivent à l’infection et que les taux de survie ont augmenté à des endroits où des populations avaient précédemment été décimées par le SMB. Toutefois, les taux de survie accrus ne sont pas suffisants pour soutenir une tendance positive en matière de croissance démographique (Maslo et al., 2015). L’ensemble de l’aire de répartition canadienne de la petite chauve-souris brune devrait être touchée par le SMB d’ici 2025 à 2028 (COSEWIC, 2013).
chauve-souris nordique
Avant l’apparition du SMB
Des données indiquent que la chauve-souris nordique serait moins commune que la petite chauve-souris brune, en partie parce que la répartition de la chauve-souris nordique est plus limitée au Canada et dépend des régions forestières (COSEWIC, 2013). Des observations estivales indiquent que l’espèce est relativement commune dans le sud des Territoires du Nord-Ouest, et peu commune aux limites ouest et nord de son aire de répartition (Jung et al., 2014; Wilson et al., 2014). À certains sites de l’est du pays (p. ex. Terre-Neuve-et-Labrador, Île-du-Prince-Édouard et Nouvelle-Écosse), le nombre d’individus était plus ou moins égal à celui des petites chauves-souris brunes (Park et Broders, 2012). Cependant, les dénombrements effectués dans des hibernacles individuels à l’hiver ont indiqué que les chauves-souris nordiques étaient relativement peu nombreuses (c.-à-d. < 100) (Barbour et Davis, 1969; Amelon et Burhans, 2006). Ces données pourraient résulter de difficultés associées à la détection de la chauve-souris nordique dans les hibernacles, car l’espèce occupe souvent les failles profondes (COSEWIC, 2013).
La taille de la population canadienne de la chauve-souris nordique est inconnue, mais elle pourrait avoir dépassé aussi le million d’individus avant l’apparition du SMB (COSEWIC, 2013). Par contre, NatureServe (2015) estime que la taille de la population mondiale était relativement petite avant l’apparition du SMB (entre 2 500 et 100 000 individus). Toutefois, NatureServe précise que cette estimation est fondée sur les faibles nombres constatés dans les hibernacles (qui pourraient être liés à des problèmes de détectabilité). De plus, l’estimation de NatureServe semble reposer principalement sur les dénombrements effectués dans la partie de l’aire de répartition qui se trouve aux États-Unis. D’après Harvey (1992) et D. Morningstar (comm. pers., 2015), l’espèce est probablement plus commune et abondante dans la partie septentrionale (c.-à-d. boréales) de son aire de répartition mondiale que dans le sud (COSEWIC, 2006).
Après l’apparition du SMB
Le déclin des populations de la chauve-souris nordique dans le nord-est des États-Unis s’est produit au même rythme que celui de la petite chauve-souris brune; un résultat prévu puisque les deux espèces présentent des caractéristiques du cycle vital similaires, et partagent souvent les mêmes hibernacles. Par conséquent, il a été prédit que la chauve-souris nordique aura probablement aussi fonctionnellement disparu (c.-à-d. 1 % de la population avant l’apparition du SMB) dans le nord-est des États-Unis d’ici 2026 (Frick et al., 2010a). Toutefois, de nouvelles données concernant la petite chauve-souris brune donnent à penser qu’un petit nombre d’individus survit à l’infection et que les taux de survie ont augmenté à des endroits où des populations avaient précédemment été décimées par le SMB, une tendance qui pourrait également s’appliquer à la chauve-souris nordique. La totalité de l’aire de répartition canadienne de la chauve-souris nordique devrait être touchée par le SMB entre 2025 et 2028 (COSEWIC, 2013).
Pipistrelle de l’Est
Avant l’apparition du SMB
Bien qu’on ne dispose que de trop peu de données pour estimer avec fiabilité la taille de la population de la pipistrelle de l’Est, on sait que l’espèce était relativement rare dans les Maritimes, au Québec et dans certaines régions de l’Ontario (COSEWIC, 2013). Elle est aussi rare dans les États adjacents du Vermont (Darling et Smith, 2011) et du Maine (Zimmerman et Glanz, 2000). En plus d’être peu communes, les pipistrelles de l’Est tendent à hiberner seules dans les hibernacles, souvent dans les parties les plus profondes des grottes, où l’accès aux humains est limité; c’est pourquoi elles peuvent être plus difficiles à détecter durant l’hibernation que d’autres espèces (Hitchcock, 1949; Fujita et Kunz, 1984; Sandel et al., 2001; COSEWIC, 2013).
La taille de la population canadienne de la pipistrelle de l’Est avant l’apparition du SMB est inconnue, mais le rapport de situation du COSEPAC (2013) fournit une estimation grossière de moins de 20 000 individus au Canada. NatureServe (2015) estime que la taille de la population mondiale totalisait entre 10 000 et 1 000 000 d’individus avant l’apparition du SMB. En Nouvelle-Écosse, il a été estimé qu’il y avait entre 1 000 et 2 000 femelles adultes (H. Broders, comm. pers. in COSEWIC, 2013). Dans l’ensemble de son aire de répartition canadienne, l’espèce représentait entre 0,2 et 4,5 % des individus dénombrés dans divers hibernacles (Hitchcock, 1949, 1965; Mainguy et Desrosiers, 2011; Vanderwolf et al., 2012).
Après l’apparition du SMB
Le déclin subi par la population de la pipistrelle de l’Est dans les régions touchées par le SMB au Canada et aux États-Unis est probablement semblable à celui qui a été observé chez la petite chauve-souris brune et la chauve-souris nordique, quoique les déclins observés chez cette espèce soient moins directs (COSEWIC, 2013). Cela s’explique, en partie, par le petit nombre de pipistrelles de l’Est qui a été dénombré dans les hibernacles canadiens faisant l’objet d’un suivi, et par l’indication d’une migration latitudinale saisonnière qu’affiche l’espèce (Fraser et al., 2012); ces deux facteurs peuvent influer sur l’interprétation des tendances de la population canadienne.
Les déclins observés depuis l’apparition du SMB ont été variables. Le déclin moyen de la population dans 5 États du nord-est s’élevait à 75 % (de 16 à 95 %) entre 2006 et 2010, et 13 de 36 hibernacles ont affiché un déclin de 100 % (Turner et al., 2011). Le suivi acoustique mené au cours des étés de 2007 à 2009 dans l’État de New York a permis d’observer un déclin de la population du même ordre que ceux qui ont été mentionnés précédemment (c.-à-d. 78 % entre 2008 et 2009) (Dzal et al., 2011). Dans l’est de l’Ontario, au Québec et en Nouvelle-Écosse, certains signes montrent que la population de la pipistrelle de l’Est pourrait avoir chuté jusqu’à 94 % par rapport aux niveaux d’avant l’apparition du SMB (Mainguy et Desrosiers, 2011; L. Hale, comm. pers. in COSEWIC, 2013). Dans le sud de l’Ontario, d’importants déclins ont également été observés dans huit emplacements où un suivi acoustique avait été fait avant l’apparition du SMB, puis de nouveau en 2014 (D. Morningstar, comm. pers.). Au Nouveau-Brunswick, les déclins enregistrés aux hibernacles individuels se sont établis entre 30 % et plus de 75 % (D. McAlpine et K. Vanderwolf, données inédites in COSEWIC, 2013; D. McApline, comm. pers. in COSEWIC, 2013). NatureServe (2015) indique que la taille de la population mondiale actuelle est inconnue, mais dépasse probablement encore 10 000 individus.
3.3 Besoins de la petite chauve-souris brune, de la chauve-souris nordique et de la pipistrelle de l’Est
Les besoins en matière d’habitat des chauves-souris des régions tempérées varient selon la saison. L’habitat se compose de : 1) l’habitat d’hivernage (c.-à-d. les hibernacles, comme des grottes, des mines abandonnées et des puits) utilisé pour l’hibernation et la survie hivernale; 2) l’habitat d’estivage, qui comprend les aires de repos (pour les colonies de maternité et les mâles) et l’habitat d’alimentation à distance de vol des dortoirs et gîtes de maternité (Sasse et Perkins, 1996; Norquay et al., 2013); 3) l’habitat de rassemblement utilisé à la fin de l’été et au début de l’automne aux fins de la reproduction et de la socialisation (Fenton, 1969; Randall et Broders, 2014). Les sites de rassemblement sont aussi habituellement utilisés comme hibernacles (Fenton, 1969; Randall et Broders, 2014).
Habitat d’hivernage et de rassemblement
Les chauves-souris en hibernation survivent à l’hiver en utilisant les réserves de graisse qu’elles ont emmagasinées durant l’été et l’automne (Jonasson et Willis, 2011). L’hibernation permet aux chauves-souris insectivores qui vivent à l’année dans une même région de survivre lorsque la température ambiante diminue et lorsque les insectes ne sont plus disponibles en hiver. Les chauves-souris en hibernation réduisent au minimum l’utilisation de leurs réserves de graisse en abaissant leur métabolisme ainsi que leur température corporelle à un niveau qui ne dépasse que de quelques degrés la température ambiante régnant dans l’hibernacle (c.-à-d. elles entrent dans un état de torpeurnote5) (Henshaw et Folk, 1966).
Les hibernacles utilisés par la petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est sont généralement des ouvertures souterraines, comme des grottes, des mines abandonnées, des puits et des tunnels, mais à certains sites il est possible que seules certaines sections précises soient utilisées pour l’hibernation. Les sections utilisées pour l’hibernation présentent habituellement une température variant entre 2 °C et 10 °C (Fenton, 1970; Anderson et Robert, 1971; Vanderwolf et al., 2012), ainsi qu’un taux d’humidité relative supérieur à 80 % permettant de réduire les pertes d’eau par évaporation (Cryan et al., 2010, voir aussi Kurta, 2014). Certaines caractéristiques structurelles, comme le nombre d’ouvertures, la superficie et la longueur de la grotte, ainsi que l’angle des chambres peuvent agir sur la stabilité et les valeurs d’humidité et de température (Davis, 1970; Raesly et Gates, 1987). En raison des microclimats spécifiques et stables requis par les chauves-souris, les mêmes hibernacles sont habituellement réutilisés d’une année à l’autre par les chauves-souris en hibernation.
Les chauves-souris préfèrent les microclimats stables, car les fluctuations de température peuvent les faire sortir de leur torpeur. Les chauves-souris s’éveillent pour s’abreuver, se toiletter ou s’accoupler (Whitaker et Rissler, 1993; Thomas, 1995), mais elles consomment une part considérable de leur réserve énergétique limitée lors de leur éveil (Thomas et al., 1990). Les déplacements vers des sites plus convenables peuvent accélérer l’épuisement de leur réserve énergétique limitée, mais ils peuvent aussi constituer une adaptation à des fins de conservation d’énergie à long terme.
Aux endroits où leurs aires de répartition se chevauchent, les trois espèces de chauves-souris pourraient être présentes dans les mêmes hibernacles, mais peuvent se trouver dans différentes sections de ceux-ci. La chauve-souris nordique et la pipistrelle de l’Est n’hibernent habituellement pas dans les bâtiments, contrairement à la petite chauve-souris brune qui peut le faire dans l’ouest du Canada (C. Lausen, comm. pers.), où les températures hivernales sont relativement élevées. On en sait toutefois peu sur l’habitat d’hivernage de la petite chauve-souris brune et de la chauve-souris nordique dans l’ouest du pays.
Les chauves-souris se rassemblent dans leur habitat de rassemblement à la fin de l’été et au début de l’automne. Les sites de rassemblement peuvent servir de lieux d’accouplement, d’aires de repos durant la migration et de sites sociaux servant au transfert d’information et/ou permettant aux individus d’évaluer des sites d’hibernation potentiels (Fenton, 1969; Randall et Broders, 2014). Le comportement de rassemblement se produit souvent à l’intérieur des entrées ou des ouvertures des hibernacles, ou autour de celles-ci. La petite chauve-souris brune et la chauve-souris nordique se rassemblent et hibernent souvent aux mêmes endroits (Randall et Broders, 2014), mais la proportion de chauves-souris qui visitent un site de rassemblement par rapport à celles qui demeurent au site pour hiberner est inconnue (Johnson et al., 2015). Les groupes de rassemblement de la petite chauve-souris brune et de la chauve-souris nordique dans l’est du Canada sont composés d’individus qui proviennent de divers sites d’estivage; ainsi le patrimoine génétique des individus qu’on y trouve peut couvrir des superficies relativement grandes (Burns et al., 2014; Johnson et al., 2015; Segers et Broders, 2015).
Peu d’études ont tenté de définir les caractéristiques externes de l’habitat qui déterminent le choix des hibernacles et des sites de rassemblement. En Nouvelle-Écosse, un relevé des sites de rassemblement naturels et anthropiques (mines abandonnées), qui seraient aussi des hibernacles, a révélé que le degré de protection qu’offre l’entrée (c.-à-d. couvert forestier et/ou parois rocheuses protégeant des éléments), la longueur de cours d’eau dans un rayon de 2 km du site et la longueur totale de la chambre de l’hibernacle étaient des facteurs de prévision importants de l’activité de rassemblement de la petite chauve-souris brune et de la chauve-souris nordique (Randall et Broders, 2014). De manière générale, les sites de rassemblement présentaient des entrées plus exposées, une plus grande longueur totale de rivières, de ruisseaux et de cours d’eau à l’intérieur d’un rayon de 2 km, et des chambres plus longues/profondes que les sites examinés où l’activité de rassemblement était faible ou nulle (Randall et Broders, 2014). Par exemple, une augmentation de 10 % du degré de protection à l’entrée d’un hibernacle a fait en sorte que la probabilité de rassemblement a diminué de 50 %; par ailleurs un prolongement de 10 km d’un cours d’eau dans un rayon de 2 km a fait doubler la probabilité de rassemblement (Randall et Broders, 2014).
Petite chauve-souris brune
Les petites chauves-souris brunes semblent tirer un avantage énergétique et en conservation d’eau en se regroupant durant l’hibernation. Au Michigan, Kurta et Smith (2014) ont observé que 78 % des individus hibernaient en groupes, et qu’il était plus probable de les trouver en groupes (plutôt que seuls) à basse température. Dans l’ouest du Canada, le nombre de petites chauves-souris brunes hibernant ensemble pourrait être considérablement moins élevé que dans le nord-est de l’Amérique du Nord; les individus hibernent probablement seuls ou en petits groupes à l’ouest des Rocheuses (Jung et al., 2014). Une récente étude de radiotélémétrie effectuée dans la forêt pluviale tempérée du sud-est de l’Alaska a permis de trouver des petites chauves-souris brunes hibernant seules dans des éboulis rocheux sur des versants boisés et escarpés, et sous des mottes racinaires d’arbres et de souches (K. Blejwas, comm. pers.). La petite chauve-souris brune affiche une grande fidélité aux hibernacles (Norquay et al., 2013). Une étude de marquage et recapture effectuée au Manitoba et dans le nord-ouest de l’Ontario a établi un taux de changement d’hibernacle de seulement 4 % des individus marqués, au cours de la période d’étude (Norquay et al., 2013).
Chauve-souris nordique
La chauve-souris nordique peut hiberner dans les portions de grottes plus froides que celles dont a besoin la petite chauve-souris brune (Barbour et Davis, 1969). Une étude des mines abandonnées dans le nord du Michigan a révélé que la chauve-souris nordique et la petite chauve-souris brune cohabitaient dans 92 % des mines occupées par Myotis spp., et que 75 % des chauves-souris nordiques hibernaient seules (Kurta et Smith, 2014). Les individus de la chauve-souris nordique retournent généralement dans le même hibernacle, mais pas toujours durant deux années consécutives (Caceres et Barclay, 2000). Naughton (2012) avance que l’espèce est fidèle à un groupe d’hibernacles, et non à un seul.
Pipistrelle de l’Est
La pipistrelle de l’Est est l’espèce qui se montre la plus exigeante des trois espèces en matière d’habitat d’hivernage. Elle choisit souvent les sections les plus profondes des grottes ou des mines, où la température varie le moins, a de fortes préférences quant au taux d’humidité, et utilise des parois moins froides par rapport aux autres espèces (Fujita et Kunz, 1984; Raesly et Gates, 1987; Briggler et Prather, 2003; Kurta et Smith, 2014). Une étude des hibernacles au Nouveau-Brunswick indique que la pipistrelle de l’Est hiberne sur la partie inférieure des parois des grottes (Vanderwolf et al., 2012). Même si la pipistrelle de l’Est a tendance à utiliser les mêmes hibernacles que la petite chauve-souris brune et la chauve-souris nordique, relativement peu (c.-à-d. ≤ 10) de pipistrelles de l’Est ont été trouvées dans un hibernacle au Canada, possiblement parce qu’elles ont tendance à hiberner seules (c.-à-d. pas en groupe) dans les portions les plus profondes des grottes/mines. La pipistrelle de l’Est affiche une forte fidélité aux hibernacles (Sandel et al., 2001; Damm et Geluso, 2008).
Habitat d’estivage
Habitat de repos
Les aires de repos permettent la thermorégulation, offrent un abri contre les intempéries et les prédateurs, et servent de lieux d’interaction sociale (Kunz, 1982; Barclay et Kurta, 2007). Les individus peuvent régulièrement changer de site de repos et ainsi peuvent utiliser tout un réseau de sites dans une même aire de repos (Barclay et Brigham, 1996; Sasse et Perkins, 1996; Caceres et Barclay, 2000). La tendance à changer de site de repos peut dépendre de l’espèce, du sexe, de l’âge, de l’état reproducteur et du type de site de repos (p. ex. naturel ou anthropique) (Garroway et Broders, 2008; Randall et al., 2014).
Le choix de l’aire de repos se fait en fonction de nombreuses caractéristiques à diverses échelles spatiales (Fabianek et al., 2011). Par exemple, l’essence d’arbre, le diamètre, la hauteur, l’état de décomposition, la disponibilité d’un milieu de repos, l’exposition au soleil et d’autres caractéristiques peuvent agir sur le choix des individus à l’échelle de la structure de repos (Garroway et Broders, 2008; Slough, 2009; Poissant et al., 2010; Olson et Barclay, 2013). À l’échelle d’un peuplement, le choix de l’aire de repos peut dépendre des ouvertures dans le couvert forestier, du nombre de chicots disponibles, de la densité des arbres, de la proximité par rapport à un plan d’eau, etc. (Kalcounis-Rüppell et al., 2005; Garroway et Broders, 2008; Henderson et Broders, 2008). À l’échelle du paysage, des caractéristiques telles que l’âge des forêts, leur composition et leur degré de fragmentation peuvent agir sur le choix du site de repos (Henderson et Broders, 2008; Fabianek et al., 2011). L’espèce peut également utiliser des milieux boisés et forestiers dans des zones urbaines et suburbaines comme aires de repos, en plus d’utiliser des structures construites par l’homme que l’on trouve dans les paysages urbains et suburbains (petite chauve-souris brune, en particulier).
De nombreuses espèces de chauves-souris (dont la petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est) préfèrent se reposer dans des peuplements forestiers plus vieux (Barclay et Brigham, 1996). Les forêts plus vieilles offrent davantage de chicots (Crampton et Barclay, 1996; Krusic et al., 1996) et d’habitat d’alimentation sous un couvert relativement fermé (Jung et al., 1999).
De manière générale, les femelles mettent bas et élèvent leurs petits au sein de colonies de maternité au printemps ou à l’été. En raison de la tendance des individus à changer de site de repos, une colonie peut être définie comme un ensemble de groupes composés d’individus qui s’associent régulièrement et de groupes qui se mélangent entre eux (Olson et Barclay, 2013). Le fait de se reposer en groupe permet vraisemblablement aux individus d’accomplir une thermorégulation sociale et d’économiser de l’énergie (Willis et Brigham, 2007).
Les mâles des trois espèces se reposent durant le jour dans diverses structures, et changent souvent de site de repos durant l’été. L’habitat de repos des mâles comprend les crevasses rocheuses, l’écorce soulevée, le feuillage et les trous d’arbre (Fenton et Barclay, 1980; Caceres et Barclay, 2000; Broders et Forbes, 2004; Huynh, 2009; Randall et al., 2014; Fabianek et al., 2015). Les petites chauves-souris brunes et les chauves-souris nordiques mâles se reposent souvent dans de grands chicots de grand diamètre, en début ou en milieu de décomposition, et situés dans de petites clairières ou à proximité de celles-ci dans des forêts matures ou anciennes (Broders et Forbes, 2004; Jung et al., 2004; Fabianek et al., 2015).
Petite chauve-souris brun
La petite chauve-souris brune est l’une de seulement quelques espèces de chauves-souris qui utilisent les bâtiments et d’autres structures anthropiques (p. ex. dortoirs à chauves-souris, ponts et granges) pour se reposer (particulièrement pour former des colonies de maternité). Cependant, l’espèce utilise aussi le couvert forestier, du feuillage, de l’écorce, des crevasses rocheuses et d’autres structures (Fenton et Barclay, 1980; Slough, 2009; Coleman et Barclay, 2011; Randall et al., 2014).
Les colonies de maternité peuvent compter des centaines de femelles et leurs petits. Les femelles affichent une forte tendance à se reposer dans des arbres de grand diamètre, mais les différentes caractéristiques recherchées peuvent varier considérablement durant l’été (Olson et Barclay, 2013). On pense que les femelles choisissent une colonie de maternité préférée malgré le fait qu’elles doivent alors parcourir de plus grandes distances pour s’alimenter, sans doute en raison du nombre limité de sites de colonies de maternité convenables (Broders et al., 2006; Randall et al., 2014). Les petites chauves-souris brunes femelles présentent un degré relativement élevé de philopatrienote6 (Frick et al., 2010b). Les aires de repos sont généralement utilisées chaque année, et des sites de repos naturels individuels peuvent être utilisés pendant plus de 10 ans (M. Brigham, comm. pers.). Les petites chauves-souris brunes sont particulièrement fidèles aux structures anthropiques, et peuvent utiliser un même site pendant plus de 50 ans (M. Brigham, comm. pers.). Elles affichent aussi une forte fidélité aux structures anthropiques à l’intérieur d’une même année; Randall et al., (2014) ont constaté que la plupart des femelles qui utilisaient des structures anthropiques au Yukon ne changeaient pas d’aire de repos durant l’été. Néanmoins, on a rapporté que des petites chauves-souris brunes changeaient de sites aménagés par l’homme d’une année à l’autre et au cours d’une même année afin de répondre à leurs besoins (p. ex. thermorégulation) (voir par exemple Syme et al., 2001). Par exemple, à l’aide d’un marquage au moyen d’un transpondeur passif intégré, on a rapporté une utilisation mixte dans une colonie de maternité se trouvant dans une structure construite par l’homme en Ontario. Certains individus demeuraient au site de repos pendant plusieurs nuits, d’autre le visitaient à l’occasion, et de nombreux individus ne le visitaient que la nuit, mais n’y demeuraient pas durant le jour, ce qui laisse croire que les individus utilisaient également d’autres aires de repos dans la région (D. Morningstar, données inédites).
Les mâles se reposent individuellement ou en petits groupes, et changent périodiquement d’aires de repos. Au Québec, les mâles changent d’aire de repos environ aux deux jours (Fabianek et al., 2015). Ils utilisent diverses structures, notamment des bâtiments, des crevasses rocheuses, du feuillage, de l’écorce soulevée et des trous d’arbre (Huynh, 2009; Randall et al., 2014). Au Nouveau-Brunswick et au Québec, les petites chauves-souris brunes mâles se reposent principalement dans des peuplements de conifères ou des peuplements mixtes dominés par des conifères, où l’on trouve un grand nombre de chicots (Broders et Forbes, 2004; Fabianek et al., 2015).
Chauve-souris nordique
La chauve-souris nordique se repose seule ou en petits groupes et préfère les arbres (sous l’écorce soulevée ou dans des trous ou des crevasses d’arbre), mais elle peut aussi être trouvée dans des structures anthropiques (p. ex. sous des bardeaux) (Sasse et Perkins, 1996; Foster et Kurta, 1999; Caceres et Barclay, 2000; Carter et Feldhamer, 2005).
Les colonies de maternité de la chauve-souris nordique sont fortement associées au couvert forestier, aux cours d’eau et aux caractéristiques des arbres (p. ex. essence, hauteur, diamètre, âge et état de décomposition) (Caceres et Barclay, 2000; Broders et Forbes, 2004; Broders et al., 2006). Les femelles préfèrent se reposer dans de grands arbres de grand diamètre, en début ou au milieu du processus de décomposition (Sasse et Perkins, 1996; Caceres et Barclay, 2000; Silvis et al., 2015a). Les colonies de maternité situées à Terre-Neuve-et-Labrador, en Nouvelle-Écosse et au Nouveau-Brunswick se trouvaient généralement dans des arbres plus gros que la moyenne (Broders et Forbes, 2004; Garroway et Broders, 2008; Park et Broders, 2012). Au Nouveau-Brunswick et à l’Île-du-Prince-Édouard, les chauves-souris nordiques femelles se reposaient principalement dans des arbres au milieu du processus de décomposition, dans des peuplements de feuillus tolérant l’ombre (Broders et Forbes, 2004; Henderson et Broders, 2008). Broders et Forbes (2004) ont attribué cette préférence à la vulnérabilité de ces essences d’arbres à la décomposition et au bris de branches (ce qui produit de l’habitat disponible pour le repos), à leur grande longévité (ce qui permet des utilisations répétées par les chauves-souris) et à leur habitat des hautes terres, qui offre un ensoleillement accru (ce qui réduit les coûts en énergie des chauves-souris pour maintenir leur température corporelle). Les chauves-souris nordiques femelles ont davantage recours à des structures anthropiques dans les endroits où l’habitat est fragmenté, et où l’on trouve peu d’arbres potentiels pour le repos (Henderson et Broders, 2008). En Nouvelle-Écosse, les colonies de maternité des chauves-souris nordiques sont formées de femelles affichant un degré élevé de parenté maternelle, probablement causé par la philopatrie des femelles (Patriquin et al., 2013). Les femelles changent d’arbre de repos environ tous les 1 à 5 jours, mais les sites de repos sont habituellement rassemblés dans une même aire (Sasse et Perkins, 1996; Caceres et Barclay, 2000; Carter et Feldhamer, 2005; Broders et al., 2006; Olson, 2011). La plus grande aire de repos enregistrée au Canada faisait 300 ha, en Alberta (Olson, 2011).
Les mâles se reposent généralement seuls, sous l’écorce soulevée ou dans les trous d’arbres au milieu du processus de décomposition (Broders et Forbes, 2004). Au Nouveau-Brunswick et au Québec, les chauves-souris nordiques mâles se reposent dans des peuplements de conifères ou des peuplements mixtes dominés par des conifères (Broders et Forbes, 2004; Fabianek et al., 2015). Au Québec, les mâles changent de site de repos environ aux deux jours (Fabianek et al., 2015).
Pipistrelle de l’Est
Les préférences de la pipistrelle de l’Est en matière de sites de repos sont moins bien connues. La plupart des sites de repos se trouvent dans des milieux forestiers, où l’espèce s’alimente également. La pipistrelle de l’Est peut aussi se reposer dans des amas de feuilles mortes et de lichens (Veilleux et al., 2003; Perry et Thill, 2007; Poissant et al., 2010). En Nouvelle-Écosse, 30 chauves-souris munies de radioémetteurs se reposaient dans de grands amas de lichens arboricoles (Usnea spp.) qui poussaient sur des conifères ou des feuillus situés relativement près de plans d’eau (Poissant et al., 2010).
Les femelles se reposent seules ou en petites colonies. En Nouvelle-Écosse, jusqu’à 18 pipistrelles de l’Est ont été trouvées dans un seul amas (Poissant et al., 2010). Dans les paysages davantage modifiés par l’homme, les colonies de maternité peuvent se trouver dans des granges ou d’autres structures anthropiques semblables (Fujita et Kunz, 1984). En Nouvelle-Écosse, la pipistrelle de l’Est affiche une fidélité aux petites aires de repos (< 78 ha) au cours d’une même année et d’une année à l’autre (Poissant, 2009). En Indiana, les femelles sont revenues chaque été au même endroit (d’une superficie de 0,4 ha) et ont utilisé chaque année le même groupe de 4 à 6 arbres, ce qui laisse croire qu’elles accordent une certaine préférence aux structures familières (et possiblement limitées) (Veilleux et Veilleux, 2004).
Les mâles se reposent individuellement (Veilleux et Veilleux, 2004; Perry et Thill, 2007; Poissant, 2009). Un mâle solitaire ayant été pisté en Nouvelle-Écosse se reposait seul dans du lichen arboricole (Usnea trichodea) (Poissant, 2009). En Arkansas, les mâles préféraient se reposer dans les feuilles mortes des chênes (Quercus spp.) sur des sites présentant un faible couvert ainsi que davantage de feuillus d’étage intermédiaire et de grands pins d’étage dominant que ce que l’on trouve aléatoirement dans la nature (Perry et Thill, 2007).
Besoins en matière d’alimentation
La petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est sont des prédateurs des insectes et exploitent des concentrations de proies abondantes à l’échelle locale, qui peuvent être dispersées dans le temps et l’espace. Il est compliqué de repérer les aires d’alimentation des chauves-souris en raison de biais liés au sexe, de différences entre les espèces, de variations saisonnières en ce qui a trait à l’utilisation de l’habitat par les femelles (p. ex. période de gestation, période d’allaitement ou période de non reproduction) et de la disponibilité et de la configuration de l’habitat d’alimentation (Henry et al., 2002; Owen et al., 2003; Broders et al., 2006; Randall et al., 2014).
Petite chauve-souris brune
La nuit, la petite chauve-souris brune se nourrit d’insectes (p. ex. papillons de nuit, éphémères, diptères, coléoptères et phryganes) et d’araignées (Moosman et al., 2012; Thomas et al., 2012; Clare et al., 2014). Son régime alimentaire peut néanmoins varier considérablement en fonction de facteurs saisonniers, géographiques et environnementaux (Moosman et al., 2012; Clare et al., 2014). Les nuits où la récolte est bonne, au pic de l’activité estivale, le mâle consomme environ la moitié de son poids corporel; la femelle en lactation peut quant à elle consommer une quantité d’insectes équivalant à son poids corporel (Anthony et Kunz, 1977). Les chauves-souris chassent surtout durant les quelques heures qui suivent le coucher du soleil et qui précèdent son lever (Fenton, 1970; Kunz, 1973; Broders et al., 2003). Dans les régions septentrionales (au nord du 60e parallèle nord) où les nuits d’été sont courtes, les femelles gravides semblaient modifier leur comportement de chasse en ne montrant qu’une seule période d’activité maximale. De plus, elles chassaient pendant un moins grand nombre d’heures que leurs consœurs vivant plus au sud, mais compensaient ce temps réduit en montrant un taux plus élevé de capture d’insectes (Talerico, 2008; Reimer, 2013).
La petite chauve-souris brune en quête de nourriture est le plus souvent associée aux milieux ouverts, comme les étangs et les routes, et les forêts dont le couvert est ouvert (de 0 à 50 %) (Segers et Broders, 2014), mais des individus ont aussi été observés glanantnote7 leurs proies dans des forêts (Ratcliffe et Dawson, 2003; Jung et al., 2014), et utilisant la végétation se trouvant en bordure des lacs et des cours d’eau (Fenton et Barclay, 1980). Des petites chauves-souris brunes vivant dans un milieu boréal du Yukon se déplaçaient sur une distance de 3,8 ± 0,7 km à partir de leur site de repos diurne pour se rendre à leurs aires d’alimentation, et les femelles se rendaient beaucoup plus loin que les mâles (Randall et al., 2014). Au Québec, le domaine vital des femelles en lactation est 42 % plus petit (moyenne de 17,6 ha) que celui des femelles gravides (moyenne de 30,1 ha) (Henry et al., 2002).
Chauve-souris nordique
La chauve-souris nordique se nourrit d’insectes (p. ex. papillons de nuit, coléoptères, guêpes et diptères) et d’araignées (Lacki et al., 2009; Dodd et al., 2012; Thomas et al., 2012) dont l’origine est principalement terrestre (Broders et al., 2014). Contrairement à la petite chauve-souris brune, qui recherche surtout de la nourriture au dessus des plans d’eau et s’alimente en vol, la chauve-souris nordique s’alimente plus fréquemment en bordure et à l’intérieur des forêts et, bien qu’elle se nourrisse d’insectes volants, elle glane aussi ses proies (Caceres et Barclay, 2000; Ratcliffe et Dawson, 2003).
Des chauves-souris nordiques femelles ont été observées en train de chasser le long de ruisseaux à l’abri du couvert forestier dans l’Île-du-Prince-Édouard (Henderson et Broders, 2008). En Virginie-Occidentale, les chauves-souris nordiques femelles s’alimentaient principalement dans des peuplements de feuillus âgés de 70 à 90 ans comportant des corridors routiers (Owen et al., 2003) et, au Kentucky, la chauve-souris nordique a été observée en train de chasser le long de crêtes et à mi pente, plutôt qu’en bas de pente (Lacki et al., 2009). Dans une forêt intensivement aménagée de Virginie-Occidentale, la superficie moyenne du domaine vital des chauves-souris nordiques gravides ou en lactation était de 65 ha (Owen et al., 2003). Au Nouveau-Brunswick, Broders et al., (2006) ont constaté que les mâles et les femelles parcouraient des distances très différentes entre leurs aires de repos et d’alimentation. En moyenne, la distance parcourue par les femelles entre les aires de repos successives était deux fois plus grande que celle parcourue par les mâles (457 m par rapport à 158 m) (Broders et al., 2006). Ces auteurs pensent que les femelles se rendaient plus loin parce que les colonies de maternité étaient situées dans des milieux pauvres en nourriture (Broders et al., 2006).
Pipistrelle de l’Est
Comme la petite chauve-souris brune, la pipistrelle de l’Est se nourrit d’insectes (p. ex. diptères, coléoptères, guêpes et papillons de nuit) la nuit venue et avant le lever du jour, en utilisant l’écholocation (Fujita et Kunz, 1984; Naughton, 2012). Chaque nuit, les mâles consomment au moins la moitié de leur poids corporel en insectes, et les femelles gravides et en lactation peuvent consommer une quantité d’insectes supérieure à leur poids corporel (Naughton, 2012).
La recherche de nourriture a surtout lieu dans les zones riveraines boisées, au dessus des plans d’eau (p. ex. étangs et rivières), ainsi que dans des aires relativement ouvertes (Ethier et Fahrig, 2011). En Nouvelle-Écosse, Farrow et Broders (2011) ont observé des pipistrelles de l’Est en train de s’alimenter au dessus d’un cours d’eau, mais ont constaté davantage d’activité à l’échelle du paysage aux endroits où le couvert forestier était plus important, ce qui laisse croire que cette espèce pourrait éviter les régions déboisées aux fins de l’agriculture, du développement urbain et de l’exploitation forestière. Les distances entre les sites de repos et les aires d’alimentation sont généralement inconnues, mais à certains endroits elles peuvent atteindre 5 km (Quinn et Broders, 2007).
Migration
La petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est sont considérées comme des espèces migratrices de courte distance, quittant chaque année leur habitat d’hivernage dans toutes les directions pour atteindre leur habitat d’estivage (Fraser et al., 2012; COSEWIC, 2013). Au Manitoba et en Ontario, la petite chauve-souris brune migre à l’échelle régionale sur une distance de 35 à 554 km (valeur médiane de 463 km) (Fenton, 1970; Dubois et Monson, 2007; Norquay et al., 2013). Les déplacements migratoires de la chauve-souris nordique ne sont pas bien compris, mais il est probable qu’ils soient semblables à ceux de la petite chauve-souris brune. La pipistrelle de l’Est a quant à elle été observée se déplacer sur une distance de 53 à 780 km (Griffin, 1940; COSEWIC, 2013). En outre, Fraser et al., (2012) ont constaté que certaines pipistrelles de l’Est effectuent une migration latitudinale annuelle, particulièrement les individus qui sont à la limite nord de l’aire de répartition de l’espèce. Cette migration pourrait être liée au besoin des individus de demeurer au chaud, puisqu’ils hibernent souvent seuls (COSEWIC, 2013). Cette théorie est appuyée par Thorne (2015), qui a observé un plus grand nombre de détections de pipistrelles de l’Est à la fin de l’été (c.-à-d. août-septembre) sur les îles des Grands Lacs de l’Ontario.
Comme il a été décrit plus haut, les sites de rassemblement pourraient être utilisés comme haltes migratoires (Fenton, 1969) et sont probablement utilisés chaque année (Rydell et al., 2014). Lorsque des individus traversent de grands plans d’eau, des péninsules et des îles peuvent aussi servir de haltes (Dzal et al., 2009; Thorne, 2015). Par exemple, des pipistrelles de l’Est utilisent l’île Amherst du lac Ontario, et la pointe Long, dans le lac Érié, durant leur migration pour se reposer (Dzal et al., 2009; Thorne, 2015).
Facteurs limitatifs
Les trois espèces sont longévives, et les femelles ne produisent qu’un seul petit (petite chauve-souris brune et chauve-souris nordique) ou 2 petits (pipistrelle de l’Est) par année. De tels caractères du cycle vital accroissent la vulnérabilité de ces populations de chauves-souris aux hausses du taux de mortalité des adultes. De plus, le taux de survie des jeunes de l’année est faible (de 0,23 à 0,46) (Frick et al., 2010b). Une étude réalisée récemment sur une période de 16 ans au New Hampshire, avant l’apparition du SMB, a établi le taux de croissance démographique annuel de la petite chauve-souris brune à 1,008 (Frick et al., 2010b). Chez 22 sous-populations du nord-est des États-Unis, on a estimé que le taux de croissance de la population variait entre 0,98 et 1,2 (Frick et al., 2010a). Les taux de croissance des populations de chauves-souris nordiques et de pipistrelles de l’Est ont été estimés à 1,03 et à 1,04, respectivement (Langwig et al., 2012). Le taux de croissance démographique prévu pour la petite chauve-souris brune dans le nord-est des États-Unis après l’apparition du SMB était de 0,95 (Maslo et al., 2015).
Ces espèces sont grégaires, ce qui augmente leur vulnérabilité à la propagation de pathogènes (comme le champignon responsable du SMB) (Langwig et al., 2012). On ne sait pas si leur nature coloniale et sociale produit des seuils d’abondance, au sein des colonies ou des sous-populations, sous lesquels la survie ou le succès de reproduction des individus diminue et/ou sous lesquels la population se trouve incapable de se rétablir.
On ne sait pas non plus si la disponibilité de sites d’hivernage aux conditions microclimatiques convenables constitue un facteur limitatif au Canada.
4. Menaces
4.1. Évaluation des menaces
Dans les régions où les populations locales de chauves-souris ont diminué de façon importante à cause de la présence du SMB, l’ampleur relative des autres menaces augmente, car la mortalité d’un petit nombre des individus restants (en particulier d’adultes) peut avoir des répercussions sur la survie des populations locales, sur leur rétablissement et, peut être, sur le développement chez elles d’une résistance au champignon responsable du SMB. Par conséquent, le niveau de préoccupation et la gravité de l’impact des menaces autres que le SMB sur les populations de chauves-souris seront généralement élevés dans les régions du Canada qui sont touchées par le SMB, par rapport aux régions qui ne sont pas encore touchées par le SMB. Ces différences dans l’évaluation des menaces sont présentées au tableau 2.
| Catégorie de la menace | Menace | Zones | Niveau de préoccu-pationNoteade tableau 2 | Étendue | Occurrence | Fréquence | GravitéNotebde tableau 2 | Certitude causaleNotecde tableau 2 |
|---|---|---|---|---|---|---|---|---|
| Espèce ou génome exotique, envahissant ou introduit | Syndrome du museau blanc (Pseudogymnoascus destructans) | Zones touchées par le SMB | Très élevé | Généralisée | Courante | Continue | Élevée | Élevée |
| Espèce ou génome exotique, envahissant ou introduit | Syndrome du museau blanc (Pseudogymnoascus destructans) | Zones pas encore touchées par le SMB | Très élevé | Généralisée | Imminente | Continue | Élevée | Élevée |
| Espèce ou génome exotique, envahissant ou introduit | Chats domestiques retournés à l’état sauvage ou laissés en liberté | - | Inconnu | Localisée | Courante | Continue | Inconnue | Faible |
| Perte ou dégradation de l’habitat | Destruction ou dégradation des hibernacles | Zones touchées par le SMB | Élevé | Localisée | Courante | Continue | Élevée | Élevée |
| Perte ou dégradation de l’habitat | Destruction ou dégradation des hibernacles | Zones non touchées par le SMB | Élevé | Localisée | Courante | Continue | Élevée | Élevée |
| Perte ou dégradation de l’habitat | Destruction ou dégradation des sites de repos | Zones touchées par le SMB | Élevé | Localisée | Courante | Continue | Élevée | Élevée |
| Perte ou dégradation de l’habitat | Destruction ou dégradation des sites de repos | Zones non touchées par le SMB | Moyen | Localisée | Courante | Continue | Modérée | Élevée |
| Perte ou dégradation de l’habitat | Destruction, dégradation ou conversion de l’habitat d’alimentation | Zones touchées par le SMB | Moyen | Généralisée | Courante | Continue | Inconnue | Moyenne |
| Perte ou dégradation de l’habitat | Destruction, dégradation ou conversion de l’habitat d’alimentation | Zones non touchées par le SMB | Moyen-faible | Généralisée | Courante | Continue | Inconnue | Moyenne |
| Perturbation ou dommage | Collisions avec des éoliennes ou barotraumatisme associé aux éoliennesNotedde tableau 2 | Zones touchées par le SMB | Élevé | Localisée | Courante | Saisonnière (printemps, été, automne) | Élevée | Élevée |
| Perturbation ou dommage | Collisions avec des éoliennes ou barotraumatisme associé aux éoliennesNotedde tableau 2 | Zones non touchées par le SMB | Moyen | Localisée | Courante | Saisonnière (printemps, été, automne) | Modérée-faible | Moyenne |
| Perturbation ou dommage | Préjudices intentionnels aux individus | Zones touchées par le SMB | Élevé | Localisée | Courante | Continue | Élevée | Élevée |
| Perturbation ou dommage | Préjudices intentionnels aux individus | Zones non touchées par le SMB | Moyen-faible | Localisée | Courante | Continue | Modérée-faible | Moyenne |
| Perturbation ou dommage | Dérangement découlant d’activités récréatives ou scientifiques | Zones touchées par le SMB | Moyen-élevé | Localisée | Courante | Continue | Élevée | Moyenne |
| Perturbation ou dommage | Dérangement découlant d’activités récréatives ou scientifiques | Zones non touchées par le SMB | Moyen | Localisée | Courante | Continue | Modérée | Moyenne |
| Perturbation ou dommage | Dérangement découlant d’activités industrielles (p. ex. pratiques de foresterie et exploitation minière) | Zones touchées par le SMB | Moyen-faible | Localisée | Courante | Continue | Modérée | Faible |
| Perturbation ou dommage | Dérangement découlant d’activités industrielles (p. ex. pratiques de foresterie et exploitation minière) | Zones non touchées par le SMB | Faible | Localisée | Courante | Continue | Faible | Faible |
| Pollution | Mercure | - | Inconnu | Généralisée (est du Canada) | Courante | Continue | Inconnue | Faible |
| Pollution | Autres substances chimiques toxiques | - | Inconnu | Généralisée | Courante | Continue | Inconnue | Faible |
| Pollution | Pollution lumineuse | - | Inconnu | Généralisée | Courante | Continue | Inconnue | Faible |
| Climat et catastrophes naturelles | Modifications de l’habitat ou de la dynamique prédateurs-proies résultant des changements climatiques | - | Inconnu | Généralisée | Courante | Continue | Inconnue | Faible |
| Mortalité accidentelle | Collisions avec des véhicules | - | Inconnu | Généralisée | Courante | Continue | Inconnue | Faible |
4.2. Description des menaces
Les menaces sont décrites ici dans l’ordre où elles sont présentées dans le tableau 2.
Syndrome du museau blanc (Pseudogymnoascus destructans)
Le syndrome du museau blanc (SMB), causé par le champignon dermatophytenote8 Pseudogymnoascus destructans (anciennement appelé Geomyces destructans), est la plus grande menace pesant sur la survie et le rétablissement de la petite chauve-souris brune, de la chauve-souris nordique et de la pipistrelle de l’Est. La plupart des hibernacles connus du nord-est des États-Unis et de l’est du Canada (en excluant Terre-Neuve-et-Labrador) connaissent des déclins massifs à cause de la présence du SMB (U.S. Fish and Wildlife Service, 2015).
Le champignon proviendrait d’Europe (Lindner et al., 2011; Pikula et al., 2012; Ren et al., 2012; Warnecke et al., 2012; Leopardi et al., 2015), et il a été découvert pour la première fois aux États-Unis en 2006 (Lorch et al., 2011), et au Canada, en 2010 (U.S. Fish and Wildlife Service, 2015). Le champignon croît dans les mêmes conditions microclimatiques que celles observées à l’intérieur des hibernacles utilisés durant l’hiver par les trois espèces de chauves-souris. Le champignon colonise la peau des chauves-souris, cause des érosions de l’épiderme, et endommage les glandes sudoripares, les glandes sébacées, les muscles, les tissus conjonctifs, les vaisseaux sanguins et les follicules pileux (Meteyer et al., 2009; Cryan et al., 2010). Les ailes et les oreilles se couvrent de taches blanchâtres à la surface, et le museau devient souvent couvert d’un duvet blanc.
Les stades précoces du SMB ne sont pas nécessairement visibles chez tous les individus infectés. Le SMB se caractérise par un taux métabolique élevé associé à la croissance fongique sur l’épiderme, ce qui stimule l’hyperventilation et accroît les périodes d’éveil, qui contribuent à la déshydratation et à la perte d’électrolytes (Warnecke et al., 2012, Warnecke et al., 2013; Verant et al., 2014). Les derniers stades du SMB sont associés à des lésions cutanées plus importantes et plus graves, lesquelles accroissent la fréquence des éveils, la perte d’eau et la dépense énergétique (Warnecke et al., 2012; Warnecke et al., 2013; Verant et al., 2014). L’épuisement des réserves d’énergie est accéléré par la durée réduite des épisodes de torpeur et par des changements physiologiques aigus à mesure que la pathologie associée au SMB progresse, et entraîne finalement la mort (Frank et al., 2014; Verant et al., 2014). Les chauves-souris infectées par le SMB sont plus susceptibles de voler (de façon erratique) durant l’hiver (Carr et al., 2014). Les chauves-souris qui survivent jusqu’au printemps peuvent se retrouver avec des ailes endommagées (percées de trous) et montrer des signes de stress physiologique ainsi qu’un succès reproducteur réduit (Reeder et Turner, 2008; Meteyer et al., 2009; Reichard et Kunz, 2009; Powers et al., 2012). Toutefois, presque tous les cas de mortalité associés au SMB ont été observés durant l’hibernation, alors que les fonctions immunitaires des chauves-souris sont réduites (Cryan et al., 2010). De plus, Fuller et al., (2011) ont suivi des individus de petite chauve-souris brune et ont observé que les dommages causés à leurs ailes par le SMB guérissaient dans une certaine mesure pendant l’été. La prévalence du SMB décroît durant l’été, probablement parce que la température corporelle des chauves-souris augmente au-delà de la température requise pour la croissance de P. destructans (Langwig et al., 2015b).
Dans l’est du Canada et le nord-est des États-Unis, le taux de mortalité associé au SMB est habituellement faible (c.-à-d. 20 %) durant la première année où la maladie est détectée, puis il devient élevé (c.-à-d. > 70 %) en l’espace de 2 ans (Frick et al., 2010a). Dans les hibernacles connus de l’est du Canada, le nombre de petites chauves-souris brunes et de chauves-souris nordiques hibernantes a connu un déclin d’environ 94 % (COSEWIC, 2013). Le nombre de pipistrelles de l’Est a également montré un déclin précipité d’environ 75 % dans les hibernacles connus (Turner et al., 2011; COSEWIC, 2013).
Taux de propagation
À partir de l’épicentre, à Albany, dans l’État de New York, le taux de propagation du SMB au Canada est approximativement de 200 à 250 km par année (COSEWIC, 2013). En date du 29 mai 2015, la présence du SMB était enregistrée dans 26 États et 5 provinces; la présence du P. destructans était confirmée dans 2 autres États (U.S. Fish and Wildlife Service, 2015) (figure 1; tableau 1). Ceci représente environ 17 % de l’aire de répartition canadienne de la petite chauve-souris brune, 28 % de l’aire de répartition canadienne de la chauve-souris nordique, et 100 % de l’aire de répartition canadienne de la pipistrelle de l’Est qui ont été touchées par le SMB (figure 1). Le SMB est détecté dans des sites additionnels chaque année au Canada, la plus récente détection (c.-à-d. 2015) de P. destructans ayant été faite dans le nord-ouest de l’Ontario, près d’Atikokan (U.S. Fish and Wildlife Service, 2015). On ignore si le SMB s’est propagé jusqu’au Labrador, de même que dans les régions les plus au nord de l’Ontario et du Québec, car les données sur les hibernacles sont limitées dans ces régions. À ce jour, les tests visant les hibernacles de l’île de Terre-Neuve ont donné des résultats négatifs (S. Pardy Moores, comm. pers., 2015). La région de la Côte-Nord, au Québec, est également exempte du SMB.
Transmission
La transmission a lieu par le contact entre les chauves-souris, par le contact des chauves-souris avec un hibernacle contaminé, de même que par des mécanismes anthropiques (p. ex. touristes, spéléologues et chercheurs qui ne suivent pas les protocoles de décontamination adéquats). (Lorch et al., 2011; Lorch et al., 2013). La fréquence des contacts physiques entre les chauves-souris hibernantes varie selon l’espèce, et n’est pas bien corrélée avec les taux d’infection (Kilpatrick, 2013; Langwig et al., 2015b). La transmission de P. destructans ne semble pas être associée à la taille des colonies durant l’hiver ou à l’introduction d’individus vulnérables après la saison de reproduction (Langwig et al.; 2015b).
Les spores du Pseudogymnoascus destructans dans le sol et les murs des hibernacles peuvent demeurer viables pendant des années, voire des décennies, ce qui a le potentiel d’empêcher le rétablissement de ces espèces (Langwig et al., 2012; Hoyt et al., 2014).
Infection des portions toujours indemnes de l’aire de répartition canadienne de la petite chauve-souris brune et de la chauve-souris nordique
Si le SMB continue de se propager à la vitesse actuelle, tous les hibernacles du Canada et des États-Unis seront infectés d’ici 2025 à 2028 (Maher et al., 2012; COSEWIC, 2013; O’Regan et al., 2014).
Au Canada, à mesure que le SMB s’approche des régions moins boisées du sud-ouest du Manitoba, la sécheresse relative et le faible nombre d’arbres dans les Prairies laissent croire que la transmission pourrait se faire plus lentement. Il est toutefois possible que le SMB se propage vers l’ouest par d’autres voies : depuis le sud et/ou depuis des régions boisées situées au nord des Prairies. De plus, malgré certaines indications démontrant que les Rocheuses restreignaient historiquement le flux génique des chauves-souris entre les régions de l’ouest et de l’est, on observe une mixité, et il est donc peu probable que les montagnes jouent le rôle de barrière empêchant le SMB d’atteindre la côte Ouest (Russell et al., 2012).
Des échantillons de petite chauve-souris brune recueillis sur l’île de Terre-Neuve ont révélé une différenciation génétique et une moins grande connectivité génétique lorsque comparés à d’autres échantillons prélevés dans l’est du Canada, ce qui indique que les chauves-souris se déplacent peu entre Terre-Neuve et les autres régions (McLeod et al., 2015). Ceci donne à penser que la probabilité de transmission est plus faible sur l’île qu’elle ne l’est entre d’autres sites d’échantillonnage. Néanmoins, les chauves-souris d’autres régions séparées par des passages océaniques de largeur similaire ne sont pas génétiquement isolées, et la propagation par les chauves-souris jusqu’à Terre-Neuve demeure donc possible (McLeod et al., 2015).
À cause de la transmission par l’homme des spores de P. destructans, le SMB pourrait atteindre les populations indemnes plus rapidement que ce à quoi on pourrait s’attendre par contact entre les chauves-souris. P. destructans a probablement été introduit en Amérique du Nord par les vêtements de touristes ayant visité des grottes en Europe (Okoniewski et al., 2010). Les personnes qui visitent de multiples grottes sans décontaminer leurs vêtements ou leur équipement accroissent substantiellement les risques que P. destructans soit transmis aux hibernacles indemnes de SMB. Par ailleurs, des chauves-souris peuvent être transportées par inadvertance. Par exemple, on a déjà signalé des chauves-souris transportées vers la Colombie-Britannique dans la cale à marchandises d’un navire (P. Govindarajulu, comm. pers.) et dans les auvents de fourgonnettes de camping (C. Lausen, comm. pers). De telles incidences ont la capacité de faire augmenter grandement le taux de propagation du SMB.
Résistance et traitement
Un petit pourcentage d’individus pourrait jouir d’une résistance ou d’une immunité génétique aux effets de P. destructans, laquelle pourrait être transmise à leur descendance. En Europe centrale, P. destructans a été détecté dans environ 63 % des hibernacles échantillonnés, de même que chez plusieurs espèces de chauves-souris, mais aucune mortalité attribuable au SMB n’a été observée, ce qui laisse croire que les populations des espèces européennes pourraient être résistantes ou tolérantes au SMB (Wibbelt et al., 2010, Horacek et al., 2012). Reichard et al., (2014) ont observé qu’un petit nombre (113/2 095 individus bagués) de petites chauves-souris brunes, en Nouvelle-Angleterre, avaient survécu à 1 à 6 hivers depuis l’apparition du SMB, et que certains d’entre eux montraient des signes de succès reproducteur. En Ontario, des chercheurs ont également rapporté de petits nombres de petites chauves-souris brunes survivant au SMB et se reproduisant (D. Morningstar, comm. pers.).
Un nombre important d’études sont en cours dans le but de trouver les causes ultimes, les traitements et les mesures d’atténuation possibles à l’égard du SMB. La composante moléculaire majeure responsable des effets de P. destructans a été découverte et pourrait constituer une cible en matière de lutte contre le SMB (O’Donoghue et al., 2015). De nouvelles recherches prometteuses ont également permis d’isoler, dans le cadre d’essais en laboratoire, une enzyme qui est présente naturellement sur la peau des chauves-souris et qui semble inhiber l’invasion des tissus par P. destructans (Hoyt et al., 2015). De plus, des recherches ont révélé que des substances produites par la bactérie Rhodococcus rhodochrous, présente dans le sol, et par la levure Candida albicans pourraient présenter un potentiel en tant qu’agents de lutte biologique contre P. destructans (Cornelison et al., 2014; Raudabaugh et Miller, 2015).
Chats domestiques retournés à l’état sauvage ou laissés en liberté
Les chats domestiques laissés en liberté ou retournés à l’état sauvage sont des prédateurs d’un nombre substantiel d’oiseaux (Calvert et al., 2013), de petits mammifères (Loss et al., 2013), de reptiles et d’amphibiens (Loyd et al., 2013). Ancillotto et al., (2013) avancent que les chats constitueraient une menace importante pour les chauves-souris. En Colombie-Britannique, le Community Bat Programs of British Columbia reçoit régulièrement des appels et des rapports anecdotiques de chats ayant tué des chauves-souris en Colombie-Britannique (J. Craig, comm. pers.). Les espèces de chauves-souris qui choisissent les structures construites par l’homme (p. ex. granges) comme sites de repos, par exemple la petite chauve-souris brune, sont probablement plus vulnérables à cette menace, car elles risquent de se trouver à proximité de chats. En Italie, des chauves-souris adultes femelles de milieux ruraux ou de milieux urbains peu denses étaient plus susceptibles d’être la proie de chats (Ancillotto et al., 2013). Au Yukon, les chats ont tendance à s’en prendre aux petites chauves-souris brunes juvéniles ayant récemment appris à voler (T. Jung, comm. pers.).
Destruction ou dégradation des hibernacles
La petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est ont besoin de conditions microclimatiques précises durant toute leur période d’hibernation. Par conséquent, toute activité faisant en sorte qu’un hibernacle devient inaccessible pour les chauves-souris ou modifiant la température, le taux d’humidité, la circulation de l’air ou d’autres caractéristiques microclimatiques de l’hibernacle peut donc détruire ou dégrader l’habitat.
La pratique de sceller les entrées des mines, des grottes et des puits creusés est devenue de plus en plus commune au cours des dernières décennies, probablement en raison de préoccupations en matière de santé et sécurité ainsi que de problèmes éventuels de responsabilité civile associés. Si les structures sont utilisées comme hibernacles, le fait d’en sceller l’entrée peut constituer une source potentiellement importante de perte d’habitat. Par exemple, lorsque l’entrée d’un hibernacle, au Kentucky, a été bloquée par une nouvelle boutique de cadeaux, des milliers de chauves-souris de l’Indiana (Myotis sodalis) se sont agrippées aux murs de l’édifice plutôt que de chercher un autre hibernacle (Murphy, 1987). Le fait de bloquer ne serait-ce que de petites entrées peut entraîner un changement de température à l’intérieur des hibernacles, car le régime de circulation d’air y est ainsi modifié (U.S. Fish and Wildlife Service, 2007).
Les activités industrielles, comme l’exploitation de carrières, l’exploration et l’exploitation de mines, l’agriculture, la construction de barrages et l’exploitation forestière peuvent aussi causer, empirer ou accélérer le blocage de la circulation d’air, modifier les conditions hydrologiques ou microclimatiques, potentiellement causer l’inondation de l’hibernacle, ou dégrader directement l’habitat (McAlpine, 1983; U.S. Fish and Wildlife Service, 2007). De plus, les entrées de mines ou de grottes peuvent s’effondrer si de la machinerie lourde (p. ex. équipement servant à la récolte de bois ou à l’extraction minière) est utilisée à proximité de zones fragiles de l’hibernacle (McAlpine, 1983; U.S. Fish and Wildlife Service, 2007). Une fois que l’entrée est bloquée et que les chauves-souris ne peuvent plus entrer dans un hibernacle, ce dernier n’est plus utilisé. Les activités de remise en état d’anciens sites miniers peuvent également nuire aux hibernacles et aux chauves-souris qui les utilisent. Lors de l’enlèvement d’un chevalement dans le cadre d’activités de remise en état d’une ancienne mine en Ontario, en janvier 2011, de 50 à 60 chauves-souris ont été découvertes; elles se sont envolées, puis ont fini par mourir (P. Davis, comm. pers.). À l’inverse, le déclassement de mines actives ou semi-actives (p. ex. en fermant les pompes à eau) peut entraîner l’inondation d’un hibernacle. Les sociétés minières pourraient remettre en activité des mines précédemment abandonnées à des fins d’extraction en raison des fluctuations des prix des minéraux, mais on en sait peu sur la fréquence de cette pratique au Canada. On suppose que la prévalence est faible, mais celle-ci pourrait être préoccupante dans certaines régions du pays.
Les modifications en raison de la présence de touristes (p. ex. plateformes d’observation), de vandalisme intentionnel ou de l’érection de barrières physiques (p. ex. clôtures) peuvent restreindre ou modifier le régime de circulation d’air, ou encore modifier d’autres caractéristiques microclimatiques de l’hibernacle (U.S. Fish and Wildlife Service, 2007). Les barrières sont souvent considérées comme la technique la plus efficiente et la plus efficace pour limiter l’accès des humains aux hibernacles, mais même les barrières dites inoffensives pour les chauves-souris peuvent faire en sorte que ces dernières évitent l’hibernacle, entrent en collision avec la barrière, ou changent de comportement (Spanjer et Fenton, 2005; U.S. Fish and Wildlife Service, 2007; Derusseau et Huntly, 2012; Diamond et Diamond, 2014). L’installation de barrières devrait être faite suivant une conception adéquate, et une surveillance des chauves-souris devrait être effectuée pour s’assurer que les barrières n’entraînent pas d’effets négatifs sur celles-ci.
Destruction ou dégradation des sites de repos
Des trois espèces, la petite chauve-souris brune est celle qui utilise le plus régulièrement les bâtiments et les dortoirs à chauves-souris pour établir ses colonies de maternité. Le nombre de colonies de chauves-souris pourrait être en déclin en raison de la quantité limitée de structures disponibles et des tentatives d’exclusion des chauves-souris par les propriétaires fonciers (Kunz et Reynolds, 2003). Comme les femelles ont tendance à montrer un degré relativement élevé de fidélité, le fait d’exclure les chauves-souris de colonies de maternité antérieurement occupées dans des structures fabriquées par l’humain serait considéré comme une perte d’habitat. De manière similaire, une perte d’habitat surviendrait si un dortoir à chauves-souris antérieurement occupé était enlevé d’un site.
Tout type d’activité de développement entraînant l’élimination d’arbres ou de paysages boisés (p. ex. aménagement des terres, exploration géologique, puits pétroliers et gaziers) a le potentiel de détruire ou de dégrader les aires de repos des trois espèces de chauves-souris. Par exemple, les activités forestières et de récolte de bois (p. ex. coupe de récupération) peuvent éliminer des parcelles de forêt mature, de même que des chicots individuels pouvant être utilisés par les mâles et les femelles pour se reposer.
Les effets de l’enlèvement d’arbres ou de l’exclusion de sites de repos pourraient dépendre de la disponibilité additionnelle d’habitat convenable, du moment de l’année, de l’espèce de chauve-souris, du sexe des individus ainsi que d’autres facteurs. L’exclusion des sites de repos pourrait faire diminuer le succès reproducteur, modifier l’étendue du domaine vital, modifier l’abondance moyenne des colonies, et amoindrir la fidélité aux sites (Brigham et Fenton, 1986; Neilson et Fenton, 1994; Borkin et al., 2011; Chaverri et Kunz, 2011). La petite chauve-souris brune pourrait abandonner des aires de repos après avoir été exclue de sites de repos (Neilson et Fenton, 1994). Toutefois, en fonction de la disponibilité de l’habitat, les chauves-souris pourraient utiliser un autre arbre pour se reposer si un arbre ayant servi de dortoir est enlevé en dehors de la saison de reproduction (Silvis et al., 2015b). Dans le cas des chauves-souris nordiques ayant établi leur site de repos dans le Kentucky, le nombre de sites de repos, les caractéristiques des sites et l’espace global utilisé n’ont pas changé après que les sites très utilisés et 24 % des sites secondaires aient été enlevés de façon expérimentale avant la période de repos (Silvis et al., 2015b). Cependant, les distances parcourues entre les sites de repos successifs ont doublé dans les zones où des sites de repos secondaires ont été enlevés (Silvis et al., 2015b). Néanmoins, Silvis et al., (2015b) ont observé que les conditions forestières locales et les caractéristiques sociales/comportementales de l’espèce qui utilise le site de repos pourraient influer sur les limites de tolérance à l’égard de la perte de sites de repos.
Destruction, dégradation ou conversion de l’habitat d’alimentation
L’élimination, la dégradation et la fragmentation de l’habitat d’alimentation (p. ex. forêts, milieux humides et zones riveraines) peuvent être causées par diverses sources anthropiques, notamment l’exploitation forestière, l’agriculture, l’exploitation pétrolière et gazière, l’exploration et l’exploitation minières ainsi que le développement urbain et résidentiel. Les taux de récolte associés aux pratiques forestières au Canada sont le plus élevés au Québec, en Colombie-Britannique et en Ontario. Ils ont été relativement stables au Canada des années 1980 à 2008 (Masek et al., 2011), mais sont plus faibles depuis 2008 (NFD, 2014). La conversion des terres a été intensive dans certaines portions des aires de répartition de ces espèces. Par exemple, 73 % de la forêt mixte boréale en Saskatchewan a été transformée pour faire place à l’agriculture, 25 % de cette forêt ayant été perdue entre 1966 et 1994 (Hobson et al., 2002). Young et al., (2006) ont calculé un taux annuel de changement de la couverture forestière le long de la bordure sud de la zone boréale albertaine de -0,82 %. On estime que la perte de milieux humides au Canada est d’environ 70 % dans les régions peuplées, le drainage à des fin agricoles étant responsable de la majorité (85%) des conversions connues (Haak, 2008).
De manière générale, de nombreuses espèces de chauves-souris évitent les grandes zones de coupe à blanc ou ouvertes (p. ex. Henderson et Broders, 2008), mais les lisières boisées et végétalisées pourraient constituer des lieux où certaines chauves-souris peuvent s’alimenter (Krusic et al., 1996; Grindal et Brigham, 1998). Les lisières peuvent offrir une protection contre les prédateurs et le vent, et/ou contenir une concentration de proies (Swystun et al., 2001; Henderson et Broders, 2008). La petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est sont toutes trois associées aux forêts ou aux arbres pour la réalisation d’au moins une partie de leur cycle annuel, et sont donc susceptibles d’être touchées par les activités pouvant entraîner la fragmentation, la dégradation et l’élimination de la forêt. Toutefois, les résultats des recherches liées à ces effets potentiels varient selon l’espèce, la quantité d’habitat disponible, la cause de la dégradation de la forêt, l’échelle spatiale étudiée et la disponibilité d’insectes (Grindal et Brigham, 1999; Swystun et al., 2001; Henderson et al., 2008; Ethier et Fahrig, 2011; Segers et Broders, 2014; Pauli et al., 2015).
La fragmentation des forêts peut entraîner la création d’éléments linéaires favorables à la petite chauve-souris brune, mais elle peut aussi faire en sorte de réduire la disponibilité de l’habitat de la chauve-souris nordique (Broders et Forbes, 2004; Broders et al., 2006; Segers et Broders, 2014). À l’inverse, Ethier et Fahrig (2011) ont observé que la fragmentation des forêts (indépendamment de la densité des forêts) était positive pour la petite chauve-souris brune et la chauve-souris nordique (Ethier et Fahrig, 2011). En Alberta, la petite chauve-souris brune et la chauve-souris nordique étaient actives à la lisière des forêts et dans les parcelles résiduelles, mais leur activité était significativement réduite au centre des blocs de coupe (Hogberg et al., 2002). À l’Île-du-Prince-Édouard, la chauve-souris nordique préférait de façon significative le couvert forestier aux aires ouvertes pour se déplacer et s’alimenter (Henderson et Broders, 2008). Au Québec, Myotis spp. et la pipistrelle de l’Est étaient le plus actives dans les espaces verts à l’intérieur des zones forestières les moins fragmentées (Fabianek et al., 2011). En Ontario, l’abondance de la pipistrelle de l’Est était négativement corrélée à la quantité de couvert forestier (Ethier et Fahrig, 2011), mais en Nouvelle-Écosse, les pipistrelles de l’Est étaient moins actives dans les paysages déboisés (p. ex. pour l’agriculture, l’aménagement et la production de bois) (Farrow et Broders, 2011). Farrow et Broders (2011) ont conclu que la pipistrelle de l’Est est une espèce associée aux forêts qui est négativement touchée par les pratiques réduisant l’étendue des forêts à l’échelle du paysage.
Dans les paysages dominés par des terres agricoles, certaines espèces suivent des éléments linéaires de la forêt pour se déplacer et s’alimenter (Henderson et Broders, 2008). À l’Île-du-Prince-Édouard, les chauves-souris nordiques se déplaçaient en suivant une haie d’arbres dans un paysage dominé par des terres agricoles (Henderson et Broders, 2008). Au Québec, Myotis spp. et la pipistrelle de l’Est n’ont pas été directement observées en train d’utiliser des milieux ouverts (p. ex. des terres cultivées ou en jachère, et des terrains de golf), mais elles étaient actives dans les zones boisées adjacentes à ces éléments (Fabianek et al., 2011). L’intensification des activités agricoles, qui fait en sorte d’éliminer les haies et les bords de champs pourrait restreindre l’habitat d’alimentation et de déplacement (Wickramasinghe et al., 2003).
Les milieux humides et les zones autour des plans d’eau (p. ex. zones riveraines et lisières forestières) sont des milieux importants pour l’alimentation des petites chauves-souris brunes, des chauves-souris nordiques et des pipistrelles de l’Est. Les activités qui dégradent ou qui éliminent les milieux humides ont le potentiel d’entraîner des effets négatifs sur la disponibilité et la qualité de l’habitat d’alimentation. La perte de milieux humides, dans le sud de l’Ontario, où les trois espèces sont présentes, a été importante et se poursuit (pertes additionnelles de 3,5 % de 1982 à 2002) (Federal Provincial and Territorial Governments of Canada, 2010). Dans l’aire de répartition de la petite chauve-souris brune, on estime que les pertes de milieux humides, dans la région des fondrières des Prairies du Canada va de 40 à 71 % (Federal Provincial and Territorial Governments of Canada, 2010). La perte et la dégradation de milieux humides se poursuivent dans cette région, principalement en raison de l’intensification des activités agricoles.
Les routes peuvent aussi agir comme barrières pour les chauves-souris en restreignant leurs déplacements et en modifiant leur utilisation de l’habitat (Abbott et al., 2012; Bennett et Zurcher, 2013; Kitzes et Merenlender, 2014; Abbott et al., 2015). Les chauves-souris sont moins susceptibles de traverser une route au vol compte tenu de l’accroissement du bruit causé par la circulation (Bennett et Zurcher, 2013). Le bruit causé par la circulation pourrait également réduire les activités en vol et l’efficacité de la recherche de nourriture en interférant avec l’écholocation et l’ouïe (Abbott et al., 2015).
Collisions avec des éoliennes ou barotraumatisme associé aux éoliennes
Les chauves-souris peuvent être tuées par collision directe avec les pales des éoliennes (Horn et al., 2008) ou par suite d’un barotraumatisme causé par la chute rapide de la pression de l’air derrière les pales (Baerwald et al., 2008; Grodsky et al., 2011; Rollins et al., 2012). Les éoliennes représentent l’une des plus importantes sources de mortalité d’origine humaine chez les chauves-souris (Cryan et Brown, 2007; Cryan, 2011). Les résultats d’études portant sur la mortalité dans divers sites aux États-Unis et en Europe donnent à penser que le taux annuel de mortalité des chauves-souris va de 0 à plus de 50 cas de mortalité par éolienne, mais les protocoles de collecte de données, les plans expérimentaux et les méthodes d’analyse variaient substantiellement d’un parc éolien à l’autre (Kunz et al., 2007; Arnett et al., 2008; Cryan, 2011; Hayes, 2013; Smallwood, 2013). Kunz et al., (2007) ont prédit que, d’ici 2020, pas moins de 110 000 chauves-souris pourraient être tuées annuellement aux États-Unis, en se fondant sur une moyenne de 2,3 chauves-souris par turbine par année. Cryan (2011) indique qu’il pourrait s’agir d’une sous-estimation considérable, et a fourni une estimation de 450 000 chauves-souris tuées annuellement, en se fondant sur un taux de mortalité moyen publié de 11,6 chauves-souris par mégawatt par année. Smallwood (2013) a estimé qu’environ 888 000 chauves-souris étaient tuées chaque année.
Par rapport aux espèces qui migrent sur de longues distances, comme la chauve-souris cendrée (Lasiurus cinereus), la chauve-souris rousse (Lasiurus borealis) et la chauve-souris argentée (Lasionycteris noctivagans), les espèces du genre Myotis présentent un taux de mortalité par des éoliennes plus faible (p. ex. de 0 à 13 % des cas de mortalité) (Arnett et al., 2008). Ce taux de mortalité est probablement attribuable au fait que ces chauves-souris migrent sur de plus courtes distances, et volent généralement sous les turbines durant l’été (Reynolds, 2006).
Au Canada, on estime que 15,5 ± 3,8 chauves-souris sont tuées par éolienne chaque année (Zimmerling et Francis, données inédites). En se fondant sur 4 019 éoliennes installées (le nombre d’éoliennes qui étaient installées au Canada en décembre 2013), environ 52 100 chauves-souris (ICnote9 à 95 % : 28 690-75 316) sont tuées chaque année par des éoliennes (Zimmerling et Francis, données inédites). Au Canada, d’après les données obtenues avant et après l’apparition du SMB, les mortalités de petites chauves-souris brunes représentaient 13 % de toutes les mortalités de chauves-souris associées aux éoliennes (environ 7 000 individus), la majorité des cas de mortalité (88 %) ayant lieu en Ontario (Zimmerling et Francis, données inédites). Dans un parc éolien situé en Ontario, les cas de mortalité de chauves-souris concernaient principalement la petite chauve-souris brune; cette espèce comptait pour 46 % de tous les cas de mortalité en juillet, et pour 38 % d’avril à septembre (OMNRF, données inédites). Les cas de mortalité de chauves-souris nordiques représentent un peu moins de 1 % de tous les cas de mortalité associés aux éoliennes (environ 440 individus) au Canada (Zimmerling et Francis, données inédites). À une centrale éolienne située en Colombie-Britannique, les petites chauves-souris brunes et les chauves-souris nordiques représentaient 44 % de toutes les mortalités de chauves-souris enregistrées, la plupart ayant lieu en juillet et en août (Hemmera, 2011). Dans certains parcs éoliens de l’est des États-Unis, les pipistrelles de l’Est mortes représentaient pas moins de 25,4 % des cas de mortalité (Arnett et al., 2008), alors que, au Canada, moins de 5 carcasses (c.-à-d. moins de 0,1 % de toutes les carcasses) ont été découvertes durant les relevés de carcasses (Zimmerling et Francis, données inédites). On ignore si ces espèces sont moins vulnérables aux effets des éoliennes en raison des différences qu’elles présentent en matière de vol, de comportement de chasse et d’habitat, ou si leurs populations sont simplement moins abondantes, ce qui fait que les individus sont généralement peu communs autour des parcs éoliens. Néanmoins, même de faibles taux de mortalité ont le potentiel d’être biologiquement importants pour les espèces relativement rares. Il est possible que de futurs parcs éoliens, s’ils sont situés accidentellement à proximité de zones à forte concentration d’individus (p. ex. sites de repos, hibernacles), entraînent des taux de mortalité élevés.
On s’attend à ce que le taux de mortalité augmente avec le nombre d’éoliennes. Dans les zones touchées par le SMB, l’importance biologique de toute mortalité pourrait augmenter considérablement. La mortalité de quelques individus pourrait avoir des répercussions sur la capacité des populations locales de se rétablir et de développer une résistance au champignon.
À l’heure actuelle, les mesures d’atténuation visant à réduire la mortalité des chauves-souris liée au développement éolien peuvent comprendre la mise en drapeau des pales ou la hausse de la vitesse d’enclenchement lorsque les risques pour les chauves-souris sont particulièrement élevés (p. ex. la nuit, au pic de la migration) (Baerwald et al., 2009). Baerwald et al., (2009) ont montré que ces techniques d’atténuation avaient réduit les cas de mortalité de chauves-souris d’environ 60 % dans un site du sud-ouest de l’Alberta. Arnett et al., (2009, 2013b) ont observé que le réglage à la vitesse à laquelle la turbine commence à tourner et à générer de l’énergie avait réduit les cas de mortalité de chauves-souris d’environ 73 % (de 44 à 93 %) dans un parc éolien situé en Pennsylvanie, avec une marge de ~ 1 % en perte d’énergie annuellement. L’émission d’ultrasons pourrait également réduire le nombre de cas de mortalité de chauves-souris attribuables aux éoliennes en dissuadant les chauves-souris d’approcher de la source sonore (Arnett et al., 2013a). Dans certaines circonstances, les techniques opérationnelles d’atténuation pourraient comprendre l’arrêt périodique de certaines turbines durant les périodes présentant un plus haut risque.
Préjudices intentionnels aux individus
Certaines espèces de chauves-souris, notamment la petite chauve-souris brune, utilisent souvent des structures fabriquées par l’homme comme sites pour établir leurs colonies de maternité ou leurs hibernacles. Le bruit, l’accumulation d’excréments, et la crainte de contracter l’histoplasmosenote10 et la rage pourraient être à l’origine de l’extermination de colonies de maternité. Peu de données sont disponibles afin de déterminer la prévalence et l’impact de l’élimination des colonies de maternité. La majeure partie des données sont anecdotiques, car les exigences en matière de rapports visant les entreprises de lutte contre les espèces sauvages nuisibles varient d’un territoire à l’autre (COSEWIC, 2013). Le fait de sceller l’entrée d’une colonie de maternité occupée entraînerait aussi fort probablement la mort de tous les individus se trouvant à l’intérieur. Certaines colonies de maternité pourraient contenir la majorité des femelles reproductrices et de la descendance à l’intérieur d’une vaste zone. L’élimination des colonies pourrait donc avoir des répercussions importantes sur les populations locales.
Des préjudices intentionnels causés à des individus se trouvant à l’intérieur d’hibernacles ont également été rapportés. Par exemple, en 1989, toutes les chauves-souris (~ 800 petites chauves-souris brunes et chauves-souris nordiques) ont été retirées pour être incinérées du seul hibernacle connu de chauves-souris nordiques de l’Île-du-Prince-Édouard (Brown et al., 2007). Bien que les chauves-souris aient été sauvées de l’incinération, les efforts visant à les garder pendant l’hiver ont échoué et elles ont toutes péri (Brown et al., 2007).
Certaines provinces et certains territoires ont pris des mesures visant à réduire les risques de préjudices intentionnels. Par exemple, le ministère des Ressources naturelles du Nouveau-Brunswick a retiré ces espèces de la liste des espèces sauvages nuisibles aux termes de la Loi sur le poisson et la faune du Nouveau-Brunswick, appuyant ainsi les solutions non létales en matière de gestion des espèces sauvages nuisibles. Voir la section 2, intitulée Information sur la situation de l’espèce pour en savoir davantage sur la législation protégeant les individus.
Dérangement découlant d’activités récréatives ou scientifiques
La présence d’humains (Thomas, 1995) ou la manipulation de chauves-souris en hibernation peuvent faire sortir ces dernières de leur torpeur (Speakman et al., 1991). Lorsqu’elles sont profondément endormies, les chauves-souris ne sont généralement pas dérangées par le bruit ambiant (Harrison, 1965), mais certains individus peuvent réagir au bruit et à la lumière, sortir de leur torpeur, et se mettre à voler (Thomas, 1995). Ces individus peuvent alors déclencher une cascade de réveils résultant de leurs activités tactiles chez les chauves-souris qui se trouvent à proximité (p. ex. tentatives de copulation, retour au perchoir) (Thomas, 1995). Même les visites non intrusives peuvent provoquer une importante consommation de graisses (épuisement précoce des réserves énergétiques), une famine, une réduction des réserves énergétiques destinées à la reproduction, et la mort (Gaisler et al., 1981; Boyles et Brack, 2009; Olson et al., 2011). L’abondance de la population de petites chauves-souris brunes a augmenté de façon importante dans une grotte située en Alberta après que l’accès durant l’hiver et l’automne ait été restreint pour réduire le degré de perturbation durant l’hibernation et le rassemblement (Olson et al., 2011). La tolérance aux perturbations est liée à la durée de l’hiver ainsi qu’au nombre de visites et à leur fréquence; les visites répétées s’échelonnant sur plusieurs jours consécutifs ont les effets les plus graves (Boyles et Brack, 2009). Comme les chauves-souris atteintes du SMB vivent davantage de périodes d’éveil (Reeder et al., 2012), les effets additionnels des réveils causés par l’homme dans les hibernacles touchés par le SMB pourraient être importants.
Les touristes, les spéléologues, les utilisateurs récréatifs et les chercheurs sont les principaux visiteurs des hibernacles. Les visites qui ont lieu l’été (période de la plupart des visites) ont probablement moins de répercussions directes sur les chauves-souris parce que le site n’est pas utilisé ou que les chauves-souris peuvent refaire leurs réserves de graisse. Pour limiter les visites durant toute l’année, des barrières ont été installées à certains hibernacles, des groupes de spéléologues ont publié des lignes directrices (p. ex. Speleological Society of Manitoba) (SSM, 2015), et les chercheurs spécialistes des chauves-souris ont réduit le nombre et la durée de leurs visites.
Les activités dans une colonie de maternité peuvent être préoccupantes si elles dérangent les chauves-souris ou font en sorte que ces dernières abandonnent la colonie de maternité pour d’autres sites. La manipulation de chauves-souris à des fins de recherche pourrait également entraîner des conséquences sur l’énergie ou la condition physique de celles-ci, mais on ignore l’ampleur de ces activités et l’importance des effets qu’elles pourraient avoir, mais on suppose que celles-ci sont faibles.
Dérangement découlant d’activités industrielles
L’exploration minière, l’exploitation forestière et les autres activités industrielles pourraient menacer les chauves-souris si elles causent du bruit, de la lumière et des vibrations près des hibernacles, et perturber ainsi les chauves-souris en hibernation en les faisant sortir de leur torpeur. Par exemple, à l’automne 2008, une entreprise d’exploration minière a mené des activités d’exploration dans une galerie d’accès d’une ancienne mine, en Ontario, et a réveillé de nombreuses chauves-souris de leur torpeur (Anonymous, 2008).
De manière similaire, le bruit et les vibrations dans les zones où l’on trouve des colonies de maternité pourraient entraîner une réduction du succès reproducteur, et faire en sorte que les chauves-souris abandonnent le site pour en trouver d’autres. (McCracken, 2011). Comme les chauves-souris dépendent de l’écholocation ou des sons générés par leurs proies pour chasser, les bruits d’origine humaine pourraient également interférer avec la chasse et nuire à la détection des proies (Bunkley et al., 2015). Toutefois, une étude portant sur des stations de compression associées à l’extraction de gaz naturel dans le Nouveau-Mexique n’a révélé aucune différence importante entre le degré d’activité des petites chauves-souris brunes dans les sites comportant des compresseurs bruyants et celui observé aux plateformes d’exploitation plus tranquilles (Bunkley et al., 2015).
Mercure
Le mercure est un élément présent naturellement qui est enrichi dans l’environnement par les activités humaines. Le transport atmosphérique à longue distance et le dépôt subséquent constituent la principale source de mercure pour de nombreux milieux aquatiques dans une grande partie du paysage (Fitzgerald et al., 1998; U.S. Geological Survey, 2000). Le mercure biodisponible est entraîné aussi dans les bassins hydrographiques au cours des activités d’exploitation forestière, de la création de réservoirs hydroélectriques et de diverses activités industrielles connexes (Porvari et al., 2003; Vuori et al., 2003; Wiener et al., 2003). Les concentrations de mercure dans les réseaux trophiques aquatiques sont habituellement corrélées avec de faibles pH, de sorte que dans les réseaux trophiques d’eau douce du Canada, elles vont en s’accroissant, tout comme le pH, d’ouest en est (Depew et al., 2013).
Les chauves-souris semblent particulièrement sensibles à l’accumulation de métaux lourds parce que la plupart des espèces sont longévives, occupent les niveaux trophiques supérieurs, se nourrissent d’insectes aquatiques émergents, ont des taux métaboliques élevés et consomment beaucoup de nourriture. Selon des études menées récemment dans le nord-est des États-Unis, l’accumulation de mercure dans les échantillons de sang et de fourrure prélevés chez des petites chauves-souris brunes et des chauves-souris nordiques, de toutes les classes d’âge, à proximité de sites contaminés par le SMB était significativement plus élevée que l’accumulation de mercure mesurée à proximité de sites non contaminés (Karouna-Renier et al., 2014; Yates et al., 2014). Cependant, Karouna-Renier et al., (2014) n’ont pas observé de différences significatives sur le plan des effets génotoxiques (c.-à-d. dommages à l’ADN) du mercure entre les sites contaminés et les sites non contaminés. Les concentrations de mercure chez des petites chauves-souris brunes échantillonnées en Nouvelle-Écosse variaient d’une colonie à l’autre en fonction de l’acidité du lac avoisinant, et 48 % des individus échantillonnés ont affiché des concentrations supérieures à une concentration seuil associée à des changements neurochimiques chez d’autres espèces de chauves-souris en Virginie (Little et al., 2015b). Sur les 344 petites chauves-souris brunes échantillonnées dans des colonies de maternité du Canada atlantique (Nouvelle-Écosse, Île-du-Prince-Édouard et Terre-Neuve-et-Labrador), 37 % affichaient des concentrations dépassant le seuil des effets neurochimiques (Little et al., 2015a). Ces récentes études soulèvent des questions en ce qui concerne les effets du mercure et d’autres contaminants de l’environnement sur le succès de la reproduction, les réactions physiologiques (p. ex. réponse immunitaire) et la survie.
Autres substances chimiques toxiques
Les effets sublétaux de substances chimiques rapportés chez les chauves-souris comprennent l’altération du vol et de la capacité de rechercher de la nourriture, qui entraînent un risque de prédation accru et une accumulation d’énergie moindre, une immunodépression, une réduction du succès reproducteur et des modifications sur le plan de l’activité métabolique (Clark et Lamont, 1976; Eidels et al., 2007; Kannan et al., 2010). On ne sait pas encore quel est l’effet de la contamination sublétale sur la vulnérabilité des chauves-souris au SMB, mais on a mesuré des concentrations élevées de contaminants organiques dans les tissus adipeux de la petite chauve-souris brune, et ce, tant dans des populations en santé que dans des populations touchées par le SMB (Kannan et al., 2010).
La pulvérisation de pesticides dans les milieux agricoles et forestiers est susceptible de réduire l’abondance des insectes dont se nourrissent les chauves-souris. L’application généralisée et/ou continue de pesticides (comme celle qui pourrait être pratiquée pour lutter contre les chenilles de la tordeuse des bourgeons de l’épinette [Choristoneura fumiferana] ou le dendroctone du pin ponderosa [Dendroctonus ponderosae], ou dans les paysages agricoles) est susceptible d’avoir une incidence considérable sur la disponibilité de la nourriture et la physiologie. Même à l’échelle locale, au Royaume-Uni, l’activité des chauves-souris était significativement plus élevée dans les milieux aquatiques de fermes biologiques que dans ceux se trouvant dans des fermes conventionnelles, ce qui laisse croire à une plus grande disponibilité de proies dans les zones où l’utilisation de substances agrochimiques est moindre (Wickramasinghe et al., 2003).
Les insecticides néonicotinoïdes ont été introduits dans les années 1990; ils représentent actuellement la classe d’insecticides la plus utilisée sur la planète, et leur utilisation ne cesse d’augmenter (Sparks, 2013; Douglas et Tooker, 2015). Bien qu’ils soient généralement utilisés sur les terres agricoles, on les a détectés dans des milieux humides (Main et al., 2014) et dans des cours d’eau au Canada (Environment Canada, 2011; Xing et al., 2013), et on en trouve fréquemment à des concentrations dépassant les lignes directrices pour la qualité de l’eau (Morrissey et al., 2015). Les insecticides néonicotinoïdes ont un impact négatif sur les populations d’insectes (et, par conséquent, sur les insectes pouvant servir de proies aux chauves-souris) (Goulson, 2013); certaines des plus importantes proies (mouches, phryganes et éphémères) de la petite chauve-souris brune, de la chauve-souris nordique et de la pipistrelle de l’Est font partie des insectes aquatiques les plus sensibles aux insecticides néonicotinoïdes (Morrissey et al., 2015). La disponibilité réduite de proies pourrait faire augmenter la durée de la période de chasse, réduire les réserves de graisses des chauves-souris et/ou accroître le temps qu’elles passent en état de torpeur et, au final, mener à une piètre condition physique, et entraîner un déclin des taux de reproduction et/ou de survie. (Talerico, 2008, Reimer, 2013). En plus de réduire l’abondance des populations de proies, les néonicotinoïdes causent des effets sublétaux directs sur le succès reproducteur, le développement, la fonction immunitaire et la croissance chez de nombreux vertébrés (Gibbons et al., 2015). Mason et al., (2013) ont formulé l’hypothèse selon laquelle les milliers d’invertébrés consommés par les chauves-souris exposeraient inévitablement ces dernières à de faibles doses cumulatives de toxines. À ce jour, aucune recherche ne s’est penchée sur les effets directs ou indirects des néonicotinoïdes sur les chauves-souris.
L’incidence accrue de la prolifération saisonnière d’algues pourrait également représenter une menace pour ces espèces. Les proliférations d’algues peuvent être naturelles, mais l’occurrence mondiale de proliférations d’algues nuisibles ou toxiques semble augmenter (Hallegraeff, 1993; Anderson et al., 2002). Les proliférations d’algues sont le résultat d’un apport accru en nutriments dans les plans d’eau. Le phosphore et l’azote de source industrielle ou agricole, ou provenant d’eaux usées, sont les deux plus importants apports d’origine humaine (Anderson et al., 2002). Ces apports donnent lieu à la production d’algues nuisibles et/ou toxiques, notamment d’une substance chimique appelée microcystine. On sait que la microcystine cause des irritations cutanées, des vomissements, le cancer du foie, et la mort chez les humains, le bétail, les animaux domestiques et de nombreux organismes aquatiques (Kuiper-Goodman et al., 1999; Sivonen et Jones, 1999). Des chercheurs ont observé le transfert de microcystine depuis des écosystèmes aquatiques jusque dans des écosystèmes terrestres, notamment par l’émergence des insectes aquatiques (Smith et al., 2008) qui, à leur tour, sont ingérés par les chauves-souris. De la microcystine a été détectée dans tous les échantillons fécaux (n = 20) de petite chauve-souris brune près d’un lac, au Michigan, qui connaît des proliférations d’algues saisonnières (Woller-Skar et al., 2015). D’autres études sont nécessaires pour en comprendre les effets sur les individus et sur les populations de chauves-souris, mais cette toxine pourrait représenter une menace encore non reconnue pour les populations de chauves-souris (Woller-Skar et al., 2015). Une autre toxine associée aux proliférations d’algues (Anabaena flos-aquae) a été associée à un épisode de mortalité massive de chauves-souris (y compris de Myotis spp.), en Alberta (Pybus et al., 1986).
Pollution lumineuse
La modification (p. ex. moment, étendue spatiale et signature spectrale) des régimes d’éclairement naturel attribuable à des sources lumineuses artificielles peut avoir divers effets directs et indirects sur certaines espèces en ce qui touche l’alimentation, la reproduction, la communication, l’utilisation de l'habitat et le comportement de déplacement (Stone et al., 2009; Gaston et al., 2013; Mathews et al., 2015). Les effets pourraient être bénéfiques (p. ex. disponibilité accrue de nourriture), neutres ou nuisibles (p. ex. vulnérabilité à la prédation accrue, collisions avec des structures lumineuses) (Kyba et al., 2011).
Pour les chauves-souris en particulier, lorsque les insectes proies se concentrent autour de sources lumineuses, l’efficacité de l’alimentation peut être accrue, ce qui est considéré comme étant bénéfique pour certaines espèces (Entwistle et al., 2001; Lacoeuilhe et al., 2014; Mathews et al., 2015). Dans le sud-ouest de l’Ontario, Furlonger (1987) a observé que toutes les espèces de chauves-souris rencontrées exploitaient les concentrations d’insectes autour des sources lumineuses artificielles, mais ce comportement n’était pas important chez Myotis spp.; aucune pipistrelle de l’Est n’a été observée. De manière générale, on a observé que les chauves-souris qui présentent une charge alaire élevée ou moyenne et qui volent rapidement exploitent les insectes autour des lampadaires, alors que les chauves-souris glaneuses et celles qui détectent leurs proies au son du battement de leurs ailesnote11 s’alimentent rarement, voire jamais, autour des lampadaires (Mathews et al., 2015). De manière similaire, en France, les espèces insectivores aériennesnote12 sont tolérantes à la lumière, alors que les espèces qui volent lentement connaîtraient plutôt un risque de prédation élevé lorsque le degré de luminosité est élevé, et donc n’utilisent pas les zones éclairées pour s’alimenter (Lacoeuilhe et al., 2014). La petite chauve-souris brune est considérée comme une espèce insectivore aérienne et dotée d’un vol efficace et habile, et devrait donc tirer avantage des sources lumineuses. La chauve-souris nordique vole lentement et chasse souvent en vol stationnaire, et la pipistrelle de l’Est vole lentement, de façon erratique, en virevoltant; ces deux espèces ne devraient donc pas chasser près des sources lumineuses (Naughton, 2012).
Bien que cela semble bénéfique pour certaines espèces de chauves-souris, la pollution lumineuse est tenue comme responsable du déclin de nombreuses populations d’insectes qui sont attirés par la lumière (p. ex. papillons de nuit, insectes aquatiques et autres insectes terrestres (Frank, 1988; Perkin et al., 2014; MacGregor et al., 2015). De nombreux insectes sont attirés par la lumière artificielle, ce qui influe sur leur dispersion et leur orientation, de même que sur leur reproduction, leur accouplement, leur crypticité, et leur capacité d’échapper aux prédateurs. Des individus connaissent une mortalité directe, en volant jusqu’à l’épuisement, en brûlant vifs, ou en devenant prisonniers des réceptacles contenant les lumières (Frank, 1988; Horváth et al., 2009; Perkin et al., 2014). Ces phénomènes réduisent à leur tour la biomasse et l’abondance, et peuvent modifier la composition relative des populations d’insectes, et causer des répercussions dans la chaîne alimentaire en perturbant les relations proies-prédateurs, la pollinisation et les fonctions écosystémiques (Hölker et al., 2010; Kyba et al., 2011).
En Hongrie, l’illumination des sites de repos des espèces Myotis qui nichent dans des maisons a entraîné l’effondrement de colonies entières et la réduction du taux de croissance des juvéniles (Boldogh et al., 2007). Ces phénomènes sont survenus en raison de l’émergence retardée des sites de repos ayant entraîné des occasions ratées d’alimentation durant le pic d’activité des insectes. On présume que l’évitement des zones éclairées est dû au risque de prédation accru et/ou aux effets négatifs sur la capacité d’orientation des chauves-souris (Boldogh et al., 2007; Lacoeuilhe et al., 2014).
Les effets de la lumière artificielle semblent variables et propres aux espèces. Peu de recherches directement dédiées à l’acquisition d’une meilleure compréhension des effets de la pollution lumineuse ont été réalisées sur ces trois espèces de chauves-souris au Canada, et de plus amples études sont nécessaires.
Modifications de l’habitat ou de la dynamique prédateurs-proies résultant des changements climatiques
Les effets des changements climatiques sur les chauves-souris sont inconnus. Les chauves-souris (en particulier les femelles en lactation) sont plus susceptibles de perdre de l’eau par évaporation que les autres mammifères, ce qui laisse croire qu’elles pourraient être vulnérables aux températures accrues associées aux changements climatiques (Webb et al., 1995; Chruszcz et Barclay, 2002; Adams et Hayes, 2008). Adams (2010) a observé des déclins importants sur le plan de la reproduction chez la petite chauve-souris brune durant les années imitant les conditions prédites dans les scénarios relatifs aux futurs changements climatiques (c.-à-d. disponibilité réduite d’eau).
Les autres effets directs comprennent la destruction de sites de repos et/ou d’hibernacles en raison de l’augmentation de la fréquence des tempêtes susceptibles de survenir dans le futur (Jones et Rebelo, 2013). Bien que les chauves-souris hibernantes au Canada puissent bénéficier de la hausse des températures due aux changements climatiques, des températures plus élevées pourraient aussi perturber l’hibernation, réduire les quantités d’eau et accroître les cas de maladie (Sherwin et al., 2013). Humphries et al., (2002) ont prédit que les changements climatiques causeraient une expansion de l’aire de répartition de la petite chauve-souris brune vers le nord en 80 ans.
L’étendue, l’intensité et la fréquence des feux de forêt devraient continuer de s’accroître en raison du réchauffement et des printemps et des étés plus secs (Flannigan et al., 2009; de Groot et al., 2013; Girardin et al., 2013). De manière similaire, les infestations d’insectes forestiers (p. ex. la présence de tordeuses des bourgeons de l’épinette et de dendroctones du pin ponderosa) devraient s’intensifier avec les changements climatiques (Mattson et Haack, 1987). Ces processus ont la capacité de modifier de vastes zones boisées et de causer la mortalité d’arbres entiers (Fleming et al., 2002), mais ils peuvent aussi faire en sorte que des chicots deviennent disponibles comme sites de repos pour les chauves-souris et/ou accroissent la disponibilité locale de proies (Wilson et Barclay, 2006). Par conséquent, les effets ultimes sur les populations de chauves-souris et leur habitat sont inconnus.
En plus de leurs effets directs, les changements climatiques pourraient avoir un impact indirect sur la survie des chauves-souris à cause de leurs effets sur les populations d’insectes (Arlettaz et al., 2001). Dans le nord-est du continent, on peut s’attendre à des hivers plus humides et à des étés plus secs en raison des changements climatiques (Hayhoe et al., 2007; Huntington et al., 2009). Les petites chauves-souris brunes femelles adultes présentent un taux de survie annuel réduit durant les années plus sèches. On présume que ce phénomène est associé au lien entre le degré d’humidité et la disponibilité d’insectes émergents (Frick et al., 2010b). Le moment du pic de l’abondance de certains insectes survient également plus tôt (Both et al., 2009). De tels changements pourraient influer sur le synchronisme qui existe entre la période de densité maximale des proies et la période de reproduction des chauves-souris (Jones et al., 2009), et donc sur la survie des petits. Les petits des chauves-souris ont besoin d’une quantité suffisante de proies pour produire les tissus adipeux nécessaires à leur survie hivernale (Kunz et al., 1998).
Collisions avec des véhicules
Les collisions avec des véhicules peuvent entraîner la mortalité directe de chauves-souris (Medinas et al., 2013). Le moment de la saison, le milieu environnant et la densité du trafic influent sur le nombre de collisions avec des véhicules (Lesiński et al., 2011; Medinas et al., 2013). Les taux de mortalité sont le plus élevés à proximité des aires de repos et des aires d’alimentation actives (Medinas et al., 2013), et les espèces adaptées aux forêts, comme la chauve-souris nordique et la pipistrelle de l’Est, sont les plus à risque en raison de leur vol bas et lent caractéristique (Abbott et al., 2015). Il existe également des mentions anecdotiques de chauves-souris entrant en collision avec des véhicules et appareils non traditionnels/récréatifs, par exemple des embarcations aquatiques (p. ex. bateaux, véhicules marins personnels, et planches à voile), des lignes de pêche, et des véhicules tout-terrain. La gravité de cette menace pour les populations de petites chauves-souris brunes, de chauves-souris nordiques et de pipistrelles de l’Est au Canada est inconnue.
5. Objectifs en matière de population et de répartition
Il n’existe pas d’estimation fiable de l’abondance actuelle ou passée des populations de petites chauves-souris brunes, de chauves-souris nordiques et de pipistrelles de l’Est au Canada. Par conséquent, les tendances en matière de population seront estimées en calculant, à l’aide des données relatives aux hibernacles et aux aires de repos connus et étudiés précédemment dans l’ensemble de l’aire de répartition canadienne de l’espèce (telles que présentées dans COSEWIC, 2013), un indice des tendances de la population totale; ces données seront bonifiées par des relevés et des données de suivi présentés à la section 6.2 du présent programme de rétablissement, intitulée Orientation stratégique pour le rétablissement.
Petite chauve-souris brune et chauve-souris nordique
Les objectifs en matière de population visant précisément une région sont définis en fonction de l’état actuel (2015) du SMB au Canada : les régions touchées par le SMB et les régions qui ne sont pas encore touchées par le SMB (voir la figure 1). L’actuel front de propagationnote13 se trouve dans le nord-ouest de l’Ontario, près d’Atikokan (en date du 29 mai 2015) (U.S. Fish and Wildlife Service, 2015).
Objectif en matière de répartition
- L’objectif en matière de répartition établi pour la petite chauve-souris brune et la chauve-souris nordique consiste à maintenir (ou à rétablir, le cas échéant) la zone d’occurrence antérieure à l’apparition du SMB (zone englobant l’aire de répartition géographique connue de l’espèce au Canada, telle qu’elle est illustrée aux figures 1 et 2).
Objectifs en matière de population (à l’intérieur des régions touchées par le SMB)
- Dans les régions touchées par le SMB, l’objectif à court terme (de 12 à 18 ans) en matière de population consiste à maintenir (et à accroître, dans la mesure du possible) la population à son niveau actuel (2015).
- Dans les régions touchées par le SMB, l’objectif à long terme (plusieurs générations) en matière de population est une population autosuffisantenote14, résilientenote15, et redondantenote16.
Objectif en matière de population (régions non touchées par le SMB)
- Dans les régions qui ne sont pas encore touchées par le SMB, l’objectif en matière de population consiste à maintenir (et à accroître, dans la mesure du possible) la population à son niveau actuelnote17.
L’aire de répartition du SMB chevauche environ respectivement 28 % et 17 % des aires de répartition canadiennes de la petite chauve-souris brune et de la chauve-souris nordique, et prend de l’expansion à un rythme moyen de 200 à 250 kilomètres par année (COSEWIC, 2013). Comme les conditions propices à la prolifération de P. destructans existent dans des régions non encore touchées par le SMB, sans mesures d’atténuation, les populations canadiennes entières des deux espèces seront probablement touchées d’ici 2025 à 2028 (COSEWIC, 2013). Par conséquent, on a jugé qu’une période de 12 à 18 ans convenait à l’objectif à court terme en matière de population.
L’objectif à long terme en matière de population s’appuie sur les faibles taux de croissance des populations des deux espèces, ce qui fait en sorte que leur rétablissement pourrait prendre plusieurs générations (c.-à-d. des centaines d’années) (voir la section Facteurs limitatifs). On ne sait pas dans quelle mesure les populations canadiennes (et continentales) de petites chauves-souris brunes et de chauves-souris nordiques seront capables de se rétablir entièrement à leurs niveaux historiques dans les régions touchées par le SMB. L’objectif pour les régions encore non touchées par le SMB prend en considération le fait qu’accroître l’effectif des populations (là où cela est possible) améliorera le potentiel de rétablissement des populations (p. ex. capacité de repeupler des régions touchées par le SMB et d’accroître la probabilité de découvrir des individus qui présentent une résistance au SMB).
La prévention de l’introduction du SMB dans les hibernacles se trouvant dans les régions non encore touchées (p. ex. dans les Prairies, et dans le nord et l’ouest du Canada) constitue le facteur le plus important pour empêcher la perte additionnelle d’individus. Au Canada, à mesure que le SMB s’approche des régions moins boisées du sud-est du Manitoba, la sécheresse relative et la faible densité des arbres laissent croire que la transmission pourrait se faire plus lentement. On reconnaît néanmoins qu’il n’est peut-être pas possible d’empêcher la propagation du SMB.
Pipistrelle de l’Est
Objectif en matière de répartition
- L’objectif en matière de répartition établi pour la pipistrelle de l’Est consiste à rétablir (puis à maintenir) la zone d’occurrence antérieure à l’apparition du SMB (la zone englobant l’aire de répartition géographique connue de l’espèce au Canada, telle qu’elle est illustrée à la figure 3).
Objectif à court terme (10 ans) en matière de population
- L’objectif à court terme en matière de population consiste à maintenir (et à accroître, dans la mesure du possible) la population à son niveau actuel (2015) au cours des 10 prochaines années.
On a jugé qu’une période de 10 ans convenait à l’objectif à court terme en matière de population, car il faudra de nombreuses années pour acquérir les données qui permettront d’établir si la population s’est stabilisée ou a augmenté. On s’attend à ce que des recherches approfondies soient menées durant cette période afin de mettre au point des traitements du SMB pour les individus ou les hibernacles. De plus, les critères d’évaluation du COSEPAC comprennent un examen des changements relatifs à la population sur des périodes de 10 ans.
Objectif à long terme en matière de population
- L’objectif à long terme en matière de population est une population autosuffisante, résiliente et redondante.
On ne sait pas dans quelle mesure la population de pipistrelles de l’Est sera capable de se rétablir entièrement à ses niveaux historiques. L’objectif à long terme en matière de population s’appuie sur l’hypothèse voulant que, advenant l’acquisition d’une résistance au SMB par les individus ou de la découverte d’un traitement de la maladie, les faibles taux de croissance des populations de l’espèce fassent en sorte que leur rétablissement pourrait prendre plusieurs générations (c.-à-d. des centaines d’années) (voir la section Facteurs limitatifs).
Étant donné que la population canadienne de pipistrelles de l’Est se trouve dans la portion nord-est de l’aire de répartition continentale de l’espèce et que la majeure partie de l’aire de répartition et de la population se trouve aux États-Unis et jusqu’à la côte est de l’Amérique centrale, toute fluctuation de la population continentale aura une incidence déterminante sur le caractère réalisable du rétablissement de l’espèce au Canada.
Ces objectifs seront revus au moment d’établir le rapport requis (art. 46 de la LEP) sur la mise en œuvre du présent programme de rétablissement et les progrès réalisés vers leur atteinte, dans un délai de cinq ans après la publication du présent programme dans le Registre public des espèces en péril. Ces objectifs pourraient être revus à mesure que de nouveaux renseignements sur le SMB et les populations de chauves-souris au Canada deviendront accessibles.
6. Stratégies et approches générales pour l’atteinte des objectifs
6.1. Mesures déjà achevées ou en cours
La liste de mesures qui suit n’est pas exhaustive, mais elle illustre les principaux domaines visés et met en contexte les stratégies générales de rétablissement décrites à la section 6.2. Les mesures suivantes sont achevées ou en cours :
À l’échelle internationale
- En avril 2015, une lettre d’intention concernant les activités visant à promouvoir la conservation des chauves-souris dans les États-Unis du Mexique, les États-Unis d’Amérique et le Canada a été signée par des représentants des trois pays afin d’accroître la collaboration et la coordination en matière de conservation des chauves-souris en Amérique du Nord.
- Le North American Bat Monitoring Program (NABat) met en place un effort conjoint de suivi des chauves-souris à l’échelle du continent, tant à l’échelle locale qu’à l’échelle de leur aire de répartition, afin d’obtenir des données fiables qui faciliteront la prise de décisions efficace concernant leur conservation. Un plan visant le North American Bat Monitoring Program a été publié en juin 2015 (Loeb et al., 2015).
- La North American Bat Conservation Alliance (NABCA) facilite la communication entre les organisations dédiées à la conservation des chauves-souris dans l’ensemble de l’Amérique du Nord, définit les priorités en matière de conservation et traite des questions liées à la conservation.
- Le Northeast Bat Working Group et le Western Bat Working Group permettent la mise en commun d’informations entre les organismes, les organisations, l’industrie et les individus intéressés par l’étude, la gestion et la conservation des chauves-souris, et facilitent la collaboration multi-États (Northeast Bat Working Group, 2015; Western Bat Working Group, 2015).
- La North American Society for Bat Research fait la promotion de la recherche et élabore des études sur les chauves-souris, et coordonne un symposium annuel nord-américain sur la recherche visant les chauves-souris (Northern American Symposium on Bat Research), (NASBR, 2015).
- Le Fish and Wildlife Service des États-Unis finance la recherche et coordonne chaque année la tenue d’un atelier ou d’une conférence sur le SMB qui rassemble des chercheurs du monde entier pour y présenter de nouveaux résultats et pour élaborer des stratégies de gestion.
Échelle nationale
- Les membres du Réseau canadien de la santé de la faune (RCSF) travaillent en collaboration avec les organismes fédéraux, provinciaux et territoriaux, et les organisations non gouvernementales à l’élaboration de protocoles de décontamination nationaux et à l’évaluation de produits, coordonnent le suivi des chauves-souris et du SMB à l’échelle nationale ainsi que le signalement en temps opportun de la maladie, et précisent les lacunes dans les connaissances et les besoins en matière de gestion des données au Canada. Le RCSF dirige le comité canadien interorganisationnel sur le syndrome du museau blanc dont font partie cinq groupes de travail technique. Le comité interorganisationnel a mis à jour un document intitulé A National Plan to Manage White Nose Syndrome in Bats in Canada (en anglais seulement) en février 2015, et il continuera probablement à jouer un rôle important dans la mise en œuvre des mesures visant à lutter contre le SMB à l’échelle nationale (Canadian Wildlife Health Cooperative, 2015a).
- Le RCSF, la NABCA et Environnement Canada travaillent actuellement à étendre la portée du Edubat Project au Canada afin d’accroître l’éducation et la sensibilisation du public à l’égard des chauves-souris (BatsLive, 2015).
- À l’échelle fédérale, provinciale et territoriale, la présence de chauves-souris est prise en considération dans le cadre des examens préalables et de la délivrance de permis relatifs aux projets d’aménagement des terres, et durant les évaluations environnementales partout au Canada. Des mesures d’atténuation sont mises en oeuvre au besoin pour limiter les effets nuisibles.
- Environnement Canada élabore des pratiques de gestion bénéfiques (PGB) à l’intention des secteurs de l’exploitation forestière, de l’énergie éolienne, de l’exploitation minière et de la gestion des espèces sauvages nuisibles, ainsi que pour la gestion des chauves-souris dans les bâtiments.
- Des chercheurs de l’Université de Winnipeg et de l’Université Trent étudient la réponse génétique des chauves-souris avant l’apparition du SMB et après l’apparition du SMB au Canada.
- La Fédération canadienne de la faune mène plusieurs activités de sensibilisation aux chauves-souris (Canadian Wildlife Federation, 2015). Elle a mis en place, par exemple, un programme de distribution de dortoirs à l’échelle du pays pour encourager les citoyens à faire un suivi de l'utilisation qu’en font les chauves-souris.
- Plusieurs parcs nationaux au Canada effectuent un suivi des chauves-souris à l’aide d’un protocole national qui a été élaboré par l’Agence Parcs Canada et participent aux activités du programme NABat.
- Avec l’appui du RCSF, l’Agence Parcs Canada a produit une vidéo pour illustrer l’utilisation de protocoles de décontamination et présenter des renseignements sur les chauves-souris et le SMB.
- Aux termes du Règlement général sur les parcs nationaux, les cavernes qui se trouvent dans le réseau des parcs nationaux du Canada sont fermées à moins que le directeur du parc n’en autorise expressément l’ouverture.
- L’Agence Parcs Canada a préparé une ébauche de lignes directrices visant les hibernacles ainsi que les chauves-souris qui occupent des sites de repos durant la période de reproduction.
Ouest et nord du Canada
- Le Western Canada Bat Network (WCBN) permet la mise en commun d’informations entre les groupes et les individus intéressés par l’étude, la gestion et la conservation des chauves-souris dans l’ouest du Canada, en Alaska, et dans certains États du nord-ouest des États-Unis, principalement au moyen d’un bulletin semestriel.
- En Colombie-Britannique, les Community Bat Programs of British Columbia font la promotion de la conservation des chauves-souris sur les terres privées, offrent des ressources aux propriétaires qui ont des problèmes avec les chauves-souris et font participer les scientifiques amateurs à la collecte de données sur les populations de chauves-souris. Ils réalisent également des dénombrements de l’émergence d’aires de repos dans des colonies de maternité pour établir des données de référence concernant l’abondance relative, à partir desquelles les futurs déclins pourront être mesurés (Community Bat Programs of BC, 2014).
- Les Community Bat Programs of BC ont élaboré des PGB en matière de techniques de lutte antiparasitaire et lancé des initiatives de sensibilisation avec des entreprises provinciales de lutte antiparasitaire (Community Bat Programs of BC, 2014).
- La British Columbia Bat Action Team, en collaboration avec le ministère de l’Environnement de la Colombie-Britannique, achève actuellement de définir les PGB concernant les activités spéléologiques et les industries minière et éolienne.
- L’activité des chauves-souris durant l’hiver fait l’objet d’un suivi dans tout le sud de la Colombie-Britannique par Mme Cori Lausen (Ph.D.) (Wildlife Conservation Society Canada), Environnement Canada-Service canadien de la faune, le ministère de l’Environnement de la Colombie-Britannique (Mme Purnima Govindarajulu) et d’autres organismes.
- Le ministère de l’Environnement de la Colombie-Britannique et Mme Cori Lausen ont élaboré des protocoles d’hygiène appropriés pour les chercheurs spécialistes des chauves-souris, les spéléologues et les autres personnes qui visitent les milieux souterrains occupés par les chauves-souris, ou qui y travaillent.
- Le ministère de l’Environnement de la Colombie-Britannique et le Musée royal de la Colombie-Britannique (Royal British Columbia Museum) archivent les données sur les mortalités accidentelles de chauves-souris et sur l’ADN des chauves-souris pour établir des données de base pour la Colombie-Britannique. Une évaluation sanitaire complète, y compris des tests visant à déceler le SMB, la rage et d’autres parasites est menée par la Dre Chelsea Himsworth (ministère de l’Agriculture de la Colombie-Britannique) sur toutes les carcasses de chauves-souris mortes accidentellement qui sont récupérées.
- Mme Cori Lausen dirige un projet de liaison (Bats and Cavers Project) avec la communauté de spéléologues de la Colombie-Britannique et de l’Alberta pour cartographier l’utilisation des grottes et d’autres milieux souterrains par les chauves-souris.
- Le ministère de l’Environnement et du Développement durable des ressources de l’Alberta a élaboré des lignes directrices pour réduire les impacts du développement de l’énergie éolienne sur les chauves-souris ainsi que des protocoles pour les relevés à effectuer avant et après la construction.
- L’Alberta Bat Action Team élabore des protocoles, détermine les priorités en matière de recherche et de gestion, et facilite le partage d’information.
- Le gouvernement du Yukon étudie la petite chauve-souris brune et la chauve-souris nordique afin de mieux rapporter leur occurrence, leur état reproducteur et leur aire de répartition au Yukon.
- Les gouvernements du Yukon et des Territoires du Nord-Ouest éduquent le public dans le cadre d’activités d’interprétation et par la publication de brochures.
- Le gouvernement du Yukon participe à divers projets de recherche, notamment à l’étude des effets des perturbations naturelles, de l’importance des forêts anciennes près des rives, et au suivi à long terme de certaines colonies de maternité.
- Le gouvernement des Territoires du Nord-Ouest rassemble des renseignements de base sur les chauves-souris de l’ensemble des Territoires du Nord-Ouest et cherche des hibernacles encore non découverts. En ce qui concerne les hibernacles connus, il assure un suivi du SMB et une surveillance des populations, et veille à la gestion de la planification.
- Divers partenaires (notamment le gouvernement des Territoires du Nord-Ouest, le Sahtu Renewable Resources Board, l’industrie, des chercheurs universitaires et des membres de la communauté) ont installé des enregistreurs acoustiques visant la détection des chauves-souris à plusieurs endroits dans les régions du Sahtu, du Dehcho, du South Slave et du North Slave des Territoires du Nord-Ouest pour en apprendre davantage sur la répartition et les habitudes des chauves-souris dans ces régions.
Centre du Canada
- Le ministère des Richesses naturelles et des Forêts de l’Ontario a élaboré des lignes directrices pour réduire au minimum les impacts des parcs éoliens sur les chauves-souris, et travaille en collaboration avec le ministère du Développement du Nord et des Mines et l’industrie minière pour réduire au minimum les perturbations industrielles pour les chauves-souris et leur habitat.
- Le guide d’aménagement forestier pour la conservation de la biodiversité à l’échelle du peuplement et du site du gouvernement de l’Ontario (en anglais seulement; Forest Management Guide for Conserving Biodiversity at the Stand and Sites Scales) comprend des directives visant à maintenir les habitats et les caractéristiques des habitats convenables, notamment les hibernacles (Ontario Ministry of Natural Resources, 2010).
- Le ministère des Richesses naturelles et des Forêts de l’Ontario a élaboré le Plan de lutte contre le syndrome du museau blanc de l’Ontario (Ontario Ministry of Natural Resources and Forestry, 2015).
- Le ministère des Richesses naturelles et des Forêts de l’Ontario assure un suivi acoustique des populations de chauves-souris durant l’été et l’hiver partout en Ontario.
- Le ministère des Forêts, de la Faune et des Parcs du Québec, en collaboration avec le Centre de la science de la biodiversité du Québec (CSBQ) et l’Université de Winnipeg, a créé un site Web (français : chauve-souris.ca, anglais : BatWatch) afin de promouvoir un projet de science citoyenne pour la surveillance des colonies de maternité dans le Centre du Canada (Québec, Ontario et Manitoba). Le site Web présente de la documentation sur les chauves-souris, leur conservation, et les PGB concernant les chauves-souris dans les immeubles. Il héberge en outre une base de données sur les colonies de maternité, dans laquelle les utilisateurs peuvent entrer une aire de repos et avoir accès aux dénombrements annuels.
- Environnement Canada a recueilli des données radar et acoustiques dans le sud de l’Ontario afin de déterminer si les chauves-souris migrent sur un large front ou si elles migrent en se concentrant le long de caractéristiques linéaires du paysage.
- Une surveillance estivale des populations effectuée par l’Université de Guelph (University of Guelph) et par Myotistar est en cours en Ontario.
- Myotistar et Gray Owl Environmental Inc. (avec l’appui d’Environnement Canada et de la National Speleological Society) suivent rigoureusement l’utilisation des aires de repos dans un nombre important d’aires de repos d’estivage, près de Cambridge, en Ontario, où les chauves-souris survivent et se reproduisent malgré la présence du SMB.
Est du Canada:
- Le ministère des Forêts, de la Faune et des Parcs du Québec continue à faire le suivi de la propagation du SMB et à surveiller les populations de chauves-souris durant l’été en menant des relevés acoustiques et des dénombrements des colonies de maternité. Un suivi plus intensif est prévu dans la région de la Côte-Nord, où le SMB n’a pas été détecté.
- Une équipe de rétablissement des chauves-souris du Québec a été mise sur pied en 2014. L’équipe élabore actuellement un plan de rétablissement pour la province et coordonne l’adoption des mesures de rétablissement à l’échelle de la province.
- Les populations de chauves-souris font l’objet d’une surveillance régulière par le ministère de la Défense nationale à la Base des Forces canadiennes Valcartier.
- L’Université St. Mary’s (St. Mary’s University) et Environnement Canada évaluent les concentrations de mercure chez la petite chauve-souris brune dans le Canada atlantique.
- Le Musée du Nouveau-Brunswick a suivi la propagation du SMB ainsi que le taux de mortalité qui y est associé dans les hibernacles connus de toute la province durant des années précédant et suivant la propagation du SMB, et il continue de réaliser des recherches sur l’omniprésence du pathogène, la microfaune des grottes et les conditions environnementales.
- Le Musée du Nouveau-Brunswick, en collaboration avec le ministère des Ressources naturelles du Nouveau-Brunswick, a établi un programme de communication des observations afin de recueillir des données sur les chauves-souris en vol durant le jour en hiver, et d’obtenir ainsi de nouveaux renseignements sur la répartition des trois espèces dans la province.
- Le ministère des Ressources naturelles du Nouveau-Brunswick a élaboré des lignes directrices concernant les relevés sur la mortalité des chauves-souris et des oiseaux avant et après la construction de parcs éoliens au Nouveau-Brunswick.
- La Forest, Fish and Wildlife Division de l’Île-du-Prince-Édouard encourage le signalement des observations de chauves-souris et travaille avec le Réseau canadien de la santé de la faune à mettre en œuvre les programmes de surveillance des chauves-souris.
- Le programme Nova Scotia Bat Conservation du Department of Natural Resources de la Nouvelle-Écosse fait un suivi des chauves-souris durant le printemps, l’été et l’automne.
- L’Université St. Mary’s effectue un suivi des dénombrements durant l’hiver aux hibernacles, en Nouvelle-Écosse.
- L’Université St. Mary’s étudie les populations de petites chauves-souris brunes ainsi que le comportement social de l’espèce, en collaboration avec le Department of Environment and Conservation de Terre-Neuve-et-Labrador, dans la province.
- Le gouvernement de Terre-Neuve-et-Labrador poursuit sa surveillance du SMB et effectue le suivi des populations connues. En collaboration avec la Memorial University of Newfoundland et Parcs Canada, le suivi acoustique est effectué pour déterminer la présence des espèces et leur abondance. Des relevés visant la petite chauve-souris brune et la chauve-souris nordique au Labrador sont réalisés afin de mieux étayer les données sur leur occurrence, leur état reproducteur et leur aire de répartition.
6.2. Commentaires à l’appui du tableau de planification du rétablissement
Le Réseau canadien de la santé de la faune (comité canadien interorganisationnel sur le syndrome du museau blanc) a publié une version révisée du document intitulé A National Plan to Manage White Nose Syndrome in Bats in Canada (en anglais seulement) en février 2015 (Canadian Wildlife Health Cooperative, 2015b). Dans la mesure du possible, les approches présentées au tableau 3 ont été établies de manière à s’harmoniser avec les initiatives décrites dans ce plan. Lorsque cela était approprié, les approches ont été classées selon qu’elles sont applicables aux régions non touchées par le SMB ou aux régions touchées par le SMB (et au front de propagation).
| Menace ou élément limitatif | Stratégie générale pour le rétablissement | PrioritéNoteeof Table 3 | Description générale des approches de recherche et de gestion |
|---|---|---|---|
| Lacunes à combler dans les connaissances en vue du rétablissement | Suivi et relevés | Élevée | Ensemble de l’aire de répartition
|
| Lacunes à combler dans les connaissances en vue du rétablissement | Suivi et relevés | Moyenne |
|
| - | - | Basse | Effectuer le suivi des tendances des proies des chauves-souris dans toute leur aire de répartition canadienne. |
| Lacunes à combler dans les connaissances en vue du rétablissement et toutes les menaces | Recherche | Élevée | Ensemble de l’aire de répartition
Régions touchées par le SMB (et front de propagation)
Régions non touchées par le SMB
|
| Lacunes à combler dans les connaissances en vue du rétablissement et toutes les menaces | Recherche | Moyenne |
|
| Lacunes à combler dans les connaissances en vue du rétablissement et toutes les menaces | Éducation et sensibilisation, et partenariats | Élevée |
|
| Toutes les menaces | Conservation et gestion des espèces et de leur habitat | Élevée | Ensemble de l’aire de répartition
Régions touchées par le SMB (et front de propagation)
Régions non touchées par le SMB
|
| Toutes les menaces | Conservation et gestion des espèces et de leur habitat | Moyenne |
Régions non touchées par le SMB
|
| Toutes les menaces | Lois et politiques | Élevée |
|
6.3. Commentaires à l’appui du tableau de planification du rétablissement
Le rétablissement de la petite chauve-souris brune, de la chauve-souris nordique et de la pipistrelle de l’Est exigera un engagement, des ressources, une collaboration et une coopération de la part des compétences fédérales, provinciales et territoriales, des conseils de gestion des ressources fauniques, des peuples autochtones, des experts et des chercheurs spécialistes des espèces, des collectivités locales, des propriétaires fonciers, des divers secteurs industriels et des autres parties intéressées du Canada et des États-Unis. Étant donné la vaste aire de répartition des espèces dans tout le pays, il sera important de surveiller la propagation du SMB, des hibernacles, des colonies de maternité, des tendances des populations et de la répartition des trois espèces de chauves-souris de sorte que l’efficacité des activités de rétablissement puisse être évaluée et améliorée, au besoin.
Il faudra adopter une approche globale de recherche et de suivi (couvrant tous les stades du cycle vital annuel des espèces et l’ensemble de la zone d’occurrence) pour mieux comprendre la situation de chaque espèce ainsi que les facteurs limitatifs, les menaces importantes et l’utilisation de l’habitat par chacune des espèces. À l’heure actuelle, il n’existe pas d’estimations fiables des populations de l’une ou l’autre des trois espèces de chauves-souris, et il n’est pas réaliste de s’attendre à ce que des estimations des populations soient produites à court terme. Si l’on veut juger de la réussite des mesures de conservation et de gestion et déterminer si les objectifs en matière de population et de répartition sont atteints, il faudra mettre en place un programme de suivi efficace pour mesurer les changements relatifs dans l’abondance des chauves-souris dans le temps. Afin d’assurer une certaine uniformité quant à la méthode d’échantillonnage dans tout le pays, il faudrait utiliser, dans la mesure du possible, le protocole du North American Bat Monitoring Program (NABat) comme cadre d’échantillonnage national canadien (Loeb et al., 2015).
Étant donné la vitesse à laquelle le SMB se propage au Canada, il faut mener rapidement et de manière efficiente des activités de recherche et de suivi du champignon pour ne rater aucune possibilité. Il faudra probablement faire appel à un grand nombre de chercheurs, de gouvernements, de secteurs industriels, de collectivités autochtones et de volontaires pour coordonner les activités, communiquer efficacement les résultats, mettre en commun les ressources et partager les conclusions de manière efficiente (Langwig et al., 2015a). Dans la mesure du possible, les activités et priorités en matière de recherche devront être coordonnées par des groupes établis (p. ex. North American Bat Conservation Alliance et RCSF) afin d’éviter le dédoublement des activités et le double emploi des ressources. Si on veut réussir à empêcher la propagation du SMB (voir la section 5 : Objectifs en matière de population et de répartition), il faudra continuer de mener des recherches afin de trouver un traitement des individus et/ou des hibernacles infectés par le SMB ou des méthodes visant à réduire considérablement la propagation de P. destructans ou à la prévenir.
Comme il a été mentionné à la section portant sur les menaces (section 4 : Menaces), dans les régions où les populations de chauves-souris locales ont connu un grave déclin à cause du SMB, le niveau de préoccupation quant à toute autre menace potentielle est accru (Langwig et al., 2015a). Il devient de plus en plus important de connaître l’importance et les facteurs de risque associés aux menaces pesant sur chacune des trois espèces de chauves-souris (voir l’annexe B), de manière à ce que les mesures d’atténuation appropriées soient adoptées en temps opportun.
Tandis que les activités de suivi et de recherche nécessaires sont menées en Amérique du Nord, les données scientifiques disponibles peuvent fournir une base de connaissances permettant de conserver les habitats connus et d’atténuer les menaces pesant sur les espèces.
7. Habitat essentiel
L’habitat essentiel est l’habitat nécessaire à la survie ou au rétablissement d’une espèce. En vertu de l’alinéa 41(1)c) de la LEP, les programmes de rétablissement doivent inclure une désignation de l’habitat essentiel de l’espèce, dans la mesure du possible, et des exemples d’activités susceptibles d’entraîner la destruction de cet habitat.
7.1. Désignation de l’habitat essentiel de l’espèce
La désignation de l’habitat essentiel dans le présent document est jugée partielle et insuffisante pour satisfaire les objectifs en matière de population et de répartition. Un calendrier des études requises pour obtenir les données nécessaires à l’achèvement de la désignation de l’habitat essentiel a été établi (voir la section 7.2 : Calendrier des études visant à désigner l’habitat essentiel). Dans le présent programme de rétablissement, l’habitat essentiel est partiellement désigné pour les hibernacles selon les meilleures données accessibles pour chaque espèce en date d’octobre 2015.
Hibernacles
La petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est utilisent des hibernacles pour survivre lorsque la température ambiante baisse et que les insectes ne sont pas accessibles. Les hibernacles sont donc nécessaires à la survie et au rétablissement de ces espèces. Les hibernacles convenables pourraient être limitatifs pour ces espèces (OMNR, 2010).
En raison de préoccupations relatives à la sécurité des personnes, des mesures visant à réduire au minimum la perturbation des chauves-souris et de la difficulté de trouver des chauves-souris hibernantes dans des structures complexes, il est souvent impossible de dénombrer l’ensemble des chauves-souris qui utilisent un hibernacle. En outre, la découverte d’un individu hibernant peut parfois indiquer la présence d’autres individus non détectés qui utilisent l’hibernacle.
Occupation
- Tout site où a été observée une petite chauve-souris brune, une chauve-souris nordique ou une pipistrelle de l’Est en hibernation durant l’hiver au moins une fois depuis 1995 est désigné habitat essentiel.
La période (≥ 1995) reconnaît que la petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est font preuve d’une grande fidélité à l’égard des hibernacles, que certains sites individuels pourraient être utilisés par des chauves-souris hibernantes pendant des décennies, et que les hibernacles convenables pourraient être limitatifs.
Aux sites où il y avait un habitat d’hibernation adéquat, mais où il a été impossible de vérifier que des chauves-souris y hibernaient bel et bien (p. ex. l'endroit était inaccessible ou qu’on évitait d’y entrer pour déranger le moins possible les chauves-souris), le rassemblement (une activité qui se produit normalement à proximité ou à l’intérieur d’un hibernacle) a été considéré comme un indicateur de l’utilisation d’un site pour l’hibernation. Par conséquent, ces sites de rassemblement ont été inclus dans la désignation de l’habitat essentiel.
Les sites jugés contenir de l’habitat non convenable (p. ex. l’habitat convenable n’existe plus, ou encore où les chauves-souris en hibernation n’ont pas survécu à l’hiver) n’ont pas été désignés comme habitat essentiel; ces sites ne comprenaient pas de sites touchés par le SMB. La persistance à long terme du pathogène responsable du SMB, P. destructans, dans les hibernacles influe sur le caractère convenable des grottes et des mines pour maintenir des populations de chauves-souris autosuffisantes et résilientes. Néanmoins, les hibernacles touchés par le SMB sont considérés comme de l’habitat essentiel parce qu’ils ne doivent ni disparaître ni être modifiés pour aider le rétablissement des populations dans l’éventualité qu’un traitement ou que des mesures de décontamination soient découverts, ou que les espèces développent une résistance naturelle à la maladie.
Les connaissances sont limitées en ce qui concerne l’importance des associations d’habitats, leur configuration autour des hibernacles et l’échelle géographique à laquelle leurs effets se font sentir, le cas échéant, sur la prévisibilité de l’occurrence des chauves-souris dans ces sites. À l’heure actuelle, les connaissances liées à l’emplacement des hibernacles sont également limitées dans l’ensemble de l’aire de répartition de ces espèces de chauves-souris. De plus, les difficultés liées à la confirmation de l’identification des petites chauves-souris brunes dans les régions de la Colombie-Britannique où la chauve-souris Yumaest également présente limitent la capacité de confirmer l’utilisation des hibernacles par cette espèce. Il est nécessaire de combler les lacunes dans les connaissances pour achever la désignation de l’habitat essentiel en ce qui concerne les hibernacles, et ces lacunes seront abordées dans le cadre de l’achèvement du calendrier des études (section 7.2).
Caractéristiques biophysiques
- Les hibernacles des trois espèces sont habituellement souterrains, p. ex. des grottes, des mines abandonnées, des puits creusés à la main, des caves ou des tunnels où le degré de luminosité et le niveau sonore sont faibles.
- Les hibernacles comprennent généralement des sections où la température est relativement stable (de 2 à 10 ˚C) et où le taux d’humidité est élevé et stable (> 80 %).
Un seul hibernacle peut comprendre plusieurs entrées et sorties ainsi que de vastes réseaux souterrains de galeries. Ces éléments font tous partie de la définition d’un hibernacle en tant qu’habitat essentiel (peu importe où les chauves-souris hibernantes se trouvent dans la structure), car 1) les individus peuvent utiliser plusieurs zones dans la structure, et il n’est pas toujours possible de déterminer leur utilisation, et 2) le réseau doit généralement rester entier et intact pour maintenir les conditions microclimatiques (p. ex. circulation d’air, température et humidité).
Les sites utilisés pour l’hibernation dans l’ouest du Canada, en particulier le long de la côte du Pacifique, peuvent être très différents de ceux utilisés ailleurs dans les aires de répartition des espèces au Canada, et notre connaissance de l’emplacement et des caractéristiques biophysiques de ces hibernacles est très limitée (Jung et al., 2014). Les chauves-souris vivant dans certaines régions de la Colombie-Britannique peuvent employer des stratégies différentes pour survivre durant l’hiver. On dispose de peu de renseignements sur les habitudes hivernales et la façon dont les chauves-souris utilisent les sites d’hivernage dans ces régions. Ces lacunes dans les connaissances sont abordées dans le calendrier des études (section 7.2). Le fait de combler ces lacunes permettra d’achever la désignation de l’habitat essentiel en ce qui concerne les hibernacles dans ces régions.
Emplacements géographiques
Les zones renfermant de l’habitat essentiel de la petite chauve-souris brune, de la chauve-souris nordique et de la pipistrelle de l’Est sont présentées aux figures 4 à 20. L’habitat essentiel se trouve dans des quadrillages UTM de référence là où les critères d’habitat essentiel (occupation et caractéristiques biophysiques) décrits dans la présente section sont respectés. L’habitat essentiel est présenté sous forme de quadrillages UTM qui représentent toutes les espèces présentes dans une province ou un territoire en particulier, et l’habitat essentiel désigné peut inclure une ou plusieurs des espèces concernées. Les carrés du quadrillage UTM présentés dans ces figures font partie d’un système de quadrillage national de référence qui indique la zone géographique générale renfermant de l’habitat essentiel. L’habitat essentiel est présenté à l’intérieur des quadrillages UTM de référence afin de respecter les protocoles provinciaux et territoriaux d’utilisation des données sur les espèces en péril (et les ententes connexes) et de protéger les espèces et leur habitat des perturbations et de l’introduction potentielle du SMB. La taille du quadrillage utilisée pour montrer l’habitat essentiel (c.-à-d. 10, 50 ou 100 km2) est liée à la capacité et aux risques de découvrir l’emplacement de l’habitat essentiel (tel que le perçoivent les propriétaires des données). Il est possible d’obtenir des renseignements supplémentaires sur l’emplacement de l’habitat essentiel pour soutenir la protection de l’espèce et de son habitat, sur justification, en communiquant avec la section responsable de la planification du rétablissement d’Environnement Canada, à l’adresse: ec.planificationduretablissement-recoveryplanning.ec@canada.ca.
Au total, 192 hibernacles ont été désignés comme habitat essentiel à Terre-Neuve-et-Labrador, en Nouvelle-Écosse, au Nouveau-Brunswick, au Québec, en Ontario, au Manitoba, en Alberta, en Colombie-Britannique, et dans les Territoires du Nord-Ouest, d’après les données d’octobre 2015. L’emplacement des hibernacles au Yukon, en Saskatchewan et au Nunavut n’est pas connu. Il n’y a pas de données sur l’emplacement des hibernacles à l’Île-du-Prince-Édouard en raison de questions liées à la vie privée touchant les propriétaires fonciers.
Colonies de maternité
Les colonies de maternité sont utilisées pour mettre bas et élever les petits et contribuent clairement à la survie et au rétablissement des trois espèces de chauves-souris. Toutefois, les emplacements de la vaste majorité des colonies de maternité sont actuellement inconnus ou non documentés, ou encore Environnement Canada n’a pas accès aux données à cet égard. Par conséquent, il n’est pas possible de déterminer quelles colonies de maternité sont nécessaires à la survie ou au rétablissement des espèces, de sorte que les colonies de maternité ne sont pas désignées comme habitat essentiel dans le présent programme de rétablissement.
Une fois que d’autres données sur les emplacements et les caractéristiques des colonies de maternité seront disponibles, il sera possible d’établir des critères pour déterminer les colonies de maternité qui sont nécessaires à la survie ou au rétablissement des espèces comme habitat essentiel. Les critères visant à déterminer les colonies de maternité qui sont de l’habitat essentiel tiendraient sans doute compte de l’espèce, du nombre d’individus utilisant la colonie, de la présence ou non de la colonie dans une région touchée par le SMB et du nombre d’autres colonies de maternité connues dans les environs.
Les travaux requis pour obtenir les données nécessaires et établir les critères relatifs à la désignation de colonies de maternité comme habitat essentiel sont indiqués dans le calendrier des études (section 7.2).
Comme pour les hibernacles, les connaissances sur l’emplacement et les caractéristiques biophysiques des colonies de maternité dans l’ouest du Canada sont très limitées, et les caractéristiques de l’habitat peuvent différer grandement de celles que l’on observe ailleurs dans l’aire de répartition canadienne des espèces (Jung et al., 2014). Ces lacunes dans les connaissances doivent être comblées pour achever la désignation de l’habitat essentiel pour les colonies de maternité et seront abordées dans le cadre de l’achèvement du calendrier des études (section 7.2).
Désignation à l’échelle du paysage
L’aire de répartition géographique des espèces, les menaces qui pèsent sur elles et la spécificité de l’habitat de la petite chauve-souris brune (et possiblement de la chauve-souris nordique) semblent indiquer que l’habitat essentiel associé à l’habitat d’estivage (c.-à-d. aires de repos et d’alimentation) devrait éventuellement être désigné à l’échelle du paysage. Cela permettrait la gestion à long terme de l’habitat nécessaire à la survie et au rétablissement des espèces. Ce type de désignation refléterait la mosaïque dynamique de conditions de l’habitat qui sont disponibles et requises dans le paysage. Néanmoins, l’information accessible n’est pas adéquate pour désigner actuellement l’habitat essentiel à l’échelle du paysage, pour les raisons suivantes :
- Il y a un manque de données sur la présence et l’abondance des chauves-souris dans de grandes parties de leurs aires de répartition.
- Les besoins en matière d’habitat peuvent varier dans l’ensemble des aires de répartition des espèces. Des unités de gestion (c.-à-d. unités géographiques dans lesquelles l’habitat essentiel serait géré) doivent être établies de manière à refléter le plus possible les variations de l’utilisation de l’habitat et les régimes de gestion.
- Il y a un manque de compréhension et de données pour indiquer la configuration appropriée des caractéristiques biophysiques importantes.
- Il n’est pas clair si certains milieux d’estivage présentant des caractéristiques biophysiques spécifiques conviennent mieux à l’espèce que d’autres sur le plan fonctionnel. Par exemple, certains milieux pourraient abriter de plus fortes densités d’individus et/ou favoriser le succès de reproduction.
- Les relations entre les perturbations causées par l’activité humaine et la qualité de l’habitat sont mal connues. Il est nécessaire de mieux comprendre ces relations pour pouvoir s’assurer qu’une quantité suffisante d’habitat convenable est disponible pour ces espèces et déterminer les seuils d’étendue et d’intensité à partir desquels les activités humaines deviendraient susceptibles d’entraîner la destruction de l’habitat essentiel.
Il faudra de nombreuses années pour recueillir suffisamment de données afin de combler les lacunes énumérées ci-dessus. Par conséquent, un calendrier des études à long terme est présenté à la section 7.2 pour aborder la question de la désignation de l’habitat d’estivage à l’échelle du paysage.
Autres habitats
À l’heure actuelle, les sites de repos des mâles, les voies migratoires et les sites de rassemblement ne sont pas désignés comme habitat essentiel. En effet, il n’est pas clair si l’habitat de repos des mâles ou les voies migratoires sont nécessaires à la survie ou au rétablissement de chaque espèce. Pour le moment, les connaissances sur les besoins en matière d’habitat sur lesquels repose le choix des importants sites de rassemblement sont insuffisantes pour déterminer les caractéristiques biophysiques de ces sites. La détermination à savoir si les sites de repos des mâles et les voies migratoires doivent être désignés comme habitat essentiel et des études sur l’importance et les caractéristiques biophysiques des sites de rassemblement sont incluses dans le calendrier des études (section 7.2).
En résumé, l’habitat essentiel de la petite chauve-souris brune, de la chauve-souris nordique et de la pipistrelle de l’Est peut être désigné partiellement à l’heure actuelle. Un calendrier des études a été établi afin d’obtenir les données nécessaires pour achever la désignation de l’habitat essentiel nécessaire à l’atteinte des objectifs en matière de population et de répartition. Même si le calendrier des études à court terme s’étend sur 10 ans, la désignation de l’habitat essentiel pourra être mise à jour au fur et à mesure que de nouvelles données deviendront disponibles, soit dans un programme de rétablissement révisé, soit dans un ou plusieurs plans d’action.
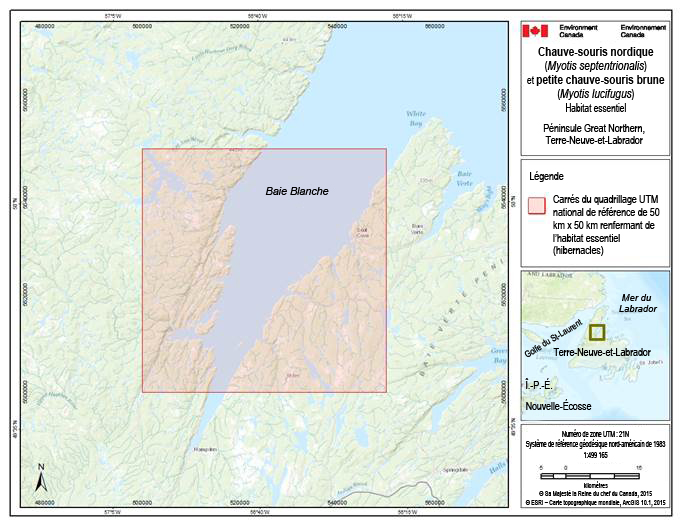
Description longue pour la figure 4
Carré du quadrillage d’une grille universelle transverse de Mercator (UTM) normalisée (bordure rouge et remplissage semi-transparent), à une résolution de 50 x 50, renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus) et de la chauve-souris nordique (Myotis septentrionalis) à Terre-Neuve-et-Labrador. Le carré du quadrillage couvre les portions est et ouest de la baie White de l’île de Terre-Neuve. Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel, mais la carte à une résolution plus fine n’est pas montrée. L’habitat essentiel de ces espèces se trouve dans ce carré du quadrillage UTM, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés).
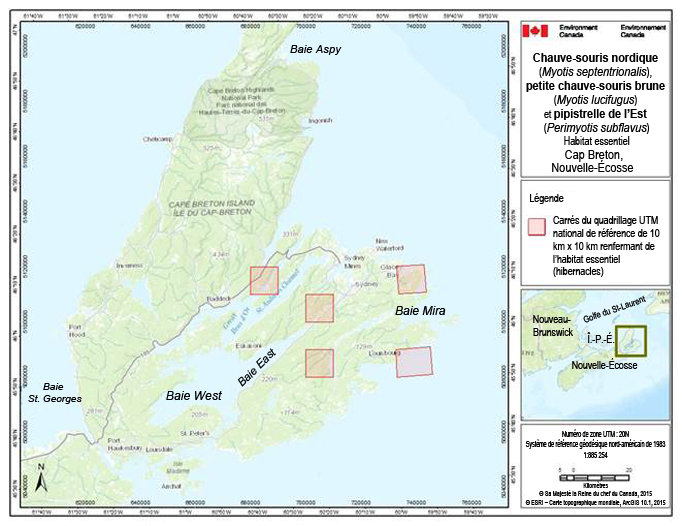
Description longue pour la figure 5
Carrés du quadrillage (bordure rouge et remplissage semi-transparent) renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus), de la chauve-souris nordique (Myotis septentrionalis) et de la pipistrelle de l’Est (Perimyotis subflavus) dans le nord de la Nouvelle-Écosse et sur l’île du Cap Breton. L’habitat essentiel de ces espèces se trouve dans le carré du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Les carrés du quadrillage UTM de référence se trouvant à l’intersection de zones UTM sont fusionnés avec les carrés adjacents. Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée. Les (quatre) carrés du quadrillage englobant l’habitat essentiel de ces espèces sont situés dans le sud-est de l’île du Cap Breton et au nord du chenal Saint Andrews (un carré).
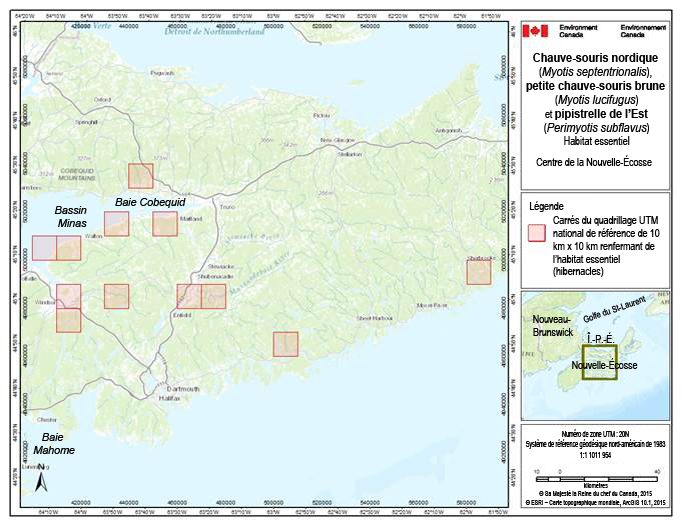
Description longue pour la figure 6
Carrés du quadrillage (douze) (bordure rouge et remplissage semi-transparent) renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus), de la chauve-souris nordique (Myotis septentrionalis) et de la pipistrelle de l’Est (Perimyotis subflavus) dans le centre et dans la partie continentale de la Nouvelle-Écosse. L’habitat essentiel de ces espèces se trouve dans les carrés du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée. La plupart des carrés du quadrillage (dix) englobant de l’habitat essentiel se trouvent dans la portion est de la partie continentale de la Nouvelle-Écose, au sud de la baie Minas, et au nord et au sud de la baie Cobequid, de même qu’au nord d’Enfield. Des carrés isolés se trouvent également dans le centre-sud de la côte de la partie continentale, et au sud de Sherbrooke.

Description longue pour la figure 7
Carrés du quadrillage (deux) (bordure rouge et remplissage semi-transparent) renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus), de la chauve-souris nordique (Myotis septentrionalis) et de la pipistrelle de l’Est (Perimyotis subflavus) dans la vallée d’Annapolis, dans la partie continentale de la Nouvelle-Écosse. L’habitat essentiel de ces espèces se trouve dans les carrés du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée. Un carré du quadrillage se trouve au nord de Middelton, et un autre, au sud de Middleton.
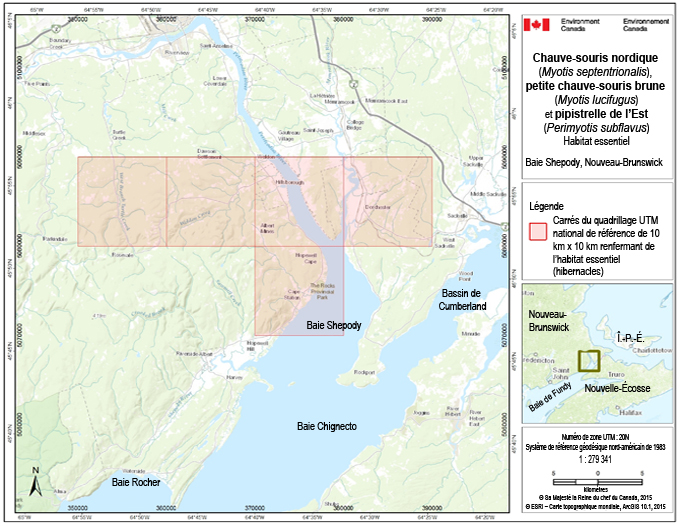
Description longue pour la figure 8
Carrés du quadrillage renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus), de la chauve-souris nordique (Myotis septentrionalis) et de la pipistrelle de l’Est (Perimyotis subflavus) au Nouveau-Brunswick (région de la baie Shepody). L’habitat essentiel de ces espèces se trouve dans les carrés du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée. Les carrés du quadrillage renfermant de l’habitat essentiel sont continus depuis l’embouchure de la baie Shepody, et d’ouest en est, de Peticodiac à Dorchester.
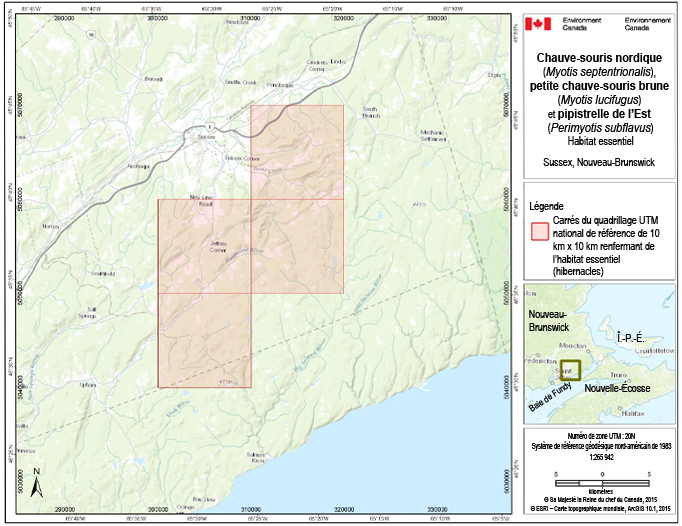
Description longue pour la figure 9
Carrés du quadrillage (cinq) renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus), de la chauve-souris nordique (Myotis septentrionalis) et de la pipistrelle de l’Est (Perimyotis subflavus) dans le sud-est du Nouveau-Brunswick (région de Sussex). L’habitat essentiel de ces espèces se trouve dans les carrés du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée. Les carrés du quadrillage renfermant de l’habitat essentiel englobent une zone au sud de Jeffries Corner, le long de la rivière Hammond, et une zone à l’est de Sussex Corner, le long de la rivière Trout.

Description longue pour la figure 10
Carré du quadrillage (bordure rouge et remplissage semi-transparent) renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus), de la chauve-souris nordique (Myotis septentrionalis) et de la pipistrelle de l’Est (Perimyotis subflavus) dans le centre-sud du Nouveau-Brunswick, et englobant la grande région de Saint John, la région de Grand Bay-Westfield, et la portion sud de la péninsule de Kingston. L’habitat essentiel de ces espèces se trouve dans ce carré du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée. Les carrés du quadrillage UTM de référence se trouvant à l’intersection de zones UTM sont fusionnés avec les carrés adjacents.
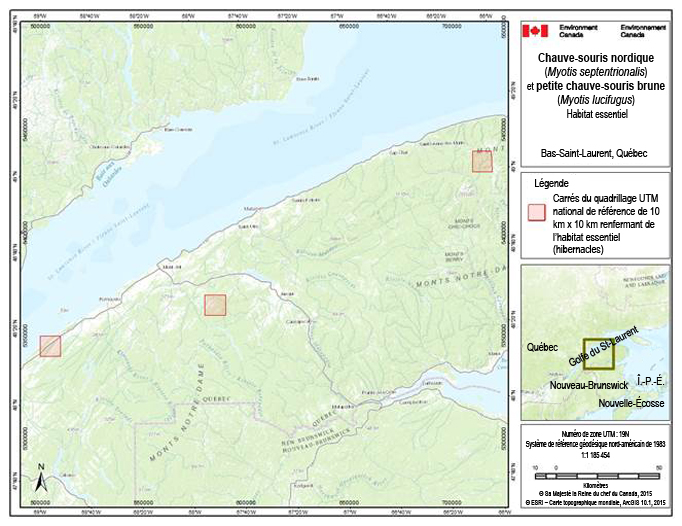
Description longue pour la figure 11
Carrés du quadrillage renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus) et de la chauve-souris nordique (Myotis septentrionalis) au Québec, le long de la rive sud de l’embouchure du fleuve Saint-Laurent (région du Bas-Saint-Laurent). Les emplacements des carrés du quadrillage renfermant de l’habitat essentiel sont isolés et discontinus les uns par rapport aux autres. L’habitat essentiel de ces espèces se trouve dans les carrés du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée.

Description longue pour la figure 12
Carrés du quadrillage renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus), de la chauve-souris nordique (Myotis septentrionalis) et de la pipistrelle de l’Est (Perimyotis subflavus) au Québec (région des Cantons de l’Est). Les carrés du quadrillage renfermant de l’habitat essentiel sont largement dispersés dans la région, et trois carrés représentent des zones géographiques adjacentes où de l’habitat essentiel a été désigné. L’habitat essentiel de ces espèces se trouve dans les carrés du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée.
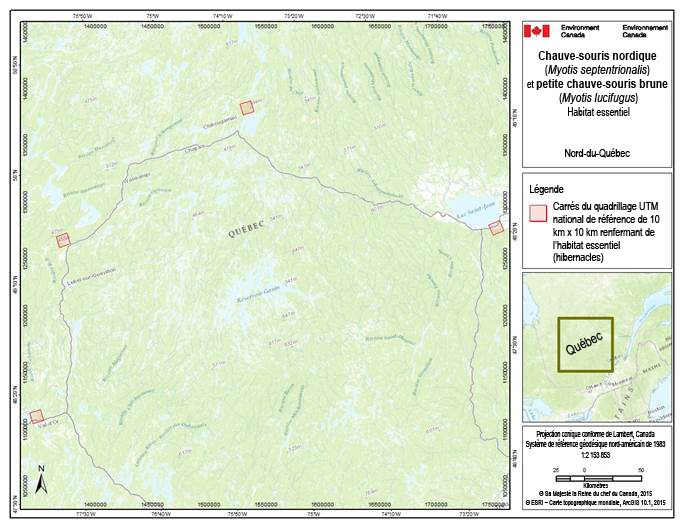
Description longue pour la figure 13
Carrés du quadrillage renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus) et de la chauve-souris nordique (Myotis septentrionalis) au Québec (région du Nord-du-Québec). Les carrés du quadrillage renfermant de l’habitat essentiel sont très dispersés dans le nord du Québec, et sont situés près de Val-d’Or, au nord de Lebel-sur-Quevillon, à l’est de Chibougamau, et au sud-est du lac Saint-Jean. L’habitat essentiel de ces espèces se trouve dans les carrés du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée.
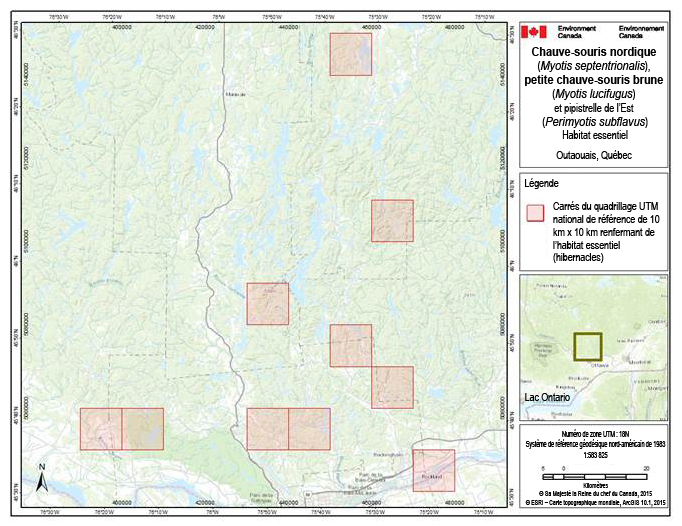
Description longue pour la figure 14
Carrés du quadrillage (dix) (bordure rouge et remplissage semi-transparent) renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus), de la chauve-souris nordique (Myotis septentrionalis) et de la pipistrelle de l’Est (Perimyotis subflavus) au Québec (région de l’Outaouais). Les carrés du quadrillage renfermant de l’habitat essentiel sont principalement situés dans le sud et l’est de l’Outaouais, et leur dispersion est modérée dans la portion sud, et plus grande dans la portion nord. L’habitat essentiel de ces espèces se trouve dans les carrés du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée.
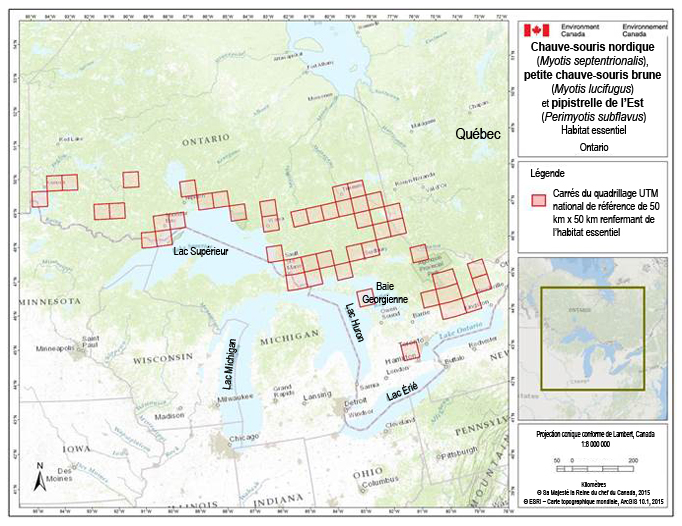
Description longue pour la figure 15
Carrés du quadrillage (47) (bordure rouge et remplissage semi-transparent) renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus), de la chauve-souris nordique (Myotis septentrionalis) et de la pipistrelle de l’Est (Perimyotis subflavus) en Ontario. Les carrés du quadrillage renfermant de l’habitat essentiel sont largement distribués dans le sud de la forêt boréale en Ontario, et sont fortement concentrés dans le nord-est de l’Ontario, le long de la frontière du Québec, sur la rive nord du lac Huron, et dans le centre de la vallée de l’Outaouais-parc Algonquin, et un carré isolé se trouve dans le sud de l’Ontario, entre le lac Érié et le lac Ontario. L’habitat essentiel de ces espèces se trouve dans les carrés du quadrillage UTM de référence de 50 km x 50 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée. Les carrés du quadrillage UTM de référence se trouvant à l’intersection de zones UTM sont fusionnés avec les carrés adjacents.
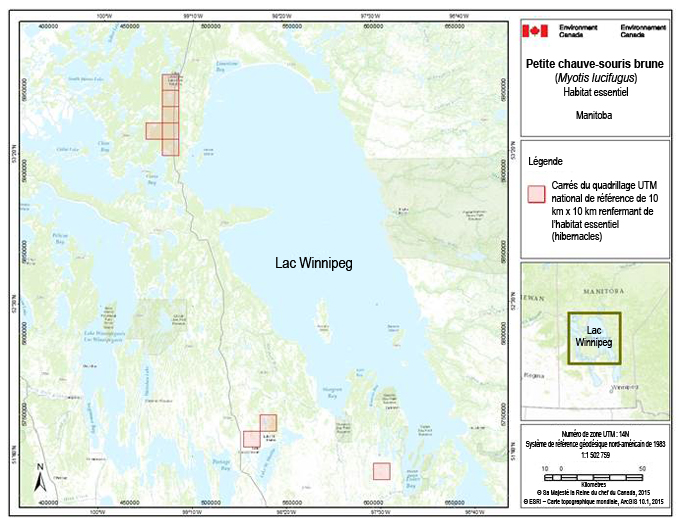
Description longue pour la figure 16
Carrés du quadrillage (9) (bordure rouge et remplissage semi-transparent) renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus) au Manitoba. Les carrés du quadrillage renfermant de l’habitat essentiel sont très concentrés au nord-ouest du lac Winnipeg, au nord de Grand Rapids, et des carrés plus isolés se trouvent au nord du lac St. Martin et à l’ouest de la baie Fisher. L’habitat essentiel de cette espèce se trouve dans les carrés du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée.
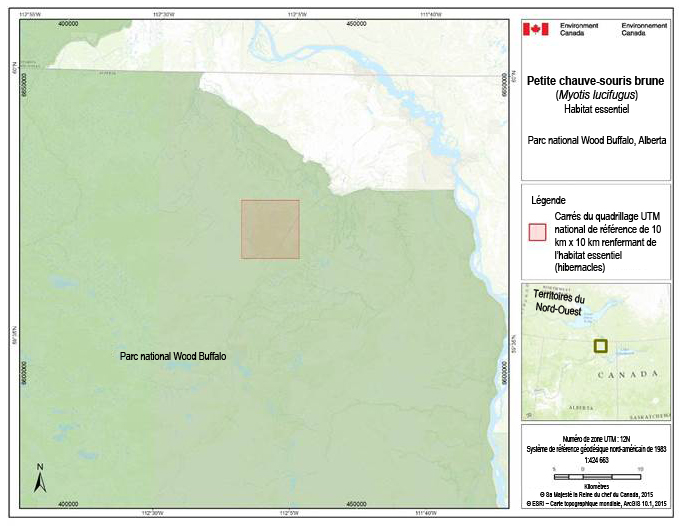
Description longue pour la figure 17
Carrés de grille renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus) en Alberta (région du parc national Wood Buffalo). L’habitat essentiel est cartographié dans un carré unique isolé se trouvant dans la portion nord-est du parc national Buffalo Wood. L’habitat essentiel de cette espèce se trouve dans ce carré du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée.
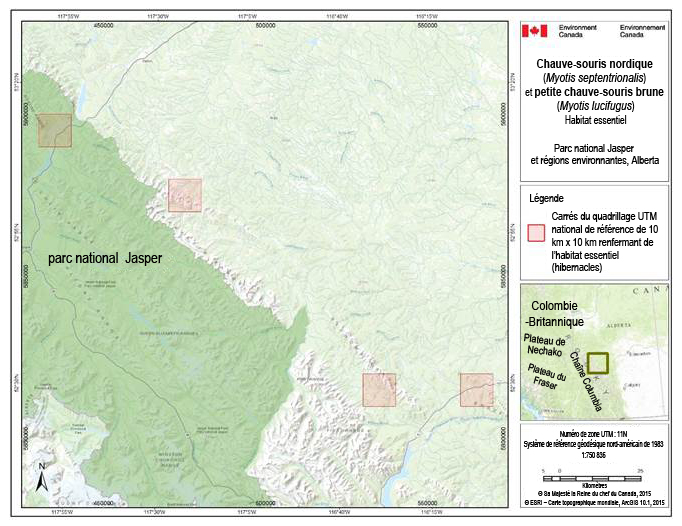
Description longue pour la figure 18
Carrés du quadrillage (4) (bordure rouge et remplissage semi-transparent) renfermant de l’habitat essentiel de la chauve-souris nordique (Myotis septentrionalis) et de la petite chauve-souris brune (Myotis lucifugus) en Alberta (région du parc national Jasper et environs). Les carrés du quadrillage renfermant l’habitat essentiel sont largement dispersés le long de la limite est du parc national Jasper, et se trouvent notamment à des emplacements près de Pochahontas, au nord de Mountain Park, et dans des emplacements plus au sud-est, le long de la chaîne de montagnes Bighorn et près de Nordegg. L’habitat essentiel de ces espèces se trouve dans ces carrés du quadrillage UTM de référence de 10 km x 10 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée.
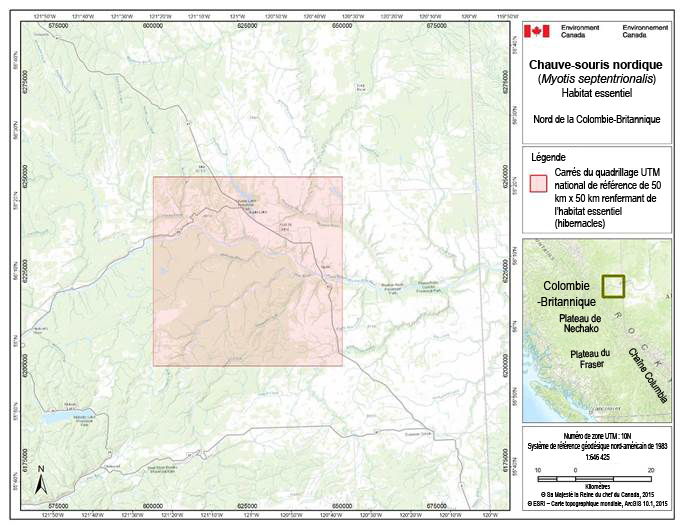
Description longue pour la figure 19
Carré du quadrillage (bordure rouge et remplissage semi-transparent) renfermant de l’habitat essentiel de la chauve-souris nordique (Myotis septentrionalis) dans le nord-est de la Colombie-Britannique. La zone délimitée par l’habitat essentiel englobe une région au sud-ouest de Fort St. John. L’habitat essentiel de cette espèce se trouve dans ce carré du quadrillage UTM de référence de 50 km x 50 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée.
Description longue pour la figure 20
Carré du quadrillage renfermant de l’habitat essentiel de la petite chauve-souris brune (Myotis lucifugus) dans les Territoires du Nord-Ouest. L’habitat essentiel de cette espèce se trouve dans ce carré du quadrillage UTM de référence de 100 km x 100 km, là où la description de l’habitat essentiel est respectée (c.-à-d. les hibernacles ont été désignés). Ce système de quadrillage national de référence indique la zone géographique renfermant de l’habitat essentiel; la carte détaillée de l’habitat essentiel n’est pas montrée.
7.2 Calendrier des études visant à désigner l’habitat essentiel
Un calendrier des études a été élaboré afin de fournir l’information nécessaire pour compléter la désignation de l’habitat essentiel (tableaux 4 et 5).
| Description de l’activité | Justification | Échéancier |
|---|---|---|
| Collaborer avec les chercheurs, les provinces/territoires, les collectivités autochtones et les organisations non gouvernementales afin de rendre disponibles les données sensibles et les utiliser pour la désignation de l’habitat essentiel. | Le manque de données disponibles (particulièrement sur les structures construites par les humains) constitue un obstacle majeur à la désignation de l’habitat essentiel. | 2016-2017 |
| Effectuer des relevés dans les régions abritant des hibernacles et colonies de maternité présumés, mais non confirmés. | La connaissance des emplacements des hibernacles et des colonies de maternité est limitée. De plus, il est nécessaire de confirmer si ceux-ci sont utilisés par des petites chauves-souris brunes ou par des chauves-souris Yuma en Colombie-Britannique. Ces renseignements doivent être connus afin de désigner complètement l’habitat essentiel. | 2016-2025 |
| Préciser les caractéristiques biophysiques des hibernacles et des colonies de maternité (particulièrement dans les parties ouest et nord des aires de répartition des espèces). | On connaît les caractéristiques biophysiques générales, mais il est essentiel de les préciser davantage et de comprendre les habitudes hivernales des chauves-souris afin de désigner complètement l’habitat essentiel. Les connaissances à cet égard sont limitées particulièrement dans les parties ouest et nord des aires de répartition des espèces. | 2016-2025 |
| Déterminer les emplacements et les caractéristiques, notamment biophysiques, des sites de rassemblement. | On ignore l’importance des sites de rassemblement individuels pour la survie et le rétablissement des espèces et les caractéristiques biophysiques importantes de ces sites. | 2016-2025 |
| Établir les critères de désignation des colonies de maternité comme habitat essentiel. | Il y a un manque de données appropriées pour établir des critères scientifiques. | Le cas échéant |
| Description de l’activité | Justification | Échéancier |
|---|---|---|
| Effectuer plus de relevés et de suivis dans l’habitat d’estivage, aux sites stratégiques. | Il y a peu de données sur l’abondance et autres mesures de la qualité de l’habitat d’estivage dans plusieurs régions du pays. Il est nécessaire d’effectuer plus de relevés et de suivis dans des sites prédéterminés. | 2016-2031 |
| Déterminer si les sites de repos propres aux mâles et les voies de migration sont considérés nécessaires à la survie et au rétablissement des espèces et devraient donc être désignés habitat essentiel. | On ignore si ces habitats (ou même une partie d’entre eux) devraient être considérés comme de l’habitat essentiel. | 2019-2025 |
| Déterminer la configuration appropriée des caractéristiques biophysiques du paysage. | Pour désigner l’habitat essentiel à l’échelle du paysage, il est nécessaire de comprendre les caractéristiques biophysiques dont ont besoin les espèces à cette échelle et déterminer comment elles doivent être configurées pour répondre aux besoins des espèces. | 2016-2031 |
| Déterminer la qualité de l’habitat dans les aires de répartition des espèces. | Des données sur l’abondance, la productivité et autres mesures de qualité de l’habitat permettraient de relever les régions qui contribuent de façon disproportionnée à la survie ou au rétablissement des espèces. | 2016-2031 |
| Déterminer l’ampleur et l’intensité des activités susceptibles d’entraîner la destruction de l’habitat essentiel. | Il est nécessaire de mieux comprendre la relation entre les perturbations anthropiques et la qualité de l’habitat pour s’assurer qu’il y a suffisamment d’habitat convenable pour les espèces et déterminer l’ampleur et l’intensité des activités susceptibles d’entraîner la destruction de l’habitat essentiel. | 2016-2031 |
| Déterminer la quantité d’habitat d’estivage convenable requise pour atteindre les objectifs en matière de population et de répartition. | On ignore si les espèces sont limitées par la quantité d’habitat d’estivage au Canada. Il est nécessaire de déterminer s’il y a suffisamment d’habitat au Canada pour atteindre les objectifs en matière de population et de répartition. |
2032 |
| Élaborer et valider des modèles de l’habitat d’estivage afin de déterminer où les caractéristiques biophysiques sont présentes en quantité, en qualité et en configuration adéquates pour atteindre les objectifs en matière de population et de répartition. | Les résultats des études énumérées plus haut permettront de mettre au point des modèles pour déterminer l’emplacement, la quantité et la qualité des milieux qui devraient être désignés habitat essentiel d’estivage. | 2032-2036 |
7.3. Activités susceptibles d’entraîner la destruction de l’habitat essentiel
La présente sous-section d’un programme de rétablissement décrit les activités susceptibles d’entraîner la destruction de l’habitat essentiel; des exemples des activités en cause sont donnés. De l’information est fournie sur les impacts potentiels de ces activités sur l’habitat essentiel et les populations des espèces de chauves-souris.
La destruction de l’habitat essentiel est déterminée au cas par cas. On peut parler de destruction lorsqu’il y a dégradation d’une partie de l’habitat essentiel, soit de façon permanente ou temporaire, à un point tel que l’habitat essentiel n’est plus en mesure d’assurer ses fonctions lorsqu’exigé par l’espèce. La destruction peut découler d’une activité unique à un moment donné ou des effets cumulés d’une ou de plusieurs activités au fil du temps. Des activités susceptibles d’entraîner la destruction de l’habitat essentiel des espèces sont décrites plus bas; il peut toutefois exister d’autres activités destructrices.
Hibernacles
Les activités susceptibles d’entraîner la destruction des hibernacles désignés comme habitat essentiel comprennent, sans toutefois s’y limiter, les suivantes : les activités entraînant l’introduction du SMB dans les hibernacles qui étaient auparavant exempts de la maladie, les activités qui entraînent l’effondrement des murs et des plafonds, toute activité qui rend l’hibernacle inaccessible ou non disponible aux chauves-souris, ou les activités qui modifient la température, le taux d’humidité, la circulation d’air ou d’autres caractéristiques microclimatiques en dehors des limites acceptables pour les espèces de chauves-souris dont on a désigné l’habitat essentiel.
| Description de l’activité | Description des effets possibles |
|---|---|
| Visiteurs (p. ex. chercheurs, spéléologues, touristes) qui ne suivent pas les protocoles de décontamination appropriés. | Destruction directe permanente ou temporaire de l’habitat par l’introduction du SMB. |
| Modifications pour accommoder les visiteurs (p. ex. construction d’un poste d’observation, modification de l’entrée de l’hibernacle) | Destruction directe permanente ou temporaire de l’habitat ou effets indirects (p.ex. modifications des conditions microclimatiques, limitation de l’accès des chauves-souris au site). |
| Érection d’obstacles physiques (p. ex. portes ou barrières) qui réduisent l’accès des chauves-souris au site ou son utilisation par ellesnotef | Destruction directe permanente ou temporaire de l’habitat et/ou effets indirects (p.ex. limitation de l’accès des chauves-souris au site, modifications de la circulation d’air, de la température ou d’autres conditions microclimatiques). |
| Remplissage de puits | Destruction directe permanente de l’habitat. |
| Vandalisme | Destruction directe permanente ou temporaire de l’habitat et/ou effets indirects (p.ex. limitation de l’accès des chauves-souris au site, enlèvement de barrières qui étaient destinées à limiter l’accès des humains au site, modifications de la circulation d’air, de la température ou d’autres conditions microclimatiques). |
| Les activités causant une trop grande perturbation (p. ex. lumière, bruit, vibrations ou présence d’humains) pourraient faire sortir des chauves-souris de leur torpeur, et ces individus pourraient alors déclencher une cascade de réveils chez des chauves-souris voisines et/ou provoquer l’abandon d’un site. Les impacts les plus graves sont associés à la présence répétée d’humains durant plusieurs journées consécutives. | Il peut en résulter une destruction temporaire de l’habitat du fait d’une réduction de la capacité de l’hibernacle d’assurer la survie des chauves-souris durant l’hivernage. Les réveils résultant d’une trop grande perturbation peuvent provoquer un accroissement de la consommation des graisses (et un épuisement prématuré des réserves énergétiques), une famine, une réduction des réserves énergétiques destinées à la reproduction et, ultimement, la mort. |
| L’exploitation de carrières, l’exploration et l’exploitation de mines, l’exploitation forestière, l’agriculture, la construction de barrages et d’autres pratiques industrielles qui causent, empirent ou accélèrent le blocage de la circulation d’air dans les hibernacles ou leur inondationnoteg | Destruction directe permanente ou temporaire de l’habitat et/ou effets indirects (p.ex. modifications des caractéristiques microclimatiques, effondrement du plafond ou de parois, limitation de l’accès au site). |
8. Mesure des progrès
Les indicateurs de rendement présentés ci-dessous proposent un moyen de définir et de mesurer les progrès vers l’atteinte des objectifs en matière de population et de répartition.
Petite chauve-souris brune et chauve-souris nordique
- La zone d’occurrence de la petite chauve-souris brune et de la chauve-souris nordique se maintient (ou, le cas échéant, se rétablit) à son étendue d’avant l’apparition du SMB (à vérifier tous les cinq ans).
- À court terme (de 12 à 18 ans), dans les régions touchées par le SMB, la population de chaque espèce se maintient à son niveau actuel (2015) ou, si possible, augmente au-delà de ce niveau.
- À long terme (nombreuses générations), dans les régions touchées par le SMB, la population de chaque espèce est autosuffisante, résiliente et redondante.
- Dans les régions qui ne sont pas encore touchées par le SMB, la population de chaque espèce se maintient à son niveau actuel ou, si possible, augmente au-delà de ce niveau (à vérifier tous les cinq ans).
Pipistrelle de l’Est
- La zone d’occurrence de la pipistrelle de l’Est est rétablie (puis maintenue) à son étendue d’avant l’apparition du SMB (à vérifier tous les cinq ans).
- À court terme (10 prochaines années), la population se maintient à son niveau actuel (2015) ou, si possible, augmente au-delà de ce niveau.
- À long terme (nombreuses générations), la population est autosuffisante, résiliente et redondante.
9. Énoncé sur les plans d’action
Un ou plusieurs plans d’action visant la petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est seront publiés dans le Registre public des espèces en péril dans les trois ans suivant la publication de la version finale du programme de rétablissement.
10. Références
Abbott, I. M., A. Berthinussen, E. Stone, M. Boonman, M. Melber et J. Altringham. 2015. Bats and Roads. Pages 290-299 In R. van der Ree, D. J. Smith, et C. Grilo (eds.). Handbook of Road Ecology. John Wiley and Sons, Ltd. Chichester, UK.
Abbott, I. M., S. Harrison et F. Butler. 2012. Clutter-adaptation of bat species predicts their use of under-motorway passageways of contrasting sizes – a natural experiment. Journal of Zoology 287(2): 124-132.
Adams, R. A. 2010. Bat reproduction declines when conditions mimic climate change projections for western North America. Ecology 91(8): 2437-2445.
Adams, R. A. et M. A. Hayes. 2008. Water availability and successful lactation by bats as related to climate change in arid regions of western North America. Journal of Animal Ecology 77(6): 1115-1121.
Amelon, S. et D. Burhans. 2006. Conservation assessment: Myotis septentrionalis (northern long-eared bat) in the Eastern United States. Pages 69-82 In F. Thompson (ed.). Conservation Assessements of Five Forest Bat Species in Eastern United States. United States Department of Agriculture Forest Service General Technical Report. NC.
Ancillotto, L., M. T. Serangeli et D. Russo. 2013. Curiosity killed the bat: domestic cats as bat predators. Mammalian Biology 78(5): 369-373.
Anderson, D. M., P. M. Glibert et J. M. Burkholder. 2002. Harmful algal blooms and eutrophication: nutrient sources, composition and consequences. Estuaries 25(4): 704-726.
Anderson, J. et C. Robert. 1971. A new unipolar electrode for electrocardiography in small mammals. Journal of Mammalogy 52: 469-471.
Anonymous. 2008. Sarissa Trip Report Chapleau / Nemegosenda Property. [consulté le 21 juillet 2015].
Anthony, E. L. et T. H. Kunz. 1977. Feeding strategies of the little brown bat, Myotis lucifugus, in southern New Hampshire. Ecology: 775-786.
Arlettaz, R., P. Christe, A. Lugon, N. Perrin et P. Vogel. 2001. Food availability dictates the timing of parturition in insectivorous mouse-eared bats. Oikos 95(1): 105-111.
Arnett, E., C. D. Hein, M. Schirmacher, M. Huso et J. M. Szewczak. 2013a. Evaluating the effectiveness of an ultrasonic acoustic deterrent for reducing bat fatalities at wind turbines. PLoS One 8(9): e65794.
Arnett, E., G. Johnson, W. Erickson et C. Hein. 2013b. A synthesis of operational mitigation studies to reduce bat fatalities at wind energy facilities in North America. National Renewable Energy Laboratory, Austin, TX.
Arnett, E. B., W. Brown, W. P. Erickson, J. K. Fiedler, B. L. Hamilton, T. H. Henry, A. Jain, G. D. Johnson, J. Kerns et R. R. Koford. 2008. Patterns of bat fatalities at wind energy facilities in North America. The Journal of Wildlife Management 72(1): 61-78.
Arnett, E. B., M. Schirmacher, M. Huso et J. Hayes. 2009. Effectiveness of changing wind turbine cut-in speed to reduce bat fatalities at wind facilities. Bats and Wind Energy Cooperative, Bat Conservation International, Austin, TX.
Baerwald, E. F., G. H. D'Amours, B. J. Klug et R. M. Barclay. 2008. Barotrauma is a significant cause of bat fatalities at wind turbines. Current Biology 18(16): R695-R696.
Baerwald, E. F., J. Edworthy, M. Holder et R. M. Barclay. 2009. A large scale mitigation experiment to reduce bat fatalities at wind energy facilities. The Journal of Wildlife Management 73(7): 1077-1081.
Barbour, R. W. et W. H. Davis. 1969. Bats of America. University Press of Kentucky. Lexington, KY. 286 pp.
Barclay, R. et A. Kurta. 2007. Ecology and behaviour of bats roosting in tree cavities and under bark. Pages 17-60 In M. J. Lacki, J. P. Hayes et A. Kurta (eds.). Bats in Forests: Conservation and Management. John Hopkins University Press. Baltimore, MD.
Barclay, R. R. et R. M. Brigham. 1996. Bats and Forests Symposium. British Columbia, Ministry of Forests Research Program. Victoria, BC.
BatsLive. 2015. Project EduBat.. [consulté le 18 juin 2015].
Bennett, V. J. et A. A. Zurcher. 2013. When corridors collide: road related disturbance in commuting bats. The Journal of Wildlife Management 77(1): 93 101.
Boldogh, S., D. Dobrosi et P. Samu. 2007. The effects of the illumination of buildings on house-dwelling bats and its conservation consequences. Acta Chiropterologica 9(2): 527-534.
Borkin, K., C. O’Donnell et S. Parsons. 2011. Bat colony size reduction coincides with clear-fell harvest operations and high rates of roost loss in plantation forest. Biodiversity and Conservation 20(14): 3537-3548.
Both, C., C. A. Van Turnhout, R. G. Bijlsma, H. Siepel, A. J. Van Strien et R. P. Foppen. 2009. Avian population consequences of climate change are most severe for long-distance migrants in seasonal habitats. Proceedings of the Royal Society B: Biological Sciences 277: 1259-1266.
Boyles, J. G. et V. Brack. 2009. Modeling survival rates of hibernating mammals with individual-based models of energy expenditure. Journal of Mammalogy 90(1): 9-16.
Briggler, J. T. et J. W. Prather. 2003. Seasonal use and selection of caves by the eastern pipistrelle bat (Pipistrellus subflavus). The American Midland Naturalist 149(2): 406-412.
Brigham, R. M. et M. B. Fenton. 1986. The influence of roost closure on the roosting and foraging behaviour of Eptesicus fuscus (Chiroptera: Vespertilionidae). Canadian Journal of Zoology 64(5): 1128-1133.
Broders, H. G., L. E. Burns et S. C. McCarthy. 2013. First records of the Northern Myotis (Myotis septentrionalis) from labrador and summer distribution records and biology of little brown bats (Myotis lucifugus) in southern Labrador. Canadian Field-Naturalist 127(3): 266-269.
Broders, H. G., L. J. Farrow, R. N. Hearn, L. M. Lawrence et G. J. Forbes. 2014. Stable isotopes reveal that little brown bats have a broader dietary niche than northern long-eared bats. Acta Chiropterologica 16(2): 315-325.
Broders, H. G. et G. J. Forbes. 2004. Interspecific and intersexual variation in roost-site selection of northern long-eared and little brown bats in the Greater Fundy National Park ecosystem. Journal of Wildlife Management 68(3): 602-610.
Broders, H. G., G. J. Forbes, S. Woodley et I. D. Thompson. 2006. Range extent and stand selection for roosting and foraging in forest-dwelling Northern Long-Eared Bats and Little Brown Bats in the Greater Fundy Ecosystem, New Brunswick. The Journal of Wildlife Management 70(5): 1174-1184.
Broders, H. G., D. F. McAlpine et G. J. Forbes. 2001. Status of the eastern pipistrelle (Pipistrellus subflavus) (Chiroptera: Vespertilionidae) in New Brunswick. Northeastern Naturalist 8(3): 331-336.
Broders, H. G., G. M. Quinn et G. J. Forbes. 2003. Species status, and the spatial and temporal patterns of activity of bats in southwest Nova Scotia, Canada. Northeastern Naturalist 10(4): 383-398.
Brown, J. A., D. F. McAlpine et R. Curley. 2007. Northern Long-eared Bat, Myotis septentrionalis (Chiroptera: Vespertilionidae), on Prince Edward Island: first records of occurrence and over-wintering. The Canadian Field-Naturalist 121(2): 208-209.
Bunkley, J. P., C. J. McClure, N. J. Kleist, C. D. Francis et J. R. Barber. 2015. Anthropogenic noise alters bat activity levels and echolocation calls. Global Ecology and Conservation 3: 62-71.
Burles, D. W., M. B. Fenton, R. M. Barclay, R. M. Brigham et D. Volkers. 2014. Aspects of the winter ecology of bats on Haida Gwaii, British Columbia. Northwestern Naturalist 95(3): 289-299.
Burns, L. E., T. R. Frasier et H. G. Broders. 2014. Genetic connectivity among swarming sites in the wide ranging and recently declining little brown bat (Myotis lucifugus). Ecology and Evolution 4(21): 4130-4149.
Caceres, M. C. et R. M. Barclay. 2000. Myotis septentrionalis. Mammalian Species 634: 1-4.
Calvert, A. M., C. A. Bishop, R. D. Elliot, E. A. Krebs, T. M. Kydd, C. S. Machtans et G. J. Robertson. 2013. A synthesis of human-related avian mortality in Canada. Avian Conservation and Ecology 8(2): 11.
Canadian Wildlife Federation. 2015. Help the Bats. Kanata, ON. [consulté le 19 juin 2015]. (Également disponible en français : Fédération canadienne de la faune. 2015. Aidez les chauves-souris, Kanata, Ont.).
Canadian Wildlife Health Cooperative. 2015a. Bat White Nose Syndrome. [consulté le 22 avril 2015]. (Également disponible en français : Réseau canadien de la santé de la faune. 2015a. Syndrome du museau blanc).
Canadian Wildlife Health Cooperative. 2015b. A national plan to manage White Nose Syndrome in bats in Canada. Canadian Wildlife Health Cooperative: Canada's Inter-agency White Nose Syndrome Committee, Saskatoon, SK.
Carr, J. A., R. F. Bernard et W. H. Stiver. 2014. Unusual bat behavior during winter in Great Smoky Mountains National Park. Southeastern Naturalist 13(2): N18-N21.
Carter, T. C. et G. A. Feldhamer. 2005. Roost tree use by maternity colonies of Indiana bats and northern long-eared bats in southern Illinois. Forest Ecology and Management 219(2–3): 259-268.
Chaverri, G. et T. H. Kunz. 2011. Response of a specialist bat to the loss of a critical resource. PLoS One 6(12): e28821.
Chruszcz, B. et R. Barclay. 2002. Thermoregulatory ecology of a solitary bat, Myotis evotis, roosting in rock crevices. Functional Ecology 16(1): 18-26.
Clare, E. L., W. O. C. Symondson, H. Broders, F. Fabianek, E. E. Fraser, A. MacKenzie, A. Boughen, R. Hamilton, C. K. R. Willis, F. Martinez-Nuñez, A. K. Menzies, K. J. O. Norquay, M. Brigham, J. Poissant, J. Rintoul, R. M. R. Barclay et J. P. Reimer. 2014. The diet of Myotis lucifugus across Canada: assessing foraging quality and diet variability. Molecular Ecology 23(15): 3618-3632.
Clark, D. R. et T. G. Lamont. 1976. Organochlorine residues in females and nursing young of the big brown bat (Eptesicus fuscus). Bulletin of Environmental Contamination and Toxicology 15(1): 1-8.
Coleman, J. L. et R. M. Barclay. 2011. Influence of urbanization on demography of little brown bats (Myotis lucifugus) in the prairies of North America. PLoS One 6(5): e20483.
Community Bat Programs of BC. 2014. Community Bat Programs Help People and Bats. [consulté le 22 avril 2015].
Cornelison, C. T., M. K. Keel, K. T. Gabriel, C. K. Barlament, T. A. Tucker, G. E. Pierce et S. A. Crow. 2014. A preliminary report on the contact-independent antagonism of Pseudogymnoascus destructans by Rhodococcus rhodochrous strain DAP96253. BMC Microbiology 14(1): 246.
COSEWIC. 2006. COSEWIC assessment and status report on the Rusty Blackbird Euphagus carolinus in Canada. Committee on the Status of Endangered Wildlife in Canada, Ottawa, ON. (Également disponible en français : COSEPAC. 2013. Évaluation et Rapport de situation du COSEPAC sur le Quiscale rouilleux Euphagus carolinus au Canada, Comité sur la situation des espèces en péril au Canada, Ottawa (Ont.)).
COSEWIC. 2013. COSEWIC assessment and status report on the Little Brown Myotis Myotis lucifugus, Northern Myotis Myotis septentrionalis and Tri-colored Bat Perimyotis subflavus in Canada. Committee on the Status of Endangered Wildlife in Canada, Ottawa, ON. (Également disponible en français : COSEPAC. 2013. Évaluation et Rapport de situation du COSEPAC sur la petite chauve-souris brune (Myotis lucifugus), chauve-souris nordique (Myotis septentrionalis) et la pipistrelle de l’Est (Perimyotis subflavus) au Canada, Comité sur la situation des espèces en péril au Canada, Ottawa (Ont.)).
Crampton, L. et R. Barclay. 1996. Habitat selection by bats in fragmented and unfragmented aspen mixedwood stands of different ages Page 292 In M. Brigham et R. Barclay (eds.). Bats and Forests Symposium. BC Ministry of Forests Victoria, BC.
Cryan, P. M. 2011. Wind turbines as landscape impediments to the migratory connectivity of bats. Environmental Law 41: 355.
Cryan, P. M. et A. C. Brown. 2007. Migration of bats past a remote island offers clues toward the problem of bat fatalities at wind turbines. Biological Conservation 139(1): 1-11.
Cryan, P. M., C. U. Meteyer, J. G. Boyles et D. S. Blehert. 2010. Wing pathology of white-nose syndrome in bats suggests life-threatening disruption of physiology. BMC Biology 8(1): 135.
CWHC. 2015. CWHC. 2015. Canadian Wildlife Health Cooperative. CWHC, Saskatoon, SK. [consulté le 19 juillet 2015]. (Également disponible en français : RCSF. 2015. Réseau canadien de la santé de la faune, RCSF, Saskatoon (Sask.)).
Damm, J. P. et K. Geluso. 2008. Use of a mine by eastern pipistrelles (Perimyotis subflavus) in east central Nebraska. Western North American Naturalist 68(3): 382-389.
Darling, S. et R. Smith. 2011. Assessment of Vermont cave bat populations and proposal to list bat species. Vermont Fish and Wildlife Department, VT.
Davis, W. et H. Hitchcock. 1995. A new longevity record for the bat Myotis lucifugus. Bat Research News 36(1): 6.
Davis, W. H. 1970. Hibernation: ecology and physiological ecology. Biology of Bats 1: 265-300.
de Groot, W. J., M. D. Flannigan et A. S. Cantin. 2013. Climate change impacts on future boreal fire regimes. Forest Ecology and Management 294: 35-44.
Depew, D. C., N. M. Burgess et L. M. Campbell. 2013. Modelling mercury concentrations in prey fish: derivation of a national-scale common indicator of dietary mercury exposure for piscivorous fish and wildlife. Environmental Pollution 176: 234-243.
Derusseau, S. N. et N. J. Huntly. 2012. Effects of gates on the nighttime use of mines by bats in northern Idaho. Northwestern Naturalist 93(1): 60-66.
Diamond, G. F. et J. M. Diamond. 2014. Bats and mines: evaluating Townsend's Big-Eared Bat (Corynorhinus townsendii) maternity colony behavioral response to gating. Western North American Naturalist 74(4): 416-426.
Dirzo, R., H. S. Young, M. Galetti, G. Ceballos, N. J. Isaac et B. Collen. 2014. Defaunation in the Anthropocene. Science 345(6195): 401-406.
Dodd, L. E., M. J. Lacki, E. R. Britzke, D. A. Buehler, P. D. Keyser, J. L. Larkin, A. D. Rodewald, T. B. Wigley, P. B. Wood et L. K. Rieske. 2012. Forest structure affects trophic linkages: how silvicultural disturbance impacts bats and their insect prey. Forest Ecology and Management 267: 262-270.
Douglas, M. R. et J. F. Tooker. 2015. Large-scale deployment of seed treatments has driven rapid increase in use of neonicotinoid insecticides and preemptive pest management in US field crops. Environmental Science and Technology 49(8): 5088-5097.
Dubois, J. E. et K. M. Monson. 2007. Recent distribution records of the Little Brown Bat, Myotis lucifugus, in Manitoba and Northwestern Ontario. The Canadian Field-Naturalist 121(1): 57-61.
Dzal, Y., L. A. Hooten, E. L. Clare et M. Brock-Fenton. 2009. Bat activity and genetic diversity at Long Point, Ontario, an important bird stopover site. Acta Chiropterologica 11(2): 307-315.
Dzal, Y., L. P. McGuire, N. Veselka et M. B. Fenton. 2011. Going, going, gone: the impact of white-nose syndrome on the summer activity of the little brown bat (Myotis lucifugus). Biology Letters 7(3): 392-394.
Edmonds, S. T., D. C. Evers, D. A. Cristol, C. Mettke-Hofmann, L. L. Powell, A. J. McGann, J. W. Armiger, O. P. Lane, D. F. Tessler et P. Newell. 2010. Geographic and seasonal variation in mercury exposure of the declining Rusty Blackbird. The Condor 112(4): 789-799.
Eidels, R. R., J. O. Whitaker Jr et D. W. Sparks. 2007. Insecticide residues in bats and guano from Indiana. Proceedings of the Indiana Academy of Science 116(1): 50-57.
Ellison, L., T. O’Shea, M. Bogan, A. Everette et D. Schneider. 2003. Existing data on colonies of bats in the United States: summary and analysis of the US Geological Survey’s bat population database. Pages 127-237 In T. J. O'Shea et M. A. Bogan (eds.). Monitoring trends in bat populations of the United States and territories: problems and prospects. U.S. Geological Survey. Fort Collins, CO.
Entwistle, A. C., S. Harris, A. M. Hutson, P. Racey, A. Walsh, S. D. Gibson, I. Hepburn et J. Johnston. 2001. Habitat management for bats: a guide for land managers, land owners and their advisors. Joint Nature Conservation Committee, Peterborough, UK.
Environment Canada. 2011. Presence and levels of priority pesticides in selected Canadian aquatic ecosystems. Water Science and Technology Directorate, Ottawa, ON. (Également disponible en français : Environnement Canada. 2011. Présence et concentrations des pesticides prioritaires dans certains écosystèmes aquatiques canadiens, Direction des sciences et de la technologie de l’eau, Ottawa (Ont.)).
Environment Canada. 2015a. Recovery Strategy for Canada Warbler (Cardellina canadensis) in Canada [Proposed]. Ottawa, ON. (Également disponible en français : Environnement Canada. 2015a. Programme de rétablissement de la Paruline du Canada (Cardellina canadensis) au Canada [Proposition], Ottawa (Ont.)).
Environment Canada. 2015b. Recovery Strategy for the Common Nighthawk (Chordeiles minor) in Canada [Proposed]. Ottawa, ON. (Également disponible en français : Environnement Canada. 2015b. Programme de rétablissement de l’Engoulevent d’Amérique (Chordeiles minor) au Canada [Proposition], Ottawa (Ont.)).
Ethier, K. et L. Fahrig. 2011. Positive effects of forest fragmentation, independent of forest amount, on bat abundance in eastern Ontario, Canada. Landscape Ecology 26(6): 865-876.
Fabianek, F., D. Gagnon et M. Delorme. 2011. Bat distribution and activity in Montréal Island green spaces: responses to multi-scale habitat effects in a densely urbanized area. Ecoscience 18(1): 9-17.
Fabianek, F., M. A. Simard, E. B. Racine et A. Desrochers. 2015. Selection of roosting habitat by male Myotis bats in a boreal forest. Canadian Journal of Zoology 93(7): 539.
Farrow, L. J. et H. G. Broders. 2011. Loss of forest cover impacts the distribution of the forest-dwelling tri-colored bat (Perimyotis subflavus). Mammalian Biology 76(2): 172-179.
Federal Provincial and Territorial Governments of Canada. 2010. Canadian Biodiversity: Ecosystem Status and Trends 2010. Ottawa, ON. [consulté en octobre 2015]. (Également disponible en français : Les gouvernements fédéral, provinciaux et territoriaux du Canada. 2010. Biodiversité canadienne : état et tendances des écosystèmes en 2010. Ottawa, Ont.).
Fenton, M. B. 1969. Summer activity of Myotis lucifugus (Chiroptera: Vespertilionidae) at hibernacula in Ontario and Quebec. Canadian Journal of Zoology 47(4): 597-602.
Fenton, M. B. 1970. A technique for monitoring bat activity with results obtained from different environments in southern Ontario. Canadian Journal of Zoology 48(4): 847-851.
Fenton, M. B. et R. M. Barclay. 1980. Myotis lucifugus. Mammalian Species 142: 1-8.
Fitzgerald, W. F., D. R. Engstrom, R. P. Mason et E. A. Nater. 1998. The case for atmospheric mercury contamination in remote areas. Environmental Science and Technology 32(1): 1-7.
Flannigan, M., B. Stocks, M. Turetsky et M. Wotton. 2009. Impacts of climate change on fire activity and fire management in the circumboreal forest. Global Change Biology 15(3): 549-560.
Fleming, R., J.-N. Candau et R. McAlpine. 2002. Landscape-scale analysis of interactions between insect defoliation and forest fire in central Canada. Climatic Change 55(1-2): 251-272.
Foster, R. et A. Kurta. 1999. Roosting ecology of the northern bat (Myotis septentrionalis) and comparisons with endangered Indiana bat (Myotis sodalis). Journal of Mammalogy 80: 659-672.
Francl, K. E., W. M. Ford, D. W. Sparks et V. Brack Jr. 2012. Capture and reproductive trends in summer bat communities in West Virginia: assessing the impact of white-nose syndrome. Journal of Fish and Wildlife Management 3(1): 33-42.
Frank, C. L., A. Michalski, A. A. McDonough, M. Rahimian, R. J. Rudd et C. Herzog. 2014. The resistance of a North American bat species (Eptesicus fuscus) to white-nose syndrome (WNS). PLoS One 9(12): e113958.
Frank, K. D. 1988. Impact of outdoor lighting on moths: an assessment. Journal of the Lepidopterists' Society 42(2): 63-93.
Fraser, E. E., L. P. McGuire, J. L. Eger, F. J. Longstaffe et M. B. Fenton. 2012. Evidence of latitudinal migration in tri-colored bats, Perimyotis subflavus. PLoS One 7(2): e31419.
Frick, W. F., J. F. Pollock, A. C. Hicks, K. E. Langwig, D. S. Reynolds, G. G. Turner, C. M. Butchkoski et T. H. Kunz. 2010a. An emerging disease causes regional population collapse of a common North American bat species. Science 329(5992): 679-682.
Frick, W. F., D. S. Reynolds et T. H. Kunz. 2010f. Influence of climate and reproductive timing on demography of little brown myotis Myotis lucifugus. Journal of Animal Ecology 79(1): 128-136.
Fujita, M. S. et T. H. Kunz. 1984. Pipistrellus subflavus. Mammalian Species 228: 1-6.
Fuller, N. W., J. D. Reichard, M. L. Nabhan, S. R. Fellows, L. C. Pepin et T. H. Kunz. 2011. Free-ranging little brown myotis (Myotis lucifugus) heal from wing damage associated with white-nose syndrome. EcoHealth 8(2): 154-162.
Furlonger, C., H. Dewar et M. Fenton. 1987. Habitat use by foraging insectivorous bats. Canadian Journal of Zoology 65(2): 284-288.
Gaisler, J., V. Hanak et I. Horacek. 1981. Remarks on the current status of bat populations in Czechoslovakia. Myotis 18(19): 68-75.
Garroway, C. J. et H. G. Broders. 2008. Day roost characteristics of northern long-eared bats (Myotis septentrionalis) in relation to female reproductive status. Ecoscience 15(1): 89-93.
Gaston, K. J., J. Bennie, T. W. Davies et J. Hopkins. 2013. The ecological impacts of nighttime light pollution: a mechanistic appraisal. Biological Reviews 88(4): 912-927.
Gibbons, D., C. Morrissey et P. Mineau. 2015. A review of the direct and indirect effects of neonicotinoids and fipronil on vertebrate wildlife. Environmental Science and Pollution Research 22(1): 103-118.
Girardin, M. P., A. A. Ali, C. Carcaillet, O. Blarquez, C. Hély, A. Terrier, A. Genries et Y. Bergeron. 2013. Vegetation limits the impact of a warm climate on boreal wildfires. New Phytologist 199(4): 1001-1011.
GNWT. 2015a. NWT Species at Risk Little Brown Myotis. Government of Northwest Territories, Yellowknife, NT. [consulté le 21 juillet 2015].
GNWT. 2015b. NWT Species at Risk Northern Myotis. Government of the Northwest Territories, Yellowknife, NT. [consulté le 22 juillet 2015].
Goulson, D. 2013. Review: An overview of the environmental risks posed by neonicotinoid insecticides. Journal of Applied Ecology 50(4): 977-987.
Griffin, D. 1940. Migrations of New England bats. Bulletin of the Museum of Comparative Zoology 86: 217-246.
Grindal, S. D. et R. M. Brigham. 1998. Short-term effects of small-scale habitat disturbance on activity by insectivorous bats. The Journal of Wildlife Management: 996-1003.
Grindal, S. D. et R. M. Brigham. 1999. Impacts of forest harvesting on habitat use by foraging insectivorous bats at different spatial scales. Ecoscience: 25-34.
Grindal, S. D., C. I. Stefan et C. Godwin-Sheppard. 2011. Diversity, distribution, and relative abundance of bats in the oil sands regions of northeastern Alberta. Northwestern Naturalist 92(3): 211-220.
Grodsky, S. M., M. J. Behr, A. Gendler, D. Drake, B. D. Dieterle, R. J. Rudd et N. L. Walrath. 2011. Investigating the causes of death for wind turbine-associated bat fatalities. Journal of Mammalogy 92(5): 917-925.
Haak, D. 2008. Sustainable Agriculture Land Management around Wetlands on the Canadian Prairies. In A. a. A.-F. Canada, ed. Agriculture and Agri-Food Canada, Ottawa, ON. (Également disponible en français : Gestion durable des terres agricoles voisines des milieux humides dans les Prairies canadiennes. In A. a. A.-F. Canada, ed. Agriculture et Agroalimentaire Canada, Ottawa, Ont.).
Hallegraeff, G. M. 1993. A review of harmful algal blooms and their apparent global increase. Phycologia 32(2): 79-99.
Harrison, J. B. 1965. Temperature effects on responses in the auditory system of the little brown bat Myotis l. lucifugus. Physiological Zoology: 34-48.
Harvey, M. J. 1992. Bats of the eastern United States. Arkansas Game and Fish Commission and United States Fish and Wildlife Service, Center for the Management, Utilization, and Protection of Water Resources, Tennessee Technological University, Cookeville, TN.
Harvey, M. J., J. S. Altenbach et T. L. Best. 2011. Bats of the United States and Canada. Johns Hopkins University Press. Baltimore, MD. 202 pp.
Hayes, M. A. 2013. Bats killed in large numbers at United States wind energy facilities. BioScience 63(12): 975-979.
Hayhoe, K., C. P. Wake, T. G. Huntington, L. Luo, M. D. Schwartz, J. Sheffield, E. Wood, B. Anderson, J. Bradbury et A. DeGaetano. 2007. Past and future changes in climate and hydrological indicators in the US Northeast. Climate Dynamics 28(4): 381-407.
Hemmera. 2011. Raptor and Migratory Bird and Bat Monitoring and Follw-up Report 2010 and Recommendations for 2011. Hemmera, Vancouver, BC.
Henderson, L. E. et H. G. Broders. 2008. Movements and resource selection of the Northern Long-Eared Myotis (Myotis septentrionalis) in a forest-agriculture landscape. Journal of Mammalogy 89(4): 952-963.
Henderson, L. E., L. J. Farrow et H. G. Broders. 2008. Intra-specific effects of forest loss on the distribution of the forest-dependent northern long-eared bat (Myotis septentrionalis). Biological Conservation 141(7): 1819-1828.
Henderson, L. E., L. J. Farrow et H. G. Broders. 2009. Summer distribution and status of the bats of Prince Edward Island, Canada. Northeastern Naturalist 16(1): 131-140.
Henry, M., D. W. Thomas, R. Vaudry et M. Carrier. 2002. Foraging distances and home range of pregnant and lactating Little Brown Bats (Myotis lucifugus). Journal of Mammalogy 83(3): 767-774.
Henshaw, R. E. et G. E. Folk. 1966. Relation of thermoregulation to seasonally changing microclimate in two species of bats (Myotis lucifugus and M. sodalis). Physiological Zoology: 223-236.
Hitchcock, H. B. 1949. Hibernation of bats in southeastern Ontario and adjacent Quebec. Canadian Field-Naturalist 63(1): 47-59.
Hitchcock, H. B. 1965. Twenty-three years of bat banding in Ontario and Quebec. Canadian Field-Naturalist 79: 4-14.
Hobson, K. A., E. M. Bayne et S. L. Van Wilgenburg. 2002. Large-scale conversion of forest to agriculture in the boreal plains of Saskatchewan. Conservation Biology 16(6): 1530-1541.
Hogberg, L. K., K. J. Patriquin et R. M. Barclay. 2002. Use by bats of patches of residual trees in logged areas of the boreal forest. The American Midland Naturalist 148(2): 282-288.
Hölker, F., C. Wolter, E. K. Perkin et K. Tockner. 2010. Light pollution as a biodiversity threat. Trends in Ecology and Evolution 25(12): 681-682.
Horacek, I., J. Zukal, T. Bartonika et N. Martinkova. 2012. Ecology of geomycosis in central Europe. 5th Annual White-nose Syndrome Symposium, Madison, WI.
Horn, J. W., E. B. Arnett et T. H. Kunz. 2008. Behavioral responses of bats to operating wind turbines. The Journal of Wildlife Management 72(1): 123-132.
Horváth, G., G. Kriska, P. Malik et B. Robertson. 2009. Polarized light pollution: a new kind of ecological photopollution. Frontiers in Ecology and the Environment 7(6): 317-325.
Hoyt, J. R., T. L. Cheng, K. Langwig, M. M. Hee, W. F. Frick et A. M. Kilpatrick. 2015. Bacteria isolated from bats inhibit the growth of Pseudogymnoascus destructans, the causative agent of white-nose syndrome. PLoS One 10(4): e0121329.
Hoyt, J. R., K. E. Langwig, J. Okoniewski, W. F. Frick, W. B. Stone et A. M. Kilpatrick. 2014. Long-term persistence of Pseudogymnoascus destructans, the causative agent of white-nose syndrome, in the absence of bats. EcoHealth: 1-4.
Humphries, M. M., D. W. Thomas et J. R. Speakman. 2002. Climate-mediated energetic constraints on the distribution of hibernating mammals. Nature 418(6895): 313-316.
Huntington, T. G., A. D. Richardson, K. J. McGuire et K. Hayhoe. 2009. Climate and hydrological changes in the northeastern United States: recent trends and implications for forested and aquatic ecosystems. Canadian Journal of Forest Research 39(2): 199-212.
Huynh, H. M. 2009. Another record of foliage roosting in the Little Brown Bat, Myotis lucifugus, in Canada. The Canadian Field-Naturalist 123(3): 265.
Johnson, L. N., B. A. McLeod, L. E. Burns, K. Arseneault, T. R. Frasier et H. G. Broders. 2015. Population genetic structure within and among seasonal site types in the little brown bat (Myotis lucifugus) and the northern long-eared bat (M. septentrionalis). PLoS One 10(5): e0126309.
Jonasson, K. A. et C. K. Willis. 2011. Changes in body condition of hibernating bats support the thrifty female hypothesis and predict consequences for populations with white-nose syndrome. PLoS One 6(6): e21061.
Jones, G., D. S. Jacobs, T. H. Kunz, M. R. Willig et P. A. Racey. 2009. Carpe noctem: the importance of bats as bioindicators. Endangered Species Research 8(1-2): 93-115.
Jones, G. et H. Rebelo. 2013. Responses of bats to climate change: learning from the past and predicting the future. Pages 457-478 In R. A. Adams et S. C. Pedersen (eds.). Bat Evolution, Ecology, and Conservation. Springer.
Jung, T. S., K. M. Blejwas, C. L. Lausen, J. M. Wilson et L. E. Olson. 2014. Concluding remarks: what do we need to know about bats in northwestern North America? Northwestern Naturalist 95(3): 318-330.
Jung, T. S., B. G. Slough, D. W. Nagorsen, T. A. Dewey et T. Powell. 2006. First records of the Northern Long-eared Bat, Myotis septentrionalis, in the Yukon Territory. The Canadian Field-Naturalist 120(1): 39-42.
Jung, T. S., I. D. Thompson et R. D. Titman. 2004. Roost site selection by forest-dwelling male Myotis in central Ontario, Canada. Forest Ecology and Management 202(1): 325-335.
Jung, T. S., I. D. Thompson, R. D. Titman et A. P. Applejohn. 1999. Habitat selection by forest bats in relation to mixed-wood stand types and structure in central Ontario. The Journal of Wildlife Management: 1306-1319.
Kalcounis-Rüppell, M. C., J. M. Psyllakis et R. M. Brigham. 2005. Tree roost selection by bats: an empirical synthesis using meta-analysis. Wildlife Society Bulletin 33(3): 1123-1132.
Kannan, K., S. H. Yun, R. J. Rudd et M. Behr. 2010. High concentrations of persistent organic pollutants including PCBs, DDT, PBDEs and PFOS in little brown bats with white-nose syndrome in New York, USA. Chemosphere 80(6): 613-618.
Karouna-Renier, N. K., C. White, C. R. Perkins, J. J. Schmerfeld et D. Yates. 2014. Assessment of mitochondrial DNA damage in little brown bats (Myotis lucifugus) collected near a mercury-contaminated river. Ecotoxicology 23(8): 1419-1429.
Kilpatrick, M. 2013. Transmission of Geomyces destructans between bats and the environment. International Bat Research Conference San Jose, Costa Rica.
Kitzes, J. et A. Merenlender. 2014. Large roads reduce bat activity across multiple species. PLoS One 9(5): e96341.
Krusic, R. A., M. Yamasaki, C. D. Neefus et P. J. Pekins. 1996. Bat habitat use in white mountain national forest. The Journal of Wildlife Management: 625-631.
Kuiper-Goodman, T., I. Falconer et J. Fitzgerald. 1999. Human health aspects. Pages 113-153 In I. Chorus et J. Bartram (eds.). Toxic Cyanobacteria in Water, A Guide to Their Public Health Consequences, Monitoring and Management. Spon Press. New York, Ny.
Kunz, T. et M. Tuttle. 2009. White-nose syndrome science strategy meeting II., Austin, TX.
Kunz, T. H. 1973. Resource utilization: temporal and spatial components of bat activity in central Iowa. Journal of Mammalogy: 14-32.
Kunz, T. H. 1982. Roosting ecology in bats. Pages 1-56 In T. H. Kunz (ed.). Ecology of Bats. Plenum Press. New York, NY.
Kunz, T. H., E. B. Arnett, W. P. Erickson, A. R. Hoar, G. D. Johnson, R. P. Larkin, M. D. Strickland, R. W. Thresher et M. D. Tuttle. 2007. Ecological impacts of wind energy development on bats: questions, research needs, and hypotheses. Frontiers in Ecology and the Environment 5(6): 315-324.
Kunz, T. H. et J. D. Reichard. 2010. Status review of the little brown myotis (Myotis lucifugus) and determination that immediate listing under the Endangered Species Act is scientifically and legally warranted. Boston University, Boston, MA.
Kunz, T. H. et D. S. Reynolds. 2003. Bat colonies in buildings. Pages 91-102 In T. J. O'Shea et M. A. Bogan (eds.). Monitoring Trends in Bat Populations of the United States and Territories: Problems and Prospects. US Geological Survey, Springfield, VA.
Kunz, T. H., J. A. Wrazen et C. D. Burnett. 1998. Changes in body mass and fat reserves in prehibernating little brown bats (Myotis lucifugus). Ecoscience: 8-17.
Kurta, A. 2014. The misuse of relative humidity in ecological studies of hibernating bats. Acta Chiropterologica 16(1): 249-254.
Kurta, A. et S. M. Smith. 2014. Hibernating bats and abandoned mines in the Upper Peninsula of Michigan. Northeastern Naturalist 21(4): 587-605.
Kyba, C. C., T. Ruhtz, J. Fischer et F. Hölker. 2011. Cloud coverage acts as an amplifier for ecological light pollution in urban ecosystems. PLoS One 6(3): e17307-e17307.
Lacki, M. J., D. R. Cox, L. E. Dodd et M. B. Dickinson. 2009. Response of Northern Bats (Myotis septentrionalis) to prescribed fires in Eastern Kentucky forests. Journal of Mammalogy 90(5): 1165-1175.
Lacoeuilhe, A., N. Machon, J.-F. Julien, A. Le Bocq et C. Kerbiriou. 2014. The influence of low intensities of light pollution on bat communities in a semi-natural context. PLoS One 9(10): e103042.
Langwig, K., J. Voyles, M. Q. Wilber, W. F. Frick, K. A. Murray, B. M. Bolker, J. P. Collins, T. L. Cheng, M. C. Fisher, J. R. Hoyt, D. L. Lindner, H. I. McCallum, R. Puschendorf, E. B. Rosenblum, M. Toothman, C. K. R. Willis, C. J. Briggs et A. M. Kilpatrick. 2015a. Context dependent conservation responses to emerging wildlife diseases. Frontiers in Ecology and the Environment 13: 195-202.
Langwig, K. E., W. F. Frick, J. T. Bried, A. C. Hicks, T. H. Kunz et A. Marm Kilpatrick. 2012. Sociality, density dependence and microclimates determine the persistence of populations suffering from a novel fungal disease, white nose syndrome. Ecology Letters 15(9): 1050-1057.
Langwig, K. E., W. F. Frick, R. Reynolds, K. L. Parise, K. P. Drees, J. R. Hoyt, T. L. Cheng, T. H. Kunz, J. T. Foster et A. M. Kilpatrick. 2015d. Host and pathogen ecology drive the seasonal dynamics of a fungal disease, white-nose syndrome. Proceedings of the Royal Society of London B: Biological Sciences 282(1799): 20142335.
Lausen, C. L., T. S. Jung et J. M. Talerico. 2008. Range extension of the northern long-eared bat (Myotis septentrionalis) in the Yukon. Northwestern Naturalist 89(2): 115-117.
Leopardi, S., D. Blake et S. J. Puechmaille. 2015. White Nose Syndrome fungus introduced from Europe to North America. Current Biology 25(6): R217-R219.
Lesiński, G., A. Sikora et A. Olszewski. 2011. Bat casualties on a road crossing a mosaic landscape. European Journal of Wildlife Research 57(2): 217-223.
Lindner, D. L., A. Gargas, J. M. Lorch, M. T. Banik, J. Glaeser, T. H. Kunz et D. S. Blehert. 2011. DNA-based detection of the fungal pathogen Geomyces destructans in soils from bat hibernacula. Mycologia 103(2): 241-246.
Little, M. E., N. M. Burgess, H. Broders et L. M. Campbell. 2015a. Distribution of mercury in archived fur from little brown bats across Atlantic Canada. Environmental Pollution 207: 52-28.
Little, M. E., N. M. Burgess, H. G. Broders et L. M. Campbell. 2015b. Mercury in little brown bat (Myotis lucifugus) maternity colonies and its correlation with freshwater acidity in Nova Scotia, Canada. Environmental Science and Technology 49(4): 2059-2065.
Loeb, S. C., T. J. Rodhouse, L. E. Ellison, C. L. Lausen, J. D. Reichard, K. M. Irvine, T. E. Ingersoll, J. T. Coleman, W. E. Thogmartin, J. R. Sauer, C. M. Francis, M. L. Bayless, T. R. Stanley et D. H. Johnson. 2015. A Plan for the North American Bat Monitoring Program (NABat). United States Department of Agriculture: Forest Service Research and Development, Asheville, NC.
Lorch, J. M., C. U. Meteyer, M. J. Behr, J. G. Boyles, P. M. Cryan, A. C. Hicks, A. E. Ballmann, J. T. Coleman, D. N. Redell et D. M. Reeder. 2011. Experimental infection of bats with Geomyces destructans causes white-nose syndrome. Nature 480(7377): 376-378.
Lorch, J. M., L. K. Muller, R. E. Russell, M. O'Connor, D. L. Lindner et D. S. Blehert. 2013. Distribution and environmental persistence of the causative agent of white-nose syndrome, Geomyces destructans, in bat hibernacula of the eastern United States. Applied and Environmental Microbiology 79(4): 1293-1301.
Loss, S. R., T. Will et P. P. Marra. 2013. The impact of free-ranging domestic cats on wildlife of the United States. Nature 4: 1396.
Loyd, K. A. T., S. M. Hernandez, J. P. Carroll, K. J. Abernathy et G. J. Marshall. 2013. Quantifying free-roaming domestic cat predation using animal-borne video cameras. Biological Conservation 160(0): 183-189.
MacGregor, C. J., M. J. Pocock, R. Fox et D. M. Evans. 2015. Pollination by nocturnal Lepidoptera, and the effects of light pollution: a review. Ecological Entomology 40(3): 187-198.
Maher, S. P., A. M. Kramer, J. T. Pulliam, M. A. Zokan, S. E. Bowden, H. D. Barton, K. Magori et J. M. Drake. 2012. Spread of white-nose syndrome on a network regulated by geography and climate. Nature 3: 1306.
Main, A. R., J. V. Headley, K. M. Peru, N. L. Michel, A. J. Cessna et C. A. Morrissey. 2014. Widespread use and frequent detection of neonicotinoid insecticides in wetlands of Canada's prairie pothole region. PLoS One 9(3): e92821.
Mainguy, J. et N. Desrosiers. 2011. Cave-dwelling bats in the province of Quebec: historical data about hibernacula population surveys. Ministère des Ressources naturelles et de la Faune, QC.
Masek, J. G., W. B. Cohen, D. Leckie, M. A. Wulder, R. Vargas, B. de Jong, S. Healey, B. Law, R. Birdsey et R. Houghton. 2011. Recent rates of forest harvest and conversion in North America. Journal of Geophysical Research: Biogeosciences (2005–2012) 116(G4).
Maslo, B., M. Valent, J. F. Gumbs et W. F. Frick. 2015. Conservation implications of ameliorating survival of little brown bats with white-nose syndrome. Ecological Applications 25(7): 1832-1840.
Mason, R., H. Tennekes, F. Sánchez-Bayo et P. U. Jepsen. 2013. Immune suppression by neonicotinoid insecticides at the root of global wildlife declines. Journal of Environmental Immunology Toxicology 1(1): 3-12.
Mathews, F., N. Roche, T. Aughney, N. Jones, J. Day, J. Baker et S. Langton. 2015. Barriers and benefits: implications of artificial night-lighting for the distribution of common bats in Britain and Ireland. Philosophical Transactions of the Royal Society of London B: Biological Sciences 370(1667): 20140124.
Mattson, W. J. et R. A. Haack. 1987. The role of drought in outbreaks of plant-eating insects. BioScience: 110-118.
McAlpine, D. F. 1983. Status and conservation of solution caves in New Brunswick. The New Brunswick Museum, St. John, NB.
McCracken, G. F. 2011. Cave conservation: special problems of bats. Pages 68-95 In J. Tyburec, J. Chenger, T. Snow et C. Geiselman, eds. Bat Conservation International: Bat Conservation and Management Workshop. Bat Conservation International, Portal, AZ.
McLeod, B. A., L. E. Burns, T. Frasier et H. Broders. 2015. Effect of oceanic straits on gene flow in the recently endangered little brown bat (Myotis lucifugus) in maritime Canada: implications for the spread of white-nose syndrome. Canadian Journal of Zoology 93(999): 427-437.
Medinas, D., J. T. Marques et A. Mira. 2013. Assessing road effects on bats: the role of landscape, road features, and bat activity on road-kills. Ecological Research 28(2): 227-237.
Meteyer, C. U., E. L. Buckles, D. S. Blehert, A. C. Hicks, D. E. Green, V. Shearn-Bochsler, N. J. Thomas, A. Gargas et M. J. Behr. 2009. Histopathologic criteria to confirm white-nose syndrome in bats. Journal of Veterinary Diagnostic Investigation 21(4): 411-414.
Moosman, P. R., H. H. Thomas et J. P. Veilleux. 2012. Diet of the widespread insectivorous bats Eptesicus fuscus and Myotis lucifugus relative to climate and richness of bat communities. Journal of Mammalogy 93(2): 491-496.
Morrissey, C. A., P. Mineau, J. H. Devries, F. Sanchez-Bayo, M. Liess, M. C. Cavallaro et K. Liber. 2015. Neonicotinoid contamination of global surface waters and associated risk to aquatic invertebrates: A review. Environment International 74: 291-303.
Murphy, M. 1987. Vandals destroy hibernating Indiana Bats. BATS Magazine 5(2): 5-8.
Nagorsen, D. et R. Brigham. 1993. Bats of British Columbia: Royal British Columbia museum handbook. University of British Columbia Press, Vancouver, BC.
NASBR. 2015. North American Society for Bat Research. Ypsilanti, MI. [consulté le 1er octobre 2015].
Natureserve. 2015. NatureServe Explorer: An online encyclopedia of life [application Web]. Version 7.0. Natureserve, Arlington, VA. U.S.A. [consulté le 20 avril 2015].
Naughton, D. 2012. The Natural History of Canadian Mammals. University of Toronto Press. Toronto, ON. 784 pp.
Neilson, A. L. et M. B. Fenton. 1994. Responses of little brown myotis to exclusion and to bat houses. Wildlife Society Bulletin: 8 14.
NFD. 2014. National Forestry Database. Natural Resources Canada and Canadian Forest Service, Ottawa, ON. [consulté le 20 août 2014]. (Également disponible en français : BDNF. 2014. Base de données nationale sur les forêts, Ressources naturelles Canada et le Service canadien des forêts, Ottawa (Ont.).)
Norquay, K. J. O., F. Martinez Nunez, J. E. Dubois, K. M. Monson et C. K. R. Willis. 2013. Long distance movements of little brown bats (Myotis lucifugus). Journal of Mammalogy 94(2): 506 515.
Northeast Bat Working Group. 2015. Northeast Bat Working Group. [consulté le 22 avril 2015].
O'Regan, S. M., K. Magori, J. T. Pulliam, M. A. Zokan, R. R. B. Kaul, H. D. Barton et J. M. Drake. 2014. Multi-scale model of epidemic fadeout: Will local extirpation events inhibit the spread of white-nose syndrome? Ecological Applications 25: 621-633.
O’Donoghue, A. J., G. M. Knudsen, C. Beekman, J. A. Perry, A. D. Johnson, J. L. DeRisi, C. S. Craik et R. J. Bennett. 2015. Destructin-1 is a collagen-degrading endopeptidase secreted by Pseudogymnoascus destructans, the causative agent of white-nose syndrome. Proceedings of the National Academy of Sciences: 201507082.
Okoniewski, J., J. Haines, A. Hicks, K. Langwig, R. VonLinden et C. Dobony. 2010. Detection of the conidia of Geomyces destructans in northeast hibernacula, at maternal colonies, and on gear – some findings based on microscopy and culture. Page 18 WNS Symposium, Pittsburg, Pennsylvania.
Olson, C. R. 2011. The roosting behaviour of Little Brown Bats (Myotis lucifugus) and Northern Long-eared Bats (Myotis septentrionalis) in the boreal forest of northern Alberta. University of Calgary, Calgary, AB.
Olson, C. R. et R. M. Barclay. 2013. Concurrent changes in group size and roost use by reproductive female little brown bats (Myotis lucifugus). Canadian Journal of Zoology 91(3): 149-155.
Olson, C. R., D. P. Hobson et M. J. Pybus. 2011. Changes in population size of bats at a hibernaculum in Alberta, Canada, in relation to cave disturbance and access restrictions. Northwestern Naturalist 92(3): 224-230.
OMNRF. 2015. Ontario: Species at Risk. [consulté le 3 mai 2015]. (Également disponible en français : MRNFO. 2015. Ontario : Espèces en péril.)
Ontario Ministry of Natural Resources. 2010. Forest Management Guide for Conserving Biodiversity at the Stand and Site Scales. Ontario Ministry of Natural Resources, Ontario.
Ontario Ministry of Natural Resources and Forestry. 2015. Ontario's White-nose Syndrome Response Plan. Wildlife Section, Species Conservation Policy Branch, Ontario.
Owen, S. F., M. A. Menzel, W. M. Ford, B. R. Chapman, K. V. Miller, J. W. Edwards et P. B. Wood. 2003. Home-range size and habitat used by the northern myotis (Myotis septentrionalis). The American Midland Naturalist 150(2): 352-359.
Park, A. C. et H. G. Broders. 2012. Distribution and roost selection of bats on Newfoundland. Northeastern Naturalist 19(2): 165-176.
Patriquin, K. J., F. Palstra, M. L. Leonard et H. G. Broders. 2013. Female northern myotis (Myotis septentrionalis) that roost together are related. Behavioral Ecology 24(4): 949-954.
Pauli, B., P. Zollner, G. Haulton et G. Shao. 2015. The simulated effects of timber harvest on suitable habitat for Indiana and northern long-eared bats.
Perkin, E. K., F. Hölker et K. Tockner. 2014. The effects of artificial lighting on adult aquatic and terrestrial insects. Freshwater Biology 59(2): 368-377.
Perry, R. et R. Thill. 2007. Tree roosting by male and femal eastern pipistrelles in a forested landscape. Journal of Mammalogy 88: 974-981.
Pikula, J., H. Bandouchova, L. Novotný, C. U. Meteyer, J. Zukal, N. R. Irwin, J. Zima et N. Martínková. 2012. Histopathology confirms white-nose syndrome in bats in Europe. Journal of Wildlife Diseases 48(1): 207-211.
Poissant, J. 2009. Roosting and social ecology of the tri-colored bat, Perimyotis subflavus, in Nova Scotia. St. Mary's University, Halifax, NS.
Poissant, J. A., H. G. Broders et G. M. Quinn. 2010. Use of lichen as a roosting substrate by Perimyotis subflavus, the tricolored bat, in Nova Scotia. Ecoscience 17(4): 372-378.
Porvari, P., M. Verta, J. Munthe et M. Haapanen. 2003. Forestry practices increase mercury and methyl mercury output from boreal forest catchments. Environmental Science and Technology 37(11): 2389-2393.
Powers, L., E. Pritchard, K. Lau et B. Francis. 2012. Does Geomyces destructans infection reduce female fertility in Myotis lucifugus? North America Symposium on Bat Research, Puerto Rico.
Pybus, M., D. Hobson et D. Onderka. 1986. Mass mortality of bats due to probable blue-green algal toxicity. Journal of Wildlife Diseases 22(3): 449-450.
Quinn, G. M. et H. G. Broders. 2007. Roosting and foraging ecology of eastern pipistrelle (Perimyotis subflavus) bats in SW Nova Scotia. Nova Scotia Habitat Conservation Fund c/o NS Department of Natural Resources, Halifax, NS.
Raesly, R. L. et J. E. Gates. 1987. Winter habitat selection by north temperate cave bats. American Midland Naturalist: 15-31.
Randall, J. et H. G. Broders. 2014. Identification and characterization of swarming sites used by bats in Nova Scotia, Canada. Acta Chiropterologica 16(1): 109-116.
Randall, L. A., T. S. Jung et R. M. Barclay. 2014. Roost-site selection and movements of Little Brown Myotis (Myotis lucifugus) in southwestern Yukon. Northwestern Naturalist 95(3): 312-317.
Ratcliffe, J. M. et J. W. Dawson. 2003. Behavioural flexibility: the little brown bat, Myotis lucifugus, and the northern long-eared bat, M. septentrionalis, both glean and hawk prey. Animal Behaviour 66(5): 847-856.
Raudabaugh, D. B. et A. N. Miller. 2015. Effects of trans, trans-farnesol on Pseudogymnoascus destructans and several closely related species. Mycopathologia.
Reeder, D. et G. Turner. 2008. Working together to combat white-nose syndrome: a report of a meeting on 9–11 June 2008. Bat Research News 49(7).
Reeder, D. M., C. L. Frank, G. G. Turner, C. U. Meteyer, A. Kurta, E. R. Britzke, M. E. Vodzak, S. R. Darling, C. W. Stihler et A. C. Hicks. 2012. Frequent arousal from hibernation linked to severity of infection and mortality in bats with white-nose syndrome. PLoS One 7(6): e38920.
Reichard, J. D., N. W. Fuller, A. B. Bennett, S. R. Darling, M. S. Moore, K. E. Langwig, E. D. Preston, S. v. Oettingen, C. S. Richardson et D. Scott Reynolds. 2014. Interannual survival of Myotis lucifugus (Chiroptera: Vespertilionidae) near the epicenter of white-nose syndrome. Northeastern Naturalist 21(4): N56-N59.
Reichard, J. D. et T. H. Kunz. 2009. White-nose syndrome inflicts lasting injuries to the wings of little brown myotis (Myotis lucifugus). Acta Chiropterologica 11(2): 457-464.
Reimer, J. et L. Kaupas. 2013. South Slave region bat research summary 2013: University of Calgary. Environment and Natural Resources, Government of Northwest Territiories, Fort Smith, NT.
Reimer, J. P. 2013. Nocturnality under the mignight sun: behavioural adaptations of the little brown bat (Myotis lucifugus) at 60° N latitude, Calgary, AB.
Ren, P., K. H. Haman, L. A. Last, S. S. Rajkumar, M. K. Keel et V. Chaturvedi. 2012. Clonal spread of Geomyces destructans among bats, Midwestern and Southern United States. Emergent Infectious Disease 18(5): 883-885.
Reynolds, D. S. 2006. Monitoring the potential impact of a wind development site on bats in the northeast. Journal of Wildlife Management 70(5): 1219-1227.
Rollins, K. E., D. K. Meyerholz, G. D. Johnson, A. P. Capparella et S. S. Loew. 2012. A forensic investigation into the etiology of bat mortality at a wind farm: barotrauma or traumatic injury? Veterinary Pathology Online 49(2): 362-371.
Russell, A., M. Vonhof et E. Claire. 2012. Phylogeographic analyses reveal cryptic subdivisions and unexpected connections among Myotis lucifugus populations. North America Symposium on Bat Research, Puerto Rico.
Rydell, J., L. Bach, P. Bach, L. G. Diaz, J. Furmankiewicz, N. Hagner-Wahlsten, E.-M. Kyheröinen, T. Lilley, M. Masing et M. M. Meyer. 2014. Phenology of migratory bat activity across the Baltic Sea and the south-eastern North Sea. Acta Chiropterologica 16(1): 139-147.
Sandel, J. K., G. R. Benatar, K. M. Burke, C. W. Walker, J. Lacher, Thomas E et R. L. Honeycutt. 2001. Use and selection of winter hibernacula by the eastern pipistrelle (Pipistrellus subflavus) in Texas. Journal of Mammalogy 82(1): 173-178.
Sasse, D. et P. Perkins. 1996. Summer roosting ecology of northern long-eared bats (Myotis septentrionalis) in the White Mountain National Forest. Pages 91-101 In Bats and Forests Symposium. British Columbia Ministry of Forests Victoria, BC.
Scott, F. W. et A. J. Hebda. 2004. Annotated list of the mammals of Nova Scotia. Proceedings of the Nova Scotian Institute of Science (NSIS) 42(2).
Segers, J. et H. Broders. 2014. Interspecific effects of forest fragmentation on bats. Canadian Journal of Zoology 92(8): 665-673.
Segers, J. L. et H. G. Broders. 2015. Carbon (δ 13 C) and nitrogen (δ 15 N) stable isotope signatures in bat fur indicate swarming sites have catchment areas for bats from different summering areas. PLoS One 10(4): e0125755.
Sherwin, H. A., W. I. Montgomery et M. G. Lundy. 2013. The impact and implications of climate change for bats. Mammal Review 43(3): 171-182.
Silvis, A., W. M. Ford et E. R. Britzke. 2015a. Day-roost tree selection by northern long-eared bats--What do non-roost tree comparisons and one year of data really tell us? Global Ecology and Conservation 3(0): 756-763.
Silvis, A., W. M. Ford et E. R. Britzke. 2015b. Effects of hierarchical roost removal on Northern Long-Eared Bat (Myotis septentrionalis) maternity colonies. PLoS One 10(1).
Sivonen, K. et G. Jones. 1999. Cyanobacterial toxins. Pages 41-111 In I. Chorus et J. Bartram (eds.). Toxic Cyanobacteria in Water, a Guide to Their Public Health Consequences, Monitoring and Management. Spon Press. New York, NY.
Slough, B. G. 2009. Behavioral thermoregulation by a maternity colony of little brown bats in the Yukon. Northwestern Naturalist: 47-51.
Slough, B. G. et T. S. Jung. 2007. Diversity and distribution of the terrestrial mammals of the Yukon Territory: A review. The Canadian Field-Naturalist 121(2): 119-127.
Slough, B. G. et T. S. Jung. 2008. Observations on the natural history of bats in the Yukon. Northern Review(29): 127-150.
Smallwood, K. S. 2013. Comparing bird and bat fatality rate estimates among North American wind energy projects. Wildlife Society Bulletin 37(1): 19-33.
Smith, J. L., G. L. Boyer, E. Mills et K. L. Schiulz. 2008. Toxicity of microcystin-LR, a cyanobacterial toxin, to multiple life stages of the burroeing mayfly, Hexagenia, and possible implications for recruitment. Environmental Toxicoloogy 23(4): 499-506.
Spanjer, G. R. et M. B. Fenton. 2005. Behavioral responses of bats to gates at caves and mines. Wildlife Society Bulletin 33(3): 1101-1112.
Sparks, T. C. 2013. Insecticide discovery: an evaluation and analysis. Pesticide biochemistry and physiology 107(1): 8-17.
Speakman, J., P. Webb et P. Racey. 1991. Effects of disturbance on the energy expenditure of hibernating bats. Journal of Applied Ecology: 1087-1104.
SSM. 2015. Speleological Society of Manitoba. Speleological Society of Manitoba. [consulté le 16 juillet 2015].
Stone, E. L., G. Jones et S. Harris. 2009. Street lighting disturbs commuting bats. Current Biology 19(13): 1123-1127.
Stone, E. L., G. Jones et S. Harris. 2012. Conserving energy at a cost to biodiversity? Impacts of LED lighting on bats. Global Change Biology 18(8): 2458-2465.
Swystun, M. B., J. M. Psyllakis et R. M. Brigham. 2001. The influence of residual tree patch isolation on habitat use by bats in central British Columbia. Acta Chiropterologica 3(2): 197-201.
Syme, D. M., M. B. Fenton et J. Zigouris. 2001. Roosts and food supplies ameliorate the impact of a bad summer on reproduction by the bat, Myotis lucifugus LeConte (Chiroptera: Vespertilionidae). Ecoscience: 18-25.
Talerico, J. M. 2008. The behaviour, diet and morphology of the little brown bat (Myotis lucifugus) near the northern extent of its range in Yukon Canada. University of Calgary, Calgary, AB.
Thomas, D. W. 1995. Hibernating bats are sensitive to nontactile human disturbance. Journal of Mammalogy 76(3): 940-946.
Thomas, D. W., M. Dorais et J.-M. Bergeron. 1990. Winter energy budgets and cost of arousals for hibernating little brown bats, Myotis lucifugus. Journal of Mammalogy: 475-479.
Thomas, H. H., P. R. Moosman, J. P. Veilleux et J. Holt. 2012. Foods of bats (Family Vespertilionidae) at five locations in New Hampshire and Massachusetts. The Canadian Field-Naturalist 126(2): 117-124.
Thorne, T. J. 2015. The role of islands in the migration of bats across Lake Erie and Lake Ontario: Lasiurus borealis, Lasiurus cinereus and Perimyotis subflavus. The University of Western Ontario, London, ON.
Trombulak, S. C., P. E. Higuera et M. DesMeules. 2001. Population trends of wintering bats in Vermont. Northeastern Naturalist 8(1): 51-62.
Turner, G. G., D. Reeder et J. T. Coleman. 2011. A five-year assessment of mortality and geographic spread of white-nose syndrome in North American bats, with a look at the future. Update of white-nose syndrome in bats. Bat Research News: 13.
Turner, R. W. 1974. Mammals of the Black Hills of South Dakota and Wyoming. University of Kansas. Lawrence, KS. pp.
U.S. Fish and Wildlife Service. 2007. Indiana Bat (Myotis sodalis) draft recovery plan: first revision. U.S. Fish and Wildlife Service, Fort Snelling, MN.
U.S. Fish and Wildlife Service. 2012. North American bat death toll exceeds 5.5 million from white-nose syndrome. U.S. Fish and Wildlife Service, Arlington, VA.
U.S. Fish and Wildlife Service. 2015. White-nose Syndrome. Hadley, MA. [consulté le 3 mai 2015].
U.S. Geological Survey. 2000. Mercury in the environment, fact sheet 146-00. [consulté en août 2014].
USDA. 2015. U.S. Forest Service Research Team Releases Bats Treated for WNS. [consulté le 6 juillet 2015].
van Zyll de Jong, C. G. 1985. Handbook of Canadian Mammals: Bats. National Museum of Natural Sciences. Ottawa, ON. 212 pp. (Également disponible en français : Van Zyll de Jong, C. G. 1985. Traité des mammifères du Canada - Les chauves-souris, Musée national des sciences naturelles, Ottawa (Ont.), 215 p.).
Vanderwolf, K. J., D. F. McAlpine, G. J. Forbes et D. Malloch. 2012. Bat populations and cave microclimate prior to and at the outbreak of white-nose syndrome in New Brunswick. The Canadian Field-Naturalist 126(2): 125-134.
Veilleux, J. P. et S. L. Veilleux. 2004. Intra-annual and interannual fidelity to summer roost areas by female eastern pipistrelles, Pipistrellus subflavus. The American Midland Naturalist 152(1): 196-200.
Veilleux, J. P., J. O. Whitaker Jr et S. L. Veilleux. 2003. Tree-roosting ecology of reproductive female eastern pipistrelles, Pipistrellus subflavus, in Indiana. Journal of Mammalogy 84(3): 1068-1075.
Verant, M. L., M. U. Carol, J. R. Speakman, P. M. Cryan, J. M. Lorch et D. S. Blehert. 2014. White-nose syndrome initiates a cascade of physiologic disturbances in the hibernating bat host. BMC Physiology 14(1): 10.
Vuori, K.-M., O. Siren et H. Luotonen. 2003. Metal contamination of streams in relation to catchment silvicultural practices: a comparative study in Finnish and Russian headwaters. Boreal Environment Research 8(1): 61-70.
Warnecke, L., J. M. Turner, T. K. Bollinger, J. M. Lorch, V. Misra, P. M. Cryan, G. Wibbelt, D. S. Blehert et C. K. Willis. 2012. Inoculation of bats with European Geomyces destructans supports the novel pathogen hypothesis for the origin of white-nose syndrome. Proceedings of the National Academy of Sciences 109(18): 6999-7003.
Warnecke, L., J. M. Turner, T. K. Bollinger, V. Misra, P. M. Cryan, D. S. Blehert, G. Wibbelt et C. K. Willis. 2013. Pathophysiology of white-nose syndrome in bats: a mechanistic model linking wing damage to mortality. Biology Letters 9(4): 20130177.
Webb, P., J. Speakman et P. Racey. 1995. Evaporative water loss in two sympatric species of vespertilionid bat, Plecotus auritus and Myotis daubentoni: relation to foraging mode and implications for roost site selection. Journal of Zoology 235(2): 269-278.
Western Bat Working Group. 2015. Western Bat Working Group. [consulté le 22 avril 2015].
Whitaker, J. O. et L. J. Rissler. 1993. Do bats feed in winter? American Midland Naturalist: 200-203.
Wibbelt, G., A. Kurth, D. Hellmann, M. Weishaar, A. Barlow, M. Veith, J. Prüger, T. Görföl, L. Grosche et F. Bontadina. 2010. White-nose syndrome fungus (Geomyces destructans) in bats, Europe. Emerging Infectious Diseases 16(8): 1237.
Wickramasinghe, L. P., S. Harris, G. Jones et N. Vaughan. 2003. Bat activity and species richness on organic and conventional farms: impact of agricultural intensification. Journal of Applied Ecology 40(6): 984-993.
Wiener, J. G., D. P. Krabbenhoft, G. H. Heinz et A. M. Scheuhammer. 2003. Ecotoxicology of mercury. Pages 409-463 In D. J. Hoffman, B. A. Rattner, G. A. Burton, Jr. et J. Cairns, Jr. (eds.). Handbook of Ecotoxicology, 2nd Edition. CRC Press. Boca Raton, FL.
Wilder, A. P. 2014. Spatial, ecological and genetic correlates of the geographic expansion of an infectious disease, white-nose syndrome in bats. University of California, Santa Cruz, CA.
Willis, C. K. et R. M. Brigham. 2007. Social thermoregulation exerts more influence than microclimate on forest roost preferences by a cavity-dwelling bat. Behavioral Ecology and Sociobiology 62(1): 97-108.
Wilson, J. M. et R. M. Barclay. 2006. Consumption of caterpillars by bats during an outbreak of western spruce budworm. The American Midland Naturalist 155(1): 244-249.
Wilson, J. M., J. P. Reimer, D. Allaire et C. L. Lausen. 2014. Diversity and distribution of bats in the Northwest Territories. Northwestern Naturalist 95(3): 197-218.
Woller-Skar, M. M., D. N. Jones, M. R. Luttenton et A. L. Russell. 2015. Mycrocystin detected in little brown bats (Myotis lucifugus). The American Midland Naturalist 174(2): 331-334.
Xing, Z., L. Chow, H. Rees, F. Meng, S. Li, B. Ernst, G. Benoy, T. Zha et L. M. Hewitt. 2013. Influences of sampling methodologies on pesticide-residue detection in stream water. Archives of Environmental Contamination and Toxicology 64(2): 208-218.
Yates, D. E., E. M. Adams, S. E. Angelo, D. C. Evers, J. Schmerfeld, M. S. Moore, T. H. Kunz, T. Divoll, S. T. Edmonds et C. Perkins. 2014. Mercury in bats from the northeastern United States. Ecotoxicology 23(1): 45-55.
Young, J. E., G. A. Sánchez-Azofeifa, S. J. Hannon et R. Chapman. 2006. Trends in land cover change and isolation of protected areas at the interface of the southern boreal mixedwood and aspen parkland in Alberta, Canada. Forest Ecology and Management 230(1–3): 151-161.
Zimmerman, G. S. et W. E. Glanz. 2000. Habitat use by bats in eastern Maine. The Journal of Wildlife Management 64(4): 1032-1040.
Communications personnelles
Blejwas, K. 2015. Biologiste régional de la faune, Alaska Department of Fish and Game, Juneau (Alaska).
Brigham, M. 2015. Professeur, University of Regina, Regina (Saskatchewan)
Broders, H. 2015. Professeur agrégé, St. Mary’s University, Halifax (Nouvelle-Écosse).
Govindarajulu, P. 2015. Amphibian, Reptile, and Small Mammal Specialist, British Columbia Ministry of Environment, Victoria (Colombie-Britannique).
Jung, T. 2015. Biologiste principal de la faune, Whitehorse (Yukon).
Lausen, C. 2015. Birchdale Ecological Ltd, Kaslo (Colombie-Britannique).
Morningstar, D. 2015. Terrestrial Ecologist, Golder Associates Ltd, Cambridge (Ontario).
Pardy Moores, S. 2015. Gestionnaire principal – Endangered Species and Biodiversity, Department of Environment and Conservation, Cornerbrook (Terre-Neuve)
Annexe A : Effets sur l’environnement et sur les espèces non ciblées
Une évaluation environnementale stratégique (EES) est effectuée pour tous les documents de planification du rétablissement en vertu de la LEP conformément à la Directive du Cabinet sur l’évaluation environnementale des projets de politiques, de plans et de programmes. L’objet de l’EES est d’incorporer les considérations environnementales à l’élaboration des projets de politiques, de plans et de programmes publics pour appuyer une prise de décisions éclairée du point de vue de l’environnement et d’évaluer si les résultats d’un document de planification du rétablissement peuvent affecter un élément de l’environnement ou tout objectif ou cible de la Stratégie fédérale de développement durable (SFDD).
La planification du rétablissement vise à favoriser les espèces en péril et la biodiversité en général. Il est cependant reconnu que des programmes peuvent, par inadvertance, produire des effets environnementaux qui dépassent les avantages prévus. Le processus de planification fondé sur des lignes directrices nationales tient directement compte de tous les effets environnementaux, notamment des incidences possibles sur des espèces ou des habitats non ciblés. Les résultats de l’EES sont directement inclus dans le programme lui-même, mais également résumés dans le présent énoncé, ci-dessous.
Le SMB touche d’autres espèces de chauves-souris qui ne sont pas considérées dans le présent programme de rétablissement (p. ex. chauve-souris pygmée [Myotis leibii]) (U.S. Fish and Wildlife Service, 2015). Toute approche qui atténue l’impact ou la propagation du SMB sera donc fort probablement avantageuse pour ces autres espèces. Il est toutefois possible que d’autres espèces de chauves-souris dont les populations sont peu touchées par le SMB (p. ex. grande chauve-souris brune [Eptesicus fuscus]) profitent du déclin des populations de petites chauves-souris brunes, de chauves-souris nordiques et de pipistrelles de l’Est en occupant la niche écologique qui est vacante depuis peu (Francl et al., 2012). On ne sait pas comment le rétablissement des trois espèces en péril touchera ces autres espèces de chauves-souris dont les populations ont augmenté récemment.
Bon nombre des menaces possibles définies dans le présent programme de rétablissement représentent aussi des menaces pour d’autres espèces en péril. Les approches visant à réduire au minimum ces menaces pourraient également profiter à d’autres espèces. Ainsi, le Quiscale rouilleux (Euphagus carolinus) serait sensible à la contamination par le mercure dans l’est du Canada (Edmonds et al., 2010), et les chats domestiques laissés en liberté ou retournés à l’état sauvage sont considérés comme une menace potentielle pour de nombreuses espèces d’oiseaux (Calvert et al., 2013), notamment d’autres espèces en péril, comme l’Engoulevent d’Amérique (Chordeiles minor) (Environment Canada, 2015b). La conservation des forêts autour des hibernacles et des sites de repos peut être bénéfique pour d’autres espèces (à l’échelle locale) qui sont menacées elles aussi par l’élimination des forêts (p. ex. Paruline du Canada [Cardellina canadensis]) (Environment Canada, 2015a).
Les populations de chauves-souris consomment des quantités considérables d’insectes chaque nuit et limitent donc les populations d’insectes à l’échelle locale. Les initiatives qui contribuent au rétablissement des populations de chauves-souris pourraient causer, à l’échelle locale, des déclins des populations d’insectes (dont certaines ont déjà subi des déclins spectaculaires) (Dirzo et al., 2014). En revanche, les stratégies dans le cadre desquelles on évalue le déclin des insectes proies, mène des recherches, atténue les menaces mutuelles potentielles ou sensibilise le public au sujet de ces menaces peuvent favoriser le rétablissement des populations d’insectes possiblement appauvries.
La possibilité que le présent programme de rétablissement entraîne des effets négatifs imprévus sur l’environnement et sur d’autres espèces a été examinée. La majorité des mesures recommandées sont non intrusives, y compris les relevés, les recherches et les activités de sensibilisation du public. Ce programme de rétablissement est peu susceptible de produire d’importants effets négatifs.
Annexe B : Autres besoins en matière d’études des menaces connues et présumées
La liste suivante présente certaines des études nécessaires pour comprendre les menaces (autres que le SMB) pesant sur la petite chauve-souris brune, la chauve-souris nordique et la pipistrelle de l’Est et leur habitat.
Perturbation ou dommage
- Déterminer les effets de différents niveaux et types de bruit sur le comportement et la biologie des chauves-souris tout au long de leur cycle vital.
- Déterminer les effets des activités de recherche sur le stress et la survie des chauves-souris.
- Examiner davantage l’emplacement et les caractéristiques des éoliennes au Canada qui sont susceptibles de toucher considérablement les populations de chauves-souris.
- Étudier de manière approfondie le réglage des éoliennes et leurs effets à l’échelle des populations.
- Continuer à faire un suivi de la fréquence des collisions avec des éoliennes au Canada et élaborer un programme de suivi systématique des parcs éoliens dans toute l’aire de répartition des chauves-souris.
- Étudier les effets et les caractéristiques des collisions entre des chauves-souris et des véhicules au Canada.
- Étudier les effets des collisions de chauves-souris avec des véhicules et des appareils non traditionnels/récréatifs (p. ex. bateaux, véhicules aériens sans pilote, et lignes de pêche).
Perte ou dégradation de l’habitat
- Déterminer les effets des activités forestières courantes (p. ex. sylviculture et coupe sélective) sur la disponibilité des arbres pouvant servir de sites de repos, et sur le comportement, la biologie et les déplacements des chauves-souris dans toute leur aire de répartition.
- Établir les superficies (et les caractéristiques) de récolte forestière, d’exploitation forestière et de sylviculture qui permettent de conserver suffisamment d’habitat convenable pour les populations de chauves-souris dans toute leur aire de répartition.
- Continuer à évaluer les effets de la fragmentation des forêts associée à diverses sources (p. ex. agriculture et construction de routes).
- Étudier l’importance de la perte d’habitat causée par des infestations d’insectes (p. ex. dendroctone du pin ponderosa).
- Étudier davantage les effets de l’exclusion des colonies de maternité des structures anthropiques.
- Étudier davantage l’utilisation de dortoirs pour atténuer la perte de structures anthropiques ou naturelles servant de sites de repos.
Pollution
- Étudier davantage l’exposition des chauves-souris au mercure et à d’autres polluants dans leur aire de répartition.
- Déterminer les effets possibles du mercure sur la biologie, la survie et le comportement des chauves-souris.
- Établir les effets des néonicotinoïdes et d’autres pesticides largement utilisés sur les chauves-souris.
- Préciser les effets sur les chauves-souris des techniques visant à réduire la propagation de la tordeuse des bourgeons de l’épinette.
- Déterminer les effets de la pollution lumineuse sur le comportement des chauves-souris, leur efficacité de recherche de nourriture et leurs proies.
Espèces non indigènes problématiques
- Déterminer le risque de prédation lié aux humains dans les zones urbaines et rurales (p. ex. prédation par les chats).
Climat et catastrophes naturelles
- Déterminer les impacts des changements climatiques sur ces espèces de chauves-souris, leurs proies et leur habitat.
- Étudier les impacts potentiels des infestations d’insectes et des feux de forêt sur ces espèces de chauves-souris, leurs proies et leur habitat.