Document d'orientation sur la classification des médicaments vétérinaires et des aliments du bétail
Table des matières
- 1. Introduction
- 2. Portée et application
- 3. Principes directeurs
- 4. Critères de classification
- 5. Processus de décision de classification
- 6. Mise en application
Liste des annexes
- Annexe A - Troubles nutritionnels
- Annexe B - Diagramme de classification Médicament vs Aliment
- Annexe C - Liste des ingrédients médicinaux connus
- Annexe D - Indications (ou allégations) relatives au stress
- Annexe E 1 - Agents de détoxification des mycotoxines (ADM)
- Annexe E-2 : Produits microbiens viables (PMV)
- Annexe E-3 : Produits à base d'acide
1. Introduction
1.1 Renseignements généraux
Au Canada, les produits consommés par les animaux d'élevage sont réglementés en grande partie comme des médicaments vétérinaires ou des aliments du bétail.
Les médicaments vétérinaires (ci-après désignés sous le nom de «médicaments») sont réglementés par Santé Canada en vertu de la Loi et du Règlement sur les aliments et drogues. À Santé Canada, la Direction des médicaments vétérinaires (DMV) a pour mandat d'évaluer et de surveiller l'innocuité, la qualité et l'efficacité, d'établir des normes et de promouvoir l'usage prudent des médicaments vétérinaires, y compris les produits de santé naturels vétérinaires, administrés aux animaux destinés à l'alimentation et de compagnie. La classification d'un produit établie par la DMV est dictée par les exigences de la Loi et du Règlement sur les aliments et drogues.
Les aliments du bétail (ci-après désignés sous le nom d'«aliments») sont réglementés en vertu de la Loi relative aux aliments du bétail et du Règlement sur les aliments du bétail, administrés par l'Agence canadienne d'inspection des aliments (ACIA). L'ACIA vérifie que les aliments fabriqués et vendus au Canada ou importés sont salubres, efficaces et bien étiquetés. Des aliments efficaces assurent la production et la santé du bétail.
1.2 Définitions
Conformément à la Loi sur les aliments et drogues, sont compris parmi les «drogues» (ou médicaments) les substances ou mélanges de substances fabriqués, vendus ou présentés comme pouvant servir :
- au diagnostic, au traitement, à l'atténuation ou à la prévention d'une maladie, d'un désordre, d'un état physique anormal ou de leurs symptômes, chez l'être humain ou les animaux;
- à la restauration, à la correction ou à la modification des fonctions organiques chez l'être humain ou les animaux;
- à la désinfection des locaux où des aliments sont gardés.
Conformément à la Loi sur les aliments du bétail, un «aliment» est défini comme les substances ou mélanges de substances renfermant notamment des acides aminés, des produits antioxydants, des glucides, des condiments, des enzymes, des lipides, des éléments minéraux, des produits azotés non protéiques, des protéines, des vitamines, des liants pour agglomérés, des colorants, des agents moussants ou des aromatisants, lorsque cette substance ou ce mélange est fabriqué ou vendu pour servir, directement ou après adjonction à une autre de ces substances ou de ces mélanges, aux fins suivantes, ou est décrit comme devant servir :
- à la consommation par des animaux de ferme;
- à l'alimentation des animaux de ferme;
- à empêcher ou corriger des troubles nutritionnels chez les animaux de ferme.
Une définition et une interprétation d'un trouble nutritionnel figurent à l'annexe A.
1.3 Contexte
Le chevauchement des définitions de ces deux types de produits pose un défi en ce sens que les produits nutritionnels et non nutritionnels peuvent être classés soit comme médicament, soit comme aliment, ou comme médicament et aliment. Par le passé, les difficultés liées à l'interprétation des définitions de médicament et d'aliment ont créé une grande confusion, qui a mené à des inefficacités à l'égard de l'évaluation et à l'approbation des produits, ainsi qu'aux activités de conformité et d'application de la loi. Il faut donc disposer d'un processus de classification clair et transparent pour certains produits destinés aux espèces d'élevage.
1.4 Buts et objectifs
Le présent document d'orientation vise à présenter des lignes directrices et des critères en matière de classification afin de préciser les différences entre les médicaments et les aliments du bétail et d'aider à déterminer la supervision réglementaire appropriée pour un produit destiné aux espèces d'élevage. Les objectifs visés sont les suivants :
- améliorer la transparence du processus de classification, améliorer la cohérence des décisions des organismes de réglementation et rendre ces dernières plus prévisibles auprès des intervenants;
- dissiper la confusion de l'industrie et fournir une meilleure orientation aux fabricants de tels produits quant à l'organisme réglementaire approprié, aux présentations et aux processus d'approbation d'un produit.
2. Portée et application
2.1 Portée
La méthode de classification exposée dans le présent document s'applique à une vaste gamme de produits devant uniquement être administrés par voie orale et destinés seulement aux animaux d'élevage (bovins laitiers et bovins de boucherie, moutons, poissons, chèvres, poulets, dindes, canards, oies, lapins, chevaux et porcs), ainsi qu'à différents types de production animale (p. ex., bovins laitiers et bovins de boucherie, poulets à griller et poules pondeuses). Dans certains cas, des produits ne tombent ni dans la catégorie des médicaments, ni dans la catégorie des aliments. Ces produits peuvent être classés (et ainsi réglementés) comme produits biologiques vétérinaires, instruments médicaux à usage vétérinaire, désinfectants, pesticides ou produits de consommation. Prenez note que ces types de produit dépassent la portée de cette orientation et qu'ils ne seront pas abordés plus en détail dans le présent document. Les aliments médicamenteux sont clairement définis dans la réglementation et sont également exclus de la portée du présent document d'orientation sur la classification.
2.2 Application
Le présent document d'orientation s'applique aux produits (médicaments et aliments) qui sont assujettis au processus d'évaluation préalable à la commercialisation (nouveaux produits) et aux produits existants vendus sur le marché canadien (produits dont la vente est autorisée). Le présent document doit être utilisé de concert avec d'autres outils réglementaires de Santé Canada (DMV) et de l'ACIA, tels que des politiques, des lignes directrices, des règlements et les annexes sur les aliments du bétail.
3. Principes directeurs
Pour que la classification d'un produit soit conforme aux deux mandats réglementaires, on appliquera les principes directeurs suivants :
- Le principal élément à prendre en compte sera le respect de la définition de drogue (ou médicament) dans la Loi sur les aliments et drogues et celle d'aliment dans la Loi relative aux aliments du bétail. L'orientation sera conforme aux objectifs de Santé Canada et de l'ACIA et à leur cadre réglementaire respectif, y compris la santé et la sécurité du public.
- Lors du processus de classification, il sera tenu compte des décisions de classification d'autres autorités réglementaires internationales vétérinaires.
- En règle générale, le risque potentiel pour la santé d'un ingrédient ou d'un produit ne constitue pas un facteur de classification - on prend en compte ce facteur durant l'évaluation de l'innocuité du produit (APRÈS sa classification). Les cadres réglementaires établis en vertu des lois sur les drogues (médicaments) et les aliments du bétail prévoient une série de mesures de contrôle pour atténuer les risques que présente un produit. Si ces risques sont jugés inacceptables, la vente de ce produit ne sera pas approuvée, sans égard à sa classification.
- La détermination de la classification d'un médicament ou d'un aliment peut découler de l'examen d'un seul des plus pertinents critères de classification énumérés ci-dessous, mais généralement, elle comprend l'examen de multiples critères pris dans leur ensemble.
- Selon le produit, certains critères n'ont peut-être pas la même valeur pour appuyer la décision relative à la classification.
- Certains produits peuvent présenter aussi bien une valeur nutritionnelle que thérapeutique, selon les différences de concentrations d'ingrédients, des recommandations posologiques/taux d'inclusion ou d'autres facteurs.
L'évaluation exhaustive de chacun des critères énoncés ci-dessous permet de cerner les différences entre médicaments et aliments en vue de faciliter la classification réglementaire. Pour obtenir une approche étape par étape du processus de classification, veuillez consulter le document Diagramme de classification Médicament vs Aliment (voir l'annexe B).
4. Critères de classification
4.1 Voie d'administration
Le fait qu'une substance ou un produit soit administré dans des aliments ou dans l'eau n'a pas d'incidence importante sur la classification réglementaire d'un produit.
4.2 Mode d'administration
4.2.1 Forme définitive du produit
La forme du produit fait référence à la forme définitive dans laquelle une substance ou un produit est disponible et prêt à être utilisé/administré, sans autre transformation. Les formes courantes des produits thérapeutiques (ou formes « posologiques ») comprennent les comprimés, les capsules, les bolus, les aérosols ou inhalateurs, les crèmes, les lotions, les solutions ou suspensions et les implants.
La forme d'un produit dépend habituellement de la voie d'administration de la substance en question. La plupart des produits sous forme posologique sont considérés comme des médicaments, à quelques exceptions près, en fonction d'autres critères (p. ex., objectif, étiquette). Les produits dont la forme permet une consommation volontaire (purée, liquide, agglomérés, flocons, blocs à volonté, etc.) sont généralement (mais non exclusivement) considérés comme des aliments.
4.2.2 Administration forcée
En règle générale, les produits par administration forcée (administrés oralement par gavages à l'aide d'un outil ou d'un instrument approprié) sont considérés comme des médicaments. Toutefois, certains produits administrés par un système de pompe ou de pâte avec une seringue non injectable qui :
- sont étiquetés pour inclusion dans l'aliment du bétail; et
- ne présentent aucune allégation médicamenteuse;
sont réglementés en vertu de la Loi relative aux aliments du bétail et du Règlement sur les aliments du bétail. Tous ces produits doivent indiquer sur l'étiquette la forme physique particulière du produit (p. ex., pâte) afin d'être considérés comme des aliments.
Tous les autres produits par administration forcée continueront d'être règlementés comme des médicaments.
4.3 Ingrédients médicinaux connus
De par leur nature, certains ingrédients sont intrinsèquement médicinaux ou thérapeutiques, soit en raison de leurs caractéristiques, de leur fonction (activité) et de leurs effets sur l'organisme, soit en raison de leur rôle dans la formulation. Par exemple, certaines substances comme la pénicilline, la néomycine, ou des extraits de plantes comme la digitaline ou la digoxine, ont une fonction ou activité thérapeutique intrinsèque. Ces connaissances découlent généralement de la littérature scientifique ou de manuels de référence. Dans le cas d'un produit à ingrédients multiples, si un ou plusieurs ingrédients de sa composition ont des vertus ou des effets thérapeutiques, le produit serait considéré comme un médicament. De plus, certains ingrédients végétaux ont un usage thérapeutique généralement reconnu et aucun usage nutritionnel. Ces types d'ingrédients végétaux sont considérés comme des ingrédients médicinaux et sont classés dans la catégorie des médicaments.
Pour vous aider à déterminer les ingrédients actuellement considérés comme étant de nature médicinale (thérapeutique), veuillez consulter l'annexe C pour obtenir la définition et la liste alphabétique des ingrédients médicinaux connus.
4.4 Représentation/but d'utilisation
Les éléments clés de la classification d'un produit sont la représentation (1) et le but d'utilisation (2) :
- La représentation d'un produit comprend des indications (qui peuvent être explicites ou implicites), des allégations relatives à la santé présentées sur l'étiquette par un mot, une phrase, une image, un symbole, un paragraphe ou une inférence, des prospectus de conditionnement ou des publicités (y compris de l'information disponible sur Internet), ainsi que son but et ses antécédents d'utilisation.
- Le but d'un produit est l'effet souhaité suivant son administration à une espèce animale en particulier, dans une situation particulière ou dans des conditions précises (p. ex., animal en santé ou malade, besoins nutritionnels). On tient également compte de l'activité ou des propriétés du ou des ingrédients présents dans un produit pour fournir de l'information sur l'effet visé (ou souhaité).
Ensemble, ces caractéristiques servent à créer une image claire de ce qu'est le produit et de ses vertus. Bien que le critère de « représentation d'utilisation » ne soit pas considéré comme le seul fondement sur lequel s'appuie une décision de classification, il peut être pris en considération et influencer la décision définitive, en raison de son incidence sur le but du produit. Par conséquent, une indication/allégation sur l'étiquette d'un produit ou dans le matériel publicitaire constitue un facteur important mais non déterminant à prendre en compte lors de la classification d'un produit.
Toutefois, les indications (ou allégations) présentes sur un produit, qu'elles soient ou non justifiables, seront utilisées pour déterminer l'organisme réglementaire approprié auquel une présentation devra être soumise. Pour les produits dont la classification entre médicaments et aliments est incertaine, les demandes doivent être soumises à la DMV, la porte d'accès en matière de classification.
Remarques concernant la publicité :
Au cours du processus de classification, la manière de publiciser ou de promouvoir un produit peut être examinée par la DMV et la Division des aliments pour animaux (DAA) de l'ACIA. À eux seuls, les sites Web ne sont pas interprétés comme faisant partie de l'étiquette d'un produit. Par contre, les allégations présentées dans les médias (comprenant les sites Web de divers intervenants ainsi que les médias sociaux) peuvent être considérées comme une preuve du but d'utilisation du produit pour des fins de classification.
4.4.1 Indications (allégations) ou buts thérapeutiques
Les allégations, indications ou buts thérapeutiques font référence au traitement d'une maladie, d'un trouble, d'un état physique anormal ou du traitement et de l'atténuation de ses symptômes, ou de la modification d'une fonction organique (telle que la digestion). Des allégations thérapeutiques ne peuvent être faites que pour des produits ayant un but ou un usage thérapeutique (des médicaments); par conséquent, elles ne sont pas convenables pour des aliments du bétail. Voici quelques exemples d'allégations thérapeutiques (ou de médicament) :
- les allégations relatives à un traitement (le traitement d'une maladie [acétose], une condition [intoxication] ou un état anormal [blessures, œdème] ou ses symptômes [diarrhée]);
- les allégations relatives au contrôle (contrôle des parasites intestinaux, contrôle de la reproduction);
- les allégations relatives à la prévention (prévient la mammite, prévient l'acétose, prévient le ballonnement, prévient la coccidiose), excluant les allégations relatives à la prévention des carences nutritionnelles;
- les allégations relatives aux atténuations (atténue la sévérité des pneumonies, soulage la douleur associée aux coliques, soulage les inflammations, réduit l'incidence de la fourbure, réduit les risques de mortalité précoce);
- les allégations de rendement de production animale (allégations relatives à la production), qui ne sont pas appuyées par un but ou un mode d'action nutritionnels (stimuler la production d'œufs, augmenter le nombre de petits par portée).
Remarque : Cette liste d'indications acceptables pour les médicaments n'est pas exhaustive et d'autres indications ou allégations non acceptables pour les aliments du bétail devraient faire l'objet d'une évaluation plus approfondie pour fins de classification.
4.4.2 Indication (allégations) ou buts nutritionnels
Les aliments ne sont pas censés avoir des activités ou des effets thérapeutiques. Les produits qui ont de tels effets ne sont pas considérés comme des aliments mais comme des médicaments. Les aliments sont normalement distribués pendant un certain temps dans le cadre d'un programme alimentaire équilibré dans le but de répondre aux besoins nutritionnels essentiels à la santé, à la croissance et à la production du bétail. Ces aliments peuvent aussi englober des produits sans valeur nutritive comme des agents aromatisants, des agglomérants, des agents de conservation, des agents antiagglomérants et d'autres produits qui contribuent à la fabrication, à l'entreposage ou à l'appétence des aliments du bétail. Les aliments sont aussi connus comme des excipients (supports) pour administrer des produits thérapeutiques, notamment les aliments médicamenteux.
Les indications ou buts nutritionnels font référence à la présence d'un ou de plusieurs éléments nutritifs ou substances nutritives, reconnus scientifiquement pour couvrir les besoins nutritionnels essentiels à la croissance, à la santé et à la production des animaux d'élevage. Un énoncé qui indique, suggère ou propose que la consommation d'un élément nutritif ou d'une substance nutritive en particulier réduit de façon importante l'incidence ou prévient le développement d'une maladie, d'une carence ou d'un trouble nutritionnel chez un animal en santé peut aussi être acceptable dans cette catégorie d'allégations. Voici des exemples d'allégations nutritionnelles qui seraient acceptables pour des aliments du bétail :
- les allégations relatives à la prévention d'un trouble nutritionnel, sauf celles liées à la prévention d'une maladie (prévention de la « maladie du muscle blanc » chez le bétail causée par une carence en sélénium; prévention de l'anémie causée par une carence en fer chez les porcelets néonataux; prévention de la scoliose causée par une carence en vitamine C chez les salmonidés);
L'annexe A contient des renseignements supplémentaires sur les troubles nutritionnels. - les allégations relatives au rendement (production) des animaux dans un contexte nutritionnel (augmentation de la production laitière en distribuant aux animaux des acides aminés digestibles dans l'intestin grêle; en comparaison avec une source non protégée du même élément nutritif);
- la biodisponibilité accrue des éléments nutritifs (minéraux organiques complexes dont l'allégation indique une biodisponibilité accrue par rapport à une certaine source inorganique; enzymes, comme les phytases, pour accroître le phosphore disponible).
Il se peut aussi que les aliments n'aient pas de valeur nutritive, selon les allégations ou les caractéristiques ci-dessous :
- la préservation des éléments nutritifs (p. ex., additifs pour fourrages, inhibiteurs de moisissures, antioxydants pour aliments du bétail) non justifiée par un effet thérapeutique ou un mode d'action (consulter la section 4.7 Mode d'action);
- les substances auxiliaires visant à faciliter ou à améliorer les propriétés relatives à la fabrication ou à la manutention d'un aliment (p. ex., agents liants pour le cubage, agents antiagglomérants, porteurs, etc.) non justifiées par un effet thérapeutique ou un mode d'action;
- les colorants servant à colorer les aliments ou les tissus/œufs des animaux d'élevage;
- les agents aromatisants servant à créer l'arôme les aliments.
Remarque : Les produits dont l'étiquette comporte des allégations nutritionnelles devront être enregistrés auprès de l'ACIA avant d'être importés, fabriqués et vendus au Canada. Ces types d'allégations seront autorisés à la condition qu'ils soient justifiés par des données scientifiques pertinentes ayant été évaluées et approuvées par la Division des aliments pour animaux (DAA).
4.5 Composition
Bien qu'à elle seule la composition d'un produit ne détermine pas nécessairement sa classification, la présence d'un ingrédient, ou sa concentration, peut aider à déterminer la bonne classification réglementaire de ce produit.
4.5.1 Type d'ingrédients
Les composantes d'un produit, ou ses ingrédients, sont évalués pour déterminer l'activité ou le but de ce produit. La nature de chaque ingrédient, ses caractéristiques intrinsèques, ses propriétés physiques et chimiques, le degré de modification (p. ex., composé, extrait, isolat) et ses fonctions et rôles dans le produit font l'objet d'une enquête détaillée pour fournir des éléments de preuve à l'appui de l'utilisation visée du produit.
4.5.2 Concentration (ou niveaux) des ingrédients
La concentration ou la teneur d'un ingrédient peut s'avérer utile pour déterminer son rôle particulier dans la formulation et son but visé dans l'ensemble du produit. Un ingrédient peut avoir une fonction particulière jusqu'à ce qu'il atteigne un certain niveau ou concentration, puis présenter un effet pharmacologique ou thérapeutique à une concentration plus élevée (p. ex., propylène glycol d'une concentration de 1 % ou moins = ingrédient inerte vs propylène glycol d'une concentration de 50 % ou de 100 % = ingrédient actif).
De plus, un ingrédient nutritionnel comme une vitamine ou un minéral peut avoir un effet thérapeutique en plus grande quantité, en fonction de sa concentration dans le produit et des recommandations posologiques (p. ex., calcium, fer, cuivre, zinc, vitamine A, vitamine C, certaines plantes et huiles végétales, etc.).
4.6 Mode d'emploi
4.6.1 Recommandations posologiques/taux d'alimentation
La posologie recommandée ou le taux d'administration d'un produit peut aider à en déterminer le but thérapeutique ou nutritionnel. Par exemple, un régime posologique très précis peut suggérer un but thérapeutique ou l'effet prévu d'un produit.
Les taux d'inclusion ou les recommandations posologiques sont souvent prises en considération pour classer des produits comme des médicaments, plus particulièrement les produits vitaminés, de minéraux ou d'électrolytes. Pour les aliments du bétail, le taux d'alimentation est utilisé pour déterminer si la quantité finale d'un ingrédient ou d'un élément nutritif distribuée à une espèce particulière respecte ou dépasse les normes réglementaires (p. ex., niveaux de supplémentation recommandés par le National Research Council, tableau 4; teneurs et limites maximales prescrites dans les annexes IV et V du Règlement sur les aliments du bétail, etc.).
4.6.2 Durée du traitement/de l'alimentation et moment de l'administration
La durée du traitement et le moment de l'administration sont des critères qui ne permettent pas automatiquement une classification en tant que médicament ou aliment.
Ces détails relatifs au mode d'emploi ne sont généralement pas utiles ou pertinents pour la classification d'un produit comme médicament. Ils varient considérablement d'un médicament à un autre, puisqu'ils sont étroitement associés aux espèces animales et à la maladie (ou condition) pour lesquelles des médicaments doivent être administrés.
En général, les produits considérés comme des aliments font partie d'un programme alimentaire équilibré et doivent être distribués pendant un certain temps de façon continue. La durée de la supplémentation en minéraux ou en vitamines peut varier en fonction des périodes physiologiques précises pendant la durée de production des animaux. Par exemple, la distribution d'un produit nutritionnel à des vaches laitières en lactation ou en gestation, ou la distribution de minéraux pendant les premiers jours de vie des porcelets, seraient cohérents avec un régime de supplémentation des aliments.
4.7 Mode d'action
En biologie, un mode d'action fait référence à la manière ou au mécanisme par lequel on obtient une action, un effet ou un résultat dans un organisme. Le mode d'action et son effet sont souvent liés à la structure chimique d'un ingrédient ou d'une substance. Habituellement, une substance présente son action par une interaction entre cette substance et un constituant cellulaire, communément appelé un récepteur, ce qui donne lieu à une réponse directe ou bloque la réponse à un autre agent. De nombreux sites récepteurs ou enzymes peuvent déclencher une réponse biologique à une substance.
4.7.1 Modes d'action thérapeutiques
Un mode d'action thérapeutique est une interaction biochimique par laquelle un ingrédient (ou un mélange d'ingrédients) produit un effet pharmacologique. Par exemple, l'acide acétylsalicylique (substance chimique) produit une inhibition irréversible de l'enzyme cyclo-oxygénase (mode d'action), laquelle supprime la production de prostaglandines et de thromboxanes (effet physiologique), ce qui a pour conséquence de réduire la douleur et l'inflammation (effet thérapeutique).
Comme pour une action pharmacologique, les actions immunologiques et métaboliques sont également considérées comme des interactions biochimiques menant à une réponse biologique particulière. Une action immunologique est une action qui se produit dans ou sur le corps en stimulant et/ou en mobilisant les cellules et/ou les produits du système immunitaire. Une action métabolique comprend une altération, y compris l'arrêt, le démarrage ou le changement de rapidité des processus chimiques normaux participant aux fonctions corporelles normales et disponibles pour ces fonctions (p. ex., un répartiteur lipido-protidique pour stimuler la croissance).
Lorsqu'un ingrédient ou un produit a une action qui rétablit, change ou affecte la ou les fonction(s) physiologique(s) d'un animal au-delà des effets physiologiques généralement reconnus de la nutrition, cette action répond à la définition de drogue (médicament) selon la Loi sur les aliments et drogues et est considérée comme étant de nature thérapeutique.
Modes d'action compatibles avec les médicaments
- un mécanisme indirect pour stimuler l'appétit (stimulation du système nerveux central);
- un mode d'action à la fois dans les aliments et chez les animaux (substance antifongique ajoutée en concentration élevée aux aliments en vue de prévenir la moisissure dans les aliments et la mycotoxicose chez les animaux du bétail);
- tout mode d'action à l'intérieur de l'animal, non lié au processus digestif;
- un mécanisme d'action interne particulier, notamment :
- modification des cellules ou des fonctions cellulaires
(p. ex., stimulation des cellules au moyen de l'insuline pour qu'elles absorbent le glucose dans le sang); - modification d'une protéine, d'un enzyme, d'un acide aminé, ou de son activité;
- modification d'un organe ou de son activité
(p. ex., diminution de la taille de la thyroïde ou de son activité); - modification, élimination ou blocage d'une voie métabolique;
- modification des cellules ou des fonctions cellulaires
- des mécanismes de biorégulation (p. ex., rétroaction biologique) qui contrôlent l'expression et/ou la modification de certaines composantes biologiques.
- une stimulation artificielle du système immunitaire non spécifique (inné) :
- étapes de la reconnaissance :
- la production d'un nombre accru de cellules ou de protéines immunologiques;
- l'activation des réactions complémentaires;
- étapes de l'élimination :
- activité phagocytaire accrue des cellules immunologiques;
- activité cytotoxique accrue des cellules immunologiques;
- augmentation de la migration cellulaire et de la réaction inflammatoire;
- étapes de la reconnaissance :
- une action sur la flore intestinale (substance/produit qui n'est pas absorbé par le corps et qui agit directement dans la lumière intestinale) qui peut avoir un certain effet prophylactique/thérapeutique.
Remarque : Cette liste de modes d'action acceptables pour les médicaments n'est pas exhaustive. D'autres modes d'action nécessiteraient une description complète et une évaluation plus approfondie aux fins de classification.
4.7.2 Modes d'action nutritionnels
Le mode d'action nutritionnel pourrait être défini comme un processus au cours duquel des éléments nutritifs reconnus (lorsqu'ils sont distribués aux concentrations requises) sont digérés ou absorbés par l'animal pour assurer le maintien des fonctions physiologiques, entraînant des différences mineures dans l'activité biologique, sans modifier de façon significative et durable les réactions cellulaires, tissulaires, organiques et métaboliques du corps. Ce processus provient habituellement de taux physiologiques établis et reconnus de croissance, de maintien et/ou de production qui caractérisent la bonne santé des animaux d'élevage.
Dans le contexte des aliments, on entend par « élément nutritif » toute substance pouvant être métabolisée par un animal pour lui donner de l'énergie et pour former ou maintenir les tissus afin de répondre aux besoins nutritionnels scientifiquement justifiés. Il y a six types d'éléments nutritifs : les minéraux, les vitamines, les matières grasses, les protéines, les glucides et l'eau.
Modes d'action compatibles avec les aliments
- une action directement dans l'aliment, avant la consommation, en vue d'améliorer ou de conserver la valeur nutritive de cet aliment, d'en faciliter ou d'en améliorer la fabrication ou la manutention, et d'en modifier la couleur ou l'odeur (p. ex., agglomérants de granules, agents antiagglomérants, colorants alimentaires, agents aromatisants, inhibiteurs de moisissures, agglomérants de mycotoxines;
- une action limitée au processus normal de digestion des aliments (p. ex., absorption des minéraux et des vitamines par les muqueuses intestinales, amélioration de la digestibilité et de la biodisponibilité des éléments nutritifs).
Remarque : La liste des mécanismes d'action acceptables relatifs aux aliments n'est pas exhaustive.
Le mode d'action n'est pas toujours un critère définitif et devrait être évalué conjointement avec d'autres critères tels que les particularités physiologiques de l'espèce ciblée (p. ex., ruminants vs non-ruminants), l'intention d'utilisation et les concentrations des ingrédients, avant qu'une décision finale ne soit prise au sujet de la classification.
5. Processus de décision de classification
La Direction des médicaments vétérinaires (DMV) et la Division des aliments pour animaux (DAA) de l'ACIA encouragent les promoteurs à amorcer le processus de classification de leurs produits en utilisant le présent document d'orientation, ainsi que le diagramme et les annexes qu'il contient. Après avoir établi d'eux-mêmes qu'un produit se trouve dans la catégorie des médicaments, ils peuvent communiquer avec la DMV pour obtenir des renseignements sur les exigences de présentation d'une demande. Ils peuvent également consulter la section Médicaments vétérinaires sur le site Web de Santé Canada pour plus de détails.
Lorsqu'il est déterminé qu'un produit est un aliment, une demande d'enregistrement peut être présentée à la DAA. On peut consulter la section sur les Directives réglementaires du site Web de l'ACIA pour obtenir des renseignements sur le processus d'enregistrement.
Si des questions de classification persistent ou si des enjeux sont soulevés suite à la lecture du présent document, les promoteurs devraient communiquer avec la DMV, qui est le guichet d'accès unique en matière de classification. La DMV collaborera ensuite avec la DAA pour partager l'information et discuter en vue de parvenir à une décision conjointe quant à la classification du produit. Le demandeur sera informé par écrit de la décision finale concernant la classification réglementaire du produit. Les décisions relatives aux médicaments seront communiquées par la DMV, et les décisions relatives aux aliments seront transmises par la DAA.
Un modèle de classification a été élaboré pour faciliter l'organisation et la présentation de l'information nécessaire par l'industrie en vue d'établir la juste classification d'un produit. Veuillez communiquer avec la DMV pour obtenir ce modèle.
Les demandes de classification de la part de l'industrie doivent inclure une lettre d'accompagnement, le modèle de classification dûment rempli et la documentation à l'appui. Toutes les demandes de classification doivent être présentées par écrit (par courrier, par courriel ou par télécopieur) à la DMV.
Toute demande de révision de la classification devrait aussi être présentée par écrit à la DMV et être accompagnée d'une justification scientifique valable, en plus de la documentation à l'appui appropriée. La DMV consultera au besoin la DAA.
6. Mise en application
Le présent document d'orientation entrera en vigueur à la date de publication en ligne. La publication, la coordination et la mise en œuvre du présent document seront la responsabilité conjointe de la DMV de Santé Canada et de la DAA de l'ACIA. Pour toutes questions ou demandes de renseignements supplémentaires sur le contenu du présent document, veuillez communiquer avec la DMV.
Annexe A
Troubles nutritionnels
1. Définitions :
- Élément nutritif :
Tel qu'indiqué à la section 4.7.2 « Modes d'action nutritionnels » (deuxième paragraphe), on entend par « élément nutritif » toute substance pouvant être métabolisée par un animal pour lui donner de l'énergie et pour former ou maintenir les tissus afin de répondre aux besoins nutritionnels reconnus scientifiquement. Il y a six types d'éléments nutritifs : les minéraux, les vitamines, les matières grasses, les protéines, les glucides et l'eau.
- Maladie :
-
Dégradation de l'état normal d'un corps animal ou végétal vivant ou de l'une de ses parties qui interrompt ou modifie le rendement des fonctions vitales, ce qui se manifeste habituellement en différenciant les signes et les symptômes, et est une réaction à des facteurs environnementaux (comme la malnutrition, les risques industriels ou le climat), à des agents infectants particuliers (notamment des vers, des bactéries, des toxines ou des virus), à des défauts inhérents de l'organisme (comme des anomalies génétiques) ou à une combinaison de ces facteurs. [Traduction libre]
(Référence du texte anglais : Merriam -Webster Medical Dictionary)
En bref, une maladie fait référence aux dommages à un organe, à une partie, à une structure ou à un système du corps qui causent le mauvais fonctionnement de ce dernier ou un état de santé menant à un tel dysfonctionnement.
Exemples : Maladies cardiaques, diabète, obstruction de la voie biliaire principale.
- Tonique ou fortifiant :
Conformément au paragraphe 2. (1) Interprétation du Règlement de 1983 sur les aliments du bétail, « tonique ou fortifiant » désigne un aliment minéral qui est formulé pour corriger ou aider à corriger une carence alimentaire et qui est annoncé comme tel, et dont l'usage doit cesser lorsque la carence est corrigée (p. ex., produit à ingrédient unique de magnésium ou de zinc).
- Trouble nutritionnel :
Tout trouble chez l'animal directement ou indirectement causé par un manque d'éléments nutritifs ou un déséquilibre nutritionnel dans l'alimentation.
Les troubles métaboliques et multifactoriels dans lesquels les éléments nutritifs jouent un important rôle ne sont pas considérés comme des troubles nutritionnels. Voici quelques exemples de telles conditions : hypocalcémie post-partum (fièvre vitulaire), acétonémie (cétose) ou toxémie de gestation, acidose métabolique, fourbure, déplacement abomasal, entéro-toxémie, urolithiase (calcul urinaire).
2. Critères :
Critères de détection d'un trouble nutritionnel :
- La présence d'une carence, d'un excédent ou d'un déséquilibre au niveau d'un élément nutritif particulier dans l'alimentation;
- La relation de cause à effet entre les signes cliniques d'une maladie et l'absence d'un élément nutritif dans l'alimentation;
- L'administration de suppléments alimentaires prévient et/ou règle le trouble.
Tous les critères doivent être présents pour qu'une condition soit considérée comme un trouble nutritionnel.
| Aliment | Médicament| |
|---|---|
| Carence alimentaire | Besoin anormal de l'animal (carence due à une maladie) |
| Interférence entre les éléments nutritifs de l'alimentation | Manque d'absorption du corps (dû à une maladie) |
| Augmentation physiologique (normale) des besoins de l'animal (p. ex., parturition, lactation, sudation, etc.) | Besoin anormal de l'animal (secondaire à une maladie) (p. ex., déshydratation suite à une diarrhée, bicarbonate en présence d'acidose métabolique) |
| Espèces pertinentes (les espèces ayant un besoin nutritionnel reconnu) | Espèces n'ayant aucune carence reconnue ou aucun besoin nutritionnel |
| Ingrédients vitaminiques/minéraux provenant d'une source alimentaire approuvée et reconnue de vitamines/minéraux | La nouvelle source peut avoir d'autres propriétés ou buts |
| Données scientifiques à l'appui d'un but nutritionnel pour un élément nutritif particulier | Données scientifiques à l'appui d'un but thérapeutique pour un élément nutritif particulier |
Si l'un des critères relatifs aux médicaments mentionnés ci-dessus est rempli, l'ingrédient ou le produit ne sera pas considéré comme un aliment, mais plutôt comme un médicament.
Toute allégation faisant référence au traitement ou indication thérapeutique associée à ces troubles nutritionnels (maladies) entraînerait la classification du produit comme médicament. Des allégations faisant référence à la prévention/correction seraient acceptables pour les aliments dans les situations suivantes :
- Prévention :
- lorsque l'aliment vise à répondre à des besoins nutritionnels; et
- lorsque l'aliment vise à prévenir un trouble nutritionnel causé par une carence au niveau d'un élément nutritif particulier, en modifiant le régime alimentaire.
- Correction : En ce qui concerne la correction d'un trouble nutritionnel particulier causé par une carence au niveau d'un élément nutritif particulier, en modifiant le régime alimentaire.
- Des sources nutritionnelles approuvées sont utilisées comme supplémentation en éléments nutritifs (p. ex., annexe IV du Règlement sur les aliments du bétail).
Remarque : Veuillez noter que les produits dont l'étiquette comporte ce genre d'allégations devront être enregistrés auprès de l'ACIA avant d'être importés, fabriqués et vendus au Canada.
Annexe B
Diagramme de classification Médicament vs Aliment
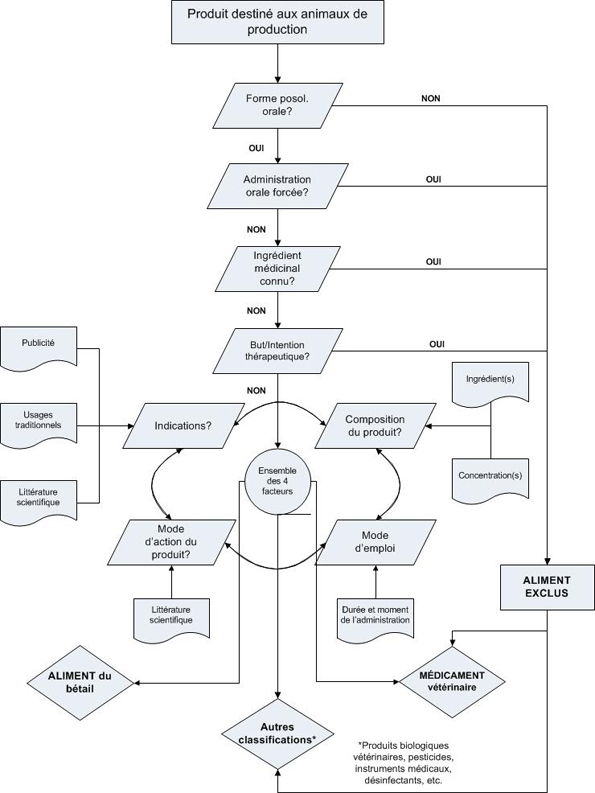
Équivalent textuel
L'annexe A est composée du diagramme de classification Médicament vs Aliment. Ce schéma graphique a pour but d'expliquer la démarche logique, étape par étape, du procédé de classification présentement utilisé par la DMV, ainsi que les interactions entre les différents critères de classification. Pour commercer, seuls les produits destinés aux animaux de ferme peuvent passer par ce processus. Les produits destinés à d'autres espèces ne sont pas pertinents au niveau de l'interface Aliment/médicament. Ensuite, les questions suivantes sont posées, dans l'ordre présenté ci-dessous, dans le but d'exclure dès le début une classification possible d'aliment :
- Est-ce que le produit est présenté sous une forme posologique orale ou est-il administré par voie orale? Non = pas un aliment
- Est-ce que le produit est administré par voie orale forcée? Oui = pas un aliment
- Est-ce que le produit contient un ingrédient médicinal connu? Oui = pas un aliment
- Est-ce que le produit a un but d'utilisation ou une intention thérapeutique? Oui = pas un aliment
Pour répondre à cette dernière question, il faut examiner un groupe de quatre (4) facteurs ou critères de classification, individuellement et ensemble :
- les indications sur l'étiquette du produit (qui sont évaluées conjointement avec la publicité, les usages traditionnels et la littérature scientifique associé à ce produit);
- la composition du produit (qui est influencée par les types d'ingrédient et leur concentration);
- le mode d'action (qui est appuyé par la littérature scientifique); et
- le mode d'emploi (qui pourrait ou non être influencé par la durée et le moment de l'administration).
Après avoir répondu aux dernières questions, il est possible d'obtenir une classification en tant que médicament vétérinaire (réponse positive), aliment (réponse négative) ou autres. Les autres classifications possibles de produit destiné aux animaux englobent les produits biologiques vétérinaires, les pesticides, les instruments médicaux, les désinfectants, etc.)
Annexe C
Ingrédients médicinaux connus
1. Introduction
Un ingrédient médicinal connu est une substance, une partie d'une substance ou une combinaison de substances associée à une propriété thérapeutique (médicinale) ou à un effet pharmacologique. En se fondant sur de nombreuses demandes de classification, la DMV et la DAA ont pu établir une liste des substances classées comme ingrédients médicinaux. Ces classifications se sont appuyées sur les connaissances scientifiques existantes au moment de la demande et sur les indications proposées par le promoteur. Toutefois, certains ingrédients médicinaux peuvent également avoir un but non médicinal, en fonction de la concentration ou d'autres facteurs. À titre informatif, la liste contenant ces « exceptions » provient des ingrédients énumérés dans les annexes IV et V du Règlement sur les aliments du bétail et qui sont utilisés dans les aliments à des fins non médicinales.
Remarques importantes :
- La liste suivante a été dressée uniquement pour les besoins du présent document en vue de faciliter la classification des produits. Il ne s'agit pas d'une liste exhaustive. Toutefois, nous prenons l'engagement de la réviser/mettre à jour régulièrement.
- Cette liste n'inclut pas les classifications associées à des renseignements exclusifs.
- Si une substance ne figure pas dans la liste ci-dessous et que vous souhaitez en déterminer la classification, vous pouvez transmettre à la DMV le modèle aux fins de classification. Si vous avez des questions ou des commentaires, pour recevoir toute autre directive, ou pour obtenir ce modèle, veuillez communiquer avec la DMV.
| Nom des ingrédients médicinaux | Synonymes(s) | Exception(s) (ingrédients approuvés en tant qu'aliments du bétail) |
|---|---|---|
| A | ||
| Achillea millefolium (achillée millefeuille) (plante entière) |
Millefeuille | - |
| Acide folique a, b (a : prévention d'anomalies congénitales chez les femelles en gestation; traitement de l'insuffisance pancréatique et de la thromboembolie fémorale; à utiliser avec des médicaments faisant interférence à l'absorption du folate; pour la prévention ou le traitement de l'entérite) |
Vitamine B9 | Ingrédient vitaminé |
| Acides humiques et leurs sels de sodiuma (immuno-stimulant, antiviral, antioxydant) |
Humate | - |
| Acide hyaluronique | - | - |
| Acide nucléique du thymus | - | - |
| Acide tannique | - | - |
| Adénosine-5-monophosphate | Acide 5'-adénylique | - |
| Aloe vera (aloès) (plante entière) |
- | - |
| Alcaloïdes d'ergot et leurs sels | Claviceps purpurea (ergot) | - |
| Alpha-galactosidase | - | - |
| Arabinogalactane | - | - |
| Arabinogalactane de mélèze | - | - |
| Arctium lappa (plante entière, feuille, à l'exception de l'extrait de fruit (antioxydant) |
Bardane | - |
| Argousier (plante entière, jus de la plante, huile du fruit) |
Hippophae rhamnoides | - |
| Attapulgitea,b (a : traitement de la diarrhée non infectieuse chez les veaux) (b : 25,8 mg/kg p.c. et plus) |
- | Annexe IV, partie I, article 8.118 Agent antiagglomérant ne dépassant pas 0,25 % de l'aliment fini Émulsifiant : max 2,5 % du supplément liquide |
| Arsenical | - | - |
| B | ||
| Belladone (substance homéopathique) |
Atropa belladonna, solanacée mortelle | - |
| Bentonite a, b (a : prévention ou traitement de la diarrhée) (b : environ 400 mg/ml et plus) |
Montmorillonite | Annexe IV, partie I, articles 8.5, 8.6, et 8.89 Agent antiagglomérant ou de pelletisation ne dépassant pas 2 % de la ration totale |
| Bicarbonate de sodiuma (prévention et traitement de la déshydratation, de l'acidose métabolique et d'autres déséquilibres électrolytiques) |
- | Annexe IV, partie I, article 6.71 Ingrédient minéral approuvé comme source de sodium; aussi utilisé comme ingrédient dans les aliments tamponnés pour les vaches laitières et les bovins de boucherie nourris avec des rations riches en grains |
| Bituminosulphonates | - | - |
| Boswellia serrata | Boswellia | - |
| Broméline | - | - |
| Bromure de potassium | - | - |
| C | ||
| Calendula officinalis (plante entière) |
Souci officinal | - |
| Carnitine, sels et dérivés | L-carnitine, Lévocarnitine | L-carnitine : Annexe IV, partie I, article 5.6.16 Aliments porcins : utilisés comme source d'acide aminé ne dépassant pas 0,1 % de la ration totale |
| Cartilage de requin | Squalus acanthias | - |
| Carya basilike | Poudre d'enveloppes de noyer noir, poudre de Juglans nigra |
- |
| Caséine thyroactive | Thyroprotéine | - |
| Centella asiatica, (plante entière, extrait de cette plante et ses principes actifs) |
- | - |
| Chamazulène | Extrait de camomille | - |
| Chanvrea (tige, graine, huile, ayant une teneur en tétrahydrocannabinol [THC] inférieure 0,3 %) (stimuler le système immunitaire, réduire l'inflammation, etc.) (teneur en THC supérieure à 0,3 % = substance contrôlée) |
Cannabis sativa | - |
| Charbon activé | - | - |
| Chardon-Marie | Silybum marianum | - |
| Chlorhydrate d'éphédrine | - | - |
| Chlorhydrate de glucosamine | - | - |
| Chlorhydrate de quinine | - | - |
| Chou palmiste (plante entière, extrait lipostérolique, extrait du fruit) |
Serenoa repens | - |
| Chrome a (pour la régulation de la glycémie) |
- | Levure enrichie de chrome déshydratée : Annexe IV, partie II, article 6.38
Aliment pour bovins laitiers durant leur première lactation approuvé comme source de chrome à un niveau ne dépassant pas 0,4 ppm de chrome dans l'aliment complet Propionate de chrome |
| Coenzyme Q10 | - | - |
| Cotylédon de fenugrec | - | - |
| Cuivre calcium édétate | - | - |
| Cuivre glycinate | - | - |
| D | ||
| Diacétate de sodiuma (contrôler la salmonelle chez les animaux) |
- | - |
| N, N-diméthylglycine | Chlorhydrate de diméthylglycine | - |
| E | ||
| Echinacea angustifolia (échinacée à feuilles étroites) | Echinacea purpurea (échinacée pourpre, échinacée américaine) | - |
| Eleutherococcus senticosus | Ginseng sibérien, éleuthérocoque | - |
| Enzymes pancréatiques | Amylase, lipase, protéase | - |
| Equisetum arvense | Prêle | - |
| Eucalyptus globulus (plante entière, huile essentielle) |
- | - |
| Eucalyptus polybractea | Eucalyptus à bractées multiples | - |
| Eupatorium perfoliatum (eupatoire perfoliée) (plante entière) |
Eupatoire, trioste orangé, herbe à souder | - |
| Eurycoma longifolia (tongkat ali) | Ginseng malaisien | - |
| Extrait de cannebergea, (séché) (contribue à prévenir les infections urinaires) |
- | - |
| Extrait de Streptococcus thermophilus (streptocoques) | - | - |
| Extrait de Yucca shidigeraa (pour l'ostéo-arthrite et les troubles gastriques) |
- | Annexe IV, partie II, article 8.61 Approuvé comme composant d'agent désodorisant Taux d'inclusion typique : 20 - 40 g/tonne d'aliment complet |
| F | ||
| Facteur de croissance de l'épiderme | EGF | - |
| Feuilles de framboisier (séchées, poudre) |
Feuilles de Rubus idaeus | - |
| Filipendula ulmaria | Reine-des-prés | - |
| G | ||
| Gamma-oryzanola (pour stimuler la libération de testostérone et d'hormone de croissance, antioxydant, antiacide, pour stimuler le système immunitaire) |
Huile de son de riz, extrait de son de riz, Oryza sativa L. | - |
| Gingko biloba | Gingko, arbre aux quarante écus | - |
| Glucoheptonate de calcium | - | - |
| L-Glutaminea (préserver la muqueuse intestinale, contribuer à la réparation cellulaire) |
- | - |
| H | ||
| Hamamelis virginiana (plante entière,extrait) |
Hamamélis | - |
| Harpagophytum procumbens | Racine de griffe du diable | - |
| Hespéridine | Bioflavonoïde, complexe de bioflavonoïde, extrait de bioflavonoïde, bioflavonoïde d'agrumes | Annexe V, partie I, article 14.7 Le dihydrochalcone de néohespéridine (un dérivé de l'hespéridine) est approuvé comme un ingrédient de saveur ne dépassant pas 100 ppm dans l'aliment complet |
| Huile de bourrache | Borago officinalis huile de graines | - |
| Huile de menthea (stimuler le système immunitaire et contrôler la surcroissance des bactéries intestinales) |
Mentha x piperita | Annexe V, partie I, article 16.20 Ingrédient de saveur ne dépassant pas 100 ppm dans l'aliment complet ou la ration totale |
| Huile d'origan b (50 ppm et plus dans un aliment complet) |
- | Annexe V, partie II, article 15.1 Ingrédient de saveur ne dépassant pas 50 ppm dans l'aliment complet |
| Huile minérale b (concentration de 100 %) |
Huile minérale lourde | Annexe IV, partie I, article 8.33 Utilisé pour réduire la poussière et comme lubrifiant ne dépassant pas 3,0 % dans les mélanges de minéraux et 0,6 % dans la ration totale |
| Hyaluronate de sodium | - | - |
| Hydroxocobalamine (forme crystalline) | Vitamine B12a | - |
| I | ||
| Inosine | - | - |
| J | ||
| Juglans nigra (plante entière) |
Noyer noir | - |
| K | ||
| Kaolinb (plus de 2,5 % dans le produit) |
- | Annexe IV, partie I, article 8.87 Agent antiagglomérant ne dépassant pas 2,5 % de l'aliment fini |
| L | ||
| Lévulinate de calcium | - | - |
| Lobelia inflata | Lobélie gonflée | - |
| M | ||
| Mélatonine | - | - |
| Méthylsulfonylméthane | MSM | - |
| Morinda citrifolia (mûrier de Java) (plante entière, feuilles, racine, extrait du fruit) |
Noni | - |
| Morus nigra | Mûrier noir | - |
| Moule verte | Perna canaliculus | - |
| Myristoléate de cétyle | Acide myristoléique (ester hexadécylique de) | - |
| O | ||
| Oxygène (solubilisé sous forme posologique orale) | - | - |
| P | ||
| Papaver rhoeas | Graines de pavot rouge, coquelicot | - |
| Pau-d'arco | Handroanthus impetiginosus, lapacho rouge, Taheebo | - |
| Peroxyde d'hydrogène | - | - |
| Peumus boldus | Boldea fragrans | - |
| Pidolate de calcium | - | - |
| Propylèneglycol b (100 à 130 grammes/vache/jour aux environs du vêlage) |
- | Annexe IV, partie I, article 8.43 Agent d'émulsification Niveau d'incorporation habituel : 0,01-0,02 % |
| Psyllium (plante entière, grains, coque) |
Plantago ovata | Annexe IV, partie II, article 8.55 L'enveloppe de la graine de Psyllium est approuvée comme source de fibre alimentaire en quantité ne dépassant pas 2,0 % de la ration totale |
| Q | ||
| Quercétine | Elytrigia repens, chiendent | - |
| R | ||
| Rehmannia glutinosa | Digitale-pourpre de Chine | - |
| Rumex crispus | Patience crépue | - |
| S | ||
| S-adénosylméthionine | SAM | - |
| Salicylate de sodium | - | Annexe IV, partie I, article 8.55 Utilisé comme composante d'agent de contrôle des moisissures dans les aliments |
| Saule blanc (plante entière, écorce de la tige) |
Salix alba | - |
| Sélénite de sodiuma (traitement de la dystrophie musculaire) |
- | Annexe IV, partie I, article 6.77 Ingrédient minéral approuvé comme source de sélénium Le maximum réglementaire est de 0,3 mg/kg dans la ration totale pour la plupart du bétail; 0,1 mg/kg pour les aliments complets de poissons et lapins |
| Sels de calcium, lorsqu'ils sont vendus pour le traitement de l'hyperphosphatémie |
- | - |
| Solidago virgaurea | Verge d'or | - |
| Spirulina maxima, Spirulina platensis (plante entière) |
Arthrospira platensis, cyanobactéries, Aphanizomenon flos-aquae (AFA) | - |
| Sulfate de chondroïtine | - | - |
| Sulfate de cuivre a, c (pour le traitement de l'aspergillose et de l'hexamitiase chez la volaille) |
- | - |
| Sulfate de glucosamine | - | - |
| Sulfate de quinine | - | - |
| Symphytum officinale | Consoude | - |
| T | ||
| Taxifoline | - | - |
| Triméthylglycine | TMG, bétaïne | - |
| Tussilago farfara | Tussilage farfara | - |
| U | ||
| Ulmus rubra | Orme rouge | - |
| Urtica dioica (plante entière, jus extrait) |
Ortie commune, ortie dioïque, | - |
| Uva ursi (feuilles séchées, poudre de feuilles, extrait liquide) |
Arctostaphylos uva-ursi, raisin d'ours |
- |
| V | ||
| Valeriana officinalis (valériane officinale) (plante entière) |
Racine de valériane | - |
| Verbena officinalis (verveine officinale) (plante entière) |
Verveine | - |
| Vitamine Cb,c (b : 5,5 mg/g et plus) (c : chez la volaille) |
Acide L-ascorbique ou L-ascorbate |
Annexe IV, partie I, article 7.1.2 Ingrédients vitaminés Les niveaux acceptables sont ceux recommandés par le National Research Council (NRC) |
| Vitamine K1 | Phytonadione | - |
| Vitex agnus-castus (plante entière) |
Arbre au poivre, gattilier | - |
| Z | ||
| Zéolites | Aluminosilicates (minéraux) | Annexe IV, partie II, article 8.59 Agent antiagglomérant ne dépassant pas 2,0 % de l'aliment complet L'aluminosilicate de sodium calcium et l'aluminosilicate de sodium sont énumérés dans la partie I de l'annexe IV comme agents antiagglomérants à un niveau ne dépassant pas 2,0 % de l'aliment complet |
| Zinc a,b (a : pour le traitement de la diarrhée) (b : 2 mg/g (2 000 mg/kg) et plus) |
- | Annexe IV, partie I, article 6.85 L'oxyde de zinc est approuvé comme source de zinc Tableau IV : Le maximum permis dans les aliments complets pour porcs est de 500 mg/kg |
Annexe D
Indications (ou allégations) relatives au stress
1. Introduction
Par le passé, la quasi-totalité des indications ou allégations où figure le mot « stress » étaient associées à des fins thérapeutiques, d'où une classification en tant que médicament. Le but de cette annexe est de fournir aux intervenants des précisions plus détaillées concernant :
- l'acceptabilité de l'utilisation du mot « stress » dans les indications de produits; et
- le type d'indications relatives au stress considérées de nature thérapeutique (ou médicamenteuse), ainsi que les indications considérées de nature non thérapeutique et acceptables pour des aliments du bétail.
2. Définition
Aux fins du présent document, « stress » est défini comme étant « la somme des réactions biologiques à des stimuli négatifs - de nature physique, mentale ou émotionnelle, tant internes qu'externes-, qui ont tendance à perturber l'homéostasie d'un organisme. Si ces réactions sont inappropriées, elles peuvent engendrer des problèmes de santé. Ce terme est également utilisé en référence aux stimuli qui suscitent des réactions, p. ex. chaleur, nutrition, lactation, claustration, transport. »
(selon le Comprehensive Veterinary Dictionary de Baillère)
3. a) Critères d'acceptabilité des indications relatives au stress
- Clarté :
Le terme « stress » est trop général pour décrire l'état d'un animal. Il est recommandé d'éviter le mot « stress » dans l'étiquetage et la publicité de produits car il s'agit d'un terme vague, imprécis et ambiguë. - Spécificité :
Lorsque le mot stress est utilisé, il doit être assorti de qualificatifs concrets et mesurables. Pour préciser le contexte, l'indication doit inclure la ou les causes du stress, l'impact (les conséquences), le but ou l'intention visée par l'utilisation du produit et/ou le moment de son administration.
Des exemples d'indications (allégations) inacceptables sont présentés dans le tableau 3.1 à la fin de ce document.
3. b) Critères de classification des indications relatives au stress
- Les indications (allégations) relatives au stress seront classifiées comme étant thérapeutiques ou non thérapeutiques indépendamment du moment où survient l'événement ou le changement causant le stress ou du moment de l'administration du produit.
- Une indication (allégation) relative au stress est considérée de nature thérapeutique si elle s'applique à :
- un produit visant à prévenir ou à traiter des conséquences sévères ou graves (dont des signes cliniques et des maladies) résultant d'un événement ou d'un changement stressant; et/ou
- un produit affectant directement la fonction physiologique ou la structure des organes d'animaux en situation stressante.
En d'autres termes, les allégations relatives à l'atténuation de signes cliniques ou à l'altération de la structure ou de la fonction d'organes résultant d'un e situation stressante ne sont appropriées seulement que si elles s'appliquent à des médicaments vétérinaires.
- Une indication (allégation) relative au stress est considérée de nature non thérapeutique si elle s'applique à :
- un produit fournissant un apport en nutriments ou visant un but nutritionnel; et/ou
- un produit soutenant le rendement de production animale (c.-à-d. les allégations relatives à la production) lors d'événements stressants ou de procédures liées aux pratiques usuelles d'élevage (p. ex. vaccination, castration, écornage ou écourtage de la queue).
Des exemples d'indications thérapeutiques et non thérapeutiques sont aussi présentés dans le tableau 3.1 ci-dessous. Veuillez noter que ce tableau n'est proposé qu'à titre indicatif seulement et qu'il ne constitue pas une liste exhaustive et complète.
| Indications relatives au stress (de nature thérapeutique) considérées acceptables | Indications relatives au stress (de nature non thérapeutique) considérées acceptables | Indications relatives au stress considérées inacceptables |
|---|---|---|
|
|
|
4. Autres considérations
Veuillez noter que, comme dans toutes classifications, les critères et le processus décrits dans le diagramme sur la classification des médicaments/aliments (surtout ceux figurant dans le cercle) seront respectés lors de la classification d'un produit à utiliser en périodes de stress.
Annexe E-1
Agents de détoxification des mycotoxines (ADM)
1. Contexte
Les mycotoxines sont des composés toxiques produits par différents types de champignons (surtout des genres Aspergillus, Penicillium et Fusarium). Dans des conditions environnementales favorables, particulièrement celles reliées à la température et de l'humidité, ces champignons peuvent proliférer dans les aliments du bétail, par exemple les grains céréaliers, et produire des mycotoxines. Dans le but de réduire la contamination mycotoxinique, on a eu recours à plusieurs techniques et produits, dont la thermothérapie, la séparation physique, le trempage, le décorticage et le nettoyage des graines. L'utilisation d'agents de détoxification des mycotoxines (ADM) est une technique qui est abordée dans cette annexe. Le but général des ADM est d'assurer la salubrité des aliments du bétail, d'éviter que des résidus nocifs n'entrent dans la chaîne d'alimentation et de prévenir les maladies animales. En raison des difficultés encourues lors de la classification des ADM suite à leurs différentes utilisations, les critères de classification précédemment utilisés ont fait l'objet d'un e révision et ont été davantage clarifiés :
2. Définition
Agents de détoxification des mycotoxines (ADM) : Les ADM sont des substances ou des mélanges de substances intégrés dans une matrice d'aliment en vue d'atténuer la toxicité de mycotoxines connues, en réduisant l'exposition des animaux aux mycotoxines. Pour obtenir ce résultat, on peut réduire leur réactivité en misant sur la fixation directe, en réduisant leur biodisponibilité ou leur absorption intestinale, ou en favorisant leur excrétion.
3. Critères de classification pertinents
3. a) Mode d'action
Les ADM peuvent être réglementés en tant que médicament vétérinaire ou aliment du bétail selon le mode d'action démontré ou allégué par le promoteur du produit.
- Si le mode d'action implique les fonctions physiologiques de l'organisme de l'animal (p. ex. fixation à la muqueuse gastro-intestinale, stimulation d'un e réaction immunitaire ou d'un e réaction enzymatique endogène, absorption dans le système circulatoire, transformation métabolique), alors un ADM pourrait être classifié en tant que médicament vétérinaire.
À titre d'exemple, des enzymes digestives peuvent inactiver certaines mycotoxines. Un autre exemple : un produit mixte constitué d'un e substance agglomérante et d'un ingrédient facilitant les processus de détoxication hépatique. - Si le mode d'action se produit dans la matrice d'aliment avant l'ingestion par l'animal de l'aliment traité (p. ex., fixation à la mycotoxine ou inactivation), alors le produit pourrait être classifié en tant qu'aliment du bétail. Un ADM peut également être considéré comme un aliment du bétail si son activité se produit après solubilisation à l'intérieur des voies intestinales et tant que son effet ne dépend pas d'une absorption systémique.
À titre d'exemple, les aluminosilicates agissent sur certaines mycotoxines, empêchant qu'elles soient absorbées par le système digestif. Un autre exemple : la dégradation enzymatique ou la biotransformation de mycotoxines par des enzymes exogènes en vue de réduire le potentiel de toxicité.
Les produits ayant un double mode d'action ou ayant d'autres modes d'action devraient être soumis à la Direction des Médicaments Vétérinaires (DMV) pour une évaluation plus approfondie aux fins de classification.
3. b) Indications relatives aux mycotoxines
Les indications concernant la prévention de maladies chez les animaux ou les indications relatives au traitement de signes cliniques de mycotoxicose (ou de maladies associées) seraient considérées de nature thérapeutique. Les produits assortis de telles indications seraient classifiés en tant que médicaments vétérinaires. Des exemples d'indications acceptables pour des médicaments vétérinaires sont présentés dans le tableau ci-dessous :
Tableau 3-1 : Indications thérapeutiques (ou médicamenteuses)
- Prévention de l'aflatoxicose chez les poulets en croissance
- Prévention de la mortalité associée aux toxines d'Aspergillus chez la volaille
- Réduction des avortements ou de la mortinatalité chez les truies associés à l'ingestion de zéaralénone
- Prévention des vomissements, de la diarrhée et d'autres effets nocifs causés par les toxines Fusarium chez le porc
- Prévention du pied de fétuque chez les chevaux
Les indications relatives à la réduction de la contamination d'aliments du bétail par des modes d'action acceptables dans les aliments pourraient être considérées des indications non thérapeutiques. Les produits assortis de telles indications pourraient être classifiées en tant qu'aliments du bétail. Des exemples d'indications acceptables pour des aliments du bétail sont présentés dans le tableau ci-dessous :
Tableau 3-2 : Indications non thérapeutiques (dont nutritives)
- Réduction (minimisation ou prévention) de l'exposition à l'ochratoxine A dans les aliments du bétail
- Inactivation de la vomitoxine (désoxynivalénol) dans les aliments du bétail
- Diminution de la biodisponibilité de l'aflatoxine B1 par agglomération dans les aliments du bétail
Dégradation de la fumonisine B1 et de la zéaralénone dans les aliments du bétail
4. Autres considérations
- Veuillez noter que l'utilisation d'ADM ne sera pas autorisée dans les aliments du bétail qui ne sont pas conformes aux normes canadiennes sur les mycotoxines.
- Comme dans toutes classifications, les critères et le processus décrits dans le diagramme sur la classification des médicaments/aliments du bétail seront respectés.
Annexe E-2 : Produits microbiens viables (PMV)
1. Introduction
1.1 Contexte
À l'heure actuelle, de nombreux produits microbiens viables (PMV) sont considérés comme étant des médicaments vétérinaires principalement en raison de leurs allégations et/ou modes d'action. La Direction des médicaments vétérinaires (DMV) de Santé Canada et la Division des aliments pour animaux de l'Agence canadienne d'inspection des aliments (ACIA) offrent différents processus d'enregistrement en démontrant plus de souplesse au niveau de la classification. Les critères de classification des PMV ont été réexaminés, reconnaissant que le mode d'action de ces produits peut entraîner une modification de la microflore intestinale et de l'environnent intestinal sans nécessairement les classifier en tant que médicaments vétérinaires. Les PMV classifiés en tant qu'aliments pourraient être inclus dans une nouvelle catégorie de "Modificateurs gastro-intestinaux" qui peut être indiqué sur l'étiquette. Les produits de la catégorie de modificateurs de gastro-intestinaux seraient également assortis d'une allégation nutritionnelle ou de production / performance conforme aux produits réglementés par la Loi sur les aliments du bétail et pourraient être étiquetés comme tels avec des allégations similaires à celles dans le tableau E-2.1.
1.2 But et portée
La présente annexe vise à donner des directives et des précisions sur la nouvelle classification réglementaire des produits contenant des micro-organismes viables destinés aux espèces d'animaux de ferme. Les PMV sont donnés aux animaux de ferme en tant que source de cellules viables dont le but principal dans l'alimentation consiste à avoir des effets bénéfiques chez les espèces d'animaux de ferme ciblées.
À noter que les organismes non viables et leurs produits, de même que les inoculums pour le fourrage, sont exclus de la portée de cette annexe précise. Se reporter au document principal pour obtenir les facteurs pertinents à prendre en compte en matière de classification.
2. Définitions
Les produits microbiens viables sont des produits contenant des micro-organismes vivants (bactéries, levures, champignons, algues et/ou protozoaires). Ces produits peuvent être composés d'une biomasse de micro-organismes vivants ou d'une souche unique particulière. Ils peuvent inclure des souches microbiennes uniques ou multiples, et ils peuvent être intégrés (sous forme diluée) à des produits comme des aliments mélangés, des bolus ou d'autres formes posologiques.
3. Critères de classification pertinents
Lors de toute classification de produit, les critères décrits dans le document d'orientation devraient être considérés. Les critères additionnels suivants seront considérés dans la classification des PMV destinés aux espèces d'animaux de ferme.
3.1 Propriétés des souches microbiennes
Les propriétés des souches microbiennes ou des mélanges de souches peuvent être considérées lors de la classification d'un produit. Les souches ayant des propriétés antimicrobiennes connues, telles que la production de bactériocines, la production de peptides antimicrobiens et/ou de bactériophages, peuvent être considérées comme étant des médicaments.
3.2 But d'utilisation et indications (allégations)
Une indication (ou allégation) doit être fournie pour tous les produits microbiens viables. Ces allégations doivent être fondées sur un résultat mesurable et appuyées par des données scientifiques valables. L'allégation proposée est un facteur clé considéré lors de la classification, comme suit :
- Les allégations thérapeutiques peuvent inclure la prévention ou le traitement d'un état pathologique ou d'un trouble de santé, l'atténuation des signes cliniques ou la diminution du risque de maladies. Les produits avec des allégations thérapeutiques sont considérés comme étant des médicaments. Il peut s'agir de produits microbiens viables qui prétendent cibler un ou des pathogènes particuliers à l'intérieur du tractus gastro-intestinal, réduire la charge pathogène ou prévenir ou traiter un état pathologique particulier.
- Les allégations relatives à la nutrition ou au rendement et à la production font référence à l'apport de nutriments, de manière directe ou en raison de leur meilleure disponibilité, et à leur digestion ou à leur absorption. Les produits avec des allégations en lien avec le maintien, la croissance et le rendement amélioré des animaux peuvent être classifiés comme aliments du bétail.
- Les allégations de santé générales sont des avantages escomptés dans le maintien ou la promotion de la santé et du bien-être des animaux. Les allégations de santé générales peuvent être acceptables pour la notification de produits de santé animale (PSA)Note de bas de page 1.
Les énoncés qui font référence au remplacement des antimicrobiens» sont inacceptables pour tous les produits. Les allégations des produits doivent être indépendantes, sans faire référence à un autre produit ou type de produit. Des exemples sont présentés dans le tableau E-2.1 ci-dessous :
| Loi sur les aliments et drogues; Règlement sur les aliments et drogues | Loi relative aux aliments du bétail; Règlement de sur les aliments du bétail | |
|---|---|---|
| Allégations thérapeutiques — Nouveau médicament (numéro d'identification du médicament) | Allégations de santé générales — PSA (numéro de notification) | Allégations concernant les aliments — Aliments (numéro d'enregistrement) |
Traitement/prévention des maladies:
Réduction des pathogènes:
|
|
Digestion:
Production et rendement:
|
|
||
Remarque: À noter que ce tableau n'est proposé qu'à titre indicatif et qu'il ne constitue pas une liste exhaustive. Si l'allégation ou l'indication d'un produit ne figure pas dans la liste ci-dessus, veuillez communiquer avec la DMV (qui sert de guichet unique pour la classification) afin de procéder à une évaluation approfondie.
3.3 Formes posologiques
Conformément au document d'orientation, les formes posologiques qui nécessitent une administration forcée (p.ex. bolus et comprimés) sont réglementées en vertu de la Loi sur les aliments et drogues. Les formes posologiques qui ne nécessitent pas une administration forcée peuvent être réglementées, soit en vertu de la Loi sur les aliments et drogues, soit en vertu du Règlement sur les aliments du bétail, selon les autres critères de classification. Dans le but d'assurer une surveillance réglementaire et une application des normes uniformes en matière de sécurité, d'efficacité et de qualité, les produits administrés sous forme posologique orale seront réglementés tel qu'il est illustré au tableau E-2.2.
| Mode d'administration orale | Loi sur les aliments et drogues; Règlement sur les aliments et drogues | Loi relative aux aliments du bétail; Règlement sur les aliments du bétail | |
|---|---|---|---|
| Allégations thérapeutiques — Nouveau médicament (numéro d'identification du médicament) | Allégations de santé générales — PSA (numéro de notification) | Allégations concernant les aliments — Aliments (numéro d'enregistrement) | |
| Administration forcée (p.ex. bolus, comprimé, breuvage) | Oui | Oui | Non |
| Mélangé dans les aliments | Oui | Non | Oui |
| Répandu sur les aliments | Oui | Non | Oui |
| Dans l'eau | Oui | Non | Oui |
Pour de plus amples renseignements sur les PSA et la voie de notification de PSA:
4. Autres facteurs
Tel qu'indiqué dans le document d'orientation, le critère «mode d'action» n'est pas toujours précis et n'est pas nécessairement utilisé pour la classification de produits microbiens viables. Cette approche se justifie par le fait que les différents modes d'action de ces produits sont complexes, mal compris, peuvent se présenter en combinaison et varient selon l'environnement intestinal. Par conséquent, les modes d'action qui font référence à la flore intestinale ne mèneront plus automatiquement à eux seuls à la classification d'un produit en tant que médicament. Cette décision remplace l'approche de classification précédente élaborée par la DMV et la Division des aliments pour animaux (DAA) dans un protocole d'entente de 1997.
- Il est possible que pour certains produits microbiens viables, d'autres critères doivent être considérés pour la classification (p.ex., la concentration, la dose et les conditions d'utilisation).
- Lorsqu'une allégation est proposée pour la classification, il faut considérer attentivement les preuves justificatives disponibles et l'utilisation prévue du produit dans le cadre d'un programme complet de gestion de la santé mis en œuvre sous la supervision d'un vétérinaire ou d'un spécialiste en nutrition animale.
Annexe E-3
Produits à base d'acide
1. Introduction
1.1. Contexte
Les produits à base d'acide (PBA) et leurs sels sont souvent appelés « acidifiants ». Ils contiennent 1 ou plusieurs substances ayant des propriétés acides. Ils ont des utilisations reconnues dans l'administration orale aux animaux de ferme.
Les produits ayant des propriétés acidifiantes peuvent être destinés à agir dans l'animal pour prévenir une maladie ou cibler et réduire un agent pathogène particulier. Cette action correspondrait davantage à un médicament vétérinaire. Auparavant, un produit aurait été classifié en tant que médicament vétérinaire s'il faisait référence à une modification de l'environnement gastro-intestinal. L'ajout de la catégorie « modificateurs gastro-intestinaux » dans les aliments permet de reconnaître un PBA dans les aliments pour sa capacité à modifier localement l'environnement gastro-intestinal.
1.2 Objet et portée
Cette annexe vise à fournir des directives et des précisions sur la classification des PBA destinés à être utilisés par voie orale chez les animaux de ferme, soit comme médicaments vétérinaires, incluant les produits de santé animale (PSANote de bas de page 1), soit comme aliments pour animaux de ferme.
Les PBA présentant des allégations liées à la désinfection ou l'assainissement d'un objet ou d'une surface inanimés sont exclus de la portée de la présente annexe. Ils ne se situent pas à l'interface médicament-aliment.
2. Classifications possibles pour les PBA
2.1 Produits à base d'acide comme médicaments vétérinaires
Les produits à base d'acide destinés à l'alimentation des animaux de ferme qui sont considérés comme des médicaments peuvent être classifiés comme de nouveaux médicaments vétérinaires ou des produits de santé animale (PSA).
2.2 Produits à base d'acide comme aliments
En tant qu'aliments, tous les PBA étaient auparavant enregistrés en tant qu'acidifiants. Des allégations alimentaires typiques pour ces produits pouvaient être :
- pour réduire le pH des aliments solides lorsqu'ajoutés à une matrice d'aliment
- pour acidifier l'eau dans les zones avec des sources d'eau alcalines
- pour être utilisés comme agents de conservation ou inhibiteurs de moisissure dans de la nourriture solide ou liquide (par exemple, dans le lait de remplacement)
Les PBA seront désormais divisés en trois catégories:
- les ajusteurs de pH
- les agents de conservation et inhibiteurs de moisissure
- les modificateurs gastro-intestinaux
Le terme « acidifiant » ne sera plus utilisé comme catégorie d'aliments. Chaque catégorie est définie plus en détail comme suit.
- Ajusteurs de pH
- sont ajoutés aux aliments pour animaux de ferme y compris les aliments liquides, ou à l'eau pour ajuster ou maintenir le pH en raison de leur pouvoir tampon
- l'acidification des aliments peut réduire de manière significative le pH alimentaire, ce qui :
- améliore la digestibilité des nutriments des aliments
- peut influencer l'activité de certaines enzymes digestives dans l'estomac (par exemple le pepsinogène)
- Agents de conservations et inhibiteurs de moisissures
- peuvent être ajoutés aux aliments avant et pendant la transformation pour:
- réduire le pH à des niveaux défavorables à la croissance d'organismes putréfiants (microbiens ou fongiques) ou
- pour prévenir d'autres changements chimiques indésirables dans l'aliment comme tel
- sont destinés à agir sur l'aliment, plutôt que dans l'animal.
- peuvent être ajoutés aux aliments avant et pendant la transformation pour:
- Modificateurs gastro-intestinaux
- agissent au niveau du tractus gastro-intestinal (TGI) afin d'améliorer l'absorption et la digestibilité des nutriments
- peuvent être protégés (par exemple, encapsulés) afin de transiter dans le TGI et atteindre la cible prévue
3. Critères de classification pertinents
Comme pour toute classification de produit à l'interface médicament-aliment, les critères décrits dans le document d'orientation devraient être consultés. Les critères supplémentaires suivants pourraient être utiles pour guider la classification des PBA.
3.1 Caractéristiques des acides
Une caractéristique essentielle des acides concerne leur capacité à se dissocier et à changer leur charge. Ceci entraîne des associations métaboliques et des modes d'action différents.
La formule moléculaire, le pH du milieu ou de l'environnement dans lequel le produit est censé agir, et la valeur pKa de l'acide pourraient devenir des critères importants pour la classification. Ces caractéristiques peuvent soutenir l'utilisation prévue des produits soit nutritionnelle, thérapeutique ou de bien-être général.
Il est important de noter que le type d'acide (par exemple, l'acide citrique, acétique ou formique) ne détermine pas la classification du produit. La classification ou la catégorisation des aliments qui contiennent des acides similaires peut changer selon divers facteurs comme:
- s'il s'agit ou non d'un sel,
- leur poids moléculaire
- leurs concentrations ou formulations
- s'ils sont utilisés à des fins différentes
3.2 Lieu d'action
Un produit qui présente une absorption systémique et un lieu d'action dans l'animal en dehors du TGI peut indiquer une action plus conforme à une utilisation thérapeutique ou de santé générale. Pour cette raison, un tel produit serait probablement classifié comme un médicament vétérinaire, incluant les PSA. La classification ultérieure en tant que médicament vétérinaire dépendra également du mode d'action, des ingrédients et de l'utilisation prévue du produit.
En général, les produits qui agissent dans l'aliment, à l'extérieur de l'animal, sont susceptibles d'être classifiés comme ajusteur de pH, agent de conservation ou inhibiteur de moisissure. Les actions localisées dans le TGI peuvent justifier une classification comme modificateur gastro-intestinal (aliment). Les actions au sein du TGI ayant des actions antimicrobiennes ou antiparasitaires manifestes pour prévenir ou traiter les maladies continuent d'être classifiées comme drogues nouvelles vétérinaires.
Les modificateurs gastro-intestinaux peuvent agir sur plusieurs sites et induire divers effets. Ceci peut mener à une amélioration de la digestion et de l'absorption ainsi qu'à une utilisation efficace de l'énergie, par exemple en:
- réduisant le pH gastrique
- augmentant le temps de rétention gastrique
- modifiant la morphologie de la muqueuse
- améliorant les valeurs d'énergie métabolisable de l'alimentation
La protection d'un produit acide par encapsulation permet une action ciblée sur un endroit particulier du TGI, contrairement aux ajusteurs de pH, aux agents de conservation ou aux inhibiteurs de moisissure, dont le site d'action se trouve dans l'aliment.
3.3 Usage auquel le produit est destiné et indications (allégations)
Une indication (ou allégation) doit être fournie pour tous les PBA, quelle que soit leur classification. Ces allégations devraient être fondées sur un résultat mesurable et appuyées par des données scientifiques valables.
3.3.1 Médicaments vétérinaires
Les allégations thérapeutiques, conformes à celles des drogues nouvelles vétérinaires, peuvent inclure la prévention ou le traitement d'une condition ou d'un état pathologique, l'atténuation des signes cliniques ou la réduction du risque de maladie. Les produits à base d'acide avec des allégations thérapeutiques peuvent cibler un pathogène particulier, réduire la charge pathogène ou prévenir et/ou traiter une maladie.
Les allégations de santé générale sont compatibles avec celles des PSA. Elles peuvent inclure les bénéfices attendus en matière de maintien ou de promotion de la santé et du bien-être des animaux. Les allégations des PSA notifiés sont de nature générale et ne peuvent inclure la prévention, le traitement ou l'atténuation d'une maladie ou d'un désordre.
3.3.2 Aliments
Les allégations nutritionnelles ou de production/performance sont compatibles avec les aliments pour animaux de ferme. Elles font référence à l'apport de nutriments (directement ou par le biais de leur meilleure disponibilité) et à leur digestion ou absorption. Ceci peut être effectué au moyen de modifications gastro-intestinales. Les produits présentant des allégations relatives au maintien, à la croissance et au rendement amélioré des animaux peuvent être acceptés comme aliments pour animaux de ferme.
Des exemples d'allégations sont fournis dans le tableau ci-après.
| Loi sur les aliments et drogues et ses règlements | Loi relative aux aliments du bétail et ses règlements | |
|---|---|---|
| Allégations thérapeutiques – Drogue nouvelle (numéro d'identification du médicament) |
Allégations de santé générale – PSATableau E-3.1 Note de bas de page 1 (numéro de notification) |
Allégations d'aliments – Aliments (numéro d'enregistrement) |
Prévention/traitement des maladies:
Réduction des pathogènes:
Autre:
|
|
Ajusteur de pH:
Modificateur gastro-intestinal:
Digestion:
Production et de performance:
|
Remarque : Ce tableau est présenté à titre d'illustration uniquement. Il ne doit pas être considéré comme une liste exhaustive et complète. Si l'indication d'un produit ne figure pas dans le tableau, veuillez contacter la Direction des médicaments vétérinaires (en tant que guichet unique pour la classification) pour une évaluation plus approfondie.
|
||
3.4 Formes posologiques
Conformément au document d'orientation, les formes posologiques qui nécessitent une administration forcée (par exemple, les bolus et les comprimés) sont réglementées en vertu du Règlement sur les aliments et drogues, en tant que drogues nouvelles vétérinaires ou PSA. Les formes posologiques orales qui ne nécessitent pas une administration forcée peuvent être réglementées soit en vertu du Règlement sur les aliments et drogues, soit en vertu du Règlement sur les aliments du bétail, selon les autres critères de classification. Dans le but d'assurer une surveillance réglementaire et une application de normes uniformes en matière d'innocuité, d'efficacité et de qualité, les produits administrés sous forme posologique orale seront réglementés tel qu'illustré dans le tableau E-3.2.
| Drogue nouvelleTableau E-3.2 Note de bas de tableau 1 Numéro d'identification du médicament |
Produits de santé animaleTableau E-3.2 Note de bas de tableau 1 Numéro de notification |
AlimentTableau E-3.2 Note de bas de tableau 2 Numéro d'enregistrement |
|
|---|---|---|---|
| Administration forcée (par exemple, bolus, comprimé, gavage) |
Oui | Oui | Non |
| Mélangé dans les aliments | Oui | NonTableau E-3.2 Note de bas de tableau 3 | Oui |
| Sur l'aliment | Oui | Oui | Oui |
| Dans l'eau | Oui | Oui | Oui |
|
|||
Note de bas de page
- Note de bas de page 1
-
Les produits de santé animale sont des médicaments vétérinaires sous forme posologique utilisés pour maintenir ou promouvoir la santé et le bien-être des animaux. Les PSA ne peuvent être vendus ou présentés pour être utilisés dans le diagnostic, le traitement et l'atténuation d'une maladie, d'un trouble ou d'un état physique anormal, ou de ses symptômes. À l'heure actuelle, les PSA déclarés ne peuvent être mélangés aux aliments pour lesquels s'applique le Règlement sur les aliments du bétail.
Pour de plus amples renseignements sur les PSA et la voie de notification de PSA:
Détails de la page
- Date de modification :