Pratiques de base et précautions additionnelles visant à prévenir la transmission des infections dans les milieux de soins
Partie A : Introduction aux pratiques de base et aux précautions additionnelles
I. Introduction
Les Pratiques de base et précautions additionnelles visant à prévenir la transmission des infections dans les milieux de soins représentent les pratiques de PCI à suivre dans tous les milieux de soins au Canada, ainsi que les pratiques et processus exigés en matière de soins. Les présentes lignes directrices ont pour objet de définir et de préconiser des pratiques et des précautions de PCI qui visent à prévenir la transmission des infections dans tous les milieux de soins. Ces lignes directrices s'adressent aux professionnels en prévention des infections (PPI). Il est recommandé aux personnes qui manquent d'expérience dans le domaine de la PCI de faire appel aux compétences des PPI de leur organisation ou de leur région.
La présente révision préconise l'application systématique de pratiques de base et de précautions additionnelles sur tout le continuum des soins et énonce les modifications apportées à l'application des précautions additionnelles dans les milieux autres que les soins de courte durée. Les présentes lignes directrices devraient permettre d'élaborer des recommandations précises pour une région donnée qui soient adaptées aux particularités locales, telles que la nature des établissements existants, le risque de contracter une infection, la nature des milieux de soins, le type de soins et le niveau d'éducation et de sensibilisation des travailleurs de la santé (TS) qui dispensent les soins. Ce document comprend les principes nécessaires à la prévention de la transmission de microorganismes d'un patient à l'autre, d'un patient à un TS et d'un TS à un patient sur tout le continuum des soins. Ce document ne présente pas une approche globale de la reconnaissance, du signalement et de la gestion des éclosions, mais fournit des recommandations visant à prévenir certaines des situations épidémiques les plus fréquents (p. ex. hygiène respiratoire pour prévenir les éclosions de virus respiratoire; nettoyage de l'environnement et hygiène des mains pour prévenir les éclosions de Clostridium difficile et de norovirus). Aux fins du présent document, le terme « patient » inclut les personnes qui reçoivent des soins de santé et que l'on désigne traditionnellement ou généralement par les termes patient, client ou résident. On trouve dans ce document des principes relatifs à la transmission, ainsi que des pratiques de base et des précautions additionnelles, pour les milieux de soins de courte durée, de SLD, de soins préhospitaliers et de soins à domicile. Aux fins du présent document, les soins de courte durée comprennent les milieux de soins ambulatoires, comme les services des urgences des hôpitaux, et les interventions chirurgicales (ambulatoires) ou autres interventions ambulatoires invasives autonomes ou associées à un établissement (p. ex. les unités d'endoscopie, d'hémodialyse, les unités de soins ambulatoires pour blessés).
A. Principes qui sous-tendent le présent document
Le présent document reconnaît certains principes :
- Les pratiques de base devraient être systématiquement appliquées aux soins dispensés à tous les patients sur tout le continuum des soins.
- La conformité aux pratiques de base peut réduire la transmission des microorganismes dans les milieux de soins.
- Les aspects individuels des pratiques de base sont déterminés par une évaluation du risque au point de service (ERPS) (c'est-à-dire un examen qui comprend l'évaluation de la tâche à effectuer ou des soins à prodiguer, le tableau clinique du patient, l'état physique de l'environnement et le milieu de soins).
- Les microorganismes peuvent être transmis par des sujets symptomatiques et asymptomatiques, ce qui renforce l'importance du respect systématique des pratiques de base pour tous les patients et dans tous les milieux de soins.
- Outre les pratiques de base, on devrait utiliser des précautions avec les patients atteints d'infections présumées ou connues ou colonisés par des microorganismes, pour lesquels les pratiques de base ne suffisent pas à prévenir la transmission.
- Les précautions additionnelles devraient être prises de façon empirique, en fonction de la maladie ou du tableau clinique des patients. On peut les modifier ou les abandonner selon le microorganisme précis identifié.
- Les programmes de PCI visent principalement à réduire le risque d'acquisition d'une infection associée aux soins de santé (IASS) à un niveau minimum; il sera peut-être impossible d'obtenir un risque zéro dans chaque cas, mais il faut néanmoins y tendre. Les conséquences de la transmission croisées de microorganismes devraient être comparées aux conséquences (effets indésirables et coûts) des précautions prises.
- L'application des précautions additionnelles peut varier entre les milieux de soins de courte durée, de SLD, de soins ambulatoires, de soins préhospitaliers et de soins à domicile. On devrait tenir compte des données épidémiologiques locales dans l'application des précautions additionnelles.
Modifications importantes amenées par la présente révision :
- Les TS sont censés utiliser au point de service un DMBA à titre de méthode privilégiée d'hygiène des mains dans tous les milieux de soins, à moins qu’une exception ne s’applique (c.-à-d. lorsque les mains sont visiblement souillées par des matières organiques ou si l’exposition à un norovirus et à des agents pathogènes sporulés comme Clostridium difficile est fortement soupçonnée ou avérée, y compris au cours d’éclosions impliquant ces organismes).
- Les chambres de malades hospitalisés individuelles sont préférées aux chambres communes et comprennent des toilettes et un lavabo à l'usage du patient, ainsi que des lavabos réservés au lavage des mains à l'usage des TS.
- L'hygiène respiratoire, une stratégie comprenant diverses mesures visant à réduire au minimum la transmission des agents pathogènes des voies respiratoires sur tout le continuum des soins, a été mise en œuvre.
- La recommandation concernant la séparation spatiale entre un patient atteint d'une infection respiratoire transmissible par gouttelettes présumée ou confirmée qui tousse (source infectée) et un autre patient non atteint de cette infection (hôte réceptif) est passée de 1 mètre à 2 mètres. Lorsque l'on évalue les risques, il se peut qu'une distance de 1 mètre soit suffisante pour les jeunes enfants et les autres patients dont la toux n'est pas assez forte pour projeter les gouttelettes à 2 mètres.
- Des stratégies ont été mises en œuvre pour réduire la production d'aérosols au cours des interventions médicales générant des aérosols (IMGA) sur les patients qui présentent des signes et des symptômes de tuberculose (TB) présumée ou confirmée, de SRAS présumé ou confirmé ou d'infection respiratoire présumée ou confirmée avec agent pathogène des voies respiratoires émergent. (Consulter l'analyse des IMGA à la partie A, section II, C, 2c et les stratégies de réduction de la production d'aérosols à la partie B, section IV, sous-section iii, 1b.) Des pratiques de base et des précautions contre la transmission par gouttelettes, comme il est indiqué, doivent être suivies pour les IMGA effectuées sur les autres patients.
- La recommandation que les patients adultes atteints d’une infection respiratoire virale connue ou présumée (pratique actuelle en pédiatrie) devraient être soumis à des précautions contre la transmission par contact et par gouttelettes a été modifiée.
- On a réaffirmé que les TS doivent respecter une technique aseptique pour les interventions invasives et pour la manipulation et l'administration des médicaments à prendre par voie parentérale et des systèmes intraveineux.
- Les organisations de soins de santé sont tenues d'effectuer une évaluation du risque organisationnel (ERO), c'est-à-dire d'évaluer l'environnement des soins de santé afin de déterminer le risque d'exposition aux microorganismes et de mettre en œuvre les mesures de contrôle appropriées (p. ex. conception des établissements de santé et nettoyage, désinfection et stérilisation du matériel de soins aux patients).
- On insiste sur le fait que les TS sont tenus d'effectuer une ERPS avant chaque interaction avec un patient, en tenant compte du patient, de son environnement et de la nature de l'interaction.
B. Pratiques de base
Les pratiques de base sont les pratiques de PCI à respecter pour les soins de base dispensés à tous les patients en tout temps et dans tous les milieux de soins. Elles sont déterminées par les circonstances du patient, l'environnement et la tâche à effectuer.
En réalisant une évaluation du risque organisationnel (ERO) (consulter la partie A, section III, B) et en remédiant aux insuffisances, on obtient le cadre nécessaire pour s'assurer que les composantes pertinentes de la hiérarchie des mesures de contrôle liée aux pratiques de base sont en place pour réduire au minimum le risque d'exposition et de transmission des microorganismes dans les milieux de soins.
Les TS effectuent une ERPS pour déterminer les mesures de PCI appropriées pour dispenser des soins sécuritaires aux patients (c.-à-d. protéger les patients contre la transmission de microorganismes) et pour protéger les TS contre l'exposition aux microorganismes (liée, p. ex. à la projection de gouttelettes de sang, de liquides organiques, de sécrétions des voies respiratoires ou d'autres sécrétions ou excrétions, et aux aiguilles et autres objets pointus et tranchants contaminés). (Consulter la partie A, section III, C.)
Les pratiques de base comprennent :
- l'évaluation du risque au point de service;
- le programme d'hygiène des mains (y compris le DMBA au point de service);
- le contrôle à la source (triage, diagnostic et traitement rapides, hygiène respiratoire, séparation spatiale);
- l'hébergement, le placement et les déplacements des patients;
- la technique aseptique;
- l'utilisation d'un EPI;
- la manipulation sécuritaire des objets pointus et tranchants et la prévention de la transmission des pathogènes à diffusion hématogène;
- la gestion de l'environnement où sont dispensés les soins aux patients;
- la gestion de l'environnement où sont dispensés les soins aux patients;
- le nettoyage et la désinfection du matériel non critique destiné aux soins aux patients;
- la gestion du linge et des déchets;
- l'éducation des patients, des familles et des visiteurs;
- la gestion des visiteurs.
C. Précautions additionnelles
Les précautions additionnelles sont appliquées lorsque les caractéristiques de transmission ou l'incidence d'une infection par un microorganisme précis (p. ex. les microorganismes à faible dose infectieuse, comme Shigella spp., les microorganismes qui se propagent par gouttelettes, comme le virus respiratoire syncytial [RSV] ou les microorganismes importants du point de vue épidémiologique, comme les microorganismes résistants aux antibiotiques [MRA]) ou de syndromes ne peuvent pas être complètement prévenus par les pratiques de base. Ces précautions devraient également être prises lorsque les interventions médicales augmentent le risque de transmission d'un agent infectieux précis (p. ex. les IMGA) ou lorsque la situation clinique empêche l'application systématique des pratiques de base (p. ex. soins dispensés à un jeune enfant, à un adulte incontinent ou à une personne ayant une déficience cognitive). La manière d'appliquer les précautions additionnelles dépend du milieu de soins (soins de courte durée, soins ambulatoires, soins préhospitaliers, SLD et soins à domicile).
Les précautions additionnelles sont généralement réparties en :
- précautions contre la transmission par contact, pour les microorganismes à très faible dose infectieuse ou dans les situations où l'on s'attend à une forte contamination de l'environnement du patient;
- précautions contre la transmission par gouttelettes, pour les microorganismes qui sont principalement transmis par grosses gouttelettes;
- précautions contre la transmission par voie aérienne, pour les microorganismes qui sont transmis par voie aérienne sur une longue période et une longue distance par de petites particules.
Certaines infections peuvent nécessiter une combinaison de précautions additionnelles (contre la transmission par contact, par gouttelettes et par voie aérienne), puisque certains microorganismes peuvent être transmis par plus d'une voie. L'application des pratiques de base se poursuit même avec l'application de précautions additionnelles.
En réalisant une ERO (consulter la partie A, section III, B) et en remédiant aux insuffisances, on obtient le cadre nécessaire pour s'assurer que les composantes pertinentes de la hiérarchie des mesures de contrôle (consulter la partie A, section III, A) liée aux pratiques de base sont en place pour réduire au minimum le risque d'exposition et de transmission des agents infectieux dans les milieux de soins.
D. Évolution des précautions d'isolement
Les précautions d'isolement ont évolué depuis l'époque des hôpitaux où étaient confinés les patients atteints de certaines maladies transmissibles qui constituaient un problème important de santé publique, telles que la variole, la diphtérie et la tuberculoseNote de bas de page 1. Avec le recul de ces maladies, les patients ont été hébergés dans des services spéciaux d'isolement des hôpitaux généraux et, finalement, dans des chambres à un lit faisant partie des services ordinaires de soins. Au fil du temps, les précautions d'isolement ont été étendues à tous les patients atteints d'une infection jugée transmissible. Les maladies infectieuses ont été classées en fonction du principal mécanisme présumé de transmission et, pour chaque catégorie de transmission, des précautions particulières ont été recommandéesNote de bas de page 2. Les précautions à prendre pour chaque catégorie étaient indiquées sur une fiche imprimée. Elles étaient faciles à apprendre et à appliquer. Toutefois, les lignes directrices fondées sur des catégories ont eu tôt fait de générer de l'insatisfaction. Les mécanismes de transmission de la maladie ne correspondaient pas toujours aux catégories établies, ce qui se traduisait par un recours excessif ou inadéquat aux techniques offrant une barrière physique (ci-après appelées « techniques de protection »). Les travailleurs de la santé voulaient jouir d'une plus grande latitude dans l'application des précautions d'isolementNote de bas de page 3, Note de bas de page 4.
On a donc conçu un nouveau système, fondé sur les maladies, qui permettait d'adapter les précautions d'isolement aux besoins de chaque patient et de chaque microorganisme. Les hôpitaux étaient libres de choisir entre le système fondé sur les catégories et celui fondé sur les maladiesNote de bas de page 3. Des techniques de protection particulières (p. ex. chambres à un lit, systèmes de traitement de l'air, gants, blouses et masques) ont été établies en fonction du diagnostic ou des symptômes du patient ou du microorganisme qui avait été isolé, ainsi que des caractéristiques comportementales du patient (p. ex. âge, état mental, mobilité, continence). Les précautions d'isolement ont été inscrites sur une fiche ou indiquées en cochant des cases. Le système fondé sur les maladies a permis d'éliminer les mesures inutiles et de rendre plus efficace l'utilisation des installations et du matériel. On estimait que ces précautions contribueraient à accroître l'observance, étant donné qu'elles reposaient sur une assise plus solide sur le plan épidémiologique. Une plus grande importance a été accordée à la prise de décisions par les TS. Ce système présentait toutefois un certain nombre d'inconvénients. Il demandait davantage de connaissances, d'initiative et de responsabilité de la part des TS. Le choix des techniques indiquées pour un patient donné demandait du temps, et il y avait un risque d'erreur lorsque les TS n'étaient pas bien informés ou étaient pressés ou lorsque le diagnostic était incorrectNote de bas de page 5, Note de bas de page 6.
La modification la plus importante a été apportée aux précautions d'isolement lorsqu'on a constaté que le VIH (virus de l'immunodéficience humaine) pouvait être transmis à des TS par des patients atteints d'une infection non diagnostiquéeNote de bas de page 7. Il ne suffisait plus, désormais, d'appliquer les précautions contre les pathogènes transmissibles par le sang en se fondant sur les symptômes ou le diagnostic. Pour faire face à ce problème, on a étendu à tous les patients l'utilisation des précautions applicables au sang et aux liquides organiques. Ces précautions, appelées précautions universelles applicables au sang et aux liquides organiques, comprennent les mesures de protection, telles que le port de gants lors des contacts avec le sang et certains autres liquides organiques; le port d'une blouse, d'un masque et d'une protection des yeux lorsque la peau ou les vêtements risquent d'être contaminés ou éclaboussés par ces liquides; des mesures visant à prévenir les blessures causées par des aiguilles contaminées et d'autres instruments pointus ou tranchants, et les protocoles de nettoyage des déversements de sang et de sécurité en laboratoire.
Les précautions universelles visaient expressément à éviter que des patients ne transmettent des agents pathogènes aux TS par voie sanguine. Le principe à la base des précautions universelles était le suivant : il est impossible de savoir quels sont les patients porteurs d'agents pathogènes transmissibles par le sang. Les précautions universelles étaient employées conjointement avec le système d'isolement fondé sur les catégories ou celui fondé sur les maladies lorsque les patients présentaient des symptômes précis ou étaient atteints d'une infection particulièreNote de bas de page 8, Note de bas de page 9.
De l'avis de certains, les précautions d'isolement étaient insatisfaisantes, car elles ne tenaient pas compte du fait que des microorganismes pathogènes peuvent être présents, dans des substances organiques, chez des patients asymptomatiques. C'est pour combler cette lacune qu'on a conçu un nouveau système d'isolement, les précautions applicables aux liquides organiques, qui permettaient d'adapter les mesures de protection à l'intervention plutôt qu'au diagnostic. Ce système étendait les mesures de protection à tous les contacts directs avec le sang, les liquides organiques, les sécrétions et les substances humides de l'organisme ainsi qu'avec la peau non intacteNote de bas de page 10, Note de bas de page 11, Note de bas de page 12.
Il fallait porter des gants lors de tous ces contacts. Les blouses, les masques et une protection des yeux étaient recommandés lors des interventions présentant un risque de souillures ou d'éclaboussures. Les précautions applicables aux liquides organiques tenaient pour acquis que tous les individus sont porteurs d'agents potentiellement pathogènes, présents dans les sites et les substances humides de l'organisme, et que tous également risquent de contracter ces infections, par inoculation des muqueuses et de la peau non intacte. Les précautions applicables aux liquides organiques visaient à empêcher la transmission en faisant en sorte que les mains des TS ne soient pas contaminées. On observait une certaine confusion quant à la nécessité du lavage des mains après l'enlèvement des gants. Les précautions applicables aux liquides organiques n'empêchaient ni la transmission par l'intermédiaire de gouttelettes ni la transmission par voie aérienneNote de bas de page 13, Note de bas de page 14.
Le Centers for Disease Control and Prevention (CDC) des États-Unis ont révisé en 1996 leurs lignes directrices relatives à l'isolement en retenant, de chacun des systèmes antérieurs, les recommandations qui leur semblaient les plus pertinentesNote de bas de page 13. Ces lignes directrices ne s'appliquaient qu'aux établissements de soins de courte durée dispensés à des patients hospitalisés. C'est ainsi qu'ils ont conçu un système à deux paliers, comprenant les précautions standard, qui s'appliquent à tous les patients, et trois catégories de précautions fondées sur la transmission, qui visent des infections particulières nécessitant des mesures additionnelles. Les précautions standard tiennent compte du risque de transmission par contact avec des patients asymptomatiques et avec des éléments contaminés de l'environnement du patient infecté ou colonisé. Le port de gants est non seulement recommandé pour tous les contacts, conformément aux précautions applicables aux liquides organiques, mais aussi pour des contacts avec des objets contaminés. Les trois catégories de précautions additionnelles ont été fondées sur les modes de transmission connus ou présumés (par voie aérienne, par gouttelettes, par contact) et les caractéristiques du patient. Les précautions contre la transmission par contact étaient plus étendues qu'auparavant, en ce sens que toutes les personnes qui pénétraient dans la chambre du patient devaient appliquer les techniques de protectionNote de bas de page 13. Le document 2007 Guideline for Isolation Précautions: Preventing Transmission of Infectious Agents in Healthcare Setting Note de bas de page 15fournit des recommandations qui peuvent être appliquées dans tous les milieux de soins et ajoute quelques nouveaux aspects aux précautions standard.
E. Historique des lignes directrices relatives à l'isolement au Canada
Les lignes directrices relatives à la prévention des infections et à l'isolement ont été publiées à l'origine en 1985 par le Comité directeur des lignes directrices pour la prévention et le contrôle des infections, mis sur pied par le Bureau de l'épidémiologie des maladies transmissibles du Laboratoire de lutte contre la maladie de Santé Canada. Ces lignes directrices, révisées en 1990Note de bas de page 16, étaient rédigées selon une perspective fondée sur la maladie et dressaient une liste de précautions particulières à prendre pour une maladie ou un microorganisme donnés. Dans la version révisée de 1990, on a ajouté une liste de symptômes qui devait guider la détermination des précautions d'isolement. Les précautions universellesNote de bas de page 17, Note de bas de page 18, Note de bas de page 19, qui ont été intégrées à la version révisée de 1990, avaient été énoncées dans des documents distincts publiés en 1987, 1988 et 1989. Des SLD de longue durée ont été publiées en 1986 et révisées en 1994Note de bas de page 20. On n'y aborde pas expressément les questions liées à l'isolement dans les établissements de SLD, le lecteur étant invité à consulter le Guide de prévention des infections - Techniques d'isolement et précautions de 1990 de Santé CanadaNote de bas de page 16. Des recommandations relatives à la prévention de la tuberculose ont été publiées en 1996Note de bas de page 21. Des lignes directrices révisées, publiées en 1997, traitent de la prévention de la transmission de pathogènes à diffusion hématogèneNote de bas de page 22, et des entérocoques résistants à la vancomycine (ERV)Note de bas de page 23.
Des lignes directrices relatives à l'isolation et des précautions révisées, intitulées Pratiques de base et précautions additionnelles visant à prévenir la transmission des infections dans les établissements de santé, ont été publiées en 1999Note de bas de page 24. Le terme « pratiques de base » a été choisi pour bien souligner que ce niveau de soins devrait être dispensé à tous les patients, en tout temps et dans tous les milieux de soins. Lorsque les pratiques de base ne suffisent pas, il faudrait prendre des « précautions additionnelles ». Les Pratiques de base et précautions additionnelles visant à prévenir la transmission des infections dans les établissements de santé de 1999 présentaient des recommandations propres aux milieux de soins de courte durée, de soins de longue durée, de soins ambulatoires et de soins à domicile. Les recommandations relatives aux milieux de soins de courte durée ne différaient en principe pas des précautions standard et des précautions fondées sur la transmission publiées par le CDC en 1996, bien que le document canadien soit plus détaillé.
F. Changements observés dans les populations de patients et les systèmes de prestation des soins
Au cours des dix dernières années, les systèmes de prestation des soins ont fait l'objet d'une constante restructuration. La population de patients des hôpitaux de soins de courte durée a continué de se transformer et compte maintenant davantage de sujets à risque élevé d’IASS. Grâce à de nouvelles technologies et à des traitements agressifs, dont beaucoup affaiblissent les réactions de défense de l'hôte, des patients autrefois condamnés survivent aujourd'hui. Les greffes d'organes et de cellules souches hématopoïétiques, l'infection par le VIH et le vieillissement de la population ont encore accru le nombre de patients à risque élevé. Ce changement est à l'origine d'une augmentation du nombre de patients gravement malades dans les établissements de soins de courte durée et du degré de gravité des maladies traitées dans les établissements de SLD (qui fournissent des soins complexes, comme la thérapie intraveineuse, l'hémodialyse ou la ventilation artificielle), ainsi que de la réalisation d'interventions invasives et de traitements complexes en traitement de jour ou en milieu ambulatoire, ce qui expose la population au risque d'infections associées aux soins de santé. De nombreuses maladies sont désormais traitées en consultation externe ou à domicile. En outre, le vieillissement de la population a augmenté la demande de services de soins de santé au même moment où le pays connaît une pénurie de TS.
Les IASS posent un risque potentiel sur tout le continuum des soins, des soins préhospitaliers aux hôpitaux de soins de courte durée, aux centres de réadaptation, aux établissements de SLD, aux maisons de soins infirmiers, aux centres de soins aux adultes en résidence, aux centres de soins ambulatoires et aux services de soins à domicile. Il arrive fréquemment que des patients soient transférés d'un établissement à l'autre et, à l'intérieur d'un même établissement, d'un niveau de soins à un autreNote de bas de page 25; il n'est pas rare non plus que des patients ayant subi un traumatisme (comme les soldats de retour du frontNote de bas de page 26 ou les personnes qui ont été hospitalisées à l'étranger) soient rapatriés dans un établissement canadien. Ces transferts augmentent le risque de transmission de microorganismes résistants aux antibiotiques.
G. Fardeau des infections associées aux soins de santé
Les infections associées aux soins de santé (p. ex. les infections du site opératoire, les bactériémies associées à l'utilisation d'un cathéter veineux central) entraînent un lourd fardeau de la maladie chez les Canadiens et représentent un problème de santé publique importantNote de bas de page 27, Note de bas de page 28, Note de bas de page 29. Ce fardeau pèse également sur le système de soins de santé canadien, et les Canadiens n'ont pas toujours accès aux soins en temps opportun.
Aucun relevé complet des occurrences d'IASS n'a été effectué au Canada; cependant, on estime généralement que 5 % à 10 % des Canadiens hospitalisés sont atteints d'une IASSNote de bas de page 30. Une enquête menée auprès d'hôpitaux sentinelles canadiens en février 2002 par Gravel et al. a permis d'établir que 10,5 % des patients adultes hospitalisés et 9,1 % des patients pédiatriques hospitalisés faisant partie de l'enquête avaient été atteints d'une IASSNote de bas de page 28, Note de bas de page 29. En 2009, Gravel et al. ont répété l'enquête avec un groupe d'hôpitaux similaires. Ils ont constaté que 12,3 % des patients adultes et 7,2 % des patients pédiatriques étaient atteints d'une IASS le jour de l'enquête. Entre les deux enquêtes, le nombre de patients faisant l'objet de précautions d'isolement a quasiment doublé (de 7,7 % à 14,8 %), ce qui est principalement dû à l'incidence de l'infection par C. difficile et des microorganismes résistants aux antibiotiques (communication personnelle, Programme canadien de surveillance des infections nosocomiales, 2010). Après avoir extrapolé les données américaines, Zoutman et al. ont estimé qu'environ 220 000 IASS se déclarent chaque année au Canada, et que l'on peut attribuer plus de 8 000 décès aux IASSNote de bas de page 27. Le type, la fréquence et la gravité des infections associées aux soins de santé varient. Par exemple, les infections urinaires associées aux soins de santé figurent parmi les IASS les plus fréquentes, mais n'ont pas de répercussions très graves sur les patientsNote de bas de page 31. En revanche, le taux de mortalité associé à la pneumonie liée à la ventilation méchanique, plus rare, dépasse 10 %Note de bas de page 32.
Le traitement des infections associées aux soins de santé est également coûteux. Aux États-Unis, on estime que les coûts attribuables au traitement des IASS varient de 1 257 dollars américains pour les infections urinaires à 9 986 dollars américains pour la pneumonie associée à la ventilation artificielleNote de bas de page 30. Les coûts d'hospitalisation par patient pour une cohorte de patients infectés en hôpital par le Staphylococcus aureus résistant à la méthicilline (SARM) et un groupe de comparaison correspondant de patients non infectés ont été examinés dans le cadre d'une étude visant à déterminer les coûts supplémentaires attribuables au SARM dans un hôpital canadien. Les coûts d'hospitalisation médians totaux par patient atteint de SARM nosocomial (colonisé et infecté) s'élevaient à 14 841 $, alors que les coûts correspondant pour les patients non infectés du groupe de comparaison atteignaient 5 844 $, ce qui laisse entendre des coûts supplémentaires de 8 997 $ par patient atteint de SARMnosocomial. Les coûts supplémentaires associés à la prévention d'un cas de SARMnosocomial s'élevaient à 19,77 $. Les auteurs ont laissé entendre qu'il est possible d'améliorer le rapport coût-efficacité en raccourcissant les séjours hospitaliersNote de bas de page 33.
Les patients atteints d'IASS occupent des lits d'hôpital en forte demande (p. ex. les infections du site opératoire acquises en milieu de soins prolongent les séjours hospitaliers de 25,7 jours en moyenne)Note de bas de page 30 et l'étude et le traitement de ces infections mobilisent d'autres ressources limitées en soins de santé. Les infections associées aux soins de santé représentent donc un obstacle important à l'accès aux soins pour les patients atteints d'autres maladies.
Toutes les interventions thérapeutiques présentent des risques potentiels, y compris le risque d'infection, et des avantages potentiels. À l'heure actuelle, toutes les IASS ne sont pas évitables. Cependant, elles ne sont pas inévitables; on sait depuis de longues annéesNote de bas de page 34 que les démarches organisées de prévention des IASS sont très efficaces pour réduire la fréquence de ces dernières. Il existe un écart entre les infections associées aux soins de santé que l'on pourrait éviter et celles que l'on évite actuellement, car les TS de première ligne ne connaissent pas bien les stratégies de prévention et de les mettent pas en œuvre, et les gestionnaires et administrateurs des soins de santé n'accordent pas une priorité adéquate aux stratégies de prévention des IASS.
L'application des Pratiques de base et précautions additionnelles visant à prévenir la transmission des infections dans les milieux de soins est un aspect important d'une approche globale de la prévention des IASS. En adoptant les recommandations figurant dans ce document sur tout le continuum des soins, il est possible d'alléger le fardeau des IASS qui pèse sur les Canadiens et sur le système de soins de santé canadien.
H. Trouver l'équilibre entre les risques et les avantages liés à la prévention de la transmission croisée
Idéalement, le mode de prestation des soins devrait permettre de maximiser la probabilité de prévenir toute transmission de microorganismes pathogènes, à partir de tous les patients colonisés asymptomatiques ainsi qu’à partir de tous les patients symptomatiques, dans tous les milieux de soins. Mais c'est un objectif utopique. Il n'est pas toujours possible de prévenir la transmission des microorganismes dans les milieux de soins, et les efforts déployés en ce sens risqueraient d'engendrer des coûts supplémentaires et d'imposer des contraintes qui affecteraient la qualité de vie du patient ou d'écarter des interventions ou des actes médicaux potentiellement bénéfiques. Par conséquent, les pratiques de PCI devraient être adaptées au niveau des soins dispensés et au risque inhérent qu'ils présentent pour la personne et la population en cas d'infection éventuelle. Les précautions dont la rentabilité est évidente dans une unité de soins intensifs (USI) ou un service de soins de courte durée pourraient ne pas être aussi utiles ni aussi indiquées pour les patients d'un établissement de SLD.
Il convient d'éviter de prendre des précautions additionnelles superflues. Il est évident que les pratiques d'isolement peuvent être stigmatisantes et préjudiciables sur le plan psychologique, et qu'elles présentent un risque inhérent d'effets indésirables pour la qualité des soins dispensés (p. ex. erreurs médicales)Note de bas de page 35, Note de bas de page 36, Note de bas de page 37, Note de bas de page 38, Note de bas de page 39. En outre, les pratiques d'isolement inutiles sont coûteuses et mobilisent des ressources limitées en soins de santé dont d'autres patients pourraient bénéficier. Par conséquent, il ne faudrait mettre en œuvre que des pratiques d'isolement de PCI qui sont clairement indiquées dans le milieu où les soins sont dispensés, et on devrait les supprimer dès que possible.
Dans la majorité des cas, les précautions qui s'imposent sont claires, à la lumière des données disponibles. Dans d'autres circonstances, il peut s'avérer nécessaire d'adapter certaines mesures en fonction des différents types d'établissements, en se fondant sur une évaluation des risques et des avantages. Il convient d'examiner côte à côte les avantages découlant d'une réduction du risque de transmission et le coût (sur le plan de la qualité de vie, le caractère adéquat des soins médicaux et les dépenses engagées) des précautions requises pour obtenir cette réduction du risque.
II. Principes relatifs à la transmission des microorganismes
A. Chaîne de l'infection
C'est grâce à l'analyse des données épidémiologiques que nous pouvons prévenir les maladies, car elle permet d'expliquer la répartition des maladies (d'un patient à l'autre, d'un endroit à l'autre et au fil du temps) et de définir les facteurs modifiables qui ont des répercussions sur leur apparition et leur issue. Elle justifie les mesures de contrôle visant à réduire au minimum la transmission de microorganismes et à diminuer, en fin de compte, l'incidence des IASS chez les patients et des infections professionnelles chez les TS.
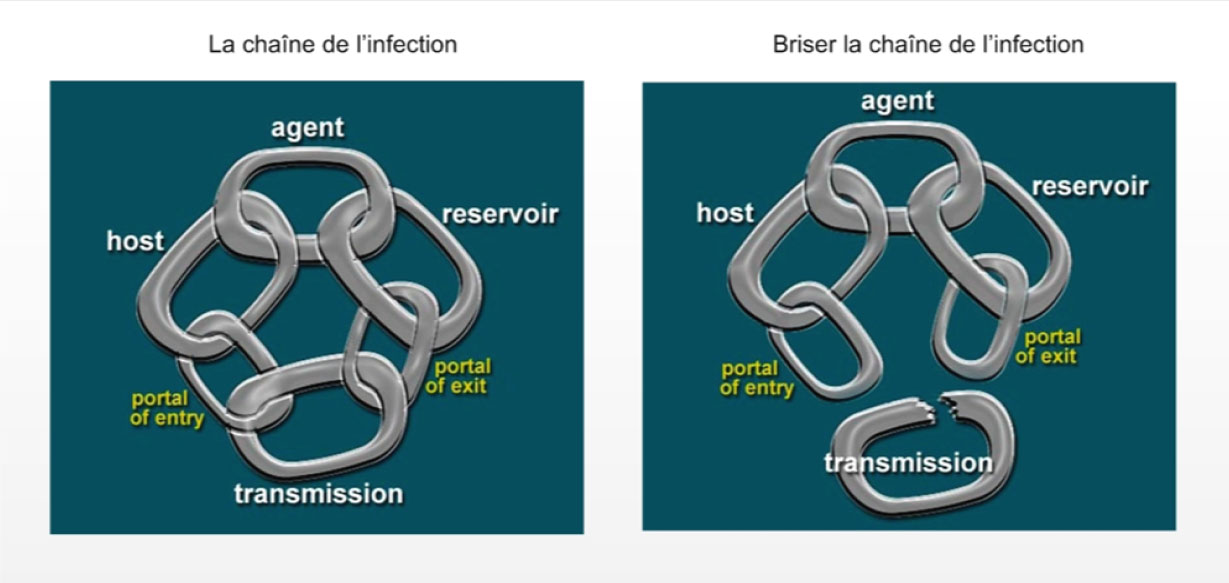
La transmission des microorganismes peut entraîner un portage passager ou une colonisation à long terme, une infection asymptomatique ou une maladie clinique. On appelle colonisation la présence de microorganismes en croissance ou multiplication dans ou sur un hôte, mais sans invasion des tissus ou lésion cellulaire. L'infection est le stade auquel les microorganismes sont capables de se multiplier dans l'organisme et provoquent une réaction des défenses immunitaires de l'hôte. Une infection peut entraîner ou non une maladie clinique (infection symptomatique). Pour qu'une infection survienne, il faut qu'un ensemble de liens étroits et complexes existent entre la source de l'agent infectieux (le microorganisme), l'hôte réceptif et l'environnement, et que les microorganismes soient transmis de la source à l'hôte réceptif. Un cadre conceptuel utile pour comprendre ces liens complexes est la chaîne de l'infection, qui peut être composée de six maillons (illustrés dans la figure 1a) : l'agent infectieux, le réservoir, la porte de sortie, le mode de transmission, la porte d'entrée et l'hôte réceptif. Il est possible de prévenir une infection en brisant n'importe lequel des maillons de la chaîne de l'infection (figure 1b).
Figure 1a et 1b. Chaîne de l'infection
Autorisation d'utiliser les images fournie par la Dre Donna Moralejo, professeure agrégée,
Memorial University School of Nursing, St. John's, Terre-Neuve-et-Labrador
Description textuelle
La figure 1 illustre la chaîne de l'infection qui est un cadre conceptuel utile pour comprendre ces liens complexes qui peut être composée de six maillons : l'agent infectieux, le réservoir, la porte de sortie, le mode de transmission, la porte d'entrée et l'hôte réceptif.
La figure 1b illustre qu'il est possible de prévenir une infection en brisant n'importe lequel des maillons de la chaîne de l'infection tel qu'illustré dans la figure 1a.
Voici une brève explication de chacun des maillons :
1. Agents infectieux (microorganismes)
Ils comprennent les bactéries, les virus, les champignons et les parasites. Ils peuvent appartenir soit à la flore endogène (c.-à-d. les propres microorganismes du patient), soit à la flore exogène (c'est-à-dire les microorganismes étrangers au patient, qui proviennent par exemple d'autres personnes, de plantes ou d'objets inanimés). Qu'ils proviennent d'autres parties du corps, d'une autre personne ou d'un autre objet, les microorganismes sont considérés comme faisant partie de la flore passagère si le patient n'en est que temporairement porteur (consulter la partie A, section II, B). Les antimicrobiens, les désinfectants et l'hygiène des mains par DMBA tuent les microorganismes et brisent ce maillon de la chaîne de l'infection, lorsque c'est possible. Les caractéristiques d'un microorganisme donné influent sur la facilité avec laquelle il se transmet. Les microorganismes qui peuvent survivre dans les conditions du milieu et rester viables sur des objets inanimés, comme le matériel de soins aux patients, ont une probabilité de transmission plus élevéeNote de bas de page 40, Note de bas de page 41, Note de bas de page 42, Note de bas de page 43 tel que ceux avec une dose infectieuse est minime (p. ex. Shigella)Note de bas de page 44.
2. Réservoirs dans les établissements de santé
Les humains, les animaux et l'environnement sont les réservoirs d'agents infectieux (microorganismes) que l'on rencontre dans le domaine des soins de santé. L'hygiène des mains suivant le contact avec des personnes ou leur environnement, la préparation préopératoire de la peau et le nettoyage de l'environnement réduisent le nombre de microorganismes présents dans un réservoir, ce qui contribue à briser ce maillon de la chaîne de l'infection (consulter la partie A, section II, B).
3. Portes de sortie
Une porte de sortie est la voie par laquelle un agent infectieux (microorganisme) quitte le réservoir, bien que tous les réservoirs n'aient pas une porte de sortie évidente (p. ex. l'environnement). Les agents infectieux, selon leur nature, sont contenus dans les réservoirs que sont le sang, les liquides organiques, les excrétions, les sécrétions et la peau humaine, et quittent le réservoir par l'appareil respiratoire, les voies gastro-intestinales ou le système tégumentaire (peau et muqueuses). La réduction des excrétions ou des sécrétions, ou le recouvrement des portes de sortie (p. ex. pansements sur les plaies, masques), brisent ce maillon de la chaîne de transmission de l'infection.
4. Voies de transmission
Les voies de transmission des agents infectieux (microorganismes) sont par convention classées en cinq catégories : transmission par contact, par gouttelettes, par voie aérienne, par véhicule commun ou par vecteur. On devrait noter qu'il n'est pas toujours possible de limiter avec précision la transmission des nombreuses variétés de microorganismes, ainsi que les infections qu'ils peuvent causer, à un nombre restreint de modes de transmission soigneusement maîtrisés. Ces catégories de transmission ne sont néanmoins avérées très utiles pour décrire la propagation des microorganismes dans les populations. Les voies de transmission varient selon le microorganisme en question. Certains microorganismes peuvent emprunter plus d'une voie de transmission (consulter la partie A, section II, C). L'utilisation appropriée de barrières et le respect des mesures d'hygiène des mains brise ce maillon de la chaîne de transmission de l'infection.
5. Portes d'entrée
Une porte d'entrée est la voie par laquelle un agent infectieux pénètre dans un hôte. Parmi les portes d'entrée, on compte, par exemple, les muqueuses des voies respiratoires, le tractus gastro-intestinal, le tractus urinaire, les lésions cutanées (p.ex. les plaies) et les dispositifs comme les lignes intraveineuses. Il est possible de briser ce maillon de la chaîne de l'infection en protégeant les portes d'entrée, soit en recouvrant les plaies, en portant un équipement de protection individuelle, en réduisant les ruptures des barrières mécaniques de la peau et des muqueuses, en utilisant du matériel stérilisé lorsque c'est nécessaire ou en pratiquant l’hygiène des mains pour que ces dernières ne transmettent pas des microorganismes à une porte d'entrée.
6. Hôte réceptif
Pour qu'une infection survienne, la personne doit être réceptive à l'égard de l'agent infectieux (microorganisme). La plupart des virus animaux n'infectent pas les humains, car ces derniers n'ont pas les récepteurs cellulaires appropriés; les personnes qui ont des anticorps en circulation contre les maladies qui peuvent être prévenues par vaccin ne sont pas infectées, car la réaction immunitaire empêche l'agent infectieux de se multiplier (consulter la partie A, section II, D). Il est possible de briser ce maillon de la chaîne de l'infection en maximisant les mécanismes de défense de l'hôte (p. ex. grâce à l'immunisation, à une nutrition optimale, à la réduction de la consommation de tabac et au contrôle du diabète).
B. Sources ou réservoirs d'agents infectieux (microorganismes)
Les sources ou réservoirs d'agents infectieux transmis dans les établissements de santé peuvent être d'origine humaine ou environnementale. Les portes de sortie varient selon le réservoir et l'agent infectieux.
1. Sources d'origine humaine
Les personnes sources peuvent être atteintes d'une maladie active, être asymptomatiques ou en période d'incubation de l'infection, ou encore être colonisées par des microorganismes de façon passagère ou pour une durée indéterminée, en particulier sur la peau et les muqueuses. Les réservoirs humains comprennent les patientsNote de bas de page 45, Note de bas de page 46, Note de bas de page 47, Note de bas de page 48, Note de bas de page 49, Note de bas de page 50, Note de bas de page 51, Note de bas de page 52, les TSNote de bas de page 53, Note de bas de page 54, Note de bas de page 55, Note de bas de page 56, Note de bas de page 57, Note de bas de page 58, Note de bas de page 59, Note de bas de page 60, Note de bas de page 61, Note de bas de page 62, Note de bas de page 63, les membres du ménage et les autres visiteursNote de bas de page 64, Note de bas de page 65, Note de bas de page 66, Note de bas de page 67, Note de bas de page 68.
La transmission des microorganismes dans les établissements de santé est renforcée par la présence de patients qui souillent visiblement l'environnement ou qui ne respectent pas des normes d'hygiène adéquates, y compris l'hygiène respiratoire; de patients qui ont une déficience cognitive; de patients qui ont des sécrétions ou des excrétions qui ne sont pas contenues; de patients dont l'exsudat est impossible à contenir avec un pansement; de patients atteints d'incontinence fécale si les selles ne peuvent être contenues à l'aide de produits pour l'incontinence ou de couches, et de patients atteints d'infections des voies respiratoires ou d'infections gastro-intestinalesNote de bas de page 48, Note de bas de page 69, Note de bas de page 70, en particulier les nouveau-nés.
2. Sources d'origine animale
Ce mode de transmission des IASS n'est ni fréquent, ni habituel dans la plupart des milieux de soins, bien que l'avènement de la zoothérapie dans les soins de courte durée et la présence d'animaux de compagnie à domicile et dans les établissements de SLD donnent lieu à quelques occasions d'infection zoonotiqueNote de bas de page 71, Note de bas de page 72. Des chercheurs ont récemment démontré que le SARM et C. difficile se transmettent aux chiens en visite, ce qui souligne l'importance de l'hygiène des mains avant et après le contact avec les animaux dans les milieux de soinsNote de bas de page 73, Note de bas de page 74.
3. Sources d'origine environnementale
Les facteurs environnementaux peuvent soit favoriser, soit entraver la transmission des microorganismes. L'environnement pourrait jouer un rôle plus important dans la survie et la croissance de certains microorganismes qu'on ne le croyait auparavant, ce qui vient confirmer l'importance de réduire au minimum la contamination de l'environnement par les sécrétions et les excrétions des patients, d'éviter les contacts inutiles des mains avec les surfaces de l'environnement et de s'assurer que des normes élevées en matière de nettoyage de l'environnement sont respectées.
Les virus respiratoiresNote de bas de page 75, Note de bas de page 76, Note de bas de page 77, le rotavirus, le norovirusNote de bas de page 78, Note de bas de page 79, Note de bas de page 80, Note de bas de page 81 et les spores de C. difficileNote de bas de page 82, Note de bas de page 83 survivent pendant des périodes prolongées dans l'environnement et qui pourrai être une source de transmission. Le rôle de l'environnement est de plus en plus reconnu comme une importante source de transmission des microorganismes résistants aux antibiotiques de patient à patientNote de bas de page 84, Note de bas de page 85.
L'environnement mobile (c.-à-d. le matériel et les articles communs à plusieurs patients), s'il n'est pas nettoyé entre chaque utilisation, peut augmenter le risque d'exposition à la flore microbienne des autres patients et être une source de transmission. La liste 1 comprend des exemples d'articles impliqués dans la transmission des infections ou qui sont des sources de contamination connues.
Liste 1 : Exemples de sources de contamination environnementales
- 1a. Articles de soins aux patients impliqués dans la transmission des infections
- Brassards de tensiomètre contaminés, transmission de C. difficileNote de bas de page 86 et de Klebsiella spp.Note de bas de page 87
- Thermomètres contaminés, transmission des ERV et de C. difficileNote de bas de page 42, Note de bas de page 88, Note de bas de page 89, Note de bas de page 90
- Appareils d'aérosol ultrasonores, transmission de SARMNote de bas de page 91
- Appareils réutilisables de prélèvement d'échantillons de sang capillaire au bout du doigt, transmission de l'hépatite BNote de bas de page 92
- Surfaces environnementales à côté des lits de bébé, comme les comptoirs, les chevets de berceaux, les sucettes, les jouets, transmission du virus respiratoire syncytialNote de bas de page 77
- Jouets, transmission de Pseudomonas aeruginosa multirésistantNote de bas de page 93
- 1b. Articles de soins aux patients contaminés, mais pas clairement impliqués dans la transmission des infections
- Sonnettes d'appel contaminées par les ERVNote de bas de page 94
- Tables de chevet, côtés de lit et meubles contaminés par les ERVNote de bas de page 94, Note de bas de page 95, Note de bas de page 96 et SARMNote de bas de page 70
- Garrots, dispositifs de surveillance, otoscopes, stéthoscopesNote de bas de page 97, Note de bas de page 98, Note de bas de page 99, Note de bas de page 100, Note de bas de page 101, Note de bas de page 102, Note de bas de page 103, Note de bas de page 104
- OrdinateursNote de bas de page 105, Note de bas de page 106, Note de bas de page 107, Note de bas de page 108, claviers d'ordinateur, robinetsNote de bas de page 109
- JouetsNote de bas de page 110, Note de bas de page 111, Note de bas de page 112
- Mobilier, matelas, rideaux, lingeNote de bas de page 113, Note de bas de page 114, Note de bas de page 115, Note de bas de page 116, Note de bas de page 117, Note de bas de page 118
- Habillement, cravatesNote de bas de page 119, Note de bas de page 120, dossiers médicauxNote de bas de page 121
C. Exposition aux agents infectieux et voies de transmission
1. Exposition aux agents infectieux (microorganismes)
Il y a exposition lorsqu'un hôte réceptif entre en contact avec une source infectée ou un environnement contaminé (p. ex. des objets animés ou inanimés, ou des particules dans l'air). Toutes les expositions n'entraînent pas une transmission et une infection. La probabilité de la transmission et de l'infection est fonction de plusieurs facteurs, comme la réceptivité de l'hôte, la présence de récepteurs hôtes du microorganisme, la taille de l'inoculum du microorganisme, sa viabilité et sa virulence, ainsi que l'efficacité de la hiérarchie des mesures de contrôle (consulter la partie A, section III, A) utilisées par une organisation et des protections individuelles portées par un TS.
La figure 2 illustre le continuum de l'exposition aux agents infectieux propre à la transmission par contact, par gouttelettes ou par voie aérienne à laquelle pourrait être soumis un hôte réceptif lorsqu'il entre en contact avec une source infectée ou un environnement contaminé (contact physique ou passif, en personne ou étroit [à une distance de 2 mètres d'une source infectée qui tousse]) et lorsqu'il inhale un microorganisme (sous forme d'aérosol ou de gouttelettes). La recherche a permis de démontrerNote de bas de page 122, Note de bas de page 123, Note de bas de page 124 que des gouttelettes et des particules en suspension peuvent se trouver dans l'air à proximité (jusqu'à 2 mètres) d'une source qui tousse ou éternue. En outre, une partie des grosses particules (gouttelettes) peut se dessécher (et diminuer de taille) pendant qu'elle est en suspension et devenir de fait des noyaux de gouttelettes. Les particules d'un diamètre de 1 µm à 10 µm peuvent pénétrer jusque dans les canaux alvéolaires (c'est-à-dire au-delà des cordes vocales), mais peuvent également être déposées dans les voies respiratoires, comme il est indiqué dans la figure 3.
Figure 2. Exposition aux particules
Élaboré par le groupe de travail sur le Plan canadien de lutte contre la pandémie d'influenza-Annexe F, 2008
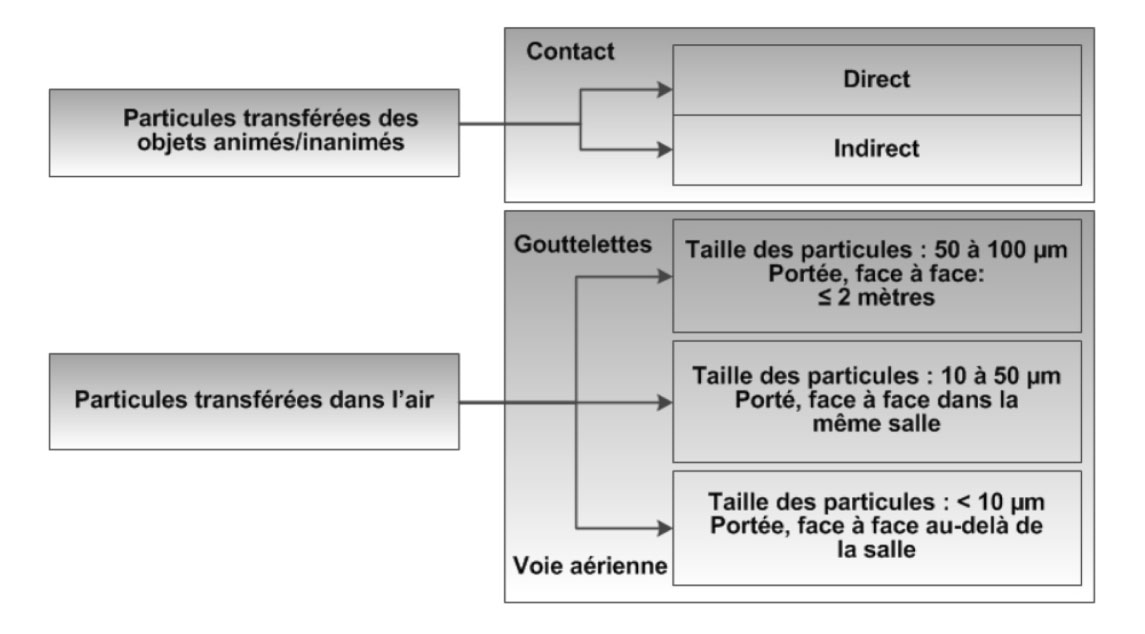
Description textuelle
La figure 2 illustre le continuum de l'exposition aux agents infectieux propre à la transmission par contact, par gouttelettes ou par voie aérienne à laquelle pourrait être soumis un hôte réceptif lorsqu'il entre en contact avec une source infectée ou un environnement contaminé (contact physique ou passif, en personne ou étroit [à une distance de 2 mètres d'une source infectée qui tousse]) et lorsqu'il inhale un microorganisme (sous forme d'aérosol ou de gouttelettes). La recherche a permis de démontrerNote de bas de page 122, Note de bas de page 123, Note de bas de page 124 que des gouttelettes et des particules en suspension peuvent se trouver dans l'air à proximité (jusqu'à 2 mètres) d'une source qui tousse ou éternue. En outre, une partie des grosses particules (gouttelettes) peut se dessécher (et diminuer de taille) pendant qu'elle est en suspension et devenir de fait des noyaux de gouttelettes.
Figure 3. Régions où se déposent les particules de tailles diverses dans les voies respiratoiresNote de bas de page 125
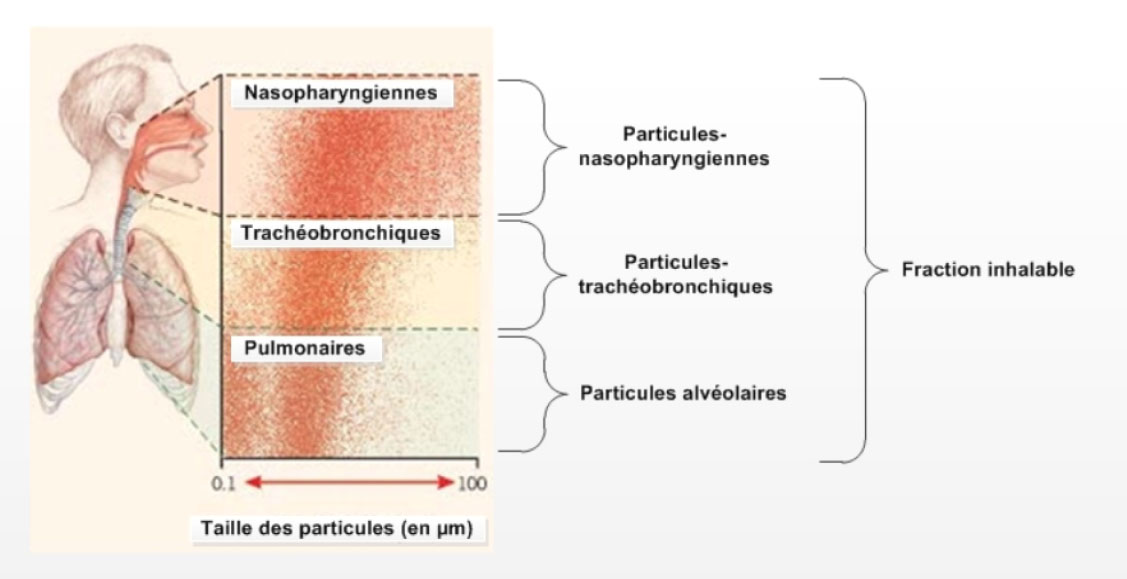
Description textuelle
La figure 3 illustre les particules d'un diamètre de 1 µm à 10 µm pouvant pénétrer jusque dans les canaux alvéolaires (c'est-à-dire au-delà des cordes vocales), mais pouvant également être déposées dans les voies respiratoires.
a. Continuum de l'exposition par gouttelettes et par voie aérienne
La probabilité d'une exposition à un aérosol infectieux par voie aérienne est influencée par plusieurs facteurs, outre la proximité de la source infectée avec l'hôte. Ces facteurs comprennent la taille des particules qui contiennent l'agent infectieux, la viabilité de ce dernier et l'environnement animé et inanimé d'une chambre (p. ex. la concentration des particules virales dans un noyau de gouttelette, la concentration de l'aérosol dans la chambre, l'humidité relative, la direction de la circulation de l'air et le nombre de renouvellements d'air par heure dans la chambre [RAH]).
Des particules de plusieurs tailles différentes sont évacuées des voies respiratoires humaines pendant qu'une personne tousse, éternue ou parle, ou au cours des interventions médicales. La taille de ces particules et la distance à laquelle elles seront projetées dépend de la force générée par la personne ou l'intervention. Les grosses particules (d'un diamètre supérieur à 10 µm) tombent rapidement (en quelques secondes) sur le solNote de bas de page 125. Cependant, les petites particules peuvent rester en suspension pendant une période bien plus longue, de l'ordre des dixièmes de secondes pour une gouttelette de 10 µm de diamètre et de l'ordre des minutes ou des heures pour les petits noyaux de gouttelettes. Les particules qui restent dans l'air pendant plusieurs minutes ou plusieurs heures (d'un diamètre inférieur à 10 µm) peuvent être transportées par des courants d'air sur une distance mesurable et peuvent sortir de la chambre; on considère qu'elles représentent une exposition par voie aérienne.
2. Voies de transmission
Selon la terminologie de la PCI, les voies de transmission des microorganismes sont classées par convention en cinq catégories : transmission par contact, par gouttelettes, par voie aérienne, par véhicule commun et par vecteur. Les voies de transmission varient en fonction des microorganismes. Pour la plupart des microorganismes, la transmission passe principalement par une seule voie, comme le contact direct ou indirect (p. ex. le rotavirus ou C. difficile), les gouttelettes (p. ex. la coqueluche) ou la voie aérienne (p. ex. Mycobacterium tuberculosis). Cependant, certains agents infectieux peuvent être transmis par plus d'une voie (p. ex. le virus respiratoire syncytial peut être transmis par gouttelettes ou par contact).
a. Exposition et transmission par contact
Il y a exposition par contact lorsque des microorganismes sont transférés par contact physique entre une source infectée et un hôte ou par l'intermédiaire d'un objet inanimé, qui transfère les microorganismes à un hôte de façon passiveNote de bas de page 24. Les mains peuvent être contaminées par contact avec une source infectée ou avec des surfaces ou objets inanimés contaminés dans l'environnement immédiat d'une source infectéeNote de bas de page 77, Note de bas de page 126, Note de bas de page 127, Note de bas de page 128.
L'exposition par contact comprend le contact direct et le contact indirect :

Figure 4. Contact direct, où la peau de deux personnes entre en contact
- Il y a exposition par contact direct lorsqu'un contact physique direct (surface corporelle contre surface corporelle, sans protections) entre un sujet infecté ou colonisé et un hôte, comme une poignée de main (illustré à la figure 4), se solde par le transfert de microorganismes.
- Une exposition par contact indirect comprend le transfert passif de microorganismes d'un hôte qui entre en contact avec un objet qui sert d'intermédiaire, comme des mains contaminées qui ne sont pas lavées entre les épisodes de soins aux patientsNote de bas de page 129, Note de bas de page 130, le matériel de soins aux patients contaminé (p. ex. les chaises hygiéniques, les fauteuils roulants, la base des thermomètres électroniques, les brassards de tensiomètre, le matériel de surveillance)Note de bas de page 90, Note de bas de page 92, Note de bas de page 131, Note de bas de page 132, les surfaces comme les côtés de litNote de bas de page 77 qui ne sont pas bien nettoyées et désinfectées d'un patient à l'autre ou les dispositifs qui présentent un défaut de fabrication qui prévient leur retraitement approprié. Parmi les autres objets inanimés qui se trouvent dans l'environnement du patient et pourraient être impliqués, on compte les ordinateursNote de bas de page 105, Note de bas de page 106, Note de bas de page 107, Note de bas de page 108, Note de bas de page 109, les jouetsNote de bas de page 93, Note de bas de page 110 et les dispositifs de loisir électroniques qui ne sont pas nettoyés ou désinfectés entre chaque patient, comme l'indique la figure 5.

Figure 5. Contact indirect, où il y a contact avec un objet inanimé qui peut servir de véhicule à la transmission de pathogènes
Il y a transmission par contact lorsqu'une exposition par contact se solde par la colonisation ou l'infection d'un hôte réceptif par une dose infectieuse d'un microorganisme provenant d'une source infectée ou contaminée.
Les microorganismes transmis par contact comprennent de nombreux agents importants pour les milieux de soins sur le plan épidémiologique, comme C. difficile, les microorganismes résistants aux antibiotiques (p. ex. SARM, les ERV) et les virus qui causent la gastroentérite (consulter l'annexe VI). D'autres agents infectieux, en particulier les virus respiratoires (p. ex. le virus respiratoire syncytial, le virus de la grippe, le para-influenza et le rhinovirus) qui sont évacués en grosses gouttelettes, restent viables sous forme de gouttelettes qui se déposent sur des objets dans l'environnement immédiat du patient et qui survivent assez longtemps sur les surfaces pour être ramassées par les mains des patients ou des TSNote de bas de page 75, Note de bas de page 76, Note de bas de page 124, Note de bas de page 133.
Prière de consulter la liste 3 et le tableau 5, qui comprennent une liste des microorganismes transmis par contact. La prévention et le contrôle des agents infectieux transmis par contact comprennent l'observation des pratiques de base et des précautions contre la transmission par contact.
b. Exposition et transmission par gouttelettes

Figure 6. Transmission par gouttelettes, où de grosses particules respirables se déplacent sur une distance pouvant atteindre 2 mètres
Il y a exposition par gouttelettes lorsque des gouttelettes contenant des microorganismes sont propulsées dans l'air sur une courte distance (c.-à-d. jusqu'à 2 mètres)Note de bas de page 122, Note de bas de page 123, Note de bas de page 124 et se déposent sur les muqueuses d'un hôte. Les gouttelettes peuvent également contaminer l'environnement immédiat lorsqu'elles se déposent sur des surfaces; elles peuvent alors contribuer à la transmission par contact, tel qu'il est indiqué à la figure 6.
Les gouttelettes sont générées naturellement par une source infectée, principalement lorsque la personne tousse, éternue ou parleNote de bas de page 134, ou artificiellement par des IMGA. Les interventions médicales générant des aérosols peuvent également produire des gouttelettes infectieuses plus petites qui se déplacent sur de plus grandes distances que celles qui sont naturellement générées par les patients (consulter la partie A, section II, C, 2c, qui contient une analyse plus détaillée des IMGA). La toux et les éternuements de certaines personnes (p. ex. les jeunes enfants ou les personnes âgées frêles) peuvent ne pas être assez puissants pour propulser des gouttelettes à une distance de 2 mètresNote de bas de page 135.
Des gouttelettes de divers diamètres (consulter la figure 2) peuvent contaminer l'environnement immédiat lorsqu'elles se déposent sur les surfaces. Certains microorganismes peuvent rester viables pendant des périodes prolongées et contribuer à la transmission par contact (p. ex. certains virus respiratoires)Note de bas de page 136. Les grosses particules d'aérosol (d'un diamètre supérieur à 10 µm) retombent sur les surfaces en quelques secondes. L'exposition par gouttelettes ne peut se produire que si la source et l'hôte sont très proches (à moins de 2 mètres). Certains microorganismes évacués sous forme de grosses gouttelettes sont très fragiles et ne survivent pas à l'extérieur d'un hôte humain ou sur les surfaces (p. ex. Bordetella pertussis, le méningocoque).
Il y a transmission par gouttelettes lorsque des gouttelettes qui contiennent une dose infectieuse de particules viables sont projetées dans l'air sur une courte distance (c.-à-d. sur moins de 2 mètres) et déposées sur les muqueuses des yeux, du nez ou de la bouche d'un hôte réceptif,et lorsque ces gouttelettes parviennent à vaincre les autres mécanismes de défense de l'hôte.
Les microorganismes transmis par gouttelettes comprennent les virus qui causent des infections des voies respiratoires (p. ex. le virus respiratoire syncytial, la grippe, le virus para-influenza, le rhinovirus, l'adénovirus), la rubéole, les oreillons et Bordetella pertussis.
Prière de consulter la liste 4 et le tableau 5, qui comprennent une liste des agents infectieux transmis par gouttelettes. La prévention et le contrôle des infections transmises par gouttelettes comprennent l'immunisation pour les maladies que l'on peut prévenir par vaccin et l'observation des pratiques de base et des précautions contre la transmission par gouttelettes.
c. Exposition et transmission par voie aérienne
Figure 7. Transmission par voie aérienne, où de petites particules se déplacent sur de longues distances
Il y a exposition par voie aérienne si de petites particules (c.-à-d. des aérosols qui contiennent des noyaux de gouttelettes) contenant des microorganismes viables sont générées, projetées sur de courtes ou de longues distances et inhalées. Les aérosols qui contiennent des microorganismes viables sont générés naturellement par une source infectée, principalement lorsque la personne tousse, éternue ou parle, ou artificiellement par des IMGA. Une exposition par voie aérienne peut survenir à la suite immédiate de la génération des particules (c.-à-d. la projection directe d'un aérosol contenant des quantités viables de microorganismes dans l'air, directement interceptés par l'appareil respiratoire d'un hôte réceptif) ou après un certain temps. Les noyaux de gouttelettes peuvent rester en suspension dans l'air pendant très longtemps avant de se déposer, ce qui fait qu'un hôte réceptif peut inhaler l'aérosol pendant toute la durée de sa suspension, comme il est indiqué dans la figure 7.
Une transmission par voie aérienne peut survenir lorsque des microorganismes viables contenus dans un aérosol de sécrétions provenant d'une source infectée sont projetés dans l'air sur une courte distance (c.-à-d. à moins de 2 mètres) ou sur une longue distance (c.-à-d. à plus de 2 mètres) et sontNote de bas de page 122, Note de bas de page 123, Note de bas de page 124 inhalés, entrent en contact avec les récepteurs des voies respiratoires d'un hôte réceptif, parviennent à vaincre les mécanismes de défense de l'hôte et provoquent une maladie. Pour qu'il y ait transmission de l'infection, les microorganismes contenus dans les particules doivent pouvoir rester viables dans l'air pendant une période prolongée et l'hôte réceptif doit être exposé à une concentration suffisante (dose infectieuse) de ces microorganismes viables. Une infection ne peut survenir que si les récepteurs appropriés des agents infectieux sont présents au site d'exposition. La figure 3 illustre les diverses régions des voies respiratoires, la classification des particules selon la taille et les régions correspondantes où elles se déposentNote de bas de page 125.
Le virus de la varicelle et du zonaNote de bas de page 137, Mycobacterium tuberculosisNote de bas de page 138, Note de bas de page 139, Note de bas de page 140, le virus de la rougeoleNote de bas de page 141, Note de bas de page 142, le virus de la variole et l'orthopoxvirose simienne Note de bas de page 143, Note de bas de page 144 sont des agents infectieux transmis par voie aérienne. On a signalé que la transmission du virus de la rougeole peut se produire jusqu'à 90 minutes suivant le départ du proposant de la chambreNote de bas de page 141, Note de bas de page 145.
Prière de consulter la liste 5 et le tableau 5, qui comprennent une liste des microorganismes transmis par voie aérienne. La prévention et le contrôle des infections transmises par voie aérienne comprennent l'immunisation contre les virus que l'on peut éviter par vaccin et l'observation des pratiques de base et des précautions contre la transmission par voie aérienne, telles que décrites à la partie B, section IV, sous-section iii. Selon les précautions particulières contre la transmission par voie aérienne, seuls les TS immunisés peuvent soigner des patients atteints de varicelle ou de rougeole, et la circulation de l'air doit être contrôlée. Le contrôle de la circulation de l'air permet de s'assurer que les systèmes de ventilation fournissent des taux de renouvellement de l'air adéquats et des différences de pression appropriées pour maintenir la direction de l'écoulementNote de bas de page 146, Note de bas de page 147 dans une chambre d'isolement pour infections à transmission aérienne.
Des renseignements concernant la durée requise pour éliminer les particules aériennes d'une chambre sans source génératrice d'aérosols en permanence sont fournis à l'annexe VIII. Il faut attendre qu'un certain temps se soit écoulé avant qu'un nouveau patient ou un membre du personnel soignant puisse entrer dans une chambre sans appareil de protection respiratoire.
Interventions médicales générant des aérosols
Les interventions médicales générant des aérosols peuvent produire des aérosols en raison de la manipulation artificielle des voies respiratoires. Plusieurs types d'IMGA ont été associés à une augmentation du risque de transmission de la tuberculose ou du SRASNote de bas de page 148. On devrait reconnaître que, même s'il y a consensus au sujet de la propagation des infections par ces interventions, qui est corroborée par quelques éléments probants, des recherches plus poussées sont nécessaires pour obtenir des preuves plus solides concernant les dangers que présentent ces interventions. Le risque de transmission d'une infection peut augmenter pendant une IMGA, car cette dernière peut générer un volume élevé d'aérosols respirables qui peuvent être projetés sur une plus longue distance que celle des modèles de dispersion naturelleNote de bas de page 122, Note de bas de page 149. Ces interventions sont, notamment:
- l'intubation et les interventions connexes (p. ex. la ventilation manuelle, l'aspiration endotrachéale ouverte)Note de bas de page 150, Note de bas de page 151, Note de bas de page 152;
- la réanimation cardio-respiratoireNote de bas de page 152;
- la bronchoscopieNote de bas de page 153;
- l'induction de l'expectorationNote de bas de page 154;
- la thérapie avec aérosol par nébulisationNote de bas de page 155, Note de bas de page 156;
- la ventilation non invasive en pression positive (pression positive expiratoire continue ou à deux niveaux)Note de bas de page 157.
On se demande si d'autres types d'IMGA pourraient entraîner la génération d'aérosols pouvant causer une transmission. Cependant, aucun article publié ne documente la transmission des infections respiratoires, y compris la tuberculose, SRAS et la grippe, par les moyens suivantsNote de bas de page 136, Note de bas de page 158, Note de bas de page 159, Note de bas de page 160:
- la ventilation par oscillation à haute fréquence
- les soins liés à la trachéostomie
- la kinésithérapie de drainage
- l’écouvillonnage du nasopharynx et les aspirats rhinopharyngés.
Avant d'effectuer une IMGA, on devrait évaluer les patients avec soin pour détecter tout signe ou tout symptôme de tuberculose, de SRAS ou d'infection respiratoire par un pathogène en émergence dont on ne connaît pas complètement la voie de transmissionNote de bas de page 150, Note de bas de page 151, Note de bas de page 152, Note de bas de page 153, Note de bas de page 154, Note de bas de page 155, Note de bas de page 156, que ces maladies soient connues ou présumées, et de mettre en œuvre des stratégies de réduction de la génération d'aérosols (consulter la partie B, section IV, sous-section iii, 1b). On devrait également mettre en œuvre des stratégies de réduction de la production d'aérosols lorsque des IMGA doivent être effectuées sur des patients atteints de fièvre hémorragique viraleNote de bas de page 161. En ce qui concerne les nouveaux virus de la grippe ou l'émergence de nouveaux pathogènes, il faut consulter le site Web de l'ASPC, qui comprend des documents d'orientation précis (http://www.phac-aspc.gc.ca/nois-sinp/guide/pubs-fra.php). On devrait respecter les pratiques de base et prendre des précautions contre la transmission par contact ou par gouttelettes, tel qu'il est indiqué, pour la réalisation des IMGA sur des patients qui ne manifestent aucun signe ou symptôme de tuberculose, de SRAS ou d'infection respiratoire émergente connus ou présumés. Les autres interventions qui peuvent générer des aérosols et dont on a établi qu'elles transmettent la tuberculose comprennent les interventions (p. ex. l'irrigation) qui peuvent transformer les bacilles de la tuberculose viables provenant de lésions non respiratoires en aérosolsNote de bas de page 162, Note de bas de page 163, Note de bas de page 164 et l'utilisation de scies alternatives durant l'autopsie de patients atteints de tuberculoseNote de bas de page 165, Note de bas de page 166. Il est recommandé de prendre des précautions contre la transmission par voie aérienne lorsque l'on effectue ces interventions sur des patients atteints de tuberculose présumée ou confirmée.
d. Transmission par véhicule commun
Figure 8. Exemple de transmission par véhicule commun : un flacon à doses multiples contaminé
Dans les cas de transmission par un véhicule commun, une unique source contaminée, comme un aliment, un flacon à doses multiplesNote de bas de page 167, Note de bas de page 168, Note de bas de page 169, Note de bas de page 170, Note de bas de page 171, Note de bas de page 172, Note de bas de page 173, un soluté intraveineuxNote de bas de page 174 ou du matériel transmet l'infection à de nombreux hôtes. Le contrôle est effectué en respectant des normes appropriées pour la préparation des aliments et des médicaments et pour la décontamination du matériel, tel qu'il est indiqué à la figure 8.
e. Transmission par vecteur

Figure 9. Les maladies transmises par des insectes sont un exemple de transmission par vecteur
Ce mode de transmission désigne la transmission par des insectes vecteurs. On peut la prévenir en respectant des normes adéquates pour la construction et l'entretien des hôpitaux, en tenant les fenêtres fermées ou couvertes de moustiquaires et en assurant un entretien ménager adéquat des lieuxNote de bas de page 175. Ce mode de transmission n'a pratiquement jamais été signalé dans les hôpitaux canadiens. Consulter la figure 9.
D. Facteurs de l'hôte
Pour qu'une transmission survienne, les microorganismes doivent avoir accès à un hôte réceptif par une porte d'entrée vulnérable. Le risque de transmission dépend de la réceptivité de l'hôte. Il se peut que les mécanismes de défense de l'hôte, s'ils sont normaux, puissent éliminer quelques microorganismes; cependant, si ces derniers sont nombreux, les mécanismes de défense seront dépassés. Un hôte immunovulnérable pourrait ne pas être capable d'éliminer même quelques microorganismes. Les mécanismes de défense de l'hôte, aussi bien non spécifiques (p. ex. flore normale, peau intacte, neutrophiles et macrophages) que spécifiques (anticorps, réactions immunitaires à médiation cellulaire), peuvent être altérés par l'âge, une maladie sous-jacente (p. ex. le diabèteNote de bas de page 176, Note de bas de page 177, le VIHNote de bas de page 178, une tumeur maligne ou une greffeNote de bas de page 179), les facteurs génétiques ou les médicaments. Les autres facteurs qui peuvent faciliter l'acquisition de microorganismes sont les interventions invasives ou chirurgicales, la radiothérapie, les lésions cutanées et la rupture des barrières normales, comme c'est le cas en présence d'appareils médicaux invasifs (p. ex. les tubes endotrachéaux, les sondes urétrales à demeure et les dispositifs intravasculaires)Note de bas de page 180, Note de bas de page 181, Note de bas de page 182, et le traitement des plaies.
E. Résultats de la transmission d'agents infectieux (microorganismes)
L'apparition d'une colonisation, d'une infection asymptomatique ou d'une maladie clinique (infection symptomatique) à la suite d'une transmission est fonction de la pathogénicité et de la virulence de l'agent infectieux (microorganisme), de la taille de l'inoculum et de l'intégrité des mécanismes de défense de l'hôte (consulter la partie A, section II, D). Par pathogénicité, on entend la capacité du microorganisme à causer une maladie (c.-à-d. à nuire à l'hôte). Certains microorganismes sont pathogènes en soi, c'est-à-dire capables de provoquer une maladie chez n'importe quel hôte réceptif (p. ex. le virus de la varicelle), alors que d'autres sont opportunistes et n'entraînent une infection que dans des circonstances particulières (p. ex. les staphylocoques à coagulase négative chez les personnes qui ont des prothèses). La virulence renvoie à l'intensité de la pathogénicité et est liée à la capacité à entraîner une morbidité et une mortalité (p. ex. la virulence du virus Ebola est élevée; celle du rhinovirus est faible). Plusieurs facteurs influent sur la virulence d'un microorganisme : production de toxines, pouvoir envahissant, présence d'une capsule, mécanismes d'adhérence et capacité de survivre à l'intérieur des cellules hôtes. La taille de l'inoculum renvoie au nombre de microorganismes transmis à l'hôte. La pathogénicité de certains microorganismes est très élevée et un inoculum de petite taille est suffisant pour causer une maladie (p. ex. Shigella).
1. Colonisation
On appelle colonisation la présence de microorganismes en croissance ou multiplication dans un hôte ou sur un hôte, mais sans invasion des tissus ou lésion cellulaire. La plupart des microbes sont beaucoup plus souvent à l'origine d'une colonisation que d'une maladie clinique. La colonisation du nasopharynx par des bacilles aérobies Gram négatif est favorisée par la gravité de la maladie, la malnutrition, une chirurgie importante, l'alcoolisme et le diabèteNote de bas de page 183. La colonisation par Staphylococcus aureus est fréquente chez les personnes normales en bonne santé. Certaines populations de patients sont fortement colonisées par S. aureus (p. ex. les patients dialysés, les utilisateurs de drogues injectables et les patients atteints de diabète sucré ou d'affections cutanées)Note de bas de page 184.
Les perturbations de la flore intestinale normale engendrées par les antibiotiques favorisent la croissance excessive d'entérocoques et de bacilles aérobies Gram négatif endogènes et accroissent le risque de colonisation par des microorganismes exogènes, notamment les levures et les bactéries résistantes aux antibiotiquesNote de bas de page 40, Note de bas de page 183. La présence d'une flore intestinale normale ou endogène est un mécanisme de défense contre la colonisation du tractus gastro-intestinal par des microorganismes exogènes. La flore endogène (p. ex. les bactéries qui résident dans les voies respiratoires ou dans le tractus gastro-intestinal) peut également causer des IASSNote de bas de page 185, Note de bas de page 186, Note de bas de page 187, Note de bas de page 188, Note de bas de page 189, Note de bas de page 190, Note de bas de page 191, Note de bas de page 192, Note de bas de page 193. Une fois les microorganismes résistants aux antibiotiques acquis, leur portage pourrait être la norme dans certaines populations de patients. La colonisation par des souches résistantes de Pseudomonas aeruginosa ou de Burkholderia cepacia est fréquente chez les personnes atteintes de fibrose kystique. Une colonisation persistante par des ERV a été mise en évidence chez les patients dialysésNote de bas de page 194 et dans d'autresNote de bas de page 195, Note de bas de page 196 populations.
2. Infection infraclinique ou asymptomatique
Une infection peut être associée ou non à une maladie clinique. L'infection peut causer des changements cellulaires et tissulaires qui peuvent être détectables en l'absence de signes ou de symptômes manifestes. Il s'agit d'une infection infraclinique ou asymptomatique.
3. Maladie clinique ou infection symptomatique
Lorsque les changements cellulaires et tissulaires sont suffisants pour produire des signes et des symptômes manifestes, la personne est atteinte d'une maladie clinique dont l'intensité peut aller de faible à forte, selon le microorganisme et l'état de santé de l'hôte.
III. Mesures de contrôle visant à réduire l'exposition des travailleurs de la santé aux microorganismes et la transmission de ces derniers
A. Hiérarchie des mesures de contrôle visant à réduire l'exposition aux agents infectieux et la transmission de ces derniers
La collaboration entre les professionnels de la PCI et de la santé au travail et les ingénieurs chargés de la construction des établissements de santé a permis de mieux comprendre et appliquer un cadre de mesures et d'interventions à deux vitesses, qui permet aux organisations de soins de santé d'évaluer le risque d'exposition des TS (y compris les bénévoles) aux microorganismes et aux autres dangers dans le milieu de travail, ainsi que l'efficacité de leurs propres mesures d'atténuation.
L'approche idéale pour contenir un danger consiste à mettre en œuvre une hiérarchie de mesures de contrôle. Les interventions techniques représentent le premier niveau de contrôle. Si ce niveau de contrôle n'est pas possible ou adéquat, on passe aux interventions administratives. L’EPI arrive en dernier dans la hiérarchie des mesures de contrôle. Les équipements de protection individuelle ne sont pas les premières mesures à prendre, car leur utilisation varie selon la conformité du travailleur de la santé à leur usage. En comprenant les mesures de contrôle techniques, administratives (qui comprennent les pratiques de soins aux patients) et l'EPI, les organisations de soins de santé peuvent déterminer comment l'environnement de chaque milieu de soins (p. ex. l'infrastructure, le matériel, les processus et les pratiques) augmente ou diminue la probabilité qu'un hôte réceptif (p. ex. un patient, un TS, un visiteur) soit exposé à un microorganisme ou à un réservoir dans le milieu de soins en question.
1. Mesures de contrôle techniques
Au niveau des mesures de contrôle techniques, on réduit le risque d'exposition à un agent infectieux ou à une source infectée en appliquant des méthodes d'isolement ou de ventilation. Les mesures de contrôle techniques ne dépendent pas de la conformité avec les stratégies de prévention de l'exposition. Ces mesures de contrôle sont généralement établies et gérées dans la structure de l'immeuble, ce qui élimine le choix de les appliquer ou non et réduit la possibilité d'erreurs individuelles. À ce titre, elles offrent une protection plus efficace.
2. Mesures de contrôle administratives
Le niveau des mesures de contrôle administratives fournit une infrastructure de politiques, procédures et pratiques de soins aux patients destinées à prévenir l'exposition d'un hôte réceptif à un agent infectieux ou sa transmission durant la prestation des soins de santé. Pour que ces mesures réussissent à prévenir la transmission de microorganismes ou à détecter les cas d'infection, elles doivent être mises en œuvre dès la première rencontre avec la source infectée et maintenues jusqu'à ce que cette source ait quitté le milieu de soins ou ne soit plus contagieuse. Pour que des mesures administratives puissent prévenir la transmission des infections, l'organisation de soins de santé doit s'engager à fournir les ressources nécessaires pour les mettre en œuvre.
3. Équipement de protection individuelle
Bien que l'utilisation des mesures liées à l'équipement de protection individuelle soit la plus visible dans la hiérarchie des mesures de contrôle, elles constituent le niveau le plus faible et ne devraient pas faire office de programme de prévention primaire isolé. Le niveau de l'EPI se réfère à la disponibilité et à l'usage approprié de protections que peut porter un hôte réceptif pour introduire une barrière physique entre lui et un agent infectieux ou une source infectée. Ces protections comprennent les gants, les blouses, la protection du visage, la protection des yeux (dont les écrans faciaux ou les masques dotés de visières) et les appareils de protection respiratoire. L'organisation de soins de santé joue un rôle déterminant pour veiller à ce que les EPI appropriés soient mis à la disposition des patients, des TS, des visiteurs, des entrepreneurs, etc., afin d'éviter l'exposition à un agent infectieux ou à une source infectée.
Si l'institution de santé met l'accent sur la disponibilité et l'utilisation de divers EPI à l'exclusion des autres niveaux de la hiérarchie des mesures de contrôle, toutes les personnes qui évoluent dans le milieu de soins, y compris les patients, les TS et les autres membres du personnel, bénéficieront d'une protection non optimale. Parmi les mesures de contrôle, l'utilisation efficace et appropriée de l'EPI est celle qui dépend le plus de la conformité et de la compétence de l'utilisateur; par conséquent, cette mesure de contrôle est la plus facilement compromise (ce qui entraîne une protection inefficace contre un agent infectieux ou une source infectée). L'utilisation d'un EPI est la dernière mesure de protection de la hiérarchie des mesures de contrôle visant à réduire au minimum l'exposition et la transmission subséquente (consulter l'annexe X).
Liste 2 : Exemples de mesures de prévention selon la hiérarchie des mesures de contrôle
- 2a. Niveau 1 : exemples de mesures techniques
- Contrôle à la source :
- chambre individuelle avec toilettes privées, lavabo à l'usage du patient et lavabos réservés au lavage des mains à l'usage du personnel de soins;
- chambres d'isolement pour infections à transmission aérienne;
- signalisation qui dirige les patients symptomatiques atteints d'une infection respiratoire vers des entrées séparées (pendant les éclosions dans les collectivités);
- barrières physiques (p. ex. cloisons dans les zones de triage pour éviter l'exposition aux patients symptomatiques atteints d'une infection respiratoire);
- séparation spatiale appropriée (dans les chambres de patient, les salles d'attente et à domicile);
- ventilation appropriée et ventilation naturelle à domicile, s'il y a lieu.
- Installation :
- de DMBA au point de service;
- de récipients pour objets pointus et tranchants au point d'utilisation;
- de distributeurs accessibles et en bon état de marche pour les produits d'hygiène des mains (DMBA, savon, lotion, essuie-tout) et les produits d'hygiène ou d'étiquette respiratoire;
- de lavabos réservés au lavage des mains à l'usage des TS.
- Nombre approprié de chaises hygiéniques
- Équipement de protection individuelle en quantité suffisante et accessible
- Nombre approprié de poubelles automatiques accessibles pour l'élimination des essuie-tout, des mouchoirs en papier, des masques, des gants, etc.
- 2b. Niveau 2 : exemples de mesures administratives
- Ressources appropriées pour le diagnostic et le traitement des infections ou des colonisations et pour l'immunisation des patients et des membres du personnel
- Soutien de l'organisation à des services de PCI et de santé au travail efficaces et à la gestion des éclosions
- Politiques appropriées en matière de santé au travail et de sécurité, y compris l'évaluation préalable au placement, les restrictions professionnelles, le programme de protection respiratoire, la manipulation sécuritaire des objets pointus et tranchants, la prévention de l'exposition aux pathogènes à diffusion hématogène et les programmes d'immunisation
- Éducation des travailleurs de la santé
- Politiques, procédures et ressources à l'appui de l'application :
- de l'évaluation du risque au point de service;
- de DMBA au point de service comme norme de soins dans tous les milieux;
- des pratiques de base comme norme de soins pour tous les patients dans tous les milieux;
- contrôle à la source (instructions pour les patients)
- Placement, hébergement et déplacements des patients
- 2c. Niveau 3 : exemples d'équipements de protection individuelle visant à prévenir l'exposition des patients, des travailleurs de la santé et des autres membres du personnel
- À la suite d'une ERPS, l'EPI à porter pour appliquer les pratiques de base et les précautions additionnelles de façon appropriée peut comprendre :
- des gants;
- des blouses;
- des masques (chirurgicaux ou opératoires utilisés par les travailleurs de la santé ou les sources infectées);
- une protection du visage (masques et protection des yeux, écrans faciaux ou masques dotés de visières);
- des appareils de protection respiratoire (consulter l’annexe V, glossaire)
B. Rôle que joue l'organisation dans la réduction de l'exposition aux agents infectieux et de la transmission de ces derniers
1. Évaluation du risque organisationnel
Toute organisation de soins de santé a l'importante responsabilité d'évaluer les composantes de la hiérarchie des mesures de contrôle (c.-à-d. d'effectuer une ERO) afin de réduire au minimum le risque d'exposition aux microorganismes et de transmission de ces derniers dans les milieux de soins. Cette ERO est au centre de la préparation et de la planification de toute organisation de soins de santé concernant la protection de toutes les personnes (p. ex. les patients, les TS, les visiteurs, les entrepreneurs) contre les IASS dans tous les milieux de soins. Les organisations sont tenues d'informer et de former les TS au sujet de l'ERO de l'organisation et de ses conséquences sur leurs pratiques. Par exemple, la disponibilité des chambres d'isolement pour infections à transmission aérienne opérationnelles peut avoir une incidence sur le moment et l'endroit où les IMGA sont exécutées et pourrait influencer l'ERPS effectuée par les TS.
On devrait effectuer une ERO chaque année et la renouveler en cas de réorganisation, de restructuration, de construction ou de rénovation majeure. L'évaluation du risque organisationnel doit être effectuée à tous les niveaux des milieux de soins, y compris les soins préhospitaliers, les soins de courte durée, les SLD, les soins ambulatoires et les soins à domicile. Il est important que l'ERO soit systématiquement et continuellement évaluée afin de s'assurer que les politiques, les procédures et les programmes :
- sont cohérents dans toute l'organisation;
- permettent d'atteindre les objectifs énoncés;
- sont conformes aux règlements applicables en vigueur.
L'évaluation du risque organisationnel permet de caractériser la population de patients d'une organisation, le niveau et l'intensité des soins de santé dispensés et des ressources disponibles, y compris les travailleurs aux compétences diverses. Elle doit évaluer l'efficacité des mesures de contrôle en vigueur et l'ampleur de la hiérarchie des mesures de contrôle visant à prévenir les IASS.
Pour effectuer une ERO, une organisation doit :
- déterminer les situations ou les conditions dans lesquelles des microorganismes infectieux (dangers) peuvent exister;
- évaluer le potentiel d'exposition aux microorganismes et de transmission de ces derniers;
- déterminer les conséquences de l'exposition au microorganisme;
- déterminer la gravité de la maladie causée par le microorganisme;
- déterminer les conséquences de la transmission du microorganisme pour les personnes, les organisations et la collectivité;
- évaluer les mesures de contrôle disponibles qui sont en place (p. ex. les mesures techniques et administratives et les EPI) pour atténuer l'exposition au microorganisme ou la transmission de ce dernier dans le milieu de soins en question.
2. Mesures de contrôle organisationnelles
Une fois l'ERO terminée, on peut mettre en œuvre des mesures de contrôle pour répondre à toute préoccupation. De telles mesures de contrôle, décrites ci-dessous, peuvent se situer à un ou plusieurs niveaux de la hiérarchie des mesures de contrôle. Une ventilation appropriée et la conception de l'hôpital (p. ex. les chambres d'isolement pour infections à transmission aérienne, les chambres individuelles) représentent des mesures techniques, alors que l'éducation des TS, les pratiques de base et les précautions additionnelles, ainsi que la santé au travail (p. ex. les programmes de protection respiratoire) sont des mesures administratives.
Mesures techniques—Conception, rénovation et construction de l'établissement de santé
La conception d'un établissement est un exemple de mesure techniqueNote de bas de page 197, Note de bas de page 198, Note de bas de page 199, Note de bas de page 200, Note de bas de page 201, Note de bas de page 202, Note de bas de page 203. La conception des chambres, les systèmes de ventilation, les modèles de circulation de l'air et des personnes dans les chambres, l'emplacement des distributeurs de DMBA et des lavabos réservés au lavage des mains, ainsi que les barrières physiques qui séparent les patients dans les salles à plusieurs lits et dans les salles d'attente sont tous des exemples de mesures techniques. En se conformant aux recommandations en matière de séparation spatiale (c'est-à-dire, dans l'idéal, une proportion élevée de chambres individuelles ou une séparation de 2 mètres entre chaque patient) pour la conception de nouveaux établissements de santé, la planification de la rénovation d'établissements existants ou la réorganisation des zones de soins aux patients, une organisation de soins de santé renforce sa capacité à prévenir la transmission des infections.
La conception d'un établissement de santé ayant trait à la PCI comprend également des chambres d'isolement pour infections à transmission aérienne dont le nombre, l'emplacement et le type sont adéquats; des zones à ventilation et filtration spéciales, comme les zones de triage et d'attente dans les services d'urgence; le traitement de l'air et les besoins en ventilation dans les services de chirurgie et les laboratoires, les systèmes d'échappement locaux pour les agents dangereux et d'autres zones spéciales; des réseaux d'alimentation en eau qui limitent l'espèce Legionella et les pathogènes opportunistes hydriques. Il faut également envisager des surfaces aux caractéristiques privilégiées (du produit idéal), telles que les surfacesNote de bas de page 201, Note de bas de page 202 :
- faciles à entretenir, à réparer et à nettoyer;
- qui ne favorisent pas la prolifération microbienne;
- non poreuses, lisses;
- durables;
- renouvelables;
- facile à installer, à démolir et à remplacer;
- sans joints;
- solide, résistant aux chocs.
Les professionnels en prévention des infections devraient être inclus du début à la fin des projets (c.-à-d. pour la conception de nouveaux établissements de santé, la planification de rénovation d'établissements existants ou la réorganisation des zones de soins aux patients)Note de bas de page 197, Note de bas de page 198, Note de bas de page 202, Note de bas de page 203, Note de bas de page 204, Note de bas de page 205, Note de bas de page 206.
Mesures techniques—Chauffage, ventilation et climatisation dans les établissements de santé
Pour s'assurer que les systèmes de ventilation fonctionnent de façon optimale afin d'éliminer les particules et l'excès d'humidité, les organisations sont tenues de concevoir, de construire, d'installer et d'entretenir des systèmes de ventilation conformément aux recommandations techniques et aux recommandations du fabricant. Des recommandations relatives aux systèmes de chauffage, de ventilation et de climatisation propres aux établissements de santé ont été publiéesNote de bas de page 146, Note de bas de page 147, Note de bas de page 207. Veuillez consulter la dernière édition des Normes canadiennes pour la lutte antituberculeuse, pour plus amples informations spécifique à la Mycobacterium tuberculosis.
Les milieux de soins qui dispensent ou pourraient dispenser des soins à des patients atteints d'infections transmissibles par voie aérienne présumées ou confirmées devraient avoir un nombre adéquat de chambres d'isolement pour infections à transmission aérienne (également appelées salles en pression négative)Note de bas de page 138, Note de bas de page 208, Note de bas de page 209, Note de bas de page 210, Note de bas de page 211. L’ERO devrait permettre de déterminer le nombre de chambres d'isolement nécessaire. Il est recommandé de prévoir des chambres d'isolement pour infections à transmission aérienne dans les zones suivantes des établissements de santé, y compris, notamment, les services d'urgence, les milieux de soins intensifs, les unités des malades hospitalisés et les unités de bronchoscopie et d'autopsieNote de bas de page 138, Note de bas de page 209, Note de bas de page 210, Note de bas de page 211, Note de bas de page 212.
Ce document ne fait pas de recommandation spécifique au nombre de renouvellement d'air par heure mais fourni aux organisations de soins de santé les recommandations déjà publiées (consulter le tableau 1 Recommandations pour la ventilation dans les zones suivantes des établissements de santé). Il y a un besoin de faire des recherches plus poussées dans ce domaine, ainsi que d’obtenir des indications et preuves supplémentaires pour les besoins de ventilation par la collaboration des experts en ingénierie et en sciences biomédicales.
| Zone | CSA, 2010 | ASHRAE, 2008 | CDC, 2005 |
|---|---|---|---|
| Unité d’autopsie | 20 RAH | 12 RAH | 12 RAH |
| Unité de bronchoscopie, chambre d’induction d’expectoration | 20 RAH | 12 RAH | 12 RAH |
| Chambre d'isolement pour infections à transmission aérienne | 12 RAH | 12 RAH | |
Nouvelle construction (existante) |
12 RAH (au moins 6 RAH) |
- CSA Z317.2-10 Special Requirements for Heating, Ventilation, and Air Conditioning (HVAC) Systems in Health Care FacilitiesNote de bas de page 146.
- ASHRAE American Society of Heating, Refrigerating and Air-conditioning Engineers, Ventilation of Health Care FacilitiesNote de bas de page 147.
- CDC Centers for Disease Control, Guidelines for Preventing the Transmission of Mycobacterium Tuberculosis in Health-care SettingsNote de bas de page 207.
Il n'entre pas dans la portée du présent document de donner des recommandations spécifiques concernant le chauffage, la ventilation et la climatisation des salles d'opération; ces dernières sont disponibles auprès du Facility Guidelines InstituteNote de bas de page 201 et de l'Association canadienne de normalisationNote de bas de page 146.
Mesures techniques—Contrôle à la source
Les mesures de contrôle à la source servent à prévenir la dissémination de microorganismes à partir d'une source contagieuse. Dans tout milieu de soins, les patients et les autres personnes qui présentent des symptômes devraient recevoir des instructions concernant le respect du contrôle à la source dès la première rencontre (p. ex. le triage dans les services d'urgence, les milieux d'évaluation aiguë, la réception et les salles d'attente des services d'urgence, les cliniques de consultation externe et les cabinets de médecin) et dans les endroits stratégiques (p. ex. ascenseurs, cafétéria) dans les milieux de soins ambulatoires et hospitaliers. Des politiques et des procédures (mesures administratives) devraient être mises en œuvre pour élaborer un programme de contrôle à la source. Les mesures de contrôle à la source peuvent comprendre, entre autresNote de bas de page 124, Note de bas de page 148:
- la signalisation à l'entrée des milieux de soins en vue de la reconnaissance rapide des symptômes (p. ex. dépistage des syndromes);
- les entrées et salles d'attente séparées pour les patients symptomatiques;
- la séparation spatiale;
- les barrières physiques pour l'évaluation aiguë;
- l'identification, le diagnostic et le traitement précoces des infections (p. ex. tuberculose, norovirus);
- l'hygiène respiratoire;
- l'hygiène des mains;
- le placement des patients (p. ex. zones de soins aux patients, chambres individuelles ou chambres d'isolement pour infections à transmission aérienne);
- les stratégies de réduction des aérosols pendant les IMGA (consulter la partie B, section IV, sous-section iii, 1b).
Mesures techniques—Contrôle à la source—Séparation spatiale
Il faudrait mettre en œuvre une séparation spatiale appropriée et des recommandations d'espacement visant à diminuer l'exposition des patients et des visiteurs aux microorganismes dans les zones de soins cliniques et les salles d'attente. Il faudrait envisager une distance de 2 mètres entre une source infectée qui tousse ou éternue (p. ex. une personne symptomatique atteinte d'une maladie respiratoire aiguë) et un hôte réceptif non protégé (p. ex. les patients, les travailleurs de la santé, les visiteurs, les entrepreneurs) afin de prévenir la transmission des particules contagieuses par gouttelettesNote de bas de page 122, Note de bas de page 123, Note de bas de page 124.
On devrait inclure des recommandations concernant la séparation spatiale dans le cadre de la conception de nouveaux établissements de santé ou de la planification de rénovation d'établissements existants (consulter la partie A, section III, B, 2).
Mesures techniques—Contrôle à la source—Hygiène respiratoire
L'hygiène respiratoire renvoie à une combinaison de mesures qui visent à réduire au minimum la transmission des agents pathogènes des voies respiratoiresNote de bas de page 45, Note de bas de page 48, Note de bas de page 148, Note de bas de page 213, Note de bas de page 214, Note de bas de page 215. Ces mesures de contrôle à la source concernent toutes les personnes qui manifestent des symptômes d'infection respiratoire, dès leurs arrivées en milieu de soins, et ces mesures sont maintenues à chaque rencontre ultérieure (p. ex. triage dans les services d'urgence, réception aux cliniques de soins ambulatoires ou dans les cabinets des prestataires de soins de santé, ainsi qu'aux endroits stratégiques, comme dans les ascenseurs et les cafétérias). Elles nécessitent d'éduquer et d'encourager toutes les personnes (patients, TS et visiteurs) qui ont les capacités physiques et cognitives de le faire à pratiquer l'hygiène respiratoire. Les mesures précises peuvent comprendre des panneaux d'instruction, des programmes éducatifs et le matériel d'hygiène respiratoire mis à disposition (p. ex. mouchoirs en papier, poubelles automatiques doublées de plastique, DMBA).
De plus amples renseignements se trouvent dans le document de l'Agence de la santé publique du Canada intitulé Guide de prévention des infections. Prévention de la pneumonie associée aux soins de santéNote de bas de page 216.
Mesures techniques—Contrôle à la source—Hygiène des mains
Les obstacles organisationnels liés aux mesures techniques, comme le manque d'accessibilité et d'entretien des installations réservées à l'hygiène des mains et un mauvais accès aux produits d'hygiène des mains, ont des conséquences négatives sur le respect des mesures d'hygiène des mains. Les organisations sont tenues de s'assurer que de tels obstacles soient éliminés. Les lecteurs peuvent se référer aux lignes directrices pour la PCI de l'Agence de la santé publique du Canada intitulées Pratiques en matière d’hygiène des mains dans les milieux de soinsNote de bas de page 217.
Mesures techniques—Contrôle à la source—Placement des patients
Récemment, pour augmenter l'accès aux lits de malades hospitalisés peu nombreux et réduire l'entassement dans les services d'urgence, certains hôpitaux canadiens ont élaboré des protocoles de « surcapacité » ou de « pleine capacité » (c'est-à-dire qu'ils admettent des patients dans des unités de malades hospitalisés qui fonctionnent déjà à pleine capacité)Note de bas de page 218. L’énoncé de position de l’Association des infirmières et infirmiers du Canada (AIIC) « Les protocoles relatifs à la surcapacité et la capacité dans le système de santé du Canada » indiquait que de tels protocoles pourraient avoir un effet sur la sécurité des patients et des infirmières, dont une hausse du nombre et de la sévérité des événements indésirables, et ont des inquiétudes concernant le contrôle de maladies infectieusesNote de bas de page 218. L’AIIC conseille aux hôpitaux de prendre toutes les mesures nécessaires pour éviter d'utiliser les protocoles de surcapacité et de ne pas considérer ces derniers comme une norme de prestation de services hospitaliers. Les hôpitaux qui utilisent des protocoles de surcapacité ou de pleine capacité à court terme devraient élaborer et mettre en œuvre des politiques et des pratiques qui réduisent au minimum le risque de propagation des infections causé par l'entassement et le manque de personnel. Les patients qui se présentent à l'hôpital atteints d'infections aiguës transmissibles (y compris, entre autres, les vomissements, la diarrhée, la fièvre, la toux, le coryza, l'essoufflement) ne sont pas des candidats au placement en surcapacité.
Mesures techniques—Contrôle à la source—Stratégies de réduction des aérosols pendant les interventions médicales générant des aérosols
Consulter l'analyse des IMGA à la partie A, section II, C, 2c et les stratégies de réduction de la production d'aérosols à la partie B, section IV, sous-section iii, 1b.
3. Mesures de contrôle administratives
Programme de santé au travail
L'un des objectifs du programme de santé au travail consiste à répertorier les situations qui présentent un risque d'exposition ou de transmission potentielles d'un microorganisme du TS à d'autres personnes et vice-versa. Les composantes du programme de la santé au travail qui appuient le recours à des pratiques de base et à des précautions additionnelles pour prévenir l'exposition à des microorganismes ou la transmission de ces derniers se trouvent dans les lignes directrices de l’ASPC en matière de PCI intitulées La prévention et la lutte contre les infections professionnelles dans le domaine de la santéNote de bas de page 219 et comprennent :
- évaluation préalable au placement (au moment de l'embauche);
- immunisation contre les maladies infectieuses que l'on peut prévenir par vaccin;
- dépistage de la tuberculose (évaluation préalable au placement et dépistage, selon les politiques de l'organisation);
- immunisation annuelle contre la grippe;
- politiques de gestion des TS atteints d'infections;
- gestion des allergies au latex et à d'autres composants des gants;
- prévention de l'exposition aux agents pathogènes à diffusion hématogène, y compris un programme de manipulation sécuritaire des objets pointus et tranchants (consulter ci-dessous);
- gestion des TS qui ne peuvent pas porter d'EPI (p. ex. les appareils de protection respiratoire).
Les composantes importantes du programme de la santé au travail qui appuient le recours à des pratiques de base et à des précautions additionnelles se trouvent dans les lignes directrices de l'ASPC en matière de PCI intitulées La prévention et la lutte contre les infections professionnelles dans le domaine de la santéNote de bas de page 219 et comprennent :
- la gestion des TS qui ne peuvent pas se conformer aux recommandations en matière d'hygiène des mains (pour de plus amples renseignements, veuillez consulter les lignes directrices pour la PCI de l'ASPC intitulées Pratiques en matière d’hygiène des mains dans les milieux de soinsNote de bas de page 217;
- programme de protection respiratoire (consulter ci-dessous).
Programme de santé au travail—Manipulation sécuritaire des objets pointus et tranchants et prévention de l'exposition aux pathogènes à diffusion hématogène
La prévention des blessures causées par des objets pointus et tranchants et de l'exposition des TS aux agents pathogènes à diffusion hématogène fait partie des pratiques de base.
Les personnes qui utilisent des objets pointus et tranchants doivent recevoir une formation concernant leur manipulation sécuritaire afin d'éviter de se blesser et de blesser d'autres personnes qui pourraient entrer en contact avec l'objet pendant ou après les interventions. Les programmes de sécurité devraient comprendre l'ouverture d'une enquête officielle sur toutes les blessures par objet tranchant qui surviennent dans le milieu de travailNote de bas de page 220. Les composantes d'un programme de prévention des blessures par objet pointu et tranchant ont été publiéesNote de bas de page 221, Note de bas de page 222. Le manuel du CDC concernant la conception, la mise en œuvre et l'évaluation d'un programme de prévention des blessures par objet pointu et tranchant est accessible sur le site Web du CDC (http://www.cdc.gov/sharpssafety/resources.html, en anglais seulement).
Il a été établi que l'utilisation de dispositifs à conception sécuritaire, comme les dispositifs avec aiguille protégée, les systèmes sans aiguille avec orifices auto-scellants et les seringues équipées de caractéristiques de sécurité, réduit les blessures par piqûre d'aiguilleNote de bas de page 220, et leur utilisation est reconnue comme étant une priorité dans les stratégies de réduction des risquesNote de bas de page 223. Dans certaines provinces ou certains territoires, ces dispositifs de sécurité sont exigés par les règlements (prière de consulter les règlements locaux). L'organisation de soins de santé devrait faire preuve de prudence dans son choix de dispositifs sans aiguilleNote de bas de page 224, Note de bas de page 225, Note de bas de page 226, Note de bas de page 227, car on a établi que certains modèles présentent un risque pour les patientsNote de bas de page 228, Note de bas de page 229, Note de bas de page 230, Note de bas de page 231, Note de bas de page 232.
Programme de santé au travail—Programme de protection respiratoire
La protection respiratoire prévoit l'utilisation d'un appareil de protection respiratoire pour prévenir l'inhalation d'aérosols contenant des particules contagieuses. On devrait utiliser des appareils de protection respiratoire pour soigner les patients que l'on présume ou que l'on sait infectés par des agents pathogènes des voies respiratoires (p. ex. la tuberculose, la rougeole) et, dans certaines situations, pendant les IMGA (consulter la partie B, section IV, sous-section iii, 7). Les organisations de soins de santé qui utilisent des appareils de protection respiratoire devraient avoir mis en place un programme de protection respiratoireNote de bas de page 233. Le programme de protection respiratoire devrait prévoir des examens de santé en milieu de travail, des tests d'ajustement ou de rajustement et une formation pour tous les TS qui pourraient porter un appareil de protection respiratoire. L'organisation devrait s'engager à élaborer, à mettre en œuvre, à tenir à jour et à évaluer le programme de protection respiratoire.
Les organisations de soins de santé sont responsables du choix de la marque, du modèle et de la taille des appareils de protection respiratoire qui seront utilisés par les membres de leur personnel et devraient tenir compte de la diversité du personnel soignant et de la population de patients. Elles devraient s'assurer que leur personnel a accès aux modèles et aux tailles d'appareil de protection respiratoire recommandés, tel que l'exigent le code du travail et les règlements sur la santé au travail locaux.
Les organisations devraient tenir compte de ce qui suit :
- Lorsqu'elles choisissent des appareils de protection respiratoire, elles devraient accorder la préférence à ceux qui sont naturellement bien ajustés.
- Il se peut que l'organisation doive se procurer des appareils de protection respiratoire auprès de plus d'un fabricant pour qu'ils soient ajustés à tout l'éventail des groupes ethniques et structures du visage représentés dans sa main-d'œuvre.
- Un test d'ajustement est utilisé pour évaluer dans quelle mesure un type de respirateur correspond à une personne donnée en évaluant les fuites autour de la figure. La littérature publiée concernant les test d'ajustement des respirateurs dans le cadre des soins de santé ne sont pas concluantesNote de bas de page 234, Note de bas de page 235, Note de bas de page 236, cependant, la plupart des juridictions canadiennes exigent un test d’ajustement pour les travailleurs de la santé afin de déterminer leur capacité à obtenir une étanchéité satisfaisante lors de l'utilisation des respirateursNote de bas de page 233. Par conséquence, les travailleurs de la santé sont référés aux règlements provinciaux et territoriaux concernant les tests d'ajustement. En l'absence d'une telle réglementation, consulter les autorités de santé publique provinciaux/territoriaux responsables. La plupart des juridictions précisent que les tests d'ajustement doivent se répéter selon un horaire fixe (p. ex. au moins tous les 2 ans)Note de bas de page 233, ou tel que défini par les règlements provinciaux et territoriaux, ou plus fréquemment si les conditions du visage changent (p. ex., gain ou perte de poids, soins dentaires).
- Si une organisation décide de changer la marque ou le modèle des appareils de protection respiratoire à utiliser, elle devrait savoir que les tests d'ajustement ne sontvalables d'une marque ou d'un modèle d'appareil de protection respiratoire à l'autre.
- Les organisations de soins de santé devraient élaborer des politiques à l'égard des TS qui ne peuvent pas obtenir un ajustement optimal autour du visage lorsqu'elles portent un appareil de protection respiratoire (p. ex. les personnes qui ont des déformations du visage, les hommes qui portent la barbe).
Les travailleurs de la santé devraient tenir compte de ce qui suit :
- Ils ne devraient utiliser que les appareils de protection respiratoire avec lesquels ils ont fait un test d'ajustement.
- Les travailleurs de la santé devraient connaître les applications, les avantages et les limites, ainsi que l'utilisation correcte du modèle d'appareil de protection respiratoire dont ils ont fait l'essai (consulter l'annexe X).
- Chaque fois qu'un TS met un appareil de protection respiratoire, il devrait vérifier l'ajustement (ce que l'on appelle quelquefois une test d'étanchéité) pour que l'appareil de protection respiratoire fonctionne correctementNote de bas de page 233.
Éducation des travailleurs de la santé
Tous les TS devraient recevoir une formation concernant les politiques et les procédures de PCI pendant leur formation professionnelle, leur orientation professionnelle, lors de certaines circonstances particulières (p. ex. les éclosions, l'arrivée de nouveau matériel ou de nouveaux renseignements) et de façon régulière. Les organisations de soins de santé sont tenues d'offrir cette formation et il incombe aux TS de saisir les occasions de formation. La planification et l'évaluation des programmes éducatifs destinés aux apprenants adultes sont complexes, et il faudrait consulter les ressources appropriées (p. ex. Association pour la prévention des infections à l'hôpital et dans la communauté-Canada, compétences de base en matière de PCI pour les TSNote de bas de page 237, planification de programmes pour les apprenants adultes)Note de bas de page 238. Il est important que les sujets, les méthodes et les documents d'éducation et de formation soient appropriés pour le niveau de compréhension et de responsabilité des TS. Le contenu des séances d'éducation et de formation sur les pratiques de base et les précautions additionnelles devrait inclure, entre autres, les principes suivants :
- l'évaluation du risque au point de service;
- la transmission des microorganismes (chaîne de l'infection);
- la prévention de l'exposition aux microorganismes (y compris le contrôle à la source);
- l'importance de l'immunisation;
- les connaissances au sujet de l'état immunitaire par rapport aux maladies que l'on peut éviter par vaccin (p. ex. la varicelle);
- les indications concernant l'hygiène des mains (DMBA au point de service comme méthode privilégiée) à moins qu’une exception ne s’applique (c.-à-d. lorsque les mains sont visiblement souillées par des matières organiques ou si l’exposition à un norovirus et à des agents pathogènes sporulés comme Clostridium difficile est fortement soupçonnée ou avérée, y compris au cours d’éclosions impliquant ces organismes);
- les indications concernant l'application correcte de la technique aseptique;
- la manipulation et l'élimination sécuritaires des objets pointus et tranchants;
- le nettoyage et la désinfection du matériel non critique destiné aux soins aux patients d'un patient à l'autre;
- l'éducation des patients et des visiteurs;
- les indications concernant l'utilisation appropriée de l'EPI;
- la mise en œuvre des précautions additionnelles;
- la modification des pratiques pendant les éclosions;
- la façon d'utiliser le tableau 4 pour mettre en œuvre des précautions additionnelles de manière empirique;
- la façon d'utiliser le tableau 5 pour modifier ou abandonner des précautions additionnelles.
Retraitement du matériel de soins aux patients—Retraitement du matériel réutilisable
Un retraitement approprié (c.-à-d. le nettoyage, la désinfection et la stérilisation) des appareils médicaux réutilisables (p. ex. matériel, instruments) est important pour prévenir la transmission de microorganismes et fait obligatoirement partie des soins de santé qui doivent être dispensés selon les lignes directricesNote de bas de page 239, Note de bas de page 240 et les normes publiéesNote de bas de page 241, Note de bas de page 242, Note de bas de page 243, Note de bas de page 244, Note de bas de page 245.
Spaulding a élaboré un système de classification des spécifications de nettoyage, de désinfection et de stérilisation du matériel utilisé pour les soins aux patientsNote de bas de page 246. Ce système répartit les appareils médicaux, l'équipement et le matériel chirurgical en trois catégories (non critiques, semi-critiques et critiques) en fonction du risque d'infection que présente leur utilisationNote de bas de page 247. Les travailleurs de la santé doivent pouvoir reconnaître les articles semi-critiques et critiques et les retraiter à un haut degré de désinfection ou de stérilisation. Les travailleurs de la santé doivent également pouvoir reconnaître le matériel non critique et s'assurer qu'il est propre avant de l'utiliser (consulter « Nettoyage de l'environnement » ci-dessous).
Le retraitement des appareils médicaux réutilisables peut être effectué au sein d'un hôpital ou d'un établissement de santé régional, ou être sous-traité à une entreprise de retraitement tierce. En cas de sous-traitance à des entreprises de retraitement tierces, les règlements provinciaux ou territoriaux devraient être appliqués. Les appareils réutilisables doivent être retraités par un personnel formé sous la supervision de personnes ayant reçu une formation spéciale. Dans la mesure du possible, le retraitement devrait être effectué de façon centralisée et faire l'objet de vérifications régulières. Lorsque cela n'est pas possible, il est préférable d'utiliser des dispositifs à usage unique jetables.
Des processus plus rigoureux et très spécifiques doivent servir à reconnaître et à retraiter le matériel contaminé par des prions (agents responsables des encéphalopathies spongiformes transmissibles, comme la maladie de Creutzfeldt-Jakob). Les lecteurs devraient consulter les lignes directrices de l'ASPC propres à ce sujetNote de bas de page 248, Note de bas de page 249, Note de bas de page 250 pour obtenir de plus amples renseignements.
Retraitement du matériel de soins aux patients—Retraitement et réutilisation des dispositifs à usage unique
Les dispositifs conçus et vendus comme étant à usage unique ne doivent être ni retraités, ni réutilisés. Cependant, un sondage effectué en 2006 dans le cadre de recherches sur les pratiques de retraitement et de réutilisation des dispositifs à usage unique (DUU) dans les hôpitaux canadiens de soins de courte durée a permis d'établir que 28 % des hôpitaux retraitent les DUU, soit à l'interne, soit en sous-traitanceNote de bas de page 251. Ces résultats étaient similaires aux résultats d'un sondage canadien effectué en 2000Note de bas de page 252. Les préoccupations soulevées par le retraitement des DUU comprennent l'augmentation du risque d'effets indésirables pour le patient, les questions d'ordre éthique et la rentabilité du retraitementNote de bas de page 251. Le retraitement des DUU se fait selon un processus qui permet de s'assurer que l'utilisation d'un DUU qui a déjà servi pour un patient est sans danger pour un autre patient. Ce processus comprend le nettoyage, les essais de fonctionnement, le remballage, le réétiquetage, les essais de recherche de substances pyrogènes, la désinfection et la stérilisationNote de bas de page 253. Les organisations de soins de santé qui embauchent des entreprises de retraitement tierces à ces fins doivent se conformer aux lois provinciales ou territoriales. Au moment de la rédaction du présent document, il n'existait aucun processus de réglementation des entreprises tierces de retraitement des DUU au Canada. De ce fait, les établissements qui décident de retraiter les DUU doivent retenir les services d'établissements réglementés par la Food and Drug Administration aux États-Unis.
Retraitement du matériel de soins aux patients—Nettoyage et désinfection du matériel de soins aux patients non critique
La contamination du matériel de soins aux patients, des articles présents dans l'environnement du patient ainsi que de l'environnement du patient a été documentée et impliquée dans la transmission des infections. Consulter la liste 1, Exemples de sources de contamination environnementales. Les articles usagés ou potentiellement contaminés qui sont entrés en contact avec la peau intacte du patient devraient toujours être nettoyés et désinfectés avant d'être utilisés avec un autre patient. Consulter le point ci-dessous concernant le nettoyage de l'environnement du patient.
Nettoyage de l'environnement
Les mesures visant à réduire au minimum l'exposition à la contamination environnementale comprennent Note de bas de page 239:
- réserver le matériel médical non critique à un seul patientNote de bas de page 254
- attribuer la responsabilité du nettoyage et de la désinfection de routine du matériel de soins aux patientsNote de bas de page 255, Note de bas de page 256, Note de bas de page 257, Note de bas de page 258
- s'assurer que le nettoyage de l'environnement est effectué conformément à une procédure et à une fréquence bien établie et qu'il est documenté et supervisé par des membres du personnel ayant reçu une formation adéquate et consacrés à cette tâche
- s'assurer que les surfaces sont construites en matériaux facilement nettoyables au point d'utilisationNote de bas de page 201, Note de bas de page 202
- augmenter la fréquence du nettoyage et de la désinfection des surfaces fréquemment touchéesNote de bas de page 70, Note de bas de page 82, Note de bas de page 95, Note de bas de page 254, Note de bas de page 259, Note de bas de page 260
- surveiller la conformité avec les pratiques de nettoyage de l'environnement recommandéesNote de bas de page 261, Note de bas de page 262, Note de bas de page 263
- s'assurer que les chambres font l'objet d'un nettoyage final après la sortie d'hôpital du patient et après l'arrêt des précautionsNote de bas de page 263 (consulter l'annexe VII)
- déterminer quel produit utiliser pour le nettoyage de routine de l'environnement
Dans les situations où certains organismes sont transmis en permanence (p. ex. le norovirus, le rotavirus, C. difficile), il faut peut-être envisager d'utiliser des produits désinfectants précisNote de bas de page 78, Note de bas de page 239, Note de bas de page 264, Note de bas de page 265. En cas d'éclosion ou de transmission permanente, les chambres qui hébergent des patients infectés par C. difficile devraient être décontaminées et nettoyées avec des produits de nettoyage qui contiennent du chlore (au moins 1 000 ppm) ou d'autres agents sporicidesNote de bas de page 43, Note de bas de page 266, Note de bas de page 267, Note de bas de page 268, Note de bas de page 269, Note de bas de page 270, Note de bas de page 271.
De plus amples renseignements sont disponibles dans le document du CDC/Healthcare Infection Control Practices Advisory Committee intitulé Guideline for Disinfection and Sterilization in Healthcare FacilitiesNote de bas de page 239 et dans le document du CDC intitulé Guidelines for Environmental Infection Control in Health-Care FacilitiesNote de bas de page 72.
Déchets
La plupart des déchets générés dans les milieux de soins ne sont pas plus dangereux que les déchets domestiquesNote de bas de page 272, Note de bas de page 273, Note de bas de page 274. Les règlements locaux peuvent exiger un traitement spécial des objets pointus et tranchants et de certains déchets biomédicaux (p. ex. les éponges, les pansements ou les champs opératoires imbibés de sang ou de sécrétions)Note de bas de page 275. Les poubelles devraient être placées à des endroits commodes et s'ouvrir de préférence de façon automatique. Des règlements locaux peuvent s'appliquer.
De plus amples renseignements sont disponibles dans le document (en anglais seulement) de l'Association canadienne de normalisation intitulé Handling of Waste Materials in Health Care Facilities and Veterinary Health Care FacilitiesNote de bas de page 275.
Linge
Bien que le linge des établissements de santé puisse être contaminé par des agents pathogènes, le risque de transmission d'une maladie est négligeableNote de bas de page 117, Note de bas de page 276, Note de bas de page 277. Il faudrait manipuler le linge sale avec soin pour éviter la dissémination des microorganismesNote de bas de page 278, Note de bas de page 279. Aucun traitement spécial du linge des patients pour lesquels on prend des précautions additionnelles n'est requisNote de bas de page 276, Note de bas de page 280.
Si des descentes de linge sont utilisées, elles devraient être conçues, entretenues et utilisées correctement, de façon à réduire au minimum la dissémination des aérosols provenant du linge contaminéNote de bas de page 281, Note de bas de page 282.
Le linge propre devrait être transporté et entreposé de façon à prévenir la manipulation par inadvertance ou la contamination par la poussière, qui pourrait contenir des spores fongiques nocives pour les patients immunovulnérablesNote de bas de page 72.
De plus amples renseignements se trouvent dans le document du CDC intitulé Guidelines for Environmental Infection Control in Health-Care FacilitiesNote de bas de page 72.
Gestion des cadavres
Aucune recommandation spéciale n'est associée à la manipulation de cadavres, à leur préparation pour l'autopsie ou à leur transfert à une entreprise de pompes funèbres. Les pratiques de base appliquées correctement et systématiquement et les précautions additionnelles indiquées avant le décès (transmission par contact ou par voie aérienne) sont suffisantes. Les précautions contre la transmission par gouttelettes sont une exception et ne sont pas nécessaires post mortem. Certaines provinces et certains territoires peuvent avoir établi des règlements sur les maladies transmissibles.
Gestion des animaux et des animaux de compagnie
La zoothérapie en milieux de soins pourrait être bénéfique pour les patients. La responsabilité des politiques et des procédures relatives au contrôle de la santé des animaux et à la PCI pour les interventions en zoothérapie dans les établissements de santé incombe à l'organisation. Des recommandations relatives aux pratiques en matière de PCI concernant le contrôle de la santé des animaux et les interventions en zoothérapie dans les établissements de santé ont été publiéesNote de bas de page 71, Note de bas de page 72.
C. Rôle du travailleur de la santé
1. Évaluation du risque au point de service
Avant chaque interaction avec un patient, les TS sont tenus d'évaluer le risque d'infection que peuvent présenter un patient, une situation ou une intervention pour eux-mêmes, les autres patients, les visiteurs et les TS. L'ERPS est une évaluation des variables (facteurs de risque) associées à l'interaction entre le TS, le patient et l'environnement du patient; ces variables servent à évaluer et à analyser le potentiel d'exposition aux agents infectieux et à déterminer les risques de transmissionNote de bas de page 283. Cette ERPS est basée sur un jugement à propos de la situation clinique (y compris l'état clinique, physique, émotionnel et mental du patient) et sur des renseignements à jour concernant la façon dont l'organisation de soins de santé a conçu et mis en œuvre des mesures de contrôle techniques et administratives, ainsi que la disponibilité et l'utilisation des EPI. Les mesures de contrôle sont basées sur l'évaluation des variables (facteurs de risque) relevées.
Les travailleurs de la santé devraient habituellement effectuer plusieurs ERPS par jour afin d'appliquer les mesures de contrôle, pour leur propre sécurité et pour celles des patients et des autres personnes se trouvant dans l'environnement de soins de santé.
Par exemple, un TS effectue une ERPS lorsqu'il évalue un patient et sa situation pour :
- déterminer la priorité pour les chambres individuelles ou pour la sélection des compagnons de chambre si les chambres doivent être communes;
- déterminer la possibilité d'une exposition à du sang, des liquides organiques, des sécrétions et des excrétions, ainsi que la possibilité de contact avec une peau non intacte, et prendre les mesures de contrôle appropriées (p. ex. un EPI) pour prévenir l'exposition;
- appliquer des stratégies visant à réduire la production d'aérosols pendant les IMGA (consulter la partie B, section IV, sous-section iii, 1b);
- déterminer la nécessité des précautions additionnelles lorsque les pratiques de base ne suffisent pas pour prévenir l'exposition.
Facteurs de risque ayant une incidence sur les mesures de contrôle
Les mesures de contrôle visant à prévenir l'exposition ou la transmission peuvent varier selon le microorganisme, l'état du patient, la situation ou l'intervention et le milieu de soins. Par exemple, les mesures visant à réduire la transmission des infections respiratoires sont différentes des mesures visant à réduire la transmission des infections gastro-intestinales. Certains patients (p. ex. les jeunes enfants, les adultes incontinents et les personnes ayant une déficience cognitive) ou certaines interventions précises sur certains patients peuvent augmenter le risque de transmission; elles exigent donc des mesures de contrôle différentes. Les travailleurs de la santé courent le risque d'exposition aux virus respiratoires le plus élevé lorsqu'ils soignent des patients qui produisent des sécrétions respiratoires en grandes quantités ou qui toussent fréquemment et sont incapables de prendre soin d'eux-mêmes, y compris l'hygiène respiratoire et l'hygiène des mains. On a établi que les interventions telles que les IMGA augmentent la transmission de la tuberculoseNote de bas de page 153 et du SRASNote de bas de page 150, Note de bas de page 152, Note de bas de page 284 et, par conséquent, requièrent des mesures de contrôle précises (consulter la partie B, section IV, sous-section iii, 1b).
Certaines infections se transmettent plus facilement dans les milieux de soins pédiatriques que dans les milieux de soins pour adultes. L'infection est une cause fréquente du recours aux soins de santé chez les jeunes enfants, qui hébergent souvent des microorganismes, en particulier des virus respiratoires et gastro-intestinaux, qu'ils peuvent excréter, même s'ils sont asymptomatiquesNote de bas de page 181, Note de bas de page 285. Les jeunes enfants sont également vulnérables à de nombreuses infections, car ils n'ont pas encore développé d'immunité à l'égard de nombreux microorganismes. La proximité de nombreuses personnes contagieuses et d'hôtes réceptifs favorise la transmission, tout comme les caractéristiques de comportement des jeunes enfants, comme l'incontinence, une hygiène inadéquate, le port fréquent des mains, des jouets et d'autres objets à la bouche, le fait de baver et le contact direct entre des enfants qui jouent ensemble. En outre, il est probable que les TS et les parents touchent fréquemment l'enfant des mains pendant les soins de base. Les jouets communs, les salles de jeu et les frères et sœurs en visite peuvent également contribuer au risque de transmissionNote de bas de page 181, Note de bas de page 285.
Le risque varie selon le milieu de soins (p. ex. les soins préhospitaliers, les soins de courte durée, les SLD, les soins ambulatoires et les soins à domicile). Par conséquent, les mesures de contrôle devraient souvent être modifiées en fonction du milieu de soins, car il serait peu approprié d'imposer le même degré de précautions dans chaque milieu. Le modèle de soins habituel dans les établissements de SLD consiste à offrir un milieu semblable à celui de la maison, avec participation aux activités de la vie quotidienne. On devrait adopter une approche équilibrée qui offre un environnement sans danger tout en évitant les mesures inutilement contraignantes qui pourraient nuire au bien-être général ou à la qualité de vie de la personneNote de bas de page 286. Les soins préhospitaliers peuvent présenter un risque accru de transmission, car il s'agit d'un environnement non contrôléNote de bas de page 287.
Le risque de transmission croisée peut augmenter lorsque les patients partagent une chambre au lieu d'être hébergés dans des chambres individuellesNote de bas de page 48, Note de bas de page 201, Note de bas de page 202, Note de bas de page 288, Note de bas de page 289, Note de bas de page 290, Note de bas de page 291, Note de bas de page 292, Note de bas de page 293, Note de bas de page 294, Note de bas de page 295, Note de bas de page 296, Note de bas de page 297, Note de bas de page 298, Note de bas de page 299, Note de bas de page 300, Note de bas de page 301, Note de bas de page 302.
Connaissances et compétences nécessaires pour effectuer une évaluation du risque au point de service
Les travailleurs de la santé devraient avoir des connaissances, des compétences et des ressources suffisantes pour effectuer une ERPS avant chaque interaction avec un patient afin d'appliquer les mesures de contrôle appropriées. Pour effectuer une ERPS, chaque TS devrait comprendre les principes suivants, en tenant compte du niveau de soins qu'il offre, de son niveau d'instruction et de son travail ou de ses responsabilités particulières :
- les maillons de la chaîne de l'infection;
- les variables qui influent sur la transmission des microorganismes, qui peuvent comprendre le type d'exposition, la taille de l'inoculum, la réceptivité de l'hôte et les méthodes de contrôle qui permettent de réduire le risque;
- les caractéristiques des microorganismes, qui peuvent comprendre les réservoirs, l'infectiosité, le mode de transmission, la période d'incubation, la période de contagion et la virulence;
- les pratiques et les activités liées aux soins aux patients qui contribuent à l'exposition aux microorganismes;
- les risques d'exposition propres au milieu de soins;
- les circonstances relatives au milieu;
- le niveau de risque et les mesures de contrôle appropriées à mettre en place pour réduire le risque de transmission des microorganismes;
- la façon de consulter le service de PCI pour trouver une réponse à toute question ou préoccupation;
- les mesures de contrôle qui peuvent être différentes d'un microorganisme et d'un milieu de soins à l'autre.
Application des évaluations du risque au point de service
Chaque TS peut envisager de poser des questions afin de déterminer le risque d'exposition et le potentiel de transmission des microorganismes pendant les interactions avec les patients lorsqu'il effectue une ERPS. Voici quelques exemples de questions pertinentes :
- Quel contact le TS aura-t-il avec le patient?
- Quelles tâches ou interventions le TS va-t-il effectuer? Y a-t-il un risque d'éclaboussures ou de projection de gouttelettes?
- Si le patient souffre de diarrhée, est-il incontinent? S'il est incontinent, les selles peuvent-elles être contenues dans un produit pour adultes incontinents?
- Le patient est-il capable de pratiquer l’hygiène des mains et est-il disposé à le faire?
- Le patient se trouve-t-il en chambre commune?
Les tableaux 2 et 3 donnent un aperçu de quelques-uns des facteurs de risque relevés dans les questions ci-dessous, qu'il faut envisager lorsque l'on effectue une ERPS, en prenant une infection par C. difficile et la grippe saisonnière comme exemples. Les tableaux décrivent l'évolution du risque d'exposition et de la transmission potentielle en fonction des variables associées à la source infectée, à l'environnement et à l'hôte réceptif. Les facteurs de risque à envisager dans le cadre de l'ERPS, tels qu’ils sont décrits dans les tableaux 2 et 3, comprennent ce qui suit.
- Une source infectée : l'ERPS devrait évaluer la nature changeante des symptômes de la source infectée et de l'environnement afin de déterminer l'EPI que devrait porter le TS, les autres membres du personnel et les visiteurs. L'ERPS devrait également déterminer s'il faut déplacer le patient en chambre individuelle équipée d'une salle de bains privée et si d'autres pratiques devraient être modifiées en cas d'évolution de l'état du patient.
- Un hôte réceptif : l'ERPS devrait évaluer si une infection s'est développée chez l'hôte réceptif, comme une infection par C. difficile (p. ex. une infection croisée provenant d'un compagnon de chambre ou d'un TS) ou si le risque posé par une source infectée a augmenté ou diminué (p. ex. la diarrhée a empiré, ou les selles sont désormais solides). L'ERPS devrait permettre de déterminer l'EPI approprié à porter pour soigner le patient dans diverses situations. On peut citer les exemples suivants : changer des couches, prendre la tension artérielle ou apporter un plateau-repas sans contact avec le patient ou l'environnement, déterminer s'il faut déplacer le patient ou ses compagnons de chambre dans une autre unité, déterminer s'il faut renforcer l'entretien ménager, et toute autre pratique de soins nécessaire en raison de l'évolution du risque d'acquisition de C. difficile.
| Source | Risque de transmission élevé | Faible risque de transmission |
|---|---|---|
| Agent infectieux/ source infectée |
Diarrhée fréquente | Selles solides |
| Incontinence | Continence | |
| Mauvaise hygiène | Bonne hygiène | |
| Incapacité à prendre soin de soi en raison de l'état physique, de l'âge ou d'une déficience cognitive | Capacité à prendre soin de soi | |
| Environnement | Rapport patients/infirmières élevé | Faible rapport patients/infirmières |
| Salle de bains et lavabo communs | Chambre individuelle, toilettes privées dans la chambre, lavabo réservé au lavage des mains à l'usage du patient | |
| Chaise hygiénique commune sans nettoyage entre les patients | Chaise hygiénique individuelle | |
| Pas d'hygiène des mains au point de service | Hygiène des mains au point de service | |
| Pas de lavabo réservé au lavage des mains à l'usage du personnel, lavabo utilisé à d'autres fins ou lavabo sale | Lavabo réservé au lavage des mains accessible et propre à l'usage du personnel | |
| Entretien ménager inadéquat | Entretien ménager approprié | |
| Hôte réceptif (patient) | Reçoit des soins directs | Capacité à prendre soin de soi |
| Mauvaise hygiène personnelle | Bonne hygiène personnelle |
| Source | Risque de transmission élevé | Faible risque de transmission |
|---|---|---|
| Agent infectieux/ source infectée |
Sécrétions respiratoires abondantes | Sécrétions respiratoires minimales |
| Toux ou éternuements fréquents | Toux ou éternuements peu fréquents | |
| Mesures d'hygiène respiratoire non respectées | Conformité avec les pratiques d'hygiène respiratoire | |
| Premiers stades de la maladie | En convalescence | |
| Incapacité à prendre soin de soi | Capacité à prendre soin de soi | |
| Nouveau-nés et enfants (prolongation potentielle de l'excrétion virale et de la contamination environnementale) | Adultes | |
| Immunovulnérable (prolongation potentielle de l'excrétion virale) | Immunocompétent | |
| Placement ou groupement des patients en cohortes inadéquats | Placement ou groupement des patients en cohortes adéquats | |
| Environnement | Rapport patients/infirmières élevé | Faible rapport patients/infirmières |
| Contact prolongé ou fréquent avec la source infectée | Contact limité avec la source infectée | |
| Chambre et salle de bains communes | Chambre et salle de bains individuelles | |
| Entretien ménager inadéquat | Entretien ménager approprié | |
| Matériel de soins aux patients commun non nettoyé entre les épisodes de soins aux patients | Matériel réservé à un seul patient ou nettoyage et désinfection du matériel entre chaque utilisation | |
| Séparation spatiale inadéquate entre la source infectée et l'hôte réceptif (moins de 2 mètres) | Séparation spatiale adéquate entre la source infectée et l'hôte réceptif (au moins 2 mètres) | |
| Non-respect des normes de nettoyage et de désinfection | Respect des normes de nettoyage et de désinfection | |
| Hôte réceptif (patient) |
Incapacité à prendre soin de soi | Capacité à prendre soin de soi |
| Maladie sous-jacente | Pas de maladie sous-jacente | |
| Réceptif | Immunisé ou rétabli d'une maladie | |
| Immunovulnérable | Immunocompétent | |
| Hôte réceptif (TS ou autre membre du personnel) |
Application inadéquate des mesures techniques, administratives et liées à l'EPI | Effectue une ERPS et choisit l'EPI approprié pour le niveau de risque |
| Hygiène des mains inadéquate | Respecte les mesures d'hygiène des mains | |
| Source infectée qui tousse et éternue activement et n'est pas capable de contenir les sécrétions | Respecte les mesures d'hygiène respiratoire | |
| Non immunisé contre la souche du virus de la grippe en circulation | Immunisé contre le virus de la grippe en circulation plus de deux semaines avant l'exposition | |
| Immunovulnérable | Immunocompétent |
Application des mesures de contrôle à la suite de l'évaluation du risque au point de service
Des précautions additionnelles doivent être prises conformément aux politiques et aux procédures de l'organisation. L'ERPS des circonstances du patient, l'environnement et la tâche à effectuer déterminent les mesures de contrôle à prendre. Les mesures de contrôle sont prises au niveau des pratiques de soins du TS et de l'EPI dans la hiérarchie des mesures de contrôle. Elles peuvent comprendre :
- hygiène des mains; le DMBA au point de service doit être disponible et utilisé (norme de soins escomptée pour tous les TS dans tous les milieux de soins)
- placement et hébergement des patients; il faut donner la priorité aux patients qui présentent un exsudat ou une diarrhée impossibles à contenir et les placer dans une chambre individuelle, ou placer un patient atteint d'une infection à transmission aérienne présumée ou confirmée dans une chambre d'isolement pour infections à transmission aérienne, avec la porte fermée
- traitement des infections actives
- sélection des compagnons de chambre en chambre commune ou pour le transport en ambulance commune (et par d'autres modes de transport, comme l'ambulance aérienne, les taxis), en tenant compte de l'état immunitaire des patients qui seront potentiellement exposés à certaines infections (p. ex. rougeole, oreillons, rubéole, varicelle)
- déplacements des patients; il faut limiter le déplacement des patients symptomatiques au sein de la zone ou de l'établissement de soins ou à l'extérieur de l'établissement, le cas échéant, pour l'étiologie microbienne présumée ou confirmée
- affectation du personnel; en tenant compte de l'état immunitaire des TS qui seront potentiellement exposés à certaines infections (p. ex. la rougeole, les oreillons, la rubéole et la varicelle)
- sélection de l'équipement de protection individuelle approprié; il faut porter l'EPI approprié pour l'infection ou la colonisation présumée ou confirmée
- nettoyage et désinfection du matériel de soins aux patients non critique et de l'environnement du patient
- gestion du linge et des déchets
- restriction de l'accès aux visiteurs, s'il y a lieu
- réévaluation de la nécessité de poursuivre ou d'abandonner les précautions additionnelles
2. Mesures de contrôle visant à réduire l'exposition des travailleurs de la santé aux agents infectieux et la transmission de ces derniers
Pratiques de base
Les pratiques de base sont un ensemble complet de mesures de PCI élaborées en vue d'une utilisation dans les soins de base dispensés à tous les patients en tout temps et dans tous les milieux de soins. Les pratiques de base visent à réduire ou à prévenir les IASS chez toutes les personnes d'un milieu de soins, y compris les patients, les TS, les visiteurs et les entrepreneurs. Les pratiques de base ont recours à différents aspects de toutes les composantes de la hiérarchie des mesures de contrôle pour contrôler l'agent infectieux ou la source infectée, protéger l'hôte réceptif et assurer l'hygiène de l'environnement.
Tous les TS (p. ex. les médecins, les infirmières, les auxiliaires médicaux, les étudiants, les bénévoles et autres) sont tenus de se conformer aux pratiques de base et d'attirer avec tact l'attention des contrevenants sur le non-respect de ces pratiques. Personne n'est dispensé de se conformer aux pratiques de base.
Les patients et les visiteurs sont tenus de se conformer aux pratiques de base dans les cas indiqués. Tous les TS sont tenus d'enseigner les principes de base aux patients et aux visiteurs (p. ex. l'hygiène des mains, le port d'un EPI).
Pratiques de base—Hygiène des mains
C'est Semmelweiss, en 1847, qui a pour la première fois observé que la désinfection des mains permettait de réduire les infections nosocomiales; depuis lors, l'efficacité de cette mesure a été maintes fois confirméeNote de bas de page 303, Note de bas de page 304. Il est avéré que l'utilisation d'un DMBA réduit les taux d'IASSNote de bas de page 217, Note de bas de page 305. L'hygiène des mains avec DMBA au point de service est la norme de soins escomptée pour tous les TS dans tous les milieux de soins.
On a établi une tendance cohérente selon laquelle une réduction des taux d'infection est associée à l'amélioration de l'hygiène des mainsNote de bas de page 305, Note de bas de page 306, Note de bas de page 307, Note de bas de page 308, Note de bas de page 309. Cependant, il est difficile de maintenir les taux améliorés d'hygiène des mains et la réduction des IASS, car les taux retombent souvent aux taux antérieurs une fois l'étude terminée et les interventions de promotion de l'hygiène des mains abandonnéesNote de bas de page 310, Note de bas de page 311. Prière de consulter les lignes directrices pour la PCI de l'ASPC intitulées Pratiques en matière d’hygiène des mains dans les milieux de soinsNote de bas de page 217 pour obtenir de plus amples renseignements.
Pratiques de base—Placement et hébergement des patients
L'hébergement des patients hospitalisés en chambres individuelles facilite les activités de PCI. Les chambres individuelles avec toilettes privées, lavabo à l'usage du patient et lavabo réservé au lavage des mains à l'usage du personnel soignant peuvent réduire les possibilités de transmission croisée entre les patients, en particulier si le patient a une mauvaise hygiène, contamine l'environnement ou ne peut pas se conformer aux mesures de PCI en raison d'une déficience physique, comportementale ou cognitiveNote de bas de page 201, Note de bas de page 202, Note de bas de page 289, Note de bas de page 290, Note de bas de page 291, Note de bas de page 292, Note de bas de page 293, Note de bas de page 294, Note de bas de page 295, Note de bas de page 296, Note de bas de page 297, Note de bas de page 298, Note de bas de page 299, Note de bas de page 300, Note de bas de page 301, Note de bas de page 302. Le TS, en consultation avec le coordonnateur des lits ou le coordonnateur de l'hébergement, ou avec des PPI, selon le cas, devrait sélectionner l'hébergement le plus approprié en fonction de l'ERPS et de l'établissement des priorités d'utilisation des chambres individuelles et des chambres d'isolement pour infections à transmission aérienne, si elles sont peu nombreuses.
Pratiques de base—Déplacements des patients
Le déplacement des patients renvoie au transfert ou le transport des patients au sein et à l'extérieur d'un établissement et aux activités des patients. Les activités et le transport des patients présentent un potentiel d'exposition aux microorganismes et de transmission de ces derniers, en raison des contacts involontaires avec d'autres patients, avec des articles de soins et les surfaces de l'environnement. Il ne faut pas transporter des patients d'une unité de soins, d'un service ou d'un établissement à l'autre à moins que cela ne soit nécessaire du point de vue médical. On devrait éviter les transferts de patients fréquents, car ils augmentent le nombre d'interactions avec le personnel et les autres patients et les possibilités de transmissionNote de bas de page 25.
Pratiques de base—Technique aseptique pour les injections, les interventions intravasculaires et les autres interventions invasives
La technique aseptique est la prévention intentionnelle du transfert de microorganismes de la surface du corps du patient à un site corporel normalement stérile ou d'une personne à une autre en maintenant le nombre de microbes à un minimum irréductible. La technique aseptique, quelquefois appelée technique stérile, consiste en mesures conçues pour rendre la peau du patient, les fournitures et les surfaces les plus exempts de microorganismes que possible. De telles pratiques sont appliquées au cours d'interventions qui exposent les sites normalement stériles du patient (p. ex. le système intravasculaire, le canal de l'épendyme, l'espace sous-dural, le tractus urinaire), de façon à les protéger contre les microorganismes. Les composantes de la technique aseptique préalables à une intervention peuvent comprendre ce qui suit : la préparation de la peau du patient à l'aide d'un antiseptique; l'hygiène des mains, de préférence par un DMBA ou, si ce produit n'est pas accessible, par un savon antimicrobien; des gants stériles, une blouse, un masque, un équipement et des draps; et le fait de maintenir un milieu stérile.
Si l'antisepsie cutanée n'est pas correctement effectuée avant l'injection de médicaments, les vaccins ou les ponctions veineuses, des infections peuvent en résulterNote de bas de page 312, Note de bas de page 313. La chlorhexidine contenue dans l'alcool inactive les microorganismes sur la peau de façon plus efficace que la plupart des autres antiseptiques; cette substance est l'antiseptique de choix pour la préparation de la peau avant l'insertion d'un cathéter veineux central et d'un cathéter de l'artère pulmonaireNote de bas de page 314, Note de bas de page 315, Note de bas de page 316, Note de bas de page 317. Les données factuelles issues de la recherche laissent entendre que des barrières aseptiques maximales (y compris un bonnet, un masque, une blouse chirurgicale stérile à longues manches, des gants stériles et un grand drap chirurgical stérile (qui couvre tout le lit) pendant l'insertion) réduisent les taux d'infection associés à l'insertion d'un cathéter veineux centralNote de bas de page 228, Note de bas de page 318, Note de bas de page 319, Note de bas de page 320, Note de bas de page 321. Comme les études publiées diffèrent du point de vue des populations de patients, de la méthodologie et des milieux de soins, des recherches plus approfondies sont nécessaires.
On a signalé l'apparition d'une méningite après une myélographie et d'autres interventions rachidiennes; elle est généralement causée par la flore respiratoire de la personne qui pratique l'interventionNote de bas de page 322, Note de bas de page 323, Note de bas de page 324, Note de bas de page 325, Note de bas de page 326, Note de bas de page 327, Note de bas de page 328, Note de bas de page 329. On a associé le fait que la personne pratiquant l'intervention ne porte pas de masque facial pendant l'interventionNote de bas de page 325, Note de bas de page 327, Note de bas de page 329, Note de bas de page 330, ou ne le porte pas correctementNote de bas de page 328, à la survenue d'infections. La technique aseptique utilisée pour les interventions stériles, comme le placement d'un cathéter ou l'injection d'une substance dans le canal de l'épendyme ou dans l'espace sous-dural (p. ex. pendant les myélogrammes, les ponctions lombaires, la chimiothérapie intrathécale et l'anesthésie rachidienne ou péridurale), comprend l'hygiène des mains par DMBA, la préparation du site grâce à un antiseptique, l'utilisation d'un masqueNote de bas de page 331, le port de gants stériles et le fait de maintenir un champ stérile.
Les draps chirurgicaux servent à prévenir le transfert de microorganismes de l'environnement au patient pendant le déroulement de l'intervention. Le port de masques empêche les microorganismes présents dans le nez et la bouche des TS de contaminer le champ stérile.
Une technique aseptique appropriée pour l'insertion des cathéters urinaires comprend un équipement stérile (p. ex. gants, draps chirurgicaux, éponges et cathéters), une solution stérile ou antiseptique pour nettoyer le méat et une pochette à usage unique de gelée lubrifiante stérile pour l'insertionNote de bas de page 31.
La technique aseptique à appliquer pour le prélèvement de médicaments ou d'autres substances stériles de tout flacon ou de tout autre contenant comprend l'hygiène des mains, l'utilisation d'alcool pour préparer le bouchon de caoutchouc ou l'orifice d'injection (attendre que l'alcool sèche), les aiguilles et seringues stériles à usage unique et la conformité avec les instructions du fabricant. On a associé la transmission des virus de l'hépatite B et de l'hépatite C et d’autres agents à la réutilisation d'aiguilles ou de seringues ayant servi à prélever des agents dans des flacons à usages multiples, à l'utilisation incorrecte de l'équipement de surveillance de la glycémie et à la réutilisation d'une aiguille et d'une seringue pour administrer des médicaments à plusieurs patientsNote de bas de page 92, Note de bas de page 167, Note de bas de page 168, Note de bas de page 169, Note de bas de page 170, Note de bas de page 171, Note de bas de page 172, Note de bas de page 173, Note de bas de page 174, Note de bas de page 332.
Les recommandations en matière de sécurité des injections sont les suivantesNote de bas de page 333 :
- Ne pas administrer des médicaments avec la même seringue à plus d'un patient, même en changeant d'aiguille
- Considérer qu'une seringue ou une aiguille est contaminée après l'avoir utilisée pour pénétrer dans une poche pour perfusion intraveineuse ou un dispositif de transfusion ou pour s'y brancher
- Ne pas pénétrer un flacon ou une poche avec une seringue ou une aiguille usagée
- Ne pas utiliser des médicaments conditionnés sous forme de flacon à usage unique pour plus d'un patient
- Dans la mesure du possible, attribuer les médicaments conditionnés sous forme de flacon à usages multiples à un seul patient
- Suivre des pratiques de PCI correctes pendant la préparation et l'administration des médicaments injectables
Pratiques de base—Équipement de protection individuelle
L'équipement de protection individuelle consiste en des protections portées par les TS pour protéger le patient contre la transmission de microorganismes et le TS contre l'exposition à des microorganismes à diffusion hématogène et à d'autres microorganismes (p. ex. les projections de gouttelettes de sang, de liquides organiques, de sécrétions ou d'excrétions des voies respiratoires ou autres). Les organisations de soins de santé sont tenues de s'assurer que les TS ont accès à un EPI approprié pour les tâches à effectuer et les soins dispensés au patient et qu'ils ont reçu une formation sur son utilisation (tel qu’il est décrit dans le rôle de l'organisation, consulter la partie A, section III, B).
Les travailleurs de la santé devraient connaître parfaitement l'utilisation et les limites de l'EPI spécifique mis à leur disposition et être capables de déterminer ce qui est nécessaire en évaluant le risque d'exposition au sang, aux liquides organiques, aux sécrétions et aux excrétions, aux muqueuses et à la peau non intacteNote de bas de page 22, Note de bas de page 219 pendant les interactions avec les patients. L'ERPS permet au TS de détecter les dangers et de sélectionner un EPI à la mesure des dangers qu'il pourrait rencontrer durant leur interaction de soins aux patients. L'EPI sélectionné devrait maximiser la protection en tenant compte de la dextérité et du confort.
Il est également important d'effectuer une ERPS pour savoir si le port d'un EPI est nécessaire, afin de ne pas accorder trop d'importance à l'EPI et d'éviter les mauvaises utilisations ou le gaspillage. Si l'on se fie trop à l'EPI, on pourrait avoir un faux sentiment de sécurité. L'utilisation et l'enlèvement inappropriés d'un EPI peuvent entraîner l'exposition accidentelle du TSNote de bas de page 334 ou du patient à des agents infectieux ou la contamination de l'environnement du patientNote de bas de page 335. On peut éviter de gaspiller un EPI en maximisant le nombre de soins cliniques dispensés à chaque entrée dans la chambre du patient.
L'efficacité de l'EPI dépend fortement de son bon usage. L'usage approprié et correct de l'EPI comprend :
- une évaluation du risque au point de service pour déterminer si un équipement de protection individuelle est nécessaire
- le recours à une technique correcte pour mettre et enlever l'EPI (consulter l'annexe X)
- le recours à une technique correcte pendant le port de l'EPI (p. ex. éviter de s'auto-contaminer)
- l'élimination de l'équipement de protection individuelle dans des récipients désignés à cet effet immédiatement après son utilisation, suivie de mesures d'hygiène des mains
Pratiques de base—Gants (consulter également l'annexe IX)
Le port de gants ne remplace pas l'hygiène des mains, mais est considéré comme une mesure de protection supplémentaire. Pour les pratiques de base, le port de gants dépend de l'ERPS du patient, de l'environnement et de l'interactionNote de bas de page 336. Les gants servent à réduire la transmission de microorganismes d'un patient à l'autre ou d'un site corporel à l'autre, ainsi qu'à réduire le risque d'exposition des TS au sang, aux liquides organiques, aux sécrétions et aux excrétions, aux muqueuses, aux plaies exsudatives et à la peau non intacte; ils sont également utilisés pour manipuler des objets ou toucher des surfaces visiblement ou potentiellement souilléesNote de bas de page 22, Note de bas de page 219, Note de bas de page 337, Note de bas de page 338. Les gants n'éliminent pas complètement la contamination des mainsNote de bas de page 337, car ces dernières peuvent être contaminées pendant le port de gants défectueux ou au cours de l'enlèvement des gantsNote de bas de page 339, Note de bas de page 340, Note de bas de page 341. Par conséquent, il faut pratiquer l’hygiène des mains après avoir ôté les gants. L'utilisation de gants pourrait donner à la personne qui les porte un faux sentiment de sécurité et se traduire par une négligence de l'hygiène des mainsNote de bas de page 342, Note de bas de page 343, Note de bas de page 344, Note de bas de page 345.
Il est important d'évaluer les gants et de choisir ceux qui sont le plus appropriés dans une situation donnée. La sélection des gants doit comprendre l'évaluation de leur durabilité pendant l'utilisation, de la rigueur et de la durée des interventions pratiquées, du potentiel d'exposition aux microorganismes infectieux ou à d'autres substances dangereuses, et de la sécurité de l'utilisateur (p. ex. allergies au latex)Note de bas de page 346. Il est également important de tenir compte de facteurs comme le confort et l'ajustement.
Les gants médicaux non stériles jetables destinés aux soins habituels aux patients sont fabriqués en nitrile, en latex ou en vinyleNote de bas de page 347. Les gants poudrés en latex ont été associés à des allergies au latexNote de bas de page 348. Les personnes qui ont une hypersensibilité de type I au caoutchouc naturel doivent porter des gants sans latex; ces derniers doivent également être portés pour soigner des patients qui ont ce type de réaction allergique au latexNote de bas de page 346.
La qualité de la protection offerte par les gants d'examen dépend de la matière dont est faite le gant, de la qualité de la production et des pressions subies pendant l'utilisationNote de bas de page 346, Note de bas de page 347. On a observé des taux de défectuosité plus élevés avec les gants en vinyle qu'avec les gants en latex ou en nitrile lors d'essais en situations cliniques simulées et réellesNote de bas de page 340, Note de bas de page 341, Note de bas de page 346, Note de bas de page 347.
L'intégrité des gants en latex peut être détériorée par l'utilisation de lotions ou de crème à base de pétroleNote de bas de page 349, Note de bas de page 350. Certains DMBA peuvent interagir avec la poudre qui reste sur les mains des TS après l'enlèvement de gants poudrés et former des particules granuleuses sur les mainsNote de bas de page 339, Note de bas de page 341. En enfilant des gants avant de se sécher les mains après avoir utilisé un DMBA, on augmente considérablement le risque de perforation des gantsNote de bas de page 351.
Il ne faut jamais nettoyer des gants à usage unique avec du savon, du gluconate de chlorhexidine ou de l'alcool en vue de les réutiliser, car le nettoyage porte atteinte à leur intégrité et ne s'est pas avéré efficace pour éliminer les microorganismes inoculésNote de bas de page 339, Note de bas de page 352, Note de bas de page 353.
L'utilisation de gants pour prévenir la transmission des agents pathogènes à diffusion hématogène est analysée dans les lignes directrices de l'ASPC en matière de PCI intitulées La prévention et la lutte contre les infections professionnelles dans le domaine de la santé Note de bas de page 219.
Pratiques de base—Blouses à longues manches et autres vêtements
Pour les pratiques de base, les travailleurs de la santé portent des blouses à longues manches, selon les indications de l'évaluation du risque, afin de protéger la peau non couverte et les vêtements pendant les interventions et les activités de soins aux patients qui risquent de les souiller ou de produire des éclaboussures ou la projection de gouttelettes de sang, de liquides organiques, de sécrétions ou d'excrétionsNote de bas de page 22, Note de bas de page 219. Les blouses devraient être munies de poignets et couvrir le TS à l'avant et l'arrière, du cou à mi-cuisse. Les blouses comprennent les blouses d'isolement (réutilisables ou jetables, imperméables aux fluides ou stériles). Le type de blouses sélectionné dépend de ce qui suit :
- le degré prévu de contact avec des substances infectieuses
- le potentiel de pénétration de la blouse par du sang et des liquides organiques (imperméabilité aux fluides lorsque l'on prévoit une forte contamination par les liquides, comme en salle d'opération et pendant la dialyse)
- le besoin de stérilité (p. ex. salle d'opération, insertion d'un cathéter central)
Rien ne prouve que le port systématique de blouses pour tous les soins aux patients a un effet positif sur la prévention des IASS, même dans les unités à haut risque (p. ex. unité de soins intensifs néonatales, USI, unité de greffe de cellules souches hématopoïétiques, unité de soins aux brûlés)Note de bas de page 354, Note de bas de page 355, Note de bas de page 356, Note de bas de page 357. Le port de blouse universel n'a aucun effet sur les taux d'IASS dans les USI néonatauxNote de bas de page 358, Note de bas de page 359 ou pédiatriquesNote de bas de page 360 ou sur les taux de colonisation des nouveau-nés dans les unités de soins postpartumNote de bas de page 361, Note de bas de page 362.
En laboratoire, la blouse de laboratoire est considérée comme un EPI. Hors laboratoire, les TS peuvent porter des vêtements comme des uniformes, des blouses de laboratoire et des combinaisons de chirurgie pour les raisons de confort, de commodité ou d'identité, mais ces vêtements ne jouent aucun rôle dans la prévention des infections (c'est-à-dire qu'on ne les considère pas comme un EPI). Pour des raisons d'esthétique et de déontologie, les vêtements et les uniformes des TS devraient être propres. On a effectué des recherches pour savoir s'il était sans danger de laver le linge des TS à domicile, et on n'a détecté aucune augmentation des taux d'infectionNote de bas de page 363.
Pratiques de base—Protection du visage
On a signalé que la transmission de l'hépatite C pouvait se produire en raison d'éclaboussures de sang dans la conjonctiveNote de bas de page 364, Note de bas de page 365 et la transmission du VIH par éclaboussures de sang sur le visageNote de bas de page 366. Une étude visant à examiner le risque de contamination des yeux des radiologues pendant les interventions vasculaires invasives a établi que 6,7 % des interventions produisent des éclaboussuresNote de bas de page 367. La protection du visage comprend les masques et la protection des yeux, les écrans faciaux ou les masques dotés de visières. Par protection des yeux, on entend les masques munis d'une protection oculaire intégrée, les lunettes de sécurité ou les écrans faciaux. On détermine s'il faut porter une protection du visage pendant les soins courants aux patients selon l'ERPS de l'interaction avec le patient et la tâche à effectuer. Les interactions qui comprennent des activités susceptibles de provoquer la toux, des éclaboussures ou la projection de gouttelettes de sang, de liquides organiques, de sécrétions ou d'excrétions, et les interventions qui pourraient exposer les muqueuses des yeux, du nez ou de la bouche justifient une protection du visageNote de bas de page 22, Note de bas de page 219.
Les masques comprennent les masques chirurgicaux et les masques opératoires; aucun masque précis ne s'est révélé supérieur aux autres en matière de protection du visage. Les masques ont plusieurs utilités : comme protection contre les éclaboussures et la projection de gouttelettesNote de bas de page 22, Note de bas de page 219; comme protection contre les sources contagieusesNote de bas de page 368, Note de bas de page 369; comme protection pendant les interventions aseptiques ou stérilesNote de bas de page 331; comme protection des hôtes réceptifs lorsqu'ils se trouvent à moins de 2 mètres de patients pour lesquels on prend des précautions contre la transmission par gouttelettesNote de bas de page 135, Note de bas de page 213, Note de bas de page 368, Note de bas de page 369, Note de bas de page 370, Note de bas de page 371, Note de bas de page 372, Note de bas de page 373, Note de bas de page 374, Note de bas de page 375, Note de bas de page 376.
Pratiques de base—Gestion des visiteurs
On devrait élaborer et mettre en œuvre des politiques relatives aux visites afin d'équilibrer le risque de transmission de maladies infectieuses et la promotion de soins axés sur le patient et la familleNote de bas de page 377. Il est prouvé que les visiteurs transmettent diverses infections, y compris la tuberculoseNote de bas de page 66, Note de bas de page 378, la coquelucheNote de bas de page 64 et les virus des voies respiratoires dans les milieux de santéNote de bas de page 46, Note de bas de page 67, Note de bas de page 379, Note de bas de page 380, Note de bas de page 381, Note de bas de page 382, Note de bas de page 383. L'exclusion des personnes qui présentent des signes et des symptômes d'infections contagieuses devrait réduire ce risque. En ce qui concerne les visites essentielles, il faut donner la consigne au visiteur atteint d'une infection de prendre des mesures pour réduire le risque de transmission (p. ex. porter un masque en cas d'infection des voies respiratoires, pratiquer l’hygiène des mains de façon appropriée, rester dans la chambre du patient, éviter les endroits publics, éviter le contact avec d'autres patients ou avec le matériel de soins aux patients).
Précautions additionnelles
Les précautions additionnelles sont prises lorsque les caractéristiques de transmission naturelle de microorganismes précis (p. ex. les microorganismes important du point de vue épidémiologique, comme C. difficile, les microorganismes résistants aux antibiotiques, la gastroentérite virale et les infections respiratoires émergentes; consulter l'annexe VI) ou lorsque les syndromes ne sont pas complètement maîtrisés par les pratiques de base. Des précautions additionnelles peuvent être nécessaires lorsque les interventions médicales augmentent artificiellement le risque de transmission d'un microorganisme donné, ou lorsque exigés par la situation clinique (p. ex. soins à un jeune enfant, adulte incontinent ou personne ayant une déficience cognitive). Les précautions additionnelles sont propres au milieu de soins (p. ex. soins de courte durée, soins ambulatoires, soins préhospitaliers, SLD et soins à domicile). Les précautions additionnelles sont généralement réparties en :
- précautions contre la transmission par contact, pour les microorganismes ayant une petite dose infectieuse ou dans les situations où l'on s'attend à une forte contamination de l'environnement du patient (consulter la liste 3)
- précautions contre la transmission par gouttelettes, pour les microorganismes qui sont transmis par grosses gouttelettes (consulter la liste 4)
- précautions contre la transmission par voie aérienne, pour les microorganismes qui sont transmis sur une longue période et une longue distance par de petites particules (consulter la liste 5)
Précautions additionnelles—Mise en œuvre et abandon des précautions additionnelles
Les précautions additionnelles devraient être prises dès que la présence d'une maladie ou de facteurs de risque est présumée ou déterminée. Il n'est pas nécessaire d'attendre la confirmation du diagnostic pour prendre des précautions additionnelles.
L'organisation est responsable de ce qui suit :
- désigner le personnel chargé au quotidien de la mise en œuvre des précautions additionnelles
- préciser les procédures de notification à suivre une fois les précautions mises en œuvre
- désigner la personne chargée de la modification ou de l'arrêt des précautions
- désigner la personne qui a la responsabilité ultime de prendre des décisions concernant les précautions, la gestion des éclosions et l'attribution des lits
Le TS est responsable de ce qui suit :
- s'assurer que des précautions additionnelles appropriées sont appliquées pour les patients
- s'assurer que les patients ne font pas l'objet de précautions additionnelles superflues
- s'assurer que les précautions sont chaque jour passées en revue, ajustées s'il y a lieu selon les nouveaux renseignements et cessées lorsqu'elles ne sont plus indiquées
Pour réduire au minimum la transmission des microorganismes, on devrait évaluer les patients pour découvrir tout signe d'infection ou d'infection potentielle au moment de l'admission (dans les milieux de soins en hôpital) ou dès la première rencontre, puis régulièrement tout au long de leur séjour, selon l'ERPS. Les résultats de l'évaluation devraient être communiqués aux autres membres du personnel qui dispensent des soins à ce patient et peuvent être documentés dans le dossier du patient. Dans le cas du patient qui est atteint ou qu'on soupçonne d'être atteint d'une maladie nécessitant des précautions additionnelles qui vont au-delà des pratiques de base, ces précautions devraient être mises en œuvre le plus tôt possible par des mécanismes déclencheurs comme le diagnostic, les symptômes de l'infection, les résultats des analyses de laboratoire et l'évaluation des facteurs de risque. Il n'est pas nécessaire d'attendre un diagnostic précis ou une confirmation microbiologique avant de mettre en œuvre des précautions additionnelles lorsque l'ERPS révèle clairement la présence d'un syndrome ou de facteurs de risque liés à une maladie potentiellement transmissible.
Tous les TS sont tenus de se conformer aux précautions additionnelles (en plus des pratiques de base) et d'attirer avec tact l'attention des contrevenants sur le non-respect de ces pratiques. Les patients et les visiteurs sont également tenus de se conformer aux précautions additionnelles dans les cas indiqués. Tous les TS sont chargés d'enseigner les principes de base des pratiques de base et des précautions additionnelles.
Précautions additionnelles—Hébergement
Lorsque le nombre de chambres individuelles est limité, c'est l'ERPS qui détermine les priorités en matière de placement des patients dans ces chambres. On accorde la priorité des chambres individuelles aux patients :
- qui doivent faire l'objet de précautions additionnellesNote de bas de page 299, Note de bas de page 300;Note de bas de page 292, Note de bas de page 301, Note de bas de page 302;
- dont on a déterminé qu'ils présentent un risque élevé de transmission de microorganismesNote de bas de page 69 (p. ex. incontinence fécaleNote de bas de page 290, Note de bas de page 291, Note de bas de page 384, sécrétions non contenues)Note de bas de page 48, Note de bas de page 385;
- dont on a déterminé qu'ils courent un risque plus élevé d'acquisition et d'effets indésirables découlant de la transmission de microorganismes (p. ex. immunosuppressionNote de bas de page 379, Note de bas de page 386, Note de bas de page 387, plaies ouvertes, sondes à demeure, séjours prolongés prévus)Note de bas de page 388;
- qui dépendent des TS pour les activités de la vie quotidienneNote de bas de page 288.
Les facteurs à prendre en considération en ce qui concerne les chambres communes (lorsqu'une chambre individuelle n'est pas disponible) comprennent ce qui suit :
- sélectionner des compagnons de chambre appropriés;
- éviter de placer les patients qui courent des risques élevés de complications s'ils deviennent infectés dans la même chambre que des patients atteints d'infections transmissibles, qui ont la diarrhée ou des plaies ouvertes;
- définir les limites de la zone d'un patient potentiellement contaminé au sein de la chambre commune;
- prévenir les risques de transmission découlant de l'usage commun de lavabos et de toilettes;
- évaluer les activités des compagnons de chambre et de leurs visiteurs.
On a réussi à contrôler la transmission de certains microorganismes en affectant une même chambre aux patients dont on sait qu'ils sont infectés par le même microorganisme (groupement en cohortes) ou en attribuant les patients non infectés à une unité ou à un service différentNote de bas de page 285, Note de bas de page 389, Note de bas de page 390, Note de bas de page 391, Note de bas de page 392, Note de bas de page 393, Note de bas de page 394. Il est difficile de déterminer les avantages que présente le groupement par cohortes pour la gestion des éclosions dues aux microorganismes résistants aux antibiotiques, y compris SARM Note de bas de page 47, Note de bas de page 390 et les ERVNote de bas de page 395, Note de bas de page 396, Note de bas de page 397, les organismes Gram négatifNote de bas de page 53, Note de bas de page 398 et des éclosions dues à d'autres agents infectieuxNote de bas de page 399, Note de bas de page 400, Note de bas de page 401, car plusieurs autres mesures de contrôle ont été mises en œuvre au cours de ces éclosions publiées.
Précautions additionnelles—Hébergement—Chambres d'isolement pour infections à transmission aérienne
Les chambres d'isolement pour infections à transmission aérienne avec ventilation par pression négative (c.-à-d. que l'air arrive dans la chambre depuis le corridor extérieur par la porte et est éliminé directement à l'extérieur du bâtiment ou filtré avant d'être remis en circulation) sont conçues pour les patients atteints d'une infection à transmission aérienne présumée ou confirmée, dont :
- la rougeole;
- la tuberculose pulmonaire (y compris la tuberculose pleuropulmonaire ou laryngienne);
- la variole, l'orthopoxvirose simienne;
- la varicelle;
- le zona disséminé.
Il faut effectuer les IMGA chez les patients atteints de tuberculose, de SRAS, de fièvre hémorragique virale et d'infections respiratoires par un agent pathogène émergent dont on ne connaît pas encore complètement la voie de transmission dans une chambre d'isolement pour infections à transmission aérienne (consulter l'annexe VI, point 4).
Dans les milieux où le nombre de chambres d'isolement est limité, les patients atteints d'une tuberculose pulmonaire contagieuse confirmée ou présumée ont la priorité. En ce qui concerne la rougeole, la varicelle et le zona disséminé, on peut évaluer le risque de transmission par rapport à la présence de patients ou de TS non immunisés. Les TS non immunisés ne devraient pas soigner des patients atteints de rougeole, de varicelle ou de zona disséminé. Les patients non immunisés ne devraient pas partager la chambre de patients atteints de rougeole, de varicelle ou de zona.
Lorsque aucune chambre d'isolement pour infections à transmission aérienne n'est disponible, le patient doit être temporairement hébergé dans une chambre individuelle avec la porte fermée, à bonne distance des patients à haut risque. Il faudrait transférer le patient à un établissement équipé de chambres d'isolement dès que possible du point de vue médical.
- Soins préhospitaliers : les patients devraient porter un masque et être transportés séparément. Pour le transport de plusieurs patients, il faudrait tenir compte du risque de transmission, tel qu'il est indiqué ci-dessus, et prendre des mesures de contrôle (p. ex. le personnel de l'ambulance devrait être limité au personnel médical nécessaire; si possible, il faudrait ouvrir une fenêtre de l'ambulance; dans la mesure du possible, la fenêtre qui sépare le chauffeur et l'espace où se trouve le patient devrait être fermée).
- Soins ambulatoires : si possible, les patients devraient remettre leur rendez-vous ou emprunter une entrée séparée. À leur arrivée, les patients devraient porter un masque, pratiquer l’hygiène des mains et être placés le plus rapidement possible dans une salle d'examen à la porte fermée.
- Milieux de soins à domicile : les membres de la famille qui n'ont pas été exposés au patient ou qui ne sont pas immunisés devraient éviter de demeurer dans le même lieu. La ventilation naturelle (p. ex. les fenêtres ouvertes) contribuera à dissiper les microorganismes de la chambre.
Précautions additionnelles—Déplacements des patients
Lorsque des précautions additionnelles sont nécessaires, les patients ne devraient quitter leur chambre que lorsqu'ils le doivent pour des raisons médicales. Il est important que les TS du lieu d'origine et ceux du lieu de destination pour le transport du client communiquent afin de s'assurer la continuité des précautions et de diminuer les temps d'attente inutiles dans les endroits publics. On devrait prendre des mesures de contrôle à la source (p. ex. demander au patient de pratiquer l’hygiène des mains avant de quitter sa chambre, de couvrir les lésions cutanées, de porter un masque).
Précautions additionnelles—Équipement de protection individuelle—Gants
Les gants sont utilisés pour soigner tous les patients pour lesquels on prend des précautions contre la transmission par contact. L'efficacité de gants portés de façon appropriée dans la prévention de la contamination des mains des TS est avérée; les gants réduisent le transfert potentiel de microorganismes provenant de patients colonisés ou infectés aux TS et d'un patient à l'autre par l'intermédiaire des mains des TSNote de bas de page 130, Note de bas de page 337, Note de bas de page 342, Note de bas de page 402, Note de bas de page 403. Un essai prospectif contrôlé portant sur l'efficacité des gants en vinyle à prévenir la transmission de C. difficile a permis d'établir une diminution considérable de l'incidence des maladies associées à C. difficile pendant la période d'intervention de six moisNote de bas de page 338. Dans une étude, une éclosion de SARM a été contrôlée grâce au port de gants lors de tout contact avec les patients et leur environnement immédiatNote de bas de page 404.
Les gants deviennent contaminés pendant leur utilisation. S'ils sont utilisés de façon inappropriée, ils peuvent entraîner la transmission de microorganismesNote de bas de page 98, Note de bas de page 343, Note de bas de page 345, Note de bas de page 405, Note de bas de page 406. On a associé la transmission de C. difficileNote de bas de page 86, de SARM et d'Acinetobacter spp.Note de bas de page 407 au fait de ne pas changer de gants entre deux patients. Le fait de ne pas changer de gants entre les activités de soins et les interventions auprès d'un même patient après être entré en contact avec des matières qui pourraient contenir des microorganismes en concentration élevée (p. ex. après avoir manipulé une sonde urinaire à demeureNote de bas de page 408, ou après l'aspiration d'un tube endotrachéal)Note de bas de page 407 peut entraîner la contamination des sites corporels propres ou de l'environnement du patientNote de bas de page 86.
Précautions additionnelles—Équipement de protection individuelle—Blouses à longues manches
Il est difficile de déterminer les avantages que présente l'utilisation de blouses à longues manches comme mesure de contrôle pour prévenir la transmission, car l'usage de blouses et des interventions multiples (p. ex. gants, renforcement de l'hygiène des mains, isolement et groupement par cohortes) sont souvent mis en œuvre de façon simultanée et il est impossible de reconnaître les avantages particuliers de chacune de ces mesuresNote de bas de page 403, Note de bas de page 409.
Les blouses sont utilisées comme précaution contre la transmission par contact si l'on prévoit un contact direct des vêtements avec le patient ou avec des surfaces contaminées de l'environnement. Bien que les blouses puissent être contaminées par des agents pathogènes potentiels après des soins administrés à un patient infecté ou colonisé (p. ex. SARMNote de bas de page 70, ERVNote de bas de page 98 et C. difficileNote de bas de page 119), rien ne prouve que les blouses ont été impliquées dans la transmission de ces agents pathogènes à d'autres personnes.
Précautions additionnelles—Équipement de protection individuelle—Protection du visage
La protection du visage comprend les masques et la protection des yeux, les écrans faciaux ou les masques dotés de visières. Il faut porter une protection du visage lorsque l'on se trouve à moins de 2 mètres d'un patient qui tousse ou qui éternue et qui est atteint d'une infection respiratoire transmissible présumée ou confirméeNote de bas de page 216, Note de bas de page 219.
Les yeux sont une porte d'entrée importante pour certains agents pathogènes. Ces derniers peuvent s'introduire directement dans l'œil par l'intermédiaire des gouttelettes respiratoires générées pendant la toux ou l'aspiration ou par auto-inoculation si l'on se touche les yeux avec des doigts contaminésNote de bas de page 48. Il a été prouvé que le port d'une protection des yeux pendant tous les soins dispensés aux enfants atteints de virus respiratoire syncytial réduit l'acquisition de cette infection par les TSNote de bas de page 410, Note de bas de page 411, probablement en empêchant les contacts entre les mains et les yeux.
Précautions additionnelles—Équipement de protection individuelle—Protection des voies respiratoires
La protection des voies respiratoires contre les infections à transmission aérienne comprend l'utilisation d'un appareil de protection respiratoire (consulter l’annexe V : glossaire), qui permet d'éviter l'inhalation de microorganismes en suspension dans l'airNote de bas de page 233. Une protection respiratoire pourrait se révéler nécessaire dans le cadre des précautions contre la transmission aérienne ou des IMGA sur certains patients. L'ERPS permet de déterminer s'il faut utiliser un appareil de protection respiratoire ou prendre des précautions contre la transmission par voie aérienne. Les facteurs à prendre en compte sont l'agent infectieux précis, l'état infectieux connu ou présumé du patient en question, l'activité de soins à effectuer, l'état immunitaire du TS et la capacité du patient à respecter les mesures d'hygiène respiratoire (consulter la partie A, section III, B, 3).
Précautions additionnelles—Gestion des visiteurs
L'état des visiteurs ne devrait pas leur faire courir le risque de tomber gravement malades s'ils contractent l'infection du patient (p. ex. un visiteur atteint d'une maladie chronique des poumons pourrait contracter un virus respiratoire, ou un visiteur non immunisé pourrait attraper la varicelle). Les visiteurs devraient prendre les précautions nécessaires pour prévenir la transmission indirecte à d'autres patients (p. ex. hygiène des mains, ne pas partager les articles personnels).
En règle générale, les visiteurs devraient avoir accès au même EPI que celui qu'utilise le personnel lorsqu'il dispense des soins directs au patient. On manque de données confirmant l'utilisation d'un EPI par les visiteurs. Il faudrait tenir compte de ce qui suit lorsque l'on demande aux visiteurs de porter un EPI :
- L'équipement de protection individuelle pourrait ne pas être nécessaire si le visiteur a pu être déjà exposé à l'infection avant l'admission.
- Le port d'un équipement de protection individuelle pourrait être pertinent si le visiteur rend visite à plusieurs patients d'un même établissement. Dans ce cas, la personne devrait changer d'EPI avant de rendre visite à un patient différent.
Précautions additionnelles—Les organismes importants du point de vue épidémiologiques qui nécessitent des précautions additionnelles comprennent les maladies suivantes (consulter également l'annexe VI) :
- C. difficile;
- certains microorganismes résistants aux antibiotiques;
- la gastroentérite virale;
- les infections respiratoires émergentes.