Rapport coût-efficacité de la prophylaxie par palivizumab pour le virus respiratoire syncytial (VRS) : Un examen systématique
Télécharger en format PDF
(1 617 Ko, 42 pages)
Organisation : Santé Canada
Date de publication : 2023-02-01
Date de publication : 1 février 2023
Sur cette page
- Conflits d'intérêts
- Abréviations
- Table des matières (sommaire)
- Sommaire
- Introduction
- Méthodologie
- Résultats
- Caractéristiques de l'étude
- Évaluation de la qualité
- Population de l'étude
- Résultats de l'étude
- Évaluations économiques dont les résultats sont exprimés en coût par AVAQ
- Évaluations économiques dont les résultats sont exprimés en coût par hospitalisation évitée
- Évaluations économiques dont les résultats sont exprimés dans d'autres ratios
- Évaluations économiques dans un contexte canadien
- Rapport coût-efficacité chez les prématurés
- Paramètres clés du modèle
- Paramètres d'influence
- Discussion
- Conclusion
- Figures et tableaux
- Figure 1. Recherche documentaire et sélection des études
- Figure 2. Résultats de l'évaluation de la qualité
- Figure 3. Rapport coût-efficacité du PVZ chez les prématurés pour lesquels le RCED était inférieur à 200 000 $ par AVAQ
- Figure 4. Paramètres les plus influents rapportés
- Tableau 1. Résumé des caractéristiques de l'étude et du modèle
- Tableau 2. Résumé du rapport coût-efficacité de l'étude (résultats non ajustés et ajustés en dollars canadiens de 2017)
- Tableau 3. Résumé des estimations du rapport coût-efficacité par état de santé et par perspective
- Tableau 4. Caractéristiques et conclusions des études sur le contexte canadien
- Documents supplémentaires
- Références
Conflits d'intérêts
Les auteurs n'ont aucun conflit d'intérêts en lien avec ce rapport à divulguer.
Abréviations
AC, âge chronologique; AG, âge gestationnel; AVAQ, année de vie ajustée par la qualité; AVG, année de vie gagnée; DBP, dysplasie bronchopulmonaire; CAD, dollar canadien; cAVAQ, coût par année de vie ajustée par la qualité; cAVG, coût par année de vie gagnée; rapport CE, rapport coût-efficacité; CPC, cardiopathie congénitale; CPCSH, cardiopathie congénitale hémodynamiquement significative; É.-U., États-Unis; FK, fibrose kystique; FR, facteur de risque; MPC, maladie pulmonaire chronique; HE, hospitalisation évitée; HVRS; hospitalisation due au virus respiratoire syncytial; RCED, rapport coût-efficacité différentiel; OCDE, Organisation de coopération et de développement économiques; PPA, parité des pouvoirs d'achat; PVZ, palivizumab; R.-U., Royaume-Uni; sAG, semaines d'âge gestationnel; SR, scénario de référence; VRS, virus respiratoire syncytial; USD, dollar américain
Table des matières (sommaire)
Cet examen systématique étudie le rapport coût-efficacité de la prophylaxie par palivizumab contre le virus respiratoire syncytial, stratifié selon le contexte et les sous-groupes de population infantile relativement à la prise de décision en matière de politique de santé.
Sommaire
Contexte : La prophylaxie par palivizumab (PVZ) est utilisée comme une immunisation passive contre le virus respiratoire syncytial (VRS). Toutefois, en raison de ses coûts d'acquisition élevés, la valeur de cette intervention n'est pas claire. L'objectif de cette étude était d'examiner systématiquement le rapport coût-efficacité de la prophylaxie par PVZ comparativement à l'absence de prophylaxie chez les nourrissons de moins de 24 mois.
Méthodologie : L'examen systématique a suivi les lignes directrices PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses). Trois bases de données ont été consultées : Medline, Embase et Cochrane Library pour les termes relatifs au VRS, au PVZ, au rapport coût-efficacité, à l'économie de la santé et aux évaluations économiques. Ont été incluses les évaluations économiques (p. ex., les analyses coût-avantage, coût-efficacité et coût-utilité) réalisées dans les pays de l'Organisation de coopération et de développement économiques et publiées entre 2000 et 2018. L'évaluation de la qualité a été réalisée à l'aide de la liste de contrôle de l'institut Joanna Briggs pour les évaluations économiques. Les coûts ont été ajustés en dollars canadiens de 2017, en utilisant la parité des pouvoirs d'achat et les taux d'inflation. Les résultats ont été stratifiés en fonction des résultats utilisés, de la perspective de l'étude et d'autres facteurs de risque (p. ex., prématurité, maladie pulmonaire chronique et cardiopathie congénitale) pour le VRS. Les paramètres ayant une incidence sur le rapport coût-efficacité ont été résumés.
Résultats : Au total, 28 évaluations économiques répondaient aux critères d'inclusion, dont 20 étaient des analyses coût-utilité et 8 des analyses coût-efficacité. La plupart des études ont été menées aux États-Unis (n=6), au Canada (n=5), aux Pays-Bas (n=3), au Royaume-Uni (n=3) et en Espagne (n=3). Dans l'ensemble, les études incluses étaient considérées comme étant de bonne à haute qualité; 23 études ont répondu à plus de 80 % des critères de la liste de contrôle. La prophylaxie par PVZ a varié d'une stratégie dominante (c.-à-d. moins coûteuse et plus efficace) à un rapport coût-efficacité différentiel de 2 975 489 $/année de vie ajustée par la qualité selon le cadre de l'étude, la perspective, la population (facteurs de risque, nombre de semaines d'âge gestationnel à la naissance) et les principaux paramètres de saisie du modèle, comme la réduction des hospitalisations dues au VRS (39 %-96 %), la mortalité liée au VRS (1 %-8,1 %) et le coût du PVZ (1 099 $-2 198 $ par flacon de 100 mg). Du point de vue du payeur, le rapport coût-efficacité de la prophylaxie par PVZ a été estimé pour les nourrissons nés prématurément à 29 à 35 semaines d'âge gestationnel (RCED : 6 216 $/année de vie ajustée par la qualité à 938 623 $/année de vie ajustée par la qualité, n=21), 82 % des estimations étant inférieures à 50 000 $/année de vie ajustée par la qualité. Les trois principaux paramètres influents signalés étaient : la réduction des taux d'hospitalisation due au VRS, le coût du PVZ et le taux d'actualisation.
Conclusions : Les résultats du rapport coût-efficacité du PVZ en tant que prophylaxie du VRS étaient hétérogènes d'une étude à l'autre, allant d'un rapport dominant (c.-à-d. moins coûteux et plus efficace) à un rapport très peu efficace. Les résultats ont varié en fonction du contexte de l'étude, de la population d'intérêt, de l'épidémiologie locale du VRS et de la structure des soins de santé, ainsi que des paramètres clés du modèle, comme la réduction des taux d'hospitalisation, les coûts d'acquisition du VRS, les schémas posologiques et l'utilisation des flacons. Le PVZ peut être considéré comme étant rentable dans des sous-groupes précis : les nourrissons atteints de dysplasie broncho-pulmonaire/maladie pulmonaire chronique, les nourrissons atteints de cardiopathie congénitale, les nourrissons à terme issus de communautés éloignées précises présentant des taux de base élevés d'hospitalisation due au VRS, et les prématurés avec ou sans complications pulmonaires. Aucune tendance générale n'a été détectée entre les seuils d'âge gestationnel et les résultats du rapport coût-efficacité. Aucune tendance n'a été observée non plus lorsqu'elle a été stratifiée par perspective.
Introduction
Le virus respiratoire syncytial (VRS) est la cause la plus fréquente d'infections des voies respiratoires inférieures chez les nourrissons et les jeunes enfants au monde.Note de bas de page 1 Il s'agit d'un virus omniprésent que près de 100 % des nourrissons contracteront dans les 2 ans suivant leur naissance.Note de bas de page 2Note de bas de page 3Note de bas de page 4 Le VRS est une infection respiratoire saisonnière qui constitue une cause importante de morbidité et de mortalité. On estime que le virus est à l'origine de 90 % ou moins des hospitalisations pédiatriques attribuables à la bronchiolite et de 50 % ou moins des hospitalisations pédiatriques attribuables à la pneumonie.Note de bas de page 1Note de bas de page 5 Les facteurs de risque (FR) de VRS sévère chez les nourrissons sont les suivants : naissance prématurée, cardiopathie congénitale (CPC), dysplasie bronchopulmonaire (DBP)/maladie pulmonaire chronique (MPC), fibrose kystique (FK), syndrome de Down et affaiblissement du système immunitaire.Note de bas de page 6Note de bas de page 7Note de bas de page 8
Bien qu'il n'existe actuellement aucun vaccin pour prévenir l'infection par le VRS, une prophylaxie passive est disponible depuis 1998 avec le palivizumab (PVZ). Note de bas de page 9 Le PVZ est un anticorps monoclonal murin humanisé, administré mensuellement par injection intramusculaire, et a montré une réduction significative du taux global d'hospitalisation due au VRS (HVRS). Note de bas de page 10 Toutefois, en raison de ses coûts d'acquisition élevés, le rapport coût-efficacité (CE) de cette intervention a fait l'objet de nombreux débats. Depuis l'année 2000, 8 examens ont résumés le rapport CE du PVZ, dont la moitié a été réalisée il y a plus de 10 ans.Note de bas de page 11Note de bas de page 12Note de bas de page 13Note de bas de page 14 Une étude récente d'Andabaka et al. en 2013 a signalé que les résultats de l'évaluation économique sont incohérents d'une étude à l'autre, allant d'un rapport CE élevé à un rapport CE nul selon le scénario.Note de bas de page 15
L'objectif de cette étude était de fournir une mise à jour sur le rapport CE de l'immunisation passive par PVZ pour la prévention du VRS chez les nourrissons et les enfants de 24 mois ou moins et, dans la mesure du possible, de stratifier les résultats par population à risque afin d'éclairer les décisions politiques pour ces groupes. Les évaluations économiques réalisées dans les pays à revenu élevé de l'Organisation de coopération et de développement économiques (OCDE) après l'année 2000 ont été incluses afin de limiter l'hétérogénéité de la santé de base de la population, des systèmes de santé et de la qualité des soins. Cet examen fournit une mise à jour indispensable pour soutenir la prise de décision en matière de politique de santé concernant la prophylaxie par PVZ, en mettant particulièrement l'accent sur les résultats du rapport CE en fonction de l'âge gestationnel (AG) à la naissance pour les prématurés, qui a toujours constitué un domaine d'incertitude clinique et politique.Note de bas de page 16Note de bas de page 17Note de bas de page 18
Méthodologie
Cet examen systématique a été réalisé pour étayer les recommandations du Comité consultatif national de l'immunisation (CCNI) fondées sur des données probantes concernant la prophylaxie par PVZ du VRS, qui sont présentées dans la déclaration du CCNI intitulée « Utilisation recommandée du palivizumab pour réduire les complications de l'infection par le virus respiratoire syncytial (VRS) chez les nourrissons » publiée le 1er juin 2022. L'examen systématique original a été publié dans le Journal of Pediatrics en 2019 Note de bas de page 19. Aux fins du présent supplément du CCNI, des changements ont été apportés au rapport et à la discussion de l'examen original pour répondre aux besoins de la prise de décision du Comité, y compris la monnaie indiquée en dollars canadiens (CAD), une section sur les études canadiennes, d'autres sous-groupes indiqués et des commentaires supplémentaires.
Stratégie de recherche
L'examen systématique a suivi les lignes directrices PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses) (Annexe 1).Note de bas de page 20 La stratégie de recherche a été élaborée avec un bibliothécaire de l'Agence de la santé publique du Canada (LG). La recherche de la littérature scientifique a porté sur des études en anglais et en français publiées dans 3 bases de données électroniques : Medline et E-pub Ahead of Print, In-Process & Other Non-Indexed Citations (interface Ovid), Embase (interface Ovid) et la Cochrane Library, qui comprenait la Health Technology Assessment Database (HTA), la National Health Service Economic Evaluation Database (NHS EED) et la Database of Abstracts of Reviews of Effects (DARE). La recherche a utilisé des rubriques de sujets médicaux et des mots-clés liés aux concepts suivants : virus respiratoire syncytial, palivizumab, évaluations économiques et rapport CE. La stratégie de recherche primaire a été élaborée dans Medline et adaptée à d'autres bases de données pour tenir compte du vocabulaire et des fonctionnalités propres à chaque base. Une liste complète des termes de recherche et la stratégie de recherche complète pour Medline sont résumées dans l'Annexe 2. Les listes de référence des articles pertinents et des examens systématiques ont été consultées manuellement.
Critères d'admissibilité
Le protocole et les critères d'admissibilité des études sont publiés sur PROSPERO (CRD42018104977). Ont été incluses les évaluations économiques complètes (p. ex., analyse coût-avantages, analyse coût-efficacité et analyse coût-utilité) comparant la prophylaxie par PVZ contre le VRS à tout comparateur (p. ex., en l'absence de prophylaxie) pour les nourrissons âgés de 24 mois ou moins, selon les lignes directrices actuelles du CCNI du Canada. Note de bas de page 21 Les évaluations économiques ont été incluses si elles ont été menées dans les pays de l'OCDE entre 2000 et 2018 (date à laquelle l'examen a été réalisé), et ont rapporté des résultats liés à un ratio différentiel de coût par unité d'effet (p. ex., coût par année de vie ajustée par la qualité [cAVAQ], coût par cas évité, coût par année de vie gagnée [cAVG] et ratio coût-avantages). Les études de minimisation des coûts, les études sur le coût de la maladie et les analyses d'impact budgétaire ont été exclues. Ont également été exclues les études réalisées hors des pays de l'OCDE, les études publiées dans une langue autre que l'anglais ou le français, et les études publiées avant l'année 2000.
Extraction et analyse des données
Tous les niveaux de sélection, d'extraction des données et d'évaluation de la qualité ont été effectués en double. Les conflits ont été discutés et résolus par consensus. L'extraction des données a été guidée par CHEERS (Consolidated Health Economics Evaluation and Reporting Statement). Note de bas de page 22 Les données suivantes ont été recueillies : caractéristiques de l'étude (année de publication, pays, conception de l'étude, perspective de l'étude, horizon temporel, actualisation, résultats primaires et secondaires, utilisation de seuils coût/efficacité, sources de financement), caractéristiques de la population étudiée (tranche d'âge, AG, états de santé, contexte), paramètres clés (incidence du VRS/taux d'hospitalisation, taux de mortalité, séquelles, coût du PVZ, nombre de doses) et résultats (rapports coût-efficacité différentiels [RCED], scénarios de référence [SR], analyses de scénarios, type d'analyse de sensibilité et paramètres influents). La qualité des études incluses a été évaluée à l'aide de la liste de contrôle d'évaluation critique des évaluations économiques de l'institut Joanna Briggs (JBI). Note de bas de page 23 Une étude était de « grande qualité » si elle répondait à plus de 80 % des critères de la liste de contrôle du JBI. Note de bas de page 24 La liste de contrôle de l'Organisation mondiale de la santé destinée aux programmes de vaccination pour apprécier les évaluations économiques n'a pas été utilisée, car le PVZ n'est pas considéré comme un vaccin.
Les caractéristiques de l'étude et de la population ont été résumées de manière descriptive. Les résultats CE ont été ajustés en CAD de 2017 en utilisant les taux de parité des pouvoirs d'achat (PPA) de l'OCDE Note de bas de page 25 et des taux d'inflation de la Banque du Canada. Les RCED non ajustés et ajustés ont été récapitulés. Dans ce supplément, la devise n'a pas été actualisée jusqu'en 2022 afin de conserver les prix sur lesquels le CCNI avait délibéré. Des analyses de sous-groupes ont été réalisées pour résumer le rapport CE des études menées d'un point de vue canadien, et des études faisant état du rapport CE en coûts/AVAQ pour les prématurés. Pour les études incluant des prématurés, les RCED ont été stratifiés en fonction de l'AG à la naissance (semaines) et représentés graphiquement pour indiquer visuellement la dispersion des estimations de ces RCED et les éventuelles tendances liées à l'AG. Le nombre d'estimations et la proportion d'entre elles qui sont rentables à différents seuils ont été résumés. La méta-analyse du rapport CE n'était pas appropriée en raison de l'hétérogénéité du cadre de l'étude, des conceptions de modèles, des paramètres utilisés, de la population et de la perspective adoptée dans les études.
Résultats
Caractéristiques de l'étude
La recherche documentaire systématique a permis de cibler 237 enregistrements uniques dont 30 répondaient aux critères d'admissibilité et ont été inclus dans cet examen (Figure 1).Note de bas de page 14 Note de bas de page 26Note de bas de page 27 Note de bas de page 28Note de bas de page 29Note de bas de page 30Note de bas de page 31Note de bas de page 32Note de bas de page 33Note de bas de page 34Note de bas de page 35Note de bas de page 36Note de bas de page 37Note de bas de page 38Note de bas de page 39Note de bas de page 40Note de bas de page 41Note de bas de page 42Note de bas de page 43Note de bas de page 44Note de bas de page 45Note de bas de page 46Note de bas de page 48Note de bas de page 49Note de bas de page 9Note de bas de page 50Note de bas de page 51Note de bas de page 52Note de bas de page 53Note de bas de page 54 Les conclusions de 2 étudesNote de bas de page 33Note de bas de page 53 ont été mises à jour en utilisant des données plus récentes;Note de bas de page 34Note de bas de page 41 par conséquent, seules les études les plus récentes ont été incluses dans cet examen. Les 28 études incluses ont été publiées entre 2000 et 2018, la plupart ayant été menées aux États-Unis (É.-U.) (n=6), au Canada (n=5), aux Pays-Bas (n=3), au Royaume-Uni (R.-U.) (n=3) et en Espagne (n=3). Le reste des études ont été menées dans les pays suivants : l'Autriche (n=2), l'Allemagne (n=2), l'Italie (n=1), le Mexique (n=1), la Nouvelle-Zélande (n=1) et la Suède (n=1). Les caractéristiques des études sont résumées dans le Tableau 1.
Parmi les 28 évaluations économiques (20 analyses coût-utilité, 8 analyses CE), 23 études ont utilisé des modèles d'arbre de décision, 4 ont utilisé des modèles de cohorte de Markov et une a réalisé une microsimulation. Deux évaluations économiques se sont appuyées sur un essai clinique et les autres ont été considérées comme étant axées sur un modèle. Toutes les études ont effectué une analyse de sensibilité déterministe; 15 études ont effectué des analyses de sensibilité probabiliste.
Évaluation de la qualité
La plupart des études (83 %) ont répondu à plus de 80 % des critères de la liste de contrôle d'évaluation de la qualité du JBI (Annexe 3). Les 2 éléments de la liste de contrôle qui ont été les moins respectés étaient les suivants : (1) les résultats de l'étude comprenaient tous les sujets de préoccupation des utilisateurs (39 %); et 2) tous les coûts et résultats pertinents étaient déterminés (75 %). Dans l'ensemble, les études incluses dans cet examen ont été considérées comme étant de qualité relativement élevée (Figure 2).
III.3
Dans 14 études, l'âge chronologique (AC) du patient était explicitement indiqué comme étant inférieur à 24 mois, tandis que les 14 autres études devaient évaluer le rapport CE du PVZ chez les nourrissons de moins de 24 mois sur la base des lignes directrices de leur pays respectif sur l'utilisation du PVZ. Les populations de nourrissons à haut risque ont souvent été étudiées et, dans certains cas, se chevauchaient : prématurés (35 semaines ou moins d'âge gestationnel [sAG]) (n=19), DBP ou MPC (n=13), CPC (n=11) et autres FR (n=6).
Résultats de l'étude
Les analyses de SR ont été menées presque également du point de vue sociétal (n=13) ou du point de vue du payeur du système de santé (n=15). Huit des 15 études portant sur la perspective du payeur ont effectué des analyses supplémentaires d'un point de vue sociétal. L'horizon temporel s'étendait de 6 mois à vie, et une étudeNote de bas de page 50 n'a pas indiqué d'horizon temporel (Tableau 1). Les taux d'actualisation se situaient entre 3 % et 5 %; 5 études n'ont pas procédé à une actualisation en raison d'un horizon temporel d'un an ou moinsNote de bas de page 26Note de bas de page 35Note de bas de page 36 Note de bas de page 47Note de bas de page 48 et 3 études n'ont pas indiqué de taux d'actualisation.Note de bas de page 43Note de bas de page 50Note de bas de page 51 La majorité des études étaient commanditées par l'industrie (n=17, 61 %). Le rapport CE a été présenté sous forme de RCED, principalement représenté par le coût différentiel par AVAQ supplémentaire (n=20) et le coût par hospitalisation évitée (cHE) (n=6). Dans la suite de cet examen, les résultats sont présentés sous forme de RCED ajustés (CAD de 2017); les RCED originaux non ajustés sont résumés dans le Tableau 2.
Évaluations économiques dont les résultats sont exprimés en coût par AVAQ
Pour les études faisant état d'un rapport CE différentiel par unité d'AVAQ, le Tableau 3 résume le nombre d'estimations, les fourchettes de RCED et la proportion d'estimations sous les seuils sélectionnés de 50 000 $/AVAQ à 200 000 $/AVAQ, stratifiés par sous-groupes de population et perspective d'étude. Du point de vue du payeur du système de santé, il y avait 22 estimations variables du rapport CE pour les prématurés, se situant entre 6 216 $/AVAQ et 938 623 $/AVAQ.Note de bas de page 14Note de bas de page 29Note de bas de page 30Note de bas de page 31Note de bas de page 34Note de bas de page 38Note de bas de page 39Note de bas de page 41Note de bas de page 49 Les sous-groupes présentant le nombre d'estimations le plus élevé sont les prématurés présentant des FR (n=14)Note de bas de page 27Note de bas de page 39Note de bas de page 41Note de bas de page 42 où le RCED était compris entre 215 $/AVAQ et 205 563 $/AVAQ, les nourrissons atteints de CPC (n=10)14 29 31 32 34 37 où le RCED se situait entre 11 668 $/AVAQ et 164 946 $/AVAQ, et les nourrissons atteints de DBP/MPC (n=6)Note de bas de page 29Note de bas de page 31Note de bas de page 34Note de bas de page 37Note de bas de page 49 où le RCED se situait entre 4 786 $/AVAQ et 46 821 $/AVAQ. Au seuil de 100 000 $/AVAQ, 86 % des estimations pour les prématurés, 86 % des estimations pour les prématurés ayant des FR, 90 % des estimations pour les nourrissons atteints de CPC et 100 % des estimations pour les nourrissons atteints de DBP/MPC ont été considérées comme étant rentables. Les autres FR pris en compte chez les prématurés étaient l'AC au début de la saison du VRS, les frères et sœurs d'âge scolaire, la fréquentation d'une garderie, le tabagisme pendant la grossesse, le sexe masculin et la FK (chez les enfants nés à terme uniquement).Note de bas de page 27Note de bas de page 39Note de bas de page 41Note de bas de page 44Note de bas de page 54 D'un point de vue sociétal, la prophylaxie par PVZ a été considérée comme une stratégie dominante (c.-à-d. moins coûteuse et plus efficace) dans certains cas pour les prématurés,Note de bas de page 30Note de bas de page 44Note de bas de page 54les nourrissons à terme (avec ou sans autres FR)Note de bas de page 42 et les nourrissons atteints de CPC.Note de bas de page 31
Évaluations économiques dont les résultats sont exprimés en coût par hospitalisation évitée
Six (6) études ont indiqué le rapport CE en tant que cHE,Note de bas de page 14Note de bas de page 26Note de bas de page 35Note de bas de page 36Note de bas de page 43Note de bas de page 50 dont 3 étaient financées par l'industrie.Note de bas de page 26Note de bas de page 36Note de bas de page 43 L'étude de Banerji et coll. a porté sur des nourrissons nés à terme et en santé du point de vue du payeur, dans différentes régions de l'Arctique canadien, et a comparé 2 scénarios de prophylaxie par PVZ pour les nourrissons âgés de moins de 6 mois. Le RCED pour la prophylaxie par le PVZ allait d'une valeur dominante (dans des régions arctiques spécifiques) à 593 250 $/HE dans les Territoires du Nord-Ouest.Note de bas de page 26 Toujours du point de vue du payeur, l'étude de Hampp et al. a été menée en Floride (É.-U.) et a étudié le rapport CE chez les prématurés (moins de 32 sAG) et les enfants à terme atteints de CPC, de MPC et d'une combinaison des 3 FR. Les RCED se situaient entre 413 127 $/HE (prématurés) et 2 924 911 $/HE (nourrissons à terme en bonne santé sans MPC ni CPC).Note de bas de page 50
D'un point de vue sociétal, l'étude réalisée par Rietveld et al. en 2010 dans le sud-ouest des Pays-Bas a étudié des prématurés (de moins de 28 sAG) présentant des FR supplémentaires (sexe masculin, poids de naissance de moins de 2 500 grammes et DBP). Le RCED se situait entre 24 875 $/HE et 1 572 268 $/HE selon le mois de la prophylaxie. La prophylaxie par PVZ a présenté le RCED le plus faible au cours du mois de décembre, tandis que le mois d'octobre a révélé le RCED le plus élevé (indiquant un mauvais rapport qualité-prix). Cette étude a recommandé une politique d'immunisation restreinte sur la base de ses résultats.Note de bas de page 35 Roeckl-Wiedmann et al. ont mené en 2003 une étude dans le sud de l'Allemagne sur des prématurés (moins de 35 sAG) présentant des FR supplémentaires. Les RCED se situaient entre 11 821 $/HE et 364 462 $/HE pour les prématurés atteints de MPC et les prématurés ayant des FR (garçon, absence de MPC, absence de frères et sœurs à l'école), respectivement. Cette étude a également recommandé une utilisation restreinte du PVZ chez les prématurés atteints de MPC.Note de bas de page 36 En Nouvelle-Zélande, Vogel et al. ont étudié des prématurés (moins de 28 sAG, 29-31 sAG) et des nourrissons atteints de MPC. Le RCED se situait entre 33 376 $/HE pour les prématurés sortis de l'hôpital sous oxygène et 193 859 $/HE pour les prématurés (29-31 sAG) atteints de MPC. Les auteurs ont conclu que l'intervention était plus rentable pour les prématurés sortis de l'hôpital sous oxygène, suivis des prématurés de 28 sAG ou moins.Note de bas de page 43
Évaluations économiques dont les résultats sont exprimés dans d'autres ratios
Trois études ont fait état du rapport CE de la prophylaxie par PVZ dans d'autres unités : coût pour éviter un jour d'hospitalisation,Note de bas de page 51 cAVGNote de bas de page 52 et coût par épisode d'infection par le VRS évité.47 Deux des 3 études ont réalisé des analyses dans une perspective sociétale.Note de bas de page 51Note de bas de page 52 Harris et al. ont mené une évaluation économique sur les nourrissons à terme atteints de CPC dans l'Ouest canadien. Le RCED du SR était de 18 155 $ par jour d'HE.Note de bas de page 51 Hascoet et al. ont étudié des prématurés (moins de 32 sAG) atteints de DBP et des nourrissons présentant une CPCHS en France. Le RCED du SR était de 43 856 $/AVG et de 33 450 $/AVG pour les prématurés atteints de DBP et les prématurés atteints de CPC, respectivement. À l'origine, cette étude a utilisé un seuil de rentabilité (non ajusté) de 45 000 euros/AVG et a considéré que la prophylaxie était rentable pour les 2 sous-groupes en France.Note de bas de page 52 Enfin, une étude de Lofland et al. a étudié les prématurés atteints de MPC aux É.-U. Leur modèle s'est servi d'une réduction de l'incidence de l'infection par le VRS au lieu d'une approche de réduction des hospitalisations, allant de 50 % (66 494 $ par épisode d'infection par le VRS évité) à 83 % de réduction, où la prophylaxie par le PVZ a été considérée comme une stratégie dominante (c.-à-d. moins coûteuse et plus efficace).Note de bas de page 47
Évaluations économiques dans un contexte canadien
Dans un contexte canadien, 5 études ont été incluses dans cet examen.Note de bas de page 26 Note de bas de page 27Note de bas de page 41Note de bas de page 42Note de bas de page 51 Trois études ont examiné le rapport CE du PVZ chez les nourrissons nés à terme (une dont les sujets sont atteints de FK,Note de bas de page 27 2 menées dans l'Arctique canadien)Note de bas de page 26Note de bas de page 42, une chez les prématurés 41 et une autre dernière chez les nourrissons atteints de CPC.51 La plupart des études ont utilisé un horizon à vie (60 %), ont présenté les résultats du point de vue du payeur du système de santé (80 %), en unités de coût/AVAQ (60 %), ont effectué une analyse de scénario (100 %) et une analyse de sensibilité déterministe (100 %). L'étude sur les enfants nés à terme et atteints de FK de McGirr et al. était la seule à ne pas être financée par l'industrie.Note de bas de page 27
Ces études supposent l'administration de 4,5 à 6 doses de PVZ par saison de VRS à un coût de 1 599 à 1 718 $ (CAD de 2017) par 100 mg de PVZ. L'efficacité réelle du PVZ a été mesurée par la réduction des HVRS, qui se situait entre 42 % et 96 %. Les taux de mortalité n'ont été incorporés que dans 2 modèles, à 1 % et 8,1 %.Note de bas de page 41Note de bas de page 42 Les séquelles ont été intégrées dans 2 modèles (l'un lié au VRS, l'autre à la FK).Note de bas de page 27Note de bas de page 41 Les caractéristiques et les conclusions de l'étude sont résumées dans le Tableau 4.
Dans l'ensemble, 4 des 5 études ont conclu que l'utilisation de la vaccination passive par PVZ était rentable en fonction de leurs modèles et de la population cible.Note de bas de page 26Note de bas de page 41Note de bas de page 42Note de bas de page 51 Tam et coll. ont considéré que le PVZ était rentable pour tous les nourrissons de l'île de Baffin âgés de moins d'un an d'AC (46 151 $/AVAQ), les nourrissons à haut risque de VRS (391 $/AVAQ), les nourrissons des régions éloignées (28 965 $/AVAQ), les nourrissons de moins de 6 mois des régions éloignées ou les régions éloignées présentant des taux élevés de VRS (dominant – c.-à-d. moins coûteux et plus efficace). Toutefois, par rapport à un seuil de 100 000 $/AVAQ, il n'était pas rentable pour les nourrissons de moins de 6 mois ou les nourrissons de moins d'un an résidant à Iqaluit.Note de bas de page 42 De même, Banerji et al. ont conclu que les programmes PVZ qu'ils proposent seraient rentables dans certaines régions arctiques, mais pas dans toutes. Les 2 études attribuent la probabilité de ces résultats aux coûts élevés des hospitalisations dans ces régions.Note de bas de page 26Note de bas de page 42 Du point de vue du payeur, le PVZ a été considéré comme étant rentable pour les prématurés (35 119 $/AVAQ),Note de bas de page 41 tandis que du point de vue sociétal, le PVZ a donné un RCED de 18 155 $/jour d'HE dans l'étude de Harris et al. Bien qu'aucun seuil de rentabilité n'ait été utilisé, Harris et al. ont conclu que la prophylaxie par PVZ était probablement rentable.Note de bas de page 51 Il a été déterminé que le PVZ pour les nourrissons à haut risque atteints de FK n'était probablement pas rentable (167 107 $/AVAQ).Note de bas de page 27
Les paramètres les plus influents dans les 5 études canadiennes étaient les suivants : les taux d'HVRS,Note de bas de page 26Note de bas de page 42 le coût du PVZNote de bas de page 27Note de bas de page 51 et le coût des hospitalisations26 42 qui comprend les frais médicaux d'hospitalisation et les frais de transport vers le centre médical.
Rapport coût-efficacité chez les prématurés
Le rapport CE de la prophylaxie par PVZ comparativement à l'absence de prophylaxie par PVZ était très variable. Selon certaines études, le PVZ est une stratégie dominante (c.-à-d. moins coûteuse et plus efficace que l'absence de PVZ), tandis qu'une étude a révélé un RCED de 2 975 489 $/AVAQ chez les prématurés. Comme les études ont estimé le rapport CE pour des fourchettes variables de sAG, toutes les estimations n'ont pas pu être regroupées en intervalles prédéfinis. Par exemple, les estimations de moins de 29 sAG n'ont pas été regroupées sous les estimations de moins de 32 sAG, car la répartition des sAG dans chaque groupe de prématurés ne pouvait pas être déduite ou raisonnablement supposée. Du point de vue du payeur, le RCED de la prophylaxie par PVZ chez les nourrissons nés à moins de 29 sAG (n=3) se situait entre 6 216 $/AVAQ et 24 009 $/AVAQ.Note de bas de page 37Note de bas de page 38 Pour les nourrissons nés à 29 à 32 sAG, le RCED (n=3) se situait entre 9 989 $/AVAQ et 58 872 $/AVAQ.Note de bas de page 37 Note de bas de page 38 À moins de 32 sAG et à moins de 33 sAG, 2 estimations (12 710 $/AVAQ à 25 065 $/AVAQ)30 et 3 estimations (16 434 $/AVAQ à 42 730 $/AVAQ) ont été établies, respectivement.Note de bas de page 34Note de bas de page 49 Dans la fourchette de 32 à 35 sAG (qui comprend 2 estimations à 32-35 sAG et 4 estimations à 33-35 sAG), il y avait 6 estimations de RCED pour les prématurés (26 170 $/AVAQ à 919 073 $/AVAQ),Note de bas de page 34Note de bas de page 37Note de bas de page 39Note de bas de page 41Note de bas de page 49 et 14 estimations de RCED pour les prématurés présentant des FR supplémentaires (215 $/AVAQ à 205 563 $/AVAQ).Note de bas de page 39Note de bas de page 41 Pour les prématurés nés à moins de 35 sAG, il y avait 5 estimations entre 30 650 $/AVAQ et 938 623 $/AVAQ.Note de bas de page 14Note de bas de page 29Note de bas de page 31Note de bas de page 34 Dans les analyses de sous-groupes de prématurés nés à moins de 35 sAG et souffrant de DBP/MPC, 4 estimations se situaient entre 15 202 $/AVAQ et 131 874 $/AVAQ.Note de bas de page 14Note de bas de page 29Note de bas de page 31Note de bas de page 49
D'un point de vue sociétal, les estimations concernant les prématurés nés à 26-28 sAG ont été entièrement extraites de El-Hassan et al. dont les RCED étaient compris entre 165 301 $/AVAQ et 2 406 619 $/AVAQ.Note de bas de page 46 Pour les prématurés nés à moins de 29 sAG, il y avait 5 estimations de RCED entre 22 765 $/AVAQ et 1 359 641 $/AVAQ.Note de bas de page 28 Le rapport CE du PVZ d'un point de vue sociétal variait d'une étude à l'autre pour les prématurés nés entre 29 et 35 sAG dont les estimations de RCED étaient comprises entre 449 264 $/AVAQ et 1 083 976 $/AVAQ (29-30 sAG),Note de bas de page 46 étant une stratégie dominante (c.-à-d. moins coûteuse et plus efficace à moins de 32 sAG),Note de bas de page 30Note de bas de page 44Note de bas de page 54 32 390 $/AVAQ et 338 823 $/AVAQ (32-35 sAG)39 48 et 25 678 $/AVAQ et 983 064 $/AVAQ (moins de 35 sAG).Note de bas de page 14Note de bas de page 34 Chez les prématurés (moins de 35 sAG) présentant des complications pulmonaires, 3 études ont fait état d'estimations distinctes de RCED entre 18 717 $/AVAQ et 138 282 $/AVAQ.Note de bas de page 14Note de bas de page 29Note de bas de page 31 Six estimations ont été rapportées pour les prématurés présentant des FR entre 21 931 $/AVAQ et 635 172 $/AVAQ (21 931 $/AVAQ à 61 229 $/AVAQ pour 2 estimations de 32-34 sAG, 52 299 $/AVAQ à 635 172 $/AVAQ pour 4 estimations de 32-35 sAG).Note de bas de page 44Note de bas de page 54
Les RCED ont été stratifiés et tracés pour la prophylaxie par le PVZ exprimés en coût/AVAQ chez les prématurés selon les sAG. La Figure 3 présente 57 des 72 RCED estimés, stratifiés selon la perspective de l'étude, qui ont été évalués à moins de 200 000 $/AVAQ.Note de bas de page 14Note de bas de page 28Note de bas de page 29Note de bas de page 30Note de bas de page 31Note de bas de page 33Note de bas de page 34Note de bas de page 37Note de bas de page 38Note de bas de page 39Note de bas de page 41Note de bas de page 44Note de bas de page 46Note de bas de page 49Note de bas de page 53Note de bas de page 54Dans la Figure 3, 50 des 56 (89 %) estimations de RCED pour les prématurés (avec ou sans autres problèmes de santé) étaient inférieures au seuil de 100 000 $/AVAQ. Parmi les 16 estimations de RCED exclues de la Figure 3, 8 (soit la moitié de toutes les estimations) provenaient d'une seule étude d'El-Hassan et al.Note de bas de page 46 tandis que les autres étaient des estimations uniques provenant d'autres études.Note de bas de page 28 Note de bas de page 37Note de bas de page 41Note de bas de page 44Note de bas de page 48Note de bas de page 54
Paramètres clés du modèle
La réduction de l'HVRS utilisée dans les modèles variait entre 39 % pour les nourrissons atteints de MPC au R.-U.Note de bas de page 37 et 96 % chez les nourrissons en bonne santé dans un contexte arctique canadien.26 La mortalité a été signalée dans 19 études, allant de 1 %Note de bas de page 42Note de bas de page 52 et 8,11 %Note de bas de page 34 pour diverses populations de nourrissons. Le nombre de doses de PVZ par saison se situait entre une moyenne de 3,88 doses dans une saison de 5 mois en Espagne Note de bas de page 39 et 6 doses dans une saison de 6 mois de VRS dans l'Arctique canadien.Note de bas de page 26 La plupart des études ont évalué le rapport CE en supposant 5 doses de PVZ par saison de VRS (n=17) tandis que 3 études n'ont pas indiqué le calendrier des doses.Note de bas de page 37Note de bas de page 48Note de bas de page 50 Le coût d'un flacon de 100 mg de PVZ en CAD de 2017 se situait entre 1 099 $ (étude du R.-U.)Note de bas de page 37 et 2 198 $ (étude des É.-U.).Note de bas de page 46
Paramètres d'influence
Les paramètres les plus influents rapportés dans les 28 études (Figure 4) étaient les suivants : Taux d’HVRS (43 %),Note de bas de page 26Note de bas de page 29Note de bas de page 31Note de bas de page 32Note de bas de page 35Note de bas de page 36Note de bas de page 37Note de bas de page 41Note de bas de page 42Note de bas de page 44Note de bas de page 50Note de bas de page 54 coût du PVZ (36 %),Note de bas de page 27 Note de bas de page 32Note de bas de page 35Note de bas de page 36Note de bas de page 44Note de bas de page 46Note de bas de page 47Note de bas de page 50Note de bas de page 51Note de bas de page 54, taux d’actualisation (32 %)Note de bas de page 28Note de bas de page 29Note de bas de page 30Note de bas de page 31Note de bas de page 32Note de bas de page 34Note de bas de page 37Note de bas de page 38Note de bas de page 40 et efficacité potentielle du PVZ (29 %).Note de bas de page 35Note de bas de page 36Note de bas de page 37 Note de bas de page 43Note de bas de page 44Note de bas de page 48Note de bas de page 50Note de bas de page 54 D’autres paramètres ont eu une influence dans de multiples études, notamment : la réduction du taux de mortalité, l’incidence du VRS (et/ou des séquelles), le gaspillage de médicaments résultant de l’utilisation des flacons, les valeurs d’utilité (qualité de vie liée à la santé) et le schéma posologique.
Discussion
Sommaire des résultats
L'examen systématique a permis d'identifier 28 évaluations économiques pertinentes provenant de pays de l'OCDE et évaluant le rapport CE de la prophylaxie par PVZ comparativement à l'absence de prophylaxie. Les estimations les plus rentables concernaient les prématurés, ce qui est cohérent avec leur risque plus élevé de VRS.Note de bas de page 68 Dans presque toutes les catégories de nourrissons (à terme, prématurés, avec ou sans FR supplémentaires), la majorité (>50 %) des estimations du rapport CE étaient inférieures au seuil de 100 000 $/AVAQ. La seule exception à cette règle concerne les estimations relatives aux prématurés dans une perspective sociétale, où seulement 48 % des estimations étaient inférieures à 100 000 $/AVAQ. Cette exception est probablement le résultat d'un grand groupe d'estimations (n=8, 35 % de l'ensemble pour ce sous-groupe) extraites d'une seule étude qui se situaient entre 347 803 $/AVAQ et 2 975 489 $/AVAQ.Note de bas de page 46 Les raisons possibles des RCED plus élevés de cette étude sont les suivantes : utilisation du coût ajusté le plus élevé pour un flacon de 100 mg de PVZ, soit 2 198 $, suivi des nourrissons uniquement jusqu'à l'âge de 8 ans et, comme le suggèrent les auteurs, surestimation de l'impact de l'apparition ultérieure de l'asthme sur la qualité de vie liée à la santé (utilité). Une analyse de sensibilité réduisant le coût du PVZ de 25 % ou réduisant l'impact de l'asthme sur l'utilité a permis d'obtenir des RCED inférieurs à 200 000 $/AVAQ (USD) et à 100 000 $/AVAQ (USD), respectivement.Note de bas de page 46
D'après cet examen, le rapport CE de la prophylaxie par PVZ varie en fonction de la population et du contexte. Afin de faciliter les comparaisons et de résumer les résultats, tous les RCED ont été ajustés en CAD de 2017 par AVAQ et stratifiés en fonction de l'AG à la naissance et des FR du VRS dans la Figure 3. Pour les nourrissons à terme et prématurés atteints de DBP/MPC, le RCED était inférieur à 50 000 $/AVAQ dans 8 des 10 estimations du point de vue du payeur. Tous les autres sous-groupes de nourrissons (à terme, prématurés, CPC, autres FR) ont donné des résultats incohérents pour la prophylaxie par PVZ, l'intervention étant parfois dominante (c.-à-d. moins coûteuse et plus efficace) et présentant un RCED allant jusqu'à 938 623 $/AVAQ dans d'autres scénarios. Lorsque l'on stratifie les naissances prématurées en fonction de sAG, les données probantes font défaut pour les enfants nés à moins de 28 sAG, en particulier du point de vue du payeur. Aucune tendance précise n'a été décelée entre les sAG et le RCED, dans l'ensemble ou stratifiée par perspective. Toutefois, alors que les estimations concernant les prématurés étaient disponibles à 26 à 35 sAG, les prématurés présentant des FR supplémentaires ou une DBP/MPC étaient limités à 33-35 sAG. En général, on s'attendrait à ce que les RCED du point de vue sociétal soient inférieurs à ceux du point de vue du payeur, mais d'après cet examen, cette tendance n'existe pas pour 2 raisons : 1) les estimations du point de vue du payeur et de la société provenaient de différentes études et; 2) l'hétérogénéité des conceptions de modèles et des différences entre les coûts spécifiques au contexte et l'épidémiologie du VRS.
Évaluations économiques dans un contexte canadien
Cinq évaluations économiques ont été réalisées dans un contexte canadien. Si 4 des 5 études ont utilisé la perspective du payeur du système de santé, l'horizon temporel, le taux d'actualisation et le rapport CE des résultats varient. Les populations étaient différentes dans toutes les études : nourrissons à terme atteints de FK, nourrissons à terme de l'Arctique canadien, prématurés et nourrissons atteints de CPC. Les études de Tam et al. et de Banerji et al. ont également conclu que la prophylaxie par PVZ était rentable pour la plupart des sous-groupes de nourrissons dans l'Arctique canadien en raison des coûts élevés des hospitalisations (p. ex., le transport). Les conclusions de l'étude de Tam et al. concernaient les nourrissons de la région de Baffin tandis que Banerji et al. ont inclus les populations de 8 régions arctiques : les Territoires du Nord-Ouest, le Nunavut, le Nunavut sans Iqaluit, les 3 sous-régions du Nunavut (Kitikmeot, Kivalliq et Qikiqtaaluk), la région de Qikiqtaaluk sans Iqaluit et le Nunavik (nord du Québec). Les 2 études ont été menées du point de vue du payeur du système de santé et ont utilisé des coûts de PVZ similaires (220 à 226 $ par kilogramme de poids du nourrisson, coût initial). Compte tenu des populations étudiées, des contextes cliniques et du coût des médicaments et des ressources, les études de Tam et al. et de Banerji et al. peuvent être considérées comme généralisables à d'autres territoires ou régions éloignées du Canada pour les nourrissons à haut risque de VRS.
Les 3 autres études sont également considérées comme étant généralisables à la plupart des provinces canadiennes étant donné qu'elles ont utilisé des coûts de PVZ similaires (1 468 $ - 1 505 $ par flacon de 100 mg, coûts originaux) à ceux des provinces canadiennes, qu'elles ont utilisé des schémas posologiques proches de 5 injections par saison (4,5 à 5,39 flacons par saison), qu'elles ont utilisé les coûts des soins de santé de la Colombie-Britannique et de l'Ontario et qu'elles ont inclus des paramètres de modèle pertinents pour le système de santé canadien. Bien que des données probantes aient été recueillies pour diverses sous-populations des grandes provinces et des territoires, le rapport CE de la prophylaxie par PVZ pour les nourrissons des petites provinces canadiennes (p. ex., les provinces maritimes) faisait défaut.
Hétérogénéité des résultats : Paramètres clés
Étant donné que la prophylaxie par le PVZ a été jugée comme étant rentable dans certains contextes, mais non dans d'autres, cet examen résume les paramètres influents les plus fréquemment rapportés qui affectent le RCED. Ils comprenaient les taux d'HVRS et le coût du PVZ utilisé. La réduction des HVRS a varié considérablement entre 39 % et 96 % selon la population d'intérêt et la source des données. Le coût d'un flacon de 100 mg de PVZ se situe également entre 1 099 $ et 2 198 $ (CAD de 2017). L'influence de ces 2 paramètres était attendue étant donné que la réduction des HVRS et du VRS est essentielle pour réduire les coûts et les séquelles futures, tandis que les coûts du PVZ sont directement liés au RCED. Toutefois, il était intéressant de noter que l'utilisation du flacon et le schéma posologique n'ont eu une incidence sur le RCED que dans 4 études,Note de bas de page 29Note de bas de page 30Note de bas de page 40Note de bas de page 43 et 3 études,Note de bas de page 39Note de bas de page 43Note de bas de page 49 respectivement.
Dans les études portant sur le gaspillage de médicaments par l'utilisation de flacons, les RCED ont fluctué jusqu'à 50 % selon l'utilisation supposée des flacons. Dans une étude néo-zélandaise, l'hypothèse de l'absence de partage des flacons (un flacon entier de 100 mg est utilisé par injection) a entraîné une augmentation des coûts pouvant atteindre 50 %,Note de bas de page 43 tandis qu'une autre étude menée en Espagne a conclu à un RCED inférieur lorsque des flacons de 50 mg étaient utilisés au lieu de 100 mg.Note de bas de page 30 Il a été suggéré dans la littérature et par les médecins que l'efficacité de l'utilisation des flacons peut être atteinte pour le PVZ. Note de bas de page 56 De nombreuses études n'ont pas évalué de scénarios dans lesquels l'utilisation des flacons devient plus efficace ou le nombre de doses supposées est réduit, ce qui demeure une question qui devrait être abordée dans de futures études.
Comparaison avec la littérature
Le rapport CE de la prophylaxie par PVZ a été exploré dans de multiples examens au cours des 2 dernières décennies,Note de bas de page 11Note de bas de page 12Note de bas de page 14 mais seulement 4 ont été publiés entre 2010 et 2013.Note de bas de page 15Note de bas de page 57Note de bas de page 58Note de bas de page 59 Ces résultats et conclusions sont cohérents avec d'autres examens et sont plus comparables à un examen systématique de Smart et al. publiée en 2010, où les auteurs ont rapporté une gamme de RCED (CAD de 2009) pour la prophylaxie par PVZ : de dominant (c.-à-d. moins coûteux et plus efficace) jusqu'à 3 365 768 $/AVAQ selon la population étudiée, les résultats et les paramètres du modèle.Note de bas de page 59 Le présent travail s'est ajouté à l'examen Smart en capturant des études réalisées de 2010 à la mi-2018 mais a limité le champ d'application aux pays de l'OCDE, et a ajusté les différences d'inflation en utilisant les taux de PPA de l'OCDE. Les examens d'Andabaka et al. et de Prescott et al. ont également conclu que le rapport CE du PVZ était incohérent.Note de bas de page 15Note de bas de page 58 Hussman et al. ont effectué un examen de l'ensemble de la prophylaxie du VRS et ont inclus des études comparant le PVZ et d'autres interventions (p. ex., immunoglobuline intraveineuse-VRS).Note de bas de page 57 Le présent examen est le premier à mettre à jour le rapport CE de la prophylaxie par PVZ comparativement à l'absence de prophylaxie depuis la mise à jour des lignes directrices de l'American Academy of Pediatrics (AAP) de 2014.Note de bas de page 60
Généralisabilité des études incluses au contexte canadien
La plupart des résultats des études peuvent être largement généralisés au système de santé canadien puisque les critères d'admissibilité prévoyaient des évaluations économiques réalisées dans des pays de l'OCDE, dont tous les membres, à l'exception des É.-U. et de la Suisse, ont des composantes de soins de santé semblables à celles du Canada.Note de bas de page 61 La seule exception est constituée par les 6 études réalisées aux É.-U. Les autres études réalisées aux Pays-Bas, au R.-U., en Espagne, en Autriche, en Allemagne, en Italie, en Nouvelle-Zélande et en Suède prévoient un financement partiel du système public par les recettes fiscales générales.Note de bas de page 61 Toutefois, le choix du payeur ou de la perspective sociétale peut influer sur les coûts inclus dans l'analyse. Par exemple, le rapport CE d'un point de vue sociétal inclut les éventuels coûts indirects, les frais à la charge des patients ou les pertes de productivité, qui peuvent varier d'un pays à l'autre, quel que soit le financement du système de santé.
D'après 3 études canadiennes, le coût par flacon de 100 mg de PVZ utilisé dans les modèles se situait entre 1 599 $ et 1 718 $ (CAD de 2017). Les modèles du R.-U. ont utilisé un coût de PVZ plus faible, de 1 099 à 1 240 $ par flacon de 100 mg, et les autres études (à l'exception de celles des É.-U.) ont dispersé entre 1 386 et 2 035 $ (CAD de 2017). Le nombre de doses par saison supposé ou calculé dans le cadre de ces évaluations économiques variait entre 3,88 et 6 doses. La Société canadienne de pédiatrie recommande jusqu'à 5 doses de PVZ par saison pour les nourrissons âgés de 24 mois ou moins. Note de bas de page 62 Dans le sous-ensemble de pays ayant une structure de soins de santé similaire à celle du Canada, presque tous les modèles ont supposé 5 doses de PVZ par saison, à l'exception de Resch et al (Autriche),Note de bas de page 34 Banerji et al. (Canada),Note de bas de page 26 Nuijten et al, Sanchez-Luna et al et de Schmidt et al (tous d'Espagne), où le nombre moyen de doses était de 4 par saison.Note de bas de page 30Note de bas de page 39Note de bas de page 40 De plus, les FR du VRS modélisés sont conformes à ceux publiés dans la littérature canadienne : naissance prématurée, CPC, DBP/MPC, sexe masculin.Note de bas de page 8
Malgré les similitudes dans le coût et le schéma posologique de la prophylaxie par PVZ, les taux de réduction des HVRS variaient de 39 % à 96 % selon la population de nourrissons et la littérature référencée. De nombreuses études ont cité l'essai IMpact-RSV pour les paramètres de leur modèle, un essai qui inclut le Canada et qui a conclu que la réduction des HVRS était de 78 % pour les prématurés, de 39 % pour les enfants atteints de DBP/MPC et de 55 % pour l'ensemble des enfants. Le sous-groupe de sujets canadiens de l'essai IMpact-RSV aurait montré une réduction globale de 40 % des HVRS. Cette tendance était similaire à celle observée chez les sujets américains (56 %) et britanniques (64 %). Note de bas de page 63 La question 11 de la liste de contrôle d'évaluation de la qualité du JBI évalue la transférabilité. Deux examinateurs indépendants ont conclu que 24 des 28 études étaient généralisables sur la base des attributs de leur modèle (structure, paramètres) et des résultats rapportés. Les résultats obtenus aux É.-U. peuvent avoir une généralisation limitée lors de l'évaluation de cette partie de la liste de contrôle.
Limites de l'étude
Cet examen présente de nombreuses limites. Les différences dans la conception des modèles, les taux d'HVRS utilisés, l'évolution de la maladie, les perspectives et les contextes nous ont empêchés de fournir des conclusions définitives sur la valeur de cette intervention. L'examen a tenté de résumer le rapport CE de cette intervention effectuée de 2000 à 2018 mais les modifications apportées aux recommandations de l'American Academy Pediatrics aux É.-U. (et des décideurs dans les autres pays respectifs) au fil du temps peuvent affecter la conception du modèle et les données d'entrée. Enfin, l'examen peut être assujetti à des biais de publication et de langue puisqu'il n'a pas effectué de recherche dans la littérature grise ni inclus d'articles non rédigés en anglais ou en français.
Points forts de l'étude
Malgré ces limites, cet examen fournit un sommaire complet du rapport CE de la prophylaxie par PVZ dans les pays de l'OCDE afin d'informer les décideurs de la valeur estimée de cette intervention chez les nourrissons à terme, les prématurés et les nourrissons à haut risque de VRS (p. ex., CPC, DBP/MPC). La Figure 3 montre tous les résultats de SR et les analyses de scénarios, ce qui donne une idée du nombre d'études (et d'estimations) qui se situent sous des seuils de rentabilité précis, tant du point de vue des payeurs que de la société. Toutes les estimations ont été normalisées en CAD de 2017, ce qui nous a permis de regrouper, stratifier et de comparer les estimations du rapport CE. Ces RCED ajustés devraient être utiles pour les décideurs de programmes où les coûts peuvent être considérablement sous-estimés s'ils ne sont pas ajustés de manière appropriée.
Conclusion
Les résultats du rapport CE du PVZ en tant que prophylaxie du VRS étaient hétérogènes d'une étude à l'autre, allant d'un rapport dominant (c.-à-d. moins coûteux et plus efficace) à un rapport très peu efficace. Les résultats variaient en fonction du contexte de l'étude, de la population d'intérêt, de l'épidémiologie locale du VRS et de la structure des soins de santé, ainsi que des paramètres clés du modèle, comme la réduction des taux d'hospitalisation, les coûts d'acquisition du VRS, les schémas posologiques et l'utilisation des flacons. D'après les conclusions de nombreux auteurs, la prophylaxie du VRS par le PVZ peut être considérée comme étant rentable dans certains sous-groupes de nourrissons. Du point de vue du payeur, les auteurs ont conclu que le PVZ était considéré comme étant rentable chez les nourrissons atteints de DBP/MPC, les nourrissons atteints de CPC, les nourrissons à terme provenant de communautés éloignées précises et les prématurés avec ou sans complications pulmonaires. Aucune tendance générale n'a été détectée entre les seuils d'AG précis et les résultats du rapport CE, globalement ou stratifiés par perspective. Parmi les 2 études menées dans le Nord canadien, les auteurs ont conclu que le PVZ était considéré comme étant rentable dans certains contextes où les taux d'HVRS de base étaient très élevés, évitant ainsi des coûts d'hospitalisation et d'évacuation médicale élevés.
Figures et tableaux
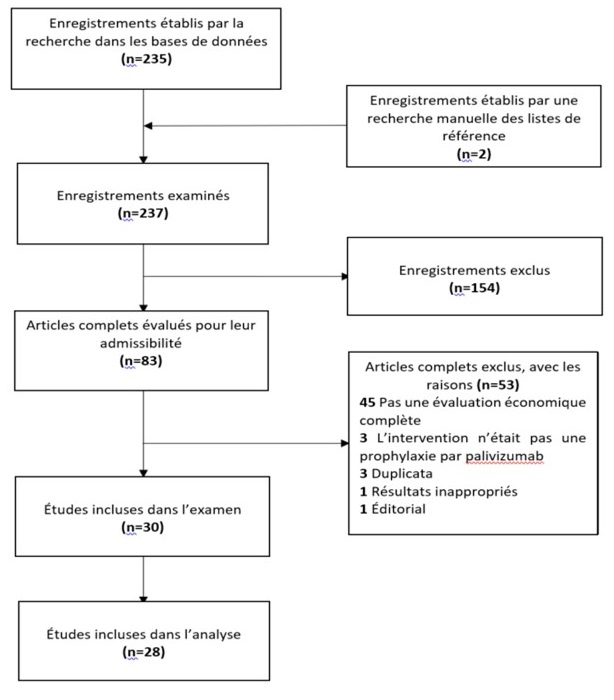
Figure 1 - descriptif
L'organigramme montre le nombre d'enregistrements recherchés et sélectionnés. Il y a eu 235 enregistrements identifiés à travers la recherche des bases de données et deux enregistrements identifiés à travers une recherche manuelle des listes de référence, soit un total de 237 enregistrements. Les 237 enregistrements ont été sélectionnés, et 154 enregistrements ont été exclus, avec 83 textes complets restants. Après avoir évalué l'admissibilité des textes complets, 53 articles ont été exclus pour les raisons suivantes : une évaluation économique non complète (n = 45), une intervention non prophylaxie par palivizumab (n = 3), des doubles (n = 3), des résultats inappropriés (n = 1), un éditorial (n = 1). Par conséquent, 30 textes complets ont été inclus dans l'examen, dont 28 seulement ont été inclus dans l'analyse.
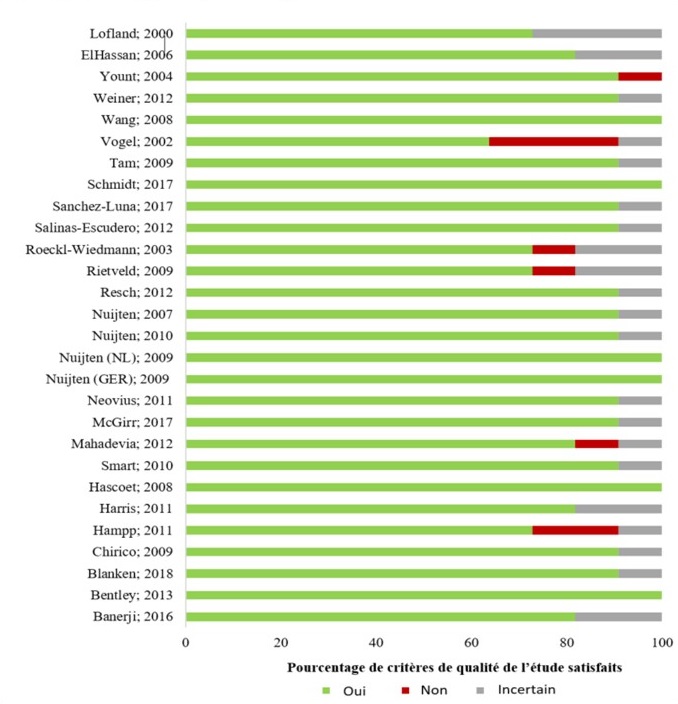
Figure 2 - descriptif
| Auteur; année | Oui | Non | Incertain | % Oui | % Non | % Incertain |
|---|---|---|---|---|---|---|
| Banerji; 2016 | 9,00 | 0,00 | 2,00 | 81,82 | 0,00 | 18,18 |
| Bentley; 2013 | 11,00 | 0,00 | 0,00 | 100,00 | 0,00 | 0,00 |
| Blanken; 2018 | 10,00 | 0,00 | 1,00 | 90,91 | 0,00 | 9,09 |
| Chirico; 2009 | 10,00 | 0,00 | 1,00 | 90,91 | 0,00 | 9,09 |
| Hampp; 2011 | 8,00 | 2,00 | 1,00 | 72,73 | 18,18 | 9,09 |
| Harris; 2011 | 9,00 | 0,00 | 2,00 | 81,82 | 0,00 | 18,18 |
| Hascoet; 2008 | 11,00 | 0,00 | 0,00 | 100,00 | 0,00 | 0,00 |
| Smart; 2010 | 10,00 | 0,00 | 1,00 | 90,91 | 0,00 | 9,09 |
| Mahadevia; 2012 | 9,00 | 1,00 | 1,00 | 81,82 | 9,09 | 9,09 |
| McGirr; 2017 | 10,00 | 0,00 | 1,00 | 90,91 | 0,00 | 9,09 |
| Neovius; 2011 | 10,00 | 0,00 | 1,00 | 90,91 | 0,00 | 9,09 |
| Nuijten (GER); 2009 | 11,00 | 0,00 | 0,00 | 100,00 | 0,00 | 0,00 |
| Nuijten (NL); 2009 | 11,00 | 0,00 | 0,00 | 100,00 | 0,00 | 0,00 |
| Nuijten; 2010 | 10,00 | 0,00 | 1,00 | 90,91 | 0,00 | 9,09 |
| Nuijten; 2007 | 10,00 | 0,00 | 1,00 | 90,91 | 0,00 | 9,09 |
| Resch; 2012 | 10,00 | 0,00 | 1,00 | 90,91 | 0,00 | 9,09 |
| Rietveld; 2009 | 8,00 | 1,00 | 2,00 | 72,73 | 9,09 | 18,18 |
| Roeckl-Wiedmann; 2003 | 8,00 | 1,00 | 2,00 | 72,73 | 9,09 | 18,18 |
| Salinas-Escudero; 2012 | 10,00 | 0,00 | 1,00 | 90,91 | 0,00 | 9,09 |
| Sanchez-Luna; 2017 | 10,00 | 0,00 | 1,00 | 90,91 | 0,00 | 9,09 |
| Schmidt; 2017 | 11,00 | 0,00 | 0,00 | 100,00 | 0,00 | 0,00 |
| Tam; 2009 | 10,00 | 0,00 | 1,00 | 90,91 | 0,00 | 9,09 |
| Vogel; 2002 | 7,00 | 3,00 | 1,00 | 63,64 | 27,27 | 9,09 |
| Wang; 2008 | 11,00 | 0,00 | 0,00 | 100,00 | 0,00 | 0,00 |
| Weiner; 2012 | 10,00 | 0,00 | 1,00 | 90,91 | 0,00 | 9,09 |
| Yount; 2004 | 10,00 | 1,00 | 0,00 | 90,91 | 9,09 | 0,00 |
| ElHassan; 2006 | 9,00 | 0,00 | 2,00 | 81,82 | 0,00 | 18,18 |
| Lofland; 2000 | 8,00 | 0,00 | 3,00 | 72,73 | 0,00 | 27,27 |
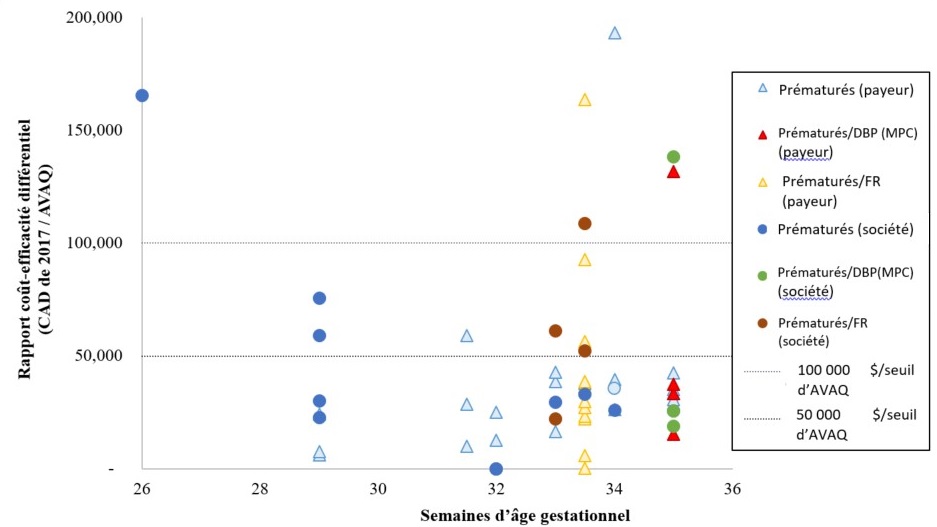
Figure 3 - descriptif
| sAG | Perspective |
RCED (CAD de 2017/AVAQ) | |
|---|---|---|---|
Prématurés |
|||
| 29 | Payeur |
6 216 | |
| 29 | Payeur |
7 494 | |
| 29 | Payeur |
24 009 | |
| 31,5 | Payeur |
9 989 | |
| 31,5 | Payeur |
28 429 | |
| 31,5 | Payeur |
58 872 | |
| 32 | Payeur |
12 710 | |
| 32 | Payeur |
25 065 | |
| 33 | Payeur |
16 434 | |
| 33 | Payeur |
38 733 | |
| 33 | Payeur |
42 730 | |
| 33,5 | Payeur |
37 815 | |
| 34 | Payeur |
26 170 | |
| 34 | Payeur |
35 530 | |
| 34 | Payeur |
39 642 | |
| 34 | Payeur |
193 068 | |
| 35 | Payeur |
30 650 | |
| 35 | Payeur |
33 257 | |
| 35 | Payeur |
35 216 | |
| 35 | Payeur |
42 600 | |
| 35 | Payeur |
938 623 | |
| 26 | Sociétal |
165 301 | |
| 26 | Sociétal |
1 331 595 | |
| 27 | Sociétal |
2 078 481 | |
| 28 | Sociétal |
347 803 | |
| 28 | Sociétal |
2 406 619 | |
| 29 | Sociétal |
22 765 | |
| 29 | Sociétal |
30 000 | |
| 29 | Sociétal |
58 922 | |
| 29 | Sociétal |
75 595 | |
| 29 | Sociétal |
1 359 641 | |
| 29,5 | Sociétal |
449 264 | |
| 29,5 | Sociétal |
1 083 976 | |
| 31 | Sociétal |
1 944 890 | |
| 32 | Sociétal |
- | |
| 32 | Sociétal |
- | |
| 32 | Sociétal |
- | |
| 32 | Sociétal |
2 975 489 | |
| 33 | Sociétal |
29 470 | |
| 33,5 | Sociétal |
32 930 | |
| 33,5 | Sociétal |
338 823 | |
| 34 | Sociétal |
25 990 | |
| 35 | Sociétal |
25 678 | |
| 35 | Sociétal |
983 064 | |
Prématurés and BPD |
|||
35 |
Payeur | 15 202 | |
35 |
Payeur | 33 412 | |
35 |
Payeur | 37 362 | |
35 |
Sociétal | 18 717 | |
35 |
Sociétal | 25 684 | |
Prématurés and CLD |
|||
35 |
Payeur | 131 874 | |
35 |
Sociétal | 138 282 | |
Prématurés et facteurs de risque |
|||
33,5 |
Payeur | 215 | |
33,5 |
Payeur | 5 906 | |
33,5 |
Payeur | 22 173 | |
33,5 |
Payeur | 23 309 | |
33,5 |
Payeur | 27 216 | |
33,5 |
Payeur | 29 901 | |
33,5 |
Payeur | 35 119 | |
33,5 |
Payeur | 36 356 | |
33,5 |
Payeur | 38 566 | |
33,5 |
Payeur | 54 308 | |
33,5 |
Payeur | 56 479 | |
33,5 |
Payeur | 92 649 | |
33,5 |
Payeur | 163 744 | |
33,5 |
Payeur | 205 563 | |
33,5 |
Payeur | 919 073 | |
33 |
Sociétal | 21 931 | |
33 |
Sociétal | 61 229 | |
33,5 |
Sociétal | 52 299 | |
33,5 |
Sociétal | 108 685 | |
33,5 |
Sociétal | 385 488 | |
33,5 |
Sociétal | 635 172 | |
Remarque : Estimations incluses (n=56), les RCED > 200 000 $/AVAQ n'ont pas été saisis (n=16). Point de vue du payeur : prématurés (32-35 sAG) avec FR : 205 563 $/AVAQ, 41 prématurés (<35 sAG) : 938 623 $/AVAQ, 14 prématurés (32-35 sAG) : 919 073 $/AVAQ. 41 Sociétal : prématurés (26 sAG) : 1 331 595 $/AVAQ, 46 prématurés (27 sAG) : 2 078 481 $/AVAQ, 46 prématurés (28 sAG) : 2 406 619 $/AVAQ, 46 prématurés (28 sAG) : 347 803 $/AVAQ, 46 prématuré (<29 sAG) : 1 359 641 $/AVAQ, 28 prématurés (29-30 sAG) : 1 083 976 $/AVAQ, 46 prématurés (29-30 sAG) : 449 264 $/AVAQ, 46 prématurés (31 sAG) : 1 944 890 $/AVAQ, 46 prématurés (32 sAG) : 2 975 489 $/AVAQ, 46 prématurés (32-35 sAG) : 338 823 $/AVAQ, 48 prématurés (<35 sAG) : 983 064 $/AVAQ, 14 prématurés (32-35 sAG) avec FR : 635 172 $/AVAQ 54 et 385 488 $/AVAQ. 44 |
|||
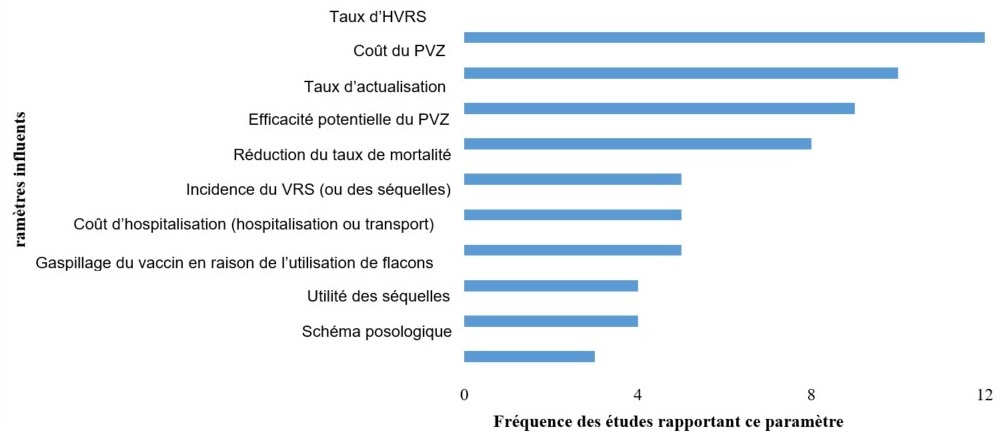
Figure 4 - descriptif
| Paramètres influents | Fréquence des études rapportant ce paramètre |
|---|---|
| Taux d'HVRS | 12 |
| Coût du PVZ | 10 |
| Taux d'actualisation | 9 |
| Efficacité potentielle du PVZ | 8 |
| Réduction du taux de mortalité | 5 |
| Incidence du VRS (ou des séquelles) | 5 |
| Coût d'hospitalisation (hospitalisation ou transport) | 5 |
| Gaspillage du vaccin en raison de l'utilisation de flacons | 4 |
| Utilité des séquelles | 4 |
| Schéma posologique | 3 |
| Auteurs, année | Pays | Perspective | Type d'analyse | Existant ou basé sur un modèle?; Type de modèle | Mesure des résultats | Population | Horizon temporel | Taux d'actualisation | Financement de l'industrie |
|---|---|---|---|---|---|---|---|---|---|
| Banerji 2016Note de bas de page 26 |
Canada | Payeur | ACE | Basé sur un modèle; Analyse de décision | cHE | Nourrissons à terme | 6 mois | s. o. | Abbott/MedImmune (subventions) |
| Bentley 2011Note de bas de page 37 | R.-U. | Payeur | ACU | Basé sur un modèle; Analyse de décision | cAVAQ | Prématurés, CPC, MPC | À vie | 3,5 % | AbbVie |
| Blanken 2018Note de bas de page 38 | Pays-Bas | Sociétal | ACU | Existant; Analyse de décision | cAVAQ | Prématurés | 1 an | s. o. | Inconnu : Subventions de MedImmune et d'AbbVie pour des études menées à l'initiative de chercheurs |
| Chirico 2009Note de bas de page 49 | Italie | Payeur | ACU | Basé sur un modèle; Simulation | cAVAQ | Prématurés, DBP | À vie | 3 % | Abbott |
| ElHassan 2006Note de bas de page 46 | É.-U. | Sociétal | ACU; ACA | Basé sur un modèle; cohorte de Markov | cAVAQ | Prématurés sans MPC | 8 ans | 3 % | Aucun |
| Hampp 2011Note de bas de page 50 | É.-U. | Payeur | ACE | Basé sur un modèle; Analyse de décision | cHE | Prématurés et à terme (avec ou sans CPC, MPC) | RN | NR | Aucun |
| Harris 2011Note de bas de page 51 | Canada | Sociétal | ACE; ACA | Basé sur un modèle; Analyse de décision | Coût par jour d'HE | Nourrissons atteints de CPC | 5 ansNote de bas de page a | NR | Inconnu : Honoraires (< 1 000 $) de Abbott |
| Hascoet 2008Note de bas de page 52 | France | Sociétal (SR) et payeur | ACE; ACA | Basé sur un modèle; Analyse de décision | cAVG | Prématurés atteints de CPC ou de DBP | À vie | 3 % | Abbott France |
| Lofland 2000Note de bas de page 47 | É.-U. | Payeur | ACE | Existant; Analyse de décision | Coût par infection de VRS évitée | Prématurés atteints de MPC | 6 mois | s. o. | MedImmune, Inc. |
| Mahadevia 2012Note de bas de page 54 | É.-U. | Sociétal | ACU | Basé sur un modèle; Analyse de décision | cAVAQ | Prématurés | À vie | 3 % | MedImmune LLC |
| McGirr 2017Note de bas de page 27 | Canada | Payeur | ACU | Basé sur un modèle; cohorte de Markov | cAVAQ | Nourrissons à terme atteints de FK | À vie | 5 % | Aucun |
| Neovius 2011Note de bas de page 28 | Suède | Sociétal | ACU | Basé sur un modèle; cohorte de Markov | cAVAQ | Prématurés | À vie | 3 % | Abbott Scandinavia |
| Nuijten 2009Note de bas de page 32 | Allemagne | Sociétal (SR) et payeur | ACU | Basé sur un modèle; Analyse de décision | cAVAQ | Nourrissons atteints de CPC | À vie | 5 % | Abbott |
| Nuijten 2009Note de bas de page 31 | Pays-Bas | Payeur (SR) et sociétal | ACU | Basé sur un modèle; Analyse de décision | cAVAQ | Prématurés, DBP, CPC | À vie | 4 %, 1,5 %Note de bas de page a | Abbott GmbH & Co. Allemagne |
| Nuijten Note de bas de page 30 | Espagne | Payeur (SR) et sociétal | ACU | Basé sur un modèle; Analyse de décision | cAVAQ | Prématurés | À vie | 3 % | Abbott GmbH & Co. Allemagne |
| Nuijten 2007Note de bas de page 29 | R.-U. | Payeur (SR) et sociétal | ACU | Basé sur un modèle; Analyse de décision | cAVAQ; cHE | Prématurés, DBP, CPC | À vie | 3,5 % | Abbott GmbH & Co. Allemagne |
| Resch 2012Note de bas de page 33Note de bas de page 34 | Autriche | Payeur (SR) et sociétal | ACU | Basé sur un modèle; Analyse de décision | cAVAQ | Prématurés, DBP, CPC | À vie | 5 % | Aucun |
| Rietveld 2010Note de bas de page 35 | Pays-Bas | Sociétal | ACE | Basé sur un modèle; Analyse de décision | cHE | Prématurés, DBP | 1 an | s. o. | Aucun |
| Roeckl-Wiedmann 2003Note de bas de page 36 | Allemagne | Sociétal | ACE | Basé sur un modèle; Analyse de décision | cHE | Prématurés présentant des FR | 1 an | s. o. | Abbott Laboratories, Allemagne |
| Salinas-Escudero 2012Note de bas de page 38 | Mexique | Payeur | ACU | Basé sur un modèle; Analyse de décision | cAVAQ | Prématurés | À vie | 3 % | Abbott Laboratories, Mexique |
| Sanchez-Luna 2017Note de bas de page 39 | Espagne | Payeur (SR) et sociétal | ACU | Basé sur un modèle; Analyse de décision | cAVAQ | Prématurés présentant des FR | 6 ans | 3 % | Aucun |
| Schmidt 2017Note de bas de page 40 | Espagne | Sociétal | ACU | Basé sur un modèle; état de Markov (structure en arbre de décision la première année et structure de Markov les années suivantes) | cAVAQ | Nourrissons atteints de CPC | À vie | 3 % | AbbVie (subvention) |
| Smart 2010Note de bas de page 41Note de bas de page 53 | Canada | Payeur (SR) et sociétal | ACU | Basé sur un modèle; Analyse de décision | cAVAQ | Prématurés présentant des FR | À vie | 5 % | Inconnu : Autres relations avec Abbott |
| Tam 2009Note de bas de page 42 | Canada | Payeur (SR) et sociétal | ACU | Basé sur un modèle; Analyse de décision | cAVAQ | NR | À vie | 5 % | Abbott Laboratories/ Abbott International (subvention) |
| Vogel 2002Note de bas de page 43 | Nouvelle-Zélande | Sociétal | ACE; ACA | Basé sur un modèle; Analyse de décision | Coût par cas évité | Prématurés, MPC | 3 ansNote de bas de page b | NR | Abbott (subvention) |
| Wang 2008Note de bas de page 14 | R.-U. | Payeur (SR) et sociétal | ACU | Basé sur un modèle; Analyse de décision | cAVAQ | Prématurés, DBP, CPC, MPC, nourrissons à terme avec FR | À vie | 3,5 % | Aucun |
| Weiner 2012Note de bas de page 44 | É.-U. | Sociétal | ACU | Basé sur un modèle; Analyse de décision | cAVAQ | Prématurés présentant des FR | À vie | 3 % | MedImmune LLC |
| Yount 2004Note de bas de page 45 | É.-U. | Sociétal | ACU; ACA | Basé sur un modèle; Analyse de décision | cAVAQ | Nourrissons atteints de CPC | À vie | 3 % | Aucun |
Définitions : ACA, analyse coût-avantage; ACE, analyse coût-efficacité; ACU, analyse coût-utilité; AVAQ, année de vie ajustée par la qualité; AVG, année de vie gagnée; cAVAQ, coût par année de vie ajustée par la qualité; cHE, coût par hospitalisation évitée; CPC, cardiopathie congénitale; DBP, dysplasie bronchopulmonaire; É.-U., États-Unis; FR, facteur de risque; FK, fibrose kystique; MPC, maladie pulmonaire chronique; NR, non rapporté; R.-U., Royaume-Uni; s. o., sans objet; SR, scénario de référence.
|
|||||||||
| Auteur, année |
Devise originale, VP utilisée | RCED (original) | RCED (ajusté, CAD de 2017) |
Résultats (contexte) | Analyse de sensibilité | Conclusions de l'étude | |
|---|---|---|---|---|---|---|---|
Banerji |
CAN 2011; 50 000 $ par admission à l'hôpital |
4 633 | 5 042 | cHE |
Scénario BNote de bas de page a Nunavut sans Iqaluit | Déterministe |
Le PVZ était rentable dans les régions de Kitikmeot et de Kivalliq et au Nunavik. Le scénario B (par rapport au scénario A) était plus rentable dans toutes les régions, sauf dans la région de Kitikmeot. |
| 14 545 | 15 829 | Scénario BNote de bas de page a, Nunavut | |||||
| 15 601 | 16 979 | Scénario BNote de bas de page a, Nunavik | |||||
| 22 954 | 24 981 | Scénario ANote de bas de page b, région de Kivalliq | |||||
| 28 580 | 31 104 | Scénario ANote de bas de page b, Nunavut sans Iqaluit | |||||
| 30 230 | 32 899 | Scénario ANote de bas de page b, Nunavik | |||||
| 41 404 | 45 060 | Scénario ANote de bas de page b, Nunavut | |||||
| 105 259 | 114 554 | Scénario BNote de bas de page a, région de Qikiqtaaluk sans Iqaluit | |||||
| 133 407 | 145 187 | Scénario BNote de bas de page a, région de Qikiqtaaluk | |||||
| 166 600 | 181 311 | Scénario ANote de bas de page b, région de Qikiqtaaluk sans Iqaluit | |||||
| 211 444 | 230 115 | Scénario ANote de bas de page b, région de Qikiqtaaluk | |||||
| 326 441 | 355 267 | Scénario BNote de bas de page a, TNO | |||||
| 545 115 | 593 250 | Scénario ANote de bas de page b, TNO | |||||
| Dominant | Dominant | Scénario ANote de bas de page b, région de Kitikmeot | |||||
| Dominant | Dominant | Scénario BNote de bas de page a, région de Kitikmeot | |||||
| Dominant | Dominant | Scénario BNote de bas de page a, région de Kivalliq | |||||
Bentley |
GB 2010; 20 000 £/ AVAQ et |
3 845 | 7 494 | cAVAQ gagnée |
Prématurés (<29 sAG) | Déterministe; probabiliste |
Le PVZ prophylactique représente une utilisation économiquement viable des ressources du NHS pour les nourrissons (âgés de moins de 24 mois) atteints de CPC, les nourrissons (âgés de moins de 24 mois) atteints de MPC et les prématurés nés à 32 sAG ou moins et les prématurés nés à 33-35 sAG lorsque des FR supplémentaires sont pris en compte. |
| 19 168 | 37 360 | Nourrissons atteints de MPC | |||||
| 30 205 | 58 872 | Prématurés (29-32 sAG) | |||||
| 33 216 | 64 741 | Nourrissons atteints de CPC | |||||
| 99 056 | 193 068 | Prématurés (33-35 sAG) | |||||
| Blanken 2018Note de bas de page 48 |
NLD 2015; 80 000 €/ AVAQ | 214 748 | 338 823 | cAVAQ gagnée | Prématurés (32-35 sAG) | Déterministe; probabiliste | |
Chirico |
ITA 2007; 50 000 €/ AVAQ |
2 732 | 4 786 | cAVAQ gagnée |
DBP | Déterministe |
Par rapport à l'absence de prophylaxie, le PVZ est rentable pour la prévention de l'infection par le VRS chez les prématurés à haut risque. |
| 8 677 | 15 202 | Prématurés (<35 sAG, mixte) avec DBP | |||||
| 9 380 | 16 434 | Prématurés (<33 sAG) | |||||
| 14 937 | 26 170 | Prématurés (33-35 sAG) | |||||
ElHassan 2006Note de bas de page 46 |
É.-U. 2002; 200 000 $/ AVAQ |
103 053 | 165 301 | cAVAQ gagnée |
SR, prématurés (26 sAG), politique d'utilisation ciblée | Déterministe |
Notre modèle soutient la mise en œuvre de lignes directrices plus restrictives pour la prophylaxie par PVZ. Le PVZ s'est révélé rentable pour certains nourrissons dans le cadre d'une analyse qui tenait compte du risque accru d'asthme sévère après une infection par le VRS. Nous avons trouvé des preuves que les conséquences sanitaires à long terme du VRS sont essentielles pour déterminer le rapport CE de l'intervention. |
| 216 830 | 347 803 | SR, prématurés (28 sAG), politique d'utilisation ciblée | |||||
| 280 083 | 449 264 | SR, prématurés (29-30 sAG), politique d'utilisation ciblée | |||||
| 675 780 | 1 083 976 | SR, prématuré (29-30 sAG) | |||||
| 830 152 | 1 331 595 | SR, prématurés (26 sAG) | |||||
| 1 212 497 | 1 944 890 | SR, prématurés (31 sAG) | |||||
| 1 295 781 | 2 078 481 | SR, prématurés (27 sAG) | |||||
| 1 500 351 | 2 406 619 | SR, prématurés (28 sAG) | |||||
| 1 855 000 | 2 975 489 | SR, prématurés (32 sAG) | |||||
Hampp |
É.-U. 2010; NR (comparé à 8 910 $/ hospitalisa-tion) |
302 103 | 413 127 | cHE |
Prématurés (<32 sAG) | Déterministe; probabiliste |
Le coût de l'immunoprophylaxie par le PVZ dépassait de loin l'avantage économique de la prévention des hospitalisations, même chez les nourrissons présentant le risque le plus élevé d'infection par le VRS. |
| 361 727 | 494 663 | Prématurés (<32 sAG) et CPC | |||||
| 368 048 | 503 307 | Prématurés (<32 sAG) et MPC | |||||
| 522 490 | 714 507 | À terme, MPC et CPC | |||||
| 823 868 | 1 126 642 | À terme, CPC seulement | |||||
| 920 033 | 1 258 148 | Tout FR (indication) | |||||
| 1 322 422 | 1 808 416 | À terme, MPC uniquement | |||||
| 2 138 870 | 2 924 911 | Aucun FR (indication) | |||||
Harris |
CAN 2007; NR |
8 292 | 9 704 | Coût du traitement d'un enfant par saison de VRS | SR | Déterministe |
Notre étude contribue au corpus croissant de la littérature qui suggère que le PVZ n'est pas rentable chez les enfants de moins de 2 ans atteints de CPC hémodynamiquement significative (CPCHS) |
| 15 513 | 18 155 | Coût pour éviter un jour d'hospitalisa-tion | SR | ||||
Hascoet |
FRA 2006; 45 000 €/ AVAQ |
10 172 | 16 368 | cAVG |
Prématurés (<32 sAG) avec DBP (soins de santé) | Déterministe; probabiliste |
La prophylaxie du VRS par le PVZ chez les prématurés atteints de DBP ou de CPCHS peut être considérée comme étant rentable en France. |
| 20 788 | 33 450 | Prématurés (<32 sAG) avec cardiopathie (sociétal) | |||||
| 27 255 | 43 856 | Prématurés (<32 sAG) avec DBP (sociétal) | |||||
Lofland |
É.-U. 2000; NR |
1 008 | 1 693 | Coût par épisode d'infection par le VRS évité |
SR, prématurés (sAG NR), réduction de 81 % de l'incidence de l'infection par le VRS (5 % contre 26 %) | Déterministe |
Le coût différentiel par épisode d'infection à VRS évité variait de 0 (économies) à 39 591 $ pour une prophylaxie par PVZ de 2 500 $ et de 2 702 $ à 79 706 $ pour une prophylaxie par PVZ de 4 500 $. Les cliniciens peuvent utiliser ces renseignements pour établir si le traitement prophylactique par PVZ est rentable dans leur contexte de pratique clinique. |
| 39 591 | 66 494 | Prématurés (sAG NR), réduction de 50 % de l'incidence de l'infection par le VRS (5 % contre 10 %) | |||||
| Dominant | Dominant | Prématurés (sAG NR), réduction de 83 % de l'incidence de l'infection par le VRS (5 % contre 28 %) | |||||
Mahadevia 2012Note de bas de page 54 |
É.-U. 2010; NR (comparativement à 157 000 $/ AVAQ, du vaccin contre le méningococci-que) |
44 774 | 61 229 | cAVAQ gagnée |
Groupe 2, prématurés (32-35 sAG) avec FRNote de bas de page c | Déterministe |
Le PVZ est resté rentable pour les nourrissons à haut risque admissibles aux lignes directrices dans les secteurs public et privé. Les nourrissons admissibles aux lignes directrices comprenaient les nourrissons de <32 sAG, 32-34 sAG avec les FR de l'AAP 2009, et de 32-35 sAG avec les FR de l'AAP 2006. Le PVZ n'était pas rentable chez les nourrissons de 32–35 sAG avec 1 FR. |
| 79 477 | 108 685 | Groupe 3, prématurés (32-35 sAG) avec FRNote de bas de page d | |||||
| 464 476 | 635 172 | Groupe 4, prématurés (32-35 sAG) avec FRNote de bas de page e | |||||
| Dominant | Dominant | Groupe 1, prématurés (<32 sAG)Note de bas de page f | |||||
McGirr |
CAN 2013; 50 000 $/ AVAQ |
157 332 | 167 107 | cAVAQ gagnée |
FK à haut risque < 2 ans (risque élevé de maladie sévère attribuable au VRS) | Déterministe |
Le PVZ n'est pas rentable au CAN selon les seuils couramment utilisés. Toutefois, étant donné la rareté de la FK et l'impact budgétaire relativement faible, on peut l'envisager. |
| 652 560 | 693 105 | Tous les cas de FK < 2 ans | |||||
Neovius |
SWE 2009; 500 000 SEK/AVAQ |
148 293 | 22 765 | cAVAQ gagnée |
Prématurés (<29 sAG) ajoutant une respiration sifflante à l'asthme | Déterministe; probabiliste |
Sur la base d'une VP de 500 000 SEK/AVAQ, le PVZ s'est révélé rentable par rapport à l'absence de prophylaxie pour les nourrissons nés à <29 semaines si l'on suppose que l'infection sévère par le VRS augmente le risque ultérieur d'asthme ou de mortalité. |
| 195 420 | 30 000 | SR, Prématurés (<29 sAG) | |||||
| 383 825 | 58 922 | Prématurés (<29 sAG) à l'exclusion de l'effet indirect sur l'asthme | |||||
| 492 430 | 75 595 | Prématurés (<29 sAG) à l'exclusion de l'effet indirect sur la mortalité | |||||
| 8 856 829 | 1 359 641 | Prématurés (<29 sAG) en excluant l'effet indirect de la mortalité et de l'asthme | |||||
Nuijten |
DEU 2 006; 20 000 €/ AVAQ |
2 221 | 3 772 | cAVAQ gagnée |
SR, Paramètres d'étude CARDIAC, sociétal | Déterministe; probabiliste |
Cette analyse a montré que le PVZ représente un moyen rentable de prophylaxie contre l'infection sévère par le VRS nécessitant une hospitalisation chez les nourrissons atteints de CPCHS. |
| 9 528 | 16 184 | SR, paramètres d'étude CARDIAC, y compris l'asthme, le payeur | |||||
| 9 529 | 16 185 | SR, sociétal | |||||
| 11 126 | 18 898 | SR, paramètres d'étude CARDIAC, hors asthme, payeur | |||||
| 16 673 | 28 320 | SR, coûts médicaux directs (y compris l'asthme), payeur | |||||
| 18 266 | 31 025 | SR, coûts médicaux directs (hors asthme), payeur | |||||
| 123 439 | 209 666 | SR, hors mortalité, sociétal | |||||
Nuijten |
NLD 2006; 30 000 €/AVAQ |
7 067 | 11 668 | cAVAQ gagnée |
SR – CPC | Déterministe; probabiliste |
Le PVZ offre une prophylaxie rentable contre le VRS chez les nourrissons à haut risque. L'utilisation du PVZ chez ces enfants entraîne des avantages sanitaires et économiques à court et à long terme. |
| 11 336 | 18 717 | SR – prématurés (<35 sAG, amalgame) avec DBP (coûts totaux, sociétal) | |||||
| 18 563 | 30 650 | Prématurés (<35 sAG, amalgame) | |||||
| 20 236 | 33 412 | SR, prématurés (<35 sAG, amalgame) avec DBP | |||||
| 23 461 | 38 737 | Sous-populations DBP | |||||
| Dominant | Dominant | SR – CPC (coûts totaux, sociétal) | |||||
Nuijten |
2006 ESP; 30 000 €/ AVAQ |
6 498 | 12 710 | cAVAQ gagnée |
SR, inclusion des coûts du traitement des séquelles chez les prématurés (<32 sAG) | Déterministe; probabiliste |
Le PVZ constitue une méthode rentable de prophylaxie contre les maladies sévères attribuables au VRS chez les prématurés en Espagne. |
| 12 814 | 25 065 | SR, prématurés (<32 sAG) | |||||
| Dominant | Dominant | SR, prématurés (<32 sAG), perspective sociétale | |||||
Nuijten |
GB 2003; 25 000 £/ AVAQ |
6 664 | 14 891 | cAVAQ gagnée |
CPC | Déterministe; probabiliste |
Cette étude suggère que la prophylaxie par PVZ contre l'infection sévère par le VRS chez les enfants à haut risque peut être rentable du point de vue du NHS. |
| 11 494 | 25 684 | SR, prématurés (<35 sAG) avec coûts indirects (sociétaux) | |||||
| 14 883 | 33 257 | Prématurés (<35 sAG) | |||||
| 16 720 | 37 362 | SR, prématurés (<35 sAG) avec DBP | |||||
| 20 953 | 46 821 | DBP seulement | |||||
AUT 2010; 40 693 €/ |
3 045 | 4 949 | cAVAQ gagnée |
SR, CPC, y compris le traitement des sifflements récurrents, sociétal | Déterministe |
Nos résultats basés sur des données épidémiologiques à long terme à l'échelle nationale suggèrent que le PVZ est rentable dans la prévention de la maladie à VRS chez les nourrissons à haut risque. |
|
| 7 818 | 12 706 | SR, CPC, y compris le traitement des sifflements récurrents | |||||
| 8 484 | 13 788 | SR, CPC | |||||
| 15 800 | 25 678 | SR, pour tous les prématurés (<35 sAG, amalgame), y compris le traitement des sifflements récurrents, sociétal | |||||
| 15 992 | 25 990 | SR, prématurés (33-35 sAG), y compris le traitement des sifflements récurrents, sociétal | |||||
| 17 554 | 28 529 | SR, DBP, y compris le traitement des sifflements récurrents, sociétal | |||||
| 18 133 | 29 470 | SR, prématurés (<33 sAG), y compris le traitement des sifflements récurrents, sociétal | |||||
| 21 669 | 35 216 | SR, pour tous les prématurés (<35 sAG, amalgame), y compris le traitement des sifflements récurrents | |||||
| 21 862 | 35 530 | SR, prématurés (33-35 sAG), y compris le traitement des sifflements récurrents | |||||
| 22 515 | 36 591 | SR, DBP, y compris le traitement des sifflements récurrents | |||||
| 23 833 | 38 733 | SR, prématurés (<33 sAG), y compris le traitement des sifflements récurrents | |||||
| 24 392 | 39 642 | SR, prématurés (33-35 sAG) | |||||
| 24 654 | 40 068 | SR, DBP | |||||
| 26 212 | 42 600 | SR, pour tous les prématurés (<35 sAG, amalgame) | |||||
| 26 292 | 42 730 | SR, prématurés (<33 sAG) | |||||
Rietveld |
NLD 2000; NR (1 325 $ à 8 700 $, moyenne de 5 787 $/ hospitalisa-tion) |
13 190 | 24 875 | cHE |
Nourrisson de sexe masculin, prématuré (< 28 sAG), poids de naissance < 2 500 g, avec DBP (décembre) | Déterministe |
Les coûts mensuels par HE étaient plus élevés pour les enfants sans DBP et les enfants dont l'AG était plus élevé. Les coûts différentiels par HE étaient toujours élevés. L'immunisation passive était toujours la plus rentable en décembre. Il est donc recommandé d'adopter une politique de vaccination restrictive en ne vaccinant les enfants atteints de DBP que pendant les mois à haut risque. Les coûts de l'immunisation passive devraient être considérablement réduits pour atteindre un bon rapport CE. |
| 30 795 | 58 076 | Nourrisson de sexe masculin, prématuré (< 28 sAG), poids de naissance < 2 500 g, avec DBP (janvier) | |||||
| 31 055 | 58 567 | Nourrisson de sexe masculin, prématuré (< 28 sAG), poids de naissance < 2 500 g, avec DBP (novembre) | |||||
| 47 145 | 88 911 | Nourrisson de sexe masculin, prématuré (< 28 sAG), poids de naissance < 2 500 g, avec DBP (février) | |||||
| 105 120 | 198 246 | Nourrisson de sexe masculin, prématuré (< 28 sAG), poids de naissance < 2 500 g, avec DBP (mars) | |||||
| 395 860 | 746 554 | Nourrisson de sexe masculin, prématuré (< 28 sAG), poids de naissance < 2 500 g, avec DBP (avril) | |||||
| 833 695 | 1 572 268 | Nourrisson de sexe masculin, prématuré (< 28 AG), poids de naissance < 2 500 g, avec DBP (octobre) | |||||
Roeckl-Wiedmann 2003Note de bas de page 36 |
DEU 2 000; NR |
6 639 | 11 821 | cHE |
Groupe A, prématurés (<35 sAG)Note de bas de page g | Déterministe |
En raison des conclusions de notre analyse de CE, nous recommandons une utilisation restreinte de la prophylaxie par PVZ chez les prématurés atteints de MPC dans leur combinaison de risque. Les résultats de cette analyse CE ne justifient pas l'utilisation généralisée du PVZ chez les prématurés. Le PVZ était le plus rentable pour les nourrissons de sexe masculin atteints de MPC qui avaient des frères et sœurs fréquentant des groupes de garderie, et qui sont sortis de l'hôpital entre octobre et décembre. |
| 25 288 | 45 028 | Groupe B, prématurés (<35 sAG) avec FRNote de bas de page h | |||||
| 52 838 | 94 084 | Groupe C, prématurés (<35 sAG) avec FRNote de bas de page i | |||||
| 204 684 | 364 462 | Groupe D, prématurés (<35 sAG) avec FRNote de bas de page j | |||||
Salinas-Escudero 2012Note de bas de page 38 |
É.-U. 2009; 50 000 $/ AVAQ, et 3x le PIB/ habitant |
4 539 | 6 216 | cAVAQ gagnée |
Couverture partielle, prématurés (< 29 sAG) | Déterministe; probabiliste |
La prophylaxie par le PVZ pour les nouveau-nés prématurés nés ≤ 32 semaines a donné lieu à une solution de rechange rentable. Lorsque l'on évalue le RCED/AVAQ et AVG par rapport au seuil de 50 000 $ USD, toutes les tranches d'âge du groupe prophylactique sont rentables. |
| 7 294 | 9 989 | Couverture partielle, prématurés (29-32 sAG) | |||||
| 17 532 | 24 009 | Couverture complète, prématurés (<29 sAG) | |||||
| 20 760 | 28 429 | Couverture complète, prématurés (29-32 sAG) | |||||
Sanchez-Luna 2017Note de bas de page 39 |
2016 ESP; 30 000 €/ AVAQ |
11 550 | 22 173 | cAVAQ gagnée |
Sous-groupe A (payeur),prématurés (32-35 sAG) avec FR : 2 majeurs, 2 mineursNote de bas de page k | Déterministe; probabiliste |
Parmi 1 000 simulations pour Monte Carlo, 85,70 % des cas présentaient un RCUD inférieur à 30 000 €/AVAQ. Le PVZ est efficace pour prévenir les infections à VRS chez les prématurés de 32-35 sAG en Espagne, y compris dans des sous-groupes précis à haut risque. |
| 14 177 | 27 216 | Sous-groupe B (payeur),prématurés (32-35 sAG) avec FR : 2 majeurs, 1 mineurNote de bas de page l | |||||
| 17 153 | 32 930 | SR (sociétal), prématurés (32-35 sAG) | |||||
| 18 938 | 36 356 | Sous-groupe C (payeur), prématurés (32-35 sAG) avec FR : 2 FR majeursNote de bas de page m | |||||
| 19 698 | 37 815 | SR (payeur), prématurés (32-35 sAG) | |||||
| Schmidt 2017Note de bas de page 40 |
2016 ESP; 30 000 €/ AVAQ | 15 748 | 30 232 | cAVAQ gagnée | SR | Déterministe; probabiliste | PSA a démontré que la probabilité de la prophylaxie par PVZ rentable à un seuil de 30 000 €/AVAQ était de 92,7 %. Le RCED est resté en dessous de ce seuil pour la plupart des analyses de scénarios extrêmes. La prophylaxie par le PVZ s'est révélée être une intervention de santé rentable selon les normes de rentabilité communément admises en Espagne (RCED inférieur au seuil de 30 000 €/ AVAQ). |
CAN 2010; 50 000 $/ AVAQ |
192 | 215 | cAVAQ gagnée |
Prématurés (32-35 sAG), au moins quatre FR | Déterministe; probabiliste |
Les RCED du PVZ sont restés assez stables de 2007 à 2010. La recommandation initiale indiquant que le PVZ est rentable chez les nourrissons nés entre 32 et 35 sAG présentant au moins 2 FR, ou présentant un risque modéré à élevé selon un modèle d'évaluation du risque, ne change pas. |
|
| 5 274 | 5 906 | Prématurés (32-35 sAG), outil d'évaluation du risque, risque élevé (65-100) | |||||
| 20 814 | 23 309 | SR, prématurés (32-35 sAG), (y compris l'asthme) | |||||
| 26 701 | 29 901 | Prématurés (32-35 sAG), trois FR | |||||
| 31 360 | 35 119 | SR, prématurés (32-35 sAG), (hors asthme) | |||||
| 34 438 | 38 566 | Prématurés (32-35 sAG), outil d'évaluation du risque, risque moyen (résultat de 49-64) | |||||
| 48 495 | 54 308 | SR, prématurés (32-35 sAG), taux de mortalité (1,2 %) | |||||
| 50 434 | 56 479 | SR, prématurés (32-35 sAG), taux de mortalité (1,0 %) | |||||
| 82 732 | 92 649 | Prématurés (32-35 sAG), 2 FR | |||||
| 146 218 | 163 744 | Prématurés (32-35 sAG), un FR | |||||
| 183 561 | 205 563 | Prématurés (32-35 sAG), outil d'évaluation du risque, faible risque (résultat de 0-48) | |||||
| 820 701 | 919 073 | Prématurés (32-35 sAG), zéro FR (prématurés seulement) | |||||
Tam 2009Note de bas de page 42 |
CAN 2007; 50 000 à 75 000 $/ |
334 | 391 | cAVAQ gagnée |
Haut risque < 1 an | Déterministe; probabiliste |
Le PVZ est une option rentable pour la prévention du VRS chez les nourrissons inuits de l'île de Baffin, est très rentable chez les nourrissons de l'Arctique âgés de moins d'un an résidant précisément hors d'Iqaluit et constitue une stratégie dominante pour les enfants de moins de 6 mois dans les régions éloignées. Toutefois, le PVZ n'est pas rentable par rapport à l'absence de traitement pour les nourrissons de tous âges résidant à Iqaluit. |
| 7 822 | 9 154 | Baffin < 6 mois, sociétal | |||||
| 10 190 | 11 925 | Baffin < 6 mois | |||||
| 22 383 | 26 195 | En dehors d'Iqaluit (régions éloignées) < 1 an, sociétal | |||||
| 24 750 | 28 965 | À l'extérieur d'Iqaluit (régions éloignées) < 1 an | |||||
| 37 070 | 43 383 | Tous les nourrissons de l'île de Baffin < 1 an, sociétal | |||||
| 39 435 | 46 151 | Tous les nourrissons de l'île de Baffin < 1 an | |||||
| 100 872 | 118 052 | Résidant à Iqaluit <6 mois, sociétal | |||||
| 103 235 | 120 817 | Résidant à Iqaluit <6 mois | |||||
| 149 782 | 175 291 | Résidant à Iqaluit <1 an, sociétal | |||||
| 152 145 | 178 057 | Résidant à Iqaluit <1 an | |||||
| Dominant | Dominant | Nourrissons éloignés < 6 mois | |||||
| Dominant | Dominant | Risque élevé < 6 mois | |||||
| Dominant | Dominant | Risque élevé < 1 an, sociétal | |||||
| Dominant | Dominant | Nourrissons éloignés < 6 mois, sociétal | |||||
| Dominant | Dominant | risque élevé < 6 mois, sociétal | |||||
Vogel |
NZL 2000; NR |
28 700 | 33 376 | Coût par cas évité |
Prématurés (32-35 sAG) avec MPC, sortis de l'hôpital sous oxygène | Déterministe |
Si l'on accorde de l'importance à la prévention de la morbidité, les groupes prioritaires pour la prophylaxie par PVZ sont les prématurés sortis de l'hôpital sous oxygène, suivis des prématurés de 28 sAG ou moins. |
| 32 000 | 37 213 | Prématurés (<=28 sAG), pas de MPC | |||||
| 60 000 | 69 775 | Cohorte totale, prématurés (32-35 sAG) avec MPC, sociétal | |||||
| 65 000 | 75 590 | Prématurés (<=28 sAG) avec MPC | |||||
| 98 000 | 113 966 | Prématurés (29-31 sAG), pas de MPC | |||||
| 166 700 | 193 859 | Prématurés (29-31 sAG) avec MPC | |||||
Wang 2008Note de bas de page 14 |
GB 2006; 30 000 £/ AVAQ |
51 800 | 107 070 | cHE | Prématurés (<35 sAG) et enfants sans MPC | Déterministe |
Selon ce modèle, la prophylaxie par PVZ n'est pas une stratégie rentable pour les prématurés et les enfants atteints de CPC par rapport à l'absence de prophylaxie, tant du point de vue du NHS que de la société. Ces résultats résistent aux analyses probabilistes et autres analyses de sensibilité. La prophylaxie par le PVZ n'est pas non plus une stratégie rentable pour les prématurés ou les nourrissons atteints de MPC qui ne présentent aucun autre FR. Les analyses de sous-groupes ont montré que la prophylaxie par le PVZ chez les enfants atteints de MPC peut être rentable, à un seuil de VP de 30 000 £/AVAQ. |
| 63 800 | 131 874 | cAVAQ gagnée |
Prématurés (<35 sAG) et enfants atteints de MPC | ||||
| 66 900 | 138 282 | Prématurés (<35 sAG) et enfants atteints de MPC (sociétal) | |||||
| 67 600 | 139 729 | cHE |
Prématurés (<35 sAG) et enfants atteints de MPC | ||||
| 78 600 | 162 466 | CPC | |||||
| 79 800 | 164 946 | cAVAQ gagnée |
CPC | ||||
| 83 200 | 171 974 | CPC (sociétal) | |||||
| 454 100 | 938 623 | Prématurés (<35 sAG) et enfants sans MPC | |||||
| 475 600 | 983 064 | Prématurés (<35 sAG) et enfants sans MPC (sociétal) | |||||
Weiner |
É.-U. 2010; 157 000 $/ AVAQ (RCED le plus élevé pour le vaccin contre le méningococ-cique) |
16 037 | 21 931 | cAVAQ gagnée |
SR Groupe 2, prématurés (32-34 sAG) avec FRNote de bas de page n | Déterministe; probabiliste |
Le PVZ, lorsqu'il était dosé conformément à l'étiquetage approuvé par la FDA, était soit économique, soit rentable chez les nourrissons actuellement admissibles aux lignes directrices dans la population Medicaid. Le PVZ n'a pas démontré son rapport CE chez les nourrissons de 32-35 sAG avec <=1 FR. |
| 38 244 | 52 299 | SR Groupe 3, prématurés (32-35 sAG) avec FRNote de bas de page o | |||||
| 281 892 | 385 488 | SR Groupe 4, prématurés (32-35 sAG) avec FRNote de bas de page p | |||||
| Dominant | Dominant | SR Groupe 1, prématurés (<32 sAG)Note de bas de page q | |||||
| Yount 2004Note de bas de page 45 |
É.-U. 2002; NR | 114 337 | 183 401 | cAVAQ gagnée | SR, temporaire, CPC | Déterministe | Le coût de la prophylaxie par PVZ était élevé par rapport aux bénéfices réalisés. Compte tenu du grand nombre de patients atteints de CPC qui pourraient être considérés comme des candidats à la prophylaxie du VRS (>6 000 patients par an aux É.-U.), l'utilisation systématique du PVZ chez les jeunes enfants atteints de CPC doit être évaluée davantage. |
Définitions : AC, âge chronologique; AG, âge gestationnel; AUT, Autriche; AVAQ, année de vie ajustée par la qualité; AVG, année de vie gagnée; CAD, dollar canadien; CAN, Canada; cAVAQ, coût d'année de vie ajustée par la qualité; cAVG, coût par année de vie gagnée; CE, coût-efficacité; cHE, coût par hospitalisation évitée; CPC, cardiopathie congénitale; CPCHS, cardiopathie congénitale hémodynamiquement significative; DBP, dysplasie broncho-pulmonaire; DEU, Allemagne; ESP, Espagne; É.-U., États-Unis; EUR, euros; FDA, Food and Drug Administration; FK, fibrose kystique; FR, facteurs de risque; FRA, France; GBP, livres sterling; GBR : Grande-Bretagne; HE, hospitalisation évitée; ITA, Italie; MPC, maladie pulmonaire chronique; NHS, National Health Service; NLD, Pays-Bas; NR, non rapporté; NZD, dollars néo-zélandais; NZL, Nouvelle-Zélande; PVZ, palivizumab; RCED, rapport coût-efficacité différentiel; RCUD, rapport coût-utilité différentiel; sAG, semaines d'âge gestationnel; SEK, couronne suédoise; SR, scénario de référence; SWE, Suède; TNO, Territoires du Nord-Ouest; USD, dollars US; VP, volonté de payer; VRS, virus respiratoire syncytial. Notes de bas de table
|
|||||||
Perspective |
DBP/MPC |
CPC |
Prématuré |
Prématuré avec DBP/MPC |
Prématuré avec FRNote de bas de page a |
FK |
Arctique canadienNote de bas de page b |
|
|---|---|---|---|---|---|---|---|---|
| Tous les nourrissons | Zones à haut risque | |||||||
| Le point de vue du payeur | ||||||||
| Nombre d'estimations | 6 | 10 | 22 | 4 | 14 | 2 | 6 | 2 |
| RCED (minimum) | 4 786 | 11 668 | 6 216 | 15 202 | 215 | 167 107 | Dominant | Dominant |
| RCED (maximum) | 46 821 | 164 946 | 938 623 | 131 874 | 205 563 | 693 105 | 178 057 | 391 |
| Proportion d'estimations qui permettent de réduire les coûts | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,17 | 0,50 |
| Proportion d'estimations de rentabilité inférieures à 50 000 $/AVAQ | 1,00 | 0,80 | 0,82 | 0,75 | 0,64 | 0,0 | 0,67 | 1,00 |
| Proportion d'estimations de rentabilité inférieures à 100 000 $/AVAQ | 1,00 | 0,90 | 0,86 | 0,75 | 0,86 | 0,0 | 0,67 | 1,00 |
| Proportion d'estimations de rentabilité inférieures à 200 000 $/AVAQ | 1,00 | 1,00 | 0,91 | 1,00 | 0,92 | 0,50 | 1,00 | 1,00 |
| Perspective sociétale | ||||||||
| Nombre d'estimations | 1 | 8 | 23 | 3 | 6 | 0 | 6 | 2 |
| RCED (minimum) | 28 529 | Dominant | Dominant | 18 717 | 21 931 | s. o. | Dominant | Dominant |
| RCED (maximum) | 28 529 | 209 666 | 2 975 489 | 138 282 | 635 172 | s. o. | 175 291 | Dominant |
| Proportion d'estimations qui permettent de réduire les coûts | 0,0 | 0,13 | 0,13 | 0,0 | 0,0 | s. o. | 0,17 | 1,00 |
| Proportion d'estimations de rentabilité inférieures à 50 000 $/AVAQ | 1,00 | 0,63 | 0,39 | 0,67 | 0,17 | s. o. | 0,67 | 1,00 |
| Proportion d'estimations de rentabilité inférieures à 100 000 $/AVAQ | 1,00 | 0,63 | 0,48 | 0,67 | 0,50 | s. o. | 0,67 | 1,00 |
| Proportion d'estimations de rentabilité inférieures à 200 000 $/AVAQ | 1,00 | 0,88 | 0,52 | 1,00 | 0,67 | s. o. | 1,00 | 1,00 |
Remarque : Tous les RCED sont exprimés en CAD de 2017/AVAQ. Définitions : AVAQ, année de vie ajustée par la qualité; CPC, cardiopathie congénitale; DBP, dysplasie bronchopulmonaire; FK : fibrose kystique; FR, facteur de risque; MPC, maladie pulmonaire chronique, RCED, rapport coût-efficacité différentiel, s. o., sans objet. Notes de bas de table
|
||||||||
| Auteurs, année | Dosage | Coût par unité (non ajusté) | Hospitalisation | Mortalité | Séquelles-VRS | Conclusions | ||
| PVZ | Non PVZ | Réduction (%) | ||||||
|---|---|---|---|---|---|---|---|---|
| Tam et al., 2009 | 5 (par saison) | Coût unitaire du flacon : NR; $220/kg nourrisson |
1,4 - 11,4 % | 6,3 - 51,2 % | 78 % | 1 % (les 2 groupes) | N | Du point de vue du payeur, le PVZ est rentable pour tous les nourrissons de l'île de Baffin < 1 an d'AC (RCED : 46 151 $/AVAQ), les nourrissons à haut risque de VRS (391 $/AVAQ), les nourrissons des régions éloignées (28 965 $/AVAQ), les nourrissons de moins de 6 mois des régions éloignées ou à haut risque de VRS (dominant). Il n'était pas rentable pour les nourrissons < 12 mois résidents à Iqaluit. |
| Smart et al., 2010 | 5,39 flacons (par saison) | 50 mg : 752 $ 100 mg : 1 505 $ |
1,8 % | 10,0 % | NR (82 % de calcul rétroactif) | 3,9 % (les 2 groupes)Note de bas de page a | O | Du point de vue du payeur, le PVZ est rentable pour les prématurés lorsqu'il exclut l'asthme (35 119 $/AVAQ), et lorsqu'il inclut l'asthme (23 309 $/AVAQ). |
| Harris et al., 2011 | 4,5 (par saison) | 100 mg : 1 468 $ | 1,7 % | 2,9 % | NR (42 % de calcul rétroactif) | NR; 0,2 % (1/41, pas de PVZ); 0% (0/292, PVZ) | N | D'un point de vue sociétal, le PVZ chez les nourrissons atteints de CPC : RCED de 18 155 $/jour d'HE. Aucun seuil n'a été utilisé, mais l'étude a conclu que cette stratégie était rentable pour la population de nourrissons atteints de CPC. |
| Banerji et al., 2016 | 6; (par mois, hyp. maximale) | Coût unitaire du flacon : NR; $226/kg enfant | NR | NR | 96 % | NR | N | Du point de vue du payeur, les 2 scénarios de programme PVZ proposés étaient tous 2 rentables dans certaines régions de l'Arctique canadien, mais pas dans toutes (fourchette de RCED, dominante à 45 060 $/AVAQ). Le PVZ est rentable dans ces régions pour les nourrissons à terme en raison des coûts élevés des hospitalisations. |
| McGirr et al., 2017 | 5 (mensuel sur une saison de 5 mois) | 100 mg : 1 505 $ | 1,7 % (en supposant une réduction de 55 %)Note de bas de page b | 3,8 % | 55 % | NR (décès lié à la FK utilisé) | Y (FK) | Il est peu probable que le PVZ soit rentable pour tous les nourrissons atteints de FK (RCED : 693 105 $/AVAQ) et pour les nourrissons à haut risque atteints de FK (RCED : 167 107 $/AVAQ). |
Définitions : AC, âge chronologique; AVAQ, année de vie ajustée par la qualité; CPC, cardiopathie congénitale; FK, fibrose kystique; HE, hospitalisation évitée; N, non; NR, non rapporté; O, oui; PVZ, palivizumab; RCED, rapport coût-efficacité différentiel; VRS, virus respiratoire syncytial. Notes de bas de table
|
||||||||
Documents supplémentaires
| Section/sujet | No | Élément de la liste de vérification | Rapporté à la page no |
Titre |
|||
| Titre | 1 | Indiquer le rapport comme étant un examen systématique, une méta-analyse, ou les deux. | 1 |
Résumé |
|||
| Sommaire structuré | 2 | Fournir un sommaire structuré comprenant, le cas échéant : le contexte; les objectifs; les sources de données; les critères d'admissibilité de l'étude, les participants et les interventions; les méthodes d'évaluation et de synthèse de l'étude; les résultats; les limites; les conclusions et les implications des principaux résultats; le numéro d'enregistrement de l'examen systématique. | 4-5 |
Introduction |
|||
| Justification | 3 | Décrire la raison d'être de l'examen dans le contexte de ce qui est déjà connu. | 6 |
| Objectifs | 4 | Fournir un énoncé explicite des questions abordées en faisant référence aux participants, aux interventions, aux comparaisons, aux résultats et au plan de l'étude (PICOS). | 6 |
Méthodes |
|||
| Protocole et enregistrement | 5 | Indiquer si un protocole d'examen existe, s'il peut et où il peut être consulté (p. ex., l'adresse Internet) et, s'il est disponible, fournir les renseignements d'enregistrement, y compris le numéro d'enregistrement. | 7 |
| Critères d'admissibilité | 6 | Préciser les caractéristiques de l'étude (p. ex., PICOS, durée du suivi) et les caractéristiques du rapport (p. ex., années considérées, langue, statut de publication) utilisées comme critères d'admissibilité, en donnant une justification. | 7 |
| Sources d'information | 7 | Décrire toutes les sources d'information (p. ex., les bases de données avec les dates de couverture, les contacts avec les auteurs des études pour cibler des études supplémentaires) dans la recherche et la date de la dernière recherche. | 6-7 |
| Recherche | 8 | Présenter la stratégie de recherche électronique complète pour au moins une base de données, y compris les limites utilisées, de sorte qu'elle puisse être répétée. | Supplémentaire 2 |
| Sélection des études | 9 | Indiquer le processus de sélection des études (c.-à-d., sélection, admissibilité, inclusion dans l'examen systématique et, le cas échéant, inclusion dans la méta-analyse). | 7-8 |
| Processus de collecte des données | 10 | Décrire la méthode d'extraction des données des rapports (p. ex., formulaires pilotés, indépendamment, en double) et tout processus d'obtention et de confirmation des données auprès des enquêteurs. | 7-8 |
| Éléments de données | 11 | Énumérer et définir toutes les variables pour lesquelles des données ont été recherchées (p. ex., PICOS, sources de financement) et toutes les hypothèses et simplifications faites. | 7-8 |
| Risque de biais dans les études individuelles | 12 | Décrire les méthodes utilisées pour évaluer le risque de biais des études individuelles (en précisant si cela a été fait au niveau de l'étude ou du résultat), et comment ces renseignements seront utilisés dans toute synthèse de données. | 7-8 |
| Mesures de synthèse | 13 | Indiquer les principales mesures de synthèse (p. ex., le rapport de risque, la différence de moyennes). | 7-8 |
| Synthèse des résultats | 14 | Décrire les méthodes de traitement des données et de combinaison des résultats des études, le cas échéant, y compris les mesures de cohérence (p. ex., I2) pour chaque méta-analyse. | 7-8 |
| Risque de biais dans les études | 15 | Préciser toute évaluation du risque de biais qui pourrait affecter les données probantes cumulées (p. ex., biais de publication, rapports sélectifs au sein des études). | s. o. |
| Analyses complémentaires | 16 | Décrire les méthodes d'analyses supplémentaires (p. ex., analyses de sensibilité ou de sous-groupes, méta-régression), si elles ont été effectuées, en indiquant celles qui ont été pré-spécifiées. | 7-8 |
Résultats |
|||
| Sélection des études | 17 | Indiquer le nombre d'études sélectionnées, évaluées pour leur admissibilité et incluses dans l'examen, avec les raisons des exclusions à chaque étape, idéalement avec un organigramme. | 8 |
| Caractéristiques de l'étude | 18 | Pour chaque étude, présenter les caractéristiques pour lesquelles les données ont été extraites (p. ex., taille de l'étude, PICOS, période de suivi) et fournir les citations. | 8 |
| Risque de biais dans les études | 19 | Présenter les données sur le risque de biais de chaque étude et, s'il y a lieu, toute évaluation du niveau de résultat (voir le point 12). | 8 |
| Résultats des études individuelles | 20 | Pour tous les résultats considérés (avantages ou inconvénients), présenter, pour chaque étude : (a) des données sommaires simples pour chaque groupe d'intervention; (b) des estimations de l'effet et des intervalles de confiance, idéalement avec un graphique en forêt. | 8-13 |
| Synthèse des résultats | 21 | Présenter les résultats de chaque méta-analyse effectuée, y compris les intervalles de confiance et les mesures de cohérence. | s. o. |
| Risque de biais dans les études | 22 | Présenter les résultats de toute évaluation du risque de biais entre les études (voir le point 15). | s. o. |
| Analyse complémentaire | 23 | Indiquer les résultats d'analyses complémentaires, le cas échéant (p. ex., analyses de sensibilité ou de sous-groupes, méta-régression [voir le point 16]). | 9-13 |
Discussion |
|||
| Sommaire des données probantes | 24 | Résumer les principales conclusions, y compris la probité des données probantes pour chaque résultat principal; tenir compte de leur pertinence pour les groupes clés (p. ex., les professionnels de la santé, les utilisateurs et les décideurs). | 13-15 |
| Limites | 25 | Discuter des limites de l'étude et des résultats (p. ex., le risque de biais), et de l'examen (p. ex., l'extraction incomplète de la recherche établie, le biais de rapport). | 15 |
| Conclusions | 26 | Fournir une interprétation générale des résultats dans le contexte d'autres données probantes, et des implications pour les recherches futures. | 15-16 |
Financement |
|||
| Financement | 27 | Décrire les sources de financement de l'examen systématique et les autres soutiens (p. ex., la fourniture de données); le rôle des bailleurs de fonds de l'examen systématique. | 3 |
De : Moher D, Liberati A, Tetzlaff J, Altman DG, The PRISMA Group (2009). Preferred Reporting Items for Systematic Reviews and Meta-Analyses : The PRISMA Statement. PLoS Med 6(7) : e1000097. doi:10.1371/journal.pmed1000097. |
|||
Annexe 2. Stratégie de recherche
| Numéro | Recherches | Résultats |
|---|---|---|
| 1 | exp Anticorps, Monoclonaux/ou exp agents antiviraux/ou exp immunoglobulines/ou (protéine d'anticorps ou agent antiviral* ou médicament antiviral* ou agent antiviral* ou médicament antiviral* ou substance antivirale ou antiviraux ou agent antivirus* ou médicament antivirus* ou anti-RSV ou anticorps clonal ou endobuline ou flebogamma ou flebogammadif ou gamastan ou gamimmune ou gamimune ou gamma globuline* ou gamma-globuline* ou gammaglobuline* ou gammar ou gamuline ou globuman ou anticorps humanisé ou anticorps monoclonal humanisé ou anticorps d'hybridome ou Ig ou igam ou igc ou immunoglobuline ou immunoglobine ou immunoglobuline* ou immunosérum globuline* ou immuno gamma globuline* ou immunogammaglobuline* ou immunoglobine* ou immunoglobuline* ou immunoprotéine* ou intragam ou intraglobine f ou isiven ou iveegam ou ivega ou mAbs ou MEDI 493 ou anticorps monoclonal ou anticorps monoclonal ou palivizumab ou panglobuline* ou immunisation passive ou sandoglobine* ou sandoglobuline* ou synagis ou tegelin* ou veinoglobuline* ou venoglobuline* ou inhibiteur viral ou agent virostatique* ou agent virucide* ou agent virustatique* ou vivaglobine). tw, kf, nm. | 1 043 332 |
| 2 | infections par le virus respiratoire syncytial/pc | 1417 |
| 3 | infections par le virus respiratoire syncytial/ou virus respiratoire syncytial humain/ou virus respiratoire syncytial/ou (virus respiratoire syncytial* ou VRS*). tw. | 18 025 |
| 4 | prophylaxie/ou (contrôle ou protection de la santé ou immunoprophylaxie ou prévention ou mesures préventives ou médicament préventif ou thérapie préventive ou traitement préventif ou institution prophylactique ou gestion prophylactique ou médicament prophylactique ou thérapie prophylactique ou traitement prophylactique ou prophylaxie). tw. | 2 762 004 |
| 5 | 2 ou (3 et 4) | 4221 |
| 6 | et/1,5 | 1760 |
| 7 | exp Infant/ or exp Child/ or Gestational Age/ or exp Pediatrics/ or Schools, Nursery/ or (infant* or infancy or newborn* or baby* or babies or neonat* or preterm* or prematur* or preemie* or gestation* or gestational age or child or children or preschool* or kid or kids or toddler* or pediatric* or paediatric* or peadiatric* or nursery school*).tw. | 3053948 |
| 8 | Économie/ | 26 937 |
| 9 | exp "Coûts et analyse des coûts"/ | 217482 |
| 10 | Économie, soins infirmiers/ | 3981 |
| 11 | Économie, Médecine/ | 8964 |
| 12 | Economie, Pharmaceutique/ | 2794 |
| 13 | exp Economie, Hôpital/ | 23 019 |
| 14 | Économie, Dental/ | 1897 |
| 15 | exp "Frais et charges"/ | 29 368 |
| 16 | exp Budgets/ | 13 335 |
| 17 | budget*.ti,ab,kf. | 26174 |
| 18 | (économique* ou coût ou coûts ou coûteux ou coûtant ou prix ou prix ou prix ou pharmacoéconomique* ou pharmaco-économique* ou dépenses ou dépenses ou frais ou dépenses ou financier ou finances ou financé).ti,kf. | 202619 |
| 19 | (économique* ou coût ou coûts ou coûteux ou coûtant ou prix ou prix ou prix ou pharmacoéconomique* ou pharmaco-économique* ou dépenses ou dépenses ou frais ou dépenses ou financier ou finances ou financé).ab. /freq=2 | 246 788 |
| 20 | (cost* adj2 (effective* ou utilit* ou benefit* ou minimi* ou analy* ou outcome ou outcomes)).ab,kf. | 138081 |
| 21 | (valeur adj2 (argent ou monétaire)).ti,ab,kf. | 2025 |
| 22 | modèles exp, économiques/ | 13 464 |
| 23 | modèle économique*. ab, kf. | 2837 |
| 24 | chaînes de markov/ | 12 909 |
| 25 | markov.ti, ab, kf. | 19 178 |
| 26 | méthode monte carlo/ | 25 573 |
| 27 | monte carlo.ti, ab, kf. | 43 481 |
| 28 | exp Théorie de la décision/ | 11 145 |
| 29 | (décision* adj2 (arbre* ou analyse* ou modèle*)).ti,ab,kf. | 19525 |
| 30 | ou/8-29 | 647 482 |
| 31 | et/6-7, 30 | 230 |
| 32 | exp australie/ ou autriche/ ou exp états baltes/ ou exp belgique/ ou exp canada/ ou chili/ ou république tchèque/ ou exp "pays scandinaves et nordiques"/ ou exp france/ ou exp allemagne/ ou grèce/ ou hongrie/ ou exp irlande/ ou israel/ ou exp italie/ ou exp japon/ ou exp république de corée/ ou luxembourg/ ou mexico/ ou exp pays-bas/ ou exp nouvelle zélande/ ou pologne/ ou exp portugal/ ou slovaquie/ ou slovénie/ ou exp espagne/ ou exp suisse/ ou turquie/ ou exp royaume-uni/ ou exp états-unis/ ou (australie* ou nouvelle galles du sud ou queensland ou tasmanie ou victoria ou sydney ou melbourne ou brisbane ou autriche* ou vienne ou viennois* ou belgique* ou belge* ou bruxelles ou flamand* ou canad* ou ottawa* ou colombie britannique* ou colombie britannique* ou vancouver* ou alberta* ou edmonton* ou calgar* ou saskatchewan* ou regina* ou saskatoon* ou manitoba* ou winnipeg* ou ontari* ou toronto* ou quebec* ou montreal* ou nouveau brunswick* ou nouveau brunswick* ou fredericton* ou nova scotia* ou nouvelle ecosse* ou halifax* ou haligonian* ou prince edward island* ou ile du prince edouard* ou pei ou charlottetown* ou newfoundland* ou terre neuve* ou labrador* ou nfld ou yukon* ou whitehorse* ou northwest territor* ou territoires du nord ouest* ou nwt ou yellowknife* ou nunavut* ou iqaluit* ou chile* ou santiago ou tchèque* ou prague ou danemark* ou danois ou danois* ou féroé* ou copenhague ou estonie* ou tallinn ou finlande* ou finnois* ou helsinki* ou france* ou français* ou paris* ou marseille ou lyon ou lille ou nice ou toulouse ou bordeaux ou allemagne* ou deutschland* ou berlin* ou hambourg ou munich ou cologne ou francfort ou stuttgart ou dusseldorf ou grèce* ou hellénique* ou grecque* ou athènes ou macédoine* ou hongrie* ou hongroise* ou budapest ou iceland* ou reykjavik ou ireland* ou irish* ou dublin* ou israel* ou jerusalem ou tel aviv ou italy ou italian* ou rome ou milan ou naples ou turin ou sicily ou japan* ou tokyo ou yokohama ou osaka ou nagoya ou sapporo ou kobe ou kyoto ou korea* ou seoul ou busan ou daegu ou daejeon ou gwangju ou incheon ou ulsan ou lettonie* ou riga ou lituanie* ou vilnius ou luxembourg* ou pays-bas* ou hollande* ou néerlandais* ou amsterdam ou rotterdam ou hague ou nouvelle-zélande* ou aotearoa ou wellington ou auckland ou maori ou mexic* ou norvège* ou norwegian* ou oslo ou pologne* ou polonais ou warsaw ou krakow ou wroclaw ou lodz ou portug* ou lisbonne ou slovaque* ou bratislava ou slovénie* ou slovène* ou ljubljana ou espagne* ou espagnol* ou espagnol* ou madrid ou barcelone ou catalonia* ou valencia* ou seville ou zaragoza ou malaga ou basque ou scandinavie* ou sweden ou swedish ou swede* ou stockholm ou switzerland* ou swiss* ou zurich ou geneva ou bern ou turkey ou turkish ou istanbul ou constantinople ou britain* ou britannique* ou royaume-uni* ou scotland* ou scottish ou wales* ou welsh ou england* ou belfast ou london ou manchester ou glasgow ou birmingham ou leeds ou bradford ou liverpool ou alabama* ou alaska* ou arizona* ou arkansas* ou california* ou colorado* ou connecticut* ou delaware* ou florida* ou georgia* ou hawaii* ou idaho* ou illinois* ou indiana* ou iowa* ou kansas* ou kentucky* ou louisiana* ou maine* ou maryland* ou massachusetts* ou michigan* ou minnesota* ou mississippi* ou missouri* ou montana* ou nebraska* ou nevada* ou new hampshire* ou new jersey* ou new mexico* ou new york* ou caroline du nord* ou dakota du nord* ou ohio* ou oklahoma* ou oregon* ou pennsylvanie* ou rhode island* ou caroline du sud* ou dakota du sud* ou tennessee* ou texas* ou utah* ou vermont* ou virginie* ou washington* ou virginie occidentale* ou wisconsin* ou wyoming* ou montgomery* ou juneau* ou anchorage* ou phoenix* ou little rock* ou sacramento* ou los angeles* ou san diego* ou san francisco* ou denver* ou hartford* ou dover* ou tallahassee* ou miami* ou orlando* ou atlanta* ou honolulu* ou boise* ou springfield* ou chicago* ou des moines* ou topeka* ou frankfort* ou baton rouge* ou new orleans* ou augusta* ou annapolis* ou boston* ou lansing* ou detroit* ou st ?paul* ou jackson* ou jefferson city* ou helena* ou lincoln* ou carson city* ou reno* ou las vegas* ou concord* ou trenton* ou santa fe* ou albany* ou raleigh* ou bismarck* ou columbus* ou oklahoma city* ou salem* ou harrisburg* ou providence* ou columbia* ou peirre* ou nashville* ou austin* ou dallas* ou salt lake city* ou montpelier* ou richmond* ou olympia* ou seattle* ou charleston* ou madison* ou cheyenne* ou district de columbia* ou usa ou États-Unis). tw, kf. | 4 128 242 |
| 33 | 31 et 32 | 117 |
| 34 | limiter 33 à (yr="2000 -Current" et (anglais ou français)) | 104 |
| 35 | (commentaire ou éditorial ou lettre ou nouvelles). pt. | 1 825 216 |
| 36 | 34 pas 35 | 91 |
Auteur; année |
Évaluation critique : Liste de contrôle de l'institut Joanna Briggs |
||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | |
| Banerji; 2016 | O | I | O | O | O | O | O | O | O | I | O |
| Bentley; 2013 | O | O | O | O | O | O | O | O | O | O | O |
| Blanken; 2018 | O | O | O | O | O | O | O | O | O | I | O |
| Chirico; 2009 | O | O | O | O | O | O | O | O | O | I | O |
| Hampp; 2011 | O | O | N | O | I | O | N | O | O | O | O |
| Harris; 2011 | O | O | I | O | O | O | I | O | O | O | O |
| Hascoet; 2008 | O | O | O | O | O | O | O | O | O | O | O |
| Smart; 2010 | O | O | O | O | O | O | O | O | O | I | O |
| Mahadevia; 2012 | O | O | N | O | O | O | O | O | O | I | O |
| McGirr; 2017 | O | O | O | O | O | O | O | O | O | I | O |
| Neovius; 2011 | O | O | O | O | O | O | O | O | O | I | O |
| Nuijten; 2009_DEU | O | O | O | O | O | O | O | O | O | O | O |
| Nuijten; 2009_NLD | O | O | O | O | O | O | O | O | O | O | O |
| Nuijten; 2010 | O | O | O | O | O | O | O | O | O | I | O |
| Nuijten; 2007 | O | O | O | O | O | I | O | O | O | O | O |
| Resch; 2012 | O | O | O | O | I | O | O | O | O | O | O |
| Rietveld; 2009 | O | O | N | O | O | O | O | O | O | I | I |
| Roeckl-Wiedmann; 2003 | O | O | N | O | O | O | O | O | O | I | I |
| Salinas-Escudero; 2012 | O | O | O | O | O | O | O | O | O | I | O |
| Sanchez-Luna; 2017 | O | O | O | O | O | O | O | O | O | I | O |
| Schmidt; 2017 | O | O | O | O | O | O | O | O | O | O | O |
| Tam; 2009 | O | O | O | O | O | O | O | O | O | I | O |
| Vogel; 2002 | O | O | N | O | O | O | N | O | O | I | N |
| Wang; 2008 | O | O | O | O | O | O | O | O | O | O | O |
| Weiner; 2012 | O | O | O | O | O | O | O | O | O | I | O |
| Yount; 2004 | O | O | O | O | O | O | O | O | O | O | N |
| ElHassan; 2006 | O | O | O | O | O | O | O | O | O | I | O |
| Lofland; 2000 | O | O | I | O | I | I | O | O | O | I | O |
Définitions : |
|||||||||||
Questions 23 : 1. Y a-t-il une question bien définie? 2. Existe-t-il une description complète des solutions de rechange? 3. Tous les coûts et résultats importants et pertinents pour chaque solution de rechange sont-ils établis? 4. L'efficacité clinique a-t-elle été établie? 5. Les coûts et les résultats sont-ils mesurés avec précision? 6. Les coûts et les résultats sont-ils évalués de manière crédible? 7. Les coûts et les résultats sont-ils ajustés pour tenir compte des différences de calendrier? 8. Existe-t-il une analyse différentielle des coûts et des conséquences? 9. Des analyses de sensibilité ont-elles été réalisées pour étudier l'incertitude des estimations de coûts ou de conséquences? 10. Les résultats de l'étude incluent-ils toutes les questions qui préoccupent les utilisateurs? 11. Les résultats sont-ils généralisables au contexte d'intérêt de l'examen?
Références
- Note de bas de page 1
-
Meates-Dennis M. Bronchiolite. Arch Dis Child Educ Pr Ed. 2005;90:81-86.
- Note de bas de page 2
-
Collins CL, Pollard AJ. Respiratory syncytial virus infections in children and adults. J Infect. 2002;45(1):10-17.
- Note de bas de page 3
-
Glezen WP, Paredes A, Allison JE, Taber LH, Frank AL. Risk of respiratory syncytial virus infection for infants from low-income families in relationship to age, sex, ethnic group, and maternal antibody level. J Pediatr. 1981;98(5):708-715.
- Note de bas de page 4
-
Hall CB. Respiratory Syncytial Virus and Parainfluenza Virus. N Engl J Med. 2001;344(25):1917-1928.
- Note de bas de page 5
-
Paes BA, Frcpc M, Mitchell I, et al. A decade of respiratory syncytial virus epidemiology and prophylaxis: Translating evidence into everyday clinical practice Case presentation. Can Respir J. 2011;18(2):e10-e19.
- Note de bas de page 6
-
Simoes EA. Respiratory syncytial virus infection. Lancet. 1999;354(9181):847-852. doi:10.1016/S0140-6736(99)80040-3.
- Note de bas de page 7
-
Sánchez-Solis M, Gartner S, Bosch-Gimenez V, Garcia-Marcos L. Is palivizumab effective as a prophylaxis of respiratory syncytial virus infections in cystic fibrosis patients? A meta-analysis. Allergol Immunopathol (Madr). 2015;43(3):298-303. doi:10.1016/J.ALLER.2013.09.003.
- Note de bas de page 8
-
Wang EE, Law BJ, Stephens D. Pediatric Investigators Collaborative Network on Infections in Canada (PICNIC) prospective study of risk factors and outcomes in patients hospitalized with respiratory syncytial viral lower respiratory tract infection. J Pediatr. 1995;126(2):212-219
- Note de bas de page 9
-
American Academy of Pediatrics. Palivizumab granted licensure for prophylaxis of RSV disease. AAP News. http://www.aappublications.org/content/14/10/10.3. Publié le 1er octobre 1998. Consulté le 19 décembre 2018.
- Note de bas de page 10
-
The IMpact-RSV Study Group. Palivizumab, a Humanized Respiratory Syncytial Virus Monoclonal Antibody, Reduces Hospitalization From Respiratory Syncytial Virus Infection in High-risk Infants. Pediatrics. 1999;102(3):531-537. doi:10.1542/peds.99.4.645.
- Note de bas de page 11
-
Embleton ND, Harkensee C, Mckean MC. Palivizumab for preterm infants. Is it worth it? Arch Dis Child Fetal Neonatal Ed. 2005;90(4):286-289.
- Note de bas de page 12
-
Fenton C, Scott LJ, Plosker GL. Palivizumab: a review of its use as prophylaxis for serious respiratory syncytial virus infection. Paediatr Drugs. 2004;6(3):177-197.
- Note de bas de page 13
-
Harkensee C, Brodlie M, Embleton ND, Mckean M. Passive immunization of preterm infants with palivizumab against RSV infection. J Infect. 2006;52(1):2-8. doi:10.1016/j.jinf.2005.08.003.
- Note de bas de page 14
-
Wang D, Cummins C, Bayliss S, Sandercock J, Burls A. Immunoprophylaxis against respiratory syncytial virus (RSV) with palivizumab in children: a systematic review and economic evaluation. Health Technol Assess. 2008;12(36):1-86.
- Note de bas de page 15
-
Andabaka T, Nickerson JW, Rojas-Reyes MX, Rueda JD, Vrca VB, Barsic B. Monoclonal antibody for reducing the risk of respiratory syncytial virus infection in children. Cochrane Database Syst Rev. 2013;(4):1-106. doi:10.1002/14651858.CD006602.pub4.
- Note de bas de page 16
-
Byington CL, Munoz FM. Palivizumab Prophylaxis for Healthy Preterm Infants: More Data Supporting American Academy of Pediatrics Guidelines. 2016. doi:10.1542/peds.2016-1494.
- Note de bas de page 17
-
Chabra S. Precise Gestational Age Definitions Needed for Palivizumab Prophylaxis in Preterm Infants. Am J Respir Crit Care Med. 2018;197(5):680-680. doi:10.1164/rccm.201708-1605LE.
- Note de bas de page 18
-
Embleton N, Harkensee C, Mckean MC. Palivizumab for preterm infants. Is it worth it? Arch Dis Child Fetal Neonatal Ed. 2005;90:F286-F289. doi:10.1136/adc.2004.058081.
- Note de bas de page 19
-
Mac S, Sumner A, Duchesne-Belanger S, et al. Cost-Effectiveness of Palivizumab for Respiratory Syncytial Virus: A Systematic Review. Pediatrics 2019;143:e20184064 doi:10.1542/peds.2018-4064
- Note de bas de page 20
-
Moher D, Liberati A, Tetzlaff J, et al. Preferred reporting items for systematic reviews and meta-analyses: The PRISMA statement. PLoS Med. 2009;6(7):1-6.
- Note de bas de page 21
-
Comité consultatif national de l'immunisation (CCNI). Déclaration sur l'utilisation recommandée de l'anticorps monoclonal anti-RSV (palivizumab). Can Commun Dis Rep. 2003;29 (ACS-7):1-13.
- Note de bas de page 22
-
Husereau D, Drummond M, Petrou S, Carswell C, Moher D, Greenberg D. Consolidated Health Economic Evaluation Reporting Standards (CHEERS)--Explanation and elaboration: A report of the ISPOR Health Economic Evaluations Publication Guidelines Task Force. Value Heal. 2013;16:231-250.
- Note de bas de page 23
-
Gomersall J, Jadote Y, Xue Y, Lockwood S, Riddle D, Preda A. Conducting systematic reviews of economic evaluations. Int J Evid Based Heal. 2015;13(3):170-178.
- Note de bas de page 24
-
Patel H, Sander B, Nelder MP. Long-term sequelae of West Nile virus-related illness: Une revue systématique. Lancet Infect Dis. 2015;15(8):951-959. http://dx.doi.org/10.1016/S1473-3099(15)00134-6.
- Note de bas de page 25
-
OCDE. Purchasing power parities (PPP) (indicator). doi:10,178 7/1290ee5a-en.
- Note de bas de page 26
-
Banerji A, Panzov V, Young M, et al. Hospital admissions for lower respiratory tract infections among infants in the Canadian Arctic: a cohort study. C Open. 2016;4(4):E615-E622. doi:10.9778/cmajo.20150051.
- Note de bas de page 27
-
McGirr AA, Schwartz KL, Allen U, Solomon M, Sander B. The cost-effectiveness of palivizumab in infants with cystic fibrosis in the Canadian setting: A decision analysis model. Hum Vaccines Immunother. 2017;13(3):599-606. doi:10.1080/21645515.2016.1235670.
- Note de bas de page 28
-
Neovius K, Buesch K, Sandström K, Neovius M. Cost-effectiveness analysis of palivizumab as respiratory syncytial virus prophylaxis in preterm infants in Sweden. Acta Paediatr Int J Paediatr. 2011;100(10):1306-1314. doi:10.1111/j.1651-2227.2011.02309.x.
- Note de bas de page 29
-
Nuijten MJC, Wittenberg W, Lebmeier M. Cost Effectiveness of Palivizumab for Respiratory Syncytial Virus Prophylaxis in High-Risk Children. Pharmacoeconomics. 2007;25(1):55-71. doi:10.2165/00019053-200725010-00006.
- Note de bas de page 30
-
Nuijten MJ, Wittenberg W. Cost effectiveness of palivizumab in Spain : An analysis using observational data. Eur J Heal Econ. 2010;11(1):105-115. doi:10.1007/s10198-009-0206-x.
- Note de bas de page 31
-
Nuijten M, Lebmeier M, Wittenberg W. Cost effectiveness of palivizumab for RSV prevention in high-risk children in the Netherlands. J Med Econ. 2009;12(4):291-300. doi:10.3111/13696990903316961.
- Note de bas de page 32
-
Nuijten M, Lebmeier M, Wittenberg W. Cost effectiveness of palivizumab in children with congenital heart disease in Germany. J Med Econ. 2009;12(4):301-308. doi:10.3111/13696990903347172.
- Note de bas de page 33
-
Resch B, Gusenleitner W, Nuijten MJC, Lebmeier M, Wittenberg W. Cost-effectiveness of palivizumab against respiratory syncytial viral infection in high-risk children in Austria. Clin Ther. 2008;30(4):749-760. doi:10.1016/j.clinthera.2008.03.014.
- Note de bas de page 34
-
Resch B, Sommer C, Nuijten MJC, et al. Cost-effectiveness of Palivizumab for Respiratory Syncytial Virus Infection in High-risk Children, Based on Long-term Epidemiologic Data From Austria. Pediatr Infect Dis J. 2012;31(1):e1-e8. doi:10.1097/INF.0b013e318235455b.
- Note de bas de page 35
-
Rietveld E, Steyerberg EW, Polder JJ, et al. Passive immunization against respiratory syncytial virus: A cost-effectiveness analysis. Arch Dis Child. 2010;95(7):493-498. doi:10.1136/adc.2008.155556.
- Note de bas de page 36
-
Roeckl-Wiedmann I, Liese JG, Grill E, Fischer B, Carr D, Belohradsky BH. Economic evaluation of possible prevention of RSV-related hospitalizations in premature infants in Germany. Eur J Pediatr. 2003;162(4):237-244. doi:10.1007/s00431-002-1106-6.
- Note de bas de page 37
-
Bentley A, Filipovic I, Gooch K, Büsch K. A cost-effectiveness analysis of respiratory syncytial virus (RSV) prophylaxis in infants in the United Kingdom. Health Econ Rev. 2013;3(1):1-12. doi:10.1186/2191-1991-3-18.
- Note de bas de page 38
-
Salinas-Escudero G, Martínez-Valverde S, Reyes-López A, et al. Cost-effectiveness analysis of the use of palivizumab in the prophylaxis of preterm patients in Mexico. Salud Publica Mex. 2012;54(1):47-59.
- Note de bas de page 39
-
Sanchez-Luna M, Burgos-Pol R, Oyagüez I, et al. Cost-utility analysis of Palivizumab for Respiratory Syncytial Virus infection prophylaxis in preterm infants: Update based on the clinical evidence in Spain. BMC Infect Dis. 2017;17(1):1-11. doi:10.1186/s12879-017-2803-0.
- Note de bas de page 40
-
Schmidt R, Majer I, García Román N, Rivas Basterra A, Grubb EB, Medrano López C. Palivizumab in the prevention of severe respiratory syncytial virus infection in children with congenital heart disease; a novel cost-utility modeling study reflecting evidence-based clinical pathways in Spain. Health Econ Rev. 2017;7(1). doi:10.1186/s13561-017-0181-3.
- Note de bas de page 41
-
Smart KA, Paes BA, Lanctôt KL. Changing costs and the impact on RSV prophylaxis. J Med Econ. 2010;13(4):705-708. doi:10.3111/13696998.2010.535577.
- Note de bas de page 42
-
Tam DY, Banerji A, Paes BA, Hui C, Tarride J-E, Lanctôt KL. The cost effectiveness of palivizumab in term Inuit infants in the Eastern Canadian Arctic. J Med Econ. 2009;12(4):361-370. doi:10.3111/13696990903442155.
- Note de bas de page 43
-
Vogel AM, McKinlay MJ, Ashton T, et al. Cost-effectiveness of palivizumab in New Zealand. J Paediatr Child Health. 2002;38(4):352-357. doi:10.1046/j.1440-1754.2002.00790.x.
- Note de bas de page 44
-
Weiner LB, Masaquel AS, Polak MJ, Mahadevia PJ. Cost-effectiveness analysis of palivizumab among pre-term infant populations covered by Medicaid in the United States. J Med Econ. 2012;15(5):997-1018. doi:10.3111/13696998.2012.672942.
- Note de bas de page 45
-
Yount LE, Mahle WT. Economic Analysis of Palivizumab in Infants With Congenital Heart Disease. Pediatrics. 2004;114(6):1606-1611. doi:10.1542/peds.2004-0224.
- Note de bas de page 46
-
Elhassan NO, Sorbero MES, Hall CB, Stevens TP, Dick AW. Cost-effectiveness analysis of palivizumab in premature infants without chronic lung disease. Arch Pediatr Adolesc Med. 2006;160(10):1070-1076. doi:10.1001/archpedi.160.10.1070.
- Note de bas de page 47
-
Lofland JH, Touch SM, O'Connor JP, et al. Palivizumab for respiratory syncytial virus prophylaxis in high-risk infants: A cost-effectiveness analysis. Clin Ther. 2000;22 (11) : 1357-1369. doi:10.1016/S0149-2918(00)83032-5.
- Note de bas de page 48
-
Blanken MO, Frederix GW, Nibbelke EE, et al. Cost-effectiveness of rule-based immunoprophylaxis against respiratory syncytial virus infections in preterm infants. Eur J Pediatr. 2018;177:133-144. doi:10.1007/s00431-017-3046-1.
- Note de bas de page 49
-
Chirico G, Ravasio R, Sbarigia U. Cost-utility analysis of palivizumab in Italy: Results from a simulation model in the prophylaxis of respiratory syncytial virus infection (RSV) among high-risk preterm infants. Ital J Pediatr. 2009;35(4):1-12. doi:10.1186/1824-7288-35-4.
- Note de bas de page 50
-
Hampp C, Kauf TL, Saidi AS, Winterstein AG. Cost-effectiveness of respiratory syncytial virus prophylaxis in various indications. Arch Pediatr Adolesc Med. 2011;165(6):498-505. doi:10.1001/archpediatrics.2010.298.
- Note de bas de page 51
-
Harris KC, Anis AH, Crosby MC, Cender LM, Potts JE, Human DG. Economic Evaluation of Palivizumab in Children With Congenital Heart Disease: A Canadian Perspective. Can J Cardiol. 2011;27(4):523.e11-523.e15. doi:10.1016/j.cjca.2010.12.064.
- Note de bas de page 52
-
Hascoet JM, Fagnani F, Charlemagne A, Vieux R, Roze JC, Bendjenana H. [Methodological aspects of economic evaluation in pediatrics: illustration by RSV infection prophylaxis in the French setting]. Arch Pediatr. 2008;15(12):1739-1748. doi:10.1016/j.arcped.2008.09.024.
- Note de bas de page 53
-
Lanctot K, Masoud S, Paes B, et al. The cost-effectiveness of palivizumab for respiratory syncytial virus prophylaxis in premature infants with a gestational age of 32–35 weeks: a Canadian-based analysis. Curr Med Res Opin. 2008;24(11):3223-3237. doi:10.1185/03007990802484234.
- Note de bas de page 54
-
Lanctot K, Masoud S, Paes B, et al. The cost-effectiveness of palivizumab for respiratory syncytial virus prophylaxis in premature infants with a gestational age of 32–35 weeks: a Canadian-based analysis. Curr Med Res Opin. 2008;24(11):3223-3237. doi:10.1185/03007990802484234.
- Note de bas de page 55
-
Wang T, Sangha O, Phillips C, et al. Outcomes of Children Treated for Lyme Disease. J Rheumatogy. 1998;25(11):2249-2253.
- Note de bas de page 56
-
Seeler RA, Schatz B. Palivizumab (Synagis)--cohorting babies to reduce waste. Pediatrics. 1999;104(5 Pt 1):1170-1171. doi:10.1542/PEDS.104.5.1170.
- Note de bas de page 57
-
Hussman JM, Li A, Paes B, Lanctôt KL. A review of cost-effectiveness of palivizumab for respiratory syncytial virus. Expert Rev Pharmacoeconomics Outcomes Res. 2012;12(5):553-568. doi:10.1586/erp.12.45.
- Note de bas de page 58
-
Prescott WA, Doloresco F, Brown J, Paladino JA. Cost Effectiveness of Respiratory Syncytial Virus Prophylaxis. Pharmacoeconomics. 2010;28(4):279-293. doi:10.2165/11531860-000000000-00000.
- Note de bas de page 59
-
Smart KA, Lanctôt KL, Paes BA. The cost effectiveness of palivizumab: a systematic review of the evidence. J Med Econ. 2010;13(3):453-463. doi:10.3111/13696998.2010.499749.
- Note de bas de page 60
-
Committee on Infectious Diseases and Bronchiolitis Guidelines Committee. Updated Guidance for Palivizumab Prophylaxis Among Infants and Young Children at Increased Risk of Hospitalization for Respiratory Syncytial Virus Infection. Pediatrics. 2014;134(2):415-420. doi:10.1542/peds.2014-1665.
- Note de bas de page 61
-
The Commonwealth Fund. 2015 International Profiles of Health Care Systems.; 2015. http://www.commonwealthfund.org/~/media/files/publications/fund-report/2016/jan/1857_mossialos_intl_profiles_2015_v7.pdf.
- Note de bas de page 62
-
Robinson J, Le Saux N, Société canadienne de pédiatrie, Comité des maladies infectieuses et d'immunisation. Prévenir les hospitalisations pour l'infection par le virus respiratoire syncytial. Pediatr Child Heal. 2015;20(6):321-326. https://cps.ca/fr/documents/position/prevenir-les-hospitalisations-pour-infection-par-le-vrs.
- Note de bas de page 63
-
The IMpact-RSV Study Group. Palivizumab, a Humanized Respiratory Syncytial Virus Monoclonal Antibody, Reduces Hospitalization From Respiratory Syncytial Virus Infection in High-risk Infants. Pediatrics. 1998;102(3):531-537. www.aappublications.org/news. Consulté le 1 février 2019.
