Ébauche d’évaluation préalable - Groupe des halogénures d’alkyle
Titre officiel : Ébauche d’évaluation préalable - Groupe des halogénures d’alkyle
Numéros de registre du Chemical Abstracts Service
74-96-4
75-00-3
106-94-5
156-60-5
Environnement et Changement climatique Canada
Santé Canada
Mars 2022
Sommaire
En vertu des articles 68 et ou 74 de la Loi canadienne sur la protection de l’environnement, 1999 (LCPE), les ministres de l’Environnement et de la Santé ont réalisé une évaluation préalable portant sur quatre substances formant le « groupe des halogénures d’alkyle » dans le Plan de gestion des produits chimiques. Le tableau ci-dessus présente le numéro d’enregistrement du Chemical Abstracts Service (NE CAS Note de bas de page 1 ), le nom sur la Liste intérieure (LI) et le nom commun de ces substances.
| NE CAS | Nom sur la LI | Nom commun |
|---|---|---|
| 74-96-4 | Bromoéthane | Bromoéthane |
| 75-00-3 | Chloroéthane | Chloroéthane |
| 106-94-5a | 1-Bromopropane | 1-Bromopropane |
| 156-60-5b | 1,2-Dichloroéthylène | trans-Dichloroéthylène |
a Cette substance n’a pas été identifiée en vertu du paragraphe 73(1) de la LCPE, mais est visée par la présente évaluation, car elle est considérée comme prioritaire en raison d’autres préoccupations liées à la santé humaine.
b Cette substance n’a pas été identifiée en vertu du paragraphe 73(1) de la LCPE, mais est visée par la présente évaluation, car elle est considérée comme prioritaire en raison d’établissement des priorités d’évaluation des risques(EPER).
Toutes les substances du groupe des halogénures d’alkyle sont synthétisées commercialement. De plus, le bromoéthane et le 1-bromopropane sont présents à l’état naturel. D’après les renseignements fournis lors d’une enquête réalisée aux termes de l’article 71 de la LCPE, entre 1000 kg et 10 000 kg de 1-bromopropane auraient été synthétisés au Canada en 2008. Aucune activité de production n’a été déclarée pour les autres substances. Les importations au Canada de bromoéthane, de chloroéthane et de 1-bromopropane ont été déclarées en quantités totales allant jusqu’à 1 000 000 kg en 2008, et de trans-dichloroéthylène en quantité de 382 744 kg en 2011. Trois des quatre substances du groupe des halogénures d’alkyle, le chloroéthane, le 1-bromopropane et le trans-dichloroéthylène, peuvent être présents dans un certain nombre de produits offerts aux consommateurs, notamment les nettoyants ou les dégraissants liquides ou en aérosol, les fluides de démarrage en aérosol (aide au démarrage des moteurs), les produits de chasse d’air pour la climatisation, les aérosols de démoulage en silicone et les mousses isolantes en aérosol.
Les risques pour l’environnement associés aux substances du groupe des halogénures d’alkyle ont été caractérisés à l’aide de la Classification du risque écologique (CRE) des substances organiques, une méthode fondée sur le risque qui tient compte de plusieurs paramètres liés au danger et à l’exposition, et sur une pondération des multiples éléments de preuve pour déterminer la classification des risques. Les profils de danger reposent principalement sur des paramètres liés au mode d’action toxique, à la réactivité chimique, aux seuils de toxicité interne établis à partir du réseau trophique, à la biodisponibilité et à l’activité chimique et biologique. Parmi les paramètres pris en compte pour les profils d’exposition, il y a le taux d’émission potentielle, la persistance globale et le potentiel de transport à grande distance. Une matrice de risques est utilisée pour attribuer aux substances un potentiel de préoccupation faible, moyen ou élevé, fondé sur leurs profils de danger et d’exposition. La CRE a permis de déterminer que les substances du groupe des halogénures d’alkyle ont un potentiel faible de causer des effets nocifs pour l’environnement.
Compte tenu de tous les éléments de preuve contenus dans la présente ébauche d’évaluation préalable, les quatre substances du groupe des halogénures d’alkyle présentent un risque d’effets nocifs faible sur l’environnement. Il est proposé de conclure que le bromoéthane, le chloroéthane, le 1-bromopropane et le trans-dichloroéthylène do not meet the criteria under paragraphs 64(a) or (b) of CEPA ne satisfont pas aux critères énoncés aux alinéas 64a) ou b) de la LCPE, car elles ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
Le risque présenté par les substances du groupe des halogénures d’alkyle pour la santé humaine a été caractérisé à partir des renseignements disponibles sur les effets sur la santé et l’exposition. Les évaluations de l’Organisation mondiale de la santé, de l’Organisation de coopération et de développement économiques, du Centre international de recherche sur le cancer, ainsi que de l’Agence de protection de l’environnement (EPA) des États-Unis ont été utilisées pour étayer la caractérisation des effets sur la santé dans la présente évaluation préalable.
La population générale du Canada peut être exposée au bromoéthane principalement par l’air intérieur et l’air ambiant. Le bromoéthane ne devrait pas être présent dans les produits disponibles pour les consommateurs. Les effets critiques considérés pour le bromoéthane sont la métaplasie respiratoire de l’épithélium olfactif de la cavité nasale et le cancer. Compte tenu du risque supplémentaire de cancer prévu au cours de la vie posé par l’exposition par voie aérienne, le cancer ne devrait pas présenter un risque préoccupant pour la santé. Les marges entre les estimations de l’exposition et les effets critiques observés dans les études sur les animaux ont été jugées adéquates pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé autres que le cancer.
La population générale du Canada peut être exposée au chloroéthane principalement par l’air intérieur et l’air ambiant, et de l’utilisation d’un liquide de démarrage en aérosol. Les effets critiques déterminés pour le chloroéthane sont la toxicité pour le développement et le cancer. Compte tenu du risque supplémentaire de cancer prévu au cours de la vie posé par l’exposition par voie aérienne, le cancer ne devrait pas présenter un risque préoccupant pour la santé. Les marges entre les estimations de l’exposition et les effets critiques observés dans les études sur les animaux ont été jugées adéquates pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé autres que le cancer.
La population générale du Canada peut être exposée au 1-bromopropane principalement par l’air intérieur et par l’utilisation d’aérosols de démoulage en silicone, d’aérosols de nettoyage pour appareils électroniques et de produits de chasse d’air pour la climatisation automobile, la principale voie d’exposition étant l’inhalation. Les effets critiques déterminés pour le 1-bromopropane sont le cancer, la toxicité pour le développement et la neurotoxicité. Compte tenu du risque supplémentaire de cancer prévu au cours de la vie posé par l’exposition par voie aérienne, le cancer ne devrait pas présenter un risque préoccupant pour la santé. Les marges entre les estimations de l’exposition et les effets critiques observés dans les études sur les animaux ont été jugées potentiellement inadéquates pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé autres que le cancer. En particulier, les marges entre l’estimation de l’exposition et les effets sur le développement dus à l’utilisation d’aérosol de démoulage en silicone, d’aérosol de nettoyage pour appareils électroniques et de produits de chasse d’air pour la climatisation automobile devraient présenter un risque pour la santé.
La population générale du Canada peut être exposée au trans-dichloroéthylène principalement par l’air intérieur et l’air ambiant, et par l’utilisation de détachants pour textile. L’immunotoxicité du trans-1,2-dichlorothène a été considérée comme l’effet critique de l’exposition chronique, et les effets sur le développement ont été considérés comme l’effet critique de l’exposition aiguë. Les marges entre les estimations de l’exposition et les effets critiques observés dans les études sur les animaux ont été jugées adéquates pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé autres que le cancer.
À la lumière des renseignements présentés dans la présente ébauche d’évaluation préalable, il est proposé de conclure que le bromoéthane, le chloroéthane et le trans-dichloroéthylène ne satisfont pas aux critères de l’alinéa 64c) de la LCPE, car ils ne pénètrent ou ne peuvent pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger pour la vie ou la santé humaine au Canada.
À la lumière des renseignements présentés dans la présente ébauche d’évaluation préalable, il est proposé de conclure que le 1-bromopropane satisfait au critère du paragraphe 64c) de la LCPE, car elle pénètre ou peut pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie et la santé humaines.
Par conséquent, il est proposé de conclure que le 1-bromopropane satisfait à un ou plusieurs des critères énoncés à l’article 64 de la LCPE et que le bromoéthane, le chloroéthane et le trans-dichloroéthylène ne répondent à aucun des critères définis à l’article 64 de la LCPE.
Il est aussi proposé de conclure que le 1-bromopropane satisfait au critère de persistance, mais non au critère de bioaccumulation, au sens du Règlement sur la persistance et la bioaccumulation pris en vertu de la LCPE.
1. Introduction
En vertu des articles 68 et 74 de la Loi canadienne sur la protection de l’environnement, 1999 (LCPE), les ministres de l’Environnement et de la Santé ont réalisé l’évaluation préalable de quatre parmi huit substances appelées collectivement le groupe des halogénures d’alkyle ou d’aryle dans le cadre du Plan de gestion des produits chimiques, pour déterminer si ces quatre substances présentent ou peuvent présenter un risque pour l’environnement et la santé humaine. Trois de ces quatre substances ont été jugées prioritaires, car elles répondaient aux critères de catégorisation du paragraphe 73(1) de la LCPE ou en raison d’autres préoccupations pour la santé humaine. Une des substances de ce groupe, le trans-dichloroéthylène (NE CAS 156-60-5), ne répondait pas aux critères de catégorisation; cependant, elle a été intégrée à la présente évaluation, car elle a été jugée prioritaire selon l’approche décrite pour l’établissement des priorités d’évaluation des risques (EPER), compte tenu du volume élevé dans le commerce et la faible dose de référence (DR) (ECCC 2009). L’EPER est une approche développée par ECCC et SC et consiste en un processus cyclique par lequel les deux ministères compilent de nouvelles données sur des substances spécifiques, évaluent ces données et déterminent si des mesures supplémentaires sur les substances peuvent être justifiées (ECCC, SC 2015).
Les quatre autres substances (tableau 1-1) sont des halogénures d’aryle, qui ont été prises en compte dans le document sur l’approche scientifique : classification du risque écologique des substances organiques (ECCC, 2016), et dans le document sur l’Approche fondée sur le seuil de préoccupation toxicologique (SPT) pour certaines substances (Santé Canada, 2016), ou par l’approche adoptée dans l’Évaluation rapide de substances auxquelles l’exposition de la population générale est limitée (ECCC, SC 2018a), et ont été jugées peu préoccupantes pour la santé humaine et l’environnement. À ce titre, elles ne sont pas traitées davantage dans le présent rapport. Les conclusions concernant ces quatre substances sont fournies dans les évaluations énumérées ci-dessous (tableau 1-1). Les quatre substances abordées dans la présente évaluation préalable seront ci-après appelées les halogénures d’alkyle.
| NE CAS | Nom figurant sur la Liste intérieure | Approche utilisée pour évaluer la substance | Références |
|---|---|---|---|
| 74-88-4 | Iodométhane | CRE/Examen préalable rapide | ECCC, SC 2018a |
| 77-47-4 | Hexachlorocyclopentadiène | CRE/SPT | ECCC, SC 2018b |
| 126-99-8 | 2-Chlorobuta-1,3-diène | CRE/Examen préalable rapide | ECCC, SC 2018a |
| 630-20-6 | 1,1,1,2-Tétrachloroéthane | CRE/Examen préalable rapide | ECCC, SC 2018a |
Les risques pour l’environnement associés aux substances du groupe des halogénures d’alkyle ont été caractérisés au moyen de l’approche de CRE (ECCC 2016a). La CRE décrit les dangers d’une substance à l’aide de paramètres clés, y compris le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne obtenus à partir du réseau trophique, la biodisponibilité, ainsi que l’activité chimique et biologique, et elle tient compte de l’exposition possible des organismes dans les milieux aquatique et terrestre, d’après des facteurs comme les taux d’émission potentiels, la persistance globale et le potentiel de transport à grande distance dans l’atmosphère. Les divers éléments de preuve sont combinés afin d’identifier les substances nécessitant une évaluation plus poussée de leur potentiel d’effets nocifs sur l’environnement ou présentant une faible probabilité d’effets nocifs sur l’environnement.
Lors de l’évaluation des risques pour la santé humaine, les quatre substances du groupe des halogénures d’alkyle ont été examinées séparément. Les substances du groupe des halogénures d’alkyle actuellement évaluées ont fait l’objet d’un examen à l’échelle internationale par des rapports d’évaluation initiale (SIAR) sur l’Ensemble de données de dépistage (EDD) du Programme sur les substances à volume de production élevé de l’Organisation pour la coopération et le développement économiques (OCDE), du Programme de sécurité chimique de l’Organisation mondiale de la santé (OMS), de la Environment Protection Agency des États-Unis (EPA des É.-U), et du Centre International de recherche sur le cancer(CIRC). Ces évaluations sont soumises à un examen rigoureux (notamment par un comité de lecteurs) et à une approbation. les Résumés succincts internationaux sur l’évaluation des risques chimiques de l’OMS, les SIAR de l’OCDE sur l’EDD, les monographies du CIRC, ainsi que les évaluations de l’EPA ont été utilisés pour étayer la caractérisation des effets sur la santé de la présente évaluation préalable.
La présente ébauche d’évaluation préalable tient compte des données sur les propriétés chimiques, le devenir dans l’environnement, les dangers, les utilisations et les expositions, notamment les données supplémentaires fournies par les intervenants. Des données pertinentes ont été relevées jusqu’en mars 2019. Toutefois, des études ou des renseignements plus récents obtenus auprès de pairs à l’interne ou étrangers peuvent aussi être cités. Des données empiriques tirées d’études clés ainsi que des résultats de modélisations ont été utilisés pour tirer nos conclusions. Lorsqu’elle était disponible et pertinente, l’information présentée dans des évaluations effectuées par d’autres administrations a été prise en compte.
La présente ébauche d’évaluation préalable a été préparée par le personnel du Programme d’évaluation des risques de la LCPE travaillant à Santé Canada et à Environnement et Changement climatique Canada. Elle inclut des intrants provenant d’autres programmes de ces deux ministères. Le volet de l’évaluation portant sur l’environnement est fondé sur le document décrivant la Classification du risque écologique (publié le 30 juillet 2016), qui a fait l’objet d’un examen externe par les pairs et ainsi que d’une période de commentaires du public de 60 jours. Les commentaires externes ont été pris en compte, toutefois Santé Canada et Environnement et Changement climatique Canada demeurent responsables du contenu définitif et des conclusions de la présente ébauche d’évaluation préalable.
La présente ébauche d’évaluation préalable est axée sur des renseignements essentiels pour déterminer si les substances satisfont aux critères énoncés à l’article 64 de la LCPE. Pour ce faire, les renseignements scientifiques ont été étudiés et intégrés à une approche basée sur le poids de la preuve et le principe de précaution Note de bas de page 2 . Dans le présent document, nous présentons ces renseignements essentiels et les éléments sur lesquels se fondent les conclusions proposées.
2. Identité des substances
Le tableau 2‑1 ci-après contient le numéro d’enregistrement du Chemical Abstracts Service (NE CAS), le nom sur la Liste intérieure (LI), le ou les noms communs et les acronymes des substances individuelles du groupe des halogénures d’alkyle.
| NE CAS | Nom sur la LI (nom commun) | Structure chimique et formule moléculaire a | Masse moléculaire (g/mol)a |
|---|---|---|---|
| 74-96-4 | Bromoéthane | 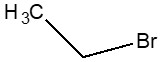 C2H5Br
C2H5Br
|
108,97 |
| 75-00-3 | Chloroéthane (Chlorure d’éthyle) | 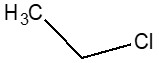 C2H5Cl
C2H5Cl
|
64,51 |
| 106-94-5 | 1-Bromopropane | 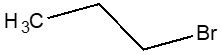 C3H7Br
C3H7Br
|
122,99 |
| 156-60-5 | trans-Dichloroéthylène | 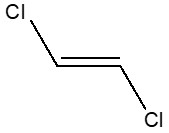 C2H2Cl2
C2H2Cl2
|
96,94 |
a Les données proviennent de ChemIDplus (2018).
3. Propriétés physiques et chimiques
Un résumé des principales propriétés physiques et chimiques des substances du groupe des halogénures d’alkyle est présenté dans le tableau 3‑1. D’autres propriétés physiques et chimiques sont indiquées dans ECCC (2016 b).
| Nom commun | Pression de vapeur (Pa) a,b,c | Constante de la loi de Henry (Pa·m3/mol)a,b,c | Solubilité dans l’eau (mg/l)a,b,c | Log Koe (sans dimension)a,b |
|---|---|---|---|---|
| Bromoéthane | 62 262 | 750d | 9000 | 1,61 |
| Chloroéthane | 134 389e | 1125f | 6710 | 1,43 |
| 1-bromopropane | 14 772e | 742d,e | 2450e | 2,1 |
| Trans-dichloroéthylène | 44 130d | 950f | 4520 | 2,09 |
Abréviation : Koe= coefficient de partage octanol-eau
a Données de PhysProp (2013)
b Basé sur des données expérimentales, sauf indication contraire
c Mesure effectuée à 25 °C, sauf indication contraire
d La valeur a été extrapolée sur la base d’une mesure expérimentale en dehors de la plage de température de mesure de la valeur indiquée
e Source : Environmental Protection Agency des États-Unis (2020); Mesure à 20 °C
f Mesure à 24 °C
4. Sources et utilisations
Le bromoéthane et le 1-bromopropane sont d’origine naturelle. Le bromoéthane et le 1-bromopropane sont produits par les algues (HSDB 2002, 2013). Le bromoéthane peut également être rejeté dans l’environnement par des gaz volcaniques (HSDB 2002). Toutes les substances du groupe des halogénures d’alkyle sont synthétisées commercialement et elles ont été visées par des enquêtes menées en vertu de l’article 71 de la LCPE (Canada 2009, 2012). Le tableau 4‑1 présente un résumé des renseignements déclarés sur les quantités totales fabriquées et importées des substances du groupe des halogénures d’alkyle.
| Nom commun | Production totalea (kg) | Total des importationsa (kg) | Année de déclaration | Référence de l’enquête |
|---|---|---|---|---|
| Bromoéthane | ND | 10 000 - 100 000 | 2008 | Canada 2009 |
| Chloroéthane | ND | 100 000 - 1 000 000 | 2008 | Canada 2009 |
| 1-bromopropane | 1 000 - 10 000 | 105 600 - 256 200 | 2008 | Canada 2009 |
| Trans-dichloroéthylène | NR | 382 744 | 2011 | Canada 2012 |
Abréviations : ND = aucune valeur déclarée au-delà du seuil de déclaration de 100 kg.
a Les valeurs reflètent les quantités déclarées en réponse aux enquêtes menées en vertu de l’article 71 de la LCPE (Canada 2009, 2012). Voir les enquêtes pour les inclusions et exclusions spécifiques (annexes 2 et 3).
Aux États-Unis, le site web ChemView a indiqué que le volume de production nationale (année de déclaration 2015) de 1-bromopropane se situait entre 10 000 000 et 50 000 000 livres (environ 4 500 000 à 22 500 000 kg), et entre 1 000 000 et 10 000 000 livres (environ 450 000 à 4 500 000 kg) pour le trans-dichloroéthylène (EPA des États-Unis 2018a).
Le tableau 4‑2 présente un résumé des principales utilisations (notamment les utilisations commerciales ainsi que des utilisations par les consommateurs) du groupe des halogénures d’alkyle, selon les renseignements fournis dans le cadre des enquêtes menées en vertu de l’article 71 de la LCPE (Canada 2009, 2012).
| Principales utilisationsa | Bromoéthane | Chloroéthane | 1-bromopropane | Trans-dichloroéthylène |
|---|---|---|---|---|
| Nettoyage et entretien de mobilier | N | N | O | O |
| Munitions | N | N | O | N |
| Lubrifiants et graisses | N | N | O | N |
| intermédiaire industriel | O | N | N | N |
| Modérateur de procédés pétrochimiques | N | O | N | N |
| Mousses isolantes | N | N | N | O |
| Appareils médicaux | N | N | N | O |
| Dégraissant | N | N | O | N |
| Détergent | N | N | O | N |
| Entretien d’automobile | N | N | O | N |
Abréviations : O = oui, utilisation déclarée pour cette substance; N = non, utilisation non déclarée pour cette substance
a Utilisation non confidentielle déclarée dans le cadre de l’enquête menée en vertu de l’article 71 de la LCPE (Canada 2009, 2012). Voir les enquêtes pour les inclusions et exclusions spécifiques (annexes 2 et 3).
L’examen des fiches signalétiques (FS) des produits accessibles au public (FSS) et d’autres renseignements publics n’a relevé aucun produit à base de bromoéthane destiné aux consommateurs au Canada. Le chloroéthane peut être présent dans les fluides de démarrage (FS 2017a); le 1-bromopropane peut être présent dans les aérosols de démoulage en silicone (FS 2016a), les aérosol de nettoyage pour appareils électroniques (FS 2017 b) et comme solvant dans les produits de chasse d’air pour la climatisation automobile (FS 2017c). Le trans-dichloroéthylène peut être présent dans les poudres de nettoyage de tâches des textiles (FS 2017d), et les nettoyants ou dégraissants pour équipement électrique ou pièces électroniques (FS 2010, 2014), les produits de chasse d’air pour la climatisation automobile (FS 2015a) et les mousses isolantes en aérosol (FS 2016 b, 2016c). Le 1-bromopropane Le 1-bromopropane peut également être utilisé dans le commerce pour le nettoyage à sec (EPA des États-Unis 2020). Vivre à proximité d’un nettoyeur à sec peut également constituer une voie d’exposition potentielle.
5. Devenir et comportement dans l’environnement
Selon les modèles utilisés dans la CRE (ECCC 2016b), le bromoéthane et le 1-bromopropane devraient persister dans l’atmosphère, mais pas dans l’eau, les sédiments ou le sol.
Selon les modèles utilisés dans la CRE (ECCC 2016b), le chloroéthane et le trans-dichloroéthylène devraient persister dans l’atmosphère, l’eau, les sédiments et le sol. Toutefois, étant donné la pression de vapeur élevée et la constante de la loi de Henry du chloroéthane et du trans-dichloroéthylène, ces substances devraient se volatiliser dans l’atmosphère à partir du sol et de l’eau.
Compte tenu de leur faible Koe et de leurs faibles facteurs de bioconcentration (ECCC 2016b), le bromoéthane, le chloroéthane, le 1-bromopropane et le trans-dichloroéthylène ne devraient pas se bioaccumuler dans les organismes de manière significative.
6. Potentiel de causer des effets nocifs sur l’environnement
6.1 Caractérisation des risques pour l’environnement
Les risques pour l’environnement associés aux substances du groupe des halogénures d’alkyle ont été caractérisés au moyen de l’approche de la classification du risque écologique des substances organiques (CRE) (ECCC 2016a). La CRE est une approche fondée sur les risques qui tient compte de plusieurs paramètres liés au danger et à l’exposition et qui repose sur la pondération de plusieurs éléments de preuve pour classer le risque. Les divers éléments de preuve sont combinés afin de distinguer les substances présentant une puissance plus ou moins élevée et un potentiel d’exposition plus ou moins élevé dans divers milieux. Cette approche réduit l’incertitude globale de la caractérisation des risques comparativement à une approche de caractérisation qui reposerait sur un seul paramètre dans un seul milieu (p. ex. la concentration létale médiane) pour la caractérisation.
Les données sur les propriétés physico-chimiques, le devenir (demi-vies chimiques dans divers milieux et biotes, coefficients de partage et bioconcentration dans les poissons), l’écotoxicité aiguë pour les poissons et les volumes de produits chimiques importés et fabriqués au Canada proviennent de publications scientifiques, de bases de données empiriques accessibles (p. ex. la boîte à outils QSAR de l’OCDE, 2014) et des résultats des enquêtes menées conformément à l’article 71 de la LCPE ou ont été produites à l’aide de modélisations de la relation (quantitative) structure-activité (QSAR) ou du devenir du bilan massique ou de la bioaccumulation. Ces données ont été utilisées comme entrées dans d’autres modèles de bilan massique ou pour compléter les profils de danger et d’exposition des substances.
Les profils de danger reposent principalement sur des paramètres liés au mode d’action toxique, à la réactivité chimique, aux seuils de toxicité interne établis à partir du réseau trophique, à la biodisponibilité et à l’activité chimique et biologique. Les profils d’exposition sont également fondés sur de nombreux paramètres, dont les taux d’émission potentielle, la persistance globale et le potentiel de transport à grande distance. Les profils de danger et d’exposition ont été comparés aux critères de décision, permettant ainsi de classer les potentiels de danger et d’exposition de chaque substance organique comme faibles, moyens ou élevés D’autres règles ont été appliquées (p. ex. cohérence de la classification, marge d’exposition) pour raffiner les classifications préliminaires du danger et de l’exposition.
Une matrice de risques a été utilisée pour attribuer à chaque substance un risque potentiel faible, moyen ou élevé, fondé sur la classification de son danger et de son exposition. Les classifications du risque potentiel au moyen de la CRE ont été vérifiées à l’aide d’une approche en deux étapes. La première étape servait à ajuster les résultats de la classification du risque de moyen ou élevé à faible pour les substances présentant un faible taux d’émission estimé dans l’eau après le traitement des eaux usées, représentant un faible potentiel d’exposition. La deuxième étape servait à examiner les résultats de la classification du potentiel de risque faible selon des scénarios de risque relativement prudents, à l’échelle locale (c.-à-d. dans la zone à proximité immédiate du point de rejet) et conçus pour protéger l’environnement, afin de déterminer si la classification du risque potentiel devrait être accrue.
La CRE s’appuie sur une approche pondérée afin de réduire au minimum le potentiel de sous-classification et de surclassification des dangers, de l’exposition et des risques subséquents. Les approches équilibrées pour tenir compte des incertitudes sont décrites plus en détail dans le document de référence (ECCC 2016a). Voici une description de deux des zones d’incertitude les plus importantes. Les erreurs dans les valeurs de toxicité aiguë empiriques et modélisées pourraient entraîner des modifications dans la classification du danger, en particulier en ce qui a trait aux paramètres reposant sur des valeurs de résidus dans les tissus (c.-à-d. mode d’action toxique), dont un grand nombre sont des valeurs prédites à partir de modèles QSAR (boîte à outils QSAR de l’OCDE 2014). Cependant, l’impact de cette erreur est atténué par le fait qu’une surestimation de la létalité médiane conduira à une valeur prudente (protectrice) pour les résidus dans les tissus, utilisée pour l’analyse des résidus corporels critiques. L’erreur dans la sous-estimation d’une toxicité aiguë sera atténuée par le recours à d’autres paramètres de danger, comme le profilage structural du mode d’action, la réactivité et/ou l’affinité de liaison à l’œstrogène. Les changements ou les erreurs dans les quantités chimiques pourraient entraîner des classifications différentes de l’exposition, car la classification de l’exposition et du risque dépend grandement du taux d’émission et des quantités utilisées. Les résultats de la CRE représentent donc l’exposition et le risque au Canada, fondés sur les quantités actuellement utilisées, et pourraient ne pas représenter les tendances futures.
Les données essentielles et les facteurs à considérer, utilisés pour élaborer les profils spécifiques des substances du groupe des anthraquinones, ainsi que les résultats de la classification du danger, de l’exposition et des risques figurent dans ECCC (2016 b).
Les classifications de danger et d'exposition pour les quatre substances du groupe des halogénures d’alkyle sont résumées dans le Tableau 6‑1.
| Nom commun | Classification du danger selon la CRE | Classification de l’exposition selon la CRE | Classification des risques selon la CRE |
|---|---|---|---|
| Bromoéthane | modéré | faible | faible |
| Chloroéthane | modéré | élevé | moderate |
| 1-bromopropane | modéré | faible | faible |
| Trans-dichloroéthylène | faible | élevé | faible |
D’après les données prises en compte dans l’approche de CRE, le potentiel d’exposition au bromoéthane et au 1-bromopropane a été classé faible. Le bromoéthane et le 1-bromopropane ont été classé comme des substances présentant un potentiel de danger modéré sur la base d’alertes structurelles de QSAR de l’OCDE, 2014 qui ont identifié ces substances comme étant des fixateurs potentiels d’ADN et de protéines. Le potentiel de risque écologique de bromoéthane et de 1-bromopropane a été classé faible. Les effets potentiels et la façon dont ils peuvent se manifester dans l’environnement n’ont pas été étudiés plus avant en raison de la faible exposition de ces substances. Au vu des profils actuels d’utilisation, il est peu probable que le bromoéthane et le 1-bromopropane suscitent des préoccupations pour l’environnement au Canada.
D’après les données prises en compte dans l’approche de CRE, le potentiel d’exposition de chloroéthane a été classé élevé en raison de sa demi-vie extrêmement longue dans l’atmosphère et d’une grande quantité importée annuellement, selon les renseignements communiqués en réponse à une enquête menée en vertu de l’article 71 de la LCPE (Environnement Canada 2013). Le chloroéthane a été classé comme présentant un danger modéré sur la base des alertes structurelles de la boîte à outils QSAR de l’OCDE (2014) qui a déterminé que cette substance comme liant potentiel de l’ADN et des protéines. Le chloroéthane a été classé comme substance ayant un potentiel modéré de risque pour l’environnement. Compte tenu de sa classification globale comme ayant un potentiel modéré de risque écologique, il est peu probable que cette substance suscite des préoccupations pour l’environnement au Canada. Comme le chloroéthane est actuellement utilisé en grande quantité au Canada, il est peu probable que les variations des profils d’emploi entraînent une augmentation importante des risques pour l’environnement.
D’après les données prises en compte dans l’approche de CRE, le trans-dichloroéthylène a été classé comme substance ayant un potentiel d’exposition élevé en raison de sa demi-vie extrêmement longue dans l’atmosphère et d’une grande quantité importée annuellement, selon les renseignements communiqués en réponse à une enquête menée en vertu de l’article 71 de la LCPE (Environnement Canada 2013). Le trans-dichloro-1,2 a été classé comme substance présentant un faible potentiel de danger, et donc, un faible risque écologique. Étant donné les profils d’utilisation actuels, il est peu probable que le trans-dichloroéthylène suscite des préoccupations pour l’environnement au Canada.
7. Potentiel de causer des effets nocifs sur la santé humaine
7.1 Bromoéthane
7.1.1 Évaluation de l’exposition
7.1.1.1 Milieux de l’environnement
Aucune donnée fiable de surveillance environnementale de la présence du bromoéthane dans l’eau, le sol, la poussière ou les aliments n’a été relevée au Canada ou ailleurs. Compte tenu de sa pression de vapeur très élevée et de la constante de la loi de Henry, le bromoéthane devrait se volatiliser dans l’atmosphère à partir du sol et de l’eau. Par conséquent, l’exposition au bromoéthane dans les milieux naturels devrait se produire principalement à partir de l’atmosphère.
Les concentrations de bromoéthane mesurées dans l’air ambiant et intérieur au Canada sont présentées à l’annexe A, et sont résumées ci-dessous.
Le bromoéthane a été surveillé dans le cadre du programme du Réseau national de surveillance de la pollution atmosphérique (RNSPA) entre 1991 et 2013. Les concentrations moyennes dans l’air ambiant mesurées à plusieurs sites au Canada allaient de non détecté (limite de détection en laboratoire [LD] = 0,043 à 0,058 µg/m3) à 0,068 µg/m3 et les concentrations du 95e percentile allaient de non détecté à 0,050 µg/m3 (ECCC 2019)). Les concentrations de bromoéthane dans l’air ambiant ont également été mesurées dans le cadre de sept études canadiennes sur la qualité de l’air menées à Windsor, Régina, Halifax, Edmonton, Montréal, Sault-Ste-Marie et Ottawa (Santé Canada 2010a, 2010 b, 2010c, 2012, 2013), [Communication personnelle de Tim Shin et Ron Garson, BQEA, 27 mai 2021; source non citée. Les détails de la conception de l’étude ont été présentés ailleurs (c.-à-d., Dales et coll. 2013, Mallach et coll. 2017)]. La moyenne géométrique et le 95e percentile des concentrations de bromoéthane dans l’air ambiant mesurés dans toutes ces études canadiennes étaient inférieurs à la limite de détection en laboratoire (LD = 0,022 à 0,074 µg/m3).
Les concentrations de bromoéthane dans l’air intérieur ont également été mesurées dans les sept études canadiennes mentionnées ci-dessus, ainsi qu’à Swan Lake, au Manitoba, dans le cadre de l’Étude de la qualité de l’air intérieur des Premières nations (communication personnelle de Tim Shin et Ron Garson, BQEA, Santé Canada, 27 mai 2021; source non citée, les détails de la conception de l’étude ont été présentés ailleurs [Weichenthal et coll. 2012]). La moyenne géométrique et le 95e percentile des concentrations de bromoéthane dans l’air intérieur étaient équivalente à la LD dans toutes les études (c.-à-d. 0,074 µg/m3).
L’exposition des individus au bromoéthane a également été mesurée dans le cadre d’une étude sur l’air à Windsor, en Ontario (Santé Canada, 2010c). Les échantillons d’air individuel tiennent compte des expositions au bromoéthane dans l’air intérieur et de l’air ambiant de différents endroits, notamment la maison, le bureau et le transport. Le bromoéthane n’a été détecté dans aucun des échantillons d’exposition des individus recueillis en hiver et en été ( LD = 0,070 µg/m3).
Lors du traitement des résultats inférieurs à la limite de détection en laboratoire (LD) des études canadiennes sur la qualité de l’air menées à Halifax, Edmonton, Montréal, Sault-Ste-Marie et Ottawa (communication personnelle de Tim Shin et Ron Garson, BQEA, Santé Canada, 27 mai 2021; source non citée, les détails de la conception de l’étude ont été présentés ailleurs [Dales et coll. 2013, Mallach et coll. 2017]), les valeurs utilisées dans l’analyse statistique ont été les valeurs rapportées. Les résultats ont été jugés valides, car le temps de rétention et les ions cibles/les ions qualificatifs dans le chromatogramme obtenue par chromatographie en phase gazeuse-spectrométrie de masse (CG-SM) répondaient aux critères d’analyse du laboratoire. Concernant l’analyse statistique des études canadiennes sur la qualité de l’air menées à Regina et à Windsor (Santé Canada 2010 b, 2010c), les valeurs inférieures à la LD ont été rapportées à la moitié de la LD. De plus, lorsqu’aucun pic ou d’ions cibles/de qualification n’a été observé dans le chromatogramme CG-SM du laboratoire, la concentration de bromoéthane a été déclarée comme étant nulle, car les critères de quantification n’étaient pas respectés. Les résultats ont été jugés valides et remplacés par une valeur proche de zéro (0,0001 µg/m3) ou par une valeur égale à la moitié de la limite de détection minimum (LDM) correspondante pour calculer les statistiques descriptives par transformation logarithmique.
La limite de détection de laboratoire la plus élevée des études susmentionnées a été utilisée pour estimer l’exposition de la population générale au bromoéthane dans l’air (c.-à-d. 0,074 µg/m3), car la concentration de bromoéthane du 95e percentile le plus élevé était inférieure à la LD.
7.1.1.2 Produits disponibles pour les consommateurs
Aucun produit disponible pour les consommateurs n’a été identifié pour le bromoéthane; par conséquent, pour la population générale du Canada ne devrait pas être exposée au bromoéthane par l’intermédiaire de produits disponibles pour les consommateurs.
7.1.2 Évaluation des effets sur la santé
L’OMS (2002) a résumé la documentation sur les effets sur la santé et a caractérisé le danger du bromoéthane. L’OMS (2002) a été utilisée pour étayer la caractérisation des effets sur la santé dans la présente évaluation préalable. Le CIRC a classé le bromoéthane dans le groupe 3 (non classifiable quant à sa cancérogénicité pour les humains) (CIRC 1999). Dans son Système général harmonisé (SGH), l’Agence européenne des produits chimiques (ECHA) a classé le bromoéthane comme un cancérogène de catégorie 2 (Carc. 2) (Avertissement H351 : soupçonné de causer le cancer) (ECHA 2018). Une recherche documentaire a été effectuée sur la période de l’année précédant le rapport d’OMS 2002 à mars 2019. Aucune étude sur les effets sur la santé susceptible d’avoir un impact sur la caractérisation des risques (c.-à-d. donner lieu à des critères d’effets différents ou à des points de départ plus bas que ceux indiqués par l’OMS 2002, le NTP 1989, Great Lakes Chemical Corporation 2002 et le CIRC 1999) n’a été identifiée.
Il existe peu d’information sur les propriétés toxicocinétiques de bromoéthane (OMS 2002). L’absorption se produit chez les animaux suite à l’exposition par voie orale, respiratoire et cutanée; cependant, le niveau d’absorption de bromoéthane n’est pas connu (Schwander 1936; Miller et Haggard 1943 cité dans OMS 2002). Après son inhalation par les animaux, le bromoéthane se distribue au moins jusqu’au cerveau et au foie (Leuze 1922; Abreu et Emerson 1940, cités dans OMS 2002). La majeure partie du bromoéthane absorbé peut être éliminée sous forme inchangée par l’air expiré, l’urine ou les matières fécales. Les premières études ont indiqué la possibilité de débromation et de conjugaison avec le glutathion (Heppel et Porterfield 1948; Thomson et coll. 1958; Barnsley et coll. 1964; Johnson 1965; Jones 1973, cité dans OMS 2002)
Aucune étude formelle de toxicité pour la reproduction n’a été réalisée chez l’animal; cependant, l’apparition d’une atrophie testiculaire sévère chez tous les rats mâles (F344/N) exposés à 7 200 mg/m3 pendant 14 semaines dans une étude d’inhalation de 14 semaines indique un potentiel d’effets sur la fertilité masculine (OMS 2002). Par conséquent, une concentration sans effet nocif observé (CSENO) de 3600 mg/m3 et une concentration minimale avec effet nocif observé (CMENO) de 7200 mg/m3 sont retenues pour le critère de toxicité pour la reproduction (Roycroft 1989 tel que cité dans OMS 2002).
Le bromoéthane est considéré génotoxique dans le test d’Ames avec et sans activation métabolique (OMS 2002). Le bromoéthane est mutagène dans un essai d’échange de chromatides sœurs sur des cellules d’ovaire de hamster chinois en culture, avec et sans activation métabolique. Dans l’ensemble, l’OMS et le CIRC ont conclu que la génotoxicité était préoccupante, mais qu’il n’était pas possible actuellement de quantifier de manière fiable le niveau de risque pour la santé humaine (OMS 2002). Aucune donnée sur la génotoxicité in vivo chez les animaux de laboratoire ou les humains n’était disponible.
Une étude de cancérogénicité par inhalation a été menée sur des rats (F344/N) et des souris (B6C3F1). Les animaux testés ont été exposés à 0, 450, 900 et 1 800 mg/m3 (6 heures/jour, 5 jours/semaine) (50/sexe/concentration) pendant deux ans. Chez les rats, la CSENO identifiée chez les rats mâles était de 450 mg/m3 sur la base d’un effet non cancérigène, la métaplasie respiratoire de l’épithélium olfactif de la cavité nasale, à la LOAEC de 900 mg/m3 (Roycroft 1989 cité par l’OMS 2002). Chez la souris, une augmentation de l’incidence des tumeurs utérines (adénomes, adénocarcinomes ou carcinomes épidermoïdes combinés) liée à la dose a été observée (0/50, 4/50, 5/47, 27/48 par rapport à la plage d’incidence antérieure pour les témoins du laboratoire d’étude (moyenne ± écart-type) : 4/335 [1% +/- 2%]). (Roycroft 1989 cité dans OMS 2002). Une limite inférieure de la dose de référence (DR10) associée à une incidence d’augmentation de 10 % des tumeurs utérines de 448 mg/m3 a été calculée à l’aide du logiciel Benchmark Dose Software (BMDS version 3.1 USEPA). Le mécanisme de formation des tumeurs demeure incertain. Il n’y a pas de données disponibles sur la capacité du bromoéthane à causer le cancer dans la population humaine potentiellement exposée (OMS 2002). Dans l’ensemble, l’OMS a conclu qu’il existe un risque de cancérogénicité sur la base des résultats de Roycroft (1989) cités dans OMS (2002), qui sont possiblement à l’origine de la classification Carc 2 du SGH de l’ECHA, ainsi que de la classification Carc 2 de l’EPA.
Un facteur de pente du cancer de 0,0073 (mg/kg p.c./jour)-1 chez l’humain basé sur les tumeurs utérines chez la souris et calculé par la California Environmental Protection Agency (Cal EPA 2012) a été utilisé pour les estimations quantitatives du risque de cancer du bromoéthane pour la population canadienne (annexe B). Ce facteur de pente du cancer chez l’humain a été obtenu en ajustant le modèle multistade aux données dose-réponse de l’étude du National Toxicity Program (NTP) (1989) sur des souris femelles et en utilisant le facteur d’échelle interespèces applicable (Cal EPA, 2012). La dose quotidienne moyenne pour la durée de vie (DQMV) du bromoéthane dans l’air a été modifiée à l’aide de facteurs d’ajustement en fonction de l’âge (FAFA) (annexe B, tableau B-1).
7.1.3 Caractérisation des risques pour la santé humaine
Le tableau 7‑1 présente les valeurs pertinentes d’exposition et de danger associées au bromoéthane, ainsi que les marges d’exposition (ME) obtenues, pour la détermination de risques d’effets sur la santé autres que le cancer.
| Scénario d’exposition | Concentration d’exposition | Concentration d’effet critique | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Exposition par inhalation de l’air | 0,000074 mg/m3 | DR10 aug. = 80 mg/m3 dans une étude d’exposition par inhalation de 2 ans chez le rata | Métaplasie respiratoire de l’épithélium olfactive à 900 mg/m3 | 1 086 000 |
Abréviations : ME : Marge d’exposition; DR10aug. : dose de référence associée à une incidence d’augmentation de 10% de l’effet.
a Une DR10 de 448 mg/m3 a été déterminée à partir de cette étude. Lorsque l’exposition est amortie sur 24 heures/jour, 7 jours/semaine, cette DR10 est corigée à 80 mg/m3.
Concernant l’exposition au bromoéthane par inhalation, la comparaison des effets critiques autres que le cancer avec les estimations des concentrations d’exposition dans l’air a donné lieu à une ME jugée adéquate pour tenir compte des incertitudes des bases de données sur les effets sur la santé et l’exposition.
La dose quotidienne moyenne pour la durée de vie (DQMV) de bromoéthane dans l’air a été utilisée pour calculer l’augmentation du risque de cancer au cours de la vie. La DQMV a été établie à 1,88 x 10-5 mg/kg p.c./jour (annexe B, tableau B-2). Ces facteurs ont ensuite été appliqués au calcul du risque de cancer pour chaque groupe d’âge (voir l’annexe B, tableau B-3). Le risque de cancer au cours de la vie obtenu en utilisant le facteur de pente du cancer de 0,0073 (mg/kg p.c./jour)-1 et appliquant les FAFA appropriés aux estimations de l’exposition donne un risque de cancer de 4,3 x 10-7, ce qui est jugé acceptable compte tenu des incertitudes dans les bases de données sur l’exposition et les dangers.
L’exposition de la population générale au bromoéthane n’est pas préoccupante aux niveaux actuels, cependant cette substance est considérée comme ayant un effet préoccupant sur la santé en raison de sa cancérogénicité potentielle (classification ECHA GHS Carc 2). Par conséquent, il pourrait y avoir un risque pour la santé humaine si l’exposition venait à augmenter.
7.1.4 Incertitudes dans l’évaluation des risques pour la santé humaine
Les principales sources d’incertitude sont présentées au tableau suivant.
| Principales sources d’incertitude | Impact |
|---|---|
| Aucune donnée fiable de surveillance environnementale dans l’eau, le sol, la poussière ou les aliments au Canada n’était disponible. | +/- |
| Absence d’études sur la toxicité pour le développement | +/- |
+ = incertitude avec potentiel de causer une surestimation de l’exposition/risques; - = incertitude avec potentiel de causer une sous-estimation de l’exposition/risques; +/- = potentiel inconnu de surestimation ou de sous-estimation du risque.
7.2 Chloroéthane
7.2.1 Évaluation de l’exposition
7.2.1.1 Milieux de l’environnement
Aucune donnée fiable de surveillance environnementale du chloréthane dans l’eau, le sol, la poussière ou les aliments n’a été relevée au Canada ou ailleurs. Compte tenu de sa pression de vapeur très élevée et de la constante de la loi de Henry, le chloroéthane devrait se volatiliser du sol et de l’eau. On s’attend donc à ce que l’exposition au chloroéthane dans les milieux environnementaux se produise principalement dans l’air.
Les concentrations de chloroéthane mesurées dans l’air ambiant et l’air intérieur au Canada sont présentées à l’annexe A, et sont résumées ci-dessous.
Le chloroéthane a été surveillé par le programme du Réseau national de surveillance de la pollution atmosphérique (RNSPA) entre 1991 et 2016. Les concentrations moyennes dans l’air ambiant mesurées à différents sites à travers le Canada étaient comprises entre non détectées (LD = 0,027 à 0,069 µg/m3) à 0,176 µg/m3 et les concentrations du 95e percentile étaient comprises entre non détectées (LD = 0,044 à 0,069 µg/m3) à 0,368 µg/m3 (ECCC 22019). Les concentrations de chloroéthane dans l’air ambiant ont également été mesurées dans le cadre de sept études canadiennes sur l’air menées à Windsor, Regina, Halifax, Edmonton, Montréal, Sault-Ste-Marie et Ottawa (Santé Canada 2010a, 2010 b, 2010c, 2012, 2013, [communication personnelle de Tim Shin et Ron Garson, BQEA, Santé Canada, 27 mai 2021; source non citée, les détails de la conception de l’étude ont été présentés ailleurs (Dales et coll. 2013, Mallach et coll. 2017)]). Les concentrations moyennes géométriques dans l’air ambiant de ces villes canadiennes étaient inférieures à la LD (0,027 à 0,115 µg/m3) dans toutes les études, et les concentrations du 95e percentile étaient comprises entre non détectées et 0,060 µg/m3 (LD : 0,039 µg/m3).
Les concentrations de chloroéthane dans l’air intérieur ont également été mesurées au cours des sept études canadiennes mentionnées ci-dessus, ainsi qu’à Swan Lake, au Manitoba, dans le cadre de l’Étude de la qualité de l’air intérieur des Premières nations (communication personnelle de Tim Shin et Ron Garson, BQEA, Santé Canada, 27 mai 2021; source non citée, les détails de la conception de l’étude ont été présentés ailleurs [c.-à-d. Weichenthal et coll. 2012]). La moyenne géométrique et le 95e percentile des concentrations de chloroéthane mesurées dans l’air intérieur de ces villes canadiennes étaient comprises entre valeurs non détectées (LD = 0,027 à 0,115 µg/m3) et 0,092 µg/m3 et entre non détectées (LD = 0,062 à 0,115 µg/m3) et 0,233 µg/m3, respectivement.
La concentration de chloroéthane a également été mesurée dans l’air individuel dans le cadre de l’étude sur l’air de Windsor en Ontario (Santé Canada, 2010c). Les concentrations moyennes géométriques en hiver et en été étaient à la LD, et les concentrations du 95e percentile n’ont pas été détectées (LD = 0,115 µg/m3) et de 0,160 µg/m3 en été et en hiver, respectivement.
Lors du traitement des résultats inférieurs à la limite de détection en laboratoire (LD) des études canadiennes sur la qualité de l’air menées à Halifax, Edmonton, Montréal, Sault-Ste-Marie et Ottawa (communication personnelle de Tim Shin et Ron Garson, BQEA, Santé Canada, 27 mai 2021; source non citée, les détails de la conception de l’étude ont été présentés ailleurs [Dales et coll. 2013, Mallach et coll. 2017]), les valeurs utilisées dans l’analyse statistique ont été les valeurs rapportées. Concernant l’analyse statistique des études canadiennes sur la qualité de l’air menées à Regina et à Windsor (Santé Canada 2010 b, 2010c), les valeurs inférieures à la LD ont été rapportées à la moitié de la LD. De plus, lorsqu’aucun pic ou d’ions cibles/de qualification n’a été observé dans le chromatogramme CG-SM du laboratoire, la concentration de chloroéthane a été déclarée comme étant nulle, car les critères de quantification n’étaient pas respectés. Les résultats ont été jugés valides et remplacés par une valeur proche de zéro (0,0001 µg/m3) ou par une valeur égale à la moitié de LD correspondante pour calculer les statistiques descriptives par transformation logarithmique.
La concentration la plus élevée du 95e percentile mesurée dans l’air ambiant ou intérieur au Canada (c.-à-d. 0,368 µg/m3 dans le cadre du programme de RNSPA; 2252 échantillons analysés en 1996) (ECCC 2019) ont été utilisée pour estimer l’exposition de la population générale au chloroéthane provenant de l’air.
7.2.1.2 Produits disponibles pour les consommateurs
L’utilisation de produits disponibles pour les consommateurs (par exemple, aide au démarrage de moteur ou fluide de démarrage) contenant du chloroéthane peut entraîner une exposition de la population générale par voie cutanée et/ou par inhalation. Les fluides de démarrage devraient être utilisés de façon intermittente et par des adultes.
Les estimations de l’exposition aux fluides de démarrage représentent le niveau d’exposition cutanée et respiratoire le plus élevé (appelé scénario sentinelle) pour les groupes d’âge concernés et sont présentées dans le tableau 7‑3. Les estimations de l’exposition potentielle sont basées sur des hypothèses prudentes. Les détails sont présentés dans l’annexe C.
| Substance | Scénario d’exposition au produit | Concentration (%)a | Voie d’exposition | Per event internal exposure (mg/kg p.c.) | Concentration moyenne par événement (mg/m3) |
|---|---|---|---|---|---|
| Chloroéthane | Fluide de démarrage (aérosol) | 1 | Cutanée | 0,0027 | - |
| Chloroéthane | Fluide de démarrage (aérosol) | 1 | Respiratoire | 0,00065 | 4,2 |
a FS 2017a
7.2.1.3 Biosurveillance
Des données de biosurveillance ont été repérées dans la National Health and Nutrition Examination Survey des É.-U. (NHANES) (enquête nationale sur la nutrition et la santé) portant sur le chloroéthane (2013-2014) (CDC 2014). Le chloroéthane n’a pas été détecté dans le sang entier analysé dans la population américaine. Aucune donnée de biosurveillance canadienne n’est disponible.
7.2.2 Évaluation des effets sur la santé
L’OCDE (2006) a résumé la documentation sur les effets sur la santé et a caractérisé le danger du chloroéthane. L’OCDE (2006) a été utilisée pour étayer la caractérisation des effets sur la santé dans la présente évaluation préalable. Le CIRC a classé le chloroéthane dans le groupe 3 (inclassable quant à sa cancérogénicité pour les humains) (CIRC 1999). L’ECHA a classé le chloroéthane comme Carc. 2 du SGH (Avertissement H351 : soupçonné de causer le cancer) (ECHA 2018b).
Une recherche documentaire a été effectuée sur la période de l’année précédant le rapport de l’OCDE (2006) (c’est-à-dire avril 2005) à mars 2019. Aucune étude sur les effets sur la santé susceptible d’avoir un impact sur la caractérisation des risques (c.-à-d. donner lieu à des critères d’effets différents ou à des points de départ plus bas que ceux indiqués par l’OCDE (2006), l’ATSDR (2018), le NTP (1989) et le CIRC (1999) n’a été identifiée.
Le chloroéthane est rapidement absorbé par les poumons après une exposition par inhalation (OCDE 2006). Chez les humains exposés brièvement au chloroéthane par inhalation, 30 % de la dose absorbée était éliminée en une heure par l’haleine (Morgan et coll. 1970 dans ATSDR 2018). La concentration la plus élevée relevée dans le corps des animaux au cours des études de toxicité a été relevée dans le tissu gras autour du rein et la concentration la plus faible dans le liquide céphalorachidien (Konietzko 1984 dans ATSDR 2018). Chez la souris et le rat, le métabolisme implique la conjugaison avec le glutathion (GSH) et l’oxydation par des monooxygénases dépendantes du cytochrome P-450 pour produire du s-éthyl-glutathion et de l’acétaldéhyde, respectivement (ATSDR 1998). Certains métabolites sont évacués dans l’urine, tandis que le chloroéthane non métabolisé est exhalé.
Une étude d’exposition par inhalation de 11 jours a été menée chez la souris (B6C3F1). Les animaux testés ont été exposés pendant 11 jours à des doses de 0, 660, 3250 ou 13 088 mg/m3 (23 heures/jour) (7 /sexe/concentration). La CSENO a été établie à 3250 mg/m3 sur la base d’une hausse du poids relatif moyen du foie chez les mâles et les femelles et d’une hausse de la vacuolisation hépatocellulaire (glycogène ou graisse) et la CMENO a été établie à 13 088 mg/m3 (IRIS 1991, Landry et coll. 1989, cités dans OCDE 2006).
Une étude d’inhalation de 13 semaines a été menée sur le rat (F344/N) et la souris (B6CF1). Les animaux testés ont été exposés pendant 13 semaines à des doses de 0, 6544, 13 088, 26 000 ou 50 000 mg/m3 (6 heures/jour, 5 jours/semaine) (10 /sexe/concentration). La CSENO a été établie à 26 000 mg/m3 sur la base d’une hausse du ratio foie/poids corporel chez les rats mâles et les souris femelles et d’une baisse du poids corporel chez les rats des deux sexes à la CSENO de 50 000 mg/m3 (NTP 1989 dans OECD 2006).
Une étude des effets d’exposition par inhalation pour le développement a été menée sur la souris (CF-1), par la voie d’exposition respiratoire. Les animaux testés ont été exposés du 6e au 15e jour de gestation à des doses de 0, 1308, 3926 ou 13 088 mg/m3 (6 heures/jour) (30 /sexe/concentration). La CSENO a été établie à 3926 mg/m3 sur la base d’un retard d’ossification fœtale et la CMENO à 13 088 mg/m3 (Scortichini et coll. 1986 dans OECD 2006).
Des études in vitro montrent que le chloroéthane est mutagène dans l’essai d’Ames, avec et sans activation métabolique (OCDE 2006). Le chloroéthane a également induit des mutations génétiques dans les systèmes des mammifères, avec et sans activation métabolique. Les études in vivo (par exemple, clastogénicité et dommages à l’ADN) n’ont révélé aucune génotoxicité pour le chloroéthane (OCDE 2006). Il est donc possible de conclure que le chloroéthane est génotoxique in vitro, mais pas in vivo.
Une étude de cancérogénicité par inhalation a été réalisée sur les rats (F344/N) ainsi que les souris (B6C3F1). Les animaux d’essai ont été exposés pendant deux ans à des doses de 0 et 39 264 mg/m3 (6 heures/jour, 5 jours/semaine) (50 /sexe/concentration). Chez les souris, il y avait une activité cancérigène pour les femelles à 39 264 mg/m3, indiquée par des tumeurs utérines (carcinomes) (0/49, 43/50 pour 0 et 39 264 mg/m3 respectivement) et la fourchette d’incidence historique pour les témoins du laboratoire d’étude (moyenne +/- écart-type) est de 4/335 (1% +/- 2%) (NTP 1989 cité dans OECD 2006). Comme les animaux avaient été exposés à une seule concentration, il n’a pas été possible d’examiner la relation dose-réponse en fonction des différentes concentrations. D’autres types de tumeurs ont été observés chez les animaux d’essai, notamment des tumeurs du cerveau, de la peau, du système hématopoïétique, des reins, du tractus urogénital, du foie et des poumons. Il convient de noter que l’étude sur les souris mâles a été jugée inadéquate pour la cancérogénicité en raison de la faible survie du groupe exposé due à une infection ascendante des voies urinaires (OCDE 2006). Cependant, l’incidence des lésions non néoplasiques de différents systèmes a également été notée chez les souris mâles (c.-à-d. les systèmes alimentaire, cardiovasculaire, endocrinien, le système général du corps, les systèmes génital, musculo-squelettique, nerveux et respiratoire). Concernant les lésions néoplasiques, cette étude n’a pas permis d’établir une CSENO. Cependant, une CMENO égale à 39 264 mg/m3 a été établie chez les souris femelles sur la base d’une augmentation des tumeurs utérines (NTP 1989 dans OCDE 2006). Il convient de noter que les résultats du NTP (1989) cités par l’OCDE (2006) sont probablement à la base de la classification Carc 2 du SGH de l’ECHA. Le CIRC (1999) a examiné la même étude de cancérogénicité et a jugé le chloroéthane non classifiable quant à sa cancérogénicité chez l’homme (Groupe 3).
Un facteur de pente du cancer chez l’humain de 0,0025 (mg/kg p.c./jour)-1 basé sur les tumeurs utérines chez la souris et calculé par la California Environmental Protection Agency (Cal EPA) (2001) a été utilisé pour estimer quantitativement le risque de cancer associé au chloroéthane pour la population canadienne (annexe B). Ce facteur de pente du cancer chez l’humain a été obtenu en utilisant un cas particulier du modèle multistade (modèle à stade unique), dans lequel une seule étape est utilisée, et le facteur d’échelle interespèces applicable obtenu par l’équation d’échelle interespèces mise à jour (qhumain = qanimal - (p.c.h / p.c.a)1/4. Il convient de noter que le règlement original de la Proposition 65 (la Safe Drinking Water and Toxic Enforcement Act de 1986) a été mis à jour en 2011. Par conséquent, le rapport entre le poids corporel humain et le poids corporel animal est porté à la puissance 1/4 au lieu de la puissance 1/3. (Communication personnelle de l’Office of Environmental Health Hazard Assessment (OEHHA), California Environmental Protection Agency au Bureau de la qualité de l’air et de l’eau (BQEA), Santé Canada, 3 juillet 2019).
7.2.3 Caractérisation des risques pour la santé humaine
Le tableau 7‑4 présente toutes les valeurs d’exposition et de danger pertinentes pour le chloroéthane, ainsi que les ME obtenues, pour la détermination de risques d’effets sur la santé autres que le cancer.
| Scénario d’exposition | Concentration d’exposition | Niveau d’effet critique | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Exposition par inhalation de l’air | 0,000368 mg/m3 | CSENO aj = 982 mg/m3 sur la base d’une étude de la toxicité par inhalation pour le développement durant 10 jours de gestation a | etard d’ossification fœtale chez la souris à 13 088 mg/m3 | 2 700 000 |
| Exposition par inhalation par événement : fluide de démarrage (aérosol) | 4,2 mg/m3 | CSENO = 3926 mg/m3 sur la base d’une étude de la toxicité par inhalation pour le développement durant 10 jours de gestation | etard d’ossification fœtale chez la souris à 13 088 mg/m3 | 935 |
| Exposition par inhalation par événement : fluide de démarrage (aérosol) | 0,0027 mg/kg p.c. (interne) | CSENO(cutanée) = 478 mg/kg p.c. sur la base d’une étude de la toxicité par inhalation pour le développement durant 10 jours de gestation b | etard d’ossification fœtale chez la souris à 13 088 mg/m3 | 177 000 |
Abréviations : ME, marge d’exposition; CSENOaj, concentration sans effet indésirable observé, ajustée pour tenir compte des expositions quotidiennes de 24 h.
a Une CSENO de 3 926 mg/m3 a été établie dans cette étude. Lorsque l’exposition est amortie à 24 heures/jour, 7 jours/semaine, cette CSENO est ajustée à 982 mg/m3.
b La CSENO équivalente à l’exposition cutanée de 478 mg/kg p.c. a été déterminée comme suit : CSENO(cutanée) = CSENO(inhalation) x taux de ventilation ¸ Poids corporel, où CSENO(inhalation) = 3926 mg/m3, taux de ventilation = 1,5 m3/h pour 6 heures, et poids corporel = 74 kg.
En ce qui concerne l’exposition par inhalation au chloroéthane, la comparaison des effets critiques sur la santé autres que le cancer aux concentrations d’exposition dans l’air et d’exposition due à l’utilisation du fluide de démarrage a donné lieu à des ME jugées adéquates pour tenir compte des incertitudes des bases de données sur les effets sur la santé et l’exposition. Il convient de noter qu’il n’a pas été nécessaire de quantifier les scénarios par événement, car la concentration de 13 088 mg/m3 était excessive. Concernant l’exposition cutanée au fluide de démarrage, la comparaison des effets critiques non liés au cancer avec les estimations de l’exposition par absorption produit une ME jugée adéquate pour tenir compte des incertitudes dans les bases de données sur les effets sur la santé et l’exposition. Ces ME sont également jugées adéquates pour tenir compte de l’exposition potentielle de tiers (c.-à-d. les non-utilisateurs).
La dose quotidienne moyenne pour la durée de vie (DQMV) du chloroéthane dans l’air a été utilisée calculer la hausse incrémentielle du risque de cancer au cours de la vie. La DQMV a été établie à 6.35 x 10-5 mg/kg p.c./jour (annexe B, tableau B-4). Les facteurs d’ajustement en fonction de l’âge (FAFA) recommandés par l’EPA des États-Unis (2005) ont été pris en compte et ajustés aux groupes d’âge de Santé Canada (voir annexe B, tableau B-1). Ces facteurs ont ensuite été appliqués au calcul du risque de cancer pour chaque groupe d’âge (voir l’annexe B, tableau B-5). Le risque de cancer au cours de la vie obtenu en utilisant le facteur de pente du cancer de 0,0025 (mg/kg p.c./jour)-1 et en appliquant les FAFA appropriés aux estimations de l’exposition donne un risque cancérogène de 5,0 x 10-7 qui est jugé acceptable compte tenu des incertitudes dans les bases de données sur l’exposition et les dangers.
L’exposition de la population générale au chloroéthane n’est pas préoccupante aux niveaux actuels, cependant cette substance est considérée comme ayant un effet préoccupant sur la santé en raison de sa cancérogénicité potentielle (classification ECHA GHS Carc 2). Par conséquent, il pourrait y avoir un risque pour la santé humaine si l’exposition venait à augmenter.
7.2.4 Incertitudes dans l’évaluation des risques pour la santé humaine
Les principales sources d’incertitude sont présentées au tableau suivant.
| Principale source d’incertitude | Impact |
|---|---|
| Aucune donnée fiable de surveillance environnementale dans l’eau, le sol, la poussière ou les aliments au Canada n’était disponible. | +/- |
| Aucune donnée sur l’absorption cutanée du chloroéthane. | - |
| Absence d’études sur la toxicité par voie cutanée | +/- |
+ = incertitude avec potentiel de causer une surestimation de l’exposition/risques; - = incertitude avec potentiel de causer une sous-estimation de l’exposition/risques; +/- = potentiel inconnu de surestimation ou de sous-estimation du risque.
7.3 1-bromopropane
7.3.1 Évaluation de l’exposition
7.3.1.1 Milieux de l’environnement
Aucune donnée fiable de surveillance environnementale dans l’eau, le sol, la poussière ou les aliments au Canada ou ailleurs n’était disponible. Compte tenu de sa pression de vapeur très élevée et de la constante de la loi de Henry, le 1-bromopropane devrait se volatiliser dans l’atmosphère à partir du sol et de l’eau. Par conséquent, l’exposition au 1-bromopropane dans les milieux naturels devrait se produire principalement à partir de l’atmosphère.
Les données sur le 1-bromopropane provenant de la surveillance de l’air intérieur au Canada ont été repérées. Les concentrations de 1-bromopropane mesurées dans l’air intérieur au Canada sont présentées à l’annexe A, et sont résumées ci-dessous.
Le 1-bromopropane a été mesuré dans l’étude nationale sur l’air intérieur au Canada menée en 2012-2013 dans le cadre du troisième cycle de l’Enquête canadienne sur les mesures de la santé (ECMS) (Canada 2013). Li et coll. (2019) ont examiné les résultats de cette étude menée sur une période de 24 mois pour surveiller 88 composés organiques volatils (COV) dans 3524 résidences canadiennes. Cette substance a été détectée dans l’air intérieur à une faible fréquence (0,3 %), avec une limite de détection de la méthode (LDM) de 0,29 µg/m3 et une concentration maximale de 3,1 µg/m3. Elle n’a donc pas été détectée dans la quasi-totalité des mesures de l’air intérieur (99,7 %).
Vivre à proximité d’un nettoyeur à sec peut également être une source potentielle d’exposition, car le nettoyage à sec a été établi comme un Scénario d’exposition professionnelle (EPA des États-Unis 2020); cependant, il n’existe aucune donnée canadienne pour ce scénario d’exposition.
Le Department of Health and Human Services des États-Unis a modélisé la dispersion atmosphérique pour estimer les concentrations de 1-bromopropane dans l’air ambiant à proximité des installations de fabrication de mousse industrielle qui utilisent cette (Morris et Wolf 2003, cité dans NTP 2016). Cependant, selon une réponse à une enquête menée en vertu de l’article 71 de la LCPE (Canada 2009), la fabrication de mousse ne constitue pas une utilisation au Canada (voir le tableau 4‑2), et ces données de modélisation n’ont pas été jugées pertinentes pour les expositions au Canada.
Par prudence, la concentration maximale de l’étude sur l’air intérieur de l’ECMS (Canada 2013) (3,1 µg/m3) a été utilisée pour estimer l’exposition de la population générale au 1-bromopropane dans les résidences canadiennes.
7.3.1.2 Produits disponibles pour les consommateurs
L’exposition de la population générale au 1-bromopropane peut provenir de l’utilisation de produits disponibles pour les consommateurs, notamment les aérosols de démoulage en silicone, les aérosols de nettoyage pour appareils électroniques et les produits de chasse d’air pour la climatisation automobile. Ces produits se trouvent sur le marché canadien actuel. On s’attend uniquement à des utilisations intermittentes de ces produits par des adultes. Aucune utilisation par les enfants n’a été signalée pour le 1-bromopropane dans les réponses aux enquêtes menées en vertu de l’article 71 de la LCPE (Canada 2009, 2012).
Les estimations d’exposition provenant de produits disponibles pour les consommateurs qui ont été jugés pertinents pour la population générale du Canada et qui représentent le plus haut niveau d’exposition potentielle par voie cutanée et par inhalation (appelés scénarios sentinelles) pour les groupes d’âge pertinents sont présentées dans le tableau 7‑6 et le tableau 7‑7. Les expositions potentielles ont été estimées sur la base d’hypothèses prudentes. Les détails sont présentés à l’annexe C.
Bien que la principale voie d’exposition soit considérée comme étant l’inhalation, l’exposition cutanée peut également se produire par contact avec la peau dans le cas de formulations liquides de produits de consommation (par exemple, les produits de chasse d’air pour la climatisation automobile), par dépôt de vapeur ou de brouillard sur la peau dans le cas de formulations de produits en aérosol (par exemple, les aérosols de démoulage en silicone, les aérosols de nettoyants pour appareils électroniques). Une étude in vitro limitée utilisant de l’épiderme humain a établi l’absorption cutanée du 1-bromopropane à 0,16 % pour un scénario d’exposition restreint (p. ex. éclaboussures sur la peau où l’on s’attend à une évaporation rapide et où l’exposition ne se poursuit pas) (Frasch et coll. 2011). La même étude révèle que l’absorption cutanée pour les expositions restreintes ou continues peut être substantielle lorsque le 1-bromopropane ne peut pas s’évaporer facilement (par exemple, le contact direct avec le matériau pendant l’utilisation du produit ou après l’application). Cependant, cette étude n’a pas mesuré les résidus de 1-bromopropane liés à la peau et a signalé un écart-type important, ce qui pourrait indiquer la difficulté de répartition uniforme d’une petite dose qui s’évapore rapidement de la surface exposée de la peau. Par ailleurs, l’EPA des États-Unis (2020) note que la vitesse du vent dans l’air intérieur utilisée dans l’étude est élevée et peut entraîner une sous-estimation de l’absorption cutanée. En ajustant pour une vitesse de vent plus typique pour l’intérieur, l’EPA des États-Unis (2020) a estimé l’absorption cutanée à 0,29 %.
| Substance | Scénario d’utilisation de produit | Concentration (%) | Voie d’exposition | Exposition interne par événement (mg/kg p.c. par jour) |
|---|---|---|---|---|
| 1-bromopropane | Aérosols de démoulage en silicone | 30a | Dermal | 0,0031 |
| 1-bromopropane | Aérosols de nettoyage pour appareils électroniques | 44 b | Dermal | 0,0071 |
| 1-bromopropane | Produits de chasse d’air pour la climatisation automobile | 100c | Dermal | 0,00047 |
a FS 2016a
b FS 2017b
c FS2017c
| Substance | Scénario d’utilisation de produit | Concentration (%) | Voie d’exposition | Concentration moyenne par événement (mg/m3) | Concentration atmosphérique MPT sur 6 heures (mg/m3) |
|---|---|---|---|---|---|
| 1-bromopropane | Aérosols de démoulage en silicone | 30a | Inhalation | 2490 | 208 |
| 1-bromopropane | Aérosols de nettoyage pour appareils électroniques | 44 b | Inhalation | 1980 | 165 |
| 1-bromopropane | Produits de chasse d’air pour la climatisation automobile | 100c | Inhalation | 1100 | 92 |
Abréviation: MPT moyenne pondérée dans le temps
a FS 2016a
b FS 2017b
c FS 2017c
7.3.1.3 Biosurveillance
Il a été proposé d’utiliser la N-acétyl-S-(n-propyl)-L-cystéine (AcPrCys) comme biomarqueur de l’exposition au 1-bromopropane . 'AcPrCys a été identifiée dans l’urine de travailleurs exposés professionnellement, et sa corrélation avec les concentrations de 1-bomopropane dans l’air ambiant provenant d’activités professionnelles a été démontrée (EPA des États-Unis 2020). L’AcPrCys a également été détecté dans l’urine de la population générale, par exemple, dans des échantillons d’urine d’enfants et d’adultes dans le cadre de la National Health and Nutrition Examination Survey des É.-U. (NHANES) (enquête nationale sur la nutrition et la santé) à environ 3-4 µg/L (moyenne géométrique)). Elle a également été mesurée au cours de l’étude américaine National Children’s Vanguard Study (2009-2010) dans l’urine de femmes enceintes qui en sont à leur troisième trimestre (relevé dans 99 % des 488 échantillons) à une concentration médiane de 2,6 ng/ml (Boyle et coll. 2016), ce qui est nettement inférieur à la moyenne géométrique rapportée dans la NHANES. Alors que les études menées en milieu professionnel établissent l’AcPrCys comme le biomarqueur le plus prédictif disponible d’exposition au 1-bromopropane , l’omniprésence de l’AcPrCys chez la population générale suggère également que ce métabolite pourrait ne pas être spécifique au 1-bromopropane , car l’exposition de la population générale devrait être limitée (EPA des États-Unis 2020).
7.3.2 Évaluation des effets sur la santé
Le résumé de la documentation sur les effets sur la santé et la caractérisation du danger pour le 1-bromopropane réalisés par l’EPA des États-Unis (2020) ont été utilisés pour informer la caractérisation des effets sur la santé de la présente évaluation préalable. Le CIRC a classé le 1-bromopropane dans le groupe 2B (Possiblement cancérogène pour l’humain en raison de données suffisantes chez l’animal et insuffisantes chez l es humains) (CIRC 2018). L’ECHA a classé le 1-bromopropane dans la catégorie Repr 1B du SGH (H360FD : peut nuire à la fertilité; peut nuire à l’enfant à naître) (ECHA 2018c).
Une recherche documentaire a été effectuée sur la période allant de l’année précédant l’EPA des États-Unis (2020) à mai 2019. Aucune nouvelle étude sur les effets sur la santé qui aurait un impact sur la caractérisation des risques (c.-à-d. qui donnerait lieu à des critères d’effet différents ou à des points de départ plus bas que ceux indiqués dans EPA des États-Unis (2020) n’a été identifiée.
Il existe peu d’informations toxicocinétiques sur le 1-bromopropane. Des études menées sur des humains et des animaux indiquent que le 1-bromopropane est facilement absorbé par la voie respiratoire, cutanée et orale. L’inhalation devrait être la voie d’exposition prédominante. Après l’absorption, il devrait se séparer dans les graisses, en raison de son coefficient de partage graisse:sang. Le 1-bromopropane peut se lier directement au glutathion ou peut être oxydé par le CYP2E1. Il peut ensuite subir une oxydation et/ou se lier au glutathion et finalement s’évacuer dans l’urine sous forme de dérivés de l’acide mercapturique, notamment la N-acétyl-S-(n-propyl)-L-cystéine. On sait que le métabolisme du 1-bromopropane par le CYP2E1 produit des métabolites mutagènes. La sécrétion du 1-bromopropane s’effectue principalement par l’expiration, de moindres quantités étant évacuées dans l’urine et les matières fécales (EPA des États-Unis 2020).
Une étude de neurotoxicité comportementale due à l’exposition par inhalation a été menée sur des rats mâles (F344). Les animaux d’essais ont été exposés pendant 3 semaines (8 heures/jour) à des doses de 10, 50, 200 et 1000 ppm (50, 251, 1006 et 5028 mg/m3) (Honma et coll. 2003, cité dans EPA des États-Unis 2020). Le niveau d’effet critique et le critère de danger correspondaient à une DRÉT1 de 18,2 ppm (91,5 mg/m3), pour la baisse du temps de traction (c.-à-d. le temps de suspension à une barre) (où DRÉT1 est la limite de confiance inférieure à une réponse de référence [RR] d’un écart-type de 1 (ÉT1)). La CMENO de ce paramètre a été établie à 200 ppm (1 006 mg/m3). Ce paramètre est compatible avec la neurotoxicité périphérique, qui a également été signalée dans des études sur les humains et d’autres études sur des animaux de laboratoire (Honma et coll. 2003 tel que cité dans EPA des États-Unis 2020).
Une étude d’effets d’exposition par inhalation sur la reproduction sur 2 générations a été menée chez le rat (SD). Les animaux d’essai (25/sexe/concentration) ont été exposés pendant ≥ 70 jours (6h/jour) avant l’accouplement, pendant toute la période de gestation jusqu’au 20e jour de gestation à des doses de 100, 250, 500 ou 750 ppm (503, 1258, 2515 ou 3773 mg/m3). Les femelles exposées à 750 ppm n’étant pas gravides, l’exposition des F1 a été limitée aux trois groupes de doses les plus faibles (c. -à-d. 100, 200 et 500 ppm, soit 503, 1258 et 2515 mg/m3). Toutes les femelles F0 et F1 ont été autorisées à donner naissance à leurs petits et les élever jusqu’au sevrage au 21e jour de lactation. Des effets sur les paramètres de la reproduction des mâles et des femelles et sur le fœtus en développement ont été observés, à partir de 250 ppm (1 259 mg/m3). Les effets observés chez les mâles comprenaient la diminution de la motilité des spermatozoïdes, des changements dans la morphologie des spermatozoïdes et la diminution des indices d’accouplement et de fertilité. Les effets observés chez les femelles comprennent la diminution du nombre de corps jaunes, de follicules antraux et de foyers d’implantation. Une augmentation de la durée du cycle œstral a également été observée ainsi qu’une augmentation du nombre de femelles F0 ayant accouplé sans donner naissance. Parmi les effets sur le développement figurent une diminution de la taille des portées vivantes, une diminution du poids corporel des petits et une diminution du poids du cerveau. Le Niveau d’effet critique et le critère de danger correspondaient à une DR1 égale à 23 ppm (116 mg/m3), pour la perte post-implantation chez les femelles F0 (où DR1 est la DR à une RR de 1%). Cette étude a également relevé des modifications histopathologiques dans le foie (hausse de la vacuolisation hépatocellulaire des hépatocytes centrolobulaires; DR10 = 143,5 ppm, soit 721,8 mg/m3) et le rein (augmentation de l’incidence de minéralisation pelvienne; DRL10 = 135 ppm; 679,1 mg/m3) (WIL Research 2001 cité dans EPA des États-Unis 2020).
Une étude de cancérogénicité d’exposition par inhalation de 2 ans a été menée chez les rats (F344) et les souris (B3C3F1). Les animaux d’essai ont été exposés pendant 105 semaines (6 heures/jour, 5 jours/semaine) à 0, 125, 250 ou 500 ppm (0, 269, 1258 ou 2515 mg/m3 pour les rats) et à 62,5, 125 et 250 ppm (0, 314, 629 ou 1 258 mg/m3 pour les souris) (50/sexe/concentration). Chez les souris femelles, une augmentation significative de l’incidence des adénomes alvéolaires/bronchiolaires ou carcinomes a été observée à toutes les doses testées (1/50, 9/50, 8/50, 14/50 pour des combinaisons d’adénome et de carcinome à 0, 314, 629 ou 1258 mg/m3, respectivement). Sur la base de cette étude, L’EPA des États-Unis a établi une dose de référence (DR10) de 78 ppm (396 mg/m3) et une limite inférieure de l’intervalle de confiance à 95 % de la dose de référence (DR10) de 54,1 ppm (272 mg/m3) pour les combinaisons d’adénome alvéolaire/bronchiolaire et de carcinome chez les souris femelles (NTP 2011 tel que cité dans EPA des États-Unis 2020). Une augmentation significative des incidences combinées de kératoacanthome carcinome et de spinocellulaire (rat mâle) et d’adénome du gros intestin (rat femelle) a également été observée, mais à des points de départ plus élevés. L’incidence accrue des tumeurs chez les rats et les souris, observées dans plusieurs organes, et l’apparition de tumeurs rares (par exemple, adénomes intestinaux), constituent des preuves suffisantes de cancérogénicité chez les animaux.
Le CIRC a classé le 1-bromopropane dans le groupe 2B (possiblement cancérogène pour l’homme, en raison de données suffisantes chez l’animal et insuffisantes chez les humains)(CIRC 2018). Le CIRC (2018) a également conclu qu’il existe des preuves modérées du caractère génotoxique du 1-bromopropane. L’EPA des États-Unis (2020) déclare que les preuves d’un mode d’action mutagène du 1-bromopropane suggèrent une tendance de cancérogénicité sans être concluantes. Il existe des preuves de mutagénicité et de dommages à l’ADN in vitro. Cependant, la génotoxicité in vivo est incertaine. Les résultats de la génotoxicité in vitro sont mitigés (résultats équivoques dans des bactéries et positifs pour le lymphome de souris et essais de Comet), cependant, les essais in vivo (létalité dominante, micronoyaux et mutation génétique chez des souris transgéniques) ont produit des résultats négatifs. Il existe également des preuves que le 1-bromopropane contribue à un processus de cancérogenèse en plusieurs étapes par le stress oxydatif, l’immunosuppression et la prolifération cellulaire.
Le risque d’exposition au 1-bromoproprane lié à l’utilisation de produits disponibles pour les consommateurs a été évalué par l’EPA des États-Unis dans le cadre du programme Toxic Substances Control Act (TSCA), et une évaluation finale des risques a été publiée en 2020 (EPA des États-Unis 2020. Des estimations de l’exposition aiguë au 1-bromopropane par inhalation chez les utilisateurs et les non-utilisateurs (personnes présentes) ont été calculées pour l’utilisation de produits suivants par les consommateurs : accélérateurs pour adhésifs, nettoyants tout usage en aérosol, nettoyants pour taches/détachant, produits de nettoyage/élimination de moisissures, nettoyants/dégraissant tout usage en aérosol, nettoyants/dégraissants en aérosol pour les appareils électroniques, nettoyants pour pièces de monnaie et ciseaux, produits de chasse d’air pour automobiles et produits d’isolation. Les expositions cutanées aiguës au 1-bromopropane ont été évaluées uniquement pour les personnes qui utilisent les produits. Pour toutes les utilisations par les consommateurs mentionnées ci-dessus, à l’exception de produits d’isolation, les estimations ont été obtenues par des calculs. L’EPA des États-Unis a conclu que les ME étaient inadéquates pour l’exposition aiguë par inhalation à huit produits de consommation : accélérateurs pour adhésifs, nettoyants tout usage en aérosol, nettoyants pour taches/détachant, produits de nettoyage/élimination de moisissures, nettoyants/dégraissant tout usage en aérosol, nettoyants/dégraissants en aérosol pour les appareils électroniques, nettoyants pour pièces de monnaie et ciseaux et produits de chasse d’air pour automobiles. Les éléments de base impliquaient les préoccupations relatives aux effets négatifs sur le développement qui peuvent survenir à la suite d’une exposition unique au 1-bromopropane pendant une période critique de sensibilité (EPA des États-Unis 2020). En raison des mêmes préoccupations, l’EPA des États-Unis a jugé les ME inadéquates pour quatre expositions cutanées aiguës des consommateurs provenant de : nettoyants tout usage en aérosol, nettoyants pour taches/détachant, nettoyants/dégraissants tout usage en aérosol, produits de chasse d’air pour la climatisation automobile. Cependant,à l’exception d’aérosols de démoulage en silicone, aérosols de nettoyage pour appareils électroniques, et de produits de chasse d’air pour la climatisation automobile. Aucune preuve n’a été relevée indiquant que les produits spécifiés par l’EPA des États-Unis sont disponibles pour les consommateurs au Canada.
7.3.3 Caractérisation des risques pour la santé humaine
Le tableau 7‑8 contient toutes les valeurs pertinentes d’exposition au 1-bromopropane et les dangers associés, ainsi que les marges d’exposition qui en découlent (ME) pour établir des risques autres que le cancer.
| Scénario d’exposition | Concentration d’exposition | Niveau d’effet critique | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Exposition quotidienne par inhalation de l’air | 0,0031 mg/m3 | DR0,1(aug) = 30,5 mg/m3 selon une étude de neurotoxicité comportementale chez le rata | Neurotoxicité ( baisse du temps de traction) chez le rat mâle à 1006 mg/m3 | 9800 |
| Exposition par inhalation par événement : aérosols de démoulage en silicone | 208 mg/m3 | DRÉT1 = 116 mg/m3 selon une étude de toxicité respiratoire pour la reproduction de deux générations de rats | Toxicité pour le développement ( perte après l’implantation) à 2515 mg/m3 | 1 |
| Exposition par inhalation par événement : aérosols de nettoyage pour appareils électroniques | 165 mg/m3 | DRÉT1 = 116 mg/m3 selon une étude de toxicité respiratoire pour la reproduction de deux générations de rats | Toxicité pour le développement ( perte après l’implantation) à 2515 mg/m3 | 1 |
| Exposition par inhalation par événement : produits de chasse d’air pour la climatisation automobile (fluide) | 120 mg/m3 | DRÉT1 = 116 mg/m3 selon une étude de toxicité respiratoire pour la reproduction de deux générations de rats | Toxicité pour le développement ( perte après l’implantation) à 2515 mg/m3 | 1 |
| Exposition par voie cutanée par événement : aérosols de nettoyage pour appareils électroniques | 0.0071 mg/kg p.c. (interne) | DRÉT1 (cutanée) = 14,1 mg/kg p.c./jour selon une étude de toxicité respiratoire pour la reproduction de deux générations de rats b | Toxicité pour le développement ( perte après l’implantation) à 2515 mg/m3 | 2000 |
Abréviations : DR - Limite inférieure de l’intervalle de confiance; ME, Marge d’exposition
a La DR0,1 a été établie à 91,5 mg/m3 dans cette étude. Lorsqu’une exposition est amortie sur 24 heures/jour, 7 jours/semaine, cette DR0,1 a été ajusté à 30,5 mg/m3
b L’équivalent de la DRÉT1 pour l’exposition cutanée a été établi à 14,1 mg/kg p.c./jour selon le calcul suivant : DRÉT1(cutanée) = DRÉT1(inhalation) x taux de ventilation ¸ poids corporel, où DRÉT1(inhalation) = 116 mg/m3, taux de ventilation = 1,5 m3/heure pour 6 heures, et poids corporel = 74 kg.
Concernant l’exposition au 1-bromopropane par inhalation à partir de l’air, la comparaison des effets critiques autres que le cancer aux estimations de la concentration d’expositions dans l’air a donné lieu à une ME jugée adéquate pour tenir compte des incertitudes dans les bases de données sur les effets sur la santé et l’exposition. Cependant, en raison de la toxicité pour la reproduction (classification Repr. 1B du SGH de l’ECHA) de cette substance, cette exposition pourrait être préoccupante pour la santé humaine si elle devait augmenter. Concernant l’exposition par inhalation à des produits de consommation, les marges d’exposition entre les effets critiques et l’estimation de l’absorption de 1-bromopropane , qui sont également prises en considération pour tenir compte des expositions potentielles des personnes non concernées (c.-à-d. les non-utilisateurs), sont jugées potentiellement inadéquates pour tenir compte des incertitudes dans les bases de données. Pour l’exposition cutanée aux produits de consommation, les marges d’exposition entre les effets critiques et l’estimation de l’absorption de 1-bromopropane sont jugées adéquates pour tenir compte des incertitudes dans les bases de données sur les effets sur la santé et l’exposition.
Le risque unitaire d’exposition par inhalation de 1 x 10-6 (µg/m3)-1 chez les humains, basé sur l’adénome ou le carcinome alvéolaire/bronchiolaire chez les souris femelles, dérivé par l’EPA des États-Unis (2020), a été utilisé pour calculer des estimations quantitatives du risque de cancer associé au 1-bromopropane pour la population canadienne (annexe B). Ce risque unitaire d’exposition par inhalation a été obtenu en ajustant le modèle multistade aux données dose-réponse de l’étude du NTP (2011) sur les souris femelles (EPA des États-Unis 2020). La dose# quotidienne moyenne pour la durée de vie (DQMV) pour le 1-bromopropane dans l’air a été modifiée à l’aide de facteurs d’ajustement en fonction de l’âge (FAFA) (annexe B, tableau B-1). La DQMV pour le 1-brompropane dans l’air a été utilisée pour calculer la hausse incrémentielle du risque de cancer au cours de la (RCAV). La DADL a été déterminée comme étant de 0,69 µg/kg p.c./jour (Annexe B, Tableau B-6. La a été établie à 0,69 µg/kg p.c./jour (annexe B, tableau B-6). Ces facteurs ont ensuite été utilisés pour calculer le risque de cancer pour chaque groupe d’âge (voir l’annexe B, tableau B-7). Le risque de cancer au cours de la vie qui a été calculé en utilisant le risque unitaire par inhalation de 1 x 10-6 (µg/m3)-1 et en appliquant les FAFA appropriés aux estimations de l’exposition. Le risque de cancet ainsi obtenu est de 4,3 x 10-6, une valeur jugée acceptable compte tenu des incertitudes des bases de données sur l’exposition et le danger. Cependant, en raison de la cancérogénicité potentielle (classification 2B du CIRC), cette substance pourrait être une source de préoccupations pour la santé humaine si l’exposition venait à augmenter.
7.3.4 Incertitudes de l’évaluation des risques pour la santé humaine
Les plus importantes sources d’incertitude sont présentées au tableau suivant.
| Principales sources d’incertitude | Impact |
|---|---|
| Aucune donnée fiable de surveillance environnementale de l’air ambiant, de l’eau, du sol, de la poussière ou des aliments au Canada n’était disponible. | +/- |
| Aucune donnée sur l’exposition liée à la vie à proximité d’un nettoyeur à sec | - |
| Absence d’étude sur la toxicité due à l’exposition cutanée | +/- |
+ = incertitude avec potentiel de surestimation de l’exposition/risque; – = incertitude avec potentiel de sous-estimation du risque d’exposition; +/ – = potentiel inconnu de surestimation ou de sous-estimation du risque.
7.4 Trans-dichloroéthylène
7.4.1 Évaluation de l'exposition
7.4.1.1 Milieux environnementaux
Aucune donnée fiable de surveillance environnementale n’a été identifiée pour le trans-dichloroéthylène dans l’eau, le sol, la poussière ou les aliments au Canada ni ailleurs. Compte tenu de sa pression de vapeur très élevée et de la constante de la loi de Henry, on s’attend à ce que le trans-dichloroéthylène se volatilise à partir du sol et de l’eau. Par conséquent, l’exposition au trans-dichloroéthylène dans les milieux naturels devrait se produire principalement dans l’air.
Les concentrations de trans-dichloroéthylène mesurées dans l’air ambiant et intérieur au Canada sont présentées à l’annexe A, et sont résumées ci-dessous.
Entre 1990 et 2013, le trans-dichloroéthylène a été surveillé par le programme du RNSPA, dont les mesures de concentrations moyennes dans l’air ambiant à divers sites à travers le Canada étaient comprises entre les valeurs non détectées (LD de 0,013 à 0,083 µg/m3) et 0,065 µg/m3 (LD : 0,013 µg/m3) et les concentrations du 95e percentile entre les valeurs non détectées et 0,060 µg/m3 (LD : 0,013 µg/m3) (ECCC 2019). Les concentrations de trans-dichloroéthylène dans l’air ambiant ont également été mesurées dans le cadre sept études canadiennes sur la qualité de l’air menées à Windsor, Régina, Halifax, Edmonton, Montréal, Sault-Ste-Marie et Ottawa (Santé Canada 2010a, 2010 b, 2010c, 2012, 2013), [Communication personnelle de Tim Shin et Ron Garson, BQEA, 27 mai 2021; source non citée. Les détails de la conception de l’étude ont été présentés ailleurs (c.-à-d., Dales et al. 2013, Mallach et al. 2017)]). La moyenne géométrique et le 95e percentile des concentrations mesurées dans l’air ambiant de ces villes canadiennes se situaient respectivement entre des valeurs non détectées (la LD se situait entre 0,018 et 0,042) et 0,042 µg/m3 et entre des valeurs non détectées et 0,314 µg/m3.
Les concentrations de trans-dichloroéthylène dans l’air intérieur ont également été mesurées dans les sept mêmes études canadiennes mentionnées ci-dessus, ainsi qu’à Swan Lake, en Ontario, dans le cadre du projet de l’Étude de la qualité de l’air intérieur des Premières nations (Santé Canada 2010a, 2010 b, 2010c, 2012, 2013) [Communication personnelle de Tim Shin et Ron Garson, BQEA, 27 mai 2021; source non citée. Les détails de la conception de l’étude ont été présentés ailleurs (c.-à-d., c.-à-d. Weichenthal et coll. 2012)]). La moyenne géométrique et le 95e percentile des concentrations de trans-dichloroéthylène mesurées dans l’air intérieur de ces villes canadiennes se situaient entre les valeurs non détectées (la LD se situait entre 0,018 et 0,055) et 0,535 µg/m3 et entre les valeurs non détectées et 0,255 µg/m3, respectivement.
Le trans-dichloroéthylène a également été mesuré dans l’air individuel lors de l’étude sur l’air à Windsor, en Ontario (Santé Canada, 2010c). Les concentrations géométriques et celles du 95e percentile en hiver et en été étaient à la LD (0,069 µg/m3).
Lors du traitement des résultats inférieurs à la limite de détection en laboratoire (LD) des études canadiennes sur la qualité de l’air menées à Halifax, Edmonton, Montréal, Sault-Ste-Marie et Ottawa (communication personnelle de Tim Shin et Ron Garson, BQEA, Santé Canada, 27 mai 2021; source non citée, les détails de la conception de l’étude ont été présentés ailleurs [c.-à-d. Dales et coll. 2013, Mallach et coll. 2017]), les valeurs utilisées dans l’analyse statistique ont été les valeurs rapportées. Les résultats ont été jugés valides, car le temps de rétention et les ions cibles/les ions qualificatifs dans le chromatogramme obtenu par chromatographie en phase gazeuse-spectrométrie de masse (CG-SM) répondaient aux critères d’analyse du laboratoire. Concernant l’analyse statistique des études canadiennes sur la qualité de l’air menées à Regina et à Windsor (Santé Canada 2010 b, 2010c), les valeurs inférieures à la LD ont été rapportées à la moitié de la LD. De plus, lorsqu’aucun pic ou d’ions cibles/de qualification n’a été observé dans le chromatogramme CG-SM du laboratoire, la concentration de trans-dichloroéthylène a été déclarée comme étant nulle, car les critères de quantification n’étaient pas respectés. Les résultats ont été jugés valides et remplacés par une valeur proche de zéro (0,0001 µg/m3) ou par une valeur égale à la moitié de la limite de détection minimum (LDM) correspondante pour calculer les statistiques descriptives par transformation logarithmique.
La concentration du 95e percentile la plus élevée mesurée dans l’air ambiant ou intérieur au Canada (c.-à-d. 0,314 µg/m3 dans l’étude effectuée à Regina; échantillonnage de cinq jours dans 101 foyers) (Santé Canada, 2010 b) a été utilisée pour estimer l’exposition de la population générale au trans-dichloroéthylène dans l’air. Cette concentration mesurée par la surveillance de l’air a été convertie en une dose interne pour la comparaison avec le Niveau d’effet critique (voir l’annexe D pour plus de détails)).
7.4.1.2 Produits disponibles pour les consommateurs
L’utilisation de produits disponibles pour les consommateurs contenant du trans-dichloroéthylène peut entraîner une exposition de la population générale par voie cutanée et/ou par inhalation. Selon les types de produits utilisés par les consommateurs (par exemple, nettoyant ou dégraissant pour les appareils électriques ou les pièces électroniques, nettoyant en poudre pour les taches sur les textiles, produits de chasse d’air pour la climatisation automobile et mousse isolante en aérosol), on s’attend à une utilisation intermittente par des personnes adultes. De plus, aucune utilisation destinée aux enfants n’a été déclarée pour le trans-dichloroéthylène en réponse aux enquêtes menées en vertu de l’article 71 de la LCPE (Canada 2009, 2012).
Les produits d’isolation en mousse à deux composants pulvérisée à basse pression contenant du trans-dichloroéthylène sont disponibles en vente libre chez les détaillants dans des systèmes ( trousses ) fournissant jusqu’à environ 0,04 mètre cube (15 pieds-planche) de mousse pulvérisée (soit un emballage de 0,99 kg). Les produits d’isolation en mousse à deux composants pulvérisée à basse pression contenant du trans-dichloroéthylène sont disponibles en vente libre chez les détaillants dans des systèmes ( trousses ) fournissant jusqu’à environ 0,04 mètre cube (15 pieds-planche) de mousse pulvérisée (soit un emballage de 0,99 kg). Bien que l’étiquette du produit indique qu’il est « destiné à un usage professionnel », la disponibilité et le faible volume du produit n’excluent pas son utilisation par des bricoleurs. C’est pourquoi un scénario a été élaboré pour les propriétaires de maisons qui utilisent des produits d’isolation en mousse pulvérisée pour de petits projets (p. ex., pour isoler les espaces, les fissures, les joints de dilatation et autres fuites d’air).
Les estimations d’exposition au détachant en poudre pour textile ont été jugées pertinentes pour la population générale du Canada et représentent le niveau le plus élevé d’exposition potentielle par voie cutanée et par inhalation (appelées scénarios sentinelles) pour les groupes d’âge pertinents. Elles sont présentées dans le tableau 7‑10. Les expositions potentielles ont été estimées à partir d’hypothèses prudentes. Les détails sont présentés à l’annexe C. D’autres scénarios d’utilisation potentielle du trans-dichloroéthylène ont été envisagés (réfrigérant, nettoyant ou dégraissant, mousse d’isolation), mais ils ont conduit à des estimations d’exposition plus faibles que celles présentées dans le tableau 7‑10.
| Substance | Scénario d’exposition au produit | Concentration (%)a | Voie d’exposition | Dose interne le jour de l’exposition (mg/kg p.c.) | Concentration moyenne le jour de l’exposition (mg/m3) |
|---|---|---|---|---|---|
| Trans-dichloroéthylène | nettoyant en poudre pour les taches sur les textiles (aérosol) | 60 | Cutanée | 0,259 | - |
| Trans-dichloroéthylène | détachant en poudre pour textile (aérosol) | 60 | Respiratoire | 4,40 | 22,0 |
a FS 2017d
-: sans objet
7.4.1.3 Biosurveillance
Des données de biosurveillance ont été repérées dans la National Health and Nutrition Examination Survey des É.-U. (NHANES) (enquête nationale sur la nutrition et la santé) portant sur le trans-dichloroéthylène (2013-2012) (CDC 2013). Le trans-dichloroéthylène n’a pas été détecté dans le sang entier analysé dans la population américaine. Aucune donnée de biosurveillance canadienne n’est disponible.
7.4.2 Évaluation des effets sur la santé
L’EPA des États-Unis (2020) a résumé la documentation sur les effets sur la santé et a caractérisé le danger du trans-dichloroéthylène. Une recherche documentaire a été effectuée sur la période allant de l’année précédant l’EPA des États-Unis (2020) à mars 2019). Aucune nouvelle étude sur les effets sur la santé qui aurait un impact sur la caractérisation des risques (c.-à-d. qui donnerait lieu à des critères d’effet différents ou à des points de départ plus bas que ceux indiqués dans EPA des États-Unis (2020) n’a été identifiée. La présente section fournit les paramètres critiques et les niveaux d’effet correspondants à utiliser pour la caractérisation des risques, tels que cités directement par l’EPA des États-Unis (2010).
Peu de données toxicocinétiques sont disponibles sur le trans-dichloroéthylène (EPA des États-Unis 2010). Des études menées sur des animaux indiquent est facilement absorbé par la voie respiratoire, et malgré l’absence d’études sur l’absorption cutanée, ses propriétés physico-chimiques indiquent qu’il est également susceptible d’être absorbé après une exposition cutanée. Le trans-1,2-dichloréthène est principalement métabolisé par le CYP2E1 en dichloroacétaldéhyde, qui est facilement converti en acide dichloroacétique et en dichoro-,2-éthanol. Un métabolisme ultérieur par le GSH est peu probable. Aucune information n’est disponible sur l’élimination du trans-dichloroéthylène.
Une étude d’exposition répétée de 13 semaines a été menée chez des souris (CD-1), par voie orale. Les animaux d’essai (8-12/sexe/dose) ont été exposés pendant 90 jours à 0, 17, 175 ou 287 mg/kg p.c./jour (mâles), ou à 0, 23, 224 ou 452 mg/kg p.c./jour (femelles) par l’eau potable. La DRÉT1 d’immunotoxicité a été établie à 65 mg/kg p.c./jour, mesurée par une baisse, chez les souris mâles, du nombre de cellules productrices d’anticorps de la rate contre les érythrocytes de mouton (Shopp et al. 1985, cité dans EPA des États-Unis 2010), et la CMENO a été établie à 175 mg/kg p.c./jour. The EPA des États-Unis (2010) a conclu que cet effet indiquait une suppression du système immunitaire humoral.
Des effets sur le foie et le thymus ont également été observés dans d’autres études de toxicité subchroniques par voie orale, mais avec des points de départ plus élevés (c.-à-d. 190 et 138,5 mg/kg p.c./jour pour les effets sur le foie et le thymus respectivement) (Barnes et al. 1985, cité dans EPA des États-Unis 2010; NTP 2002, cité dans EPA des États-Unis 2010).
Une étude d’exposition répétée par inhalation de 16 semaines a été menée chez des rats femelles (SPR Wistar). Les animaux d’essai ont été exposés pendant 1, 2, 8 ou 16 semaines (8 heures/jour, 5 jours/semaine) à un air contenant 792 mg/m3 (6/concentration) de trans-dichloroéthylène. Des effets, notamment sur le foie, ont été observés à la concentration d’essai de 792 mg/m3 et se sont manifestés par une accumulation de graisse dans les lobules du foie et les cellules de Kupffer, un effet dont l’incidence et la gravité augmentaient également avec la durée de l’exposition (Freundt et al. 1977, cité dans EPA des États-Unis 2010).
Une étude d’exposition répétée par inhalation de 90 jours a été menée chez les rats (Crl:CD®BR). Les animaux d’essai ont été exposés pendant 6 heures/jour, 5 jours/semaine à 0, 792, 3960 ou 15 800 mg/m3 (15/sexe/concentration). Une diminution du nombre de lymphocytes a été observée (significative uniquement à la dose élevée chez les mâles), mais la signification toxicologique de cette diminution était incertaine en raison du niveau élevé de variabilité chez les animaux témoins pour ce paramètre entre les études, et de la possibilité que cet effet soit dû au stress plutôt qu’à l’exposition au trans-dichloroéthylène. Cependant, il a également été signalé que le trans-dichloroéthylène était irritant pour les rats à une concentration de 7940 mg/m3 (Hurtt et al. 1993, cité dans EPA des États-Unis 2010). Par conséquent, il est possible que la diminution du nombre de lymphocytes reflète une augmentation des niveaux de glucocorticoïdes liée au stress et une redistribution des globules blancs entre le sang et d’autres composants immunitaires chez le rat. Le Niveau d’effet critique était donc un CSENO de 15 800 mg/m3 (Dupont et al. 1998, cité dans EPA des États-Unis 2010).
Bien que les effets sur le foie soient l’effet le plus couramment observé à la suite d’une exposition orale au trans-dichloroéthylène, les preuves de la toxicité pour le foie ont été jugées incohérentes par l’EPA des États-Unis (2010); l’étude d’exposition par inhalation de 16 semaines sur des rats (SPR Wistar) a révélé des effets sur le foie à 792 mg/m3, alors que l’étude d’inhalation de 13 semaines sur des rats (Crl:CD®BR) n’a révélé aucun effet sur le foie à cette concentration ni à des concentrations supérieures. Par conséquent, les données des deux études subchroniques d’exposition par inhalation décrites ci-dessus (Freundt et coll. 1977 et Dupont et coll. 1998, respectivement) ont été jugées insuffisantes par l’EPA des États-Unis pour établir une concentration de référence pour l’exposition par inhalation.
Une étude de toxicité pour le développement due à l’exposition par inhalation a été menée chez le rat (Crl:CD®BR). Des femelles gravides (N=24) ont été exposées aux JG 7-16 (6 heures/jour) à 0, 7920, 23760 et 47520 mg/m3 de cette substance. La CSENO pour le développement a été établie par de cette étude à 23 760 mg/m3 selon une diminution du poids corporel du fœtus (Dupont 1988, cité dans EPA des États-Unis, 2010), qui a été observée à 47 520 mg/m3 en présence d’une toxicité chez les mères (c.-à-d. une diminution du poids corporel chez les mères et de la consommation alimentaire) (Dupont 1988, cité dans EPA des États-Unis, 2010).
Aucune étude sur le potentiel cancérigène du trans-dichloroéthylène n’est disponible (p. ex. études épidémiologiques chez les humains ni études chroniques chez les animaux de laboratoire) et les études de génotoxicité in vivo et in vitro ont donné des résultats globalement négatifs (EPA des États-Unis 2010). Des résultats faibles, mais positifs ont été obtenus dans des lymphocytes humains lors des tests du micronoyau et essais de Comet (Tafazoli et Kisch-Volders, 1996, cités dans EPA des États-Unis 2010); cependant, ces résultats ne sont pas cohérents avec l’ensemble de la base de données sur la génotoxicité et doivent être confirmés.
7.4.3 Caractérisation des risques pour la santé humaine
Le tableau 7‑11 provides the relevant exposure and hazard values for trans-dichloroéthylène, as well as resultant margins of exposure (MEs), for determination of non-cancer risk.
| Scénario d’exposition | Concentration d’exposition | Niveau d’effet critique | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Exposition par inhalation de l’air | 0,00023 mg/kg p.c./joura | DRÉT1 = 65 mg/kg p.c./jour fondée sur une étude de 90 jours à doses répétées dans l’eau potable chez la souris mâle | Mesure d’immunotoxicité par la baisse du nombre de CPA contre les érythrocytes de mouton, à 175 mg/kg p.c./jour | 283 000 |
| Exposition par inhalation au détachant en poudre pour textile (fluide) | 22,0 mg/m3 | CSENO = 23 760 mg/m3 fondée sur une étude de toxicité pour le développement due à l’exposition par inhalation chez le rat. | Diminution du poids corporel du fœtus à 47 520 mg/m3 | 1100 |
| Exposition cutanée au détachant en poudre pour textile (fluide) | 0,259 mg/kg p.c. (interne) | CSENO( cutanée) = 2 890 mg/m3 fondée sur une étude de toxicité pour le développement due à l’exposition par inhalation chez le rat b | Diminution du poids corporel du fœtus à 47 520 mg/m3 | 11 000 |
Abréviations : CPA, cellules productrices d’anticorps; ME, marge d’exposition; CSENO, concentration sans effet nocif observé; DRÉT1, limite de confiance inférieure à une réponse de référence [RR] d’un écart-type de 1 (ÉT1) ajusté)
a Estimation de la dose journalière potentielle due à l’exposition par inhalation dans l’air de la sous-population la plus exposée (c.-à-d. les enfants de 1 an), calculée à partir de la concentration la plus élevée du 95e percentile mesurée au Canada. Les estimations de la dose journalière potentielle pour toutes les sous-populations sont présentées à l’annexe D.
b La CSENO équivalente à l’exposition cutanée de 2980 mg/kg p.c. a été déterminée comme suit : CSENO(cutanée) = CSENO(inhalation) x taux de ventilation ¸ Poids corporel, où CSENO(inhalation) = 23 760 mg/m3, taux de ventilation = 1,5 m3/h pour 6 heures, et poids corporel = 74 kg.
Concernant le trans-dichloroéthylène, la comparaison des effets critiques non liés au cancer associés à l’exposition par inhalation à partir de l’air et de l’exposition par inhalation et par voie cutanée à des produits utilisés par les consommateurs avec les estimations de concentrations d’exposition produit une ME jugée adéquate pour tenir compte des incertitudes dans les bases de données sur les effets sur la santé et l’exposition. Les ME obtenues pour l’exposition par inhalation aux produits de consommation sont également jugées adéquates pour tenir compte de l’exposition potentielle de tiers (c.-à-d. les non-utilisateurs).
7.4.4 Sources d’incertitude dans la caractérisation des risques
Les plus importantes sources d’incertitude sont présentées au tableau suivant.
| Principale source d’incertitude | Impact |
|---|---|
| Aucune donnée fiable de surveillance environnementale de l’eau, du sol, de la poussière ou des aliments au Canada n’était disponible. | +/- |
| Absence d’étude sur la toxicité pour la reproduction et d’étude de cancérogénicité | +/- |
| Absence d’étude sur la toxicité due à l’exposition cutanée | +/- |
| La base de données ne permet pas de déterminer clairement la sensibilité aux effets sur le foie des espèces et des souches | +/- |
+ = incertitude quant au potentiel de surestimation de l’exposition/risque; – = incertitude quant au potentiel de sous-estimation du risque d’exposition; +/ – = potentiel inconnu de surestimation ou de sous-estimation du risque.
8. Conclusion
Compte tenu de tous les éléments de preuve contenus dans la présente ebauche d’évaluation préalable, les quatre substances du groupe des halogénures d’alkyle présentent un faible risque d’effets nocifs sur l’environnement Il est proposé de conclure que le bromoéthane, le chloroéthane, le 1-bromopropane et le trans-dichloroéthylène ne satisfont pas aux critères énoncés aux alinéas 64a) et b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
À la lumière des renseignements contenus dans la présente évaluation préalable, il est proposé de conclure que le bromoéthane, le chloroéthane et le trans-dichloroéthylène ne répondent pas aux critères de l'alinéa 64c) de la LCPE, car ils ne pénètrent pas dans l'environnement en une quantité, à une concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
À la lumière des renseignements contenus dans la présente évaluation préalable, il est proposé de conclure que le 1-bromopropane satisfait aux critères du paragraphe 64c) de la LCPE, car il pénètre ou peut pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la santé ou la vie humaine.
Par conséquent, il est proposé de conclure que le 1-bromopropane satisfait à un ou plusieurs des critères de l’article 64 de la LCPE, que le bromoéthane, le chloroéthane et le trans-dichloroéthylène ne satisfont pas à aucun des critères del’article 64 de la Loi canadienne sur la protection de l’environnement.
ll est aussi proposé de conclure que le 1-bromopropane répond aux critères de persistance, mais ne répond pas aux critères de bioaccumulation énoncés dans le Règlement sur la persistance et la bioaccumulation de la LCPE.
Références
[ATSDR] Agency for Toxic Substances and Disease Registry. 2018. Toxicology profile for chloroéthane [PDF] [consulté le 30 janvier 2019]. (disponible en anglais seulement)
Boyle EB, Viet SM, Wright DJ, Merrill LS, Alwis KU, Blount BC, Mortensen ME, Moye Jr. J, Dellarco M. 2016. Assessment of Exposure to VOCs among Pregnant Women in the National Children’s Study. Int J Environ Res Public Health. 13(4):376. (disponible en anglais seulement)
Boublík T, Fried V, Hála E. 1984. The vapour pressures of pure substances: Selected values of the temperature dependence of the vapour pressures of some pure substances in the normal and low pressure region (2nd Revised ed.). Amsterdam, The Netherlands: Elsevier Science Publishers. (disponible en anglais seulement)
Canada. Ministère de l’Environnement. 2009. Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances inanimées (chimiques) inscrites sur la Liste intérieure [PDF] . Gazette du Canada, Partie I, vol. 143, no. 40, p. 2945-2956.
Canada. Ministère de l’Environnement. 2012. Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances de la Liste intérieure [PDF]. Gazette du Canada, Partie I, vol. 146, no. 48, Supplément.
Canada. 2013. Enquête canadienne sur les mesures de la santé. (ECMS). Cycle 3. 2012-2013.
[Cal EPA] California Environmental Protection Agency. 2012. No significant risk level (NSRL) for the proposition 65 carcinogen bromoéthane [PDF] [consulté le 4 mars 2019]. (disponible en anglais seulement)
ChemIDplus [base de données]. 2018. Bethesda (MD): US National Library of Medicine. [précisée; consulté le; consulté le 30 octobre 2018]. (disponible en anglais seulement)
[CIRC] Centre international de recherche sur le cancer. 1999. Bromoethane (Group 3) [PDF]. [consulté le 25 février 2019]. (disponible en anglais seulement)
[CIRC] Centre international de recherche sur le cancer. 1999. Chloroethane (Group 3) [PDF]. [consulté le 25 février 2019]. (disponible en anglais seulement)
[CIRC] Centre international de recherche sur le cancer. 2018. Some industrial chemicals. Monogr Eval Carcinog Risk Chem Hum. 115:37-67. (disponible en anglais seulement)
[ConsExpo Web] Consumer Exposure Web Model. 2018. Bilthoven (NL): Rijksinstituut voor Volksgezondheid en Milieu [National Institute for Public Health and the Environment]. (disponible en anglais seulement)
Dales R, Kauri LM, Sabit C, Mamun M, Weichenthal SA, Ryswyk KV, Kumarathasan P, Thomson E, Vincent R, Broad G, Liu L. 2013. Acute changes in lung function associated with proximity to a steel plant: A randomized study. Environ Int. 55:15-19. (disponible en anglais seulement)
[ECCC] Environnement et Changements climatiques Canada. 2009. Recherche de substances. [consulté le 24 octobre 2019]. (disponible en anglais seulement)
[ECCC, SC] Environnement et Changements climatiques Canada, Santé Canada. 2015. Identification des priorités d’évaluation des risques : Résultats de l’examen de 2015 [PDF]. Ottawa (Ontario): Gouvernement du Canada.
[ECCC] Environnement et Changements climatiques Canada. 2016. Document sur l’approche scientifique : Classification du risque écologique des substances organiques. Ottawa (Ontario) : Gouvernement du Canada.
[ECCC, SC] Environnement et Changements climatiques Canada, Santé Canada. 2018a. Évaluation rapide de substances auxquelles l’exposition de la population générale est limitée. Ottawa (Ontario) : Gouvernement du Canada.
[ECCC, SC] Environnement et Changements climatiques Canada, Santé Canada. 2018 b. Évaluation préalable substances jugées comme étant peu préoccupantes au moyen de l’approche de la Classification du risque écologique des substances organiques et de l’approche fondée sur le seuil de préoccupation toxicologique (SPT). Ottawa (Ontario) : Gouvernement du Canada.
[ECCC] Environnement et Changements climatiques Canada. 2019. Produits de données du Programme SNPA [consulté le 16 avril 2019].
[ECHA] Agence européenne des produits chimiques. 2019. Summary of classification and labelling - bromoethane. [consulté le 24 octobre 2019]. (disponible en anglais seulement)
[ECHA] Agence européenne des produits chimiques. 2019. Summary of classification and labelling – chloroethane. [consulté le 24 octobre 2019]. (disponible en anglais seulement)
Environment Canada. 2013. Données de la Mise à jour de l’inventaire de la LIS recueillies en vertu du de l’article 71 de la Loi canadienne sur la protection de l’environnement de 1999 : Avis modifiant l’Avis concernant certaines substances de la Liste intérieure. Données préparées par : Environnement Canada, Santé Canada ; Programme des substances existantes.
[EPA des États-Unis] United States Environmental Protection Agency. 1987. Household solvent products: A national usage survey [PDF]. (EPA-OTS 560/5-87-005). Washington (DC): EPA des États-Unis, Office of Toxic Substances, Office of Pesticides and Toxic Substances. (disponible en anglais seulement)
[EPA des États-Unis] United States Environmental Protection Agency. 1989. Bromomethane; CASRN 74-83-8 Carcinogenicity Assessment (II.). Washington (DC): EPA des États-Unis. [consulté le 2019 March 15]. (disponible en anglais seulement)
[EPA des États-Unis] United States Environmental Protection Agency. 2005. Supplémental guidance for assessing susceptibility from early-life exposure to carcinogens [PDF]. Washington (DC): EPA des États-Unis. [consulté le 2019 March]. (disponible en anglais seulement)
[EPA des États-Unis] United States Environmental Protection Agency. 2010. Toxicological Review of cis-1,2-dichloroethylene and trans-1,2-dichloroethylene. Washington (DC): EPA des États-Unis. EPA/635/R-09/006F. (disponible en anglais seulement)
[EPA des États-Unis] United States Environmental Protection Agency. 2011. Chapter 6: Inhalation Rates. Exposure Factors Handbook 2011 Edition (Final). Washington (DC): EPA des États-Unis. EPA/600/R-09/052F. (disponible en anglais seulement)
[EPA des États-Unis] United States Environmental Protection Agency. 2016. TSCA Work Plan Chemical Risk Assessment PEER REVIEW DRAFT 1-bromopropane : (n-Propyl Bromide) Spray Adhesives, Dry Cleaning, and Degreasing Uses NE CAS: 106-94-5 [PDF]. Washington (DC): EPA des États-Unis. [consulté le 15 April 2019]. (disponible en anglais seulement)
[EPA des États-Unis] United States Environmental Protection Agency. 2018a. ChemView [base de données sur Internet]. Washington (DC): EPA des États-Unis. [updated 2018 October 26; consulté le 31 October 2019]. (disponible en anglais seulement)
[EPA des États-Unis] United States Environmental Protection Agency. 2018 b. Problem Formulation of the Risk Evaluation for 1-bromopropane [PDF] . Washington (DC): EPA des États-Unis. [consulté le 15 April 2019]. (disponible en anglais seulement)
[EPA des États-Unis] US Environmental Protection Agency. 2020. Risk Evaluation for 1-bromopropane [PDF]. Washington (DC): EPA des États-Unis, Office of Chemical Safety and Pollution Prevention. [consulté le 12 août 2020]. (disponible en anglais seulement)
Frasch HF, Dotson GS and Barbero AM. 2011. In vitro human epidermal penetration of 1-bromopropane. J Tox Env Health, Part A. 74(19):1249-1260. (disponible en anglais seulement)
Great Lake Chemical Corporation. 2002. Test Plan for Ethyl bromide (NE CAS 74-96-4) [PDF]. [consulté le 19 décembre 2019]. (disponible en anglais seulement)
[HSDB] Hazardous Substances Data Bank, 2002 [Database]. Ethyl bromide. Bethesda (MD): National Library of Medicine. [consulté le 28 novembre 2018]. (disponible en anglais seulement)
[HSDB] [HSDS] Hazardous Substances Data Bank, 2013 [Database]. 1-bromopropane . Bethesda (MD): National Library of Medicine. [consulté le 28 novembre 2018]. (disponible en anglais seulement)
Konietzko H. 1984. Chlorinated ethanes: Sources, distribution, environmental impact and health effects. Hazard Assessment of Chemicals. 3:401-448. (disponible en anglais seulement)
Li Y, Cakmak S, Zhu J. 2019. Profiles and monthly variations of selected volatile organic compounds in indoor air in Canadian homes: results of Canadian national indoor air survey 2012-2013. Environ Int. 126:134–144. (disponible en anglais seulement)
Mallach G, St-Jean M, MacNeill M, Aubin D, Wallace L, Shin T, Van Ryswyk K, Kulka R, You H, Fugler D, et al. 2017. Exhaust ventilation in attached garages improves residential indoor air quality. Indoor Air. 27(2):487-499. (disponible en anglais seulement)
Morgan A, Black A, Belcher DR. 1970. The excretion in breath of aliphatic halogenated hydrocarbons following administration by inhalation. Ann Occup Hyg. 13:210-233. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2010. HFE Super Cleaner Degreaser [PDF]. Burlington (ON): MG Chemicals. [consulté le 11 avril 2019]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2014. Contact Cleaner 2000 Precision Cleaner [PDF]. Warminster, (PA): CRC Industries Inc. [consulté le 8 février 2019]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2015a. Dura II A/C Flush Solvent [PDF]. Lewisvill (TX): MicroCare Corporation. [consulté le 11 avril 2019]. (disponible en anglais seulement)
[MSDS] Safety Data Sheet. 2016a. Silicone Mold Release [PDF]. Warminster (PA): CRC Industries Inc. [consulté le September 2019]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2016 b. Touch ‘n Foam Professional System 15 CCMC Part-A [PDF]. Pacific (MO): Convenience Products. [consulté le 11 avril 2019]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2016c. Touch ‘n Foam Professional System 15 CCMC Part-B [PDF]. Pacific (MO): Convenience Products. [consulté le 11 avril 2019]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2017a. Ace Starting Fluid [PDF]. Brampton (ON): Kleen-Flo Tumber Ind. Ltd. [consulté le 21 novembre 2018]. (disponible en anglais seulement)
[MSDS] Safety Data Sheet. 2017 b. Tool Crib Electric Contract Cleaner [PDF]. Sycamore (IL): Seymour of Sycamore. [consulté en septembre 2019]. (disponible en anglais seulement)
[MSDS] Safety Data Sheet. 2017c. Johnsen’s Premium A/C Flush Non-Flammable 1 Gallon [PDF]. Cleburne (TX): Technical Chemical Company. [consulté en septembre 2019]. (disponible en anglais seulement)
[MSDS] Material Safety Data Sheet. 2017d. AlbaChem Spot Lifter II [PDF]. Long Island City (NY): Albatross USA Inc. [consulté le 8 février 2019]. (disponible en anglais seulement)
[NTP] National Toxicology Program (États-Unis). 1989. Toxicology and carcinogenesis studies of bromoéthane (ethyl bromide) (CAS No. 74-96-4) in F344/N rats and B6C3F1 mice (inhalation studies) [PDF]. [consulté le 20 décembre 2018]. (disponible en anglais seulement)
[NTP] National Toxicology Program (États-Unis). 1989. Toxicology and carcinogenesis studies of chloroéthane (ethyl chloride) (CAS No. 75-00-3) in F344/N rats and B6C3F1 mice (inhalation studies) [PDF]. [consulté le 10 janvier 2019]. (disponible en anglais seulement)
[NTP] National Toxicology Program (États-Unis). 2016. Reports on Carcinogens, Fourteenth Edition. 1-bromopropane [PDF]. [consulté le 22 février 2019]. (disponible en anglais seulement)
[OCDE] Organisation pour la coopération et le développement économiques . 2006. SIDS Initial Assessment Report for SIAM22 [PDF] [consulté le 1er février 2019]. (disponible en anglais seulement)
OCDE – Boîte à outils QSAR [Outil de références croisées]. 2014. Version 3.3. Paris (FROrganisation de coopération et de développement économiques, Laboratory of Mathematical Chemistry. (disponible en anglais seulement)
[PhysProp] Interactive PhysProp Database [Base de données]. 2013. Syracuse (NY): SRC, Inc. [consulté le 25 mai 2018]. (disponible en anglais seulement)
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [Institut national néérlandais de la santé publique et de l’environnement (Pays-Bas)]. 2014. General fact sheet: general default parameters for estimating consumer exposure: Version mise à jour pour ConsExpo 4 [PDF]. Bilthoven (Pays-Bas) : RIVM. Rapport no : 090013003/2014. [consulté en septembre 2019]. (disponible en anglais seulement)
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [Institut national néérlandais de la santé publique et de l’environnement (Pays-Bas)]. 2018. Cleaning products fact sheet: default parameters for estimating consumer exposure: updated version for ConsExpo 4 [PDF]. Bilthoven (Pays-Bas) : RIVM. Rapport no : 2016-0179. [consulté en septembre 2019]. (disponible en anglais seulement)
Santé Canada. 1998. Facteurs d’exposition pour l’évaluation de l’absorption quotidienne totale de substances prioritaires par la population générale du Canada. Rapport non publié. Ottawa (Ontario) : Santé Canada, Direction de l’hygiène du milieu.
Santé Canada 2010a. Étude sur l’insuffisance cardiaque congestive de Montréal. 2008-2010.
Santé Canada. 2010 b. Étude sur la qualité de l’air intérieur à Regina (2007): Sommaire des données d’échantillonnage des composés organiques volatiles [PDF]. Ottawa (Ontario) : Gouvernement du Canada. [consulté le 24 avril 2019].
Santé Canada. 2010c. Étude l’évaluation de l’exposition à Windsor (2005-2006) : Sommaire des données d’échantillonnage des composés organiques volatiles [PDF]. Ottawa (Ontario) : Gouvernement du Canada. [consulté le 24 avril 2019].
Santé Canada. 2012. Étude sur la qualité de l’air intérieur à Halifax (2009): Sommaire des données d’échantillonnage des composés organiques volatiles. Ottawa (Ontario) : Gouvernement du Canada.
Santé Canada. 2013. Étude sur la qualité de l’air intérieur à Edmonton (2010): Sommaire des données d’échantillonnage des composés organiques volatiles [PDF]. Ottawa (Ontario) : Gouvernement du Canada. [consulté le 2019 April 24].
Santé Canada. 2013. Document d’orientation provisoire sur l’évaluation des risques pour la santé humaine associés à une exposition de courte durée aux substances cancérogènes présentes dans les sites contaminés [PDF]. Ottawa (Ontario) : Gouvernement du Canada. [consulté le 7 mai 2019].
Santé Canada. 2015. Tableau de la consommation alimentaire obtenu à l’aide de Statistique Canada, Enquête sur la santé dans les collectivités canadiennes, cycle 2.2, Nutrition (2004). Fichier de partage. Ottawa (Ontario) : Gouvernement du Canada.
Santé Canada. 2016. Document d’évaluation scientifique : Approche fondée sur le seuil de préoccupation toxicologique (SPT) pour certaines substances. Ottawa (Ontario) : Gouvernement du Canada.
Santé Canada. 2018. Draft backgrounder document on updated default body surface areas for use in ESRAB assessments. Unpublished report. Ottawa (Ontario) : Gouvernement du Canada. (disponible en anglais seulement)
Weichenthal S, Mallach G, Kulka R, Black A, Wheeler A, You H, St-Jean M, Kwiatkowski R, Sharp D. 2012. A randomized double blind cross-over study of indoor air filtration and acute changes in cardiorespiratory health in a First Nations community. Indoor Air. 23(3):175-184. (disponible en anglais seulement)
[WHO] World Health Organization. 2002. Concise International Chemical Assessment Document 42 Bromoéthane [PDF]. [consulté le 14 janvier 2019]. (disponible en anglais seulement)
Annexe A. Concentrations des substances du groupe des halogénures d’alkyle mesurées dans l’air au Canada
| Année d’échantillonnage | Limite de détection de laboratoire (µg/m3) | Nombre d’échantillons | % d’échantillons >LD | Fourchette de concentration (µg/m3) | Moyenne géométrique des concentrations (µg/m3) | 95e percentile (µg/m3) |
|---|---|---|---|---|---|---|
| 1990 | 0,043 | 0 | ‒ | ‒ | ‒ | ‒ |
| 1991 | 0,043 | 443 | 0,0 | < LD | ‒ | < LD |
| 1992 | 0,043 | 3 040 | 0,3 | < LD-0,065 | < LD | < LD |
| 1993 | 0,043 | 2 588 | 0,4 | < LD-0,211 | 0,068 | < LD |
| 1994 | 0,043 | 2 803 | 1,4 | < LD-0,580 | 0,066 | < LD |
| 1995 | 0,043 | 2 179 | 0,6 | < LD-0,152 | < LD | < LD |
| 1996 | 0,043 | 2 252 | 1,4 | < LD-0,094 | < LD | < LD |
| 1997 | 0,043 | 2 000 | 5,2 | < LD-0,563 | < LD | 0,043 |
| 1998 | 0,043 | 2 287 | 0,0 | < LD-0,121 | < LD | < LD |
| 1999 | 0,043 | 2 252 | 19,2 | < LD-0,080 | < LD | 0,050 |
| 2000 | 0,043 | 2 469 | 5,3 | < LD-0,100 | < LD | 0,050 |
| 2001 | 0,043 | 3 027 | 4,6 | < LD-0,150 | < LD | < LD |
| 2002 | 0,043 | 3 437 | 1,9 | < LD-0,125 | < LD | < LD |
| 2003 | 0,043 | 6 095 | 0,1 | < LD-0,098 | < LD | < LD |
| 2004 | 0,043 | 3 253 | 0,0 | < LD | < LD | < LD |
| 2005 | 0,043 | 3 135 | 0,6 | < LD-0,225 | < LD | < LD |
| 2006 | 0,043 | 2 849 | 1,1 | < LD-2,931 | < LD | < LD |
| 2007 | 0,043 | 2 740 | 0,3 | < LD-0,188 | < LD | < LD |
| 2008 | 0,043 | 3 330 | 0,1 | < LD-0,174 | < LD | < LD |
| 2009 | 0,043 | 3 296 | 1,8 | < LD-20,318 | < LD | < LD |
| 2010 | 0,043 | 2 772 | 0,1 | < LD-0,393 | < LD | < LD |
| 2011 | 0,043 | 2 459 | 0,1 | < LD-0,063 | < LD | < LD |
| 2012 | 0,043 | 2 548 | 0,1 | < LD-0,098 | < LD | < LD |
| 2013 | 0,058 | 1 381 | 0,1 | < LD-0,084 | < LD | < LD |
| 2014 | 0,059 | 0 | ‒ | ‒ | ‒ | ‒ |
| 2015 | 0,075 | 0 | ‒ | ‒ | ‒ | ‒ |
| 2016 | 0,093 | 0 | ‒ | ‒ | ‒ | ‒ |
Abréviation : LD = limite de détection
| Saison | Type d’échantillon, durée d’échantillonnage, lieu | LD (µg/m3) | Nombre d’échantillons | Fourchette de concentration (µg/m3) | % foyers > LDa | Moyenne géométrique (µg/m3) | 95e percentile (µg/m3) |
|---|---|---|---|---|---|---|---|
| Été | Intérieur, 24 heures, Edmontonc | 0,065 | 328 | < LD | 0,0 | < LD | < LD |
| Été | Extérieur, 24 heures, Edmontonc | 0,065 | 324 | < LD | 0,0 | < LD | < LD |
| Hiver | Intérieur, 24 heures, Edmontonc | 0,035 | 337 | < LD-0,067 | 2,0 | < LD | < LD |
| Hiver | Extérieur, 24 heures, Edmontonc | 0,035 | 332 | < LD | 0,0 | < LD | < LD |
| Été | Intérieur, 24 heures, Halifaxd | 0,036 | 331 | < LD | 0,0 | < LD | < LD |
| Été | Extérieur, 24 heures, Halifax | 0,036 | 324 | < LD-0,154 | 2,0 | < LD | < LD |
| Hiver | Intérieur, 24 heures, Halifaxd | 0,036 | 312 | < LD | 0,0 | < LD | < LD |
| Hiver | Extérieur, 24 heures, Halifaxd | 0,036 | 287 | < LD | 0,0 | < LD | < LD |
| Été | Intérieur, 24 heures, Reginae | 0,034 | 105 | < LD | 0,0 b | < LD | < LD |
| Été | Intérieur, 5 jReginae | 0,034 | 101 | < LD | 0,0 b | < LD | < LD |
| Été | Extérieur, 24 heures, Reginae | 0,034 | 108 | < LD | 0,0 b | < LD | < LD |
| Été | Extérieur, 5 j, Reginae | 0,034 | 97 | < LD | 0,0 b | < LD | < LD |
| Hiver | Intérieur, 24 heures, Reginae | 0,034 | 105 | < LD | 0,0 b | < LD | < LD |
| Hiver | Intérieur, 5 j, Reginae | 0,034 | 89 | < LD | 1,1 b | < LD | < LD |
| Hiver | Extérieur, 24 heures, Reginae | 0,034 | 94 | < LD | 0,0 b | < LD | < LD |
| Été | Intérieur, 24 heures, Windsorf | 0,070 | 217 | < LD | 0,0 | < LD | < LD |
| Été | Extérieur, 24 heures, Windsorf | 0,070 | 216 | < LD | 0,0 | < LD | < LD |
| Été | Personal, 24-hr, Windsorf | 0,070 | 207 | < LD | 0,0 | < LD | < LD |
| Hiver | Intérieur, 24 heures, Windsorf | 0,070 | 232 | < LD-0,070 | 2,1 | < LD | < LD |
| Hiver | Extérieur, 24 heures, Windsorf | 0,070 | 201 | < LD | 0,0 | < LD | < LD |
| Hiver | Personal, 24-hr, Windsorf | 0,070 | 225 | < LD | 0,0 | < LD | < LD |
| Été | Intérieur, 24 heures, Windsorf | 0,074 | 211 | < LD | 0,0 | < LD | < LD |
| Été | Extérieur, 24 heures, Windsorf | 0,074 | 214 | < LD | 0,0 | < LD | < LD |
| Hiver | Intérieur, 24 heures, Windsorf | 0,074 | 224 | < LD | 0,0 | < LD | < LD |
| Hiver | Extérieur, 24 heures, Windsorf | 0,074 | 214 | < LD | 0,0 | < LD | < LD |
| N.D. | Intérieur, 24 heures, Montrealg | 0,065 | 285 | < LD | 0,0 | < LD | < LD |
| N.D. | Extérieur, 24 heures, Montrealg | 0,036 | 200 | < LD | 0,0 | < LD | < LD |
| Été | Extérieur, 24 heures, Sault Ste-Marieh | 0,029 | 108 | < LD | 0,0 | < LD | < LD |
| Hiver | Intérieur, 24 heures, Swan Lakei | 0,025 | 67 | < LD | 0,0 | < LD | < LD |
| Hiver | Intérieur, 7 j, Swan Lakei | 0,025 | 54 | < LD | 0,0 | < LD | < LD |
| Hiver | Intérieur, 48 h, Ottawaj | 0,022 | 166 | < LD | 3,0 | < LD | < LD |
| Hiver | Extérieur, 48 h, Ottawaj | 0,022 | 151 | < LD | 0,0 | < LD | < LD |
| Hiver | Garage, 48 h, Ottawaj | 0,022 | 206 | < LD | 0,0 | < LD | < LD |
Abréviations : LD, limite de détection; N.D. = Non disponible
a Pourcentage de foyers dont au moins un échantillon indique des valeurs supérieures à la limite de détection.
b Pourcentage d’échantillons dont la valeur est supérieure à la limite de détection.
c Santé Canada 2013
d Santé Canada 2012
e Santé Canada 2010b
f Santé Canada 2010c
g Santé Canada 2010 a
h Communication personnelle de Tim Shin et Ron Garson, BQEA, 27 mai 2021; source non cité. Les détails de la conception de l’étude ont été présentés ailleurs (c.-à-d., Dales et coll. 2013).
i Communication personnelle de Tim Shin et Ron Garson, BQEA, 27 mai 2021; source non cité. Les détails de la conception de l’étude ont été présentés ailleurs (c.-à-d., Weichenthal et coll. 2013) .
j Communication personnelle de Tim Shin et Ron Garson, BQEA, 27 mai 2021; source non cité. Les détails de la conception de l’étude ont été présentés ailleurs (c.-à-d., Mallach et coll.. 2017).
| Année d’échantillonnage | Limite de détection de laboratoire (µg/m3) | Nombre d’échantillons | % d’échantillons >LD | Fourchette de concentration (µg/m3) | Moyenne géométrique (µg/m3) | 95e percentile (µg/m3) |
|---|---|---|---|---|---|---|
| 1990 | 0,027 | 0 | ‒ | ‒ | ‒ | ‒ |
| 1991 | 0,027 | 443 | 24,4 | < LD-2,680 | 0,176 | 0,258 |
| 1992 | 0,027 | 3 040 | 22,2 | < LD-2,857 | 0,085 | 0,235 |
| 1993 | 0,027 | 2 588 | 13,6 | < LD-2,728 | 0,158 | 0,183 |
| 1994 | 0,027 | 2 803 | 33,4 | < LD-49,673 | 0,117 | 0,317 |
| 1995 | 0,027 | 2 179 | 42,3 | < LD-4,613 | 0,062 | 0,230 |
| 1996 | 0,027 | 2 252 | 67,0 | < LD-2,664 | 0,059 | 0,368 |
| 1997 | 0,027 | 2 000 | 90,4 | < LD-5,729 | 0,084 | 0,198 |
| 1998 | 0,027 | 2 287 | 77,8 | < LD-3,100 | 0,061 | 0,180 |
| 1999 | 0,027 | 2 253 | 98,8 | < LD-1,890 | 0,086 | 0,180 |
| 2000 | 0,027 | 2 475 | 99,6 | < LD-2,350 | 0,082 | 0,160 |
| 2001 | 0,027 | 6 537 | 59,1 | < LD-4,355 | 0,040 | 0,113 |
| 2002 | 0,027 | 6 451 | 51,2 | < LD-0,724 | 0,031 | 0,089 |
| 2003 | 0,027 | 9 995 | 14,4 | < LD-0,422 | < LD | 0,047 |
| 2004 | 0,027 | 8 530 | 6,4 | < LD-2,390 | < LD | 0,030 |
| 2005 | 0,027 | 7 716 | 8,6 | < LD-0,937 | < LD | 0,032 |
| 2006 | 0,027 | 7 536 | 10,7 | < LD-0,388 | < LD | 0,037 |
| 2007 | 0,027 | 6 412 | 14,2 | < LD-0,330 | < LD | 0,040 |
| 2008 | 0,027 | 7 066 | 13,6 | < LD-0,183 | < LD | 0,038 |
| 2009 | 0,027 | 6 621 | 9,9 | < LD-2,927 | < LD | 0,034 |
| 2010 | 0,027 | 7 532 | 8,2 | < LD-0,909 | < LD | 0,032 |
| 2011 | 0,027 | 6 933 | 12,8 | < LD-0,144 | < LD | 0,038 |
| 2012 | 0,027 | 6 506 | 8,5 | < LD-0,324 | < LD | 0,032 |
| 2013 | 0,067 | 3 437 | 0,7 | < LD-0,190 | < LD | < LD |
| 2014 | 0,069 | 4 811 | 1,6 | < LD-0,176 | < LD | < LD |
| 2015 | 0,044 | 4 435 | 1,5 | < LD-0,436 | < LD | < LD |
| 2016 | 0,065 | 2 192 | 0,2 | < LD-0,101 | < LD | < LD |
Abréviation : LD = limite de détection
| Saison | Type d’échantillon, durée d’échantillonnage, lieu | LD (µg/m3) | Nombre d’échantillons | Fourchette de concentration (µg/m3) | % homes >LDa | Moyenne géométrique (µg/m3) | 95e percentile (µg/m3) |
|---|---|---|---|---|---|---|---|
| Été | Intérieur, 24 heures, Edmontonc | 0,062 | 328 | < LD-0,105 | 12,0 | < LD | < LD |
| Été | Extérieur, 24 heures, Edmontonc | 0,062 | 324 | < LD-0,071 | 2,0 | < LD | < LD |
| Hiver | Intérieur, 24 heures, Edmontonc | 0,028 | 337 | < LD-0,493 | 52,0 | < LD | 0,053 |
| Hiver | Extérieur, 24 heures, Edmontonc | 0,028 | 332 | < LD-0,258 | 14,0 | < LD | < LD |
| Été | Intérieur, 24 heures, Halifaxd | 0,028 | 331 | < LD-0,132 | 90,0 | < LD | 0,064 |
| Été | Extérieur, 24 heures, Halifaxd | 0,028 | 324 | < LD-0,230 | 56,0 | < LD | 0,036 |
| Hiver | Intérieur, 24 heures, Halifaxd | 0,028 | 312 | < LD-0,110 | 90,0 | < LD | 0,053 |
| Hiver | Extérieur, 24 heures, Halifaxd | 0,028 | 287 | < LD-0,102 | 58,0 | < LD | 0,044 |
| Été | Intérieur, 24 heures, Reginae | 0,039 | 105 | < LD-0,383 | 53,3 b | < LD | 0,100 |
| Été | Intérieur, 5 jReginae | 0,039 | 101 | < LD-0,415 | 64,2 b | 0,040 | 0,113 |
| Été | Extérieur, 24 heures, Reginae | 0,039 | 108 | < LD-0,125 | 12,0 b | < LD | 0,052 |
| Été | Extérieur, 5 j, Reginae | 0,039 | 97 | < LD-0,187 | 124,4 b | < LD | 0,060 |
| Hiver | Intérieur, 24 heures, Reginae | 0,039 | 105 | < LD-0,273 | 43,8 b | < LD | 0,113 |
| Hiver | Intérieur, 5 jReginae | 0,039 | 89 | < LD-0,450 | 52,8 b | < LD | 0,100 |
| Hiver | Extérieur, 24 heures, Reginae | 0,039 | 94 | < LD-0,080 | 3,2 b | < LD | 0,020 |
| Été | Intérieur, 24 heures, Windsorf | 0,115 | 217 | < LD-1,120 | 48,9 | < LD | 0,230 |
| Été | Extérieur, 24 heures, Windsorf | 0,115 | 216 | < LD-0,165 | 2,2 | < LD | < LD |
| Été | Personal, 24-hr, Windsorf | 0,115 | 207 | < LD-1,020 | 38,6 | < LD | 0,160 |
| Hiver | Intérieur, 24 heures, Windsorf | 0,115 | 232 | < LD-1,150 | 2,1 | < LD | < LD |
| Hiver | Extérieur, 24 heures, Windsorf | 0,115 | 201 | < LD | 0,0 | < LD | < LD |
| Hiver | Personal, 24-hr, Windsorf | 0,115 | 225 | < LD-0,360 | 8,5 | < LD | < LD |
| Été | Intérieur, 24 heures, Windsorf | 0,110 | 211 | < LD-0,390 | 23,9 | < LD | 0,123 |
| Été | Extérieur, 24 heures, Windsorf | 0,110 | 213 | < LD-0,162 | 6,7 | < LD | < LD |
| Hiver | Intérieur, 24 heures, Windsorf | 0,110 | 224 | < LD-0,115 | 2,1 | < LD | < LD |
| Hiver | Extérieur, 24 heures, Windsorf | 0,110 | 213 | < LD | 0,0 | < LD | < LD |
| NA | Intérieur, 24 heures, Montrealg | 0,028 | 285 | < LD-0,433 | 77,8 | 0,059 | 0,147 |
| NA | Extérieur, 24 heures, Montrealg | 0,062 | 200 | < LD-0,136 | 55,6 | < LD | < LD |
| Été | Outdoor, 42-hr, Sault Ste-Marieh | 0,027 | 108 | < LD-0,068 | 100,0 | < LD | 0,040 |
| Hiver | Intérieur, 24 heures, Swan Lakei | 0,045 | 67 | < LD -0,300 | 81,0 | 0,071 | 0,220 |
| Hiver | Intérieur, 7 j, Swan Lakei | 0,045 | 54 | < LD-0,267 | 95,2 | 0,092 | 0,233 |
| Hiver | Intérieur, 48 h, Ottawaj | 0,027 | 166 | < LD-0,080 | 97,0 | < LD | 0,036 |
| Hiver | Extérieur, 48 h, Ottawaj | 0,027 | 151 | < LD-0,036 | 69,7 | < LD | < LD |
| Hiver | Garage, 48-hr, Ottawaj | 0,027 | 206 | < LD-0,108 | 97,0 | < LD | 0,040 |
Abréviation : LD = limite de détection; N.D. = Non disponible
a Pourcentage de foyers dont au moins un échantillon indique des valeurs supérieures à la limite de détection.
b Pourcentage d’échantillons dont la valeur est supérieure à la limite de détection.
c Santé Canada 2013
d Santé Canada 2012
e Santé Canada 2010b
f Santé Canada 2010c
g Santé Canada 2010 a
h Communication personnelle de Tim Shin et Ron Garson, BQEA, 27 mai 2021; source non cité. Les détails de la conception de l’étude ont été présentés ailleurs (c.-à-d., Dales et coll. 2013).
i Communication personnelle de Tim Shin et Ron Garson, BQEA, 27 mai 2021; source non cité. Les détails de la conception de l’étude ont été présentés ailleurs (c.-à-d., Weichenthal et coll. 2013) .
j Communication personnelle de Tim Shin et Ron Garson, BQEA, 27 mai 2021; source non cité. Les détails de la conception de l’étude ont été présentés ailleurs (c.-à-d., Mallach et coll.. 2017).
| Type of sample | % detected | MDL (µg/m3) | Maximal concentration (µg/m3) |
|---|---|---|---|
| Indoor | 0.3 | 0.29 | 3.1 |
Abbreviation: MDL, method detection limit
| Année d’échantillonnage | Lab detection limit (µg/m3) | Nombre d’échantillons | % d’échantillons >LD | Fourchette de concentration (µg/m3) | Moyenne géométrique (µg/m3) | 95e percentile (µg/m3) |
|---|---|---|---|---|---|---|
| 1990 | 0.013 | 1 326 | ‒ | < LD-0.000 | ‒ | < LD |
| 1991 | 0.013 | 1 327 | 2.1 | < LD-0.139 | 0.036 | < LD |
| 1992 | 0.013 | 3 040 | 2.7 | < LD-0.223 | < LD | < LD |
| 1993 | 0.013 | 2 588 | 0.9 | < LD-0.267 | 0.065 | < LD |
| 1994 | 0.013 | 2 803 | 0.9 | < LD-0.075 | 0.014 | < LD |
| 1995 | 0.013 | 2 179 | 17.8 | < LD-0.098 | 0.017 | 0.028 |
| 1996 | 0.013 | 2 252 | 31.3 | < LD-0.135 | 0.023 | 0.039 |
| 1997 | 0.013 | 2 000 | 44.7 | < LD-0.220 | 0.030 | 0.060 |
| 1998 | 0.013 | 2 287 | 8.2 | < LD-0.060 | 0.018 | 0.018 |
| 1999 | 0.013 | 2 219 | 67.9 | < LD-0.070 | 0.035 | 0.050 |
| 2000 | 0.013 | 2 469 | 96.2 | < LD-0.830 | 0.028 | 0.040 |
| 2001 | 0.013 | 3 027 | 93.4 | < LD-0.070 | 0.029 | 0.040 |
| 2002 | 0.013 | 3 437 | 84.8 | < LD-0.102 | 0.023 | 0.041 |
| 2003 | 0.013 | 6 095 | 1.0 | < LD-0.817 | < LD | < LD |
| 2004 | 0.013 | 3 253 | 1.0 | < LD-0.849 | < LD | < LD |
| 2005 | 0.013 | 3 135 | 1.3 | < LD-0.233 | < LD | < LD |
| 2006 | 0.013 | 2 849 | 1.2 | < LD-0.398 | < LD | < LD |
| 2007 | 0.013 | 2 740 | 3.2 | < LD-0.516 | < LD | < LD |
| 2008 | 0.013 | 3 330 | 3.7 | < LD-0.371 | < LD | < LD |
| 2009 | 0.013 | 3 296 | 5.6 | < LD-0.349 | < LD | 0.014 |
| 2010 | 0.013 | 2 772 | 23.2 | < LD-2.013 | < LD | 0.044 |
| 2011 | 0.013 | 2 459 | 39.4 | < LD-0.587 | < LD | 0.058 |
| 2012 | 0.013 | 2 548 | 31.3 | < LD-0.277 | < LD | 0.048 |
| 2013 | 0.041 | 1 381 | 8.3 | < LD-2.230 | < LD | 0.059 |
| 2014 | 0.042 | 0 | ‒ | ‒ | ‒ | ‒ |
| 2015 | 0.052 | 0 | ‒ | ‒ | ‒ | ‒ |
| 2016 | 0.083 | 0 | ‒ | ‒ | ‒ | ‒ |
| Saison | Type d’échantillon, durée d’échantillonnage, lieu | LD (µg/m3) | Nombre d’échantillons | Fourchette de concentration (µg/m3) | % homes >LDa | Moyenne géométrique (µg/m3) | 95e percentile (µg/m3) |
|---|---|---|---|---|---|---|---|
| Été | Intérieur, 24 heures, Edmontonc | 0.042 | 328 | < LD-0.135 | 28.0 | < LD | 0.055 |
| Été | Extérieur, 24 heures, Edmontonc | 0.042 | 324 | < LD-0.114 | 34.0 | < LD | 0.046 |
| Hiver | Intérieur, 24 heures, Edmontonc | 0.021 | 337 | < LD-0.484 | 50.0 | < LD | 0.120 |
| Hiver | Extérieur, 24 heures, Edmontonc | 0.021 | 332 | < LD-0.292 | 58.0 | < LD | 0.056 |
| Été | Intérieur, 24 heures, Halifaxd | 0.018 | 331 | < LD-5.084 | 28.0 | < LD | 0.028 |
| Été | Extérieur, 24 heures, Halifaxd | 0.018 | 324 | < LD-0.550 | 28.0 | < LD | 0.024 |
| Hiver | Intérieur, 24 heures, Halifaxd | 0.018 | 312 | < LD | 0.0 | < LD | < LD |
| Hiver | Extérieur, 24 heures, Halifaxd | 0.018 | 287 | < LD | 0.0 | < LD | < LD |
| Été | Intérieur, 24 heures, Reginae | 0.019 | 105 | < LD-2.045 | 10.5 b | < LD | 0.205 |
| Été | Intérieur, 5 jReginae | 0.019 | 101 | < LD-3.305 | 10.9 b | < LD | 0.255 |
| Été | Extérieur, 24 heures, Reginae | 0.019 | 108 | < LD-0.605 | 7.4 b | < LD | 0.098 |
| Été | Extérieur, 5 j, Reginae | 0.019 | 97 | < LD-0.413 | 10.3 b | < LD | 0.314 |
| Hiver | Intérieur, 24 heures, Reginae | 0.019 | 105 | < LD-0.933 | 1.0 b | < LD | < LD |
| Hiver | Intérieur, 5 jReginae | 0.019 | 89 | < LD-1.190 | 1.1 b | < LD | < LD |
| Hiver | Extérieur, 24 heures, Reginae | 0.019 | 94 | < LD | 0.0 b | < LD | < LD |
| Été | Intérieur, 24 heures, Windsorf | 0.069 | 217 | < LD | 0.0 | < LD | < LD |
| Été | Extérieur, 24 heures, Windsorf | 0.069 | 216 | < LD | 0.0 | < LD | < LD |
| Été | Personal, 24-hr, Windsorf | 0.069 | 207 | < LD | 0.0 | < LD | < LD |
| Hiver | Intérieur, 24 heures, Windsorf | 0.069 | 232 | < LD | 0.0 | < LD | < LD |
| Hiver | Extérieur, 24 heures, Windsorf | 0.069 | 201 | < LD | 0.0 | < LD | < LD |
| Hiver | Personal, 24-hr, Windsorf | 0.069 | 225 | < LD | 0.0 | < LD | < LD |
| Été | Intérieur, 24 heures, Windsorf | 0.055 | 211 | < LD-0.110 | 2.2 | < LD | < LD |
| Été | Extérieur, 24 heures, Windsorf | 0.055 | 214 | < LD-0.065 | 2.2 | < LD | < LD |
| Hiver | Intérieur, 24 heures, Windsorf | 0.055 | 224 | < LD | 0.0 | < LD | < LD |
| Hiver | Extérieur, 24 heures, Windsorf | 0.055 | 214 | < LD | 0.0 | < LD | < LD |
| NA | Intérieur, 24 heures, Montrealg | 0.042 | 285 | < LD-1.263 | 55.6 | < LD | 0.060 |
| NA | Extérieur, 24 heures, Montrealg | 0.018 | 200 | < LD-0.084 | 53.7 | 0.019 | 0.053 |
| Été | Outdoor, 42-hr, Sault Ste-Marieh | 0.021 | 108 | < LD-2.228 | 100.0 | 0.042 | 0.088 |
| Hiver | Intérieur, 24 heures, Swan Lakei | 0.020 | 67 | < LD-0.013 | 0.0 | < LD | < LD |
| Hiver | Intérieur, 7 j, Swan Lakei | 0.020 | 54 | < LD-0.027 | 9.5 | < LD | < LD |
| Hiver | Intérieur, 48 h, Ottawaj | 0.017 | 166 | < LD-20.672 | 36.4 | 0.535 | 0.184 |
| Hiver | Extérieur, 48 h, Ottawaj | 0.017 | 151 | < LD-0.132 | 33.3 | < LD | 0.028 |
| Hiver | Garage, 48-hr, Ottawaj | 0.017 | 206 | < LD-16.764 | 42.4 | 0.460 | 0.136 |
Abréviations : LD, limite de détection; N.D. = Non disponible
a Pourcentage de foyers dont au moins un échantillon indique des valeurs supérieures à la limite de détection.
b Pourcentage d’échantillons dont la valeur est supérieure à la limite de détection
c Santé Canada 2013
d Santé Canada 2012
e Santé Canada 2010b
f Santé Canada 2010c
g Santé Canada 2010 a
h Communication personnelle de Tim Shin et Ron Garson, BQEA, 27 mai 2021; source non cité. Les détails de la conception de l’étude ont été présentés ailleurs (c.-à-d., Dales et coll. 2013).
i Communication personnelle de Tim Shin et Ron Garson, BQEA, 27 mai 2021; source non cité. Les détails de la conception de l’étude ont été présentés ailleurs (c.-à-d., Weichenthal et coll. 2013) .
>j Communication personnelle de Tim Shin et Ron Garson, BQEA, 27 mai 2021; source non cité. Les détails de la conception de l’étude ont été présentés ailleurs (c.-à-d., Mallach et coll.. 2017).
Annexe B. Calcul du risque de cancer associé au bromoéthane, au chloroéthane et au 1-bromopropane
Afin d’estimer le risque de cancer lié à l’exposition au bromoéthane, au chloroéthane et au 1-bromopropane, une dose journalière moyenne à vie (DJMV) provenant de l’air a été calculée à l’aide de l’équation suivante (Santé Canada 2013):
DJMV = taux d’exposition x durée d’exposition / durée de vie
où,
taux d’exposition = absorption quotidienne en µg/kg p.c./jour
durée d’exposition = durée d’exposition pendant l’étape du cycle de vie (années)
durée de vie = années d’une vie = 80 ans
Estimations de l’apport quotidien et hypothèses pour divers groupes d’âge dans la population générale du Canada :
- De 0 à 5 mois : Poids présumé de 6,3 kg (Santé Canada 2015) et respiration de 3,7 m3 d’air par jour (EPA des États-Unis 2011).
- 6 à 11 mois : Poids présumé de 9,1 kg (Santé Canada, 2015) et volume d’air respiré de 5,4 m3 par jour (EPA des États-Unis, 2011).
- 1 an : Poids présumé de 11,0 kg (Santé Canada, 2015) et volume d’air respiré de 8,0 m3 par jour (EPA des États-Unis, 2011).
- 2 à 3 ans : Poids présumé de 15 kg (Santé Canada, 2015) et volume d’air respiré de 9,2 m3 par jour (EPA des États-Unis, 2011).
- 4 à 8 ans : Poids présumé de 23 kg (Santé Canada, 2015) et volume d’air respiré de 11,1 m3 par jour (EPA des États-Unis, 2011).
- 9 à13 ans : Poids présumé de 42 kg (Santé Canada, 2015) et volume d’air respiré de 13,9 m3 par jour (EPA des États-Unis, 2011).
- 14 à 18 ans : Poids présumé de 62 kg (Santé Canada 2015) et respiration de 15,9 m3 d’air par jour (EPA des États-Unis 2011).
- ≥19 ans : Poids présumé de 74 kg (Santé Canada 2015) et respiration de 15,1 m3 d’air par jour (EPA des États-Unis 2011).).
Pour les cancérogènes sans seuil agissant par un mode d’action mutagène, il est recommandé d’appliquer des facteurs d’ajustement en fonction de l’âge (FAFA) au facteur de pente du cancer avec une exposition moyenne à vie afin de tenir compte de la sensibilité de la période d’exposition spécifique à l’âge (Santé Canada 2013). Par conséquent, les FAFA (EPA des États-Unis, 2005) ont été ajustés aux groupes d’âge de Santé Canada (voir le tableau B-1) et appliqués.
| Étape de vie | Age (ans) | FAFA |
|---|---|---|
| Nourrisson | 0 à 5 mois | 10 |
| Nourrisson | 6 à 11 mois | 10 |
| Tout-petit | 1 | 10 |
| Tout-petit | 2 à 3 | 3 |
| Enfant | 4 à 8 | 3 |
| Pré-adolescent | 9 à 13 | 3 |
| Adolescent | 14 à 18 | 1,8a |
| Adulte | 19 et plus | 1 |
a FAFA14–18 = (FAFA14–15 x D14-15/D14-18)+(FAFA16-18 x D16-18/D14-18) = 1,8, où Di = Durée d’exposition (années) [FAFA14–18 = (3 x 2/5) + (1x3/5) = 1,8]
Bromoéthane:
| Voie d’exposition | 0 à 5 mois | 6 à 11 mois | 1 an | 2 à 3ans | 4 à 8 ans | 9 à 13 ans | 14 à 18 ans | 19 ans et plus |
|---|---|---|---|---|---|---|---|---|
| Air ambianta | 5,43E-03 | 5,49E-03 | 6,73E-03 | 5,67E-03 | 4,46E-03 | 3,06E-03 | 2,37E-03 | 1,89E-03 |
| Air intérieura | 3,80E-02 | 3,84E-02 | 4,71E-02 | 3,97E-02 | 3,12E-02 | 2,14E-02 | 1,66E-02 | 1,32E-02 |
| Absorption totale | 4,35E-02 | 4,39E-02 | 5,38E-02 | 4,54E-02 | 3,57E-02 | 2,45E-02 | 1,90E-02 | 1,51E-02 |
a Estimation de l’exposition quotidienne à 0,074 µg/m3 en utilisant la DL la plus élevée des données de surveillance de l’air au Canada (c.-à-d. le programme du RNSPA sept études canadiennes sur l’air menées à Windsor, Regina, Halifax, Edmonton, Montréal, Sault-Ste-Marie et Ottawa (Santé Canada 2010a, 2010 b, 2010c, 2012, 2013, [communication personnelle de Tim Shin et Ron Garson, BQEA, Santé Canada, 27 mai 2021; source non citée, les détails de la conception de l’étude ont été présentés ailleurs (Dales et coll. 2013, Mallach et coll. 2017 )]). L’hypothèse sous-tend que les Canadiens passent 3 heures par jour à l’extérieur (Santé Canada 1998).
Les estimations de la dose journalière provenant de l’air, présentées dans le tableau B-2, ont été utilisées pour calculer la dose journalière moyenne à vie (DJMV) pour la population générale.
DJMV provenant de l’air:
DJMV : (4,35E-02x0,5/80) + (4,39E-02x0,5/80) + (5,38E-02x1/80) + (4,54E-02x2/80) + (3,57E-02x5/80) + (2,45E-02x5/80) + (1,90E-02x5/80) + (1,51E-02x61/80)
=1,88E-02 µg/kg p.c./jour or 1,88E-05 mg/kg p.c./jour
Les FAFA du tableau B-1 ont ensuite été utilisés dans le calcul du risque de cancer pour chaque groupe d’âge et utilisés pour calculer le risque de cancer au cours de la vie (voir le tableau B-3).
| Groupe d’âge | Risque de cancer selon l’âgea |
|---|---|
| 0 à 5 mois | 1,98E-08 |
| 6 à 11 mois | 2,00E-08 |
| 1 an | 4,91E-08 |
| 2 à 3 ans | 2,48E-08 |
| 4 à 8 ans | 4,89E-08 |
| 9 à 13 ans | 3,35E-08 |
| 14 à 18 ans | 1,51E-07 |
| 19 ans et plus | 8,41E-08 |
| Risque de cancer au cours de la vieb = | 4,3E-07 |
a Risque de cancer selon l’âge = [facteur de pente du cancer (mg/kg p.c./jour)-1 x FAFA x estimation de l’exposition (mg/kg p.c./jour) x durée moyennegroupe d’âge] ; exemple pour les nourrissons âgés de 0 à 5 mois = 0,0073 (mg/kg p.c./jour)-1 x 10 x (4,35E-5 mg/kg p.c./jour x 0,5/80)/1000 = 1,98E-08
b Risque de cancer au cours de la vie = somme de tous les calculs de risque par âge
Chloroéthane:
| Voie d’exposition | 0 à 5 mois | 6 à 11 mois | 1 an | 2 à 3ans | 4 à 8 ans | 9 à 13 ans | 14 à 18 ans | 19 + ans |
|---|---|---|---|---|---|---|---|---|
| Air ambianta | 2,70E-02 | 2,73E-02 | 3,35E-02 | 2,82E-02 | 2,22E-02 | 1,52E-02 | 1,18E-02 | 9,39E-03 |
| Air intérieurb | 1,20E-01 | 1,21E-01 | 1,48E-01 | 1,25E-01 | 9,84E-02 | 6,75E-02 | 5,23E-02 | 4,16E-02 |
| Absorption totale | 1,47E-01 | 1,48E-01 | 1,82E-01 | 1,53E-01 | 1,21E-01 | 8,27E-02 | 6,41E-02 | 5,10E-02 |
a Exposition quotidienne estimée à 0,368 µg/m3 lorsqu’on utilise la concentration la plus élevée du 95e percentile mesurée dans l’air ambiant au Canada (c.-à-d. le programme du RNSPA). L’hypothèse sous-tend que les Canadiens passent 3 heures par jour à l’extérieur (Santé Canada 1998).
b Exposition quotidienne estimée à 0,233 µg/m3 en utilisant la concentration la plus élevée du 95e percentile mesurée dans l’air intérieur au Canada (Santé Canada 2010a, 2010 b, 2010c, 2012, 2013, [communication personnelle de Tim Shin et Ron Garson, BQEA, Santé Canada, 27 mai 2021; source non citée, les détails de la conception de l’étude ont été présentés ailleurs (Dales et coll. 2013, Mallach et coll. 2017 et Weichenthal et coll. 2012 )]).
Les estimations de l’absorption quotidienne à partir de l’air, présentées au tableau B-4, ont été utilisées pour calculer la dose quotidienne moyenne pour la durée de vie de la population générale.
DJMV provenant de l’air:
DJMV : 1,47E-01x0,5/80) + (1,48E-01x0,5/80) + (1,82E-01x1/80) + (1,53E-01x2/80) + (1,21E-01x5/80) + (8,27E-02x5/80) + (6,41E-02x5/80) + (5,10E-02x61/80)
= 6,35E-02 µg/kg p.c./jour ou 6,35E-05 mg/kg p.c./jour
Les FAFA du tableau B-1 ont ensuite été utilisés dans le calcul du risque de cancer pour chaque groupe d’âge et utilisés pour calculer le risque de cancer au cours de la vie (voir le tableau B-5).
| Groupe d’âge | Risque de cancer selon l’âgea |
|---|---|
| 0 à 5 mois | 2,29E-08 |
| 6 à 11 mois | 2,32E-08 |
| 1 an | 5,68E-08 |
| 2 à 3 ans | 2,87E-08 |
| 4 à 8 ans | 5,65E-08 |
| 9 à 13 ans | 3,88E-08 |
| 14 à 18 ans | 1,75E-07 |
| 19 ans et plus | 9,72E-08 |
| Risque de cancer au cours de la vieb = | 5,0E-07 |
a Risque de cancer selon l’âge = [facteur de pente du cancer (mg/kg p.c./jour)-1 x FAFA x estimation de l’exposition (mg/kg p.c./jour) x durée moyennegroupe d’âge] ; exemple pour les nourrissons âgés de 0 à 5 mois = 0,0025 (mg/kg p.c./jour)-1 x 10 x (1,47E-04 mg/kg p.c./jour x 0,5/80)/1000 = 2,29E-08
b Risque de cancer au cours de la vie = somme de tous les calculs de risque par âge
1-bromopropane :
| Voie d’exposition | 0 à 5 mois | 6 à 11 mois | 1 an | 2 à 3 ans | 4 à 8 ans | 9 à 13 ans | 14 à 18 ans | 19 + ans |
|---|---|---|---|---|---|---|---|---|
| Air intérieura | 1,59 | 1,61 | 1,97 | 1,66 | 1,31 | 8,98 | 0,696 | 0,553 |
a Exposition quotidienne estimée à 3,1 µg/m3 en utilisant la concentration maximale mesurée dans les foyers canadiens (Li et coll. 2019).
Les estimations de l’absorption quotidienne dans l’air présentées au tableau B-6 ont été utilisées pour calculer la dose quotidienne moyenne pour la durée de vie pour la population générale.
DJMV provenant de l’air:
DJMV: (1,59x0,5/80) + (1,61x0,5/80) + (1,97x1/80) + (1,66x2/80) + (1,31x5/80) + (0,898x5/80) + (0,696x5/80) + (0,553x61/80)
=0,690 µg/kg p.c./jour
Les FAFA du tableau B-1 ont ensuite été utilisés dans le calcul du risque de cancer pour chaque groupe d’âge et utilisés pour calculer le risque de cancer au cours de la vie (voir le tableau B-3).
| Groupe d’âge | Risque de cancer selon l’âgea |
|---|---|
| 0 à 5 mois | 1,70E-07 |
| 6 à 11 mois | 1,70E-07 |
| 1 an | 3,39E-07 |
| 2 à 3 ans | 2,03E-07 |
| 4 à 8 ans | 5,09E-07 |
| 9 à 13 ans | 5,09E-07 |
| 14 à 18 ans | 3,05E-07 |
| 19 ans et plus | 2,07E-06 |
| Risque de cancer au cours de la vieb = | 4,3E-06 |
a Risque de cancer selon l’âge = [facteur de pente du cancer (mg/kg p.c./jour)-1 x FAFA x estimation de l’exposition (mg/kg p.c./jour) x dure moyenne groupe d’âge], où le facteur de pente du cancer selon l’âge (µg/kg p.c./jour)-1 = risque unitaire d’exposition par inhalation (µg/m3)-1 x poids corporel (kg) / taux d’inhalation (m3/day). (Exemple pour les nourrissons de 0 à 5 mois : Facteur de pente du cancer spécifique à l’âge = 1 x 10-6 (µg/m3)-1 x 6,3 kg / 3,7 m3/jour = 1.7 x 10-6 (µg/kg p.c./jour)-1, et risque de cancer selon l’âge = 1,7 x 10-6 (µg/kg p.c./jour)-1 x 10 x (1,7x 10-6 µg/kg p.c./jour x 0,5/80) = 1,7x 10-7)
b Risque de cancer au cours de la vie = somme de tous les calculs de risque par âge
Annexe C. Estimation des expositions humaines par inhalation et par voie cutanée dues aux produits disponibles pour les consommateurs - Scénarios Sentinelles
Les hypothèses utilisées dans les scénarios pour estimer l’exposition aux substances du groupe des halogénures d’alkyle provenant de produits potentiellement disponibles pour les consommateurs au Canada sont résumées dans les tableaux C-1. Ces produits ne devraient pas être utilisés par des enfants. Ainsi, les expositions ont été estimées en fonction du poids présumé (74 kg) d’un adulte (Santé Canada 2015), du taux d’inhalation d’un adulte (15,1 m3/jour) (EPA des États-Unis 2011) et des habitudes d’utilisation d’un adulte. Les expositions ont été estimées à l’aide de ConsExpo Web version 1.0.5 (ConsExpo Web 2018). Les paramètres par défaut de la version ConsExpo Web ont été utilisés, sauf indication contraire.
| Scénario | Substance | Hypothèses |
|---|---|---|
| Starting fluid (engine starting aid) (spray) | Chloroéthane |
Concentration maximale : 1% (FS 2017a) Fréquence : 8 fois par an (jugement professionnel) Par inhalation : exposition à l’aérosol, émission instantanée. Masse émise : 14,4 g (jugement professionnel) Durée de l’exposition : 1 min (jugement professionnel) Volume de la pièce : 34 m3 (garage) Taux de ventilation : 1,5/heure (garage) Taux d’inhalation chez l’adulte : 15,1 m3/jour (EPA des États-Unis 2011) Par voie cutanée : Contact direct, taux constant Surface exposée : 2 190 cm2 (adulte, somme de la surface des mains et des avant-bras, Santé Canada 2018b). Taux de contact : 100 mg/min (pour les bombes aérosols, RIVM 2018) Durée d’émission : 12 secondes (sur la base d’une masse libérée de 14,4 g et d’un taux de génération de masse de 1,2 g/sec pour les bombes aérosols (RIVM 2018) |
| Aérosols de démoulage en silicone | 1-bromopropane |
Concentration maximale : 30% (FS 2016a) Fréquence : 12 fois par an (jugement professionnel) Par inhalation - Exposition à la vapeur, émission instantanée Masse émise : 192 g (EPA des États-Unis 1987 dans EPA des États-Unis 2020) Durée d’exposition : 30 minutes (EPA des États-Unis 1987 dans EPA des États-Unis 2020) Volume de la pièce : 20 m³ (pièce non spécifiée dans RIVM 2014 ; s’aligne sur la sélection de la pièce utilitaire (20 m³) dans EPA des États-Unis 2020) Taux de ventilation : 0,6 par heure (pour une pièce non spécifiée, RIVM 2014) Taux d’inhalation chez l’adulte : 15,1 m³/jour (EPA des États-Unis 2011) Exposition cutanée : Contact direct, taux constant Surface exposée : 2 190 cm2 (adulte, somme de la surface des mains et des avant-bras, Santé Canada 2018b). Taux de contact : 100 mg/min (pour les bombes aérosols, RIVM 2018) Durée d’émission : 160 secondes (sur la base d’une masse émise de 192 g et d’un taux de génération de masse de 1,2 g/sec pour les bombes aérosols (RIVM 2018)). Fraction absorbée : 0,29 % (EPA des États-Unis 2020) |
| Produits de chasse d’air pour la climatisation automobile (fluides) | 1-bromopropane |
Concentration maximale : 100% (FS 2017c)
Fréquence : 1 fois par an (jugement professionnel) Inhalation : exposition à la vapeur, évaporation - émission constante Quantité de produit : 573 g (EPA des États-Unis 2020) Durée d’exposition : 30 minutes (EPA des États-Unis 1987 dans EPA des États-Unis 2020) Volume de la pièce : 34 m³ (garage dans RIVM 2014) Taux de ventilation : 1,5 par heure (pour le garage, RIVM 2014) Taux d’inhalation chez l’adulte : 15,1 m³/jour (EPA des États-Unis 2011) Température d’utilisation : 20 °C (EPA des États-Unis 2019) Pression de vapeur : 110.8 mmHg (Boublik et coll. 1984 dans EPA des États-Unis 2020) Coefficient de transfert de masse : 3,47 m/hr (EPA des États-Unis 2020) Surface d’émission : 730 cm² (EPA des États-Unis 2020) Durée d’émission : 30 minutes (durée de l’activité de chargement/chasse d’aire du fluide; EPA des États-Unis 1987 dans EPA des États-Unis 2020) Exposition cutanée : Contact direct, utilisation instantanée Surface exposée : 2190 cm² (adulte, somme de la surface des mains et des avant-bras, Santé Canada 2018b) Quantité de produit : 0,0121 g (basé sur la valeur par défaut de ConsExpo de 0,01 ml, multiplié par la densité du produit de 1,21 g/cm3; RIVM 2018) Fraction absorbée : 0,29% |
| Nettoyant pour contacts pour appareils électroniques (aérosol) | 1-bromopropane |
Concentration maximale : 44,4 % (FS 2017 b) Fréquence : 2 fois par an (jugement professionnel) Inhalation: exposition à la vapeur – émission instantanée Masse émise : 293 g (EPA des États-Unis 1987 dans EPA des États-Unis 2020) Durée d’exposition : 30 minutes (EPA des États-Unis 1987 dans EPA des États-Unis 2020) Volume de la pièce : 58 m³ (salle de séjour dans RIVM 2014; s’aligne sur la sélection de la salle de séjour dans EPA des États-Unis 2020) Taux de ventilation : 0,5 par heure (pour une salle de séjour, RIVM 2014) Taux d’inhalation chez l’adulte : 15,1 m³/jour (EPA 2011) Température d’utilisation : 20 °C (EPA des États-Unis 2020) Pression de vapeur : 110,8 mmHg (Boublik et coll. 1984 dans EPA des États-Unis 2020) Exposition cutanée : Contact direct, taux constant Surface exposée : 2 190 cm2 (adulte, somme de la surface des mains et des avant-bras, Santé Canada 2018b) Taux de contact : 100 mg/min (pour les bombes aérosols, RIVM 2018) Durée d’émission : 244 secondes (sur la base d’une masse émise de 293 g et d’un taux de génération de masse de 1,2 g/sec pour les aérosols (RIVM 2018) Fraction absorbée : 0,29 % (EPA des États-Unis 2020) |
| Détachant en poudre pour textile (aérosol) | Trans-dichloroéthylène |
Concentration maximale : 60% (FS 2017d) Fréquence : 12 fois par an (jugement professionnel) Inhalation : exposition à l’aérosol, émission instantanée. Masse émise : 23 g (avis professionnel) Durée d’exposition : 1 heure (avis professionnel) Volume de la pièce : 20 m3 (pièce non spécifiée) Taux de ventilation : 0.6/h (pièce non spécifiée) Taux d’inhalation chez l’adulte : 15.1 m3/jour (EPA des États-Unis 2011) Exposition cutanée : Contact direct, taux constant Surface exposée : 2190 cm2 (adulte, somme de la surface des mains et des avant-bras, Santé Canada 2018b) Taux de contact : 100 mg/min (bombes aérosols, RIVM 2018) Durée d’émission : 19,2 seconds (19,2 secondes (sur la base d’une masse émise de 23 g et d’un taux de génération de masse de 1,2 g/sec pour les bombes aérosols [RIVM 2018]) |
Annexe D. Estimation de la dose quotidienne due à l’exposition par inhalation au trans-dichloroéthylène dans l’air
| Groupe | 0 à 5 mois | 6 à 11 mois | 1 an | 2 à 3 ans | 4 à 8 ans | 9 à 13 ans | 14 à 18 ans | 19 ans et plus |
|---|---|---|---|---|---|---|---|---|
| Concentration dans l’air (95e percentile) (0,314 µg/m3) | 0,18 | 0,19 | 0,23 | 0,19 | 0,15 | 0,10 | 0,08 | 0,06 |
a La concentration la plus élevée du 95e percentile mesurée dans l’air au Canada a été convertie en doses quotidiennes estimées pour chaque sous-groupe de la population à l’aide de l’équation suivante : Dose interne (µg/kg p.c./jour) = concentration (µg/m3) × absorption par inhalation à 100 % × taux d’inhalation (TI) (m3/jour) ÷ poids corporel (p.c.) (kg), où les facteurs d’exposition pour le groupe d’âge étaient les suivants : 0 à 5 mois : p.c. = 6,3 kg, TI = 3,7 m3/jour ; 6 à 11 mois : p.c. = 9,1 kg, TI = 5,4 m3/jour ; 1 an : p.c. = 11 kg ; TI = 8,0 m3/jour ; 2 à 3 ans : p.c. = 15 kg, TI = 9,2 m3/jour ; 4 à 8 ans : p.c. = 23 kg, TI = 11,1 m3/jour ; 9 à 13 ans : p.c. = 42 kg, TI = 13,9 m3/jour ; 14 à 18 ans : Poids = 62 kg, RI = 15,9 m3/jour ; 19 ans et plus : Poids = 74 kg, RI = 15,1 m3/jour (Santé Canada 2015, EPA des États-Unis 2011)
