Évaluation préalable - Groupe des triarylméthanes
Title officiel : Évaluation préalable - Groupe des triarylméthanes
Numéros d’enregistrement du Chemical Abstracts Service
548-62-9, 569-64-2, 1324-76-1, 2390-59-2, 2390-60-5, 3844-45-9
Environnement et Changement climatique Canada
Santé Canada
No de cat. : En14-423/2020F-PDF
ISBN 978-0-660-35888-8
Octobre 2020
Sommaire
En vertu de l’article 68 ou 74 de la Loi canadienne sur la protection de l’environnement 1999 (LCPE), la ministre de l’Environnement et la ministre de la Santé ont réalisé une évaluation préalable des six substances appelées collectivement « groupe des triarylméthanes » dans le Plan de gestion des produits chimiques. L’évaluation de ces six substances a été jugée prioritaire, car elles satisfont aux critères de catégorisation du paragraphe 73(1) de la LCPE ou ont été déclarées d’intérêt prioritaire en raison d’autres préoccupations. Une septième substance avait été, initialement, incluse dans le groupe. Toutefois, d’autres approches ont permis de déterminer qu’elle est peu préoccupante, et la conclusion pour cette substance est présentée dans un rapport distinctNote de bas de page 1 . Par conséquent, la présente évaluation préalable porte sur les six substances énumérées dans le tableau ci‑dessous. Les six substances visées par la présente évaluation préalable sont dénommées collectivement sous le nom « groupe des triarylméthanes ».
| N° CASa | Nom dans la Liste intérieure des substances | Nom commun |
|---|---|---|
| 548-62-9b | Chlorure de [4-[4,4’-bis(diméthylamino)benzhydrylidène]cyclohexa-2,5-dién-1-ylidène]diméthylammonium | Basic Violet 3 |
| 569-64-2 | Chlorure de [4-[α-[4-(diméthylamino)phényl]benzylidène]cyclohexa-2,5-dién-1-ylidène]diméthylammonium | Malachite Green |
| 1324-76-1b | Acide [(4-{(4-anilinophényl)[4-(phénylimino)cyclohexa-2,5-dién-1-ylidène]méthyl}phényl)amino]benzènesulfonique | Pigment Blue 61 |
| 2390-59-2 | Chlorure de (4-{bis[4-(diéthylamino)phényl]méthylène}cyclohexa-2,5-dién-1-ylidène)diéthylammonium | Basic Violet 4 |
| 2390-60-5 | Chlorure de (4-{4-(diéthylamino)-α-[4-(éthylamino)-1-naphtyl]benzylidène}cyclohexa-2,5-dién-1-ylidène)diéthylammonium | Basic Blue 7 |
| 3844-45-9b | Dihydrogéno(éthyl)(4-{4-[éthyl(3-sulfonatobenzyl)]amino]-2’-sulfonatobenzhydrylidène}cyclohexa-2,5-dién-1-ylidène)(3-sulfonatobenzyl)ammonium, sel de disodium | Brilliant Blue FCF |
a Le numéro d’enregistrement du Chemical Abstracts Service (n° CAS) est la propriété de l’American Chemical Society et toute utilisation ou redistribution, sauf quand cela est requis pour des exigences réglementaires ou pour des rapports au gouvernement du Canada quand l’information et les rapports sont requis en vertu d’une loi ou d’une politique administrative, est interdite sans l’autorisation écrite préalable de l’American Chemical Society.
b Cette substance n’a pas été identifiée en vertu du paragraphe 73(1) de la LCPE, mais est visée par la présente évaluation, car elle est considérée d’intérêt prioritaire en raison d’autres inquiétudes pour la santé humaine.
Les triarylméthanes sont principalement utilisés comme colorants et ne sont pas présents naturellement dans l’environnement. Ils sont employés comme colorants ou pigments dans les encres, les encres en poudre et les colorants, dans les produits en papier et les articles manufacturés, et ils peuvent également être utilisés dans les matériaux d’emballage alimentaire, pour usage commercial et de consommation. Les substances de ce groupe sont également utilisées dans d’autres produits disponibles aux consommateurs, y compris les cosmétiques (p. ex., crème pour le corps, produits capillaires, colorants capillaires, maquillage, parfum), les produits de nettoyage et les produits de traitement pour l’eau d’aquarium, ainsi que dans d’autres produits industriels et de laboratoire. Le Brilliant Blue FCF est également utilisé dans les aliments, les produits de santé naturels, les produits antiparasitaires, les médicaments d’ordonnance et en vente libre, ainsi que dans une gamme d’autres produits disponibles aux consommateurs. Selon les renseignements présentés pour l’année de déclaration 2008 ou 2011, les six substances ont été importées au Canada en quantités variant de 1 000 à 100 000 kg chacune, et le Brilliant Blue FCF a été fabriqué au Canada en quantités variant de 100 à 1 000 kg.
Les substances du groupe des triarylméthanes peuvent être rejetées dans l’environnement canadien par leur utilisation au Canada dans la teinture et le désencrage du papier, ainsi que par la formulation, la fabrication et l’utilisation par les consommateurs des produits contenant ces substances. On s’attend à des rejets dans le milieu aquatique provenant de sources diffuses et ponctuelles. Ces substances peuvent également être rejetées dans les milieux terrestres. Si le Pigment Blue 61 est rejeté dans le milieu aquatique, il est susceptible de se comporter comme une particule et de se déposer dans les sédiments du lit. Les autres triarylméthanes seront chargés à un pH pertinent pour l’environnement et auront tendance à se sorber sur les solides dissous et en suspension. Par conséquent, ces substances peuvent être transportées dans la colonne d’eau ou se déposer dans les sédiments du lit. Les substances du groupe des triarylméthanes ont tendance à persister dans l’eau, les sédiments et le sol. Elles ont un faible potentiel de bioaccumulation dans les lipides des organismes aquatiques. Cependant, les colorants non sulfonés (c.‑à‑d. le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7) peuvent plutôt se lier aux protéines et s’accumuler dans d’autres types de tissu des poissons.
Les données expérimentales sur la toxicité aiguë des colorants non sulfonés montrent qu’ils peuvent avoir des effets nocifs sur les organismes aquatiques à de faibles concentrations. Des effets nocifs sur les organismes aquatiques ont été observés pour le Brilliant Blue FCF à des concentrations relativement plus élevées, alors qu’aucun effet n’a été observé à la limite de solubilité du Pigment Blue 61. Des scénarios d’exposition de l’environnement ont été élaborés pour le rejet à l’égout des produits utilisés contenant ces substances, et pour les rejets des sites industriels. Des analyses des quotients de risque ont été effectuées pour comparer les concentrations estimées en milieu aquatique aux concentrations entraînant des effets nocifs dans les organismes aquatiques pour différents scénarios d’exposition. Les scénarios pour la teinture et le désencrage du papier ont indiqué que les colorants de triarylméthane non sulfonés présentent un risque pour les organismes aquatiques, alors que les scénarios portant sur la formulation générale des produits, la manutention des produits et l’utilisation par les consommateurs n’en présentent pas. Les scénarios d’exposition au Brilliant Blue FCF n’ont pas indiqué de risque pour les organismes aquatiques, et le Pigment Blue 61 ne devrait pas poser de risque pour les organismes aquatiques, car il devrait se comporter davantage comme une particule et ne sera probablement pas biodisponible.
Compte tenu de tous les éléments de preuve contenus dans la présente évaluation préalable, le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7 présentent un risque d’effets nocifs sur l’environnement. Il est conclu que le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7 satisfont aux critères de l’alinéa 64a) de la LCPE, car ils pénètrent ou peuvent pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique. Toutefois, il est conclu que le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7 ne satisfont pas aux critères de l’alinéa 64b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à mettre en danger l’environnement essentiel pour la vie. Il est également conclu que le Brilliant Blue FCF et le Pigment Blue 61 ne satisfont pas aux critères des alinéas 64a) ou b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
Pour la population générale du Canada, les principales sources d’exposition aux teintures des substances du groupe des triarylméthanes sont attribuables à l’utilisation de produits disponibles aux consommateurs qui contiennent ces substances, et dans les milieux naturels (p. ex., l’eau potable). L’exposition potentielle par voie orale au Basic Violet 3, au Malachite Green, au Basic Violet 4, au Basic Blue 7 et au Brilliant Blue FCF a été estimée en fonction des concentrations potentielles dans l’eau potable. L’exposition potentielle par voie cutanée et par voie orale au Brilliant Blue FCF a été établie d’après l’utilisation des produits de santé naturels et des cosmétiques, et l’exposition par voie orale découlant de son utilisation comme additif alimentaire. L’exposition potentielle au Malachite Green, au Basic Violet 4 et au Basic Blue 7 a été établie d’après l’utilisation de cosmétiques (colorants capillaires). L’exposition potentielle par inhalation au Brilliant Blue FCF, par l’utilisation de parfum, a également été caractérisée. L’exposition par inhalation aux autres substances du groupe des triarylméthanes n’a pas été jugée préoccupante en raison de leur volatilité négligeable et de leurs utilisations potentielles. Étant donné les propriétés physiques et chimiques et les utilisations répertoriées du Pigment Blue 61, on ne s’attend pas à ce que la population générale du Canada y soit exposée.
Dans des études de laboratoire, on n’a pas constaté que le Basic Violet 3 cause une toxicité pour le développement ou la reproduction, mais il est génotoxique et cancérogène. D’après les renseignements sur les effets sur la santé d’une substance structurellement apparentée, l’effet critique du Malachite Green pour la santé est la toxicité pour le développement. Le Pigment Blue 61 n’a pas été considéré comme présentant un risque élevé pour la santé humaine d’après les classifications établies par d’autres organismes nationaux ou internationaux pour ce qui est de la cancérogénicité, de la génotoxicité ou de la toxicité pour le développement ou la reproduction. Le Basic Violet 4 et la substance structurellement apparentée au Basic Blue 7 ne sont pas génotoxiques. D’après les renseignements sur les effets sur la santé des substances structurellement apparentées, le Basic Violet 4 et le Basic Blue 7 ne sont pas jugés toxiques pour le développement ou la reproduction, mais pourraient être cancérogènes. Le Brilliant Blue FCF est mal absorbé par voie orale et cutanée, n’est pas toxique pour le développement ou la reproduction, n’est pas génotoxique et n’est pas cancérogène.
Pour ce qui est du Basic Violet 3, du Basic Violet 4, du Basic Blue 7 et du Brilliant Blue FCF, la comparaison des niveaux d’exposition de la population générale et des niveaux auxquels des effets critiques sur la santé ont été observés donne des marges d’exposition jugées adéquates pour tenir compte des incertitudes dans les bases de données sur l’exposition et sur les effets sur la santé pour ce qui est des effets cancérogènes et non cancérogènes. Par contre, une comparaison similaire de l’exposition liée à l’utilisation du Malachite Green dans les colorants capillaires et les a donné des marges d’exposition qui sont considérées comme potentiellement insuffisantes pour réduire les incertitudes dans les effets sur la santé et les bases de données sur l’exposition, d’autant plus que des effets critiques sur la santé ont été observés à la plus faible dose d’essai.
À la lumière des renseignements contenus dans la présente évaluation préalable, il est conclu que le Malachite Green satisfait au critère du paragraphe 64c) de la LCPE, car il pénètre ou peut pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaines. Il est également conclu que le Basic Violet 3, le Pigment Blue 61, le Basic Violet 4, le Basic Blue 7 et le Brilliant Blue FCF ne satisfont pas au critère de l’alinéa 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaines.
Par conséquent, il est conclu que le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7 satisfont à un ou plusieurs des critères énoncés à l’article 64 de la LCPE. Il est conclu que le Pigment Blue 61 et le Brilliant Blue FCF ne satisfont à aucun des critères énoncés à l’article 64 de la LCPE. Enfin, il est conclu que le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7 répondent aux critères de persistance, mais pas à ceux de bioaccumulation, critères qui sont énoncés dans le Règlement sur la persistance et la bioaccumulation de la LCPE.
1. Introduction
En vertu des articles 68 ou 74 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE] (Canada 1999), la ministre de l’Environnement et la ministre de la Santé ont effectué une évaluation préalable de six des sept substances désignées collectivement comme « groupe des triarylméthanes » dans le cadre du Plan de gestion des produits chimiques, afin de déterminer si ces six substances présentent ou pourraient présenter un risque pour l’environnement ou la santé humaine. Il a été jugé prioritaire d’évaluer ces six substances, car elles satisfont aux critères de catégorisation du paragraphe 73(1) de la LCPE ou ont été déclarées d’intérêt prioritaire en raison d’autres préoccupations liées à la santé humaine (ECCC et SC [modifié en 2017]).
La septième substance, portant le no CASNote de bas de page 2 632-99-5, faisait initialement partie du groupe des triarylméthanes. Toutefois, cette substance a été évaluée dans le Document sur l’approche scientifique : Classification du risque écologique des substances organiques (ECCC 2016), et par l’approche appliquée dans l’Examen préalable rapide des substances avec une exposition limitée pour la population générale (ECCC, SC 2018), et elle a été jugée peu préoccupante tant pour la santé humaine que pour l’environnement. C’est pourquoi le présent rapport n’en fera pas état. Les conclusions pour cette substance sont présentées dans l’Évaluation préalable pour l’examen préalable rapide des substances avec une exposition limitée pour la population générale (ECCC, SC 2018). Les six substances faisant l’objet de la présente évaluation préalable seront ci-après désignées par le nom collectif « groupe des triarylméthanes ».
Bien que tous les triarylméthanes aient des caractéristiques structurales communes et des utilisations fonctionnelles similaires comme pigments ou colorants dans de nombreux secteurs, il existe une variabilité notable au sein de ce groupe en ce qui concerne la structure globale et les propriétés physico-chimiques de ces substances. Pour tenir compte de cette variabilité, chaque substance a été évaluée individuellement.
Certains triarylméthanes faisant actuellement l’objet d’une évaluation ont été examinés au niveau international par le Comité mixte FAO/OMS expert des additifs alimentaires (JECFA), l’Autorité européenne de sécurité des aliments (EFSA), l’Environmental Protection Agency (EPA) des États-Unis, la Commission européenne (CE) et le National Toxicology Program (NTP), en plus des évaluations existantes. Ces évaluations font l’objet d’un examen rigoureux. Santé Canada et Environnement et Changement climatique Canada considèrent que ces évaluations sont fiables.
Pour la présente évaluation préalable, nous avons pris en compte des renseignements sur les propriétés chimiques, le devenir dans l’environnement, les dangers, les utilisations et l’exposition, y compris des renseignements soumis par des parties intéressées. Des données pertinentes ont été obtenues jusqu’en avril 2017. D’autres données ont été présentées par des intervenants jusqu’en juin 2019. Nous avons utilisé des données empiriques tirées d’études clés ainsi que certains résultats de modélisation pour formuler nos conclusions. Quand ils étaient disponibles et pertinents, nous avons tenu compte de renseignements présentés dans des évaluations faites par d’autres autorités compétentes.
Le personnel du Programme d’évaluation des risques de la LCPE de Santé Canada et d’Environnement et Changement climatique Canada a rédigé la présente évaluation préalable qui inclut la contribution d’autres programmes de ces deux ministères. Les parties de la présente évaluation préalable portant sur la santé humaine et l’écologie ont fait l’objet d’examens ou de consultations externes. Des commentaires sur les parties techniques pertinentes pour l’environnement ont été reçus de Mme Isabel Beauchesne, de M. Geoff Granville (GCGranville Consulting Corp.) et de M. Jarai Mon. Des commentaires sur les parties techniques ayant trait à la santé humaine ont été reçus de la part de mesdames Theresa Lopez, Jennifer Flippin et Joan Garey, de Tetra Tech. En outre, l’ébauche de la présente évaluation préalable (publiée le 8 décembre 2018) a été soumise à une consultation publique de 60 jours. Même si les commentaires externes ont été pris en compte, Santé Canada et Environnement et Changement climatique Canada assument l’entière responsabilité du contenu final et des conclusions de la présente évaluation préalable.
La présente évaluation préalable repose sur des renseignements permettant de déterminer si les substances satisfont aux critères énoncés à l’article 64 de la LCPE. Pour ce faire, les renseignements scientifiques ont été étudiés et intégrés à une approche basée sur le poids de la preuve et le principe de précautionNote de bas de page 3. Dans le présent document, nous présentons ces renseignements essentiels et les éléments sur lesquels se fonde la conclusion.
2. Identité des substances
Les numéros CAS, les noms figurant sur la LIS et les noms communs des substances individuelles du groupe des triarylméthanes sont présentés dans le tableau 2‑1.
| N° CAS | Nom dans la LI (nom commun) | Structure chimique et formule moléculaire | Masse moléculaire (g/mol) |
|---|---|---|---|
| 548-62-9 | Chlorure de [4-[4,4’-bis(diméthylamino)benzhydrylidène]cyclohexa-2,5-dién-1-ylidène]diméthylammonium. (Basic violet 3 b) | ![[Cl-].CN(C)c1ccc(C(c2ccc(N(C)C)cc2)=C2C=CC(=[N+](C)C)C=C2)cc1](/content/dam/eccc/images/pded/triarylmethanes/20200818-fig21a.jpg) C25H30N3.Cl C25H30N3.Cl | 407,99 |
| 569-64-2 | Chlorure de [4-[α-[4-(diméthylamino)phényl]benzylidène]cyclohexa-2,5-dién-1-ylidène]diméthylammonium. (Malachite green) | ![[Cl-].CN(C)c1ccc(C(c2ccccc2)=C2C=CC(=[N+](C)C)C=C2)cc1](/content/dam/eccc/images/pded/triarylmethanes/20200818-fig21b.jpg) C23H25N2.Cl C23H25N2.Cl | 364,92 |
| 1324-76-1 | Acide [(4-{(4-anilinophényl)[4-(phénylimino)cyclohexa-2,5-dién-1-ylidène]méthyl}phényl)amino]benzènesulfonique]. (Pigment blue 61) | ![O=S(C(C=C1)=CC=C1NC2=CC=C(/C(C3=CC=C(NC4=CC=CC=C4)C=C3)=C5C=C/C(C=C\5)=N/C6=CC=CC=C6)C=C2)([O-])=O](/content/dam/eccc/images/pded/triarylmethanes/20200818-fig21c.jpg) C37H29N3O3S C37H29N3O3S | 595,72 |
| 2390-59-2 | Chlorure de (4-{bis[4-(diéthylamino)phényl]méthylène}cyclohexa-2,5-dién-1-ylidène)diéthylammonium. (Basic violet 4) | ![[Cl-].CCN(CC)c1ccc(C(c2ccc(N(CC)CC)cc2)=C2C=CC(=[N+](CC)CC)C=C2)cc1](/content/dam/eccc/images/pded/triarylmethanes/20200818-fig21d.jpg) C31H42N3.Cl C31H42N3.Cl | 492,15 |
| 2390-60-5 | Chlorure de (4-{4-(diéthylamino)-α-[4-(éthylamino)-1-naphtyl]benzylidène}cyclohexa-2,5-dién-1-ylidène)diéthylammonium. (Basic blue 7) | ![[Cl-].CCNc1ccc(C(c2ccc(N(CC)CC)cc2)=C2C=CC(=[N+](CC)CC)C=C2)c2ccccc12](/content/dam/eccc/images/pded/triarylmethanes/20200818-fig21e.jpg) C33H40N3.Cl C33H40N3.Cl | 514,15 |
| 3844-45-9 | Dihydrogéno(éthyl)(4-{4-[éthyl(3-sulfonatobenzyl)]amino]-2’-sulfonatobenzhydrylidène}cyclohexa-2,5-dién-1-ylidène)(3-sulfonatobenzyl)ammonium, sel de disodium. (Brilliant blue FCF) | ![[Na+].[Na+].CCN(Cc1cccc(S(=O)(=O)[O-])c1)c1ccc(C(c2ccccc2S(=O)(=O)[O-])=C2C=CC(=[N+](CC)Cc3cccc(S(=O)(=O)[O-])c3)C=C2)cc1](/content/dam/eccc/images/pded/triarylmethanes/20200818-fig21f.jpg) C37H34N2O9S3.Na2 C37H34N2O9S3.Na2 | 792,86 |
a Les numéros correspondants du Colour index (C.I.) (Sigma-Aldrich c2017) : Basic Violet 3 : 42555; Malachite Green : 42000; Basic Violet 4 : 42600; Basic Blue 7 : 42595; Pigment Blue 61 : 42765 :1; Brilliant Blue FCF : 42090.
b Le Basic Violet 3 (no CAS 548-62-9) est communément appelé dans la littérature « violet cristal » ou encore « violet de Paris ». Le terme « Basic Violet 3 » était à l’origine utilisé pour décrire un mélange de colorants de pararosaniline de méthyle (violet de méthyle), mais il est maintenant couramment utilisé pour désigner le composant unique « Basic Violet 3 ». Dans les études de toxicologie examinées dans le présent document, le terme « Basic Violet 3 » désignait des préparations commerciales contenant au moins 96 % de la substance no CAS 548-62-9, le reste étant principalement du violet de méthyle ou de la pentaméthylpararosaniline (Aidoo et coll. 1990).
2.1 Choix des analogues et utilisation de modèles QSAR
Une approche par lecture croisée utilisant des données provenant d’analogues ainsi que les résultats des modèles de relation quantitative structure-activité (QSAR), le cas échéant, a été utilisée pour éclairer les évaluations des effets environnementaux et sur la santé humaine. On a choisi des analogues dont la structure ou la fonction était similaire à celle des substances de ce groupe (propriétés physico-chimiques et toxicocinétique similaires) et pour lesquels on pouvait utiliser des données empiriques pertinentes pour faire des comparaisons avec des substances pour lesquelles les données empiriques étaient limitées. Ainsi, on a déterminé l’applicabilité des modèles QSAR au cas par cas. Les détails des données obtenues par lecture croisée et des modèles QSAR choisis sont examinés plus en détail dans les sections Évaluation des effets environnementaux et Évaluation des effets sur la santé, dans le présent rapport. L’identité des analogues utilisés pour cette évaluation est présentée dans le tableau 2‑2.
| No CAS | Nom commun | Structure chimique et formule moléculaire | Masse moléculaire (g/mol) | Substance(s) cible(s) pour les analogues |
|---|---|---|---|---|
| 6417-46-5 | Pigment blue 56 | 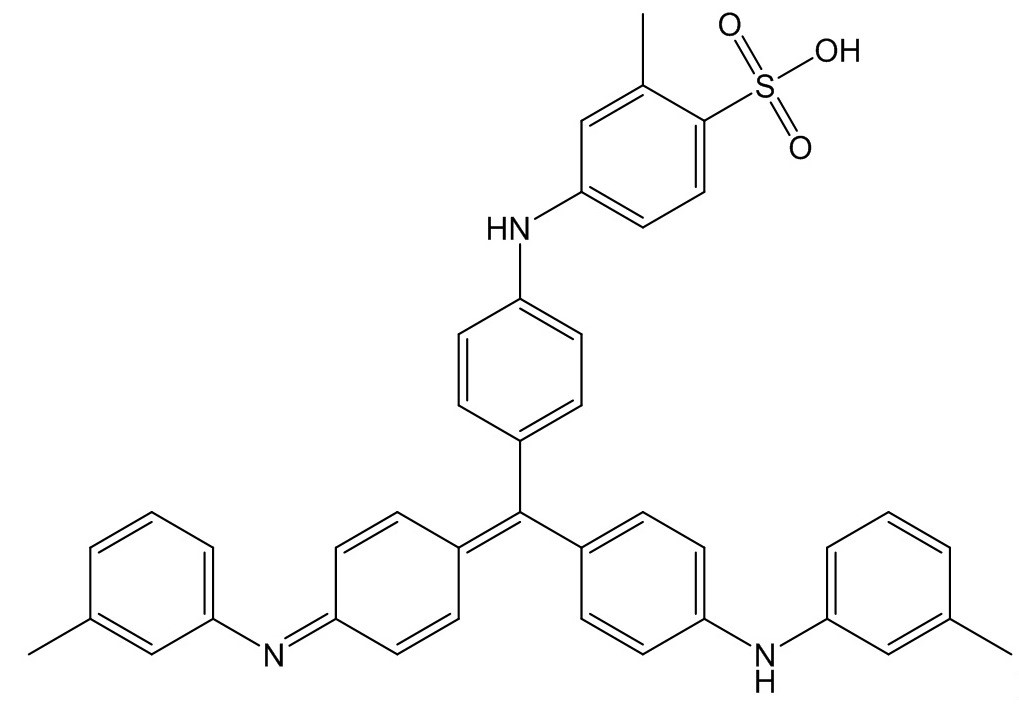 C40H35N3O3S C40H35N3O3S | 637,80 | Pigment blue 61 |
| 2437-29-8 | Oxalate de vert de malachite | /C.O=C(O)C(O)=O.O=C([O-])C([O-])=O.O=C([O-])C([O-])=O.CN(C)C(C=C4)=CC=C4/C(C5=CC=CC=C5)=C6C=C/C(C=C/6)=[N+](C)/C](/content/dam/eccc/images/pded/triarylmethanes/20200818-fig22b.jpg) C46H50N4.C2H2O4.2C2HO4 C46H50N4.C2H2O4.2C2HO4 | 927,02 | Malachite green |
| 63157-72-2 | Acétate de violet d’éthyle | /CC.O=C([O-])C](/content/dam/eccc/images/pded/triarylmethanes/20200818-fig22c.jpg) C31H42N3.C2H3O2 C31H42N3.C2H3O2 | 515,74 | Basic violet 4, Basic Blue 7 |
| 2580-56-5 | Basic blue 26 | /C.[Cl-]](/content/dam/eccc/images/pded/triarylmethanes/20200818-fig22d.jpg) C33H32N3.Cl C33H32N3.Cl | 506,09 | Basic blue 7 |
a D’autres substances dans le groupe des triarylméthanes (p. ex., le Basic Violet 3, le Malachite Green) ont également été utilisées comme analogues. Leur utilisation est indiquée dans les sections pertinentes.
3. Propriétés physiques et chimiques
Un résumé des propriétés physiques et chimiques des triarylméthanes est présenté dans les tableaux 3‑1 et 3‑2.
Lorsque les données expérimentales étaient limitées ou non disponibles, on a utilisé des modèles QSAR pour générer des données sur la pression de vapeur, la constante de la loi d’Henry, le coefficient de partage octanol-eau (Koe), le coefficient de partage carbone organique-eau (Kco) et le coefficient de partage octanol-air (Koa). Bon nombre de ces modèles sont principalement fondés sur des méthodes d’addition de fragment (c.‑à‑d. qu’ils reposent sur la structure du produit chimique) et n’acceptent généralement que la forme neutre (c.‑à‑d. non ionisée) d’un produit chimique comme intrant (sous forme du simplified molecular-input line-entry system ou SMILES). Ainsi, la forme non ionisée a été utilisée comme intrant du modèle au besoin. Lorsque plus d’un modèle approprié ou d’un résultat empirique valide était disponible pour une propriété donnée, la moyenne a été prise comme valeur clé pour ce paramètre. Les valeurs clés choisies pour l’estimation de la pression de vapeur, de la solubilité dans l’eau, de la valeur log Koe, du coefficient de partage air-eau (log Kae) et de la valeur log Koa ont été ajustées par la méthode des moindres carrés (Cole et Mackay 2000; Schenker et coll. 2005) et ces valeurs représentent des propriétés internes cohérentes en matière de partage, compte tenu des contraintes thermodynamiques.
Quatre des colorants évalués – Basic Violet 3, Malachite Green, Basic Violet 4 et Basic Blue 7 – sont des sels chlorés. En tant que sels, ils se dissocient dans l’eau pour produire le groupement de colorant organique cationique correspondant et le contre-ion chlorure. Ces substances sont oxydées en espèces chargées au cours de leur synthèse et devraient conserver cette charge positive dans l’environnement. Les valeurs de pKa n’ont pas été rapportées, car elles ne s’appliquent pas à ces charges permanentes, qui seraient présentes dans toute la plage de pH. En plus de la charge permanente, la spéciation de ces substances dans les fluides biologiques dépendrait également du pH (ACD/Percepta c1997-2015).
Le Brilliant Blue FCF est un sel disodique comportant trois groupes sulfonate dans sa structure. À un pH égal ou supérieur à 4, plus de 95 % des molécules auront un seul groupe amine qui sera chargé positivement et les trois groupes acide sulfonique seront chargés négativement, ce qui donnera une charge négative nette (ACD/Percepta c1997-2015).
Contrairement aux autres triarylméthanes, le Pigment Blue 61 devrait se comporter davantage comme une particule semblable aux autres pigments organiques. Le diamètre médian des particules de cette substance est de 294 µm (ECHA c2007-2017a). Les propriétés physiques et chimiques de pigments de nombreuses classes structurales ne se prêtent souvent pas à des prédictions par modèle, parce qu’elles sont généralement considérées à l’extérieur du domaine d’applicabilité du modèle (p. ex., domaines des paramètres structuraux ou des propriétés). En raison des caractéristiques de leur structure moléculaire, les pigments organiques ont tendance à avoir une très faible solubilité. Par conséquent, il est raisonnable de représenter le coefficient de partage octanol-eau pour les substances peu solubles par le rapport de la solubilité dans l’octanol sur la solubilité dans l’eau (Soct/Seau) (ECHA 2017). Pour le Pigment Blue 61, la valeur log (Soct/Seau) a été estimée à 3,99 sur la base d’une solubilité dans l’octanol de 23,8 mg/L et d’une solubilité dans l’eau de 2,5 µg/L.
| Propriété | Basic violet 3 | Malachite green | Basic violet 4 | Basic blue 7 | Référence(s) |
|---|---|---|---|---|---|
| Solubilité dans l’eau, valeur ajustée (mg/L) | 1,8×104 | 1,3×104 | 6,7×103 | 2,1×104 | ACD/Percepta c1997-2015; Baughman et coll. 1994; Green 1990; SCBT c2007-2017; WATERNT 2010; WSKOWWIN 2010 |
| Solubilité dans l’eau, valeur expérimentale (mg/L) | 4,0×103 | 4,0×104 | 9,0×103 | 2,0×104 | Baughman et coll. 1994; Green 1990; SCBT c2007-2017 |
| Pression de vapeur (Pa) a | 1,8×10-10 | 3,6×10-9 | 3,3×10-11 | 4,0×10-13 | MPBPWIN 2008 |
| Constante de la loi d’Henry (Pa·m3/mol) | 2,0×10-12 | 1,2×10-10 | 1,1×10-11 | 3,9×10-14 | HENRYWIN 2008 |
| Log Kae (sans dimension) | -14,8 | -13,4 | -15,0 | -17,4 | Schenker et coll. 2005 |
| Log Koe, valeur ajustée (sans dimension) | 0,7 | 0,6 | 4,7 | 4,8 | ACD/Percepta, c1997-2015; KOWWIN 2010 |
| Log Koe, valeur expérimentale (sans dimension) | 0,5 | 0,6 | 2,4 | S.O. | ECHA c2007-2017b; Hansch et coll. 1995; Tsai et coll. 1991 |
| Log Kco (sans dimension) | 1,2 | 1,2 | 3,4 | 3,5 | KOCWIN 2010 |
| Log Koa (sans dimension) | 15,5 | 14,0 | 19,7 | 22,3 | KOAWIN 2010 |
Abréviations : N.D. = non disponible.
a Comme les triarylméthanes sont des solides à la température ambiante, les pressions de vapeur du liquide sous-refroidi ont été calculées.
| Propriété | Pigment blue 61 | Brilliant blue FCF | Référence(s) |
|---|---|---|---|
| Solubilité dans l’eau, valeur ajustée (mg/L) | S.O. | 1,8×103 | ECHA c2007-2017a; Green 1990; ACD/Percepta c1997-2015; WATERNT 2010; WSKOWWIN 2010 |
| Solubilité dans l’eau, valeur expérimentale (mg/L) | 2,5×10-3 | 3,0×104 | ECHA c2007-2017a; Green 1990 |
| Solubilité dans l’octanol (mg/L) | 23,8 | S.O. | ECHA, c2007-2017a |
| Pression de vapeur (Pa) a | S.O. | 3,0×10-42 | MPBPWIN 2008 |
| Constante de la loi d’Henry (Pa·m3/mol) | S.O. | 1,4×10-31 | HENRYWIN 2008 |
| Log Kae (sans dimension) | S.O. | -38,4 | Schenker et coll. 2005 |
| Log Koe, valeur ajustée (sans dimension) | S.O. | 0,3 | ACD/Percepta c1997-2015; KOWWIN 2010 |
| Log Koe (sans dimension) | 3,99 b | 0,02 | ACD/Percepta c1997-2015; ECHA c2007-2017a; KOWWIN 2010 |
| Log Kco (sans dimension) | < 1,3–4,9 | 0,3 | ECHA c2007-2017a; KOCWIN 2010 |
| Log Koa (sans dimension) | S.O. | 37,3 | KOAWIN 2010 |
Abréviations : S.O. = sans objet, N.D. = non disponible.
a Comme les triarylméthanes sont des solides à la température ambiante, les pressions de vapeur du liquide sous-refroidi ont été calculées.
b Pour estimer la valeur log Koe pour les pigments, on calcule le rapport de la solubilité empirique dans l’octanol sur la solubilité empirique dans l’eau.
4. Sources et utilisations
Aucun des triarylméthanes n’est présent à l’état naturel. Ces substances ont été incluses dans les enquêtes menées en vertu de l’article 71 de la LCPE pour les années de déclaration 2008 (Basic Violet 3, Malachite Green) ou 2011 (Pigment Blue 61, Basic Violet 4, Basic Blue 7, Brilliant Blue FCF) (Canada 2009, 2012). La fabrication du Brilliant Blue FCF au Canada a été déclarée en une quantité comprise entre 100 et 1 000 kg au cours de l’année civile 2011 (Environnement Canada 2013). Conformément aux enquêtes menées en vertu de l’article 71, pour l’année de déclaration 2008 ou 2011, les six substances ont été importées au Canada en quantités comprises entre 1 000 et 100 000 kg chacune (Environnement Canada 2009, 2013).
Au Canada et dans le monde, les six triarylméthanes sont principalement utilisés comme colorants, dans un large éventail d’applications potentielles. Les tableaux 4‑1 et 4‑2 présentent un résumé des utilisations de ces substances au Canada.
| Principales utilisations a | VG | VM | PB61 | VE | BB7 | BBFCF |
|---|---|---|---|---|---|---|
| Substances utilisées à des fins agricoles(autres que pesticides) | N | N | N | N | N | O |
| Matériel d’artisanat et de loisir (y compris les usages pour enfants) | N | N | N | N | N | O |
| Nettoyage et entretien des meubles | N | N | N | N | N | O |
| Aliments et boissons | N | N | N | N | N | O |
| Encre, encre en poudre et colorants | N | O | O | N | N | O |
| Détergents à lessive et à vaisselle | N | N | N | N | N | O |
| Entretien des pelouses et des jardins | N | N | N | N | N | O |
| Instruments médicaux | O b | N | N | N | N | N |
| Peintures et revêtements | N | N | N c | N | N c | O |
| Produits, mélanges ou articles manufacturés en papier | O | O | N | O | N | N |
| Produits de soins personnels | N | N | N | N | N | O |
Abréviations : VG = Basic Violet 3, VM = Malachite Green, PB61 = Pigment Blue 61, VE = Basic Violet 4, BB7 = Basic Blue 7, BBFCF = Brilliant Blue FCF, O = oui (cette utilisation a été déclarée pour cette substance), N = non (cette utilisation n’a pas été déclarée pour cette substance).
a Renseignements non confidentiels sur les utilisations déclarées dans le cadre des enquêtes menées en vertu de l’article 71 de la LCPE (Environnement Canada, 2009, 2013). Voir les enquêtes pour les inclusions ou les exclusions particulières (annexes 2 et 3).
b Utilisation déclarée comme substance de laboratoire destinée à être utilisée dans des dispositifs médicaux.
c Bien que cette substance n’ait pas été déclarée lors des enquêtes menées en vertu de l’article 71, on sait que cette substance est utilisée au Canada dans les peintures et les revêtements, mais à des volumes inférieurs au seuil de déclaration pour les enquêtes menées en vertu de l’article 71 de la LCPE, soit 100 kg/an (communication personnelle, courriels de l’Association canadienne de l’industrie de la peinture et du revêtement à Environnement et Changement climatique Canada, 2016-2017; sans référence).
| Utilisation | VG | VM | PB61 | VE | BB7 | BBFCF |
|---|---|---|---|---|---|---|
| Matériel d’artisanat et de loisir (y compris les usages pour enfants) | N | N a | N | N | N | N |
| Additif alimentaire b | N | N | N | N | N | O c |
| Matériau d’emballage alimentaire b, d | O | N | O | N | N | O |
| Additifs indirects b | N | N | N | N | N | O e |
| Produits de formulation dans des produits antiparasitaires homologués au Canada f | N | N | N | N | N | O g |
| Base de données interne sur les produits pharmaceutiques, présents comme ingrédients médicinaux ou non médicinaux dans les désinfectants ou dans des médicaments destinés aux humains ou aux animaux au Canada h | N i | N | N | N | N | O j |
| Base de données d’ingrédients de produits de santé naturels k | O l | N | N | N | N | O m |
| Base de données des produits de santé naturels homologués présents comme ingrédients médicinaux ou non médicinaux dans des produits de santé naturels au Canada k | N | N | N | N | N | O n |
| Dispositifs médicaux homologués au Canadao | Op | N | N | N | N | N |
| Présence signalée dans les cosmétiques selon les déclarations faites à Santé Canada en vertu du Règlement sur les cosmétiques q | N | O r | N | O r | O s | O t |
| Encres (y compris les encres d’impression) u | O | O | O | O | O | O |
| Produit de traitement de l’eau d’aquarium | N | O v | N | N | N | N |
Abréviations : VG = Basic Violet 3, VM = Malachite Green, PB61 = Pigment Blue 61, VE = Basic Violet 4, BB7 = Basic Blue 7, BBFCF = Brilliant Blue FCF, O = oui (cette utilisation a été déclarée pour cette substance) et N = non (cette utilisation n’a pas été déclarée pour cette substance).
a Anciennement présent dans des marqueurs artisanaux, d’après l’information accessible au public, mais il a été confirmé, depuis, que le produit n’est plus offert au Canada; MSDS 2014.
b Communication personnelle, courriels de la Direction des aliments, Santé Canada, au Bureau d’évaluation du risque des substances existantes, Santé Canada, 2016-2017; 2019; sans référence.
c Santé Canada [modifié, 2015a].
d Utilisation possible dans les matériaux d’emballage alimentaire.
e Répertorié comme composant possible des additifs indirects (p. ex., nettoyants et détergents à vaisselle) utilisés dans les usines de transformation des aliments.
f Communication personnelle, courriel de l’Agence de réglementation de la lutte antiparasitaire de Santé Canada au Bureau d’évaluation du risque des substances existantes de Santé Canada, 17 mars 2017, sans référence.
g ARLA 2010.
h Communication personnelle, courriel de la Direction des produits thérapeutiques de Santé Canada au Bureau d’évaluation du risque des substances existantes de Santé Canada, 2016, sans référence.
i Auparavant déclaré comme ingrédient médicinal (c.‑à‑d. principe actif [p.a.]); DPD [modifié, 2015], mais les identifications numériques de drogues (DIN) ont été révoqués et tous les produits qui étaient sur le marché au Canada ont été rappelés (Santé Canada 2019).
j Déclaré comme ingrédient non médicinal (INM) dans une vaste gamme de médicaments d’ordonnance et en vente libre, y compris les médicaments contre les allergies et les rhumes; Canada 1978.
k Communication personnelle de la Direction des produits de santé naturels et sans ordonnance de Santé Canada au Bureau d’évaluation du risque des substances existantes de Santé Canada, 2017-2017, sans référence.
l Déclaré dans la Base de données d’ingrédients de produits de santé naturels (BDIPSN) avec un rôle non lié aux produits de santé naturels, car il ne s’agit pas d’une substance naturelle figurant à l’annexe 1 du Règlement sur les produits de santé naturels (BDIPSN [modifié, 2017]).
m Déclaré dans la BDIPSN avec un rôle non médicinal en tant qu’additif colorant dans les produits de santé naturels (BDIPSN [modifié, 2017]). Également associé à une dose journalière admissible allant jusqu’à 6 mg/kg p.c./j, d’après le JECFA (2017).
n Déclaré dans la Base de données des produits de santé naturels homologués (BDPSNH) comme ingrédient non médicinal dans une variété de produits de santé naturels actuellement homologués, y compris les suppléments d’entraînement, les suppléments multivitaminés/minéraux, les produits de traitement de l’acné et les dentifrices (BDPSNH [modifié, 2016]).
o Communication personnelle, courriel envoyés par le Bureau des matériels médicaux de Santé Canada, au Bureau d’évaluation du risque des substances existantes de Santé Canada, 2019, sans référence.
p Déclaré dans certains pansements stériles homologués faits de mousse de polyuréthane (Santé Canada 2019)
q Communication personnelle, courriels envoyés par la Direction de la Sécurité des produits de consommation de Santé Canada, au Bureau d’évaluation du risque des substances existantes de Santé Canada, 2016-2017, sans référence.
r Utilisation déclarée dans les colorants capillaires semi-permanents
s Utilisation déclarée dans les colorants capillaires semi-permanents et les revitalisants capillaires.
t Utilisation déclarée dans une grande variété de cosmétiques, y compris les crèmes pour le corps, divers produits capillaires, le maquillage et les parfums.
u Utilisation générale présumée au Canada; Herbst et Hunger 2004; Hunger 2003.
v Peut être disponible au Canada pour des produits de traitement de l’eau d’aquarium, d’après l’information accessible au public; Hikari USA 2016.
Le Brilliant Blue FCF est un produit de formulation utilisé dans des produits antiparasitaires actuellement homologués (comme il est indiqué dans le tableau 4-2 ci‑dessus) et il figure sur la Liste des produits de formulation de pesticides de l’Agence de réglementation de la lutte antiparasitaire (ARLA 2010).
Sur le plan international, l’utilisation du Basic Violet 3 comme colorant dans des cosmétiques a déjà été déclarée (Diamante et coll. 2009; AGDH 2014; EWG c2007-2017). Cependant, au Canada, il figure actuellement sur la Liste critique des ingrédients de cosmétique (Santé Canada [modifié, 2015b])Note de bas de page 4 comme ingrédient interdit et, en Europe, son utilisation est maintenant interdite dans les cosmétiques, y compris les colorants capillaires (EC 2009). En Europe, le Malachite Green est également interdit dans les cosmétiques, et le Basic Violet 4 et le Basic Blue 7 sont interdits dans les colorants capillaires (EC 2009). Les colorants et pigments à base de triarylméthanes sont généralement reconnus à l’échelle internationale pour leur utilisation dans l’industrie des encres d’imprimerie, en particulier dans l’emballage (Herbst et Hunger 2004), la teinture du papier et des textiles, et également dans les cosmétiques, les médicaments et les aliments (Hunger 2003). Le Basic Violet 3 et le Malachite Green sont également utilisés en laboratoire comme indicateurs de pH et comme colorants biologiques (Hunger 2003).
5. Rejets dans l’environnement
Une seule entreprise de fabrication de produits chimiques a déclaré l’utilisation du Malachite Green à l’Inventaire national de rejet des polluants, soit des rejets ≤ 0,004 tonne par année dans tous les milieux environnementaux entre 2003 et 2007 (INRP 1993-2015).
Des triarylméthanes peuvent être rejetés dans l’eau par les installations industrielles qui effectuent le désencrage et la teinture du papier (pour les substances associées à ces utilisations), la formulation ou la fabrication de produits de consommation, ainsi que par leur utilisation par les consommateurs. Les diverses utilisations de produits de consommation contenant ces substances pourraient donner lieu à des rejets à l’égout qui rejoignent les systèmes de traitement des eaux uséesNote de bas de page 5 (STEU), et éventuellement les eaux de surface.
L’épandage intentionnel de produits agricoles contenant du Brilliant Blue FCF pourrait entraîner des rejets dans les eaux de surface, par ruissellement.
6. Devenir et comportement dans l’environnement
6.1 Distribution dans l’environnement
On ne s’attend pas à ce que les triarylméthanes soient rejetés dans l’atmosphère en raison de leurs utilisations prévues et de leurs propriétés physico-chimiques. Les pressions de vapeur et les constantes de la loi d’Henry de ces substances sont très faibles, substances présentes sous forme cationique dans l’environnement (exception faite du Brilliant Blue FCF et du Pigment Blue 61). Ces propriétés indiquent que la volatilisation serait négligeable à partir de la surface du sol et des eaux de surface. On ne s’attend donc pas à ce que ces substances présentent un transport atmosphérique à grande distance.
Compte tenu des utilisations déclarées des triarylméthanes, on s’attend à ce que ces substances se retrouvent dans les eaux de surface. Les caractéristiques des STEU et l’affinité des triarylméthanes pour les solides dissous et en suspension déterminent la mesure dans laquelle ces substances se retrouvent dans les eaux de surface. En général, la plupart des triarylméthanes devraient être associés, dans une large mesure, aux solides dissous et en suspension. Bien que les caractéristiques du Brilliant Blue FCF le rendent moins susceptible de se sorber sur les particules dans l’environnement, une certaine sorption peut se produire, selon les conditions du milieu (German-Heins et Flury 2000).
Le Pigment Blue 61 a une très faible solubilité, tandis que les autres substances sont toutes solubles dans l’eau. Dans le milieu aquatique, le Pigment Blue 61 est susceptible de se comporter comme une particule et de se déposer dans les sédiments du lit, tandis que les autres substances se dissocient, libérant la molécule ionique du triarylméthane et le contre-ion associé. Les colorants non sulfonés existeront sous forme de cations à un pH observé dans l’environnement et auront donc une affinité pour les particules chargées négativement de la colonne d’eau (p. ex., acides humiques et fulviques, matériaux argileux), bien qu’une fraction d’entre eux puisse demeurer dans la colonne d’eau. Les processus de sorption seraient dominés par des interactions électrostatiques en raison des sites de sorption chargés négativement sur le carbone organique dissous et les solides en suspension, bien que le carbone organique puisse aussi jouer un faible rôle (Kah et Brown 2006; Droge et Goss 2012, 2013). Le Brilliant Blue FCF existera également à l’état chargé (avec une charge nette négative). Par conséquent, son devenir dans l’environnement sera également tributaire des interactions électrostatiques. Ces colorants peuvent être transportés dans l’eau, et les solides en suspension peuvent éventuellement se déposer dans les sédiments du lit, où les colorants sorbés sont susceptibles de demeurer, à moins qu’il n’y ait un mélange et un transport des sédiments du lit. Par conséquent, les colorants de triarylméthane non sulfonés se lieront probablement aux particules et se déposeront sur les sédiments, tandis que le Brilliant Blue FCF, en raison de sa solubilité élevée et de son caractère anionique, est plus susceptible de rester dans l’eau.
Le devenir des triarylméthanes dans les sols sera également tributaire de leurs caractéristiques de sorption. En raison de sa grande solubilité et de son caractère anionique, le Brilliant Blue FCF pourrait, dans certaines conditions, se déplacer dans l’eau interstitielle du sol. Le Pigment Blue 61 ne devrait pas être mobile, étant donné sa piètre solubilité dans l’eau, ni non plus les colorants de triarylméthane non sulfonés. Bien que l’échange d’ions soit complexe et mal compris (Droge et Goss 2012, 2013), on s’attend à ce que les colorants de triarylméthane aient une affinité pour les particules chargées et soient mobiles ou non, selon la teneur en humidité et le type de sol, le degré d’érosion ou le ruissellement. Par exemple, les colorants de triarylméthane non sulfonés seraient probablement moins mobiles dans les sols à forte teneur en matières organiques ou en argile (Droge et Goss 2012, 2013; Kah et Brown 2006). En outre, pour les cations organiques tels que les colorants de triarylméthane non sulfonés, l’affinité pour la sorption dépend en outre de la concurrence avec les autres cations organiques présents dans les sols (Droge et Goss 2012). De plus, l’adsorption du Brilliant Blue FCF semble être influencée par la force ionique de la solution du sol (German-Heins et Flury 2000).
6.2 Persistance dans l’environnement
D’après l’Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers (ETAD, 1995), les colorants, à part quelques exceptions, sont considérés comme essentiellement non biodégradables en conditions aérobies. L’évaluation répétée de la biodégradabilité immédiate et intrinsèque de plus de 80 colorants différents, au moyen de tests de dépistage acceptés (p. ex., les tests de l’OCDE), a confirmé cette caractéristique (Pagga et Brown 1986; ETAD 1992). Bien qu’il existe des preuves que les colorants de triarylméthane se dégradent avec le temps (Bumpus et Brock 1988; Andrews et coll. 1990; Perez-Estrada et coll. 2008; Ogugbue et Sawidis 2011), les données de modélisation (BIOWIN 2008) indiquent que la biodégradation des triarylméthanes sera relativement lente, avec des demi-vies extrapolées (le cas échéant), allant de plusieurs semaines à plusieurs mois, certaines de ces substances étant considérées récalcitrantes.
Comme les autres pigments organiques, le Pigment Blue 61 ne devrait pas se biodégrader dans les systèmes aquatiques (ECHA c2007-2017a).
Par conséquent, les triarylméthanes devraient être persistants dans les milieux naturels (eau, sédiments et sol), avec des demi-vies prévues supérieures à 182 jours pour l’eau et le sol, et supérieures à 365 jours pour les sédiments (BIOWIN 2008). Le potentiel d’exposition, dans le temps et dans l’espace, des organismes à ces substances dans l’environnement est donc accru.
6.3 Potentiel de bioaccumulation
Les données empiriques sur le Malachite Green et les données modélisées pour d’autres substances du groupe indiquent que ces triarylméthanes ne sont pas susceptibles de faire l’objet d’une bioaccumulation dans les organismes aquatiques (tableau 6‑1). Cependant, en raison de la nature cationique des colorants de triarylméthane non sulfonés, les valeurs de Koe et de solubilité dans l’octanol, utilisées pour estimer le facteur de bioconcentration (FBC) et le facteur de bioaccumulation (FBA) à partir des modèles, notamment le modèle FBCFBA d’EPIWIN (2010), pourraient ne pas être de bons indicateurs de bioaccumulation pour ces substances. Ces colorants de triarylméthane sont plus susceptibles de se retrouver dans les protéines des membranes cellulaires que dans les lipides, cette séparation étant estimée à l’aide des valeurs de Koe et de solubilité dans l’octanol.
| Nom commun | Organisme d’essai | Concentration expérimentale mg/L (durée) | FBC (L/kg) | FBA (L/kg) | Référence |
|---|---|---|---|---|---|
| Basic violet 3 | Poissons | S.O. | 3,2 | 1,4 | FBCFBA 2010 |
| Malachite green | Carpe | 0,002–0,02(56 jours) | 75– 91 | S.O. | NITE 2002 |
| Basic violet 4 a | Poissons | N.D. | 1 091 | 1 191 | FBCFBA 2010 |
| Basic blue 7 a | Poissons | N.D. | 2 104 | 2 717 | FBCFBA 2010 |
| Pigment blue 61 | Poissons | N.D. | 476 b | S.O. | ECHA, c2007-2017a |
| Brilliant blue FCF | Poissons | N.D. | 3,2 | 0,9 | FBCFBA 2010 |
Abréviations : FBC = facteur de bioconcentration; FBA = facteur de bioaccumulation; N.D., non disponible.
a Valeurs FBC/FBA mi-trophiques estimées, y compris les taux de biotransformation estimés (méthode d’Arnot-Gobas), avec l’hypothèse que les valeurs log Koe sont supérieures à 4.
b Le FBC est calculé sous forme de concentration dans le biote (1,19 mg/L) divisée par la concentration dans l’eau (0,0025 mg/L), selon la méthode de Gobas et Morrison (2000).
Il semble que l’accumulation potentielle de triarylméthanes dans les tissus des poissons se ferait probablement par liaison aux protéines et à l’ADN (Docampo et Moreno 1990; Mani et Bharagava 2016). Cela est confirmé par le fait que certains triarylméthanes sont couramment utilisés comme colorants biologiques dans les laboratoires, parce qu’ils colorent facilement les acides aminés des protéines (Mani et Bharagava 2016).
Une fois solubilisés dans l’eau naturelle, les colorants de triarylméthane non sulfonés peuvent se fixer à la surface de divers tissus (p. ex., branchies des poissons, algues, surfaces cutanées) ou à des aliments. Bien qu’on ne sache pas clairement si ces colorants de triarylméthane traversent le tractus gastro-intestinal pour se rendre jusqu’à la circulation sanguine, il est raisonnable d’estimer qu’une fraction d’entre eux pourrait se lier aux protéines plasmatiques (Enoch et coll. 2011). Il a été démontré que le Malachite Green est persistant dans le tissu des poissons (Lanzing 1965; Poe et Wilson 1983; Srivasta et coll. 2004; Xie et coll. 2012).
Bien qu’on ait mesuré des triarylméthanes (en particulier le Malachite Green) dans les tissus des poissons (Jiang et coll. 2009; Zhijun et coll. 2011), ces substances sont susceptibles d’être dépurées du corps en raison de leurs propriétés physiques et chimiques (Bergwerff et coll. 2004; Niska et coll. 2009).
Le Brilliant Blue FCF est susceptible de se comporter différemment des colorants de triarylméthane non sulfonés, car on s’attend à ce qu’il soit chargé négativement (anionique) à un pH observé dans l’environnement et qu’il soit donc moins susceptible de se retrouver dans les membranes cellulaires, par rapport aux substances cationiques. De plus, comme il est très soluble dans l’eau, on ne s’attend pas à ce qu’il se répartisse dans les lipides stockés dans les poissons ni, par conséquent, qu’il s’accumule dans les organismes aquatiques.
Contrairement aux autres colorants de triarylméthane, le Pigment Blue 61 est une substance neutre aux pH observés dans l’environnement et, par conséquent, ne devrait pas interagir de façon électrostatique avec divers milieux. Une estimation de la valeur du log Koe peut donc être calculée de façon fiable et être donc utilisée pour estimer la valeur du FBC. Une teneur moyenne en lipides de 5 % chez le poisson (Geyer et coll. 1985) est couramment utilisée pour normaliser la teneur en lipides du corps entier, d’après des lignes directrices reconnues (OCDE TG 305). La solubilité du Pigment Blue 61 dans l’octanol de 23,8 mg/L (tableau 3‑2) et la teneur moyenne en lipides de 5 % chez le poisson ont été utilisées pour estimer une concentration maximale de la substance dans le poisson de 1,19 mg/L. Ainsi, la valeur du FBC pour le Pigment Blue 61, calculée selon la méthode de Gobas et Morrison (2000), est de 476 (tableau 6‑1). Par conséquent, on ne s’attend pas à ce que le Pigment Blue 61 s’accumule dans les poissons (Anliker et Moser 1987).
Dans l’ensemble, les données sur le Brilliant Blue FCF et le Pigment Blue 61 indiquent que ces substances ont un faible potentiel de bioaccumulation. Les données expérimentales disponibles et les résultats modélisés révèlent que les colorants de triarylméthane non sulfonés peuvent avoir un certain potentiel de bioaccumulation, mais à des niveaux bien inférieurs aux critères énoncés dans le Règlement sur la persistance et la bioaccumulation, pris en vertu de la LCPE. On ne s’attend pas à ce que les colorants de triarylméthane non sulfonés fassent l’objet d’une bioaccumulation importante dans les tissus lipidiques des organismes aquatiques. Cependant, ils peuvent interagir avec les protéines et se lier avec celles-ci, ce qui peut entraîner une certaine bioaccumulation dans les autres tissus.
7. Risque d’effets nocifs sur l’environnement
7.1 Évaluation des effets environnementaux
7.1.1 Mode et mécanisme d’action
À l’aide de la boîte à outils QSAR de l’OCDE permettant de classifier le mode d’action, on a classé les triarylméthanes comme étant « réactif, sans précision ». De plus, certains résultats du modèle de liaison AR de ToxCast indiquent un potentiel d’effets de type endocrinien. Les triarylméthanes semblent provoquer trois grands types d’effets cellulaires.
Tout d’abord, selon les données, ils causent une perturbation dans les mitochondries. Le Basic Violet 3 semble se concentrer dans les mitochondries des animaux où il perturbe ces organelles en agissant comme agent découpleur de la phosphorylation oxydative (Docampo et Moreno 1990). Il peut augmenter l’activité de l’ATPase, avoir des effets sur la régulation de la respiration et interférer avec la synthèse de l’ATP (Docampo et Moreno 1990). De même, des études ont montré que le Malachite Green peut endommager les mitochondries et provoquer une altération nucléaire (Gerundo et coll. 1991), qui peut entraîner une augmentation de la glycolyse, un phénomène courant dans les cellules cancéreuses (Xu et coll. 2005).
En deuxième lieu, les triarylméthanes peuvent agir en se liant à l’ADN et aux protéines. Des études ont indiqué que le Basic Violet 3 se lie à l’ADN et interagit avec deux paires de bases A-T adjacentes, provoquant un entortillement, une flexion sévère ou le déroulement de la double hélice de l’ADN. Il en résulte une altération chromosomique et des lésions (Docampo et Moreno 1990). Les triarylméthanes sont couramment utilisés comme colorants biologiques dans les laboratoires, car ils colorent facilement les acides aminés des protéines (Mani et Bharagava 2016).
En troisième lieu, les triarylméthanes peuvent causer des effets nocifs en produisant des radicaux libres dans les cellules. Le Basic Violet 3 peut être photo-réduit en une espèce réactive de l’oxygène (ROS) à base de carbone par une exposition à la lumière visible (Docampo et coll. 1988). Dans des conditions aérobies, une action photo-dynamique se produit, au cours de laquelle les radicaux libres s’auto-oxydent. On croit que cette action photo-réductrice se fait par l’intermédiaire des produits de réduction de l’oxygène (Docampo et coll. 1988). Il a également été démontré que le Malachite Green déclenche l’appauvrissement des réserves intracellulaires dans les organismes et, comme le Basic Violet 3, augmente les concentrations de ROS (Dhamgaye et coll. 2012). Il existe des données donnant à penser qu’une accumulation excessive de ROS peut entraîner une nécrose (Xu et coll. 2005).
Les triarylméthanes peuvent également causer des effets nocifs dans les organismes par des effets physiques. Il a été démontré que le Malachite Green accélère la fréquence de ventilation et de respiration chez les poissons, car il obstrue les branchies avec des particules, augmente la production de mucus et cause des lésions épithéliales (Ross et coll. 1985).
En règle générale, en raison de la similarité de leurs caractéristiques physico-chimiques, les quatre colorants de triarylméthane non sulfonés devraient avoir un mécanisme d’action commun expliquant leurs effets nocifs dans l’environnement.
Bien qu’on manque de données sur les effets du Basic Violet 4 et du Basic Blue 7, on s’attend à ce qu’ils agissent de la même façon que le Basic Violet 3 et le Malachite Green, étant donné leur structure similaire. Le Brilliant Blue FCF et le Pigment Blue 61 devraient toutefois présenter une toxicité moindre en raison de la présence de groupes acide sulfonique (SO3). Les études ont montré que l’augmentation du nombre de groupes SO3 sur une molécule la rend plus hydrophile et diminue la toxicité de la substance (Mon et coll. 2006).
7.1.2 Effets sur les organismes aquatiques
Bien que la toxicité aiguë du Basic Violet 3 et du Malachite Green pour les organismes aquatiques ait été bien caractérisée, on dispose de peu données sur le Brilliant Blue FCF, et on manque de données sur la toxicité aquatique du Basic Violet 4, du Basic Blue 7 et du Pigment Blue 61. Compte tenu des similarités entre les colorants de triarylméthane non sulfonés, les données toxicologiques disponibles pour le Basic Violet 3 et le Malachite Green ont été utilisées par lecture croisée pour évaluer la toxicité du Basic Violet 4 et du Basic Blue 7.
Les études disponibles portant sur les effets environnementaux de ces substances comprennent des données sur les poissons, les invertébrés et les algues. D’après les données disponibles, qui proviennent principalement d’études de toxicité aiguë, les organismes les plus sensibles semblent être les poissons d’eau douce. Les principales études sur les organismes aquatiques sont répertoriées à l’annexe A (tableau A-1).
La valeur critique de toxicité choisie pour les organismes aquatiques pour les quatre colorants non sulfonés (c.‑à‑d. le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7) était une CL50 sur 96 h de 0,03 mg/L, obtenue dans une étude sur la toxicité du Malachite Green chez le crapet arlequin (Bills et coll. 1977). Un facteur d’évaluation de 30 a été appliqué pour tenir compte de l’extrapolation de la toxicité aiguë à la toxicité chronique (facteur de 10) et de l’incertitude entourant les substances dont le mode d’action devrait être réactif (facteur de 3). Aucune extrapolation n’a été nécessaire pour tenir compte des variations interspécifiques, car il existe des données sur les effets sur un grand nombre d’espèces (c.‑à‑d. plus de 10), appartenant à plusieurs groupes taxonomiques différents. La concentration estimée sans effet (CESE) pour les colorants non sulfonés a donc été calculée, et s’établit à 0,001 mg/L. Cette valeur indique que le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7 (individuellement et collectivement) pourraient causer des effets nocifs sur les organismes aquatiques à de faibles concentrations.
Bien qu’aucune donnée sur la reproduction ou le développement n’ait été trouvée pour les organismes aquatiques, il existe des données selon lesquelles l’oxalate de vert de malachite est toxique pour le développement des mammifères (voir la section 8.2).
Pour ce qui est du Brilliant Blue FCF, une étude empirique de toxicité en milieu aquatique était disponible. Le critère d’effet traduisant la plus grande sensibilité, dans cette étude, était une CL50 sur 96 h de 180 mg/L chez le saumon rouge (Wan et coll. 1991). Comme le colorant testé dans l’étude consistait en 50 % de Brilliant Blue FCF, on estime que la CL50 pour le Brilliant Blue FCF serait la moitié de cette valeur, c.‑à‑d. une CL50 de 90 mg/L, en supposant que la toxicité augmente linéairement et que les autres composants (agent tensioactif et autres produits de formulation) ne contribuent pas à la toxicité globale de la substance à l’essai. Un facteur d’évaluation de 600 a été appliqué pour tenir compte de l’extrapolation des effets médians létaux à court terme aux effets faibles sublétaux à long terme (facteur de 10) et des variations interspécifiques, car l’ensemble de données portait sur six espèces d’un même groupe taxonomique (facteur de 20), et pour tenir compte du mode d’action réactif pour cette substance (facteur de 3). La CESE obtenue pour cette substance était de 0,15 mg/L.
Les études en milieu aquatique portant sur le Pigment Blue 61 et son analogue, le Pigment Blue 56, n’ont montré aucun effet à des concentrations bien supérieures à leurs limites de solubilité (2,5 µg/L), ce qui indique qu’à l’état le plus dissous, le Pigment Blue 61 ne devrait avoir aucun effet nocif. Par conséquent, aucune CESE pour le Pigment Blue 61 n’a été calculée.
7.1.3 Effets sur les organismes vivant dans les sédiments et les sols
Les données sur la toxicité des triarylméthanes pour les sols et les sédiments sont très limitées. Une étude disponible de toxicité du Malachite Green pour le sol a indiqué une CL50 sur 14 jours de 1,45 mg/kg pour les lombrics (Gopinathan et coll. 2015). Les colorants de triarylméthane qui sont utilisés comme colorants biologiques (comme le Malachite Green et le Basic Violet 3) peuvent se lier à l’ADN et à des protéines. Cette activité pourrait potentiellement causer des effets nocifs entraînant la mort dans les organismes qui respirent par la peau, comme les lombrics, en entravant les fonctions respiratoires de la peau. C’est le cas des lombrics exposés à un colorant à base de xanthène, une substance qui se lie également à l’ADN et aux protéines (Princz et coll. 2014).
Compte tenu des données limitées sur l’écotoxicité et la caractérisation de l’exposition à ces substances (dont il est question à la section suivante), les valeurs CESE pour les sols et les sédiments n’ont pas été calculées pour aucun des triarylméthanes.
7.2 Évaluation de l’exposition dans l’environnement
L’exposition potentielle des organismes aux triarylméthanes dans l’environnement se fera principalement par les eaux de surface. Aucune donnée de surveillance environnementale n’était disponible pour aucune de ces substances. Par conséquent, les expositions ont été estimées pour des scénarios clés. La caractérisation de l’exposition s’est concentrée sur des scénarios qui représentent les situations d’exposition de l’environnement les plus probables pour les quatre colorants non sulfonés collectivement, et pour le Brilliant Blue FCF. Ces scénarios comprenaient leur utilisation dans la teinture et le désencrage du papier, la formulation générale des produits, et les produits de consommation qui sont rejetés à l’égout et transportés vers les STEU. Pour les quatre scénarios, une approche probabiliste a été utilisée.
| Scénario | Description du scénario | Substances incluses |
|---|---|---|
| 1 | Teinture du papier | 4 substances non sulfonées (Basic Violet 3, Malachite Green, Basic Violet 4 et Basic Blue 7) |
| 1 | Teinture du papier | Brilliant blue FCF |
| 2 | Désencrage du papier | 4 substances non sulfonées, comme ci-dessus |
| 2 | Désencrage du papier | Brilliant blue FCF |
| 3 | Utilisation générale comme produit de formulation | 4 substances non sulfonées, comme ci-dessus |
| 4 | Produits de consommation | Brilliant blue FCF |
Les rejets de colorants non sulfonés dans les eaux de surface devraient se produire par l’intermédiaire des STEU industriels pour les scénarios 1 et 2, et des STEU industriels et hors site pour le scénario 3. En raison de leurs propriétés physico-chimiques, ces colorants se retrouveront en grande partie dans les boues. Comme les boues provenant des STEU sur place ne seraient pas épandues sur les terres agricoles ou les pâturages, un scénario d’exposition pour le sol n’a pas été élaboré pour les colorants non sulfonés. Le Brilliant Blue FCF est présent dans les produits de consommation et on s’attend à ce que les rejets dans les eaux de surface soient attribuables à des STEU. Cependant, étant donné ses propriétés physico-chimiques (faible affinité pour les solides en suspension) et le manque de données sur sa toxicité pour les sols qui permettraient de calculer une CESE pour le sol, aucun scénario d’exposition du sol n’a été élaboré pour cette substance. Enfin, des scénarios d’exposition n’ont pas été élaborés pour le Pigment Blue 61, parce qu’il a une très faible solubilité dans l’eau, que ses effets sur les organismes aquatiques n’ont été observés que bien au-delà de sa limite de solubilité dans l’eau en présence d’un émulsifiant, et qu’il n’y avait pas de donnée disponible pour les organismes vivant dans le sol. On s’attend à ce qu’il se comporte comme une particule, en raison de sa taille médiane et de sa faible solubilité dans l’eau, de sorte qu’il ne serait probablement pas biodisponible.
7.2.1 Calcul des concentrations environnementales estimées et hypothèses générales
Les concentrations environnementales estimées (CEE) ont été calculées collectivement pour les quatre colorants non sulfonés (Basic Violet 3, Malachite Green, Basic Violet 4, Basic Blue 7) et pour le Brilliant Blue FCF, selon les scénarios d’exposition pertinents. Les scénarios de rejets industriels étaient fondés sur la capacité de production maximale des installations, plutôt que sur les quantités utilisées déclarées pour les substances individuelles. On a supposé que l’un ou l’autre des colorants de triarylméthane non sulfonés pouvait être substitué pour un autre. Par conséquent, aucune distinction n’a été faite entre les différentes substances, et une seule plage collective de CEE pour les colorants de triarylméthane non sulfonés a été calculée. Les CEE représentent les concentrations potentielles de ces substances dans le plan d’eau récepteur près du point de rejet d’un STEU. Les valeurs CEE sont présentées pour chacun des scénarios d’exposition, et un résumé des principales hypothèses figure à l’annexe B.
Dans tous les cas, les CEE en milieu aquatique ont été calculées d’après une fourchette de taux d’élimination applicables au type de technologies de traitement employées par le STEU en cause, et d’après les propriétés physico-chimiques des triarylméthanes. Toutes les CEE en milieu aquatique ont également été calculées d’après un facteur de dilution basé sur le 10e centile du débit du plan d’eau récepteur, avec plafonnement à 10.
7.2.2 Scénario 1 : Teinture du papier
Dans ce scénario, 32 usines de pâtes et papiers au Canada qui effectuent la teinture du papier ont été prises en compte. Deux valeurs de CEE ont été calculées, une pour l’utilisation des quatre colorants de triarylméthane non sulfonés pour la teinture du papier, et la deuxième pour la teinture du papier à l’aide du Brilliant Blue FCF.
L’information a été compilée pour chacune de ces installations, notamment d’après leurs données sur la capacité de production de papier connue, le nombre de jours d’exploitation, les débits de rejet dans l’eau, les débits des plans d’eau récepteurs et les technologies utilisées pour le traitement sur place des eaux usées. L’information sur le rejet ou non des installations dans un autre STEU (hors site) a également été prise en compte. D’autres paramètres clés qui n’étaient pas propres à un site particulier ont été estimés sous forme de plages de distribution et appliqués à tous les sites. Ces paramètres comprenaient le taux d’utilisation du produit, la fraction de la substance chimique dans le produit colorant, le taux de rétention et le taux d’élimination pour un type de traitement des eaux usées donné. Voir l’annexe B (tableau B-1) pour un résumé des paramètres et des hypothèses pour les triarylméthanes non sulfonés et le Brilliant Blue FCF. Ces paramètres, ainsi que l’information de chaque site, ont été utilisés dans une analyse de Monte-Carlo qui a donné une plage de CEE. Ces CEE ont ensuite été comparées aux CESE pour les colorants non sulfonés et aux CESE pour le Brilliant Blue FCF, respectivement.
Pour tous les colorants de triarylméthane non sulfonés, les CEE calculées dans les plans d’eau récepteurs près du point de rejet allaient de 1,45 × 10-9 à 425 µg/L, et 28 % des itérations donnaient des CEE supérieures à la CESE (1 µg/L).
Pour ce qui est du Brilliant Blue FCF, les CEE calculées dans les plans d’eau récepteurs près du point de rejet allaient de 2,41 × 10-8 à 479 µg/L. Dans ce cas, moins de 1 % des itérations donnaient des CEE supérieures à la CESE (150 µg/L).
7.2.3 Scénario 2 : Désencrage du papier
Dans ce scénario, il s’agissait de déterminer l’élimination du papier recyclé des encres contenant les colorants de triarylméthane. Deux CEE ont été calculées, une pour les quatre colorants non sulfonés et une pour le Brilliant Blue FCF, en supposant qu’une partie du papier recyclé était imprimée avec une encre contenant un ou plusieurs des quatre colorants non sulfonés ou avec du Brilliant Blue FCF.
Le papier recyclé peut contenir des colorants de triarylméthane, aussi bien dans la fibre du papier que dans les colorants utilisés pour colorer le papier lui-même, ainsi que dans les encres imprimées sur le papier. On a donc supposé que le désencrage n’enlève que l’encre (et le colorant qu’elle contient) fixée à la surface du papier, et non le colorant lié à la fibre de papier et qui a servi à colorer le papier (Liu et coll. 2007). Une hypothèse clé est la masse de la substance dans le papier à recycler, qui a été estimée en utilisant la capacité d’une usine de désencrage donnée. Parmi les autres hypothèses concernant la composition du papier recyclé, mentionnons la couverture moyenne de l’encre, la densité moyenne du papier, et la couverture de l’encre (voir le tableau B-2). Pour une pile donnée de papier destiné au recyclage, on a ainsi obtenu une teneur fractionnaire de l’encre située entre 0,004 et 0,01 gramme d’encre par gramme de papier (g encre/g papier). Cette estimation est corroborée par les estimations européennes de la teneur en encre du papier destiné au recyclage, qui se chiffre entre 0,003 et 0,07 g encre/g papier (OCDE 2009).
Ce scénario a porté sur treize usines de recyclage de pâtes et papiers, et sur leur capacité individuelle connue de recyclage, le débit de leurs effluents, leurs STEU sur place et leurs facteurs de dilution. Les hypothèses comprenaient un facteur d’émission fractionnaire d’encre (0,02 à 0,2; Beatson 2012) et la fraction de triarylméthane dans l’encre (1 × 10-4 et 2 × 10-2) en fonction du poids. Une incertitude importante dans le calcul des valeurs CEE est la proportion réelle des colorants de triarylméthane dans l’encre. Un résumé des principales hypothèses figure à l’annexe B (tableau B-2). Ces paramètres ont été utilisés dans une analyse de Monte-Carlo qui a donné une plage CEE.
Pour l’un ou l’autre des colorants de triarylméthane non sulfonés, les CEE calculées dans les plans d’eau récepteurs près du point de rejet allaient de 5,5 × 10-5 à 231 µg/L, et 50 % des itérations donnaient des CEE supérieures à la CESE (1 µg/L).
Pour ce qui est du Brilliant Blue FCF, les CEE calculées dans les plans d’eau récepteurs près du point de rejet allaient de 1,8 × 10-6 à 136 µg/L. Dans ce cas, aucune des itérations n’a donné de CEE supérieure à la CESE (150 µg/L).
7.2.4 Scénario 3 : Utilisation générale comme produits de formulation
Une analyse probabiliste a été effectuée afin de déterminer les CEE associées aux rejets de colorants de triarylméthane par les installations qui utilisent ces substances dans la formulation de produits. Comme les quatre colorants non sulfonés présentent le plus grand danger, ce scénario d’exposition a porté sur l’estimation d’une CEE pour la formulation générale des produits contenant l’une ou l’autre de ces quatre substances. Pour ce calcul, nous avons utilisé les données propres au site de l’entreprise de formulation qui avait déclaré la plus grande quantité utilisée de colorants de triarylméthane non sulfonés au Canada. Dans ce scénario, on a utilisé des données comme les facteurs d’émission basés sur le bilan massique allant de 0,5 % à 1,1 %. On a tenu compte de l’élimination secondaire sur place et hors site, et de la dilution élevée dans l’environnement. Si l’une ou l’autre de ces conditions n’était pas présente dans une installation traitant de grandes quantités de colorants de triarylméthane non sulfonés, l’approfondissement de ce scénario pourrait avoir un impact sur le résultat, ce qui pourrait être préoccupant. Un résumé des hypothèses figure à l’annexe B (tableau B-3). Ces paramètres ont été utilisés dans une analyse de Monte-Carlo qui a donné une plage CEE.
Pour tous les colorants de triarylméthane non sulfonés, les CEE calculées dans les plans d’eau récepteurs près du point de rejet allaient de 3,6 × 10-3 à 2,4 µg/L. Moins de 2 % des itérations donnaient des CEE supérieures à la CESE (1 µg/L).
7.2.5 Scénario 4 : Produits de consommation
Ce scénario a été élaboré pour le Brilliant Blue FCF, en raison de son utilisation dans les produits de consommation. On s’attend à ce que le Brilliant Blue FCF soit présent partout au Canada, vu son utilisation dans ces produits. Par conséquent, la CEE est estimée à l’aide du modèle aquatique des rejets de produits de consommation (modèle interne d’Environnement et Changement climatique Canada). Il s’agit d’un modèle probabiliste canadien, basé sur la population, utilisé pour estimer l’exposition environnementale résultant des rejets par les installations de traitement des eaux usées, des produits chimiques présents dans les produits de consommation qui sont mis à l’égout. Les données sur la distribution comprennent les facteurs de dilution (calculés d’après le 10e centile du débit des plans d’eau récepteurs), du type de traitement employé par les STEU et des rejets par habitant. On a employé un large éventail d’utilisations possibles de produits chimiques pour tenir compte de l’importation de produits manufacturés contenant ces substances.
Les CEE calculées pour le Brilliant Blue FCF dans les plans d’eau récepteurs sont de 3,0 x 10-9 à 455 µg/L près du point de rejet. Moins de 0,01 % des CEE sont supérieures à la CESE (150 µg/L).
Dans le pire des scénarios, on a utilisé des quantités supérieures à celles qui ont été déclarées dans le cadre de l’enquête menée en vertu de l’article 71 de la LCPE, pour tenir compte d’une utilisation maximale du Brilliant Blue FCF. Des CEE en milieu aquatique simulées et relativement élevées (supérieures à 150 µg/L) étaient largement associées aux produits disponibles aux consommateurs, atteignant 3 grammes de Brilliant Blue FCF par jour par personne, ou encore une masse totale de Brilliant Blue FCF atteignant 45 millions kg par année, ce qui dépasse grandement la masse totale déclarée par année dans l’enquête menée en vertu de l’article 71. Par exemple, en tenant compte des concentrations connues de Brilliant Blue FCF dans le shampoing, et même si 100 % des Canadiens utilisaient du shampoing contenant cette substance, la CEE au 95e centile ne dépasserait pas la CESE de 150 µg/L. Bien qu’il existe d’autres produits utilisés par les consommateurs qui contribueraient également aux rejets dans l’environnement, on ne s’attend pas à ce qu’ils se traduisent par des concentrations environnementales importantes, étant donné les faibles concentrations de Brilliant Blue FCF dans ces produits.
7.3 Caractérisation des risques pour l’environnement
L’approche retenue dans la présente évaluation préalable des risques pour l’environnement consistait à examiner les données d’évaluation et à élaborer des conclusions fondées sur la méthode du poids de la preuve et le principe de précaution. Des données ont été recueillies pour déterminer le potentiel des triarylméthanes de causer des risques pour l’environnement au Canada. Diverses données probantes directes ont été examinées pour appuyer la caractérisation du risque écologique.
7.3.1 Analyse des quotients de risque
Pour l’analyse des quotients de risque, on a comparé les estimations de l’exposition (valeurs CEE; voir la section 7.2 sur l’évaluation de l’exposition dans l’environnement) avec les renseignements sur la toxicité écologique (CESE; voir la section 7.1 sur l’évaluation des effets environnementaux) pour déterminer s’il existe un potentiel d’effets nocifs dans l’environnement au Canada. Pour calculer les quotients de risque (QR), on divise la CEE par la CESE pour les compartiments environnementaux pertinents et les scénarios d’exposition connexes. Les QR n’ont pas été calculés pour le Pigment Blue 61. Le tableau 7‑2 présente les QR pour les cinq autres colorants de triarylméthane qui peuvent être rejetés dans l’eau via les eaux usées.
| Scénario d’exposition | Plage de CEE (µg/L) | CESE en milieu aquatique (µg/L) | Plage des QR | Pourcentage des itérations ayant un QR > 1 |
|---|---|---|---|---|
| Teinture du papier (colorants de triarylméthane non sulfonés) | 1,45×10-9 à 425a | 1a | 1,45×10-9 à 425 | 28 |
| Teinture du papier (Brilliant Blue FCF) | 2,41×10-8 à 479b | 150b | 1,61×10-10 à 3,19 | < 1 |
| Désencrage du papier (colorants de triarylméthane non sulfonés) | 5,5×10-5 à 231a | 1 a | 5,5×10-5 à 231 | 50 |
| Désencrage du papier (Brilliant Blue FCF) | 1,8×10-6 à 136b | 150 b | 1,2×10-8 à 0,91 | 0 |
| Utilisation générale comme produit de formulation (colorants de triarylméthane non sulfonés) | 3,6×10-3 à 2,4 a | 1 a | 3,6×10-3 à 2,4 | 2 |
| Produits utilisés par les consommateurs (Brilliant Blue FCF) | 3,0×10-9 à 455 | 150 b | 2,0×10-11 à 3,0 | 0,01 |
a Un ou l’autre des colorants de triarylméthane non sulfonés (Basic Violet 3, Malachite Green, Basic Violet 4 et Basic Blue 7).
b Brilliant blue FCF.
Comme l’indique le tableau 7.2, en ce qui concerne le scénario de teinture du papier pour chacun des quatre colorants non sulfonés, 28 % des itérations avaient un QR supérieur à 1. Les QR simulés varient en fonction de la combinaison de paramètres, comme le taux d’utilisation du produit colorant, le taux de rétention, la concentration de la substance colorante au triarylméthane dans le produit colorant et le taux d’élimination. Par exemple, un taux d’utilisation supérieur de produit colorant (> 0,2 kg de produit colorant par tonne de papier) mènera à une probabilité supérieure que le QR dépasse 1. Cependant, le taux d’utilisation des produits colorants dans le papier est souvent inférieur à cette valeur (communication personnelle, courriel de l’Association des produits forestiers du Canada à Environnement et Changement climatique Canada, 2017; sans référence).
Pour le scénario de désencrage des colorants non sulfonés, 50 % des itérations ont un QR supérieur à 1. Les simulations avec les colorants non sulfonés commençaient à dépasser la CESE lorsque ces colorants atteignaient 1 % des colorants utilisés dans les encres du papier imprimé destiné au recyclage. Les CEE simulées pour le scénario de désencrage du papier avec le Brilliant Blue FCF ont commencé à dépasser la CESE lorsque le Brilliant Blue FCF était supposé représenter plus de 60 % des colorants utilisés dans les encres sur du papier imprimé destiné au recyclage. Cependant, il est peu probable que cette situation se produise.
Le scénario élaboré pour la formulation générale et la manutention des produits, à partir de données obtenues du fabricant qui a déclaré les plus grandes quantités utilisées, n’a pas dépassé la CESE, car on a tenu compte des facteurs détaillés propres au site, notamment les facteurs d’émission basés sur le bilan massique, l’élimination secondaire sur place et hors site, et la forte dilution dans l’environnement. Cependant, les simulations de la formulation générale et de la manutention des produits pour un scénario générique, compte tenu des installations de préparation des produits chimiques au Canada qui pourraient répondre à cette demande du marché, ont montré un certain potentiel de dépassement de la CESE pour les colorants de triarylméthane non sulfonés.
7.3.2 Examen des données probantes
Afin de caractériser le risque écologique des triarylméthanes, on a tenu compte des renseignements techniques pour diverses données probantes (comme il en est question dans les sections pertinentes du présent rapport), données qui ont été pondérées qualitativement. Les principales données probantes à l’appui de la conclusion de l’évaluation, pour les quatre colorants de triarylméthane non sulfonés, sont présentées dans le tableau 7‑3, avec une analyse globale du poids de la preuve fournie à la section 7.3.3. Le niveau de confiance désigne l’influence combinée de la qualité et de la variabilité des données, des lacunes dans les données, de la causalité, de la plausibilité et de toute extrapolation requise pour la donnée probante. La pertinence désigne l’impact de la donnée probante lorsque nous déterminons le potentiel de la substance à causer des effets nocifs pour l’environnement canadien. Les qualificateurs utilisés dans l’analyse varient de faibles à élevés, et la pondération de chaque donnée variait selon cinq résultats possibles.
| Donnée probante | Niveau de confiancea | Pertinence pour l’évaluationb | Importance accordéec |
|---|---|---|---|
| Similarité de la structure chimique, par lecture croisée | Élevé | Élevée | Élevée |
| Devenir et comportement dans l’environnement (nature ionique) | Modéré | Élevée | Modérée à élevée |
| Persistance dans l’environnement (c.‑à‑d. eau, sédiments, sol) | Modéré | Modérée | Modérée |
| Bioaccumulation dans les organismes aquatiques | Faible | Modérée | Faible à modérée |
| Mode d’action (réactif) | Modéré | Modérée | Modérée |
| CESE pour les organismes aquatiques | Élevé | Élevée | Élevée |
| CEE : scénario de teinture du papier | Modéré | Élevée | Modérée à élevée |
| CEE : scénario de désencrage du papier | Faible | Faible | Faible |
| CEE : scénario de formulation générale et de manutention des produits | Modéré | Élevée | Modérée à élevée |
| QR : teinture du papier | Modéré | Élevée | Modérée à élevée |
| QR : désencrage du papier | Faible | Faible | Faible |
| QR : formulation générale et manutention des produits | Modéré | Élevée | Modérée à élevée |
a On détermine le degré de confiance en fonction de la qualité des données, de leur variabilité, des lacunes dans les données et de l’adéquation des données.
b La pertinence renvoie aux effets de la donnée probante dans l’évaluation.
c La pondération de chaque donnée probante se fait selon le niveau de confiance et la pertinence de l’évaluation combinés.
Un niveau de confiance modéré à élevé serait attribué aux données évaluées pour le Brilliant Blue FCF et le Pigment Blue 61, mais ces données ont une faible pertinence pour montrer le potentiel que ces substances peuvent causer des effets nocifs dans l’environnement canadien. Ces principales données probantes portaient sur le devenir et le comportement dans l’environnement, la persistance, le potentiel de bioaccumulation, le potentiel de causer des effets nocifs sur les organismes aquatiques, et les QR qui ont été calculés.
7.3.3 Poids de la preuve pour déterminer le potentiel de causer des effets nocifs dans l’environnement canadien
Les quatre colorants de triarylméthane non sulfonés (Basic Violet 3, Malachite Green, Basic Violet 4 et Basic Blue 7) ont une structure chimique et une masse moléculaire similaires. Ils sont solubles dans l’eau et ont une pression de vapeur négligeable. Par conséquent, on présume qu’ils se comportent de la même façon dans l’environnement en ce qui concerne à la fois leur devenir et leurs effets sur les organismes. S’ils sont rejetés dans le milieu aquatique, une fraction de la quantité rejetée peut résider dans la colonne d’eau, étant donné leur solubilité dans l’eau. À un pH observé dans l’environnement, ces substances sont susceptibles de se répartir dans des solides en suspension chargés négativement et dissous. Cette adsorption peut être ou non irréversible. Par conséquent, ces substances peuvent être transportées dans l’eau loin des sources ou elles peuvent se déposer dans les sédiments du lit. Compte tenu de l’utilisation de ces colorants de triarylméthane non sulfonés, on s’attend à ce qu’ils soient éliminés en grande partie lors du traitement industriel des eaux usées, en raison du transfert de ces colorants aux matières organiques. Comme les boues provenant de ces STEU sur place ne seraient pas épandues sur les terres agricoles ou les pâturages, les colorants de triarylméthane non sulfonés ne se retrouveraient pas dans le sol, et l’exposition par ce milieu ne serait pas préoccupante.
On s’attend à ce que ces quatre colorants soient persistants dans les milieux naturels (eau, sédiments et sol). Ainsi, le risque d’exposition des organismes, dans le temps et dans l’espace, à ces colorants dans l’environnement s’en trouve accru. On s’attend à ce que ces substances présentent un faible risque de bioaccumulation dans les tissus lipidiques des organismes aquatiques, d’après des données expérimentales limitées et des résultats de modélisation. Cependant, le Basic Violet 3 et le Malachite Green peuvent interagir et se lier aux protéines et à l’ADN, comme en témoigne leur utilisation opérationnelle comme colorants de laboratoire. À l’aide de la boîte à outils QSAR de l’OCDE pour la classification du mode d’action, les triarylméthanes ont été classés comme « réactifs, sans précision ». De plus, les résultats du modèle de liaison AR de ToxCast indiquent un risque d’effets de type endocrinien. Cependant, aucune donnée empirique montrant de tels effets n’était disponible. La toxicité aiguë du Basic Violet 3 et du Malachite Green pour divers organismes aquatiques est bien documentée et il a été montré que ces substances peuvent causer des effets nocifs sur les organismes aquatiques à de faibles concentrations (µg/L). Les organismes les plus sensibles semblent être les poissons d’eau douce.
Selon les informations communiquées en réponse aux enquêtes menées en vertu de l’article 71 de la LCPE, ces triarylméthanes sont principalement utilisés dans la teinture du papier, des encres et des encres en poudre, et sont formulés pour être utilisés dans une large gamme de produits de consommation et à usage commercial. Bien qu’il n’existe pas d’information sur leurs concentrations dans l’environnement canadien, les valeurs CEE ont été calculées pour des scénarios d’exposition pertinents en fonction de leurs utilisations. D’après la comparaison des CEE avec les CESE pour les quatre colorants non sulfonés (Basic Violet 3, Malachite Green, Basic Violet 4 et Basic Blue 7), les résultats des scénarios de teinture et de désencrage du papier indiquent que ces substances présentent un risque pour les organismes aquatiques.
Le Pigment Blue 61 devrait se comporter davantage comme une particule, comme les autres pigments organiques. Compte tenu de ses propriétés physiques et chimiques, il devrait être persistant dans l’environnement et présenter un faible risque de bioaccumulation dans les organismes aquatiques. Les études de toxicité en milieu aquatique disponibles pour le Pigment Blue 61 et son analogue, le Pigment Blue 56, n’ont révélé aucun effet à des concentrations allant jusqu’à la limite de solubilité dans l’eau, et une étude n’a montré des effets qu’à des concentrations bien supérieures à la limite de solubilité avec l’utilisation d’un émulsifiant. Par conséquent, une CESE en milieu aquatique n’a pu être établie. Cette substance ne devrait pas présenter de risque pour les organismes aquatiques. Il n’y avait pas de données sur les organismes qui vivent dans les sols. Cependant, compte tenu des propriétés des pigments, on s’attend à ce que le Pigment Blue 61 soit adsorbé en particules sur les sols et ne soit probablement pas biodisponible.
Le Brilliant Blue FCF est très soluble dans l’eau et devrait être persistant dans l’environnement. Comme il s’agit d’un anion, il est moins susceptible de se lier aux sédiments ou aux matières organiques, il a un faible risque de bioaccumulation dans les organismes aquatiques et sa toxicité pour les organismes aquatiques peut être atténuée par ses groupes acide sulfonique (voir le tableau 7.1). Cependant, la CESE calculée est inférieure à 1 mg/L, car le facteur d’évaluation utilisé est relativement élevé en raison de l’ensemble limité de données. Les CEE calculées pour les scénarios d’exposition montrent qu’il existe un risque selon les hypothèses utilisées. Cependant, les conditions qui donnent lieu à des QR supérieurs à 1 ne sont pas susceptibles d’être atteintes. Compte tenu de ces renseignements, le Brilliant Blue FCF ne devrait pas présenter un risque pour les organismes aquatiques.
En résumé, l’information évaluée pour les quatre colorants non sulfonés (Basic Violet 3, Malachite Green, Basic Violet 4 et Basic Blue 7) démontre qu’ils pourraient causer des effets nocifs dans l’environnement au Canada, et les renseignements disponibles pour le Pigment Blue 61 et le Brilliant Blue FCF montrent qu’ils présentent un faible potentiel de causer des effets nocifs dans l’environnement au Canada.
Il a également été déterminé que le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7 répondent aux critères de persistance, mais non aux critères de bioaccumulation, énoncés dans le Règlement sur la persistance et la bioaccumulation, pris en vertu de la LCPE.
7.3.4 Sensibilité de la conclusion à l’égard des principales incertitudes
Aucune donnée sur la toxicité pour les milieux aquatiques n’a été trouvée pour le Basic Violet 4 ou le Basic Blue 7, et les données disponibles pour le Basic Violet 3 indiquent que les effets nocifs peuvent se produire à des concentrations légèrement supérieures à celles du Malachite Green. Les propriétés chimiques semblables de ces quatre substances justifient l’utilisation d’une approche par extrapolation pour établir la toxicité pour les organismes aquatiques, et le risque d’effets nocifs du Malachite Green pour les organismes aquatiques est bien documenté. Par conséquent, des études empiriques supplémentaires de toxicité pour les autres substances ne modifieraient probablement pas la conclusion. Bien que les données sur la bioaccumulation de ces quatre colorants soient limitées, les résultats modélisés, ainsi que leurs propriétés physico-chimiques, corroborent le faible risque prévu de bioaccumulation de ces substances dans les organismes aquatiques. Des renseignements supplémentaires sur le risque de bioaccumulation auraient également une faible incidence sur la conclusion.
Il subsiste une incertitude quant au risque que ces substances aient des effets chroniques sur la reproduction ou le développement des espèces aquatiques, et quant aux concentrations auxquelles ces effets se produiraient. Bien qu’il existe des données indiquant que certains colorants de triarylméthane se lient aux protéines et à l’ADN, on ne sait pas si cela pourrait avoir des effets sur la reproduction ou le développement, et on ne disposait pas de données empiriques sur ces types d’effets pour les organismes aquatiques. La discussion sur la toxicité du Malachite Green pour le développement des mammifères figure à la section 8.2 de la présente évaluation. Étant donné le mécanisme pouvant causer des effets sur le développement des mammifères, il serait raisonnable de s’attendre à des effets semblables chez d’autres types d’organismes. Cette incertitude est toutefois atténuée par l’utilisation de facteurs d’évaluation supplémentaires dans le calcul des CESE afin de tenir compte du mode d’action réactif de ces colorants de triarylméthane. La disponibilité d’études empiriques sur la toxicité de ces substances pour le développement des organismes aquatiques permettrait d’affiner les CESE.
Les scénarios d’exposition indiqués pour les triarylméthanes sont élaborés d’après les renseignements obtenus lors des enquêtes menées en vertu de l’article 71 de la LCPE, du suivi auprès des intéressés et des données provenant de la littérature. Faute de données précises, des hypothèses réalistes sont formulées afin de calculer les CEE. Pour les scénarios de teinture et de désencrage du papier, la confiance à l’égard des CEE pourrait augmenter si on disposait de données plus détaillées sur la masse de teinture utilisée dans les installations, les taux d’utilisation des substances et les facteurs d’émission. En particulier, pour le scénario de désencrage, on pourrait ajuster ce scénario si on connaissait mieux la façon dont les usines de recyclage du papier filtrent leurs matières premières (pour estimer la masse de la substance) et si on avait des données plus fiables sur les facteurs d’émission pour les colorants à base d’eau utilisés dans les encres. Une connaissance plus détaillée de ces facteurs aurait une incidence sur ces scénarios, car on pourrait ainsi mieux comprendre comment l’exposition est considérablement réduite. Cependant, les données actuelles sont suffisantes pour soutenir la conclusion selon laquelle il existe un risque d’effets nocifs dans l’environnement résultant de l’utilisation des colorants de triarylméthane non sulfonés dans la teinture du papier et les encres.
8. Risque de causer des effets nocifs sur la santé humaine
8.1 Évaluation de l’exposition
L’exposition potentielle aux triarylméthanes par les milieux naturels, les aliments et les produits de consommation est traitée dans la présente section. Pour chaque substance, des scénarios d’exposition se traduisant par les expositions les plus élevées ont été choisis afin de caractériser le risque.
Milieux environnementaux
Les triarylméthanes n’ont été ni trouvés ni mesurés dans aucun milieu naturel au Canada.
Les utilisations des triarylméthanes sont fondées sur des renseignements présentés conformément à un avis émis en vertu de l’article 71 de la LCPE (Environnement Canada 2009, 2013), les renseignements sur les produits fournis à Santé Canada et les données accessibles au public. Les renseignements indiquent que les rejets de ces substances dans l’environnement canadien peuvent résulter de l’utilisation par les consommateurs de produits contenant ces substances (c.‑à‑d. rejets à l’égout) et de divers procédés industriels. Comme il est décrit à la section Évaluation de l’exposition dans l’environnement (section 7.2), on s’attend à ce que les rejets aient principalement lieu aux STEU, mais les technologies de traitement peuvent ne dégrader que partiellement ces substances, dont une partie se retrouvera dans les biosolides. Par conséquent, les rejets environnementaux de ces substances pourraient contribuer à l’exposition de la population générale par l’eau potable. On s’attend à ce que le Brilliant Blue FCF contribue potentiellement à l’exposition de la population générale par l’eau potable en raison des rejets de produits de consommation à l’égout, alors que l’utilisation des autres substances au Canada ne devrait pas occasionner de tels rejets, en raison de l’utilisation limitée ou nulle de ces substances dans des produits de consommation qui pourraient être versés ou lessivés à l’égout. De plus, on s’attend à ce que l’utilisation des cinq colorants au Canada pourrait contribuer à l’exposition par l’eau potable en raison de rejets industriels (p. ex., teinture du papier, désencrage du papier et formulation générale des produits, comme il est indiqué à la section 7.2).
Étant donné l’absence de données sur les eaux de surface ou l’eau potable pour les triarylméthanes au Canada ou ailleurs, les concentrations théoriques de chaque colorant à base de triarylméthane dans les eaux de surface, utilisées comme substitut de l’eau potable, ont été calculées à partir des distributions prévues des CEE à la section 7.2. La distribution des CEE dans les scénarios pour les produits industriels et de consommation potentiels pour les colorants de triarylméthane non sulfonés et le Brilliant Blue FCF a été examinée, le cas échéant.
Les plages de CEE décrites à la section 7.2 pour chacun des quatre scénarios de rejets représentent les concentrations potentielles de colorants de triarylméthane dans un plan d’eau récepteur près du point de rejet d’un STEU. Il est probable que ces scénarios, qui ont été élaborés afin d’évaluer l’exposition dans l’environnement, seraient trop prudents dans le contexte de l’évaluation de l’exposition par l’eau potable, qui devrait se produire en aval plutôt qu’au point de rejet. L’un des principaux paramètres d’entrée dans les scénarios de la section 7.2 était l’application d’un plafond de 10 au facteur de dilution. Cependant, l’utilisation d’un tel plafond ne serait pas nécessairement représentative d’un scénario réaliste pour évaluer l’exposition par l’eau potable plus en aval et pourrait donner lieu à une surestimation de la concentration de chacune des substances qui pourraient être présentes dans l’eau potable. Par conséquent, les CEE au 50e centile pour les scénarios de teinture du papier, de désencrage du papier et de formulation générale des produits ont été sélectionnées (c.‑à‑d. plutôt que la borne supérieure des plages décrites à la section 7.2). Ces scénarios sont jugés plus réalistes pour ce qui est d’évaluer l’exposition par l’eau potable, tout en demeurant prudents.
On a utilisé la CEE au 50e centile pour la concentration estimée du Brilliant Blue FCF dans les eaux de surface due aux rejets de produits de consommation.
On a calculé l’estimation théorique de la consommation d’eau potable chez les nourrissons nourris au lait maternisé (0 à 6 mois). Les concentrations résultantes dans les eaux de surface et les estimations théoriques de la consommation pour ce qui est des colorants de triarylméthane dans l’eau potable sont présentées dans le tableau 8‑1. Les concentrations théoriques n’ont pas été estimées pour le pigment dans ce groupe de triarylméthanes, à savoir le Pigment Blue 61, car on ne s’attend pas à ce qu’il se répartisse dans l’eau.
| Scénario d’exposition | Concentration dans les eaux de surface, décrite à la section 7.2 (mg/L) | Exposition par les rejets dans l’environnement des nourrissons nourris au lait maternisé (mg/kg p.c./j) b |
|---|---|---|
| Teinture du papier (colorants de triarylméthane non sulfonés) a | 3,2 × 10-4 (50e centile) | 3,4 × 10-5 |
| Teinture du papier (Brilliant Blue FCF) | 1 × 10-3 (50e centile) | 2,2 × 10-4 |
| Désencrage du papier (colorants de triarylméthane non sulfonés) a | 9,5 × 10-4 (50e centile) | 1,0 × 10-4 |
| Désencrage du papier (Brilliant Blue FCF) | 3,7 × 10-4 (50e centile) | 3,2 × 10-5 |
| Utilisation générale comme produit de formulation (colorants de triarylméthane non sulfonés) a | 2,1 × 10-4 (50e centile) | 2,2 × 10-5 |
| Produits de consommation (Brilliant Blue FCF) | 4,0 × 10-5 (50e centile) | 4,3 × 10-6 |
Abréviation : S.O. = Sans objet
a Colorants de triarylméthane non sulfonés = Basic Violet 3, Malachite Green, Basic Violet 4 et Basic Blue 7.
b Une consommation d’eau potable de 0,8 L/j et un poids corporel de 7,5 kg ont été utilisés (Santé Canada 1998).
Pour estimer le risque de cancer dû à l’exposition quotidienne au Basic Violet 3, une dose quotidienne moyenne à vie (DQMV) a été calculée (annexe C). L’apport d’eau potable et les poids corporels de Santé Canada (1998) ont été utilisés pour les nourrissons nourris au lait maternisé, les tout-petits, les enfants, les adolescents et les adultes. La DQMV pour l’ingestion journalière de Basic Violet 3 par l’eau potable a été estimée à 2,3 × 10-5 mg/kg p.c./j (pour le scénario de désencrage du papier, car il représente l’exposition la plus élevée). Comme d’autres valeurs d’exposition ont été établies pour le Malachite Green, le Basic Violet 4, le Basic Blue 7 et le Brilliant Blue FCF et qu’elles étaient plus élevées que celles que l’on retrouve dans les milieux naturels, la DQMV n’a pas été calculée pour ces substances.
Pour ce qui est du Pigment Blue 61, on ne s’attend pas à ce que l’exposition à cette substance par les milieux naturels se produise, en raison de divers facteurs : ses quantités commerciales limitées au Canada, sa volatilité négligeable, sa très faible solubilité dans l’eau, et son élimination prévue par les systèmes de traitement des eaux.
Aliments
À l’exception du Brilliant Blue FCF, les triarylméthanes n’ont pas été signalés dans les aliments. Selon le JECFA, le Basic Violet 3 et le Malachite Green peuvent être présents dans les sous-produits des animaux, les viandes ou les poissons sous forme de résidus, en raison de leur utilisation continue dans les médicaments vétérinaires et en aquaculture (EFSA 2016; JECFA 2009, 2014). L’utilisation d’aucune de ces substances n’est actuellement approuvée pour les animaux aquatiques destinés à la consommation humaine et dans les aliments du bétail au Canada (ACIA 2015; Santé Canada [modifié, 2010]). L’exposition de la population générale à des quantités trace de ces substances dans les aliments, en raison d’utilisation non conforme, ou dans du poisson importé n’a pas été jugée préoccupante pour la santé des consommateurs (ACIA 2012; communication personnelle, courriel du Bureau de la gestion du risque, Santé Canada, au Bureau d’évaluation du risque des substances existantes, Santé Canada, 2016; sans référence). Trois substances (Basic Violet 3, Pigment Blue 61 et Brilliant Blue FCF) peuvent être utilisées dans des matériaux d’emballage alimentaire qui entrent en contact avec les aliments. Le Brilliant Blue FCF peut également être présent dans les additifs indirects (p. ex., nettoyants et détergents à vaisselle) utilisés dans les usines de transformation des aliments. L’exposition à ces substances due à leur présence dans les emballages alimentaires ou comme composant d’un additif indirect (p. ex., dans les procédés de transformation des aliments) devrait être négligeable (communication personnelle, courriels de la Direction des aliments, Santé Canada, au Bureau d’évaluation du risque des substances existantes, Santé Canada, 2016-2017, 2019; sans référence).
Au Canada, l’utilisation du Brilliant Blue FCF est permise comme additif alimentaire dans un certain nombre d’aliments, à une concentration maximale de 100 ppm, isolément, ou en combinaison avec du vert solide FCF conformément au point 4 de la Liste des colorants autorisés (Liste des additifs alimentaires autorisés) (Santé Canada [modifié, 2015a]). Son utilisation est également permise dans le fromage feta à une concentration maximale de 0,10 ppm et dans le caviar de lompe à une concentration maximale de 450 ppm conformément aux points 4 et 9), respectivement, de la Liste des colorants autorisés (Liste des additifs alimentaires autorisés) (Santé Canada [modifié, 2015a]). L’exposition au Brilliant Blue FCF par le régime alimentaire a été estimée d’après les concentrations mesurées par l’Agence canadienne d’inspection des aliments dans le cadre de ses enquêtes ciblées sur les colorants alimentaires (ACIA 2010, 2011), et les données sur les composantes du rappel alimentaire de 24 heures, selon l’Enquête sur la santé dans les collectivités canadiennes – Cycle 2.2, volet Nutrition (Statistique Canada 2004). Lorsqu’il n’y avait pas de données disponibles pour une catégorie particulière d’aliments, la concentration de Brilliant Blue FCF mesurée dans un aliment de couleur similaire a été appliquée. Au 90e centile, l’exposition alimentaire estimée maximale de Brilliant Blue FCF en raison de son utilisation comme additif alimentaire, sur une base de poids corporel, était pour les enfants de 4 à 8 ans, à 330 µg/kg p.c./j (communication personnelle, courriels de la Direction des aliments, Santé Canada, au Bureau d’évaluation du risque des substances existantes, Santé Canada, 2016- 2017; sans référence).
Compte tenu des renseignements ci-dessus, l’exposition potentielle de la population générale au Brilliant Blue FCF, en raison de la consommation d’aliments et d’eau potable, devrait être beaucoup plus faible que l’exposition potentielle par l’utilisation des produits de consommation. L’exposition au Basic Violet 3 et au Pigment Blue 61 par les aliments et l’emballage alimentaire au Canada devrait être négligeable. On s’attend à ce que l’exposition aux trois autres substances du groupe des triarylméthanes par les aliments au Canada soit nulle.
Produits disponibles aux consommateurs
L’exposition due à l’utilisation de produits disponibles aux consommateurs contenant des triarylméthanes a été évaluée. Les scénarios pour ces produits qui donnent lieu à l’exposition potentielle maximale pour chaque substance par voie orale, par voie cutanée et par inhalation sont présentés dans les tableaux 8‑2, 8‑3 et 8‑4, respectivement. Dans chaque cas, l’exposition potentielle a été estimée d’après des hypothèses prudentes et à l’aide de valeurs par défaut provenant de scénarios d’exposition d’organismes sentinelles (voir l’annexe C pour de plus amples détails).
Pour estimer le risque de cancer, on a utilisé l’exposition générale quotidienne par groupe d’âge, sauf lorsqu’une moyenne pour la durée de la vie était requise (voir la section 8.3, Caractérisation des risques pour la santé humaine). Dans le cas des scénarios pour lesquels un tel ajustement était requis, les DQMV ont été calculées.
| Substance | Scénario pour le produit | Groupe d’âge | Exposition générale par événement (mg/kg p.c.) | Exposition générale quotidienne (mg/kg p.c./j) |
|---|---|---|---|---|
| Brilliant blue FCF | Utilisation non médicinale dans un produit de santé naturel | Adulte | S.O. | 2,82 |
Abréviation : S.O. = sans objet.
L’utilisation déclarée du Basic Violet 3 comme pigment (ou dans un pigment) dans les produits en papier, les mélanges ou les articles fabriqués est restreinte aux applications commerciales au Canada. L’utilisation déclarée du malachhite green comme colorant dans l’encre, l’encre en poudre et les colorants est également limitée à des applications commerciales, et son utilisation déclarée dans les produits de papier, les mélanges et les articles manufacturés ne devrait pas entraîner d’exposition par voie orale. Par conséquent, l’exposition potentielle par voie orale à ces substances, via les produits disponibles aux consommateurs, n’est pas prévue. De même, étant donné son utilisation déclarée comme pigment dans les encres d’impression et qui est restreinte aux applications commerciales au Canada, on ne s’attend pas non plus à une exposition potentielle par voie orale au Pigment Blue 61 par les produits utilisés par les consommateurs.
Pour ce qui est de l’exposition potentielle estimée par la voie cutanée, on a utilisé l’approche du flux maximal (Jmax) (Williams et coll. 2016) pour le Malachite Green, le Basic Violet 4 et le Basic Blue 7 afin de caractériser de façon détaillée les doses systémiques (voir l’annexe C). Une étude du flux cutané réalisée par Lucová et coll. (2013) a montré que la pénétration cutanée du Brilliant Blue FCF dans une émulsion d’huile dans l’eau est pratiquement négligeable. Dans cette étude, la quantité cumulative de Brilliant Blue FCF.00 (émulsion d’huile dans l’eau) absorbé dans l’épiderme et appliqué sur un échantillon ex vivo de peau d’oreille porcine intacte et de pleine épaisseur (1 ± 0,07 mm) à une charge cutanée de 250 ng/cm2 pendant 24 heures, est de 14 ng/cm2 (avec un écart-type de 3 ng/cm2). Toute quantité de Brilliant Blue FCF qui aurait pu être présente dans le fluide récepteur ou dans le derme était en deçà de la limite de quantification. Comme la couche cornée n’était pas séparée de l’épiderme viable, la quantité totale absorbée dans l’épiderme de 17 ng/cm2 (14 ng/cm2 plus 1 écart-type) a été utilisée de façon prudente afin d’estimer l’absorption cutanée de Brilliant Blue FCF dans cette évaluation. Une étude d’absorption percutanée in vitro de Brilliant Blue FCF a également été trouvée (SCCNFP 2004), qui a également démontré qu’il n’y avait pas de perméation mesurable au travers de la peau (c.‑à‑d. jusque dans le fluide récepteur), mais a estimé de manière prudente une absorption potentielle maximale de 6,2 µg/cm2 pour une préparation de gel capillaire colorant et de 35,2 µg/cm2 pour le colorant pur, d’après la limite de détection et les résidus liés à la peau. Sur la base de considérations relatives à la formulation, l’étude de Lucová et coll. (2013) a été jugée plus pertinente pour le scénario de crème pour le corps, et a donc été utilisée.
| Substance | Scénario pour le produit | Groupe d’âge | Exposition générale par événement (mg/kg p.c.) | Exposition générale quotidienne (mg/kg p.c./j) |
|---|---|---|---|---|
| Malachite green | Colorants capillaires (semi-permanents) | Adolescent | 0,337 | 0,0033 |
| Malachite green | Colorants capillaires (semi-permanents) | Adulte | 0,282 | 0,0102 |
| Basic violet 4 | Colorants capillaires (semi-permanents) | Adolescent | 0,0589 | 0,00058 |
| Basic violet 4 | Colorants capillaires (semi-permanents) | Adulte | 0,0494 | 0,00178 |
| Basic blue 7 | Colorants capillaires (semi-permanents) | Adolescent | 0,0177 | 0,000175 |
| Basic blue 7 | Colorants capillaires (semi-permanents) | Adulte | 0,0148 | 0,000533 |
| Brilliant blue FCF | Crème pour le corps | Nourrisson | S.O. | 0,0068 |
| Brilliant blue FCF | Crème pour le corps | Adulte | S.O. | 0,0041 |
Abréviation : S.O. = sans objet.
Afin d’estimer le risque de cancer dû à une exposition cutanée intermittente par événement, une DQMV de 0,00134 mg/kg p.c./j a été calculée pour le Basic Violet 4 dans les colorants capillaires utilisés par les adolescents et les adultes. Pour tous les autres scénarios d’exposition cutanée pour lesquels le risque de cancer a été estimé, on a utilisé l’exposition générale quotidienne par groupe d’âge (voir la section 8.3, Caractérisation des risques pour la santé humaine).
Bien qu’il puisse y avoir un contact cutané avec le Pigment Blue 61 présent dans les encres d’impression, la solubilité de ce pigment est très faible et par conséquent il ne se solubilise pas facilement dans la sueur (BfR 2007). Par conséquent, il ne traverse pas facilement la peau intacte et par conséquent une exposition générale n’est pas prévue. De même, le contact cutané potentiel avec le Basic Violet 3, d’après son utilisation déclarée comme pigment (ou utilisée dans les pigments) des produits en papier, des mélanges ou des articles fabriqués, ne devrait pas donner lieu à une exposition générale. On ne s’attend pas à la migration de la substance du papier, dans lequel elle est un pigment, à l’encre (p. ex., encre d’impression) et son absorption subséquente par la peau intacte. Les pigments utilisés dans les encres d’imprimerie sont fréquemment des colorants (p. ex., le Basic Violet 3) rendus insolubles par leur complexion avec un ion métal (IARC 1996). De plus, l’exposition générale au Basic Violet 3 en raison de son utilisation comme colorant du papier ne serait pas prévue, car on s’attendrait à ce que les colorants contenus dans la matrice du papier présentent une migration minimale dans un scénario d’exposition cutanée.
L’exposition estimée au Brilliant Blue FCF contenu dans les parfums en aérosol est présentée ci-dessous.
| Substance | Scénario pour le produit | Groupe d’âge | Exposition générale par événement (mg/kg p.c.) | Exposition générale quotidienne (mg/kg p.c./j) |
|---|---|---|---|---|
| Brilliant blue FCF | Parfum | Adolescent | S.O. | 0,00064 |
| Brilliant blue FCF | Parfum | Adulte | S.O. | 0,00054 |
Abréviation : S.O. = sans objet
En raison de la très faible pression de vapeur (10-13 mm Hg ou moins, à 25 °C) des six membres du groupe des triarylméthanes, toute exposition potentielle à des produits non en aérosol, par inhalation, a été jugée limitée.
8.2 Évaluation des effets sur la santé
Il y avait peu de données sur les dangers particuliers de quelques triarylméthanes. On a donc examiné des analogues d’après la similarité de leurs propriétés physiques et chimiques, de leur métabolisme et de leur structure. Les données sur les substances chimiques seront présentées d’abord, suivies des données sur les analogues qui ont été utilisées pour mieux comprendre la caractérisation des effets des triarylméthanes sur la santé.
Basic violet 3
La toxicité du Basic Violet 3 a été examinée par le JECFA (2014) et par Diamante et coll. (2009). La Commission européenne (CE) a classé le Basic Violet 3 comme substance cancérogène 2 (ou 1B si la concentration en cétones de Michler est égale ou supérieure à 0,1 %) (CE 2008). Chez le rat ou la souris, le Basic Violet 3 administré par gavage unique ou sur une base quotidienne pendant une semaine à raison de 4 à 7 mg/kg p.c.(/j) a été rapidement absorbé, mais mal, puis distribué essentiellement dans le gras, le foie, les reins et, dans une moindre mesure, dans les muscles, les ovaires et les testicules (McDonald et coll. 1984; McDonald 1989). Il est métabolisé par réduction et déméthylation, et les métabolites principalement réduits comme la leucoviolet du Basic Violet 3 sont présents dans les tissus (McDonald et Cerniglia 1984; McDonald 1989). Le Basic Violet 3 a été principalement (66 % à 73 %) éliminé dans les matières fécales, et dans une moindre mesure dans l’urine (moins de 8 %) (McDonald et coll. 1984; McDonald 1989; Docampo et Moreno 1990). La toxicité du Basic Violet 3 pour le développement a été évaluée chez le lapin et le rat. Chez des lapines gavées aux jours de gestation (JG) 6 à 19 à raison de 0, 0,5, 1 ou 2 mg/kg p.c./j de Basic Violet 3, et sacrifiés au JG 30, à la dose minimale entraînant un effet nocif observé (DMENO) de 0,5 mg/kg p.c./j, on a constaté une diminution du poids corporel des fœtus et de la toxicité maternelle (mortalité accrue, diminution du poids corporel et de la prise de poids corporel, signes cliniques comme la respiration sifflante, la diarrhée et la congestion) (NTP 1983). Aucune dose sans effet nocif observé (DSENO) n’a été déterminée, car elle était la plus faible dose d’essai (JECFA, 2014). En comparaison, aucun effet n’a été observé à la plus faible dose d’essai de 2,5 mg/kg p.c./j chez les rats l’ayant reçue par gavage aux JG 6 à 15 et sacrifiés au JG 20 (NTP 1982). La toxicité maternelle (signes cliniques de toxicité et diminution de la prise de poids corporel) a été observée seulement à la dose de 5 mg/kg p.c./j, avec une toxicité pour le développement (fréquence accrue de la 13e côte raccourcie, hydronéphrose et urétérohydrose) observée à 10 mg/kg p.c./j (NTP 1982).
Dans une étude de toxicité pour la reproduction sur trois générations chez le rat exposé au Basic Violet 3 par le régime alimentaire, aucun effet sur la reproduction n’a été observé jusqu’à la dose d’essai maximale de 30 mg/kg p.c./j (Littlefield 1988). Les parents ont été exposés à 0, 5, 15 ou 30 mg/kg p.c./j pendant 80 jours avant l’exposition préaccouplement, puis on a procédé à deux accouplements pour produire les portées F1a et b. Les rats F1a (2/sexe/portée) ont été utilisés pour l’étude de cancérogénicité chronique (Littlefield et coll. 1989). Les rats F1b (1/sexe/portée) ont ensuite été accouplés après 100 à 140 jours pour produire les portées F2a, et cet accouplement a été répété pour produire les portées F2b, qui ont, de la même façon, produit les portées F3a. La DSENO parentale était de 15 mg/kg p.c./j d’après une diminution du poids corporel à 30 mg/kg p.c./j (Littlefield 1988). Aucune DSENO n’a été établie pour les descendants en raison de la dilatation focale accrue du cortex et des tubules rénaux et de la nécrose du thymus chez les animaux sevrés F3a (2/sexe/portée) à la DMENO de 5 mg/kg p.c./j et au-delà (Littlefield 1988). Dans des études par le régime alimentaire sur 13 semaines, on a également constaté une légère diminution du poids corporel chez les rats ayant reçu 25 mg/kg p.c./j et une augmentation du poids du foie chez des chiens ayant reçu jusqu’à 16 mg/kg p.c./j, les deux doses ayant été les doses maximales d’essai (Littlefield et coll. 1989).
Les résultats des études de génotoxicité du Basic Violet 3 ont été mitigés, mais dans l’ensemble, on a jugé la substance génotoxique in vitro, d’après les résultats positifs aux essais de mutation cellulaire (Aidoo et coll. 1990), d’aberration chromosomique (Au et coll. 1978, Au et Hsu 1979) et de liaison et de réparation de l’ADN (Müller et Gautier 1975, Wakelin et coll. 1981) examinés dans Mani et Bharagava (2016). Par contre, le Basic Violet 3 n’a pas eu d’effet sur la fréquence des aberrations chromosomiques chez la souris exposée par l’eau potable à une dose allant jusqu’à 8 mg/kg p.c./j pendant un mois, ni causé de lésions à l’ADN des lymphocytes de la rate chez la souris exposée à une dose allant jusqu’à 6 mg/kg p.c. par voie intraveineuse pendant une heure (Au et Hsu 1979; Aidoo et coll. 1990). Dans une étude de cancérogénicité de 2 ans chez des souris ayant reçu environ 0, 11/14, 32/36 et 64/71 mg/kg p.c./j (mâles/femelles), le Basic Violet 3 avait accéléré l’érythropoïèse dans la rate et causé l’atrophie des ovaires chez les femelles à la plus faible dose d’essai de 14,3 mg/kg p.c./j (Littlefield 1984; Littlefield et coll. 1985). À la dose d’environ 36 mg/kg p.c./j et plus, on a observé une augmentation des adénomes et carcinomes hépatiques chez les femelles, et chez les mâles à la dose de 64 mg/kg p.c./j, ainsi qu’une mortalité accrue chez les femelles. Dans une étude de cancérogénicité de deux ans chez le rat exposé au Basic Violet 3 par le régime alimentaire, aucun effet nocif n’a été observé à la plus faible dose d’essai de 30/40 mg/kg p.c./j (mâles/femelles). À la DMENO de 80/100 mg/kg p.c./j (mâles/femelles), on a constaté une mortalité accrue (mâles) et une augmentation des adénomes des cellules folliculaires de la thyroïde (femelles), ainsi que des adénomes hépatocellulaires chez les deux sexes (Littlefield et coll. 1989).
La fréquence des carcinomes hépatocellulaires chez les souris femelles de 2 ans était de 7/185, 5/93, 30/93 ou 73/95 pour 0, 14, 36 ou 71 mg/kg p.c./j, respectivement. La relation dose-réponse pour les deux types de tumeurs était similaire (la fréquence des adénomes hépatocellulaires chez les souris femelles à 2 ans était de 8/185, 8/93, 36/93, 20/95 pour 0, 14, 36 ou 71 mg/kg p.c./j, respectivement) (JECFA 2014). Afin de déterminer le risque accru de développer un carcinome hépatocellulaire, le JECFA (2014) a utilisé le logiciel de détermination de la dose de référence de l’EPA des États‑Unis (BMDS, version 2.2) pour établir que l’utilisation du modèle à plusieurs stades donnait un ajustement acceptable, présentait la plus faible valeur du critère d’information d’Akaike, et avait la plus faible valeur de doses repères pour le risque supplémentaire de 10 % (19,9 mg/kg p.c./j) et une dose de référence (DR) plus faible que la limite de confiance de 95 % pour le risque supplémentaire de 10 % (DR10 de 16,8 mg/kg p.c./j), parmi les modèles.
Malachite green
Le Malachite Green a été étudié dans le cadre d’une étude de cancérogénicité du programme NTP (2005) et par l’EFSA (2016). Lorsque des rats ou des souris ont reçu 5 ou 30 mg/kg p.c./j de Malachite Green pendant 1 mois, cette substance était demeurée essentiellement non métabolisée dans le foie, mais réduite en leucobase du Malachite Green, et dans une moindre mesure, en mono et didesméthyl du Malachite Green ou mono et didesméthylleucobase du Malachite Green (Culp et coll. 1999). On a considéré que l’oxalate de vert de malachite était un analogue du Malachite Green, d’après les similarités physico-chimiques et structurales (p. ex., la structure de l’oxalate de vert de malachite est identique à celle du Malachite Green, sauf que le fragment anionique du sel est l’oxalate plutôt que le chlorure). Dans une étude sur le développement de lapins ayant été gavés avec 0, 5, 10 ou 20 mg/kg p.c./j d’oxalate de vert de malachite aux JG 6 à 18 et sacrifiés au JG 30, la DSENO maternelle était de 5 mg/kg p.c./j (Meyer et Jorgenson 1983). À la dose de 10 mg/kg p.c./j, la consommation d’aliments, le poids corporel et la prise de poids corporel ont diminué chez les mères. À la dose de 5 mg/kg p.c./j et plus, on a observé une augmentation des pertes avant implantation, une augmentation des résorptions fœtales précoces, une diminution de la survie fœtale, une baisse du poids corporel des fœtus et une augmentation des écarts squelettiques. Bien que cette étude sur le développement des lapins avec l’oxalate de vert de malachite comportait des limites (p. ex. un nombre inconnu de cas d’altération du développement par portée) et l’absence d’une relation dose-effet nette chez les fœtus, des effets nocifs sur le développement ont été observés à la dose d’essai la plus faible. Selon cette étude, le Malachite Green devrait avoir des effets sur le développement à 5 mg/kg p.c./j, d’après l’augmentation des pertes avant implantation, l’augmentation des résorptions fœtales précoces, la diminution de la survie fœtale, la diminution du poids corporel des fœtus et l’augmentation des écarts squelettiques à la plus faible dose d’essai, soit 5 mg/kg p.c./j.
Le Malachite Green n’était pas génotoxique in vitro dans les essais de mutation cellulaire, le test d’aberration chromosomique et le test des comètes (Au et Hsu 1979; Ferguson et Baguley 1988; Panandiker et coll. 1994; Fessard 1999; NTP 2004; Bose et coll. 2005; Stammati et coll. 2005). D’autre part, il a également inhibé la réplication de l’ADN catalysée par la polymérase I, a induit des ruptures d’ADN sur un seul brin et s’est révélé cytotoxique in vitro (Wolfe 1977; Panandiker et coll. 1994; Stammati et coll. 2005). On a observé des signes mixtes de génotoxicité in vivo, avec micronoyaux négatifs, sur gènes mutants Hprt ou cII chez des souris ayant reçu 0 ou 43 mg/kg p.c./j pendant quatre ou six semaines (Mittelstaedt et coll. 2004), mais on a constaté des signes d’aberrations chromosomiques, de fragmentation de l’ADN, d’échange de chromatides sœurs et de formation d’adduits à l’ADN chez des souris ou des rats gavés ou nourris avec environ 4 à 78 mg/kg p.c./j de Malachite Green pendant quatre semaines (Culp et coll. 1999; Donya et coll. 2012; Kasem et coll. 2016).
Dans une étude de cancérogénicité par le régime alimentaire de 2 ans chez des souris femelles, aucune toxicité générale ou tumeur n’a été observée jusqu’à la dose d’essai maximale de 67 mg/kg p.c./j de Malachite Green (NTP 2005). Par contre, des rats femelles ayant reçu 0, 7, 21 ou 43 mg/kg p.c./j de Malachite Green pendant 2 ans ont présenté une DSENO de 7 mg/kg p.c./j, d’après une diminution de 9 % du poids corporel et une légère augmentation des tumeurs à la DMENO de 21 mg/kg p.c./j et plus (NTP 2005). La présence d’adénomes et de carcinomes des cellules folliculaires de la thyroïde [fréquence combinée : 0/46, 0/48, 3/47 (6 %), 2/46 chez les témoins aux doses élevées, respectivement, avec une plage historique pour les témoins jusqu’à 3 %], et des adénomes hépatocellulaires [1/48, 1/48, 3/48 (6 %), 4/48 chez les témoins aux doses élevées, respectivement, avec une plage historique pour les témoins jusqu’à 0,6 %] a été corroborée pour les deux par de légers changements non néoplasiques (follicules kystiques dans la glande thyroïde, foyers d’éosinophiles dans le foie) à la DMENO de 21 mg/kg p.c./j (NTP 2005). À la dose de 43 mg/kg p.c./j, on a observé une légère augmentation des carcinomes des glandes mammaires [2/48, 2/48, 1/48, 5/48 (10 %) pour les témoins aux doses élevées, respectivement, plage historique pour les témoins jusqu’à 4 %] et une augmentation du poids relatif du foie chez les rats femelles. Aucune variation des hormones thyroïdiennes n’a été observée dans une étude satellite de 21 jours chez des rats ayant reçu 60 mg/kg p.c./j de Malachite Green (NTP 2005). Dans une étude par voie orale de quatre mois chez le rat, les foyers d’éosinophiles hépatocellulaires accrus, obtenus avec 13 mg/kg p.c./j de Malachite Green dans l’eau potable, ont été transformés en carcinomes hépatocellulaires par une induction à la diéthylnitrosamine, et s’accompagnaient d’une augmentation du poids relatif du foie et de changements du cycle cellulaire (Sundarrajan et coll. 2000). Le NTP considère qu’il existe des preuves équivoques de cancérogénicité chez les rats femelles, d’après l’augmentation des tumeurs thyroïdiennes combinées et l’augmentation marginale des adénomes hépatocellulaires et des carcinomes de la glande mammaire.
Pigment blue 61
On n’a pas jugé que le Pigment Blue 61 présente un risque élevé pour la santé humaine, d’après les classifications faites par d’autres organismes nationaux ou internationaux en ce qui concerne sa cancérogénicité, sa génotoxicité, sa toxicité pour le développement ou pour la reproduction. Il n’est pas non plus inscrit sur la Liste des substances extrêmement préoccupantes candidates en vue d’une autorisation de l’Agence européenne de produits chimiques (ECHA [modifié, 2016]). Des études plus poussées sur ses effets sur la santé ne sont pas nécessaires en ce moment, car la population générale du Canada devrait y être faiblement exposée.
Basic violet 4
Le Basic Violet 4 n’était pas génotoxique dans des essais in vitro de mutation inverse sur des bactéries, ni dans un essai de mutation génique sur des cellules de mammifères (cellules L5178Y de lymphomes de souris) (Seifried et coll. 2006). La toxicité du Basic Violet 4 a été déterminée au moyen de son analogue, l’acétate de violet d’éthyle (no CAS 63157-72-2) (ECHA c2007-2017b). Tout comme dans le cas du Malachite Green et de son analogue, l’oxalate de vert de malachite, la structure de l’acétate de violet d’éthyle est identique à celle du Basic Violet 4, sauf que le fragment anionique du sel est l’acétate au lieu du chlorure. Lorsqu’aucune donnée sur l’acétate de violet d’éthyle n’était disponible, le Basic Violet 3 a également été utilisé comme analogue, car il est lui aussi similaire au Basic Violet 4 en ce qui concerne les propriétés physico-chimiques et la structure chimique.
Dans une étude de la toxicité de l’acétate de violet d’éthyle sur le développement, on n’a constaté aucun effet maternel ou sur le développement jusqu’à la dose d’essai maximale de 12 mg/kg p.c./j chez le rat (ECHA c2007-2017b). Ces résultats concordaient avec ceux d’une étude par gavage de quatre semaines chez le rat, avec l’acétate de violet d’éthyle, dans laquelle aucun effet nocif n’a été observé à 10 mg/kg p.c./j, mais on avait constaté une courbe dose-réponse prononcée, car une toxicité grave a été observée chez les deux sexes entre 20 et 30 mg/kg p.c./j (y compris la mortalité, une diminution du poids corporel et de la prise de poids corporel, une consommation moindre d’aliments et une mauvaise condition générale) (ECHA c2007-2017b).
D’après une étude de toxicité pour la reproduction sur trois générations chez des rats exposés à 0, 5, 15 ou 30 mg/kg p.c./j de Basic Violet 3 par le régime alimentaire (Littlefield 1988), le Basic Violet 4 peut avoir des effets sur les descendants (dilatation focale du cortex et des tubules rénaux, et nécrose du thymus chez les animaux sevrés de la portée F3a) et réduire la prise de poids corporel chez les mères à 5 mg/kg p.c./j, mais on ne prévoit aucun effet sur la reproduction.
D’après la similarité structurale du Basic Violet 3 avec le Basic Violet 4, on suppose qu’il est peu probable que le Basic Violet 4 à une dose allant jusqu’à 6 ou 8 mg/kg p.c.(/j) augmente les aberrations chromosomiques ou endommage l’ADN chez la souris (Au et Hsu 1979; Littlefield et coll. 1985; Aidoo et coll. 1990; Diamante et coll. 2009). Une étude de cancérogénicité de deux ans chez des souris exposées au Basic Violet 3 par voie alimentaire indique que cette substance peut causer une accélération de l’érythropoïèse dans la rate et une atrophie des ovaires chez les femelles à 14 mg/kg p.c./j et plus, et une augmentation des tumeurs hépatocellulaires à 36 mg/kg p.c./j et plus, avec une DR10 de 16,8 mg/kg p.c./j, pour un risque accru de carcinomes hépatocellulaires chez les souris femelles (Littlefield 1984; Littlefield et coll. 1985; JECFA 2014). En plus des similarités dans la structure chimique et les propriétés physico-chimiques du Basic Violet 3 et du Basic Violet 4, l’applicabilité des données du Basic Violet 3 pour caractériser le potentiel cancérogène du Basic Violet 4 était corroborée par les similarités dans leurs profils chimiques et les prévisions du modèle (Q)SAR (Derek Nexus 2016; Leadscope Model Applier 2016; OCDE QSAR Toolbox 2013; Times 2016). De plus, les voies métaboliques prévues par Times (2016) indiquent que le Basic Violet 4 peut subir les mêmes transformations métaboliques que le Basic Violet 3 (Docampo et Moreno 1990), ce qui corrobore la lecture croisée du Basic Violet 3 appliquée au Basic Violet 4, en l’absence d’étude de cancérogénicité propre à cette dernière substance chimique.
Basic blue 7
En l’absence de données sur les dangers propres au Basic Blue 7, la toxicité de cette substance était fondée sur celle d’analogues présentant des similarités physico-chimiques et structurales, le Basic Violet 4 et l’acétate de violet d’éthyle étant plus semblables au Basic Blue 7 que le Basic Blue 26 ou le Basic Violet 3. Sur la base d’une étude de quatre semaines et d’une étude de la toxicité pour le développement chez des rats ayant reçu par gavage de l’acétate de violet d’éthyle, l’administration d’une dose allant jusqu’à 12 mg/kg p.c./j de Basic Blue 7 par gavage ne devrait pas entraîner d’effets nocifs sur le développement, mais une toxicité générale, y compris la mortalité, serait prévue à 20 mg/kg p.c./j et plus (ECHA c2007-2017c). Une dose atteignant 30 mg/kg p.c./j de Basic Blue 7 dans le régime alimentaire ne devrait pas causer d’effet sur la reproduction, d’après une étude sur 3 générations avec le Basic Violet 3 administré à des rats (Littlefield 1988; JECFA 2014). La génotoxicité in vitro et in vivo du Basic Blue 7 devrait être négative, étant donné la génotoxicité négative du Basic Violet 4 in vitro (Seifried et coll. 2006; ECHA c2007-2017b) et du Basic Blue 26 (Nagai 1959; Janik-Spiechowicz et coll. 1997), et la génotoxicité négative in vivo du Basic Violet 3 ou du Basic Blue 26 (Janik-Spiechowicz et coll. 1997). Compte tenu d’une étude de cancérogénicité de 2 ans chez des souris exposées au Basic Violet 3 par voie alimentaire, le Basic Blue 7 devrait accélérer l’érythropoïèse dans la rate et l’atrophie des ovaires chez les femelles à 14 mg/kg p.c./j et plus, et augmenter la fréquence des tumeurs hépatocellulaires à 36 mg/kg p.c./j et plus, avec une DR10 de 16,8 mg/kg p.c./j pour un risque accru de carcinomes hépatocellulaires chez les souris femelles (Littlefield 1984; Littlefield et coll. 1985; JECFA 2014). En plus des similarités dans la structure chimique et les propriétés physico-chimiques du Basic Violet 3 et du Basic Blue 7, l’applicabilité des données du Basic Violet 3 pour caractériser le potentiel cancérogène du Basic Blue 7 a été corroborée par des similarités dans leurs profils chimiques et les prévisions du modèle (Q)SAR (Derek Nexus 2016; Leadscope Model Applier 2016; OCDE QSAR Toolbox 2013; Times 2016). Comme dans le cas du Basic Violet 4, les voies métaboliques prédites par Times (2016) indiquent que le Basic Blue 7 peut subir les mêmes transformations métaboliques que le Basic Violet 3 (Docampo et Moreno 1990), ce qui renforce la lecture croisée du Basic Violet 3 appliquée au Basic Blue 7 en l’absence d’une étude de cancérogénicité propre à cette dernière substance.
Brilliant blue FCF
Le Brilliant Blue FCF a été examiné par le JECFA (1969), l’EFSA (2010) et l’EPA (2013). Il était mal absorbé par voie orale (2 % chez les rats femelles dont les voies biliaires étaient ligaturées) et éliminé presque entièrement (95,5 à 99,99 %), sous forme de composé d’origine dans les matières fécales en trois jours (Brown et coll. 1980; Phillips et coll. 1980; EFSA 2010). Il y a eu deux études sur l’absorption cutanée in vitro du Brilliant Blue FCF, comme il est décrit à la section 8.2 (SCCNFP 2004; Lucová et coll. 2013). Aucun effet nocif n’a été observé chez le rat ayant reçu du Brilliant Blue FCF pendant 75 semaines par le régime alimentaire, ce qui a permis d’établir une DSENO de 1 500 mg/kg p.c./j comme dose d’essai maximale (Mannell et coll. 1962; US EPA 2013). La substance n’était pas mutagène et n’a pas endommagé l’ADN in vitro (Borzelleca et coll. 1990) ni les micronoyaux ou l’ADN chez les souris in vivo (EFSA 2010). Les résultats positifs de génotoxicité in vitro étaient attribuables à la pureté de la matière d’essai (Borzelleca et coll. 1990), ce qui peut également expliquer l’augmentation des micronoyaux dans les lymphocytes humains due au Brilliant Blue FCF in vitro (Kus et Eroglu 2015).
Dans une étude de toxicité pour la reproduction par voie alimentaire de deux ans, avec une phase in utero, chez le rat, on a observé une diminution du poids corporel moyen terminal et du taux de survie chez les femelles à la DMENO de 1 318 mg/kg p.c./j, et à une DSENO de 631 mg/kg p.c./j, sans effet sur la reproduction (Borzelleca et coll. 1990, EFSA 2010, US EPA 2013). La DSENO pour les mâles était de 1 072 mg/kg p.c./j. Conformément à ces résultats, aucun effet sur la reproduction n’a été observé dans une étude de toxicité pour la reproduction sur trois générations par voie alimentaire chez le rat (US EPA 2013), bien qu’il y ait eu une diminution du poids corporel (descendants qui allaitaient et rats F1 et F2 [l’examen de l’EFSA ne donnait pas de détails concernant leur âge]) à la dose d’essai maximale de 1 000 mg/kg p.c./j dans cette étude limitée (Bio/dynamics Inc., 1972, 1973). Dans une étude sur la reproduction et le développement chez les descendants de souris, aucun effet nocif n’a été constaté aux doses de 347 à 1 287 mg/kg p.c./j chez les mâles et les femelles, les indications de neurotoxicité potentielle chez les descendants n’ayant été observées qu’à des doses élevées de 1 032 à 3 856 mg/kg p.c./j (diminution du réflexe de redressement depuis une surface au jour postnatal 4, diminution de l’activité horizontale après 8 semaines et augmentation de l’activité spontanée chez les femelles) (Tanaka et coll. 2012).
Aucune tumeur n’a été observée jusqu’à la dose d’essai maximale de 2 500 mg/kg p.c./j dans des études de 2 ans par le régime alimentaire chez le rat, ou de 7 354/8 966 mg/kg p.c./j (mâles/femelles) chez la souris, études qui étaient limitées par un manque de détails, y compris la description du protocole (Wilheim et Ivy 1953; Klinke 1955; Hansen et coll. 1966; US EPA 2013). Cette substance peut avoir des effets sur le système endocrinien, d’après la recherche dans les bases de données Toxcast et Tox21 (JMPR 2016). Aucun effet sur le développement n’a été relevé dans les études du Brilliant Blue FCF chez le rat ou le lapin (Burnett et coll. 1974), dans des études dont les détails étaient limités (EFSA 2010; US EPA 2013), et aucune neurotoxicité pour le développement n’a été observée in vitro (Lau et coll. 2006). Compte tenu des renseignements disponibles, aucun effet préoccupant sur la santé n’a été relevé pour le Brilliant Blue FCF.
8.3 Caractérisation des risques pour la santé humaine
Les points de départ retenus pour la caractérisation des risques sont résumés à l’annexe D. Les tableaux 8-5 à 8-8 contiennent toutes les estimations pertinentes de l’exposition (points de départ de la concentration de l’effet critique) aux triarylméthanes, ainsi que les marges d’exposition résultantes. Les études d’exposition par voie orale sont utilisées pour caractériser le danger après une exposition par voie cutanée ou par inhalation en l’absence de données sur les dangers propres à ces voies d’exposition. Pour ce qui est des scénarios d’exposition par événement (pour le Malachite Green, le Basic Violet 4 et le Basic Blue 7), on juge qu’un point de départ d’une étude de toxicité pour le développement est pertinent pour la phase prénatale et les jeunes, car les effets chez ces derniers semblent indiquer qu’ils y sont sensibles.
Pour ce qui est de l’exposition quotidienne au Malachite Green, compte tenu du fait que son profil de génotoxicité est mixte et qu’aucun effet cancérogène n’a été observé à une dose inférieure à 21 mg/kg p.c./j, on estime que l’utilisation de la DMENO de 5 mg/kg p.c./j dans l’étude de toxicité pour le développement assure une protection contre ces effets observés à des doses d’exposition supérieures.
Milieux environnementaux
| Scénario d’exposition | Exposition générale (mg/kg p.c./j) | Niveau d’effet critique (mg/kg p.c. /j) | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Eau potable, exposition quotidienne, Basic Violet 3 | 0,00010 | DMENO 0,5 (DMinE) | Toxicité maternelle (mortalité accrue, diminution du poids corporel et prise de poids corporel, signes cliniques) et diminution du poids corporel des fœtus | 5 000 |
| Eau potable, DQMV, Basic Violet 3 | 0,000023 | DR10 = 16,8 | Carcinomes hépatocellulaires accrus | 730 000 |
| Eau potable, exposition quotidienne, Malachite Green | 0,00010 | DMENO 0,5 (DMinE) | Augmentation des pertes préimplantation, augmentation des résorptions fœtales précoces, diminution de la survie fœtale, diminution du poids corporel des fœtus et augmentation des déviations du squelette | 50 000 |
Abréviations : DR10 = dose de référence pour une limite inférieure de confiance à 95 % pour un niveau de risque supplémentaire de 10 %; DMENO = dose minimale entraînant un effet nocif observé; DMinE = dose minimale d’essai; ME = marge d’exposition; DSENO = dose sans effet nocif observé; .
On estime que ces marges d’exposition sont adéquates pour tenir compte des incertitudes dans les bases de données sur l’exposition et sur les effets sur la santé pour les effets cancérogènes et non cancérogènes.
Produits disponibles aux consommateurs
| Scénario d’exposition | Exposition générale [mg/kg p.c. (/j)] | Niveau d’effet critique [mg/kg p.c. (/j)] | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Utilisation non médicinale dans un produit de santé naturel, adulte, exposition quotidienne, Brilliant Blue FCF | 2,82 | DSENO 631 | Diminution du poids corporel et du taux de survie des femelles à 1 318 mg/kg p.c./j | 220 |
Abréviations : ME = marge d’exposition; DSENO = dose sans effet nocif observé.
Les autres expositions potentielles par voie orale au Brilliant Blue FCF, y compris par le rouge à lèvres ou le baume à lèvres (tout-petits, adultes), les médicaments contre le rhume ou les allergies (enfants ou adultes) et l’ingestion par le régime alimentaire allaient de 0,1 à 1 mg/kg p.c. (/j), avec des ME de 630 à 6 300. Ces marges d’exposition sont jugées adéquates pour tenir compte des incertitudes dans les bases de données sur l’exposition et sur les effets sur la santé non cancérogènes. De plus, l’exposition estimée par voie orale au Brilliant Blue FCF (y compris son utilisation dans un produit de santé naturel) est inférieure à la limite supérieure de la dose journalière admissible (DJA) de 6 mg/kg p.c./j établie par l’EFSA, et subséquemment adoptée par le JECFA en 2017, alors que la limite supérieure précédente pour la DJA de 12,5 mg/kg p.c./j a été retirée, en raison d’un facteur d’incertitude de 100 appliqué à la DSENO de 631 mg/kg p.c./j (EFSA 2010, JECFA 2017). Une approche qualitative d’évaluation des risques, comme celle utilisée par l’EPA (2013), a également été examinée, car aucun effet nocif n’avait été observé dans des études de toxicité chronique par le régime alimentaire jusqu’à 2 500 mg/kg p.c./j chez le rat et de plus de 7 354 mg/kg p.c./j chez la souris, ni dans une étude de toxicité pour la reproduction chez le rat sur 3 générations jusqu’à 1 000 mg/kg p.c./j. Cependant, une évaluation quantitative des risques a été réalisée, car ces autres études souffraient d’un manque de détails, la DMENO de 1 318 mg/kg p.c./j était basée en partie sur un taux de survie réduit, et le point de départ était en accord avec l’EFSA (2010).
| Scénario d’exposition | Exposition générale (mg/kg p.c. [/j]) | Niveau d’effet critique (mg/kg p.c. [/j]) | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Colorants capillaires (semi-permanents), adolescent et adulte, exposition quotidienne, Malachite Green | 0,0033 (adolescent); 0,0102 (adulte) | DMENO 5 (DMinE) | Pertes préimplantation accrues, résorptions fœtales précoces accrues, diminution du taux de survie des fœtus, diminution du poids corporel des fœtus et écarts squelettiques accrus | 1 500 (adolescent); 490 (adulte) |
| Colorants capillaires (semi-permanents), adolescent et adulte, exposition par événement, Malachite Green | 0,337 (adolescent); 0,282 (adulte) | DMENO 5 (DMinE) | Pertes préimplantation accrues, résorptions fœtales précoces accrues, diminution du taux de survie des fœtus, diminution du poids corporel des fœtus et écarts squelettiques accrus | 15 (adolescent); 18 (adulte) |
| Colorants capillaires (semi-permanents), adolescent et adulte, exposition par événement, Basic Violet 4 | 0,0589 (adolescent); 0,0494 (adulte) | DSENO 12 (DMaxE) | Aucun effet sur les mères ou le développement n’a été observé | 200 (adolescent); 240 (adulte) |
| Colorants capillaires (semi-permanents), adolescent et adulte, exposition par événement, Basic Blue 7 | 0,0177 (adolescent); 0,0148 (adulte) | DSENO 12 (DMaxE) | Aucun effet sur les mères ou le développement n’a été observé | 680 (adolescent); 810 (adulte) |
| Crème pour le corps, nourrisson et adulte, exposition quotidienne, Brilliant Blue FCF | 0,0068 (nourrisson); 0,0041 (adulte) | DSENO 12,6 a | Diminution du poids corporel et du taux de survie des femelles à 1 318 mg/kg p.c./j | 1 900 (nourrisson); 3 100 (adulte) |
Abréviations : DMinE = dose minimale d’essai, DMaxE = dose maximale d’essai; DMENO = dose minimale entraînant un effet nocif; DSENO = dose sans effet nocif observé; ME = marge d’exposition.
a DSENO de 631 mg/kg p.c./j × taux d’absorption orale de 2 % (Brown et coll. 1980), ce qui permet d’estimer la dose interne à laquelle des effets critiques sur la santé ont été observés.
| Scénario d’exposition | Exposition générale (mg/kg p.c./j) | Niveau d’effet critique (mg/kg p.c. /j) | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Colorants capillaires (semi-permanents), DQMV, Basic Violet 4 | 0,00134 | DR10 = 16,8 | Carcinomes hépatocellulaires accrus | 13 000 |
| Colorants capillaires (semi-permanents), adolescent et adulte, exposition quotidienne, Basic Blue 7 | 0,000175 (adolescent); 0,000533 (adulte) | DR10 = 16,8 | Carcinomes hépatocellulaires accrus | 96 000 (adolescent)a; 32 000 (adulte) a |
Abréviations : DR10 = dose de référence pour une limite inférieure de confiance à 95 % pour un niveau de risque supplémentaire de 10 %; ME = marge d’exposition.
a Les ME présentées sont jugées prudentes, car les expositions n’ont pas été ajustées sous forme de doses journalières ajustées pour la durée de la vie (DQMV). De tels ajustements n’ont pas été effectués, car les ME pour chaque groupe d’âge sont jugées adéquates, et les ajustements donneraient des ME plus élevées parce que les jeunes n’utilisent habituellement pas ces produits.
Les risques d’inhalation liés à l’exposition quotidienne au Brilliant Blue FCF dans le parfum (0,00054 ou 0,00064 mg/kg p.c./j, pour les adultes ou les adolescents, respectivement) donneraient lieu à des ME de 1 200 000 et 990 000, respectivement, pour la DSENO de 631 mg/kg p.c./j. Ces marges d’exposition sont jugées adéquates pour tenir compte des incertitudes dans les bases de données sur l’exposition et sur les effets sur la santé pour les effets non cancérogènes.
Les ME liées à l’exposition cutanée au Malachite Green variaient de 15 à 1 500 (colorants capillaires) pour tous les groupes d’âge. Ces marges pourraient être insuffisantes pour tenir compte des incertitudes dans les bases de données sur l’exposition et sur les effets sur la santé pour les effets non cancérogènes, car la DMENO choisie comme point de départ était la dose minimale d’essai.
La comparaison des expositions générales estimées par voie cutanée et voie orale, à l’intérieur de la plage des doses d’effets critiques donne lieu aux ME suivantes : Basic Violet 4 – entre 200 et 240; Basic Blue 7 – entre 680 et 810; Brilliant Blue FCF – entre 220 et 3 100. Le risque de cancer dû à l’exposition quotidienne au Basic Violet 4 ou au Basic Blue 7 donnait lieu à des ME comprises entre 13 000 et 96 000. La ME associée au risque d’inhalation de Brilliant Blue FCF était supérieure à 990 000. Ces ME ont été jugées adéquates pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé pour les effets cancérogènes et non cancérogènes.
Bien que l’exposition de la population générale au Basic Violet 3, au Basic Violet 4 et au Basic Blue 7 ne soit pas préoccupante aux niveaux actuels, on a estimé que ces substances présentent un effet préoccupant sur la santé en raison de leur cancérogénicité potentielle. Le Basic Violet 3 a été classé « Carc 2 » par la Commission européenne (ou « 1B » si la concentration en cétones de Michler est égale ou supérieure à 0,1 %) (CE 2008). Par conséquent, les effets sur la santé humaine pourraient être préoccupants si l’exposition devait augmenter.
8.4 Incertitudes de l’évaluation des risques pour la santé humaine
Les plus importantes sources d’incertitude sont présentées au tableau suivant.
| Principales sources d’incertitude | Fréquence |
|---|---|
| On ne disposait d’aucune donnée empirique sur l’absorption cutanée propre à un produit chimique donné, sauf le Brilliant Blue FCF. | +/- |
| On ne dispose pas de données canadiennes sur la surveillance des triarylméthanes dans les milieux naturels ambiants (p. ex., eaux de surface) ou l’eau potable. | +/- |
| On ne dispose pas d’études de toxicité chronique ou subchronique chez les animaux par voie cutanée ou par inhalation, et peu d’études de toxicité chronique des triarylméthanes pour les animaux par voie orale. | +/- |
| Il existe peu d’études de toxicité pour la reproduction ou le développement pour les triarylméthanes. Par exemple, on n’a trouvé aucune étude de toxicité pour la reproduction pour le Malachite Green. | +/- |
+ = incertitude quant au potentiel de surestimation de l’exposition/risque; – = incertitude quant au potentiel de sous-estimation du risque d’exposition; +/ – = potentiel inconnu de surestimation ou de sous-estimation du risque.
9. Conclusion
Compte tenu de tous les éléments de preuve contenus dans la présente évaluation préalable, le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7 présentent un risque d’effets nocifs sur l’environnement. Il est conclu que le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7 satisfont aux critères de l’alinéa 64a) de la LCPE, car ils pénètrent ou peuvent pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique. Toutefois, il est conclu que le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7 ne satisfont pas au critère de l’alinéa 64b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à mettre en danger l’environnement essentiel pour la vie.
Compte tenu de tous les éléments de preuve contenus dans la présente évaluation préalable, le Brilliant Blue FCF et le Pigment Blue 61 présentent un faible risque d’effets nocifs sur l’environnement. Il est conclu que le Brilliant Blue FCF et le Pigment Blue 61 ne satisfont pas aux critères des alinéas 64a) ou b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
À la lumière des renseignements contenus dans la présente évaluation préalable, il est conclu que le Malachite Green satisfait au critère de l’alinéa 64c) de la LCPE, car il pénètre ou peut pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaines.
À la lumière des renseignements contenus dans la présente évaluation préalable, il est conclu que le Basic Violet 3, le Pigment Blue 61, le Basic Violet 4, le Basic Blue 7 et le Brilliant Blue FCF ne satisfont pas au critère de l’alinéa 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaines.
Il est conclu que le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7 satisfont à un ou plusieurs des critères énoncés à l’article 64 de la LCPE. Il est conclu que le Pigment Blue 61 et le Brilliant Blue FCF ne satisfont à aucun des critères énoncés à l’article 64 de la LCPE.
Il est conclu que le Basic Violet 3, le Malachite Green, le Basic Violet 4 et le Basic Blue 7 répondent aux critères de persistance, mais pas à ceux de bioaccumulation, énoncés dans le Règlement sur la persistance et la bioaccumulation de la LCPE.
Références
ACD/Percepta [prediction module]. c1997-2015. Toronto (ON): Advanced Chemistry Development, Inc. [Disponible en anglais seulement]
[ACIA] Agence canadienne d’inspections des aliments. 2010. Rapport du Plan d’action pour assurer la sécurité des produits alimentaires. 2009-2010 Études ciblées Chimie. Utilisation de colorants alimentaires pour la production d’aliments transformés. Ottawa (Ont.), ACIA. Rapport no : TS-CHEM-09/10-05.
[ACIA] Agence canadienne d’inspections des aliments. 2011. Plan d’action pour assurer la sécurité des produits alimentaires. Rapport 2010-2011. Études ciblées – Chimie : Utilisation de colorants alimentaires pour la production d’aliments transformés. Ottawa (Ont.), ACIA. Rapport no : TS-CHEM-10/11.
[ACIA] Agence canadienne d’inspections des aliments. 2012. Vert malachite - Questions et réponses. Dangers chimiques et substances potentiellement cancérigènes - Fiches de renseignements. [Consulté le 29 mars 2017].
[ACIA] Agence canadienne d’inspections des aliments. 2015. Utilisation du violet de gentiane dans les aliments du bétail. RG-8 Directives réglementaires : Contaminants dans les aliments du bétail. [Consulté le 29 mars 2017].
Aidoo A, Gao N, Neft RE, Schol HM, Hass BS, Minor TY, Heflich RH. 1990. Evaluation of the genotoxicity of Gentian Violet in bacterial and mammalian cell systems. Teratog Carcinog Mutagen. 10:449-462. [Disponible en anglais seulement]
[AGDH] Australian government Department of Health. 2014. Crystal Violet and related dyes. Sydney (AU): Department of Health, National Industrial Chemicals Notification and Assessment Scheme (NICNAS). [consulté le 19 avril 2016]. [Disponible en anglais seulement]
Andrews JJ, Johnston RV, Bee DE, Arens JF. 1990. Photodeactivation of ethyl violet: A potential hazard of Sodasorb. Anesthesiology. 72(1):59-64. [Disponible en anglais seulement]
Anliker R, Moser P. 1987. The limits of bioaccumulation of organic pigments in fish: their relation to the partition coefficient and the solubility in water and octanol. Ecotoxicol Environ Saf. 13(1):43-52. [Disponible en anglais seulement]
[ARLA] Agence de réglementation de la lutte antiparasitaire. 2010. Liste des produits de formulation de l’ARLA [PDF]. Ottawa (ON), gouvernement du Canada. SC pub : 100460, No de catalogue : H114-22/2010F. [consulté le 7 avril 2017].
Au W, Hsu TC. 1979. Studies on the clastogenic effects of biologic stains and dyes. Environ Mutagen. 1:27-35. [cited in Aidoo et al. 1990]. [Disponible en anglais seulement]
Au W, Pathak S, Collie CJ, Hsu TC. 1978. Cytogenetic toxicity of Gentian Violet and Crystal Violet on mammalian cells in vitro. Mutat Res. 58:269-276. [cité dans Aidoo et al. 1990]. [Disponible en anglais seulement]
Ballantyne B, Gazzard MF, Swanston DW. 1973. Eye damage caused by Crystal Violet. Proc Br Pharmacol Soc. 49(1):181P-182P. [cité dans Diamante et al. 2009]. [Disponible en anglais seulement]
Baughman GL, Weber EJ. 1994. Transformation of dyes and related compounds in anoxic sediment: kinetics and products. Environ Sci Technol. 28(2):267-76. [cité dans EpiSuite c2000-2012]. [Disponible en anglais seulement]
[BCFBAF] Bioaccumulation Program for Microsoft Windows [modèle d’estimation]. 2010. Ver. 3.01. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Disponible en anglais seulement]
[BDIPSN] Base de données d’ingrédients de produits de santé naturels [base de données]. [modified 2017 Oct 23]. Ottawa (ON), gouvernement du Canada. [consulté le 15 janvier 2018].
[BDPP] Base de données sur les produits pharmaceutiques [base de données]. [modifiée le 17 juillet 2015]. Ottawa (ON), gouvernement du Canada. [consulté le 21 avril 2017].
[BDPSNH] Base de données sur les produits de santé naturels homologués [base de données]. [modifié le 10 août 2016]. Ottawa (ON), gouvernement du Canada. [consulté le 15 janvier 2018].
Beatson RP. 2012. Retention of MAPBAP acetate on mechanical and de-inked pulp. Rapport inédit préparé par Rodger Beatson et associés. 26 p. [Disponible en anglais seulement]
Bergwerff AA, Kuiper RV, Scherpenisse P. 2004. Persistence of residues of Malachite Green in juvenile eels (Anguilla anguilla). Aquaculture. 233(1-4):55-63. [Disponible en anglais seulement]
[BfR] Federal Institute for Risk Assessment. 2007. Introduction to the problems surrounding garment textiles. BfR Information No. 018/2007, 1 June 2007. Berlin (GR):BrR. Disponible sur demande. [Disponible en anglais seulement]
Bills TD, Chandler Jr. JH, Marking LL. 1977. Malachite green: its toxicity to aquatic organisms, persistence, and removal with activated carbon. Investigations in Fish Control. 75:1-6. [Disponible en anglais seulement]
Bio/dynamics Inc., 1972, 1973. (Unpublished reports cited in catalogue of Food Colours Volume 2. Colour Committee of the International Life sciences Institute). Bio/dynamics Inc., 1972, 1973. Unpublished reports cited in catalogue of Food Colours Volume 2. [cité dans EFSA 2010]. [Disponible en anglais seulement]
[BIOWIN] Biodegradation Probability Program for Microsoft Windows [estimation model]. 2008. Ver. 4.10. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Disponible en anglais seulement]
Boîte à outils QSAR de l’OCDE [outil d’extrapolation]. 2013. Ver. 3.2. Paris (FR): Organisation de coopération et de développement économiques, Laboratory of Mathematical Chemistry. [Disponible en anglais seulement]
Borzelleca JF, Depuka K, Hallagan JB. 1990. Lifetime toxicity/carcinogenicity studies of FD & C Blue No. 1 (Brilliant Blue FCF) in rats and mice. Fd Chem Toxicol. 28(4):221-234. [Disponible en anglais seulement]
Bose B, Motiwale L, Rao KV. 2005. DNA damage and G2/M arrest in Syrian hamster embryo cells during Malachite green exposure associated with elevated phosphorylation of ERK1 and JNK1. Cancer Lett. 230(2):260-70. [Disponible en anglais seulement]
Brown JP, Dorsky A, Enderlin FE, Hale RL, Wright VA, Parkinson TM. 1980. Synthesis of 14C-labelled FD & C Blue No. 1 (Brilliant Blue FCF) and its intestinal absorption and metabolic fate in rats. Food Cosmet Toxicol. 18(1):1-5. [Disponible en anglais seulement]
Burnett C, Agersborg H, Borzelleca J, Eagle E, Ebert A, Pierce E, Kirschman J, Scala R. 1974. Teratogenic studies with certified colors in rats and rabbits. Toxicol Appl Pharmacol. 29:121. [cité dans Borzelleca et al. 1990]. [Disponible en anglais seulement]
Bumpus JA, Brock BJ. 1988. Biodegradation of crystal violet by the white rot fungus Phanerochaete chrysosporium. Appl Environ Microbiol. 54(5):1143-50. [Disponible en anglais seulement]
Burnett C, Opdyke D. 1971. Chronic eye irritation and staining properties of some organic colors and lakes. CTFA Cosmet J. 3:18-20. [cité dans Borzelleca et al. 1990]. [Disponible en anglais seulement]
Canada. [1978]. Règlement sur les aliments et drogues. C.R.C., ch. 870.
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999). L.C. 1999, ch. 33. Gazette du Canada Partie III, vol. 22, no 3.
Canada, Ministère de l’Environnement. 2009. Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances inanimées (chimiques) [PDF]. Gazette du Canada, Partie I, vol. 143, no 40, p. 2945-2956.
Canada, Ministère de l’Environnement. 2012. Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances [PDF]. Gazette du Canada, Partie I, vol. 146, no 48, Supplément.
[CE] Commission européenne. 2008. Règlement (CE) No 1272/2008 du parlement Européen et du Conseil [PDF], of 16 December 2008 on classification, labelling and packaging of substances and mixtures, amending and repealing Directives 67/548/EEC and 1999/45/EC, and amending Regulation (EC) No 1907/2006. Off J Eur Union L. 353:1-1355.
[CE] Commission européenne. 2009. Règlement (CE) No 1223/2009 du parlement Européen et du Conseil [PDF]. Journal officiel de l’Union européenne. 342/59-209.
Ciba Ltd., Basel, safety data sheet No. T5150/A, 1989. [cité dans Flury and Fuhler 1994]. [Disponible en anglais seulement]
[CITI] Chemicals Inspection & Testing Institute Japan. 1992. Biodegradation and bioaccumulation data of existing chemicals based on the CSCL Japan. Tokyo (JP): Japan Chemical Industry Ecology-Toxicology & Information Center. [Disponible en anglais seulement]
Cole JG, Mackay D. 2000. Correlating environmntal partitioning properties of organic compounds: The three solubility approach. Environ Toxicol Chem. 19(2):265-270. [Disponible en anglais seulement]
[ConsExpo] Consumer Exposure Model. 2006. Version 4.1. Bilthoven (NL): Rijksinstituut voor Volksgezondheid en Milieu [National Institute for Public Health and the Environment]. [cité le 25 avril 2017]. [Disponible en anglais seulement]
[ConsExpo Web] Consumer Exposure Web Model. 2016. Bilthoven (NL): Rijksinstituut voor Volksgezondheid en Milieu [National Institute for Public Health and the Environment]. [Disponible en anglais seulement]
[CPMA] Color Pigments Manufacturers Association. 2016. Unpublished confidential studies submitted to Environment and Climate Change Canada (ECCC) under the Chemicals Management Plan initiative. Gatineau (QC): ECCC, Program Development and Engagement Division. Présentation reçue le 2016-11-04.
Culp SJ, Blankenship LR, Kusewitt DF, Doerge DR, Mulligan LT, Beland FA. 1999. Toxicity and metabolism of Malachite Green and LeucoMalachite Green during short-term feeding to Fischer 344 rats and B6C3F1 mice. Chem Biol Interact.122(3):153-170. [Disponible en anglais seulement]
Das JK, Sarkarb S, Hossain Sk U, Chakraborty P, Das RK, Bhattacharya. Indian S. J Med Res 137, June 2013, pp 1163-1173. [cité dans ECHA 2016]. [Disponible en anglais seulement]
Derek Nexus [toxicity prediction module]. 2016. Ver. 5.0.2. Leeds (UK): Lhasa Limited. [Disponible en anglais seulement]
Dhir SP, Sharma Sk, Munjal VP, Gupa A. 1982. Keratoconjunctivitis sicca following instillation of Gentian Violet. Indian J Ophthalmol. 30:21-22. [cité dans Diamante et al. 2009]. [Disponible en anglais seulement]
Dhamgaye S, Devaux F, Manoharlal R, Vandeputte P, Shah AH, Singh A, Prasad R. 2012. In vitro effect of Malachite Green on Candida albicans involves multiple pathways and transcriptional regulators UPC2 and STP2. Antimicrob Agents Chemother. 56(1):495-506. [Disponible en anglais seulement]
Diamante C, Bergfeld WF, Belsito DV, Klaassen CD, Marks Jr JG, Shank RC, Slaga TJ, Snyder PW, Andersen FA. 2009. Final report on the safety assessment of Basic Violet 1, Basic Violet 3, and Basic Violet 4. Int J Toxicol. 28(suppl 3):193S-204S. [Disponible en anglais seulement]
Docampo R, Moreno SN, Gadelha FR, De Souza W, Cruz, FS. 1988. Prevention of Chagas' disease resulting from blood transfusion by treatment of blood: toxicity and mode of action of gentian violet. Biomed Environ Sci. 1(4):406-413. [Disponible en anglais seulement]
Docampo R, Moreno SNJ. 1990. The metabolism and mode of action of Gentian Violet. Drug Metab Rev. 22:161-178. [cité dans JECFA 2014]. [Disponible en anglais seulement]
Donya SM, Farghaly AA, Abo-Zeid MA, Aly HF, Ali SA, Hamed MA, El-Rigal NS. 2012. Malachite green induces genotoxic effect and biochemical disturbances in mice. Eur Rev Med Pharmacol Sci. 16(4): 469-482. [cité dans ECHA 2016]. [Disponible en anglais seulement]
Droge S, Goss K. 2012. Effect of sodium and calcium cations on the ion-exchange affinity of organic cations for soil organic matter. Environ Sci Technol. 46:5894-5901. [Disponible en anglais seulement]
Droge ST, Goss K. 2013. Development and evaluation of a new sorption model for organic cations in soil: contributions from organic matter and clay minerals. Environ Sci Technol. 47:14233-14241. [Disponible en anglais seulement]
[ECCC] Environnement et Changement climatique Canada. 2016. Document sur l’approche scientifique : Classification du risque écologique des substances organiques. Ottawa (ON), gouvernement du Canada.
[ECCC] Environnement et Changement climatique Canada. 2019. Données recueillies après les commentaires du public formulés par l’Association des produits forestiers du Canada (APFC) sur l’ébauche d’évaluation préalable des triarylméthanes dans le cadre du Plan de gestion des produits chimiques (février-juin 2019). Données analysées par ECCC; Programme des substances existantes.
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada. [modified 2017 Mar 12]. Catégorisation. Ottawa (ON), gouvernement du Canada. [consulté le 25 avril 2017].
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada. 2018. Évaluation préalable rapide des substances pour lesquelles l’exposition de la population générale est limitée. Ottawa (ON), gouvernement du Canada.
[ECHA] Agence européenne des produits chimiques. c2007-2017a. Substances enregistrées. Résultats de recherche pour no CAS [1324-76-1]. Helsinki (FI): ECHA. [mis à jour le 27 décembre 2015; consulté le 20 avril 2017].
[ECHA] Agence européenne des produits chimiques. c2007-2017b. Substances enregistrées. Résultats de recherche pour no CAS [63157-72-2]. Helsinki (FI): ECHA. [mis à jour le 27 décembre 2015; consulté le 28 décembre 2016].
[ECHA] Agence européenne des produits chimiques. c2007-2017c. Substances enregistrées. Résultats de recherche pour no CAS [6441-82-3]. Helsinki (FI): ECHA. [mis à jour le 27 décembre 2015; consulté le 28 décembre 2016].
[ECHA] Agence européenne des produits chimiques. 2017. Guidance on Information Requirements and Chemical Safety Assessment, Chapter R.11: PBT/vPvB assessment [PDF]. Draft version 3. Helsinki (FI): ECHA. [Disponible en anglais seulement]
[ECHA] Agence européenne des produits chimiques. [modifié le 20 décembre 2016]. Liste des substances extrêmement préoccupantes candidates en vue d’une autorisation. Helsinki (FI): ECHA. [consulté le 27 septembre 2017].
[EFSA] Autorité européenne de sécurité des aliments, Panel on Food Additives and Nutrient Sources Added to Food (ANS). 2010. Scientific opinion on the re-evaluation of Brilliant Blue FCF (E 133) as a food additive. EFSA Journal. 8(11):1853. [Disponible en anglais seulement]
[EFSA] Autorité européenne de sécurité des aliments, Panel on contaminants in the food chain (CONTAM). 2016. Scientific opinion on Malachite Green in food. EFSA Journal. 14(7):4530. [Disponible en anglais seulement]
Enoch SJ, Ellison CM, Schultz TW, Cronin MTD. 2011. A review of the electrophilic reaction chemistry involved in covalent protein binding relevant to toxicity. Crit Rev Toxicol 41(9):783-802. [Disponible en anglais seulement]
Environnement Canada. 2009. Données de la Mise à jour de l’inventaire de la LIS recueillies en vertu du de l’article 71 de la Loi canadienne sur la protection de l’environnement de 1999 : Avis concernant certaines substances inanimées (chimiques) inscrites sur la Liste intérieure. Données préparées par Environnement Canada et Santé Canada, Programme des substances existantes.
Environnement Canada. 2013. Données de la Mise à jour de l’inventaire de la LIS recueillies en vertu du de l’article 71 de la Loi canadienne sur la protection de l’environnement de 1999 : Avis modifiant l’Avis concernant certaines substances de la Liste intérieure. Données préparées par Environnement Canada et Santé Canada, Programme des substances existantes.
[EPI Suite] Estimation Program Interface Suite for Microsoft Windows [estimation model]. c2000-2012. Ver. 4.11. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Disponible en anglais seulement]
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 1992. Draft guidelines for the the assessment of environmental exposure to dyestuffs. [Disponible en anglais seulement]
[ETAD] Ecological and Toxicological Association of Dyes and Organic Pigments Manufacturers. 1995. Health & environmental information on dyes used in Canada. An overview to assist in the implementation of the New Substances Notification Regulation under the Canadian Environmental Protection Act. Prepared by the ETAD Canadian Affiliates. Juillet 1995. Report 7/21/95. [Disponible en anglais seulement]
[EWG] Environmental Working Group. SkinDeep Cosmetics Database [database]. c2007-2017. Washington (DC): EWG. [consulté le 21 avril 2017]. [Disponible en anglais seulement]
Federal Registry. 1988. Acid Blue 9. Toxic chemical release reporting, community right-to-know. Fed. Regist. 53: 12035-12037. [cité dans Flury and Fuhler 1994]. [Disponible en anglais seulement]
Fessard V, Godard T, Heut S, Mourot A, Poul JM. 1999. Mutagenicity of Malachite Green and Leucomalachite Green in in vitro tests. J Appl Toxicol. 19:421-430. [cité dans NTP 2005]. [Disponible en anglais seulement]
Ferguson LR, Baguley BC. 1988. Verapamil as a co-mutagen in the Salmonella/mammalian microsome mutagenicity test. Mutat Res. 209:57-62. [cité dans NTP 2005]. [Disponible en anglais seulement]
Flury M, Flühler H. 1994. Brilliant Blue FCF as a dye tracer for solute transport studies - a toxicological overview. J Environ Qual 23:1108-1112. [Disponible en anglais seulement]
German-Heins J, Flury M. 2000. Sorption of Brilliant Blue FCF in soils as affected by pH and ionic strength. Geoderma 97:87-101. [Disponible en anglais seulement]
Gerundo N, Alderman DJ, Clifton-Hadely RS, Feist SW. 1991. Pathological effects of repeated doses of Malachite Green: a preliminary study. J Fish Dis. 14(5):521-532. [Disponible en anglais seulement]
Geyer H, Scheunert I, Korte F. 1985. Relationship between the lipid content of fish and their bioconcentration potential of 1,2,4-trichlorobenzene. Chemosphere. 14(5):545-555. [Disponible en anglais seulement]
Gobas FA, Morrison HA 2000. Bioconcentration and biomagnification in the aquatic environment. In: Boethling RS, Mackay D, editors. Handbook of property estimation methods for chemicals, environmental and health sciences. Boca Raton (FL), CRC Press. pp 189-231. [Disponible en anglais seulement]
Gopinathan R, Kanhere J, Banerjee J. 2015. Effect of Malachite Green toxicity on non-target soil organisms. Chemosphere. 120:637-644. [Disponible en anglais seulement]
Green FJ. 1990. The Sigma-Aldrich handbook of stains, dyes and indicators. Milwaukee (WI) : Aldrich Chemical Company, Inc. [cité dans EpiSuite c2000-2012]. [Disponible en anglais seulement]
Hansch C, Leo A, Hoekman D. 1995. Exploring QSAR hydrophobic, electronic and steric constants. ACS, Washington (DC) : ACS. [cité dans EpiSuite c2000-2012]. [Disponible en anglais seulement]
Hansen WH, Fitzhugh OG, Nelson AA, Davis KJ. 1966. Chronic toxicity of two food colors, Brilliant blue FCF and Indigotine. Toxicol Appl Pharmacol. 8:29-36. [cité dans EFSA 2010]. [Disponible en anglais seulement]
[HENRYWIN] Henry’s Law Constant Program for Microsoft Windows [estimation model]. 2008. Ver. 3.20. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Disponible en anglais seulement]
Herbst W, Hunger K. 2004. Industrial organic pigments: production, properties, applications. 3rd ed. Weinheim (DE): Wiley-VCH. [Disponible en anglais seulement]
Hernando MD, De Vettori S, Bueno MM, Fernández-Alba AR. 2007. Toxicity evaluation with Vibrio fischeri test of organic chemicals used in aquaculture. Chemosphere. 68(4):724-730. [Disponible en anglais seulement]
Hikari USA. 2016. Betta Revive. Hayward (CA): Hikari Sales USA Inc. [consulté le 27 mai 2016]. [Disponible en anglais seulement]
Hinton MJ, Eversole AG. 1978. Toxicity of ten commonly used chemicals to American eels [Includes herbicides copper sulfate and Diquat]. Proc Ann Conf S E Assoc Fish & Wildl Agencies. 32:599-604. [Disponible en anglais seulement]
Hinton MJ, Eversole AG. 1979. Toxicity of ten chemicals commonly used in aquaculture to the black eel stage of the American eel. J World Aquac Soc. 10(1-4):554-560. [Disponible en anglais seulement]
Hodge HC, Indra J, Drobeck HP, Duprey LP, Tainter ML. 1972. Acute oral toxicity of methylrosaniline chloride. Toxicol Appl Pharmacol. 22:1-5. [cité dans JECFA 2014]. [Disponible en anglais seulement]
Hunger K. 2003. Industrial dyes: chemistry, properties, applications. Weinheim (DE): Wiley-VCH. [Disponible en anglais seulement]
[IARC] IARC Working Group on the evaluation of carcinogenic risks to humans. 1996. Printing Processes and Printing Inks [PDF]. IARC Monogr Eval Carcinog Risks Hum. 65:33-147. [Disponible en anglais seulement]
IHS Markit. 2018. Dyes: CEH Chemical Economic Handbook. London (UK): IHS Markit. [Disponible en anglais seulement]
[INRP] Inventaire national des rejets de polluants. 1993-2015. INRP Jeu de données : données normalisées, substance releases normalized since 1993. Gatineau (QC), Environnement et Changement climatique Canada. Résultats de recheche pour le no CAS 569-64-2. [consulté le 3 avril 2017].
Janik-Spiechowicz E, Dziubałtowska E, Wyszyńska K. 1997. Mutagenic and genotoxic activity detected by the Ames, micronucleus and SCE tests under the influence of samples of dyes manufactured in Poland. Int J Occup Med Environ Health. 10(1):55-65. [Disponible en anglais seulement]
[JECFA] Comité mixte FAO/OMS d’experts sur les additifs alimentaires. 1969. Toxicological evaluation of some food colours, emulsifiers, stabilizers, anti-caking agents and certain other substances. Brilliant Blue FCF. WHO technical report series, no. 46A. Préparé dans le cadre de la 13e réunion du JECFA. Genève (CH): Organisation mondiale de la Santé. [Disponible en anglais seulement]
[JECFA] Comité mixte FAO/OMS d’experts sur les additifs alimentaires. 2009. Evaluation of certain veterinary drug residues in food [PDF]. Malachite Green. WHO technical report series, no. 954. Préparé dans le cadre de la 70e réunion du JECFA. Genève (CH): Organisation mondiale de la Santé. [Disponible en anglais seulement]
[JECFA] Comité mixte FAO/OMS d’experts sur les additifs alimentaires. 2014. Toxicological evaluation of certain veterinary drug residues in food [PDF]. Gentian violet. WHO Food Additives Series, No. 69. Préparé dans le cadre de la 78e réunion du JECFA. Genève (CH): Organisation mondiale de la Santé. [Disponible en anglais seulement]
[JECFA] Comité mixte FAO/OMS d’experts sur les additifs alimentaires. 2017. Toxicological information, dietary exposures and information on specifications. 84e réunion, Rome, 6-15 juin 2017. Sommaire et conclusions. Genève (CH): Organisation mondiale de la Santé. [Disponible en anglais seulement]
Jiang Y, Xie P, Liang G. 2009. Distribution and depuration of the potentially carcinogenic Malachite Green in tissues of three freshwater farmed Chinese fish with different food habits. Aquaculture. 288(1-2):1-6. [Disponible en anglais seulement]
[JMPR] Réunion conjointe FAO/OMS sur les résidus de pesticides. 2016. Pesticide residues in food, evaluations. Part II: Toxicological. Genève (CH): Organisation mondiale de la Santé. Coparrainé par l’Organisation des Nations Unies pour l’alimentation et l’agriculture et l’Organisation mondiale de la Santé.
Kah M, Brown CD. 2006. Adsorption of ionisable pesticides in soils. Rev Environ Contam Toxicol.188:149-217. [Disponible en anglais seulement]
Kanhere J, Gopinathan R, Banerjee J. 2014. Cytotoxicity and genotoxicity of Malachite Green on non-target aquatic organisms: Chlorella pyrenoidosa and Daphnia magna. Water Air Soil Pollut. 225(9):2134. [Disponible en anglais seulement]
Kasem H, Ibrahim AE, Rania HA, El Hady KA. 2016 In vivo toxicity study of Malachite Green in mice: Estimation of hepatotoxicity, oxidative stress and genotoxicity. Int. J PharmTech Res. 9(3): 58-67. [Disponible en anglais seulement]
Klinke. 1955. Mentionné dans EFSA, 2010, mais non inclus dans la liste des références. [Disponible en anglais seulement]
[KOAWIN] Octanol-Air Partition Coefficient Program for Microsoft Windows [estimation model]. 2010. Ver. 1.10. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Disponible en anglais seulement]
[KOCWIN] Organic Carbon Partition Coefficient Program for Microsoft Windows [estimation model]. 2010. Ver. 2.00. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Disponible en anglais seulement]
[KOWWIN] Octanol-Water Partition Coefficient Program for Microsoft Windows [estimation model]. 2010. Ver. 1.68. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Disponible en anglais seulement]
Kus E., Eroglu HE. 2015. Genotoxic and cytotoxic effects of sunset yellow and Brilliant Blue, colorant food additives, on human blood lymphocytes. Pak. J. Pharm. Sci, 28(1): 227-230. [Disponible en anglais seulement]
Lanzing WJR. 1965. Observations on Malachite Green in relation to its application to fish diseases. Hydrobiologia. 25(3):426-441. [Disponible en anglais seulement]
Lau K, McLean WG, Williams DP and Howard CV. 2006. Synergistic interactions between commonly used food additives in a developmental neurotoxicity test. Toxicol Sci. 90:178-187. [cité dans EFSA 2010]. [Disponible en anglais seulement]
Leadscope Model Applier [prediction module]. 2016. Ver. 2.1. Columbus (OH): Leadscope, Inc. [accès restreint]. [Disponible en anglais seulement]
Littlefield NA. 1984. Chronic toxicity and carcinogenicity studies of Gentian Violet in mice. Final report. Jefferson (AR): National Center for Toxicological Research, Division of Chemical Toxicology (NCTR technical report for experiment 304). [cité dans JECFA 2014]. [Disponible en anglais seulement]
Littlefield NA. 1988. Three-generation reproduction and toxicity studies of Gentian Violet in Fischer 344 rats. Jefferson (AR): National Center for Toxicological Research (NCTR technical report for experiments 305, 354, 355). [cité dans JECFA 2014]. [Disponible en anglais seulement]
Littlefield NA, Blackwell BN, Hewitt CC, Gaylor DW. 1985. Chronic toxicity and carcinogenicity studies of Gentian Violet in mice. Fundam Appl Toxicol. 5(5):902-912. [cité dans JECFA 2014]. [Disponible en anglais seulement]
Littlefield NA, Gaylor DW, Blackwell BN, Allen RR. 1989. Chronic toxicity/carcinogenicity studies of Gentian Violet in Fischer 344 rats: two-generation exposure. Food Chem Toxicol. 27:239-47. [cité dans JECFA 2014]. [Disponible en anglais seulement]
Liu H, Yang S, Ni Y. 2007. Using dyes for improving the optical properties of high yield pulps. Pulp & Paper Canada 108 (10): 25-29. [Disponible en anglais seulement]
Loretz LG, Api AM, Barraj LM, Burdick J, Dressler WE, Gettings SD, Han Hsu H, Pan YHL, Re TA, Renskers KJ, Rothenstein A, Scrafford CG, Sewall C. 2005. Exposure data for cosmetic products: lipstick, body lotion, and face cream. Food Chem Toxicol 43:279-291. [Disponible en anglais seulement]
Lucová M, Hojerová J. Pažoureková S, Klimová A. 2013 Absoprtion of triphenylmethane dyes Brilliant Blue and Patent Blue through intact skin, shaven skin and lingual mucosa from daily life products. Food Chem Toxicol 52:19-27. [Disponible en anglais seulement]
Lu FC, Lavallée A. 1964. The acute toxicity of some synthetic colours used in drugs and food. Can Pharm J. 97:30. [cité dans Borzelleca et al. 1990]. [Disponible en anglais seulement]
Mani S, Bharagava RN. 2016. Exposure to crystal violet, its toxic, genotoxic and carcinogenic effects on environment and its degradation and detoxification for environmental safety. Rev Environ Contam Toxicol. 237:71-104. [Disponible en anglais seulement]
Mannell WA, Grice H, Allmar M. 1962. Chronic toxicity studies on food colours. V. Observations on the toxicity of Brilliant Blue FCF, Guinea Green B and Benzyl Violet 4B in rats. J Pharm Pharmac. 14:378-384. [cité dans Borzelleca et al. 1990]. [Disponible en anglais seulement]
McDonald JJ. 1989. Metabolism of Gentian Violet in Fischer 344 rats and B6C3F1 mice. Jefferson (AR): National Center for Toxicological Research (NCTR technical report for experiments 302, 303). [cité dans JECFA 2014]. [Disponible en anglais seulement]
McDonald JJ, Cerniglia CE. 1984. Biotransformation of Gentian Violet to Leucogentian Violet by human, rat and chicken intestinal microflora. Drug Metab Dispos. 12:330-336. [cité dans JECFA 2014]. [Disponible en anglais seulement]
McDonald JJ, North CR, Breeden CR, Lai CC, Roth RW. 1984. Synthesis and disposition of 14C-labelled Gentian Violet in F344 rats and B6C3F1 mice. Food Chem Toxicol. 22:331-336. [cité dans JECFA 2014]. [Disponible en anglais seulement]
Meyer FP, Jorgenson TA. 1983. Teratological and other effects of Malachite Green on development of rainbow trout and rabbits. T Am Fish Soc. 112:818-824. [Disponible en anglais seulement]
Mittelstaedt RA, Mei N., Webb PJ, Shaddock JG, Dobrovolsky VN, McGarrity LJ, Morris SM, Chen T, Beland FA, Greenlees KJ, Heflich RH. 2004. Genotoxicity of Malachite Green and leucoMalachite Green in female Big Blue B6C3F1 mice. Mutat Res. 561:127-138. [Disponible en anglais seulement]
Mon J, Flury M, Harsh JB. 2006. A quantitative structure-activity relationships (QSAR) analysis of triarylmethane dye tracers. J Hydrol. 316(1-4):84-97. [Disponible en anglais seulement]
Müller W, Gautier F. 1975. Interactions of heteroaromatic compounds with nucleic acids. A- T-specific non-intercalating DNA ligands. Eur J Biochem. 54(2):385-394. [cité dans Docampo et Moreno 1990]. [Disponible en anglais seulement]
[MPBPWIN] Melting Point Boiling Point Program for Microsoft Windows [estimation model]. 2008. Ver. 1.43. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Disponible en anglais seulement]
[MSDS] Material Safety Data Sheet. 2014. Elmer’s Color Change Markers. Columbus (OH): Elmer’s Products Inc. [consulté le 27 mai 2016]. [Disponible en anglais seulement]
Nagai S. 1959. Induction of the respiration-deficient mutation in yeast by various synthetic dyes. Science. 130:118-1189. [cité dans Janik-Spiechowicz et al. 1997]. [Disponible en anglais seulement]
Niska K, Korkea-aho T, Lindfors E, Kiuru T, Tuomainen M, Taskinen J, Peltonen K. 2009. Disappearance of Malachite Green residues in fry of rainbow trout (Oncorhynchus mykiss) after treatment of eggs at the hatching stage. Aquaculture. 297(1-4):25-30. [Disponible en anglais seulement]
[NITE] National Institute of Technology and Evaluation. 2002. [mentionné dans la boîte à outils QSAR de l’OCDE, version 3.4.0.17]. [Disponible en anglais seulement]
[NTP] National Toxicology Program (US). 1982. Teratologic evaluation of Gentian Violet (CAS No. 548-62-9) in CD rats. Final report. Research Triangle Park (NC): United States Department of Heatlh and Human Services, Public Health Service, National Toxicology Program. Report No.: TER82079. [cité en tant que Wolkowski-Tyl dans JECFA 2014]. [Disponible en anglais seulement]
[NTP] National Toxicology Program (US). 1983. Teratologic evaluation of Gentian Violet (CAS No. 548-62-9) in New Zealand white rabbits. Final report. Research Triangle Park (NC): United States Department of Health and Human Services, Public Health Service, National Toxicology Program. Report No.: TER82080. [cité en tant que Wolkowski-Tyl dans JECFA 2014]. [Disponible en anglais seulement]
[NTP] National Toxicology Program. 2004. NTP Technical Report on the toxicity studies of Malachite Green Chloride and Leucomalachite Green (CAS Nos. 569-64-2 and 129-73-7) in F344/N rats and B6C3F1 mice (feed studies). Research Triangle Park (NC): US Department of Health and Human Services, National Toxicology Program. Report No.: 04-4416. [Disponible en anglais seulement]
[NTP] National Toxicology Program. 2005. NTP Technical Report on the toxicology and carcinogenesis studies of Malachite Green Chloride and Leucomalachite Green (CAS Nos. 560-64-2 and 129-73-7) in F344/N rats and B6C3F1 mice (feed studies). Research Triangle Park (NC): US Department of Health and Human Services, National Toxicology Program. Report No.: TR 527. [Disponible en anglais seulement]
[OCDE] Organisation de Coopération et de Développement Économiques. 2009. Emission scenario document on pulp, paper and board industry. Paris (FR): OECD, Environment Directorate. (Series on Emission Scenario Documents No. 23). Report No.: ENV/JM/MONO(2009)24. [Disponible en anglais seulement]
Ogugbue CJ, Sawidis T. 2011. Bioremediation and detoxification of synthetic wastewater containing triarylmethane dyes by Aeromonas hydrophila isolated from industrial effluent. Biotechnol Res Int. 2011:1-11. [Disponible en anglais seulement]
Panandiker A, Mauru GB, Rao KVK. 1994. Dose-response effects of Malachite Green on free radical formation, lipid peroxidation and DNA damage in Syrian hamster embryo cells and their modulation nby antioxidants. Carcinogen. 15(11):2445-2448. [Disponible en anglais seulement]
Pagga U, Brown D. 1986. The degradation of dyestuffs: Part II behaviour of dyestuffs in aerobic biodegradation tests. Chemosphere. 15(4):479-491. [Disponible en anglais seulement]
Perez-Estrada LA, Aguera A, Hernando MD, Malato S, Fernandez-Alba AR. 2008. Photodegradation of Malachite Green under natural sunlight irradiation: Kinetic and toxicity of the transformation products. Chemosphere. 70(11):2068-75. [Disponible en anglais seulement]
Phillips JC, Mendis D, Eason CT, Gangolli SD.1980. The metabolic disposition of 14C-labelled Green S and Brilliant Blue FCF in the rat, mouse and guinea-pig. Food Cosmet Toxicol. 18(1):7-13. [Disponible en anglais seulement]
Poe WE, Wilson RP. 1983. Absorption of Malachite Green by channel catfish. Prog Fish Cult. 45(4):45228-229. [Disponible en anglais seulement]
Princz J, Bonnell M, Ritchie E, Velicogna J, Robidoux P, Scroggins R. 2014. Estimation of the bioaccumulation potential of a non-chlorinated bisphenol and an ionogenic xanthene dye to Eisenia andrei in field-collected soils, in conjunction with predictive in silico profiling. Environ Toxicol Chem. 33(2):308-316. [Disponible en anglais seulement]
Ross LG, Ward KMH, Ross B. 1985. The effects of formalin, Malachite Green and suspended solids on the respiratory activity of rainbow trout, Salmo gairdneri Richardson. Aquac Res. 16(2):129- 138. [Disponible en anglais seulement]
Santé Canada. 1995. Enquête sur l’exposition des êtres humains aux contaminants dans le milieu : Un guide pour les calculs de l’exposition. Ottawa (ON), gouvernement du Canada.
Santé Canada. 1998. Exposure factors for assessing total daily intake of priority substances by the general population of Canada. Rapport non plublié. Ottawa (ON): gouvernement du Canada. [Disponible en anglais seulement]
Santé Canada. [modifié le 4 juin 2010]. Liste des drogues approuvées au Canada pour les animaux aquatiques destinés à la consommation. Ottawa (ON), gouvernement du Canada. [consulté le 29 mars 2017].
Santé Canada. [modifié le 7 octobre 2015a]. Liste des colorants autorisés. Ottawa (ON), gouvernement du Canada. [consulté le 27 septembre 2016].
Santé Canada. [modifié le 14 décembre 2015b]. Liste critique des ingrédients de cosmétiques : Liste des ingrédients dont l’usage est interdit dans les cosmétiques. Ottawa (ON), gouvernement du Canada. [consulté le 21 avril 2017].
Santé Canada. 2019. Santé Canada met les Canadiens en garde contre le risque de cancer associé au violet cristallisé. Ottawa (ON), gouvernement du Canada. [consulté le 25 juin 2019].
[SCCNFP] Scientific Committee on Cosmetic Products and Non-Food Products Intended for Consumers. 2004. Opinion of the SCCNFP concerning Acid Blue 9. COLIPA No. C40. SCCNFP/0787/04. Bruxelles (BE): Commission européenne. [Disponible en anglais seulement]
[SCCS] Scientific Committee on Consumer Safety. 2016. Revision of the SCCS notes of guidance for the testing of cosmetic ingredients and their safety evaluation, 9th revision [PDF]. Bruxelles (BE): Commission européenne. [Disponible en anglais seulement]
[SCBT] Santa Cruz Biotechnology. c2007-2017. Victoria Blue BO (CAS 2390-60-5). Dallas (TX). [Disponible en anglais seulement]
Schenker U, Macloed M, Cheringer M, Hungerbühler K. 2005. Improving data quality for environmental fate models: A least square adjustment procedure for harmonizing physicochemical properties of organic compounds. Environ Sci Technol. 39(21):8434-8441. [Disponible en anglais seulement]
Seifried HE, Seifried RM, Clarke JJ, Junghans TB, San RHC. 2006. A compilation of two decades of mutagenicity test results with the Ames Salmonella typhimurium and L5178Y mouse lymphoma cell mutation assays. Chem Res Toxicol. 19:627-644. [Disponible en anglais seulement]
[Sigma-Aldrich]: Sigma-Aldrich Co. LLC. c2017. Oakville (Ont). [consulté le 28 août 2017]. [Disponible en anglais seulement]
Srivastava S, Sinha R, Roy D. 2004. Toxicological effects of Malachite Green. Aquat Toxicol. 66(3):319-329. [Disponible en anglais seulement]
Statistique Canada. 2004. Enquête sur la santé dans les collectivités canadiennes - Nutrition (ESCC). Information détaillée pour 2004 (Cycle 2.2) [Internet]. Ottawa (ON), Statistique Canada.
Statistique Canada. 2012. Enquête canadienne sur les mesures de la santé (ECMS) - Cycle 1. Ottawa (ON), Statistique Canada.
Stammati A, Nebbia C, De Angelis I, Albo AG, Carletti M, Rebecchi C, Zampaglioni F, Dacasto M. 2005. Effects of Malachite Green (MG) and its major metabolite, Leucomalachite Green (LMG), in two human cell lines. Toxicol in Vitro. 19(7):853-858. [Disponible en anglais seulement]
Sundarrajan M, Fernandis AZ, Subrahmanyam G, Prabhudesai S, Krishnamurthy SC, Rao KV. 2000. Overexpression of G1/S cyclins and PCNA and their relationship to tyrosine phosphorylation and dephosphorylation during tumor promotion by Metanil Yellow and Malachite Green. Toxicol Lett. 116: 119-130. [Disponible en anglais seulement]
Tanaka T, Takahasi O, Inomata A, Ogata A, Nakae D. 2012. Reproductive and neurobehavioral effects of Brilliant Blue FCF in mice. Birth Defects Res B Dev Reprod Toxicol. 95(6):395-409. [Disponible en anglais seulement]
[TIMES] TIssue MEtabolism Simulator [prediction module]. 2016. Ver. 2.27.19. Bourgas (BG): University “Prof. Dr. Assen Zlatarov”, Laboratory of Mathematical Chemistry. [Disponible en anglais seulement]
Tonogai Y, Ogawa S, Ito Y, Iwaida M. 1982. Actual survey on TLm (median tolerance limit) values of environmental pollutants, especially on amines, nitriles, aromatic nitrogen compounds and artificial dyes. J Toxicol Sci. 7(3):193-302. [Disponible en anglais seulement]
Tsai RS, El Tayar N, Testa B. 1991. Toroidal coil centrifugal partition chromatography, a method for measuring partition coefficients. J Chromatogr. 538(1):119-123. [cité dans EpiSuite c2000-2012]. [Disponible en anglais seulement]
[US EPA] US Environmental Protection Agency. 2002. Flexographic ink options: A cleaner technologies substitutes assessment [PDF]. Washington (DC): US EPA, Office of Pollution Prevention and Toxics. [Disponible en anglais seulement]
[US EPA] US Environmental Protection Agency. 2011. Age dependent Adjustment Factor (ADAF) application. Final Report. Washington (DC): US EPA, Office of Water Policy. [Disponible en anglais seulement]
[US EPA] US Environmental Protection Agency. 2013. FD&C Blue No. 1; exemption from the requirement of a tolerance. Federal Register. 78(186):58886-58890. [Disponible en anglais seulement]
Van Heerden E, Van Vuren JHJ, Steyn GJ. 1995. LC50 determination for Malachite Green and formalin on rainbow trout (Oncorhynchus mykiss) juveniles. Water SA. 21(1):87-94. [Disponible en anglais seulement]
Wakelin LPG, Adams A, Hunter C, Waring MJ. 1981. Interaction of Crystal Violet with nucleic acids. Biochemistry. 20:5779-5787. [cité dans Docampo et Moreno 1990]. [Disponible en anglais seulement]
Wan MT, Watts RG, Moul DJ. 1991. Acute toxicity to juvenile pacific northwest salmonids of basacid blue NB755 and its mixture with formulated products of 2,4-D, Glyphosate, and Triclopyr. Bull Environ Contam Toxicol. 47(3):471-478. [Disponible en anglais seulement]
[WATERNT] Water Solubility Program [modèle d’estimation]. 2010. Ver. 1.01. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Disponible en anglais seulement]
White CR, Davies SJ, Henry TB. 2012. Malachite green toxicity and effects on reproductive success in zebrafish Danio rerio. Zebrafish. 9(3):135-139. [Disponible en anglais seulement]
Willheim R, Ivy AC. 1953. A preliminary study concerning the possibility of dietary carcinogenesis. Gastroenterology. 23:1-19. [cité dans EFSA 2010]. [Disponible en anglais seulement]
Williams FM, Rothe H, Barrett G, Chiodini A, Whyte J, Cronin MTD, Monteiro-Riviere NA, Plautz J, Roper C, Westerhout J. 2016. Assessing the safety of cosmetic chemicals: consideration of a flux decision tree to predict dermally delivered systemic dose for comparison with oral TTC (Threshold of Toxicological Concern). Regul Toxicol Pharmacol. 76:174-186. [Disponible en anglais seulement]
Wolfe AD. 1977. Influence of cationic triphenylmethane dyes upon DNA polymerization and product hydrolysis by Escherichia coli polymerase I. Biochemistry. 16(1):30-33. [cité dans NTP 2005]. [Disponible en anglais seulement]
Wormuth M, Scheringer M, Vollenweider M, Hungerbuhler K. 2006. What are the sources of exposure to eight frequently used pthalic acid esters in Europeans? Risk Anal 26(3):803-824. [Disponible en anglais seulement]
[WSKOWWIN] Water Solubility for Organic Compounds Program for Microsoft Windows [estimation model]. 2010. Ver. 1.42. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Disponible en anglais seulement]
Xie J, Peng T, Chen DD, Zhang QJ, Wang GM, Wang X, Guo Q, Jiang F, Chen D, Deng JJ. 2012. Determination of Malachite Green, crystal violet and their leuco-metabolites in fish by HPLC-VIS detection after immunoaffinity column clean-up. J Chromatogr B Analyt Technol Biomed Life Sci. 913-914:123-128. [Disponible en anglais seulement]
Xu R, Pelicano H, Zhou Y, Carew JS, Feng L, Bhalla KN, Keating MJ, Huang P. 2005. Inhibition of glycolysis in cancer cells: a novel strategy to overcome drug resistance associated with mitochondrial respiratory defect and hypoxia. Cancer Res. 65(2):613-621. [Disponible en anglais seulement]
Yasuhiro, N. 1984. Toxicity of agrochemicals to freshwater organisms. CV. Dyes. (in Japanese) Suisan Zoshoku 32:173-175. [cité dans Flury et Fuhler 1994]. [Disponible en anglais seulement]
Zhijun T, Lihong X, Mengmeng G, Hongyan W, Yanhua J, Zhaoxin L, Yuxiu Z. 2011. Persistence of Malachite Green and leucoMalachite Green in perch (Lateolabrax japonicus). Chin J Oceanol Limnol. 29(3):647-655. [Disponible en anglais seulement]
Annexe A. Toxicité pour les milieux aquatiques
| Nom commun | Organisme d’essai | Paramètre | Effet | Valeur (mg/L) | Référence |
|---|---|---|---|---|---|
| Basic violet 3 | Médaka (Oryzias latipes) | CL50 48 h | Mortalité | 0,1 | Tonogai et coll. 1982 |
| Malachite green | Truite arc-en-ciel (Oncorhynchus mykiss) | CL50 96 h | Mortalité | 0,25 | Bills et coll. 1977 |
| Malachite green | Crapet arlequin (Lepomis macrochirus) | CL50 96 h | Mortalité | 0,03 | Bills et coll. 1977 |
| Malachite green | Truite brune(Salmo trutta morpha lacustris) | CL50 96 h | Mortalité | 0,22 | Bills et coll. 1977 |
| Malachite green | Achigan à petite bouche (Micropterus dolomieu) | CL50 96 h | Mortalité | 0,045 | Bills et coll. 1977 |
| Malachite green | Anguille d’Amérique (Anguilla rostrata) | CL50 96 h | Mortalité | 0,27 | Hinton et Eversole 1978 |
| Malachite green | Anguille d’Amérique (Anguilla rostrata) | CL50 96 h | Mortalité | 2,86 | Hinton et Eversole 1978 |
| Malachite green | Médaka (Oryzias latipes) | CL50 48 h | Mortalité | 0,32 | CITI 1992 |
| Malachite green | Bactéries (Vibrio fischeri) | CE50 30 min. | Réduction de la biolumi-nescence | 0,031 | Hernando et coll. 2007 |
| Malachite green | Truite arc-en-ciel (Oncorhynchus mykiss) | CL50 96 h | Mortalité | 0,267 | Van Heerden et coll. 1995 |
| Malachite green | Médaka (Oryzias latipes) | CL50 48 h | Mortalité | 0,3 | Tonogai et coll. 1982 |
| Malachite green | Anguille d’Amérique (Anquilla rostrata) | CL50 96 h | Mortalité | 0,54 | Hinton et Eversole 1979 |
| Malachite green | Embryons de poisson-zèbre (Danio rerio) | CL50 96 h | Mortalité | 0,042 | White et coll. 2012 |
| Malachite green | Larve du poisson-zèbre (Danio rerio) | CL50 96 h | Mortalité | 0,376 | White et coll. 2012 |
| Oxalate de vert de malachite | Embryons de poisson-zèbre (Danio rerio) | CL50 96 h | Mortalité | 0,331 | White et coll. 2012 |
| Oxalate de vert de malachite | Embryons de poisson-zèbre (Danio rerio) | CL50 96 h | Mortalité | 0,264 | White et coll. 2012 |
| Malachite green | Cladocère (Daphnia magna) | CE50 48 h | Croissance | 0,77 | Kanhere et coll. 2014 |
| Pigment blue 61 | Poissons | Exp. aiguë | S.O. | < 70 | US EPA 2002 |
| Pigment blue 61 | Invertébrés | Exp. aiguë | S.O. | < 70 | US EPA 2002 |
| Pigment blue 61 | Algues | Exp. aiguë | S.O. | < 10 | US EPA 2002 |
| Pigment blue 61 | Poissons | Exp. chronique | S.O. | < 7 | US EPA 2002 |
| Pigment blue 61 | Invertébrés | Exp. chronique | S.O. | < 7 | US EPA 2002 |
| Pigment blue 61 | Algues | Exp. chronique | S.O. | < 1 | US EPA 2002 |
| Pigment blue 61 | Cladocère (Daphnia magna) | CE50 48 h | Immobilisation | > 0,048 | CPMA 2016 |
| Pigment blue 61 | Algues (Pseudokirchneriella subcapitata) | CSEO 72 h | Réduction du taux de croissance | 0,422 | CPMA 2016 |
| Pigment blue 61 | Algues (Pseudokirchneriella subcapitata) | CSEO 72 h | Inhibition du rendement | < 0,422 | CPMA 2016 |
| Pigment blue 56 (analogue du Pigment Blue 61) | Poisson-zèbre (Brachydanio rerio) | CL50 96 h | Mortalité | > 500 | CPMA 2016 |
| Brilliant blue FCF | Médaka (Oryzias latipes) | CL0 48 h | Mortalité | > 3 000 | Tonogai et coll. 1978 |
| Brilliant blue FCF | Daphnia sp. | CL50 48 h | Mortalité | > 1 000 | Federal Registry 1988 |
| Brilliant blue FCF | Bactéries d’égout | S.O. | Réduction de l’activité | > 300 | Ciba 1989 |
| Brilliant blue FCF | Guppy (Poecilia reticulata) | CL0 48 h | Mortalité | > 500 | Ciba 1989 |
| Brilliant blue FCF | Escargot (Indoplanorbis exustus) | CL50 48 h | Mortalité | > 100 | Yasuhiro 1984 |
| Brilliant blue FCF | Ceriodaphnia dubia | CL50 3 h | Mortalité | > 100 | Yasuhiro 1984 |
| Brilliant blue FCF | Grenouille d’étang Nagoya daruma (Rana brevipoda porosa) | CL50 48 h | Mortalité | > 100 | Yasuhiro 1984 |
| Brilliant blue FCF | Crapaud commun japonais (Bufo bufo japanicus) | CL50 48 h | Mortalité | > 100 | Yasuhiro 1984 |
| Brilliant blue FCF | Carpe (Cyprinus carpio) | CL50 48 h | Mortalité | > 100 | Yasuhiro 1984 |
| Brilliant blue FCF | Saumon coho (Oncorhynchus kisutch) | CL50 96 h | Mortalité | 116 | Wan et coll. 1991 |
| Brilliant blue FCF | Saumon quinnat (Oncorhynchus tshawytscha) | CL50 96 h | Mortalité | 185 | Wan et coll. 1991 |
| Brilliant blue FCF | Saumon kéta (Oncorhynchus keta) | CL50 96 h | Mortalité | 213,5 | Wan et coll. 1991 |
| Brilliant blue FCF | Saumon rose (Oncorhynchus gorbuscha) | CL50 96 h | Mortalité | 119,5 | Wan et coll. 1991 |
| Brilliant blue FCF | Truite arc-en-ciel (Oncorhynchus mykiss) | CL50 96 h | Mortalité | 206 | Wan et coll. 1991 |
| Brilliant blue FCF | Saumon rouge (Oncorhynchus nerka) | CL50 96 h | Mortalité | 90 | Wan et coll. 1991 |
Abréviations : S.O. = sans objet; CSEO = concentration sans effet observé; CLx = concentration létale pour x % de la population; CEx = concentration entraînant un effet pour x % de la population.
Annexe B. Hypothèses utilisées dans les scénarios d’exposition environnementale
| Nom de la variable | Type d’information | Valeur | Unité | Source des données |
|---|---|---|---|---|
| Capacité de production du papier | Valeurs propres à la fabrique | RCC | t/j | Données compilées par ECCC |
| Taux d’utilisation du produit colorant | Distribution | P10 = 0,03P50 = 0,09P90 = 0,33 | kg/t | OCDE 2009 et communication personnelle, courriel du fournisseur, à la Direction générale de l’intendance environnementale, Environnement Canada, 2013; sans référence |
| Fraction d’un produit de papier contenant la substance | Valeur unique | 1 | Fraction | Hypothèse. Dans le pire scénario, supposer qu’une installation utilise le produit chimique pour teindre tout son papier dans une certaine mesure |
| Fraction de la matière première d’une fabrique qui provient du papier recyclé a | Valeurs propres à la fabrique | RCC | Fraction | Données compilées par ECCC |
| Fraction d’une substance colorante contenant un triarylméthane non sulfoné dans un produit colorant | Distribution | P10 = 0,27 P50 = 0,47 P90 = 0,64 | Fraction | ECCC 2019, IHS Markit 2018 |
| Fraction du produit chimique (Brilliant Blue FCF) dans un produit colorant | Distribution | P10 = 0,29 P50 = 0,51 P90 = 0,75 | Fraction | Markit 2018 et hypothèses professionnelles |
| Taux de rétention | Distribution | P10 = 0,89 P50 = 0,95 P90 = 0,99 | Fraction | Beatson 2012, OCDE 2009 |
| Taux d’élimination d’un STEU secondaire | Distribution | P10 = 0,82P50 = 0,88P90 = 0,92 | Fraction | Des modèles SimpleTreat ont été utilisés pour les taux d’élimination applicables des systèmes de traitement secondaire |
| Taux d’élimination d’un STEU en lagune | Distribution | P10 = 0,84 P50 = 0,86 P90 = 0,88 | Fraction | Modèles STP-EX exécutés pour les taux d’élimination applicables pour les systèmes en lagune. |
| Taux d’élimination d’un STEU primaire | Distribution | P10 = 0,51 P50 = 0,59 P90 = 0,67 | Fraction | Modèles SimpleTreat exécutés pour les taux d’élimination applicables pour les systèmes de traitement primaire. |
| Débit des effluents | Valeurs propres à la fabrique | RCC | m3/s | Données compilées par ECCC |
| Débit pour le plan d’eau récepteur | Valeurs propres au site de la fabrique | RCC | m3/s | Données compilées par ECCC. Le débit au 10e centile est utilisé. |
| Facteur de dilution | Valeurs propres au site de la fabrique | Maximum 10 | (sans unité) | Le facteur de dilution réel est utilisé lorsque le FD est inférieur à 10. Un FD maximal de 10 est utilisé lorsque le FD est supérieur à 10. |
Abréviations : RCC = renseignements commerciaux confidentiels; FD = facteur de dilution; ECCC = Environnement et Changement climatique Canada; P10 = valeur au 10e centile de la distribution; P50 = valeur au 50e centile de la distribution; P90 = valeur au 90e centile de la distribution; STEU = système de traitement des eaux usées.
a Le type de traitement utilisé dans le calcul dépend du type de système de traitement qui est associé à chaque fabrique, qu’il soit sur place ou hors site ou les deux, selon les besoins.
| Nom de la variable | Type d’information | Plage de valeurs | Unités | Source des données |
|---|---|---|---|---|
| Capacité de l’installation de désencrer le papier | Valeurs propres à la fabrique | RCC | t/j | Données compilées par ECCC |
| Fraction du papier recouvert d’encre | Distribution uniforme | 5–50 | % | Hypothèses |
| Quantité de couverture probable pour un morceau de papier et une quantité donnée d’encre | Distribution uniforme | 150 000 – 350 000 | po2 [papier]/lb [encre] | Hypothèses |
| Densité du papier | Distribution uniforme | 75–105 | g/m2 | Données compilées par ECCC |
| Concentration de la substance chimique dans l’encre (fraction) | Distribution uniforme | 0,0001–0,02 | Fraction | Données compilées par ECCC |
| Fraction de l’encre contenant la substance chimique d’intérêt | Distribution uniforme | 0,01–1,0 | Fraction | Hypothèses |
| Coefficient d’émission | Distribution uniforme | 0,1–0,2 | Fraction | Données compilées par ECCC |
| Débit d’effluents | Valeurs propres à la fabrique | RCC | m3/s | Données compilées par ECCC |
| Débit du plan d’eau récepteur | Valeurs fondées sur le site de la fabrique | RCC | m3/s | Données compilées par ECCC. Le débit au 10e centile est utilisé. |
| Facteur de dilution | Valeurs fondées sur le site de la fabrique | Maximum 10 | Sans unité | Le facteur de dilution réel est utilisé lorsque le FD est inférieur à 10. Un FD maximal de 10 est utilisé lorsque celui-ci est supérieur à 10. |
Abréviations : RCC = renseignements commerciaux confidentiels; FD = facteur de dilution; ECCC = Environnement et Changement climatique Canada; P10 = valeur au 10e centile de la distribution; P50 = valeur au 50e centile de la distribution; P90 = valeur au 90e centile de la distribution
| Nom de la variable | Type d’information | Plage des valeurs (%) | Unités | Source des données |
|---|---|---|---|---|
| Masse de la substance chimique traitée à l’installation | Distribution log-normale | RCC | (kg/année) | Données compilées par ECCC |
| Coefficient d’émission | Distribution uniforme | 0,002–0,011 | Fraction | Données compilées par ECCC |
| Jours de rejet | Valeur unique | 250 | Jours/an | Valeur standard pour les volumes importants de substance chimique, et utilisation continue. |
| Débit de l’effluent | Valeur propre à l’installation | RCC | m3/jour | Données compilées par ECCC |
| Débit du plan d’eau récepteur | Valeur fondée sur le site de l’installation | RCC | m3/s | Données compilées par ECCC. Le débit au 10e centile est utilisé. |
| Facteur de dilution | Valeur fondée sur le site de l’installation | Maximum 10 | Sans unité | Le facteur de dilution réel est utilisé lorsque le FD est inférieur à 10. Un FD maximal de 10 est utilisé lorsque le FD est supérieur à 10. |
Abréviations : RCC = renseignements commerciaux confidentiels; FD = facteur de dilution; ECCC = Environnement et Changement climatique Canada.
Annexe C. Exposition potentielle estimée des personnes aux triarylméthanes par les produits de consommation
Toutes les hypothèses (tableau C-2) sont les hypothèses par défaut de ConsExpo (ConsExpo 2006), sauf indication contraire. Pour les estimations de l’exposition cutanée, un facteur de rétention (FR) global de 1 a été utilisé. On a présumé que l’absorption par inhalation était de 100 %.
Approche du flux maximum
Afin de raffiner l’évaluation, l’approche du flux maximum (Jmax), telle que réalisée par Williams et coll. (2016), a été utilisée pour estimer l’exposition par voie cutanée pour le Malachite Green, le Basic Violet 4 et le Basic Blue 7.
Les équations utilisées sont présentées ci-dessous. Les valeurs de solubilité dans l’eau, la valeur log Koe et la masse moléculaire (MM) ont été obtenues à partir du tableau 3-1 du présent rapport d’évaluation préalable (lorsqu’elles étaient disponibles, les valeurs expérimentales ont été utilisées). Une vérification du bilan massique a également été effectuée pour chaque scénario. Voir le tableau C-2 ci-dessous.
Kp (équation de Potts et Guy, fondée sur un vecteur aqueux) :
log Kp (en cm/h) = -2,71 + (0,71)(log Koe) – (0,0061)(masse moléculaire, en g/mol)
Jmax :
Jmax (en mg/cm2/h) = Kp (en cm/h) × solubilité dans l’eau (en mg/cm3)
Quantité théorique maximale absorbée par jour (Qabs) :
Qabs (en mg) = Jmax (en mg/cm2/h) × superficie du contact cutané (en cm2) × durée de l’exposition (en h)
Exposition générale par voie cutanée = Qabs/p.c.
On obtient ainsi, pour l’exposition générale par voie cutanée, une estimation « par événement », où la fréquence d’exposition « F » est < 1/j. Elle représente une estimation « quotidienne » où « F » est ≥ 1/j. Cependant, il est à noter qu’il n’existe pas de scénario d’exposition pour le Malachite Green, le Basic Violet 4 ou le Basic Blue 7 qui entre dans cette dernière catégorie. L’ajustement d’une estimation « par événement » pour générer une estimation de l’exposition générale quotidienne a été effectué le cas échéant.
Une vérification du bilan massique a été effectuée par comparaison des valeurs Qabs avec la quantité totale de substance sur la peau (Qapp, valeur à laquelle il est fait référence dans le tableau C-2 sous le terme « charge cutanée »).
Pour la vérification du bilan massique :
Qapp = Concentration x quantité de produit x FR (voir les scénarios d’exposition individuelle dans le tableau C-2 pour des valeurs précises; il est à noter que F ne s’applique pas à la vérification du bilan massique, car il n’existe pas de scénarios d’exposition pour lesquels la fréquence d’exposition dépasse une fois par jour).
Si Qabs > Qapp, alors la valeur Qapp (équivalente à 100 % d’absorption cutanée) a été utilisée pour caractériser la quantité absorbée. Sinon, on a utilisé la valeur Qabs.
| Scénario d’exposition substance et produit sentinelle | Groupes d’âge | Jmax (mg/cm2/h) | Qabs (mg) |
|---|---|---|---|
| Malachite green, colorants capillaires semi-permanents | Adolescent, adulte | 0,0013 | 20 |
| Basic violet 4, colorants capillaires semi-permanents | Adolescent, adulte | 8,7 x 10-4 | 13 |
| Basic blue 7, colorants capillaires semi-permanents | Adolescent, adulte | 0,072 | 1,1 x 103 |
a Voir les scénarios d’exposition dans le tableau C-2 pour la fréquence (F), si pertinent.
b Voir le tableau C-2 pour plus de détails sur les scénarios d’exposition « par événement » et « quotidienne ».
Dose quotidienne moyenne à vie (DQMV)
La DQMV a été calculée afin d’approfondir l’exposition cutanée aux scénarios d’exposition au Basic Violet 4, pour des colorants capillaires semi-permanents, afin de tenir compte de l’utilisation de ce produit par les adolescents et les adultes, et pour estimer le risque de cancer dû à l’exposition quotidienne au Basic Violet 3 par l’eau potable. Voici les hypothèses et l’équation utilisées :
EGQ : exposition générale quotidienne
Longévité moyenne (LM) : 70 ans (US EPA, 2011)
Durées des groupes d’âge (DA) : 0,5 an pour les nourrissons (0 à 0,5 an), 4,5 ans pour les tout-petits (0,5 à 4 ans), 7 ans pour les enfants (5 à 11 ans), 8 ans pour les adolescents (12 à 19 ans) et 50 ans pour les adultes (20 ans et +) (Santé Canada 1998).
DQMV = [[(EGQnourrissons × DAnourrissons) + (EGQtout-petits × DAtout-petits) + (EGQenfants × DAenfants) + (EGQadolescents × DAadolescents) + (EGQadultes × DAadultes)] / [LM]
Exposition cutanée au Brilliant Blue FCF
La dose absorbable potentielle de Brilliant Blue FCF, d’après l’étude du flux cutané par Lucová et coll. (2013) a été utilisée afin de caractériser l’exposition générale pour chaque scénario d’exposition par voie cutanée. Voici les paramètres, les algorithmes et les facteurs qui ont été utilisés :
SEP : superficie exposée de la peau
DPA : dose potentielle absorbable (pendant une exposition de 24 heures)
F : fréquence d’exposition
Conc. : concentration
FR : facteur de rétention
Exposition générale par événement = (SEP x DPA)/p.c.
Pour la vérification du bilan massique :
Charge cutanée (totale) = conc. × qté de produit × FR × F
(où « F » est seulement incorporé si > 1)
Si l’exposition générale par événement était inférieure à la charge cutanée (totale), on a utilisé l’exposition générale par événement pour caractériser l’exposition générale, étant donné l’absence d’épuisement complète de la dose. Sinon, la charge cutanée (totale) a été utilisée (en raison de l’épuisement complet de la dose). Lorsque « F » est > 1/j, on peut utiliser l’exposition générale par événement comme estimation de l’exposition générale quotidienne, car la valeur « DPA » représente la quantité cumulative absorbée sur 24 heures.
| Substance | Scénario d’exposition sentinelle | Hypothèses a |
|---|---|---|
Malachite green, Basic Violet 4 et Basic Blue 7 | Colorants capillaires (semi-permanents) | Concentration : £ 1 % pour le Malachite Green, £ 0,1 % pour le Basic Violet 4 et £ 0,03 % pour le Basic Blue 7 (2016, courriel de la Direction de la Sécurité des produits de consommation, Santé Canada au Bureau d’évaluation du risque des substances existantes, Santé Canada; sans référence) Groupe d’âge : Adolescents et adultes Poids corporel (p.c.) : 59,4 kg pour les adolescents et 70,9 kg pour les adultes. Fréquence (F) : 0,0099/j pour les adolescents (Statistique Canada 2012)b et 0,036/j pour les adultes (SCCS 2016). Quantité de produit : 35 g/application (SCCS, 2011a) Facteur de rétention (FR) : 0,1 (SCCS 2016). Superficie de contact de la peau : 637,5 cm2 (basé sur ½ de la superficie d’une tête d’adulte; Santé Canada 1995). Durée de l’exposition : 24 h/jour
Pour l’exposition par événement et l’exposition cutanée quotidienne, voir l’approche Jmax ci-dessus (Williams et coll. 2016)é
Pour la vérification du bilan massique (exposition par événement et exposition cutanée quotidienne) : Charge cutanée = conc. × quantité de produit × FR |
Brilliant blue FCF | Utilisation non médicinale dans un produit de santé naturel | Quantité par dose (Qté) : 200 mg/cuillère (2017, courriel de la Direction des produits de santé naturels et sans ordonnance, Santé Canada au Bureau d’évaluation du risque des substances existantes, Santé Canada; sans référence). Dose quotidienne maximale (DQM) = 1 cuillerée (2017, courriel de la Direction des produits de santé naturels et sans ordonnance, Santé Canada au Bureau d’évaluation du risque des substances existantes, Santé Canada; sans référence). Groupe d’âge : Adultes. Poids corporel (p.c.) : 70,9 kg Fréquence (F) = 1/j
Pour l’exposition orale quotidienne estimée : = (Qté x DQM x F)/(p.c.) |
Brilliant blue FCF | Crème pour le corps | Concentration (Conc) : £ 10 % (2016, courriel de la Direction de la Sécurité des produits de consommation, Santé Canada au Bureau d’évaluation du risque des substances existantes, Santé Canada; sans référence). Groupe d’âge : Nourrissons et adultes. Poids corporel (p.c.) : 7,5 kg pour les nourrissons et 70,9 kg pour les adultes.
Pour l’exposition cutanée quotidienne estimée : Superficie de contact de la peauc : 3 020 cm2 pour les nourrissons et 16 925 cm2 pour les adultes (Santé Canada 1995). Quantité de produit par application = 1,4 g pour les nourrissons et 4,4 g pour les adultes (Wormuth et coll. 2006; Loretz et coll. 2005). DPA : 17 ng/cm2 (Lucová et coll. 2013). Fréquence (F) = 1,7/j pour les nourrissons et 1,1/j pour les adultes (Wormuth et coll. 2006; Loretz et coll. 2005).
Voir ci-dessus au sujet de l’approche pour l’estimation de la dose potentielle absorbable. |
Brilliant blue FCF | Parfum en aérosol | Concentration : £ 30 % (2016, courriel de la Direction de la sécurité des produits de consommation de Santé Canada au Bureau de l’évaluation du risque des substances existantes de Santé Canada, sans référence). Groupe d’âge : Adolescents et adultes. Masse corporelle : 59,4 kg pour l’adolescent et 70,9 kg pour l’adulte.
Pour l’exposition par inhalation quotidienne estimée, on a utilisé les paramètres par défaut pour le modèle de pulvérisation – parfum d’eau de toilette (ConsExpo Web 2016)d, sauf indication contraire : Fréquence d’exposition : 1,7/j (Loretz et coll., 2005). Mode de diffusion : aérosol (vers la personne). Durée de la vaporisation : 0,08 min. Durée de l’exposition : 5 min. Volume de la pièce : 10 m3 Hauteur de la pièce : 2,5 m Taux de renouvellement de l’air : 2 h-1 Volume du nuage : 0,0625 m3 Taux de production de masse : 0,1 g/s Fraction dans l’air : 0,02 g/g Densité non volatile : 1,5 g/cm3 Diamètre médian des particules : 2,7 µm Diamètre maximal des particules : 50 µm Diamètre limite pour l’inhalation : 10 µm Taux d’inhalation (adulte; valeur utilisée pour les adultes et les adolescents, car elle englobe ces deux sous-populations) : 16,2 m3/j (Santé Canada 1998) |
a Les tranches d’âge étaient les suivantes : nourrissons : 0 à 6 mois, tout-petits : 0,5 à 4 ans, enfants : 5 à 11 ans, adolescents : 12 à 19 ans, adultes : 20 à 59 ans. Les poids corporels par défaut ont été obtenus de Santé Canada (1998).
b La question posée par Statistique Canada (2012) dans son enquête portait sur les « colorants capillaires » génériques et ne précisait pas le type (p. ex., colorants permanents, semi-permanents, temporaires). L’ensemble de données utilisé portait sur le groupe des 12 à 19 ans pour les colorants capillaires semi-permanents (valeur médiane utilisée).
c Surface corporelle totale moins la surface de la tête.
d Scénario par défaut pour l’application sous forme d’exposition à un produit vaporisé. On a utilisé les données de vaporisation tirées de la fiche d’information pour les eaux de toilette dans ConsExpo Web (2016).
Annexe D. Points de départ pour la caractérisation des risques pour la santé humaine
| Substance | Exposition par événement | Exposition quotidienne (générale) |
|---|---|---|
Basic violet 3 | Étude de toxicité pour le développement (lapins, gavage) Toxicité maternelle (mortalité accrue, diminution du poids corporel et prise de poids corporel, signes cliniques) et diminution du poids corporel des fœtus à la DMENO de 0,5 mg/kg p.c./j (DMinE) | Valeur par défaut pour les points de départ associés à l’exposition par événement. [La DMENO (DMinE) de 14,3 mg/kg p.c./j (érythropoïèse accrue dans la rate, atrophie des ovaires) provenant d’une étude de cancérogénicité par le régime alimentaire chez les souris femelles n’aurait pu assurer la protection contre les effets potentiels à la DMENO de 0,5 mg/kg p.c./j.] |
Malachite green | Étude de toxicité pour le développement (lapins, gavage, oxalate de vert de malachite) Pertes préimplantation accrues et résorptions fœtales précoces, diminution du taux de survie des fœtus, diminution du poids corporel des fœtus et écarts squelettiques accrus à la DMENO de 5 mg/kg p.c./j (DMinE) | Valeur par défaut pour les points de départ associés à l’exposition par événement. [La DSENO de 7 mg/kg p.c./j provenant d’une étude de cancérogénicité par le régime alimentaire chez le rat n’aurait pu assurer la protection contre les effets potentiels pour le développement à la DMENO de 5 mg/kg p.c./j.] |
Pigment blue 61 | S.O. | S.O. |
Basic violet 4 | Étude de toxicité pour le développement (rats, gavage, acétate de violet d’éthyle) Aucun effet sur les mères ou le développement n’a été observé à la DSENO de 12 mg/kg p.c./j (DMaxE) | S.O. |
Basic blue 7 | Étude de toxicité pour le développement (rats, gavage, acétate de violet d’éthyle) Aucun effet sur les mères ou le développement n’a été observé à la DSENO de 12 mg/kg p.c./j (DMaxE) | S.O. |
Brilliant blue FCF | S.O. | Étude de toxicité pour la reproduction de 2 ans, avec une phase in utero (rats, régime alimentaire) DSENO de 631 mg/kg p.c./j basée sur la diminution du poids corporel et le taux de survie chez les femelles à 1 318 mg/kg p.c./j. |
Abréviations : DMaxE = dose maximale d’essai, DMENO = dose minimale entraînant un effet nocif observé, DMinE = dose minimale d’essai, S.O. = sans objet, DSENO = dose sans effet nocif observé.
La DR10 de 16,8 mg/kg p.c./j a été utilisée pour estimer le risque de cancer dans tous les scénarios d’exposition quotidienne par voie cutanée et voie orale, pour le Basic Violet 3, le Basic Violet 4 et le Basic Blue 7. Cette valeur était basée sur l’augmentation des carcinomes hépatocellulaires chez les souris femelles ayant reçu du Basic Violet 3, dans une étude de cancérogénicité.
