Évaluation préalable pour le Défi concernant
Archivée
les siloxanes et silicones, diméthyl-, terminés par un atome d’hydrogène
Numéro de registre du Chemical Abstracts Service
70900-21-9
Environnement Canada
Santé Canada
Septembre 2011
Table des matières
- Sommaire
- Introduction
- Identité de la substance
- Propriétés physiques et chimiques
- Sources
- Utilisations
- Rejets dans l'environnement
- Devenir dans l'environnement
- Persistance et potentiel de bioaccumulation
- Potentiel d'effets nocifs sur l'environnement
- Potentiel d'effets nocifs sur la santé humaine
- Conclusion
- Références
- Annexe I : Rapport entre la viscosité, le degré de polymérisation et la masse moléculaire (Wacker, 1992, et Fendinger et al., 1997)
- Annexe II : Table de résumé des données du modèle PBT
- Annexe III : Estimation des concentrations de MHDnMH dans les milieux naturels à l'aide du modèle ChemCAN, version 6.00 (ChemCAN, 2003)
- Annexe IV : Estimations de l'exposition cutanée au MHDnMH liée à l'utilisation de soutiens-gorges jetables, de crème décolorante pour la peau, de maquillage pour les yeux et de rouge à lèvres
Conformément à l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE (1999)], les ministres de l’Environnement et de la Santé ont effectué une évaluation préalable de la substance MHDnMH (siloxanes et silicones, diméthyl-, terminés par un atome d’hydrogène), dont le numéro de registre du Chemical Abstracts Service est 70900-21-9. Une priorité élevée a été accordée à l’évaluation préalable de cette substance inscrite au Défi ministériel, car, d’après les prévisions modélisées, elle répond aux critères de la catégorisation écologique relatifs à la persistance, au potentiel de bioaccumulation et à la toxicité intrinsèque pour les organismes non humains et on croit qu’elle est commercialisée au Canada.
L’évaluation des risques que présente le MHDnMH pour la santé humaine n’a pas été jugée hautement prioritaire à la lumière des résultats fournis par les outils simples de détermination du risque d’exposition et du risque pour la santé élaborés aux fins de la catégorisation des substances de la Liste intérieure des substances. Par conséquent, la présente évaluation est axée sur les renseignements utiles à l’évaluation des risques pour l’environnement.
À l’origine, le MHDnMHC a été classé dans la catégorie des UVCB organiques (substances de composition inconnue ou variable, produits de réactions complexes ou matières biologiques) au cours de la catégorisation de la Liste intérieure des substances. D’après les nouveaux renseignements obtenus, la substance est considérée comme un polymère de siloxane organique.
Le MHDnMH n’est pas produit naturellement dans l’environnement. En 2006, entre 10 000 et 100 000 kg de cette substance ont été fabriqués au Canada, et moins de 100 kg ont été importés au pays.
Selon l’utilisation déclarée, le MHDnMH est fabriqué en tant que polymère intermédiaire, qui est par la suite exporté en vrac pour la fabrication de plastiques. Le procédé industriel utilisé entraîne le rejet du polymère en petite quantité dans les eaux usées, ainsi que dans l’air et le sol, mais dans une moindre mesure. Toutefois, les rejets totaux dans l’environnement ne sont pas importants.
Selon les données actuelles, la forme de MHDnMH commercialisée au Canada satisfait aux critères pour les polymères à exigences réglementaires réduites précisés dans le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères). Étant donné que les polymères sont souvent des mélanges complexes et que leur masse moléculaire varie en fonction du nombre d’unités répétées, deux formes du polymère de deux masses moléculaires différentes ont été prises en compte dans cette évaluation. Cette approche vise à répondre aux préoccupations liées aux formes du polymère ayant une masse moléculaire moyenne en nombre (p. ex., MHDnMH, où n = 34) et une masse moléculaire faible (p. ex., MHDnMH, où n = 5).
On a utilisé l’information relative un polymère de siloxane analogue, le polydiméthylsiloxane (PDMS), pour évaluer le MHDnMH. D’après les données sur l’analogue utilisées pour la lecture croisée, la substance devrait être persistante dans l’environnement. D’après l’information à propos de la bioaccumulation de l’analogue, et compte tenu de sa masse moléculaire relativement élevée, elle n’est probablement pas biodisponible et son potentiel de bioaccumulation dans les tissus adipeux des organismes devrait être faible. Elle répond donc aux critères de persistance énoncés dans le Règlement sur la persistance et la bioaccumulation, mais ne répond pas à ceux de bioaccumulation. Qui plus est, les nouvelles données de toxicité modélisées et les données expérimentales sur un polymère analogue indiquent que le MHDnMH représente un faible risque pour les organismes qui se trouvent dans l’eau, le sol et les sédiments.
Aux fins de la présente évaluation préalable, un scénario d’exposition prudent a été élaboré. Selon ce scénario, les rejets industriels de MHDnMH ont lieu dans le milieu aquatique. La concentration estimée dans l’environnement (CEE) dans l’eau pour les organismes aquatiques était très inférieure à la concentration estimée sans effet (CESE). Par conséquent, d’après les renseignements inclus dans la présente évaluation préalable, le MHDnMH ne devrait pas pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou la diversité biologique, ni à mettre en danger l’environnement essentiel pour la vie.
Aucune donnée empirique relative aux effets sur la santé n’a été relevée pour le MHDnMH. En s’appuyant sur les données relatives aux effets sur la santé du PDMS, et sur les évaluations de cette substance qui sont fondées sur le poids de la preuve et qui ont été réalisées par des organismes internationaux, on estime que le MHDnMH présente un faible potentiel de risque.
Selon les concentrations estimées de MHDnMH dans l’environnement (air, eau potable et sol), l’exposition de l’ensemble de la population devrait être négligeable. Cette exposition peut avoir lieu par l’utilisation de produits de consommation qui contiennent du MHDnMH. Les marges entre l’estimation de la limite supérieure d’exposition pour le MHDnMH et les niveaux associés à des effets dans le cadre des études des effets du PDMS, l’analogue, sur la santé sont considérées comme adéquates pour tenir compte des incertitudes dans les bases de données des effets sur la santé et de l’exposition. On estime donc que le MHDnMH ne pénètre pas dans l’environnement en une quantité, à une concentration ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaines.
D’après les renseignements disponibles, il est conclu que la forme à exigences réglementaires réduites du MHDnMH ne satisfait à aucun des critères de l’article 64 de la LCPE (1999).
En raison de la complexité associée à la formulation du polymère et des propriétés potentiellement dangereuses associées aux polymères ayant une faible masse moléculaire, on craint que les utilisations nouvelles MHDnMH qui ne sont ni décelées ni évaluées en vertu de la LCPE (1999) fassent en sorte que les substances répondent aux critères de l’article 64 de la Loi. Pour cette raison, il est recommandé de modifier la Liste intérieure des substances de façon à indiquer que le MHDnMH répond aux critères pour les Polymères à exigences réglementaires réduites. Si d’autres formes du MHDnMH qui ne répondent pas aux exigences réglementaires réduites sont introduites sur le marché canadien, elles seront soumises aux exigences du Règlement sur les renseignements concernant les substances nouvelles.
La Loi canadienne sur la protection de l’environnement (1999) [LCPE (1999)] (Canada, 1999) exige que les ministres de l’Environnement et de la Santé procèdent à une évaluation préalable des substances qui répondent aux critères de catégorisation énoncés dans la Loi afin de déterminer si elles présentent ou sont susceptibles de présenter un risque pour l’environnement ou la santé humaine.
Selon l’information obtenue dans le cadre de la catégorisation, les ministres ont jugé qu’une attention hautement prioritaire devait être accordée à un certain nombre de substances, à savoir :
- celles qui répondent à tous les critères environnementaux de catégorisation, notamment la persistance (P), le potentiel de bioaccumulation (B) et la toxicité intrinsèque pour les organismes aquatiques (Ti), et que l’on croit être commercialisées au Canada;
- celles qui répondent aux critères de catégorisation pour le plus fort risque d’exposition (PFRE) ou qui présentent un risque d’exposition intermédiaire (REI) et qui ont été jugées particulièrement dangereuses pour la santé humaine, compte tenu des classifications qui ont été établies par d’autres organismes nationaux ou internationaux concernant leur cancérogénicité, leur génotoxicité ou leur toxicité pour le développement ou la reproduction.
Le 9 décembre 2006, les ministres ont donc publié un avis d’intention dans la Partie I de la Gazette du Canada(Canada, 2006) dans lequel ils priaient l’industrie et les autres intervenants de fournir, selon un calendrier déterminé, des renseignements précis qui pourraient servir à étayer l’évaluation des risques, ainsi qu’à élaborer et à évaluer les meilleures pratiques de gestion des risques et de bonne gestion des produits pour ces substances jugées hautement prioritaires.
On a décidé d’accorder une attention hautement prioritaire à l’évaluation des risques pour l’environnement du MHDnMH (siloxanes et silicones, diméthyl-, terminés par un atome d’hydrogène), car cette substance a été initialement jugée persistante, bioaccumulable et intrinsèquement toxique pour les organismes aquatiques au cours de la catégorisation visant la Liste intérieure des substances (LIS), et il semble qu’elle est commercialisée au Canada. Le volet du Défi portant sur cette substance a été publié dans laGazette du Canada le 26 septembre 2009 (Canada, 2009). En même temps a été publié le profil de cette substance, qui présentait l’information technique (obtenue avant décembre 2005) sur laquelle a reposé sa catégorisation. Des renseignements sur les propriétés et les utilisations de cette substance ont été reçus en réponse au Défi.
Même si l’évaluation des risques que présente le MHDnMH pour l’environnement est jugée hautement prioritaire, cette substance ne répond pas aux critères de catégorisation pour le PFRE ou le REI, ni aux critères définissant un grave risque pour la santé humaine, compte tenu du classement attribué par d’autres organismes nationaux ou internationaux quant à sa cancérogénicité, à sa génotoxicité ou à sa toxicité sur le plan du développement ou de la reproduction.
Les évaluations préalables mettent l’accent sur les renseignements jugés essentiels pour déterminer si une substance répond aux critères énoncés à l’article 64 de la LCPE (1999). Les évaluations préalables visent à examiner des renseignements scientifiques et à tirer des conclusions fondées sur la méthode du poids de la preuve et le principe de prudence[1].
La présente évaluation préalable prend en considération les renseignements sur les propriétés chimiques, les dangers, les utilisations et l’exposition, y compris ceux fournis dans le cadre du Défi. Les données qui ont trait à l’évaluation préalable de cette substance proviennent de documents originaux, de rapports de synthèse et d’évaluation, de rapports de recherche réalisés par des intervenants et de recherches documentaires menées récemment, soit jusqu’en mai 2010 dans le cas des sections du document portant sur la santé humaine, et jusqu’en décembre 2010 dans le cas des sections portant sur les aspects écologiques. Les études les plus importantes ont fait l’objet d’une évaluation critique. Par ailleurs, il est possible que les résultats de modélisation aient servi à formuler des conclusions.
Lorsqu’ils étaient disponibles et pertinents, les renseignements contenus dans les évaluations des dangers effectués par d’autres instances ont été utilisés. La présente évaluation préalable ne constitue pas un examen exhaustif ou critique de toutes les données disponibles. Il s’agit plutôt d’un sommaire des renseignements essentiels qui appuient la conclusion proposée.
La présente évaluation préalable a été préparée par le personnel du Programme des substances existantes de Santé Canada et d’Environnement Canada et elle intègre les résultats d’autres programmes exécutés par ces ministères. La partie portant sur l’écologie a fait l’objet d’une étude consignée par des pairs ou d’une consultation de ces derniers. De plus, l’ébauche de la présente évaluation a fait l’objet d’une période de commentaires de 60 jours par le public. Bien que les commentaires reçus de l’extérieur aient été pris en considération, Santé Canada et Environnement Canada sont seuls responsables du contenu final et des résultats de l’évaluation préalable. Les approches suivies pour les évaluations préalables dans le cadre du Défi ont été examinées par un groupe indépendant, soit le Groupe consultatif du Défi.
Les principales données et considérations sur lesquelles repose l’évaluation préalable sont résumées ci-après.
Aux fins du présent document, la substance « siloxanes et silicones, diméthyl-, terminés par un atome d’hydrogène » sera appelée MHDnMH, appellation tirée de sa structure chimique. « MH » fait référence à l’atome de silicone dans les groupes terminaux, qui partage une liaison avec l’oxygène, deux liaisons avec les substituants méthyle et une liaison avec l’hydrogène. « D » symbolise les atomes de silicone de la chaîne principale, qui partagent deux liaisons avec l’oxygène et deux liaisons avec les substituants méthyle, alors que « n » représente le nombre de « D » dans le polymère.
Le MHDnMH a initialement été classé dans la LIS comme un UVCB organique. Selon de nouveaux renseignements obtenus, le MHDnMH se caractérise par 1) la présence d’une unité monomère diméthyl-siloxy et 2) la présence de groupements hydrogène et diméthyle qui sont fixés à l’atome de silicone et qui agissent comme les groupes terminaux du polymère (Environnement Canada, 2010a).
D’après les résultats de la chromatographie sur gel (CG), chaque molécule de MHDnMH aurait une masse moléculaire moyenne en nombre (Mn) d’approximativement 2 700 g/mol (Environnement Canada, 2010a), ce qui correspond en moyenne à 34 unités monomériques diméthylsiloxy (n = 34, d’après la masse moléculaire du monomère diméthylsiloxy, soit 74,15| g/mol). Toute molécule de MHDnMH contient plus de trois monomères. Les différences dans les masses moléculaires (Mm) sont principalement dues aux différences dans le nombre d’unités. Par conséquent, le MHDnMH respecte la définition d’un polymère (OCDE, 1994), résumée ci-dessous :
- molécules caractérisées par une séquence d’un ou de plusieurs types d’unités monomères;
- plus de 50 % des molécules, en poids, possèdent trois unités monomères ou plus liées par covalence à au moins une unité monomère ou un réactif;
- moins de 50 % des molécules, en poids, ont la même masse moléculaire;
- les différences dans les masses moléculaires des molécules sont principalement attribuables à la différence dans le nombre d’unités monomères.
Des oligomères considérablement plus petits (dont la plus faible masse moléculaire fait ~ 500 g/mol) ont été décelés dans le produit polymérique, mais en très faibles concentrations. En outre, d’autres produits sont vendus dans le monde sous le même no CAS (70900-21-9), notamment le polymère ayant une masse moléculaire moyenne d’environ 500 g/mol (Gelest, 2010). Cette masse correspond à un polymère comptant cinq unités monomériques de diméthylsiloxy (n = 5). En raison des aspects susmentionnés, l’évaluation porte tant sur le MHD34MH que sur le MHD5MH afin de tenir compte des polymères de masse moléculaire moyenne en nombre et des polymères de faible masse moléculaire.
L’évaluation prend en considération les données essentielles sur les principaux paramètres pour l’évaluation de la persistance, de la bioaccumulation et de l’écotoxicité des polymères de masse moléculaire moyenne en nombre et des polymères de faible masse moléculaire. Dans certains cas, lorsqu’il n’existe pas de données expérimentales pour le MHDnMH, des données expérimentales de substances chimiques analogues et des modèles fondés sur les relations quantitatives structure-activité (RQSA) sont utilisés pour combler les lacunes.
L’identité du MHDnMH est présentée dans le tableau 1 ci-dessous.
Tableau 1. Identité du MHDnMH
| Numéro de registre du Chemical Abstracts Service (no CAS) | 70900-21-9 |
| Nom dans la LIS | Siloxanes et silicones, diméthyl-, terminés par un atome d’hydrogène |
| Noms relevés dans les National Chemical Inventories (NCI)[1] | Siloxanes and Silicones, di-Me, hydrogen-terminated (TSCA, REACH, ENCS, ECL, PICCS, ASIA-PAC, NZIoC) Siloxanes and silicones, dimethyl hydrogen terminated (AICS) SILOXANE, DI-ME, HYDROGEN TERMINATED (PICCS) |
| Autres noms | Di-Me, dimethylsilyl-terminated siloxanes FH 0023 Hydrogen-terminated di-Me silicones Hydrogen-terminated di-Me siloxanes MCR-H 07 MHD6MH Polysiloxanes, di-Me, hydrogen-terminated PS 542 SE 1886A SE 1887A Silicones, di-Me, dimethylsilyl-terminated Siloxanes and Silicones, di-Me, (dimethylsilyl)-terminated XF 40A6100 Diméthylsiloxanes et silicones, terminés par un atome d’hydrogène |
Groupe chimique (groupe de la LIS) |
Polymère |
| Principale classe chimique ou utilisation | Organosiliciums |
| Principale sous-classe chimique | Siloxane |
| Formule chimique | C(4+2n)H(14+6n)O(1+n)Si(2+n) |
| Structure chimique représentative utilisée dans le modèle d’estimation[2] |  |
| SMILES[3] | MHDnMH (n = 34) ou MHD34MH : sans objet MHDnMH (n = 5) ou MHD5MH : Si(C)(C)OSi(C)(C)OSi(C)(C)OSi(C)(C)OSi(C)(C)OSi(C)(C)OSi(C)(C) |
| Masse moléculaire | MHD34MH : 2 655,45 g/mol MHD5MH : 505,10 g/mol |
[2] Cette substance est un polymère organique défini, c’est-à-dire qu’elle n’est pas un composé chimique défini; elle peut donc être caractérisée par une structure représentative. Pour cette évaluation, deux structures représentatives ont été utilisées, soit une où n = 34 et une où n = 5.
[3] Simplified Molecular Input Line Entry System.
On note que le polymère peut contenir une petite fraction d’impuretés, c’est-à-dire des monomères ou des sous-produits résiduels qui ont une masse moléculaire beaucoup plus faible. La quantité et le type d’impuretés varient en fonction d’une série de facteurs, notamment les différents procédés de fabrication et d’exploitation, les conditions de réaction ainsi que l’utilisation de catalyseurs et de promoteurs. Selon les renseignements reçus (Environnement Canada, 2010a), l’octaméthylcyclotétrasiloxane (D4, no CAS 556-67-2), le décaméthylcyclopentasiloxane (D5, no CAS 541-02-6), le dodécaméthylcyclohezasiloxane (D6, no CAS 540-97-6) et le 1,1,3,3-tétratraméthyldisiloxane (no CAS 3277-26-7) sont des monomères résiduels ou des sous-produits dans les produits polymériques qui portent le même no CAS, soit 70900-21-9. Toutefois, la concentration de ces monomères résiduels et sous-produits varie dans les polymères fabriqués par des entreprises différentes. Le D4, le D5 et le D6 ont déjà été évalués dans le cadre du Défi et, selon les résultats de la CG, le 1,1,3,3-tétratraméthyldisiloxane n’a pas été détecté dans le MHDnMH présent dans le commerce au Canada. Par conséquent, le risque associé à la présence d’impuretés dans le polymère ne sera pas pris en compte dans cette évaluation du MHDnMH.
Contrairement aux substances définies, qui ont une masse moléculaire bien précise, les polymères ont une masse moléculaire variable en fonction du nombre d’unités répétées, qui peut être de trois jusqu’à plusieurs milliers. Pour cette raison, un polymère est habituellement caractérisé par le nombre moyen d’unités répétées qu’il contient ou sa masse moléculaire moyenne en nombre.
Comme le mentionne la section « Identité de la substance », le MHD34MH représente le polymère qui est fabriqué au Canada, alors que le MHD5MH est le produit polymérique produit à l’échelle internationale et dont la masse moléculaire est de 505,10 g/mol. Les approches pour l’évaluation de ces deux produits tiennent compte des différentes masses moléculaires.
Aux fins de l’évaluation, le nombre d’unités répétées (n) peut être indiqué si l’information ne s’applique qu’à l’une des deux formes mentionnées ci-dessus. Si le nombre d’unités répétées n’est pas indiqué, l’évaluation s’applique au polymère MHDnMH (n ≥ 5) en général.
Il n’existe pas de données expérimentales sur les propriétés physiques et chimiques du MHDnMH; des données sur une substance analogue, le polydiméthylsiloxane (PDMS), ont été prises en considération dans l’évaluation.
Un analogue est un produit chimique dont la structure est semblable à celle de la substance évaluée; il devrait donc avoir des propriétés physiques et chimiques, un devenir dans l’environnement et une toxicité similaires. Lorsque des données expérimentales existent pour une propriété particulière d’un analogue, elles peuvent être utilisées pour caractériser la substance évaluée, mais les différences structurelles pouvant avoir une incidence sur la biodisponibilité doivent être notées.
Le PDMS est un autre polymère de siloxane possédant la même unité récurrente de groupements diméthyle liés au silicium de la chaîne principale –Si-O-Si–. La différence entre le MHDnMH et le PDMS réside dans les unités terminales. Contrairement au MHDnMH, où les deux unités terminales comportent un atome d’hydrogène et deux groupements méthyle, le PDMS compte trois groupements méthyle (voir le tableau 2a ci-dessous) à chacune des positions terminales. On peut exprimer la formule du PDMS comme suit : MHDnM. Ces différences ne devraient pas avoir une incidence notable sur les propriétés chimiques et physiques du MHDnMH et du PDMS (lorsque le nombre d’unités récurrentes est le même dans les deux cas). Vu la similarité de ces substances chimiques, les données expérimentales sur le PDMS ont été utilisées pour évaluer le devenir dans l’environnement, le potentiel de persistance et de bioaccumulation, ainsi que l’écotoxicité des deux formes de MHDnMH (n = 5 et n = 34) sans qu’un ajustement qualitatif ne soit nécessaire.
Tableau 2a. Structure chimique du PDMS et du MHDnMH
| Paramètre | PDMS | MHDnMH |
|---|---|---|
| Structure chimique représentative |  |
 |
MHD5MH
Pour la forme de MHDnMH de faible masse moléculaire (n = 5), plusieurs méthylsiloxanes linéaires (MDnM) ont été utilisés à titre d’analogues (voir le tableau 2b ci-dessous). Ces méthylsiloxanes linéaires (n > 3) sont du PDMS de faible masse moléculaire.
Tableau 2b. Méthylsiloxanes linéaires utilisés comme analogues du MHD5MH
| Nom chimique et no CAS | Formule | Masse moléculaire (g/mol) |
|---|---|---|
| Dodécaméthylpentasiloxane (141-63-9) | MD3M | 384,84 |
| Tétradécaméthylhexasiloxane (107-52-8) | MD4M | 459,00 |
| Hexadécaméthylheptasiloxane (541-01-5) | MD5M | 533,15 |
| Siloxanes et silicones, diméthyl-, terminés par un atome d’hydrogène (70900-21-9) | MHD5MH | 505,10 |
- « M » fait référence aux atomes de silicone dans les groupes terminaux, qui partagent une liaison avec l’oxygène et trois liaisons avec les substituants méthyle.
- « MH » fait référence aux atomes de silicone dans les groupes terminaux, qui partagent une liaison avec l’oxygène, deux liaisons avec les substituants méthyle et une liaison avec l’hydrogène.
- « D » symbolise les atomes de silicone de la chaîne principale, qui partagent deux liaisons avec l’oxygène et deux liaisons avec les substituants méthyle.
Certaines données expérimentales sur les propriétés chimiques et physiques du MDnM ont été transposées au MD4M avec certains ajustements pour tenir compte des différences structurales (c’est-à-dire le nombre d’unités récurrentes). Des modèles RQSA ont également été utilisés pour combler les lacunes lorsqu’aucune donnée expérimentale n’existait pour certaines propriétés physiques et chimiques (voir l’annexe II). Ces modèles (excepté WSKOWWIN, 2008) sont principalement fondés sur des méthodes d’addition de fragments, c’est-à-dire qu’ils s’appuient sur la structure d’un produit chimique donné. Il est indiqué que les ensembles d’étalonnage de la plupart des modèles ne comprennent pas les siloxanes; par conséquent, le MHD5MH ne fait techniquement pas partie du domaine de ces modèles. Cependant, puisqu’une molécule de faible masse comme le MHD5MH demeure neutre dans les conditions observées dans l’environnement, les estimations fondées sur ses fragments et sa masse moléculaire devraient permettre d’obtenir des valeurs approximatives.
Les propriétés physiques et chimiques modélisées pour le MHD5MH sont résumées dans le tableau 2c ci-dessous. Les données expérimentales pour les méthylsiloxanes linéaires analogues (voir le tableau 2b) sont également présentées dans ce tableau. Afin d’améliorer la fiabilité des prévisions des modèles, une méthode d’ajustement des valeurs expérimentales (AVE) a été utilisée dans les sous-modèles d’EPIsuite. Cette méthode a permis d’obtenir des estimations à partir des mesures expérimentales, qui tiennent compte des différences structurelles entre l’analogue et le MHD5MH.
Tableau 2c. Propriétés physiques et chimiques estimées du MHD5MH (masse moléculaire = 505,10 g/mol)
| Propriété | Valeur[1] | Température (°C) |
Référence |
|---|---|---|---|
| Point de fusion (ºC) |
12,02 | MPBPWIN, 2008 | |
| -59 (pour le MD4M) | Gelest, 2008a[5] | ||
| Point d’ébullition (ºC) |
317,45 | MPBPWIN, 2008 | |
| 245 (pour le MD4M) | Gelest, 2008a | ||
| Masse volumique (kg/m3) |
890 (pour le MD4M) | Gelest, 2008a | |
| Viscosité[2] (centistokes, cSt) | 2,6 (pour le MD4M) | Gelest, 2008a | |
| Pression de vapeur (Pa) |
0,10 (7,69 × 10-4 mm Hg) |
25 | MPBPWIN, 2008 |
| < 1 mm Hg (pour le MD4M) | 25 | Gelest, 2008a | |
| Constante de la loi de Henry (Pa·m3/mol) |
2,0 × 107 (2,0 × 102 atm·m3/mol) |
HENRYWIN, 2008 | |
| Log Koe (coefficient de partage octanol-eau) (sans dimension) |
6,6 | KOWWIN, 2008 | |
| 6,7 (extrapolation par l’AVE du MD4M et du MD5M)[3] |
KOWWIN, 2008 | ||
| 6,0 (pour le MD3M) 6,6 (pour le MD4M) 7,2 (pour le MD5M) 7,7 (pour le MD6M) |
Bruggeman et al., 1984 | ||
| Log Kco (coefficient de partage carbone organique-eau) (sans dimension) |
5,7 | PCKOCWIN, 2008 | |
| Solubilité dans l’eau (mg/L) |
2,2 × 10-6 à 2,7 × 10-6 (d’après des log Koe de 6,6 et 6,7) |
25 | WSKOWWIN, 2008 |
| 5,7 × 10-9 à 2,2 × 10-6 (extrapolation par l’AVE du MD4M et du MD5M)[3] |
WATERNT, 2008 | ||
| 3,4 × 10-2 (pour le MDM) 7,0 × 10-5 (pour le MD3M) 1,3 × 10-5 (estimé pour le MD4M) 5,4 × 10-7 (estimé pour le MD5M) |
25 | Varaprath et al., 1996 WSKOWWIN, 2008 | |
| Diamètre transversal (nm)[4] | 1,46 à 2,18 | CPOP, 2008 |
[2] La viscosité d’un polymère est employée pour caractériser la taille des polymères et leur masse moléculaire. Le centistokes (cSt) est l’unité de mesure de la viscosité cinématique d’un polymère.
[3] Une méthode d’ajustement des valeurs expérimentales (AVE) a été utilisée dans EPIsuite pour obtenir des estimations à partir des mesures expérimentales, qui tiennent compte des différences structurelles.
[4] Les valeurs représentent l’étendue des diamètres moléculaires maximums (c.-à-d., les valeurs Dmax) estimés à l’aide du modèle CPOP.
[5] L’information tirée de Gelest (2008a) concerne un produit de MD4M (> 95 %), avec une fraction de MD3M et des siloxanes linéaires de masse moléculaire plus élevée (< 5 %).
D’après les données expérimentales du log Koe et de la solubilité dans l’eau du MD3-6M (voir le tableau 2c), les méthylsiloxaes de faible masse moléculaire sont extrêmement hydrophobes. Leur solubilité dans l’eau est peu élevée (de l’ordre de 10-4 mg/L et moins), et leur coefficient de partage octanol-eau est élevé (log Koe= 6 ou plus).
Comme il possède un hydrure en position terminale, le MHD5MH devrait avoir une solubilité dans l’eau et un coefficient de partage octanol-eau similaire à ceux de l’analogue PDMS de masse moléculaire équivalente. Les prévisions modélisées du log Koe pour le MHD5MH sont de 6,6 sans AVE et de 6,7 avec AVE, ce qui se rapproche des coefficients de partage octanol-eau pour le MD4M (log Koe = 6,6 ) et le MD5M (log Koe = 7,2). Les valeurs estimées de la solubilité dans l’eau du MHD5MH (obtenues à partir des valeurs du log Koe) vont de 2,2 × 10-6 mg/L à 2,7 × 10-6 mg/L; elles se situent donc entre celles du MD4M (1,3 × 10-5 mg/L) et du MD5M (5,4 × 10-7 mg/L).
Selon les prévisions des modèles, le MHD5MH devrait être peu volatil et insoluble dans l’eau. La pression de vapeur estimée est modérée (0,10 Pa) et la solubilité dans l’eau, très faible (~ 2,5 × 10-6 mg/L). La constante estimée de la loi de Henry est en conséquence très élevée, soit 2,0 × 107 Pa m3/mol.
MHD34MH
La masse moléculaire moyenne en nombre du polymère commercialisé au Canada (MHD34MH) est d’environ 2 700 g/mol. Aucune composante dans le polymère ne possède une masse moléculaire inférieure à 500 g/mol, et moins de 5 % des composantes ont une masse moléculaire inférieure à 1 000 g/mol. Ni les unités terminales ni les unités récurrentes du polymère ne comportent de groupements fonctionnels cationiques ou réactifs; la masse équivalente du groupe fonctionnel (MEGF)[2] du MHD34MH est donc supérieure à 1 000 g/mol, ce qui fait que le polymère satisfait aux critères définissant les polymères à exigences réglementaires réduites dans le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères).
Le MHD34MH a une masse moléculaire moyenne en nombre d’environ 2 700 g/mol, ce qui est plus élevé que la limite acceptable dans les modèles RQSA. Le MHD34MH se situe hors du domaine d’application des modèles de sorte qu’aucun modèle RQSA ne peut être utilisé pour évaluer cette substance. Par conséquent, des données transposées du PDMS par lecture croisée ont servi à caractériser les propriétés physiques et chimiques du MHD34MH.
Dans un test de toxicité, on a établi à 0,26 mg/L la solubilité d’un PDMS avec une terminaison hydroxyle (d’approximativement n = 45 et Mm = 3 500 g/mol, d’après la viscosité de 55 cSt pour le PDMS) dans l’eau, avec une concentration à l’équilibre de 0,04 à 0,05 mg/L (Gettings et Lane, 1982). Comme l’hydroxyle en position terminale accroît la solubilité du polymère dans une certaine mesure, on s’attend à ce que la solubilité du MHD34MH dans l’eau soit inférieure à 0,26 mg/L.
Pour les polymères de masse moléculaire élevée, il existe une relation entre la viscosité et la masse moléculaire moyenne (voir l’annexe I). La viscosité est une mesure de la résistance d’un liquide à l’écoulement lorsqu’une force est appliquée sur celui-ci. Il s’agit également d’une mesure de sa capacité à s’écouler. Plus la taille de la molécule du polymère est importante (nombre plus élevé d’unités monomères et masse moléculaire moyenne plus importante), plus le polymère sera « visqueux », ce qui se traduira par une valeur de viscosité élevée (voir l’annexe I). Dans nombre des études sur le PDMS citées dans la présente évaluation, la viscosité était indiquée et a été utilisée pour caractériser la masse moléculaire des polymères.
Les polymères de siloxane ayant une masse moléculaire élevée (y compris le PDMS) ne sont pas volatils et ne devraient se retrouver dans l’air et s’y dégrader (Graiver et al., 2003). Dans le cas d’un polymère avec une masse moléculaire moyenne supérieure à 1 000 g/mol, la pression de vapeur devrait être inférieure à 1,33 × 10-6 Pa (10-8 mm Hg) et la constante de la loi de Henry, inférieure à 1,01 × 10-3 Pa•m3/mol (10-8 atm•m3/mol) (USEPA, 2008). Vu la masse moléculaire élevée (2 655,45 g/mol) du MHD34MH, la forme n = 34 du polymère devrait avoir une pression de vapeur et une constante de la loi de Henry faibles.
Les polymères de siloxane sont des liquides dont l’écoulement est relativement libre, même à des masses moléculaires élevées (la viscosité peut atteindre 500 000 cSt, ce qui équivaut à une masse moléculaire moyenne d’environ 100 000 g/mol) [Fendinger et al., 1997]. Cette situation peut être attribuée au degré élevé de souplesse de la chaîne principale du siloxane et aux faibles forces d’attraction intermoléculaires qui en résultent. Le polymère est caractérisé par un faible point de fusion et un point élevé d’ébullition. Il reste donc à l’état liquide aux températures ambiantes normales (Fendinger et al., 1997; Graiver et al., 2003).
D’après les données sur le PDMS, le MHD34MH devrait être insoluble dans l’eau et son coefficient de partage octanol-eau (Koe) devrait être élevé. Le polymère ne contient pas de groupements fonctionnels pouvant subir une hydrolyse dans l’eau. S’il est rejeté dans l’eau, il pourrait former une fine couche à la surface de l’eau en raison de sa masse volumique légèrement plus faible que celle de l’eau (environ 960 kg/m3) (Fendinger et al., 1997; Environnement Canada, 2010a; ECETOC, 1994).
En considération de ce qui précède, la forme n = 5 du MHDnMH devrait avoir une pression de vapeur modérée; par contre, la forme n = 34 du polymère devrait devenir beaucoup moins volatile avec l’allongement de la chaîne.
Le polymère (tant la forme n = 5 que n = 34) devrait être insoluble dans l’eau, sa masse volumique étant légèrement plus faible que celle de l’eau, et demeurer à l’état liquide aux températures ambiantes.
Le MHDnMH ne serait pas produit naturellement dans l’environnement.
Des enquêtes menées auprès des industries en 2005 et 2006 par le truchement d’avis publiés dans la Gazette du Canada, conformément à l’article 71 de la LCPE (1999), ont permis de recueillir des renseignements (Canada, 2006). L’objectif consistait à recueillir des données sur la fabrication et l’importation de MHDnMH au Canada. Dans l’avis de 2006, on demandait également de fournir des données sur la quantité utilisée de cette substance.
En 2005, moins de quatre entreprises ont déclaré avoir fabriqué de 100 à 1 000 kg de MHDnMH au Canada ou en avoir importé de 1 001 à 100 000 kg au pays. De plus, moins de quatre entreprises ont manifesté un intérêt pour cette substance.
En 2006, moins de quatre entreprises ont déclaré avoir fabriqué de 10 000 à 100 000 kg de MHDnMH au Canada, et moins de quatre entreprises ont déclaré en avoir importé moins de 100 kg au pays. De plus, moins de quatre entreprises ont manifesté un intérêt pour cette substance.
La quantité fabriquée, importée ou commercialisée au Canada au cours de l’année civile 1986 et déclarée pour la Liste intérieure des substances (LIS) se situe entre 100 et 1 000 kg.
Selon des renseignements obtenus de l’Environmental Protection Agency (EPA) des États-Unis, entre 4 500 et 225 000 kg (déclaration originale : 10 000 à 500 000 lb) de MHDnMH ont été importés ou produits aux États-Unis en 1994; alors qu’aucune importation ou production n’a été rapportée en 1998 et 2002 (USEPA, 2005).
De 6 000 à 60 000 kg de MHDnMH ont également été utilisés de 1999 à 2008 en Suède, et de 400 à 13 000 kg de cette substance ont été utilisés de 2000 à 2008 au Danemark (SPIN, 2006).
Des renseignements relatifs aux utilisations pour les années civiles 2005 et 2006 ont été recueillis en réponse aux avis publiés en application de l’article 71 de la LCPE (1999) (Canada, 2006 et 2009).
En 2005, du MHDnMH a été importé principalement pour la fabrication de produits chimiques de base.
En 2006, le polymère a été fabriqué comme produit intermédiaire et utilisé à l’extérieur du Canada pour la fabrication de plastiques. Au cours de la même année, ce polymère a également été importé dans un mélange d’élastomère de silicone. Il est utilisé comme agent de vulcanisation pour le caoutchouc de silicone, des adhésifs ou des revêtements protecteurs à base de résines (Environnement Canada, 2010a).
Le MHDnMH est un composant de quatre types de produits cosmétiques au Canada : adhésif pour soutien-gorge (30 à 100 % en poids), crème décolorante pour la peau (0,1 à 0,3 % en poids), rouge à lèvres (< 0,1 % en poids) et maquillage pour les yeux (< 0,1 % en poids) [SDC, 2010]. Cependant, il ne figure pas sur la Liste critique des ingrédients dont l’utilisation est restreinte ou interdite dans les cosmétiques (Santé Canada, 2009). Le MHDnMH n’est pas utilisé actuellement comme principe actif ni comme produit de formulation dans les pesticides homologués au Canada (ARLA, 2007). Il n’est pas répertorié comme additif alimentaire approuvé au titre 16 du Règlement sur les aliments et drogues(Canada, 1978). Il n’est pas utilisé dans les emballages alimentaires ni comme additif indirect (courriel de la Direction des aliments de Santé Canada adressé au Bureau de gestion du risque de Santé Canada en avril 2010, source non citée). De plus, il n’est pas inscrit ni dans la base de données interne de la Direction des produits thérapeutiques sur les produits pharmaceutiques, ni dans la base de données sur les ingrédients non médicinaux, ni dans la base de données sur les ingrédients des produits de santé naturels (BDIPSN), ni dans la base de données sur les produits de santé naturels homologués (BDPSNH) en tant qu’ingrédient médicinal ou non médicinal dans les produits pharmaceutiques finaux, les produits de santé naturels ou les médicaments vétérinaires (BDPP, 2010; BDIPSN, 2010; BDPSNH, 2010; courriel de la Direction des produits thérapeutiques de Santé Canada adressé au Bureau de gestion du risque de Santé Canada en avril 2010, source non citée).
Des codes d’utilisation de la LIS ont été indiqués pour le MHDnMH, soit :
04 – Adhésif/liant/matériau d’étanchéité/bouche-pores
25 – Humidifiant/agent d’assèchement/déshumidifiant/déshydratant
89 – Impression et reliure
Aucune autre utilisation du MHDnMH n’a été répertoriée.
Environnement Canada a mis sur pied une méthode pour estimer les pertes d’une substance pendant différentes étapes de son cycle de vie, y compris son devenir après qu’elle a été incorporée à un produit ou un article fini (Environnement Canada, 2008). Cette méthode comprend une analyse du cycle de vie et un tableur (outil de débit massique) qui intègrent les renseignements sur la fabrication, l’importation et l’utilisation des données disponibles pour la substance. En commençant par une masse définie de la substance, on évalue chaque étape du cycle de vie jusqu’à ce que toute la masse ait été prise en compte. Les facteurs pertinents sont étudiés, les incertitudes sont reconnues et des hypothèses peuvent être émises pendant chaque étape, selon les renseignements disponibles. Les pertes estimées représentent le bilan massique exhaustif de la substance au cours de son cycle de vie et elles comprennent les rejets dans les eaux usées et d’autres milieux récepteurs (sol, air), la transformation chimique, le transfert vers les activités de recyclage et le transfert vers les sites d’élimination des déchets (sites d’enfouissement, incinération). Toutefois, à moins de disposer de données précises sur le taux ou le potentiel de rejet de cette substance provenant des sites d’enfouissement et des incinérateurs, la méthode ne permet pas de quantifier les rejets dans l’environnement à partir de ces sources. En fin de compte, les pertes estimées fournissent le premier volet de l’analyse de l’exposition à une substance et aident à estimer les rejets dans l’environnement et à mettre l’accent sur la caractérisation de l’exposition dans l’évaluation.
En général, les rejets d’une substance dans l’environnement peuvent découler de différentes pertes de la substance pendant sa fabrication, son utilisation industrielle ainsi que son utilisation commerciale et par les consommateurs. Ces pertes peuvent être regroupées en sept types : 1) déversements dans les eaux usées; 2) émissions atmosphériques; 3) pertes dans le sol; 4) transformation chimique; 5) élimination dans les sites d’enfouissement; 6) élimination par incinération; et 7) élimination par recyclage (c.-à-d. que le recyclage est considéré comme une perte et n’est plus pris en considération). Elles sont estimées à partir de données issues d’enquêtes réglementaires, des industries, ainsi qu’en fonction des données publiées par différents organismes. Les pertes dans les eaux usées concernent les déversements des eaux usées brutes non traitées avant tout traitement, que ce soit un traitement des eaux usées industrielles sur place ou un traitement des eaux usées hors site. De la même manière, les pertes par transformation chimique font référence aux modifications de l’identité de la substance qui ont lieu au cours des étapes de fabrication, d’utilisation industrielle ou d’utilisation commerciale et par les consommateurs, mais elles excluent celles qui ont lieu pendant les opérations de gestion des déchets telles que l’incinération et le traitement des eaux usées. Les pertes au sol incluent les rejets accidentels sur le sol ou les surfaces pavées ou non pavées pendant l’utilisation de la substance et sa durée de vie utile (p. ex., à partir de l’utilisation de machinerie agricole ou d’automobiles). Elle n’inclut toutefois pas le transfert de la substance dans le sol après l’utilisation initiale de celle-ci et sa durée de vie utile (p. ex., application au sol de biosolides et dépôts atmosphériques).
Les pertes estimées de MHDnMH au cours de son cycle de vie (fondées sur des hypothèses prudentes) sont présentées au tableau 3 (Environnement Canada, 2010b). Les pertes estimées ont été calculées en fonction des utilisations recensées en 2006.
Tableau 3. Estimation des pertes de MHDnMH pendant son cycle de vie
| Type de perte | Proportion (%) | Étapes pertinentes du cycle de vie |
|---|---|---|
| Eaux usées | 1,0 | Fabrication et utilisation à des fins industrielles |
| Émissions atmosphériques | < 0,1 | Fabrication et utilisation à des fins industrielles |
| Sol | 0,3 | Fabrication et utilisation à des fins industrielles |
| Transformation chimique | - | - |
| Sites d’enfouissement | 1,0 | Fabrication et utilisation à des fins industrielles |
| Incinération | - | - |
| Recyclage | - | - |
| Exportation | 97,7 | Fabrication et utilisation à des fins industrielles |
La majorité du polymère a été fabriquée en tant que produit intermédiaire et exportée en vrac pour la production de plastiques (Environnement Canada, 2010a).
Même s’il est possible que d’autres produits commerciaux et de consommation contenant du MHDnMH soient importés au Canada en plus de ceux déclarés au cours des enquêtes menées auprès de l’industrie, conformément à l’article 71 de la LCPE (1999), aucun renseignement ne porte sur l’ampleur de ces importations. Toutefois, la masse réelle perdue au cours de chaque étape du cycle de vie peut être supérieure aux estimations susmentionnées, si ces données étaient disponibles aux fins de la présente évaluation.
Le devenir du MHD5MH et du MHD34MH dans l’environnement peut être déduit à partir de leurs propriétés physiques et chimiques, comme nous l’avons indiqué précédemment.
MHD5MH
D’après les propriétés physiques et chimiques estimées (tableau 2), le MHD5MH se caractérise par une hydrosolubilité très faible (~2,5 × 10-6 mg/L), une pression de vapeur modérée (0,1 Pa), un faible log Koe (5,7) et une constante de la loi de Henry très élevée (2,0 × 107 Pa m3/mol. Par conséquent, sa répartition entre les différents milieux (air, sol, sédiments et eau) pourrait être importante, selon le milieu où il est rejeté et l’influence d’autres processus intervenant dans le devenir, comme l’advection et la dégradation.
Le modèle de fugacité de niveau III a servi à prédire la répartition environnementale du polymère de faible masse moléculaire, tout en tenant compte de la demi-vie dans l’air (estimée à 122,64 heures, soit 5,11 jours), dans l’eau (estimée à 4 386 heures, soit 182 jours), dans le sol (estimée à 670 heures, soit 4 semaines) et dans les sédiments (estimée à 8 760 heures, soit 365 jours). Les demi-vies utilisées pour la modélisation de la fugacité de niveau III sont estimées plus loin dans le présent rapport (voir la section « Persistance dans l’environnement »).
Tableau 4. Résultats de la modélisation de la fugacité de niveau III pour le MHD5MH (EQC, 2003)
| Substance rejetée dans : | Pourcentage de la substance répartie dans chaque milieu | |||
|---|---|---|---|---|
| Air | Eau | Sol | Sédiments | |
| l’air (100 %) | 97,6 | 0,1 | 0,2 | 2,1 |
| l’eau (100 %) | 0,1 | 3,4 | <0,1 | 96,4 |
| le sol (100 %) | 55,1 | <0,1 | 43,6 | 1,2 |
En cas de rejet dans l’air, une importante quantité de la substance devrait se répartir dans ce milieu. D’après la valeur modérée de la pression de vapeur (0,10 Pa selon le modèle) et la constante de la loi de Henry très élevée (2,0 × 107 Pa•m3/mol selon les calculs), ce polymère est semi-volatil. Par conséquent, si le MHD5MH n’était rejeté que dans l’air, il aurait tendance à demeurer dans ce milieu et à se répartir en faible quantité dans les autres milieux.
S’il est rejeté dans l’eau, il devrait fortement s’adsorber sur les matières en suspension et les sédiments, étant donné les valeurs élevées estimées du log Kco (~ 6). La volatilisation à partir de la surface de l’eau devrait être un processus négligeable de son devenir. Par conséquent, si l’eau est le milieu récepteur, le MHD5MH devrait surtout se répartir dans les sédiments et demeurer en faible quantité dans l’eau.
S’il est rejeté dans le sol, son adsorption dans ce milieu devrait être modérée (c’est-à-dire qu’il devrait être relativement immobile d’après la valeur estimée du log Kco). Puisque sa constante de la loi de Henry est très élevée, la volatilisation à partir de la surface de l’eau devrait être un processus de devenir important. En raison de sa pression de vapeur (estimée à 0,1 Pa), il pourrait cependant se volatiliser à partir des surfaces de sol. Par conséquent, s’il est rejeté dans le sol, moins de la moitié de la quantité totale de MHD5MH devrait y demeurer.
MHD34MH
En raison de la masse moléculaire élevée du MHD34MH, aucun modèle ne peut être utilisé pour prévoir le devenir de cette substance dans l’environnement. Si l’on se fonde sur les données déduites à partir du PDMS pour les propriétés physiques et chimiques, le MHD34MH demeure à l’état liquide aux températures ambiantes, n’est pas volatil et est insoluble dans l’eau.
S’il est rejeté dans l’air, une quantité négligeable devrait demeurer dans ce milieu, d’après les hypothèses selon lesquelles il possède une faible pression de vapeur et n’est pas volatil. Par conséquent, ce polymère aura tendance à se retrouver dans le sol et les sédiments.
Dans le cas d’un rejet dans l’eau, le MHD34MH en émulsion devrait s’adsorber fortement sur les matières solides en suspension et les sédiments. Dans une étude de Gettings et Lane (1982), du PDMS hydroxylé bloqué à ses extrémités (dont les propriétés chimiques et physiques sont équivalentes à celle du PDMS de 55 cSt) s’est adsorbé, à partir de la phase aqueuse, sur les particules en suspension et s’est déposé dans les sédiments sans remobilisation ultérieure sur une période de six semaines. Si on le mélangeait avec les sédiments avant l’essai, le polymère demeurait immobile pendant toute la période d’essai. Eales et Taylor (1983) ont également étudié les mouvements du PDMS (50 cSt) dans des sédiments marins. Il a été conclu que le polymère se liait fortement aux sédiments marins et que sa remobilisation dans l’eau de mer était peu probable. La volatilisation à partir de la surface de l’eau devrait être un processus négligeable quant au devenir de cette substance. Par conséquent, si l’eau est le milieu récepteur, le MHD34MH devrait surtout se répartir dans les sédiments.
S’il est rejeté dans le sol, le MHD34MH devrait se comporter comme le PDMS et fortement s’adsorber dans ce milieu (c’est-à-dire qu’il devrait être relativement immobile, d’après sa taille moléculaire importante et la valeur élevée estimée pour le log Kco). Dans une étude sur la distribution dans le sol (Battelle, 1992), on n’a observé aucun mouvement d’un 14C-PDMS (200 cSt) après son rejet dans ce milieu environnemental, et on n’a pas vu de signe de son passage en phase aqueuse ou atmosphérique. Par conséquent, s’il est rejeté dans le sol, il demeurera principalement dans ce milieu.
Persistance dans l’environnement
Aucune donnée expérimentale sur la dégradation du MHDnMH n’a été répertoriée.
MHD5MH
Les modèles RQSA ont été utilisés pour évaluer le potentiel de dégradation du polymère de faible masse moléculaire (MHD5MH). Ces prévisions sont jugées acceptables dans ce cas puisque la masse moléculaire du MHD5MH se situe dans les limites des domaines de tous les modèles.
Le tableau 5 résume les résultats des modèles RQSA en ce qui concerne la dégradation du MHD5MH dans l’eau et dans l’air.
Tableau 5. Données modélisées sur la dégradation du MHD5MH
| Processus du devenir | Modèle et base du modèle | Résultat et prévision du modèle | Demi-vie extrapolée (jours OU heures) |
|---|---|---|---|
| Air | |||
| Oxydation atmosphérique | AOPWIN, 2008[1] | t1/2 = 5,11 jours | ≥ 2 |
| Eau | |||
| Hydrolyse | HYDROWIN, 2008[1] | n.d.[2] | n.d. |
| Biodégradation primaire | |||
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 4 : enquête d’expert (résultats qualitatifs) |
3,11[3] « se biodégrade rapidement » |
< 182 |
| Biodégradation ultime | |||
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 3 : enquête d’expert (résultats qualitatifs) |
2,08[3] « ne se biodégrade pas rapidement » |
≥ 182 |
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 5 : Probabilité linéaire MITI |
-0,78[4] « ne se biodégrade pas rapidement » |
≥ 182 |
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 6 : Probabilité non linéaire MITI |
0,00[4] « ne se biodégrade pas rapidement » |
≥ 182 |
| Biodégradation (aérobie) | CATABOL c2000-2008 % DBO (demande biochimique en oxygène) |
1,68 « se biodégrade très lentement » |
≥ 182 |
[2] Le modèle ne donne pas d’estimation pour ce type de structure.
[3] Le résultat s’exprime par une valeur numérique de 0 à 5.
[4] Le résultat s’exprime par un taux de probabilité.
Une demi-vie d’oxydation atmosphérique estimée dans l’air de 5,11 jours (voir le tableau 5) indique qu’il est peu probable que le MHD5MH s’oxyde rapidement. De plus, on ne s’attend pas à ce qu’il réagisse avec l’ozone. Par conséquent, on estime que le MHD5MH est persistant dans l’air. Selon le milieu où il est rejeté, et vu la volatilité modérée et la constante de la loi de Henry très élevée attendues pour le produit, ce dernier devrait se retrouver dans l’air dans une proportion importante, comparativement à sa distribution dans les autres compartiments environnementaux.
Dans l’eau, le MHD5MH ne devrait pas subir une hydrolyse importante. Même si le sous-modèle BIOWIN 4 du modèle de biodégradation aérobie BIOWIN (2008) permet de penser que la dégradation primaire du polymère est rapide, les quatre modèles de biodégradation ultime (sous-modèles BIOWIN 3, 5, 6 et CATABOL) indiquent que la substance ne se biodégrade pas rapidement dans l’eau. En prenant en considération ces résultats, on constate que l’ensemble des modèles indique que la demi-vie de biodégradation ultime du MHD5MH est supérieure à 182 jours.
MHD34MH
Vu sa masse moléculaire élevée (2 655,45 g/mol), on considère que la forme n = 34 du polymère se situe hors du domaine des modèles RQSA pour la prédiction de la dégradation en milieu aquatique. Aux fins de la présente évaluation, les données expérimentales pour le PDMS qui sont présentées ci-dessous sont utilisées pour évaluer le potentiel de persistance du MHD34MH dans l’environnement.
Air et eau
Le PDMS n’est pas volatil et ne devrait pas se retrouver dans l’air; on considère donc qu’il n’est pas disponible pour y être dégradé davantage (Graiver et al., 2003, ECETOC, 1994). Aucune donnée n’indique non plus que le PDMS se dégrade rapidement dans le milieu aquatique. Des études réalisées sur le traitement des eaux usées révèlent qu’il n’est pas dégradé ni décomposé rapidement pendant les procédés de traitement, mais qu’il se retrouve dans les boues solides (Graiver et al., 2003). Comme le MHD34MH possède un groupe terminal formé de groupements hydrogène et diméthyle, il réagit légèrement plus que le PDMS; toutefois, il ne devrait pas réagir de façon importante dans des conditions observées dans l’environnement. D’après ces renseignements sur le PDMS, le MHD34MH ne devrait pas se dégrader rapidement dans l’air ou dans l’eau.
Sol
En ce qui concerne la dégradation dans le sol, un certain nombre d’études rapportent que la dépolymérisation et l’hydrolyse rapide, catalysée par l’argile, du PDMS dans le sol produisent les oligomères de faible masse moléculaire.
Buch et Ingebrigtson (1979) ont rapporté une demi-vie d’environ 30 jours pour un PDMS (1 000 cSt, ce qui équivaut à une masse moléculaire d’environ 15 000 g/mol) présent à une concentration de 6 000 mg/kg dans une terre végétale sèche de l’État de l’Iowa. La réaction était inhibée même avec un taux d’humidité de seulement 1 %. Dans la même étude, ils indiquent également la perte importante d’un polymère (50 cSt) par dégradation au cours de l’essai d’une durée de 53 jours.
On recense plusieurs études sur le comportement du PDMS dans le sol (résumées dans Graiver et al., 2003). Les résultats de ces études indiquent que ce polymère se dépolymérise rapidement par hydrolyse; ce phénomène brise les liaisons siloxanes et produit du PDMS oligomérique de masse moléculaire plus faible. Ladite dégradation hydrolytique catalysée par le sol s’est avérée aléatoire, c’est-à-dire qu’elle n’est pas propre à certaines liaisons en particulier et qu’elle ne commence pas nécessairement par l’extrémité de la chaîne. De plus, l’hydrolyse catalysée par des minéraux argileux dans le sol ne se produit dans aucun autre milieu (l’air, l’eau ou les sédiments) de façon importante.
Lehmann et al. (1994a) et Carpenter et al. (1995) ont également étudié la dégradation polymérique dans des conditions pédologiques plus réalistes en analysant le produit de dégradation extrait avec du CaCl2 à 0,01 M ou du tétrahydrofurane. Les résultats ont indiqué que la dégradation du PDMS (204 cSt) a eu lieu dans le sol qui a séché progressivement et est passé de 12 à 3 % d’humidité, plus rapidement que la dégradation de la substance lorsqu’on a maintenu une humidité constante du sol (12 à 13 % d’humidité) dans des chambres d’incubation.
Dans une autre expérience, Lehmann et al. (1995) ont étudié plus en profondeur 7 sols dont les propriétés étaient très différentes. Le PDMS (350 cSt) était ajouté à un sol humide qu’on laissait sécher pendant 2 semaines. Le PDMS s’est grandement dégradé au cours de cette période en produits ayant une masse moléculaire plus faible. Bien que la dégradation ait eu lieu lorsque le sol était encore humide, les taux de dégradation étaient supérieurs dans le sol le plus altéré. Toutefois, aucune corrélation n’a pu être établie entre le taux de dégradation du PDMS et les propriétés du sol mesurées (pH, % de matière organique et % d’argile).
Le taux de dépolymérisation par dégradation hydrolytique dans le sol est rapide, mais il dépend de plusieurs facteurs tels que le taux d’humidité et la température. Lehmann et al.(1995) ont rapporté que les taux globaux de dégradation du PDMS étaient plus lents dans un sol humide que dans un sol qui séchait graduellement pendant deux semaines, ce qui indique qu’une perpétuelle humidité pourrait constituer un facteur déterminant, mais que le taux d’humidité est inversement proportionnel au taux de dégradation (Lehmann et al., 1998b). De plus, les résultats de l’étude ont démontré que les températures élevées augmentaient le taux de dégradation au cours d’un cycle météorologique annuel.
Dans une autre étude (Xu, 1998), aucun PDMS n’a été décelé après 30 jours d’incubation dans la goethite, et on a observé une dégradation plus rapide encore lorsque le polymère était incubé dans la montmorillonite. Quant aux répercussions de la teneur en eau, l’étude a indiqué un taux de dépolymérisation plus rapide à une humidité relative de 32 % qu’à une humidité relative de 100 %. Compte tenu des données de terrain pour différents types de sol obtenues dans l’étude, on s’attend à ce que la demi-vie de dépolymérisation du PDMS soit inférieure à trois semaines.
Les preuves recueillies dans le cadre d’études expérimentales sur le PDMS portent à croire que la substance devrait rapidement subir une hydrolyse catalysée par l’argile dans le sol avec une demi-vie de quelques semaines; considérant cela, on s’attend à ce que le MHD34MH s’hydrolyse rapidement dans le sol et que sa demi-vie soit de quelques semaines, ce qui est largement inférieur à 182 jours; par conséquent, on considère que ce polymère n’est pas persistant dans l’environnement.
Le diméthylsilanediol (DMSD) est le principal produit issu de l’hydrolyse du PDMS dans le sol (Stevens, 1998; Craig, 2003). À la suite de la phase de décomposition du polymère, du carbone 14 a été utilisé pour détecter la source du CO2provenant de la biodégradation du PDMS marqué au carbone 14. La biodégradation du DMSD a été illustrée par Sabourin et al. (1996). Ainsi, la biodégradation du DMSD commence par l’oxydation d’un groupe méthyle, ce qui produit du méthylsilanetriol. Par la suite, le méthylsilanetriol se dégrade en CO2 et en silice.
La volatilisation peut aussi expliquer la perte de DMSD du sol et être en concurrence avec les pertes qui résultent de la biodégradation. Après le rejet de DMSD dans l’air, les groupes méthyle réagissent avec les radicaux hydroxyles qui sont générés en présence de lumière (Atkinson, 1991). Les auteurs n’ont pas observé de réaction entre les méthylsiloxanes et l’ozone ou les radicaux NO3, mais la réaction avec les radicaux hydroxyles s’est traduite par des durées de vie de 10 à 30 jours dans l’air pour plusieurs méthylsiloxanes oligomériques. Dans une autre étude similaire (Sommerlade et al., 1993), des durées de vie de 2 à 9 jours dans l’air ont été observées pour divers méthylsiloxanes oligomériques et triméthylsilanols. De plus, plusieurs produits de réaction ont permis de constater que les groupements méthyle étaient remplacés par des groupements hydroxyle.
D’après les données expérimentales sur le PDMS et la similarité structurelle entre cet analogue et le polymère, on s’attend à ce que le MHD34MH se dégrade rapidement dans le sol et ne persiste pas dans l’environnement.
Sédiments
La dégradation du PDMS a également été observée dans les sédiments; cependant, le taux de dégradation semble beaucoup plus lent que dans le sol puisque la demi-vie est de plus d’un an (Environnement Canada, 2010a).
Une expérience (Christensen, 1994) a porté sur le potentiel de dégradation du PDMS dans les sédiments d’eau douce. Une concentration de 500 ppm de PDMS (350 cSt) radiomarqué au carbone 14 a été ajoutée à des colonnes de sédiments et d’eau. Les éléments solubles dans l’eau et le gaz dégagé ont été mesurés afin de rendre compte de la dégradation. Après 56 jours, aucun 14CO2 ou 14C hydrosoluble n’a été décelé, ce qui indique l’absence de dégradation dans les sédiments au cours de la période d’essai.
Dans d’autres études d’incubation de plus longue durée, toutefois, la dégradation du PDMS dans les sédiments était évidente (Fendinger et al., 1997). À la suite d’une période d’incubation d’une année dans des conditions aérobies, 5 à 10 % du PDMS (350 cSt) a été hydrolysé en DMSD, et environ 0,25 % du 14C a été oxydé en dioxyde de carbone (Carpenter et al., 1995). Le taux et l’ampleur de la formation de DMSD et de dioxyde de carbone à partir des sédiments correspondent à peu de chose près aux taux observés par Lehmann et al. (1994a, 1994b) dans les sédiments humides (3 % pour le DMSD et 0,13 % pour le dioxyde de carbone en 6 mois). En raison de son adsorption élevée et de son immobilité dans les sédiments, de concert avec la teneur en eau du substrat, le PDSM devrait se dégrader très lentement dans les sédiments, et la demi-vie du polymère dans ce milieu devrait être supérieure à 365 jours. Cette prévision peut être extrapolée au polymère visé par l’évaluation; ainsi, le MHD34MH ne devrait pas se dégrader rapidement dans les sédiments non plus, et sa demi-vie dans ce compartiment de l’environnement devrait être supérieure à 365 jours.
D’après les données modélisées pour le polymère de faible masse moléculaire (MHD5MH) (voir le tableau 5) et les études expérimentales sur le polymère analogue (PDMS) qui ont servi à déduire les propriétés du polymère de masse moléculaire élevée (MHD34MH), le MHDnMH devrait se dégrader rapidement dans le sol (demi-vie dans le sol ≤ 182 jours). Toutefois, la substance satisfait aux critères de persistance dans l’air (demi-vie ≥ 2 jours), l’eau (demi-vie ≥ 182 jours) et les sédiments (demi-vie ≥ 365 jours) énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000). On conclut donc qu’elle est persistante dans l’environnement.
Potentiel de bioaccumulation
Il n’existe pas de données expérimentales sur la bioaccumulation du MHDnMH.
Les données expérimentales sur le méthylsiloxane linéaire analogue ont été utilisées pour prévoir le potentiel de bioaccumulation du MHD5MH. De plus, des modèles RQSA ont servi à estimer le facteur de bioaccumulation (FBA) et le facteur de bioconcentration (FBC) pour ce composé de faible masse moléculaire.
En ce qui concerne le polymère de masse moléculaire élevée, on a utilisé les données expérimentales relatives au PDMS pour évaluer le potentiel de bioaccumulation du MHD34MH.
MHD5MH
Les données modélisées sur la bioaccumulation du MHD5MH sont résumées dans le tableau 6a ci-dessous.
Tableau 6a. Données modélisées sur la bioaccumulation du MHD5MH
| Organisme d’essai | Paramètre | Valeur (poids humide en L/kg) | Référence |
|---|---|---|---|
| Poisson | FBC | 1,04 × 104 | BCFBAF, 2008 (niveau trophique intermédiaire) |
| Poisson | FBC | 7,41 × 104 | Arnot et Gobas, 2003 (niveau trophique intermédiaire) |
| Poisson | FBC | 3,24 × 104 | BBM avec facteurs atténuants, 2008 |
| Poisson | FBA | 5,48 × 106 | BCFBAF, 2008 (niveau trophique intermédiaire) |
| Poisson | FBA | 3,39 × 106 | Arnot et Gobas, 2003 (niveau trophique intermédiaire) |
Selon les prévisions modélisées (fondées sur le log Koe modélisé de 6,60), le FBA et le FBC du MHD5MH pourraient être élevés chez les poissons. Toutefois, les résultats expérimentaux indiquent des potentiels de bioaccumulation différents des méthylsiloxanes linéaires de faible masse moléculaire.
Annelin et Frye (1989) n’ont rapporté aucune absorption des oligomères linéaires du PDMS, qui ont une masse moléculaire supérieure à 384 g/mol (le MD3M étant la forme la plus petite de PDMS), par les poissons à la suite d’une exposition de plus de 5 semaines. Les résultats expérimentaux indiquent que ni le MD3M, ni le MD4M, ni le MD7M (607 g/mol) ne se sont bioconcentrés chez la truite arc-en-ciel après 35 à 77 jours d’exposition.
Dans une autre étude sur l’absorption et la rétention de PDMS par les poissons (Bruggeman et al., 1984), des méthylsiloxanes linéaires ont été ajoutés aux aliments. L’absorption quotidienne moyenne était de 1 × 10-3 mg/g de poisson pour une période de 6 à 8 semaines. À la fin de cette période, la présence de MD3M et de MD4M a été mesurée sous les seuils de détection (approximativement 3 × 10-4 mg/g) dans tous les échantillons de poissons, alors que la concentration de MD5M et des autres méthylsiloxanes linéaires ne dépassaient pas 2 × 10-3 mg/g. En comparaison de l’absorption quotidienne moyenne (1 × 10-3 mg/g), ces résultats indiquent que l’absorption, la rétention et l’accumulation de MD3-6M par l’entremise des aliments ne sont pas importantes. Pour cette raison, on peut donc s’attendre à ce que le MHD5MH, qui a une structure linéaire semblable au MD3M et au MD4M, ainsi qu’une masse moléculaire plus élevée, ait un potentiel de bioaccumulation comparable et ne se bioaccumule pas.
Selon des études menées par Dimitrov et al. (2002) et Dimitrov et al. (2005), ainsi que le Baseline Bioaccumulation Model (BBM, 2008), la probabilité qu’une molécule traverse des membranes cellulaires à la suite d’une diffusion passive diminue de façon importante lorsque le diamètre transversal maximal (Dmax) augmente. Ainsi, la probabilité qu’une diffusion passive se produise diminue de façon notable lorsque le diamètre transversal est supérieur à environ 1,5 nm et de façon encore plus importante dans le cas des molécules ayant un diamètre transversal supérieur à 1,7 nm. Sakuratani et al. (2008) ont également étudié l’effet du diamètre transversal sur la diffusion passive à l’aide d’un ensemble d’essais comptant environ 1 200 substances chimiques nouvelles et existantes. Ils ont aussi observé que les substances dont le potentiel de bioconcentration n’était pas très élevé avaient souvent un Dmax supérieur à 2,0 nm ainsi qu’un diamètre effectif (Deff) supérieur à 1,1 nm.
Selon l’estimation des propriétés physiques et chimiques du MHD5MH, cette substance a un diamètre transversal se situant entre 1,46 et 2,18 nm. D’après l’observation citée précédemment (Sakuratani et al., 2008), la forme n = 5 du polymère a un taux d’absorption limité à partir de l’eau et une biodisponibilité in vivo réduite.
D’après les données expérimentales sur les méthylsiloxanes linéaires analogues, et en tenant compte de la taille des molécules, le MHD5MH ne devrait pas se bioaccumuler chez les organismes aquatiques.
MHD34MH
Le MHD34MH a une taille moléculaire beaucoup plus importante que la forme de faible masse moléculaire (n = 5) du MHDnMH. Cette caractéristique devrait limiter sa répartition, à savoir son passage à travers les membranes biologiques, et limiter sa biodisponibilité ainsi que son potentiel de bioaccumulation dans les organismes aquatiques. Des données tirées d’études sur le PDMS sont utilisées pour caractériser le potentiel de bioaccumulation du MHDnMH (voir les données compilées dans le tableau 6b ci-dessous).
Tableau 6b. Données empiriques sur la bioaccumulation et la bioconcentration du PDMS
| Nature du polymère (masse moléculaire, viscosité ou émulsion) |
Organisme d’essai | Concentration expérimentale (mg/L) et/ou source d’exposition | Paramètre (FBA/FBC, L/kg) (FBAm[1], sans dimension) |
Référence |
|---|---|---|---|---|
| Émulsion à 15 %, 300 cSt | Crapet arlequin (Lepomis macrochirus) |
1,5 | FBC = 0,16 à 0,5 (après 2 semaines) |
Hobbs et al., 1975 |
| MD15-17M | Guppy (Poecilia reticulate) |
Saturation | FBC < 10 | Opperhuizen et al., 1987 |
| Approximativement 32 mg/kg de nourriture sèche | FBA < 0,01 | |||
| PDMS commercial Mm (g/mol): 1 200 6 000 25 000 56 000 |
Carp sp. | Concentrations mesurées dans les solutions à saturation 1,330 0,486 0,135 0,060 |
FBC = 2,9 FBC = 7,1 FBC = 386 FBC = 1 250 |
Watanabe et al., 1984a |
| Émulsion à 35 %, 50 cSt | Niveau 1 : phytoplancton (Tetraselmis sp.) Niveau 2 : mollusque (Mytilus edulis) |
70 Exposition directe par l’eau Exposition par l’eau et la nourriture |
FBC = 2,08 FBAm = 0,12 |
Aubert et al., 1985 Guillemaut et al., 1987 |
| Niveau 1 : plancton (Tatreselmis sp. Artemia salina) Niveau 2 : poisson (Carassius auratus) |
70 Exposition directe par l’eau Exposition par l’eau et la nourriture |
FBC = 1,9 FBAm = 0,05 |
||
| Niveau 1 : annélide (Nereis diversicolor) Niveau 2 : poisson (Scorpaena porcus) |
70 Exposition directe par l’eau Exposition par l’eau et la nourriture |
FBC = 0,036 FBAm = 1,4 |
||
| Niveau 1 : annélide (Nereis diversicolor) Niveau 2 : crabe (Carcinus maenas) |
70 Exposition directe par l’eau Exposition par l’eau et la nourriture |
FBC = 0,036 FBAm = 1,09 |
||
| 50 cSt | Poisson-chat (Ictalurus melas) |
Exposition par la nourriture | < seuil de détection | Annelin, 1979 |
Généralement, le PDMS de masses moléculaires variées (Mm = 1 200 g/mol et plus) se montre faiblement bioaccumulable et bioconcentrable chez les organismes aquatiques et les espèces terrestres.
Opperhuizen et al. (1987) ont quant à eux effectué une étude sur la bioaccumulation, chez Poecilla reticulate (guppy), du PDMS (5 cSt, MD15-17M). Au bout de 12 semaines d’exposition, on ne détectait pas de polymères de siloxane dans les poissons entiers.
Dans une autre étude, on a soumis des crapets arlequins (Lepomis macrochirus) à une exposition à un PDMS ayant une masse moléculaire supérieure ou égale à 5 000 g/mol pendant une période de 30 jours (Hobbs et al., 1975). On n’a trouvé aucun lien entre les taux du polymère dans les tissus et la durée ou le degréß d’exposition. On a découvert cependant que le polymère était adsorbé sur des surfaces du poisson, mais qu’il n’était pas absorbé par les cellules.
En outre, des études ont été réalisées concernant l’absorption de PDMS par d’autres espèces dans d’autres milieux naturels. Au cours d’une étude de 28 jours dirigée par Garvey et al. (1996), on a exposé des vers de terre (Eisenia foetida) à 100 et 1 000 mg/kg de PDMS dans une matrice de sol artificiel. Au terme de la phase d’exposition, les vers de terre de chaque réplicat ont été transférés dans un milieu d’exposition qui ne contenait pas de PDMS pour y subir une phase de dépuration de 14 jours. On a prélevé des échantillons au cours de la phase d’exposition de 28 jours; toutefois, on n’a pas relevé de différence statistique dans les concentrations de résidus tissulaires pour les deux groupes. En outre, le PDMS ingéré par les vers de terre et présent dans l’intestin a été rapidement dépuré pendant la période de 14 jours qui a suivi.
Kukkonen et Landrum (1995) n’ont observé aucune bioaccumulation dans des vers aquatiques vivant dans les sédiments.
Les résultats d’études relatives à d’autres organismes benthiques et terrestres (Putt, 1994; Putt et Mihaich, 1996) ont aussi indiqué un potentiel de bioaccumulation très limité pour le PDMS.
Une étude sur la carpe argentée a fait état de résultats contradictoires, selon lesquels les matériaux de PDMS ayant une masse moléculaire plus élevée subissaient une bioaccumulation supérieure à celle des composés ayant une masse moléculaire inférieure (Watanabe et al., 1984). Le fait que le rapport entre la bioaccumulation et la masse moléculaire soit l’inverse des résultats escomptés pourrait être le résultat de la contamination de la surface, et aucune indication n’était donnée pour préciser si on avait analysé les poissons entiers ou les filets. Par conséquent, ces résultats sont d’une qualité incertaine.
On a étudié la bioamplification ou les transferts par la chaîne alimentaire d’une émulsion de PDMS (50 cSt) en milieu marin (Aubert et al., 1985; Guillemaut et al., 1987). Les organismes du premier niveau trophique étaient exposés au PDMS en émulsion (50 cSt) à une concentration de 70 mg/L dans l’eau. Soit le PDMS ne subissait pas de bioconcentration dans l’eau, soit le FBC était inférieur à 2 au premier niveau trophique. La bioaccumulation entre les deux niveaux trophiques était faible, elle était comprise entre 0,05 et 1,4, ce qui indique que la bioamplification du PDMS entre deux niveaux trophiques n’est pas significative dans la chaîne alimentaire aquatique soumise à l’essai.
Selon les renseignements ci-dessus sur le PDMS, le MHD34MH ne devrait pas être biodisponible dans les organismes aquatiques ou organismes de fond. Par ailleurs, ce polymère ne se bioaccumule pas dans ces organismes.
Compte tenu de l’évaluation du potentiel de bioaccumulation des polymères ayant une masse moléculaire faible ou moyenne en nombre, il est conclu que le MHDnMH ne satisfait pas aux critères de bioaccumulation (FBA ou FBC ≥ 5 000) énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Évaluation des effets écologiques
A – Dans le milieu aquatique
Aucune donnée expérimentale sur la toxicité du MHDnMH n’a été relevée.
MHD5MH
Des modèles RQSA ont été utilisés pour estimer la toxicité aquatique du MHD5MH. Les données modélisées sont résumées dans le tableau 7 ci-dessous.
Tableau 7a. Données modélisées sur la toxicité du MHD5MH pour les organismes aquatiques
| Organisme d’essai | Type d’essai | Paramètre | Valeur (mg/L) |
Modèle |
|---|---|---|---|---|
| Poisson | Toxicité aiguë (96 heures) | CL50[1] | 0,035[*] | ECOSAR, 2008 |
| Toxicité aiguë (14 jours) | 0,038[*], [!] | |||
| Poisson (eau de mer) | Toxicité aiguë (96 heures) | CL50 | 0,035[*] | |
| Daphnie | Toxicité aiguë (48 heures) | CL50 | 0,039[*] | |
| Algues vertes | Toxicité aiguë (96 heures) | CE50[2] | 0,137[*] | |
| Mysis effilée | Toxicité aiguë (96 heures) | CL50 | 0,001[*] | |
| Poisson | Toxicité chronique (30 jours) | Vtc[3] | 0,005[*] | |
| Daphnie | Toxicité chronique | Vtc | 0,009[*] | |
| Algues vertes | Toxicité chronique | Vtc | 0,112[*] | |
| Mysis effilée | Toxicité chronique | Vtc | 0,00003[*] | |
| Poisson (eau de mer) | Toxicité chronique | Vtc | 0,072[*] | |
| Ver de terre | Toxicité chronique (14 jours) | CL50 | 293,13[*] | |
| Tête-de-boule | Toxicité aiguë (96 heures) | CL50 | 146[*] | AIEPS, 2003-2007 |
| Daphnia magna | Toxicité aiguë (48 heures) | CL50 | 13,19[*] | |
| Pseudokirchneriella subcapitata | Toxicité aiguë (72 heures) | CE50 | 14,09[*] | |
| Daphnia magna | Toxicité aiguë (48 heures) | CE50 | 0,18[*] | OASIS Forecast, 2005 |
| Pimephales promelas | Toxicité aiguë (96 heures) | CE50 | 0,43[*] |
[2] CE50- Concentration d’une substance qu’on estime susceptible de causer un effet chez 50 % des organismes d’essai.
[3] Vtc – Valeur de toxicité chronique.
[*] La concentration d’exposition est au moins dix fois supérieure à l’hydrosolubilité estimée, ce qui indique qu’aucun effet n’est prévu à saturation pour la substance à l’étude.
[!] Valeur critique de toxicité (VCT). Elle est utilisée pour dériver la concentration estimée sans effet (CESE).
Les estimations produites par les modèles en ce qui concerne la toxicité du MHD5MH en milieu aquatique sont résumées au tableau 7a. On note que les valeurs modélisées pour tous les paramètres sont beaucoup élevées que l’hydrosolubilité modélisée du MHD5MH (2,7 × 10-6 mg/L). Ces résultats permettent donc de penser qu’au niveau maximal de solubilité, le MHD5MH n’a pas d’effet observable sur les organismes aquatiques dans le cas d’une exposition à court terme. Néanmoins, pour les besoins d’une évaluation prudente de la toxicité du MHD5MH, une CL50modélisée de 0,038 mg/L sur une période de 14 jours a été utilisée comme valeur critique de toxicité (VCT) pour les poissons afin de caractériser les risques présentés par le MHD5MH pour les organismes aquatiques.
MHD34MH
Aucun modèle RQSA ne peut être utilisé pour modéliser l’écotoxicité du polymère de masse moléculaire élevée. L’information sur le PDMS a donc servi à évaluer la toxicité du MHD34MH.
Il existe plusieurs études de toxicité faisant état des effets du PDMS sur les organismes aquatiques. Les résultats de ces études sont résumés dans le tableau 7b. Comme on l’indiquait précédemment dans le présent rapport (voir la section sur le potentiel de bioaccumulation), le PDMS n’est pas absorbé par les organismes aquatiques (Annelin et Frye, 1989; Bruggeman et al., 1984); par conséquent, on ne prévoit pas d’effets de sa part. Comme le PDMS est extrêmement hydrophobe et tend à s’adsorber fortement sur les particules solides, on a employé ce polymère en émulsion dans de nombreuses études pour maintenir des concentrations d’exposition nominales constantes, bien supérieures à ce que permet la solubilité du PDMS dans l’eau.
En général, le PDMS s’est avéré peu toxique pour les poissons (voir le tableau 7b). Hill et al. (1984) ont rapporté une concentration sans effet observé (CSEO) de 91 mg/L de PDMS (émulsion de 50 cSt) chez le méné tête-de-mouton. Lors d’une autre étude, Hill a fait état d’une CL50 de 350 mg/L de PDMS (émulsion de 50 cSt) chez la plie (Hill et al., 1980). Il a été démontré que les effets toxiques des émulsions de PDMS en forte concentration étaient attribuables à l’émulsifiant utilisé (Hobbs et al., 1975; Aubertet al., 1985).
Le PDMS a également montré une faible toxicité pour les invertébrés aquatiques (voir le tableau 7b). Une étude réalisée sur les moules Mytilus sp. (Hill et al., 1984) a permis d’établir une CL50 de 1 980 mg/L de PDMS (émulsion de 50 cSt) après 96 heures. Cependant, les effets secondaires sont quelque peu difficiles à interpréter. Les formes liquides du PDMS sont insolubles dans l’eau et ont une masse volumique inférieure à 1 000 kg/m3. Par conséquent, le polymère forme une pellicule de surface dans laquelle les crustacés aquatiques ont tendance à se retrouver pris au piège. Ce piégeage peut se produire et donc interférer avec l’évaluation de la toxicité chimique du polymère.
On a aussi étudié la toxicité pour les microorganismes aquatiques et il s’est avéré que le PDMS n’était pas très dangereux pour lesdits organismes (voir le tableau 7b).
Comme les concentrations d’exposition au PDMS sont largement supérieures à la solubilité maximale attendue pour le polymère dans les études disponibles sur la toxicité en milieu aquatique, le polymère présente probablement un risque faible pour les organismes aquatiques dans les conditions ambiantes.
La valeur critique de toxicité (VCT) est tirée d’une étude de Hill et al. (1977) sur le PDMS (50 cSt, en émulsion à 35 %) puisque ce polymère a la masse moléculaire la plus proche de celle du MHD34MH de masse moléculaire moyenne en nombre. Pour les besoins de la caractérisation des risques que présente le MHD34MH pour les organismes aquatiques, une CSEO de 91 mg/L indiquée dans cette étude a été utilisée comme VCT pour dériver la concentration estimée sans effet (CESE).
Tableau 7b. Données de toxicité du PDMS sur les organismes aquatiques
| Nature du polymère (viscosité et/ou émulsion) |
Organisme d’essai | Type d’essai | Paramètre | Valeur (mg/L) | Référence | |
|---|---|---|---|---|---|---|
| Poissons | ||||||
| Non précisé | Poisson | Toxicité aiguë | CL50[1] | > 1 000 | Annelin et Humble, 1978; Hobbs et al., 1975 | |
| Non précisé | Méné (Phoxinus phoxinus) |
Toxicité semi-chronique | TL40[2] | 3 000 (8 jours) | Cabridenc, 1978 | |
| 100, 350, 12 500 cSt | Pomatoschistus minutus Gasterosteus aculeatus |
Toxicité aiguë (96 heures) | CL0[3] | À saturation | Maggi et Alzieu, 1977 | |
| Émulsion à 20 %, 50 cSt | Plie (Pleuronetes platessa) |
Toxicité aiguë (96 heures) | CE[4] | 88 | Firmin, 1984 | |
| Émulsion à 35 %, 50 cSt | Scorpène Scorpaena poreus Carassius auratus |
Toxicité aiguë | TL50[5] | 1 000 (12 heures) 2 000 (50 heures) 10 000 (4 heures) 700 (50 heures) 3 500 (24 jours) |
Aubert et al., 1985 | |
| 50 cSt | Plie (Pleuronetes platessa) |
Toxicité aiguë (96 heures) | CL50 | 350 > 10 000 à la surface de l’eau (5 mg/L dans l’eau) |
Hill et al., 1984 Hill, 1980 | |
| Émulsion à 35 %, 50 cSt | Méné tête-de-mouton (Cyprinodon variegatus) |
Toxicité chronique (33 jours) | CSEO[6]CE | 91 235 (effets mineurs observés) |
Hill et al., 1984 | |
| 350 cSt | Truite arc-en-ciel (Oncorhynchus mykiss) Salmo gairdneri) |
Nourriture modifiée sous-chronique (28 jours) | DSEO[7] | 10 000 mg/kg p.c. par jour | Mann et al., 1977 | |
| Émulsion à 30 %, 350 cSt | Crapet arlequin (Lepomis macrochiras) Truite arc-en-ciel (Salmo gairdneri) |
Toxicité aiguë (96 heures) | CL50 Hypoactivité |
> 10 000 À 1 000 et 10 000 | Hobbs et al., 1975 | |
| Invertébrés aquatiques et mollusques | ||||||
| Émulsion à 66 %, 10 à 60 000 cSt | Daphnie | Toxicité aiguë | CSEO | > 200 | Annelin et al., 1994 | |
| Émulsion, 350 cSt | Daphnia magna | Toxicité aiguë (48 heures) | CL50 | 1 000 | Spacie, 1972 | |
| 100, 350 et 12 500 | Huître plate (Ostrea edulis) Moule bleue (Mytilus edulis) Bigorneau (Littorina littorea) |
Toxicité aiguë (96 heures) |
CL0 | Saturation dans l’eau de mer | Maggi et Alzieu, 1977 | |
| Émulsion à 35 %, 50 cSt | Moule (Mytilus edulis) Crabe (Artemia salma Carcinus maenas) |
Toxicité aiguë Semi-chronique (10 jours) Semi-chronique |
TL50 TL50 CL0 CL50 Mortalité |
3 500 (96 heures) 10 000 (80 heures) (émulsifiant seulement) 700 7 000 (9 jours) 3 500 (10 jours) |
Aubert et al., 1985 | |
| Émulsion à 20 %, 50 cSt | Mytilus sp. | Toxicité aiguë (96 heures) | CL50 | 1 980 | Hill et al., 1984 | |
| 50 cSt | Mytilus sp. | Toxicité aiguë (96 heures) | CL50 | 1 020 | Hill et al., 1984 | |
| 100 cSt Émulsion à 30 %, 100 cSt Émulsion à 30 %, 350 cSt |
Daphnia magna Daphnia magna Coques (Prothaca spaminea) Choquemort (Fundulus heteroclitus) Crabe des rivages (Pachygrapsus crassipes) Crevette brune (Penaeus oxtecus) |
Toxicité aiguë (48 heures) Toxicité aiguë (48 heures) Toxicité aiguë (96 heures) |
CL50 CL50 CL50 |
44,5 (le polymère a formé une couche à la surface) 73,4 > 1 000 |
Hobbs et al., 1975 | |
| Microorganismes aquatiques (bactéries, champignons et phytoplancton) | ||||||
| Groupe terminal hydroxyle, 55 cSt | Bactéries, algues et protozoaires aérobies et anaérobies | Toxicité chronique (24 semaines) |
CSEO | > 0,26 | Gettings et Lane, 1982 | |
| 100, 350 et 12 500 cSt | Algues marines (diatomées et flagellés) | Toxicité semi-chronique (9 jours) | CSEO | Saturation dans l’eau de mer | Maggi et Alzieu, 1977 | |
| Émulsion à 35 %, 50 cSt | Phytoplancton marin (Tetraselmis sp.) | Non précisé | CMEO[8] | 350 | Maggi et Alzieu, 1977 | |
[2] TL40 – Temps requis en heures pour que 40 % des organismes d'essai meurent à concentration donnée.
[3] CL0 – Concentration d’une substance que l’on estime sans effet létal sur les organismes d’essai.
[4] CE – Concentration d’une substance que l’on estime avoir un effet toxique sur les organismes d’essai; cependant, le pourcentage d’organismes d’essai touchés ne peut être établi dans l’étude.
[5] TL50 – Temps requis en heures pour que 50 % des organismes d'essai meurent à concentration donnée.
[6] CSEO – Concentration sans effet observé, soit la concentration d’exposition la plus élevée ne causant pas d’effet statistiquement significatif par rapport aux témoins dans un essai de toxicité.
[7] DSEO – Dose sans effet observé, soit la dose d’exposition la plus élevée ne causant pas d’effet statistiquement significatif par rapport aux témoins dans un essai de toxicité.
[8] CMEO – Concentration minimale avec effet observé, soit la concentration la plus faible d’une substance causant des effets statistiquement significatifs par rapport au groupe témoin dans un essai de toxicité.
[!] VCT – Valeur critique de toxicité. On l’utilise pour dériver la concentration estimée sans effet (CESE).
Selon les prévisions des modèles, le MHD5MH ne devrait pas avoir d’effets observables sur les organismes aquatiques à une concentration correspondant à sa solubilité maximale. Le MHD34MH, dont la structure est semblable au PDMS, ne devrait pas non plus avoir d’effets importants sur les organismes aquatiques aux concentrations correspondant à sa plage de solubilité dans l’eau. Par conséquent, il est conclu que la toxicité du MHDnMH est faible pour les organismes aquatiques.
B – Dans d’autres milieux environnementaux
La principale voie d’exposition dans un milieu aquatique serait par contact avec le polymère absorbé par les sédiments, en raison de la faible hydrosolubilité de ce dernier. Par conséquent, les possibles effets toxiques du polymère sur les organismes vivant dans les sédiments sont également pris en considération dans cette évaluation préalable. De plus, comme les biosolides issus des boues traitées provenant des réseaux d’assainissement peuvent être utilisées pour augmenter les terrains agricoles et régénérer les sols, on tient compte de cette voie d’exposition des organismes terrestres au polymère.
Comme il n’existe pas de données expérimentales sur la toxicité du MHDnMH dans les sédiments ou le sol, l’information relative au PDMS est utilisée pour évaluer la toxicité du MHDnMH (voir le tableau 7c ci-dessous). En résumé, le PDMS montre une faible toxicité pour les organismes vivant dans les sédiments et les sols.
Tableau 7c. Données relatives à la toxicité du PDMS pour les organismes vivant dans les sédiments ou les sols
| Nature du polymère (viscosité et/ou émulsion) |
Organisme d’essai | Milieu et type d’essai | Paramètre | Concentration (mg/kg, sauf indication contraire) | Référence |
|---|---|---|---|---|---|
| Organismes vivant dans les sédiments | |||||
| 350 cSt | Amphipode marin (Ampelisca abdita) | Sédiments Toxicité semi-chronique (10 jours) |
CL0[1] | > 2 300 | Putt et Mihaich, 1996 |
| 350 cSt | Amphipode d’eau douce (Hyalella azteca) | Sédiments Toxicité chronique (28 jours) |
CE0[2] | > 2 200 | Putt et Mihaich, 1996 |
| PDMS (caractéris-tiques de viscosité/ émulsion non indiquées) | Ver polychète (Nereis diversicolor) | Sédiments Toxicité chronique (28 jours) |
CE0 | 1 000 | Craig et al., 1984 |
| 50 cSt | Annélides | Sédiments Toxicité aiguë (96 heures) Toxicité chronique (28 jours) |
CE0 | > 10 000 | Craig et Caunter, 1990 |
| Émulsion à 35 %, 50 cSt (eau de mer) | Ver polychète (Nereis diversicolor) | Sédiments Toxicité semi-chronique (9 jours) |
CL0 CE0 |
> 350 > 700 |
Aubert et al., 1985 |
| 350 cSt | Invertébrés benthiques (H. azteca et C. tentans) |
Sédiments Toxicité semi-chronique (10 jours) Cycle de vie (28 jours pour le H. azteca et 50 à 65 jours pour le C. tentans) |
CL0 CE0 |
> 1 000 | Henry et al., 2001 |
| Organismes vivant dans le sol | |||||
| Liquide, 350 cSt | Lombric (Eisenia fœtida) | Sol Toxicité chronique (21 jours) |
CE0 | 1 100 | Garvey et al., 1996 |
| Liquide, 350 cSt | Collembole (Folsomia candida) | Sol Toxicité chronique (21 jours) |
CSEO[3] | 250 | Garvey et al., 1996 |
| Végétaux | |||||
| Émulsion à 10 %, 10 cSt | Plantation de conifères | Sol Toxicité aiguë (tout de suite après le traitement) Toxicité chronique (1 an) |
DSEO[4] | 30 mL/m3 | Belt et al., 1977 |
| Oiseaux | |||||
| 100 cSt | Canard colvert (Anas platorhynchus) Colin de Virginie (Colinus virgianus) |
Toxicité semi-chronique (5 jours) | CL0 | > 5 000 | Hobbs et al., 1975 |
| 100 cSt | Poule Leghorn blanche | Toxicité chronique | CE0 | > 5 000 | Hobbs et al., 1975 |
[2] CE0- Concentration d’une substance dont on estime qu’elle n’a aucun effet secondaire sur les organismes d’essai.
[3] CSEO – Concentration sans effet observé, soit la concentration la plus élevée ne causant pas d’effet statistiquement significatif par rapport au groupe témoin dans un essai de toxicité.
[4] DSEO – Dose sans effet observé, soit la dose d’exposition la plus élevée ne causant pas d’effet statistiquement significatif par rapport aux témoins dans un essai de toxicité.
Les effets du PDMS (5 à 1 000 cSt) ont également été évalués chez des adultes de l’espèce Acheta domesticus (grillon domestique) exposés au polymère par application directe du produit (5 × 10-3 mg) sur la face ventrale du thorax des sujets (Levier et al., 1988). Le délai de perte du réflexe de redressement (la capacité des grillons à se remettre sur leurs pattes lorsqu’on les place sur le dos) s’est accru avec la viscosité du PDMS, et la mortalité au bout de 48 heures diminuait d’un facteur 2 lorsque la viscosité du PDMS augmentait d’un facteur 200. Un effet similaire du PDMS (10 cSt) a été observé dans une autre étude (Nielson et al., 1975).
D’après les résultats de l’étude sur le PDMS, le MHDnMH ne devrait pas présenter un potentiel de toxicité important pour les organismes vivant dans les sédiments ou les sols.
Évaluation de l’exposition de l’environnement
A – Rejets industriels
On n’a relevé aucune donnée sur les concentrations de MHDnMH dans l’environnement au Canada. Les concentrations dans l’environnement sont donc estimées en fonction de l’analyse de l’exposition pour le polymère, en tenant compte des quantités de MHD34MH fabriquées au Canada ainsi que du MHD5MH présent dans le polymère.
L’outil de débit massique a utilisé des hypothèses réalistes correspondant au scénario le plus défavorable pour les rejets de MHDnMH dans l’eau (par les effluents d’eaux usées) associés aux utilisations industrielles (tableau 3). Pour examiner la question des rejets issus des activités industrielles, un scénario propre au site a servi à estimer une concentration prudente de la substance dans un cours d’eau recevant des effluents industriels (Environnement Canada, 2010c). Le scénario vise à fournir des estimations fondées sur la quantité de la substance traitée et rejetée, le nombre de jours de traitement, le taux d’élimination de l’usine de traitement des eaux usées (UTEE) et la taille du cours d’eau récepteur.
Le scénario propre au site des rejets industriels tient compte des données sur la charge obtenues de sources telles que des enquêtes industrielles, ainsi que des connaissances sur la distribution des rejets industriels au pays, et calcule la concentration estimée dans l’environnement (CEE).
Une exposition aquatique au polymère de siloxane devrait avoir lieu si la substance est rejetée dans le cadre des utilisations industrielles vers une UTEE qui évacue subséquemment son effluent dans des eaux réceptrices. La concentration de la substance dans les eaux réceptrices près du point de rejet de l’usine de traitement des eaux usées est utilisée comme CEE pour l’évaluation du risque que pose la substance en milieu aquatique. On peut la calculer à l’aide de l’équation suivante :
Ceau-ind = [1000 × Q × L × (1 - R)] / [N × F × D]
où
Ceau-ind : concentration en milieu aquatique due aux rejets industriels, en mg/L
Q : quantité de substance totale utilisée chaque année sur un site industriel, en kg/an
L : pertes dans les eaux usées, fraction
R : taux d’élimination de l’usine de traitement des eaux usées, fraction
N : nombre de jours de rejets annuels, en jour/an
F : débit de l’effluent de l’usine de traitement des eaux usées, en m3/jour
D : facteur de dilution dans l’eau réceptrice, sans dimension
Le scénario propre au site est prudent, c’est-à-dire qu’il suppose que la quantité totale de la substance employée dans l’industrie canadienne n’est utilisée que par une seule installation industrielle sur un petit site hypothétique. Il suppose également que les pertes vers une UTEE locale sont élevées, soit 1 % de la quantité totale utilisée par suite du nettoyage de contenants de produits chimiques et d’équipement de traitement. Le débit des effluents de l’UTEE sélectionnée est estimé se situer au 10e centile (3,3 × 104 m3/j) de ses taux de rejet. Le scénario présume également que les rejets se produisent 250 jours par année, comme c’est habituellement le cas pour les petites et moyennes installations.
L’élimination du polymère dans les eaux usées dépend de sa solubilité et de sa capacité d’adsorption sur les boues. En outre, la masse moléculaire a une incidence puisque les polymères de masse moléculaire élevée sont éliminés dans une proportion élevée des effluents (c’est-à-dire avant l’étape des biosolides) comparativement aux polymères de faible masse moléculaire (USEPA, 2008). Sur la base de ces considérations, le taux d’élimination par l’UTEE est estimé à 75 % pour le MHD5MH, et à 95 % pour le MHD34MH. Le facteur de dilution dans les eaux réceptrices est de 3,8 pour ce scénario.
Pour la forme n = 5, on utilise la tranche supérieure pertinente des quantités déclarées (100 à 1 000 kg/an) pour calculer la concentration dans l’environnement.
Pour la forme n = 34, on a utilisé la tranche supérieure de la gamme de quantités déclarées en 2006, soit 10 000 à 100 000 kg/an.
D’après ces hypothèses, la CEE est de 8 × 10-5mg/L pour le MHD5MH, et de 1,6 × 10-3 mg/L pour le MHD34MH (Environnement Canada, 2010c).
Il est à noter que la voie prédominante de rejet du MHDnMH dans l’environnement est l’amendement du sol avec des biosolides. D’après la masse moléculaire élevée de la substance et sa très faible solubilité dans l’eau, et d’après les données toxicologiques concernant l’analogue (PDMS), on peut présumer que les boues enfouies ou incinérées qui contiennent du MHDnMH ne seront pas dispersées dans l’environnement. Dans le sol, la substance devrait être immobile et subir une dégradation rapide; elle n’occasionnera donc pas une exposition significative pour les organismes aquatiques ou terrestres.
B – Rejets commerciaux et par les consommateurs
Lorsqu’il est utilisé comme agent de vulcanisation pour le caoutchouc de silicone, des adhésifs ou des revêtements protecteurs à base de résines, le MHDnMH est presque entièrement incorporé dans les polymères par réticulation. La plus grande partie de la matrice adhésive devrait être envoyée dans les sites d’enfouissement avec les objets sur lesquels elle est appliquée. La quantité totale rejetée dans l’environnement (eau et sol) en raison de l’utilisation par les consommateurs devrait être très faible. Par conséquent, l’exposition de la faune à cette substance devrait être négligeable.
Caractérisation du risque écologique
La démarche suivie dans la présente évaluation préalable consistait à examiner les divers renseignements à l’appui et à tirer des conclusions suivant la méthode du poids de la preuve et le principe de prudence requis par la LCPE (1999). Les éléments de preuve pris en compte comprennent les résultats d’un calcul prudent du quotient de risque ainsi que des renseignements sur la persistance, la bioaccumulation, la toxicité, les sources et le devenir de la substance dans l’environnement.
Le MHDnMH devrait être persistant dans l’air, l’eau et les sédiments. Le polymère devrait également présenter un faible potentiel de bioaccumulation. Les volumes modérés de MHDnMH qui sont fabriqués ou utilisés au Canada, combinés aux utilisations de cette substance, indiquent un faible potentiel de rejet dans l’environnement au Canada. Lorsqu’il est rejeté dans l’eau, il pourrait demeurer à la surface comme le PDMS, mais finira par se répartir dans les sédiments. En ce qui concerne les effets du polymère dans l’eau, son potentiel de toxicité devrait être faible pour les organismes aquatiques.
Les concentrations estimées sans effet (CESE) ont été calculées séparément pour les polymères ayant une masse moléculaire faible ou moyenne en nombre.
Dans le cas du MHD5MH, une CL50modélisée de 0,038 mg/L sur une période de 14 jours a été utilisée comme VCT pour les poissons afin de caractériser le risque pour les organismes aquatiques. Il est à noter que cette valeur modélisée est plus faible que celles indiquées dans les études de laboratoire. En appliquant un facteur d’évaluation de 100 à cette VCT afin de tenir compte de la variabilité interspécifique et intraspécifique sur le plan de la sensibilité, de l’extrapolation de la toxicité chronique sur le terrain à partir de la toxicité aiguë en laboratoire ainsi que de l’incertitude associée aux prévisions modélisées, on a obtenu une CESE de 3,8 × 10-4 mg/L pour le MHD5MH.
La CESE pour le MHD34MH a été calculée en divisant la valeur de toxicité chronique sans effet de 91 mg/L (en tant que valeur expérimentale valable la plus sensible pour un PDMS, dont la masse moléculaire est la plus proche de celle du MHD34MH) par un facteur d’évaluation de 100 pour tenir compte de la variabilité interspécifique et intraspécifique sur le plan de la sensibilité et de l’incertitude associée à l’utilisation de données tirées d’un polymère analogue, ce qui donne un résultat de 0,91 mg/L.
Une analyse du quotient de risque a été effectuée pour le MHD5MH et le MHD34MH. Cette analyse fondée sur des estimations prudentes de l’exposition et sur les renseignements toxicologiques portait sur le milieu aquatique et visait à déterminer s’il existe un potentiel d’effets écologiques nocifs au Canada.
Le scénario industriel propre au site, qui est présenté ci-dessus, tient compte des plans d’eaux récepteurs réels. Il s’est traduit par une concentration estimée dans l’environnement (CEE) de 8 × 10-4 mg/L pour le MHD5MH et de 1,6 × 10-3 mg/L pour le MHD34MH (Environnement Canada, 2010c). Les quotients de risque (QR=CEE/CESE) sont d’environ 0,21 pour le MHD5MH et de 2 × 10-3 pour le MHD34MH. Par conséquent, les effets nocifs sur les organismes aquatiques sont peu probables.
Cette information porte à croire que le MHDnMH (n ≥ 5) ne devrait pas avoir d’effets nocifs sur les organismes aquatiques au Canada.
Lorsque le MHDnMH est rejeté dans un plan d’eau, il se répartit dans les matières particulaires en suspension et les sédiments benthiques, où les organismes qui y vivent seront exposés à la substance. Néanmoins, on ne dispose d’aucune donnée de surveillance environnementale propre aux organismes vivant dans les sédiments pour cette substance. D’après les données expérimentales sur la substance analogue (PDMS), la toxicité du MHDnMH devrait être faible pour les espèces benthiques. Par conséquent, compte tenu de l’exposition au polymère, on estime que les effets nocifs découlant d’une exposition au MHDnMH sont improbables pour les organismes vivant dans les sédiments au Canada.
Incertitudes dans l’évaluation des risques pour l’environnement
Une incertitude majeure dans l’évaluation découle de la complexité du polymère. À la différence d’une substance chimique définie, on peut décrire le polymère uniquement par une répartition de structures homologues ayant différentes masses moléculaires. La masse moléculaire moyenne, les fractions de différentes masses moléculaires ainsi que les impuretés varient en fonction des formulations du polymère. Il convient de noter que l’évaluation portait sur les préoccupations relatives au polymère commercialisé au Canada (MHD34MH) et comprenait également le composant ayant une masse moléculaire de 500 g/mol (MHD5MH).
Une autre incertitude majeure concerne le manque de données sur les propriétés physiques et chimiques du MHDnMH. Le polymère peut seulement être caractérisé par les structures du monomère. En raison de sa masse moléculaire supérieure à 1 000 g/mol, on considère généralement qu’il se trouve en dehors du champ d’application des modèles RQSA actuels. Par conséquent, les prévisions modélisées ne s’appliquent qu’au polymère MHD5MH, alors que les données expérimentales pour les polymères de siloxane analogues ont été utilisées pour évaluer tant le MHD5MH que le MHD34MH. La comparaison des compositions chimiques du MHDnMH et de ses analogues semble indiquer que la différence dans les unités répétées et les unités terminales n’influencera pas leurs propriétés physiques et chimiques de façon importante.
Étant donné que les ensembles d’étalonnage des modèles RQSA ne comprennent pas beaucoup de composés de siloxane, les prévisions modélisées pour le MHD5MH sont incertaines et interprétées en faisant preuve d’un jugement scientifique. Les principaux paramètres liés aux propriétés physiques et chimiques sont estimés à l’aide des modèles RQSA et comparés aux mesures expérimentales pour les méthylsiloxanes linéaires analogues afin d’effectuer une modélisation plus approfondie. En cas de conflit dans les prévisions du potentiel de bioaccumulation, davantage de poids est accordé à l’observation dans les études expérimentales sur les analogues appropriés.
L’incertitude est également liée au manque de données sur les concentrations de MHDnMH dans l’environnement au Canada. Toutefois, la majorité du polymère fabriqué devrait être exporté à l’extérieur du pays, et les rejets dans l’environnement canadien devraient être faibles.
On ne saisit pas complètement le métabolisme du polymère. Bien que la clairance observée du polymère de siloxane (PDMS) soit rapide chez le poisson, on n’a pas déterminé si ce phénomène observé était véritablement en lien avec le métabolisme.
Étant donné que le MHDnMH est utilisé dans d’autres pays, il est possible qu’il entre sur le marché canadien comme composant d’articles manufacturés ou de produits de consommation. Cependant, les renseignements obtenus dans le cadre de l’enquête menée en vertu de l’article 71 n’indiquent pas qu’il est présent dans ces types de produits au Canada. Les renseignements disponibles ne sont pas suffisants actuellement pour calculer une estimation quantitative permettant de définir l’importance de cette source. On estime cependant que les proportions de MHDnMH rejetées dans les divers milieux naturels ne seraient pas très différentes de celle estimée dans la présente évaluation. On reconnaît également la possibilité que des rejets proviennent des sites d’enfouissement et contribuent aux concentrations environnementales globales.
Évaluation de l’exposition
Milieu naturel
Aucune donnée empirique sur les concentrations de MHDnMH dans les milieux naturels au Canada n’a été relevée. D’après son profil d’utilisation, le MHDnMH ne devrait pas être présent dans les aliments et les boissons au Canada. Comme on s’attend à ce que le polymère fabriqué soit en grande partie exporté à l’extérieur du pays, les rejets dans l’environnement canadien devraient être faibles. Les concentrations environnementales ont été estimées à l’aide des pourcentages des pertes prévus par l’outil de débit massique présenté au tableau 3 de la section « Rejet dans l’environnement » (Environnement Canada, 2010b). Ces pourcentages ont été appliqués à la quantité totale de MHDnMH sur le marché au Canada en 2006. Selon une estimation prudente, cette quantité pourrait atteindre jusqu’à 100 000 kg (Environnement Canada, 2010a). On estime les pertes à 1 000 kg dans l’eau à partir des eaux usées, à 100 kg dans l’air en raison des émissions atmosphériques et à 1 300 kg dans le sol par les sites d’enfouissement et les pertes au sol.
Les pertes estimées ont été utilisées dans ChemCAN, un modèle régional de fugacité de niveau III en champ lointain propre au Canada (ChemCAN, 2003). Aux fins de la modélisation, la structure oligomérique n = 5, d’une masse moléculaire d’environ 500 g/mol, a été utilisée. Cette forme est vendue sous le no CAS 70900-21-9 dans certaines versions commerciales de ce polymère et pourrait être présente en très faibles concentrations dans d’autres versions commerciales de masse moléculaire plus élevée du polymère (p. ex. dans la forme de masse moléculaire moyenne en nombre n = 34); elle est jugée adéquate pour le modèle ChemCAN. Les concentrations environnementales estimées sont indiquées à l’annexe III. On a obtenu des valeurs prudentes de la limite supérieure d’absorption quotidienne du MHDnMH pour la population générale au Canada sur la base des concentrations environnementales estimées, qui se sont de l’ordre de nanogrammes (10-9 g par kg p.c. [kilogramme de poids corporel]) par jour. De plus, en raison de la très faible pression de vapeur du MHDnMH, les concentrations dans l’air devraient être faibles.
Produits de consommation
Le MHDnMH est principalement utilisé comme produit intermédiaire dans la production de polymères de silicone non destinés à la population générale (Environnement Canada, 2010a).
Cependant, le MHDnMH est un composant de quatre types de produits cosmétiques au Canada : adhésif pour soutien-gorge (30 à 100 % en poids), crème décolorante pour la peau (0,1 à 0,3 % en poids), rouge à lèvres (< 0,1 % en poids) et maquillage pour les yeux (< 0,1 % en poids) [SDC, 2010]. Les estimations de l’exposition liée à l’utilisation de ces produits de consommation sont présentées à l’annexe IV. L’adhésif pour soutien-gorge est présent dans le revêtement intérieur des soutiens-gorges jetables utilisés avec des vêtements sans bretelles et à dos nu. D’après ces renseignements, l’exposition liée à l’utilisation de soutiens-gorges jetables devrait être de courte durée. L’exposition aiguë potentielle par contact avec la peau selon ce scénario a été estimée à
4,0 × 10-3 mg/kg p.c. par événement. Les crèmes décolorantes pour la peau sont en général appliquées quotidiennement pendant environ trois mois. L’exposition cutanée qui en résulte a été estimée à 0,2 mg/kg p.c. par jour. On a présumé que les rouges à lèvres étaient appliqués quatre fois par jour. L’exposition orale quotidienne liée à cette utilisation a été estimée à 5,6 × 10-4mg/kg p.c. par jour. Dans le cas du maquillage pour les yeux, on a présumé qu’il était appliqué deux fois par jour. L’exposition cutanée quotidienne liée à cette utilisation a donc été estimée à 2,8 × 10-4 mg/kg p.c. par jour.
La confiance dans les estimations de l’exposition à partir de l’environnement est faible. Aucune donnée n’a été relevée dans la littérature en ce qui concerne les concentrations de cette substance dans les milieux naturels. Les estimations de l’exposition liée à l’utilisation de produits de consommation ont été fondées sur les modèles, et la confiance dans les estimations est modérée.
Évaluation des effets sur la santé
Aucune donnée empirique relative aux effets sur la santé n’a été relevée pour le MHDnMH. On estime que les modèles de relations quantitatives structure-activité [R(Q)SA] actuels ne sont pas adaptés à la prévision des effets des polymères sur la santé.
Les produits commerciaux de MHDnMH comprennent des molécules de différentes masses moléculaires en fonction du nombre d’unités répétées dans ces molécules. Le MHDnMH et le polydiméthylsiloxane (PDMS, no CAS 63148-62-9) sont considérés comme des analogues structurels (voir le tableau 1 de la section « Identité de la substance »). Pour cette raison, les données sur les effets du PDSM sur la santé ont été jugés adéquates pour servir de base à l’évaluation des effets potentiels sur la santé associés à une exposition au MHDnMH.
Le Centre d'écologie et de toxicologie de l'industrie chimique européenne s’est penché sur le PDMS (viscosité de 10 à 100 000 cSt) dans le cadre d’une évaluation conjointe des produits chimiques de base (ECETOC, 1994). Cette évaluation indique que les résultats des études de génotoxicité in vitro réalisées avec des bactéries et des cellules de mammifères ne font état d’aucun potentiel mutagène ou clastogène pour le PDMS (ECETOC, 1994).
Le PDMS présente un faible potentiel de toxicité et n’entraîne pas de mortalité lorsque les concentrations testées excèdent les doses limites par inhalation ainsi que par voie orale ou cutanée. Lorsque sa viscosité est faible, le PDMS s’est avéré légèrement irritant pour les yeux, mais il ne constitue pas un irritant ou un sensibilisant pour la peau (ECETOC, 1994).
Les effets liés à une administration orale de PDMS sur les rats, les souris et les chiens ont fait l’objet d’études dans lesquelles les périodes d’exposition variaient de 4 semaines à 2 ans. La dose minimale avec effet nocif observé (DMENO) a été établie à 375 mg/kg p.c. par jour en fonction de l’augmentation des ulcères superficiels de l’estomac observée chez les souris mâles, mais pas chez les souris femelles, exposés pendant 76 semaines à du PDMS présent dans leur nourriture. Les effets d’une exposition cutanée au PDMS pour des périodes de 4 semaines à un an ont également été étudiés chez les lapins et les singes. La dose sans effet nocif observé (DSENO) a été établie à 2 000 mg/kg p.c. par jour, soit la seule dose à l’essai, chez les singes (4 macaques bruns mâles par groupe) après une application cutanée de PDMS (350 cSt), 5 fois par semaine pendant 26 mois. Les études sur l’exposition par inhalation au PDMS ont quant à elles été menées sur le chat, le lapin, le cobaye (un animal pour chacune de ces espèces), le rat et la souris. Cependant, en raison de la faible pression de vapeur du PDMS, les concentrations entraînant des effets n’ont pu être déterminées (ECETOC, 1994).
La toxicité du PDMS sur le développement a été étudiée chez les lapins. Le PDMS était administré durant la gestation par voie cutanée ou par injection sous-cutanée. La toxicité du PDMS sur le développement a également été étudiée chez les rats via des injections sous-cutanées. Dans les deux études d’administration cutanée chez les lapins le PDMS a été administré à une dose de 200 mg/kg p.c. par jour; une étude utilisant du PDMS 10 cSt et l’autre du PDMS 350 cSt. Même si deux études sur la toxicité par voie cutanée ont rapporté de faibles incidences d’hernie ombilicale, d’hippocratisme digital et de malformation de la partie avant du crâne, ces résultats n’étaient pas significatifs sur le plan statistique. Les quatre études comprenant des injections sous-cutanées ont également fait état d’effets nocifs sur le développement qui étaient significatifs sur le plan statistique à toutes les doses testées. En outre, le PDMS (10 à 1 000 cSt) ne s’est pas montré cytotoxique pour les cellules embryonnaires humaines (ECETOC, 1994; Siddiqui, 1994; Siddiqui et al., 2002).
La toxicité du PDMS (350 cSt) pour la reproduction a été étudiée chez des rats mâles et femelles auxquels on a administré cette substance par injection sous-cutanée pendant deux semaines avant l’accouplement et chez des singes mâles qui y ont été exposés par voie cutanée à une dose de 2 000 mg/kg p.c. par jour pendant 26 mois avant qu’ils s’accouplent avec des femelles réceptives. Aucun effet sur la fertilité, la performance reproductrice des mâles ou le développement n’a été observé (ECETOC, 1994).
Une étude de 2 ans a été réalisée sur l’absorption alimentaire de PDMS (10 cSt) par des rats à des doses de 0, 100, 300 ou 1 000 mg/kg p.c. par jour (Meeks et al., 2005). Une irritation locale des yeux a été observée chez les rats mâles et femelles de tous les groupes de traitement après 24 mois ainsi que du canal lacrymo-nasal (échelle microscopique) chez les mâles ayant reçu une dose de 1 000 mg/kg p.c. par jour. Une augmentation significative sur le plan statistique de l’incidence d’adénomes des cellules des îlots pancréatiques a été notée chez les rats mâles auxquels on a administré une dose de 1 000 mg/kg p.c. par jour. Les chercheurs n’ont pas considéré ces effets comme étant liés au traitement puisqu’ils n’ont constaté aucune augmentation des changements prénéoplasiques en rapport avec l’étude, ainsi qu’en raison de l’absence d’effets chez les femelles traitées, de l’incidence élevée d’adénomes des cellules des îlots pancréatiques dans le groupe des animaux témoins en rétablissement et des diverses incidences publiées pour ce type de tumeurs chez les animaux témoins. Par ailleurs, ils n’ont observé aucun autre effet lié au traitement. Ils ont établi la DSEO pour l’oncogénicité à 1 000 mg/kg p.c. par jour, soit la dose la plus élevée de l’étude. Qui plus est, une irritation oculaire a été observée dans le cadre d’une étude de 13 semaines menée sur des rats exposés par voie alimentaire à une dose de 5 000 ppm (700 mg/kg p.c. par jour) de PDMS (10 ou 350 cSt) [Siddiqui et al., 2002].
L’absorption de PDMS (35 à 1 200 cSt) par voie orale a été étudiée chez des rats auxquels des doses uniques ou répétées (13 jours) ont été administrées. Les taux globaux d’absorption étaient inférieurs à 0,2 % à des doses allant jusqu’à 2 500 mg/kg p.c. L’absorption de PDMS (100 cSt) par voie cutanée a été étudiée chez des sujets humains volontaires à une dose allant jusqu’à 50 mg/kg p.c. pour une période de 10 jours. Aucune absorption cutanée n’a été observée (ECETOC, 1994). De plus, le PDMS n’a pas eu d’incidence sur l’absorption gastro-intestinale du glucose chez les sujets (ECETOC, 1994).
Dans l’ensemble, les données disponibles indiquent que le PDMS ne présente pas de danger pour la santé des humains (ECETOC, 1994). Le PISSC (2009) a établi à 0,8 mg/kg p.c. une dose journalière acceptable temporaire de PDMS par jour en se basant sur une DSEO de 150mg/kg p.c. par jour provenant d’une étude de 3 mois menée sur le rat exposé par voie alimentaire (seule cette dose de 150mg/kg p.c. par jour fut utilisée dans l’étude) et en tenant compte d’un certain nombre de considérations associées entre autres à l’irritation oculaire ayant été observée dans d’autres études de toxicité chronique ou subchronique par voie orale. Dans la présente évaluation préalable, la dose minimale avec effet observé de 375 mg/kg p.c. par jour, qui est issue d’une étude de 76 semaines effectuée avec le PDMS comme il est indiqué ci-dessus, est utilisée pour la caractérisation du risque associé au MHDnMH.
La confiance dans l’évaluation des effets toxicologiques du MHDnMH est modérée. Bien qu’aucune information toxicologique propre à la substance n’ait été relevée, il a été jugé approprié d’utiliser les données sur la toxicité du PDMS comme information de base pour l’évaluation des effets potentiels du MHDnMH sur la santé, puisque ces deux substances possèdent des propriétés physiques et chimiques similaires.
Caractérisation du risque pour la santé humaine
Aucune donnée empirique relative aux effets sur la santé n’a été relevée pour le MHDnMH. En s’appuyant sur les données relatives aux effets sur la santé pour le PDMS, une substance analogue, et sur les évaluations de cette substance qui sont fondées sur le poids de la preuve et qui ont été réalisées par des organismes internationaux, on estime que le MHDnMH présente un faible potentiel de risque.
L’exposition environnementale (par l’air, l’eau potable et le sol) au MHDnMH a été estimée comme étant de l’ordre des nanogrammes (10-9 mg) par kg p.c. par jour et donc a été considérée comme étant négligeable. Aucun risque d’exposition à cette substance par l’entremise d’aliments ou de boissons n’est prévu. Une exposition peut toutefois avoir lieu par l’utilisation de produits de consommation qui contiennent du MHDnMH. Les estimations prudentes de la limite supérieure d’exposition au MHDnMH par les voies cutanée et orale liées à l’utilisation de produits de consommation (2,8 ×10-4à 0,2 mg/kg p.c. par jour pour les expositions quotidiennes cutanées; 5,6 × 10-4 mg/kg p.c. par jour pour les expositions quotidiennes par voie orale; et 4,0 × 10-3mg/kg p.c. par événement pour les expositions aigües cutanées) sont inférieures de plusieurs ordres de grandeur à la dose minimale d’effet nocif pour l’exposition cutanée (2 000 mg/kg p.c. par jour; une dose d’effet n’a pas été déterminée) établie pour la substance analogue, le PDMS (PISSC, 2009). Ces marges d’exposition sont jugées adéquates pour tenir compte des incertitudes liées aux bases de données concernant les effets sur la santé et l’exposition.
En raison de la faible pression de vapeur du MHDnMH, l’exposition par inhalation liée à l’utilisation de produits de consommation qui en contiennent est jugée négligeable.
Incertitudes de l’évaluation des risques pour la santé humaine
Il existe une incertitude quant à l’estimation de l’exposition de l’ensemble de la population aux concentrations de MHDnMH dans l’environnement en raison de l’utilisation de modèles et du manque de données canadiennes. Toutefois, comme on connaît les quantités commercialisées pour l’année civile 2006, on les a combinées à des pourcentages de perte estimés à l’aide de l’outil de débit massique d’Environnement Canada afin de modéliser les concentrations dans l’environnement. Comme la valeur maximale des quantités commercialisées a été utilisée dans la modélisation, les résultats modélisés devraient représenter des estimations prudentes de l’exposition environnementale.
En ce qui concerne l’exposition cutanée et orale par l’entremise des produits de consommation, les concentrations maximales présentes dans les produits cosmétiques (selon le Système de déclaration des cosmétiques) ont été utilisées afin d’obtenir des estimations prudentes. Une incertitude persiste quant à la probabilité d’utiliser des adhésifs pour soutien-gorge et des crèmes décolorantes étant donné que la seule utilisation relevée en réponse à un avis publié en application de l’article 71 de la LCPE (1999) était liée à la fabrication d’un article qui n’est pas destiné à la population générale au Canada.
En raison de l’absence de données pour le MHDnMH, un analogue structurel, le PDMS, a été utilisé pour identifier des effets possibles du MHDnMH sur la santé humaine. Bien que l’évaluation des effets sur la santé soit principalement fondée sur les données pour une substance analogue, les marges entre les niveaux d’exposition à partir des milieux naturels ou découlant de l’utilisation de produits de consommation et les niveaux associés à des effets sur la santé dans les études expérimentales ont été considérées comme étant adéquates pour tenir compte des incertitudes dans les bases de données des effets sur la santé et de l’exposition.
Selon les renseignements indiqués dans la présente évaluation préalable, la forme de MHDnMH commercialisée au Canada satisfait aux critères pour les polymères à exigences réglementaires réduites définis dans le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères).
Selon les renseignements disponibles, on estime que le MHDnMH ne pénètre pas dans l’environnement en une quantité, à une concentration ou dans des conditions qui ont ou peuvent avoir un effet nuisible immédiat ou à long terme sur l’environnement ou sa diversité biologique, ou qui constituent ou peuvent constituer un danger pour l’environnement essentiel pour la vie. De plus, le MHDnMH satisfait aux critères de persistance, mais ne satisfait pas aux critères de bioaccumulation définis dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
À la lumière des renseignements disponibles, il est conclu que le MHDnMH ne pénètre pas dans l’environnement en une quantité ou concentration, ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Par conséquent, il est conclu que la forme de MHDnMH pour laquelle les exigences réglementaires sont réduites ne satisfait à aucun des critères énoncés à l’article 64 de la LCPE (1999).
En raison de la complexité associée à la formulation du polymère et des propriétés potentiellement dangereuses associées aux polymères ayant un faible masse moléculaire, on craint que de nouvelles activités qui font intervenir le MHDnMH et qui n’ont pas été relevées ni évaluées en vertu de la LCPE (1999) puissent faire en sorte que les substances répondent aux critères de l’article 64 de laLoi. Pour cette raison, il est recommandé de modifier la Liste intérieure des substances de façon à indiquer que le MHDnMH répond aux critères pour les polymères à exigences réglementaires réduites. Si d’autres formes du MHDnMH qui ne répondent pas aux exigences réglementaires réduites sont introduites sur le marché canadien, elles seront soumises aux exigences du Règlement sur les renseignements concernant les substances nouvelles.
Annelin, R.B. 1979. Rapport interne no I-0005-0669 de la Dow Corning. Cité dans Fendinger et al., 1997.
[AIEPS] Artificial Intelligence Expert System. 2003-2007. Version 2.05. Ottawa (Ont.) : Environnement Canada. Modèle élaboré par Stephen Niculescu. Disponible auprès d’Environnement Canada, Division de l’évaluation écologique, Section de l’évaluation des substances chimiques nouvelles.
Annelin, R.B., Frye, C.L. 1989. The piscine bioconcentration characteristics of cyclic and linear oligomeric permethylsiloxane.The Science of the Total Environment 83:1.
Annelin, R.B., Humble, D.A. 1978. Rapport noI-0005-0596 de la Dow Corning. Cité dans Fendinger et al., 1997.
Annelin, R.B., Klein, R., Varaprath, S. 1994. Rapport interne no 1994-I-0000 de la Dow Corning Corp. Cité dans Fendinger et al., 1997.
[AOPWIN] Atmospheric Oxidation Program for Windows [modèle d’estimation]. 2008. Version 1.92a. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[ARLA] Agence de réglementation de la lutte antiparasitaire. 2007. Note réglementaire REG 2007-04 de l’Agence de réglementation de la lutte antiparasitaire (ARLA) : liste des produits de formulation de l’ARLA. Ottawa (Ont.) : Santé Canada, ARLA. [consultée le 14 mai 2010].
Arnot, J.A., Gobas, F.A.P.C. 2003. A generic QSAR for assessing the bioaccumulation potential of organic chemicals in aquatic food webs. QSAR Comb. Sci. 22(3):337-345.
Atkinson R. 1991. Kinetics of the Gas-Phase Reactions of a Series of Organosilicon Compounds with OH and NO3Radicals and Ozone at 297 ± 2K. Environmental Science and Technology 25:863.
Aubert, M., Aubert, J., Augier, H., Guillemaut, C. 1985. Study of the toxicity of some silicone compounds in relation to marine biological chains. Chemosphere 14:127-138.
Battelle. 1992. Fate and effects of PDMS: Soil amendment sludge disposal. Rapport pour la Dow Corning Corporation, étude no SC 900090 du Battelle. 8 mai 1992. Battelle, Columbus Lab., Ohio, États-Unis. Cité dans ECETOC, 1994.
[BBM] Baseline Bioaccumulation Model. 2008. Gatineau (Qc) : Environnement Canada, Division des substances existantes. [Modèle basé sur celui de Dimitrov et al. 2005]. Disponible sur demande.
[BCFBAF] Bioaccumulation Program for Windows [modèle d’estimation]. 2008. Version 3.00. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[BDIM DPT] Base de données sur les ingrédients non médicinaux de la Direction des produits thérapeutiques [base de données exclusive]. 2010 [consultée en avril 2010]. Disponible auprès de Santé Canada, Division des produits thérapeutiques.
Belt, G.H., King, J.G., Haupt, H.F. 1977. Augmenting summer stream flow by use of silicone antitranspirant. Water Resour. Res. 13(2):267-272.
[BIOWIN] Biodegradation Probability Program for Windows [modèle d’estimation]. 2008. Version 4.10. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
Bruggeman, W.A., Weber-Fung, D., Opperhuizen, A., Van der Steen, J., Wijbenga, A., Hutzinger, O. 1984. Absorption and retention of polydimethylsiloxanes (silicones) in fish: preliminary experiments.Toxicological and experimental chemistry 7:287-296.
Buch, R.R., Ingebrigtson, D.N. 1979. Rearrangement of Polydimethylsiloxane Fluids on Soil. Environmental Science and Technol. 13:676.
Cabridenc, R. 1978. Polydimethylsiloxanes, IRNS. Cité dans le rapport no U/83/208(605) de la TNO à la CEE. Evaluation of the impact of Organo Silicone Compounds on the Aquatic Environment. TNO, La Haye (Pays-Bas). Cité dans ECETOC, 1994.
Canada. 1978. Règlement sur les aliments et drogues. C.R.C., ch. 870. Règlement sur les aliments et drogues.
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999). L.C. 1999, ch. 33, Gazette du Canada, Partie III, vol. 22, n° 3.
Canada. 2000. Loi canadienne sur la protection de l’environnement (1999) : Règlement sur la persistence et la bioaccumulation, C.P. 2000-348, 23 mars 2000, DORS/2000-107,Gazette du Canada, Partie II, vol. 134, n° 7.
Canada. Ministère de l’Environnement, ministère de la Santé. 2006. Loi canadienne sur la protection de l’environnement (1999) : Avis d’intention d’élaborer et de mettre en œuvre des mesures d’évaluation et de gestion des risques que certaines substances présentent pour la santé des Canadiens et leur environnement, Gazette du Canada, Partie I, vol. 140, n° 49.
Canada. Ministère de l’Environnement. 2009. Loi canadienne sur la protection de l’environnement (1999) :Avis concernant les substances du groupe 11 du Défi,Gazette du Canada, Partie I, vol. 143, n° 39.
Canada. Santé Canada. 2010. Base de données d’ingrédients de produits de santé naturels homologués. [base de données sur Internet].
Canada. Santé Canada. 2010. Base de données sur les ingrédients des produits de santé naturels [base de données sur Internet].
Canada. Santé Canada. 2010. Base de données d'ingrédients de produits de santé naturels[base de données sur Internet].
Carpenter, J.C., Cella, J.A., Dorn, S.B. 1995. Study of the degradation of polydimethylsiloxanes on soil. Environmental Science and Technology 29:864-868.
Carpenter, J.C., Leib, T.K., Sabourin, C.L., Spivack, J.L. 1996. Abstract no. PO 578, 17e réunion annuelle de la SETAC, Washington (DC). Cité dans Fendinger et al., 1997.
[CATABOL] Probabilistic assessment of biodegradability and metabolic pathways [modèle informatique]. c2004-2008. Version 5.10.2. Bourgas (Bulgarie) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. CATALOGIC.
ChemCAN [Level III fugacity model of 24 regions of Canada]. 2003. Version 6.00. Peterborough (Ont.) : Trent University, Le centre canadien de modélisation et de chimie environnementales [consulté en mai 2010].
Christensen, K. 1994. Silicone Environmental Health and Safety Council Study Report, Document ID no. 47. Cité dans Fendingeret al., 1997.
[ConsExpo] Consumer Exposure Model [en ligne]. 2006. Version 4.1. Bilthoven (Pays-Bas) : Rijksinstituut voor Volksgezondheid en Milieu (Institut néérlandais de la santé publique et l’environnement). Sécurité des produits.
[CPOP] Canadian POPs Model. 2008. Gatineau (Qc) : Environnement Canada, Division de l’évaluation écologique; Bourgas (Bulgarie) : Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. [Modèle basé sur celui de Mekenyan et al., 2005]. Disponible auprès de la Division de l’évaluation écologique d’Environnement Canada. Voir également Mekenyan et al, 2005.
Craig, P.J. 2003. Organometallic compounds in the environment. John Wiley & Sons Ltd, Angleterre.
Craig, N.C.D., Caunter, J.E., Eales, G.J. 1984. ICI Let. Brixham (Royaume-Uni). Document rédigé pour le Centre européen des silicones. Rapport no I-9039-0004 de la Dow Corning.
Craig, N.C.D., Caunter, J.E. 1990. The effects of polydimethylsiloxane (PDMS) in sediment on the polychaete worm Nereis diversicolor. Chemosphere 21(6):751-759.
Dimitrov, S.D., Dimitrova, N.C., Walker, J.D., Veith, G.D., Mekenyan, O.G. 2002. Predicting bioconcentration factors of highly hydrophobic chemicals. Effects of molecular size. Pure Appl. Chem. 74(10):1823-1830.
Dimitrov, S., Dimitrova, N., Parkerton, T., Comber, M., Bonnell, M., Mekenyan, O. 2005. Base-line model for identifying the bioaccumulation potential of chemicals. SAR QSAR Environ. Res. 16(6):531-554.
Eales, G.J., Taylor, D. 1983. A study of the movement of a polydimethylsiloxane fluid in sediment columns – Phase 2. Rapport I-9039-002 de la Dow Corning. Cité dans ECETOC, 1994.
[ECETOC] Centre d’écologie et de toxicologie de l’industrie chimique européenne. 1994. Joint Assessment of Commodity Chemicals No. 26: Linear Polymethylsiloxanes (viscosity 10 – 100 000 centistokes) CAS No. 63148-62-9. Bruxelles (Belgique) : ECETOC. Rapports JACC.
[ECOSAR] Ecological Structural Activity Relationships [Internet]. 2008. Version 1.00. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
Environnement Canada. 2008. Guidance for Conducting Ecological Assessments under CEPA, 1999, Science Resource Technical Series, Technical Guidance Module: Mass Flow Tool. Document de travail. Gatineau (Qc) : Environnement Canada, Division de l’évaluation écologique. Disponible sur demande.
Environnement Canada. 2010a. Données sur les substances du lot 11 recueillies en vertu de l’article 71 de la Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances identifiées dans le onzième lot du Défi. Données recueillies par Environnement Canada, Division de la mobilisation et de l’élaboration des programmes.
Environnement Canada. 2010b. Assumptions, limitations and uncertainties of the Mass Flow Tool for MHDnMH, CAS RN 70900-21-9. Document provisoire interne. Gatineau (Qc) : Environnement Canada, Division de l’évaluation écologique. Disponible sur demande.
Environnement Canada. 2010c. Industrial Release Report: CAS RN 70900-21-9. Le 19 mai 2010. Gatineau (Qc) : Environnement Canada, Division de l’évaluation écologique. Disponible sur demande.
Environnement Canada, Santé Canada. 2008a. Évaluation préalable pour le Défi : Octamethylcyclotetrasiloxane(D4), n° CAS 556-67-2 [en ligne]. Ottawa (Ont.) : Environnement Canada, Santé Canada. [consulté en mai 2010].
Environnement Canada, Santé Canada. 2008b. Évaluation préalable pour le Défi : Décaméthylcyclopentasiloxane (D5), n° CAS 541-02-6 [en ligne]. Ottawa (Ont.) : Environnement Canada, Santé Canada. [consulté en mai 2010].
Environnement Canada, Santé Canada. 2008c. Évaluation préalable pour le Défi : Décaméthylcyclopentasiloxane (D6), n° CAS 540-97-6 [en ligne]. Ottawa (Ont.) : Environnement Canada, Santé Canada. [consulté en mai 2010].
[EPIsuite] Estimation Programs Interface Suite for Microsoft Windows [modèle d’estimation]. 2008. Version 4.00. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[EQC] Equilibrium Criterion Model. 2003. Version 2.02. Peterborough (Ont.) : Trent University, Canadian Environmental Modelling Centre. Le centre canadien de modélisation et de chimie environnementales.
Fendinger, N.J., Lehmann, R.G., Mihaich, E.M. 1997. Polydimethylsiloxane. Organosilicon Materials. The Handbook of Environmental Chemistry. Berlin, Heidelberg (Allemagne) : Springer-Verlag.
Firmin, R. 1984. Les composés organosiliciés et l’environnement aquatique. Mémoire, Sciences Environnement, Université Libre de Bruxelles. Cité dans le rapport no U/83/208(605) de la TNO à la CEE. Evaluation of the Impact of Organo Silicon Compouns on the Aquatic Environment. TNO, La Haye (Pays-Bas). Cité dans ECETOC, 1994.
Garvey, N., Collins, M.K., Mihaich, E.M. 1996. Abs no. 256, 17e réunion annuelle de la SETAC, Washington (DC) [cité dans Graiver et al., 2003].
Gelest. 2008a. Fiche signalétique : Tetradecamethylhexasiloxane - SIT7089.0. Gelest, Inc., Morrisville (PA) 19067. [consultée en décembre 2010].
Gelest. 2008b. Fiche signalétique : Poly(dimethylsiloxane), hydride terminated – DMS-H03. Gelest, Inc., Morrisville (PA). [consultée le 17 mai 2010].
Gelest. 2010. Silicone réactif : forger de nouveaux liens de polymère. Gelest Inc. Morrisvile (PA) 19067.
Gettings, R.L., Lane, T.H. 1982. Rapport interne noI0005-10957 de la Dow Corning Corp. Cité dans ECETOC, 1994.
Graiver, D., Farminer, K.W., Narayan, R. 2003. A review of the fate and effects of silicones in the environment. Journal of Polymers and the Environment 11(4):129-136.
Guillenaut, G., Aubert, J., Augier, H. 1987. Study on organosilicon contamination and toxicity in relation to the marine biomass. Revue Internationale d’Océanographie Médicale85/86:88.
Henry, K.S., Wieland, W.H., Powell, D.E., Giesy, J.P. 2001. Laboratory analyses of the potential toxicity of sediment-associated polydimethylsiloxne to benthic macroinvertebrates. Environmental Toxicology and Chemistry20(11):2611-2616.
[HENRYWIN] Henry’s Law Constant Program for Microsoft Windows [modèle d’estimation]. 2008. Version 3.20. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
Hill, R.W. 1980. Determination of acute toxicity of DC 561 and DC X2-3168 to mussel (Mytilus edulis), rapport 19039 (6 et 8) de la DC. Cité dans le rapport no U/83/208(605)de la TNO à la CEE. Evaluation of the Impact of Organo Silicone Compounds on the Aquatic Environment. TNO, La Haye (Pays-Bas). Cité dans ECETOC, 1994.
Hill, R.W., Young, B.E., Eales, G.J. 1980. Imperial Chemical Industries Ltd., Brixham, TQ58BA, Angleterre. Determination of acute toxicity of Dow Corning DC 561 to the plaice (Pleuronectes platessa). Rapport no BL/B/2052 rédigé pour la Dow Corning (rapport no I-9030-5 de la DC).
Hill, R.W., Young, B.E., Eales, G.J. 1984. Imperial Chemical Industries Ltd., Brixham, TQ58BA, England. Effect of an organosilicon formulation on embryos and larvae of the sheepshead minnow (Cyprinodon variegatus). Rapport no BL/B/2392A rédigé pour le Centre européen des silicones. 34 p. (rapport no I-9039-0003 de la DC). Cité dans Fendinger et al., 1997 et ECETOC, 1994.
Hobbs, E.J., Keplinger, M.L., Calandra, J.C. 1975. Toxicity of polydimethylsiloxanes in certain environmental systems.Environmental Research 10:397-406.
[HYDROWIN] Hydrolysis Rates Program for Microsoft Windows [modèle d’estimation]. 2008. Version 2.00. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[IARC] International Agency for Research on Cancer Working Group on the Evaluation of Carcinogenic Risks to Humans. 1990. Monographies du CIRC sur l’évaluation des risques de cancérogénicité pour l’homme. Vol.74 : Surgical implants and other foreign bodies.
Kukkonen, J., Landrum, P.F. 1995. Effects of sediment-bound polydimethylsiloxane on the bioavailability and distribution of benzo[a]pyrene in lake sediment to Lumbriculus variegates.Environmental Toxicology and Chemistry 14:523-531.
[KOCWIN] The Soil Adsorption Coefficient Program [modèle d’estimation]. 2008. Version 2.00. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation.
[KOWWIN] Octanol-Water Partition Coefficient Program for Microsoft Windows [modèle d’estimation]. 2008. Version 1.67. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
Lehmann, R.G., Varaprath, S., Frye, C.L. 1994a. Degradation of silicone polymers in soil. Environmental Toxicology and Chemistry 13:1061-1064.
Lehmann, R.G., Varaprath, S., Frye, C.L. 1994b. Fate of silicone degradation products (silanols) in soil. Environmental Toxicology and Chemistry 13:1753-1759.
Lehmann, R.G., Varaprath, S., Annelin, R.B., Arndt, J. 1995. Degradation of silicone polymer in a variety of soils.Environmental Toxicology and Chemistry 14:1299-1305.
Lehmann, R.G., Miller, J.R., Xu, S., Singh, U.B., Reece, C.F. 1998. Degradation of silicone polymer at different soil moistures.Environmental Science and Technology 32:1260-1264.
Levier, R.R. 1988. Permethylated siloxane insect toxicants. Silicon chemistry. COREY-GASPAR – Ellis Howood Publishers – Chap. 15 : 153-160. Cité dans ECETOC, 1994.
Maggi, P., Alzieu, C. 1977. Étude de la nocivité d’huiles polydiméthyl -siloxane à l’égard d’organismes marins. Science et Pêche, Bulletin de l’Institut des Pêches Maritimes. 269:1-3. Cité dans Fendinger et al., 1997; Stevens et al., 2001, et ECETOC, 1994.
Mann, H., Ollenschlager, B., Reichenback-Klinke, H.H. 1977. Reichenbach-Klinke, Untersuchunger zur Wirkung von Siliconölen auf Regenbogenforellen. Fisch. Umwelt. 3:19. Cité dans Fendinger et al., 1997 et ECETOC, 1994.
Meeks, R.G., Jean, P.A., Mertens, J.W., Regan, K.S., Crissman, J.W., Plotzke, K.P. 2005. Chronic toxicity and oncogenicity study of polydimethylsiloxane (PDMS) 10 Cst fluid in Fisher 344 rats.Toxicol. Sci. 84(1-S):308.
Mekenyan, G., Dimitrov, S.D., Pavlov, T.S., Veith, G.D. 2005. POPs: A QSAR system for creating PBT profiles of chemicals and their metabolites. SAR and QSAR Environmental Research16(1-2):103-133.
[MPBPWIN] Melting Point Boiling Point Program for Microsoft Windows [modèle d’estimation]. 2008. Version 1.43. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[NCI] National Chemical Inventories [base de données sur CD-ROM]. 2009. Issue 1. Columbus (OH) : American Chemical Society [consultée en mai 2010]. Inventaires chimiques nationaux.
Nielson, W.R., Heinlein, J.P., Haigh, W.G. 1975. Acaridical and insectisidal activity of various silicone fluids. TSCA 8(c) Submission 87-8215084. Cité dans ECETOC, 1994.
Noll, W. 1968. Chemistry and Technology of Silicones. New York (NY) : Academic Press. [cité dans USEPA, 2008]
[OCDE] Organisation de coopération et de développement économiques. 1994. Groupe des produits chimiques et Comité de gestion. Rapport du président, Troisième réunion des experts de l’OCDE sur les polymères, à Tokyo, du 14 au 16 avril 1993.
[OASIS Forecast] Optimized Approach based on Structural Indices Set [en ligne]. 2005. Version 1.20. Bourgas (Bulgarie) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. Logiciels OASIS.
Opperhuizen A, Van Der Velde EW, Gobas FAPC, Liem DAK, Van Der Steen JMD, Hutzinger O. 1985. Relationship between bioconcentration in fish and steric factors of hydrophobic chemicals.Chemosphere 14: 1871-1896.
[PCKOCWIN] Organic Carbon Partition Coefficient Program for Windows [modèle d’estimation]. 2008. Version 2.00. Washington (DC) : United States Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[PISSC] Programme international sur la sécurité des substances chimiques. 2009. Polydimethylsiloxane. Geneva (Suisse) : Organisation mondiale de la santé. (WHO Food Additives Series 60, 3.1.7). Financé conjointement par l’Organisation des Nations-Unies pour l’alimentation et l’agriculture et l’Organisation mondiale de la santé. Évaluation de la sécurité de certains additifs alimentaires
Putt, A.E. 1994. Polydimethylsiloxane (PDMS) – the subchronic toxicity to midge larvae (chironomus tentans) under flow-through conditions. Springborn Laboratories, Inc. Rapport no94-4-5235 présenté au Silicones Environmental Health and Safety Council [cité dans Fendinger et al., 1997].
Putt, A.E., Mihaich, E.M. 1996. Effect of sediment-bound polydimethyl-siloxane (PDMS) to aquatic invertebrates. Abs no. 257, 17e réunion annuelle de la SETAC, Washington (DC) [cité dans Fendinger et al., 1997].
Recherche de produits pharmaceutiques en ligne [base de données sur Internet]. 2010. Ottawa (Ont.) : Santé Canada [consultée en avril 2010].
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2006a. General fact sheet: Limiting conditions and reliability, ventilation, room size, body surface area. Version mise à jour pour ConsExpo 4 [en ligne]. Bilthoven (Pays-Bas) : RIVM (Institut national néérlandais de la santé publique et de l’environnement). Rapport 320104002/2006 du RIVM [consulté en mai 2010].
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2006b. Cosmetics fact sheet: To assess the risks for the consumer [en ligne]. Bilthoven (Pays-Bas) : RIVM (Institut national néérlandais de la santé publique et de l’environnement). Rapport 320104001/2006 du RIVM [consulté en mai 2010].
Sabourin, C.L., Carpenter, J.C., Leib, T.K., Spivack, J.L. 1996. Biodegradation of dimethylsilanediol in soils. Appl. Environ. Microbiol. 62(12):4352-60.
Santé Canada. 1998. Exposure factors for assessing total daily intake of priority substances by the general population of Canada. Rapport inédit. Ottawa (Ont.) : Santé Canada, Direction de l’hygiène du milieu.
Santé Canada. 2009. Liste critique des ingrédients dont l’utilisation est restreinte ou interdite dans les cosmétiques – septembre 2009 [en ligne]. Ottawa (Ont.) : Santé Canada, Sécurité des produits de consommation [consultée le 14 mai 2010].
Sakuratani, Y., Noguchi, Y., Kobayashi, K., Yamada, J., Nishihara, T. 2008. Molecular size as a limiting characteristic for bioconcentration in fish. J. Environ. Biol. 29(1):89-92.
[SDC] Système de déclaration des cosmétiques [base de données exclusive]. 2010. Disponible auprès de Santé Canada, Division des cosmétiques.
Siddiqui, W.H. 1994. Developmental toxicity evaluation of Dow Corning & Ntilde; antifoam A compound, food grad in rabbits.Teratology 49:397.
Siddiqui, W.H., Schardein, J.L., Cassidy, S.L., Meeks, R.G. 1994. Reproductive and developmental toxicity studies of silicone elastomer Q7-2423/Qw7-2551 in rats and rabbits.
Siddiqui, W.H., Blee, M.B., Tompkins, E.C., Meeks, R.G. 2002. 13-weeks dietary and developmental toxicity studies of polydimethylsiloxanes (PDMS) in rats and rabbits.Toxicologist 22(1-S):232.
Sommerlade, R., Parlar, H., Wrobel, D., Kochs, P. 1993. Product analysis and kinetics of the gas-phase reactions of selected organosilicon compounds with OH radicals using a smog chamber-mass spectrometer system. Environmental Science and Technology27 (12): 2435–2440.
Spacie, A. 1972. Acute toxicity of SAG 10 and SAG 350 silicone antifoam to aquatic organisms. Rapport interne, Union Carbide Chemicals Corp., Danbury (États-Unis). Cité dans ECETOC, 1994.
[SPIN] Substances in Preparations in Nordic Countries [base de données sur Internet]. 2006. Copenhague (Danemark) : Conseil des ministres des pays nordiques. Substances dans les préparations dans les pays nordiques[consulté en mai 2010].
Stevens, C. 1998. Environmental degradation pathways for the breakdown of polydimethylsiloxanes. Journal of Inorganic Biochemistry 69(3):203-207.
Stevens, C., Powell, D.E., Mäkelä, P., Karman, C. 2001. Fate and effects of polydimethylsiloxane (PDMS) in marine environments.Marine Pollution Bulletin 42(7):536-543.
[USEPA] United States Environmental Protection Agency. 2008. Interpretive assistance document for assessment of polymers. United States Environmental Protect Agency.
[USEPA] United States Environmental Protection Agency. 2005. Toxic Substances Control Act-Inventory Update Rule (TSCA-IUR) - Information on High Production Volume (HPV) Chemicals. United States Environmental Protection Agency. [consulté en décembre 2005 et en janvier 2006].
Varaprath, S., Frye, C.L., Hamelink, J. 1996. Aqueous solubility of permethylsiloxanes (silicones). Environmental Toxicology and Chemistry 15(8):1263-1265.
Wacker. 1992. Wacker-Broschüre: Silicone Fluids AK, Wacker Chemie AG, Munich, Allemagne. Cité dans ECETOC, 1994.
Watanabe, N., Nakamura, T., Watanabe, E., Sato, E., Ose, Y. 1984a. Bioconcentration potential of polydimethylsiloxane (PDMS) fluids by fish. Science of the Total Environment38:167.
Watanabe, N., Yasuda, Y., Kato, K., Nakanura, T., Funasaka, R., Shimokawa, K., Sato, E., Ose, Y. 1984b. Determination of trace amounts of siloxanes in water, sediments and fish tissues by inductively coupled plasma emission spectrometry. Science of the Total Environment 34(1-2):169-176.
[WATERNT] Water Solubility Program [modèle d’estimation]. 2008. Version 1.01. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[WSKOWWIN] Water Solubility for Organic Compounds Program for Microsoft Windows [modèle d’estimation]. 2008. Version 1.41. Washington (DC) : United States Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
Xu, S. 1998. Hydrolysis of poly(dimethylsiloxanes) on clay minerals as influenced by exchangeable cations and moisture.Environmental Science and Technology 32(20):3162-3168.
Annexe I : Rapport entre la viscosité, le degré de polymérisation et la masse moléculaire (Wacker, 1992, et Fendinger et al., 1997)
Annexe Ia. Données relatives au PDMS (Wacker, 1992, et Fendinger et al., 1997)
| Viscosité (cSt) | Nombre moyen d’unités D* | Masse moléculaire moyenne en nombre (g/mol) |
|---|---|---|
| 10 | 15 | 1 300 |
| 50 | 40 | 3 000 |
| 100 | 70 | 5 000 |
| 1 000 | 200 | 15 000 |
| 10 000 | 500 | 37 000 |
| 100 000 | 1 000 | 74 000 |
Annexe Ib. Données relatives au PDMS, tirées de Noll (1968, citées dans USEPA, 2008)
| Viscosité (cSt) | Nombre moyen d’unités D | Masse moléculaire moyenne en nombre (g/mol) |
|---|---|---|
| 60 | 50 | 3 600 |
| 140 | 110 | 8 000 |
| 440 | 230 | 17 000 |
| 680 | 280 | 21 000 |
| 1 440 | 400 | 30 000 |
| 10 000 | 800 | 60 000 |
| 50 000 | 1 200 | 88 000 |
| 100 000 | 1 400 | 103 000 |
| 300 000 | 1 900 | 143 000 |
Les prévisions modélisées ont seulement été appliquées au MHD5MH et à ses analogues (méthylsiloxanes linéaires de faible masse moléculaire), avec comme seules données d’entrée les SMILES, les masses moléculaires et les données expérimentales.
| Paramètres d’entrée des modèles | Propriétés physico-chimiques et devenir EPIsuite, 2008 (tous les modèles, notamment : |
|||
|---|---|---|---|---|
| MHD5MH (70900-21-9) |
MD3M (141-63-9) |
MD4M (107-52-8) |
MD5M (541-01-5) |
|
| Code SMILES | Si(C)(C)OSi(C) (C)OSi(C)(C) OSi(C)(C)OSi (C)(C)OSi(C) (C)OSi(C)(C) |
O([Si](O[Si](O [Si](C)(C)C)(C) C)(C)C)[Si](O [Si](C)(C)C)(C) C |
O([Si](O[Si](O [Si](C)(C)C)(C) C)(C)C)[Si](O [Si](O[Si](C)(C) C)(C)C)(C)C |
O([Si](O[Si](O [Si](O[Si](C)(C) C)(C)C)(C)C) (C)C)[Si](O[Si] (O[Si](C)(C)C) (C)C)(C)C |
| Masse moléculaire (g/mol) | 505,10 | 384,84 | 459,00 | 533,15 |
| Point de fusion (oC) | ||||
| Point d’ébullition (°C) | ||||
| Température (oC) | ||||
| Masse volumique (kg/m3) | ||||
| Pression de vapeur (Pa) | ||||
| Constante de la loi de Henry (Pa·m3/mol) | ||||
| Koe (coefficient de partage octanol-eau, sans dimension) | 6,0 | 6,6 | 7,2 | |
| Solubilité dans l’eau (mg/L) | 7,0 × 10-5 | |||
Annexe III : Estimation des concentrations de MHDnMH dans les milieux naturels à l’aide du modèle ChemCAN, version 6.00 (ChemCAN, 2003)[1]
| Milieu[2] | Concentration estimée |
|---|---|
| Air ambiant[3] | 1,74 ng/m3 |
| Eau de surface | 0,128 ng/L |
| Sol | 1,47 × 10-3 ng/g de solides |
| Sédiments | 9,09 ng/g de solides |
[2] Les concentrations du débit entrant par défaut, soit 2 ng/m3 dans l’air et 3 ng/L dans l’eau ont été précisées par ChemCAN, version 6.00.
[3] La demi-vie de dégradation oxydative dans l’air a été estimée à 5,125 jours (AOPWIN, 2008) et à 3 semaines dans le sol (selon les données sur la dégradation du PDMS dans le sol).
Annexe IV : Estimations de l’exposition cutanée au MHDnMH liée à l’utilisation de soutiens-gorges jetables, de crème décolorante pour la peau, de maquillage pour les yeux et de rouge à lèvres
| Produit | Hypothèses | Exposition estimée |
|---|---|---|
| Adhésif pour soutien-gorge[1] | Dose appliquée = (épaisseur du produit sur la peau) (surface exposée) (100 %) (densité du produit) / poids corporel
= (0,002 m) (0,1575 m2) (1) (0,90 kg/m3) / 70,9 kg = 0,284 mg / 70,9 kg = 4,0 × 10-3 mg/kg p.c. |
Dose aiguë = 4,0 × 10-3 mg/kg p.c. par événement |
| Crème décolorante pour la peau[1] | Utilisation du modèle ConsExpo v4.1 (ConsExpo, 2006).
|
Dose cutanée quotidienne : 0,2 mg/kg p.c. par jour |
| Maquillage pour les yeux1 | Utilisation du modèle ConsExpo v4.1 (ConsExpo, 2006).
|
Dose cutanée chronique : 2,8 × 10-4 mg/kg p.c. par jour |
| Rouge à lèvres[1] | Utilisation du modèle ConsExpo v4.1 (ConsExpo, 2006).
|
Dose orale chronique : 5,6 × 10-4 mg/kg p.c. par jour |
Notes de bas de page
[2] La masse équivalente du groupe fonctionnel (MEGF) est, pour les groupements cationiques, le rapport entre la masse du polymère et le nombre de moles du groupement cationique. Ainsi, les polymères comportant relativement peu de groupements cationiques se caractérisent par une MEGF élevée.
Cette page Web a été archivée dans le Web
L'information dont il est indiqué qu'elle est archivée est fournie à des fins de référence, de recherche ou de tenue de documents. Elle n'est pas assujettie aux normes Web du gouvernement du Canada et elle n'a pas été modifiée ou mise à jour depuis son archivage. Pour obtenir cette information dans un autre format, veuillez communiquer avec nous.
Archivée
les siloxanes et silicones, diméthyl-, terminés par un atome d’hydrogène
Numéro de registre du Chemical Abstracts Service
70900-21-9
Environnement Canada
Santé Canada
Septembre 2011
Table des matières
- Sommaire
- Introduction
- Identité de la substance
- Propriétés physiques et chimiques
- Sources
- Utilisations
- Rejets dans l'environnement
- Devenir dans l'environnement
- Persistance et potentiel de bioaccumulation
- Potentiel d'effets nocifs sur l'environnement
- Potentiel d'effets nocifs sur la santé humaine
- Conclusion
- Références
- Annexe I : Rapport entre la viscosité, le degré de polymérisation et la masse moléculaire (Wacker, 1992, et Fendinger et al., 1997)
- Annexe II : Table de résumé des données du modèle PBT
- Annexe III : Estimation des concentrations de MHDnMH dans les milieux naturels à l'aide du modèle ChemCAN, version 6.00 (ChemCAN, 2003)
- Annexe IV : Estimations de l'exposition cutanée au MHDnMH liée à l'utilisation de soutiens-gorges jetables, de crème décolorante pour la peau, de maquillage pour les yeux et de rouge à lèvres
Conformément à l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) [LCPE (1999)], les ministres de l’Environnement et de la Santé ont effectué une évaluation préalable de la substance MHDnMH (siloxanes et silicones, diméthyl-, terminés par un atome d’hydrogène), dont le numéro de registre du Chemical Abstracts Service est 70900-21-9. Une priorité élevée a été accordée à l’évaluation préalable de cette substance inscrite au Défi ministériel, car, d’après les prévisions modélisées, elle répond aux critères de la catégorisation écologique relatifs à la persistance, au potentiel de bioaccumulation et à la toxicité intrinsèque pour les organismes non humains et on croit qu’elle est commercialisée au Canada.
L’évaluation des risques que présente le MHDnMH pour la santé humaine n’a pas été jugée hautement prioritaire à la lumière des résultats fournis par les outils simples de détermination du risque d’exposition et du risque pour la santé élaborés aux fins de la catégorisation des substances de la Liste intérieure des substances. Par conséquent, la présente évaluation est axée sur les renseignements utiles à l’évaluation des risques pour l’environnement.
À l’origine, le MHDnMHC a été classé dans la catégorie des UVCB organiques (substances de composition inconnue ou variable, produits de réactions complexes ou matières biologiques) au cours de la catégorisation de la Liste intérieure des substances. D’après les nouveaux renseignements obtenus, la substance est considérée comme un polymère de siloxane organique.
Le MHDnMH n’est pas produit naturellement dans l’environnement. En 2006, entre 10 000 et 100 000 kg de cette substance ont été fabriqués au Canada, et moins de 100 kg ont été importés au pays.
Selon l’utilisation déclarée, le MHDnMH est fabriqué en tant que polymère intermédiaire, qui est par la suite exporté en vrac pour la fabrication de plastiques. Le procédé industriel utilisé entraîne le rejet du polymère en petite quantité dans les eaux usées, ainsi que dans l’air et le sol, mais dans une moindre mesure. Toutefois, les rejets totaux dans l’environnement ne sont pas importants.
Selon les données actuelles, la forme de MHDnMH commercialisée au Canada satisfait aux critères pour les polymères à exigences réglementaires réduites précisés dans le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères). Étant donné que les polymères sont souvent des mélanges complexes et que leur masse moléculaire varie en fonction du nombre d’unités répétées, deux formes du polymère de deux masses moléculaires différentes ont été prises en compte dans cette évaluation. Cette approche vise à répondre aux préoccupations liées aux formes du polymère ayant une masse moléculaire moyenne en nombre (p. ex., MHDnMH, où n = 34) et une masse moléculaire faible (p. ex., MHDnMH, où n = 5).
On a utilisé l’information relative un polymère de siloxane analogue, le polydiméthylsiloxane (PDMS), pour évaluer le MHDnMH. D’après les données sur l’analogue utilisées pour la lecture croisée, la substance devrait être persistante dans l’environnement. D’après l’information à propos de la bioaccumulation de l’analogue, et compte tenu de sa masse moléculaire relativement élevée, elle n’est probablement pas biodisponible et son potentiel de bioaccumulation dans les tissus adipeux des organismes devrait être faible. Elle répond donc aux critères de persistance énoncés dans le Règlement sur la persistance et la bioaccumulation, mais ne répond pas à ceux de bioaccumulation. Qui plus est, les nouvelles données de toxicité modélisées et les données expérimentales sur un polymère analogue indiquent que le MHDnMH représente un faible risque pour les organismes qui se trouvent dans l’eau, le sol et les sédiments.
Aux fins de la présente évaluation préalable, un scénario d’exposition prudent a été élaboré. Selon ce scénario, les rejets industriels de MHDnMH ont lieu dans le milieu aquatique. La concentration estimée dans l’environnement (CEE) dans l’eau pour les organismes aquatiques était très inférieure à la concentration estimée sans effet (CESE). Par conséquent, d’après les renseignements inclus dans la présente évaluation préalable, le MHDnMH ne devrait pas pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou la diversité biologique, ni à mettre en danger l’environnement essentiel pour la vie.
Aucune donnée empirique relative aux effets sur la santé n’a été relevée pour le MHDnMH. En s’appuyant sur les données relatives aux effets sur la santé du PDMS, et sur les évaluations de cette substance qui sont fondées sur le poids de la preuve et qui ont été réalisées par des organismes internationaux, on estime que le MHDnMH présente un faible potentiel de risque.
Selon les concentrations estimées de MHDnMH dans l’environnement (air, eau potable et sol), l’exposition de l’ensemble de la population devrait être négligeable. Cette exposition peut avoir lieu par l’utilisation de produits de consommation qui contiennent du MHDnMH. Les marges entre l’estimation de la limite supérieure d’exposition pour le MHDnMH et les niveaux associés à des effets dans le cadre des études des effets du PDMS, l’analogue, sur la santé sont considérées comme adéquates pour tenir compte des incertitudes dans les bases de données des effets sur la santé et de l’exposition. On estime donc que le MHDnMH ne pénètre pas dans l’environnement en une quantité, à une concentration ou dans des conditions qui constituent ou peuvent constituer un danger au Canada pour la vie ou la santé humaines.
D’après les renseignements disponibles, il est conclu que la forme à exigences réglementaires réduites du MHDnMH ne satisfait à aucun des critères de l’article 64 de la LCPE (1999).
En raison de la complexité associée à la formulation du polymère et des propriétés potentiellement dangereuses associées aux polymères ayant une faible masse moléculaire, on craint que les utilisations nouvelles MHDnMH qui ne sont ni décelées ni évaluées en vertu de la LCPE (1999) fassent en sorte que les substances répondent aux critères de l’article 64 de la Loi. Pour cette raison, il est recommandé de modifier la Liste intérieure des substances de façon à indiquer que le MHDnMH répond aux critères pour les Polymères à exigences réglementaires réduites. Si d’autres formes du MHDnMH qui ne répondent pas aux exigences réglementaires réduites sont introduites sur le marché canadien, elles seront soumises aux exigences du Règlement sur les renseignements concernant les substances nouvelles.
La Loi canadienne sur la protection de l’environnement (1999) [LCPE (1999)] (Canada, 1999) exige que les ministres de l’Environnement et de la Santé procèdent à une évaluation préalable des substances qui répondent aux critères de catégorisation énoncés dans la Loi afin de déterminer si elles présentent ou sont susceptibles de présenter un risque pour l’environnement ou la santé humaine.
Selon l’information obtenue dans le cadre de la catégorisation, les ministres ont jugé qu’une attention hautement prioritaire devait être accordée à un certain nombre de substances, à savoir :
- celles qui répondent à tous les critères environnementaux de catégorisation, notamment la persistance (P), le potentiel de bioaccumulation (B) et la toxicité intrinsèque pour les organismes aquatiques (Ti), et que l’on croit être commercialisées au Canada;
- celles qui répondent aux critères de catégorisation pour le plus fort risque d’exposition (PFRE) ou qui présentent un risque d’exposition intermédiaire (REI) et qui ont été jugées particulièrement dangereuses pour la santé humaine, compte tenu des classifications qui ont été établies par d’autres organismes nationaux ou internationaux concernant leur cancérogénicité, leur génotoxicité ou leur toxicité pour le développement ou la reproduction.
Le 9 décembre 2006, les ministres ont donc publié un avis d’intention dans la Partie I de la Gazette du Canada(Canada, 2006) dans lequel ils priaient l’industrie et les autres intervenants de fournir, selon un calendrier déterminé, des renseignements précis qui pourraient servir à étayer l’évaluation des risques, ainsi qu’à élaborer et à évaluer les meilleures pratiques de gestion des risques et de bonne gestion des produits pour ces substances jugées hautement prioritaires.
On a décidé d’accorder une attention hautement prioritaire à l’évaluation des risques pour l’environnement du MHDnMH (siloxanes et silicones, diméthyl-, terminés par un atome d’hydrogène), car cette substance a été initialement jugée persistante, bioaccumulable et intrinsèquement toxique pour les organismes aquatiques au cours de la catégorisation visant la Liste intérieure des substances (LIS), et il semble qu’elle est commercialisée au Canada. Le volet du Défi portant sur cette substance a été publié dans laGazette du Canada le 26 septembre 2009 (Canada, 2009). En même temps a été publié le profil de cette substance, qui présentait l’information technique (obtenue avant décembre 2005) sur laquelle a reposé sa catégorisation. Des renseignements sur les propriétés et les utilisations de cette substance ont été reçus en réponse au Défi.
Même si l’évaluation des risques que présente le MHDnMH pour l’environnement est jugée hautement prioritaire, cette substance ne répond pas aux critères de catégorisation pour le PFRE ou le REI, ni aux critères définissant un grave risque pour la santé humaine, compte tenu du classement attribué par d’autres organismes nationaux ou internationaux quant à sa cancérogénicité, à sa génotoxicité ou à sa toxicité sur le plan du développement ou de la reproduction.
Les évaluations préalables mettent l’accent sur les renseignements jugés essentiels pour déterminer si une substance répond aux critères énoncés à l’article 64 de la LCPE (1999). Les évaluations préalables visent à examiner des renseignements scientifiques et à tirer des conclusions fondées sur la méthode du poids de la preuve et le principe de prudence[1].
La présente évaluation préalable prend en considération les renseignements sur les propriétés chimiques, les dangers, les utilisations et l’exposition, y compris ceux fournis dans le cadre du Défi. Les données qui ont trait à l’évaluation préalable de cette substance proviennent de documents originaux, de rapports de synthèse et d’évaluation, de rapports de recherche réalisés par des intervenants et de recherches documentaires menées récemment, soit jusqu’en mai 2010 dans le cas des sections du document portant sur la santé humaine, et jusqu’en décembre 2010 dans le cas des sections portant sur les aspects écologiques. Les études les plus importantes ont fait l’objet d’une évaluation critique. Par ailleurs, il est possible que les résultats de modélisation aient servi à formuler des conclusions.
Lorsqu’ils étaient disponibles et pertinents, les renseignements contenus dans les évaluations des dangers effectués par d’autres instances ont été utilisés. La présente évaluation préalable ne constitue pas un examen exhaustif ou critique de toutes les données disponibles. Il s’agit plutôt d’un sommaire des renseignements essentiels qui appuient la conclusion proposée.
La présente évaluation préalable a été préparée par le personnel du Programme des substances existantes de Santé Canada et d’Environnement Canada et elle intègre les résultats d’autres programmes exécutés par ces ministères. La partie portant sur l’écologie a fait l’objet d’une étude consignée par des pairs ou d’une consultation de ces derniers. De plus, l’ébauche de la présente évaluation a fait l’objet d’une période de commentaires de 60 jours par le public. Bien que les commentaires reçus de l’extérieur aient été pris en considération, Santé Canada et Environnement Canada sont seuls responsables du contenu final et des résultats de l’évaluation préalable. Les approches suivies pour les évaluations préalables dans le cadre du Défi ont été examinées par un groupe indépendant, soit le Groupe consultatif du Défi.
Les principales données et considérations sur lesquelles repose l’évaluation préalable sont résumées ci-après.
Aux fins du présent document, la substance « siloxanes et silicones, diméthyl-, terminés par un atome d’hydrogène » sera appelée MHDnMH, appellation tirée de sa structure chimique. « MH » fait référence à l’atome de silicone dans les groupes terminaux, qui partage une liaison avec l’oxygène, deux liaisons avec les substituants méthyle et une liaison avec l’hydrogène. « D » symbolise les atomes de silicone de la chaîne principale, qui partagent deux liaisons avec l’oxygène et deux liaisons avec les substituants méthyle, alors que « n » représente le nombre de « D » dans le polymère.
Le MHDnMH a initialement été classé dans la LIS comme un UVCB organique. Selon de nouveaux renseignements obtenus, le MHDnMH se caractérise par 1) la présence d’une unité monomère diméthyl-siloxy et 2) la présence de groupements hydrogène et diméthyle qui sont fixés à l’atome de silicone et qui agissent comme les groupes terminaux du polymère (Environnement Canada, 2010a).
D’après les résultats de la chromatographie sur gel (CG), chaque molécule de MHDnMH aurait une masse moléculaire moyenne en nombre (Mn) d’approximativement 2 700 g/mol (Environnement Canada, 2010a), ce qui correspond en moyenne à 34 unités monomériques diméthylsiloxy (n = 34, d’après la masse moléculaire du monomère diméthylsiloxy, soit 74,15| g/mol). Toute molécule de MHDnMH contient plus de trois monomères. Les différences dans les masses moléculaires (Mm) sont principalement dues aux différences dans le nombre d’unités. Par conséquent, le MHDnMH respecte la définition d’un polymère (OCDE, 1994), résumée ci-dessous :
- molécules caractérisées par une séquence d’un ou de plusieurs types d’unités monomères;
- plus de 50 % des molécules, en poids, possèdent trois unités monomères ou plus liées par covalence à au moins une unité monomère ou un réactif;
- moins de 50 % des molécules, en poids, ont la même masse moléculaire;
- les différences dans les masses moléculaires des molécules sont principalement attribuables à la différence dans le nombre d’unités monomères.
Des oligomères considérablement plus petits (dont la plus faible masse moléculaire fait ~ 500 g/mol) ont été décelés dans le produit polymérique, mais en très faibles concentrations. En outre, d’autres produits sont vendus dans le monde sous le même no CAS (70900-21-9), notamment le polymère ayant une masse moléculaire moyenne d’environ 500 g/mol (Gelest, 2010). Cette masse correspond à un polymère comptant cinq unités monomériques de diméthylsiloxy (n = 5). En raison des aspects susmentionnés, l’évaluation porte tant sur le MHD34MH que sur le MHD5MH afin de tenir compte des polymères de masse moléculaire moyenne en nombre et des polymères de faible masse moléculaire.
L’évaluation prend en considération les données essentielles sur les principaux paramètres pour l’évaluation de la persistance, de la bioaccumulation et de l’écotoxicité des polymères de masse moléculaire moyenne en nombre et des polymères de faible masse moléculaire. Dans certains cas, lorsqu’il n’existe pas de données expérimentales pour le MHDnMH, des données expérimentales de substances chimiques analogues et des modèles fondés sur les relations quantitatives structure-activité (RQSA) sont utilisés pour combler les lacunes.
L’identité du MHDnMH est présentée dans le tableau 1 ci-dessous.
Tableau 1. Identité du MHDnMH
| Numéro de registre du Chemical Abstracts Service (no CAS) | 70900-21-9 |
| Nom dans la LIS | Siloxanes et silicones, diméthyl-, terminés par un atome d’hydrogène |
| Noms relevés dans les National Chemical Inventories (NCI)[1] | Siloxanes and Silicones, di-Me, hydrogen-terminated (TSCA, REACH, ENCS, ECL, PICCS, ASIA-PAC, NZIoC) Siloxanes and silicones, dimethyl hydrogen terminated (AICS) SILOXANE, DI-ME, HYDROGEN TERMINATED (PICCS) |
| Autres noms | Di-Me, dimethylsilyl-terminated siloxanes FH 0023 Hydrogen-terminated di-Me silicones Hydrogen-terminated di-Me siloxanes MCR-H 07 MHD6MH Polysiloxanes, di-Me, hydrogen-terminated PS 542 SE 1886A SE 1887A Silicones, di-Me, dimethylsilyl-terminated Siloxanes and Silicones, di-Me, (dimethylsilyl)-terminated XF 40A6100 Diméthylsiloxanes et silicones, terminés par un atome d’hydrogène |
Groupe chimique (groupe de la LIS) |
Polymère |
| Principale classe chimique ou utilisation | Organosiliciums |
| Principale sous-classe chimique | Siloxane |
| Formule chimique | C(4+2n)H(14+6n)O(1+n)Si(2+n) |
| Structure chimique représentative utilisée dans le modèle d’estimation[2] | 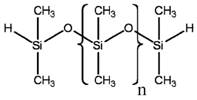 |
| SMILES[3] | MHDnMH (n = 34) ou MHD34MH : sans objet MHDnMH (n = 5) ou MHD5MH : Si(C)(C)OSi(C)(C)OSi(C)(C)OSi(C)(C)OSi(C)(C)OSi(C)(C)OSi(C)(C) |
| Masse moléculaire | MHD34MH : 2 655,45 g/mol MHD5MH : 505,10 g/mol |
[2] Cette substance est un polymère organique défini, c’est-à-dire qu’elle n’est pas un composé chimique défini; elle peut donc être caractérisée par une structure représentative. Pour cette évaluation, deux structures représentatives ont été utilisées, soit une où n = 34 et une où n = 5.
[3] Simplified Molecular Input Line Entry System.
On note que le polymère peut contenir une petite fraction d’impuretés, c’est-à-dire des monomères ou des sous-produits résiduels qui ont une masse moléculaire beaucoup plus faible. La quantité et le type d’impuretés varient en fonction d’une série de facteurs, notamment les différents procédés de fabrication et d’exploitation, les conditions de réaction ainsi que l’utilisation de catalyseurs et de promoteurs. Selon les renseignements reçus (Environnement Canada, 2010a), l’octaméthylcyclotétrasiloxane (D4, no CAS 556-67-2), le décaméthylcyclopentasiloxane (D5, no CAS 541-02-6), le dodécaméthylcyclohezasiloxane (D6, no CAS 540-97-6) et le 1,1,3,3-tétratraméthyldisiloxane (no CAS 3277-26-7) sont des monomères résiduels ou des sous-produits dans les produits polymériques qui portent le même no CAS, soit 70900-21-9. Toutefois, la concentration de ces monomères résiduels et sous-produits varie dans les polymères fabriqués par des entreprises différentes. Le D4, le D5 et le D6 ont déjà été évalués dans le cadre du Défi et, selon les résultats de la CG, le 1,1,3,3-tétratraméthyldisiloxane n’a pas été détecté dans le MHDnMH présent dans le commerce au Canada. Par conséquent, le risque associé à la présence d’impuretés dans le polymère ne sera pas pris en compte dans cette évaluation du MHDnMH.
Contrairement aux substances définies, qui ont une masse moléculaire bien précise, les polymères ont une masse moléculaire variable en fonction du nombre d’unités répétées, qui peut être de trois jusqu’à plusieurs milliers. Pour cette raison, un polymère est habituellement caractérisé par le nombre moyen d’unités répétées qu’il contient ou sa masse moléculaire moyenne en nombre.
Comme le mentionne la section « Identité de la substance », le MHD34MH représente le polymère qui est fabriqué au Canada, alors que le MHD5MH est le produit polymérique produit à l’échelle internationale et dont la masse moléculaire est de 505,10 g/mol. Les approches pour l’évaluation de ces deux produits tiennent compte des différentes masses moléculaires.
Aux fins de l’évaluation, le nombre d’unités répétées (n) peut être indiqué si l’information ne s’applique qu’à l’une des deux formes mentionnées ci-dessus. Si le nombre d’unités répétées n’est pas indiqué, l’évaluation s’applique au polymère MHDnMH (n ≥ 5) en général.
Il n’existe pas de données expérimentales sur les propriétés physiques et chimiques du MHDnMH; des données sur une substance analogue, le polydiméthylsiloxane (PDMS), ont été prises en considération dans l’évaluation.
Un analogue est un produit chimique dont la structure est semblable à celle de la substance évaluée; il devrait donc avoir des propriétés physiques et chimiques, un devenir dans l’environnement et une toxicité similaires. Lorsque des données expérimentales existent pour une propriété particulière d’un analogue, elles peuvent être utilisées pour caractériser la substance évaluée, mais les différences structurelles pouvant avoir une incidence sur la biodisponibilité doivent être notées.
Le PDMS est un autre polymère de siloxane possédant la même unité récurrente de groupements diméthyle liés au silicium de la chaîne principale –Si-O-Si–. La différence entre le MHDnMH et le PDMS réside dans les unités terminales. Contrairement au MHDnMH, où les deux unités terminales comportent un atome d’hydrogène et deux groupements méthyle, le PDMS compte trois groupements méthyle (voir le tableau 2a ci-dessous) à chacune des positions terminales. On peut exprimer la formule du PDMS comme suit : MHDnM. Ces différences ne devraient pas avoir une incidence notable sur les propriétés chimiques et physiques du MHDnMH et du PDMS (lorsque le nombre d’unités récurrentes est le même dans les deux cas). Vu la similarité de ces substances chimiques, les données expérimentales sur le PDMS ont été utilisées pour évaluer le devenir dans l’environnement, le potentiel de persistance et de bioaccumulation, ainsi que l’écotoxicité des deux formes de MHDnMH (n = 5 et n = 34) sans qu’un ajustement qualitatif ne soit nécessaire.
Tableau 2a. Structure chimique du PDMS et du MHDnMH
| Paramètre | PDMS | MHDnMH |
|---|---|---|
| Structure chimique représentative | 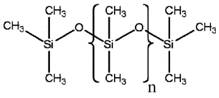 |
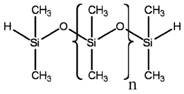 |
MHD5MH
Pour la forme de MHDnMH de faible masse moléculaire (n = 5), plusieurs méthylsiloxanes linéaires (MDnM) ont été utilisés à titre d’analogues (voir le tableau 2b ci-dessous). Ces méthylsiloxanes linéaires (n > 3) sont du PDMS de faible masse moléculaire.
Tableau 2b. Méthylsiloxanes linéaires utilisés comme analogues du MHD5MH
| Nom chimique et no CAS | Formule | Masse moléculaire (g/mol) |
|---|---|---|
| Dodécaméthylpentasiloxane (141-63-9) | MD3M | 384,84 |
| Tétradécaméthylhexasiloxane (107-52-8) | MD4M | 459,00 |
| Hexadécaméthylheptasiloxane (541-01-5) | MD5M | 533,15 |
| Siloxanes et silicones, diméthyl-, terminés par un atome d’hydrogène (70900-21-9) | MHD5MH | 505,10 |
- « M » fait référence aux atomes de silicone dans les groupes terminaux, qui partagent une liaison avec l’oxygène et trois liaisons avec les substituants méthyle.
- « MH » fait référence aux atomes de silicone dans les groupes terminaux, qui partagent une liaison avec l’oxygène, deux liaisons avec les substituants méthyle et une liaison avec l’hydrogène.
- « D » symbolise les atomes de silicone de la chaîne principale, qui partagent deux liaisons avec l’oxygène et deux liaisons avec les substituants méthyle.
Certaines données expérimentales sur les propriétés chimiques et physiques du MDnM ont été transposées au MD4M avec certains ajustements pour tenir compte des différences structurales (c’est-à-dire le nombre d’unités récurrentes). Des modèles RQSA ont également été utilisés pour combler les lacunes lorsqu’aucune donnée expérimentale n’existait pour certaines propriétés physiques et chimiques (voir l’annexe II). Ces modèles (excepté WSKOWWIN, 2008) sont principalement fondés sur des méthodes d’addition de fragments, c’est-à-dire qu’ils s’appuient sur la structure d’un produit chimique donné. Il est indiqué que les ensembles d’étalonnage de la plupart des modèles ne comprennent pas les siloxanes; par conséquent, le MHD5MH ne fait techniquement pas partie du domaine de ces modèles. Cependant, puisqu’une molécule de faible masse comme le MHD5MH demeure neutre dans les conditions observées dans l’environnement, les estimations fondées sur ses fragments et sa masse moléculaire devraient permettre d’obtenir des valeurs approximatives.
Les propriétés physiques et chimiques modélisées pour le MHD5MH sont résumées dans le tableau 2c ci-dessous. Les données expérimentales pour les méthylsiloxanes linéaires analogues (voir le tableau 2b) sont également présentées dans ce tableau. Afin d’améliorer la fiabilité des prévisions des modèles, une méthode d’ajustement des valeurs expérimentales (AVE) a été utilisée dans les sous-modèles d’EPIsuite. Cette méthode a permis d’obtenir des estimations à partir des mesures expérimentales, qui tiennent compte des différences structurelles entre l’analogue et le MHD5MH.
Tableau 2c. Propriétés physiques et chimiques estimées du MHD5MH (masse moléculaire = 505,10 g/mol)
| Propriété | Valeur[1] | Température (°C) |
Référence |
|---|---|---|---|
| Point de fusion (ºC) |
12,02 | MPBPWIN, 2008 | |
| -59 (pour le MD4M) | Gelest, 2008a[5] | ||
| Point d’ébullition (ºC) |
317,45 | MPBPWIN, 2008 | |
| 245 (pour le MD4M) | Gelest, 2008a | ||
| Masse volumique (kg/m3) |
890 (pour le MD4M) | Gelest, 2008a | |
| Viscosité[2] (centistokes, cSt) | 2,6 (pour le MD4M) | Gelest, 2008a | |
| Pression de vapeur (Pa) |
0,10 (7,69 × 10-4 mm Hg) |
25 | MPBPWIN, 2008 |
| < 1 mm Hg (pour le MD4M) | 25 | Gelest, 2008a | |
| Constante de la loi de Henry (Pa·m3/mol) |
2,0 × 107 (2,0 × 102 atm·m3/mol) |
HENRYWIN, 2008 | |
| Log Koe (coefficient de partage octanol-eau) (sans dimension) |
6,6 | KOWWIN, 2008 | |
| 6,7 (extrapolation par l’AVE du MD4M et du MD5M)[3] |
KOWWIN, 2008 | ||
| 6,0 (pour le MD3M) 6,6 (pour le MD4M) 7,2 (pour le MD5M) 7,7 (pour le MD6M) |
Bruggeman et al., 1984 | ||
| Log Kco (coefficient de partage carbone organique-eau) (sans dimension) |
5,7 | PCKOCWIN, 2008 | |
| Solubilité dans l’eau (mg/L) |
2,2 × 10-6 à 2,7 × 10-6 (d’après des log Koe de 6,6 et 6,7) |
25 | WSKOWWIN, 2008 |
| 5,7 × 10-9 à 2,2 × 10-6 (extrapolation par l’AVE du MD4M et du MD5M)[3] |
WATERNT, 2008 | ||
| 3,4 × 10-2 (pour le MDM) 7,0 × 10-5 (pour le MD3M) 1,3 × 10-5 (estimé pour le MD4M) 5,4 × 10-7 (estimé pour le MD5M) |
25 | Varaprath et al., 1996 WSKOWWIN, 2008 | |
| Diamètre transversal (nm)[4] | 1,46 à 2,18 | CPOP, 2008 |
[2] La viscosité d’un polymère est employée pour caractériser la taille des polymères et leur masse moléculaire. Le centistokes (cSt) est l’unité de mesure de la viscosité cinématique d’un polymère.
[3] Une méthode d’ajustement des valeurs expérimentales (AVE) a été utilisée dans EPIsuite pour obtenir des estimations à partir des mesures expérimentales, qui tiennent compte des différences structurelles.
[4] Les valeurs représentent l’étendue des diamètres moléculaires maximums (c.-à-d., les valeurs Dmax) estimés à l’aide du modèle CPOP.
[5] L’information tirée de Gelest (2008a) concerne un produit de MD4M (> 95 %), avec une fraction de MD3M et des siloxanes linéaires de masse moléculaire plus élevée (< 5 %).
D’après les données expérimentales du log Koe et de la solubilité dans l’eau du MD3-6M (voir le tableau 2c), les méthylsiloxaes de faible masse moléculaire sont extrêmement hydrophobes. Leur solubilité dans l’eau est peu élevée (de l’ordre de 10-4 mg/L et moins), et leur coefficient de partage octanol-eau est élevé (log Koe= 6 ou plus).
Comme il possède un hydrure en position terminale, le MHD5MH devrait avoir une solubilité dans l’eau et un coefficient de partage octanol-eau similaire à ceux de l’analogue PDMS de masse moléculaire équivalente. Les prévisions modélisées du log Koe pour le MHD5MH sont de 6,6 sans AVE et de 6,7 avec AVE, ce qui se rapproche des coefficients de partage octanol-eau pour le MD4M (log Koe = 6,6 ) et le MD5M (log Koe = 7,2). Les valeurs estimées de la solubilité dans l’eau du MHD5MH (obtenues à partir des valeurs du log Koe) vont de 2,2 × 10-6 mg/L à 2,7 × 10-6 mg/L; elles se situent donc entre celles du MD4M (1,3 × 10-5 mg/L) et du MD5M (5,4 × 10-7 mg/L).
Selon les prévisions des modèles, le MHD5MH devrait être peu volatil et insoluble dans l’eau. La pression de vapeur estimée est modérée (0,10 Pa) et la solubilité dans l’eau, très faible (~ 2,5 × 10-6 mg/L). La constante estimée de la loi de Henry est en conséquence très élevée, soit 2,0 × 107 Pa m3/mol.
MHD34MH
La masse moléculaire moyenne en nombre du polymère commercialisé au Canada (MHD34MH) est d’environ 2 700 g/mol. Aucune composante dans le polymère ne possède une masse moléculaire inférieure à 500 g/mol, et moins de 5 % des composantes ont une masse moléculaire inférieure à 1 000 g/mol. Ni les unités terminales ni les unités récurrentes du polymère ne comportent de groupements fonctionnels cationiques ou réactifs; la masse équivalente du groupe fonctionnel (MEGF)[2] du MHD34MH est donc supérieure à 1 000 g/mol, ce qui fait que le polymère satisfait aux critères définissant les polymères à exigences réglementaires réduites dans le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères).
Le MHD34MH a une masse moléculaire moyenne en nombre d’environ 2 700 g/mol, ce qui est plus élevé que la limite acceptable dans les modèles RQSA. Le MHD34MH se situe hors du domaine d’application des modèles de sorte qu’aucun modèle RQSA ne peut être utilisé pour évaluer cette substance. Par conséquent, des données transposées du PDMS par lecture croisée ont servi à caractériser les propriétés physiques et chimiques du MHD34MH.
Dans un test de toxicité, on a établi à 0,26 mg/L la solubilité d’un PDMS avec une terminaison hydroxyle (d’approximativement n = 45 et Mm = 3 500 g/mol, d’après la viscosité de 55 cSt pour le PDMS) dans l’eau, avec une concentration à l’équilibre de 0,04 à 0,05 mg/L (Gettings et Lane, 1982). Comme l’hydroxyle en position terminale accroît la solubilité du polymère dans une certaine mesure, on s’attend à ce que la solubilité du MHD34MH dans l’eau soit inférieure à 0,26 mg/L.
Pour les polymères de masse moléculaire élevée, il existe une relation entre la viscosité et la masse moléculaire moyenne (voir l’annexe I). La viscosité est une mesure de la résistance d’un liquide à l’écoulement lorsqu’une force est appliquée sur celui-ci. Il s’agit également d’une mesure de sa capacité à s’écouler. Plus la taille de la molécule du polymère est importante (nombre plus élevé d’unités monomères et masse moléculaire moyenne plus importante), plus le polymère sera « visqueux », ce qui se traduira par une valeur de viscosité élevée (voir l’annexe I). Dans nombre des études sur le PDMS citées dans la présente évaluation, la viscosité était indiquée et a été utilisée pour caractériser la masse moléculaire des polymères.
Les polymères de siloxane ayant une masse moléculaire élevée (y compris le PDMS) ne sont pas volatils et ne devraient se retrouver dans l’air et s’y dégrader (Graiver et al., 2003). Dans le cas d’un polymère avec une masse moléculaire moyenne supérieure à 1 000 g/mol, la pression de vapeur devrait être inférieure à 1,33 × 10-6 Pa (10-8 mm Hg) et la constante de la loi de Henry, inférieure à 1,01 × 10-3 Pa•m3/mol (10-8 atm•m3/mol) (USEPA, 2008). Vu la masse moléculaire élevée (2 655,45 g/mol) du MHD34MH, la forme n = 34 du polymère devrait avoir une pression de vapeur et une constante de la loi de Henry faibles.
Les polymères de siloxane sont des liquides dont l’écoulement est relativement libre, même à des masses moléculaires élevées (la viscosité peut atteindre 500 000 cSt, ce qui équivaut à une masse moléculaire moyenne d’environ 100 000 g/mol) [Fendinger et al., 1997]. Cette situation peut être attribuée au degré élevé de souplesse de la chaîne principale du siloxane et aux faibles forces d’attraction intermoléculaires qui en résultent. Le polymère est caractérisé par un faible point de fusion et un point élevé d’ébullition. Il reste donc à l’état liquide aux températures ambiantes normales (Fendinger et al., 1997; Graiver et al., 2003).
D’après les données sur le PDMS, le MHD34MH devrait être insoluble dans l’eau et son coefficient de partage octanol-eau (Koe) devrait être élevé. Le polymère ne contient pas de groupements fonctionnels pouvant subir une hydrolyse dans l’eau. S’il est rejeté dans l’eau, il pourrait former une fine couche à la surface de l’eau en raison de sa masse volumique légèrement plus faible que celle de l’eau (environ 960 kg/m3) (Fendinger et al., 1997; Environnement Canada, 2010a; ECETOC, 1994).
En considération de ce qui précède, la forme n = 5 du MHDnMH devrait avoir une pression de vapeur modérée; par contre, la forme n = 34 du polymère devrait devenir beaucoup moins volatile avec l’allongement de la chaîne.
Le polymère (tant la forme n = 5 que n = 34) devrait être insoluble dans l’eau, sa masse volumique étant légèrement plus faible que celle de l’eau, et demeurer à l’état liquide aux températures ambiantes.
Le MHDnMH ne serait pas produit naturellement dans l’environnement.
Des enquêtes menées auprès des industries en 2005 et 2006 par le truchement d’avis publiés dans la Gazette du Canada, conformément à l’article 71 de la LCPE (1999), ont permis de recueillir des renseignements (Canada, 2006). L’objectif consistait à recueillir des données sur la fabrication et l’importation de MHDnMH au Canada. Dans l’avis de 2006, on demandait également de fournir des données sur la quantité utilisée de cette substance.
En 2005, moins de quatre entreprises ont déclaré avoir fabriqué de 100 à 1 000 kg de MHDnMH au Canada ou en avoir importé de 1 001 à 100 000 kg au pays. De plus, moins de quatre entreprises ont manifesté un intérêt pour cette substance.
En 2006, moins de quatre entreprises ont déclaré avoir fabriqué de 10 000 à 100 000 kg de MHDnMH au Canada, et moins de quatre entreprises ont déclaré en avoir importé moins de 100 kg au pays. De plus, moins de quatre entreprises ont manifesté un intérêt pour cette substance.
La quantité fabriquée, importée ou commercialisée au Canada au cours de l’année civile 1986 et déclarée pour la Liste intérieure des substances (LIS) se situe entre 100 et 1 000 kg.
Selon des renseignements obtenus de l’Environmental Protection Agency (EPA) des États-Unis, entre 4 500 et 225 000 kg (déclaration originale : 10 000 à 500 000 lb) de MHDnMH ont été importés ou produits aux États-Unis en 1994; alors qu’aucune importation ou production n’a été rapportée en 1998 et 2002 (USEPA, 2005).
De 6 000 à 60 000 kg de MHDnMH ont également été utilisés de 1999 à 2008 en Suède, et de 400 à 13 000 kg de cette substance ont été utilisés de 2000 à 2008 au Danemark (SPIN, 2006).
Des renseignements relatifs aux utilisations pour les années civiles 2005 et 2006 ont été recueillis en réponse aux avis publiés en application de l’article 71 de la LCPE (1999) (Canada, 2006 et 2009).
En 2005, du MHDnMH a été importé principalement pour la fabrication de produits chimiques de base.
En 2006, le polymère a été fabriqué comme produit intermédiaire et utilisé à l’extérieur du Canada pour la fabrication de plastiques. Au cours de la même année, ce polymère a également été importé dans un mélange d’élastomère de silicone. Il est utilisé comme agent de vulcanisation pour le caoutchouc de silicone, des adhésifs ou des revêtements protecteurs à base de résines (Environnement Canada, 2010a).
Le MHDnMH est un composant de quatre types de produits cosmétiques au Canada : adhésif pour soutien-gorge (30 à 100 % en poids), crème décolorante pour la peau (0,1 à 0,3 % en poids), rouge à lèvres (< 0,1 % en poids) et maquillage pour les yeux (< 0,1 % en poids) [SDC, 2010]. Cependant, il ne figure pas sur la Liste critique des ingrédients dont l’utilisation est restreinte ou interdite dans les cosmétiques (Santé Canada, 2009). Le MHDnMH n’est pas utilisé actuellement comme principe actif ni comme produit de formulation dans les pesticides homologués au Canada (ARLA, 2007). Il n’est pas répertorié comme additif alimentaire approuvé au titre 16 du Règlement sur les aliments et drogues(Canada, 1978). Il n’est pas utilisé dans les emballages alimentaires ni comme additif indirect (courriel de la Direction des aliments de Santé Canada adressé au Bureau de gestion du risque de Santé Canada en avril 2010, source non citée). De plus, il n’est pas inscrit ni dans la base de données interne de la Direction des produits thérapeutiques sur les produits pharmaceutiques, ni dans la base de données sur les ingrédients non médicinaux, ni dans la base de données sur les ingrédients des produits de santé naturels (BDIPSN), ni dans la base de données sur les produits de santé naturels homologués (BDPSNH) en tant qu’ingrédient médicinal ou non médicinal dans les produits pharmaceutiques finaux, les produits de santé naturels ou les médicaments vétérinaires (BDPP, 2010; BDIPSN, 2010; BDPSNH, 2010; courriel de la Direction des produits thérapeutiques de Santé Canada adressé au Bureau de gestion du risque de Santé Canada en avril 2010, source non citée).
Des codes d’utilisation de la LIS ont été indiqués pour le MHDnMH, soit :
04 – Adhésif/liant/matériau d’étanchéité/bouche-pores
25 – Humidifiant/agent d’assèchement/déshumidifiant/déshydratant
89 – Impression et reliure
Aucune autre utilisation du MHDnMH n’a été répertoriée.
Environnement Canada a mis sur pied une méthode pour estimer les pertes d’une substance pendant différentes étapes de son cycle de vie, y compris son devenir après qu’elle a été incorporée à un produit ou un article fini (Environnement Canada, 2008). Cette méthode comprend une analyse du cycle de vie et un tableur (outil de débit massique) qui intègrent les renseignements sur la fabrication, l’importation et l’utilisation des données disponibles pour la substance. En commençant par une masse définie de la substance, on évalue chaque étape du cycle de vie jusqu’à ce que toute la masse ait été prise en compte. Les facteurs pertinents sont étudiés, les incertitudes sont reconnues et des hypothèses peuvent être émises pendant chaque étape, selon les renseignements disponibles. Les pertes estimées représentent le bilan massique exhaustif de la substance au cours de son cycle de vie et elles comprennent les rejets dans les eaux usées et d’autres milieux récepteurs (sol, air), la transformation chimique, le transfert vers les activités de recyclage et le transfert vers les sites d’élimination des déchets (sites d’enfouissement, incinération). Toutefois, à moins de disposer de données précises sur le taux ou le potentiel de rejet de cette substance provenant des sites d’enfouissement et des incinérateurs, la méthode ne permet pas de quantifier les rejets dans l’environnement à partir de ces sources. En fin de compte, les pertes estimées fournissent le premier volet de l’analyse de l’exposition à une substance et aident à estimer les rejets dans l’environnement et à mettre l’accent sur la caractérisation de l’exposition dans l’évaluation.
En général, les rejets d’une substance dans l’environnement peuvent découler de différentes pertes de la substance pendant sa fabrication, son utilisation industrielle ainsi que son utilisation commerciale et par les consommateurs. Ces pertes peuvent être regroupées en sept types : 1) déversements dans les eaux usées; 2) émissions atmosphériques; 3) pertes dans le sol; 4) transformation chimique; 5) élimination dans les sites d’enfouissement; 6) élimination par incinération; et 7) élimination par recyclage (c.-à-d. que le recyclage est considéré comme une perte et n’est plus pris en considération). Elles sont estimées à partir de données issues d’enquêtes réglementaires, des industries, ainsi qu’en fonction des données publiées par différents organismes. Les pertes dans les eaux usées concernent les déversements des eaux usées brutes non traitées avant tout traitement, que ce soit un traitement des eaux usées industrielles sur place ou un traitement des eaux usées hors site. De la même manière, les pertes par transformation chimique font référence aux modifications de l’identité de la substance qui ont lieu au cours des étapes de fabrication, d’utilisation industrielle ou d’utilisation commerciale et par les consommateurs, mais elles excluent celles qui ont lieu pendant les opérations de gestion des déchets telles que l’incinération et le traitement des eaux usées. Les pertes au sol incluent les rejets accidentels sur le sol ou les surfaces pavées ou non pavées pendant l’utilisation de la substance et sa durée de vie utile (p. ex., à partir de l’utilisation de machinerie agricole ou d’automobiles). Elle n’inclut toutefois pas le transfert de la substance dans le sol après l’utilisation initiale de celle-ci et sa durée de vie utile (p. ex., application au sol de biosolides et dépôts atmosphériques).
Les pertes estimées de MHDnMH au cours de son cycle de vie (fondées sur des hypothèses prudentes) sont présentées au tableau 3 (Environnement Canada, 2010b). Les pertes estimées ont été calculées en fonction des utilisations recensées en 2006.
Tableau 3. Estimation des pertes de MHDnMH pendant son cycle de vie
| Type de perte | Proportion (%) | Étapes pertinentes du cycle de vie |
|---|---|---|
| Eaux usées | 1,0 | Fabrication et utilisation à des fins industrielles |
| Émissions atmosphériques | < 0,1 | Fabrication et utilisation à des fins industrielles |
| Sol | 0,3 | Fabrication et utilisation à des fins industrielles |
| Transformation chimique | - | - |
| Sites d’enfouissement | 1,0 | Fabrication et utilisation à des fins industrielles |
| Incinération | - | - |
| Recyclage | - | - |
| Exportation | 97,7 | Fabrication et utilisation à des fins industrielles |
La majorité du polymère a été fabriquée en tant que produit intermédiaire et exportée en vrac pour la production de plastiques (Environnement Canada, 2010a).
Même s’il est possible que d’autres produits commerciaux et de consommation contenant du MHDnMH soient importés au Canada en plus de ceux déclarés au cours des enquêtes menées auprès de l’industrie, conformément à l’article 71 de la LCPE (1999), aucun renseignement ne porte sur l’ampleur de ces importations. Toutefois, la masse réelle perdue au cours de chaque étape du cycle de vie peut être supérieure aux estimations susmentionnées, si ces données étaient disponibles aux fins de la présente évaluation.
Le devenir du MHD5MH et du MHD34MH dans l’environnement peut être déduit à partir de leurs propriétés physiques et chimiques, comme nous l’avons indiqué précédemment.
MHD5MH
D’après les propriétés physiques et chimiques estimées (tableau 2), le MHD5MH se caractérise par une hydrosolubilité très faible (~2,5 × 10-6 mg/L), une pression de vapeur modérée (0,1 Pa), un faible log Koe (5,7) et une constante de la loi de Henry très élevée (2,0 × 107 Pa m3/mol. Par conséquent, sa répartition entre les différents milieux (air, sol, sédiments et eau) pourrait être importante, selon le milieu où il est rejeté et l’influence d’autres processus intervenant dans le devenir, comme l’advection et la dégradation.
Le modèle de fugacité de niveau III a servi à prédire la répartition environnementale du polymère de faible masse moléculaire, tout en tenant compte de la demi-vie dans l’air (estimée à 122,64 heures, soit 5,11 jours), dans l’eau (estimée à 4 386 heures, soit 182 jours), dans le sol (estimée à 670 heures, soit 4 semaines) et dans les sédiments (estimée à 8 760 heures, soit 365 jours). Les demi-vies utilisées pour la modélisation de la fugacité de niveau III sont estimées plus loin dans le présent rapport (voir la section « Persistance dans l’environnement »).
Tableau 4. Résultats de la modélisation de la fugacité de niveau III pour le MHD5MH (EQC, 2003)
| Substance rejetée dans : | Pourcentage de la substance répartie dans chaque milieu | |||
|---|---|---|---|---|
| Air | Eau | Sol | Sédiments | |
| l’air (100 %) | 97,6 | 0,1 | 0,2 | 2,1 |
| l’eau (100 %) | 0,1 | 3,4 | <0,1 | 96,4 |
| le sol (100 %) | 55,1 | <0,1 | 43,6 | 1,2 |
En cas de rejet dans l’air, une importante quantité de la substance devrait se répartir dans ce milieu. D’après la valeur modérée de la pression de vapeur (0,10 Pa selon le modèle) et la constante de la loi de Henry très élevée (2,0 × 107 Pa•m3/mol selon les calculs), ce polymère est semi-volatil. Par conséquent, si le MHD5MH n’était rejeté que dans l’air, il aurait tendance à demeurer dans ce milieu et à se répartir en faible quantité dans les autres milieux.
S’il est rejeté dans l’eau, il devrait fortement s’adsorber sur les matières en suspension et les sédiments, étant donné les valeurs élevées estimées du log Kco (~ 6). La volatilisation à partir de la surface de l’eau devrait être un processus négligeable de son devenir. Par conséquent, si l’eau est le milieu récepteur, le MHD5MH devrait surtout se répartir dans les sédiments et demeurer en faible quantité dans l’eau.
S’il est rejeté dans le sol, son adsorption dans ce milieu devrait être modérée (c’est-à-dire qu’il devrait être relativement immobile d’après la valeur estimée du log Kco). Puisque sa constante de la loi de Henry est très élevée, la volatilisation à partir de la surface de l’eau devrait être un processus de devenir important. En raison de sa pression de vapeur (estimée à 0,1 Pa), il pourrait cependant se volatiliser à partir des surfaces de sol. Par conséquent, s’il est rejeté dans le sol, moins de la moitié de la quantité totale de MHD5MH devrait y demeurer.
MHD34MH
En raison de la masse moléculaire élevée du MHD34MH, aucun modèle ne peut être utilisé pour prévoir le devenir de cette substance dans l’environnement. Si l’on se fonde sur les données déduites à partir du PDMS pour les propriétés physiques et chimiques, le MHD34MH demeure à l’état liquide aux températures ambiantes, n’est pas volatil et est insoluble dans l’eau.
S’il est rejeté dans l’air, une quantité négligeable devrait demeurer dans ce milieu, d’après les hypothèses selon lesquelles il possède une faible pression de vapeur et n’est pas volatil. Par conséquent, ce polymère aura tendance à se retrouver dans le sol et les sédiments.
Dans le cas d’un rejet dans l’eau, le MHD34MH en émulsion devrait s’adsorber fortement sur les matières solides en suspension et les sédiments. Dans une étude de Gettings et Lane (1982), du PDMS hydroxylé bloqué à ses extrémités (dont les propriétés chimiques et physiques sont équivalentes à celle du PDMS de 55 cSt) s’est adsorbé, à partir de la phase aqueuse, sur les particules en suspension et s’est déposé dans les sédiments sans remobilisation ultérieure sur une période de six semaines. Si on le mélangeait avec les sédiments avant l’essai, le polymère demeurait immobile pendant toute la période d’essai. Eales et Taylor (1983) ont également étudié les mouvements du PDMS (50 cSt) dans des sédiments marins. Il a été conclu que le polymère se liait fortement aux sédiments marins et que sa remobilisation dans l’eau de mer était peu probable. La volatilisation à partir de la surface de l’eau devrait être un processus négligeable quant au devenir de cette substance. Par conséquent, si l’eau est le milieu récepteur, le MHD34MH devrait surtout se répartir dans les sédiments.
S’il est rejeté dans le sol, le MHD34MH devrait se comporter comme le PDMS et fortement s’adsorber dans ce milieu (c’est-à-dire qu’il devrait être relativement immobile, d’après sa taille moléculaire importante et la valeur élevée estimée pour le log Kco). Dans une étude sur la distribution dans le sol (Battelle, 1992), on n’a observé aucun mouvement d’un 14C-PDMS (200 cSt) après son rejet dans ce milieu environnemental, et on n’a pas vu de signe de son passage en phase aqueuse ou atmosphérique. Par conséquent, s’il est rejeté dans le sol, il demeurera principalement dans ce milieu.
Persistance dans l’environnement
Aucune donnée expérimentale sur la dégradation du MHDnMH n’a été répertoriée.
MHD5MH
Les modèles RQSA ont été utilisés pour évaluer le potentiel de dégradation du polymère de faible masse moléculaire (MHD5MH). Ces prévisions sont jugées acceptables dans ce cas puisque la masse moléculaire du MHD5MH se situe dans les limites des domaines de tous les modèles.
Le tableau 5 résume les résultats des modèles RQSA en ce qui concerne la dégradation du MHD5MH dans l’eau et dans l’air.
Tableau 5. Données modélisées sur la dégradation du MHD5MH
| Processus du devenir | Modèle et base du modèle | Résultat et prévision du modèle | Demi-vie extrapolée (jours OU heures) |
|---|---|---|---|
| Air | |||
| Oxydation atmosphérique | AOPWIN, 2008[1] | t1/2 = 5,11 jours | ≥ 2 |
| Eau | |||
| Hydrolyse | HYDROWIN, 2008[1] | n.d.[2] | n.d. |
| Biodégradation primaire | |||
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 4 : enquête d’expert (résultats qualitatifs) |
3,11[3] « se biodégrade rapidement » |
< 182 |
| Biodégradation ultime | |||
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 3 : enquête d’expert (résultats qualitatifs) |
2,08[3] « ne se biodégrade pas rapidement » |
≥ 182 |
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 5 : Probabilité linéaire MITI |
-0,78[4] « ne se biodégrade pas rapidement » |
≥ 182 |
| Biodégradation (aérobie) | BIOWIN, 2008[1] Sous-modèle 6 : Probabilité non linéaire MITI |
0,00[4] « ne se biodégrade pas rapidement » |
≥ 182 |
| Biodégradation (aérobie) | CATABOL c2000-2008 % DBO (demande biochimique en oxygène) |
1,68 « se biodégrade très lentement » |
≥ 182 |
[2] Le modèle ne donne pas d’estimation pour ce type de structure.
[3] Le résultat s’exprime par une valeur numérique de 0 à 5.
[4] Le résultat s’exprime par un taux de probabilité.
Une demi-vie d’oxydation atmosphérique estimée dans l’air de 5,11 jours (voir le tableau 5) indique qu’il est peu probable que le MHD5MH s’oxyde rapidement. De plus, on ne s’attend pas à ce qu’il réagisse avec l’ozone. Par conséquent, on estime que le MHD5MH est persistant dans l’air. Selon le milieu où il est rejeté, et vu la volatilité modérée et la constante de la loi de Henry très élevée attendues pour le produit, ce dernier devrait se retrouver dans l’air dans une proportion importante, comparativement à sa distribution dans les autres compartiments environnementaux.
Dans l’eau, le MHD5MH ne devrait pas subir une hydrolyse importante. Même si le sous-modèle BIOWIN 4 du modèle de biodégradation aérobie BIOWIN (2008) permet de penser que la dégradation primaire du polymère est rapide, les quatre modèles de biodégradation ultime (sous-modèles BIOWIN 3, 5, 6 et CATABOL) indiquent que la substance ne se biodégrade pas rapidement dans l’eau. En prenant en considération ces résultats, on constate que l’ensemble des modèles indique que la demi-vie de biodégradation ultime du MHD5MH est supérieure à 182 jours.
MHD34MH
Vu sa masse moléculaire élevée (2 655,45 g/mol), on considère que la forme n = 34 du polymère se situe hors du domaine des modèles RQSA pour la prédiction de la dégradation en milieu aquatique. Aux fins de la présente évaluation, les données expérimentales pour le PDMS qui sont présentées ci-dessous sont utilisées pour évaluer le potentiel de persistance du MHD34MH dans l’environnement.
Air et eau
Le PDMS n’est pas volatil et ne devrait pas se retrouver dans l’air; on considère donc qu’il n’est pas disponible pour y être dégradé davantage (Graiver et al., 2003, ECETOC, 1994). Aucune donnée n’indique non plus que le PDMS se dégrade rapidement dans le milieu aquatique. Des études réalisées sur le traitement des eaux usées révèlent qu’il n’est pas dégradé ni décomposé rapidement pendant les procédés de traitement, mais qu’il se retrouve dans les boues solides (Graiver et al., 2003). Comme le MHD34MH possède un groupe terminal formé de groupements hydrogène et diméthyle, il réagit légèrement plus que le PDMS; toutefois, il ne devrait pas réagir de façon importante dans des conditions observées dans l’environnement. D’après ces renseignements sur le PDMS, le MHD34MH ne devrait pas se dégrader rapidement dans l’air ou dans l’eau.
Sol
En ce qui concerne la dégradation dans le sol, un certain nombre d’études rapportent que la dépolymérisation et l’hydrolyse rapide, catalysée par l’argile, du PDMS dans le sol produisent les oligomères de faible masse moléculaire.
Buch et Ingebrigtson (1979) ont rapporté une demi-vie d’environ 30 jours pour un PDMS (1 000 cSt, ce qui équivaut à une masse moléculaire d’environ 15 000 g/mol) présent à une concentration de 6 000 mg/kg dans une terre végétale sèche de l’État de l’Iowa. La réaction était inhibée même avec un taux d’humidité de seulement 1 %. Dans la même étude, ils indiquent également la perte importante d’un polymère (50 cSt) par dégradation au cours de l’essai d’une durée de 53 jours.
On recense plusieurs études sur le comportement du PDMS dans le sol (résumées dans Graiver et al., 2003). Les résultats de ces études indiquent que ce polymère se dépolymérise rapidement par hydrolyse; ce phénomène brise les liaisons siloxanes et produit du PDMS oligomérique de masse moléculaire plus faible. Ladite dégradation hydrolytique catalysée par le sol s’est avérée aléatoire, c’est-à-dire qu’elle n’est pas propre à certaines liaisons en particulier et qu’elle ne commence pas nécessairement par l’extrémité de la chaîne. De plus, l’hydrolyse catalysée par des minéraux argileux dans le sol ne se produit dans aucun autre milieu (l’air, l’eau ou les sédiments) de façon importante.
Lehmann et al. (1994a) et Carpenter et al. (1995) ont également étudié la dégradation polymérique dans des conditions pédologiques plus réalistes en analysant le produit de dégradation extrait avec du CaCl2 à 0,01 M ou du tétrahydrofurane. Les résultats ont indiqué que la dégradation du PDMS (204 cSt) a eu lieu dans le sol qui a séché progressivement et est passé de 12 à 3 % d’humidité, plus rapidement que la dégradation de la substance lorsqu’on a maintenu une humidité constante du sol (12 à 13 % d’humidité) dans des chambres d’incubation.
Dans une autre expérience, Lehmann et al. (1995) ont étudié plus en profondeur 7 sols dont les propriétés étaient très différentes. Le PDMS (350 cSt) était ajouté à un sol humide qu’on laissait sécher pendant 2 semaines. Le PDMS s’est grandement dégradé au cours de cette période en produits ayant une masse moléculaire plus faible. Bien que la dégradation ait eu lieu lorsque le sol était encore humide, les taux de dégradation étaient supérieurs dans le sol le plus altéré. Toutefois, aucune corrélation n’a pu être établie entre le taux de dégradation du PDMS et les propriétés du sol mesurées (pH, % de matière organique et % d’argile).
Le taux de dépolymérisation par dégradation hydrolytique dans le sol est rapide, mais il dépend de plusieurs facteurs tels que le taux d’humidité et la température. Lehmann et al.(1995) ont rapporté que les taux globaux de dégradation du PDMS étaient plus lents dans un sol humide que dans un sol qui séchait graduellement pendant deux semaines, ce qui indique qu’une perpétuelle humidité pourrait constituer un facteur déterminant, mais que le taux d’humidité est inversement proportionnel au taux de dégradation (Lehmann et al., 1998b). De plus, les résultats de l’étude ont démontré que les températures élevées augmentaient le taux de dégradation au cours d’un cycle météorologique annuel.
Dans une autre étude (Xu, 1998), aucun PDMS n’a été décelé après 30 jours d’incubation dans la goethite, et on a observé une dégradation plus rapide encore lorsque le polymère était incubé dans la montmorillonite. Quant aux répercussions de la teneur en eau, l’étude a indiqué un taux de dépolymérisation plus rapide à une humidité relative de 32 % qu’à une humidité relative de 100 %. Compte tenu des données de terrain pour différents types de sol obtenues dans l’étude, on s’attend à ce que la demi-vie de dépolymérisation du PDMS soit inférieure à trois semaines.
Les preuves recueillies dans le cadre d’études expérimentales sur le PDMS portent à croire que la substance devrait rapidement subir une hydrolyse catalysée par l’argile dans le sol avec une demi-vie de quelques semaines; considérant cela, on s’attend à ce que le MHD34MH s’hydrolyse rapidement dans le sol et que sa demi-vie soit de quelques semaines, ce qui est largement inférieur à 182 jours; par conséquent, on considère que ce polymère n’est pas persistant dans l’environnement.
Le diméthylsilanediol (DMSD) est le principal produit issu de l’hydrolyse du PDMS dans le sol (Stevens, 1998; Craig, 2003). À la suite de la phase de décomposition du polymère, du carbone 14 a été utilisé pour détecter la source du CO2provenant de la biodégradation du PDMS marqué au carbone 14. La biodégradation du DMSD a été illustrée par Sabourin et al. (1996). Ainsi, la biodégradation du DMSD commence par l’oxydation d’un groupe méthyle, ce qui produit du méthylsilanetriol. Par la suite, le méthylsilanetriol se dégrade en CO2 et en silice.
La volatilisation peut aussi expliquer la perte de DMSD du sol et être en concurrence avec les pertes qui résultent de la biodégradation. Après le rejet de DMSD dans l’air, les groupes méthyle réagissent avec les radicaux hydroxyles qui sont générés en présence de lumière (Atkinson, 1991). Les auteurs n’ont pas observé de réaction entre les méthylsiloxanes et l’ozone ou les radicaux NO3, mais la réaction avec les radicaux hydroxyles s’est traduite par des durées de vie de 10 à 30 jours dans l’air pour plusieurs méthylsiloxanes oligomériques. Dans une autre étude similaire (Sommerlade et al., 1993), des durées de vie de 2 à 9 jours dans l’air ont été observées pour divers méthylsiloxanes oligomériques et triméthylsilanols. De plus, plusieurs produits de réaction ont permis de constater que les groupements méthyle étaient remplacés par des groupements hydroxyle.
D’après les données expérimentales sur le PDMS et la similarité structurelle entre cet analogue et le polymère, on s’attend à ce que le MHD34MH se dégrade rapidement dans le sol et ne persiste pas dans l’environnement.
Sédiments
La dégradation du PDMS a également été observée dans les sédiments; cependant, le taux de dégradation semble beaucoup plus lent que dans le sol puisque la demi-vie est de plus d’un an (Environnement Canada, 2010a).
Une expérience (Christensen, 1994) a porté sur le potentiel de dégradation du PDMS dans les sédiments d’eau douce. Une concentration de 500 ppm de PDMS (350 cSt) radiomarqué au carbone 14 a été ajoutée à des colonnes de sédiments et d’eau. Les éléments solubles dans l’eau et le gaz dégagé ont été mesurés afin de rendre compte de la dégradation. Après 56 jours, aucun 14CO2 ou 14C hydrosoluble n’a été décelé, ce qui indique l’absence de dégradation dans les sédiments au cours de la période d’essai.
Dans d’autres études d’incubation de plus longue durée, toutefois, la dégradation du PDMS dans les sédiments était évidente (Fendinger et al., 1997). À la suite d’une période d’incubation d’une année dans des conditions aérobies, 5 à 10 % du PDMS (350 cSt) a été hydrolysé en DMSD, et environ 0,25 % du 14C a été oxydé en dioxyde de carbone (Carpenter et al., 1995). Le taux et l’ampleur de la formation de DMSD et de dioxyde de carbone à partir des sédiments correspondent à peu de chose près aux taux observés par Lehmann et al. (1994a, 1994b) dans les sédiments humides (3 % pour le DMSD et 0,13 % pour le dioxyde de carbone en 6 mois). En raison de son adsorption élevée et de son immobilité dans les sédiments, de concert avec la teneur en eau du substrat, le PDSM devrait se dégrader très lentement dans les sédiments, et la demi-vie du polymère dans ce milieu devrait être supérieure à 365 jours. Cette prévision peut être extrapolée au polymère visé par l’évaluation; ainsi, le MHD34MH ne devrait pas se dégrader rapidement dans les sédiments non plus, et sa demi-vie dans ce compartiment de l’environnement devrait être supérieure à 365 jours.
D’après les données modélisées pour le polymère de faible masse moléculaire (MHD5MH) (voir le tableau 5) et les études expérimentales sur le polymère analogue (PDMS) qui ont servi à déduire les propriétés du polymère de masse moléculaire élevée (MHD34MH), le MHDnMH devrait se dégrader rapidement dans le sol (demi-vie dans le sol ≤ 182 jours). Toutefois, la substance satisfait aux critères de persistance dans l’air (demi-vie ≥ 2 jours), l’eau (demi-vie ≥ 182 jours) et les sédiments (demi-vie ≥ 365 jours) énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000). On conclut donc qu’elle est persistante dans l’environnement.
Potentiel de bioaccumulation
Il n’existe pas de données expérimentales sur la bioaccumulation du MHDnMH.
Les données expérimentales sur le méthylsiloxane linéaire analogue ont été utilisées pour prévoir le potentiel de bioaccumulation du MHD5MH. De plus, des modèles RQSA ont servi à estimer le facteur de bioaccumulation (FBA) et le facteur de bioconcentration (FBC) pour ce composé de faible masse moléculaire.
En ce qui concerne le polymère de masse moléculaire élevée, on a utilisé les données expérimentales relatives au PDMS pour évaluer le potentiel de bioaccumulation du MHD34MH.
MHD5MH
Les données modélisées sur la bioaccumulation du MHD5MH sont résumées dans le tableau 6a ci-dessous.
Tableau 6a. Données modélisées sur la bioaccumulation du MHD5MH
| Organisme d’essai | Paramètre | Valeur (poids humide en L/kg) | Référence |
|---|---|---|---|
| Poisson | FBC | 1,04 × 104 | BCFBAF, 2008 (niveau trophique intermédiaire) |
| Poisson | FBC | 7,41 × 104 | Arnot et Gobas, 2003 (niveau trophique intermédiaire) |
| Poisson | FBC | 3,24 × 104 | BBM avec facteurs atténuants, 2008 |
| Poisson | FBA | 5,48 × 106 | BCFBAF, 2008 (niveau trophique intermédiaire) |
| Poisson | FBA | 3,39 × 106 | Arnot et Gobas, 2003 (niveau trophique intermédiaire) |
Selon les prévisions modélisées (fondées sur le log Koe modélisé de 6,60), le FBA et le FBC du MHD5MH pourraient être élevés chez les poissons. Toutefois, les résultats expérimentaux indiquent des potentiels de bioaccumulation différents des méthylsiloxanes linéaires de faible masse moléculaire.
Annelin et Frye (1989) n’ont rapporté aucune absorption des oligomères linéaires du PDMS, qui ont une masse moléculaire supérieure à 384 g/mol (le MD3M étant la forme la plus petite de PDMS), par les poissons à la suite d’une exposition de plus de 5 semaines. Les résultats expérimentaux indiquent que ni le MD3M, ni le MD4M, ni le MD7M (607 g/mol) ne se sont bioconcentrés chez la truite arc-en-ciel après 35 à 77 jours d’exposition.
Dans une autre étude sur l’absorption et la rétention de PDMS par les poissons (Bruggeman et al., 1984), des méthylsiloxanes linéaires ont été ajoutés aux aliments. L’absorption quotidienne moyenne était de 1 × 10-3 mg/g de poisson pour une période de 6 à 8 semaines. À la fin de cette période, la présence de MD3M et de MD4M a été mesurée sous les seuils de détection (approximativement 3 × 10-4 mg/g) dans tous les échantillons de poissons, alors que la concentration de MD5M et des autres méthylsiloxanes linéaires ne dépassaient pas 2 × 10-3 mg/g. En comparaison de l’absorption quotidienne moyenne (1 × 10-3 mg/g), ces résultats indiquent que l’absorption, la rétention et l’accumulation de MD3-6M par l’entremise des aliments ne sont pas importantes. Pour cette raison, on peut donc s’attendre à ce que le MHD5MH, qui a une structure linéaire semblable au MD3M et au MD4M, ainsi qu’une masse moléculaire plus élevée, ait un potentiel de bioaccumulation comparable et ne se bioaccumule pas.
Selon des études menées par Dimitrov et al. (2002) et Dimitrov et al. (2005), ainsi que le Baseline Bioaccumulation Model (BBM, 2008), la probabilité qu’une molécule traverse des membranes cellulaires à la suite d’une diffusion passive diminue de façon importante lorsque le diamètre transversal maximal (Dmax) augmente. Ainsi, la probabilité qu’une diffusion passive se produise diminue de façon notable lorsque le diamètre transversal est supérieur à environ 1,5 nm et de façon encore plus importante dans le cas des molécules ayant un diamètre transversal supérieur à 1,7 nm. Sakuratani et al. (2008) ont également étudié l’effet du diamètre transversal sur la diffusion passive à l’aide d’un ensemble d’essais comptant environ 1 200 substances chimiques nouvelles et existantes. Ils ont aussi observé que les substances dont le potentiel de bioconcentration n’était pas très élevé avaient souvent un Dmax supérieur à 2,0 nm ainsi qu’un diamètre effectif (Deff) supérieur à 1,1 nm.
Selon l’estimation des propriétés physiques et chimiques du MHD5MH, cette substance a un diamètre transversal se situant entre 1,46 et 2,18 nm. D’après l’observation citée précédemment (Sakuratani et al., 2008), la forme n = 5 du polymère a un taux d’absorption limité à partir de l’eau et une biodisponibilité in vivo réduite.
D’après les données expérimentales sur les méthylsiloxanes linéaires analogues, et en tenant compte de la taille des molécules, le MHD5MH ne devrait pas se bioaccumuler chez les organismes aquatiques.
MHD34MH
Le MHD34MH a une taille moléculaire beaucoup plus importante que la forme de faible masse moléculaire (n = 5) du MHDnMH. Cette caractéristique devrait limiter sa répartition, à savoir son passage à travers les membranes biologiques, et limiter sa biodisponibilité ainsi que son potentiel de bioaccumulation dans les organismes aquatiques. Des données tirées d’études sur le PDMS sont utilisées pour caractériser le potentiel de bioaccumulation du MHDnMH (voir les données compilées dans le tableau 6b ci-dessous).
Tableau 6b. Données empiriques sur la bioaccumulation et la bioconcentration du PDMS
| Nature du polymère (masse moléculaire, viscosité ou émulsion) |
Organisme d’essai | Concentration expérimentale (mg/L) et/ou source d’exposition | Paramètre (FBA/FBC, L/kg) (FBAm[1], sans dimension) |
Référence |
|---|---|---|---|---|
| Émulsion à 15 %, 300 cSt | Crapet arlequin (Lepomis macrochirus) |
1,5 | FBC = 0,16 à 0,5 (après 2 semaines) |
Hobbs et al., 1975 |
| MD15-17M | Guppy (Poecilia reticulate) |
Saturation | FBC < 10 | Opperhuizen et al., 1987 |
| Approximativement 32 mg/kg de nourriture sèche | FBA < 0,01 | |||
| PDMS commercial Mm (g/mol): 1 200 6 000 25 000 56 000 |
Carp sp. | Concentrations mesurées dans les solutions à saturation 1,330 0,486 0,135 0,060 |
FBC = 2,9 FBC = 7,1 FBC = 386 FBC = 1 250 |
Watanabe et al., 1984a |
| Émulsion à 35 %, 50 cSt | Niveau 1 : phytoplancton (Tetraselmis sp.) Niveau 2 : mollusque (Mytilus edulis) |
70 Exposition directe par l’eau Exposition par l’eau et la nourriture |
FBC = 2,08 FBAm = 0,12 |
Aubert et al., 1985 Guillemaut et al., 1987 |
| Niveau 1 : plancton (Tatreselmis sp. Artemia salina) Niveau 2 : poisson (Carassius auratus) |
70 Exposition directe par l’eau Exposition par l’eau et la nourriture |
FBC = 1,9 FBAm = 0,05 |
||
| Niveau 1 : annélide (Nereis diversicolor) Niveau 2 : poisson (Scorpaena porcus) |
70 Exposition directe par l’eau Exposition par l’eau et la nourriture |
FBC = 0,036 FBAm = 1,4 |
||
| Niveau 1 : annélide (Nereis diversicolor) Niveau 2 : crabe (Carcinus maenas) |
70 Exposition directe par l’eau Exposition par l’eau et la nourriture |
FBC = 0,036 FBAm = 1,09 |
||
| 50 cSt | Poisson-chat (Ictalurus melas) |
Exposition par la nourriture | < seuil de détection | Annelin, 1979 |
Généralement, le PDMS de masses moléculaires variées (Mm = 1 200 g/mol et plus) se montre faiblement bioaccumulable et bioconcentrable chez les organismes aquatiques et les espèces terrestres.
Opperhuizen et al. (1987) ont quant à eux effectué une étude sur la bioaccumulation, chez Poecilla reticulate (guppy), du PDMS (5 cSt, MD15-17M). Au bout de 12 semaines d’exposition, on ne détectait pas de polymères de siloxane dans les poissons entiers.
Dans une autre étude, on a soumis des crapets arlequins (Lepomis macrochirus) à une exposition à un PDMS ayant une masse moléculaire supérieure ou égale à 5 000 g/mol pendant une période de 30 jours (Hobbs et al., 1975). On n’a trouvé aucun lien entre les taux du polymère dans les tissus et la durée ou le degréß d’exposition. On a découvert cependant que le polymère était adsorbé sur des surfaces du poisson, mais qu’il n’était pas absorbé par les cellules.
En outre, des études ont été réalisées concernant l’absorption de PDMS par d’autres espèces dans d’autres milieux naturels. Au cours d’une étude de 28 jours dirigée par Garvey et al. (1996), on a exposé des vers de terre (Eisenia foetida) à 100 et 1 000 mg/kg de PDMS dans une matrice de sol artificiel. Au terme de la phase d’exposition, les vers de terre de chaque réplicat ont été transférés dans un milieu d’exposition qui ne contenait pas de PDMS pour y subir une phase de dépuration de 14 jours. On a prélevé des échantillons au cours de la phase d’exposition de 28 jours; toutefois, on n’a pas relevé de différence statistique dans les concentrations de résidus tissulaires pour les deux groupes. En outre, le PDMS ingéré par les vers de terre et présent dans l’intestin a été rapidement dépuré pendant la période de 14 jours qui a suivi.
Kukkonen et Landrum (1995) n’ont observé aucune bioaccumulation dans des vers aquatiques vivant dans les sédiments.
Les résultats d’études relatives à d’autres organismes benthiques et terrestres (Putt, 1994; Putt et Mihaich, 1996) ont aussi indiqué un potentiel de bioaccumulation très limité pour le PDMS.
Une étude sur la carpe argentée a fait état de résultats contradictoires, selon lesquels les matériaux de PDMS ayant une masse moléculaire plus élevée subissaient une bioaccumulation supérieure à celle des composés ayant une masse moléculaire inférieure (Watanabe et al., 1984). Le fait que le rapport entre la bioaccumulation et la masse moléculaire soit l’inverse des résultats escomptés pourrait être le résultat de la contamination de la surface, et aucune indication n’était donnée pour préciser si on avait analysé les poissons entiers ou les filets. Par conséquent, ces résultats sont d’une qualité incertaine.
On a étudié la bioamplification ou les transferts par la chaîne alimentaire d’une émulsion de PDMS (50 cSt) en milieu marin (Aubert et al., 1985; Guillemaut et al., 1987). Les organismes du premier niveau trophique étaient exposés au PDMS en émulsion (50 cSt) à une concentration de 70 mg/L dans l’eau. Soit le PDMS ne subissait pas de bioconcentration dans l’eau, soit le FBC était inférieur à 2 au premier niveau trophique. La bioaccumulation entre les deux niveaux trophiques était faible, elle était comprise entre 0,05 et 1,4, ce qui indique que la bioamplification du PDMS entre deux niveaux trophiques n’est pas significative dans la chaîne alimentaire aquatique soumise à l’essai.
Selon les renseignements ci-dessus sur le PDMS, le MHD34MH ne devrait pas être biodisponible dans les organismes aquatiques ou organismes de fond. Par ailleurs, ce polymère ne se bioaccumule pas dans ces organismes.
Compte tenu de l’évaluation du potentiel de bioaccumulation des polymères ayant une masse moléculaire faible ou moyenne en nombre, il est conclu que le MHDnMH ne satisfait pas aux critères de bioaccumulation (FBA ou FBC ≥ 5 000) énoncés dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
Évaluation des effets écologiques
A – Dans le milieu aquatique
Aucune donnée expérimentale sur la toxicité du MHDnMH n’a été relevée.
MHD5MH
Des modèles RQSA ont été utilisés pour estimer la toxicité aquatique du MHD5MH. Les données modélisées sont résumées dans le tableau 7 ci-dessous.
Tableau 7a. Données modélisées sur la toxicité du MHD5MH pour les organismes aquatiques
| Organisme d’essai | Type d’essai | Paramètre | Valeur (mg/L) |
Modèle |
|---|---|---|---|---|
| Poisson | Toxicité aiguë (96 heures) | CL50[1] | 0,035[*] | ECOSAR, 2008 |
| Toxicité aiguë (14 jours) | 0,038[*], [!] | |||
| Poisson (eau de mer) | Toxicité aiguë (96 heures) | CL50 | 0,035[*] | |
| Daphnie | Toxicité aiguë (48 heures) | CL50 | 0,039[*] | |
| Algues vertes | Toxicité aiguë (96 heures) | CE50[2] | 0,137[*] | |
| Mysis effilée | Toxicité aiguë (96 heures) | CL50 | 0,001[*] | |
| Poisson | Toxicité chronique (30 jours) | Vtc[3] | 0,005[*] | |
| Daphnie | Toxicité chronique | Vtc | 0,009[*] | |
| Algues vertes | Toxicité chronique | Vtc | 0,112[*] | |
| Mysis effilée | Toxicité chronique | Vtc | 0,00003[*] | |
| Poisson (eau de mer) | Toxicité chronique | Vtc | 0,072[*] | |
| Ver de terre | Toxicité chronique (14 jours) | CL50 | 293,13[*] | |
| Tête-de-boule | Toxicité aiguë (96 heures) | CL50 | 146[*] | AIEPS, 2003-2007 |
| Daphnia magna | Toxicité aiguë (48 heures) | CL50 | 13,19[*] | |
| Pseudokirchneriella subcapitata | Toxicité aiguë (72 heures) | CE50 | 14,09[*] | |
| Daphnia magna | Toxicité aiguë (48 heures) | CE50 | 0,18[*] | OASIS Forecast, 2005 |
| Pimephales promelas | Toxicité aiguë (96 heures) | CE50 | 0,43[*] |
[2] CE50- Concentration d’une substance qu’on estime susceptible de causer un effet chez 50 % des organismes d’essai.
[3] Vtc – Valeur de toxicité chronique.
[*] La concentration d’exposition est au moins dix fois supérieure à l’hydrosolubilité estimée, ce qui indique qu’aucun effet n’est prévu à saturation pour la substance à l’étude.
[!] Valeur critique de toxicité (VCT). Elle est utilisée pour dériver la concentration estimée sans effet (CESE).
Les estimations produites par les modèles en ce qui concerne la toxicité du MHD5MH en milieu aquatique sont résumées au tableau 7a. On note que les valeurs modélisées pour tous les paramètres sont beaucoup élevées que l’hydrosolubilité modélisée du MHD5MH (2,7 × 10-6 mg/L). Ces résultats permettent donc de penser qu’au niveau maximal de solubilité, le MHD5MH n’a pas d’effet observable sur les organismes aquatiques dans le cas d’une exposition à court terme. Néanmoins, pour les besoins d’une évaluation prudente de la toxicité du MHD5MH, une CL50modélisée de 0,038 mg/L sur une période de 14 jours a été utilisée comme valeur critique de toxicité (VCT) pour les poissons afin de caractériser les risques présentés par le MHD5MH pour les organismes aquatiques.
MHD34MH
Aucun modèle RQSA ne peut être utilisé pour modéliser l’écotoxicité du polymère de masse moléculaire élevée. L’information sur le PDMS a donc servi à évaluer la toxicité du MHD34MH.
Il existe plusieurs études de toxicité faisant état des effets du PDMS sur les organismes aquatiques. Les résultats de ces études sont résumés dans le tableau 7b. Comme on l’indiquait précédemment dans le présent rapport (voir la section sur le potentiel de bioaccumulation), le PDMS n’est pas absorbé par les organismes aquatiques (Annelin et Frye, 1989; Bruggeman et al., 1984); par conséquent, on ne prévoit pas d’effets de sa part. Comme le PDMS est extrêmement hydrophobe et tend à s’adsorber fortement sur les particules solides, on a employé ce polymère en émulsion dans de nombreuses études pour maintenir des concentrations d’exposition nominales constantes, bien supérieures à ce que permet la solubilité du PDMS dans l’eau.
En général, le PDMS s’est avéré peu toxique pour les poissons (voir le tableau 7b). Hill et al. (1984) ont rapporté une concentration sans effet observé (CSEO) de 91 mg/L de PDMS (émulsion de 50 cSt) chez le méné tête-de-mouton. Lors d’une autre étude, Hill a fait état d’une CL50 de 350 mg/L de PDMS (émulsion de 50 cSt) chez la plie (Hill et al., 1980). Il a été démontré que les effets toxiques des émulsions de PDMS en forte concentration étaient attribuables à l’émulsifiant utilisé (Hobbs et al., 1975; Aubertet al., 1985).
Le PDMS a également montré une faible toxicité pour les invertébrés aquatiques (voir le tableau 7b). Une étude réalisée sur les moules Mytilus sp. (Hill et al., 1984) a permis d’établir une CL50 de 1 980 mg/L de PDMS (émulsion de 50 cSt) après 96 heures. Cependant, les effets secondaires sont quelque peu difficiles à interpréter. Les formes liquides du PDMS sont insolubles dans l’eau et ont une masse volumique inférieure à 1 000 kg/m3. Par conséquent, le polymère forme une pellicule de surface dans laquelle les crustacés aquatiques ont tendance à se retrouver pris au piège. Ce piégeage peut se produire et donc interférer avec l’évaluation de la toxicité chimique du polymère.
On a aussi étudié la toxicité pour les microorganismes aquatiques et il s’est avéré que le PDMS n’était pas très dangereux pour lesdits organismes (voir le tableau 7b).
Comme les concentrations d’exposition au PDMS sont largement supérieures à la solubilité maximale attendue pour le polymère dans les études disponibles sur la toxicité en milieu aquatique, le polymère présente probablement un risque faible pour les organismes aquatiques dans les conditions ambiantes.
La valeur critique de toxicité (VCT) est tirée d’une étude de Hill et al. (1977) sur le PDMS (50 cSt, en émulsion à 35 %) puisque ce polymère a la masse moléculaire la plus proche de celle du MHD34MH de masse moléculaire moyenne en nombre. Pour les besoins de la caractérisation des risques que présente le MHD34MH pour les organismes aquatiques, une CSEO de 91 mg/L indiquée dans cette étude a été utilisée comme VCT pour dériver la concentration estimée sans effet (CESE).
Tableau 7b. Données de toxicité du PDMS sur les organismes aquatiques
| Nature du polymère (viscosité et/ou émulsion) |
Organisme d’essai | Type d’essai | Paramètre | Valeur (mg/L) | Référence | |
|---|---|---|---|---|---|---|
| Poissons | ||||||
| Non précisé | Poisson | Toxicité aiguë | CL50[1] | > 1 000 | Annelin et Humble, 1978; Hobbs et al., 1975 | |
| Non précisé | Méné (Phoxinus phoxinus) |
Toxicité semi-chronique | TL40[2] | 3 000 (8 jours) | Cabridenc, 1978 | |
| 100, 350, 12 500 cSt | Pomatoschistus minutus Gasterosteus aculeatus |
Toxicité aiguë (96 heures) | CL0[3] | À saturation | Maggi et Alzieu, 1977 | |
| Émulsion à 20 %, 50 cSt | Plie (Pleuronetes platessa) |
Toxicité aiguë (96 heures) | CE[4] | 88 | Firmin, 1984 | |
| Émulsion à 35 %, 50 cSt | Scorpène Scorpaena poreus Carassius auratus |
Toxicité aiguë | TL50[5] | 1 000 (12 heures) 2 000 (50 heures) 10 000 (4 heures) 700 (50 heures) 3 500 (24 jours) |
Aubert et al., 1985 | |
| 50 cSt | Plie (Pleuronetes platessa) |
Toxicité aiguë (96 heures) | CL50 | 350 > 10 000 à la surface de l’eau (5 mg/L dans l’eau) |
Hill et al., 1984 Hill, 1980 | |
| Émulsion à 35 %, 50 cSt | Méné tête-de-mouton (Cyprinodon variegatus) |
Toxicité chronique (33 jours) | CSEO[6]CE | 91 235 (effets mineurs observés) |
Hill et al., 1984 | |
| 350 cSt | Truite arc-en-ciel (Oncorhynchus mykiss) Salmo gairdneri) |
Nourriture modifiée sous-chronique (28 jours) | DSEO[7] | 10 000 mg/kg p.c. par jour | Mann et al., 1977 | |
| Émulsion à 30 %, 350 cSt | Crapet arlequin (Lepomis macrochiras) Truite arc-en-ciel (Salmo gairdneri) |
Toxicité aiguë (96 heures) | CL50 Hypoactivité |
> 10 000 À 1 000 et 10 000 | Hobbs et al., 1975 | |
| Invertébrés aquatiques et mollusques | ||||||
| Émulsion à 66 %, 10 à 60 000 cSt | Daphnie | Toxicité aiguë | CSEO | > 200 | Annelin et al., 1994 | |
| Émulsion, 350 cSt | Daphnia magna | Toxicité aiguë (48 heures) | CL50 | 1 000 | Spacie, 1972 | |
| 100, 350 et 12 500 | Huître plate (Ostrea edulis) Moule bleue (Mytilus edulis) Bigorneau (Littorina littorea) |
Toxicité aiguë (96 heures) |
CL0 | Saturation dans l’eau de mer | Maggi et Alzieu, 1977 | |
| Émulsion à 35 %, 50 cSt | Moule (Mytilus edulis) Crabe (Artemia salma Carcinus maenas) |
Toxicité aiguë Semi-chronique (10 jours) Semi-chronique |
TL50 TL50 CL0 CL50 Mortalité |
3 500 (96 heures) 10 000 (80 heures) (émulsifiant seulement) 700 7 000 (9 jours) 3 500 (10 jours) |
Aubert et al., 1985 | |
| Émulsion à 20 %, 50 cSt | Mytilus sp. | Toxicité aiguë (96 heures) | CL50 | 1 980 | Hill et al., 1984 | |
| 50 cSt | Mytilus sp. | Toxicité aiguë (96 heures) | CL50 | 1 020 | Hill et al., 1984 | |
| 100 cSt Émulsion à 30 %, 100 cSt Émulsion à 30 %, 350 cSt |
Daphnia magna Daphnia magna Coques (Prothaca spaminea) Choquemort (Fundulus heteroclitus) Crabe des rivages (Pachygrapsus crassipes) Crevette brune (Penaeus oxtecus) |
Toxicité aiguë (48 heures) Toxicité aiguë (48 heures) Toxicité aiguë (96 heures) |
CL50 CL50 CL50 |
44,5 (le polymère a formé une couche à la surface) 73,4 > 1 000 |
Hobbs et al., 1975 | |
| Microorganismes aquatiques (bactéries, champignons et phytoplancton) | ||||||
| Groupe terminal hydroxyle, 55 cSt | Bactéries, algues et protozoaires aérobies et anaérobies | Toxicité chronique (24 semaines) |
CSEO | > 0,26 | Gettings et Lane, 1982 | |
| 100, 350 et 12 500 cSt | Algues marines (diatomées et flagellés) | Toxicité semi-chronique (9 jours) | CSEO | Saturation dans l’eau de mer | Maggi et Alzieu, 1977 | |
| Émulsion à 35 %, 50 cSt | Phytoplancton marin (Tetraselmis sp.) | Non précisé | CMEO[8] | 350 | Maggi et Alzieu, 1977 | |
[2] TL40 – Temps requis en heures pour que 40 % des organismes d'essai meurent à concentration donnée.
[3] CL0 – Concentration d’une substance que l’on estime sans effet létal sur les organismes d’essai.
[4] CE – Concentration d’une substance que l’on estime avoir un effet toxique sur les organismes d’essai; cependant, le pourcentage d’organismes d’essai touchés ne peut être établi dans l’étude.
[5] TL50 – Temps requis en heures pour que 50 % des organismes d'essai meurent à concentration donnée.
[6] CSEO – Concentration sans effet observé, soit la concentration d’exposition la plus élevée ne causant pas d’effet statistiquement significatif par rapport aux témoins dans un essai de toxicité.
[7] DSEO – Dose sans effet observé, soit la dose d’exposition la plus élevée ne causant pas d’effet statistiquement significatif par rapport aux témoins dans un essai de toxicité.
[8] CMEO – Concentration minimale avec effet observé, soit la concentration la plus faible d’une substance causant des effets statistiquement significatifs par rapport au groupe témoin dans un essai de toxicité.
[!] VCT – Valeur critique de toxicité. On l’utilise pour dériver la concentration estimée sans effet (CESE).
Selon les prévisions des modèles, le MHD5MH ne devrait pas avoir d’effets observables sur les organismes aquatiques à une concentration correspondant à sa solubilité maximale. Le MHD34MH, dont la structure est semblable au PDMS, ne devrait pas non plus avoir d’effets importants sur les organismes aquatiques aux concentrations correspondant à sa plage de solubilité dans l’eau. Par conséquent, il est conclu que la toxicité du MHDnMH est faible pour les organismes aquatiques.
B – Dans d’autres milieux environnementaux
La principale voie d’exposition dans un milieu aquatique serait par contact avec le polymère absorbé par les sédiments, en raison de la faible hydrosolubilité de ce dernier. Par conséquent, les possibles effets toxiques du polymère sur les organismes vivant dans les sédiments sont également pris en considération dans cette évaluation préalable. De plus, comme les biosolides issus des boues traitées provenant des réseaux d’assainissement peuvent être utilisées pour augmenter les terrains agricoles et régénérer les sols, on tient compte de cette voie d’exposition des organismes terrestres au polymère.
Comme il n’existe pas de données expérimentales sur la toxicité du MHDnMH dans les sédiments ou le sol, l’information relative au PDMS est utilisée pour évaluer la toxicité du MHDnMH (voir le tableau 7c ci-dessous). En résumé, le PDMS montre une faible toxicité pour les organismes vivant dans les sédiments et les sols.
Tableau 7c. Données relatives à la toxicité du PDMS pour les organismes vivant dans les sédiments ou les sols
| Nature du polymère (viscosité et/ou émulsion) |
Organisme d’essai | Milieu et type d’essai | Paramètre | Concentration (mg/kg, sauf indication contraire) | Référence |
|---|---|---|---|---|---|
| Organismes vivant dans les sédiments | |||||
| 350 cSt | Amphipode marin (Ampelisca abdita) | Sédiments Toxicité semi-chronique (10 jours) |
CL0[1] | > 2 300 | Putt et Mihaich, 1996 |
| 350 cSt | Amphipode d’eau douce (Hyalella azteca) | Sédiments Toxicité chronique (28 jours) |
CE0[2] | > 2 200 | Putt et Mihaich, 1996 |
| PDMS (caractéris-tiques de viscosité/ émulsion non indiquées) | Ver polychète (Nereis diversicolor) | Sédiments Toxicité chronique (28 jours) |
CE0 | 1 000 | Craig et al., 1984 |
| 50 cSt | Annélides | Sédiments Toxicité aiguë (96 heures) Toxicité chronique (28 jours) |
CE0 | > 10 000 | Craig et Caunter, 1990 |
| Émulsion à 35 %, 50 cSt (eau de mer) | Ver polychète (Nereis diversicolor) | Sédiments Toxicité semi-chronique (9 jours) |
CL0 CE0 |
> 350 > 700 |
Aubert et al., 1985 |
| 350 cSt | Invertébrés benthiques (H. azteca et C. tentans) |
Sédiments Toxicité semi-chronique (10 jours) Cycle de vie (28 jours pour le H. azteca et 50 à 65 jours pour le C. tentans) |
CL0 CE0 |
> 1 000 | Henry et al., 2001 |
| Organismes vivant dans le sol | |||||
| Liquide, 350 cSt | Lombric (Eisenia fœtida) | Sol Toxicité chronique (21 jours) |
CE0 | 1 100 | Garvey et al., 1996 |
| Liquide, 350 cSt | Collembole (Folsomia candida) | Sol Toxicité chronique (21 jours) |
CSEO[3] | 250 | Garvey et al., 1996 |
| Végétaux | |||||
| Émulsion à 10 %, 10 cSt | Plantation de conifères | Sol Toxicité aiguë (tout de suite après le traitement) Toxicité chronique (1 an) |
DSEO[4] | 30 mL/m3 | Belt et al., 1977 |
| Oiseaux | |||||
| 100 cSt | Canard colvert (Anas platorhynchus) Colin de Virginie (Colinus virgianus) |
Toxicité semi-chronique (5 jours) | CL0 | > 5 000 | Hobbs et al., 1975 |
| 100 cSt | Poule Leghorn blanche | Toxicité chronique | CE0 | > 5 000 | Hobbs et al., 1975 |
[2] CE0- Concentration d’une substance dont on estime qu’elle n’a aucun effet secondaire sur les organismes d’essai.
[3] CSEO – Concentration sans effet observé, soit la concentration la plus élevée ne causant pas d’effet statistiquement significatif par rapport au groupe témoin dans un essai de toxicité.
[4] DSEO – Dose sans effet observé, soit la dose d’exposition la plus élevée ne causant pas d’effet statistiquement significatif par rapport aux témoins dans un essai de toxicité.
Les effets du PDMS (5 à 1 000 cSt) ont également été évalués chez des adultes de l’espèce Acheta domesticus (grillon domestique) exposés au polymère par application directe du produit (5 × 10-3 mg) sur la face ventrale du thorax des sujets (Levier et al., 1988). Le délai de perte du réflexe de redressement (la capacité des grillons à se remettre sur leurs pattes lorsqu’on les place sur le dos) s’est accru avec la viscosité du PDMS, et la mortalité au bout de 48 heures diminuait d’un facteur 2 lorsque la viscosité du PDMS augmentait d’un facteur 200. Un effet similaire du PDMS (10 cSt) a été observé dans une autre étude (Nielson et al., 1975).
D’après les résultats de l’étude sur le PDMS, le MHDnMH ne devrait pas présenter un potentiel de toxicité important pour les organismes vivant dans les sédiments ou les sols.
Évaluation de l’exposition de l’environnement
A – Rejets industriels
On n’a relevé aucune donnée sur les concentrations de MHDnMH dans l’environnement au Canada. Les concentrations dans l’environnement sont donc estimées en fonction de l’analyse de l’exposition pour le polymère, en tenant compte des quantités de MHD34MH fabriquées au Canada ainsi que du MHD5MH présent dans le polymère.
L’outil de débit massique a utilisé des hypothèses réalistes correspondant au scénario le plus défavorable pour les rejets de MHDnMH dans l’eau (par les effluents d’eaux usées) associés aux utilisations industrielles (tableau 3). Pour examiner la question des rejets issus des activités industrielles, un scénario propre au site a servi à estimer une concentration prudente de la substance dans un cours d’eau recevant des effluents industriels (Environnement Canada, 2010c). Le scénario vise à fournir des estimations fondées sur la quantité de la substance traitée et rejetée, le nombre de jours de traitement, le taux d’élimination de l’usine de traitement des eaux usées (UTEE) et la taille du cours d’eau récepteur.
Le scénario propre au site des rejets industriels tient compte des données sur la charge obtenues de sources telles que des enquêtes industrielles, ainsi que des connaissances sur la distribution des rejets industriels au pays, et calcule la concentration estimée dans l’environnement (CEE).
Une exposition aquatique au polymère de siloxane devrait avoir lieu si la substance est rejetée dans le cadre des utilisations industrielles vers une UTEE qui évacue subséquemment son effluent dans des eaux réceptrices. La concentration de la substance dans les eaux réceptrices près du point de rejet de l’usine de traitement des eaux usées est utilisée comme CEE pour l’évaluation du risque que pose la substance en milieu aquatique. On peut la calculer à l’aide de l’équation suivante :
Ceau-ind = [1000 × Q × L × (1 - R)] / [N × F × D]
où
Ceau-ind : concentration en milieu aquatique due aux rejets industriels, en mg/L
Q : quantité de substance totale utilisée chaque année sur un site industriel, en kg/an
L : pertes dans les eaux usées, fraction
R : taux d’élimination de l’usine de traitement des eaux usées, fraction
N : nombre de jours de rejets annuels, en jour/an
F : débit de l’effluent de l’usine de traitement des eaux usées, en m3/jour
D : facteur de dilution dans l’eau réceptrice, sans dimension
Le scénario propre au site est prudent, c’est-à-dire qu’il suppose que la quantité totale de la substance employée dans l’industrie canadienne n’est utilisée que par une seule installation industrielle sur un petit site hypothétique. Il suppose également que les pertes vers une UTEE locale sont élevées, soit 1 % de la quantité totale utilisée par suite du nettoyage de contenants de produits chimiques et d’équipement de traitement. Le débit des effluents de l’UTEE sélectionnée est estimé se situer au 10e centile (3,3 × 104 m3/j) de ses taux de rejet. Le scénario présume également que les rejets se produisent 250 jours par année, comme c’est habituellement le cas pour les petites et moyennes installations.
L’élimination du polymère dans les eaux usées dépend de sa solubilité et de sa capacité d’adsorption sur les boues. En outre, la masse moléculaire a une incidence puisque les polymères de masse moléculaire élevée sont éliminés dans une proportion élevée des effluents (c’est-à-dire avant l’étape des biosolides) comparativement aux polymères de faible masse moléculaire (USEPA, 2008). Sur la base de ces considérations, le taux d’élimination par l’UTEE est estimé à 75 % pour le MHD5MH, et à 95 % pour le MHD34MH. Le facteur de dilution dans les eaux réceptrices est de 3,8 pour ce scénario.
Pour la forme n = 5, on utilise la tranche supérieure pertinente des quantités déclarées (100 à 1 000 kg/an) pour calculer la concentration dans l’environnement.
Pour la forme n = 34, on a utilisé la tranche supérieure de la gamme de quantités déclarées en 2006, soit 10 000 à 100 000 kg/an.
D’après ces hypothèses, la CEE est de 8 × 10-5mg/L pour le MHD5MH, et de 1,6 × 10-3 mg/L pour le MHD34MH (Environnement Canada, 2010c).
Il est à noter que la voie prédominante de rejet du MHDnMH dans l’environnement est l’amendement du sol avec des biosolides. D’après la masse moléculaire élevée de la substance et sa très faible solubilité dans l’eau, et d’après les données toxicologiques concernant l’analogue (PDMS), on peut présumer que les boues enfouies ou incinérées qui contiennent du MHDnMH ne seront pas dispersées dans l’environnement. Dans le sol, la substance devrait être immobile et subir une dégradation rapide; elle n’occasionnera donc pas une exposition significative pour les organismes aquatiques ou terrestres.
B – Rejets commerciaux et par les consommateurs
Lorsqu’il est utilisé comme agent de vulcanisation pour le caoutchouc de silicone, des adhésifs ou des revêtements protecteurs à base de résines, le MHDnMH est presque entièrement incorporé dans les polymères par réticulation. La plus grande partie de la matrice adhésive devrait être envoyée dans les sites d’enfouissement avec les objets sur lesquels elle est appliquée. La quantité totale rejetée dans l’environnement (eau et sol) en raison de l’utilisation par les consommateurs devrait être très faible. Par conséquent, l’exposition de la faune à cette substance devrait être négligeable.
Caractérisation du risque écologique
La démarche suivie dans la présente évaluation préalable consistait à examiner les divers renseignements à l’appui et à tirer des conclusions suivant la méthode du poids de la preuve et le principe de prudence requis par la LCPE (1999). Les éléments de preuve pris en compte comprennent les résultats d’un calcul prudent du quotient de risque ainsi que des renseignements sur la persistance, la bioaccumulation, la toxicité, les sources et le devenir de la substance dans l’environnement.
Le MHDnMH devrait être persistant dans l’air, l’eau et les sédiments. Le polymère devrait également présenter un faible potentiel de bioaccumulation. Les volumes modérés de MHDnMH qui sont fabriqués ou utilisés au Canada, combinés aux utilisations de cette substance, indiquent un faible potentiel de rejet dans l’environnement au Canada. Lorsqu’il est rejeté dans l’eau, il pourrait demeurer à la surface comme le PDMS, mais finira par se répartir dans les sédiments. En ce qui concerne les effets du polymère dans l’eau, son potentiel de toxicité devrait être faible pour les organismes aquatiques.
Les concentrations estimées sans effet (CESE) ont été calculées séparément pour les polymères ayant une masse moléculaire faible ou moyenne en nombre.
Dans le cas du MHD5MH, une CL50modélisée de 0,038 mg/L sur une période de 14 jours a été utilisée comme VCT pour les poissons afin de caractériser le risque pour les organismes aquatiques. Il est à noter que cette valeur modélisée est plus faible que celles indiquées dans les études de laboratoire. En appliquant un facteur d’évaluation de 100 à cette VCT afin de tenir compte de la variabilité interspécifique et intraspécifique sur le plan de la sensibilité, de l’extrapolation de la toxicité chronique sur le terrain à partir de la toxicité aiguë en laboratoire ainsi que de l’incertitude associée aux prévisions modélisées, on a obtenu une CESE de 3,8 × 10-4 mg/L pour le MHD5MH.
La CESE pour le MHD34MH a été calculée en divisant la valeur de toxicité chronique sans effet de 91 mg/L (en tant que valeur expérimentale valable la plus sensible pour un PDMS, dont la masse moléculaire est la plus proche de celle du MHD34MH) par un facteur d’évaluation de 100 pour tenir compte de la variabilité interspécifique et intraspécifique sur le plan de la sensibilité et de l’incertitude associée à l’utilisation de données tirées d’un polymère analogue, ce qui donne un résultat de 0,91 mg/L.
Une analyse du quotient de risque a été effectuée pour le MHD5MH et le MHD34MH. Cette analyse fondée sur des estimations prudentes de l’exposition et sur les renseignements toxicologiques portait sur le milieu aquatique et visait à déterminer s’il existe un potentiel d’effets écologiques nocifs au Canada.
Le scénario industriel propre au site, qui est présenté ci-dessus, tient compte des plans d’eaux récepteurs réels. Il s’est traduit par une concentration estimée dans l’environnement (CEE) de 8 × 10-4 mg/L pour le MHD5MH et de 1,6 × 10-3 mg/L pour le MHD34MH (Environnement Canada, 2010c). Les quotients de risque (QR=CEE/CESE) sont d’environ 0,21 pour le MHD5MH et de 2 × 10-3 pour le MHD34MH. Par conséquent, les effets nocifs sur les organismes aquatiques sont peu probables.
Cette information porte à croire que le MHDnMH (n ≥ 5) ne devrait pas avoir d’effets nocifs sur les organismes aquatiques au Canada.
Lorsque le MHDnMH est rejeté dans un plan d’eau, il se répartit dans les matières particulaires en suspension et les sédiments benthiques, où les organismes qui y vivent seront exposés à la substance. Néanmoins, on ne dispose d’aucune donnée de surveillance environnementale propre aux organismes vivant dans les sédiments pour cette substance. D’après les données expérimentales sur la substance analogue (PDMS), la toxicité du MHDnMH devrait être faible pour les espèces benthiques. Par conséquent, compte tenu de l’exposition au polymère, on estime que les effets nocifs découlant d’une exposition au MHDnMH sont improbables pour les organismes vivant dans les sédiments au Canada.
Incertitudes dans l’évaluation des risques pour l’environnement
Une incertitude majeure dans l’évaluation découle de la complexité du polymère. À la différence d’une substance chimique définie, on peut décrire le polymère uniquement par une répartition de structures homologues ayant différentes masses moléculaires. La masse moléculaire moyenne, les fractions de différentes masses moléculaires ainsi que les impuretés varient en fonction des formulations du polymère. Il convient de noter que l’évaluation portait sur les préoccupations relatives au polymère commercialisé au Canada (MHD34MH) et comprenait également le composant ayant une masse moléculaire de 500 g/mol (MHD5MH).
Une autre incertitude majeure concerne le manque de données sur les propriétés physiques et chimiques du MHDnMH. Le polymère peut seulement être caractérisé par les structures du monomère. En raison de sa masse moléculaire supérieure à 1 000 g/mol, on considère généralement qu’il se trouve en dehors du champ d’application des modèles RQSA actuels. Par conséquent, les prévisions modélisées ne s’appliquent qu’au polymère MHD5MH, alors que les données expérimentales pour les polymères de siloxane analogues ont été utilisées pour évaluer tant le MHD5MH que le MHD34MH. La comparaison des compositions chimiques du MHDnMH et de ses analogues semble indiquer que la différence dans les unités répétées et les unités terminales n’influencera pas leurs propriétés physiques et chimiques de façon importante.
Étant donné que les ensembles d’étalonnage des modèles RQSA ne comprennent pas beaucoup de composés de siloxane, les prévisions modélisées pour le MHD5MH sont incertaines et interprétées en faisant preuve d’un jugement scientifique. Les principaux paramètres liés aux propriétés physiques et chimiques sont estimés à l’aide des modèles RQSA et comparés aux mesures expérimentales pour les méthylsiloxanes linéaires analogues afin d’effectuer une modélisation plus approfondie. En cas de conflit dans les prévisions du potentiel de bioaccumulation, davantage de poids est accordé à l’observation dans les études expérimentales sur les analogues appropriés.
L’incertitude est également liée au manque de données sur les concentrations de MHDnMH dans l’environnement au Canada. Toutefois, la majorité du polymère fabriqué devrait être exporté à l’extérieur du pays, et les rejets dans l’environnement canadien devraient être faibles.
On ne saisit pas complètement le métabolisme du polymère. Bien que la clairance observée du polymère de siloxane (PDMS) soit rapide chez le poisson, on n’a pas déterminé si ce phénomène observé était véritablement en lien avec le métabolisme.
Étant donné que le MHDnMH est utilisé dans d’autres pays, il est possible qu’il entre sur le marché canadien comme composant d’articles manufacturés ou de produits de consommation. Cependant, les renseignements obtenus dans le cadre de l’enquête menée en vertu de l’article 71 n’indiquent pas qu’il est présent dans ces types de produits au Canada. Les renseignements disponibles ne sont pas suffisants actuellement pour calculer une estimation quantitative permettant de définir l’importance de cette source. On estime cependant que les proportions de MHDnMH rejetées dans les divers milieux naturels ne seraient pas très différentes de celle estimée dans la présente évaluation. On reconnaît également la possibilité que des rejets proviennent des sites d’enfouissement et contribuent aux concentrations environnementales globales.
Évaluation de l’exposition
Milieu naturel
Aucune donnée empirique sur les concentrations de MHDnMH dans les milieux naturels au Canada n’a été relevée. D’après son profil d’utilisation, le MHDnMH ne devrait pas être présent dans les aliments et les boissons au Canada. Comme on s’attend à ce que le polymère fabriqué soit en grande partie exporté à l’extérieur du pays, les rejets dans l’environnement canadien devraient être faibles. Les concentrations environnementales ont été estimées à l’aide des pourcentages des pertes prévus par l’outil de débit massique présenté au tableau 3 de la section « Rejet dans l’environnement » (Environnement Canada, 2010b). Ces pourcentages ont été appliqués à la quantité totale de MHDnMH sur le marché au Canada en 2006. Selon une estimation prudente, cette quantité pourrait atteindre jusqu’à 100 000 kg (Environnement Canada, 2010a). On estime les pertes à 1 000 kg dans l’eau à partir des eaux usées, à 100 kg dans l’air en raison des émissions atmosphériques et à 1 300 kg dans le sol par les sites d’enfouissement et les pertes au sol.
Les pertes estimées ont été utilisées dans ChemCAN, un modèle régional de fugacité de niveau III en champ lointain propre au Canada (ChemCAN, 2003). Aux fins de la modélisation, la structure oligomérique n = 5, d’une masse moléculaire d’environ 500 g/mol, a été utilisée. Cette forme est vendue sous le no CAS 70900-21-9 dans certaines versions commerciales de ce polymère et pourrait être présente en très faibles concentrations dans d’autres versions commerciales de masse moléculaire plus élevée du polymère (p. ex. dans la forme de masse moléculaire moyenne en nombre n = 34); elle est jugée adéquate pour le modèle ChemCAN. Les concentrations environnementales estimées sont indiquées à l’annexe III. On a obtenu des valeurs prudentes de la limite supérieure d’absorption quotidienne du MHDnMH pour la population générale au Canada sur la base des concentrations environnementales estimées, qui se sont de l’ordre de nanogrammes (10-9 g par kg p.c. [kilogramme de poids corporel]) par jour. De plus, en raison de la très faible pression de vapeur du MHDnMH, les concentrations dans l’air devraient être faibles.
Produits de consommation
Le MHDnMH est principalement utilisé comme produit intermédiaire dans la production de polymères de silicone non destinés à la population générale (Environnement Canada, 2010a).
Cependant, le MHDnMH est un composant de quatre types de produits cosmétiques au Canada : adhésif pour soutien-gorge (30 à 100 % en poids), crème décolorante pour la peau (0,1 à 0,3 % en poids), rouge à lèvres (< 0,1 % en poids) et maquillage pour les yeux (< 0,1 % en poids) [SDC, 2010]. Les estimations de l’exposition liée à l’utilisation de ces produits de consommation sont présentées à l’annexe IV. L’adhésif pour soutien-gorge est présent dans le revêtement intérieur des soutiens-gorges jetables utilisés avec des vêtements sans bretelles et à dos nu. D’après ces renseignements, l’exposition liée à l’utilisation de soutiens-gorges jetables devrait être de courte durée. L’exposition aiguë potentielle par contact avec la peau selon ce scénario a été estimée à
4,0 × 10-3 mg/kg p.c. par événement. Les crèmes décolorantes pour la peau sont en général appliquées quotidiennement pendant environ trois mois. L’exposition cutanée qui en résulte a été estimée à 0,2 mg/kg p.c. par jour. On a présumé que les rouges à lèvres étaient appliqués quatre fois par jour. L’exposition orale quotidienne liée à cette utilisation a été estimée à 5,6 × 10-4mg/kg p.c. par jour. Dans le cas du maquillage pour les yeux, on a présumé qu’il était appliqué deux fois par jour. L’exposition cutanée quotidienne liée à cette utilisation a donc été estimée à 2,8 × 10-4 mg/kg p.c. par jour.
La confiance dans les estimations de l’exposition à partir de l’environnement est faible. Aucune donnée n’a été relevée dans la littérature en ce qui concerne les concentrations de cette substance dans les milieux naturels. Les estimations de l’exposition liée à l’utilisation de produits de consommation ont été fondées sur les modèles, et la confiance dans les estimations est modérée.
Évaluation des effets sur la santé
Aucune donnée empirique relative aux effets sur la santé n’a été relevée pour le MHDnMH. On estime que les modèles de relations quantitatives structure-activité [R(Q)SA] actuels ne sont pas adaptés à la prévision des effets des polymères sur la santé.
Les produits commerciaux de MHDnMH comprennent des molécules de différentes masses moléculaires en fonction du nombre d’unités répétées dans ces molécules. Le MHDnMH et le polydiméthylsiloxane (PDMS, no CAS 63148-62-9) sont considérés comme des analogues structurels (voir le tableau 1 de la section « Identité de la substance »). Pour cette raison, les données sur les effets du PDSM sur la santé ont été jugés adéquates pour servir de base à l’évaluation des effets potentiels sur la santé associés à une exposition au MHDnMH.
Le Centre d'écologie et de toxicologie de l'industrie chimique européenne s’est penché sur le PDMS (viscosité de 10 à 100 000 cSt) dans le cadre d’une évaluation conjointe des produits chimiques de base (ECETOC, 1994). Cette évaluation indique que les résultats des études de génotoxicité in vitro réalisées avec des bactéries et des cellules de mammifères ne font état d’aucun potentiel mutagène ou clastogène pour le PDMS (ECETOC, 1994).
Le PDMS présente un faible potentiel de toxicité et n’entraîne pas de mortalité lorsque les concentrations testées excèdent les doses limites par inhalation ainsi que par voie orale ou cutanée. Lorsque sa viscosité est faible, le PDMS s’est avéré légèrement irritant pour les yeux, mais il ne constitue pas un irritant ou un sensibilisant pour la peau (ECETOC, 1994).
Les effets liés à une administration orale de PDMS sur les rats, les souris et les chiens ont fait l’objet d’études dans lesquelles les périodes d’exposition variaient de 4 semaines à 2 ans. La dose minimale avec effet nocif observé (DMENO) a été établie à 375 mg/kg p.c. par jour en fonction de l’augmentation des ulcères superficiels de l’estomac observée chez les souris mâles, mais pas chez les souris femelles, exposés pendant 76 semaines à du PDMS présent dans leur nourriture. Les effets d’une exposition cutanée au PDMS pour des périodes de 4 semaines à un an ont également été étudiés chez les lapins et les singes. La dose sans effet nocif observé (DSENO) a été établie à 2 000 mg/kg p.c. par jour, soit la seule dose à l’essai, chez les singes (4 macaques bruns mâles par groupe) après une application cutanée de PDMS (350 cSt), 5 fois par semaine pendant 26 mois. Les études sur l’exposition par inhalation au PDMS ont quant à elles été menées sur le chat, le lapin, le cobaye (un animal pour chacune de ces espèces), le rat et la souris. Cependant, en raison de la faible pression de vapeur du PDMS, les concentrations entraînant des effets n’ont pu être déterminées (ECETOC, 1994).
La toxicité du PDMS sur le développement a été étudiée chez les lapins. Le PDMS était administré durant la gestation par voie cutanée ou par injection sous-cutanée. La toxicité du PDMS sur le développement a également été étudiée chez les rats via des injections sous-cutanées. Dans les deux études d’administration cutanée chez les lapins le PDMS a été administré à une dose de 200 mg/kg p.c. par jour; une étude utilisant du PDMS 10 cSt et l’autre du PDMS 350 cSt. Même si deux études sur la toxicité par voie cutanée ont rapporté de faibles incidences d’hernie ombilicale, d’hippocratisme digital et de malformation de la partie avant du crâne, ces résultats n’étaient pas significatifs sur le plan statistique. Les quatre études comprenant des injections sous-cutanées ont également fait état d’effets nocifs sur le développement qui étaient significatifs sur le plan statistique à toutes les doses testées. En outre, le PDMS (10 à 1 000 cSt) ne s’est pas montré cytotoxique pour les cellules embryonnaires humaines (ECETOC, 1994; Siddiqui, 1994; Siddiqui et al., 2002).
La toxicité du PDMS (350 cSt) pour la reproduction a été étudiée chez des rats mâles et femelles auxquels on a administré cette substance par injection sous-cutanée pendant deux semaines avant l’accouplement et chez des singes mâles qui y ont été exposés par voie cutanée à une dose de 2 000 mg/kg p.c. par jour pendant 26 mois avant qu’ils s’accouplent avec des femelles réceptives. Aucun effet sur la fertilité, la performance reproductrice des mâles ou le développement n’a été observé (ECETOC, 1994).
Une étude de 2 ans a été réalisée sur l’absorption alimentaire de PDMS (10 cSt) par des rats à des doses de 0, 100, 300 ou 1 000 mg/kg p.c. par jour (Meeks et al., 2005). Une irritation locale des yeux a été observée chez les rats mâles et femelles de tous les groupes de traitement après 24 mois ainsi que du canal lacrymo-nasal (échelle microscopique) chez les mâles ayant reçu une dose de 1 000 mg/kg p.c. par jour. Une augmentation significative sur le plan statistique de l’incidence d’adénomes des cellules des îlots pancréatiques a été notée chez les rats mâles auxquels on a administré une dose de 1 000 mg/kg p.c. par jour. Les chercheurs n’ont pas considéré ces effets comme étant liés au traitement puisqu’ils n’ont constaté aucune augmentation des changements prénéoplasiques en rapport avec l’étude, ainsi qu’en raison de l’absence d’effets chez les femelles traitées, de l’incidence élevée d’adénomes des cellules des îlots pancréatiques dans le groupe des animaux témoins en rétablissement et des diverses incidences publiées pour ce type de tumeurs chez les animaux témoins. Par ailleurs, ils n’ont observé aucun autre effet lié au traitement. Ils ont établi la DSEO pour l’oncogénicité à 1 000 mg/kg p.c. par jour, soit la dose la plus élevée de l’étude. Qui plus est, une irritation oculaire a été observée dans le cadre d’une étude de 13 semaines menée sur des rats exposés par voie alimentaire à une dose de 5 000 ppm (700 mg/kg p.c. par jour) de PDMS (10 ou 350 cSt) [Siddiqui et al., 2002].
L’absorption de PDMS (35 à 1 200 cSt) par voie orale a été étudiée chez des rats auxquels des doses uniques ou répétées (13 jours) ont été administrées. Les taux globaux d’absorption étaient inférieurs à 0,2 % à des doses allant jusqu’à 2 500 mg/kg p.c. L’absorption de PDMS (100 cSt) par voie cutanée a été étudiée chez des sujets humains volontaires à une dose allant jusqu’à 50 mg/kg p.c. pour une période de 10 jours. Aucune absorption cutanée n’a été observée (ECETOC, 1994). De plus, le PDMS n’a pas eu d’incidence sur l’absorption gastro-intestinale du glucose chez les sujets (ECETOC, 1994).
Dans l’ensemble, les données disponibles indiquent que le PDMS ne présente pas de danger pour la santé des humains (ECETOC, 1994). Le PISSC (2009) a établi à 0,8 mg/kg p.c. une dose journalière acceptable temporaire de PDMS par jour en se basant sur une DSEO de 150mg/kg p.c. par jour provenant d’une étude de 3 mois menée sur le rat exposé par voie alimentaire (seule cette dose de 150mg/kg p.c. par jour fut utilisée dans l’étude) et en tenant compte d’un certain nombre de considérations associées entre autres à l’irritation oculaire ayant été observée dans d’autres études de toxicité chronique ou subchronique par voie orale. Dans la présente évaluation préalable, la dose minimale avec effet observé de 375 mg/kg p.c. par jour, qui est issue d’une étude de 76 semaines effectuée avec le PDMS comme il est indiqué ci-dessus, est utilisée pour la caractérisation du risque associé au MHDnMH.
La confiance dans l’évaluation des effets toxicologiques du MHDnMH est modérée. Bien qu’aucune information toxicologique propre à la substance n’ait été relevée, il a été jugé approprié d’utiliser les données sur la toxicité du PDMS comme information de base pour l’évaluation des effets potentiels du MHDnMH sur la santé, puisque ces deux substances possèdent des propriétés physiques et chimiques similaires.
Caractérisation du risque pour la santé humaine
Aucune donnée empirique relative aux effets sur la santé n’a été relevée pour le MHDnMH. En s’appuyant sur les données relatives aux effets sur la santé pour le PDMS, une substance analogue, et sur les évaluations de cette substance qui sont fondées sur le poids de la preuve et qui ont été réalisées par des organismes internationaux, on estime que le MHDnMH présente un faible potentiel de risque.
L’exposition environnementale (par l’air, l’eau potable et le sol) au MHDnMH a été estimée comme étant de l’ordre des nanogrammes (10-9 mg) par kg p.c. par jour et donc a été considérée comme étant négligeable. Aucun risque d’exposition à cette substance par l’entremise d’aliments ou de boissons n’est prévu. Une exposition peut toutefois avoir lieu par l’utilisation de produits de consommation qui contiennent du MHDnMH. Les estimations prudentes de la limite supérieure d’exposition au MHDnMH par les voies cutanée et orale liées à l’utilisation de produits de consommation (2,8 ×10-4à 0,2 mg/kg p.c. par jour pour les expositions quotidiennes cutanées; 5,6 × 10-4 mg/kg p.c. par jour pour les expositions quotidiennes par voie orale; et 4,0 × 10-3mg/kg p.c. par événement pour les expositions aigües cutanées) sont inférieures de plusieurs ordres de grandeur à la dose minimale d’effet nocif pour l’exposition cutanée (2 000 mg/kg p.c. par jour; une dose d’effet n’a pas été déterminée) établie pour la substance analogue, le PDMS (PISSC, 2009). Ces marges d’exposition sont jugées adéquates pour tenir compte des incertitudes liées aux bases de données concernant les effets sur la santé et l’exposition.
En raison de la faible pression de vapeur du MHDnMH, l’exposition par inhalation liée à l’utilisation de produits de consommation qui en contiennent est jugée négligeable.
Incertitudes de l’évaluation des risques pour la santé humaine
Il existe une incertitude quant à l’estimation de l’exposition de l’ensemble de la population aux concentrations de MHDnMH dans l’environnement en raison de l’utilisation de modèles et du manque de données canadiennes. Toutefois, comme on connaît les quantités commercialisées pour l’année civile 2006, on les a combinées à des pourcentages de perte estimés à l’aide de l’outil de débit massique d’Environnement Canada afin de modéliser les concentrations dans l’environnement. Comme la valeur maximale des quantités commercialisées a été utilisée dans la modélisation, les résultats modélisés devraient représenter des estimations prudentes de l’exposition environnementale.
En ce qui concerne l’exposition cutanée et orale par l’entremise des produits de consommation, les concentrations maximales présentes dans les produits cosmétiques (selon le Système de déclaration des cosmétiques) ont été utilisées afin d’obtenir des estimations prudentes. Une incertitude persiste quant à la probabilité d’utiliser des adhésifs pour soutien-gorge et des crèmes décolorantes étant donné que la seule utilisation relevée en réponse à un avis publié en application de l’article 71 de la LCPE (1999) était liée à la fabrication d’un article qui n’est pas destiné à la population générale au Canada.
En raison de l’absence de données pour le MHDnMH, un analogue structurel, le PDMS, a été utilisé pour identifier des effets possibles du MHDnMH sur la santé humaine. Bien que l’évaluation des effets sur la santé soit principalement fondée sur les données pour une substance analogue, les marges entre les niveaux d’exposition à partir des milieux naturels ou découlant de l’utilisation de produits de consommation et les niveaux associés à des effets sur la santé dans les études expérimentales ont été considérées comme étant adéquates pour tenir compte des incertitudes dans les bases de données des effets sur la santé et de l’exposition.
Selon les renseignements indiqués dans la présente évaluation préalable, la forme de MHDnMH commercialisée au Canada satisfait aux critères pour les polymères à exigences réglementaires réduites définis dans le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères).
Selon les renseignements disponibles, on estime que le MHDnMH ne pénètre pas dans l’environnement en une quantité, à une concentration ou dans des conditions qui ont ou peuvent avoir un effet nuisible immédiat ou à long terme sur l’environnement ou sa diversité biologique, ou qui constituent ou peuvent constituer un danger pour l’environnement essentiel pour la vie. De plus, le MHDnMH satisfait aux critères de persistance, mais ne satisfait pas aux critères de bioaccumulation définis dans le Règlement sur la persistance et la bioaccumulation (Canada, 2000).
À la lumière des renseignements disponibles, il est conclu que le MHDnMH ne pénètre pas dans l’environnement en une quantité ou concentration, ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Par conséquent, il est conclu que la forme de MHDnMH pour laquelle les exigences réglementaires sont réduites ne satisfait à aucun des critères énoncés à l’article 64 de la LCPE (1999).
En raison de la complexité associée à la formulation du polymère et des propriétés potentiellement dangereuses associées aux polymères ayant un faible masse moléculaire, on craint que de nouvelles activités qui font intervenir le MHDnMH et qui n’ont pas été relevées ni évaluées en vertu de la LCPE (1999) puissent faire en sorte que les substances répondent aux critères de l’article 64 de laLoi. Pour cette raison, il est recommandé de modifier la Liste intérieure des substances de façon à indiquer que le MHDnMH répond aux critères pour les polymères à exigences réglementaires réduites. Si d’autres formes du MHDnMH qui ne répondent pas aux exigences réglementaires réduites sont introduites sur le marché canadien, elles seront soumises aux exigences du Règlement sur les renseignements concernant les substances nouvelles.
Annelin, R.B. 1979. Rapport interne no I-0005-0669 de la Dow Corning. Cité dans Fendinger et al., 1997.
[AIEPS] Artificial Intelligence Expert System. 2003-2007. Version 2.05. Ottawa (Ont.) : Environnement Canada. Modèle élaboré par Stephen Niculescu. Disponible auprès d’Environnement Canada, Division de l’évaluation écologique, Section de l’évaluation des substances chimiques nouvelles.
Annelin, R.B., Frye, C.L. 1989. The piscine bioconcentration characteristics of cyclic and linear oligomeric permethylsiloxane.The Science of the Total Environment 83:1.
Annelin, R.B., Humble, D.A. 1978. Rapport noI-0005-0596 de la Dow Corning. Cité dans Fendinger et al., 1997.
Annelin, R.B., Klein, R., Varaprath, S. 1994. Rapport interne no 1994-I-0000 de la Dow Corning Corp. Cité dans Fendinger et al., 1997.
[AOPWIN] Atmospheric Oxidation Program for Windows [modèle d’estimation]. 2008. Version 1.92a. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[ARLA] Agence de réglementation de la lutte antiparasitaire. 2007. Note réglementaire REG 2007-04 de l’Agence de réglementation de la lutte antiparasitaire (ARLA) : liste des produits de formulation de l’ARLA. Ottawa (Ont.) : Santé Canada, ARLA. [consultée le 14 mai 2010].
Arnot, J.A., Gobas, F.A.P.C. 2003. A generic QSAR for assessing the bioaccumulation potential of organic chemicals in aquatic food webs. QSAR Comb. Sci. 22(3):337-345.
Atkinson R. 1991. Kinetics of the Gas-Phase Reactions of a Series of Organosilicon Compounds with OH and NO3Radicals and Ozone at 297 ± 2K. Environmental Science and Technology 25:863.
Aubert, M., Aubert, J., Augier, H., Guillemaut, C. 1985. Study of the toxicity of some silicone compounds in relation to marine biological chains. Chemosphere 14:127-138.
Battelle. 1992. Fate and effects of PDMS: Soil amendment sludge disposal. Rapport pour la Dow Corning Corporation, étude no SC 900090 du Battelle. 8 mai 1992. Battelle, Columbus Lab., Ohio, États-Unis. Cité dans ECETOC, 1994.
[BBM] Baseline Bioaccumulation Model. 2008. Gatineau (Qc) : Environnement Canada, Division des substances existantes. [Modèle basé sur celui de Dimitrov et al. 2005]. Disponible sur demande.
[BCFBAF] Bioaccumulation Program for Windows [modèle d’estimation]. 2008. Version 3.00. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[BDIM DPT] Base de données sur les ingrédients non médicinaux de la Direction des produits thérapeutiques [base de données exclusive]. 2010 [consultée en avril 2010]. Disponible auprès de Santé Canada, Division des produits thérapeutiques.
Belt, G.H., King, J.G., Haupt, H.F. 1977. Augmenting summer stream flow by use of silicone antitranspirant. Water Resour. Res. 13(2):267-272.
[BIOWIN] Biodegradation Probability Program for Windows [modèle d’estimation]. 2008. Version 4.10. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
Bruggeman, W.A., Weber-Fung, D., Opperhuizen, A., Van der Steen, J., Wijbenga, A., Hutzinger, O. 1984. Absorption and retention of polydimethylsiloxanes (silicones) in fish: preliminary experiments.Toxicological and experimental chemistry 7:287-296.
Buch, R.R., Ingebrigtson, D.N. 1979. Rearrangement of Polydimethylsiloxane Fluids on Soil. Environmental Science and Technol. 13:676.
Cabridenc, R. 1978. Polydimethylsiloxanes, IRNS. Cité dans le rapport no U/83/208(605) de la TNO à la CEE. Evaluation of the impact of Organo Silicone Compounds on the Aquatic Environment. TNO, La Haye (Pays-Bas). Cité dans ECETOC, 1994.
Canada. 1978. Règlement sur les aliments et drogues. C.R.C., ch. 870. Règlement sur les aliments et drogues.
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999). L.C. 1999, ch. 33, Gazette du Canada, Partie III, vol. 22, n° 3.
Canada. 2000. Loi canadienne sur la protection de l’environnement (1999) : Règlement sur la persistence et la bioaccumulation, C.P. 2000-348, 23 mars 2000, DORS/2000-107,Gazette du Canada, Partie II, vol. 134, n° 7.
Canada. Ministère de l’Environnement, ministère de la Santé. 2006. Loi canadienne sur la protection de l’environnement (1999) : Avis d’intention d’élaborer et de mettre en œuvre des mesures d’évaluation et de gestion des risques que certaines substances présentent pour la santé des Canadiens et leur environnement, Gazette du Canada, Partie I, vol. 140, n° 49.
Canada. Ministère de l’Environnement. 2009. Loi canadienne sur la protection de l’environnement (1999) :Avis concernant les substances du groupe 11 du Défi,Gazette du Canada, Partie I, vol. 143, n° 39.
Canada. Santé Canada. 2010. Base de données d’ingrédients de produits de santé naturels homologués. [base de données sur Internet].
Canada. Santé Canada. 2010. Base de données sur les ingrédients des produits de santé naturels [base de données sur Internet].
Canada. Santé Canada. 2010. Base de données d'ingrédients de produits de santé naturels[base de données sur Internet].
Carpenter, J.C., Cella, J.A., Dorn, S.B. 1995. Study of the degradation of polydimethylsiloxanes on soil. Environmental Science and Technology 29:864-868.
Carpenter, J.C., Leib, T.K., Sabourin, C.L., Spivack, J.L. 1996. Abstract no. PO 578, 17e réunion annuelle de la SETAC, Washington (DC). Cité dans Fendinger et al., 1997.
[CATABOL] Probabilistic assessment of biodegradability and metabolic pathways [modèle informatique]. c2004-2008. Version 5.10.2. Bourgas (Bulgarie) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. CATALOGIC.
ChemCAN [Level III fugacity model of 24 regions of Canada]. 2003. Version 6.00. Peterborough (Ont.) : Trent University, Le centre canadien de modélisation et de chimie environnementales [consulté en mai 2010].
Christensen, K. 1994. Silicone Environmental Health and Safety Council Study Report, Document ID no. 47. Cité dans Fendingeret al., 1997.
[ConsExpo] Consumer Exposure Model [en ligne]. 2006. Version 4.1. Bilthoven (Pays-Bas) : Rijksinstituut voor Volksgezondheid en Milieu (Institut néérlandais de la santé publique et l’environnement). Sécurité des produits.
[CPOP] Canadian POPs Model. 2008. Gatineau (Qc) : Environnement Canada, Division de l’évaluation écologique; Bourgas (Bulgarie) : Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. [Modèle basé sur celui de Mekenyan et al., 2005]. Disponible auprès de la Division de l’évaluation écologique d’Environnement Canada. Voir également Mekenyan et al, 2005.
Craig, P.J. 2003. Organometallic compounds in the environment. John Wiley & Sons Ltd, Angleterre.
Craig, N.C.D., Caunter, J.E., Eales, G.J. 1984. ICI Let. Brixham (Royaume-Uni). Document rédigé pour le Centre européen des silicones. Rapport no I-9039-0004 de la Dow Corning.
Craig, N.C.D., Caunter, J.E. 1990. The effects of polydimethylsiloxane (PDMS) in sediment on the polychaete worm Nereis diversicolor. Chemosphere 21(6):751-759.
Dimitrov, S.D., Dimitrova, N.C., Walker, J.D., Veith, G.D., Mekenyan, O.G. 2002. Predicting bioconcentration factors of highly hydrophobic chemicals. Effects of molecular size. Pure Appl. Chem. 74(10):1823-1830.
Dimitrov, S., Dimitrova, N., Parkerton, T., Comber, M., Bonnell, M., Mekenyan, O. 2005. Base-line model for identifying the bioaccumulation potential of chemicals. SAR QSAR Environ. Res. 16(6):531-554.
Eales, G.J., Taylor, D. 1983. A study of the movement of a polydimethylsiloxane fluid in sediment columns – Phase 2. Rapport I-9039-002 de la Dow Corning. Cité dans ECETOC, 1994.
[ECETOC] Centre d’écologie et de toxicologie de l’industrie chimique européenne. 1994. Joint Assessment of Commodity Chemicals No. 26: Linear Polymethylsiloxanes (viscosity 10 – 100 000 centistokes) CAS No. 63148-62-9. Bruxelles (Belgique) : ECETOC. Rapports JACC.
[ECOSAR] Ecological Structural Activity Relationships [Internet]. 2008. Version 1.00. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
Environnement Canada. 2008. Guidance for Conducting Ecological Assessments under CEPA, 1999, Science Resource Technical Series, Technical Guidance Module: Mass Flow Tool. Document de travail. Gatineau (Qc) : Environnement Canada, Division de l’évaluation écologique. Disponible sur demande.
Environnement Canada. 2010a. Données sur les substances du lot 11 recueillies en vertu de l’article 71 de la Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances identifiées dans le onzième lot du Défi. Données recueillies par Environnement Canada, Division de la mobilisation et de l’élaboration des programmes.
Environnement Canada. 2010b. Assumptions, limitations and uncertainties of the Mass Flow Tool for MHDnMH, CAS RN 70900-21-9. Document provisoire interne. Gatineau (Qc) : Environnement Canada, Division de l’évaluation écologique. Disponible sur demande.
Environnement Canada. 2010c. Industrial Release Report: CAS RN 70900-21-9. Le 19 mai 2010. Gatineau (Qc) : Environnement Canada, Division de l’évaluation écologique. Disponible sur demande.
Environnement Canada, Santé Canada. 2008a. Évaluation préalable pour le Défi : Octamethylcyclotetrasiloxane(D4), n° CAS 556-67-2 [en ligne]. Ottawa (Ont.) : Environnement Canada, Santé Canada. [consulté en mai 2010].
Environnement Canada, Santé Canada. 2008b. Évaluation préalable pour le Défi : Décaméthylcyclopentasiloxane (D5), n° CAS 541-02-6 [en ligne]. Ottawa (Ont.) : Environnement Canada, Santé Canada. [consulté en mai 2010].
Environnement Canada, Santé Canada. 2008c. Évaluation préalable pour le Défi : Décaméthylcyclopentasiloxane (D6), n° CAS 540-97-6 [en ligne]. Ottawa (Ont.) : Environnement Canada, Santé Canada. [consulté en mai 2010].
[EPIsuite] Estimation Programs Interface Suite for Microsoft Windows [modèle d’estimation]. 2008. Version 4.00. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[EQC] Equilibrium Criterion Model. 2003. Version 2.02. Peterborough (Ont.) : Trent University, Canadian Environmental Modelling Centre. Le centre canadien de modélisation et de chimie environnementales.
Fendinger, N.J., Lehmann, R.G., Mihaich, E.M. 1997. Polydimethylsiloxane. Organosilicon Materials. The Handbook of Environmental Chemistry. Berlin, Heidelberg (Allemagne) : Springer-Verlag.
Firmin, R. 1984. Les composés organosiliciés et l’environnement aquatique. Mémoire, Sciences Environnement, Université Libre de Bruxelles. Cité dans le rapport no U/83/208(605) de la TNO à la CEE. Evaluation of the Impact of Organo Silicon Compouns on the Aquatic Environment. TNO, La Haye (Pays-Bas). Cité dans ECETOC, 1994.
Garvey, N., Collins, M.K., Mihaich, E.M. 1996. Abs no. 256, 17e réunion annuelle de la SETAC, Washington (DC) [cité dans Graiver et al., 2003].
Gelest. 2008a. Fiche signalétique : Tetradecamethylhexasiloxane - SIT7089.0. Gelest, Inc., Morrisville (PA) 19067. [consultée en décembre 2010].
Gelest. 2008b. Fiche signalétique : Poly(dimethylsiloxane), hydride terminated – DMS-H03. Gelest, Inc., Morrisville (PA). [consultée le 17 mai 2010].
Gelest. 2010. Silicone réactif : forger de nouveaux liens de polymère. Gelest Inc. Morrisvile (PA) 19067.
Gettings, R.L., Lane, T.H. 1982. Rapport interne noI0005-10957 de la Dow Corning Corp. Cité dans ECETOC, 1994.
Graiver, D., Farminer, K.W., Narayan, R. 2003. A review of the fate and effects of silicones in the environment. Journal of Polymers and the Environment 11(4):129-136.
Guillenaut, G., Aubert, J., Augier, H. 1987. Study on organosilicon contamination and toxicity in relation to the marine biomass. Revue Internationale d’Océanographie Médicale85/86:88.
Henry, K.S., Wieland, W.H., Powell, D.E., Giesy, J.P. 2001. Laboratory analyses of the potential toxicity of sediment-associated polydimethylsiloxne to benthic macroinvertebrates. Environmental Toxicology and Chemistry20(11):2611-2616.
[HENRYWIN] Henry’s Law Constant Program for Microsoft Windows [modèle d’estimation]. 2008. Version 3.20. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
Hill, R.W. 1980. Determination of acute toxicity of DC 561 and DC X2-3168 to mussel (Mytilus edulis), rapport 19039 (6 et 8) de la DC. Cité dans le rapport no U/83/208(605)de la TNO à la CEE. Evaluation of the Impact of Organo Silicone Compounds on the Aquatic Environment. TNO, La Haye (Pays-Bas). Cité dans ECETOC, 1994.
Hill, R.W., Young, B.E., Eales, G.J. 1980. Imperial Chemical Industries Ltd., Brixham, TQ58BA, Angleterre. Determination of acute toxicity of Dow Corning DC 561 to the plaice (Pleuronectes platessa). Rapport no BL/B/2052 rédigé pour la Dow Corning (rapport no I-9030-5 de la DC).
Hill, R.W., Young, B.E., Eales, G.J. 1984. Imperial Chemical Industries Ltd., Brixham, TQ58BA, England. Effect of an organosilicon formulation on embryos and larvae of the sheepshead minnow (Cyprinodon variegatus). Rapport no BL/B/2392A rédigé pour le Centre européen des silicones. 34 p. (rapport no I-9039-0003 de la DC). Cité dans Fendinger et al., 1997 et ECETOC, 1994.
Hobbs, E.J., Keplinger, M.L., Calandra, J.C. 1975. Toxicity of polydimethylsiloxanes in certain environmental systems.Environmental Research 10:397-406.
[HYDROWIN] Hydrolysis Rates Program for Microsoft Windows [modèle d’estimation]. 2008. Version 2.00. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[IARC] International Agency for Research on Cancer Working Group on the Evaluation of Carcinogenic Risks to Humans. 1990. Monographies du CIRC sur l’évaluation des risques de cancérogénicité pour l’homme. Vol.74 : Surgical implants and other foreign bodies.
Kukkonen, J., Landrum, P.F. 1995. Effects of sediment-bound polydimethylsiloxane on the bioavailability and distribution of benzo[a]pyrene in lake sediment to Lumbriculus variegates.Environmental Toxicology and Chemistry 14:523-531.
[KOCWIN] The Soil Adsorption Coefficient Program [modèle d’estimation]. 2008. Version 2.00. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation.
[KOWWIN] Octanol-Water Partition Coefficient Program for Microsoft Windows [modèle d’estimation]. 2008. Version 1.67. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
Lehmann, R.G., Varaprath, S., Frye, C.L. 1994a. Degradation of silicone polymers in soil. Environmental Toxicology and Chemistry 13:1061-1064.
Lehmann, R.G., Varaprath, S., Frye, C.L. 1994b. Fate of silicone degradation products (silanols) in soil. Environmental Toxicology and Chemistry 13:1753-1759.
Lehmann, R.G., Varaprath, S., Annelin, R.B., Arndt, J. 1995. Degradation of silicone polymer in a variety of soils.Environmental Toxicology and Chemistry 14:1299-1305.
Lehmann, R.G., Miller, J.R., Xu, S., Singh, U.B., Reece, C.F. 1998. Degradation of silicone polymer at different soil moistures.Environmental Science and Technology 32:1260-1264.
Levier, R.R. 1988. Permethylated siloxane insect toxicants. Silicon chemistry. COREY-GASPAR – Ellis Howood Publishers – Chap. 15 : 153-160. Cité dans ECETOC, 1994.
Maggi, P., Alzieu, C. 1977. Étude de la nocivité d’huiles polydiméthyl -siloxane à l’égard d’organismes marins. Science et Pêche, Bulletin de l’Institut des Pêches Maritimes. 269:1-3. Cité dans Fendinger et al., 1997; Stevens et al., 2001, et ECETOC, 1994.
Mann, H., Ollenschlager, B., Reichenback-Klinke, H.H. 1977. Reichenbach-Klinke, Untersuchunger zur Wirkung von Siliconölen auf Regenbogenforellen. Fisch. Umwelt. 3:19. Cité dans Fendinger et al., 1997 et ECETOC, 1994.
Meeks, R.G., Jean, P.A., Mertens, J.W., Regan, K.S., Crissman, J.W., Plotzke, K.P. 2005. Chronic toxicity and oncogenicity study of polydimethylsiloxane (PDMS) 10 Cst fluid in Fisher 344 rats.Toxicol. Sci. 84(1-S):308.
Mekenyan, G., Dimitrov, S.D., Pavlov, T.S., Veith, G.D. 2005. POPs: A QSAR system for creating PBT profiles of chemicals and their metabolites. SAR and QSAR Environmental Research16(1-2):103-133.
[MPBPWIN] Melting Point Boiling Point Program for Microsoft Windows [modèle d’estimation]. 2008. Version 1.43. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[NCI] National Chemical Inventories [base de données sur CD-ROM]. 2009. Issue 1. Columbus (OH) : American Chemical Society [consultée en mai 2010]. Inventaires chimiques nationaux.
Nielson, W.R., Heinlein, J.P., Haigh, W.G. 1975. Acaridical and insectisidal activity of various silicone fluids. TSCA 8(c) Submission 87-8215084. Cité dans ECETOC, 1994.
Noll, W. 1968. Chemistry and Technology of Silicones. New York (NY) : Academic Press. [cité dans USEPA, 2008]
[OCDE] Organisation de coopération et de développement économiques. 1994. Groupe des produits chimiques et Comité de gestion. Rapport du président, Troisième réunion des experts de l’OCDE sur les polymères, à Tokyo, du 14 au 16 avril 1993.
[OASIS Forecast] Optimized Approach based on Structural Indices Set [en ligne]. 2005. Version 1.20. Bourgas (Bulgarie) : Bourgas Prof. Assen Zlatarov University, Laboratory of Mathematical Chemistry. Logiciels OASIS.
Opperhuizen A, Van Der Velde EW, Gobas FAPC, Liem DAK, Van Der Steen JMD, Hutzinger O. 1985. Relationship between bioconcentration in fish and steric factors of hydrophobic chemicals.Chemosphere 14: 1871-1896.
[PCKOCWIN] Organic Carbon Partition Coefficient Program for Windows [modèle d’estimation]. 2008. Version 2.00. Washington (DC) : United States Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[PISSC] Programme international sur la sécurité des substances chimiques. 2009. Polydimethylsiloxane. Geneva (Suisse) : Organisation mondiale de la santé. (WHO Food Additives Series 60, 3.1.7). Financé conjointement par l’Organisation des Nations-Unies pour l’alimentation et l’agriculture et l’Organisation mondiale de la santé. Évaluation de la sécurité de certains additifs alimentaires
Putt, A.E. 1994. Polydimethylsiloxane (PDMS) – the subchronic toxicity to midge larvae (chironomus tentans) under flow-through conditions. Springborn Laboratories, Inc. Rapport no94-4-5235 présenté au Silicones Environmental Health and Safety Council [cité dans Fendinger et al., 1997].
Putt, A.E., Mihaich, E.M. 1996. Effect of sediment-bound polydimethyl-siloxane (PDMS) to aquatic invertebrates. Abs no. 257, 17e réunion annuelle de la SETAC, Washington (DC) [cité dans Fendinger et al., 1997].
Recherche de produits pharmaceutiques en ligne [base de données sur Internet]. 2010. Ottawa (Ont.) : Santé Canada [consultée en avril 2010].
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2006a. General fact sheet: Limiting conditions and reliability, ventilation, room size, body surface area. Version mise à jour pour ConsExpo 4 [en ligne]. Bilthoven (Pays-Bas) : RIVM (Institut national néérlandais de la santé publique et de l’environnement). Rapport 320104002/2006 du RIVM [consulté en mai 2010].
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu. 2006b. Cosmetics fact sheet: To assess the risks for the consumer [en ligne]. Bilthoven (Pays-Bas) : RIVM (Institut national néérlandais de la santé publique et de l’environnement). Rapport 320104001/2006 du RIVM [consulté en mai 2010].
Sabourin, C.L., Carpenter, J.C., Leib, T.K., Spivack, J.L. 1996. Biodegradation of dimethylsilanediol in soils. Appl. Environ. Microbiol. 62(12):4352-60.
Santé Canada. 1998. Exposure factors for assessing total daily intake of priority substances by the general population of Canada. Rapport inédit. Ottawa (Ont.) : Santé Canada, Direction de l’hygiène du milieu.
Santé Canada. 2009. Liste critique des ingrédients dont l’utilisation est restreinte ou interdite dans les cosmétiques – septembre 2009 [en ligne]. Ottawa (Ont.) : Santé Canada, Sécurité des produits de consommation [consultée le 14 mai 2010].
Sakuratani, Y., Noguchi, Y., Kobayashi, K., Yamada, J., Nishihara, T. 2008. Molecular size as a limiting characteristic for bioconcentration in fish. J. Environ. Biol. 29(1):89-92.
[SDC] Système de déclaration des cosmétiques [base de données exclusive]. 2010. Disponible auprès de Santé Canada, Division des cosmétiques.
Siddiqui, W.H. 1994. Developmental toxicity evaluation of Dow Corning & Ntilde; antifoam A compound, food grad in rabbits.Teratology 49:397.
Siddiqui, W.H., Schardein, J.L., Cassidy, S.L., Meeks, R.G. 1994. Reproductive and developmental toxicity studies of silicone elastomer Q7-2423/Qw7-2551 in rats and rabbits.
Siddiqui, W.H., Blee, M.B., Tompkins, E.C., Meeks, R.G. 2002. 13-weeks dietary and developmental toxicity studies of polydimethylsiloxanes (PDMS) in rats and rabbits.Toxicologist 22(1-S):232.
Sommerlade, R., Parlar, H., Wrobel, D., Kochs, P. 1993. Product analysis and kinetics of the gas-phase reactions of selected organosilicon compounds with OH radicals using a smog chamber-mass spectrometer system. Environmental Science and Technology27 (12): 2435–2440.
Spacie, A. 1972. Acute toxicity of SAG 10 and SAG 350 silicone antifoam to aquatic organisms. Rapport interne, Union Carbide Chemicals Corp., Danbury (États-Unis). Cité dans ECETOC, 1994.
[SPIN] Substances in Preparations in Nordic Countries [base de données sur Internet]. 2006. Copenhague (Danemark) : Conseil des ministres des pays nordiques. Substances dans les préparations dans les pays nordiques[consulté en mai 2010].
Stevens, C. 1998. Environmental degradation pathways for the breakdown of polydimethylsiloxanes. Journal of Inorganic Biochemistry 69(3):203-207.
Stevens, C., Powell, D.E., Mäkelä, P., Karman, C. 2001. Fate and effects of polydimethylsiloxane (PDMS) in marine environments.Marine Pollution Bulletin 42(7):536-543.
[USEPA] United States Environmental Protection Agency. 2008. Interpretive assistance document for assessment of polymers. United States Environmental Protect Agency.
[USEPA] United States Environmental Protection Agency. 2005. Toxic Substances Control Act-Inventory Update Rule (TSCA-IUR) - Information on High Production Volume (HPV) Chemicals. United States Environmental Protection Agency. [consulté en décembre 2005 et en janvier 2006].
Varaprath, S., Frye, C.L., Hamelink, J. 1996. Aqueous solubility of permethylsiloxanes (silicones). Environmental Toxicology and Chemistry 15(8):1263-1265.
Wacker. 1992. Wacker-Broschüre: Silicone Fluids AK, Wacker Chemie AG, Munich, Allemagne. Cité dans ECETOC, 1994.
Watanabe, N., Nakamura, T., Watanabe, E., Sato, E., Ose, Y. 1984a. Bioconcentration potential of polydimethylsiloxane (PDMS) fluids by fish. Science of the Total Environment38:167.
Watanabe, N., Yasuda, Y., Kato, K., Nakanura, T., Funasaka, R., Shimokawa, K., Sato, E., Ose, Y. 1984b. Determination of trace amounts of siloxanes in water, sediments and fish tissues by inductively coupled plasma emission spectrometry. Science of the Total Environment 34(1-2):169-176.
[WATERNT] Water Solubility Program [modèle d’estimation]. 2008. Version 1.01. Washington (DC) : US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
[WSKOWWIN] Water Solubility for Organic Compounds Program for Microsoft Windows [modèle d’estimation]. 2008. Version 1.41. Washington (DC) : United States Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY) : Syracuse Research Corporation. Outils d'évaluation de l'exposition et des modèles.
Xu, S. 1998. Hydrolysis of poly(dimethylsiloxanes) on clay minerals as influenced by exchangeable cations and moisture.Environmental Science and Technology 32(20):3162-3168.
Annexe I : Rapport entre la viscosité, le degré de polymérisation et la masse moléculaire (Wacker, 1992, et Fendinger et al., 1997)
Annexe Ia. Données relatives au PDMS (Wacker, 1992, et Fendinger et al., 1997)
| Viscosité (cSt) | Nombre moyen d’unités D* | Masse moléculaire moyenne en nombre (g/mol) |
|---|---|---|
| 10 | 15 | 1 300 |
| 50 | 40 | 3 000 |
| 100 | 70 | 5 000 |
| 1 000 | 200 | 15 000 |
| 10 000 | 500 | 37 000 |
| 100 000 | 1 000 | 74 000 |
Annexe Ib. Données relatives au PDMS, tirées de Noll (1968, citées dans USEPA, 2008)
| Viscosité (cSt) | Nombre moyen d’unités D | Masse moléculaire moyenne en nombre (g/mol) |
|---|---|---|
| 60 | 50 | 3 600 |
| 140 | 110 | 8 000 |
| 440 | 230 | 17 000 |
| 680 | 280 | 21 000 |
| 1 440 | 400 | 30 000 |
| 10 000 | 800 | 60 000 |
| 50 000 | 1 200 | 88 000 |
| 100 000 | 1 400 | 103 000 |
| 300 000 | 1 900 | 143 000 |
Les prévisions modélisées ont seulement été appliquées au MHD5MH et à ses analogues (méthylsiloxanes linéaires de faible masse moléculaire), avec comme seules données d’entrée les SMILES, les masses moléculaires et les données expérimentales.
| Paramètres d’entrée des modèles | Propriétés physico-chimiques et devenir EPIsuite, 2008 (tous les modèles, notamment : |
|||
|---|---|---|---|---|
| MHD5MH (70900-21-9) |
MD3M (141-63-9) |
MD4M (107-52-8) |
MD5M (541-01-5) |
|
| Code SMILES | Si(C)(C)OSi(C) (C)OSi(C)(C) OSi(C)(C)OSi (C)(C)OSi(C) (C)OSi(C)(C) |
O([Si](O[Si](O [Si](C)(C)C)(C) C)(C)C)[Si](O [Si](C)(C)C)(C) C |
O([Si](O[Si](O [Si](C)(C)C)(C) C)(C)C)[Si](O [Si](O[Si](C)(C) C)(C)C)(C)C |
O([Si](O[Si](O [Si](O[Si](C)(C) C)(C)C)(C)C) (C)C)[Si](O[Si] (O[Si](C)(C)C) (C)C)(C)C |
| Masse moléculaire (g/mol) | 505,10 | 384,84 | 459,00 | 533,15 |
| Point de fusion (oC) | ||||
| Point d’ébullition (°C) | ||||
| Température (oC) | ||||
| Masse volumique (kg/m3) | ||||
| Pression de vapeur (Pa) | ||||
| Constante de la loi de Henry (Pa·m3/mol) | ||||
| Koe (coefficient de partage octanol-eau, sans dimension) | 6,0 | 6,6 | 7,2 | |
| Solubilité dans l’eau (mg/L) | 7,0 × 10-5 | |||
Annexe III : Estimation des concentrations de MHDnMH dans les milieux naturels à l’aide du modèle ChemCAN, version 6.00 (ChemCAN, 2003)[1]
| Milieu[2] | Concentration estimée |
|---|---|
| Air ambiant[3] | 1,74 ng/m3 |
| Eau de surface | 0,128 ng/L |
| Sol | 1,47 × 10-3 ng/g de solides |
| Sédiments | 9,09 ng/g de solides |
[2] Les concentrations du débit entrant par défaut, soit 2 ng/m3 dans l’air et 3 ng/L dans l’eau ont été précisées par ChemCAN, version 6.00.
[3] La demi-vie de dégradation oxydative dans l’air a été estimée à 5,125 jours (AOPWIN, 2008) et à 3 semaines dans le sol (selon les données sur la dégradation du PDMS dans le sol).
Annexe IV : Estimations de l’exposition cutanée au MHDnMH liée à l’utilisation de soutiens-gorges jetables, de crème décolorante pour la peau, de maquillage pour les yeux et de rouge à lèvres
| Produit | Hypothèses | Exposition estimée |
|---|---|---|
| Adhésif pour soutien-gorge[1] | Dose appliquée = (épaisseur du produit sur la peau) (surface exposée) (100 %) (densité du produit) / poids corporel
= (0,002 m) (0,1575 m2) (1) (0,90 kg/m3) / 70,9 kg = 0,284 mg / 70,9 kg = 4,0 × 10-3 mg/kg p.c. |
Dose aiguë = 4,0 × 10-3 mg/kg p.c. par événement |
| Crème décolorante pour la peau[1] | Utilisation du modèle ConsExpo v4.1 (ConsExpo, 2006).
|
Dose cutanée quotidienne : 0,2 mg/kg p.c. par jour |
| Maquillage pour les yeux1 | Utilisation du modèle ConsExpo v4.1 (ConsExpo, 2006).
|
Dose cutanée chronique : 2,8 × 10-4 mg/kg p.c. par jour |
| Rouge à lèvres[1] | Utilisation du modèle ConsExpo v4.1 (ConsExpo, 2006).
|
Dose orale chronique : 5,6 × 10-4 mg/kg p.c. par jour |
Notes de bas de page
[2] La masse équivalente du groupe fonctionnel (MEGF) est, pour les groupements cationiques, le rapport entre la masse du polymère et le nombre de moles du groupement cationique. Ainsi, les polymères comportant relativement peu de groupements cationiques se caractérisent par une MEGF élevée.