Document certifié d'information sur les produits - Entités chimiques (DCIP-EC)
Ce document HTML n'est pas un modèle. Il a pour but d'afficher le contenu du formulaire aux fins de visionnement seulement.
(Version: 2017/10/30)
Résumé des renseignements sur le produit
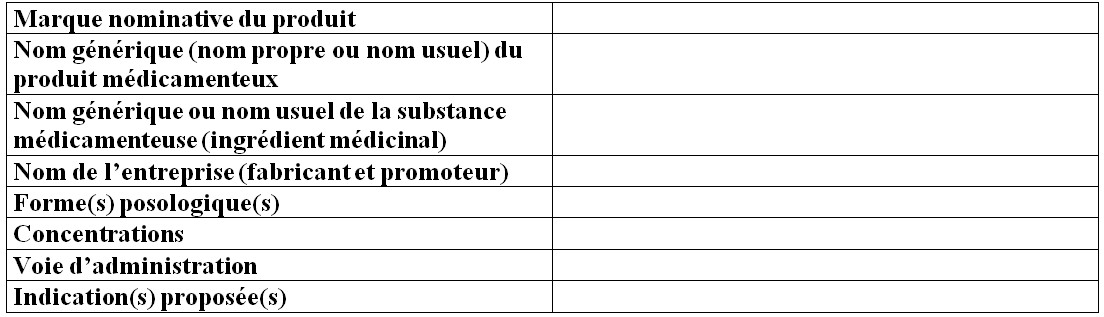
Figure 1 - Description textuel
- Marque nominative du produit
- Nom générique (nom propre ou nom usuel) du produit médicamenteux
- Nom générique ou nom usuel de la substance médicamenteuse (ingrédient médicinal)
- Nom de l’entreprise (fabricant et promoteur)
- Forme(s) posologique(s)
- Concentrations
- Voie d’administration
- Indication(s) proposée(s)
(a) Date du DCIP du promoteur :
(b) Résumé administratif : (usage réservé à Santé Canada)

Figure 2 - Description textuel
- Identificateur docuBridge
- Numéro de contrôle
- Version interne et date d’acceptation
2.3.S Substance médicamenteuse (nom, fabricant)
2.3.S.1 Renseignements généraux
2.3.S.1.2 Structure
(a) Nom de l'ingrédient pharmaceutique actif (IPA) et formule développée, incluant la stéréochimie relative et absolue :
(b) Formule moléculaire :
(c) Masse moléculaire :
2.3.S.1.3 Propriétés générales
(a) Solubilité et dose/volume de solubilité (DVS) par rapport aux limites physiologiques de pH (de 1 à 6,8)
(b) Forme polymorphique
(c) pKa
2.3.S.2 Fabrication (nom, fabricant)
2.3.S.2.1 Fabricants (nom, fabricant)
(a) Les noms, l'adresse et la responsabilité de chaque fabricant, y compris les sous-traitants, et chaque établissement ou installation de production proposé pour la fabrication et les essais :

Figure 3 - Description textuel
- Nom et adresse
- Responsabilité (par exemple, fabrication, emballage, étiquetage et essais)
- No de la FM ou no du CEP
2.3.S.2.2 Description du procédé de fabrication et des contrôles en cours de fabrication (nom, fabricant)
(a) Un schéma présentant les réactifs et les solvants :
Nom et adresse des sites de fabrication des matériaux de départ ou des intermédiaires des IPA :
Nom et structure chimique du matériau de départ ou de l’intermédiaire de l'IPA :
Fabricant :
Adresse du site de fabrication :
S.3.2 Impuretés
Impuretés potentielles ne faisant pas l'objet d'un contrôle de routine de la substance médicamenteuse :
2.3.S.4 Contrôle de la substance médicamenteuse
2.3.S.4.1 Spécifications (nom, fabricant)
(a) Spécifications de la substance médicamenteuse

Figure 4 - Description textuel
- Norme déclarée (par exemple maison, USP, B.P., Ph. Eur.)
- Version ou numéro de référence des spécifications
- Essais
- Critères d’acceptation
- Méthodes analytiques (type, source, version)
2.3.S.6 Dispositif de fermeture des contenants
(a) Description des dispositifs de fermeture des contenants utilisés pour l'entreposage et l'expédition de la substance médicamenteuse :
2.3.S.7 Stabilité
2.3.S.7.1 Sommaire et conclusions sur la stabilité
(a) Conditions d'entreposage et période de contre-essais proposées (ou durée de conservation, s'il y a lieu) :

Figure 5 - Description textuel
- Système de fermeture du contenant
- Conditions d’entreposage
- Période de contre-essais
2.3.P Produit médicamenteux (nom, forme posologique)
2.3.P.1 Description et composition du produit médicamenteux (nom, forme posologique)
(a) Composition de la forme posologique :
(i) Description de la composition, c'est-à-dire (c.-à-d.) la liste de tous les constituants de la forme posologique, doit indiquer la quantité de chaque constituant présent dans une unité posologique (y compris les surtitrages, le cas échéant) :
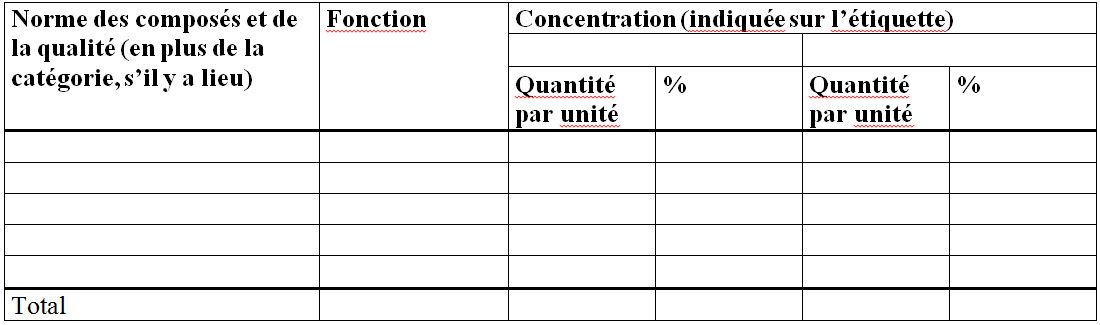
Figure 6 - Description textuel
- Norme des composés et de la qualité (en plus de la catégorie, s’il y a lieu)
- Fonction
- Concentration (indiquée sur l’étiquette)
- Quantité par unité
- %
- Quantité par unité
- %
- Total
(ii) Composition de tous les constituants qui sont des mélanges (par exemple [p. ex.], colorants, enrobages, capsules, encres d'impression) :
(b) Description des diluants de reconstitution, s'il y a lieu :
2.3.P.3 Fabrication (nom, forme posologique)
2.3.P.3.1 Fabricants (nom, forme posologique)
(a) Les noms, l'adresse et la responsabilité de chaque fabricant, y compris les sous-traitants, et chaque établissement ou installation de production proposé pour la fabrication et les essais :

Figure 7 - Description textuel
- Nom et adresse
- Responsabilité (p. ex. fabrication, emballage et essais)
- No de la FM
2.3.P.3.2 Formule des lots (nom, forme posologique)
(a) La liste de tous les ingrédients de la forme posologique devant être utilisés dans le procédé de fabrication et leur quantité par lot (y compris le surtitrage, le cas échéant) :
2.3.P.3.3 Description du procédé de fabrication et des contrôles en cours de fabrication (nom, forme posologique)
(a) Schéma du procédé de fabrication :
(b) Description narrative du procédé de fabrication, y compris le type et la capacité de fonctionnement de l'équipement ainsi que les paramètres de procédé :
2.3.P.3.4 Contrôle des étapes critiques et des intermédiaires (nom, forme posologique)
(a) Résumé des contrôles effectués aux étapes critiques du procédé de fabrication et sur les intermédiaires isolés :
2.3.P.3.5 Validation et évaluation du procédé (nom, forme posologique)
Résumé des renseignements de validation du procédé, y compris les engagements, pour les étapes critiques du procédé de fabrication (p. ex. le numéro de protocole, les paramètres) :
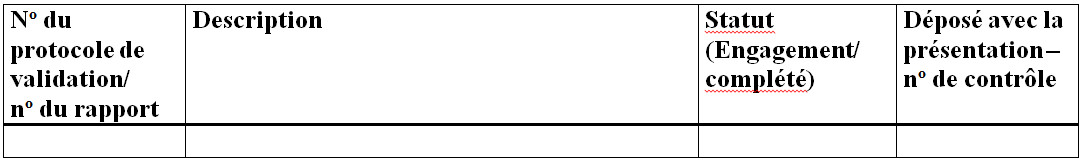
Figure 9 - Description textuel
- Nº du protocole de validation/ no du rapport
- Description
- Statut (Engagement/ complété)
- Déposé avec la présentation - no de contrôle
2.3.P.5 Contrôle du produit médicamenteux (nom, forme posologique)
2.3.P.5.1 Spécifications (nom, forme posologique)
(a) Spécifications du produit médicamenteux :
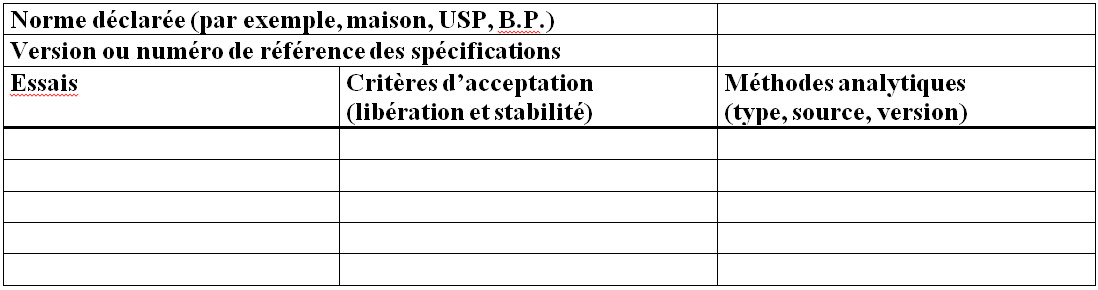
Figure 10 - Description textuel
- Norme déclarée (par exemple, maison, USP, B.P.)
- Version ou numéro de référence des spécifications
- Essais
- Critères d’acceptation (libération et stabilité)
- Méthodes analytiques (type, source, version)
2.3.P.7 Dispositif de fermeture des contenants (nom, forme posologique)
(a) Description des dispositifs de fermeture des contenants, y compris le nombre d'unités, la taille du contenant ou le volume :

Figure 11 - Description textuel
- Concentration
- Nombre d’unités
- Taille du contenant
- Description
2.3.P.8 Stabilité (nom, forme posologique)
2.3.P.8.1 Sommaire et conclusions sur la stabilité (nom, forme posologique)
(a) Durée de conservation et conditions d'entreposage proposées (et durée et conditions d'entreposage en cours d'utilisation, s'il y a lieu) :

Figure 12 - Description textuel
- Dispositif de fermeture du contenant
- Conditions d’entreposage (et conditions d’entreposage en cours d’utilisation, s’il y a lieu)
- Durée de conservation (et période limite d’utilisation, s’il y a lieu)
2.3.P.8.2 Protocole de stabilité post‑homologation et engagement à l'égard de la stabilité (nom, forme posologique)
(a) Protocole de stabilité pour les lots d'engagement :
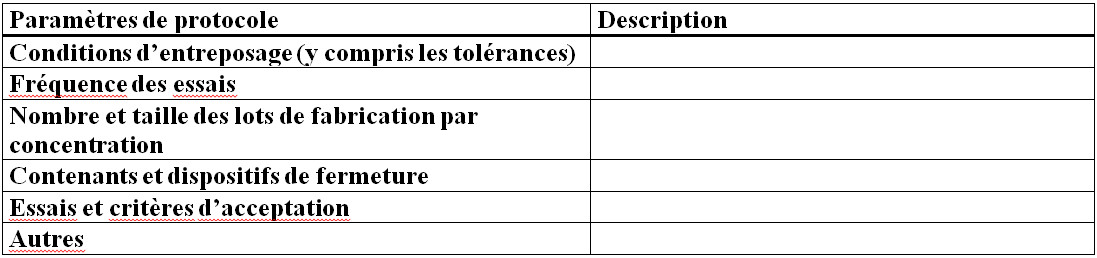
Figure 13 - Description textuel
- Paramètres de protocole
- Conditions d’entreposage (y compris les tolérances)
- Description
- Fréquence des essais
- Description
- Nombre et taille des lots de fabrication par concentration
- Description
- Contenants et dispositifs de fermeture
- Description
- Essais et critères d’acceptation
- Description
- Autres
- Description
- Conditions d’entreposage (y compris les tolérances)
(b) Protocole de stabilité pour les lots de fabrication permanents (c.-à-d. en cours) :
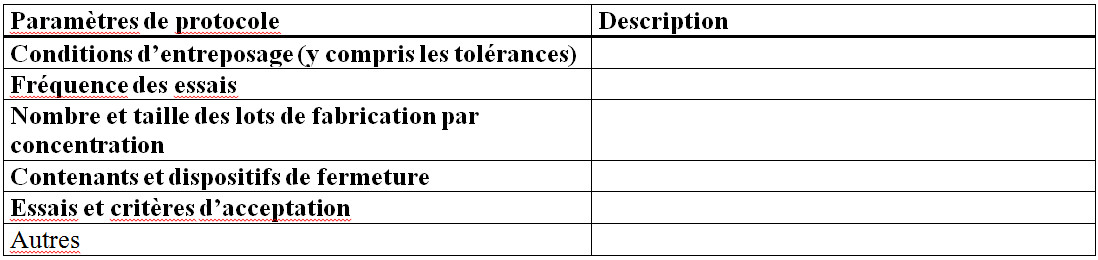
Figure 14 - Description textuel
- Paramètres de protocole
- Conditions d’entreposage (y compris les tolérances)
- Description
- Fréquence des essais
- Description
- Nombre et taille des lots de fabrication par concentration
- Description
- Contenants et dispositifs de fermeture
- Description
- Essais et critères d’acceptation
- Description
- Autres
- Description
- Conditions d’entreposage (y compris les tolérances)
2.3.P.8.3 Données sur la stabilité (nom, forme posologique)
(a) On doit appliquer la méthode des extrêmes et la méthode de la matrice aux lots d'engagement et aux lots de fabrication permanents (c.-à-d. en cours), s'il y a lieu :