Mise à jour de l’ébauche d’évaluation préalable - Groupe de certaines substances ignifuges organiques - Mélamine
Titre officiel : Mise à jour de l’ébauche d’évaluation préalable : Groupe de certaines substances ignifuges organiques 1,3,5-Triazine-2,4,6-triamine (mélamine)
No de registre du Chemical Abstracts Service 108-78-1
Environnement et Changement climatique Canada
Santé Canada
Octobre 2020
Sommaire
En vertu de l’article 74 de la Loi canadienne sur la protection de l’environnement (1999) (LCPE), le ministre de l’Environnement et le ministre de la Santé ont procédé à l’évaluation préalable de la 1,3,5-triazine-2,4,6-triamine (NR CAS 108-78-1), communément connue sous le nom de mélamine, une substance appartenant au groupe de certaines substances ignifuges organiques définit dans le cadre du Plan de gestion des produits chimiques du Canada. Ce groupe réunit dix substances organiques ayant une fonction similaire, soit leur utilisation dans des matériaux conçus pour retarder l’inflammation et la propagation du feu. La mélamine a été jugée substance d’intérêt prioritaire pour une évaluation puisqu’elle répondait aux critères de catégorisation définis au paragraphe 73(1) de la LCPE. L’ébauche d’évaluation préalable de la mélamine a été publiée en octobre 2016. Par la suite, de nouveaux renseignements importants concernant l’exposition aux produits de consommation sont devenus disponibles, en particulier les produits en mousse contenant des substances ignifuges (aussi appelées ignifugeants) telles que la mélamine. Le présent document est l’ébauche d’évaluation préalable actualisée en conséquence.
La mélamine n’est pas naturellement présente dans l’environnement. Elle n’est pas fabriquée au Canada. Cependant, on a importé entre 10 et 100 millions de kilogrammes de mélamine pure ou incorporée dans des produits dans le pays en 2011. La mélamine a de nombreuses applications industrielles au Canada. Elle est le plus souvent employée dans la fabrication de mousses de polyuréthane et de résines à base de mélamine servant à la production de stratifiés, de plastiques, de peintures et de revêtements. À l’échelle mondiale, la mélamine est utilisée principalement dans la synthèse de la résine mélamine-formaldéhyde à des fins semblables et dans les adhésifs et les mélanges à mouler. En raison de sa forte teneur en azote, la mélamine est utilisée comme engrais à l’échelle mondiale. Au Canada, les sources d’exposition environnementale à la mélamine sont principalement les flux de déchets ou les effluents d’usines de fabrication de résines à base de mélamine et, à un degré moindre, les usines de traitement qui utilisent la mélamine pour fabriquer des produits ignifugeants. Les rejets dans l’environnement peuvent être directs ou se faire via les systèmes de traitement des eaux usées municipaux.
La mélamine est une molécule compacte et stable caractérisée par une hydrosolubilité élevée, une pression de vapeur négligeable, ainsi qu’un coefficient de partage carbone organique-eau et un coefficient de partage octanol-eau de faible à négligeable. Aucune surveillance de la mélamine dans les milieux environnementaux n’a été effectuée au Canada. Lorsqu’elle est rejetée dans l’environnement, la mélamine devrait résider principalement dans l’eau et, à un degré moindre, dans le sol, selon le milieu où elle est rejetée.
La mélamine ne se dégrade pas rapidement dans l’environnement; elle a une longue demi-vie dans l’air et présente une biodégradation relativement lente dans l’eau et le sol. La mélamine a un potentiel de bioaccumulation limité dans les tissus des organismes. Elle présente de très faibles facteurs de bioconcentration chez les poissons, et l’élimination des résidus mesurée dans de nombreux organismes, dont les mammifères, les poissons et les oiseaux, est rapide.
Selon des preuves empiriques d’études à court et long terme, la mélamine présente une faible toxicité pour les organismes vivant dans l’eau et le sol. Puisque les effets toxiques de l’exposition à la mélamine étaient plus prononcés dans les études à long terme et dans les études portant sur les étapes sensibles du cycle de vie, les résultats de ces types d’études ont été généralement fourni plus de renseignements. Par contre, dans les nombreuses études à court terme, la limite de toxicité pour la mélamine n’a pu être déterminée, car aucun effet n’a été observé lors d’essais à la concentration maximale.
On s’attend à ce des procédés industriels occasionne le rejet de mélamine dans l’environnement au Canada. Bien qu’elle puisse être présente dans les produits de consommation ou des produits à usage commercial, on s’attend à ce que ces produits entraînent des rejets minimes dans l’environnement. Des scénarios basés sur le rejet de mélamine dans l’eau par l’industrie, ont été élaborés aux fins d’estimation de l’exposition. Nous avons réalisé des analyses du quotient de risque, qui intégraient des estimations prudentes de l’exposition aux données sur la toxicité pour le milieu aquatique. Ces analyses ont démontré qu’il est improbable que la mélamine pose un risque pour l’environnement au Canada.
Compte tenu de toutes les sources de données disponibles considérées par la présente ébauche d’évaluation préalable actualisée, la mélamine présente un faible risque pour l’environnement. Il est proposé de conclure que la mélamine ne répond pas aux critères énoncés aux alinéas 64a) ni b) de la LCPE, car elle ne pénètre pas dans l’environnement en une quantité, à une concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, et à mettre en danger l’environnement essentiel pour la vie.
Les produits de consommation, les aliments et les milieux naturels (eau, sol) devraient être les principales sources d’exposition de la population générale au Canada. Des données de biosurveillance provenant de populations pertinentes (États‑Unis) étaient également disponibles.
À la lumière principalement des évaluations réalisées par des organismes internationaux et des données disponibles, les effets critiques associés à l’exposition à la mélamine sont la cancérogénicité et des effets sur le système urinaire. Les données disponibles indiquent que la mélamine n’est pas génotoxique. Pour les nourrissons, les tout-petits et les adolescents (jusqu’à 18 ans), les comparaisons entre les concentrations associées à des effets critiques dans les études sur les animaux et les estimations de l’exposition résultant du fait de se coucher ou de s’asseoir sur des matelas ou des meubles en mousse contenant de la mélamine sont considérées comme potentiellement insuffisantes pour compenser les incertitudes dans les bases de données sur l’exposition et sur les effets sur la santé. Pour tous les autres types d’expositions (milieux naturels, aliments ou utilisation de produits de consommation pour tous les groupes d’âge), les comparaisons entre les concentrations associées aux effets critiques constatés dans des études sur des animaux et les estimations de l’exposition ont été jugées adéquates pour lever les incertitudes dans les bases de données sur l’exposition et sur les effets sur la santé.
Compte tenu de la potentielle inadéquation des marges entre les estimations de l’exposition et les niveaux des effets critiques constatés chez les animaux de laboratoire dans le cadre de la présente mise à jour de l’ébauche d’évaluation préalable, il est proposé de conclure que la mélamine satisfait aux critères de l’alinéa 64c) de la LCPE, car elle pénètre ou peut pénétrer dans l’environnement en une quantité ou à une concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Conclusion proposée
Il est donc proposé de conclure que la mélamine satisfait à un ou plusieurs des critères énoncés à l’article 64 de la LCPE. Il est également proposé que la mélamine satisfait au critère de persistance, mais non au critère de bioaccumulation, au sens du Règlement sur la persistance et la bioaccumulation pris en vertu de la LCPE.
Liste des abbréviations et acronymes
- ACIA
- Agence canadienne d’inspection des aliments
- AESA
- Autorité européenne de sécurité des aliments
- ARLA
- Agence de réglementation de la lutte antiparasitaire
- BGR
- Bureau de la gestion du risque
- CEE
- concentration environnementale estimée
- CIRC
- Centre international de recherche sur le cancer
- CL50
- concentration létale à 50 %
- COD
- carbone organique dissous
- CPLHP
- chromatographie en phase liquide haute performance
- DJA
- dose journalière admissible
- DMENO
- dose minimale entraînant un effet nocif observé
- DR
- dose de référence; dose repère
- DSENO
- dose sans effet nocif observé
- DSEO
- dose sans effet observé
- ECHA
- Agence européenne des produits chimiques
- EFO
- ignifugeants organiques
- FS
- fiches signalétiques
- HPVIS
- High Production Volume Information System (base de données de l’EPA)
- IMC
- indice de connectivité moléculaire
- Koe
- coefficient de partage octanol-eau
- LCPE
- Loi canadienne sur la protection de l’environnement
- LD
- limite de détection
- LIS
- Liste intérieure des substances
- Log D
- coefficient de distribution (habituellement pour l’octanol-eau)
- log Kae
- coefficient de partage air-eau
- log Kco
- coefficient de partage carbone organique-eau
- log Koa
- coefficient de partage octanol-air
- LQ
- limite de quantification
- n.d.
- non disponible
- NGAL
- lipocaline associée à la gélatinase des polynucléaires neutrophiles
- NHANES
- National Health and Nutrition Examination Survey
- OMS
- Organisation mondiale de la Santé
- PGPC
- Plan de gestion des produits chimiques
- pKa
- constante de dissociation acide
- QSAR
- relations quantitatives structure-activité
- s.o.
- sans objet
- SAS
- Systems Analysis Software
- SWISSI
- Swiss Institute of Safety and Security
1. Introduction
En vertu des articles 68 et 74 de la Loi canadienne sur la protection de l’environnement (1999) (LCPE) (Canada, 1999), le ministre de l’Environnement et la ministre la Santé procèdent l’évaluation préalable de substances afin de déterminer si elles présentent ou sont susceptibles de présenter un risque pour l’environnement ou la santé humaine.
L’Initiative des groupes de substances constitue un élément essentiel du Plan de gestion des produits chimiques (PGPC) du gouvernement du Canada. Le groupe de certaines substances ignifuges organiques comprend dix substances dont l’évaluation a été déclarée prioritaire, car elles satisfaisaient aux critères de catégorisation en vertu du paragraphe 73(1) de la LCPE ou étaient considérées comme étant prioritaires en raison de préoccupations relatives à l’environnement ou à la santé humaine (Environnement Canada et Santé Canada, 2013). Toutes ces substances ont un emploi similaire, soit leur application sur des matériaux en vue d’empêcher l’ignition et la propagation du feu. Elles sont de plus des substituts potentiels à d’autres produits ignifuges auxquels des contrôles réglementaires ou à un retrait progressif au Canada ou à l’échelle mondiale ont été imposés.
La présente mise à jour de l’ébauche d’évaluation préalable porte sur la 1,3,5‑triazine-2,4,6‑triamine, communément appelée mélamine. Cette substance a été jugée d’intérêt prioritaire pour une évaluation puisqu’elle répondait aux critères de catégorisation du paragraphe 73(1) de la LCPE. En plus de son utilisation comme produit ignifuge, la mélamine a de nombreuses autres applications (non ignifuges).
Une ébauche d’évaluation préalable de la mélamine a été publiée en octobre 2016 (ECCC, SC 2016). On y proposait que la mélamine ne fût pas nocive pour la santé humaine ou l’environnement. De nouveaux renseignements importants sur l’exposition cutanée aux produits en mousse sont ensuite devenus disponibles à la suite de consultations avec l’Agence européenne des produits chimiques (ECHA) au sujet de son rapport « Screening report – An assessment of whether the use of TCEP, TCPP and TDCP in articles should be restricted », publié en 2018. À la suite de nouvelles consultations avec d’autres instances, l’exposition cutanée aux produits en mousse contenant des ignifugeants tels que la mélamine a été réexaminée et un scénario actualisé a été adopté. À la lumière de ces renseignements, l’ébauche d’évaluation préalable actualisée est présentée dans les pages qui suivent.
La présente ébauche d’évaluation préalable actualisée tient compte des renseignements sur les propriétés chimiques, le devenir dans l’environnement, les dangers, les utilisations et l’exposition, ainsi que des renseignements supplémentaires soumis par les intervenants. Nous avons colligé des données pertinentes jusqu’en mars 2017 pour les composants « écologie » et « santé humaine », et fait des recherches ciblées dans les publications scientifiques jusqu’en mai 2018 pour la composante « santé humaine » de l’évaluation. Toutefois, des études plus récentes ou des renseignements obtenus dans le cadre de consultations internes et externes par des pairs pour les composantes « écologie » et « santé humaine » pourraient également être citées. Nous avons utilisé des données empiriques tirées d’études clés ainsi que certains résultats de modélisation pour tirer les conclusions que nous proposons. Lorsqu’ils étaient disponibles et pertinents, les renseignements contenus dans les évaluations effectuées par d’autres instances ont été utilisés.
La présente mise à jour de l’ébauche d’évaluation préalable a été préparée par le personnel du Programme des substances existantes de Santé Canada et d’Environnement Canada et elle intègre les résultats d’autres programmes exécutés par ces ministères. Les parties de la présente évaluation préalable qui portent sur la santé humaine et l’écologie ont fait l’objet d’un examen externe par écrit par des pairs ou de consultations de ces derniers. M. John Arnot, Ph. D., d’Arnot Research and Consulting, M. Laurence Deydier, Ph. D., de l’Agence européenne des produits chimiques et la Pre Miriam Diamond de l’Université de Toronto, ont fourni des commentaires sur les parties techniques concernant l’environnement. Des commentaires sur les parties techniques liées à la santé humaine ont été fournis par Mme Lynne Haber, Ph. D., de Toxicology Excellence for Risk Assessment, M. Paul Rumsby, Ph. D., du U.S. National Centre for Environmental Toxicology, et Mme Pam William, d’E Risk Sciences. De plus, l’ébauche initiale de l’évaluation préalable avait fait l’objet d’une période de consultations publiques de 60 jours. Certaines parties de l’évaluation portant sur la santé humaine ont fait l’objet de consultations écrites supplémentaires par des pairs de l’extérieur. Ces commentaires ont été reçus de MM. Richard Manderville de l’Université de Guelph, Mohamed Abou-Elwafa Abdallah de l’Université de Birmingham (Royaume-Uni) et Kebede K. Kefeni de la Tshwane University of Technology (Afrique du Sud). À la lumière de ces commentaires ainsi que des nouveaux renseignements reçus, une deuxième version de cette ébauche d’évaluation préalable est présentée ici. Santé Canada et Environnement et Changement climatique Canada ont tenu compte de ces observations externes, mais ces ministères assument l’entière responsabilité du contenu définitif et des conclusions de la présente évaluation préalable.
La présente ébauche d’évaluation préalable actualisée repose sur des renseignements essentiels pour déterminer si les substances satisfont aux critères énoncés à l’article 64 de la LCPE. À cette fin, nous avons examiné les renseignements scientifiques et adopté une approche fondée sur le poids de la preuve et le principe de précautionNote de bas de page 1. Dans le présent document, nous présentons les renseignements essentiels et les facteurs sur lesquels se fonde la conclusion proposée.
2. Identité de la substance
La substance 1,3,5-triazine-2,4,6-triamine (NR°CAS 108-78-1), ci-après désignée par son nom commun, mélamine, est un produit chimique organique défini caractérisé par sa forte teneur en azote. Elle appartient au sous-groupe de produits chimiques connus sous le nom de triazines. Il est à noter que le nom mélamine pour le produit chimique est également communément utilisé pour le plastique fait à partir de ce produit (OMS, c2014).
Les renseignements liés à la mélamine sont résumés dans le tableau 2-1.
| NR CAS | Structure chimique | Masse moléculaire (g/mole) | Formule chimique |
|---|---|---|---|
| 108-78-1 | 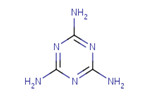 | 126.12 | C3H6N6 |
3. Propriétés physiques et chimiques
Le tableau 3-1 résume les propriétés physiques et chimiques (valeurs expérimentales et modélisées) de la mélamine qui se rapportent à son devenir dans l’environnement et à sa toxicité.
Les données empiriques sur les propriétés physico‑chimiques proviennent de publications scientifiques (Hirt et coll. 1960), de manuels de chimie (Crews et coll. c2012; Rumble 2018) et d’autres sources, y compris des résumés d’études non publiées figurant dans des bases de données compilées par d’autres instances (ECHA c2007-2013). Les modèles fondés sur les relations quantitatives structure-activité (QSAR) ont aussi été utilisés pour générer des données pour certaines des propriétés physiques et chimiques de la substance. La plupart de ces modèles s’appuient sur la forme neutre d’un produit chimique comme donnée d’entrée (forme SMILES : c1(nc(nc(n1)N)N)N). Par conséquent, sauf dans les cas indiqués, les valeurs modélisées présentées dans le tableau 3‑1 concernent la forme neutre de la substance. En général, une très bonne corrélation a été obtenue entre les valeurs empiriques et modélisées des propriétés physiques et chimiques.
La mélamine est une fine poudre cristalline blanche inodore à la température de la pièce (BASF, 2012; ECHA c2007-2013). Elle est très soluble dans l’eau (Yalkowsky et He, 2003; Crews et coll., c2012; ECHA c2007-2013) et dans l’éthanol (Rumble 2018). La mélamine a une très faible pression de vapeur (~ 10‑9 à 10-7 Pa à la température ambiante) (Hirt et coll. 1960; ECHA c2007-2013), et sa constante de la loi d’Henry calculée est de ~ 10-9 Pa·m3/mol (EPI Suite 2012). Les valeurs empiriques et modélisées du log Koe pour la mélamine sont faibles entre -1,37 et -0,38, respectivement (Hansch et coll., 1995; ECHA c2007-2013; KOWWIN 2010; ECHA c2007-2013). Les valeurs modélisées du log Kco étaient faibles, à savoir 1,5 (d’après la méthode d’estimation selon l’ICM) et -0,0 (d’après la méthode d’estimation du Koe), respectivement (EPI Suite, 2012). La mélamine est une base organique. Deux études caractérisant le potentiel d’ionisation de la mélamine ont été trouvées (Weber 1970; SWISSI 2009). Un pKa de 7,3 présenté dans le rapport du SWISSI (2009) indique que la mélamine pourrait s’ioniser dans une certaine mesure à des pH supérieurs à 7 mais pertinents pour l’environnement, alors que selon Weber (1970), avec un pKa de 5, la mélamine ne devrait pas s’ioniser sensiblement aux pH typiques de l’environnement (pH 6 à 9). En raison des détails expérimentaux limités, il n’a pas été possible de réaliser une évaluation de la fiabilité pour ces études de pKa. Toutefois, les résultats de la modélisation qui indiquent un pKa de 5 pour la mélamine appuient la conclusion selon laquelle la substance existe essentiellement sous forme de produit chimique neutre avec un pH de 6 à 9 (ACD/Percepta, 2005). Les valeurs modélisées de log D ne variaient pas selon le pH, et étaient d’environ -1,2 pour des niveaux de pH variant de 6,5 à 8 (ACD/Percepta, 2005). De plus, les données sur la toxicité pour les mammifères indiquent que la mélamine est neutre à des niveaux de pH physiologiques (voir la section sur la santé humaine). Bien que les données empiriques et modélisées indiquent que la mélamine existe sous la forme neutre et ionisée à un pH pertinent sur le plan environnemental, le poids de la preuve disponible suggère que la mélamine existe essentiellement (> ~ 90 %) sous la forme neutre à des niveaux de pH environnementaux normaux.
Propriété |
Type |
Valeur a |
Température (°C) |
Référence |
|---|---|---|---|---|
Forme physique |
Expérimental |
Solide, poudre blanche inodore |
Température ambiante |
Température ambiante BASF, 2012; ECHA c2007-2013 |
Point de fusion (ºC) |
Expérimental |
345*-361 |
s.o. |
ChemID plus 1993–; Rumble 2018; BASF 2012 |
Point de fusion (ºC) |
Modélisé |
133 |
s.o. |
MPBPVP, 2010 11 |
Point d’ébullition (ºC) |
Expérimental |
La substance se décompose avant de bouillir. |
s.o. |
BASF. 2012 |
Masse volumique (kg/m³) |
Expérimental |
1,57 |
20 |
AEPC c2007-2013 |
Pression de vapeur (Pa) |
Expérimental |
7,5 × 10-9; 4,75 × 10–8* (3,56 × 10–10 mm Hg) |
20 |
Hirt et coll., 1960; 1960; ECHA c2007-2013 |
Pression de vapeur (Pa) |
Expérimental |
9,4 × 10-8; 1,1 × 10‑7 |
25 |
Hirt et coll., 1960; Crew et coll. c2012 |
Constante de la loi d’Henry (Pa m³/mol) |
Modélisé |
1,86 × 10-9 (pression de vapeur et hydrosolubilité estimées) | 25 |
HENRYWIN, 2010 |
Log Koe (sans dimension) |
Expérimental |
-1,14* |
25 |
AEPC c2007‑2013 |
Log Koe (sans dimension) |
Expérimental |
-1,22 |
22 |
SWISSI, 2009; ECHA c2007-2013 |
Log Koe (sans dimension) |
Expérimental |
-1,37 |
s.o. |
Hansch et coll. 1995 |
Log Koe (sans dimension) |
Modélisé |
-0,38 |
s.o. |
KOWWIN, 2010 |
Log Kco (sans dimension) |
Modélisé |
1,5* (méthode d’estimation selon l’ICM) 0 (méthode d’estimation du Koe) |
s.o. |
KOCWIN, 2010 |
Log D |
Modélisé |
-1,22 à -1,18 (à un pH de 6,5 à 8,0) | s.o. |
ACD/ Percepta, 2005 Percepta 2005 |
Log Koa (sans dimension) |
Modélisé |
10,8 |
s.o. |
KOAWIN, 2010 |
Solubilité dans l’eau (mg/L) |
Expérimental |
3190, 3230*,3480 |
20 |
Crews et coll., c2012; Yalkowsky et He, 2003; ECHA c2007-2013; SWISSI, 2009 |
Solubilité dans l’eau (mg/L) |
Expérimental |
4 850 |
25 |
AEPC c2007‑2013 |
pKa (sans dimension) |
Expérimental |
5 |
25 |
Weber 1970 |
pKa (sans dimension) |
Expérimental |
pKa(base)1 = 7,3 pKa(base)2 = 11,4 |
n.d. |
SWISSI, 2009 |
pKa (sans dimension) |
Modélisé |
pKa(base) = 5,3 |
n.d. |
ACD/Percepta, 2005 Percepta 2005 |
Abréviations : log Koe : coefficient de partage octanol-eau; log Kco : coefficient de partage carbone organique-eau; log Kae : coefficient de partage air-eau; log Koa : coefficient de partage octanol-air; Log D : coefficient de distribution (habituellement pour l’octanol-eau); pKa : constante de dissociation acide; n.d. : non disponible; s.o. : sans objet; ICM : indice de connectivité moléculaire.
a Les valeurs entre parenthèses représentent les valeurs originales rapportées par les auteurs ou estimées par les modèles.
* Valeur choisie pour la modélisation.
4. Sources et utilisations
La mélamine n’est pas naturellement présente dans l’environnement. Elle peut être produite à partir d’urée, de dicyandiamide ou de cyanure d’hydrogène. L’industrie synthétise la mélamine à partir d’urée (OMS, 2009).
Une enquête menée en vertu de l’article 71 de la LCPE [1999] (Canada, 2013) et les renseignements communiqués par des parties prenantes volontaires nous indiquent qu’en 2011, entre 10 et 100 millions de kilogrammes de mélamine ont été importés au Canada (ECCC 2013-2014). On n’a pas synthétisé au Canada, de mélamine en quantités excédant le seuil de déclaration de 100 kg (ECCC 2013-2014).
Les quantités de mélamine importées au Canada étaient d’environ 13 millions de kilogrammes en 2011 selon la base de données sur le Commerce international canadien de marchandises (Statistiques Canada, 2019).
En 2007, la production mondiale de mélamine était d’environ 1,2 milliard de kilogrammes (1,2 million de tonnes). Les principaux producteurs étaient situés en Chine et en Europe occidentale (OMS, 2009). Aux États-Unis, 80 millions de kg par année sont produits et en 2011-2012, environ 1,5 à 1,6 million kg/année (1 500 à 1 600 tonnes/année) ont été importés (ICIS, c2014). Toutefois, la substance n’apparaît pas dans la base de données High Production Volume Information System de l’EPA (HPVIS) (USEPA, 2007). Dans les pays nordiques, 12,5 millions de kg de mélamine ont été utilisés en 2011, alors que les quantités rapportées entre 1999 et 2010 étaient inférieures, variant entre 4,7 millions et 10,6 millions de kg (SPIN, c2014).
Les utilisations de la mélamine sont variées et touchent de nombreux secteurs industriels, autant à l’échelle mondiale qu’au Canada. Les utilisations et applications connues de la mélamine, incluant les cas d’altération des denrées pour consommation humaine et animale, sont résumées plus bas.
Au Canada, selon les résultats de l’enquête menée en vertu de l’article 71 pour l’année 2011 et des renseignements obtenus dans le cadre de la participation volontaire de parties prenantes (ECCC 2013-2014), la mélamine est utilisée dans les peintures et revêtements commerciaux et grand public, dans les sièges et la literie en mousse (qui peuvent comprendre des produits tels que des oreillers et des matelas), et dans la résine de mélamine-formaldéhyde utilisée pour les stratifiés décoratifs (ECCC 2013-2014). La substance était également utilisée comme produit ignifuge au Canada (ECCC 2013-2014). De plus, la mélamine a des applications en tant que plastifiant dans le béton et dans les canalisations des systèmes de freins automobiles (ECCC 2013-2014). Une recherche en ligne des produits canadiens a également démontré l’usage de la substance dans le papier et les tablettes de mélamine thermofusionnés, les tableaux blancs et les panneaux de flocons, les peintures, les scellants pour les applications mécaniques, électriques et de plomberie, et dans l’encre pour impression à jet d’encre (Home Depot Canada, 2014; Home Hardware, 2014; Formica Corporation, 2013; Grand and Toy, 2014; Flakeboard Company Ltd., 2014; CSL Silicones Inc., 2014; BASF, 2014; C2012 CSL Silicones Inc. 2014; MSDS 2014). À l’échelle mondiale, la mélamine est surtout utilisée dans la synthèse des résines de mélamine–formaldéhyde pour la fabrication des stratifiés (p. ex., pour les comptoirs de cuisine, les dessus de table), les plastiques, les revêtements, les filtres commerciaux, les produits de consommation tels que les colles ou les adhésifs, et les composés de moulage pour les articles en mélamine (vaisselle et ustensiles de cuisine) (OMS 2009; Scorecard c2011).
Selon les résultats de l’enquête menée en vertu de l’article 71 de la LCPE (1999), environ 4 % de toute la mélamine importée au Canada en 2011 a été utilisé comme ignifugeant (ECCC 2013-2014), ce qui correspond à ce qui a été observé à l’échelle mondiale. La mélamine est utilisée comme ignifugeant principalement dans les mousses en polyuréthane (EFRA, 2007). La mélamine est souvent utilisée en combinaison avec de nombreux autres ignifugeants comme le phosphate bicyclique, le décabromodiphényléther (décaBDE), l’oxyde d’antimoine, le Déchlorane Plus (DP), etc., ainsi que dans les préparations de polyoléfines utilisées dans les plastiques et les élastomères, pour améliorer la capacité ignifuge générale du produit final (Weil et Choudhary, 1995). La mélamine est aussi utilisée dans la production d’autres ignifugeants, comme le cyanurate de mélamine (NR°CAS 37640-57-6), le phosphate de mélamine (NR°CAS 20208-95-1), le polyphosphate de mélamine (NR°CAS 218768-84-4), et le pyrophosphate de mélamine (NR°CAS 15541-60-3) [EFRA, 2007].
D’autres utilisations à l’échelle mondiale de la mélamine comprennent son application comme résine d’imprégnation ou adhésive dans les panneaux à base de bois pour les meubles et les planchers, ainsi que dans le papier-monnaie, les magazines glacés et les textiles (DSM, 2010).
La mélamine est utilisée en agriculture. En raison de sa teneur élevée en azote, la mélamine a été testée et utilisée comme engrais à libération lente (Wehner et Martin, 1989; OMS, 2009). De plus, la mélamine est aussi un sous-produit de la cyromazine (un insecticide), qui est un inhibiteur de croissance des insectes qui peut être appliqué en aérosol ou dans les aliments de bétail (Roberts et Hudson, 1999; Zhu et coll., 2009). Au Canada, la cyromazine est homologuée pour une utilisation dans les produits antiparasitaires contre le doryphore de la pomme de terre dans les cultures de pommes de terre et contre les insectes dans les cultures en serre (Santé Canada, 2012).
La mélamine ne figure pas en tant qu’additif alimentaire approuvé dans la Liste des additifs alimentaires autorisés publiée en vertu de la Loi sur les aliments et drogues (Santé Canada [modifiée en 2017]). Les répondants à l’enquête menée en vertu de l’article 71 de la LCPE n’ont pas signalé d’utilisations de la mélamine dans les matériaux qui entrent en contact avec les aliments (ECCC 2013-2014), mais la mélamine peut être présente dans divers produits d’emballage alimentaire au Canada (p. ex., revêtement intérieur des boîtes de conserve, à l’exception des préparations pour nourrissons; le revêtement des fermetures métalliques des pots en verre pour aliments pour bébé; les bouteilles en verre et en plastique pour les préparations liquides pour nourrissons; le papier utilisé pour emballer le pain ou la margarine; les pellicules pour l’emballage du lait) (communication personnelle de la Direction des aliments au Bureau de gestion du risque (BGR), Santé Canada; août 2013; source non citée). Selon les notifications soumises aux termes du Règlement sur les cosmétiques à Santé Canada, la mélamine n’est pas utilisée dans les produits cosmétiques au Canada (courriel de la Direction de la sécurité des produits de consommation de Santé Canada, au Bureau de l’évaluation des risques des substances existantes de Santé Canada en juillet 2013; source non citée).
En Europe, la mélamine sous forme monomérique est approuvée pour la fabrication de résines pour les applications d’emballage alimentaire destiné à entrer en contact avec les aliments, avec une limite de migration fixée à 2,5 mg/kg aliments (UE 2011). Aux États-Unis, la mélamine et le copolymère de mélamine-formaldéhyde peuvent être utilisés dans la préparation d’adhésifs pouvant entrer dans la composition d’articles destinés à emballer, à transporter ou à contenir des aliments (additif alimentaire indirect), à condition que l’adhésif soit séparé de l’aliment par une barrière fonctionnelle (US eCFR, 2014a). En outre, la résine ou le polymère de mélamine-formaldéhyde peut être utilisé comme revêtement des surfaces qui sont en contact avec les aliments (additif alimentaire indirect) dans le cas des articles destinés à produire, fabriquer, emballer, traiter, préparer, transporter ou contenir des aliments (US eCFR, 2014b).
Au Canada, la mélamine ne figure pas dans la Base de données sur les produits pharmaceutiques (BDPP) ni dans la base de données interne sur les ingrédients non médicinaux de la Direction des produits thérapeutiques à titre d’ingrédient médicinal ou non médicinal présent dans des produits pharmaceutiques finaux ou des médicaments vétérinaires (BDPP, [modifiée en 2017]; courriel adressé en juillet 2013 par la Direction des produits thérapeutiques de Santé Canada au Bureau de gestion du risque de Santé Canada, source non citée). La mélamine figure dans la Base de données sur les ingrédients des produits de santé naturels en tant que produit de santé non naturel parce qu’elle n’est pas une substance d’origine naturelle figurant à l’annexe 1 du Règlement sur les produits de santé naturels. Par conséquent, elle ne figure pas dans la Base de données sur les produits de santé naturels homologués comme étant présente dans les produits de santé naturels actuellement homologués au Canada (BDIPSN [modifiée en 2017]; BDPSNH [modifiée en 2016]).
À la suite de la découverte d’un aliment pour animaux de compagnie altéré par la mélamine aux États-Unis en 2007, et d’une préparation pour nourrissons altérée par la mélamine en Chine en 2008, des normes ont été élaborées à l’échelle internationale pour assurer la sécurité des consommateurs et faire la différence entre la présence de concentrations ambiantes de la mélamine dans les aliments et une altération intentionnelle (Santé Canada 2008, 2016a; Codex Alimentarius 2018). Au Canada, des concentrations maximales provisoires pour la mélamine ont été fixées à 0,5 mg/kg pour les préparations pour nourrissons et les produits nutritionnels de source unique, y compris les produits de substitution pour les repas, et à 2,5 mg/kg dans les produits alimentaires contenant du lait et des ingrédients dérivés du lait (Santé Canada 2016a; 2018a). Ces concentrations maximales provisoires s’appliquent à la présence de la mélamine et de l’acide cyanurique, souvent présents ensemble, afin de garantir que les aliments disponibles à la vente au Canada n’ont pas été délibérément altérés par l’un ou l’autre de ces composés (Santé Canada 2016a, 2018a).
5. Rejets dans l’environnement
La mélamine a de nombreuses utilisations industrielles et est utilisée en grandes quantités au Canada et partout dans le monde (Du et coll., 2010).
Les rejets dans l’environnement sont dus aux différentes pertes qui surviennent pendant la fabrication, l’utilisation industrielle, l’utilisation commerciale ou par les consommateurs, pendant la durée de vie utile des produits en contenant et lors de l’élimination de la substance. Les rejets potentiels devraient se produire principalement lors de la manipulation de la mélamine lorsqu’elle est ajoutée, en tant que substance pure, et lors des procédés industriels pour fabriquer les produits souhaités tels que les résines de mélamine. Ces rejets devraient principalement être causés par des émissions diffuses (fugitives) dans les installations industrielles pendant les opérations de chargement et de déchargement, la manutention ou le nettoyage de l’équipement de traitement ainsi que le transport et l’entreposage des conteneurs. On s’attend à ce que 0,6 % de la quantité totale de mélamine utilisée puisse être rejetée dans les eaux usées (OCDE, 2002).
Il est plus probable que les rejets de mélamine dans l’environnement surviennent au cours de la fabrication, de la formulation ou de l’utilisation industrielle, et non lorsque la substance est déjà incorporée dans certains produits. Les rejets de mélamine dans l’environnement canadien provenant de l’utilisation et de l’élimination de produits (commerciaux ou de consommation) ou d’articles manufacturés contenant de la mélamine devraient être diffus.
Les rejets dans l’environnement devraient être surtout occasionnés par les eaux usées. Des rejets dans le sol peuvent également se produire pendant l’épandage de boues d’épuration sous forme de biosolides sur les terres agricoles et les pâturages, mais ils devraient être minimes en raison de la propension limitée de la mélamine à se répartir dans les solides (voir la section 6).
La mélamine peut aussi être rejetée dans l’environnement lors d’applications agricoles du cyromazine, dont l’utilisation comme pesticide est approuvée au Canada. Il se transforme en mélamine dans le sol (métabolite important), les plantes (métabolite mineur) et les animaux (métabolite mineur) (FAO, 2007a, b). Une réévaluation des risques posés par la cyromazine pour l’environnement et la santé humaine est prévue par l’Agence de réglementation de la lutte antiparasitaire (ARLA) de Santé Canada (Santé Canada 2016b, 2018b).
Ces renseignements sont utilisés dans la création de scénarios de caractérisation de l’exposition pour estimer les concentrations qu’elle produit dans l’environnement.
6. Devenir et comportement dans l’environnement
6.1 Distribution dans l’environnement
D’après ses applications industrielles connues au Canada (ECCC 2013-2014), la mélamine devrait principalement être rejetée dans les eaux usées. En raison de son Kco peu élevé et de sa grande hydrosolubilité, la mélamine est peu susceptible d’être efficacement éliminée par adsorption dans les boues de stations de traitement des eaux usées. Le nouveau modèle EQC (2011) de modélisation de la fugacité de niveau III a été appliqué pour prévoir le devenir de la mélamine.
Les résultats généraux de la modélisation de la fugacité de niveau III indiquent que lorsque la mélamine est rejetée dans l’environnement, elle devrait résider surtout dans l’eau et le sol, selon le milieu de rejet (Tableau 6‑1).
Substance rejetée dans : |
Air (%) |
Eau (%) |
Sol (%) |
Sédiments(%) |
|---|---|---|---|---|
Air (100 %) |
Négligeable |
27 |
73 |
Négligeable |
Eau (100 %) |
Négligeable |
99,6 |
Négligeable |
0,4 |
Sol (100 %) |
Négligeable |
18 |
82 |
Négligeable |
Lorsque la mélamine est rejetée dans l’air, elle devrait se répartir rapidement sous forme de particules dans l’atmosphère en raison de son Koa estimé très élevé et, par conséquent, la mélamine ne devrait pas résider dans l’air. Les particules se déposent sur le sol et sur l’eau sous forme de dépôts humides et secs. De la quantité transférée depuis l’air, la majeure partie (plus de 70 %) restera dans le sol et près de 30 % se retrouvera dans l’eau.
Lorsque la mélamine est rejetée dans les eaux de surface, elle devrait résider principalement dans l’eau en raison de son hydrosolubilité élevée. On pourrait également trouver de la mélamine dans l’eau interstitielle des sédiments en raison de son hydrosolubilité élevée.
La volatilisation à partir de l’eau de surface dans l’air devrait être très lente puisque la mélamine a une pression de vapeur négligeable et une constante de la loi d’Henry très peu élevée. Somme toute, les risques de perte de mélamine par advection dans les systèmes aqueux sont limités.
La mélamine a une très faible valeur de Koe, ce qui indique un faible potentiel de sorption dans le sol et les sédiments. Toutefois, comme la mélamine est plus dense que l’eau, elle peut, jusqu’à un certain point, se déposer sur les sédiments. Lorsqu’elle est rejetée dans le sol (p. ex., lors de l’application de biosolides sur les terres agricoles), la mélamine devrait être adsorbée et s’écouler dans les systèmes aqueux. Elle ne devrait pas s’évaporer puisqu’elle est relativement non volatile.
En résumé, d’après les résultats du modèle de fugacité et des propriétés physiques et chimiques de la mélamine, celle-ci devrait principalement résider dans l’eau et le sol, et dans l’eau interstitielle des sédiments. Par conséquent, il est possible que les organismes aquatiques, benthiques et du sol y soient exposés. Aucune exposition par inhalation des organismes terrestres n’est prévue, en raison des faibles concentrations de mélamine dans l’air.
6.1.1 Potentiel de transport sur de grandes distances
Nous ne disposons pas de données de surveillance de la mélamine dans les régions éloignées (p. ex., les régions polaires).
On a déterminé que la mélamine avait de longues demi-vies dans l’air et dans l’eau. Cependant, la mélamine devrait être présente en très faibles concentrations dans l’air et on ne s’attend pas à des rejets de mélamine dans l’air d’après les utilisations connues de cette substance (voir la section Sources et utilisations). En raison de sa très haute hydrosolubilité, ainsi que de sa pression de vapeur et de sa constante de la loi d’Henry négligeables, les taux de volatilisation dans l’air à partir des eaux de surface seront probablement très faibles. Les résultats du modèle de l’outil de dépistage Pov – LRTP de l’Organisation de coopération et de développement économiques (OCDE, 2009) ont confirmé que la mélamine ne se trouvera pas dans l’air à la suite d’émissions provenant depuis les eaux de surface. Le transport à grande distance dans les milieux aquatiques est plausible compte tenu des caractéristiques de la substance et des profils de rejets et d’émissions. Le modèle TaPL3 (2003) et l’outil de dépistage Pov – LRTP (OCDE, 2009) donnent respectivement des distances de parcours caractéristiques de la mélamine dans l’eau de 120 000 km et de 2 300 km. Il convient de noter que ces distances de parcours caractéristiques ne doivent pas être interprétées comme la distance absolue pouvant être parcourue par la substance, mais plutôt comme une indication de son déplacement possible relativement long dans l’eau.
6.2 Persistance dans l’environnement
Les données empiriques et modélisées ont été prises en compte dans la détermination du potentiel de dégradation de la mélamine dans l’environnement.
La mélamine est produite à partir d’un procédé de condensation de l’urée. On peut la faire réagir avec un nombre considérable de dérivés organiques et inorganiques, comme le formaldéhyde, et créer ainsi des produits extrêmement stables. Il existe pour ceux-ci un large éventail d’utilisations industrielles et une grande variété d’emplois comme composant de produits de consommation (Ramusino et Vailati, 1982). Les utilisations industrielles de la mélamine révélées par l’enquête effectuée en vertu de l’article 71 de la LCPE [1999] (ECCC 2013-2014) laissent à penser que l’eau sera le principal milieu récepteur de la mélamine présente dans les effluents.
Une voie de biodégradation catabolique de la mélamine a été élucidée grâce à l’utilisation de souches bactériennes, à savoir Pseudomonas, Klebissiela pneumonia et Rhodococcus corallines, isolées du sol. La métabolisation de la mélamine fournit une source d’azote pour la croissance bactérienne. Cependant, la métabolisation de la mélamine est généralement lente (Shelton et coll. 1997). Dans le cadre d’une étude in vitro, Wang et coll. (2014) ont observé qu’une nouvelle souche de la bactérie CY1, étroitement liée à la β‑protéobactérie Alicycliphilus denitrificans, isolée dans des boues d’usines de fabrication de mélamine, était capable de biodégrader rapidement et complétement la mélamine.
La mélamine est métabolisée à partir de trois réactions d’hydrolyse consécutives de désamination formant tout d’abord l’amméline, puis l’ammélide et résultant en acide cyanurique (Wackett et coll. 2002; Shelton et coll. 1997). Cela a été attribué à la présence de gènes spécifiques codés par des plasmides, qui codent des enzymes dégradant la mélamine (Karns et Eaton 1997; Wackett et coll. 2002; Takagi et coll. 2012; Hatakeyama et coll. 2015). Dans les extraits exempts de cellules, il a été démontré que l’acide cyanurique subit un métabolisme supplémentaire pour devenir du biuret, de l’urée et de l’ammoniac (Cook et coll. 1985). Le métabolisme de la mélamine fournit une source d’azote pour la croissance bactérienne. Toutefois le métabolisme de la mélamine est généralement lent (Shelton et coll., 1997). On a détecté la formation d’un précipité complexe de cyanurate de mélamine, en plus des produits intermédiaires de dégradation de la mélamine (amméline, ammélide, acide cyanurique, biuret, allophanate et urée), au cours des essais de biodégradation avec la souche bactérienne CY1 (Wang et coll., 2014).
Les renseignements disponibles sur le potentiel de dégradation et de persistance de la mélamine sont classés et présentés selon les milieux naturels (c.-à-d. l’air, l’eau, le sol et les sédiments). Les données empiriques sur la biodégradation sont résumées dans le tableau 6-2, et les données modélisées sur la dégradation sont présentées à l’annexe A.
6.2.1 Air
Aucune donnée empirique portant sur le potentiel de dégradation de la mélamine dans l’air n’était disponible. Les résultats modélisés fondés sur le modèle QSAR disponible (AOPWIN, 2010) ont indiqué une demi-vie dans l’air de 16,2 jours. On s’attend par conséquent à ce que la substance ne soit pas rapidement dégradée par la réaction avec les radicaux hydroxyles présents dans l’atmosphère. La demi-vie résultant de la réaction avec l’ozone n’a pu être modélisée comme le modèle AOPWIN (2010) ne fournit pas d’estimations pour cette classe de produits chimiques. En général, la mélamine ne se dégrade pas immédiatement dans l’air et il est peu probable que la mélamine y demeure à des concentrations élevées. Les données modélisées pour l’air sont résumées à l’annexe A.
6.2.2 Eau
Dans le cas de l’eau, la dégradation par hydrolyse, la biodégradation par les microorganismes présents dans les boues et la biodégradation modélisée sont discutées ci-dessous.
6.2.2.1 Hydrolyse
La mélamine ne subit pas d’hydrolyse dans des conditions pertinentes pour l’environnement (ECHA c2007-2013). Par contre, la mélamine s’hydrolyse dans des conditions catalysées par des solutions fortement alcalines et acides comme les acides minéraux et les alcalis inorganiques (Crews et coll., 2005). Ce processus se fait par étapes, soit la perte du premier, du deuxième et du troisième groupe amines, pour produire successivement l’amméline, l’ammélide et l’acide cyanurique. La proportion de produits de réaction peut varier selon la température, la concentration et le pH (Crews et coll., 2005). Les constantes d’hydrolyse de la mélamine ont été mesurées à 100 °C et sont de 3,80 × 10-5 (OH-) et de 1,25 × 10-4 (H+) (ECHA c2007-2013).
6.2.2.2 Biodégradation par les microorganismes présents dans les boues
Plusieurs études sur la biodégradation immédiate et intrinsèque ont été menées à l’aide de boues activées et, dans certaines études, à l’aide de boues activées préadaptées, pour déterminer le potentiel de biodégradation de la mélamine dans l’eau.
Xu et coll. (2013) ont étudié la biodégradation de la mélamine à l’aide de boues activées pour deux procédés de traitement communs : le procédé Ludzack-Ettinger modifié (LEM) qui est caractérisé par des conditions anoxiques et aérobies, et le procédé par réacteur à cuve agitée en continu dans des conditions aérobies. La biodégradation de la mélamine a été observée pendant 225 jours; au 125e jour de l’étude, la concentration de mélamine dans les influents est passée à 3 mg/L. La mélamine a démontré un potentiel limité de biodégradation par les microorganismes présents dans les boues, même après l’exposition prolongée de 100 jours à 3 mg/L de mélamine qui aurait pu susciter une adaptation. Les taux d’élimination moyens avec les procédés LEM et par réacteur à cuve agitée en continu étaient semblables, soit 20 ± 15 % et 14 ± 10 % respectivement, indiquant que des conditions anoxiques et aérobies et des conditions purement aérobies n’ont pas eu d’incidence sur la biodégradation de la mélamine. Par conséquent, il est probable que les enzymes responsables de la désamination hydrolytique de la mélamine ne soient pas rapidement inhibés dans les procédés avec boues activées. À une concentration de mélamine plus élevée de 75 mg/L, on a observé une diminution de l’activité des bactéries nitrifiantes de 92 % ± 5 % dans le procédé LEM et de 82 ± 8 % dans le procédé avec réacteur à cuve agitée en continu, ainsi qu’une diminution des populations bactériennes. An et coll. (2017) ont démontré une réduction de l’efficacité de l’élimination dans une étude sur les systèmes de traitement des eaux usées, dans lesquels l’efficacité d’élimination de l’azote avait fléchi de 94 % à 79 % et à 68 % en présence de 1,0 et de 5,0 mg/L de mélamine, respectivement. An et coll. (2017) ont observé que l’élimination était principalement obtenue par adsorption de boues activées plutôt que par biodégradation. Ces résultats semblent indiquer que la mélamine peut inhiber la croissance bactérienne des boues activées lorsqu’elle est présente à des concentrations élevées.
Des études antérieures par Heukelekian et Rand (1955) et par Niemi et coll. (1987) ont porté sur la biodégradation de la mélamine en fonction de la demande biologique en oxygène (DBO). Dans ces articles, ils ont compilé les données publiées et non publiées sur les différentes classes de produits chimiques. Les résultats des études étaient présentés sous forme de tableau et les descriptions de la méthode utilisée se limitaient aux données générales sur les protocoles de l’étude ou les conditions expérimentales. Heukelekian et Rand (1955) ont présenté deux résultats sur la demande biologique en oxygène pour la mélamine, originalement publiés par Swope et coll. (1950), qui indiquaient une DBO de 0 g/g et 0,006 g/g, dans des eaux usées et après 5 jours d’incubation. À l’aide de boues activées acclimatées et sur une période de 5 jours, Niemi et coll. ont testé à nouveau le résultat d’une étude de 1984 indiquant une DBO de 1 % après une exposition de 5 jours de la mélamine à des boues activées (l’acclimatation n’a pas été observée) (Vaishnav, 1984). Les nouveaux résultats ont indiqué une DBO de 0 % et ont permis de vérifier les résultats précédents. Les résultats des tests décrits par Heukelekian et Rand (1955) et par Niemi et coll. (1987) indiquent que la mélamine a un potentiel de biodégradation lente.
On a résumé deux études non publiées réalisées par l’industrie pour le Règlement REACH (enregistrement, évaluation, autorisation et restriction des substances chimiques) de l’Union européenne. De plus l’ECHA (c2007-2013) a rendu disponibles des résumés d’études. Les résumés de deux études sur la biodégradation intrinsèque menées en 1991 et en 1993, et fondées sur le protocole 302B de l’OCDE étaient disponibles. Dans l’étude de 1991, des boues activées et des boues préadaptées provenant d’une usine de traitement des eaux usées ont été utilisées pour tester la mélamine à une concentration de 1000 mg/L (1 g/L). Les résultats d’essais sur des boues activées ont indiqué une élimination du carbone organique dissous (COD) de 16 % sur une période de 20 jours, alors qu’une élimination du COD de 10 % a été observée dans le test fait à l’aide d’inoculum adapté sur une période de 14 jours. Dans l’étude de 1993, la mélamine a été testée deux fois à une concentration de 100 mg/L à l’aide de boues activées. Après 28 jours, les deux tests ont démontré une élimination du COD de 0 % et de moins de 10 %. De plus, les résultats d’une étude de biodégradation rapide menée selon le protocole 301C de l’OCDE (ECHA c2007-2013) ont été résumés dans MITI (1992). Les résultats de cette étude indiquaient une biodégradation de la DBO de 0 %, pour 100 mg/L de mélamine sur plus de deux semaines (MITI 1992).
Dans le cadre de sa thèse de maîtrise à l’université de Salzbourg (Autriche), Fimberger (1997) a étudié la biodégradation de la mélamine dans l’eau dans des conditions variées selon un protocole de type Zahn-Wellens. Les principaux résultats de cette recherche ont été résumés dans ECHA (c2007‑2013) et OCDE (2002). La mélamine a été testée à 20 mg/L sur une période de 28 jours. Les résultats n’indiquent aucune biodégradation inhérente à l’aide de boues activées provenant d’un système de traitement des eaux usées (STEU) municipal. Une certaine biodégradation a été observée après la modification des conditions de l’étude par l’ajout de glucose. Toutefois, l’ajout d’ammoniac a inhibé la biodégradation favorisée par le glucose. Fimberger (1997) a observé que la mélamine se dissociait rapidement dans la boue provenant d’un STEU industriel où de la mélamine était produite, et qu’elle avait complètement disparu après 8 heures. Karns et Eaton (1997), Shelton et coll. (1997), et Wackett et coll. (2002) ont observé que la biodégradation s’était produite par désamination hydrolytique, produisant du dioxyde de carbone, qui est la voie présentée dans d’autres études qui avaient exploré la dégradation microbienne de la mélamine
Au cours d’une étude in vitro, on a constaté qu’une nouvelle espèce de la bactérie CY1, isolée depuis les boues d’une usine de fabrication de mélamine en Chine, pouvait dégrader complètement la mélamine. La concentration d’essai était d’environ 500 mg/L. Pendant les 24 premières heures, la bactérie CY1 a dégradé environ 64 % de la mélamine et environ 94 % s’étaient dégradées en 10 jours (Wang et coll., 2014).
Le tableau 6‑2 résume des études empiriques.
Processus de devenir |
Paramètre / unités de dégradation |
Valeur pour la dégradation |
Référence |
|---|---|---|---|
Biodégradation immédiate (aérobie) |
% DBO (5 jours) |
0; 1 |
Niemi et coll. 1987 |
Biodégradation immédiate (aérobie) |
DBO (g/g) (5 jours) |
0; 0,006 |
Heukelekian et Rand, 1955 |
Biodégradation intrinsèque (aérobie) |
% COD (28 jours) |
0; < 10 |
ECHA, 2007‑2013 |
Biodégradation intrinsèque (aérobie) |
% COD (20 jours) % COD (14 jours) |
16 10 (inoculum préadapté) |
ECHA, 2007‑2013 |
Biodégradation immédiate (aérobie) |
% DBO (14 jours) |
0 |
MITI, 1992 |
Biodégradation intrinsèque (aérobie) |
% DBO (28 jours) |
0 (boues d’un STEU municipal) |
Fimberger, 1997 |
Abréviations : DBO, demande biologique en oxygène; COD, carbone organique dissous; STEU, système de traitement des eaux usées.
En résumé, le mécanisme de biodégradation de la mélamine se fait par étapes, d’abord par la désamination hydrolytique, produisant de l’acide cyanurique, puis par le clivage de cycles pour aboutir à deux produits finaux, soit l’ammoniac et le dioxyde de carbone. Les études sur la biodégradation immédiate et intrinsèque indiquent que la biodégradation de la mélamine dans l’eau est lente. À la suite d’une exposition continue aux conditions découlant du traitement industriel d’eaux usées, une acclimatation des microorganismes est possible, laquelle entraînera une dissociation plus complète de la mélamine qui produira de l’ammoniac que la population résidente de microorganismes pourra utiliser comme source d’énergie. Toutefois, ceci ne représente pas un potentiel de biodégradation rapide, mais plutôt le processus d’adaptation de certains microorganismes. De plus, les preuves suggérant que la mélamine peut inhiber la croissance bactérienne dans la boue activée sont contradictoires. Puisque la mélamine est une molécule stable et que selon de nombreuses études (voir le tableau 6-2 ci-dessus), elle présente un faible potentiel de biodégradation dans l’eau, on considère que cette substance est persistante dans ce milieu naturel.
6.2.2.3 Biodégradation modélisée dans l’eau
En plus des données empiriques disponibles concernant la dégradation de la mélamine dans l’eau, une méthode du poids de la preuve fondée sur la méthode QSAR a été appliquée à l’aide des modèles de dégradation présentés dans le tableau 4-3.
Le taux d’hydrolyse de la mélamine n’a pas pu être déterminé à l’aide du modèle HYDROWIN (2010) puisque celui-ci ne peut fournir d’estimations pour les structures des triazines. Les sous-modèles BIOWIN de l’EPI Suite (2012) ont été utilisés pour évaluer le potentiel de biodégradation de la mélamine. Le sous‑modèle 4 de BIOWIN suggère un certain potentiel de biodégradation primaire. Les résultats des modèles de biodégradation ultime, les sous-modèles 3, 5 et 6 de BIOWIN (EPI Suite, 2012), et de CATALOGIC (2012) indiquent que la mélamine se biodégrade lentement ou pas du tout. Dans l’ensemble, les résultats des modèles indiquent un potentiel de biodégradation ultime limité, et en raison du consensus des résultats des modèles qui indiquent un faible taux de biodégradation, les preuves sont suffisantes pour suggérer que la mélamine subit une biodégradation primaire. Les résultats des modèles confirment les résultats des études empiriques sur la biodégradation (résumés dans le tableau 6-2), et indiquent que la mélamine se biodégrade lentement dans l’eau. Les résultats modélisés sur la dégradation de la mélamine dans l’eau sont résumés à l’annexe A.
6.2.3 Sol
La biodégradation de la mélamine est très lente dans le sol (Hauck et Stephenson, 1964). Cela peut s’expliquer en partie par la structure résonnante symétrique de la substance; une symétrie moléculaire tend à conférer de la stabilité (Hauck et Stephenson, 1964). Le mécanisme de biodégradation de la mélamine par réactions de désamination hydrolytique a été élucidé, in vitro, dans des bactéries isolées du sol. Elle s’explique par la présence de gènes particuliers codés par des plasmides, connus sous le nom de gènes tri A et trz B, C, D, E, qui codent les enzymes appelées amidohydrolases qui ont la capacité de convertir la mélamine par étapes en acide cyanurique, en biuret puis en urée, entraînant la dégradation en dioxyde de carbone et en ammoniac par uréase (Eaton et Karns, 1991 a,b; Karns et Eaton, 1997; Wackett et coll., 2002). Hatakeyama et Takagi (2016) ont montré que même si la dégradation de la mélamine est faible, on peut l’accroître lorsque les bactéries sont précultivées dans un milieu contenant de la mélamine.
La nitrification de la mélamine a été étudiée dans deux types de sols, soit un loam limono-argileux à un pH de 8,2, et un loam sableux fin à un pH de 5,2 (Hauck et Stephenson, 1964). De la mélamine a été appliquée à des échantillons de sol à une concentration de 0,2 mg/g de sol pendant 24 semaines. Les résultats ont indiqué que la mélamine se nitrifiait plus rapidement dans le loam limono-argileux, avec une nitrification de près de 8 % après 6 jours d’incubation, et de 18 % après 24 jours. En contrepartie, dans le loam sableux fin, la nitrification de la mélamine était de 0 % après les 12 premiers jours de l’étude, et après 24 semaines, d’environ 9 %. Ces résultats indiquent que dans un loam limono-argileux ayant un pH basique, la nitrification de la mélamine se déroule presque deux fois plus rapidement que dans un loam sableux légèrement acide. Dans un autre essai effectué avec du loam limono-argileux, la mélamine a été appliquée à une concentration de 2 mg/g de sol. Après 10 semaines d’incubation, environ 1 % de l’azote provenant de la mélamine a été détecté sous forme de nitrate et après une période d’incubation de 28 semaines, aucun nitrate n’a été détecté, possiblement en raison de l’assimilation accrue des nitrates par les microorganismes présents dans le sol (Hauck et Stephenson, 1964).
Dans une étude antérieure, Konishi et Imanishi (1941)3 avait observé que la mélamine se nitrifiait très lentement dans un sol de rizière.
En général, les résultats des études démontrent que la mélamine se biodégrade lentement dans le sol. Par conséquent, on considère que la mélamine est persistante dans le sol.
6.2.4 Sédiments
Nous n’avons trouvé aucune étude expérimentale sur la biodégradation de la mélamine dans les sédiments, et peu de modèles sont disponibles pour ce milieu. Par conséquent, un ratio d’extrapolation de 1:1:4 pour les demi-vies de biodégradation dans l’eau, le sol et les sédiments a été utilisé (Boethling et coll., 1995). Comme la demi-vie de la mélamine dans l’eau est longue et dépasse probablement 182 jours (d’après les résultats de la DBO et du COD des études sur la biodégradation de la mélamine), on peut supposer que la demi-vie de la mélamine dans les sédiments devrait être supérieure à 365 jours. Ceci indique que la mélamine devrait persister dans les sédiments.
6.3 Potentiel de bioaccumulation
Pour déterminer le potentiel de bioaccumulation de la mélamine, nous avons examiné les propriétés physiques et chimiques ainsi que les données empiriques et modélisées pertinentes.
La mélamine est hautement soluble dans l’eau, ce qui indique que cette substance est aisément biodisponible dans l’eau. Les valeurs expérimentales et modélisées du log Koe (variant de -1,37 à -0,38) pour la mélamine indiquent que cette substance a probablement un faible potentiel de bioaccumulation dans le biote en fonction de la répartition hydrophobe. De plus, la combinaison de deux valeurs de coefficient de partage, le log Koe de -1,37 et le log Koa de 10,8, indique qu’en cas d’exposition terrestre par voie alimentaire, la mélamine ne devrait pas se bioamplifier dans les chaînes trophiques terrestres comme l’avaient proposé Gobas et coll. (2003) et Kelly et coll. (2007).
Les facteurs de bioconcentration de la mélamine ont été déterminés de façon empirique chez plusieurs espèces de poissons (MITI, 1992; ECHA c2007-2013). Dans ces études en conditions statiques, on a exposé des poissons à de la mélamine. La durée de l’exposition à la mélamine et les concentrations variaient selon les études, mais on a observé qu’une concentration de mélamine à l’équilibre a été atteinte dans les tissus des poissons (MITI, 1992; ECHA, 2007‑2013). En général, ces études ont toutes démontré de très faibles FBC pour la mélamine. Chez la carpe (Cyprinus carpio), les FBC calculés étaient inférieurs à 3,8 et à 0,38 L/kg, après une exposition à la mélamine à des concentrations de 0,2 mg/L et 2 mg/L, respectivement, dans une étude sur 6 semaines (MITI, 1992). Chez des têtes-de-boule (Pimephales promelas) exposés pendant 96 heures à 0,09 mg/L de mélamine, on a observé des FBC de 0,48 et 0,26 L/kg dans les viscères et la carcasse, respectivement (ECHA c2007-2013). En tenant compte d’une période de dépuration de 72 heures dans les calculs, les valeurs des FBC étaient légèrement plus basses, soit 0,32 L/kg dans les viscères et 0,2 L/kg dans la carcasse. De la même façon, chez la truite arc-en-ciel (Oncorhynchus mykiss), les FBC étaient bien en deçà de 1 L/kg dans les muscles et les viscères après une exposition de 64 heures à une concentration de 0,09 mg/L de mélamine (les FBC étaient de 0,11 L/kg dans les viscères et de 0,05 L/kg dans les muscles) et la mélamine a rapidement été éliminée après la période de dépuration de 72 heures (ECHA c2007-2013). Le tableau 6-3 résume les résultats des études de bioconcentration chez les poissons.
Organisme d’essai |
Valeur cinétique et à l’équilibre (L/kg) a |
Référence |
|---|---|---|
Carpe (Pteronarcys californica) |
< 3,8 (0,2) < 0,38 (2,0) |
MITI, 1992 |
Tête-de-boule (Pimephales promelas) |
de 0,26 à 0,48 (0,09) |
ECHA c2007‑2013 |
Truite arc-en-ciel (Oncorhynchus mykiss) |
de 0,05 à 0,11 (0,09) |
ECHA c2007‑2013 |
a Les valeurs entre parenthèses représentent les concentrations d’essai, en mg/L, auxquelles les FBC ont été obtenus.
De plus, les valeurs modélisées des FBC chez les poissons obtenues à l’aide du modèle BCFBAF de l’EPI Suite (2012) concordaient avec les valeurs empiriques des FBC, et variaient entre 0,93 et 3,16 L/kg sur la base du poids humide pour un poisson de niveau trophique intermédiaire, en fonction de l’application de la constante du taux métabolique.
À la suite des incidents d’altération de la nourriture par la mélamine en 2007 et en 2008, de nombreuses études sur l’alimentation du bétail, des poissons, des canards et des crevettes ainsi que des singes ont été menées pour déterminer le potentiel d’accumulation de la mélamine dans les tissus. Ces études consistaient principalement à ajouter de faibles et grandes quantités de mélamine à la nourriture des animaux et à étudier les effets de la nourriture contaminée par la mélamine ou les effets d’une dose unique de mélamine dans les aliments (Qin et coll., 2010; Andersen et coll., 2008, 2011; Lightner et coll. 2009; Reimschuessel et coll., 2010; Phromkunthong et coll. 2013, 2015; Suknikom et coll. 2016). En général, les concentrations de mélamine résiduelles mesurées dans les tissus étaient faibles et suggéraient que la mélamine n’a pas un important potentiel d’accumulation dans les tissus des animaux après une exposition par les aliments. Qin et coll. (2010) ont également observé que les résidus de mélamine dans les tissus des animaux, le lait et les œufs disparaissaient pratiquement complètement après une période allant de quelques jours à deux semaines après l’arrêt de l’alimentation enrichie de mélamine. Des observations similaires de l’élimination des résidus de mélamine jusqu’à 14 jours après une dose unique par voie orale ont été notées chez les poissons (Reimschuessel et coll. 2010a). Cependant, des effets indésirables, notamment une insuffisance rénale due à la formation de cristaux rénaux ont été notés lorsque des doses élevées de 20 mg mélamine/kg ont été administrées aux poissons (Reimschuessel et coll. 2010 b; Phromkunthong et coll. 2015).
En résumé, des preuves solides et cohérentes indiquent que la mélamine ne se bioaccumule pas de manière appréciable dans les organismes aquatiques et terrestres. La mélamine possède une combinaison de propriétés chimiques et physiques qui pointe vers un faible potentiel de bioaccumulation et de très faibles FBC empiriques et modélisés chez les poissons. Des études empiriques indiquent que la mélamine a un faible potentiel d’accumulation dans les tissus des animaux lorsqu’elle est administrée par les aliments, et qu’elle s’élimine relativement rapidement. Par conséquent, d’après les preuves disponibles, on considère que le potentiel de bioaccumulation de la mélamine est faible.
6.4 Résumé du devenir dans l’environnement
La mélamine est une molécule compacte et stable (voir le tableau 2 pour la structure). La dégradation de la mélamine se fait par étapes, d’abord par la désamination hydrolytique puis par le clivage de cycles pour aboutir à deux produits finaux, l’ammoniac et le dioxyde de carbone. Dans l’environnement, la mélamine n’a pas le potentiel de se dégrader rapidement. Elle a une longue demi-vie dans l’air et une biodégradation relativement lente dans l’eau et le sol. L’application des facteurs d’extrapolation recommandés par Boethling (1995) indique que la mélamine devrait aussi avoir une longue demi-vie dans les sédiments. L’hydrolyse de la mélamine ne se produit pas sous des valeurs de pH pertinentes sur le plan environnemental (6 à 9). Toutefois, dans des conditions strictes de laboratoires, la mélamine peut s’hydrolyser pour produire de l’acide cyanurique, et une mélamine complètement dégradée peut rapidement se transformer en ammoniac lorsqu’elle est catalysée par des acides forts.
On s’attend à ce que la mélamine soit principalement rejetée dans les eaux usées par des sources industrielles. La mélamine est essentiellement non volatile et a un potentiel limité de sorption sur les particules solides. Il est peu probable que la mélamine soit éliminée efficacement par les systèmes de traitement des eaux usées (STEU), et c’est pourquoi on ne s’attend pas à ce que des concentrations élevées de mélamine soient présentes dans les biosolides destinés à être épandus sur le sol dans le cadre de pratiques d’amendement à l’aide de biosolides. Elle ne devrait pas se déplacer sur grande distance dans l’air, mais elle peut parcourir de grandes distances dans l’eau. Comme elle est rejetée dans l’eau et le sol et qu’elle a tendance à demeurer dans ces deux milieux, on s’attend à ce que les organismes aquatiques et du sol y soient exposés. La mélamine ne se bioaccumule pas de manière appréciable dans les organismes, et elle s’élimine relativement rapidement, surtout chez les poissons et les mammifères. La bioamplification dans les chaînes trophiques n’est donc pas considérable et elle ne devrait pas contribuer aux effets de la mélamine causés par l’exposition.
7. Potentiel d’effets nocifs sur l’environnement
7.1 Évaluation des effets sur l’environnement
Les effets de la mélamine sur l’environnement ont été déterminés par des données empiriques provenant d’études publiées et non publiées. Les études industrielles non publiées ont été résumées pour le Règlement REACH (règlement sur l’enregistrement, l’évaluation, l’autorisation et la restriction des produits chimiques) de l’Union européenne, et des résumés d’études étaient disponibles dans le site Web de l’ECHA (c2007‑2013). Puisque certains résumés d’études contiennent peu de détails, nous avons utilisé plusieurs études ont été utilisées pour comparer les résultats. Comme de nombreuses études sur les effets de la mélamine sur les espèces aquatiques et du sol étaient disponibles, nous n’avons pas considéré les données modélisées sur les effets.
Les nombreuses utilisations industrielles connues de la mélamine (ECCC 2013-2014) au Canada nous permettent de déduire que la majeure partie des rejets de mélamine sera dans les eaux de surface.
L’information est présentée en fonction du milieu d’exposition. Les résultats des études publiées et non publiées sont résumés ci-dessous dans le tableau 7-1 pour les microorganismes aquatiques et les invertébrés, et dans le tableau 7-2 pour les poissons et les organismes vivant dans le sol.
7.1.1 Eau
Les effets de la mélamine sur les microorganismes présents dans la boue ont été déterminés dans plusieurs études en fonction d’une exposition à court terme d’une durée maximale de 2 heures (ECHA c2007-2013; Hockenbury et Grady, 1977), et d’une exposition plus longue de 72 heures (Xu et coll., 2013). Les études d’exposition à court terme indiquent que la mélamine n’est pas fortement toxique pour les microorganismes présents dans les boues, alors que l’inhibition potentielle des boues activées par la mélamine a été observée dans des essais de 72 heures (Xu et coll. 2013), ce qui porte à croire qu’une durée d’exposition plus longue peut être un facteur important qui n’est pas bien caractérisé dans les ensembles des données disponibles. En général, les résultats des études indiquent que la mélamine est peu toxique pour les microorganismes.
Les effets de la mélamine sur les organismes unicellulaires ont été étudiés chez les protozoaires ciliés Tetrahymena pyriformis et T. thermophila, et les espèces d’algues Scenedesmus pannonicus et Selenastrum capricornutum. Les effets de la mélamine sur T. pyriformis ont été déterminés dans deux études par Wang et coll. (2009; 2011), qui ont observé que la mélamine présentait un effet inhibiteur selon la concentration. Les concentrations inhibitrices pour obtenir une réduction des effets à 50 % après une exposition de 52 heures, c.‑à‑d. les valeurs de CI50, ont été déterminées à 780 mg/L (Wang et coll., 2009) et 820 mg/L (Wang et coll. 2011). Des résultats semblables ont été observés par Li et coll. (2015) pendant une exposition de 20 heures de T. thermophila à la mélamine. Les effets sur deux espèces d’algues, S. pannonicus et S. capricornutum, ont été déterminés dans des études non publiées de 1982 (ECHA c2007-2013) et 1988 (US Testing Company, 1988) respectivement. Les résumés des études sont disponibles auprès de l’ECHA (c2007‑2013). Dans l’étude de 1982, les effets de la mélamine sur le taux de croissance ont été notés et une concentration sans effet observé (CSEO) de 320 mg/L et une concentration entraînant un effet de 50 % (CE50) de 940 mg/L ont été déterminées après une exposition de 90,5 heures. De la même façon, dans l’étude de 1988, la CSEO et la CE50 après 48 heures ont été calculées à 97 mg/L et 325 mg/L respectivement. Après 72 heures, la CSEO et la CE50 étaient de 31 mg/L et 196 mg/L, et après 96 heures, elles étaient de 98 mg/L et 325 mg/L respectivement.
Les études des effets de l’exposition des invertébrés aquatiques à la mélamine dans l’eau ne se sont intéressées qu’à une seule espèce, Daphnia magna. Les effets ont été déterminés dans deux études non publiées datant de 1978 (ECHA c2007-2013) et 1988 (ABC Laboratories, 1988), qui toutes deux présentaient les résultats pour des expositions à court terme de 24 à 48 heures, et des expositions à plus long terme pouvant s’étendre jusqu’à 21 jours. Les résumés des études sont disponibles auprès de l’ECHA (c2007‑2013). Dans l’étude de 1978, selon le sommaire de l’étude, la D. magna a été exposée à la mélamine pendant 48 heures, et de 7 à 21 jours, à des concentrations allant jusqu’à 2000 mg/L. On a estimé que la concentration jugée létale pour 50 % des organismes testés après une exposition de 48 heures, c’est‑à‑dire la CL50, excédait 2 000 mg/L. Cependant, on a noté que l’état des daphnies était pire à une concentration d’exposition beaucoup plus faible que 180 mg/L. Par conséquent, la CE50 de 48 heures pour le comportement a été établie à moins de 180 mg/L. Les CL50 sur 7 jours et 21 jours ont été estimées à > 32 et < 56 mg/L, d’après les taux de survie observés à des concentrations d’expositions de 32 et 56 mg/L, où le taux de survie à la concentration d’exposition de 32 mg/L était supérieur à 90 %, et à une concentration d’exposition de 56 mg/L, aucune daphnie n’a survécu au-delà de 7 jours d’exposition. La CSEO de 21 jours pour le taux de reproduction et de mortalité a été déterminée à 18 mg/L. Dans l’étude de 1988 (ABC Laboratories, 1988), la mélamine a été testée à des concentrations maximales de 1000 mg/L pendant 24 et 48 heures en conditions statiques. La CSEO de 48 heures a été estimée inférieure à la concentration d’exposition la plus basse de 56 mg/L comme les effets de mortalité et de comportement, y compris la quiescence, l’émersion et la tendance vers le fond du récipient d’essai, ont été observés à toutes les concentrations testées. Les valeurs CE50 pour 24 et 48 heures ont été calculées à 400 mg/L et 200 mg/L respectivement, d’après les effets nocifs totaux (ABC Laboratories, 1988).
Des effets de l’exposition à la mélamine par l’alimentation ont été observés chez la crevette tigrée (Penaeus monodon) et la crevette blanche du Pacifique (Penaeus vannamei), à la suite de l’administration d’aliments altérés par la mélamine dans des fermes à crevettes (Lightner et coll., 2009). Bien qu’elle ne soit pas représentative des concentrations d’exposition réalistes dans l’environnement, cette étude met en lumière les effets qui résultent d’autres voies d’exposition alimentaire. L’analyse des échantillons alimentaires a indiqué que la mélamine était présente à des concentrations supérieures à 100 mg/kg (déclarées en ppm). L’exposition à ces niveaux de mélamine par l’alimentation a causé l’apparition de cristaux de sel insolubles de mélamine-acide cyanurique dans la glande antennaire, qui se sont manifestés par des lésions de gravité modérée. Une mortalité accrue et la prévalence de maladie chez la crevette de ferme P. vannamei, qui avait reçu de la nourriture enrichie de mélamine, ont aussi été observées (Lightner et coll., 2009).
Les résultats des études de toxicité pour les microorganismes présents dans la boue, les organismes unicellulaires, les protozoaires et les invertébrés sont résumés dans le tableau 7-1.
Organisme d’essai |
Durée de l’essai |
Paramètre |
Valeur (mg/L) |
Référence |
|---|---|---|---|---|
Microorganismes présents dans la boue |
30 min |
CSEO (respiration) |
2 000 |
ECHA c2007-2013 |
Microorganismes présents dans la boue |
30 min |
CE10 (respiration) |
> 10 000 |
ECHA c2007-2013 |
Microorganismes présents dans la boue |
30 min |
CE20 (respiration) |
> 1 992 |
ECHA c2007-2013 |
Espèce Nitrosomonas |
2 h |
CSEO (espèce Nitrosomonas) |
100 |
Hockenbury et Grady 1977 |
Microorganismes présents dans la boue |
100 j |
CMEO (croissance de la population) |
75 |
Xu et coll. 2013 |
Protozoaire cillé (Tetrahymena thermophila) |
20 h |
CI50 (prolifération) |
1 000 |
Li et coll. 2015 |
Protozoaire cillé (Tetrahymena pyriformis) |
52 h |
CI50 (temps de croissance de la génération) |
780 |
Wang et coll. 2009 |
Protozoaire cillé (Tetrahymena pyriformis) |
52 h |
CI50 (temps de croissance de la génération) |
820 |
Wang et coll. 2011 |
Algues (Scenedesmus pannonicus) |
90,5 h |
CSEO |
320 |
ECHA c2007-2013 |
Algues (Scenedesmus pannonicus) |
90,5 h |
CE50 |
940 |
ECHA c2007-2013 |
Algues (Selenastrum capricornutum) |
48 h |
CSEO; CE50 |
97; 325 |
US Testing Company 1988; ECHA c2007-2013 |
Algues (Selenastrum capricornutum) |
72 h |
CSEO; CE50 |
31; 196 |
US Testing Company 1988; ECHA c2007-2013 |
Algues (Selenastrum capricornutum) |
96 h |
CSEO; CE50 |
98; 325 |
US Testing Company 1988; ECHA c2007-2013 |
Cladocère (Daphnia magna) |
48 h |
CE50 (mobilité) |
200* |
ABC Laboratories 1988; ECHA c2007-2013 |
Cladocère (Daphnia magna) |
24 h |
CE50 (comportement) | 400 |
ABC Laboratories 1988; ECHA c2007-2013 |
Cladocère (Daphnia magna) |
48 h |
CSEO (mobilité et comportement) |
< 56 |
ABC Laboratories 1988; ECHA c2007-2013 |
Cladocère (Daphnia magna) |
48 h |
CL50 |
> 2 000 |
ECHA c2007-2013 |
Cladocère (Daphnia magna) |
48 h |
CE50 (comportement) |
< 180 |
ECHA c2007-2013 |
Cladocère (Daphnia magna) |
7 et 21 j |
CL50 |
> 32 et < 56 |
ECHA c2007-2013 |
Cladocère (Daphnia magna) |
21 j |
CSEO (reproduction et mortalité) |
18 |
ECHA c2007-2013 |
Cladocère (Daphnia magna) |
21 j |
CSEO, CMEO (reproduction) |
> 11 |
ECHA c2007-2017 |
Abréviations : CE50 = concentration d’une substance dont on estime qu’elle a un effet sur 50 % des organismes d’essai; CL50 = concentration d’une substance dont on estime qu’elle est létale pour 50 % des organismes d’essai; CI50 = concentration médiane d’inhibition, c.‑à‑d. une estimation ponctuelle de la concentration d’une substance d’essai qui provoque une réduction de 50 % d’une mesure biologique quantitative, p. ex., le taux de croissance; CSEO = concentration sans effet observé, c.‑à‑d. la concentration la plus élevée dans un essai de toxicité ne provoquant pas d’effet statistiquement significatif par rapport aux témoins; CMEO = concentration minimale entraînant un effet observé, c.‑à‑d. la concentration la plus faible dans un essai de toxicité qui provoque un effet statistiquement significatif par rapport aux témoins.
Les effets de la mélamine ont été observés chez de nombreuses espèces de poissons selon des expositions à court et à moyen terme. Les études à court terme, qui ont pour objectif de caractériser les effets sur la mortalité, portaient sur quatre espèces de poissons : le guppy (Poecilia reticulata), la truite arc-en-ciel (Oncorhynchus mykiss), l’ide mélanote (Leuciscus idus) et le médaka (Oryzias latipes). Les résumés de ces études non publiées (1978, 1982 et 1984) sont disponibles auprès de l’ECHA (c2007‑2013) et dans la base de données japonaise MITI (1992). Les études ont habituellement été menées en suivant des protocoles similaires aux directives de l’OCDE ou de l’USEPA et comprenaient les témoins appropriés. D’après ces études, on considère que la mélamine présente une faible toxicité pour dans le cadre d’une courte exposition de poissons. Les paramètres observés étaient une CL50 sur 48 heures à 1 000 mg/L et une CSEO sur 96 heures à 3 000 mg/L pour le taux de mortalité. Bien que des morts aient été observées chez certaines espèces testées, il a été impossible de déterminer une CL50 aiguë à court terme pour la mélamine dans la plupart des études, comme les concentrations d’essai les plus élevées utilisées dans les études étaient près de la limite de solubilité de la mélamine de 4 850 mg/L (déterminée à 25 C). Les observations relatives aux autres effets physiologiques n’ont pas été mentionnées dans les résumés d’études disponibles. Les paramètres déterminés pour ces études sont résumés au tableau 7-2.
Des études à long terme ayant porté sur les effets de la mélamine ont été réalisées sur trois espèces de poissons, soit la truite arc‑en‑ciel (Salmo gairdneri), la jordanelle de Floride (Jordanella floridae) et le tête‑de‑boule (Pimephales promelas). Dans une étude de 1984 résumée dans l’ECHA (c2007‑2013), un test semi-statique a été effectué pendant 28 jours pour caractériser les taux de croissance et de mortalité chez la truite arc-en-ciel juvénile (S. gairdneri) exposée à la mélamine à des concentrations variant entre 750 et 3 000 mg/L. Un taux de mortalité d’environ 30 % a été observé aux concentrations d’exposition de 3 000 mg/L, par conséquent une CL50 supérieure à 3 000 mg/L a été attribuée pour le taux de mortalité, et la CSEO pour le taux de mortalité a été établie à 1 500 mg/L. On a également observé une perte de poids chez les poissons à des concentrations d’exposition de 1500 mg/L et 3 000 mg/L. Par conséquent, d’après ces résultats, la CSEO pour le taux de croissance peut être établie à 750 mg/L. Deux autres études à long terme menées en 1982 ont étudié les effets de l’exposition à la mélamine au cours des premiers stades du développement. Ramusino et Vailati (1982) ont déterminé les effets de la mélamine sur les taux d’éclosion et les malformations chez les embryons de truite arc-en-ciel (S. gairdneri). Les embryons ont été exposés à la mélamine à des concentrations de 125, 250, 500 et 1 000 mg/L jusqu’à l’éclosion. Aucun décès n’a été observé, cependant, une baisse de 45 % des taux d’éclosion a été observée à la plus forte concentration. Une augmentation des malformations a également été observée à toutes les concentrations, avec une augmentation marquée pouvant atteindre 90 % à la concentration de 1 000 mg/L. Il a été noté que les analyses statistiques, qui auraient tenu compte de facteurs comme la taille de l’échantillon, n’ont pas été menées et, bien que la baisse des taux d’éclosion et les malformations observées indiquent des effets évidents, il n’est pas certain que ces observations soient la preuve de différences statistiques par rapport aux témoins. D’après les résultats de l’étude, une CSEO de 1 000 mg/L pour le taux de mortalité et une CMEO de 125 mg/L pour les malformations embryonnaires peuvent être établies. Les effets de la mélamine sur le développement larvaire des œufs ont aussi été étudiés chez la jordanelle de Floride (J. floridae) et les résultats de l’étude sont résumés dans l’ECHA (c2007‑2013). Dans cette étude, cinq concentrations variant entre 100 et 1 000 mg/L de mélamine ont été testées pendant 35 jours. Aucun effet sur la capacité d’éclosion, l’apparence ou le taux de mortalité des larves n’a été observé. Des effets minimaux sur la croissance des larves ont été observés aux plus hautes concentrations d’essai, mais en général, les différences entre les poids corporels étaient négligeables (ECHA c2007-2013). Les valeurs de la CSEO et de la CE50 pour le taux de survie, le taux de croissance et l’état ont été déterminées à 1 000 mg/L et à plus de 1 000 mg/L respectivement. Une étude non publiée de 2015 sur la toxicité chronique pour le tête‑de‑boule, résumée dans ECHA (ECHA c2007-2015), indiquait une CMEO de 10,1 mg/L basée sur l’observation d’une diminution légère de la survie et de la croissance, ainsi que sur la présence de deux poissons déformés. Cinq concentrations allant de 0,618 à 10 mg/L ont été testées, et les concentrations d’exposition ont été mesurées pendant toute la durée de l’étude, soit 36 jours (ECHA c2007- 2017).
On a réalisé de nombreuses études sur l’ajout de mélamine à l’alimentation des poissons d’aquaculture (Liu et coll., 2009; Janlek et coll. 2009; Xue et coll. a, b; Phromkunthong et coll., 2013). Comme il est indiqué dans la discussion sur l’étude des crevettes (Lightner et coll., 2009), une exposition alimentaire élevée à la mélamine ne devrait pas survenir dans des conditions environnementales normales. Elle se produit plutôt lorsque la mélamine est ajoutée de manière délibérée à la nourriture donnée aux animaux de ferme. Des effets nocifs ont été observés, dont une efficacité réduite de l’alimentation, des modifications histopathologiques ainsi que des taux de croissance statistiquement plus bas chez tous les groupes nourris à la mélamine (Phromkunthong et coll., 2013). Des effets nocifs sur le système rénal des poissons ont été observés lorsque des doses élevées de mélamine étaient ajoutées à la nourriture, particulièrement lorsqu’elle était combinée à de l’acide cyanurique. La formation de calculs rénaux et une insuffisance rénale chez la truite et le poisson-chat ont été confirmées par Reimschuessel et coll. (2010 b) à la suite de l’administration de mélamine suivie d’acide cyanurique à 20 mg/kg. Des observations similaires ont été faites dans une étude non publiée de 2013 sur le tilapia rouge et résumées par l’ECHA (ECHA c2007-2017).
Les résultats des principales études menées chez les poissons sont résumés au tableau 7-2.
Organisme d’essai |
Durée de l’essai |
Paramètre |
Valeur (mg/L) |
Référence |
|---|---|---|---|---|
Médaka (Oryzias latipes) |
48 h |
CL50 |
1000 |
MITI, 1992 |
Ide mélanote (Leucisus idus melanotus) |
48 h |
CL50 |
> 500 |
ECHA c2007-2013 |
Truite arc-en-ciel (Oncorhynchus mykissa) |
96 h |
CL50 |
> 3000 |
ECHA c2007-2013 |
Truite arc-en-ciel (Oncorhynchus mykissa) |
96 h |
CSEO (mortalité) |
3000 |
ECHA c2007-2013 |
Guppy (Poecilia reticulata) |
96 h |
CL50 |
> 4 400 |
ECHA c2007-2013 |
Guppy (Poecilia reticulata) |
96 h |
CL50 |
> 4 590 |
ECHA c2007-2013 |
Guppy (Poecilia reticulata) |
96 h |
CL50 |
> 3000 |
ECHA c2007-2013 |
Truite arc-en-ciel (Salmo gairdneri) |
28 j |
CSEO (mortalité) |
1 500 |
ECHA c2007-2013 |
Truite arc-en-ciel (Salmo gairdneri) |
28 j |
CL50 |
> 3000 |
ECHA c2007-2013 |
Truite arc-en-ciel (Salmo gairdneria) |
28 j |
CMEO (croissance) |
750 |
ECHA c2007-2013 |
Truite arc-en-ciel (Salmo gairdneria) |
18 à 26 j |
CSEO (mortalité) |
1000 |
Ramusino et Vailati, 1982 |
Truite arc-en-ciel (Salmo gairdneria) |
18 à 26 j |
CMEO (malformations embryonnaires) |
125 |
Ramusino et Vailati, 1982 |
Jordanelle de Floride (Jordanella floridae) |
35 j |
CSEO (croissance, survie, état) |
1000 |
ECHA c2007-2013 |
Jordanelle de Floride (Jordanella floridae) |
35 j |
CE50 (croissance, survie, état) |
> 1000 |
ECHA c2007-2013 |
Tête-de-boule (Pimephales promelas) |
36 j |
CMEO (survie, croissance) | 10,1 |
ECHA c2007-2013 |
Abréviations : CE50 = concentration d’une substance qu’on estime susceptible de causer un effet chez 50 % des organismes d’essai; CL50 = concentration d’une substance qu’on estime susceptible de causer un décès chez 50 % des organismes d’essai; CSEO = concentration sans effet observé (concentration la plus élevée ne causant pas d’effet statistiquement significatif par rapport aux témoins dans un essai de toxicité); CMEO = concentration minimale avec effet observé (concentration la plus faible mesurée lors d’un essai de toxicité qui a un effet statistiquement significatif par comparaison avec les témoins).
a Salmo gairdneri, communément connu sous le nom de truite arc-en-ciel, a été reclassé dans le genre Oncorhynchus et, par conséquent, Salmo gairdneri est actuellement appelé Oncorhynchus mykiss (Smith et Stearley, 1989). Comme les noms latins qui sont présentés dans les publications et les sources originales sont cités, les deux noms sont mentionnés dans le tableau, c.-à-d. que Oncorhynchus mykiss et Salmo gairdneri désignent la même espèce de poisson.
Pour ce qui est du milieu aquatique, une concentration estimée sans effet (CESE) a été établie à partir de la valeur de toxicité chronique de 10,1 mg/L (c.‑à‑d. la valeur expérimentale dénotant la plus grande sensibilité, et donc la plus valide) pour le tête‑de‑boule, P. promelas, et en divisant cette valeur par un facteur d’évaluation de 5 (pour tenir compte de l’extrapolation d’un critère d’effet létal à un critère d’effet sublétal), ce qui donne une valeur de 2,0 mg/L.
7.1.2 Sol
Peu d’études caractérisant les effets de la mélamine sur les organismes présents dans le sol étaient disponibles. Les études sur les plantes dont l’orge (Hordeum vulgare), le radis (Raphanus sativus), le cresson de jardin (Lepidum sativum) et le blé commun (Triticum aestivum) étaient limitées aux protocoles nécessitant l’utilisation de percolat de mélamine, et le produit Melfasik qui contient 2,8 % de mélamine a été testé sur les pois (Pisum sativum) et le haricot commun (Phaseolus vulgaris) (ECHA c2007-2013; OCDE, 2002). Une autre étude a examiné les taux de nitrification des microorganismes du sol exposés à la mélamine par des perfusions dans le sol (Hauck et Stephenson, 1964). Les résultats de ces études indiquent généralement que la mélamine est peu toxique pour les espèces testées. Les paramètres de toxicité variaient entre une CSEO de 14 jours à 170 mg/kg déterminée pour la germination et la croissance des pois et des haricots à filet, et une CE50 de 4 jours à 1 100 mg/L pour la croissance des racines du cresson de jardin.
En raison du manque de protocoles normatifs dans les données existantes pour le sol et de l’absence de modèles QSAR fiables, la CESE n’a pas pu être déterminée pour ce milieu. Bien qu’on puisse prévoir une certaine exposition à la mélamine dans le sol à cause de l’amendement aux biosolides, il est peu probable qu’il y ait des concentrations de mélamine importantes dans les biosolides, en raison de leurs faibles valeurs de log Kco et Koe et de leur forte hydrosolubilité.
7.1.3 Sédiments
Nous n’avons trouvé aucune étude traitant des effets de la mélamine sur les organismes benthiques.
7.2 Évaluation de l’exposition de l’environnement
7.2.1 Concentrations environnementales mesurées
Nous n’avons pas trouvé de donnée sur les concentrations de la mélamine dans l’environnement canadien. En outre, la mélamine ne figure pas sur la liste des substances déclarées à l’Inventaire national des rejets de polluants (Environnement et Changement climatique Canada 2013).
À l’échelle internationale, on peut détecter des concentrations de référence de mélamine dans l’environnement à la suite de l’utilisation répandue de matières contenant cette substance (OMS, 2009). En raison de l’altération des aliments pour les animaux et du commerce international des denrées, on croit que les excréments et l’urine des animaux seraient possiblement des sources importantes d’exposition de l’environnement à la mélamine (Qui et coll., 2010). La mélamine a été mesurée dans l’eau, les sédiments et le biote au Japon et en Chine (OCDE 2002; Qin et coll. 2010), ainsi que dans les eaux usées et le sol en Chine (Qin et coll. 2010). Qui et coll. (2010) ont étudié le dépôt et l’élimination des résidus de mélamine par le bétail, ce qui a permis de mieux comprendre la contamination des sources d’aliments par la mélamine. Un résumé des détections de mélamine à l’échelle internationale apparaît ci-dessous. Au Japon, la concentration de mélamine dans l’environnement et le biote a été répertoriée de 1986 à 1994 dans le cadre de l’enquête environnementale pour la surveillance des produits chimiques menée par le ministère japonais de l’Environnement (CHRIP, c2008-; MOE, c2005). En 1986, 1987 et 1994, on a détecté de la mélamine à des concentrations variant entre 0,1 et 7,6 µg/L (limite de détection : 0,1 µg/L) dans des échantillons d’eau de surface. Durant ces mêmes années, on a également détecté de la mélamine dans des échantillons de sédiments à des concentrations entre 0,01 et 0,4 µg/g en poids sec (limite de détection : 0,01 µg/g en poids sec). En 1987, 1988 et 1986, de la mélamine a été détectée chez les poissons sauvages à des concentrations entre 0,02 et 0,55 µg/g en poids sec (la limite de détection : 0,02 µg/g en poids sec). En 1994, des mesures de mélamine dans l’air ont révélé des concentrations entre 2 et 55 ng/m³ (la limite de détection : 2 ng/m³) (CHRIP, c2008-; MOE, c2005).
Pour déterminer l’ampleur de la contamination de l’environnement et des produits alimentaires par la mélamine, Qin et coll. (2010) ont évalué la présence de mélamine dans les cultures, le sol et l’eau, y compris les eaux de surface, les eaux souterraines et les eaux usées, dans le cadre d’une étude soutenue par le ministère de l’agriculture chinois. Dans cette étude, on a prélevé des échantillons dans 21 provinces chinoises, notamment dans les cultures (maïs, soja et blé), dans un sol agricole (échantillons prélevés à au moins 150 km d’une usine de mélamine) et dans un sol à proximité d’exploitations industrielles (à 100 m des opérations où la mélamine est utilisée), dans les eaux d’irrigation (rivières et eaux souterraines), et dans les eaux usées des usines de mélamine (prélèvement dans les eaux d’égout des usines de mélamine).
Qin et coll. (2010) rapportent une concentration maximale de mélanine de 41,1 mg/kg dans les échantillons de sol et de 226,8 mg/kg dans ceux d’eaux usées collectés à proximité des usines chinoises de fabrication de mélamine. La concentration de mélamine la plus élevée mesurée dans les échantillons d’eaux d’irrigation était de 0,198 mg/L; les autres concentrations variaient entre 21 et 100 µg/L et on n’a pas détecté de mélamine dans de nombreux échantillons n’a pas (limite de détection : 20 µg/L). Dans le sol agricole, de la mélamine a été détectée dans un seul échantillon sur les 124 échantillons testés, à une concentration de 0,176 mg/kg. L’analyse des échantillons de cultures a révélé que moins de 20 % des échantillons contenaient de la mélamine à des concentrations supérieures à 0,1 mg/kg, trois échantillons contenaient plus de 1 mg/kg de mélamine et la concentration maximale de mélamine, soit à 2,05 mg/kg, a été trouvée dans un échantillon de blé. La source des niveaux observés de mélamine a été attribuée à la présence générale de mélamine dans l’environnement et à la présence de résidus de mélamine découlant de l’utilisation légitime de pesticides de la famille des triazines (comme la cyromazine) et d’engrais à base de mélamine (Qin et coll., 2010).
7.2.2 Scénarios d’exposition et concentrations environnementales estimées
Nous n’avons pas retrouvé de donnée sur les concentrations de mélamine mesurées dans l’environnement (dans l’eau, les sols ou les sédiments). Par conséquent, les concentrations environnementales ont donc été évaluées sur la base des renseignements disponibles, y compris les quantités utilisées, les estimations des taux de rejets et les caractéristiques du milieu récepteur.
La mélamine est une substance stable caractérisée par lente biodégradation potentielle dans l’environnement, un faible potentiel de bioaccumulation et un faible potentiel de toxicité pour les organismes aquatiques et du sol. La mélamine est utilisée en grandes quantités au Canada et partout dans le monde. On s’attend à ce que la majorité des rejets dans l’environnement canadien occasionnés par des activités industrielles soient dans l’eau.
La caractérisation de l’exposition repose sur des scénarios qui représentent les forts potentiels d’exposition et de rejet dans l’environnement. En général, l’ampleur des rejets est directement liée à la production ou l’utilisation d’une substance, ainsi qu’aux facteurs d’émission applicables. Pour analyser l’exposition environnementale à la mélamine au Canada, les données de l’enquête de 2011 en vertu de l’article 71, les renseignements obtenus auprès des intervenants volontaires (ECCC 2013-2014), ainsi que les renseignements provenant de la Base de données sur le Commerce international canadien de marchandises (Statistique Canada, 2019) ont été pris en compte.
Différentes compagnies déclarent importer de la mélamine comme substance pure pour l’utiliser dans des procédés industriels de création de produits comme des résines de mélamine-formaldéhyde, des plastifiants et des produits aux propriétés ignifuges, et elles importent aussi de la mélamine déjà intégrée dans des produits et des articles fabriqués (ECCC 2013-2014). Pour les utilisations industrielles, la mélamine est considérée comme étant chimiquement liée au produit fini. Bien que quelques rejets de mélamine par lixiviation (entre autres du plastique) aient été constatés, ils sont limités aux rejets provenant de la vaisselle et des ustensiles de cuisine en mélamine, et ils se produisent uniquement lorsque ces articles sont en contact avec des matrices chaudes ou tièdes comme des aliments ou l’eau (Wu et coll., 2013; Commission européenne, 2011). En ce concerne l’exposition environnementale, l’utilisation de mélamine dans les produits de consommation et commerciaux ne devrait pas conduire à d’importantes émissions dans l’environnement en raison de la très faible quantité et de la nature dispersée des émissions provoquées.
De plus, il est peu probable que l’amendement des terres agricoles avec des biosolides soit une voie d’exposition importante à la mélamine pour les organismes du sol. En raison de sa forte hydrosolubilité et de sa faible valeur de log Koe, la mélamine demeurera dans l’eau et ne s’associera pas aux biosolides.
Les estimations quantitatives des concentrations de mélamine dans les eaux de surface découlant de la fabrication de résines et du mélange destiné à fabriquer des produits aux propriétés ignifuges sont prises en compte dans la présente évaluation. Ces concentrations sont fondées sur les renseignements disponibles à propos des quantités de mélamine, des facteurs d’émission propres au secteur, des caractéristiques des systèmes de traitement des eaux usées et des caractéristiques de l’environnement récepteur.
7.2.3 Scénarios d’exposition découlant des rejets industriels dans le milieu aquatique
Pour estimer le potentiel de rejets dans l’eau découlant de l’utilisation industrielle de la mélamine dans sa forme chimique pure, nous avons élaboré des scénarios prudents pour différentes installations industrielles. Ces scénarios reposent sur les quantités utilisées en 2011 selon les déclarations (ECCC 2013‑2014), et tiennent compte des caractéristiques des plans d’eau récepteurs, du traitement des eaux usées et des activités industrielles de chaque site. Le scénario 1 contient une série de situations pouvant survenir au Canada afin de mieux caractériser les expositions causées par les différents sites industriels qui utilisent la mélamine pour fabriquer de la résine de mélamine-formaldéhyde et des composés de mélamine. Un scénario 2 considère les situations où la mélamine est intégrée à un produit aux propriétés ignifuges.
Une exposition aquatique à la mélamine pourrait avoir lieu si cette substance était rejetée en raison d’activités industrielles vers un système d’assainissement qui rejette ses effluents dans un plan d’eau de surface récepteur. La concentration de la substance dans les eaux réceptrices près du point de rejet du système d’assainissement est utilisée comme concentration environnementale estimée (CEE) dans l’évaluation du risque que pose la substance en milieu aquatique. On peut la calculer à l’aide de l’équation suivante :
Ceau–ind = [1000 × Q × L × (1 – R)] / N × F × D
où :
Ceau-ind : concentration en milieu aquatique due aux rejets industriels, en mg/L
Q : quantité de substance totale utilisée chaque année sur un site industriel, en kg/an
L : pertes dans les eaux usées, fraction
R : taux d’élimination du système d’assainissement, fraction
N : nombre de jours de rejets par année, en jour/an
F : débit de l’effluent du STEU, en m³/jour
D : facteur de dilution des eaux réceptrices, sans dimension.
Le tableau 7-3 présente les données sur la mélamine utilisées pour estimer les concentrations de la substance dans le milieu aquatique près des points de rejet industriels. Il convient de noter que l’hypothèse des pertes dans l’eau, bien qu’elle soit fondée sur des données empiriques, est considérée comme prudente pour ces pratiques industrielles particulières.
Intrant |
Scénario 1 |
Scénario 2 |
Justification et référence |
|---|---|---|---|
Quantité (kg/site) |
10000–10000000 |
10000–100000 |
Quantité de mélamine déclarée pour chaque site au Canada pour l’année 2011 (ECCC 2013-2014) |
Pertes dans les eaux usées (%) |
0,6 |
1 |
OCDE 2002 (scénario 1); Hypothèse standard d’ECCC pour le processus de mélange (scénario 2) |
Efficacité d’élimination par le STEU (%) |
0,3 – 2,1 |
2,1 |
STP-EX, 2008 (valeur estimée pour un traitement secondaire) |
Nombre de jours de rejets par année (jours) |
250 – 350 |
250 |
Base de données de l’Inventaire national des rejets de polluants de 1992 à 2013 (consulté le 11 octobre 2013) (ECCC, 2013) (scénario 1); Hypothèse normative d’ECCC (scénario 2) |
Débit de l’effluent du STEU en m³/jour |
2652 – 254260 |
45942 |
Données propres à des STEU au site |
Facteur de dilution |
10 |
10 |
Débit sortant ou débit dans l’environnement récepteur du STEU du site. Lorsqu’un facteur de dilution était supérieur à 10, nous avons utilisé une valeur maximale par défaut de 10. |
D’après les hypothèses mentionnées ci-haut, ces scénarios ont généré des CEE de 3 × 10-3 mg/L à 1,8 mg/L pour le scénario 1, et de 8 × 10-3 mg/L pour le scénario 2. Nous notons que le pourcentage de perte de 0,6 % dans les eaux usées utilisé dans le calcul repose sur les données empiriques d’installations qui fabriquent et mélangent de la mélamine (OCDE, 2002). Comme la mélamine n’est pas produite au Canada, cette évaluation des rejets de mélamine est très prudente et pourrait contribuer à une surestimation des risques.
7.3 Caractérisation des risques pour l’environnement
La démarche suivie pour produire la présente ébauche d’évaluation préalable consistait à examiner les renseignements de l’évaluation et à proposer des conclusions fondées sur le poids de la preuve et le principe de précaution. Des données ont été obtenues pour déterminer le risque que présente la mélamine dans l’environnement canadien. Les éléments de preuve examinés comprennent entre autres ceux qui sont examinés dans la présente évaluation et qui appuient la caractérisation des risques pour l’environnement au Canada. Sont également pris en compte, lorsqu’ils existent, les éléments de preuves secondaires ou indirects, y compris les décisions réglementaires et la classification des dangers ou les caractéristiques du devenir déterminées par d’autres organismes de réglementation. Selon ces renseignements, le risque d’effets nocifs pour les organismes et l’intégrité générale de l’environnement au Canada découlant de la mélamine serait faible.
7.3.1 Analyse des quotients de risque
Une analyse du quotient de risque qui intégrait des estimations prudentes de l’exposition avec les renseignements sur la toxicité a été menée pour le milieu aquatique. Les scénarios pour le milieu aquatique ont généré des concentrations environnementales estimées (CEE) allant de 3 × 10-3 mg/L à 1,8 mg/L et de 8 × 10‑3 mg/L pour les scénarios 1 et 2, respectivement. Pour les deux scénarios pour le milieu aquatique, une CESE de 2,0 mg/L a été établie à partir de la valeur de toxicité chronique de 10,1 mg/L pour le tête‑de‑boule et en appliquant un facteur d’évaluation de 5. Les quotients de risque obtenus (CEE/CESE) variaient entre 0,0015 et 0,9 pour le scénario 1. Il est à noter que les quotients de risque obtenus pour le scénario 1, soit 0,015 et 0,9, sont les quotients de risque les plus faibles et les plus élevés calculés pour les installations industrielles qui utilisent la mélamine, par conséquent, ils représentent une plage des valeurs de quotients de risque rencontrées pour cette utilisation très fréquente de la mélamine au Canada. Le quotient de risque pour le scénario 2 était de 0,004. Le tableau 7-4 présente un résumé de ces renseignements. Les résultats indiquent qu’il est peu probable que les rejets de mélamine de ces scénarios prudents nuisent aux organismes aquatiques.
Milieu |
Scénario |
CESE |
CEE |
QR |
|---|---|---|---|---|
Eau |
Scénario 1 : Rejets industriels dans l’eau découlant de l’utilisation de mélamine sous sa forme chimique pure | 2,0 (mg/L) |
3 × 10-3 – 1,8 mg/L |
0,0015 – 0,9 |
Eau |
Scénario 2 : Rejets industriels découlant du mélange de la mélamine à un produit ignifuge | 2,0 mg/L |
8 × 10-3 mg/L |
0,004 |
7.3.2 Examen des éléments de preuve et conclusion
Afin de caractériser le risque de la mélamine pour l’environnement, nous avons tenu compte des données techniques de diverses sources (décrites dans les sections pertinentes du présent rapport), qui ont été ensuite pondérées qualitativement. Les principaux éléments de preuve qui sous-tendent la conclusion de l’évaluation sont présentés dans le tableau 7-5, accompagnés d’une analyse globale du poids de la preuve donnée à la section 7.3.3. Le degré de confiance renvoie à l’influence combinée de la qualité et de la variabilité des données, des lacunes dans les données, de la causalité, de la plausibilité et de toute extrapolation requise pour les données probantes. La pertinence désigne l’effet d’une donnée probante sur le risque d’effets nocifs sur l’environnement au Canada. Les qualificateurs utilisés dans l’analyse varient de faibles à élevés, et la pondération de chaque donnée variait selon cinq résultats possibles.
Élément de preuve |
Niveau de confiance a |
Pertinence pour l’évaluation b |
Pondération c |
|---|---|---|---|
Devenir et comportement dans l’environnement |
Élevé |
Élevée |
Élevée |
Persistance dans l’environnement (eau) |
Élevé |
Élevée |
Élevée |
Transport sur de grande distance |
Modéré |
Faible |
Faible à modérée |
Bioaccumulation dans les organismes aquatiques |
Élevé |
Faible |
Modérée |
CESE pour les organismes aquatiques |
Élevé |
Élevée |
Élevée |
CEE dans l’eau |
Modéré |
Élevée |
Modérée à élevée |
QR pour l’eau |
Modéré |
Élevée |
Élevée |
a Le degré d’incertitude est déterminé en tenant compte de la qualité des données, de leur variabilité, des lacunes dans les données et du degré de pertinence des données.
b La pertinence désigne l’incidence de la preuve pour l’évaluation.
c Le caractère probant est attribué à chaque élément de preuve en fonction directe de sa pertinence dans l’évaluation ainsi que de facteurs, dont la pertinence et la qualité des données.
7.3.3 Pondération et détermination du risque de causer des effets nocifs sur l’environnement au Canada
La mélamine devrait être persistante dans l’eau, le sol et les sédiments, et devrait aussi présenter un faible potentiel de bioaccumulation. Il a aussi été démontré qu’elle présentait un potentiel faible à modéré de toxicité pour les organismes aquatiques. Les grands volumes d’importation de mélamine et les renseignements relatifs à ses utilisations indiquent un risque de rejet généralisé dans l’environnement au Canada. Une fois rejetée dans l’environnement, la mélamine devrait principalement se disperser dans l’eau. Nous avons calculé, sur la base des scénarios industriels, les concentrations environnementales estimées (CEE) découlant des utilisations industrielles de la mélamine. Les valeurs des CEE ainsi que la toxicité de la mélamine pour les organismes aquatiques, son potentiel de bioaccumulation et sa longue persistance dans le milieu aquatique sont les fondements de l’évaluation du risque d’effets nocifs sur l’environnement. Ces données indiquent que la mélamine a un faible potentiel de nuisance écologique au Canada.
7.3.4 Sensibilité de la conclusion compte tenu des principales incertitudes
Les hypothèses utilisées sont entachées d’incertitudes découlant possiblement de la surestimation des quotients de risque calculés pour les principales utilisations industrielles de la mélamine. En particulier, l’hypothèse prudente de la perte de substance de 0,6 % dans le milieu environnemental, qui est fondée sur les données empiriques des installations qui fabriquent et mélangent la mélamine, peut avoir mené à une surestimation des risques. La mélamine n’est pas fabriquée au Canada. L’absence de données de surveillance au Canada ne permet pas de dresser une comparaison directe des CEE pour vérifier si elles ont été surestimées ou sous-estimées. On a déterminé que les CEE dans l’eau pour la mélamine se situent entre 8 × 10-3 et 1,6 mg/L. Les concentrations mesurées de mélamine dans les eaux de surface des rivières au Japon se situaient entre 1 × 10-4 et 7,6 × 10-3 mg/L, et jusqu’à 1,98 × 10-1 mg/L dans les rivières de la Chine qui reçoivent des eaux d’irrigation. Donc, par rapport au nombre peu élevé de données mesurées, les CEE déterminées sont probablement prudentes.
La mélamine ne devrait pas s’associer aux boues activées, mais il est possible qu’une certaine quantité de mélamine se retrouvent dans les biosolides. Ce procédé est probablement inefficace, en raison des propriétés physiques et chimiques de la mélamine, notamment sa forte hydrosolubilité et son faible coefficient de partage carbone organique-eau dans le sol.
Les données empiriques existantes limitées sur les effets de la mélamine sur les organismes du sol et l’absence de modèles QSAR fiables pour le sol empêchent de calculer une valeur de CESE fiable. Le scénario pour le sol a donc été abandonné, car il y avait trop d’incertitudes associées aux principales données nécessaires pour son élaboration. Toutefois, en raison de la faible toxicité observée chez les organismes du sol et des concentrations de mélamine associées aux biosolides qui sont probablement faibles, le risque que présente cette voie d’exposition pour les organismes du sol n’est pas jugé considérable.
Il existe également des incertitudes concernant les effets environnementaux découlant des rejets potentiels de mélamine présente dans les ignifugeants à base de mélamine, comme le cyanurate de mélamine (NR°CAS 37640-57-6), le phosphate de mélamine (NR°CAS 20208-95-1) et le polyphosphate de mélamine (NR°CAS 218768-84-4). Ces substances ne figurent pas sur la Liste intérieure des substances et ne sont pas sujettes à la catégorisation au sens du paragraphe 73(1) de la LCPE (1999). La caractérisation des effets et des risques écologiques potentiels causés par la mélamine contenue dans les substances ignifugeantes à base de mélamine n’a pas été traitée dans la présente évaluation préalable.
8. Potentiel d’effets nocifs sur la santé humaine
8.1 Évaluation de l’exposition
Dans cette partie, nous examinons le potentiel d’exposition à la mélamine par les milieux naturels (eau potable, air, sol, poussières), les aliments, la vaisselle contenant de la mélamine et les produits de consommation, ainsi que les estimations de l’exposition basées sur les données de biosurveillance.
8.1.1 Milieux naturels et aliments
8.1.1.1 Air
Nous n’avons trouvé aucune donnée sur les concentrations de mélamine dans l’air ambiant ou l’air intérieur résidentiel.
8.1.1.2 Poussière
Nous n’avons trouvé aucune donnée sur les concentrations de mélamine dans la poussière.
8.1.1.3 Sol
Nous n’avons trouvé aucune donnée sur les concentrations de mélamine dans le sol en Amérique du Nord et ainsi aucune concentration environnementale estimée (CEE) n’a été déterminée pour le sol (voir la section 7.2). En Chine, les sols ont été testés à 100 m et à environ 150 km d’usines de fabrication de mélamine. Qin et coll. (2010) ont rapporté des concentrations entre la non-détection et 0 à 41,1 mg/kg de mélamine dans le sol à 100 m, et des concentrations entre la non-détection et 0,176 mg/kg dans les sols agricoles à environ 150 km. (Nous avons aussi abordé cette question à la sous-section 7.2.1.) Les concentrations mesurées à plus de 150 km d’une usine de fabrication de mélamine seraient plus représentatives des concentrations dans le sol auxquelles la population générale du Canada pourrait normalement être exposée. La concentration maximale mesurée dans un sol agricole à 150 km d’une usine de fabrication de mélamine en Chine a été utilisée dans une estimation déterministe de l’ingestion quotidienne.
L’estimation déterministe de l’ingestion quotidienne fondée sur l’exposition à la mélamine par le sol est négligeable pour tous les groupes d’âge.
8.1.1.4 Eau
Il n’y avait pas de données canadiennes disponibles sur la présence la mélamine dans l’eau potable ou les eaux de surface. Les seuls résultats pour les concentrations de mélamine dans l’eau potable ont été trouvés dans un rapport du groupe d’experts de l’Autorité européenne de sécurité des aliments (EFSA, 2010). Le rapport de l’EFSA indique que les données ont été fournies par des membres de l’industrie dans diverses régions du monde (n = 20 échantillons d’eau du robinet) et fait état de concentrations de mélamine allant de 10 à 200 µg/kg (moyenne : 50 µg/kg; valeurs rapportées en mg/kg pour tous les groupes alimentaires, y compris l’eau du robinet dans EFSA 2010). Les résultats pour chaque échantillon n’ont pas été rapportés n’indiquaient par le nombre d’échantillons dont la concentration de mélamine était inférieure à la limite de détection (LD).
En raison de l’absence de données canadiennes sur cette source potentielle, nous avons utilisé les données de l’EFSA pour caractériser l’exposition à la mélamine par l’eau potable. L’absorption estimée était de 5,3 et 21 µg/kg p.c./j pour les nourrissons de 0 à 6 mois nourris au lait maternisé (groupe le plus exposé), pour la tendance centrale et les concentrations limites supérieures, respectivement (voir l’annexe B).
8.1.1.5 Aliments
Comme nous l’indiquions à la partie 4, Sources et utilisations, la mélamine n’est pas répertoriée comme additif alimentaire approuvé, mais elle peut être présente dans les emballages alimentaires au Canada. Aux États‑Unis, l’utilisation de la mélamine est autorisée comme additif alimentaire indirect dans la synthèse de la résine de mélamine-formaldéhyde destinée à être utilisée dans la transformation des aliments et les emballages alimentaires.
Diverses études internationales ont étudié la migration de la mélamine présente dans le revêtement des boîtes de conserve et dans les couvercles de pots en verre vers les aliments et les boissons. Au Royaume-Uni, Bradley et coll. (2011) ont testé la migration des résines à base de mélamine-formaldéhyde et d’analogues (mélamine méthylique) utilisées pour la réticulation des revêtements intérieurs des boîtes de conserve et des couvercles métalliques des pots en verre. Pour 13 revêtements testés, les concentrations de la mélamine qui migraient jusque dans les aliments allaient de < 1,5 à 332 µg/kg selon les conditions d’utilisation (matrice fluide, variation de la température). À l’aide des mêmes conditions expérimentales, six laboratoires européens différents ont observé les mêmes taux de migration, soit de 1,5 à 327 µg/kg (EFSA, 2010). Bradley et coll. (2011) ont également testé la migration de la mélamine dans trois types d’aliments différents (les types d’aliments variaient selon l’acidité, la teneur en matières grasses et la présence de viande ou de poisson), dans diverses conditions, et les taux de migration variaient de < 23 µg/kg à 220 µg/kg. Magami et coll. (2015) ont également testé quatre substances de réticulation différentes utilisées dans des revêtements à base d’époxy des boîtes de conserve d’aliments et qui contenaient des quantités résiduelles de mélamine (< 0,1 à 0,2 %). Les revêtements ont été chauffés à la température élevée de 131 °C dans un simulant d’aliment (éthanol aqueux à 10 %) pendant différentes périodes (30 à 180 minutes) suivies de différents délais de stockage (1 à 30 jours), puis réchauffés à 131 °C pendant 1 h. Entre 7 et 60 % (sur une base molaire) de toute la mélamine contenue dans la substance réticulante utilisée avait migré depuis le revêtement. Les auteurs ont pu démontrer que le mécanisme de migration n’est pas la diffusion de la mélamine depuis le revêtement. La mélamine s’est plutôt formée par hydrolyse du revêtement, a été libérée sous forme de mélamine elle-même et n’a pas montré de tendance importante s’hydrolyser vers des analogues tels que l’amméline, l’ammélide ou l’acide cyanurique. Les données susmentionnées montrent que la mélamine peut migrer d’un emballage alimentaire vers les aliments, et que les concentrations résultantes dans les aliments augmenteront si les aliments sont chauffés, comme lors du traitement des boîtes de conserve et des bouteilles contenant des aliments (EFSA 2010).
La mélamine a été mesurée dans de nombreux aliments de nombreux pays, principalement à la suite de la découverte, en Chine, de préparations pour nourrissons altérées par la mélamine et de la déclaration, en Amérique du Nord, d’incidents liés à des aliments pour les animaux (OMS, 2009; Hilts et Pelletier, 2009; Dorne et coll., 2013). Concurremment, il y a eu une demande accrue pour des techniques d’analyse plus rapides, plus sensibles et plus précises pour déterminer les concentrations de mélamine dans ces aliments. Dans de récents examens des progrès des techniques d’analyse pour doser la mélamine dans les aliments et les produits laitiers, on a fait état de limites de détection plus faibles que celles indiquées dans l’étude de Rovina et Siddique (2015) publiée deux ans plus tôt (on est passé de 3,7 × 10-12 à 0,6 ng/g pour les produits laitiers, et à aussi peu que 1 × 10-5 mg/L pour les échantillons d’aliments, comme l’ont indiqué Lu et coll. 2017 et Nascimento et coll. 2017).
Au Canada, les enquêtes visant à mesurer les niveaux de mélamine dans les aliments ont été menées par l’Agence canadienne d’inspection des aliments (ACIA) de 2008 à 2012, principalement pour détecter les concentrations élevées causées par l’altération et pour assurer le respect des niveaux provisoires maximaux de Santé Canada pour la mélamine dans les aliments. Par conséquent, la sélection des échantillons a été biaisée et la méthode a donné des limites de détection relativement élevées. Les données de ces enquêtes n’ont pas été utilisées dans la présente évaluation.
En outre, Santé Canada a réalisé des recherches pour mesurer les concentrations de fond de mélamine dans les aliments vendus au Canada et a analysé 94 échantillons de diverses préparations pour nourrissons en vente (analysés sous la forme « tel qu’acheté »), 246 échantillons de produits laitiers et de produits de substitution à base de soja, et 378 échantillons de produits contenant des œufs, des substituts de viande à base de soja, des produits à base de poissons et des crevettes, et des produits végétaux (Tittlemier et coll. 2009, 2010a, 2010 b). Les enquêtes de Santé Canada étaient axées sur les aliments ayant la plus grande probabilité de contenir des niveaux résiduels de mélamine. Par exemple, des produits laitiers et d’autres produits contenant du lait, des produits végétauxNote de bas de page 2, ainsi que des poissons et des fruits de merNote de bas de page 3.
L’exposition à la mélamine par toutes les sources d’aliments, présentée dans le tableau 8-1, a été estimée selon une approche semi-probabiliste utilisant les concentrations moyennes de mélamine pour chaque type de denrée alimentaire échantillonné par Santé CanadaNote de bas de page 4. Les estimations de l’exposition moyenne et au 95e centile pour les différents groupes d’âge sont indiquées dans le tableau 8-1 (voir l’annexe C pour les concentrations de mélamine et la méthode d’évaluation de l’exposition)Note de bas de page 5.
Groupe d’âge (ans) a |
Moyenne |
95e centile |
|---|---|---|
< 1 |
0,715 |
1 686 |
1 à 4 |
0,464 |
1 200 |
5 à 11 |
0,316 |
1 155 |
12 à 19 |
0,215 |
0,731 |
20 + |
0,209 |
0,803 |
a Chaque catégorie d’âge comprend les deux sexes.
Ensemble, les friandises au chocolat et au café au laitNote de bas de page 6 comptent pour près de 60 % de l’exposition alimentaire à la mélamine estimée pour la population générale. La contribution élevée des friandises au chocolat découle d’un échantillon qui avait une forte concentration de mélamine, augmentant ainsi de façon significative la concentration moyenne de mélamine utilisée pour représenter tout le chocolat (soit 667,2 µg/kg)Note de bas de page 7. Étant donné que l’échantillon présentant une concentration élevée de mélamine peut être une valeur aberrante et que la concentration moyenne de mélamine dans les friandises au chocolat, si on exclut cette valeur, c’est‑à‑dire 4,9 µg/kg, la contribution totale de la mélamine provenant des friandises au chocolat est probablement plus faible.
Il convient de noter que les concentrations de mélamine dues à la migration depuis les emballages alimentaires (< 1,5 à 332 µg/kg) signalées dans les études européennes mentionnées ci-dessus correspondent à la moyenne des valeurs déclarées dans les études canadiennes de surveillance alimentaire (annexe C, plage : < 4 à 667 µg/kg).
8.1.1.6 Lait maternel
Yurdakok et coll. (2014, 2015) ont mesuré la mélamine dans le lait maternel de 77 mères allaitantes en santé à Ankara, en Turquie, de juin à septembre 2010 (les bébés étaient âgés de 3 à 10 jours). Les échantillons de lait maternel (10 mL) de chaque mère ont été analysés par CPLHR, avec une LD et une LQ de 10,6 et 41,6 µg/L respectivement. La mélamine a été détectée dans 16 des 77 échantillons (20,8 %), avec des concentrations allant de 10,1 à 76,4 µg/L (moyenne : 27,1 µg/L, ou entre la LD et la LQ), selon les auteurs. L’indice de masse corporelle n’a pas été pris en compte dans la répartition des concentrations de mélamine (les mères étaient divisées selon leur poids : poids normal, embonpoint et obésité).
Puisqu’aucune donnée canadienne sur la présence de mélamine dans le lait maternel n’a été répertoriée, les données turques ont été utilisées pour la caractérisation de l’exposition. Les estimations de l’apport quotidien chez les nourrissons de 0 à 6 mois, par la mélamine présente dans le lait maternel, sont de 2,7 et 7,6 µg/kg p.c./j pour les concentrations moyenne et maximale, respectivement.
8.1.2 Migration à partir du plastique « melaware »
La mélamine réagit avec le formaldéhyde pour produire un plastique thermodurci appelé « mélamine » ou « melaware » (terme anglais couramment utilisé utile pour distinguer le polymère du monomère) qui peut être utilisé pour fabriquer de la vaisselle ou des ustensiles de cuisine.
Des études portant sur la migration de la mélamine dans les aliments, l’eau et d’autres boissons à partir de la vaisselle de melaware ont été répertoriées. Dans une étude danoise, les concentrations de mélamine migrant dans l’eau depuis des assiettes neuves de melaware (n = 6) et de tasses usagées de cette même matière (n = 11) variaient entre < 1 500 et 2 940 µg/L à des températures de 20 à 95 °C (Lund et Petersen, 2006). Bradley et coll. (2011) ont également analysé la migration depuis des articles en melaware (bols, tasses, etc.) achetés en 2010 dans des magasins de vente au détail en Allemagne, aux Pays-Bas et au Royaume-Uni. Les concentrations de mélamine dans divers types de matrices alimentaires et liquides (sauces tomate, eau, boissons, etc.) allaient de la non-détection à 4 194 µg/kg. Les conditions expérimentales étaient également variées : certains échantillons étaient chauffés à des températures entre 40 et 100 °C, ou mis au micro-ondes, ou encore des échantillons non chauffés ont été exposés à des aliments ou des liquides chauds. Lynch et coll. (2015) ont examiné la migration de la mélamine dans 50 bols pour enfants commandés en ligne et fabriqués en Chine. Lorsque les bols étaient chauffés à une température de 95 °C pendant 30 minutes à dix reprises, la migration moyenne de mélamine dans des solutions de différents pH allait de la non-détection (LD = 4,1 µg/L) à 76,7 µg/L, et les taux de migration les plus élevés ont été constatés avec des solutions de pH 3. Les taux de migration à tous les pH diminuaient de 85 % entre le premier et le dixième épisode de chauffage.
Dans une étude taïwanaise (Chien et coll., 2011), les concentrations de mélamine dans un simulant alimentaire (acide acétique à 3 % ou eau distillée) mesurées dans des échantillons provenant de 25 tasses en melaware variaient entre 30 µg/L (à 20 °C) et 19 030 µg/L (à 90 °C), et la migration était nettement supérieure dans l’acide acétique à 3 % par rapport à l’eau distillée.
Dans une étude malaisienne, les concentrations de mélamine dans l’acide acétique à 3 % ou dans l’eau distillée mesurées dans des échantillons provenant de 246 articles de cuisine en melaware variaient entre 1,31 à 140 µg/L à 25 °C, et 4,05 à 509 µg/L à 100 °C (Chik et coll., 2011). De plus, les concentrations moyennes répertoriées de mélamine migrant dans l’eau ou d’autres boissons depuis la vaisselle en melaware à la température ambiante variaient entre 22 et 30 µg/L (Chik et coll., 2011; Chien et coll. 2011). Ces concentrations étaient à l’intérieur de la plage de concentrations utilisées pour les boissons dans l’évaluation de l’ingestion quotidienne et étaient également inférieures à la concentration moyenne trouvée dans l’eau potable de 50 µg/kg déclarée par l’EFSA (2010).
Selon les études menées sur les aliments et les boissons mentionnées ci‑dessus, les concentrations mesurées dans les aliments chauffés (100 °C) dans de la vaisselle en melaware semblent être considérablement supérieures aux concentrations mesurées dans les aliments laissés à la température ambiante. L’EFSA (2010) a étudié la migration de la mélamine dans les aliments et l’eau à partir de vaisselle en melaware, et a cité certaines des mêmes données que celles mentionnées ci-dessus, ainsi que d’autres données fournies par des pays européens (comme la Finlande, la Chypre, les Pays-Bas). L’EFSA a conclu que la migration de mélamine depuis la vaisselle en melaware est caractérisée par une variabilité élevée, selon divers facteurs comme le procédé de fabrication, les altérations à la surface causées par l’usure, le temps, la température et les conditions d’utilisation, ainsi que les caractéristiques des aliments (acides, aqueux, gras, secs). Par conséquent, une plus grande quantité de résidus de mélamine peut migrer dans les aliments.
L’EFSA a estimé l’exposition à la mélamine par la migration en utilisant des « valeurs de migration typique et élevée » pour les différentes catégories d’aliments. Les deux types de valeurs ont été jugés prudentsNote de bas de page 8. Les concentrations de mélamine estimées par l’EFSA dans chaque type d’aliments après la migration à partir d’un article contenant de la mélamine sont indiquées dans le tableau 8‑2.
Type d’aliments |
Valeur typique |
Valeur élevée |
|---|---|---|
Aliments acides |
1,0 |
5,0 |
Aliments aqueux a |
0,6 |
3,0 |
Aliments gras |
0,2 |
1,0 |
Aliments secs |
0,05 |
0,05 |
a On suppose que ces aliments ont la même masse volumique que l’eau, bien que cela ne soit pas expressément énoncé dans EFSA (2010).
L’exposition à la mélamine découlant de l’utilisation de vaisselle en melaware a été estimée à partir d’hypothèses prudentes, c.-à-d. en supposant que tous les aliments et boissons entrent en contact avec la vaisselle en melaware. Les plus grands taux de migration typique calculés par l’EFSA (aliments acides et aqueux) ont été utilisés pour estimer l’exposition par cette source (voir le tableau 8-2). Bien qu’aucune étude portant sur la migration pour la vaisselle contenant de la mélamine n’ait été répertoriée au Canada, nous supposons que les conditions et les résultats concernant la migration de mélamine depuis cette vaisselle seraient semblables aux données obtenues ailleurs. Enfin, les estimations de l’exposition pour les différents groupes d’âge ont été calculées pour une consommation alimentaire quotidienne estimée par l’EFSA (2006). (Voir le tableau 8-3)
Groupe d’âge |
Consommation d’après le type d’aliment (kg) a |
Poids corporel (kg) b |
Exposition (µg/kg p.c./j) c, d |
|---|---|---|---|
Nourrissons de 6 mois (non nourris au lait maternisé) |
Aliments et boissons pour bébés et préparations commerciales pour nourrissons en poudre = 0,5 |
7,5 |
40 |
Enfants de 1,5 an |
Boissons = 1,33 Aliments solides = 0,67 |
15,5 |
112 |
Adultes |
Boissons = 2 Aliments solides = 1 |
70 |
37 |
a Le scénario de consommation considéré a été tiré de l’EFSA (2006). Les valeurs prises en compte pour les nourrissons de 6 mois sont le 95e centile de la consommation d’aliments et de boissons pour nourrissons trouvés dans le commerce (autres que le lait maternel ou les préparations liquides pour nourrissons) et de préparations en poudre pour nourrissons, valeurs obtenues chez des nourrissons de 6 mois dans le cadre de l’étude Dortmund Nutritional and Anthropometrical Longitudinally Designed [DONALD] (0,5 kg) (Kersting et coll. 1998). Pour les enfants âgés de 1 an et demi, une consommation quotidienne de 1,33 kg de boissons et de 0,67 kg d’aliments solides a été considérée (CEC, 1993). Pour les adultes, une consommation quotidienne de 1 kg d’aliments solides et de 2 kg de boissons a été considérée. On a présumé que les boissons et les aliments ont la même masse volumique que l’eau, mais cela n’est pas expressément mentionné dans EFSA (2006) ni EFSA (2010).
b Poids - nourrissons : 7,5 kg; enfants : 15,5 kg; adultes : 70 kg (Santé Canada, 1998).
c Exposition via le melaware au plus fort taux de migration typique observé pour les aliments acides (1 mg/kg) et les aliments aqueux (0,6 mg/kg) calculée par l’EFSA (2010). Pour les nourrissons de 0 à 6 mois, le taux de migration des aliments acides de 1 mg/kg a été utilisé pour les calculs de l’absorption par les aliments et boissons pour bébés et les préparations pour nourrissons. Pour les enfants d’un an et demi et les adultes, le taux de migration pour les aliments acides de 1 mg/kg a été utilisé pour les calculs de l’absorption par les boissons, et le taux de migration pour les aliments aqueux de 0,6 mg/kg a été utilisé pour les calculs d’absorption des aliments solides.
d Exposition = (migration depuis les articles en melaware vers les matrices alimentaires (mg/kg) × consommation de ce type d’aliments par jour) / poids corporel.
8.1.3 Autres produits de consommation
Comme il est indiqué à la section 4, la mélamine est utilisée dans divers types de produits au Canada. Mentionnons entre autres les peintures, les enduits, les scellants, la mousse utilisée dans les sièges, les dossiers et les matelas, le papier et les tablettes de mélamine thermofusionnés, les tableaux blancs et les panneaux de flocons, l’encre pour impression à jet d’encre, la vaisselle et les ustensiles de cuisine contenant de la mélamine, etc.
On n’a pas évalué l’exposition via les papiers, les tablettes, les tableaux blancs et les panneaux de flocons ni l’encre pour impression à jet d’encre, en raison de divers facteurs (contact limité avec la peau, utilisation commerciale et industrielle, faibles concentrations en mélamine), car cette exposition devrait être faible, particulièrement par rapport aux autres scénarios présentés ci-dessus. De plus, le potentiel d’exposition à la mélamine par la vaisselle a été traité ci-dessus.
Articles de bricolage (peintures, scellants, enduits)
Les fiches de données de sécurité (FDS) pour les produits de peinture vendus au Canada et contenant de la mélamine montrent que la concentration maximale dans les peintures à base d’eau est de 13 % (MSDS 2013; TDS 2011). Des FDS étaient aussi disponibles pour les scellants vendus au Canada pour des utilisations mécanique, électrique et de plomberie qui contiennent de la mélamine. La concentration maximale indiquée était de 60 %Note de bas de page 9. Même si les FDS indiquaient que le produit était destiné à un usage industriel et professionnel seulement, les consommateurs peuvent quand même acheter ces produits chez les détaillants (CSL Silicones Inc. 2014; MSDS 2016).
Nous avons pris en compte les expositions ponctuelles (« par utilisation ») par inhalation et par voie cutanée des utilisateurs d’équipement de peinture en aérosol sans air comprimé, des utilisateurs de brosses et de rouleaux à peinture, et des utilisateurs de scellants et de produits de calfeutrage pour l’intérieur. Nous avons toutefois considéré les preuves disponibles suivantes pour la mélamine :
- En raison de la pression de vapeur négligeable de la mélamine, l’exposition par inhalation découlant de l’utilisation de brosses et de rouleaux à peinture est considérée comme étant négligeable. De plus, l’inhalation découlant de l’utilisation de peinture en aérosol sans air comprimé serait également négligeable puisqu’il est peu probable que cette utilisation produise des gouttelettes pouvant être aspirées par le système respiratoire (le diamètre de la majeure partie des gouttelettes serait supérieur à 15 µm).
- L’administration aiguë par voie cutanée de la mélamine chez des animaux de laboratoire n’a pas entraîné de réactivité cutanée (Fassett et Roudabush 1963; Rijcken 1995; Vernon et coll. 1990), et des composés structurellement similaires ne présentaient que des taux maximaux d’absorption cutanée de 10 à 16 % sur la peau humaine (Ademola et coll. 1993; Baynes et coll. 2005).
- Des études de toxicité aiguë par voie orale, voie cutanée et inhalation ont montré l’absence de critères de dangerosité aigus et préoccupants chez les animaux de laboratoire (BASF 1969a; US NTP 1983; Vernon et coll. 1990; Ubaidullajev et coll. 1993; Muijser 1998; OCDE 2002).
À partir ces éléments ci-dessus, il a été déterminé qu’une seule exposition à la mélamine cutanée et par inhalation découlant de l’utilisation de peinture en aérosol sans air comprimé, de brosses et de rouleaux à peinture ainsi que de scellants et de produits de calfeutrage pour l’intérieur constituait un risque de faible à négligeable pour la population générale du Canada.
Produits en mousse (sièges, matelas, etc.)
Comme il est indiqué à la section « Sources et utilisations », on trouve également la mélamine dans les sièges et la literie en mousse (ce qui peut comprendre également des produits comme les oreillers et les matelas) au Canada. Les concentrations de mélamine dans la mousse utilisée dans les sièges et les dossiers de meubles à charpente métallique étaient de l’ordre de 28 à 29 % (ECCC 2013-2014). Le programme américain CPSC (2005) a analysé six types de mousse pour meubles afin d’en déterminer la teneur en mélamine et a trouvé que les concentrations allaient de la non-détection (LD = 0,005 % p/p) à 34 % p/p. Ces valeurs correspondent aux concentrations de mélamine trouvées dans les meubles et matelas en mousse au Canada (la literie est mentionnée à la section « Sources et utilisations », et peut comprendre des produits comme les oreillers et les matelas). Quatorze sièges d’enfant de différents types et marques fabriqués en 2014 ont également été testés pour déterminer les concentrations de diverses substances ignifuges, dont la mélamine, à l’aide de deux méthodes d’analyse différentes. La mélamine a été détectée dans 3 des 14 sièges, en particulier sous forme de mousse de polyuréthane dans deux sièges et sous forme de mousse de polypropylène expansible ainsi que dans le textile d’un autre siège. La concentration dans les sièges n’a pas été mesurée (Ecology Center 2015). La mélamine a été provisoirement détectée, mais non quantifiée par CPL/spectrométrie de masse à temps de vol avec ionisation par électro-pulvérisation, dans la mousse de polyuréthane et d’autres composants de meubles fabriqués aux États‑Unis entre 2000 et 2015 (Petreas et coll. 2016). Une analyse par CPL‑SM/SM de six échantillons de mousse de polyuréthane de sources canadiennes a indiqué des concentrations de mélamine allant de la non-détection (LD = 0,031 % p/p) à 0,43 % p/p (Santé Canada 2015).
Comme la mélamine est un additif ignifugeant et peut migrer depuis une matrice, une exposition cutanée est possible si la peau entre en contact prolongé avec des meubles ou des matelas en mousse traitée à la mélamine. Cette la substance a pu avoir été transportée par la sueur, car la mélamine est très soluble dans l’eau, mais la migration peut aussi avoir eu lieu par l’intermédiaire de composants cutanés non aqueux, comme les cheveux et la kératine. La valeur log Koe, couramment utilisée comme mesure de l’hydrophobicité, a également été prise en compteNote de bas de page 10. Nous n’avons retrouvé aucune donnée sur la migration de la mélamine. On a plutôt extrapolé les taux de migration de la mélamine à partir des taux de migration en tenant compte de l’hydrosolubilité ou de la combinaison de l’hydrosolubilité et de la valeur log Koe d’autres substances ignifuges, citées dans ECHA (2018) pour le TDCPP (NR CAS 13674-87-8) et le TCEP (NRoCAS 115-96-8), et indiquées dans le tableau 8‑4. ECHA (2018) a utilisé les taux de migration du TDCPP et du TCEP pour estimer l’exposition cutanée potentielle, d’après des études d’exposition portant sur la mousse de meubles traités.
Paramètre |
PTDCP |
PTCE |
Mélamine |
|---|---|---|---|
Solubilité dans l’eau (mg/L) |
18,1 |
7820 |
3230 |
Log Koe (sans unité) |
3,69 |
1,78 |
-1,14 |
Taux de migration depuis la mousse recouverte (mg/cm2/h) a |
0,00297 |
0,0207 |
0,00936 b 0,0217 c |
a Les taux de migration de TDCPP et de TCEP ont été déterminés dans les études de migration réalisées sur de la mousse de meubles traités par l’agence danoise de protection de l’environnement (Danish EPA 2015), comme l’a indiqué l’ECHA (2018). Les taux de migration de TCEP et de TDCPP ont été déterminés pour des produits pour enfants (c.‑à‑d. sièges de retenue d’enfant, porte-bébé, matelas pour bébé) en immergeant des morceaux de mousse provenant de ces produits (habituellement avec une partie du revêtement en tissu faisant partie de l’échantillon) dans une substance simulant la sueur et en les incubant à 37 °C pendant 3 heures (Danish EPA 2015). Le taux de migration du TDCPP utilisé ici est la moyenne des taux trouvés dans tous les échantillons pour cette substance ignifuge, alors que le taux de migration du TCEP provenait d’un seul article (ECHA 2018).
b Valeur calculée en traçant une ligne droite entre les valeurs de solubilité dans l’eau et les taux de migration pour le TDCPP et le TCEP, grâce à l’équation y = (2 × 10-6 × solubilité dans l’eau) + 2,9 ×10-03.
c Valeur calculée à l’aide d’équations quadratiques basées sur les taux de migration du TDCPP et du TCEP, de la solubilité dans l’eau et de log Koe : pour le TDCPP, 0,00297 mg/cm2/h = x(log de la solubilité dans l’eau) + y(log Koe) et pour le TCEP, 0,0207 mg/cm2/h = x(log de la solubilité dans l’eau) + y(log Koe). Ainsi, 0,00297 = x(1,26) + y(3,69) et 0,0207 = x(3,89) + y(1,78). Si on résout pour x et y, on obtient : x = 0,005863 et y = -0,0012. Pour la mélamine, taux de migration = 0,005863 × (log de la solubilité dans l’eau) + (-0,0012) (log Koe) = 0,005863 × (3,51) + (-0,0012) (-1,14) = 0,0217 mg/cm2/h.
Sur cette base, nous avons calculé une fourchette des taux de migration de 0,00936 à 0,0217 mg/cm2/h pour la mélamine. En utilisant cette fourchette, nous avons estimé l’absorption par exposition cutanée pour les enfants et les adultes en contact direct avec des matelas contenant de la mousse et recouverts de tissu, et d’autres articles fabriqués de même type (p. ex., des meubles contenant de la mousse). Ce scénario est jugé représentatif du potentiel d’exposition par les dossiers en textiles sur les meublesNote de bas de page 11. Comme le montre l’annexe D, les estimations de l’exposition cutanée à la mélamine par contact cutané prolongé avec des matelas en mousse ou des meubles contenant de la mousse étaient de 0,02 à 0,36 mg/kg p.c./j et de 0,08 à 1,02 mg/kg p.c./j respectivement chez les adultes et les nourrissons. Enfin, en raison de la pression de vapeur négligeable de la mélamine, l’exposition par inhalation à la mélamine contenue dans les meubles et les matelas en mousse devrait être négligeable.
En raison des propriétés de la mélamine (additif ignifugeant, hydrosolubilité élevée), il est probable que les enfants y soient exposés en portant à la bouche un objet en mousse. Même si des données sur la concentration de mélamine des produits en mousse étaient disponibles, nous n’avons trouvé dans les publications scientifiques aucun taux de migration depuis la mousse portant expressément sur la mélamine. En l’absence de taux de migration établis pour la mise à la bouche d’objets, nous avons appliqué le même taux migration utilisé pour le scénario associé au taux de migration cutané. Comme le montre l’annexe D, les estimations de l’exposition orale à la mélamine par la mise à la bouche d’un objet en mousse sont de 0,00031 à 0,0035 mg/kg p.c./j pour les nourrissons et de 0,00030 à 0,0034 mg/kg p.c./j pour les tout-petits.
8.1.4 Biosurveillance
Panuwet et coll. (2012) ont publié les résultats des mesures de mélamine prises dans 492 échantillons d’urine humaine recueillie auprès de la population générale des États-Unis. Ces échantillons ont été recueillis aux États-Unis en 2003 et 2004 dans le cadre de l’enquête National Health and Nutrition Examination Survey (NHANES) et comprenaient des échantillons provenant de sujets masculins et féminins âgés de 6 ans et plus (USCDC, 2010a). De la mélamine a été détectée dans 76 % des échantillons (population : 6 ans et plus, moyenne géométrique : 2,37 ng/mL, 95e centile : 12 ng/mL, maximum : 161 ng/mL, LD = 0,66 ng/mL)Note de bas de page 12. Comme la répartition relative des groupes d’âge (soit 6 à 11 ans, 12 à 19 ans, etc.) n’était pas disponible dans la publication de Panuwet et coll. (2012), cette information a été tirée des données démographiques recueillies par la NHANES (USCDC, 2010b). Les concentrations de la moyenne géométrique et du 95e centile en fonction des différents groupes d’âge sont présentées dans le tableau 8-5.
En ce qui concerne les données pharmacocinétiques, aucune étude indiquant la fraction de mélamine éliminée dans l’urine humaine n’a été répertoriée. Toutefois, Mast et coll. (1983) ont démontré que 90 % de la mélamine administrée était éliminée sous forme de mélamine dans l’urine des rats mâles. Chez les chiens, Lipschitz et Stokey (1945) ont démontré que 60 à 86,5 % de la mélamine administrée était éliminée sous forme de mélamine dans les 24 heures suivant une dose unique par voie orale de mélamine. Enfin, bien que Liu et coll. (2010) aient suggéré que la quantité éliminée dans l’urine des singes était de beaucoup inférieure à la dose orale, ces auteurs n’ont pas pu présenter de bilan massique pour le profil d’élimination ni indiquer le pourcentage de la dose de mélamine éliminée dans l’urine (voir la section « Évaluation des effets sur la santé, Toxicocinétique par voie orale » et Santé Canada 2018c : annexe B, tableau B-1).
En raison de la variabilité de l’élimination urinaire entre les espèces, le plus faible pourcentage d’élimination de mélamine dans l’urine (60 %; Lipschitz et Stokey, 1945) a été utilisé pour calculer les absorptions relatives à la biosurveillance. De plus, comme on n’a pas obtenu de données sur le volume éliminé dans l’urine de chaque participant, les plages des volumes d’urine moyens pour une période type de 24 heures répertoriées dans diverses sources et indiquées dans le tableau ci-dessous ont aussi été utilisées pour calculer l’absorption (voir l’annexe E pour les plages des volumes d’urine et les références). Les absorptions d’après la biosurveillance sont présentées dans le tableau 8-5.
Groupe d’âge |
6 à 11 ans |
De 12 à 19 ans |
20 à 59 ans |
60 ans et plus |
|---|---|---|---|---|
Moyenne géométrique des concentrations de mélamine dans l’urine (ng/mL) |
5,91 |
2,06 |
2,33 |
2,93 |
Concentration supérieure de mélamine dans l’urine au 95e centile (ng/mL) e |
6,7 |
10,47 |
12,44 |
11,09 |
Nombre de participants a |
6 |
162 |
217 |
107 |
Fourchette des volumes moyens/j d’urine (L/j) b |
0,27–1,14 |
0,44–1,40 |
0,6–2,70 |
0,25–2,4 |
Poids corporel moyen (kg) c |
31,8 |
59,4 |
70,9 |
72,0 |
Absorption moyenne (µg/kg p.c./j) d |
0,08–0,35 |
0,03–0,08 |
0,03–0,15 |
0,02–0,16 |
Absorptions au 95e centile (µg/kg p.c./j) d, e, f |
0,09–0,40 |
0,13–0,41 |
0,18–0,79 |
0,06–0,62 |
a D’après l’âge des participants au moment de prélèvement de l’urine (nombre total : 492).
b Plage des volumes d’urine moyens pour 24 h répertoriées dans la littérature (voir l’annexe E).
c Poids corporels moyens pour les groupes d’âge 12-19, 20-59 et > 60, d’après Santé Canada (1998). Le poids corporel moyen calculé pour les participants âgés de 6 à 11 ans est fondé sur les données de l’USEPA (2011), car Santé Canada (1998) ne répertorie pas les poids corporels pour ce groupe d’âge.
d D’après le plus bas pourcentage d’élimination de mélamine dans l’urine d’animaux de laboratoire 24 heures suivant l’administration de la dose = 60 % (Lipschitz et Stokey, 1945; Mast et coll., 1983; Liu et coll., 2010).
e Chez les enfants de 6 à 11 ans, des concentrations de mélamine urinaire entre 0,5 et 6,7 ng/mL ont été observées chez 5 enfants, alors que cette valeur était de 161 ng/mL pour l’autre participant. En raison de la petite taille des échantillons dans ce groupe d’âge et de la possibilité que l’une des concentrations soit une valeur aberrante, un calcul de l’absorption au 95e centile serait statistiquement instable. Par conséquent, la deuxième concentration la plus élevée a été utilisée pour déterminer la limite d’absorption supérieure.
f Les estimations de l’absorption moyenne et au 95e centile ont été calculées à l’aide de l’équation suivante (Aylward et coll. 2012) :
Absorption quotidienne (µg/kg p.c./j) = [concentration dans l’urine (µg/L) × volume d’urine sur 24 h (L/j)] ÷ [fraction éliminée dans l’urine × p.c. (kg)].
Pour le groupe des 12 ans et plus, les valeurs d’absorption moyennes variaient entre 0,02 et 0,16 µg/kg p.c./j, et les valeurs d’absorption du 95e centile variaient entre 0,06 et 0,79 µg/kg p.c./j. Pour le groupe des 6 à 11 ans, les valeurs d’absorption moyennes variaient entre 0,08 et 0,35 µg/kg p.c./j. En raison de la petite taille des échantillons pour ce groupe d’âge (n = 6), les valeurs d’absorption au 95e centile n’ont pas été calculées, car elles seraient statistiquement instables. De plus, une concentration élevée de 161 ng/mL a été observée dans ce groupe d’âge, alors que les concentrations chez les 6 autres participants variaient entre 0,5 et 6,7 ng/mL. Panuwet et coll. (2102) n’ont pas indiqué si cette valeur élevée était un artefact.
D’autres études portant sur la biosurveillance ont été menées à Taïwan et à Hong Kong (voir l’annexe F), mais on a utilisé les résultats fondés sur la population des États-Unis mesurés par Panuwet et coll. (2012) comme données de substitution pour la population canadienne et ont été jugés les plus pertinents.
8.2 Évaluation des effets sur la santé
Nous résumons ici les renseignements sur les effets de la mélamine sur la santé. On trouvera de plus amples renseignements dans la documentation d’appui (Santé Canada 2018c). En termes de classification, le Centre international de recherche sur le cancer (CIRC 2019) a classé la mélamine dans le Groupe 2B (possiblement cancérogène pour les humains)Note de bas de page 13.
8.2.1 Toxicocinétique par voie orale
La mélamine a été excrétée dans l’urine de rats et de singes après l’administration de doses uniques de 1,3 et 1,4 mg/kg p.c., respectivement. Cependant, en plus de la mélamine non modifiée, les deux métabolites suivants ont été détectés chez le rat et le chien, après une dose orale importante de 250 mg/kg p.c. et de 125 mg/kg p.c. respectivement : monophosphate de dimélamine et mono-oxalate de monomélamine. De plus, selon des études toxicocinétiques poussées sur des rats, la mélamine n’a pas été métabolisée à faibles doses (comparativement à des doses plus élevées, 1,3 par rapport à 250 mg/kg p.c.), ce qui indique qu’une exposition orale à des niveaux écologiques de mélamine peut ne pas se métaboliser dans le corps. Chez les rats auxquels on a administré une dose de 1,3 mg/kg p.c./j, les calculs de bilan massique ont indiqué que 98 % de la dose avait été récupérée sous forme de mélamine 96 heures après l’administration de la dose, confirmant l’absence de métabolisme (Mast et coll., 1983). Chez les trois singes ayant reçu par gavage oral une dose de 1,4 mg/kg p.c., la quantité éliminée dans l’urine des singes était bien inférieure à la dose orale, mais les auteurs n’ont pu présenter un bilan massique pour le profil d’élimination ni indiquer les pourcentages de la dose de mélamine éliminée dans l’urine, car la mélamine n’avait pas été radiomarquée dans cette étude (Liu et coll. 2010).
Il semble y avoir une saturation de l’élimination à une dose orale de 100 mg/kg p.c./j. Avoir administré des doses de 100 mg/kg p.c. à des rats Sprague‑Dawley (SD), Wu et coll. (2010 b) ont écrit : « Environ 63,2 % de la dose administrée a été récupéré dans l’urine dans les 96 h. L’étude précédente indiquait une valeur d’élimination de 90 % (à une dose de 1,3 mg/kg p.c.) dans les 24 premières heures (Mast et coll. 1983), et cette différence pourrait résulter d’une dose beaucoup plus élevée (100 mg/kg p.c.) dans notre étude, ce qui pourrait entraîner la saturation de l’élimination urinaire et l’élimination différée dans le temps. Ce résultat laisse à penser que la plus grande partie de la dose de mélamine administrée a été absorbée et éliminée dans l’urine, sans être modifiée. »
La biodisponibilité orale de la mélamine variait de 73 ± 13 % à 98 % chez le rat, ce qui confirme une absorption orale élevée et rapide dans le tractus gastrointestinal (Yang et coll. (2009), et de Wu et coll. (2010 b). Des études réalisées par Yang et coll. (2009), Wu et coll. (2010 b) et Pang et coll. (2013) indiquent que la mélamine ne se répartit pas largement dans la plupart des tissus chez le rat après une dose unique par voie orale ou répétée pendant 14 jours à 100 mg/kg p.c., la mélamine se retrouvant surtout dans le sang. Plusieurs auteurs ont fait état de demi-vies d’élimination plasmatique allant de 1,3 à 5 h dans diverses études chez le rat et le singe après l’administration de doses uniques par voie orale de 1 à 100 mg/kg p.c. (Wu et coll. 2010 b; Jacob et coll. 2012, Dorne et coll. 2013, et Pang et coll. 2013). Dorne et coll. (2103) ont considéré que ces taux étaient comparables aux présentes doses orales et, dans tous les cas, étaient en accord avec l’observation indiquant une élimination rapide de la mélamine dans l’urine.
Wang et coll. (2103) ont réalisé une étude de toxicocinétique à doses répétées chez les porcs. Des porcs ont reçu de la mélamine dans leur alimentation à des doses de 0, 18 ou 35 mg/kg p.c./j pendant 42 jours, avec une période de récupération de 5 jours. On a constaté une augmentation des concentrations résiduelles de mélamine, liée à la dose, dans tous les tissus mesurés (plasma, encéphale, duodénum, foie, cœur, muscle et reins), et la concentration de mélamine dans les reins était nettement plus élevée que dans les autres tissus (p < 0,01), et les concentrations de résidus dans les tissus diminuaient après le retrait de la mélamine. Après 42 jours à 35 mg/kg p.c./j, la demi‑vie était de 9,90 h, avec un volume de distribution à l’équilibre de 1,07 L/kg. Bien que cette demi‑vie soit légèrement plus longue que les autres demi‑vies signalées pour d’autres espèces, cette étude confirme également que la mélamine était principalement éliminée par filtration rénale. Les auteurs ont indiqué que la clairance de la mélamine dans cette étude était conforme à celle observée chez les porcs ayant reçu des doses uniques par voie intraveineuse (0,076 L/h/kg dans cette étude par rapport à 0,061 L/h/kg) dans l’étude réalisée par Baynes et coll. (2008).
Chu et coll. (2013) ont réalisé une étude de toxicocinétique chez des rattes gravides et des rats en développement. Ils ont administré la mélamine aux femelles gravides par gavage à une dose unique de 24 mg/kg p.c. le 10e, le 15e ou le 20e jour de gestation (JG), et aux petits par gavage pendant la 2e, la 4e, la 6e ou la 8e semaine postnatale (respectivement 2SPN, 4SPN, 6SPN ou 8SPN). Comme l’ont indiqué les auteurs, la distribution de la mélamine dans le sérum maternel était environ 30 % plus élevée en fin de grossesse qu’en début de grossesse et elle était deux fois plus élevée dans le sérum postnatal chez les tout-petits précoces que chez les jeunes adultes (2SPN par rapport à 4SPN – 8SPN). La répartition de la mélamine dans les organes après la naissance était plus élevée que dans les organes avant la naissance. Chez les petits, les reins après la naissance présentaient la concentration maximale et le plus faible taux d’élimination de mélamine par rapport aux autres organes après la naissance (Cmax = 10,85 mg/kg par rapport à 1,06, à la dose de 2,36 mg/kg, et l’élimination apparente = 0,62 L par heure par rapport à 1,85 à 2,75 L par heure pour le foie, les poumons, le cœur, le cerveau et la rate, respectivement à 2SPN). La distribution accrue de la mélamine dans le sérum et les reins des jeunes rats de 2 semaines par rapport aux autres stades de vie semble indiquer un risque accru de toxicité due à la mélamine pour les reins après la naissance, selon Chu et coll. (2013). Les études sur la toxicité pour le développement de Kim et coll. (2011) et Stine et coll. (2014; voir la section « Études de toxicité pour le développement et la fertilité ») ont révélé une toxicité pour les reins chez les femelles gravides à des doses orales de 800 et 1000 mg/kg p.c./j de mélamine. Toutefois, aucune toxicité pour les reins n’a été observée chez les fœtus à ces doses (bien que d’autres effets fussent constatés) et les mères n’ont pas pu mener leur gestation à terme.
L’EFSA (2010) a également rapporté une preuve indirecte que la mélamine n’est pas métabolisée chez les humains. Dans une étude dans laquelle de l’hexaméthylmélamine marquée au 14C a été administrée à des humains oralement, 5 % de la dose d’hexaméthylmélamine (marqué au 14C) a été éliminée sous forme de mélamine dans l’urine, mais aucun métabolite de la mélamine n’a été détecté. Les auteurs ont mené la même étude chez des rats auxquels ils ont administré une dose intrapéritonéale d’hexaméthylmélamine (le cycle étant marqué au 14C). Dans ce cas, 2 % de la dose d’hexaméthylmélamine marquée au 14C a été éliminée sous forme de mélamine dans l’urine, mais aucun métabolite de mélamine n’a été détecté. Dans l’étude sur les rats comme dans celle sur les humains, seulement 5 % de la radioactivité urinaire n’a pas été détectée.
L’EFSA (2010) a résumé les données toxicocinétiques pour les animaux de laboratoire et d’élevage et pour les humains, et la description générale de la toxicocinétique de la mélamine est conforme aux conclusions des études récentes mentionnées ci‑dessus : 1) les études sur les animaux indiquent que la mélamine est rapidement absorbée par le tractus gastrointestinal et rapidement éliminée de l’organisme avec une demi‑vie dans le plasma de quelques heures à plusieurs heures; 2) l’urine est la principale voie d’élimination, et les données limitées disponibles indiquent que la substance est à peine métabolisée à des doses pertinentes pour l’environnement.
8.2.2 Cancérogénicité et toxicité chronique
Dans une étude d’une durée de deux ans, on a ajouté de la mélamine à l’alimentation de rats F344, à raison de doses de 0, 126 ou 262, et 0, 263 ou 542 pour les mâles et les femelles respectivement. Des carcinomes transitionnels sont apparus dans la vessie des rats mâles à une fréquence beaucoup plus élevée (présence ≤ 0,016) dans le groupe ayant reçu une dose élevée (8/49) que dans le groupe témoin (0/45). On a aussi observé une association statistiquement significative (p < 0,001) entre les calculs vésicaux (chez 10 mâles sur 49) et les tumeurs dans la vessie chez les rats mâles ayant reçu des doses élevées de mélamine dans leurs aliments. Aucune tumeur dans la vessie n’a été détectée chez les rats mâles ayant reçu une faible dose de mélamine (126 mg/kg p.c./j), alors que des calculs vésicaux ont été détectés chez un seul de ces 50 rats du groupe ayant reçu une faible dose (US NTP 1983; Melnick et coll., 1984). En raison de l’association statistiquement importante entre les calculs et les tumeurs dans la vessie à une dose élevée (263 mg/kg p.c./j), l’histopathologie de cette étude a été ré-évaluée. Les résultats ont indiqué une augmentation importante de néphropathies de reflux chez les rats mâles [7 sur 50 par rapport à 1 sur 49 témoins], mais aucune augmentation des calculs vésicaux [1 sur 50 par rapport à 1 sur 45 témoins] à une dose de 126 mg/kg p.c./j (Hard et coll., 2009), ce qui confirme l’absence de tumeurs à cette dose.
Dans une autre étude menée pendant deux ans chez des rats d’une lignée non spécifiée, on a ajouté à leur alimentation des doses de 0, 67 ou 667 mg/kg p.c./j. Une augmentation de la fréquence de calculs urinaires dans la vessie associée à une fréquence accrue de papillomes bénins à la dose maximale a été signalée (American Cyanamid 1955).
On a ajouté de la mélamine à l’alimentation de rats F344 pendant 24 à 30 mois, à raison de doses de 0, 5/5, 25/50 ou de 50/100 mg/kg p.c./j pour les mâles et les femelles respectivement. Aucune fréquence accrue de tumeurs de la vessie n’a été observée. Bien qu’à des doses de 5 mg/kg p.c./j et plus, une tendance liée à la dose a été observée sous forme d’une dilatation des muqueuses gastriques glandulaires et d’inflammation des muqueuses gastriques non glandulaires, on n’a pas pu préciser si cette tendance s’appliquait à un seul ou aux deux sexes. Toutefois, la source secondaire a indiqué que la DSEO serait la dose élevée (Hazleton Laboratories, 1983; cité dans : OCDE, 2002).
Deux études de 36 semaines ont été réalisées sur des rats F344 mâles. Dans la première étude, les animaux ont reçu la mélamine dans leurs aliments à raison de 0, 110, 367 ou 1100 mg/kg p.c./j (Okumura et coll. 1992), et dans l’autre, ils ont reçu la mélamine dans leurs aliments à des doses de 0, 430 ou 1200 mg/kg p.c./j (Ogasawara et coll. 1995). Dans les deux études, on a observé une augmentation liée à la dose de la fréquence de carcinomes à cellules transitionnelles des voies urinaires dans la vessie et de papillomes de la vessie, lesquels ont été associés à une augmentation liée à la dose de la fréquence de l’hyperplasie papillaire/nodulaire de l’épithélium de la vessie. Ces augmentations, ainsi qu’une augmentation non liée à la dose de calculs vésicaux, ont permis de déterminer une DMENO de 110 mg/kg p.c./j dans l’étude d’Okumura et coll. (1992). Okumura et coll. (1992) ont observé une corrélation statistique importante entre l’apparition de calculs vésicaux et des tumeurs, et ont conclu que les calculs causés par la mélamine peuvent produire des carcinomes dans la vessie. Ogasawara et coll. (1995) ont déterminé que les calculs vésicaux sont composés d’une proportion molaire égale de mélamine et d’acide urique, et ont conclu que les lésions proliférantes dans la voie urinaire des rats F344 mâles étaient directement causées par la stimulation irritante des calculs et non par les interactions moléculaires entre la mélamine ou ses métabolites et l’épithélium de la vessie.
Pendant 103 semaines, on a ajouté de la mélamine à l’alimentation de souris B6C3F1 à des doses de 0, 327 ou 523 ou de 688 ou 1065 mg/kg p.c./j pour les mâles et les femelles respectivement, puis pendant les deux semaines suivantes, elles n’ont reçu aucune mélamine. Une inflammation et une hyperplasie aiguës et chroniques de la vessie, ainsi que des calculs vésicaux, ont été observées chez les souris mâles à toutes les doses et chez les femelles à la dose élevée. Aucun effet cancérogène n’a été observé dans cette étude (US NTP 1983; Melnick et coll., 1984).
En résumé, cinq études de cancérogénicité ont été menées chez des rats et une chez des souris. Dans tous les cas, de la mélamine a été administrée aux animaux par l’alimentation. Dans quatre des études sur le rat, on a observé des tumeurs de la vessie ou des papillomes pour des doses allant de 263 à 1200 mg/kg p.c./j. Des doses plus faibles (5 à 100 mg/kg p.c./j) avaient été administrées lors de l’ature étude. Aucun effet cancérogène n’a été observé dans l’étude sur les souris exposées à la mélamine par l’alimentation pendant deux ans à des doses variant entre 327 et 1 065 mg/kg p.c./j.
8.2.3 Génotoxicité
De nombreuses études in vitro ont été menées sur la génotoxicité de la mélamine. Les résultats ont été négatifs dans toutes les études de mutation génique dans les cellules bactériennes (Salmonella typhimurium, Photobacterium phosphoreum, Saccharomyces cerevisiae) et de mammifères (lymphome de souris et ovaire de hamster chinois [CHO]), les tests d’aberration chromosomique et l’échange de chromatides sœurs dans les cellules CHO, une étude de micronoyau à l’aide de cellules CHO et des études de synthèse de l’ADN non programmé dans des hépatocytes de rats et des cellules bactériennes (E. coli et S. typhimurium) (Seiler 1973; Litton Bionetics 1977a, 1977 b, 1977c; American Cyanamid Co. 1981; American Cyanamid Co. 1982a, 1982b; Mast et coll. 1982b; Haworth et coll. 1983; Mirsalis et coll. 1983; Galloway et coll. 1987; Zeiger 1987; McGregor et coll. 1988; Elmore and Fitzgerald 1990; Ishiwata et coll. 1991; Selden et coll. 1994; Yasunaga et coll. 2004; Tu et coll. 2015). Un test non standard, qui a mesuré l’induction du prophage lambda dans l’E. coli comme indicateur de dommages à l’ADN, était positif avec et sans activation métabolique (Rossman et coll., 1991). Un test des comètes a été réalisé sur l’eucaryote unicellulaire, Tetrahymena thermophila. On a constaté une augmentation liée à la dose du pourcentage de dommages à l’ADN, du pourcentage de cellules avec queue et d’unités arbitraires de dommages à l’ADN à toutes les doses, mais l’augmentation était statistiquement significative à 2 000 et 4 000 mg/L. Comme le montre le tableau 7-1, une CI50 a également été signalée pour cet organisme (Li et coll. 2015).
Les études in vivo réalisées avec deux tests de micronoyaux (des souris avaient reçu de la mélamine par gavage oral et injection intrapéritonéale), plus un essai combinant un test de mutation du gène Pig-a (administration de mélamine à des rats par gavage oral) ont donné des résultats négatifs pour ce qui est des aberrations chromosomiques dans la moelle osseuse et le sang périphérique des souris et aucune différence significative dans les fréquences de micronoyaux ou dans les fréquences de mutation du gène Pig-a dans les globules rouges ou les réticulocytes des rats (Pharmakon Research 1981; Mast et coll. En 1993; Tu et coll. 2015). En général, la base de données sur la génotoxicité indique que la mélamine n’est pas génotoxique.
8.2.4 Mode d’action cancérogène
Le mode d’action concernant les tumeurs observées n’a pas été totalement éclairci. On a toutefois émis l’hypothèse que les tumeurs malignes de la vessie dépendent d’un mécanisme de seuil qui est causé par l’hyperplasie réactive qui se développe en réponse à une irritation localisée des tissus, puis qui se transforme en néoplasie de la vessie, et les essais standards confirment que le manque d’activité mutagène ou génotoxique y contribue, selon l’OMS (2009). L’OMS (2009) a également observé qu’une minéralisation des papilles rénales a été répertoriée dans certaines études, mais on ignore si une telle minéralisation peut se détacher et former un foyer pour la formation des calculs vésicaux.
8.2.5 Toxicité par voie orale à doses répétées
En plus des études de toxicité chronique ou de cancérogénicité, de nombreuses études de toxicité par voie orale à doses répétées ont été menées chez des rats, des souris, des lapins, des chats et des chiens, sur des périodes s’étendant entre 7 jours et 36 semaines. Dans une étude sur l’exposition par les aliments par voie orale pendant 7 jours menée sur des rats, des cristaux épars ont été observés dans les tubules rénaux à la dose d’essai de 200 mg/kg p.c./j (Jacob et coll., 2011). Dans des études de 14 jours par voie orale chez le rat (une étude par gavage, l’autre par le régime alimentaire), une étude n’a relevé aucun effet à la dose d’essai maximale de 240 mg/kg p.c./j (Kobayashi et coll. 2010), et l’autre a montré la présence de solides cristallins durs dans la vessie des mâles et des femelles à des doses de 835 et 1668 mg/kg p.c./j et plus, respectivement (les deux sexes avaient reçu des doses de 0, 417, 835, 1251, 1668 ou 2500 mg/kg p.c./j). Cette étude a trouvé une DSENO de 417 mg/kg p.c./j (US NTP 1983). Chez les souris mâles ayant reçu de la mélamine par gavage, on a observé une altération de la morphologie des spermatozoïdes et des dommages à l’ADN des testicules à 412 mg/kg p.c./j après une période d’exposition de 5 jours (à noter que les cellules germinales mâles n’ont pas été utilisées dans les études décrites sous la rubrique « Génotoxicité »), et on a observé une augmentation de l’indice apoptotique des cellules spermatogènes à 50 mg/kg p.c./j après une période d’exposition de 14 jours (Yin et coll. 2013)Note de bas de page 14. Bischoff (2017) mentionne cette étude et d’autres études chez la souris qui font état de dommages à la barrière hémato-testiculaire après l’ingestion orale de mélamine, y compris des effets sur les tubules séminifères, ainsi que sur le développement, la production et la morphologie des spermatozoïdes. Des études récentes réalisées sur des souris mâles exposées par voie orale à de la mélamine pendant des périodes de 28 et 65 jours, respectivement, ont indiqué qu’une dose de 50 mg/kg p.c./j donnait lieu à des signes cliniques de toxicité, des modifications de la structure cellulaire des testicules et à des effets plus graves sur les paramètres du sperme, la synthèse de la testostérone, les enzymes testiculaires et les concentrations de protéines qu’aux doses plus faibles (Sun et coll. 2016a; Khalil et coll. 2017).
Des études d’une durée de 28 jours chez le rat ont permis d’observer une hausse en fonction de la dose, des calculs urinaires de la vessie (contenant de la mélamine) et de l’hyperplasie (l’étude n’indque pas quels tissus), de la cristallurie et l’élimination de l’urine acide à des doses de 266 à 12 678 mg/kg p.c./j de mélamine (RTI 1982; American Cyanamid Co. 1984), ainsi que des déficits d’apprentissage et de mémoire dans une étude au cours de laquelle les rats avaient reçu par gavage de la mélamine à raison de 300 mg/kg p.c./j (An et coll. 2011; Yang et coll. 2011). Dans une autre étude de 28 jours sur des rats, la microstructure des reins a été endommagée et les paramètres de chimie clinique ont été nettement modifiés dans le sérum (azote uréique dans le sang, créatinine), dans les reins (glutamate, lactate, choline, glucose, acide aminé, 3‑hydroxybutyrate, pyruvate), dans le foie (n‑acétylglycoprotéine, choline, créatine, lactate, triméthylamine‑n‑oxyde, glutamate, glucose), et dans l’urine (succinate, citrate) à des doses de 250 à 1000 mg/kg p.c./j. Cette étude métabolomique a montré que la mélamine provoquait un dysfonctionnement rénal et perturbait le métabolisme du glucose, des protéines et de l’azote dans le foie (Sun et coll. 2012). Dans des études d’alimentation par voie orale, RTI (1982) a trouvé une DSENO de 133 mg/kg p.c./j, tandis qu’aucun effet indésirable n’avait été observé aux doses de 40 à 357 mg/kg p.c./j dans l’autre étude (American Cyanamid Co. 1984). Après 28 jours, d’administration de mélamine par gavage à des rates, n’a observé aucune lésion toxique dans les reins à 40 mg/kg p.c./j, mais constaté une hausse du nombre de follicules atrétiques, de modifications morphologiques et de nécrose dans les ovocytes et les cellules de la granulosa, ainsi qu’un nombre accru de cellules de la granulosa apoptotiques dans les ovaires à cette dose. Toutesfois, la santé générale des animaux n’a pas été affectée (Sun et coll. 2016 b).
Pour d’autres espèces, les doses testées ont permis d’observer : i) aucun effet nocif chez les chats traités à des doses pouvant aller jusqu’à 181 mg/kg p.c./j dans une étude sur l’exposition par les aliments sur 11 jours (Puschner et coll., 2007), ii) aucun effet nocif suivant l’administration de 126 mg/kg p.c./j (seule dose d’essai) dans une étude sur les lapins et les chiens sur 1 à 4 semaines (Lipschitz et Stokey, 1945a, b), et iii) une DSENO de 3 000 mg/kg p.c./j d’après la présence de solides cristallins observés dans les vessies de souris ayant reçu une dose de 6 000 mg/kg p.c./j lors d’une étude par gavage oral sur 14 jours (US NTP 1983).
Des études à court terme ont été réalisées sur la souris afin d’analyser la relation entre l’hyperplasie de la vessie et les calculs. On a ajouté de la mélamine à l’alimentation de souris mâles et femelles âgées de 4 semaines ou de 5 à 6 semaines à des doses de 0 ou 9 373 ppm, équivalant à 0 ou 1 218,5 mg/kg p.c./j, respectivement (conversion des doses selon Santé Canada 1994) pendant 14 jours, ou pendant 14 jours avec des périodes de récupération allant de 4 ou 8 jours (souris de 5 à 6 semaines) à 42 jours (souris de 3 à 4 semaines). Un autre groupe de souris âgées de 3 à 4 semaines a reçu de la mélamine dans l’alimentation aux mêmes doses pendant 56 jours, ou pendant 56 jours avec une période de récupération de 42 jours. La fréquence de l’hyperplasie épithéliale et des calculs vésicaux était de 100 % pour tous les groupes traités sans aucune période de récupération. La régression de l’hyperplasie épithéliale et des calculs vésicaux (qui s’est produite par le vieillissement rapide et l’apoptose des cellules dans les régions superficielles des tissus liés à la régression de l’hyperplasie épithéliale de la vessie) a été observée de façon plus prononcée et plus fréquente chez les souris ayant reçu une dose pendant 14 jours avec 8 jours de récupération par rapport à 4 jours de récupération seulement, et ces taux étaient importants (60 à 63 %) et/ou une régression complète (38 à 40 %) a été observée chez toutes les souris ayant reçu une dose pendant 14 ou 56 jours avec 42 jours de récupération. Lors de la régression rapide, les calculs vésicaux ont complètement disparu. La régression de l’hyperplasie épithéliale de la vessie a commencé dès le retrait de la mélamine (Sun et coll. 2014).
Trois études différentes de l’exposition par les aliments de rats sur 13 semaines ont permis d’observer des augmentations liées à la dose des calculs vésicaux, à des doses variant entre 63 et 1500 mg/kg p.c./j chez les deux sexes, ainsi qu’une augmentation des dépôts calcaires dans les tubules proximaux des reins. La DMENO la moins élevée était de 63 mg/kg p.c./j (plus basse dose d’essai) selon les effets mentionnés ci-dessus. La fréquence relative des calculs vésicaux chez les deux sexes n’a pas été modifiée lorsque les rats ont reçu une dose de 1500 mg/kg p.c./j par le régime alimentaire, selon que l’on ait ajouté ou non 1 % de chlorure d’ammonium dans l’eau potable (US NTP 1983; Melnick et coll. 1984). Deux études de 36 semaines sur des rats mâles ayant reçu des doses variant entre 110 à 1200 mg/kg p.c./j ont permis d’observer une augmentation liée à la dose de l’hyperplasie de l’épithélium de la vessie, une augmentation non liée à la dose des calculs vésicaux, ainsi qu’une diminution de la prise de poids corporel à des doses de 430 mg/kg p.c./j et plus (Okumura et coll., 1992; Ogasawara et coll., 1995). Des études de toxicité subchronique ont été menées chez d’autres espèces et des effets ont été constatés aux doses d’essai : i) 1600 mg/kg p.c./j (dose minimale d’essai) d’après la diminution du poids corporel des mâles dans une étude par alimentation orale de 13 semaines chez la souris (US NTP 1983; Melnick et coll. 1984), et ii) 1 200 mg/kg p.c./j (seule dose utilisée dans l’essai) d’après une cristallurie observée après une période de 60 à 90 jours dans une étude d’alimentation d’un an chez le chien (American Cyanamid Co. 1955).
8.2.6 Études de toxicité pour le développement et la fertilité
Trois études de toxicité pour le développement par voie orale chez le rat étaient disponibles, ainsi qu’un résumé d’une étude de toxicité pour les mères chez le lapin. Chez des rates gravides gavées à la mélamine pendant les jours de gestation 6 à 20, une toxicité pour le développement et maternelle a été observée à la dose maximale de 800 mg/kg p.c./j (diminution du poids des fœtus, fréquence accrue des variations squelettiques et ossification fœtale différée; chez les mères, on a observé une fréquence accrue des signes cliniques et des décès, une diminution de la prise de poids corporel et une toxicité rénale). Aucune toxicité pour le développement et les mères n’a été observée aux doses plus faibles (200 et 400 mg/kg p.c./j) (Kim et coll., 2011). Des rates gravides ont été gavées à la mélamine du 10e au 20e jours de gestation et des femelles non gravides ont été gavées pendant 10 jours consécutifs à une dose de 1 000 mg/kg p.c./j. Dans les deux cas, les effets comportaient des signes cliniques de toxicité (apathie, réticence à faire sa toilette, anorexie), une diminution de la prise de poids corporel, une augmentation du poids des reins et des lésions rénales (dilatation tubulaire accompagnée d’une nécrose cellulaire), ce qui correspondait bien à la fréquence des calculs rénaux, et on a trouvé de la mélamine dans le liquide amniotique des rates gravides. Les effets sur le développement comprenaient une hausse des morts fœtales précoces et tardives et une baisse de la taille des portées, du poids moyen des fœtus et de la longueur totale moyenne tête-naissance de la queue (Stine et coll., 2014). Chez des rates gravides auxquelles on a donné de la mélamine durant les jours de gestation 6 à 16, aucune toxicité pour le développement n’a été observée, mais une toxicité maternelle a été observée à la dose maximale de 1060 mg/kg p.c./j (diminution du poids corporel, sang dans l’urine, flancs renfoncés) (Hellwig et coll., 1996). Un résumé d’une étude de toxicité maternelle chez le lapin a montré des effets à 250 et 400 mg/kg p.c./j (1/6 femelles à chaque dose présentait des signes cliniques de toxicité et une diminution de la prise de poids corporel), et aucun effet à 120 mg/kg p.c./j; aucun effet sur le développement n’a été signalé (BASF 2018b). Bischoff (2017) rapporte une étude de toxicité pour la reproduction dans laquelle le nombre moyen de descendants a diminué chez les souris gravides exposées à 50 mg/kg p.c./j dans l’eau potable, mais l’article original de Duan et coll. (2015) ne fournit pas suffisamment de détails sur le protocole et seules 4 mères/groupes traités et groupes témoins, respectivement, ont été utilisées.
Comme il est indiqué dans la section « Toxicité par voie orale à doses répétées », certaines études à doses répétées ont trouvé des effets sur les testicules et les ovaires. Plusieurs études de toxicité à doses roales répétées chez les souris mâles ont montré des effets sur les tubules séminifères, le développement, la production et la morphologie des spermatozoïdes, les cellules spermatogènes, la synthèse de la testostérone, les enzymes testiculaires et les concentrations de protéines à la dose de 50 mg/kg p.c./j pour des périodes allant de 14 à 65 jours. Une étude par voie orale de 28 jours sur des rates a montré des effets sur les ovaires (ovocytes et cellules de la granulosa et un nombre accru de follicules atrétiques) à la dose de 40 mg/kg p.c./j. Une étude de 17 semaines sur l’exposition par inhalation chez le rat a démontré un trouble de la fonction hépatique et des effets sur les paramètres de biochimie sanguins à des concentrations de mélamine de 0,058 et 0,5 mg/m³. Des rats ont été accouplés après la période d’exposition de 17 semaines et des effets ont été observés chez les animaux qui avaient été exposés à 0,5 mg/m³ de mélamine (effets sur la spermatogenèse et la fertilité, et décès observés) (Ubaidellajev et coll., 1993). En raison des renseignements limités sur le protocole d’étude dans la traduction anglaise de cette étude russe, son utilité a été jugée limitée pour la caractérisation des risques.
Pour résumer, l’évaluation de la toxicité pour le développement a montré une concentration d’effet critique de 800 mg/kg p.c./j de mélamine chez le rat pour la toxicité pour le développement et les mères, mais aucune étude validée de toxicité pour la reproduction n’a été trouvée. Bien que des effets potentiels sur les ovaires et les testicules aient été observés à 40 et 50 mg/kg p.c./j respectivement, on s’attend à ce que la LICDR de 35 mg/kg p.c./j, d’après l’exposition chronique par voie orale à la mélamine, assurera une protection contre tout effet potentiel sur les organes reproducteurs.
8.2.7 Sensibilisation
La mélamine n’était pas un sensibilisant cutané pour les cobayes (Fassett et Roudabush, 1963). Cette étude est la seule traitant de la sensibilisation cutanée chez les animaux de laboratoire que nous avons trouvée.
Nous avonstrouvé un certain nombre de rapports sur des cas de sensibilisation chez des humains en milieu de travail, ainsi qu’une étude sur des travailleurs volontaires. Autant dans l’étude sur les travailleurs volontaires que dans les rapports de cas, les patients qui souffraient d’allergie au contact de produits contenant de la mélamine-formaldéhyde n’ont pas réagi au test épicutané avec la mélamine seulement (Soubrier et Burlet 1972; Fregert 1981; Isaksson et coll. 1999; Aalto-Korte et coll. 2003; Garcia-Gavin et coll. 2008).
8.2.8 Études épidémiologiques
Li et coll. (2010) on mené une vaste étude rétrospective cas-témoins humains dans laquelle ils ont comparé 683 enfants atteints de lithiase rénale (présence de calculs rénaux) à 6 498 enfants n’en souffant pas, âgés de 3 ans et moins dans les hôpitaux de Beijing, ainsi que leur exposition à la mélamine par des préparations pour nourrissons altérées. Dans cette étude, les enfants ont été exposés à 4 des 22 marques de préparations pour nourrissons altérées par la mélamine vendues à Beijing, et ils faisaient partie d’un plus grand échantillon couvrant la ville, soit 41 000 enfants, dans le cadre d’une enquête sur l’état de la santé et de l’alimentation des enfants. En général, la valeur ajustée des rapports des cotes entre la dose de mélamine et la lithiase rénale augmentait avec l’absorption d’une doses quotidienne accrue de mélamine (de 1,7 à 11,3 pour l’ingestion quotidienne de mélamine de > 0 à 0,2 mg/kg p.c./j à > 102,4 mg/kg p.c./j), et augmentait également en fonction de la prolongation de l’exposition. Chez les enfants exposés à des concentration de mélamine de < 0,2 mg/kg p.c./j, la valeur ajustée des rapports des cotes exprimant le risque de lithiase rénale était 1,7 fois plus élevée que chez les enfants non exposés à la mélamine (Li et coll., 2010; EFSA, 2010). Cette étude présente plusieurs limites (voir la section « Incertitudes de l’évaluation des risques pour la santé humaine »).
Une étude cas-témoins a été menée sur des enfants et des femmes enceintes à Hong Kong. Pour le premier projet, 152 femmes enceintes ont été recrutées en 2008, soit 74 ayant des antécédents d’exposition à des produits alimentaires contaminés à la mélamine et 78 témoins de même âge n’ayant aucun antécédent de consommation de produits alimentaires contaminés à la mélamine. L’exposition quotidienne médiane du groupe exposé à la mélamine était de 0,0015 (écart de 0,0001 à 0,08 mg/kg p.c./j). Lorsqu’on a comparé les échantillons des 20 patientes ayant le taux d’exposition à la mélamine le plus élevé à ceux de 20 témoins, aucune différence importante dans les concentrations de mélamine n’a été observée dans tous les échantillons biologiques (urine maternelle [médiane = 1,3 par rapport à 1,2 µg/mmol de créatinine chez les témoins], sang [médiane < 5 ppb pour les deux groupes], placenta, lait maternel [médiane < 50 ppb pour les deux groupes], liquide amniotique et sang ombilical; urine néonatale [médiane < 5 ppb pour les deux groupes]).
Dans le deuxième projet, on a tenté de déterminer l’utilité de la lipocaline associée à la gélatinase des polynucléaires neutrophiles (NGAL) dans l’urine comme marqueur de substitution pour la détection précoce des lésions rénales, mais aucune différence significative dans les concentrations de NGAL n’a été constatée chez 302 enfants de moins de 12 ans ayant subi une exposition prolongée à des produits laitiers contaminés par la mélamine (> 0,2 mg/kg p.c./j) qui présentaient des anomalies urinaires persistantes ou des caractéristiques cliniques évoquant des maladies rénales, et chez 203 témoins appariés en fonction de l’âge et qui n’avaient pas d’antécédents de consommation de produits laitiers contenant de la mélamine (Wong et coll. 2013).
8.2.9 Mécanismes non cancérogènes de toxicité
En ce qui concerne les paramètres non cancérogènes, les mécanismes potentiels de toxicité sur l’appareil urinaire et les autres systèmes physiologiques ont été examinés dans certaines études. Le mécanisme proposé de néphrotoxicité induite par la mélamine comprend l’induction de stress oxydatif et une réaction inflammatoire provoquée par les calculs rénaux (EFSA, 2010; Chu et Wang, 2013; Rai et coll., 2014). La section « Toxicocinétique par voie orale » montre qu’il existe un potentiel de distribution accrue de la mélamine dans le sérum et les reins des jeunes animaux de laboratoire par rapport à l’exposition à la mélamine à d’autres stades de vie, y compris les animaux gravides. Dorne et coll. (2013) ont indiqué que les effets sur le développement ou les effets neurotoxiques surviennent à des doses supérieures ou subséquentes à celles qui causent une néphrotoxicité induite par la mélamine.
8.3 Caractérisation du risque pour la santé humaine
À la lumière principalement des évaluations réalisées par des organismes internationaux (OMS 2009 et EFSA 2010) et des données disponibles, les effets critiques associés à l’exposition à la mélamine sont la cancérogénicité et des effets sur le système urinaire. Des preuves indiquent que ces effets ne sont pas causés par la mélamine en soi, mais à sa propension à former des calculs ou des cristaux dans les reins ou la vessie, et c’est l’effet irritant de ces calculs qui causent d’autres effets, comme une hyperplasie réactive et des tumeurs de la vessie chez les rats.
Les renseignements disponibles indiquent que la mélanine n’est pas génotoxique et qu’il existe un mécanisme seuil pour la cancérogénicité propre aux reins.
La DMENO globale la plus basse a été établie dans une étude par le régime alimentaire de 13 semaines chez des rats Fischer 344, dans laquelle une augmentation liée à la dose de la fréquence des calculs vésicaux et une augmentation des dépôts calcaires dans les reins (non liée à la dose) ont été observées chez les animaux ayant reçu de la mélamine dans leurs aliments à toutes les doses testées, la plus basse étant de 63 mg/kg p.c./j (US NTP 1983; Melnick et coll. 1984). De plus, comme le montre la discussion sur la cancérogénicité dans la section « Évaluation des effets sur la santé », une réévaluation des données histopathologiques dans l’étude de 2 ans chez le rat semble indiquer qu’une durée d’exposition accrue à la mélamine à des doses inférieures à celle à laquelle des tumeurs de la vessie ont été observées (263 mg/kg p.c./j) n’entraîne pas de cancérogénicité. Par conséquent, une évaluation quantitative de la cancérogénicité n’est pas nécessaire.
L’OMS (2009) a calculé une dose repère et la limite inférieure de son intervalle de confiance (LICDR10), d’après cette étude de 13 semaines sur l’exposition par voie orale, soit 44,6 et 35 mg/kg p.c./j respectivement, pour une fréquence accrue de 10 % des effets observés (urolithiase et hyperplasie de l’épithélium de la vessie). L’OMS (2009) a ensuite calculé une dose journalière admissible (DJA) de 0,2 mg/kg p.c./j à partir de la LICDR10 de 35 mg/kg p.c./j combinée à un facteur d’incertitude totale de 200, qui comprend un facteur de 100 pour la variabilité interspécifique et intraspécifique et un facteur d’incertitude supplémentaire de 2 pour « tenir pleinement compte de la sensibilité accrue potentielle des enfants et des incertitudes relatives aux données ». On a jugé que la DJA obtenue pour la mélamine pouvait être appliquée à toute la population, y compris les nourrissons. En 2008, au moment de l’incident mettant en cause des préparations pour nourrissons altérées par la mélamine, le Centre de collaboration de l’OMS pour la surveillance de la contamination des aliments au sein de la Direction des aliments de Santé Canada a participé à la rencontre des experts en toxicologie de l’OMS pour examiner la mélamine et ses analogues associés. Cette consultation a recommandé une DJA de mélamine de 0,2 mg/kg p.c./j, recommandation appuyée par Santé Canada.
L’EFSA (2010) a aussi calculé une LICDR10 et la limite inférieure de son intervalle de confiance d’après la même étude, mais a appliqué des hypothèses différentes de celles de l’OMS (2009) aux modèles de dose repère, ce qui a produit des valeurs légèrement différentes (41 et 19 mg/kg p.c./j respectivement, pour une fréquence accrue de 10 % des effets observés). L’EFSA (2010) a calculé la même DJA de 0,2 mg/kg p.c./j pour la mélamine à partir de ces données, avec un facteur d’incertitude par défaut de 100 (EFSA, 2010).
Le groupe d’experts de l’EFSA a aussi calculé une dose repère en fonction de l’étude épidémiologique de Li et coll. (2010). Il a calculé une BMD10 de 1,1 mg/kg p.c./j et une LICDR10 de 0,74 mg/kg p.c./j pour une fréquence accrue de 10 % des lithiases rénales. En raison des incertitudes que présentaient le plan d’étude et les estimations d’exposition, les données n’ont pas été jugées suffisamment fiables par l’EFSA pour être utilisées comme base pour calculer une DJA. Cependant, l’EFSA a jugé que la LICDR10 pour les humains de 0,74 mg/kg p.c./j était une preuve suffisante quant à la pertinence de la DJA de 0,2 mg/kg p.c./j calculée à partir des données sur les animaux (EFSA, 2010). Les données de l’étude épidémiologique n’étaient pas disponibles lorsque la DJA de l’OMS a été calculée (OMS, 2009).
La LICDR10 orale de 35 mg/kg p.c./j calculée par l’OMS (2009) est jugée appropriée pour caractériser les risques de l’exposition par voie orale chronique à la mélamine, puisqu’elle repose sur l’étude ayant présenté la DMENO la plus faible à 63 mg/kg p.c./j, et elle prévient la formation de calculs ou de cristaux, car les études à long terme menées sur l’exposition par les aliments chez le rat ont montré que les tumeurs de la vessie apparaissent à une dose de 263 mg/kg p.c./j de mélamine. Comme les tumeurs de la vessie semblent résulter d’une progression d’événements (passant de l’hyperplasie de la vessie à l’irritation et à la néoplasie) dus à l’exposition orale à la mélamine, cette LICDR assure également la protection contre les événements précurseurs.
Des études récentes à court terme chez le rat et la souris ont montré des effets sur les ovaires et les testicules à des DMEO orales de 40 et 50 mg/kg p.c./j, respectivement. Cependant, l’évaluation de la toxicité pour le développement a montré un niveau d’effet critique de 800 mg/kg p.c./j de mélamine chez le rat pour la toxicité maternelle et pour le développement (aucune étude validée de toxicité pour la reproduction n’a été trouvée). On s’attend à ce que la LICDR de 35 mg/kg p.c./j due à l’exposition chronique par voie orale à la mélamine assure la protection contre tout effet potentiel sur les organes reproducteurs.
Les principales sources d’exposition à la mélamine de la population générale au Canada devraient être l’utilisation de produits offerts aux consommateurs, les aliments et les milieux naturels. Compte tenu de la justification présentée à la section 9.1 (pression de vapeur négligeable, faible absorption cutanée, faible toxicité aiguë, etc.), on estime que l’exposition par voie cutanée et par inhalation à la mélamine due à l’utilisation de produits de bricole constitue un risque négligeable. Par conséquent, les marges d’exposition n’ont pas été calculées pour ces produits.
La comparaison de la tendance centrale et de la limite supérieure de l’estimation de l’absorption par les milieux naturels et les aliments, dans le cas des nourrissons nourris au lait maternisé (groupe le plus exposé), avec la LICDR10 de 35 mg/kg p.c./j, donne des marges d’exposition entre 1522 et 5833. Ces marges d’exposition sont jugées adéquates pour compenser les incertitudes dans les bases de données sur les effets sur la santé et l’exposition. Voir le tableau 8-6.
La comparaison de l’estimation de la limite supérieure de l’exposition des tout-petits via le melaware avec les résultats de la LICDR10 donne une marge d’exposition de 313. En raison de la nature prudente des hypothèses (c.-à-d. tous les aliments, ainsi que l’eau et les boissons, consommés seraient chauds et auraient été en contact avec de la vaisselle de melaware), l’exposition via l’utilisation de melaware devrait être inférieure et cette marge d’exposition est jugée adéquate pour compenser les incertitudes dans la base de données sur l’exposition et les effets sur la santé. Voir le tableau 8-6.
Scénario |
Estimation de l’exposition (mg/kg p.c./j) |
Marge d’exposition basée sur la LICDR10 de 35 mg/kg p.c./ |
|---|---|---|
Exposition par l’environnement et par les aliments pour les nourrissons de moins d’un an. |
0,0060 a (0,023) b |
1 522 (5 833) b
|
Exposition alimentaire fondée sur l’hypothèse que la vaisselle en melaware est utilisée comme source principale (enfants de 1 à 4 ans) |
0,112 c |
313 |
Exposition globale d’après les données de biosurveillance d (Enfants de 12 à 19 ans) |
0,00041 |
85 400 |
Exposition globale d’après les données de biosurveillance d (Adultes de 20 à 59 ans) |
0,00079 |
44 300 |
Exposition globale d’après les données de biosurveillance d (Adultes de 60 ans +) |
0,00062 |
56 500 |
a Total des estimations moyennes de l’exposition par l’environnement et les aliments (valeurs moyennes pour l’eau potable additionnées à la valeur moyenne pour l’ingestion quotidienne par les aliments pour les nourrissons selon l’annexe B).
b Il s’agit de la valeur limite supérieure basée sur les valeurs limites supérieures de l’absorption par les aliments et l’eau potable présentées dans le tableau B-1 de l’annexe B.
c Estimation tirée du tableau 8-3; comprend l’exposition aux aliments et aux boissons.
d Voir le tableau 9-5 pour de plus amples renseignements.
La biosurveillance de l’absorption donne une idée de l’exposition par l’ensemble des voies et sources potentielles. Les plus fort taux d’absorption de mélamine, d’après les données de biosurveillance urinaire dans la population américaine étaient de 0,41, 0,79 et 0,62 µg/kg p.c./j pour les groupes d’âge de 12 à 19 ans, 20 à 59 ans et les 60 ans et plus respectivement. Les marges d’exposition fondées sur ces valeurs d’absorption se situent entre 44 300 et 85 400 (voir le tableau 8-6). Même si les valeurs d’absorption obtenues par la biosurveillance ont aussi été calculées pour le groupe d’âge des 6 à 11 ans, en raison de la petitesse de l’échantillon (n = 6) et de l’incertitude associée à toutes les statistiques à partir desquelles elles ont été calculées, nous n’avons pas généré de marges d’expostion pour ces valeurs.
On a également tenu compte de l’exposition par voie cutanée aux produits en mousse et de l’exposition par voie orale des nourrissons et des tout-petits qui portent à la bouche des produits en mousse contenant de la mélamine, car les concentrations de mélamine dans les sièges et la literie en mousse ont été rapportées (voir la section « Évaluation de l’exposition »). Aucune étude sur la toxicité par exposition cutanée à doses répétées n’a été répertoriée, par conséquent l’étude de l’exposition par les aliments sur 13 semaines chez le rat, qui est à la base du calcul de la LICDR10 de 35 mg/kg p.c./j, a été utilisée pour la caractérisation des risques dus à l’exposition par voie orale et cutanée à la mélamine. Les marges pour l’exposition découlant des produits en mousse sont indiquées au tableau 8-7.
Scénario d’exposition |
Voie d’exposition et durée |
Estimation de l’exposition |
Niveau d’effet critique |
Type et durée de l’étude |
Marges d’exposition |
|---|---|---|---|---|---|
Mise à la bouche d’un objet en mousse (Nourrisson) |
Orale – long terme |
0,0051 à 0,0118 mg/kg p.c./j |
LICDR10 = 35 mg/kg p.c./j |
Exposition par les aliments, 13 semaines, rat |
2 970 à 6 860 |
Mise à la bouche d’un objet en mousse (Tout‑petit) |
Orale – long terme |
0,0049 à 0,0114 mg/kg p.c./j |
LICDR10 = 35 mg/kg p.c./j |
Exposition par les aliments, 13 semaines, rat |
3 070 à 7 140 |
| Position assise ou étendue sur un meuble ou un matelas en mousse (Nourrisson) | Cutanée – long terme |
0,08 à 1,02 mg/kg p.c./j |
LICDR10 = 35 mg/kg p.c./j |
Exposition par les aliments, 13 semaines, rat |
34 à 438 |
| Position assise ou étendue sur un meuble ou un matelas en mousse (Tout-petit) | Cutanée – long terme |
0,06 à 0,78 mg/kg p.c./j |
LICDR10 = 35 mg/kg p.c./j |
Exposition par les aliments, 13 semaines, rat |
45 à 583 |
| Position assise / étendue sur un meuble / matelas en mousse (Enfant) | Cutanée – long terme |
0,04 – 0,54 mg/kg p.c./j |
LICDR10 = 35 mg/kg p.c./j |
Exposition par les aliments, 13 semaines, rat |
65 à 875 |
| Position assise / étendue sur un meuble / matelas en mousse (Adolescent) | Cutanée – long terme |
0,03 – 0,47 mg/kg p.c./j |
LICDR10 = 35 mg/kg p.c./j |
Exposition par les aliments, 13 semaines, rat |
75 à 1 170 |
| Position assise / étendue sur un meuble / matelas en mousse (Adulte) | Cutanée – long terme |
0,02 à 0,36 mg/kg p.c./j |
LICDR10 = 35 mg/kg p.c./j |
Exposition par les aliments, 13 semaines, rat |
97 à 1 750 |
Étant donné les valeurs d’exposition à la mélamine estimées à partir de données de biosurveillance humaine et les hypothèses prudentes utilisées dans la modélisation de l’exposition par voie cutanée à la mélamine présente dans les matelas ou les meubles contenant de la mousse et avec lesquels les adultes sont en contact, les marge d’exposition sont jugées adéquates pour compenser les incertitudes dans les bases de données sur l’exposition et les effets sur la santé.
Étant donné que ces marge d’exposition sont basées sur la LICDR10 (qui représente une augmentation de 10 % de la fréquence des effets observés aux doses les plus élevées dans l’étude de 13 semaines par voie orale chez le rat), les marges d’exposition pour les enfants (y compris les nourrissons, les tout-petits et les jeunes jusqu’à 18 ans) dues à l’utilisation de produits de consommation, en particulier par l’exposition cutanée à la mélamine contenue dans les matelas ou meubles en mousse avec lesquels ils sont en contact, sont jugées potentiellement inadéquates pour tenir compte des incertitudes dans les bases de données sur l’exposition et les effets sur la santé. Bien que les marges d’expositions établies à partir des données de biosurveillance humaine soient plus élevées que l’exposition par voie cutanée à la mélamine contenue dans les matelas ou les meubles en mousse, les données de biosurveillance ont été jugées insuffisantes pour établir des marges d’exposition pour les groupes d’âge de moins de 12 ans. C’est un point important, car les habitudes des enfants et des nourrissons sont différentes de celles des adultes, et les données obtenues avec des animaux de laboratoire indiquent que l’exposition à la mélamine peut être plus grande aux premiers stades de vie. En outre, dans la section « Toxicocinétique par voie orale », nous décrivons une distribution accrue de la mélamine dans le sérum et les reins chez des rats de 2 semaines par rapport à des rats plus âgés (notamment des rates gravides et des rats de 2 à 8 semaines qui ont reçu de la mélamine). De plus, il existe plusieurs incertitudes dans les données de biosurveillance, car l’absorption de la mélamine n’a pas été mesurée directement, mais calculée de manière rétrospective à partir de données de biosurveillance urinaire, et les calculs de l’absorption étaient basés sur des données obtenues chez des animaux de laboratoire, car on ne disposait pas de données toxicocinétiques chez les humains (il est à noter qu’une estimation quantitative de 60 % a été utilisée pour déterminer le taux d’élimination urinaire le plus faible de la mélamine, d’après les données obtenues chez des rats et des chiens, mais Liu et coll. (2010) ont présenté des renseignements qualitatifs indiquant un taux d’élimination urinaire beaucoup plus faible chez les singes).
8.4 Incertitudes de l’évaluation des risques pour la santé humaine
Les principales sources d’incertitude sont présentées dans le tableau ci-dessous.
Source clé d’incertitude |
Effet |
|---|---|
Aucune donnée canadienne sur les concentrations dans l’eau potable, le lait maternel ou la poussière ou le sol n’était disponible. |
+ |
Les données sur les concentrations dans l’eau du robinet, le lait maternel et la poussière ou le sol étaient basées sur des échantillons de petite taille (les concentrations moyennes ou maximales ont été utilisées). |
+/– |
Des hypothèses sur la fréquence et le type de melaware utilisé dans l’évaluation de l’exposition au melaware. |
+ |
Les études épidémiologiques ont signalé l’absorption de mélamine. Ces valeurs n’ont pas été mesurées, mais calculées rétrospectivement à partir des données de consommation, et certaines présentaient d’autres limites (p. ex., EFSA [2010] a noté que dans Li et coll. [2010], le recrutement des enfants avait été fait en deux phases au lieu d’une seule, la population de référence pouvait être définie de plusieurs façons et il n’y avait pas d’information concernant la distribution des niveaux d’exposition individuels lors de l’agrégation des données d’exposition en intervalles d’exposition). |
+/– |
Détermination de la consommation de mélamine pour les adultes et les jeunes sur la base d’échantillons d’urine provenant d’une population non canadienne (États‑Unis), y compris des hypothèses concernant les voies d’exposition, la durée d’exposition par rapport au moment de l’échantillonnage, et la variabilité des volumes d’urine quotidiens entre les individus et chez ceux‑ci. |
+/– |
Hypothèse selon laquelle toute la mélamine mesurée dans l’urine est associée à une exposition directe à la mélamine. |
+ |
Hypothèse selon laquelle les concentrations de mélamine dans l’urine humaine représentent un taux d’élimination de 60 % de la dose journalière (en raison du manque de données toxicocinétiques chez les humains). |
+/– |
Études très limitées sur les dangers dus à l’exposition par voie cutanée et par inhalation. |
+/– |
Absence d’une valeur d’absorption cutanée chez les humains pour la mélamine. |
+/– |
Manque de données empiriques sur la relation entre le taux de migration de la mélamine à partir de la mousse et sa concentration dans la mousse. |
+/– |
Importance inconnue de l’effet du revêtement textile sur la migration de la mélamine depuis la mousse de polyuréthane. |
+/– |
Nous présumons que la mousse de polyuréthane était prise en compte dans l’estimation de l’exposition par contact cutané avec la mousse. |
– |
Aucun facteur de contact cutané propre à la mélamine n’a été trouvé. Nous avons émis l’hypothèse d’un facteur de 1. |
+ |
Données limitées sur l’occurrence de la coexposition à la mélamine et à l’acide cyanurique, et sur les paramètres toxicologiques connexes. |
+/– |
+ : incertitude quant au potentiel de surestimer de l’exposition/risque; – : incertitude quant au potentiel de sous-estimer l’exposition/risque; +/– : potentiel inconnu pour ce qui est de surestimer ou de sous-estimer le risque.
En ce qui concerne la dernière ligne du tableau ci‑dessus, le risque de coexposition chronique à la mélamine et à l’acide cyanurique est inconnu en raison de la fréquence limitée de cette coexposition et du peu de données toxicologiques (pour de plus amples renseignements sur l’acide cyanurique, voir Santé Canada 2018c).
9. Conclusion
Compte tenu de toutes les sources de données disponibles présentées dans la présente ébauche d’évaluation préalable, la mélamine présente un faible risque d’effets nocifs pour l’environnement. Il est proposé de conclure que la mélamine ne répond pas aux critères énoncés aux alinéas 64a) ni b) de la Loi canadienne sur la protection de l’environnement (1999), car elle ne pénètre pas dans l’environnement en une quantité, à une concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, et à mettre en danger l’environnement essentiel pour la vie.
Pour les nourrissons, les tout-petits et les jeunes (jusqu’à 18 ans), la comparaison des concentrations liées aux effets critiques dans les études sur les animaux et les estimations de l’exposition par contact avec des matelas ou des meubles en mousse et contenant de la mélamine sont jugées potentiellement inadéquates pour lever les incertitudes dans les bases de données sur l’exposition et les effets sur la santé. Pour tous les autres types d’expositions (par les milieux naturels, les aliments et l’utilisation de produits de consommation, pour tous les groupes d’âge), les comparaisons des concentrations associées aux effets critiques dans des études sur les animaux et des estimations de l’exposition ont été jugées adéquates pour compenser les incertitudes dans les bases de données sur les effets sur la santé et l’exposition. Compte tenu du caractère potentiellement inadéquat des marges entre les estimations de l’exposition et les niveaux d’effets critiques constatés chez les animaux de laboratoire dans le cadre de la présente actualisation de l’ébauche d’évaluation préalable, il est proposé de conclure que la mélamine satisfait aux critères de l’alinéa 64c) de la LCPE, car elle pénètre ou peut pénétrer dans l’environnement en une quantité ou à une concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Il est donc proposé de conclure que la mélamine satisfait à un ou plusieurs des critères énoncés à l’article 64 de la LCPE. Il est également proposé que la mélamine satisfait au critère de persistance, mais non au critère de bioaccumulation, au sens du Règlement sur la persistance et la bioaccumulation pris en vertu de la LCPE.
Références
Aalto-Korte K, Jolanki R, Estlander T. 2003. Formaldehyde-negative allergic contact dermatitis from melamine-formaldehyde resin. Contact Dermatitis. 49(4):194-196. (Disponible en anglais seulement.)
[ABC Laboratories] Analytical Bio-Chemistry Laboratories Inc. (Columbia, Missouri). 1988. Acute toxicity of CT-338-87 to Daphnia magna. Final report no.: 36645. Rapport non publié parrainé par l’American Cyanamid Company (Wayne, New Jersey). 60 p. [accès restreint] (Disponible en anglais seulement.)
ACD/Percepta. 2005. Prediction Module. Toronto (ON), Advanced Chemistry Development. [Consulté le 4 nov. 2013.] (Disponible en anglais seulement.)
[ACIA] Agence canadienne d’inspection des aliments. 2010. 2009-2010 Résidus de mélamine dans le lait de consommation, les produits à base de lait et les produits à base de soja. Résumé. Le rapport complet est disponible sur demande auprès de l’ACIA.
[ACIA] Agence canadienne d’inspection des aliments. 2011. 2010-2011 Mélamine dans les produits à base de lait et à base de soja. Résumé. Le rapport complet est disponible sur demande auprès de l’ACIA.
[ACIA] Agence canadienne d’inspection des aliments. 2012. 2011-2012 Mélamine dans des aliments sélectionnés. Résumé. Le rapport complet est disponible sur demande auprès de l’ACIA.
Ademola JI, Sedik LE, Wester RC, Maibach HI. 1993, In vitro percutaneous absorption and metabolism in man of 2-chloro-4-ethylamino-6-isopropylamine-s-triazine (Atrazine). Arch Toxicol. 67:85-91. (Disponible en anglais seulement.)
American Cyanamid Co. 1955. Melamine: acute and chronic toxicity, Report 55-21, données non publiées. [Cité dans OCDE 2002.] (Disponible en anglais seulement.)
American Cyanamid Co. 1981. Données non publiées. Study number: Raltech Study No. 81560. [Cité par OCDE 2002.] (Disponible en anglais seulement.)
American Cyanamid Co. 1982a. Données non publiées. Numéro du rapport : PH 319-AC-002-82. Date du rapport : 1982-05-20. [Cité dans OCDE 2002.] (Disponible en anglais seulement.)
American Cyanamid Co. 1982 b. Données non publiées. Numéro du rapport : Study No. PH 311-AC-002-82. [Cité dans OCDE 2002.] (Disponible en anglais seulement.)
American Cyanamid Co. 1984. Study. [Cité dans US EPA 1984.] (Disponible en anglais seulement.)
An H, Li X, Yang Q, Wang D, Xie T, Zhao J, Xu Q, Chen F, Zhong Y, Yuan Y, Zeng G. 2017. The behavior of melamine in biological wastewater treatment system. J Hazard Mater. 322:445-453. (Disponible en anglais seulement.)
An L, Li Z, Yang Z, Zhang T. 2011. Cognitive deficits induced by melamine in rats. Toxicol Lett. 206:276-280. (Disponible en anglais seulement.)
Andersen WC, Sherri B. Turnipseed SB, Christine M. Karbiwnyk CM, Evans E, Hasbrouck N, Mayer TD, Gieseker CM, Nochetto C, Stine CB, Reimschuessel R. 2011. Bioaccumulation of melamine in catfish muscle following continuous, low-dose, oral administration. J Agric Food Chem. 59:3111-3117. (Disponible en anglais seulement.)
Andersen WC, Turnipseed SB, Karbiwnyk CM, Clark SB, Madson MR, Gieseker CM, Miller RA, Rummel NG, Reimschuessel R. 2008. Determination and confirmation of melamine residues in catfish, trout, tilapia, salmon, and shrimp by liquid chromatography with tandem mass spectrometry. J Agric Food Chem. 2008(56):4340-4347. (Disponible en anglais seulement.)
[AOPWIN] Atmospheric Oxidation Program for Microsoft Windows [estimation model]. 2010. Ver. 1.92a. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. (Disponible en anglais seulement.)
Aylward LL, Kirman CR, Adgate JL, McKenzie LM, Hays SM. 2012. Interpreting variability in population biomonitoring data: Role of elimination kinetics. J Expo Sci Environ Epidemiol. 22:398-408. (Disponible en anglais seulement.)
Base de données sur les ingrédients de produits de santé naturels (BDIPSN). [Modifié le 21 juin 2017.] Ottawa (Ont.), gouvernement du Canada. [Consulté en juillet 2017.]
BASF 1969a. BASF AG, Department of Toxicology; données non publiées (XIX/5), 23.04.1969. [Cité dans OCDE 2002 et Commission européenne 2000.] Remarque : BASF 1969b est cité dans la documentation d’appui (Santé Canada 2018c). (Non disponible en français.)
BASF 1969b. BASF AG, Department of Toxicology; données non publiées (XIX/5), 23.04.1969. [Cité dans OCDE 2002 et Commission européenne 2000.] Remarque : BASF 1969b est cité dans la documentation d’appui (Santé Canada 2018c). (Non disponible en français.)
BASF 2012. GPS safety summary: melamine. BASF. [Consulté le 1er nov. 2013.] Remarque : Recherche de « melamin » dans le site Web. (Non disponible en français.)
BASF 2018b. Notice in Accordance with CEPA Section 70: Results of a maternal toxicity test with CASRN 108-78-1. Section 70 submission to Environment and Climate Change Canada, 5 Nov. 2018. 1 page. Remarque : BASF 2018a est cité dans la documentation d’appui (Santé Canada 2018c). (Non disponible en français.)
Baynes RE, Yeatts JL, Brooks JD, Riviere JE. 2005. Pre-treatment effects of trichloroethylene on the dermal absorption of the biocide, triazine. Toxicol Lett. 159:252-260. (Disponible en anglais seulement.)
Baynes, RE, Smith G, Mason SE, Barrett E, Barlow BM, Riviere JE. 2008. Pharmacokinetics of melamine in pigs following intravenous administration. Food Chem Toxicol. 46:1196–1200. (Disponible en anglais seulement.)
[BDIPSN] Base de données sur les ingrédients de produits de santé naturels. [Modifié le 10 août 2016.] Ottawa (Ont.), gouvernement du Canada. [Consulté le 24 avril 2014.]
[BDPP] Base de données sur les produits pharmaceutiques. [Modifiée le 17 févr. 2017.] Ottawa (Ont.), gouvernement du Canada. [Consulté en mars 2017.]
Bischoff K. 2017. Melamine and cyanuric acid. In: Gupta RC, editor. Reproductive and developmental toxicology, 2nd ed. Academic Press, Copyright Elsevier. p. 493-501. (Disponible en anglais seulement.)
Boethling, RS, Howard, PH, Beauman, JA, Larosche, ME. 1995. Factors for intermedia extrapolations in biodegradability assessment. Chemosphere. 30(4):741-752. (Disponible en anglais seulement.)
Bradley EL, Castle L, Day JS, Ebner I, Ehlert K, Helling R, Koster S, Leak J, Pfaff K. 2010. Comparison of the migration of melamine from melamine-formaldehyde plastics ("melaware") into various food simulants and foods themselves. Food Addit Contam Part A Chem Anal Control Expos Risk Assess. 27(12):1755-1764. (Disponible en anglais seulement.)
Bradley EL., Castle L., Day JS, Leak J. 2011. Migration of melamine from can coatings cross-linked with melamine-based resins, into food simulants and foods. Food Addit Contam Part A Chem Anal Control Expo Risk Assess. 28(2):243-250. (Disponible en anglais seulement.)
Canada, ministère de l’Environnement. 2013. Loi canadienne sur la protection de l’environnement (1999) : Avis concernant certaines substances ignifuges organiques [PDF], Gazette du Canada, Partie I, vol. 147, nº 13, p.613–633.
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999), L.C., 1999, ch. 33, Gazette du Canada, Partie III, vol. 22, nº 3.
CATALOGIC [environmental fate and ecotoxicity model]. 2012. Ver. 5.11.6. Bourgas (BG): University “Prof. Dr. Assen Zlatarov”, Laboratory of Mathematical Chemistry. (Disponible en anglais seulement.)
[CEC] Commission of the European Communities, food-science and techniques. 1993. Nutrient and energy intakes for the European Community. Reports of the Scientific Committee for Food (thirtyfirst series) [Cité dans EFSA 2006 et EFSA 2010; date de 2003 incorrecte, car la référence est EFSA 2010.] (Disponible en anglais seulement.)
[CIRC] Centre international de Recherche sur le Cancer. 1999. Melamine [PDF]. In: Some chemicals that cause tumours of the kidney or urinary bladder in rodents and some other substances. IARC Monogr Eval Carcinog Risks Hum. 73: 329–338. (Disponible en anglais seulement.).
[CIRC] Centre international de Recherche sur le Cancer. 2019. Melamine. In: Some chemicals that cause tumours of the urinary tract in rodents. IARC Monogr Eval Carcinog Risks Hum. 119: 115–172. (Disponible en anglais seulement.)
[CHRIP] Chemical Risk Information Platform (Japan). c2008- . Data Analysis Division, Chemical Management Center, National Institute of Technology and Evaluation, Japan. (Non disponible en français.)
Codex Alimentarius. 2018. Norme générale pour les contaminants et les toxines présents dans les produits de consommation humaine et animale, CXS 193-1995.
Commission européenne. 2000. IUCLID Dataset, Melamine, CAS No. 108-78-1 [Internet.] Année 2000, édition sur CD-ROM. [lieu inconnu]: European Chemicals Agency, Commission européenne. [Créée le 18 févr. 2000.] L’hyperlien n’est plus disponible. Voir IUCLID6 et rehercher le fichier « .i6z » sur la mélamine. (Disponible en anglais seulement.)
Commission européenne. 2011. The rapid alert system for food and feed (RASFF). 2011 Annual Report [PDF]. Luxembourg, Office des publications officielles des communautés européen, 48 p. (Disponible en anglais seulement.)
Cook AM, Beilstein P, Grossenbacher H, Hütter R. Ring cleavage and degradative pathway of cyanuric acid in bacteria. 1985. Biochem J. 231:25-30. (Disponible en anglais seulement.)
Crews GM, Ripperger W, Kersebohm DB, Guthner T, Mertschenk B. circa (c)2012. Melamine and Guanamines. In: Ullmann’s Encyclopedia of Industrial Chemistry. Vol. 22. Weinheim (DE): Wiley-VCH Verlag GmbH & Co. KGaA. pp. 377-392. (Disponible en anglais seulement.)
Crews GM, Ripperger W, Kersebohm DB, Voirholzer J, Güthner T, Mertschenk B. 2005. Melamine and guanamines. In: Ullmann’s encyclopedia of industrial chemistry. Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA. 17 pp. (Disponible en anglais seulement.)
CSL Silicones Inc. [internet.] 2014. Fiches signalétiques et techniques pour CSL 557/558/559 Flame Retardant Silicone Sealant [Consulté en avril 2014.] L’hyperlinen pour ces produits n’est plus disponible. Voir CSL Silicones Inc. (Disponible en anglais seulement.)
ChemIDplus [database]. 1993–. Bethesda (MD): National Library of Medicine (US). [Consulté le 19 nov. 2013.] Remarque : Recherche pour la mélamine ou le NR°CAS 108-78-1. (Disponible en anglais seulement.)
Cheminfo Services Inc. 2012. Use profile characterization for certain organic flame retardants under the Chemicals Management Plan. Préparé pour Environnement Canada. 123 pp. (Non pour distribution). (Disponible en anglais seulement.).
Chien CY, Wu CF, Liu CC, Chen BH, Huang SP, Chou YH, Chang AW, Lee HH, Pan CH, Wu WJ. et coll. 2011. High melamine migration in daily-use melamine-made tableware. J Hazard Mater. 188:350-356. (Disponible en anglais seulement.)
Chik Z, Mohamad Haron DE, Ahmad ED, Taha H, Mustafa AM. 2011. Analysis of melamine migration from melamine food contact articles. Food Addit Contam Part A Chem Anal Control Expo Risk Assess. 28(7):967-973. (Disponible en anglais seulement.)
Chu CY, Chu KO, Ho CS, Kwok SS, Chan HM, Fung KP, Wang CC. 2013. Melamine in prenatal and postnatal organs in rats. Reprod Toxicol. 35:40-47. (Disponible en anglais seulement.)
Chu CY, Wang CC. 2013. Toxicity of melamine: The public health concern. J Environ Sci Health C Environ Carcinog Ecotoxicol Rev. 31(4):342-386. (Disponible en anglais seulement.)
Danish EPA [Environmental Protection Agency.] 2015. Chemical substances in car safety seats and other textile products for children. Survey of chemical substances in consumer products No. 135. Danish Ministry of the Environment. (Disponible en anglais seulement.)
Davison JM, Noble MCB. 1981. Serial changes in 24 hour creatinine clearance during normal menstrual cycles and the first trimester of pregnancy. British Journal of Obstetrics and Gynaecology 88:10-17. (Disponible en anglais seulement.)
[DSM] Royal DSM N.V. 2010. Life sciences and materials sciences: Staying the course. Annual Report 2009 [PDF]. Heerlen (NL): Royal DSM N.V. 196 pp. (Disponible en anglais seulement.)
Dorne JL, Doerge DR, Vandenbroeck M, Fink-Gremmels J, Mennes Knutsen W, Vernazza F, Castle L, Edler L, Benford D. 2013. Recent advances in the risk assessment of melamine and cyanuric acid in animal feed. Toxicol Appl Pharmacol. 370:218-229. (Disponible en anglais seulement.)
Du X, Chu H, Huang Y, Zhao Y. 2010 Qualitative and quantitative determination of melamine by surface-enhanced raman spectroscopy using silver nanorod array substrates. Appl Spectrosc. 64(7):781-785. (Disponible en anglais seulement.)
Duan X, Dai X-X, Wang T, Liu H-L, Sun S-C. 2015. Melamine negatively affects oocyte architecture, oocyte development and fertility in mice. Hum Reprod. 30:1643-1652. (Disponible en anglais seulement.)
Eaton RW, Karns JS. 1991a. Cloning and analysis of s-triazine catabolic genes from Pseudomonas sp. strain NRRLB-12227. J Bacteriol. 173(3): 1215–1222. (Disponible en anglais seulement.)
Eaton RW, Karns JS. 1991b. Cloning and comparison of the DNA encoding ammelide aminohydrolase and cyanuric acid amidhydrolase from three s-triazine-degrading bacterial strains. J Bacteriol. 173(3):1363–1366. (Disponible en anglais seulement.)
[EC] Environnement Canada. 2013. Bases de données téléchargeables de l’Inventaire national des rejets de polluants et sommaires et tendances d’émissions des principaux polluants atmosphériques. Données sur les installations (données de l’INRP téléchargeables pour la période de 1993 à 2012 en format Microsoft Access; version du 11 octobre 2013). [Actualisé le 11 mars 2014; consulté en avril 2014.]
[EC] Environnement Canada. 2013-2014. Données sur le Groupe de certaines substances ignifuges organiques, collectées en vertu de l’article 71 de la Loi canadienne sur la protection de l’environnement (1999): Avis concernant certaines substances ignifuges organiques. Données préparées par Environnement Canada, Santé Canada; Programme des substances existantes.
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada. 2016. Ébauche d’évaluation préalable – Groupe de certaines substances ignifuges organiques : 1,3,5-Triazine-2,4,6-triamine (mélamine), Numéro de registre du Chemical Abstracts Service 108-78-1, Ottawa (Ont.), gouvernement du Canada, 100 p.
[ECHA] European Chemicals Agency. 2018. Screening report: An assessment of whether the use of TCEP, TCPP and TDCP in articles should be restricted. Version 3 [PDF]. Helsinki (FI): European Chemicals Agency. (Disponible en anglais seulement.)
[ECHA] European Chemicals Agency. c2007-2013. Registered Substances database. Search results for CAS RN 108-78-1. Helsinki (FI): ECHA. [Actualisé le 19 mars 2014; consulté le 24 mars 2017.] (Disponible en anglais seulement.)
[ECHA] European Chemicals Agency. c2007-2017. Registered Substances database. Résultat de la recherche pour CAS RN 108-78-1. Helsinki (FI): ECHA. [Consulté le 6 mars 2017.] (Disponible en anglais seulement.)
Ecology Center. 2015. Hidden passengers: Chemical hazards in children’s car seats. A technical report by Healthystuff.org. The Ecology Center, juin 2015. Ann Arbor, Michigan, U.S.A. 24 pp. (Disponible en anglais seulement.)
[EFRA] European Flame Retardants Association. 2007. Flame retardants; Frequently asked questions. Bruxelles (BE): EFRA. 37 p. [Consulté le 19 juin 2014.] L’hyperlien n’est plus disponible. (Disponible en anglais seulement.)
[EFSA] European Food Safety Authority. 2006. Opinion of the Scientific Panel on Food Additives, Flavourings, Processing Aids and Materials in Contact with Food on a request from the Commission related to 2,2-bis(4-hydroxyphenyl)propane(Bisphenol A). The EFSA Journal 428:1-75. [Cité par EFSA 2010.] (Disponible en anglais seulement.)
[EFSA] European Food Safety Authority. 2010. Scientific Opinion on Melamine in Food and Feed. EFSA Journal 8(4):1573. 145 pp. doi:10.2903/j. efsa.2010.1573. Société propriétaire : EFSA Panel on Contaminants in the Food Chain (CONTAM) et EFSA Panel on Food Contact Materials, Enzymes, Flavourings and Processing Aids (CEF). (Disponible en anglais seulement.)
Elmore E, Fitzgerald MP. 1990. Evaluation of the bioluminescence assays as screens for genotoxic chemicals. Mutation and the Environment, Part D: 379-387. Testing laboratory: Microbics Corporation, Carlsbad, California. (Disponible en anglais seulement.)
Environnement Canada, Santé Canada. 2013. Substances chimiques : Catégorisation de substances chimiques [Internet], Ottawa (Ont.), gouvernement du Canada. [Actualisé le 25 mai, 2013; consulté le 31 juillet 2013.]
[EPI Suite] Estimation Programs Interface Suite for Microsoft Windows [Estimation Model]. 2012. Version 4.1. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. (Disponible en anglais seulement.)
[FAO] Organisation des Nations Unies pour l’alimentation et l’agriculture. 2007a. Cyromazine (169) [Evaluation] [PDF]. (Disponible en anglais seulement.)
[FAO] Organisation des Nations Unies pour l’alimentation et l’agriculture. 2007 b. Cyromazine (169): Residue and analytical aspects [rapport]. (Disponible en anglais seulement.)
Fassett DW, Roudabush RL. 1963. Laboratory of Industrial Medicine, Eastman Kodak Co. Observations non publiées. [Cité dans OCDE 2002.] (Disponible en anglais seulement.)
[FDS] Fiche de données de sécurité. 2016. Matériau d’étanchéité coupe-feu imperméable 3000 WT 3M. [Consulté en mars 2017.] Compagnie 3M [Internet.]
Fimberger EA. 1997. Bestimmung von Neben- und Abbauprodukten des Melamins mittels Kapillarelektrophorese und Abbauverhalten des Melamins in Kläranlagen. Diplomarbeit zur Erlangung des Magistergrades an der Naturwissenschaftlichen Fakultät der Universität Salzburg, Austriche. Date du rapport : 1997-07-10. [Thèse de maîtrise en allemand, citée dans ECHA c2007-2013, OECD 2002.] (Non disponible en français.)
Flakeboard Company Ltd. c2012. Thermally-fused laminates (Melamines) [Internet.] [Consulté en avril 2014.] L’hyperlien original n’est plus disponible. Voir Arauco. (Disponible en anglais seulement.)
Formica Corporation. 2013. Gammes de stratifié [Internet]. [Cité en avril 2014.]
Francis WJA. 1960. Disturbances of bladder function in relation to pregnancy. The Journal of Obstetrics and Gynaecology of the British Empire. LXVII(3):353-366. (Disponible en anglais seulement.)
Fregert S. 1981. Formaldehyde dermatitis from a gypsum-melamine resin mixture. Contact Dermatitis 7:56. [Cité par OCDE 2002.] (Disponible en anglais seulement.)
[FS] Fiche signalétique. 2013. SUPER SPEC HP® LATEX FLAT FIRE RETARDANT [PDF]. Montvalue (New Jersey), Benjamin Moore & Co. Date de révision : le 5 février 2013.
[FT] Fiche technique. 2011. SUPER SPEC HP® LATEX FLAT FIRE RETARDANT. Mississauga (Ontario), Benjamin Moore & Co.
Galloway SM, Armstrong MJ, Reuben C, Colman S, Brown B, Cannon C, Bloom AD, Nakamura F, Ahmed M, Duk S, et coll. 1987. Chromosome aberrations and sister chromatid exchange in Chinese hamster ovary cells: evaluation of 108 chemicals. Environmental and Molecular Mutagenesis 10(Suppl.10):1-175. (Disponible en anglais seulement.)
Garber E, Brewer V. 2010. Enzyme-linked Immunosorbent Assay Detection of Melamine in Infant Formula and Wheat Food Products. J Food Prot. 73(4):701–707. (Disponible en anglais seulement.)
Garcia-Gavin J, Loureiro Martinez M, Fernandez-Redondo V, Seoane M-J, Toribia J. 2008. Contact allergic dermatitis from melamine formaldehyde resins in a patient with a negative patch-test reaction to formaldehyde. Dermatitis. 19:E5-E6. (Disponible en anglais seulement.)
Gobas FAPC, Kelly BC, Arnot JA. 2003. Quantitative structure activity relationships for predicting the bioaccumulation of POPs in terrestrial food-webs. QSAR Comb Sci. 22:346-351. (Disponible en anglais seulement.)
Grand & Toy. 2014. Tableau blanc en mélamine [Internet]. [Consulté en avril 2014.]
Grosse Y, Loomis D, Guyton KZ, El Ghissassi F, Bouvard V, Benbrahim-Tallaa L, Mattock H, Straif K. (on behalf of the IARC Monograph Working Group). 2017. Some chemicals that cause tumours of the urinary tract in rodents. Lancet Oncol. 18(8):1003-1004. (Disponible en anglais seulement.)
Hansch C, Leo A, Hoekman D. 1995. Exploring QSAR: Hydrophobic, Electronic, and Steric Constants, Washington (DC): American Chemical Society. (Disponible en anglais seulement.)
Hard GC, Flake GP, Sills RC. 2009. Re-evaluation of kidney histopathology from 13-week toxicity and two-year carcinogenicity studies of melamine in the F344 rat: morphologic evidence of retrograde nephropathy. Vet Pathol. 46:1248-1257. (Disponible en anglais seulement.)
Hatakeyama T, Takagi K, Yamazaki K, Sakakibara F, Ito K, Takasu E, Naokawa T, Fujii K. 2015. Mineralization of melamine and cyanuric acid as sole nitrogen source by newly isolated Arthrobacter spp. using a soil-charcoal. World J Microbiol Biotechnol. 31:785–793. (Disponible en anglais seulement.)
Hatakeyama T, Takagi K. 2016. Bacterial biodegradation of melamine-contaminated aged soil: influence of different pre-culture media or addition of activation material. Environ Sci Pollut Res. 23:14997-15002. (Disponible en anglais seulement.)
Hauck RD, Stephenson HF. 1964. Nitrification of triazine nitrogen. J Agric Food Chem. 12(2):147-151. (Disponible en anglais seulement.)
Haworth S, Lawlor T, Mortelmans K, Speck W, Zeiger E. 1983. Salmonella mutagenicity test results for 250 chemicals. Env. Mutagen.(Suppl. 1): 3-142. Testing laboratory: Case Western Reserve University. (Disponible en anglais seulement.)
Hazleton Laboratories. 1983. Raltech Report for American Cyanamid Company, 2-Year chronic feeding study of melamine in Fisher 344 rats. Données non publiées. [Cité dans OCDE 2002.] (Disponible en anglais seulement.)
Hellwig J, Gembrandt C, Hildebrandt B. 1996. Melamine – prenatal toxicity in Wistar rats after oral administration (diet), Project No. 32R0242/94007. [Cité par OCDE 2002.] (Disponible en anglais seulement.)
[HENRYWIN] Henry’s Law Constant Program for Microsoft Windows [Estimation Model]. 2011. Version 3.20. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Consulté le 5 nov. 2013.] (Disponible en anglais seulement.)
Heukelekian H, Rand MC. 1955. Biochemical oxygen demand of pure organic compounds: a report of the research committee, FSIWA. Sewage and Industrial Wastes. 27(9):1040-1053. (Disponible en anglais seulement.)
Higby K, Suiter CR, Phelps JY, Siler-Khodr T, Langer O. 1994. Normal values of urinary albumin and total protein excretion during pregnancy. Am J Obstet Gynecol. 171:984-989. (Disponible en anglais seulement.)
Hilts C, Pelletier L. 2008. Background paper on the occurrence of melamine in foods and feed. Bureau d’innocuité des produits chimiques, Direction des aliments, Direction générale des produits de santé et des aliments, Santé Canada, Ottawa (Ontario), Canada. Préparé pour la
la Réunion d’experts de l’OMS sur le aspects toxicologiques et sanitaires de la melamine et de l’acide cyanurique. Genève, Suisse 2009. (Disponible en anglais seulement.)
Hirt RC, Steger JE, Simard GL. 1960. Vapour Pressure of 2,4,6-Triamino-s-Triazine (Melamine). J Polym Sci. 43:319-323. (Disponible en anglais seulement.)
Hockenbury MR, Grady CPL. 1977. Inhibition of Nitrification Effects of Selected Organic Compounds. JWPCF 49(5):768-777(Disponible en anglais seulement.).
Home Depot Canada [Internet.] 2014. Produits contenant de la mélamine (ou en faisant mention) [Consulté en avril 2014.]
Home Hardware [internet.] 2014. Produits contenant de la mélamine (ou en faisant mention) [Citéen avril 2014.]
[HYDROWIN] Hydrolysis Rates Program for Microsoft Windows [estimation model]. 2010. Ver. 2.00. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. (Disponible en anglais seulement.).
[ICIS] Independent Chemical Information System. c2014. US Chemical Profile: melamine. Reed Business Information. [Consulté le 17 juin 2014.] (Disponible en anglais seulement.)
[ICRP] International Commission on Radiological Protection. 2003. Basic anatomical and physiological data for use in radiological protection: Reference values. ICRP Publication 89. Ann. ICRP 32(3-4). (Disponible en anglais seulement.)
Isaksson M, Zimerson E, Bruze M. 1999. Occupational dermatoses in composite production. J Occup Environ Med. 41:261-266. (Disponible en anglais seulement.)
Ishiwata H, Sugita T, Kozaki M, Maekawa A. 1991. Inhibitory effects of melamine on the growth and physiological activities of some microorganisms. J Food Hyg Soc. Japan 32:408-413. (Disponible en anglais seulement.)
Jacob CC, Reimschuessel R, Von Tungeln LS, Olson GR, Warbritton AR, Hattan DG, Beland FA, Gamboa da Costa G 2011. Dose–response assessment of nephrotoxicity from a 7-day combined exposure to melamine and cyanuric acid in F344 rats. Toxicol Sci. 119:391–397. (Disponible en anglais seulement.)
Jacob CC, Von Tungeln LS, Vanlandingham M, Beland FA, Gamboa da Costa G. 2012. Pharmacokinetics of Melamine and Cyanuric Acid and Their Combinations in F344 Rats. Toxicol Sci. 126(2):317-324. (Disponible en anglais seulement.)
Janlek P, Boonyaratpalin M, Phromkunthong W. 2009. Histological changes in hybrid catfish, Clarias macrocepalus (Günther) × Clarias gariepinus (Burchell). Thai Fisheries Gazette. 62:331–340. [En thaï.]
Karns JS, Eaton RW. 1997. Genes encoding s-triazine degradation are plasmid born in Klebisiella pneumonia strain 99. J Agric Food Chem. 45:1017-1022. (Disponible en anglais seulement.)
Kelly BC, Ikonomou MG, Blair JD, Morin AE, Gobas FAPC. 2007. Food Web-Specific Biomagnification of Persistent Organic Pollutants. Science. 317:236-239. (Disponible en anglais seulement.)
Kersting M, Alexy U, Sichert-Hellert W, Manz F, Schoch G. 1998. Measured consumption of commercial infant food products in German infants: results from the DONALD study. Dortmund Nutritional and Anthropometrical Longitudinally Designed. J Pediatr Gastroenterol Nutr. 27:547-552. [Cité par EFSA 2010.] (Disponible en anglais seulement.)
Khalil SR, Awad A, Ali SA. 2017. Melamine and/or formaldehyde exposures affect steroidogenesis via alteration of StAR protein and testosterone synthetic enzyme expression in male mice. Environ Toxicol and Pharmacol. 50:136–144. (Disponible en anglais seulement.)
Kim SH, Lee IC, Lim JH, Shin IS, Moon C, Kim SH, Park SC, Kim HC, Kim JCl. 2011. Effects of melamine on pregnant dams and embryo-fetal development in rats. J Appl Toxicol. 31:506-514. (Disponible en anglais seulement.)
[KOAWIN] Octanol Air Partition Coefficient Program for Microsoft Windows [Estimation Model]. 2010. Version 1.10. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Consulté le 5 nov. 2013.] (Disponible en anglais seulement.)
Kobayashi, T, Okada a, Fujii Y, Niimi K, Hamamoto S, Yasui t, Tozawa K, Kohri K. 2010. The mechanism of renal stone formation and renal failure induced by administration of melamine and cyanuric acid. Urol Res. 38:117-125. (Disponible en anglais seulement.)
[KOCWIN] Organic Carbon Partition Coefficient Program for Windows [Estimation Model]. 2010. Version 2.00. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Consulté le 4 nov. 2013.] (Disponible en anglais seulement.)
Kong APS, Choi KC, Ho CS, Chan MHM, Wong CK, Liu EKH, Chu WCW, Chow VCY, Lau JTF, Chan JCN. 2011. Hong Kong Chinese school children with elevated urine melamine levels: A prospective follow up study. BMC Public Health 11:354-358. (Disponible en anglais seulement.)
Konishi K, Imanishi A. 1941. Fertilizing efficacy of melamines and guanidines. J Sci Soil Manure Jpn. 15:564. [Cité par Hauck et Stephenson 1964.] (Disponible en anglais seulement.)
[KOWWIN] Octanol-Water Partition Coefficient Program for Microsoft Windows [Estimation Model]. 2010. Version 1.68. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. [Consulté le 5 nov. 2013.] (Disponible en anglais seulement.)
Lakind JS, Naiman DQ. 2008. Bisphenol A (BPA) daily intakes in the United States: Estimates from the 2003-2004 NHANES urinary BPA data. J Exposure Sci Environ Epidemiol. 18:608-615. (Disponible en anglais seulement.)
Lentner C. (Ed.). 1981. Geigy scientific tables. Vol. 1: Units of measurement, body fluids, composition of the body, nutrition. Eighth edition. Ciba-Geigy Ltd., Bâle, Suisse. (Disponible en anglais seulement.)
Li W, Li H, Zhang J, Tian X. 2015. Effect of melamine toxicity on Tetrahymena thermophile proliferation and metallothionein expression. Food Chem Toxicol. 80:1-6. (Disponible en anglais seulement.)
Li, G, Jiao S, Yin X, Deng Y, Pang X, Wang Y. 2010. The risk of melamine-induced nephrolithiasis in young children starts at a lower intake level than recommended by the WHO. Pediatr Nephrol. 25:135-141. (Disponible en anglais seulement.)
Lightner DV, Pantoja CR, Redman RM, Hasson KW, Menon JP. 2009. Case of melamine-induced pathology in penaeid shrimp fed adulterated feeds. Dis Aquat Org. 86:107-112. (Disponible en anglais seulement.)
Lipschitz WL, Stokey E. 1945. The mode of action of three new diuretics: melamine, adenine and formoguanamine. J Pharmacol Exp Ther. 83:235-249. (Disponible en anglais seulement.)
Litton Bionetics. 1977a. Mutagenicity evaluation of melamine. Données non publiées. Numéro du rapport : LBI Project No. 2838. [Cité par OCDE 2002.] (Disponible en anglais seulement.)
Litton Bionetics. 1977 b. Données non publiées. [Cité dans OCDE 2002.] (Disponible en anglais seulement.)
Litton Bionetics. 1977c. Mutagenicity evaluation of melamine. Données non publiées. Numéro du rapport : LBI Project No. 2838. [Cité dans OCDE 2002.] (Disponible en anglais seulement.)
Liu G, Li S, Jia J, Yu C, He J, Yu C, Zhu J. 2010. Pharmacokinetic study of melamine in rhesus monkey after a single oral administration of a tolerable daily intake dose. Regul Toxicol. Pharmacil. 56:193-196. (Disponible en anglais seulement.)
Liu HY, Zhang W, Xue M, Wu XF, Zheng YH, Guo LY, Sheng HJ. 2009. Acute toxicity study for melamine on Japanese sea bass (Lateolabrax japonicus). Acta Hydrobiologica Sinica 33:157–163. [En chinois.]
Liu, C-C, Wu C-F, Chen BH, Huang SP, Goggins W, Lee HH, Chou YH, Wu WJ, Huang CH, Shiea J, et coll. 2011. Low exposure to melamine increases the risk of urolithiasis in adults. Kidney Int. 80:746-752. (Disponible en anglais seulement.)
Lu Y, Xia Y, Liu G, Pan M, Li M, Lee NA, Wang S. 2017. A review of methods for detecting melamine in food samples. Crit Rev Anal Chem. 47(1):51-66. (Disponible en anglais seulement.)
Lund KH, Petersen JH. 2006. Migration of formaldehyde and melamine monomers from kitchen- and tableware made of melamine plastic. Food Addit Contam. 23(9):948-955. (Disponible en anglais seulement.)
Lynch RA, Hollen H, Johnson DL, Bartels J. 2015. The effects of pH on the migration of melamine from children’s bowls. Int J Food Contam. 2:9. DOI 10.1186/s40550-015-0017-z. (Disponible en anglais seulement.)
Magami SM, Oldring PKT, Castle L, Guthrie JT. 2015. Migration of melamine from thermally cured, amino cross-linked can coatings into an aqueous ethanol food simulant: aspects of hydrolysis, relative reactivity and migration. Food Addit Contam Part A. 32(3):403-409. (Disponible en anglais seulement.)
Mast RW, Friedman MA, Finch RA. 1982 b. Mutagenicity testing of melamine. Toxicologist 2: 172 (Abstract No. 602). (Disponible en anglais seulement.)
Mast RW, Jeffcoat AR, Sadler BM, Kraska RC, Friedman MA. 1983. Metabolism, disposition and excretion of [14C]melamine in male Fischer 344 rats. Food Chem Toxicol. 21(6):807-810. (Disponible en anglais seulement.)
Mast RW. Naismith RW, Friedman MA. 1982a. Mouse micronucleus assay of melamine. Environ Mutagen. 4:340-341 (Abstract No. Bi-8). (Disponible en anglais seulement.)
McGregor DB, Brown A, Cattanach P, Edwards I, McBride D, Riach C, Caspary WJ. 1988. Responses of the L5178Y tk+/tk mouse lymphoma cell forward mutation assay: III. 72 coded chemicals. Environ Mol Mutagen. 12:85-154. (Disponible en anglais seulement.)
Melnick R.L, Boorman GA, Haseman JK, Montali RJ, Huff J. 1984. Urolithiasis and bladder carcinogenicity of melamine in rodents. Toxicol Appl Pharmacol. 72:292-303. (Disponible en anglais seulement.)
[MITI] Ministry of International Trade & Industry (JP). 1992. Biodegradation and bioaccumulation data of existing chemicals based on the CSCL Japan. Tokyo (JP): Japan Chemical Industry Ecology–Toxicology and Information Center. (Non disponible en français.)
Mirsalis J, Tyson K, Beck J, Loh F, Steinmetz K, Contreras C, Austere L, Martin S, Spalding J. 1983. Induction of unscheduled DNA synthesis (UDS) in hepatocytes following in vivo and in vivo treatment. Environmental Mutagenesis 5: 482; Abstract no. Ef-5 in Abstracts of the Environmental Mutagen Society held at San Antonio, Texas, du 3 au 6 mars 1983. (Disponible en anglais seulement.)
[MOE] Ministry of the Environment (JP). c2005. Chemicals in the environment [Internet]. Tokyo (JP): MOE, Environmental Health Dept. [Consulté le 4 févr. 2014.] (Non disponible en français.)
[MSDS] Material Safety Data Sheet. 2014. Cromophtal® Yellow D 1085 (old Cromophtal® Yellow LA2). [Consulté en avril 2014.] BASF [internet.] (Disponible en anglais seulement.)
Muijser H. 1998. Acute (4-hour) inhalation toxicity study with Melamine in rats. Testing laboratory: Testing laboratory: TNO Nutrition and Food Research Institute, Toxicology Division. Numéro du rapport : V98.420. Société propriétaire : DSM N. V. Heerlen, Pays-Bas. Study number: 480001/002. Date du rapport : 1998-04-15. Information non publiée soumise à ECCC dans le cadre de l’initiative du PGPC. Gatineau (Qué.), Environnement et Changement climatique Canada, Division de la mobilisation et de l’élaboration de programmes. [accès restreint.] (Disponible en anglais seulement.)
Nascimento CF, Santos PM, Pereira-Filho ER, Rocha FRP. 2017. Recent advances on determination of milk adulterants. Food Chemistry 221:1232-1244. (Disponible en anglais seulement.)
Neithardt AB, Dooley SL, Borensztajn J. 2002. Prediction of 24-hour protein excretion in pregnancy with a single voided urine protein-to-creatinine ratio. Am J Obstet Gynecol. 186:883-886. (Disponible en anglais seulement.)
Niemi GJ, Gilman DV, Regal RR, Vaishnav DD. 1987. Structural features associated with degradable and persistent chemicals. Environ Toxicol Chem. 6:515-527. (Disponible en anglais seulement.)
Norris B, Smith S. 2002. Research into the mouthing behaviour of children up to 5 years old. London, England: Consumer and Competition Policy Directorate, Department of Trade and Industry, London, UK. [Cité par US EPA 2011.] (Disponible en anglais seulement.)
[OCDE] Organisation de coopération et de développement économiques. 2002. SIDS Initial Assessment Report for: Melamine; CAS RN 108-78-1. SIDS Initial Assessment Meeting 8; octobre 1998. (Disponible en anglais seulement.)
[OCDE] Organisation de coopération et de développement économiques. 2009. OECD Pov and LRTP Screening Tool [Internet]. Version 2.2. A software model for estimating overall persistence (Pov) and long-range transport potential (LRTP) of organic chemicals. [Consulté le 3 juin 2014.] (Disponible en anglais seulement.)
Ogasawara H, Imaida K, Ishiwata H, Toyoda K, Kawanishi T, Uneyama C, Hayashi S, Takahashi M, Hayashi Y. 1995. Urinary bladder carcinogenesis induced by melamine in F344 male rats: correlation between carcinogenicity and urolith formation. Carcinogenesis. 16:2773-2777. (Disponible en anglais seulement.)
Okumura M, Hasegawa R, Shirai T, Ito M, Yamada S, Fukushima S. 1992. Relationship between calculus formation and carcinogenesis in the urinary bladder of rats administered the non-genotoxic agents, thymine or melamine. Carcinogenesis. 13:1043-1045. (Disponible en anglais seulement.)
[OMS] Organisation mondiale de la Santé. 2009. Toxicological and Health Aspects of Melamine and Cyanuric Acid. Report of a WHO Expert Meeting in Collaboration with FAO (Organisation des Nations Unies pour l’alimentation et l’agriculture). Soutenu par Santé Canada. 66 p. (Disponible en anglais seulement.)
[OMS] Organisation mondiale de la Santé. c2014. Health topics: melamine [Internet]. Genève (Suisse), OMS. [Consulté le 3 févr. 2014.] (Disponible en anglais seulement.)
Pang J, Li G-Q, Li C-R, Yang X-Y, Lu X, Hu X-X, Zhai Q-Q, Zhang W-X, Jiang J-D, You X-F. 2013. Toxicokinetic study of melamine in the presence and absence of cyanuric acid in rats. J Appl Toxicol. 33:444-450. (Disponible en anglais seulement.)
Panuwet P, Nguyen JV, Wade EL, D’Souza PE, Ryan PB, Barr DB. 2012. Quantification of melamine in human urine using cation-exchange based high performance liquid chromatography tandem mass spectrometry. J Chromatogr. B 887-888:48-54. (Disponible en anglais seulement.)
Parboosingh J, Doig A. 1973. Studies of nocturia in normal pregnancy. Journal of Obstetrics and Gynaecology of the British Commonwealth 80:888-895. (Disponible en anglais seulement.)
Perucca J, Bouby N, Valeix P, Bankir L. 2007. Sex difference in urine concentration across differing ages, sodium intake, and level of kidney disease. Am J Physiol Regul Integr Comp Physiol. 292:R700–R705. (Disponible en anglais seulement.)
Petreas M, Gill R, Takaku-Pugh S, Lytle E, Parry E, Wang M, Quinn J, Park J-S. 2016. Rapid methodology to screen flame retardants in upholstered furniture for compliance with new California labeling law (SB 1019). Chemosphere. 152:353-359. (Disponible en anglais seulement.)
Pharmakon Research. 1981. Genetic toxicology – Micronucleus test. Report for American Cyanamid Company, Study No. PH 309A-AC-001-81. Données non publiées. [Cité par OCDE 2002.]
Phromkunthong W, Choochuay P, Kiron V, Nuntapong N, Boonyaratpalin M. 2015. Pathophysiological changes associated with dietary melamine and cyanuric acid toxicity in red tilapia. J Fish Disease. 38(2):161-173. (Disponible en anglais seulement.)
Phromkunthong W, Nuntapong N, Boonyaratpalin M, Kiron V. 2013. Toxicity of melamine, an adulterant in fish feeds; experimental assessment of its effect on tilapia. J Fish Disease. 36:555-568. (Disponible en anglais seulement.)
Puschner, B, Poppenga RH, Lowenstine LJ, Filigenzi MS, Pesavento PA . 2007. Assessment of melamine and cyanuric acid toxicity in cats. J Vet Diagnc Invest. 19(6): 616-24. (Disponible en anglais seulement.)
Qin Y, Lv X, Li J, Qi J, Diao Q, Liu G, Xue M, Wang J, Tong J, Zhang L, Zhang K. 2010. Assessment of melamine contamination in crop, soil and water in China and risks of melamine accumulation in animal tissues and products. Environ Int. 36:446-452. (Disponible en anglais seulement.)
Rai N, Banerjee D, Bhattacharyya R. 2014. Urinary melamine: Proposed parameter of melamine adulteration of food. Nutrition. 30:380–385. (Disponible en anglais seulement.)
Ramusino MC, Vailati G. 1982. Modification in Salmo gairdneri due to 2,4,6 triamino 1,3,5 triazine (melamine), Acta Embryol Morphol Exp. N.s. 3(1):41-48. [Cité par ECHA c2007-2013.]
Reimschuessel R, Evans E, Andersen WC, Turnipseed SB, Karbiwnyk CM, Mayer TD, Nochetto C, Rummel NG, Gieseker CM. 2010a. Residue depletion of melamine and cyanuric acid in catfish and rainbow trout following oral administration. J Vet Pharmacol Ther. 33(2):172-82. (Disponible en anglais seulement.)
Reimschuessel R, Evans ER, Stine CB, Hasbrouck N, Mayer TD, Nochetto C, Gieseker CM. 2010b. Renal crystal formation after combined or sequential oral administration of melamine and cyanuric acid. Food Chem Toxicol. 48:2898-2906. (Disponible en anglais seulement.)
Remer T, Fonteyn N, Alexy U, Berkemeyer S. 2006. Longitudinal examination of 24-h urinary iodine excretion in schoolchildren as a sensitive, hydration status-independent research tool for studying iodine status. Am J Clin Nutr. 83:639-646. (Disponible en anglais seulement.)
Revúsová V, Zvara V, Gratzlová J. 1971. Some laboratory findings in patients with urolithiasis. Int Urol Nephrol. 3(3):251-258. (Disponible en anglais seulement.)
Rijcken WRP. 1995. Primary skin irritation/corrosion study with melamine in the rabbit, confidential Notox project 146205 for DSM Melamine, 1995. [Cité par OCDE 2002.] (Disponible en anglais seulement.)
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [National Institute for Public Health and the Environment]. 2008. Chemicals in Toys. A general methodology for assessment of chemical safety of toys with a focus on elements. Bilthoven (NL): RIVM. Report No.:320003001/2008. [Consulté le 9 juillet 2018.]
Roberts TR, Hutson DH. Eds. 1999. Metabolic Pathways of Agrochemicals, Part2: Insecticides and Fungicides. Royal Society of Chemistry, MPG Books, Ltd.: Bodmin, Cornwall, UK. pp. 741–743. (Disponible en anglais seulement.)
Rossman TG, Molina M, Meyer L, Boone P, Klein CB, Wang Z, Li F, Lin WC, Kinney PL. 1991. Performance of 133 compounds in the lambda prophage induction endpoint of the Microscreen assay and a comparison with S. typhimurium mutagenicity and rodent carcinogenicity assays. Mutat Res. 260:349-367. (Disponible en anglais seulement.)
Rovina K, Siddiquee S. 2015. A review of recent advances in melamine detection techniques. J Food Compos Anal. 43:25-38. (Disponible en anglais seulement.)
[RTECS] Registry of Toxic Effects of Chemical Substances. 2013. Datasheet on melamine (108-78-1). Actualisé en septembre 2013. [Consulté le 13 février 2013.] (Disponible en anglais seulement.)
RTI. 1982. Evaluation of urolithiasis induction by melamine in male weanling Fischer 344 rats, Project No. 31T-2407 for American Cyanamid Company, données non publiées. [Cité par OCDE 2002.] (Disponible en anglais seulement.)
Rumble JR, editor. 2018. CRC Handbook of Chemistry and Physics. Internet Version 2018. Boca Raton (FL): CRC Press. 1532 pp. (Disponible en anglais seulement.)
Santé Canada, 2008. Évaluation des risques pour la santé humaine de Santé Canada appuyant la conception de normes pour la mélamine dans les aliments. Rédigé par le Bureau d’innocuité des produits chimiques, Direction des aliments, Direction générale des produits de santé et des aliments.
Santé Canada. [Modifié le 3 mai 2017.] Listes des additifs alimentaires autorisés, Ottawa Ont.), Santé Canada, Direction des aliments. [Consulté le 24 avril 2014.]
Santé Canada. 1994. L’évaluation du risque à la santé humaine des substances d’intérêt prioritaire [PDF], Ottawa (Ont.), Santé Canada.
Santé Canada. 1995. Enquête sur l’exposition des êtres humains aux contaminants dans le milieu : Un guide pour les calculs de l’exposition, Ottawa (Ont.), Les Grands Lacs: Impact sur la santé, Direction générale de la protection de la santé, Santé Canada. Disponible sur demande.
Santé Canada. 1998. Exposure factors for assessing total daily intake of priority substances by the general population of Canada. Rapport inédit. Ottawa (Ont.), Santé Canada, Direction de l’hygiène du milieu. Disponible sur demande. (Disponible en anglais seulement.)
Santé Canada. 2012. Service de transcription d’étiquettes de l’Agence de réglementation de la lutte antiparasitaire [Internet]. Recherche d’étiquette électronique pour la cyromazine. [Modifié le 8 janv. 2016; consulté le 31 mars 2017.] Ottawa (Ont.), Santé Canada, Sécurité des produits de consommation, Agence de réglementation de la lutte antiparasitaire.
Santé Canada. 2015. Determination of melamine in polyurethane foam and similar consumer products by LC-MS/MS. Project Report number 2105-2122; 9 October 2015. Product Safety Laboratory, Ottawa. 6 pp plus Appendix-1: Method C53. (Disponible en anglais seulement.)
Santé Canada. 2016a. Questions et réponses – Mélamine [Internet]. [Actualisé le 4 mai 2016.]
Santé Canada. 2016 b. Plan de travail des réévaluations et des examens spéciaux de l’Agence de réglementation de la lutte antiparasitaire pour les années 2015 à 2020. Note de réévaluation REV2016-07, le 26 février 2016. [Consulté le 31 mars 2017.] Ottawa (Ont.), Santé Canada, ARLA, 6 p.
Santé Canada. 2016c. Determination of melamine in electronic boards LC-MS/MS. Project Report number 2105-2160; 26 January 2016. Product Safety Laboratory, Ottawa. 5 pp plus Appendix-1: Method C53.1. (Disponible en anglais seulement.)
Santé Canada. 2018a. Concentrations maximales établies par Santé Canada à l’égard de contaminants chimiques dans les aliments [Internet]. [Actualisé le 25 janv. 2018.]
Santé Canada. 2018b. Plan de travail des réévaluations et des examens spéciaux de l’Agence de réglementation de la lutte antiparasitaire pour les années 2018 à 2023. Note de réévaluation REV2018-06 [PDF], le 13 avril 2018. [Consulté le 28 déc. 2018.] Ottawa (Ont.), Santé Canada, ARLA, 10 p.
Santé Canada. 2018c. Supporting documentation: Information in support of the screening assessment, Certain organic flame retardants substance grouping; 1,3,5-Triazine-2,4,6-triamine (Melamine): Human health supplementary data. Ottawa (Ont.), Environnement et Changement climatique Canada. Disponible sur demande à l’adresse : substances@ec.gc.ca (Disponible en anglais seulement.)
Scorecard (site d’information sur la pollution) [Internet.] c2011. Scorecard: Chemical profile for melamine. [Consulté le 28 janv. 2014.] Parrainé par GoodGuide (US). (Disponible en anglais seulement.)
Seiler JP. 1973. A survey on the mutagenicity of various pesticides. Experienta. 29:622-623. (Disponible en anglais seulement.)
Selden JR, Dolbeare F, Clair JH, Miller JE, McGettigan K, DiJohn JA, Dysart GR, DeLuca JG. 1994. Validation of a flow cytometric in vitro DNA repair (UDS) assay in rat hepatocytes. Mutat Res. 315(2):147-167. (Disponible en anglais seulement.)
Shelby MD, Erexson GL, Hook GJ, Tice RR. 1993. Evaluation of a three-exposure mouse bone marrow micronucleus protocol: Results with 49 chemicals. Environ Mol Mutagen. 21:160-179. (Disponible en anglais seulement.)
Shelton DR, Karns JS, McCarty GW, Durham DR. 1997. Metabolism of Melamine by Klebsiella terragena. Appl Environ Microbiol. 63(7):2832. (Disponible en anglais seulement.)
Smith GR, Stearley RF. 1989. The classification and scientific names of rainbow trout and cutthroat trouts. Fisheries. 14(1):4-10. (Disponible en anglais seulement.)
Soubrier R, Burlet P. 1972 Dermatoses provoqué par la mélamine. Arch Mal Prof. 33:202-204. [Cité par OCDE 2002.] (Disponible en anglais seulement.)
[SPIN] Substances in Preparations in Nordic Countries database [Internet]. c2014. Copenhagen (DE): Nordic Council of Ministers, Chemical Group. [Consulté le 31 janv. 2014.] (Disponible en anglais seulement.)
Statistique Canada, 2004. Enquête sur la santé dans les collectivités canadiennes – Nutrition (ESCC). Information détaillée pour 2004 (Cycle 2.2), Ottawa (Ont.), gouvernement du Canada.
Statistique Canada. 2019. Base de données sur le commerce international canadien de marchandises [Internet.] Tableau 990-0029; 29. Importations – Produits chimiques organiques (Séléction de données ; 293 361 mélamine) [Actualisé le 14 févr. 2019; consulté en févr. 2019.] Ottawa (Ont.), gouvernement du Canada.
Stine CB, Reimschuessel R, Keltner Z, Nochetto CB, Black T, Olejnik N, Scott M, Bandele O, Nemser SM, Tkachenko A et coll. 2014. Reproductive toxicity in rats with crystal nephropathy following high doses of oral melamine or cyanuric acid. Food Chem Toxicol. 68:142–153.] (Disponible en anglais seulement.)
[STP-EX] Sewage Treatment Plant Expanded Model. 2008. Windsor (Ont.): University of Windsor, Dept. of Civil and Environmental Engineering. [Modèle décrit par Seth et coll. 2008.] (Disponible en anglais seulement.)
Suknikom P, Jermnak U, Poapolathep S, Isariyodom S Giorgi M, Kumagai S, Poapothep A. 2016. Dispositions and tissue depletion of melamine in ducks. J Vet Pharmacol Ther. 39(1)90-94.] (Disponible en anglais seulement.)
Sun J, Cao Y, Zhang X, Zhao Q, Bao E, Lv Y. 2016a. Melamine negatively affects testosterone synthesis in mice. Res Vet Sci. 109:135-141.] (Disponible en anglais seulement.)
Sun J, Zhang X, Cao Y, Zhao Q, Bao E, Lv Y. 2016b. Ovarian toxicity in female rats after oral administration of melamine or melamine and cyanuric acid. PLOS One. DOI:10.1371/journal.pone.0149063.] (Disponible en anglais seulement.)
Sun Y, Jiang YN, Xu C-F, Du YX, Zhang JJ, Yan Y, Gao XL. 2014. The recovery of bladder epithelial hyperplasia caused by a melamine diet-induced bladder calculus in mice. Food Chem Toxicol. 64:378–382.] (Disponible en anglais seulement.)
Sun YJ, Wang HP, Liang YJ, Yang L, Li W, Wu YJ. 2012. An NMR-based metabonomic investigation of the subacute effects of melamine in rats. J Proteome Res. 11:2544-2550.] (Disponible en anglais seulement.)
[SWISSI] The Swiss Institute of Safety and Security. 2009. Determination of some physical-chemical properties of Melamine. Report. Assignment no.: 204611.08.0640.02. Bâle,Suisse: SWISSI. 7p. [Accès restreint.] (Disponible en anglais seulement.)
Swope HG, and Kenna M. 1950. Effect of organic compounds on biochemical oxygen demand. Sew Ind Wastes Eng. 21:467. [Cité par Niemi et coll. 1987.] (Disponible en anglais seulement.)
Takagi K, Fujii K, Yamazaki K, Harada N, Iwasaki A. 2012. Biodegradation of melamine and its hydroxy derivatives by a bacterial consortium containing a novel Nocardioides species. Appl Microbiol Biotechnol. 94:1647–1656. (Disponible en anglais seulement.)
[TaPL3] Long Range Transport and Persistence Level III model [Internet]. 2003. Version 3.0. Peterborough (Ont.), Trent University, Canadian Environmental Modelling Centre. [Consulté le 1er juin 2014.] (Disponible en anglais seulement.)
Ten Berge W. 2010. A simple dermal absorption model: Derivation and application. Chemosphere. 75:1440-1445. (Disponible en anglais seulement.)
Thorp JM, Norton PA, Lewis Wall L, Kuller JA, Eucker B, Wells E. 1999. Urinary incontinence in pregnancy and the puerperium: A prospective study. Am J Obstet Gynecol. 181:266-273. (Disponible en anglais seulement.)
Tittlemier S, Lau BP-Y, Ménard C, Corrigan C, Sparling M, Gaertner D, Pepper, K, Feeley M. 2009. Melamine in infant formula sold in Canada: Occurrence and risk assessment. J Agric Food Chem. 57:5340-5344. (Disponible en anglais seulement.)
Tittlemier S, Lau BP-Y, Ménard C, Corrigan C, Sparling M, Gaertner D, Cao X-L, Dabeka R. 2010a. Baseline levels of melamine in food items sold in Canada. I. Dairy products and soy-based dairy replacement products. Food Addit Contam Part B Surveill. 3(3):135-139. (Disponible en anglais seulement.)
Tittlemier S, Lau BP-Y, Ménard C, Corrigan C, Sparling M, Gaertner D, Cao X-L, Dabeka R, Hilts C. 2010b. Baseline levels of melamine in food items sold in Canada. II. Egg, soy, vegetable, fish and shrimp products. Food Addit Contam Part B Surveill. 3(3):140-147. (Disponible en anglais seulement.)
Tu H, Zhang M, Zhou C, Wang Z, Huang P, Ou H, Chang Y. 2015. Genotoxicity assessment of melamine in the in vivo Pig-a mutation assay and in a standard battery of assays. Mutat Res. 777:62-67. (Disponible en anglais seulement.)
Ubaidellajev RU, et coll. 1993. Gigiena i Sanitariya 58:14-16. [Cité par RTECS 2013.] [Consulté le 13 févr. 2013.] (Disponible en anglais seulement.)
[UE] Union européenne. 2011. Règlement (UE) N° 10/2011 de la Commission du 14 janvier 2011 concernant les matériaux et objets en matière plastique destinés à entrer en contact avec des denrées alimentaires. 132 p.
[US CDC] U.S. Centers for Disease Control and Prevention. 2010a. National Health and Examination Survey 2003-2004. Data Documentation, Codebook, and Frequencies. Melamine (Surplus Urine) (SSMEL_C) files. Dernière révision 2010. [Consulté en mars 2014.] (Disponible en anglais seulement.)
[US CDC] U.S. Centers for Disease Control and Prevention. 2010 b. National Health and Examination Survey 2003-2004. Demographic Data. [Consulté en mars 2014.] [US CPSC] U.S. Consumer Product Safety Commission. 2005. Analysis of FR Chemicals Added to Foams, Fabric, Batting, Loose Fill, and Barriers. Mémoire daté du 10 mai 2005. 20 p. (Disponible en anglais seulement.)
[US CPSC] U.S. Consumer Product Safety Commission. 2006. CPSC staff preliminary risk assessment of flame retardant (FR) chemicals in upholstered furniture foam. 212 pp. (Disponible en anglais seulement.)
[US eCFR] U.S. Electronic Code of Federal Regulations [Internet.] 2014a. 21 CFR 175 105 [current as of January 30, 2014.] Washington (DC): National Archives and Record Administration, Office of the Federal Register (OFR); U.S. Government Printing Office. [Consulté en janv. 2014.] (Disponible en anglais seulement.)
[US eCFR] U.S. Electronic Code of Federal Regulations [Internet.] 2014b. 21 CFR 175.300 and 175.320 [current as of January 30, 2014.] Washington (DC): National Archives and Record Administration, Office of the Federal Register (OFR); U.S. Government Printing Office. [Consulté en janv. 2014.] (Disponible en anglais seulement.)
[US EPA] U.S. Environmental Protection Agency. 1984. Cyromazine, proposed tolerance, U.S. Federal Register. 49(83):18121-18125. (Disponible en anglais seulement.)
[US EPA] U.S. Environmental Protection Agency. 2007. High Production Volume Information System (HPVIS) [database on the Internet]. Search results for CAS RN 108-78-1. Washington (DC): U.S. EPA. [Consulté le 29 janv. 2014.] (Disponible en anglais seulement.)
[US EPA] U.S. Environmental Protection Agency. 2011. Exposure factors handbook: 2011 edition. National Center for Environmental Assessment, Washington, DC; EPA/600/R-09/052F. (Disponible en anglais seulement.)
[US EPA] U.S. Environmental Protection Agency. 2012. Standard Operating Procedures for Residential Pesticide Exposure Assessment [PDF]. Office of Chemical Safety and Pollution Prevention, Washington (DC). (Disponible en anglais seulement.)
[US EPA] U.S. Environmental Protection Agency. 2015. Flame retardants used in flexible polyurethane foam: An alternatives assessment update. Report No. EPA 744-R-15-002; août 2015. U.S. EPA Design for the Environment. 832 pp. (Disponible en anglais seulement.)
[US NTP] United States National Toxicology Program. 1983. Carcinogenesis bioassay of melamine in F344/N rats and B6C3F1 mice (feed study); Technical Report Series No. 245 [PDF]. US Department of Health and Human Services. (Disponible en anglais seulement.)
[US Testing Company] United States Testing Company Inc. (Hoboken, New Jersey). 1988. Algal growth inhibition test (OECD method) using CT-338-87. Test report no.: 07383. Rapport non publié. réalisé pour l’American Cyanamid Company (Wayne, New Jersey). 8 p. [Accès restreint.] (Disponible en anglais seulement.)
Vaishnav DD. 1984. Biochemical oxygen demand data base. Element 16, Vol. 1. In: Call DJ, Brooke LT, Vaishnav DD, editors. 1984. Aquatic Pollutant Hazard Assessment and Development of Hazard Prediction Technology by Quantitative Structure-Activity Relationships. EPA-CR809234. Superior (WI): University of Wisconsin. [Cité par Niemi et coll. 1987.] (Disponible en anglais seulement.)
Van Haarst EP, Heldeweg EA, Newling DW, Schlatmann TJ. 2004. The 24-h frequency-volume chart in adults reporting no voiding complaints: defining reference vales and analysing variables. BJU International. 93:1257-1261. (Disponible en anglais seulement.)
Vernon PA, Deskin R, Dulak LH. 1990. Acute toxicologic evaluation of melamine. Cité par Parent RA, editor. Acute toxicity data. J Am Coll Toxicol Part B. 1:110. Société propriétaire : American Cyanamid Co. (Disponible en anglais seulement.)
Wackett LP, Sadowsky MJ, Martinez B, Shapir N. 2002. Biodegradation of atrazine and related s-triazine compounds: from enzymes to field studies. Appl Microbiol Biotechnol. 58(1):39–45. (Disponible en anglais seulement.)
Wang H, Gen C, Li J, Hu A. 2014. Characterization of a novel melamine-degrading bacterium isolated from a melamine-manufacturing factory in China. App Microbiol Biotechnol. 98:3287-3293. (Disponible en anglais seulement.)
Wang W, Chen H, Yu B, Mao X, Chen D. 2013. Tissue deposition and residue depletion of melamine in fattening pigs following oral administration. Food Addit Contam Part A. 31(1):7-14. (Disponible en anglais seulement.)
Wang Z, Chen L, Al-Kasir R, Han B. 2011. In vitro toxicity of melamine against Tetrahymena pyriformis cells. J Vet Sci. 12(1):27-34. (Disponible en anglais seulement.)
Wang Z, Qi X, Zou M, Zhang Z, Xu F. 2009. Cytotoxicity assessment of melamine using the ciliated protozoan Tetrahymena pyriformis. Asian J Ecotoxicol. 4(1):35-39. (Disponible en anglais seulement.)
Weber JB. 1970. Adsorption of s-triazines by montmorillonite as a function of pH and molecular structure. Soil Sci Soc Amer Proc. 34:401-404. (Disponible en anglais seulement.)
Wehner DJ, Martin DL. 1989. Melamine/urea and oxamide fertilization of Kentucky bluegrass. Urbana (IL): University of Illinois, Dept. of Horticulture. 15 pp. (Disponible en anglais seulement.)
Weil ED, Choudhary V. 1995. Flame-retarding plastics and elastomers with melamine. J Fire Sci. 13(March/April):104-126. (Disponible en anglais seulement.)
Williamson MA, Snyder LM, editors. 2011. Wallach’s Interpretation of Diagnostic Tests. 9 th Edition, mise à jour le 12 févr. 2014. Philadelphia, Pa: Lippincott Williams and Wilkins. (Disponible en anglais seulement.)
Wong CK, Chan MHM, Kwok JSS, Ho CS, Ng PC, Suen SH, Fung KP, Lau CM, Fok TF. 2013. Diagnostic tools for detection of intoxication by melamine and its analogue. Hong Kong Med J. 19(6), Supplement 8:12-15. (Disponible en anglais seulement.)
Wu AHB. 2006. Tietz clinical guide to laboratory tests. 4th ed. St. Louis (MO): Saunders Elsevier. p. 1102–1104. (Disponible en anglais seulement.)
Wu CF, Hsieh TJ, Chen BH, Liu CC, Wu MT. 2013. A cross over study of noodle soup consumption in melamine bowls and total melamine excretion in urine. JAMA Inter Med. 173(4):317-319. (Disponible en anglais seulement.)
Wu CF, Liu CC, Chen BH, Huang SP, Lee HH, Chou YC, Wu WJ, Wu MT. 2010a. Urinary melamine and adult urolithiasis in Taiwan. Clin Chim Acta. 411:184-189. (Disponible en anglais seulement.)
Wu YT, Huang CM, Lin CC, Ho WA, Lin LC, Chiu TF, Tarng DC, Lin CH, Tsai TH. 2010b. Oral bioavailability, urinary excretion and organ distribution of melamine in Sprague-Dawley rats by high-performance liquid chromatography with tandem mass spectrometry. J Agric Food Chem. 58:108-111. (Disponible en anglais seulement.)
Xu S, Zhang Y, Sims A, Bernards M, Hu Z. 2013. Fate and toxicity of melamine in activated sludge treatment systems after a long-term sludge adaptation. Water Res. 47:2307-2314. (Disponible en anglais seulement.)
Xue J, Ai Q, Mai K, Xu W, Yang Y, Liufu Z. 2011a. Effects of melamine on growth performance and skin color of darkbarbel catfish (Pelteobagrus vachelli). Aquaculture. 320:142-146. (Disponible en anglais seulement.)
Xue M, Qin Y, Wang J, Qui J, Wu X, Zheng Y, Wang Q. 2011b. Plasma pharmacokinetics of melamine and a blend of melamine and cyanuric acid in rainbow trout (Oncorhynchus mykiss). Reg Toxicol Pharmacol. 61:93-97. (Disponible en anglais seulement.)
Yalkowsky SH, He Y. 2003 Handbook of aqueous solubility data. Boca Raton (FL): CRC Press LLC. (Disponible en anglais seulement.)
Yang F, Mao Y, Zhang X, Ma Z, Zhang X. 2009. LC-MS/MS method for the determination of melamine in rat plasma: Toxicokinetic study in Sprague–Dawley rats. J Sep Sci. 32:2974-2978. (Disponible en anglais seulement.)
Yang J, An L, Yao Y, Yang Z, Zhang T. 2011. Melamine impairs spatial cognition and hippocampal synaptic plasticity by presynaptic inhibition of glutamatergic transmission in infant rats. Toxicology. 289:167-174. (Disponible en anglais seulement.)
Yasunaga K, Kiyonari A, Oikawa T, Abe N, Yoshikawa K. 2004. Evaluation of the Salmonella umu test with 83 NTP chemicals. Environ Mol Mutagen. 44:329-345. (Disponible en anglais seulement.)
Yin RH, Wang XZ, Bai WL, Wu CD, Yin RL, Li C, Liu J, Liu BS, He JB. 2013. The reproductive toxicity of melamine in the absence and presence of cyanuric acid in male mice. Res Vet Sci. 94(3):618-627. (Disponible en anglais seulement.)
Yurdakok B, Filazi A, Ekici H, Celik TH, Sireli UT. 2014. Melamine in breast milk. Toxicol Res. 3:242-246. (Disponible en anglais seulement.)
Yurdakok B, Filazi A, Ekici H, Celik TH, Sireli UT. 2015. Correction: Melamine in breast milk. Toxicol Res. 4:527. (Disponible en anglais seulement.)
Zeiger E. 1987. Carcinogenicity of mutagens: Predictive capability of the Salmonella Mutagenesis assay for rodent carcinogenicity. Cancer Research 47: 1287-1296. Testing laboratory: Haworth et coll. (1983) summarized in table 1. (Disponible en anglais seulement.)
Zhang Q, Gamboa da Costa G, Von Tungeln LS, Jacob CC, Brown RP, Goering PL. 2012. Urinary biomarker detection of melamine- and cyanuric acid-induced kidney injury in rats. Toxicol Sci. 129:1-8. (Disponible en anglais seulement.)
Zhu X, Wang, S, Liu Q, Xu Q, Xu S, Chen H. 2009. Determination of residues of cyromazine and its metabolite, melamine, in animal-derived food by gas chromatography-mass spectrometry with derivatization. J Agric Food Chem. 57:11075-11080. (Disponible en anglais seulement.)
Annexe A. Résultats de modélisationde la dégradation de la mélamine
Processus du devenir |
Modèle et base du modèle | Résultat et prévision du modèle |
Demi-vie extrapolée (jours) |
|---|---|---|---|
Oxydation atmosphérique |
AOPWIN 2010 |
t1/2 = 16,2 jours a |
≥ 2 jours |
Réaction avec l’ozone |
AOPWIN 2010 |
s.o. |
s.o. |
Abréviations : s.o. = sans objet
a L’estimation est basée sur une journée de 12 heures, et une concentration moyenne de OH dans la troposphère de 1,5 × 106 OH/cm³.
Processus du devenir |
Modèle et base du modèle | Résultat et prévision du modèle |
Demi-vie extrapolée (jours) |
|---|---|---|---|
Hydrolyse |
HYDROWIN 2010a,b |
s.o. |
s.o. |
| Biodégradation primaire (aérobie) | BIOWIN 2010b Sous-modèle 4 : enquête d’experts (résultats qualitatifs) |
3,3 c | ~ 182 |
| Biodégradation ultime (aérobie) | BIOWIN 2010b Sous-modèle 3 : enquête d’experts (résultats qualitatifs) |
2,3 c | ~ 182 |
| Biodégradation ultime (aérobie) | BIOWIN 2010b Sous-modèle 5 : Probabilité linéaire MITI |
0,02 d | ≥ 182 |
| Biodégradation ultime (aérobie) | BIOWIN 2010b Sous-modèle 6 : Probabilité non linéaire MITI |
0 d | ≥ 182 |
| Biodégradation ultime (aérobie) | CATALOGIC 2012 DBO (demande biologique en oxygène) |
% DBO = 0 « se biodégrade lentement » |
≥ 182 |
Abréviations : s.o. = sans objet.
a Le modèle ne précise pas d’estimation pour ce type de structure.
b EPI Suite (2010).
c Le résultat s’exprime par une valeur numérique de 0 à 5.
d Le résultat s’exprime par un taux de probabilité de 0 à 1.
Annexe B. Estimations de l’ingestion quotidienne de mélamine (µg/kg p.c./j) par la population générale du Canada par les aliments
Voie d’exposition |
0-6 mois nourris au lait maternel d |
0-6 mois nourris au lait maternisé e |
0-6 mois non nourris au lait maternisé e |
0,5–4 ans f |
5–11 ans g |
12–19 ans h |
20–59 ans i |
60 ans et plus j |
|
|---|---|---|---|---|---|---|---|---|---|
Aliments a |
- |
0,72 b (1,7) |
0,72 b (1,7) |
0,46c (1,2) |
0,32 (1,2) |
0,22 (0,73) |
0,21 (0,80) |
0,21 (0,80) |
|
Eau potable k |
- |
5,3 (21) |
2,0 (8,0) |
2,3 (9,0) |
1,8 (7,1) |
1,0 (4,0) |
1,1 (4,2) |
1,1 (4,4) |
|
Lait maternel |
2,7 (7,6) |
- |
- |
- |
- |
- |
- |
- |
|
Poussière / sol l |
< 0,0001 |
< 0,0001 |
< 0,0001 |
< 0,0001 |
< 0,0001 |
< 0,0001 |
< 0,0001 |
< 0,0001 |
|
Absorption totale |
2,7 (7,6) |
6,0 (22,7) |
2,7 (9,7) |
2,8 (10,2) |
2,1 (8,3) |
1,2 (4,7) |
1,3 (5,0) |
1,3 (5,2) |
|
a L’ingestion quotidienne par les aliments est fondée sur une évaluation semi-probabiliste; l’absorption moyenne est indiquée ici aux fins de discussions pour le tableau 8-6. Les valeurs entre parenthèses sont des valeurs au 95e centile. Les résultats de l’évaluation semi-probabiliste sont discutés dans le texte de la section 8.1.1 et présentés dans le tableau 8.1.
b D’après un groupe âgé de 1 an et moins plutôt que 0 à 6 mois; comprend les nourrissons nourris ou non à la préparation pour nourrissons.
c D’après un groupe âgé de 1 à 4 ans plutôt que 0,5 à 4 ans.
d Aucune donnée sur les concentrations de mélamine dans le lait maternel canadien n’a été relevée. En Turquie, la mélamine a été mesurée dans le lait maternel de 77 mères allaitantes. De la mélamine a été détectée dans 21 % des 77 échantillons, à des concentrations variant entre 10,1 et 76,4 µg/L (moyenne de 27,1 µg/L). Les concentrations moyenne et maximale de mélamine dans le lait maternel ont été utilisées pour estimer l’ingestion quotidienne.
e En supposant que le nourrisson pèse 7,5 kg, respire 2,1 m³ d’air par jour, boit 0,8 L d’eau par jour (nourri à la préparation pour nourrissons en poudre) ou 0,2 L d’eau par jour (non nourri à la préparation pour nourrissons) et ingère 30 mg de sol par jour (Santé Canada, 1998).
f En supposant que l’enfant pèse 15,5 kg, respire 9,3 m³ d’air par jour, boit 0,2 L d’eau par jour et ingère 100 mg de sol par jour (Santé Canada, 1998).
g En supposant que l’enfant pèse 31 kg, respire 14,5 m³ d’air par jour, boit 0,4 L d’eau par jour et ingère 65 mg de sol par jour (Santé Canada, 1998).
h En supposant que le jeune pèse 59,4 kg, respire 15,8 m³ d’air par jour, boit 0,4 L d’eau par jour et ingère 30 mg de sol par jour (Santé Canada, 1998).
i En supposant que la personne pèse 70,9 kg, respire 16,2 m³ d’air par jour, boit 0,4 L d’eau par jour et ingère 30 mg de sol par jour (Santé Canada, 1998).
j En supposant que la personne pèse 72 kg, respire 14,3 m³ d’air par jour, boit 0,4 L d’eau par jour et ingère 30 mg de sol par jour (Santé Canada, 1998).
k Aucune donnée sur les concentrations de mélamine dans l’eau potable canadienne n’a été relevée. Toutefois, les concentrations de mélamine dans l’eau potable répertoriées dans différentes régions du monde variaient entre 10 et 200 µg/kg (concentrations moyenne et médiane = 50 µg/kg) d’après 20 échantillons d’eau du robinet échantillonnés par l’industrie et déclarés à l’EFSA (2010). Les concentrations moyennes et maximales de mélamine dans l’eau potable ont été utilisées pour estimer l’exposition. Les valeurs entre parenthèses sont des valeurs maximales.
l Aucune donnée sur les concentrations de mélamine dans la poussière et aucune donnée sur les concentrations de mélamine dans le sol nord-américain n’ont été répertoriées. Cependant, en Chine, les sols ont été testés à une distance de 100 m et d’environ 150 km des usines de fabrication de mélamine. À 100 m, les concentrations de mélamine dans le sol variaient de 0 à 41,1 mg/kg. À environ 150 km des usines, les concentrations dans les sols agricoles variaient entre 0 et 0,176 mg/kg (Qin et coll., 2010). Comme les concentrations mesurées à plus grande distance d’une usine de fabrication de mélamine seraient plus représentatives des concentrations dans le sol du Canada, la concentration maximale mesurée dans le sol agricole à 150 km d’une usine de fabrication de mélamine a été utilisée dans une estimation déterministe de l’ingestion quotidienne.
Annexe C. Résumé des données sur l’occurrence de la mélamine utilisées pour estimer l’exposition alimentaire et la méthode d’évaluation alimentaire‡
Aliments |
Nbre d’échantillons |
Concentration moyenne de mélamine en µg/kg a (plage entre parenthèses) |
|---|---|---|
Préparation pour nourrissons – poudre (lait, soja) |
64 |
42,9 (< LD-346) |
Préparation pour nourrissons – concentrée (lait, soja) |
24 |
17,5 (5,5-34,5) |
Préparation pour nourrissons – prête à la consommation (lait, soja) |
6 |
27,5 (< LD-68,9) |
Lait – entier, 2 %,1 %, écrémé |
68 |
4,1 (< LD-7,4) |
Lait – évaporé, condensé |
17 |
8,3 (< LD-30,7) |
Lait frappé |
9 |
< LD (< LD) |
Lait en poudre |
11 |
6,3 (< LD-12,3) |
Lait au chocolat |
3 |
< LD (< LD) |
Autres boissons au lait |
6 |
23,3 (< LD-71,9) |
Crème |
4 |
< LD (< LD) |
Crème glacée, dessert de soja glacé |
11 |
< LD (< LD) |
Yogourt, boisson au yogourt |
37 |
4,2 (< LD-7,3) |
Friandise au chocolat ou au lait |
11 |
667,2 (< LD-7290) |
Café au lait, café |
15 |
87,9 (< LD-282) |
Thé au lait |
7 |
16,1 (< LD-89) |
Substituts de repas |
7 |
17,3 (< LD-53,0) |
Fromage |
7 |
< LD (< LD) |
Boissons de soja |
46 |
4,1 (< LD-6,6) |
Céréale de soja |
6 |
< LD (< LD) |
Tartinade de soja |
4 |
< LD (< LD) |
Œuf (en conserve, liquide, glacé) |
6 |
10,4 (< LD-42,1) |
Substitut de viande |
38 |
5,9 (< LD-36,4) |
Tofu |
12 |
< LD (< LD) |
Sauce (tartare, teriyaki, soja, hoisin) |
13 |
< LD (< LD) |
Mayonnaise |
16 |
4,1 (< LD-5,1) |
Pâtes, nouilles |
15 |
4,2 (< LD-5,9) |
Céréales pour petit déjeuner |
3 |
< LD (< LD) |
Barre énergétique |
14 |
5,4 (< LD-22,1) |
Crêpe, muffin, gaufre (mélange) |
17 |
< LD (< LD) |
Pâte à biscuit |
7 |
< LD (< LD) |
Gâteau (prêt à la consommation, mélange) |
18 |
4,6 (< LD-8,6) |
Tarte |
2 |
< LD (< LD) |
Saucisse sur bâtonnet, saucisse de Francfort, roulé à la saucisse |
3 |
< LD (< LD) |
Pépite ou lanière de poulet |
4 |
15,8 (< LD-27,6) |
Crevette |
75 |
71,8 (< LD-1156) |
Poisson (tilapia, sole) |
8 |
4,1 (< LD-4,8) |
Anguille |
4 |
52,2 (11,6-92,6) |
Épinards (gelés) |
4 |
8,8 (< LD-23,1) |
Pommes de terre (en conserve, séchées) |
26 |
4,9 (< LD-23,6) |
Champignons (en conserve, séchés, marinés) |
38 |
144,6 (< LD-757) |
Oignons (frais, surgelés, séchés, marinés, en poudre) |
12 |
4,3 (< LD-8,1) |
Tomates (en conserve, séchées, en pot, en jus, en soupe) |
38 |
36,9 (< LD-153) |
Mélanges de sauce en poudre |
9 |
18,4 (< LD-116) |
‡ Données provenant de Tittlemier et coll. 2009; Tittlemier et coll. 2010a; Tittlemier et coll. 2010 b.
a Une valeur équivalente à la limite de détection de 4 µg/kg a été attribuée aux échantillons dans lesquels aucune mélamine n’a été détectée; limite de détection.
Méthode et hypothèses pour l’évaluation de l’exposition par le régime alimentaire
Les données sur la consommation alimentaire sont tirées de l’Enquête sur la santé dans les collectivités canadiennes (ESCC) – Cycle 2.2 de 2004 de Statistique Canada. Les poids corporels mesurés et déclarés lors de l’ESCC ont aussi été utilisés. L’évaluation de l’ingestion alimentaire de la mélamine a été réalisée par la Direction des aliments de Santé Canada. Si les données sur la consommation de certains aliments n’étaient pas disponibles dans les données de l’ESCC (café ou thé au lait, barre énergétique), nous leur avons substitué des aliments similaires (café ou thé instantané au lait, barre de céréales). De plus, certains types d’aliments qui ont été analysés pour détecter la présence de mélamine en raison de la présence possible de protéines de lait ont été utilisés pour représenter les concentrations de tous ces types d’aliments (p. ex., produits de poulet, de saucisse et de biscuits). Dans les deux cas, l’exposition peut être surestimée en raison de la fréquence élevée de consommation des aliments de substitution ou de la présence de mélamine dans la protéine de lait, seulement. De même, les concentrations de mélamine détectées dans un certain nombre de produits transformés contenant des épinards, des pommes de terre, des champignons, des oignons et des tomates ont été utilisées pour représenter, de manière prudente, les concentrations de mélamine dans tous les produits alimentaires contenant ces légumes, y compris les légumes frais. Il est également probable que cette évaluation ait surestimé l’exposition à la mélamine par voie alimentaire.
Annexe D. Estimations de l’exposition à la mélamine par certains produits
À la lumière des renseignements disponibles, l’absorption par exposition cutanée a été estimée pour le contact direct avec des matelas et autres meubles contenant de la mousse pour les nourrissons, les tout-petits et les adultes. On a également estimé l’exposition orale pour les nourrissons et les tout-petits qui portent à la bouche (suçotent) des articles manufacturés en mousse destinés aux enfants. Les tableaux D-1 et D-2 présentent les valeurs et les paramètres d’exposition, fondés sur des hypothèses prudentes, qui sont utilisés pour estimer les expositions.
Estimations de l’absorption par voie cutanée
Absorption = [SC × FCP × FPT × M × DE × AC] / p.c.
Symbole |
Description |
Valeur |
|---|---|---|
SC a |
Superficie de contact avec la peau |
545 - 1 840 cm2 (nourrisson) 792 - 2 890 cm2 (tout-petit) 1 258 - 4 830 cm2 (enfant) 1 972 - 8 100 cm2 (adolescent) 2 033 - 9 100 cm2 (adulte) |
FCP b |
Facteur de contact avec la peau |
1 |
FPT c |
Facteur de pénétration du textile |
0,1 |
M d
|
Taux de migration |
0,00936 à 0,0217 mg/cm2/h |
DE e |
Durée de l’exposition |
12 h/j (nourrisson) 12 h/j (tout-petit) 10 h/j (enfant) 10 h/j (adolescent) 8 h/j (adulte) |
AC |
Absorption cutanée |
0,10 à 0,16 f |
p.c. g |
Poids corporel |
7,5 kg (nourrisson) 15,5 kg (tout-petit) 31,0 kg (enfant) 59,4 kg (adolescent) 70,9 kg (adulte) |
Absorption |
Absorption de mélamine (mg/kg p.c./j)
|
0,082 – 1,02 (nourrisson) 0,057 – 0,78 (tout-petit) 0,038 – 0,54 (enfant) 0,031 – 0,47 (adolescent) 0,022 – 0,36 (adulte) |
a Dans ce scénario, nous avons utilisé une fourchette de superficies de contact (SC) pour représenter le contact cutané avec un matelas. Pour la valeur faible de SC utilisée, nous présumons qu’une personne porte un short et un t-shirt couvrant la moitié de ses membres. La superficie de contact d’exposition est basée sur l’exposition de la moitié inférieure des membres (bras et jambes) et de l’arrière de la tête. Les superficies de contact des membres (Santé Canada 1995) ont été multipliées par une demie pour représenter la couverture par les vêtements, puis par un tiers, pour tenir compte de la forme triangulaire des membres, dont un seul côté est en contact direct avec le matelas (CPSC 2006). La superficie de contact de la tête (Santé Canada 1995) a été multipliée par un facteur de 0,5 dans le but de représenter l’exposition de l’arrière de la tête seulement. Pour les valeurs SC élevées utilisées, on présume que la moitié du corps est en contact cutané avec le matelas (US EPA 2012)b.
b Aucun facteur de contact avec la peau (FCP) particulier à la mélamine, c.-à-d. la fraction de substance sur une surface qui adhère à la peau, n’a été trouvé dans la littérature. Par conséquent, on a choisi une valeur de 1, car toute la quantité du produit chimique est susceptible d’être absorbée.
c Un facteur de pénétration du textile (FPT) a été appliqué pour la mélamine afin de tenir compte des taux de migration utilisés pour l’extrapolation (c.‑à‑d. le TDCPP et le TCEP) déterminés à l’aide de mousse non recouverte (ECHA 2018). Aucune donnée sur la pénétration de la mélamine dans les textiles n’a été trouvée dans la littérature. Par conséquent, une valeur de 0,1 (Driver et coll. 2007 citée dans ECHA 2018) a été utilisée pour le FPT.
d Taux de migration de la mousse depuis la surface du rembourrage (extrapolé à partir des taux de migration du TCEP et du TDCPP, indiqués dans le tableau 8-4).
e La durée d’exposition pendant le sommeil a été ajustée à partir des durées rapportées dans le CPSC américain (2006) pour les personnes qui s’assoient pour peu de temps sur un meuble en mousse, ceci afin de tenir compte des durées de sommeil plus longues par rapport à la position assise, et adaptée pour tenir compte des durées de sommeil moyennes, comme indiqué par l’EPA (2011).
f Aucune donnée sur l’absorption par voie cutanée n’a été trouvée pour la mélamine. Des composés structurellement similaires présentent des taux maximaux d’absorption cutanée de 10 à 16 % seulement pour la peau humaine (Ademola et coll. 1993; Baynes et coll. 2005).
g Santé Canada (1998).
Estimation de l’absorption par exposition par voie orale
Ingestion = [SC × M × DE] / p.c.
Symbole |
Description |
Valeur |
|---|---|---|
SC a |
Superficie exposée par la mise à la bouche |
10 cm2 (nourrisson) 10 cm2 (tout-petit) |
M b |
Taux de migration |
0,00936 à 0,0217 mg/cm2/h |
DE c |
Durée de l’exposition |
24,5 min/j (0,408 h/j) |
p.c. d |
Poids corporel |
7,5 kg (nourrisson) 15,5 kg (tout-petit) |
Absorption |
Absorption calculée en mg/kg p.c./j |
5,09 × 10-3 à 1,18 × 10-2 (nourrisson) 4,93 × 10-3 à 1,14 ×10-2 (tout-petit) |
a La superficie de contact chez les nourrissons est tirée de plusieurs références (RIVM 2008). Chez les tout‑petits, elle est basée sur le jugement scientifique professionnel qui reflète le double de la superficie de l’ouverture de la bouche d’un tout-petit.
b La plage des taux de migration de 0,00936 à 0,0217 mg/cm2/h présentée dans le scénario d’exposition par voie cutanée a également été utilisée pour l’estimation de l’exposition par voie orale. On suppose que la mélamine est complètement absorbée par voie orale et que la présence d’un revêtement textile sur un objet en mousse n’affecterait pas la migration de la mélamine (en d’autres mots, aucun facteur de pénétration du textile, FPT, n’est appliqué).
c Le temps que passent les enfants à porter à la bouche des produits en mousse comme les tapis de sieste, les sièges d’auto et les petits meubles est basé sur la durée de mise à la bouche des « autres objets » indiquée dans la publication de Norris et Smith (2002) et citée dans l’USEPA (2011).
d Santé Canada (1998).
Annexe E. Plages des volumes quotidiens types d’urine
Sexe |
Âge (années) |
Volumes moyens quotidiens d’urine (L/jour) | Référence |
|---|---|---|---|
Hommes et femmes |
6 – 11 |
0,274 – 1,14 |
ICRP, 2003; Lakind et Naiman, 2008; Lentner, 1981; Remer et coll., 2006 ; Wu, 2006 |
Hommes et femmes |
12 – 19 |
0,441 – 1,4 |
ICRP, 2003; Lakind et Naiman, 2008; Lentner, 1981; Remer et coll., 2006 |
Hommes et femmes |
20 – 59 |
0,6 – 2,03 |
Davison et Nobel 1981; Francis 1960; ICRP 2003; Lakind et Naiman 2008; Lentner 1981; Parboosingh et Doig 1973; Perucca et coll. 2007; Revúsová 1971; Van Haarst et coll. 2004; Wu, 2006 |
- |
0,8 – 2,7 |
Davison et Nobel 1981; Francis 1960; Higby et coll. 1994; Neithardt et coll. 2002; Parboosingh et Doig 1973; Thorp et coll. 1999; |
|
Hommes et femmes |
60 – 79 |
0,25 – 2,4 |
ICRP 2003; Lentner 1981; Wu 2006 |
Annexe F. Études internationales sur la mélamine
Les études de Kong et coll. (2011) et de Wu et coll. (2010a) ne peuvent être comparées à celle de Panuwet et coll. (2012), car différentes unités de mesure ont été utilisées (ng/ml ou µg/mmol de créatinine). L’étude de Liu et coll. (2011) indique des concentrations qui varient d’une quantité inférieure à la limite de détection de la méthode (LDM) à 192 ng/ml pour 422 sujets adultes de Taïwan. Ceci est comparable à la plage de concentrations trouvées chez 492 sujets de la population américaine (< limite de détection – 161 ng/mL).
Wu et coll. (2013) ont mené une étude unique sur la biosurveillance dans laquelle les concentrations de mélamine ont été mesurées dans l’urine de 12 adultes taïwanais qui ont consommé de la soupe aux nouilles chaude dans des bols en mélamine et en céramique, à différents moments. L’élimination totale de la mélamine dans l’urine était de 8,35 ± 1,91 µg 12 heures après la consommation de la soupe aux nouilles dans des bols en mélamine, et de 1,31 ± 0,44 µg 12 heures après la consommation de la soupe aux nouilles dans des bols en céramique (les volumes d’urine par personne n’ont pas été rapportés). L’élimination urinaire la plus élevée s’est produite après une période de plus de 4 à 6 heures, et était d’environ 6,8 µg/mmol de créatinine (interprétée à l’aide de la figure A de l’article). Comme l’élimination urinaire de la mélamine a une demi-vie déclarée de 6 heures, cela équivaut à environ 12,8 µg/mmol de créatinine après 24 heures. Ces valeurs correspondent à la plage de 0,02 à 20 µg/mmol de créatinine de mélamine dans l’urine rapportée par Wu et coll. (2010a) pour 22 adultes à Taïwan, indiquées dans le tableau F-1. Wu et coll. (2013) ont indiqué qu’une seule marque de bols en mélamine avait été sélectionnée pour cette étude, et d’était l’une des cinq marques testées dans l’étude de Chien et coll. (2011) (voir la section 8.1.2 « Migration depuis le melaware »).
Région |
Date de l’étude |
Nombre de sujets |
Âge |
Concentrations de mélamine |
Référence |
|---|---|---|---|---|---|
Hong Kong |
2009 |
502 : 167 hommes, 335 femmes |
6-20 |
Médiane = 0,8 (non détectable à 1 467) Non détectable dans 213 échantillons (42 %) 47 (9 %) échantillons > 7,1 µg/mmol créatinine (14 hommes, 33 femmes) |
Kong et coll., 2011 |
Taïwan |
2003-2007 |
22 témoins : 20 hommes, 2 femmes |
47-61 |
Médiane = 0,06 (0,02 à 20) µg/mmol de créatinine |
Wu et coll. 2010a |
Taïwan |
2003-2007 |
11 avec urolithiase (acide urique) : 10 hommes, 1 femme |
46-62 |
Médiane = 0,5 (0,07 à 1,18) µg/mmol de créatinine |
Wu et coll. 2010a |
Taïwan |
2003-2007 |
21 avec urolithiase (calcium) 19 hommes, 2 femmes |
48-58 |
à 58 Médiane = 0,14 (0,07 à 0,93) µg/mmol de créatinine |
Wu et coll. 2010a |
Taïwan |
2003-2007 |
211 témoins : 132 hommes, 79 femmes |
52,4 ± 11,9 (médiane = 52,0) |
< MDL [0,8] à 56 ng/mL LDM dans 168 (80 %) échantillons 23 échantillons à LDM à 3,11 ng/mL 20 échantillons ≥ 3,12 ng/mL |
Liu et coll., 2011 |
Taïwan |
2003-2007 |
211 avec urolithiase (calcium) 132 hommes, 79 femmes |
52,3 ± 12,0 (médiane = 53,0) |
< MDL [0,8] à 192 ng/mL LDM dans 80 échantillons 64 échantillons à LDM à 3,11 ng/mL 67 échantillons ≥ 3,12 ng/mL |
Liu et coll., 2011 |
Abréviations : N.D. = non détectée; LDM = limite de détection de la méthode.
