Méthode d’essai biologique servant à mesurer la survie de collemboles exposés à des contaminants dans le sol : chapitre 1
Section 1
Introduction
1.1 Contexte
L’Unité de l’élaboration et de l’application des méthodes (UEAM) d’Environnement Canada est responsable de mettre au point, de normaliser et de publier des méthodes d’essai biologique (v. annexe A) applicables à la mesure et à l’évaluation, dans des conditions de laboratoire contrôlées et définies, des effets toxiques d’échantillons de substances ou matières d’essai sur des organismes terrestres ou aquatiques (essais monospécifiques). En 1994, l’UEAM, l’Association canadienne des producteurs de pétrole et le gouvernement fédéral, par le biais du Programme de recherche et de développement énergétiques, ont lancé un programme pluriannuel afin d’étudier, de concevoir, de valider et de publier un certain nombre de méthodes d’essai normalisées pour mesurer la toxicité d’échantillons de sol contaminé ou susceptible d’être contaminé, en faisant appel à des espèces terrestres appropriées d’organismes expérimentaux. Le programme avait pour but de mettre au point des méthodes applicables à divers types de sols canadiens auxquels seraient exposées des espèces terrestres représentatives des écosystèmes de ces sols. Sa phase initiale comprenait un examen exhaustif des méthodes d’essai biologique utilisées dans le monde afin d’évaluer la toxicité de sols contaminés pour des plantes et des invertébrés terrestres. Les auteurs du rapport rédigé au terme de cet examen ont recommandé qu’Environnement Canada appuie l’élaboration, la normalisation et la publication d’un certain nombre de méthodes d’essai biologique monospécifique servant à mesurer la toxicité d’échantillons de sols, y compris pour des collemboles (Bonnell Environmental Consulting, 1994). Cette recommandation a reçu l’aval de l’administration centrale et des bureaux régionaux d’Environnement Canada (v. annexe B) ainsi que du Groupe intergouvernemental sur les essais écotoxicologiques (v. annexe C).
Depuis 1994, Environnement Canada a publié diverses méthodes d’essai biologique normalisées, dont les suivantes : Essai pour déterminer la toxicité de sols contaminés pour les vers de terre (Eisenia andrei, Eisenia fetida ou Lumbricus terrestris), SPE 1/RM/43 (EC, 2004a); Essai de mesure de la levée et de la croissance de plantes terrestres exposées à des contaminants dans le sol, SPE 1/RM/45 (EC, 2005a, modifiée en 2007).
Environnement Canada a aussi coordonné ou appuyé de nombreux essais de toxicité des sols avec diverses espèces de collemboles (Folsomia candida, Orthonychiurus folsomi et Folsomia fimetaria) exposées à des échantillons de sol non contaminé et de sol contaminé par des pesticides, des métaux, des déchets pétrochimiques ou des toxiques de référence possibles. Ces études (AquaTerra, 1998; Stephenson et coll., 1999a, 1999b, 2000a; AquaTerra et ESG, 2000; ESG, 2000, 2001, 2002; ESG et AquaTerra, 2002, 2003; Becker- van Slooten et coll., 2003, 2005; Stämpfli et coll., 2005; EC, 2007a) étaient axées sur la mise au point et la normalisation d’une méthode d’essai de toxicité létale ou sublétale d’échantillons de sol contaminé. En se basant sur ces travaux et sur les conclusions d’une série d’études interlaboratoires de validation (EC, 2007b), Environnement Canada a entrepris de préparer et de publier une méthode d’essai biologique pour réaliser des essais de toxicité d’un sol, dans laquelle on mesure la survie et la reproduction des trois espèces de collemboles susmentionnées. Cette méthode est décrite dans la première édition du présent rapport (EC, 2007c).
Un comité consultatif scientifique (v. annexe D) composé de spécialistes internationaux possédant de l’expérience dans la conception et la réalisation d’essais de toxicité d’un sol avec des collemboles a fourni des documents de référence clés qui ont été examinés et pris en considération durant l’exécution du projet. Les membres de ce comité ont également participé activement aux travaux en tant que pairs relecteurs de deux versions préliminaires de la première édition du présent document, tandis qu’un groupe élargi de personnes compétentes (v. les remerciements) a formulé des observations additionnelles après avoir examiné la dernière version préliminaire. Dans la préparation de la première édition de la méthode, Environnement Canada a tablé sur l’expérience de la communauté scientifique internationale dans la réalisation d’essais semblables visant à évaluer la toxicité d’échantillons de sol pour des collemboles (v. annexes E et F).
En 2003, l’UEAM a tenu un atelier de trois jours sur l’évaluation toxicologique de sols du Canada et sur la mise au point de méthodes d’essai normalisées. À partir de la documentation distribuée avant l’atelier (un questionnaire), des séances plénières et des discussions des groupes de travail, les participants ont cerné des domaines prioritaires en matière de recherche et développement. Ils ont recommandé de prioriser l’affectation de ressources à la mise au point de méthodes d’essai plus représentatives de sols ou d’habitats non agricoles. Étant donné que les écozones de la région boréale et de la taïga couvrent >50 % de la masse continentale du Canada et que leurs ressources pétrolières, gazières, minières et forestières revêtent une grande importance pour l’économie canadienne, il a été décidé de s’intéresser avant tout à la conception d’essais normalisés applicables à l’évaluation de contaminants présents dans des sols de la région boréale. Depuis ce temps, on a consacré plusieurs années de recherche au choix d’organismes expérimentaux sensibles convenant à la mesure de la toxicité de différents types de sols afin de répondre aux besoins de l’industrie et de satisfaire aux exigences canadiennes en matière de réglementation et de surveillance, de même qu’à la mise au point de méthodes d’essai biologique appropriées. Ainsi, Environnement Canada a préparé et publié une nouvelle méthode de mesure de la croissance de plantes terrestres indigènes de la région boréale (EC, 2013a), en plus d’effectuer des recherches sur les espèces de collemboles convenant aux essais de toxicité de sols de la forêt boréale (EC, 2010, 2013b). Le Ministère a mené de nombreuses études axées sur la mise au point de méthodes d’élevage de collemboles de l’espèce Proisotoma minuta (qui se reproduit par voie sexuée) ainsi que de méthodes d’essai faisant appel à cette espèce et à des sols des écozones de la région boréale et de la taïga. Les résultats de ces études ont mené aux indications décrites ici sur l’élevage de P. minuta, de même qu’aux procédures et conditions relatives à l’exécution d’essais toxicologiques visant à mesurer la survie et la reproduction de cette espèce dans des échantillons de sol de la forêt boréale.
Le présent document décrit en détail tant les conditions et modes opératoires connexes à l’application de la méthode d’essai que les procédures universelles de préparation et d’exécution des essais de toxicité d’un sol avec des espèces choisies de collemboles (F. candida, O. folsomi, F. fimetaria ou P. minuta). Des conseils sont aussi fournis au sujet des ensembles particuliers de conditions et de modes opératoires qui sont exigés ou recommandés lorsque la méthode d’essai biologique vise l’évaluation de différents types de substancesou matières (p. ex., des échantillons de sol ou de déchets particulaires semblables prélevés sur le terrain ou des échantillons d’une substance chimique ou plus mélangée ou mise en contact en laboratoire avec un sol naturel ou artificiel). La présente version révisée du rapport SPE 1/RM/47 renferme des indications spéciales relatives au prélèvement et à la manipulation d’échantillons de sols de la forêt boréale et de la taïga, de même qu’aux essais sur ces sols. Les paramètres biologiques établis pour les essais toxicologiques sont la survie (mortalité) et le succès de la reproduction, qu’on mesure à la fin de l’essai.
Le diagramme de la figure 1 donne un aperçu des procédures universelles abordées ici. Il énumère les aspects particuliers qui concernent expressément les essais sur des échantillons de sol ou de déchets particulaires semblables prélevés sur le terrain (p. ex., boues d’épuration, boues de forage, déblais de dragage) ou de sol enrichi en laboratoire avec une ou des substances chimiques.
Figure 1. Points à considérer dans la préparation et l’exécution d’essais de toxicité des sols avec des collemboles et divers types de substances ou matières d’essai
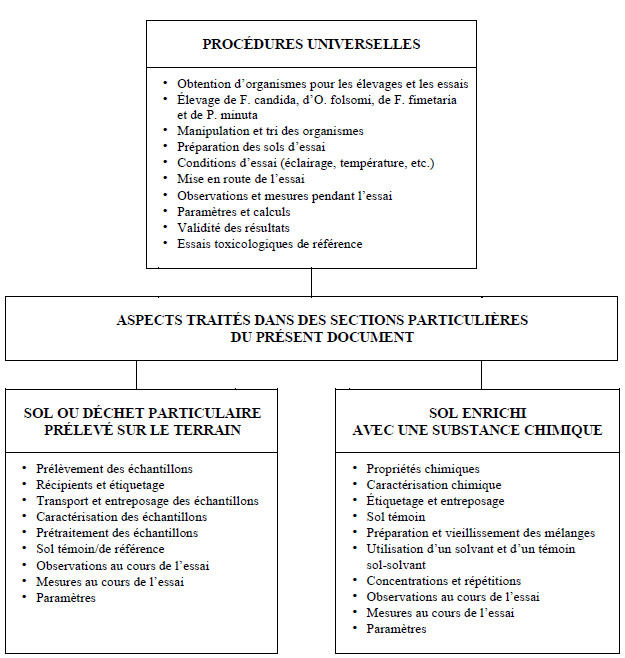
Graphique décrivant les conditions et les procédures d'essai appropriées pour l'analyse de différents types de matières
Cette figure divise les méthodes présentées dans ce document en deux catégories d’analyses spécialisées en plus d’énumérer les modes opératoires universels qui sont communs à l’analyse de toute substance. Les deux catégories spécialisées sont particulières à l’analyse du sol enrichi d’une substance chimique et du sol prélevé sur le terrain ou de déchets particulaires.
La méthode d’essai a été conçue pour évaluer la toxicité létale et sublétale d’échantillons de matière, notamment :
- un sol prélevé sur le terrain, contaminé ou susceptible d’être contaminé;
- un sol qu’on envisage d’éliminer ou d’assainir;
- un sol qui a déjà été assaini;
- des déblais de dragage destinés à être éliminés par épandage sur le sol après déshydratation;
- des boues industrielles ou ménagères et des déchets particulaires semblables qui pourraient être déposés sur le sol;
- un sol contaminé ou non contaminé (naturel ou artificiel), enrichi avec une ou des substances chimiques (p. ex., pour une évaluation du risque que posent des substances chimiques nouvelles ou d’utilisation courante).
Dans la mise au point de la présente méthode d’essai biologique, on s’est efforcé de trouver un équilibre entre les considérations scientifiques, pratiques et pécuniaires et de faire en sorte que les résultats soient suffisamment précis pour la plupart des situations dans lesquelles ils seront appliqués. On suppose que l’utilisateur a une certaine connaissance des essais de toxicité des sols. Des instructions précises en lien avec les exigences d’un protocole réglementaire ne sont pas fournies dans le présent rapport, mais ce dernier se veut néanmoins un document d’orientation utile dans le contexte d’un tel protocole et pour d’autres applications. Le présent rapport constitue une version révisée et à jour de SPE 1/RM/47 (EC, 2007c), qu’elle remplace et annule.
Le lecteur qui souhaite obtenir des indications sur la mise en œuvre de la présente méthode d’essai biologique et d’autres méthodes, de même que sur l’interprétation et l’application des données relatives aux paramètres mesurés afin de déterminer la toxicité d’un sol, est invité à consulter les sous-sections 4.12, 5.5 et 5.6.4 de EC (1999).
1.2 Identification, répartition et cycle biologique des collemboles F. candida, O. folsomi, F. fimetaria et P. minuta
Les espèces expérimentales à utiliser dans la méthode d’essai biologique décrite ici, soit F. candida, O. folsomi, F. fimetaria et P. minuta, appartiennent à la classe Collembola (embranchement Arthropoda; sous- embranchement Pancrustacea; superclasse Hexapoda). Les collemboles sont considérés actuellement comme formant une classe monophylétique (c.-à-d. dont les éléments sont issus d’un même ancêtre) de l’embranchement Arthropoda (Hopkin, 2002; Bellinger et coll., 2013). Ils ont toujours été considérés comme formant un ordre à l’intérieur de la classe Insecta; toutefois, leur emplacement par rapport à d’autres arthropodes fait l’objet d’un intense débat et, compte tenu des théories modernes de l’évolution et des progrès en phylogénie moléculaire, leur place reste à définir (Hopkin, 1997, 2002).
Parmi les arthropodes, les collemboles sont les plus abondants et les plus répandus dans les écosystèmes terrestres et on les trouve un peu partout dans la grande variété de types de sols canadiens. Des informations faisant autorité au sujet de l’identification, de la systématique, de la répartition, de la biologie, de la physiologie et du cycle biologique des collemboles, y compris les espèces F. candida, O. folsomi, F. fimetaria et P. minuta, sont fournies dans plusieurs ouvrages et sites Web, notamment : Hopkin, 1997, 2006 (http://www.stevehopkin.co.uk); Fountain et Hopkin, 2005; Bellinger et coll., 2013 (http://www.collembola.org).
Les collemboles sont des invertébrés aptérygotes (dépourvus d’ailes) du sol. La figure 2 illustre les principales parties du corps des espèces à utiliser dans la présente méthode d’essai. Le corps du collembole peut être divisé en trois parties principales : (i) la tête, qui porte une paire d’antennes, une paire d’yeux (mais pas toujours) et des pièces buccales, contenues dans la capsule céphalique; (ii) le thorax, constitué de trois segments portant chacun une paire de pattes; (iii) l’abdomen, qui compte six segments. Chez plusieurs espèces, certains des segments abdominaux sont fusionnés, ce qui rend leur distinction difficile (Hopkin, 1997; Bellinger et coll., 2013). La furca constitue l’organe de saut des collemboles. Lorsqu’elle est présente (la furca est absente ou est devenue un vestige chez certaines espèces confinées au sol), elle est située sur la face ventrale du quatrième segment abdominal et est habituellement repliée sous l’abdomen. La furca provient d’une paire d’appendices qui ont fusionné à la base pour former le manubrium. Les deux parties distales sont restées séparées et ont évolué en une paire de structures appelées dentes (au singulier, une dens). Chaque dens se termine par une griffe modifiée appelée mucron. Les collemboles utilisent leur mucron pour exercer une poussée ou pour s’accrocher au sol, ce qui leur fournit le point d’appui nécessaire pour sauter (Hopkin, 1997). Tous les collemboles sont pourvus d’un tube ventral (paire de sacs éversés à fines parois, très près l’un de l’autre, situés sur la face ventrale du premier segment abdominal) qui joue un rôle important dans les échanges de fluides avec le milieu extérieur (régulation de la teneur en eau et en sel) (Rundgren et van Gestel, 1998; Hopkin, 2000; Fountain et Hopkin, 2005), de même que dans l’ingestion de toxiques dissous dans l’eau interstitielle (Lock et Janssen, 2003). Le tube ventral permet également aux collemboles d’adhérer à des surfaces glissantes (Hopkin, 2002).
Les collemboles occupent une place cruciale dans le réseau trophique du sol, car ce sont des consommateurs de champignons, de détritus, de nématodes et de bactéries (Lee et Widden, 1996; Laskowski et coll., 1998). Ils constituent également l’un des importants groupes de proies pour les prédateurs invertébrés généralistes dans les agro-écosystèmes, tels que les acariens, les mille-pattes, les araignées, les carabes et les staphylins (Bilde et coll., 2000; OCDE, 2009). Les collemboles contribuent aux processus de décomposition et de respiration dans le sol, principalement en se nourrissant d’hyphes fongiques (Hopkin, 2000), mais leur rôle dans la formation de l’humus demeure mal connu. Dans le sol, il a été démontré qu’ils ont une incidence sur la croissance des mycorhizes et la lutte contre des maladies fongiques de certaines plantes (Laskowski et coll., 1998; Hopkin, 2000; Fountain et Hopkin, 2005). Dans les sols forestiers acides, ils représentent peut-être les invertébrés les plus importants puisque les vers de terre et les diplopodes y sont absents (OCDE, 2009). Lorsque les conditions sont favorables, on observe couramment des densités de population de collemboles de 105/m2 dans les couches de sol et de feuilles mortes (OCDE, 2009). Les collemboles sont des membres importants de la pédofaune et constituent des organismes appropriés pour l’évaluation de sols potentiellement toxiques. De plus, en comparaison d’autres organismes comme les invertébrés à corps mou (p. ex., les vers de terre), les collemboles pourraient présenter une voie ou, au moins, un taux d’exposition différents (OCDE, 2009).
Figure 2. Femelle adulte de l’espèce F. candida
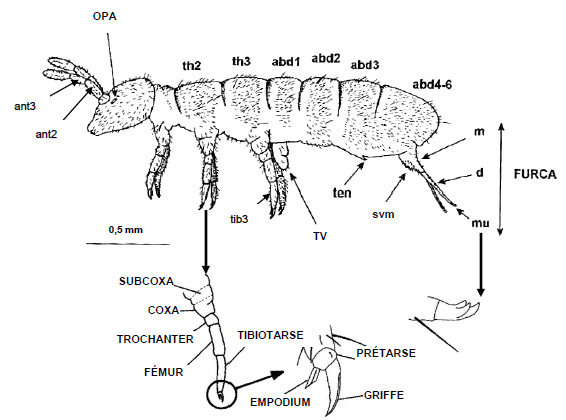
Graphique d’une femelle adulte Folsomia candida
Cette figure représente les principales parties du corps des quatre espèces décrites dans la présente méthode d’essai. La furca est normalement repliée sous l’abdomen auquel elle est rattachée par le tenaculum. Le premier segment thoracique est réduit dorsalement en comparaison du deuxième et du troisième. Les trois derniers segments abdominaux sont fusionnés. Les antennes sont divisées en quatre segments. Les autres parties principales du corps sont les suivantes : dens, manubrium, mucro, organe postantennaire, soies ventrales du manubrium et tibiotarse.
Cette figure illustre les principales parties du corps des quatre espèces décrites dans la présente méthode d’essai. La furca est normalement repliée sous l’abdomen auquel elle est rattachée par le tenaculum (ten). Le premier segment thoracique est réduit dorsalement en comparaison du deuxième (th2) et du troisième (th3); les trois derniers segments abdominaux (abd 4-6) sont fusionnés. Les antennes (ant) sont divisées en quatre segments. Les autres parties principales du corps sont les suivantes : dens (d); manubrium (m); mucron (mu); organe postantennaire (OPA); soies ventrales du manubrium (svm); tube ventral (tv); tibiotarse (tib) (d’après Fountain et Hopkin, 2005, figure 1, et Hopkin, 1997, figure 4.1, avec l’autorisation de S. Hopkin)
1.2.1 Folsomia candida
Folsomia candida Willem, 1902, espèce connue sous le nom de collembole du compost (Römbke et coll., 2006), fait partie des espèces de collemboles les plus étudiées (Hopkin, 1997). Elle appartient à la famille des Isotomidae :
- classe, Collembola
- ordre, Entomobryomorpha
- super-famille, Isotomoidea
- famille, Isotomidae
- sous-famille, Proisotominae
(Bellinger et coll., 2013). F. candida ressemble à O. folsomi en ce sens que l’organisme est dépourvu de pigments, d’yeux et d’épines anales. Toutefois, contrairement à O. folsomi, F. candida est une espèce parthénogénétique(reproduction asexuée). Les femelles pondent des œufs non fertilisés qui évoluent en descendants viables; les mâles sont complètement absents de la population. F. candida est une espèce hémi-édaphique(Schrader et coll., 1997) et possède une furca bien développée (Hopkin, 1997). Les adultes mesurent 1,5-3,0 mm de longueur lorsqu’ils arrivent à maturité (Fountain et Hopkin, 2005).
La diagnose de F. candida comprend les caractéristiques suivantes :
- absence d’ocelles;
- rapport entre la longueur de la soie la plus longue et l’extrémité de l’abdomen/la longueur du mucron se situant entre 2 et 4 environ;
- manubrium doté de nombreuses (16-32) soies ventrales (antérieures) robustes;
- dens portant 20-40 soies ventrales (antérieures) et 7-10 soies dorsales (postérieures);
- organe postantennaire très large, mais plus court que la largeur du premier segment antennaire (figure 2) (Fountain et Hopkin, 2005; Hopkin, 2006).
F. candida est une espèce présente dans la plupart des régions du monde, à l’exception de l’Afrique et de l’Inde (Hopkin, 1997). Il est difficile d’établir avec certitude ses aires de répartition biogéographique originelles, car des organismes ont été transportés partout dans le monde dans de petites portions de sol (Fountain et Hopkin, 2005). Au Canada, sa présence est limitée principalement aux régions méridionales (Christiansen et Bellinger, 1980). F. candida est une espèce indigène des sols forestiers de l’Ontario et du Québec (Addison, 1996); cependant, elle présente une faible importance écologique (elle n’est pas abondante) dans les sols des forêts boréales et des régions septentrionales du Canada (Römbke et coll., 2006). La présence de cette espèce a également été consignée en Colombie-Britannique (Skidmore, 1995). On trouve F. candida dans une variété d’habitats, dont des cavernes, des mines, des systèmes agricoles, des sols à forte teneur en matière organique (TMO), des forêts, des rives de cours d’eau et des serres (Fountain et Hopkin, 2005; Hopkin, 2006). L’espèce est bien adaptée aux sols secs. Des adaptations physiologiques empêchent le dessèchement de l’organisme, qui est en outre capable d’absorber la vapeur d’eau (Fountain et Hopkin, 2005). L’oxygène est absorbé par la cuticule (absence de trachée) et l’organisme peut survivre jusqu’à 18 h dans des conditions entièrement anaérobies ou en présence de concentrations élevées de dioxyde de carbone (Fountain et Hopkin, 2005).
Comme d’autres collemboles, F. candida se nourrit d’hyphes fongiques. Dans des études en microcosme menées en laboratoire, F. candida a montré une préférence pour les champignons croissant sur la surface de la couche de feuilles mortes plutôt que sur des particules de sol et il a été clairement montré que l’organisme est un agent important de décomposition (Fountain et Hopkin, 2005). Il a aussi été démontré que le type de champignon dont se nourrit F. candida a une incidence sur la croissance et la fécondité de l’organisme (certains taxons de champignons sont plus nutritifs que d’autres) (Fountain et Hopkin, 2005).
F. candida peut se reproduire 12-16 jours après l’éclosion (Spahr, 1981). Cependant, la première ponte se produit généralement entre 17 et 26 jours après l’éclosion, le plus souvent après 21-22 jours (K. Becker-van Slooten, Laboratoire de chimie environnementale et d’écotoxicologie, ENAC-ISTE, École polytechnique fédérale de Lausanne, Lausanne, Suisse, comm. pers., 2006). Cette espèce présente un taux de reproduction élevé et les populations consistent exclusivement en femelles parthénogénétiques. Les œufs sont pondus en petits groupes ou sur les œufs déjà déposés par d’autres femelles, formant des agrégats facilement visibles à l’œil nu dans les élevages en laboratoire. La surpopulation ou des densités de population élevées réduisent le nombre d’œufs pondus (Hopkin 1997; Fountain et Hopkin, 2005). Pendant les premiers stades larvaires, chaque ponte compte ~20 œufs, mais ce nombre augmente à 100 autour du 20e stade larvaire, avant de baisser à 60 au 30e stade (Snider, 1973; Hopkin, 1997). F. candida mue tous les 3-8 jours, passant par un court stade larvaire reproductif (~1,5 jour) en alternance avec des stades larvaires non reproductifs plus longs (~8,5 jours) (Fountain et Hopkin, 2005). L’oviposition se produit tous les 5-10 jours, selon l’âge de l’organisme (Snider, 1973). Les œufs, blancs, sphériques et mesurant 80-110 μm de diamètre, éclosent au bout de 7-10 jours. La température optimale pour une éclosion fructueuse est de 21 °C; les œufs maintenus à une température de >28 °C ne réussiront pas à éclore (Fountain et Hopkin, 2005). F. candida a une durée de vie de ~140 jours (190 jours au maximum) et peut muer jusqu’à 45 fois dans des conditions de laboratoire à 21 °C. La longévité peut presque doubler et la production d’œufs est plus élevée de ~30 % à 15 °C comparativement à 21 °C (Hopkin, 1997). Les écotoxicologues font souvent appel à F. candida pour les essais de toxicité normalisés (Hopkin, 1997). Il est très facile d’élever ces organismes en laboratoire et leur biologie et leur écologie sont très bien connues. La figure 3 montre un collembole F. candida de 10-12 jours, issu d’un élevage synchrone et prêt à être utilisé dans un essai.
1.2.2 Orthonychiurus folsomi
Orthonychiurus folsomi Schäffer, 1900 (auparavant dénommé Onychiurus folsomi), appartient à la famille des Onychiuridae :
- classe, Collembola
- ordre, Poduromorpha
- super-famille, Onychiuroidea
- famille, Onychiuridae
- sous-famille, Onychiurinae
(Bellinger et coll., 2013). O. folsomi est un petit collembole euédaphique, aveugle et peu pigmenté, qui vit dans les espaces interstitiels entre les particules de sol ou sous les pierres et le bois pourri sur la surface du sol. O. folsomi possède plusieurs caractéristiques typiques des espèces vivant en permanence dans les espaces interstitiels du sol. Ces caractéristiques, qui permettent un meilleur accès à l’habitat et qui facilitent les mouvements dans le sol (Kamplichler et Hauser, 1993), sont les suivantes : absence de furca, absence d’yeux, tégument blanchâtre, corps allongé (≤1,9 mm de longueur) avec un abdomen arrondi, pièces buccales pointant vers le bas, absence d’épines anales.
La diagnose d’O. folsomi comprend les caractéristiques suivantes :
- absence d’ocelles (lentilles oculaires);
- organe postantennaire elliptique complexe comportant 10-12 vésicules complexes;
- absence d’épines anales;
- organe sensoriel dorsal sur le troisième segment antennaire, comportant quatre papilles;
- ongle interne comportant une petite dent;
- onguicule légèrement plus court que l’ongle et sans lamelle;
- chez le mâle, tube ventral consistant en 4 soies modifiées sur le deuxième segment abdominal.
Les tibiotarses des pattes portent 9 soies distales; l’empodium, long et filamenteux, atteint la même longueur que la griffe (figure 2). Les pseudocelles, absents du premier segment thoracique, se distribuent selon la formule dorsale 32/022/33342 (ou 3) et la formule ventrale 2/010/0101 (Hopkin, 2006)Notes de bas de page1. pseudocelles sont des pores (petites zones de fine cuticule) d’où un fluide est sécrété comme mécanisme de défense lorsque l’organisme se sent menacé (p. ex., en présence d’un prédateur).
O. folsomi est une espèce commune dans les sols d’Amérique du Nord. Ce détritivore joue un rôle fonctionnel important dans le cycle des nutriments dans le sol. L’espèce se reproduit sexuellement par transfert indirect de sperme. Le sperme est produit par une paire de testicules et éjaculé par un orifice génital simple dans un spermatophore, qui est déposé sur le substrat ou directement sur la femelle. Cette dernière possède une paire d’ovaires et les œufs sont pondus individuellement, mais souvent en grappes ou en couvées. Le dimorphisme sexuel est rarement évident et il est difficile de distinguer les mâles des femelles. Les femelles sont généralement un peu plus grosses, surtout si elles sont fécondes. On peut déterminer le sexe d’un organisme en examinant la plaque génitale, mais cela exige un puissant grossissement. Des caractéristiques sexuelles secondaires subtiles peuvent parfois permettre de distinguer les mâles des femelles. Par exemple, les soies peuvent être légèrement plus courtes chez les mâles et il arrive que les pattes des mâles soient pourvues d’épines supplémentaires. La figure 4 montre le dimorphisme sexuel d’O. folsomi - ces collemboles sont issus d’un élevage synchrone et sont prêts à être utilisés dans un essai.
Snider (1983) a étudié l’oviposition, le développement des œufs et la fécondité chez O. folsomi. L’auteur a constaté que la température avait une incidence sur la durée du développement des œufs et que le temps d’éclosiondiminuait lorsque la température augmentait. À 15 °C et 21 °C, l’éclosion se produisait après 21 jours et 14 jours, respectivement; à 27 °C, il fallait compter seulement 11 jours. À 15 °C et 21 °C, le temps d’éclosion était moins variable et la viabilité des œufs était supérieure. La ponte commençait plus tôt à 21 °C (4 semaines) qu’à 15 °C (5 semaines). La taille de la ponte variait entre 15 et 45 œufs à 15 °C, et entre 12 et 36 œufs à 21 °C.
Snider (1983) a également observé que la surpopulation nuisait à la fécondité (il y avait quatre fois plus d’œufs dans les petits élevages que dans les grands) et que l’élevage en couple constituait la meilleure technique d’élevage. Contrairement à Snider, AquaTerra (1998) a observé que les élevages présentant une plus grande densité de population étaient plus productifs que les élevages contenant un plus petit nombre d’individus.
1.2.3 Folsomia fimetaria
Folsomia fimetaria Linnaeus, 1758, comme F. candida, appartient à la famille des Isotomidae :
- classe, Collembola
- ordre, Entomobryomorpha
- super-famille, Isotomoidea
- famille, Isotomidae
- sous-famille, Proisotominae
(Bellinger et coll., 2013). Comme F. candida également, F. fimetaria est une espèce hémi-édaphique (Folker-Hansen et coll., 1996; Bilde et coll., 2000; Kanal, 2004) dépourvue de pigments et d’yeux et dotée d’une furca très développée (Jensen et coll., 2003). En revanche, F. fimetaria se reproduit par voie sexuée, alors que F. candida est une espèce parthénogénétique (v. 1.2.1), et les adultes sont plus petits (0,8-1,4 mm de longueur).
La diagnose de F. fimetaria comprend les caractéristiques suivantes :
- absence d’ocelles;
- rapport entre la longueur de la soie la plus longue et l’extrémité de l’abdomen/la longueur du mucron se situant entre 3,2 et 4,0;
- manubrium doté de 4 + 4 soies apicales ventrales (antérieures), dont 3 + 3 dans une rangée transversale et 1 + 1 au-dessus;
- dens portant 18-24 soies ventrales (antérieures) et 5 soies dorsales (postérieures).
L’organe postantennaire est étroit et presque aussi long que la largeur du premier segment antennaire (Hopkin, 2006). De nos jours, il est possible de distinguer sans problème cette espèce des autres espèces appartenant au même genre en raison de la position unique des soies du manubrium et d’autres caractéristiques (Fjellberg, 1980); toutefois, il faut veiller à ne pas confondre F. fimetaria avec d’autres collemboles blancs et dépourvus d’yeux appartenant au même genre, tels que F. candida, F. lawrencei et F. litsteri (Krogh, 2004). Les collemboles F. candida (v. 1.2.1) peuvent être confondus avec ceux de l’espèce F. fimetaria et vice versa, mais il existe un bon moyen pour les distinguer : F. candida porte 2 + 2 ou 3 + 3 soies sur la face ventrale du troisième segment thoracique, alors que ces soies sont absentes chez F. fimetaria (Hopkin, 2006).
F. fimetaria est une espèce très répandue et très commune dans plusieurs types de sols allant des sols sableux aux sols limoneux et des sols à mull aux sols à mor (OCDE, 2009). Sa présence a été relevée dans des sols agricoles partout en Europe (Römbke et coll., 2006); toutefois, il existe peu de preuves que cette espèce se rencontre dans les forêts boréales ou les zones septentrionales. Au Canada, on a observé F. fimetaria dans les Territoires du Nord-Ouest, en Colombie-Britannique, en Alberta, au Manitoba, en Ontario, au Nouveau-Brunswick et à Terre-Neuve (Skidmore, 1995).
F. fimetaria est une espèce omnivore - elle se nourrit d’hyphes fongiques, de bactéries, de protozoaires et de détritus (OCDE, 2009). Dans les sols agricoles, l’organisme est considéré comme une proie importante pour les prédateurs arthropodes bénéfiques dont le rôle dans l’élimination des insectes nuisibles est reconnu. Par conséquent, F. fimetaria peut stabiliser ces populations d’insectes bénéfiques à une densité souhaitable dans les systèmes agricoles intégrés et biologiques (Laskowski et coll., 1998). On a observé chez F. fimetaria un degré élevé de sélectivité alimentaire, avec une préférence pour les champignons qui optimisent sa croissance, sa survie et sa fécondité. Ce collembole pouvait même choisir l’aliment optimal lorsqu’une espèce fongique était cultivée dans différents substrats de sol. Le haut degré de sélectivité concernant la qualité des aliments pourrait être attribuable à la production d’une odeur fongique perceptible par les collemboles de cette espèce (Jørgensen et coll., 2003).
F. fimetaria atteint la maturité sexuelle au bout de 18 jours, lorsque débute le sixième stade larvaire. Il est difficile de discerner les différences sexuelles entre mâles et femelles avant le 20e jour suivant l’éclosion. Les mâles ont un corps plus élancé et sont moitié moins longs que les femelles (Krogh, 2004). F. fimetaria présente de nombreuses caractéristiques souhaitables comme espèce à utiliser dans des essais toxicologiques, notamment la facilité avec laquelle les organismes peuvent être élevés en nombres suffisants et le fait qu’ils se reproduisent rapidement et continuellement tout au long de l’année, ce qui permet de disposer en tout temps d’organismes expérimentaux (Riepert et Kula, 1996). La figure 5 montre le dimorphisme sexuel de F. fimetaria - ces collemboles sont issus d’un élevage synchrone et sont prêts à être utilisés dans un essai.
1.2.4 Proisotoma minuta
Proisotoma minuta Tullberg, 1871, comme F. candida et F. fimetaria, appartient à la famille des Isotomidae :
- classe, Collembola
- ordre, Entomobryomorpha
- super-famille, Isotomoidea
- famille, Isotomidae
- sous-famille, Proisotominae
(Bellinger et coll., 2913). P. minuta est une espèce répandue, de couleur gris-brun. La longueur maximale des adultes est de ~1,1 mm (Hopkin, 2006). Tout comme O. folsomi et F. fimetaria, P. minuta se reproduit par voie sexuée; toutefois, ce sont ses ocelles visibles et sa pigmentation gris-brun qui distinguent cette espèce des autres.
La diagnose de P. minuta comprend les caractéristiques suivantes :
- présence d’ocelles (8 + 8);
- rapport entre la longueur de la soie la plus longue et l’extrémité de l’abdomen/la longueur du mucron se situant entre 3,2 et 4,0;
- mucron comptant 3 dents;
- manubrium doté de 1 + 1 soies ventrales;
- dens portant 6 soies ventrales (antérieures) et côté dorsal crénelé.
On a souvent confondu P. minuta avec P. tenella et P. subminuta, deux espèces semblables. Tout comme P. minuta, P. tenella affiche 8 + 8 ocelles, mais son manubrium porte 3 + 3 soies ventrales et de nombreuses soies sur le côté ventral de la dens, tandis que son mucron est doté de 2 dents. P. subminuta diffère de P. minuta par l’absence de soies ventrales sur le thorax et sur le deuxième segment de l’abdomen (abd2; v. figure 2) (Fjellberg, 2007).
On trouve P. minuta partout dans le monde - on l’a observée dans des sols d’Australie (Park, 2007), d’Asie (Stach, 1964), d’Europe (Dromph, 2003), d’Amérique du Sud (Heckman, 2001) et d’Amérique du Nord (Lartey et coll., 1989). On considère que l’espèce est largement répandue dans les sols canadiens (Dodd et Addison, 2010) : on l’a identifiée en Alberta, au Manitoba, en Ontario et au Nouveau-Brunswick (Skidmore, 1995). On a procédé à des élevages en laboratoire à partir de spécimens prélevés dans des échantillons de sol du centre de la Saskatchewan (EC, 2010).
Sur le terrain, l’espèce est hémi-édaphique, c’est-à-dire qu’elle vit dans la couche de feuilles mortes et les horizons pédologiques superficiels (Bahrndorff et coll., 2009); toutefois, des expériences de laboratoire ont montré qu’elle pouvait survivre et se reproduire dans des horizons pédologiques subsuperficiels et dans des sols présentant une grande diversité de pH et de matières organiques (EC, 2013b). En règle générale, on considère que l’espèce a une répartition cosmopolite - on la trouve tant dans des sols agricoles perturbés (Laterley et coll., 1989) que dans des sols forestiers stratifiés non perturbés (EC, 2010). À l’instar d’autres espèces de collemboles, P. minuta se nourrit d’hyphes fongiques présents dans le sol.
La maturité sexuelle (dans des conditions de laboratoire) est atteinte ~14 jours après l’éclosion. L’oviposition consiste en grappes de 30-50 œufs. Il faut compter ≥6 jours d’incubation avant l’éclosion des œufs (EC, 2013b). Dans les élevages, on peut différencier à l’œil les mâles des femelles d’après leur taille et leur forme relatives. Ainsi, les femelles sont plus grosses et leur abdomen est plus arrondi que chez les mâles, et ces derniers présentent une sensille ventrale fine et dressée sur le deuxième segment antennaire (ant2), de même que 3 sensilles courtes et dressées sur la position ventrale du troisième segment (ant3; v. figure 2). En outre, il n’y a pas de soie modifiée sur le troisième segment du tibiotarse (tib3; v. figure 2) (Fjellburg, 2007). La figure 6 montre le dimorphisme sexuel de P. minuta - ces collemboles sont issus d’un élevage synchrone et sont prêts à être utilisés dans un essai.
Figure 3. F. candida âgé de 10-12 jours, issu d’un élevage synchrone

Spécimens de Folsomia candida de 10 à 12 jours synchronisés en fonction de l’âge
Voici une image photographique prise sous la lentille d’un microscope, d’un spécimen de F. candida âgé de 10 à 12 jours. Le corps mesure environ 600 µm et les antennes y ajoutent ~150 µm de plus.
Figure 4. Dimorphisme sexuel chez des O. folsomi âgés de 28-31 jours, issus d’un élevage synchrone

Dimorphisme sexuel chez des spécimens d’Orthonychiurus folsomi âgés de 28 à 30 jours synchronisés en fonction de l’âge
Voici une image photographique prise sous la lentille d'un microscope, d’un mâle et d’une femelle O. folsomi âgés de 28 à 31 jours. La femelle mesure environ 800 µm et ses antennes y ajoutent ~150 µm de plus. Le mâle photographié est de taille d’environ 15 % inférieure à celle de la femelle.
Figure 5. Dimorphisme sexuel chez des F. fimetaria âgés de 23-26 jours, issus d’un élevage synchrone

Dimorphisme sexuel chez des spécimens de Folsomia fimetaria âgés de 23 à 26 jours synchronisés en fonction de l’âge
Voici une image photographique prise sous la lentille d'un microscope, d’un mâle et d’une femelle F. fimeraria âgés de 23 à 26 jours. La femelle mesure environ 1 mm et ses antennes y ajoutent ~220 µm de plus. Le mâle photographié est de taille d’environ 20 % inférieure à celle de la femelle.
Figure 6. Dimorphisme sexuel chez des P. minuta âgés de 14 jours, issus d’un élevage synchrone

Dimorphisme sexuel chez des spécimens de Proisotoma minuta âgés de 14 jours synchronisés en fonction de l’âge
Voici une image photographique prise sous la lentille d'un microscope, d’un mâle et d’une femelle P. minuta âgés de 14 jours. La femelle mesure environ 750 µm et ses antennes y ajoutent ~160 µm de plus. Le mâle photographié est de taille d’environ 25 % inférieure à celle de la femelle et ses segments abdominaux inférieurs sont légèrement plus étroits.
1.3 Historique de l’utilisation des collemboles dans les essais de toxicité
La mise au point de méthodes d’essai biologique pour mesurer la toxicité des sols accuse un retard par rapport aux essais portant sur d’autres milieux (p. ex., l’eau et les sédiments) (Bonnell Environmental Consulting, 1994). Ce retard est dû en partie au fait que les chercheurs et les organismes de réglementation se sont concentrés sur l’environnement aquatique. Les systèmes édaphiques présentent une plus grande complexité que les systèmes aquatiques et posent de nombreux problèmes en raison de leur manque d’homogénéité. La diversité des voies d’exposition à prendre en considération (p. ex., l’eau de porosité, les vapeurs du sol ou le contact direct avec des particules de sol), conjuguée au coût élevé de la réalisation des essais toxicologiques sur des sols, a souvent conduit les expérimentateurs à extrapoler aux expositions à des sols contaminés les résultats d’essais sur des milieux aquatiques (Bonnell Environmental Consulting, 1994).
Avant les années 1980, l’évaluation de la qualité des sols consistait principalement en des mesures des propriétés physicochimiques du sol, et c’est seulement au cours des années 1980 que les organismes responsables de l’homologation et de l’épandage des pesticides ont commencé à utiliser des méthodes d’essai biologique normalisées pour mesurer la toxicité des sols [p. ex., l’United States Environmental Protection Agency (USEPA) et l’Office of Pesticides Programs (Holst et Ellanger, 1982)]. Les collemboles sont utilisés depuis longtemps dans une large gamme d’évaluations écotoxicologiques. Une des premières études de laboratoire sur des collemboles a été réalisée par Sheals (1956) et portait sur les effets de composés organochlorés sur des microarthropodes. Sheals a notamment examiné les différences de sensibilité au DDT de diverses espèces en utilisant un papier filtre pour l’exposition (Wiles et Krogh, 1998). Dans une étude ultérieure, Scopes et Lichtenstein (1967) ont utilisé F. fimetaria dans un essai de toxicité aiguë en faisant également appel à la méthode d’exposition sur papier filtre. Thompson et Gore (1972) ont été parmi les premiers à promouvoir l’utilisation de F. candida comme espèce expérimentale lorsqu’ils ont évalué 29 insecticides au moyen de tests biologiques. Par la suite, de nombreuses études de laboratoire ont été réalisées entre les années 1970 et la fin des années 1990 avec diverses espèces de collemboles, en particulier F. candida, F. fimetaria, Onychiurus armatus (Protaphorura armata) et Orchesella cincta (Scott-Fordsmand et Krogh, 2005).
La toxicité de sols de site est devenue une « nouvelle » source de préoccupation au milieu des années 1980, et des programmes de réglementation tels que le SUPERFUND aux États-Unis et le Programme national d’assainissement des lieux contaminés (PNALC) au Canada ont été mis en place pour répondre au besoin impérieux de lignes directrices sur l’évaluation et l’assainissement des lieux contaminés hautement prioritaires. Un examen des tests biologiques existants avec des organismes entiers, pour évaluer la toxicité de sols, d’eaux douces et de sédiments d’eau douce (Keddy et coll., 1995), réalisé aux termes du PNALC, a mené à la définition d’une série d’essais utilisables immédiatement pour évaluer des lieux contaminés au Canada (Bonnell Environmental Consulting, 1994). Keddy et coll. (1995) ont conclu que la plupart des méthodes ou modes opératoires existants pour mesurer la toxicité d’échantillons de sol provenant de lieux contaminés ne permettaient pas une évaluation écotoxicologique correcte, et ils ont recommandé que des efforts soient déployés afin de mettre au point une série de méthodes d’essai biologique normalisées qui feraient appel à des espèces expérimentales et à des conditions d’essai applicables aux écosystèmes pédologiques canadiens. Le Conseil canadien des ministres de l’environnement (CCME) a publié en 1994 un cadre de travail pour l’évaluation du risque écologique (ERE) (CCME, 1994), qui a eu par la suite une incidence sur la gestion des lieux contaminés (CCME, 1996, 1997). La démarche adoptée dans l’ERE, qui s’appuyait sur les résultats d’essais toxicologiques monospécifiques, a mis en évidence la nécessité de concevoir des essais toxicologiques fiables, reproductibles et réalistes, avec des espèces terrestres pertinentes d’un point de vue écologique, pour évaluer les sols prélevés dans des lieux contaminés (Bonnell Environmental Consulting, 1994). À la fin des années 1990, les évaluations biologiques sous la forme d’essais toxicologiques sont devenues un complément utile aux analyses chimiques, notamment dans les évaluations du risque particulier à un lieu.
En 1998, Wiles et Krogh ont publié une méthode d’essai faisant appel à trois espèces de collemboles (Isotoma viridis, F. candida et F. fimetaria). La méthode a été rédigée sur le modèle d’une norme ISO, car l’Union européenne avait l’intention de la normaliser selon le système ISO de lignes directrices pour les essais biologiques (Scott-Fordsmand et Krogh, 2005). Le premier essai normalisé de toxicité d’un sol entier avec des collemboles, applicable aux expositions à des pesticides tout autant qu’à des non-pesticides dans un sol artificiel, était une méthode d’essai de reproduction publiée par l’Organisation internationale de normalisation (ISO) en 1999. Cette méthode décrit l’utilisation de F. candida comme espèce expérimentale et porte uniquement sur des sols enrichis avec une substance chimique. En 2005, l’Institut national de recherche sur l’environnement du Danemark a soumis une proposition à l’Organisation de coopération et de développement économiques (OCDE) en vue de la mise au point d’une nouvelle ligne directrice pour des essais servant à évaluer les effets de sols enrichis avec une substance chimique sur la reproduction de deux espèces de collemboles (F. candida et F. fimetaria) (OCDE, 2005), ligne directrice qui a été adoptée en 2009 (OCDE, 2009).
Aujourd’hui, les collemboles sont largement utilisés dans les essais monospécifiques pour mesurer la toxicité de substances chimiques pures, de produits chimiques ou d’échantillons de sol contaminé ou susceptible d’être contaminé par des substances chimiques, que ce soit sur le terrain ou (à des fins expérimentales) en laboratoire. Les collemboles jouent un rôle essentiel dans les fonctions du sol et constituent des indicateurs cruciaux de l’écotoxicologie du sol (Cortet et coll., 1999). Ils sont fréquemment exposés à de nombreuses substances chimiques toxiques présentes dans le sol, tels des engrais, des insecticides, des herbicides et des fongicides à usage agricole et domestique, de même qu’à des métaux lourds, des hydrocarbures pétroliers ou d’autres substances chimiques, comme les produits de préservation du bois (p. ex., le pentachlorophénol) ou des composés nitroaromatiques explosifs présents dans les sols contaminés. Les collemboles possèdent de nombreux attributs qui font d’eux des organismes convenant à l’évaluation de sols potentiellement toxiques. Les caractéristiques de leur cycle biologique, leur répartition et leur fonction écologique leur confèrent une importance sur le plan écologique (Riepert et Kula, 1996). Ils sont répandus dans la nature, présents dans une grande diversité de milieux pédologiques, souvent très abondants et faciles à prélever sur le terrain. En outre, ils peuvent être élevés ou conservés en laboratoire et ils présentent un cycle biologique relativement rapide, avec un taux de reproduction élevé (Scott-Fordsmand et Krogh, 2005). Parallèlement à la méthode d’essai normalisée avec des vers de terre, les collemboles sont de plus en plus utilisés pour évaluer les effets de substances chimiques sur des organismes non ciblés.
Au Canada, l’utilisation d’essais toxicologiques avec des collemboles comme « outils d’évaluation écotoxicologique » d’échantillons de sol de site contaminé ou susceptible d’être contaminé croît également (AquaTerra, 1998; Stephenson et coll., 1999a, 1999b, 2000a; AquaTerra et ESG, 2000; ESG, 2000, 2001, 2002; ESG et AquaTerra, 2002, 2003), et on se sert des résultats de ces essais pour :
- établir des critères nationaux de qualité des sols;
- fixer des objectifs de décontamination fondés sur le risque pour des sites donnés (p. ex., objectifs d’assainissement);
- évaluer l’efficacité des techniques d’assainissement (Stephenson et coll., 2002).
Divers auteurs ont examiné de manière approfondie l’utilisation d’essais toxicologiques avec des collemboles comme « outils d’évaluation écologique » pour estimer la toxicité de sols contaminés ou susceptibles d’être contaminés, dans le cadre d’essais séquentiels (divers niveaux) ou d’évaluations du risque (INRE, 1993; Leon et van Gestel, 1994; Keddy et coll., 1995; Römbke et coll., 1996; van Gestel et coll., 2001; Achazi, 2002; Lanno, 2003; Princz et coll., 2012). Les collemboles ont également été employés dans d’autres évaluations écotoxicologiques telles que la surveillance sur le terrain de l’évolution de populations (p. ex., Neuhauser et coll., 1989), des tests biologiques sur le terrain (p. ex., Wiles et Frampton, 1996), des études en mésocosmes et en microcosmes (p. ex., Addison et Holmes, 1995; Addison, 1996; Cortet et coll., 2003) et une large gamme d’essais en laboratoire (p. ex., Crommentuijn et coll., 1993; Addison et Holmes, 1995; Martikainen et Krogh, 1999; Fountain et Hopkin, 2001).
Diverses méthodes de laboratoire ont été examinées pour mesurer les effets de substances chimiques particulières sur des collemboles. Parmi les paramètres moins « normalisés » qui ont été étudiés, on compte : la croissance (p. ex., Folker-Hansen et coll., 1996), l’accroissement de la population (p. ex., Crommentuijn et coll., 1993), la bioaccumulation par ingestion d’aliments contaminés, la biomobilisation de toxiques et la charge corporelle (p. ex., Janssen et coll., 1991; Pedersen et coll., 2000; Fountain et Hopkin, 2001; Markweise et coll., 2001), les biomarqueurs (Stämpfli et coll., 2002). L’amélioration des méthodes d’essai ainsi que les effets des variations sur les caractéristiques du sol ou les conditions d’essai en laboratoire ont également fait l’objet d’études ou d’examens (Riepert et Kula, 1996; Sandifer et Hopkin, 1996, 1997; Smit et van Gestel, 1996, 1997, 1998; van Gestel et van Diepen, 1997; Crouau et coll., 1999; Martikainen et Krogh, 1999; Martikainen et Rantalainen, 1999; Lock et Janssen, 2001; Crouau et Cazes, 2003).
Les effets toxiques de l’exposition de collemboles à une large gamme de contaminants environnementaux ont été documentés dans des études de laboratoire sur des échantillons de sol enrichis ou contaminés avec :
- des pesticides (Thompson et Gore, 1972; Tomlin, 1975; Mola et coll., 1987; Addison et Holmes, 1995; Addison, 1996; Folker-Hansen et coll., 1996; Petersen et Gjelstrup, 1998; Martikainen et Krogh, 1999; ESG et AquaTerra, 2002; Idinger, 2002; Campiche et coll., 2006);
- des métaux (Crommentuijn et coll., 1993, 1997; Posthuma et van Straalen, 1993; Sandifer et Hopkin, 1996, 1997; Smit et van Gestel, 1996, 1997, 1998; Pedersen et coll., 1997, 1999; van Gestel et van Diepen, 1997; Scott-Fordsmand et coll., 1999; AquaTerra et ESG, 2000; Fountain et Hopkin, 2001; Pedersen et van Gestel 2001);
- des hydrocarbures pétroliers (Neuhauser et coll., 1989; ESG, 2000, 2001; ESG et AquaTerra, 2003; van Gestel et coll., 2001; Jensen et Sverdrup, 2002; Sverdrup et coll., 2002; Princz et coll., 2012);
- d’autres substances chimiques, y compris des toxiques de référence (AquaTerra, 1998; Addison et Bright, 2002; Becker-van Slooten et coll., 2003, 2005; Jensen et coll., 2003; Stämpfli et coll., 2005; EC, 2007a).
En outre, des examens de bases de données ont été résumés dans des rapports consacrés à l’étude des tendances relatives à la toxicité de divers contaminants pour les collemboles (Leon et van Gestel, 1994).
F. candida constitue depuis longtemps l’espèce de choix pour l’étude des effets d’une exposition prolongée à des contaminants sur la survie et la reproduction de collemboles, et ce, pour plusieurs raisons : les expérimentateurs connaissent bien cette espèce et ont de l’expérience dans son élevage, l’espèce a un cycle biologique rapide, est présente partout dans le monde et est souvent utilisée dans les essais toxicologiques. Le développement, la croissance et la biologie de la reproduction de F. candida dans des conditions de laboratoire ont fait l’objet de nombreuses études et sont bien documentés (Hopkin, 1997; Fountain et Hopkin, 2005). À l’issu d’un examen de l’utilisation de cette espèce comme organisme expérimental « standard », Fountain et Hopkin (2005) ont conclu que, malgré certaines critiques au sujet de la pertinence sur le terrain de l’essai de toxicité ISO avec F. candida, cette espèce joue un rôle important dans l’évaluation du risque et, partant, on continuera de l’employer dans l’établissement de nouvelles normes environnementales.
En règle générale, la plupart des résultats des expériences avec F. candida ne peuvent pas être extrapolés à d’autres espèces de collemboles en raison des différences de sensibilité parmi les espèces (Krogh, 1995; Hopkin 1997). Par exemple, dans le cas de l’atrazine, la concentration sans effet observé (CSEO) est de 600 μg/g pour F. candida, mais de seulement 40 μg/g pour O. cincta (Badejo et van Straalen, 1992). En revanche, pour le diméthoate et le cuivre, aucune différence de sensibilité n’a été observée entre F. candida et F. fimetaria (Scott- Fordsmand et Krogh, 2005); pour l’acide borique, la différence de sensibilité entre ces deux espèces est faible (Becker-van Slooten, comm. pers., 2006).
F. fimetaria est une espèce expérimentale relativement nouvelle pour les essais d’écotoxicité sublétale des sols. C’est en 1990, au Danemark, qu’un premier essai avec F. fimetaria a été mis au point dans le cadre d’une étude des effets de pesticides (Wiles et Krogh, 1998). Depuis, on s’est servi de cette espèce pour évaluer les effets toxiques de nombreux composés différents tels que le cuivre, le nickel, les phtalates, les sulfonates d’alkylbenzène linéaires, le pyrène, le diméthoate, les hydrocarbures aromatiques polycycliques, les composés aromatiques polycycliques, les produits pharmaceutiques vétérinaires et les boues d’épuration (Fabian et Petersen, 1994; Folker-Hansen et coll., 1996; Scott-Fordsmand et coll., 1997, 1999, 2000; Holmstrup et Krogh, 2001; Jensen et coll., 2001; Jensen et Sverdrup, 2002; Scott-Fordsmand et Krogh, 2004; Becker-van Slooten et coll., 2005; EC, 2007a).
Bien que la biologie et la pertinence écologique d’O. folsomi soient bien connues (Snider, 1983; v. aussi 1.2.2), l’utilisation de cette espèce dans les essais toxicologiques est relativement peu documentée et se limite à un certain nombre d’études canadiennes (AquaTerra, 1998; Stephenson et coll., 1999a, 1999b, 2000a; AquaTerra et ESG, 2000; ESG, 2000, 2001, 2002; Addison et Bright, 2002; ESG et AquaTerra, 2002, 2003; EC, 2007a).
Pour leur part, des chercheurs australiens (Greenslade et Vaughan, 2003) et canadiens (Dodd et Addison, 2010) ont recommandé d’utiliser P. minuta comme espèce expérimentale. Celle-ci est prisée en raison de son potentiel de reproduction rapide dans des conditions de laboratoire. Par contre, elle s’est avérée difficile à manipuler à cause de sa petite taille et de sa pigmentation (Greenslade et Vaughan, 2003), sans compter qu’il est difficile de distinguer les adultes des juvéniles (Dodd et Addison, 2010).
Sur le plan de la survie et de la reproduction, P. minuta et F. candida réagissent de la même façon à des toxiques inorganiques comme le zinc, l’arsenic et le cadmium, mais P. minuta est relativement plus sensible au cuivre (Greenslade et Vaughan, 2003; Nursita et coll., 2005). Comme il est indiqué dans l’étude de Sandifer et Hopkin (1996) au sujet de F. candida, P. minuta peut tolérer des concentrations élevées de plomb dans le sol (>3000 mg/kg) sans présenter de réaction toxique (Nursita et coll., 2005).
Comparativement à F. candida, P. minuta a présenté une réaction toxique moindre à des composés organiques comme le phénol et l’oxyde de tert-butyle et de méthyle (Greenslade et Vaughan, 2003; Dodd et Addison, 2010). L’exposition en laboratoire à des concentrations de α-endosulfan et de β-endosulfan provoquant une toxicité aiguë a montré que le premier de ces deux pesticides était beaucoup plus toxique que le deuxième. À des concentrations sublétales, on a observé une inhibition de la reproduction chez P. minuta, mais les organismes exposés ont pu métaboliser les deux pesticides en sulfate d’endosulfan et la production d’œufs a fini par reprendre (Park et Lees, 2004). P. minuta était également plus sensible que F. candida à des mélanges de contaminants (saumure et hydrocarbures pétroliers) présents dans des échantillons de sol de la forêt boréale (Princz et coll., 2012).
Les documents méthodologiques résumés aux annexes E et F ont orienté l’établissement de la première édition de la méthode d’essai biologique normalisée que recommande Environnement Canada pour mesurer les effets toxiques d’une exposition prolongée à un sol de site ou à sol enrichi avec une substance chimique sur la survie et la reproduction de collemboles. Cette méthode a été mise à jour et est décrite dans le présent document.