Déclaration sur la vaccination contre la rage en préexposition et la prévention des morsures d’animaux chez les voyageurs
Publication : 10 février 2026
Sur cette page
- Préambule
- Points clés pour les professionnels de la santé
- Contexte
- Méthodes utilisées pour l'élaboration des lignes directrices
- Recommandation et évaluation des données probantes sur l'utilisation de la prophylaxie par le vaccin contre la rage en préexposition chez les voyageurs canadiens
- Recommandations pour la prévention et le traitement des blessures associées aux animaux
- Autres aspects à considérer relativement au soin des plaies en cas d'exposition
- Conclusion et besoins en matière de recherche
- Abréviations
- Remerciements
- Conflits d'intérêts
- Annexe 1 : Pays où le variant canin du virus est présent et où les RIg ne sont pas facilement accessibles
- Annexe 2 : Lignes directrices sur la prévention de l'exposition aux animaux à l'intention des voyageurs
- Annexe 3 : Exemple de stratégie de recherche documentaire
- Annexe 4 : Données d'entrée du modèle pour l'estimation de la réduction des perturbations de voyage
- Annexe 5 : Données d'entrée du modèle pour l'estimation du risque de rage clinique chez les voyageurs
- Annexe 6 : Données probantes à l'appui de l'estimation du risque d'ÉIG
- Annexe 7 : Cadre de données probantes appuyant la prise de décisions
- Annexe 8 : Tableaux d'évaluation de l'applicabilité des énoncés sur les bonnes pratiques
- Notes de bas de page
- Références
Préambule
Le Comité consultatif de la médecine tropicale et de la médecine des voyages (CCMTMV) donne à l'Agence de la santé publique du Canada (ASPC) des conseils courants et à jour de nature médicale, scientifique et de santé publique concernant les maladies tropicales infectieuses et les risques pour la santé associés aux voyages internationaux. L'Agence reconnaît que les conseils et les recommandations figurant dans cette déclaration reposent sur la pratique médicale et les connaissances scientifiques les plus récentes et les diffuse dans le but d'informer les professionnels de la santé qui sont appelés à prodiguer des soins aux voyageurs.
Les personnes qui administrent ou utilisent des médicaments, des vaccins ou d'autres produits devraient bien connaître la monographie des produits ainsi que toute autre norme ou instruction approuvée concernant leur usage. Les recommandations relatives à l'usage des produits et les autres renseignements présentés ici peuvent différer de ceux figurant dans les monographies ou dans toute autre norme ou instruction approuvée pertinente qui a été établie par les fabricants autorisés. Rappelons que l'approbation demandée par les fabricants pour leurs produits, avec démonstration de leur innocuité et de leur efficacité à l'appui, ne s'applique qu'aux utilisations conformes à la monographie ou à toute autre norme ou instruction approuvée concernant leur usage.
Points clés pour les professionnels de la santé
- La rage est une zoonose virale mortelle qui se transmet principalement par des morsures de mammifères.
- Le fardeau de la rage est plus élevé dans certaines destinations de voyage, souvent parce que le virus circule chez les chiens non vaccinés.
- Il est possible d'éviter la maladie après une exposition en ayant recours à une prophylaxie post-exposition (PPE) appropriée, qui comprend généralement un vaccin contre la rage et des immunoglobulines antirabiques (RIg).
- La prophylaxie préexposition (PPrE) simplifie la prophylaxie post-exposition (PPE) en cas d'exposition à la rage, car elle permet de réduire le nombre de doses de vaccin contre la rage nécessaires et d'éliminer la nécessité d'administrer des RIg.
- Dans certaines situations, en particulier si l'accès à la PPE est incertain, le recours à la PPrE par le vaccin contre la rage avant le voyage pourrait réduire le fardeau imposé par les interactions et les interventions de soins de santé liées à la PPE contre la rage pour le patient exposé.
- L'annexe 1 contient la liste des pays pour lesquels le CCMTMV suggère d'offrir la PPrE par le vaccin contre la rage aux voyageurs. Par ailleurs, les renseignements sur le risque de contracter la rage sont accessibles sur le site voyage.gc.ca par l'entremise de conseils de santé aux voyageurs formulés par l'Agence de la santé publique du Canada. La section « Santé » de chaque page de destination fournit des détails sur l'endémicité de la rage et l'accès à la PPE.
- Outre la prophylaxie contre la rage, la prise en charge complète en cas d'exposition devrait inclure des soins minutieux des plaies et, lorsque l'exposition concerne des primates non humains, la prise en compte du virus de l'herpès simien (virus de l'herpès B).
Résumé des recommandations
1. Le CCMTMV suggère d'offrir la PPrE par le vaccin contre la rage aux voyageurs qui se rendent dans des régions où le risque de rage est relativement élevémise en garde a et où les RIg peuvent ne pas être facilement accessiblesmise en garde b
(Recommandation discrétionnaire, fondée sur des données de très faible certitude)
Remarques :
- Il s'agit d'une recommandation discrétionnaire. Le professionnel de la santé devrait examiner avec le patient les avantages et les préjudices potentiels associés à la PPrE par le vaccin contre la rage afin de l'aider à prendre une décision qui correspond à ses valeurs et à ses préférences. La discussion devrait porter sur d'éventuelles solutions de rechange et/ou complémentaires à la vaccination.
- Lorsque le variant canin du virus est présent, mais que le risque d'exposition est faible (notamment lors d'un voyage dans un centre de villégiature) ou que la durée du voyage est courte (une semaine ou moins), les avantages de la PPrE par le vaccin contre la rage peuvent être moindres et les patients peuvent choisir de ne pas la recevoir (voir l'annexe 2 pour obtenir des renseignements sur les comportements et les activités présentant un risque accru de contact avec des animaux).
- L'administration des vaccins contre la rage dans le cadre de la PPrE devrait se faire conformément au Chapitre des vaccins contre la rage du Guide canadien d'immunisation (GCI), qui fournit également des recommandations pour des groupes particuliers, comme le personnel de laboratoire, les vétérinaires, le personnel vétérinaire et les agents de protection de la faune.
- Les seuils décrivant l'ampleur des effets (c'est-à-dire les préjudices ou les avantages absolus estimés qui sont jugés importants pour la prise de décision) sont résumés au tableau 1.
Justification :
- L'avantage absolu de la PPrE pour la prévention de la rage chez les voyageurs est insignifiant.
- La PPrE par le vaccin contre la rage peut réduire d'environ 1 % la probabilité d'une perturbation de voyage liée au traitement PPE (avantage modéré; très faible certitude des données), mais peut augmenter le risque d'évènements indésirables graves associés à la vaccination de 0,08 % (préjudice modéré; très faible certitude des données). Compte tenu de ces estimations, le CCMTMV estime que de nombreux patients choisiraient de recevoir une PPrE par le vaccin contre la rage pour éviter le risque que leur voyage soit perturbé.
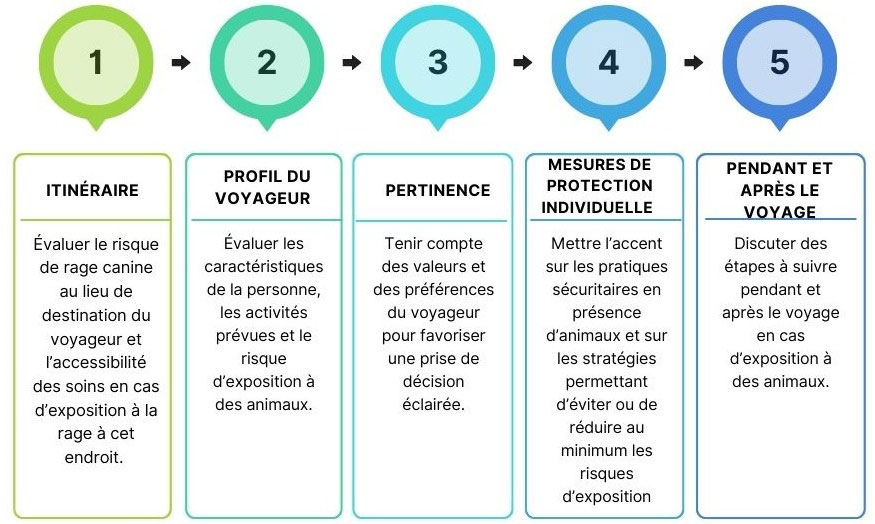
Figure 1: Texte descriptif
Itinéraire : Évaluer le risque de rage canine au lieu de destination du voyageur et l'accessibilité des soins en cas d'exposition à la rage à cet endroit.
Profil du voyageur : Évaluer les caractéristiques de la personne, les activités prévues et le risque d'exposition à des animaux.
Pertinence : Tenir compte des valeurs et des préférences du voyageur pour favoriser une prise de décision éclairée.
Mesures de protection individuelle : Mettre l'accent sur les pratiques sécuritaires en présence d'animaux et sur les stratégies permettant d'éviter ou de réduire au minimum les risques d'exposition.
Pendant et après le voyage : Discuter des étapes à suivre pendant et après le voyage en cas d'exposition à des animaux.
2. Les voyageurs devraient éviter d'être en contact avec des animaux pendant leur voyage (énoncé sur les bonnes pratiques).
Remarque :
- Voir l'annexe 2 pour obtenir des renseignements sur les lignes directrices sur la prévention de l'exposition aux animaux à l'intention des voyageurs.
3. Les voyageurs qui souffrent d'une blessure causée par un animal (par exemple, une morsure ou une griffure causée par un mammifère comme un chien, un chat, un singe ou une chauve-souris) devraient chercher à obtenir des soins dès que possible (énoncé sur les bonnes pratiques).
Remarques :
- Le lavage immédiat de la plaie avec de l'eau et du savon pendant au moins 15 minutes constitue une mesure importante pour réduire le risque d'infection après une exposition à un animal.
- L'évaluation médicale et la PPE (si elle est recommandée) ne devraient pas être retardées jusqu'au retour au Canada.
- Demander et conserver les dossiers de PPE contre la rage reçue pendant les voyages, y compris le nom des produits (RIg et/ou vaccins) et la date à laquelle ils ont été administrés. Consulter l'information clé sur l'immunisation pour connaître la liste complète des détails importants sur la vaccination.
- Chercher à obtenir des soins de santé dès que possible après le retour au Canada. Lors de la consultation, apporter les documents relatifs aux traitements reçus à l'étranger.
- Même les morsures d'animaux d'apparence mineure peuvent pénétrer les gaines tendineuses, les capsules articulaires, les os ou les nerfs, et présenter un risque de complications graves.
Contexte
La rage est une maladie virale mortelle qui est causée par des virus du genre Lyssavirus et qui peut toucher tous les mammifèresNote de bas de page 1. Environ 99 % des cas de rage humaine sont associés à des morsures de chien et au variant canin du virus dans les pays à revenu faible ou intermédiaire où la rage est endémiqueNote de bas de page 2 et où l'on estime que 50 000 à 100 000 cas surviennent chaque annéeNote de bas de page 3 Note de bas de page 4. À l'opposé, le Canada et pratiquement tous les autres pays à revenu élevé ont éliminé le cycle endémique du variant canin du virus, ce qui fait que la rage humaine y est très rareNote de bas de page 5.
Le fait de vacciner une personne après son exposition (PPE) à un animal potentiellement enragé est très efficace pour prévenir la rage. La PPrE contre la rage représente également une intervention importante pour les personnes qui présentent un risque accru d'exposition au virus de la rageNote de bas de page 6. Bien qu'elle n'élimine pas la nécessité d'une PPE contre la rage, la PPrE contre la rage permet d'avoir recours à une PPE accélérée en réduisant le nombre de doses de vaccin à administrer et en éliminant la nécessité des RIgNote de bas de page 6 :
Conformément au chapitre Vaccins contre la rage : Guide canadien d'immunisation, les recommandations actuelles en matière de PPE, sont les suivantes :
- Personnes qui n'ont pas été préalablement immunisées contre la rage
- Traitement local de la plaie
- Prophylaxie post-exposition à l'aide de RIg et administration de quatre ou cinq doses de vaccin contre la rage dès que possible.
- Personnes qui ont déjà été adéquatement immunisées contre la rage
- Traitement local de la plaie
- Prophylaxie post-exposition à l'aide de deux doses de vaccin contre la rage dès que possible.
Ces directives sont axées sur la prévention de la rage lors des voyages. L'analyse porte plus particulièrement sur l'utilisation de la PPrE chez les voyageurs qui se rendent dans des régions d'endémicité relativement forte, généralement en raison de la présence du variant canin du virus.
Caractéristiques cliniques
Le virus de la rage se transmet habituellement par la salive d'un mammifère infecté, le plus souvent par morsure, mais il peut également se propager par griffure, léchage ou contact avec de la peau ou des muqueuses lésées ou contaminées par la salive ou les tissus nerveux/le liquide céphalorachidien d'un mammifère infecté. Après l'infection, le virus se réplique dans les tissus musculaires avant de migrer vers le cerveau en passant par les nerfs périphériques.
La période d'incubation varie de moins d'une semaine à plus d'un an, mais elle se situe le plus souvent entre un et trois moisNote de bas de page 1. Les facteurs considérés comme influençant la période d'incubation sont la quantité de matériel infectieux (par exemple, la salive) introduite, le degré d'innervation de la région exposée et la proximité de la région exposée par rapport au cerveau.
Les premiers symptômes cliniques peuvent comprendre une douleur neuropathique dans la région de la plaie et de la fièvre, suivies d'une encéphalomyélite progressive. La mort survient habituellement dans les 14 jours suivant l'apparition des symptômes. Pour une description des manifestations cliniques de la rage, consulter la page Rage : Pour les professionnels de la santé.
Risque de rage et de morsures d'animaux chez les voyageurs
Sur le plan individuel, la rage reste extrêmement rare chez les voyageurs des pays occidentaux à revenu élevé qui se rendent dans des endroits où le fardeau de la maladie est plus élevé. Parmi les 23 cas signalés dans cette population entre 2013 et 2019, on n'a dégagé aucune tendance cohérente qui permettrait de définir un voyageur « habituel »Note de bas de page 7; les cas couvraient divers profils de voyage. Dans la plupart des cas, la maladie a été contractée en Asie (13/23, 57 %) ou en Afrique (7/23, 30 %). L'âge moyen était de 36 ans (de 4 à 65 ans), et les enfants de moins de 16 ans représentaient 13 % des cas. Le ratio hommes/femmes était de 2,8:1. Les migrants ayant subi une exposition dans leur pays d'origine avant leur arrivée dans leur pays d'accueil représentaient 35 % des cas, tandis que les touristes et les voyageurs rendant visite à des amis ou à des parents représentaient chacun 26 % des cas. Les autres cas ont été signalés chez les voyageurs d'affaires (9 %) et les expatriés (4 %). Les chiens constituaient la principale source d'infection (74 %), suivis des chats (9 %).
Des données recueillies à Paris, en France, entre août et septembre 2025 mettent en évidence des comportements particuliers des voyageurs qui sont liés de manière disproportionnée à l'exposition aux animauxNote de bas de page 8. Sur les 724 personnes ayant demandé des soins après une exposition, seulement 69 (9,5 %) avaient consulté un professionnel de la santé avant leur voyage. Une majorité (689/724, 95,2 %) a décrit son exposition comme étant provoquée, ce qui souligne l'importance des facteurs de risque comportementaux dans l'exposition des voyageurs aux animaux. Parmi les 339 voyageurs qui avaient signalé des incidents provoqués, 45,7 % avaient caressé des animaux ou joué avec eux, 20,6 % avaient nourri des animaux ou avaient tenté d'aider un animal malade, et 8,6 % avaient été en contact avec des animaux lors d'un repas au restaurant. Par ailleurs, 18,9 % des personnes interrogées ont déclaré avoir eu un contact accidentel avec des animaux (c'est-à-dire s'être trouvé à proximité d'animaux, avoir marché sur un animal ou avoir croisé des animaux lors d'une randonnée, d'une promenade à vélo ou à moto). En outre, 11,8 % des personnes ont subi une exposition lors d'interactions avec des singes, c'est-à-dire en les nourrissant, en les caressant ou en les photographiant.
Bien que la rage soit une maladie rare, le risque d'exposition à des animaux, notamment en cas de morsure de chien, est appréciable dans les pays où le fardeau de la maladie est élevé. Les estimations de l'incidence des morsures au cours des voyages varient, les taux déclarés allant de 0,1 à 23 pour 1 000 voyages-personnesNote de bas de page 9. Dans les destinations où le risque est élevé, les voyageurs ont au moins 1 % de probabilité d'être exposés à des animaux, ce qui équivaut à 10 morsures pour 1 000 voyages-personnes. Il s'agit d'un risque important dans le contexte de la prévention de la rage et de la prise de décision concernant la PPrE contre la rage. Plus précisément, comme les expositions à des animaux susceptibles d'être associées à la transmission de la rage sont relativement courantes, on devrait supposer que le recours à des soins de santé pour évaluer la nécessité d'une PPE contre la rage est relativement courant. Puisque l'approche à l'égard de la PPE n'est pas la même lorsqu'une personne a reçu la PPrE (pas de RIg et moins de doses de vaccin à administrer chez les personnes ayant reçu la PPrE), le fait pour une personne d'avoir reçu la PPrE peut permettre de réduire les interruptions de voyage associées à un traitement PPE contre la rage.
Méthodes utilisées pour l'élaboration des lignes directrices
Processus d'élaboration de la déclaration
La présente déclaration a été élaborée par un groupe de travail (GT) sous la direction du CCMTMV. Avec le soutien du secrétariat du CCMTMV, le groupe de travail a procédé à une analyse systématique de la littérature, fait la synthèse des données probantes, formulé des questions clés, rédigé des recommandations et élaboré la présente déclaration.
Les décisions clés à l'appui du processus d'élaboration des recommandations ont fait l'objet de discussions et ont été approuvées par l'ensemble des membres du comité. La version définitive de la déclaration et des recommandations a été approuvée par le CCMTMV.
La méthodologie GRADE (Grading of Recommendations, Assessment, Development and Evaluation) a été utilisée pour élaborer les recommandations. Les questions concernaient uniquement les Canadiens voyageant à l'étranger et ne portaient pas sur des sujets déjà abordés dans le chapitre sur les vaccins contre la rage du GCI (par exemple, les calendriers et voies d'administration de la PPrE, l'efficacité potentielle/l'efficacité réelle/l'immunogénicité des vaccins).
Question stratégique et question selon l'approche PICO
Question stratégique
Faudrait-il recommander l'administration d'une PPrE par le vaccin contre la rage aux voyageurs canadiens qui se rendent dans des destinations où le fardeau de la rage est élevé et où les RIg ne sont peut-être pas accessibles?
Question selon l'approche PICO
Population : Voyageurs canadiens qui se rendent dans une destination où le risque de rage est relativement élevé (c'est-à-dire où le variant canin du virus de la rage circule) et où les RIg peuvent ne pas être accessibles.
Intervention : PPrE contre la rage en utilisant soit le vaccin préparé sur cellules diploïdes humaines (VCDH), soit le vaccin préparé sur cellules d'embryons de poulet purifiées (VCEPP).
Comparaison : Pas de PPrE par le vaccin contre la rage
Résultats :
- prévention des cas cliniques de rage
- évitement de la maladie sérique attribuable aux RIg
- évitement des perturbations majeures des voyages
- évènements indésirables graves (ÉIG) associés à la vaccination contre la rage
Recherche documentaire
Outre la principale question stratégique énoncée ci-dessus, nous avons également examiné les questions contextuelles suivantes :
- Quels sont les principaux facteurs de risque d'exposition à la rage et de morsures d'animaux chez les voyageurs canadiens (par exemple, destination, durée du voyage)?
- Quelles sont les valeurs et les préférences des voyageurs en matière de réduction des risques qui justifieraient de recourir à une PPrE contre la rage, compte tenu des coûts et des inconvénients qui s'y rapportent?
Avec l'aide d'une bibliothécaire de référence, une stratégie de recherche a été élaborée en fonction des questions ci-dessus.
Nous avons recherché la littérature pertinente (en anglais et en français) dans Embase, MEDLINE, Global Health, CAB Abstracts et Scopus (annexe 3). Nous avons également examiné les données sur l'innocuité des vaccins de l'Advisory Committee on Immunization Practices des États-Unis (ACIP) et du Groupe consultatif stratégique d'experts sur la vaccination (SAGE). Enfin, des données non publiées et d'autres données probantes pertinentes ont été obtenues en effectuant une recherche manuelle dans des listes de références et en consultant des monographies de produits, des bases de données d'organismes gouvernementaux et des experts en la matière.
En ce qui concerne les résultats, la maladie sérique associée aux RIg a été définie comme importante au cours du processus d'élaboration des lignes directrices, étant donné les différences potentielles observées sur le plan des ÉIG entre, d'une part, le vaccin contre la rage employé seul et, d'autre part, la combinaison du vaccin contre la rage et des RIg. Les données probantes relatives à ce résultat ont été obtenues à l'aide d'une revue exploratoire.
Résultats
Dans le cadre de notre évaluation, les membres du GT ont d'abord évalué l'importance de chaque résultat, c'est-à-dire « important » ou « critique ». Ces évaluations ont ensuite été revues par le CCMTMV, l'évaluation finale de chaque résultat reflétant un consensus parmi les membres du comité.
Avantages de la PPrE par le vaccin contre la rage pour la prévention des éléments suivants :
- Cas cliniques de rage (critique) : Diagnostic de rage humaine chez les Canadiens qui ont franchi une frontière internationale entre le moment de l'infection et le diagnostic.
- Perturbations majeures des itinéraires de voyage (critique) : Quitter le lieu de destination (en raison de la non-disponibilité de la PPE recommandée) pour obtenir des soins médicaux dans le pays d'exposition dans les 48 heures suivant l'exposition à l'animal.
- Maladie sérique (important) : Réaction d'hypersensibilité médiée par des complexes immuns après l'administration de RIg.
Préjudices liés à la PPrE par le vaccin contre la rage :
- ÉIG après la vaccination (critique) : Évènements indésirables nécessitant une intervention médicale importante ou une hospitalisation, ou entraînant une invalidité permanente, ce qui correspond à des évènements indésirables de grades 3 à 5 selon les critères relatifs à la vaccination utilisés par la Food and Drug Administration (FDA) des États-UnisNote de bas de page 10.
Nous avons estimé que l'anxiété et la peur de contracter la rage à la suite d'une exposition à un animal étaient importantes, mais pas critiques pour la prise de décision. Les évènements indésirables non graves ont été considérés comme peu importants pour les décisions cliniques.
Seuils d'effets
La définition d'une gamme d'effets absolus qui représentent des préjudices ou des avantages significatifs est une composante essentielle de l'évaluation de la certitude des données probantes. En général, on considère que des effets absolus insignifiants n'influencent pas la prise de décision. En revanche, des effets absolus dont l'ampleur varie de petite à grande peuvent être jugés significatifs et influencer la prise de décision. Ce cadre permet de comparer les résultats en distinguant l'ampleur des effets importants. Par exemple, on considère généralement qu'un préjudice critique important l'emporte sur un avantage modéré.
En ce qui concerne les résultats critiques décrits dans la section Résultats, le comité a établi des seuils pour les avantages ou les préjudices en fonction de ce qui serait jugé significatif par les voyageurs. En l'absence d'études sur les valeurs et les préférences des voyageurs, l'expérience professionnelle des membres du GT, qui appuient régulièrement les voyageurs dans la prise de décisions conjointes, a été mise à contribution.
| Type d'effet | Résultat | Seuils relatifs à l'ampleur de l'effet absolu (avantages et préjudices) Nombre d'évènements/100 000 voyages-personnes |
|||
|---|---|---|---|---|---|
| Insignifiante | Petite | Modérée | Grande | ||
| Avantages (réduction du nombre d'évènements attendus) | Prévention de la rage | < 0,05 | 0,05 | 0,1 | > 0,5 |
| Perturbations majeures des voyages | < 25 | 25 | 100 à 1 000 | > 1 000 | |
| Maladie sérique attribuable aux RIg | < 50 | 50 | 100 | > 1 000 | |
| Préjudices (augmentation du nombre d'évènements attendus) | ÉIGNote de tableau a | < 5 | 5 | 10 à 100 | > 100 |
Modèle et principales hypothèses
Lors de l'évaluation des avantages et des préjudices potentiels de la PPrE contre la rage, nous avons utilisé la modélisation pour estimer la probabilité d'exposition dans les milieux à risque élevé et pour comparer les résultats en fonction du statut vaccinal des voyageurs (c'est-à-dire le fait d'avoir reçu ou non une PPrE contre la rage avant le voyage).
En raison des renseignements limités disponibles sur les répercussions de la PPrE contre la rage au sein d'une population de voyageurs pour ce qui est des résultats prédéterminés par le GT, nous avons formulé des hypothèses fondées sur les meilleures données probantes accessibles. Par exemple, dans les régions où le variant canin du virus est présent, le risque d'exposition pour les voyageurs canadiens a été estimé à 1 % par mois de voyage. Comme il y a peu de données sur les perturbations de voyage liées aux comportements de recherche d'un traitement contre la rage, nous avons modélisé l'influence potentielle de la PPrE par le vaccin contre la rage sur la continuité des activités de voyage. Cette analyse part du principe que tous les voyageurs exposés consulteront un médecin. Les perturbations majeures ont été définies comme l'impossibilité d'accéder à la PPE recommandée (c'est-à-dire le vaccin contre la rage employé seul, ou le vaccin contre la rage et les RIg) dans les 48 heures dans le pays d'exposition, obligeant le voyageur concerné à interrompre son voyage pour aller se faire soigner ailleurs.
Pour obtenir un aperçu complet des estimations et des principales hypothèses de notre modèle, consulter l'annexe 4.
Recommandation et évaluation des données probantes sur l'utilisation de la prophylaxie par le vaccin contre la rage en préexposition chez les voyageurs canadiens
1. Le CCMTMV suggère d'offrir la PPrE par le vaccin contre la rage aux voyageurs qui se rendent dans des régions où le risque de rage est relativement élevémise en garde a et où les RIg peuvent ne pas être facilement accessiblesmise en garde b
(Recommandation discrétionnaire, fondée sur des données de très faible certitude)
Remarques :
- Il s'agit d'une recommandation discrétionnaire. Le professionnel de la santé devrait examiner avec le patient les avantages et les préjudices potentiels associés à la PPrE contre la rage afin de l'aider à prendre une décision qui correspond à ses valeurs et à ses préférences. La discussion devrait porter sur d'éventuelles solutions de rechange et/ou complémentaires à la vaccination.
- Lorsque le variant canin du virus est présent, mais que le risque d'exposition est faible (notamment lors d'un voyage dans un centre de villégiature) ou que la durée du voyage est courte (une semaine ou moins), les avantages de la PPrE contre la rage peuvent être moindres et les patients peuvent choisir de ne pas la recevoir (voir l'annexe 2 pour obtenir des renseignements sur les comportements et les activités présentant un risque accru de contact avec des animaux).
- L'administration des vaccins contre la rage dans le cadre de la PPrE devrait se faire conformément dans le chapitre sur les vaccins contre la rage du GCI, qui fournit également des recommandations pour des groupes particuliers, comme le personnel de laboratoire, les vétérinaires, le personnel vétérinaire et les agents de protection de la faune.
- Les seuils décrivant l'ampleur des effets (c'est-à-dire les préjudices ou les avantages absolus estimés qui sont jugés importants pour la prise de décision) sont résumés au tableau 1.
Résumé des données probantes
Cas clinique de rage
Conformément au résumé ci-dessus et à la description de l'annexe 5, on estime que le risque de rage est extrêmement faible chez les voyageurs canadiens qui se rendent dans des pays où le fardeau de la rage est plus élevé, c'est-à-dire < 1 cas déclaré/100 millions de voyages. La figure 2 (annexe 5) présente la modélisation par le GT du risque estimé de rage clinique chez les voyageurs en provenance de pays à revenu élevé. Elle montre que le risque de rage demeure exceptionnellement rare, même si les cas cliniques représentent un résultat critique. Puisque l'avantage absolu de la PPrE pour la prévention de la rage ne peut pas dépasser le risque absolu global de maladie, nous avons jugé que cet avantage n'était pas pertinent pour la prise de décision, car il est inférieur au seuil correspondant à un effet insignifiant de < 1 cas déclaré pour 2 millions.
Interruption de voyage
Bien que les taux d'exposition des voyageurs aux animaux soient bien documentés, les données quantitatives sur le temps et les coûts financiers qui en résultent demeurent limités. Les questions clés sont les suivantes : déterminer si les voyages sont considérablement perturbés par les démarches visant à obtenir la PPE contre la rage et déterminer si la PPrE contre la rage permet d'atténuer ces perturbations. En l'absence de telles données probantes, nous avons élaboré un modèle estimant la probabilité d'une interruption de voyage à la suite d'une exposition et les avantages potentiels de la PPrE contre la rage. Dans notre cadre, l'avantage découle du fait qu'un voyageur immunisé a accès au vaccin contre la rage, et non pas aux RIg, car les RIg ne sont pas nécessaires pour les personnes qui ont reçu la PPrE. Par conséquent, le voyageur concerné évite d'avoir à se rendre dans un lieu où les RIg sont offerts. De plus amples renseignements sont fournis à l'annexe 4.
À l'aide de ce modèle, nous avons estimé que l'administration de la PPrE contre la rage permettrait d'éviter 870 perturbations majeures de voyage pour 100 000 voyages-personnes (IC à 95 % : 937 de moins à 805 de moins pour 100 000 voyages-personnes) dans les régions où le variant canin du virus est endémique et où le vaccin contre la rage serait accessible, mais pas les RIg (tableau 2). Sur le plan individuel, cela équivaut à une réduction absolue du risque de 0,87 % (soit environ 1 perturbation évitée pour 115 voyages). Nous avons jugé qu'il s'agissait d'un avantage modérément important (tableau 4)
| Mesure du risque | Sans PPrE (pour 100 000 voyages-personnes) | Avec PPrE (pour 100 000 voyages-personnes) |
|---|---|---|
| Taux de blessures causées par des animaux | 1 000 | 1 000 |
| Probabilité que les RIg ne soient pas facilement accessibles au lieu de destination | 100 % Note de tableau a | Sans objet Note de tableau b |
| Taux de voyageurs qui n'ont pas accès aux RIg lorsqu'ils en ont besoin | 1 000 Note de tableau a | Sans objet Note de tableau b |
| Probabilité que le vaccin contre la rage ne soit pas facilement accessible au lieu de destination | Sans objet Note de tableau c | 13 % |
| Taux de voyageurs qui n'ont pas accès au vaccin contre la rage lorsqu'ils en ont besoin | Sans objet Note de tableau c | 130 |
| Estimation de la réduction des perturbations majeures de voyage grâce à la PPrE | Sans objet Note de tableau d | 870 de moins |
Maladie sérique attribuable aux RIg
Dans une étude observationnelle rétrospective menée à Bangkok, en Thaïlande (1987 à 2005), des RIg équines purifiées ont été administrées à 42 965 (59,56 %) patients et des RIg humaines à 29 167 (40,44 %) patients. La maladie sérique a été signalée chez 314 des 72 132 personnes (0,44 %) ayant reçu soit des RIg équines (n = 312), soit des RIg humaines (n = 2)Note de bas de page 11. En fonction de cette probabilité de base de maladie sérique associée aux RIg, et en supposant que 1 % des voyageurs sont exposés à des animaux et reçoivent une PPE contre la rage appropriée (laquelle ne comprendrait pas de RIg si les voyageurs ont reçu une PPrE contre la rage), nous avons estimé que la PPrE permettrait d'éviter 4 cas de maladie sérique pour 100 000 voyages-personnes (IC à 95 % : 11 de moins à 0,3 de plus pour 100 000 voyages-personnes). Cet effet a été jugé insignifiant (tableau 4).
Évènements indésirables graves
Nous avons inclus treize études (annexe 6) qui contenaient des données sur l'innocuité des vaccins contre la rage, notamment la survenue d'ÉIGNote de bas de page 12 Note de bas de page 13 Note de bas de page 14 Note de bas de page 15 Note de bas de page 16 Note de bas de page 17 Note de bas de page 18 Note de bas de page 19 Note de bas de page 20 Note de bas de page 21 Note de bas de page 22 Note de bas de page 23 Note de bas de page 24. Nous avons jugé que deux ÉIG survenus parmi les 2 434 sujets vaccinés étaient possiblement liés à la vaccination contre la rage: un cas d'angio-œdème chez un enfant après une dose de rappel du VCDH, et un cas de dyspnée, d'angio-œdème et d'urticaire chez un adulte après le VCDH. Aucun des deux cas n'a été confirmé parles chercheurs de l'étude comme étant lié au vaccin. Un troisième ÉIG (c'est-à-dire une œsophagite chez un adulte après l'administration du VCDH) a été signalé, mais nous avons jugé qu'il était peu probable qu'il soit lié au vaccin.
À l'aide de ces valeurs, nous avons estimé la probabilité de survenue d'un ÉIG après l'achèvement de la série complète de vaccins contre la rage à 0,082 % (2 évènements/2 434 sujets). Nous avons ensuite élaboré un modèle de risque pour évaluer les préjudices potentiels liés au vaccin dans le contexte d'un voyage dans des régions où le risque de rage est relativement élevé (en raison de la circulation du variant canin du virus). Plus précisément, nous avons comparé les résultats des voyageurs qui avaient reçu la PPrE contre la rage à ceux qui ne l'avaient pas reçue, en supposant une probabilité de 1 % d'exposition à un animal et en partant du principe qu'ils recevraient la PPE contre la rage (tableau 3). Pour la PPrE contre la rage, comparativement à l'absence de PPrE, la différence absolue en ce qui concerne la probabilité d'ÉIG était de 82/100 000 (0,082 %), soit un ÉIG supplémentaire pour 1 220 voyageurs recevant la PPrE contre la rage. Nous avons jugé qu'il s'agissait d'un préjudice modérément important (tableau 4).
| Statut d'immunisation | Type de série vaccinale | Risque (en %) | Taux (pour 100 000 voyages-personnes) |
|---|---|---|---|
| Avec PPrE | Série vaccinale préexposition | 0,082 | 82 |
| Série vaccinale post-expositiona Note de tableau a | 0,00082 | 0,82 | |
| Total estimé | 0,083 | 83 | |
| Sans PPrE | Série vaccinale préexposition | 0 | Sans objet |
| Série vaccinale post-expositiona Note de tableau a | 0,00086 Note de tableau b | 0,86 | |
| Total estimé | 0,00086 | 1 | |
Acceptabilité, faisabilité et ressources
Lors de l'élaboration de notre recommandation, nous avons évalué l'acceptabilité et la faisabilité de l'administration de la PPrE contre la rage, par rapport à l'absence de PPrE, du point de vue des voyageurs individuels, ainsi que les aspects pertinents concernant les ressources (annexe 7). Nous n'avons pas effectué d'analyse coût-efficacité, car de telles évaluations sont généralement appliquées à l'échelle de la société ou du système de santé plutôt qu'à l'échelle individuelle. En outre, nous n'avons trouvé aucune donnée permettant de décrire précisément la volonté des voyageurs d'assumer eux-mêmes les coûts de la PPrE contre la rage. Toutefois, les données sur d'autres vaccins à prévoir en cas de voyage, comme les vaccins contre l'encéphalite japonaiseNote de bas de page 25 ou le chikungunyaNote de bas de page 26, indiquent que les voyageurs ont des points de vue variés sur les vaccins qui protègent contre des maladies qui sont peu fréquentes, mais dont les conséquences sont graves. Certains voyageurs sont disposés à payer pour une telle protection, alors que d'autres ne le sont pas. Nous sommes d'avis que cela pourrait également s'appliquer à la PPrE contre la rage, bien que, dans ce cas, les avantages perçus pourraient davantage être liés au fait que les voyageurs souhaitent éviter de perturber leur voyage plutôt que de prévenir l'infection ou la maladie.
La PPrE contre la rage est probablement réalisable pour la plupart des voyageurs, bien qu'elle puisse être limitée dans les collectivités éloignées où l'accès aux cliniques offrant la PPrE contre la rage est restreint. Il se peut également que certaines cliniques n'offrent pas la vaccination par voie intradermique en raison d'une faible demande ou de la formation limitée des fournisseurs de soins. Dans de tels cas, les voyageurs pourraient devoir recevoir des injections intramusculaires, ce qui peut être plus coûteux.
Les sommes à débourser pour recevoir la PPrE contre la rage varient en fonction de la clinique et des calendriers ou des schémas de vaccination. Au Canada, nous avons jugé que les ressources nécessaires pour recevoir la PPrE contre la rage par voyageur individuel étaient importantes (plus de 300 $ par personne par intervention). Cependant, dans les circonstances particulières auxquelles s'applique notre recommandation de PPrE contre la rage, nous croyons également que la plupart des voyageurs, qu'ils reçoivent ou non la vaccination, la jugeraient acceptable (annexe 7).
Jugement
Dans l'ensemble, nous pensons que la plupart des voyageurs opteraient pour la PPrE contre la rage en raison des avantages potentiels qu'elle offre en ce qui concerne l'évitement des interruptions de voyage, malgré l'augmentation de la probabilité d'ÉIG comparativement à l'absence de PPrE. Cette recommandation est particulièrement pertinente dans les contextes où le risque de rage est élevé en raison de la présence du variant canin du virus de la rage, et où il se peut que les RIg ne soient pas accessibles.
| Résultat | Différence absolue (pour 100 000 voyages-personnes) |
Jugement |
|---|---|---|
| Prévention des cas cliniques de rage (avantage) | Sand objet | Insignifiante |
| Évitement des perturbations majeures de voyage (avantage) | 870 de moins | Modérée |
| Évitement de la maladie sérique attribuable aux RIg (avantage) | 4 de moins | Insignifiante |
| Survenue d'ÉIG (préjudice) | 82 de plus | Modérée |
Compte tenu de ces éléments, le CCMTMV formule une recommandation discrétionnaire à l'égard de la PPrE contre la rage pour les voyageurs qui se rendent dans des régions où le variant canin du virus de la rage est présent et où il se peut que les RIg indiquées ne soient pas accessibles rapidement. Les cliniciens devraient évaluer l'itinéraire de chaque voyageur, l'accès aux soins médicaux au lieu de destination et les valeurs personnelles du voyageur, et déterminer conjointement avec le voyageur si la PPrE contre la rage est appropriée.
Recommandations pour la prévention et le traitement des blessures associées aux animaux
Les recommandations en matière de bonnes pratiques ont été élaborées conformément au cadre GRADE (voir le Processus fondé sur les preuves pour l'élaboration de lignes directrices et de recommandations liées à la médecine de voyage et à la médecine tropicale).
Recommandation 2
Les voyageurs devraient éviter tout contact avec les animaux pendant leur voyage (énoncé sur les bonnes pratiques, annexe 8).
Remarques :
- Voir l'annexe 2 pour obtenir des renseignements sur les lignes directrices sur la prévention de l'exposition aux animaux à l'intention des voyageurs.
Recommandation 3
Les voyageurs qui souffrent d'une blessure causée par un animal (par exemple, une morsure ou une griffure causée par un mammifère comme un chien, un chat, un singe ou une chauve-souris) devraient obtenir une aide médicale dès que possible (énoncé sur les bonnes pratiques, annexe 8).
Remarques :
- Le lavage immédiat de la plaie avec de l'eau et du savon pendant au moins 15 minutes constitue une mesure importante pour réduire le risque d'infection après une exposition à un animal.
- L'évaluation médicale et la PPE (si elle est recommandée) ne devraient pas être retardées jusqu'au retour au Canada.
- Demander et conserver les dossiers de PPE contre la rage reçue pendant les voyages, y compris le nom des produits (RIg et/ou vaccins) et la date à laquelle ils ont été administrés. Consulter les Dossiers de vaccination : Guide canadien d'immunisation pour connaître la liste complète des détails importants sur la vaccination.
- Chercher à obtenir des soins de santé dès que possible après le retour au Canada. Lors de la consultation, apporter les documents relatifs aux traitements reçus à l'étranger.
- Même les morsures d'animaux d'apparence mineure peuvent pénétrer les gaines tendineuses, les capsules articulaires, les os ou les nerfs, et présenter un risque de complications graves.
Autres aspects à considérer relativement au soin des plaies en cas d'exposition
Principes de prise en charge des morsures
Bien que la rage soit souvent la conséquence la plus redoutée des morsures de mammifères, la complication la plus fréquente est l'infection des tissus mous. Pour réduire ce risque, une irrigation rapide et abondante de la plaie est recommandée lorsqu'elle n'est pas remplacée par une autre forme de prise en charge médicale de la blessure (par exemple, des techniques nécessaires à la survie)Note de bas de page 27. Sauf dans des circonstances particulières, notamment l'envenimation où un nettoyage vigoureux peut aggraver les lésions tissulairesNote de bas de page 28, des soins méticuleux de la plaie et son irrigation avec une solution stérile sont des éléments essentiels de la prise en charge des morsures. Pour l'irrigation, il est préférable d'utiliser une solution saline normale ou de l'eau du robinet traitée, mais des solutions antiseptiques douces (par exemple, une solution d'iode organique à 1 %) peuvent être utilisées, à condition qu'elles n'endommagent pas les tissus viables exposésNote de bas de page 29. En outre, selon les pratiques exemplaires, il est recommandé de retirer les bagues, les montres ou tout vêtement contraignant se trouvant près de l'emplacement de la morsure dès que possible pendant l'administration des soins initiaux de la plaieNote de bas de page 30.
Malgré des soins de haute qualité, les infections de la peau et des tissus mous demeurent fréquentes à la suite de morsures. Des complications locales sont possibles, notamment la formation d'un abcès, une lymphangite, une arthrite septique, une ténosynovite et une ostéomyélite. Dans les cas les plus graves, une bactériémie peut entraîner des complications systémiques, comme une septicémie, une endocardite, une méningite ou des abcès cérébraux.
Plusieurs facteurs de risque établis augmentent la probabilité d'infection et de complications connexes, notamment :
- les morsures touchant une main ou une articulation (30 à 40 % de celles-ci deviendront infectées)Note de bas de page 31;
- les morsures de chats et de chiens;
- les morsures avec lésions par écrasement;
- le patient tarde à consulter (> 12 heures) pour des soins;
- le patient est atteint de diabète et/ou d'une autre affection affaiblissant son système immunitaireNote de bas de page 32.
Il a été démontré qu'un traitement antimicrobien prophylactique réduit le risque d'infection et peut améliorer l'issue pour le patient, en particulier dans les cas de morsures de la main ou chez les personnes présentant un risque accru de complicationsNote de bas de page 33 Note de bas de page 34. Comme il peut être difficile d'évaluer avec précision la profondeur et la gravité d'une plaie, les voyageurs devraient être informés du fait que, même dans le cas de morsures d'animaux en apparence mineures, il peut y avoir une atteinte des gaines tendineuses, des capsules articulaires, des os ou des nerfs, ce qui peut poser un risque de complications graves. Par conséquent, il est recommandé dans tous les cas de consulter un professionnel de la santé dès que possible.
Lors de la prise en charge des morsures d'animaux, il est important de tenir compte de la flore microbienne spécifique qui colonise la bouche de l'espèce animale en cause, car cela peut influencer le choix de la prophylaxie ou du traitement antimicrobien. Bien que les blessures par morsure soient souvent contaminées par divers microorganismes, certains agents pathogènes sont plus souvent associés à des espèces particulières, par exemple :
- Chats et chiens : Pasteurella spp., Capnocytophaga spp.
- Rats et souris : Spirillum minus, Streptobacillus moniliformis, Streptobacillus notomytis
- Lapins : Francisella tularensis
- Cerfs, moutons, bovins et chèvres : Parapoxvirus (par exemple, ecthyma contagieux)
Bien que cela soit extrêmement rare, les morsures peuvent présenter un risque de contamination par Clostridium tetani. Les voyageurs peuvent réduire leur risque de contracter le tétanos en suivant les recommandations du Anatoxine tétanique : Guide canadien d'immunisation, avant le voyage.
Les recommandations complètes pour le traitement des infections liées à des morsures et des complications possibles dépassent la portée de la présente déclaration et sont présentées en détail dans d'autres documentsNote de bas de page 27 Note de bas de page 31.
Virus de l'herpès B
Le virus de l'herpès B, aussi appelé virus de l'herpès du cercopithèque (CHV-1), ou Macacine herpesvirus 1, est un virus peu commun mais potentiellement mortel qui est endémique chez les singes macaques, notamment ceux que l'on trouve couramment dans les zoos ou les centres de recherche du monde entier et à l'état sauvage dans de nombreuses régions d'Asie (avec de très petites populations géographiquement limitées à de petites zones de la Floride et du Texas). Alors que les macaques sont souvent des porteurs asymptomatiques du virus, l'humain peut le contracter en cas de morsure, de griffure ou de l'exposition de muqueuses ou de lésions cutanées à de la salive, à des tissus ou à des liquides corporels de singes. Chez l'humain, l'infection par le virus de l'herpès B peut provoquer une maladie neurologique grave, notamment une encéphalite, et peut être fatale si elle n'est pas traitée rapidement. Il n'existe pas de vaccin contre ce virus.
Les voyageurs devraient se protéger en évitant strictement tout contact avec les singes, en particulier les singes macaques, et notamment éviter de les nourrir et de les caresser (annexe 2). En cas de morsure, d'égratignure ou d'exposition des muqueuses, il est important de nettoyer immédiatement et soigneusement la plaie avec du savon et de l'eau et d'obtenir des soins médicaux d'urgence afin d'envisager le recours à une prophylaxie post-exposition au moyen de médicaments antiviraux comme le valacyclovir ou l'acyclovir. Un résumé des recommandations pour la prophylaxie et le traitement de l'infection par le virus de l'herpès B est présenté ailleursNote de bas de page 35. Les personnes travaillant avec des macaques (personnel de laboratoire, vétérinaires et chercheurs sur le terrain) devraient se munir d'un équipement de protection (gants, écrans faciaux, blouses de laboratoire), appliquer des protocoles d'hygiène stricts, et nettoyer et signaler rapidement toute blessure ou exposition.
Conclusion et besoins en matière de recherche
Pour améliorer la certitude des données probantes et mieux cibler les recommandations pour les voyageurs canadiens, d'autres essais cliniques et études d'observation des populations de voyageurs canadiens sont nécessaires, y compris des études représentatives des voyageurs qui effectuent de longs séjours à l'étranger et des personnes qui rendent visite à des parents et à des amis. Les recherches futures sur la rage et la prévention des blessures causées par des animaux chez les voyageurs devraient se concentrer sur l'élargissement de l'accès à la PPE contre la rage dans les milieux à faibles ressources et l'amélioration de la surveillance mondiale afin de cerner les régions à risque élevé et les habitudes de voyage.
Les recommandations du CCMTMV peuvent être modifiées si de nouvelles données sont publiées.
Abréviations
- ACIP
- Advisory Committee on Immunization Practices
- ASPC
- Agence de la santé publique du Canada
- CCMTMV
- Comité consultatif de la médecine tropicale et de la médecine des voyages
- CCNI
- Comité consultatif national de l'immunisation
- CDC
- Centers for Disease Control and Prevention des États-Unis
- ECR
- essai comparatif randomisé
- ÉIG
- évènement indésirable grave
- FDA
- Food and Drug Administration des États-Unis
- GCI
- Guide canadien d'immunisation
- GRADE
- Grading of recommendations, assessment, development, and evaluation
- IC
- intervalle de confiance
- OMS
- Organisation mondiale de la Santé
- PPE
- prophylaxie post-exposition
- PPrE
- prophylaxie préexposition
- RIg
- immunoglobuline antirabique
- SAGE
- Groupe consultatif stratégique d'experts sur la vaccination
- VAERS
- Vaccine Adverse Effects Reporting System
- VCDH
- vaccin préparé sur cellules diploïdes humaines
- VCEPP
- vaccin préparé sur cellules d'embryons de poulet purifiées
- GT
- groupe de travail
Remerciements
La présente déclaration a été préparée par le groupe de travail sur les morsures d'animaux du CCMTMV : Y Bui (responsable), I Bogoch, A Khatib, C Rossi, S Schofield, J Smith, et a été approuvée par le CCMTMV.
Le CCMTMV tient à remercier les personnes suivantes pour leur contribution : J Blackmore, L Coward, Z Davoodi, C Jensen, A Killikelly, M Laplante, E Leonard, T Nguyen, N Santesso, J Thériault, J Vachon, B Warshawsky, et la bibliothèque de l'Agence de la santé publique du Canada.
CCMTMV Membres : M Libman (président), Y Bui (vice-présidente), K Plewes (présidente du sous-comité sur le paludisme), I Bogoch, A Khatib, P Lagacé-Wiens, J Lee et C Yansouni.
Ancien membres : A Acharya et C Greenaway
Représentants de liaison : J Pernica (Association pour la microbiologie médicale et l'infectiologie Canada), K O'Laughlin (Centers for Disease Control and Prevention des États-Unis)
Ancienne représentante de liaison : K Angelo (Centers for Disease Control and Prevention des États-Unis) et I Viel-Thériault (Société canadienne de pédiatrie).
Représentants d'office : D Marion (ministère de la Défense nationale), S Schofield (ministère de la Défense nationale), M Tunis et C Jensen (Secrétariat du Comité consultatif national de l'immunisation [CCNI], ASPC) et R Zimmer (Direction des médicaments biologiques et radiopharmaceutiques, Santé Canada).
Anciens représentants d'office : C Rossi, E Ebert
Conflits d'intérêts
Aucun déclaré
Annexe 1 : Pays où le variant canin du virus est présent et où les RIg ne sont pas facilement accessibles
Pays :
- Afghanistan
- Angola
- Arménie
- Azerbaïdjan
- Bélize
- Bénin
- Bolivie
- Cameroun
- Colombie
- Corée du Nord
- Équateur
- Éthiopie
- Gabon
- Grenade
- Guatémala
- Guinée
- Guinée équatoriale
- Guinée-Bissau
- Guyane
- Haïti
- Honduras
- Irak
- Iran
- Kazakhstan
- Kirghizistan
- Laos
- Libéria
- Libye
- Mali
- Mongolie
- Myanmar
- Nicaragua
- Ouzbékistan
- Pakistan
- République centrafricaine
- République démocratique du Congo
- République dominicaine
- République du Congo
- Saint-Kitts-et-Nevis
- Salvador
- Sierra Leone
- Somalie
- Soudan
- Sri Lanka
- Suriname
- Syrie
- Tadjikistan
- Tchad
- Turkménistan
- Vénézuéla
- Yémen
- Zambie
Annexe 2 : Lignes directrices sur la prévention de l'exposition aux animaux à l'intention des voyageurs
Pour réduire le risque de blessures ou de maladies liées aux animaux au cours d'un voyage, les voyageurs devraient prendre les précautions suivantes :
Éviter les contacts directs
- Éviter de toucher, de caresser ou de nourrir les animaux sauvages ou domestiques, même s'ils semblent amicaux ou en bonne santé.
- Se tenir loin des animaux malades ou morts.
- Éviter d'apporter des sacs de plastique ou de la nourriture lors de la visite de lieux où l'on entre facilement en contact avec des animaux, comme les temples des singes.
Suivre les directives locales
- Toujours suivre les instructions des guides ou des organisateurs de voyages, en particulier dans les réserves naturelles, les sanctuaires d'animaux ou lors des safaris.
- Respecter les barrières, les panneaux et les aires d'observation désignées.
Faire preuve de vigilance
- Demeurer attentif à tout ce qui se passe aux alentours.
- Veiller à respecter l'espace des animaux.
- Éviter de poser des gestes qui pourraient attirer les animaux, comme transporter de la nourriture visible.
Superviser les personnes vulnérables
- Surveiller attentivement les enfants et les personnes souffrant de troubles cognitifs, qui peuvent ne pas reconnaître les interactions à risque.
- Enseigner à ces personnes à signaler immédiatement tout contact avec un animal ou toute morsure ou griffure.
Planifier
- Avant de partir en voyage, repérer les centres médicaux urbains les plus proches, notamment lors de la visite de régions isolées ou sauvages.
- Garder à l'esprit que des voyages fréquents ou de longue durée peuvent accroître le risque d'exposition à des animaux.
Être conscient des activités ou des zones où le risque de contact avec des animaux est plus élevé
- La pratique d'activités dans la nature peut être associée à une probabilité accrue de contact avec des animaux comparativement aux voyages dans des centres de villégiature ou aux séjours dans des centres urbains.
- Activités pouvant être touchées :
- Voyages à vélo
- Camping
- Chasse
- Randonnée
- Spéléologie
- Visite chez des amis ou des parents
- Visite de temples où vivent des singes
- Safaris à pied
Annexe 3 : Exemple de stratégie de recherche documentaire
| Numéro de la recher-che | Stratégie de recherche | Résultats |
|---|---|---|
| 1 | ("cercopithecine herpesvirus 1" or herpes virus* B or herpes virus* simian* or "herpesvirus 1 cercopithecine" or simian herpesvirus* or " herpesvirus 1 (alpha) cercopithecine" or herpes* b or monkey b virus* or herpes* simi* or macacine herpesvirus* or rabies or dog bit* or monkey bit* or monkey scratch* or animal bit* or animal scratch*).mp. [mp=title, book title, abstract, original title, name of substance word, subject heading word, floating sub-heading word, keyword heading word, organism supplementary concept word, protocol supplementary concept word, rare disease supplementary concept word, unique identifier, synonyms, population supplementary concept word, anatomy supplementary concept word] | 19 830 |
| 2 | (risk* or incidence or prevalence or morbidity or death? or die or died or dead or mortality or epidemiol* or surveill* or demograph*).mp. [mp=title, book title, abstract, original title, name of substance word, subject heading word, floating sub-heading word, keyword heading word, organism supplementary concept word, protocol supplementary concept word, rare disease supplementary concept word, unique identifier, synonyms, population supplementary concept word, anatomy supplementary concept word] | 7 344 760 |
| 3 | (travel* or (visit* adj2 endemic*) or touris*).mp. [mp=title, book title, abstract, original title, name of substance word, subject heading word, floating sub-heading word, keyword heading word, organism supplementary concept word, protocol supplementary concept word, rare disease supplementary concept word, unique identifier, synonyms, population supplementary concept word, anatomy supplementary concept word] | 101 240 |
| 4 | (vaccin* or immuniz* or immunis* or inoculat* or injection* or booster* or intradermal* or subcutaneous* or intramuscular* or intra dermal* or sub-cutaneous* or intra muscular*).mp. [mp=title, book title, abstract, original title, name of substance word, subject heading word, floating sub-heading word, keyword heading word, organism supplementary concept word, protocol supplementary concept word, rare disease supplementary concept word, unique identifier, synonyms, population supplementary concept word, anatomy supplementary concept word] | 1 632 241 |
| 5 | (case report* or case stud*).mp. [mp=title, book title, abstract, original title, name of substance word, subject heading word, floating sub-heading word, keyword heading word, organism supplementary concept word, protocol supplementary concept word, rare disease supplementary concept word, unique identifier, synonyms, population supplementary concept word, anatomy supplementary concept word] | 2 550 403 |
| 6 | (prophylaxis or therap* or treatment* or protocol* or prevent* or guideline* or guide line* or post exposure* or postexposure* or preexposure* or pre exposure* or first aid).mp. [mp=title, book title, abstract, original title, name of substance word, subject heading word, floating sub-heading word, keyword heading word, organism supplementary concept word, protocol supplementary concept word, rare disease supplementary concept word, unique identifier, synonyms, population supplementary concept word, anatomy supplementary concept word] | 12 044 936 |
| 7 | "Herpesvirus 1, Cercopithecine"/ or rabies/ or Rabies virus/ | 13 111 |
| 8 | rabies/ep, mo | 3 237 |
| 9 | exp epidemiologic methods/ or exp demography/ | 7 705 469 |
| 10 | exp travel/ or travel medicine/ | 31 700 |
| 11 | exp immunization/ or exp immunization programs/ | 215 206 |
| 12 | rabies vaccines/ | 6 476 |
| 13 | case reports/ | 2 341 453 |
| 14 | exp therapeutics/ or "post-exposure prophylaxis"/ | 5 218 684 |
| 15 | (1 or 7) and (2 or 9) and (3 or 10) | 490 |
| 16 | 8 and (3 or 10) | 162 |
| 17 | 15 or 16 | 490 |
| 18 | limit 17 to yr="2000-Current" [epi] | 423 |
| 19 | (1 or 7) and (4 or 11) and (3 or 10) | 479 |
| 20 | 12 and (3 or 10) | 262 |
| 21 | 19 or 20 | 479 |
| 22 | limit 21 to yr="2000 -Current" [vaccination] | 392 |
| 23 | (5 or 13) and (1 or 7) and (3 or 10) | 78 |
| 24 | limit 23 to yr="2000-Current" [case reports] | 59 |
| 25 | ("cercopithecine herpesvirus 1" or herpes virus* B or herpes virus* simian* or "herpesvirus 1 cercopithecine" or simian herpesvirus* or " herpesvirus 1 (alpha) cercopithecine" or herpes* b or monkey b virus* or herpes* simi* or macacine herpesvirus*).mp. or "Herpesvirus 1, Cercopithecine"/ | 580 |
| 26 | (6 or 14) and 25 | 177 |
| 27 | limit 26 to yr="2000 -Current" [herpes B treatment] | 102 |
| 28 | Disability-Adjusted Life Years/ | 183 |
| 29 | (disability-adjusted life year? or dalys or daly or "years Lived With Disabilit*").mp. | 6 552 |
| 30 | 28 or 29 | 6 552 |
| 31 | (1 or 7) and 30 | 33 |
| 32 | limit 31 to yr="2000-current" [DAYLs] | 33 |
| 33 | 18 or 22 or 24 or 27 or 32 | 633 |
|
Remarque : L’astérisque (*) est utilisé comme symbole de troncation ou caractère générique. Il représente 0, 1 ou plusieurs caractères placés à la fin ou au milieu d’un mot. Il permet d’élargir les résultats de recherche en identifiant les différentes formes dérivées d’une même racine. |
||
Annexe 4 : Données d'entrée du modèle pour l'estimation de la réduction des perturbations de voyage
Lors de l'évaluation des avantages et des risques de la PPrE par le vaccin contre la rage, nous avons utilisé la modélisation pour estimer la probabilité d'exposition dans des milieux à risque élevé, les résultats pour la santé en cas d'exposition et les répercussions potentielles de la vaccination préexposition chez les voyageurs.
Les principales hypothèses et les données d'entrée suivantes ont été utilisées dans notre modélisation :
- S'il était indiqué que les RIg étaient accessibles à un endroit, nous avons supposé que le vaccin contre la rage l'était également.
- Nous avons supposé que les personnes ayant subi une morsure ou une griffure d'animal consulteraient immédiatement un médecin et recevraient une PPE contre conformément au Guide canadien d'immunisation.
- Dans les milieux à risque élevé où le variant canin du virus est présent (par exemple, en Asie ou en Afrique), nous avons estimé la probabilité de subir une blessure nécessitant une PPE à 1 % par mois de voyage (10 expositions pour 1 000 personnes-voyages).
Puisqu'il existe peu d'études publiées qui quantifient le temps perdu lors d'un voyage par suite de la recherche d'un traitement post-exposition contre la rage, nous avons utilisé la modélisation pour estimer les répercussions du recours à la PPrE sur les perturbations majeures de voyage. Les hypothèses et données suivantes ont été utilisées :
- Nous avons limité l'analyse aux pays où la présence du variant canin du virus est connue, car on y recense la majorité des cas de rage humaine dans le monde et il s'agit de destinations à risque accru pour les voyageurs.
- Nous avons utilisé l'accessibilité de la PPE aux lieux de destination, tel qu'elle figure dans la base de données des Centers for Disease Control and Prevention (CDC) des États-Unis (en anglais seulement) [consultée en juin 2025], comme mesure indirecte pour estimer le potentiel de perturbation des voyages. Les RIg n'étaient pas accessibles dans 46 % (53/115) des pays où le variant canin du virus est présent, tandis que le vaccin contre le rage n'était pas accessible dans 13 % (15/115) de ces pays.
- Nous avons défini une perturbation majeure de voyage comme l'impossibilité d'accéder à une PPE standard dans les 48 heures suivant l'exposition à un animal, comme indiqué dans la base de données des CDC (en anglais seulement).
- Si un traitement par RIg était indiqué et qu'il n'était pas facilement accessible dans les 48 heures au lieu de destination, nous avons supposé que les voyageurs devraient obtenir des soins ailleurs, ce qui aurait pour effet de perturber leur itinéraire de voyage.
- Nous avons supposé que les perturbations de voyage étaient plus importantes dans le cas du recours à un schéma complet de PPE contre la rage (RIg + 4 ou 5 doses de vaccin) comparativement à un schéma partiel de PPE contre la rage destiné aux voyageurs ayant reçu une PPrE contre la rage (2 doses de vaccin).
Annexe 5 : Données d’entrée du modèle pour l’estimation du risque de rage clinique chez les voyageurs
| Territoire de compétence | Cas | Région d'acquisition (nombre de cas) | Estimation du nombre de voyages (en millions) |
Taux d'attaque global |
||
|---|---|---|---|---|---|---|
| Améri-ques | Afrique | Asie | ||||
| Canada | 0 | 0 | 0 | 0 | 224 | 0/224 |
| États-Unis | 2 | 0 | 0 | 2 | 551 | 2/551 |
| Europe | 7 | 2 | 3 | 3 | 1 200 | 7/1 200 |
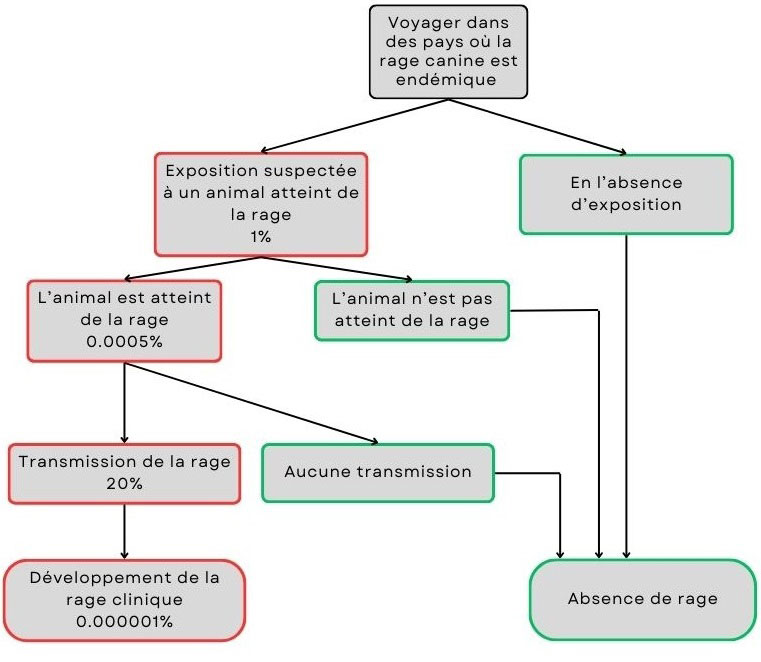
Figure 2 : Texte descriptif
Les voyageurs qui se rendent dans des pays où la rage canine est endémique courent un risque estimé à 1 % d'être exposés à un animal soupçonné d'être atteint de la rage.
- En l'absence d'exposition, il n'y a pas de risque de développer la rage.
- En cas d'exposition, il faut savoir qu'il y a 0,0005 % de probabilité que l'animal soit atteint de la rage.
- Si l'animal n'est pas atteint de la rage, il n'y a aucun risque.
- Si l'animal est atteint de la rage, il y a 20 % de probabilité que le virus soit transmis.
- S'il n'y a pas de transmission, il n'y a pas de risque.
- En cas de transmission, le voyageur peut développer des symptômes cliniques de la rage.
En combinant ces probabilités, le risque estimé de développer des symptômes cliniques de la rage chez les voyageurs qui se rendent dans des régions endémiques est d'environ 0,000001 %.
| Données d'entrée | Valeurs | Référence |
|---|---|---|
| Incidence moyenne de la rage par an chez les voyageurs | 2,6 [de 1,9 à 3,7] | Carrara, 2013Note de bas de page 36 |
| En cas d'exposition, probabilité que l'animal en cause soit atteint de la rage | 0,0005 % | Estimation Note de tableau a |
| Probabilité de transmission du virus de la rage | 20 % [de 0,1 % à 60 %] | Medley, 2017Note de bas de page 37 Cleaveland, 2022Note de bas de page 38 Hampson, 2015Note de bas de page 39 |
Annexe 6 : Données probantes à l'appui de l'estimation du risque d'ÉIG
| Étude | Vaccin | Population | Nombre | ÉIG déclarés |
|---|---|---|---|---|
| Anderson, 1980 | VCDH | Adultes et enfants | 90 | 0 |
| Ajjan, 1989 | VCDH | Adultes (étudiants en médecine vétérinaire) | 73 | 0 |
| Arora, 2004 | VCDH | Adultes | 45 | 0 |
| Briggs, 2000 | VCEPP | Patients exposés à des animaux | 136 | 0 |
| Endy, 2019 | VCEPP | Adultes | 59 | 0 |
| Guiambao, 2005 | VCEPP | Patients exposés à des animaux | 113 | 0 |
| Guiambao, 2019 | VCEPP | Adultes et enfants | 420 | 0 |
| Guiambao, 2022 | VCDH | Adultes et enfants | 307 | 0 |
| Mill, 2011 | VCDH | Adultes (voyageurs) | 420 | 0 |
| Recuenco, 2017 | VCEPP | Adultes (personnel de laboratoire, épidémiologistes et premiers intervenants) | 130 | 0 |
| Sabchareon, 1999 | VCDH | Enfants | 199 | 1Note de tableau a |
| Soentjens, 2019 | VCDH | Adultes (forces armées) | 500 | 1Note de tableau b |
| Suntharasamai, 1994 | VCEPP | Adultes (étudiants en médecine vétérinaire) | 133 | 0 |
Annexe 7 : Cadre de données probantes appuyant la prise de décisions
Question : Faudrait-il recommander l'administration d'une PPrE par le vaccin contre la rage aux voyageurs canadiens qui se rendent dans des destinations où le fardeau de la rage est élevé et où les RIg ne sont peut-être pas accessibles?
Population : Voyageurs canadiens qui se rendent dans une destination où le risque de rage est relativement élevé (c'est-à-dire où le variant canin du virus de la rage circule) et où les RIg peuvent ne pas être accessibles.
Intervention : PPrE contre la rage à l'aide du VCDH ou du VCEPP
Comparaison : Pas de PPrE contre la rage
Principaux résultats : Cas cliniques de rage, perturbations majeures des voyages, maladie sérique et ÉIG
Contexte : Voyage à l'étranger
Perspective : Individuelle
Contexte : La rage est une encéphalomyélite aiguë progressive qui est presque toujours mortelle après l'apparition des symptômes cliniques. Le CCMTMV a examiné les données disponibles et a appliqué l'approche GRADE pour formuler ses recommandations concernant la PPrE contre la rage chez les voyageurs qui se rendent dans des régions où la rage est endémique.
Conflits d'intérêts : Aucun
Évaluation
| Domaine | Jugement | Résultats de recherche et autres éléments à considérer |
|---|---|---|
| Problème : Le problème est-il une priorité? | Non Probablement pas Probablement oui Oui Variable Ne sait pas |
La rage est une maladie universellement mortelle. Bien que la PPrE soit généralement considérée comme moins urgente que la PPE, la réalité est plus complexe en raison de plusieurs facteurs, comme une faible sensibilisation à l'égard du risque de rage, des taux élevés de rage canine dans les destinations de voyage populaires et le manque d'accès rapide à des soins post-exposition. |
| Effets souhaitables : Quelle est l'ampleur des effets souhaités anticipés? | Insignifiante Petite Modérée Grande Variable Ne sait pas |
Des examens systématiques portant sur nos principaux résultats et sur les questions de recherche connexes, comme indiqué dans les méthodes d'élaboration des lignes directrices, ont été réalisés à l'aide de recherches effectuées jusqu'au 10 janvier 2024. Les données probantes relatives à la maladie sérique comme résultat ont été obtenues dans le cadre d'une revue exploratoire. Les estimations ont été utilisées pour modéliser les effets sur les résultats critiques. Les estimations représentent les effets dans les régions à risque élevé (c'est-à-dire où le variant canin du virus est présent) et où les RIg indiquées ne sont pas facilement accessibles. Voir les estimations des effets souhaitables au tableau 10. Perturbations majeures des voyages : Le nombre de perturbations majeures de voyage évitées grâce à la PPrE est de 870 pour 100 000 voyages-personnes, ce qui est jugé modéré. Cas cliniques de rage : Le risque que l'on observe des cas cliniques de rage chez les voyageurs canadiens est extrêmement faible. L'avantage lié à la PPrE contre la rage serait insignifiant. Maladie sérique : Le nombre de cas de maladies sériques évités grâce à la PPrE est estimé à 4 pour 100 000 voyages-personnes, ce qui est jugé insignifiant. Autres éléments à considérer : Le degré de certitude des données probantes a été abaissé de deux échelons pour tenir compte du risque de biais. |
| Effets indésirables : Quelle est l'ampleur des effets indésirables anticipés? | Insignifiante Petite Modérée Grande Variable Ne sait pas |
Voir les estimations des effets souhaitables au tableau 10. ÉIG : Le vaccin contre la rage (VCDH ou VCEPP) peut être associé à une augmentation modérée de la probabilité d'ÉIG. Autres éléments à considérer : |
| Certitude des données probantes : Quel est le degré global de certitude des données sur les effets? | Très faible Faible Modéré Élevé Aucune étude incluse |
Le degré global de certitude des données sur les résultats critiques est très faible. |
| Importance des résultats pour la population touchée : Y a-t-il une incertitude ou une variabilité importante quant à la valeur accordée par les voyageurs aux principaux résultats? | Incertitude ou variabilité importante Incertitude ou variabilité possiblement importante Probablement aucune incertitude ou variabilité importante Aucune incertitude ou variabilité importante |
Le GT a déterminé que les éléments suivants sont des résultats critiques ou importants pour la prise de décision : Résultats souhaités :
Bien que nous n'ayons pas trouvé de données probantes précises à cet égard, le GT croit que les voyageurs estimeraient probablement qu'il s'agit de résultats critiques ou importants. Autres éléments à considérer : |
| Équilibre entre les effets : L'équilibre entre les effets souhaitables et indésirables favorise-t-il l'intervention ou la comparaison? | Favorise la comparaison Favorise probablement la comparaison Ne favorise ni l'intervention ni la comparaison Favorise probablement l'intervention Favorise l'intervention Variable Ne sait pas |
Les avantages et les préjudices estimés étaient faibles. Cependant, nous croyons que la plupart des voyageurs accorderaient plus d'importance au fait d'éviter les perturbations de voyage qu'aux ÉIG. Par conséquent, le recours à la PPrE contre la rage a été privilégié dans les milieux à risque élevé où les RIg ne sont probablement pas facilement accessibles. |
| Considérations relatives aux ressources : Quels sont les besoins en ressources (coûts) pour l'individu? | Coûts élevés Coûts modérés Coûts faibles Coûts négligeables Variables Ne sait pas |
Les sommes à débourser varient en fonction de la clinique ainsi que des calendriers et des schémas de vaccination. Au Canada, nous avons jugé que les ressources nécessaires pour recevoir la PPrE contre la rage par chaque voyageur individuel étaient importantes (plus de 300 $ par personne par intervention). |
| Équité : | Réduit Probablement réduit Probablement pas d'impact Probablement augmenté Augmenté Variable Ne sait pas Sans objet |
Comme le point de vue adopté était celui du voyageur individuel, les considérations relatives à l'équité n'ont pas été explicitement abordées dans notre évaluation. |
| Acceptabilité : | Non Probablement pas Probablement oui Oui Variable Ne sait pas |
Nous avons jugé que l'intervention était probablement acceptable pour la plupart des personnes. Autres éléments à considérer : |
| Faisabilité : | Non Probablement pas Probablement oui Oui Variable Ne sait pas |
Nous avons jugé que l'intervention était probablement réalisable pour la plupart des personnes. Autres éléments à considérer : |
Type de recommandation
Recommandation discrétionnaire en faveur de l'intervention (PPrE contre la rage comparée à l'absence de PPrE).
Conclusions
Recommandation
Le CCMTMV suggère d'offrir la PPrE par le vaccin contre la rage aux voyageurs qui se rendent dans des régions où le risque de rage est relativement élevénote de bas de page a et où les RIg peuvent ne pas être facilement accessiblesnote de bas de page b
(Recommandation discrétionnaire, fondée sur des données de très faible certitude)
Remarques :
- Il s'agit d'une recommandation discrétionnaire. Le professionnel de la santé devrait examiner avec le patient les avantages et les préjudices potentiels associés à la PPrE par le vaccin contre la rage afin de l'aider à prendre une décision qui correspond à ses valeurs et à ses préférences. La discussion devrait porter sur d'éventuelles solutions de rechange et/ou complémentaires à la vaccination.
- Lorsque le variant canin du virus est présent, mais que le risque d'exposition est faible (notamment lors d'un voyage dans un centre de villégiature) ou que la durée du voyage est courte (une semaine ou moins), les avantages de la PPrE par le vaccin contre la rage peuvent être moindres et les patients peuvent choisir de ne pas la recevoir (voir l'annexe 2 pour obtenir des renseignements sur les comportements et les activités présentant un risque accru de contact avec des animaux).
- L'administration des vaccins dans le cadre de la PPrE devrait se faire faire conformément dans le chapitre sur les vaccins contre la rage du GCI, qui fournit également des recommandations pour des groupes particuliers, comme le personnel de laboratoire, les vétérinaires, le personnel vétérinaire et les agents de protection de la faune.
- Les seuils décrivant l'ampleur des effets (c'est-à-dire les préjudices ou les avantages absolus estimés qui sont jugés importants pour la prise de décision) sont résumés au tableau 1.
Justification :
- L'avantage absolu de la PPrE pour la prévention de la rage chez les voyageurs est insignifiant.
- La PPrE par le vaccin contre la rage peut réduire d'environ 1 % la probabilité d'une perturbation de voyage liée au traitement PPE (avantage modéré; très faible certitude des données), mais peut augmenter le risque d'évènements indésirables graves associés à la vaccination de 0,08 % (préjudice modéré; très faible certitude des données). Compte tenu de ces estimations, le CCMTMV estime que de nombreux patients choisiraient de recevoir une PPrE par le vaccin contre la rage pour éviter le risque que leur voyage soit perturbé.
| Résultats | Nombre de partici-pants (études) contribu-ant à l'estima-tion de l'effet | Partici-pants supplé-mentaires (études) pris en compte dans l'évalua-tion selon l'approche GRADE | Certitude des données probantes (GRADE) | Risque relatif (IC à 95 %) |
Effets absolus attendus | |
|---|---|---|---|---|---|---|
| Différence de risque avec la PPrE | Risque sans PPrE | |||||
| Cas cliniques de rage | Sans objet (modélisation) |
Sans objet | Sans objet | Impossible à estimer | On n'a trouvé aucune étude qui mesurait l'incidence des cas cliniques de rage lors de la comparaison du recours à la PPrE à l'absence de PPrE. Étant donné que le risque estimé de rage chez les voyageurs est extrêmement faible, c'est-à-dire environ 1 sur 100 millions, la différence entre le nombre de cas cliniques de rage chez les voyageurs ayant reçu la PPrE et ceux ne l'ayant pas reçue serait extrêmement faible. | |
| Perturba-tions majeures des voyages | Sans objetNote de tableau a(modélisation) | Sans objet | Très faibleNote de tableau b Note de tableau c | Impossible à estimer | 870 voyages de moins pour 100 000 voyages (937 de moins à 805 de moins) | 1 % |
| Maladie sérique attribuable aux RIg | 72 132 (1 étude non rando-misée) |
Sans objet | Très faibleNote de tableau b | Impossible à estimer | 4 voyages de moins pour 100 000 voyages (11 de moins à 0,3 de plus) | 0,4 % |
| ÉIG | 2 434 (13 études non rando-misées) |
(3 études non rando-misées)Note de tableau d | Très faiblesupNote de tableau b Note de tableau e | Impossible à estimer | 82 voyages de plus pour 100 000 voyages (65 de plus à 101 de plus) | 0,00086 % |
Annexe 8 : Tableaux d'évaluation de l'applicabilité des énoncés sur les bonnes pratiques
Énoncé sur les bonnes pratiques : Les voyageurs devraient éviter d'être en contact avec des animaux pendant leur voyage.
| Critères | Renseignements à l'appui |
Vérification |
|---|---|---|
| La population et les composantes de l'intervention sont claires | Sans objet | Oui |
| Le message est vraiment nécessaire en ce qui concerne la pratique réelle des soins de santé. | Adopter des pratiques sûres lors des interactions avec les animaux et éviter les contacts sont des stratégies importantes pour prévenir l'exposition à des animaux susceptibles d'être porteurs de maladies infectieuses. Cependant, le respect de ces recommandations est souvent sous-optimal. | Oui |
| La mise en œuvre de l'énoncé sur les bonnes pratiques a des conséquences nettes positives importantes. | Oui, la réduction de l'exposition aux animaux permet de diminuer le risque de blessure et de transmission des agents pathogènes dont ils peuvent être porteurs. | Oui |
| La collecte et la synthèse des données probantes constituent une mauvaise utilisation du temps, de l'énergie et des ressources limités d'un groupe d'experts sur les lignes directrices. Le coût d'option de la collecte et de la synthèse des données probantes est important et peut être évité. | Oui, cette recommandation vise à conseiller aux voyageurs de se protéger. Ces conseils reposent sur des principes bien établis de santé publique et d'atténuation des risques. Par ailleurs, le temps et les ressources nécessaires pour effectuer la collecte et la synthèse des données probantes supplémentaires feraient en sorte qu'il ne serait pas possible de répondre à d'autres priorités. | Oui |
| Il existe une justification claire, explicite et bien documentée, qui établit un lien entre les données probantes indirectes. | Oui, on peut raisonnablement s'attendre à ce que la réduction de l'exposition aux animaux réduise la probabilité de blessure et d'infection. | Oui |
| Clair et réalisable | Sans objet | Oui |
Jugement final : l'élaboration d'un énoncé sur les bonnes pratiques est appropriée.
Énoncé sur les bonnes pratiques : Les voyageurs qui souffrent d'une blessure causée par un animal (par exemple, une morsure ou une griffure causée par un mammifère comme un chien, un chat, un singe ou une chauve-souris) devraient chercher à obtenir des soins dès que possible.
| Critères | Renseignements à l'appui |
Vérification |
|---|---|---|
| La population et les composantes de l'intervention sont claires | Sans objet | Oui |
| Le message est vraiment nécessaire en ce qui concerne la pratique réelle des soins de santé. | Le fait de tarder à obtenir des soins médicaux après une blessure causée par un animal peut entraîner une maladie grave ou la mort. | Oui |
| La mise en œuvre de l'énoncé sur les bonnes pratiques a des conséquences nettes positives importantes. | Oui, le fait d'informer les voyageurs sur les mesures à prendre après une exposition à un animal peut réduire le risque d'effets néfastes sur la santé. | Oui |
| La collecte et la synthèse des données probantes constituent une mauvaise utilisation du temps, de l'énergie et des ressources limités d'un groupe d'experts sur les lignes directrices. Le coût d'option de la collecte et de la synthèse des données probantes est important et peut être évité. | Oui, cette recommandation vise à conseiller aux voyageurs de se protéger. Ces conseils reposent sur des principes bien établis de santé publique et d'atténuation des risques. Par ailleurs, le temps et les ressources nécessaires pour effectuer la collecte et la synthèse des données probantes supplémentaires feraient en sorte qu'il ne serait pas possible de répondre à d'autres priorités. | Oui |
| Il existe une justification claire, explicite et bien documentée, qui établit un lien entre les données probantes indirectes. | Oui, recommander aux voyageurs blessés d'obtenir des soins médicaux est une approche raisonnable et bien établie pour prévenir ou réduire les blessures, les infections et les décès. | Oui |
| Clair et réalisable | Sans objet | Oui |
Jugement final : l'élaboration d'un énoncé sur les bonnes pratiques est appropriée.
Notes de bas de page
- Note de bas de page a
-
C'est-à-dire où le variant canin du virus de la rage circule.
- Note de bas de page b
-
C'est-à-dire non accessibles facilement dans la majeure partie du pays dans les 48 heures suivant la consultation par le patient.
Références
- Note de bas de page 1
-
Rupprecht CE, Ertl HCJ. Lyssaviruses and Rabies Vaccines. In: Plotkin S OW, Offit P, editors. Plotkin's Vaccines. 8th ed. Philadelphia: Elsevier; 2023. p. 969-97.e13.
- Note de bas de page 2
-
World Health Organization. Rabies vaccines: WHO position paper, April 2018 - Recommendations. Vaccine. 2018;36(37):5500-3.
- Note de bas de page 3
-
Carvalho MS, Hampson K, Coudeville L, Lembo T, Sambo M, Kieffer A, et al. Estimating the Global Burden of Endemic Canine Rabies. PLoS Neglected Tropical Diseases. 2015;9(4).
- Note de bas de page 4
-
Gan H, Hou X, Wang Y, Xu G, Huang Z, Zhang T, et al. Global burden of rabies in 204 countries and territories, from 1990 to 2019: results from the Global Burden of Disease Study 2019. International Journal of Infectious Diseases. 2023;126:136-44.
- Note de bas de page 5
-
Rage : Surveillance [Internet]. Ottawa, gouvernement du Canada; [mis à jour le 3 octobre 2024]. Accessible à l'adresse : https://www.canada.ca/fr/sante-publique/services/maladies/rage/surveillance.html.
- Note de bas de page 6
-
Vaccins contre la rage : Guide canadien d'immunisation [Internet]. Ottawa, gouvernement du Canada; [mis à jour le 13 juin 2025]. Accessible à l'adresse : https://www.canada.ca/fr/sante-publique/services/publications/vie-saine/guide-canadien-immunisation-partie-4-agents-immunisation-active/page-18-vaccin-contre-rage.html.
- Note de bas de page 7
-
Gautret P, Diaz-Menendez M, Goorhuis A, Wallace RM, Msimang V, Blanton J, et al. Epidemiology of rabies cases among international travellers, 2013–2019: A retrospective analysis of published reports. Travel Medicine and Infectious Disease. 2020;36.
- Note de bas de page 8
-
Itani O. Preventing rabies in travelers [communication personnelle]. 1er octobre 2025.
- Note de bas de page 9
-
Gautret P, Parola P. Rabies vaccination for international travelers. Vaccine. 2012;30(2):126-33.
- Note de bas de page 10
-
Food and Drug Administration. Guidance for Industry: Toxicity Grading Scale for Healthy Adult and Adolescent Volunteers Enrolled in Preventive Vaccine Clinical Trials [Internet]. Federal Register; [mis à jour le 27 septembre 2007]. Accessible à l'adresse : https://www.federalregister.gov/documents/2007/09/27/E7-19155/guidance-for-industry-toxicity-grading-scale-for-healthy-adult-and-adolescent-volunteers-enrolled-in.
- Note de bas de page 11
-
Suwansrinon K, Jaijareonsup W, Wilde H, Benjavongkulchai M, Sriaroon C, Sitprija V. Sex- and age-related differences in rabies immunoglobulin hypersensitivity. Transactions of the Royal Society of Tropical Medicine and Hygiene. 2007;101(2):206-8.
- Note de bas de page 12
-
Rapheal E, Stoddard ST, Anderson KB. Surveying Health-Related Knowledge, Attitudes, and Behaviors of U.S.-Based Residents Traveling Internationally to Visit Friends and Relatives. The American Journal of Tropical Medicine and Hygiene. 2020;103(6):2591-9.
- Note de bas de page 13
-
Ajjan N, Pilet C. Comparative study of the safety and protective value, in pre-exposure use, of rabies vaccine cultivated on human diploid cells (HDCV) and of the new vaccine grown on Vero cells. Vaccine. 1989;7(2):125-8.
- Note de bas de page 14
-
Arora A, Moeller L, Froeschle J. Safety and Immunogenicity of a New Chromatographically Purified Rabies. Journal of Travel Medicine. 2006;11(4):195-200.
- Note de bas de page 15
-
Briggs D. Purified Chick Embryo Cell Culture Rabies Vaccine: interchangeability with Human Diploid Cell Culture Rabies Vaccine and comparison of one versus two-dose post-exposure booster regimen for previously immunized persons. Vaccine. 2000;19(9-10):1055-60.
- Note de bas de page 16
-
Endy TP, Keiser PB, Wang D, Jarman RG, Cibula D, Fang H, et al. Serologic Response of 2 Versus 3 Doses and Intradermal Versus Intramuscular Administration of a Licensed Rabies Vaccine for Preexposure Prophylaxis. The Journal of Infectious Diseases. 2020;221(9):1494-8.
- Note de bas de page 17
-
Quiambao BP, Dimaano EM, Ambas C, Davis R, Banzhoff A, Malerczyk C. Reducing the cost of post-exposure rabies prophylaxis: efficacy of 0.1ml PCEC rabies vaccine administered intradermally using the Thai Red Cross post-exposure regimen in patients severely exposed to laboratory-confirmed rabid animals. Vaccine. 2005;23(14):1709-14.
- Note de bas de page 18
-
Quiambao BP, Ambas C, Diego S, Bosch Castells V, Korejwo J, Petit C, et al. Intradermal post-exposure rabies vaccination with purified Vero cell rabies vaccine: Comparison of a one-week, 4-site regimen versus updated Thai Red Cross regimen in a randomized non-inferiority trial in the Philippines. Vaccine. 2019;37(16):2268-77.
- Note de bas de page 19
-
Quiambao BP, Lim JG, Bosch Castells V, Augard C, Petit C, Bravo C, et al. One-week intramuscular or intradermal pre-exposure prophylaxis with human diploid cell vaccine or Vero cell rabies vaccine, followed by simulated post-exposure prophylaxis at one year: A phase III, open-label, randomized, controlled trial to assess immunogenicity and safety. Vaccine. 2022;40(36):5347-55.
- Note de bas de page 20
-
Mills DJ, Lau CL, Fearnley EJ, Weinstein P. The Immunogenicity of a Modified Intradermal Pre‐exposure Rabies Vaccination Schedule—A Case Series of 420 Travelers. Journal of Travel Medicine. 2011;18(5):327-32.
- Note de bas de page 21
-
Recuenco S, Warnock E, Osinubi MOV, Rupprecht CE. A single center, open label study of intradermal administration of an inactivated purified chick embryo cell culture rabies virus vaccine in adults. Vaccine. 2017;35(34):4315-20.
- Note de bas de page 22
-
Sabchareon A, Lang J, Attanath P, Sirivichayakul C, Pengsaa K, Mener Valentine L, et al. A New Vero Cell Rabies Vaccine: Results of a Comparative Trial with Human Diploid Cell Rabies Vaccine in Children. Clinical Infectious Diseases. 1999;29(1):141-9.
- Note de bas de page 23
-
Soentjens P, Andries P, Aerssens A, Tsoumanis A, Ravinetto R, Heuninckx W, et al. Preexposure Intradermal Rabies Vaccination: A Noninferiority Trial in Healthy Adults on Shortening the Vaccination Schedule From 28 to 7 Days. Clinical Infectious Diseases. 2019;68(4):607-14.
- Note de bas de page 24
-
Suntharasamai P, Chaiprasithikul P, Wasi C, Supanaranond W, Auewarakul P, Chanthavanich P, et al. A simplified and economical intradermal regimen of purified chick embryo cell rabies vaccine for postexposure prophylaxis. Vaccine. 1994;12(6):508-12.
- Note de bas de page 25
-
Hills SL, Fischer M, Biggerstaff BJ. Perceptions among the U.S. population of value of Japanese encephalitis (JE) vaccination for travel to JE-endemic countries. Vaccine. 2020;38(9):2117-21.
- Note de bas de page 26
-
Lindsey N. Value of a vaccine to prevent travel-related chikungunya for US persons [Internet]. Centers for Disease Control and Prevention; 2023 Jun 22. Accessible à l'adresse : https://www.cdc.gov/acip/downloads/slides-2023-06-21-23/02-Chikungunya-Lindsey-508.pdf.(en anglais seulement)
- Note de bas de page 27
-
Stefanopoulos P, Karabouta Z, Bisbinas I, Georgiannos D, Karabouta I. Animal and human bites: evaluation and management. Acta Orthopaedica Belgica. 2004;70(1):1-10.
- Note de bas de page 28
-
Guidelines for the Management of Snakebites. Geneva: World Health Organization; 2018. [consultation le 6 octobre 2025]. Accessible à l'adresse : https://public.ebookcentral.proquest.com/choice/publicfullrecord.aspx?p=5916245.
- Note de bas de page 29
-
Rothe K, Tsokos M, Handrick W. Animal and Human Bite Wounds. Deutsches Ärzteblatt international. 2015;115(25):433-43.
- Note de bas de page 30
-
Gold BS, Dart RC, Barish RA. Bites of Venomous Snakes. New England Journal of Medicine. 2002;347(5):347-56.
- Note de bas de page 31
-
Brook I. Management of Human and Animal Bite Wounds. Advances in Skin & Wound Care. 2005;18(4):197-203.
- Note de bas de page 32
-
Stevens DL, Bisno AL, Chambers HF, Everett ED, Dellinger P, Goldstein EJC, et al. Practice Guidelines for the Diagnosis and Management of Skin and Soft-Tissue Infections. Clinical Infectious Diseases. 2005;41(10):1373-406.
- Note de bas de page 33
-
Stevens DL, Bisno AL, Chambers HF, Dellinger EP, Goldstein EJC, Gorbach SL, et al. Practice Guidelines for the Diagnosis and Management of Skin and Soft Tissue Infections: 2014 Update by the Infectious Diseases Society of America. Clinical Infectious Diseases. 2014;59(2):e10-e52.
- Note de bas de page 34
-
Medeiros IM, Saconato H. Antibiotic prophylaxis for mammalian bites. Cochrane Database of Systematic Reviews. 2001(2).
- Note de bas de page 35
-
Cohen Jeffrey I, Davenport David S, Stewart John A, Deitchman S, Hilliard Julia K, Chapman Louisa E. Recommendations for Prevention of and Therapy for Exposure to B Virus (Cercopithecine Herpesvirus1). Clinical Infectious Diseases. 2002;35(10):1191-203.
- Note de bas de page 36
-
Carrara P, Parola P, Brouqui P, Gautret P. Imported human rabies cases worldwide, 1990-2012. PLoS Neglected Tropical Diseases. 2013;7(5):e2209.
- Note de bas de page 37
-
Medley AM, Millien MF, Blanton JD, Ma X, Augustin P, Crowdis K, et al. Retrospective Cohort Study to Assess the Risk of Rabies in Biting Dogs, 2013(-)2015, Republic of Haiti. Tropical Medicine and Infectious Disease. 2017;2(2).
- Note de bas de page 38
-
Cleaveland S, Fevre EM, Kaare M, Coleman PG. Estimating human rabies mortality in the United Republic of Tanzania from dog bite injuries. Bulletin of the World Health Organization. 2002;80(4):304-10.
- Note de bas de page 39
-
Hampson K, Coudeville L, Lembo T, Sambo M, Kieffer A, Attlan M, et al. Estimating the global burden of endemic canine rabies. PLoS Neglected Tropical Diseases. 2015;9(4):e0003709.
- Note de bas de page 40
-
Dobardzic A, Izurieta H, Woo EJ, Iskander J, Shadomy S, Rupprecht C, et al. Safety review of the purified chick embryo cell rabies vaccine: Data from the Vaccine Adverse Event Reporting System (VAERS), 1997–2005. Vaccine. 2007;25(21):4244-51.
- Note de bas de page 41
-
Moro PL, Lewis P, Cano M. Adverse events following purified chick embryo cell rabies vaccine in the Vaccine Adverse Event Reporting System (VAERS) in the United States, 2006–2016. Travel Medicine and Infectious Disease. 2019;29:80-1.
- Note de bas de page 42
-
Williams M, Moro PL, Woo EJ, Paul W, Lewis P, Petersen BW, et al. Post-Marketing Surveillance of Human Rabies Diploid Cell Vaccine (Imovax) in the Vaccine Adverse Event Reporting System (VAERS) in the United States, 1990‒2015. PLoS Neglected Tropical Diseases. 2016;10(7).