Évaluation - Groupe des cétones
Numéros au registre du Chemical Abstracts Service :
- 78-93-3
- 107-87-9
- 108-10-1
- 110-12-3
- 123-42-2
- 513-86-0
- 123-54-6
- 431-03-8
- 600-14-6
- 141-79-7
Environnement et Changement climatique Canada
Santé Canada
Mai 2026
No de cat. : En84-398/2025F-PDF
ISBN : 978-0-660-79378-8
Résumé
En vertu de l’article 68 de la Loi canadienne sur la protection de l’environnement (1999) (LCPE), les ministres de l’Environnement et de la Santé ont procédé à une évaluation des 10 substances appelées collectivement « groupe des cétones » dans le Plan de gestion des produits chimiques. Le tableau ci-dessous présente le numéro au registre du Chemical Abstracts Service (no CASNote de bas de page 1) de chaque substance, le nom sur la Liste intérieure des substances (LIS) ainsi que le nom commun et l’abréviation, le cas échéant.
| No CAS | Sous-groupe | Nom sur la LIS | Nom commun (abréviation) |
|---|---|---|---|
| 78-93-3 | 1 | Butanone | Méthyl éthyl cétone (MEK) |
| 107-87-9 | 1 | Pentan-2-one | Méthyl propyl cétone (MPK) |
| 108-10-1 | 2 | 4-Méthylpentan-2-one | Méthyl isobutyl cétone (MIBK) |
| 110-12-3 | 2 | 5-Méthylexan-2-one | Méthyl isoamyl cétone (MIAK) |
| 123-42-2 | 2 | 4-Hydroxy-4-méthylpentan-2-one | Alcool de diacétone (DAA) |
| 431-03-8 | 3 | Butanedione | Diacétyle |
| 513-86-0 | 3 | Acétoïne | Acétoïne |
| 600-14-6 | 3 | Pentane-2,3-dione | 2,3-Pentanedione (2,3-PD) |
| 123-54-6 | Distincte | Pentane-2,4-dione | 2,4-Pentanedione (2,4-PD) |
| 141-79-7 | Distincte | 4-Méthylpent-3-én-2-one | Oxyde de mésityle (OM) |
Les 10 substances du groupe des cétones sont produites commercialement, sont présentes à l’état naturel dans l’environnement dans divers végétaux ou différentes denrées alimentaires ou, encore, sont produites par des microbes ou d’autres organismes. Différentes cétones sont aussi produites de manière endogène chez les humains, notamment la MEK, le diacétyle et l’acétoïne. Selon les renseignements déclarés en réponse aux enquêtes menées conformément à l’article 71 de la LCPE, seuls le DAA (23 000 kg) et la 2,3‑PD (1 200 kg) ont été fabriqués au Canada en 2011. En 2011, les quantités importées et déclarées de ces substances du groupe des cétones au Canada se situaient entre 100 kg (pour l’acétoïne) et 6 000 000 kg (pour la MEK). Au cours de la même année, aucune activité de fabrication ou d’importation canadienne dépassant le seuil de déclaration de 100 kg n’a été déclarée pour l’OM.
En général, les cétones sont surtout employées comme solvants dans différents produits, dont des produits de consommation, comme la peinture, les revêtements et les adhésifs, ainsi que dans un grand nombre d’applications industrielles, notamment comme produits chimiques intermédiaires et solvants. Ils peuvent également être utilisés comme aromatisants alimentaires, dans les cosmétiques et les produits de santé naturels, et comme formulants de produits antiparasitaires.
Les risques pour l’environnement associés aux substances du groupe des cétones ont été caractérisés selon l’approche de classification du risque écologique (CRE) des substances organiques, qui est fondée sur le risque, fait appel à plusieurs paramètres de danger et d’exposition et tient compte de multiples éléments de preuve en les pondérant. Les profils de danger sont principalement axés sur des paramètres comme le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne établis en fonction du réseau trophique, la biodisponibilité ainsi que sur l’activité chimique et biologique. Les paramètres pris en compte pour dresser les profils d’exposition sont le débit d’émission, la persistance globale et le potentiel de transport à grande distance. Nous avons utilisé une matrice des risques pour attribuer aux substances un degré de préoccupation potentielle faible, modéré ou élevé en fonction de leurs profils de danger et d’exposition. D’après le résultat de l’analyse de la CRE, il est peu probable que les substances du groupe des cétones causent des effets nocifs pour l’environnement.
Compte tenu de tous les éléments de preuve présentés dans la présente évaluation, la MEK, la MPK, la MIBK, la MIAK, le DAA, le diacétyle, la 2,3-PD, l’acétoïne, la 2,4-PD et l’OM présentent un faible risque de causer des effets nocifs pour l’environnement. Il a été conclu que la MEK, la MPK, la MIBK, la MIAK, le DAA, le diacétyle, l’acétoïne, la 2,3‑PD, la 2,4‑PD et l’OM ne satisfont à aucun des critères énoncés aux alinéas 64a) et 64 b) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
Plusieurs de ces cétones ont déjà fait l’objet d’une évaluation par des instances internationales; ces révisions et évaluations ont servi, dans la présente évaluation, à caractériser les effets sur la santé.
Pour estimer les risques pour la santé humaine, nous avons séparé 8 des substances du groupe des cétones en 3 sous-groupes et avons traité séparément les 2 autres. Concernant les substances du sous-groupe 1 (MEK et MPK), les effets critiques sur la santé comprennent des effets sur le développement pour la MEK, et un ralentissement de la prise de poids corporel pour la MEK et la MPK. La population générale du Canada est exposée à la MEK et à la MPK dans l’air, les aliments (présence d’origine naturelle ou du fait qu’ils sont utilisés comme aromatisants, le cas échéant) et les produits de consommation, y compris les cosmétiques, la peinture et les produits de bricolage. Selon les renseignements à notre disposition, la MEK serait rejetée dans l’air par des activités industrielles. Une comparaison des concentrations de MEK et de MPK présentes dans les milieux environnementaux et les aliments (lorsqu’utilisées comme aromatisants alimentaires) auxquelles la population au Canada peut être exposée avec celles associées aux effets nocifs constatés dans des études en laboratoire a donné lieu à des marges d’exposition considérées comme suffisantes pour compenser les incertitudes dans les données recensées sur l’exposition et les effets sur la santé, et utilisées pour caractériser les risques. Toutefois, les ME calculées par comparaison des concentrations associées à des effets critiques sur la santé avec celles de l’exposition à la MEK présente dans certains produits de consommation, notamment les décapants pour la peinture ou les revêtements (par exemple, les décapants pour la laque), les dissolvants d’adhésifs, les dégraissants, les diluants pour la peinture ou les revêtements, la peinture liquide et divers produits en aérosol, dont la peinture en aérosol, sont considérées comme insuffisantes pour compenser les incertitudes dans les données sur l’exposition et les effets sur la santé utilisées pour caractériser les risques. Considérant la faible toxicité aiguë de la MPK et l’absence d’effet sur le développement de l’exposition par inhalation, la présence de la MPK dans les produits de consommation ne suscite aucune préoccupation.
Concernant les substances du sous-groupe 2 (la MIBK, la MIAK et le DAA), le Centre international de recherche sur le cancer (CIRC) estime que la MIBK se range dans le groupe 2B (« est peut-être cancérogène pour l’Homme »), étant donné les « données probantes suffisantes » de cancérogénicité chez les animaux de laboratoire. Parmi les effets non cancérogènes observés lors d’études en laboratoire, mentionnons des effets sur le foie (MIBK, MIAK) et les reins (MIBK, DAA), ainsi que des effets sur le développement (MIBK, DAA). Au Canada, la population générale peut être exposée à la MIBK, à la MIAK et au DAA dans les milieux environnementaux et les aliments (présence d’origine naturelle ou, dans le cas de la MIBK, découlant de son utilisation comme aromatisant, le cas échéant) et dans des produits de consommation, notamment l’alcool à friction, les cosmétiques, les stylos‑feutres, la peinture et les produits de bricolage. D’après les renseignements, la MIBK serait également rejetée dans l’air par des activités industrielles. Une comparaison des concentrations estimatives de l’exposition à la MIBK, à la MIAK et au DAA dans les milieux environnementaux et de l’exposition à la MIBK dans les aliments (lorsqu’utilisée comme aromatisant alimentaire) avec celles des effets critiques associés a donné lieu à des marges d’exposition considérées comme suffisantes pour compenser les incertitudes dans les données recensées sur l’exposition et les effets sur la santé, et utilisées pour caractériser les risques. L’exposition à la MIBK, à la MIAK et au DAA par les aliments dans lesquels ces substances sont présentes naturellement n’a pas été jugée préoccupante pour la santé humaine. Toutefois, dans le cas de la MIBK, les marges d’exposition résultantes associées à l’utilisation de laques pour le bois, de peinture liquide et de divers produits en aérosol, notamment la peinture en aérosol, sont considérées comme insuffisantes pour compenser les incertitudes dans les données recensées sur l’exposition et les effets sur la santé, et utilisées pour caractériser les risques.
Concernant les substances du sous-groupe 3 (diacétyle, 2,3‑PD et acétoïne), des études de laboratoire ont déterminé que le diacétyle était cancérogène. En ce qui a trait au diacétyle et à la 2,3‑PD, des effets non cancéreux ont également été observés, notamment sur les voies respiratoires. Dans le cas de l’acétoïne, seule une toxicité générale a été observée aux doses élevées. La population générale du Canada est principalement exposée au diacétyle, à la 2,3‑PD et à l’acétoïne par les aliments (leur présence étant d’origine naturelle ou découlant de leur utilisation comme aromatisants, le cas échéant), ainsi qu’à la 2,3‑PD et au diacétyle, employés dans un nombre réduit de produits de consommation, dont les cosmétiques et les assainisseurs d’air, respectivement. Une comparaison des concentrations estimatives de l’exposition au diacétyle, à la 2,3‑PD et à l’acétoïne avec celles associées à des effets critiques a donné lieu à des marges d’exposition considérées comme suffisantes pour compenser les incertitudes dans les données recensées sur l’exposition et les effets sur la santé, et utilisées pour caractériser les risques.
D’après les données accessibles sur les effets de la 2,4‑PD sur la santé, cette substance causerait une toxicité générale et des effets sur le développement. La 2,4‑PD a montré un certain potentiel de génotoxicité, mais elle ne devrait pas être cancérogène. La population générale du Canada pourrait être exposée à la 2,4‑PD en raison de la présence de cette substance dans des milieux environnementaux (air et eau) et de sa présence naturelle dans les aliments. Une comparaison des concentrations estimatives de l’exposition à la 2,4‑PD avec celles associées à des effets critiques a donné lieu à des marges d’exposition considérées comme suffisantes pour compenser les incertitudes dans les données recensées sur l’exposition et les effets sur la santé, et utilisées pour caractériser les risques. Dans l’ébauche du rapport d’évaluation, la 2,4‑PD a été indiquée comme préoccupante pour la santé humaine en raison de sa présence dans un faible nombre de produits de consommation. Une étude plus approfondie a permis de confirmer que la 2,4‑PD n’est pas présente actuellement dans les produits de consommation. Par conséquent, la 2,4‑PD n’est plus considérée comme préoccupante pour la santé humaine aux concentrations d’exposition actuelles. Bien que l’exposition de la population générale à la 2,4‑PD ne soit pas préoccupante aux concentrations d’exposition actuelles, il est possible que les concentrations augmentent à l’avenir. Les effets associés à cette substance pourraient cependant devenir préoccupants pour la santé humaine, si les concentrations d’exposition devaient augmenter.
La population au Canada peut être exposée à l’OM en raison de sa présence dans l’air et dans les aliments (présence d’origine naturelle ou découlant de son utilisation comme aromatisant alimentaire, le cas échéant). L’OM ne devrait être ni cancérogène ni génotoxique. Des études de laboratoire ont permis d’associer une toxicité générale à l’exposition à l’OM. Une comparaison des concentrations estimatives de l’exposition à l’OM dans les milieux environnementaux et les aliments (lorsqu’utilisé comme aromatisant alimentaire) avec celles associées à des effets critiques a donné lieu à des marges qui sont considérées comme suffisantes pour compenser les incertitudes dans les données recensées sur l’exposition et les effets sur la santé, et utilisées pour caractériser les risques.
L’évaluation des effets sur la santé humaine a tenu compte des groupes au sein de la population canadienne qui, parce qu’ils sont plus sensibles ou davantage exposés, peuvent être plus vulnérables aux effets nocifs pour la santé. Par exemple, nous avons estimé les concentrations d’exposition en fonction de l’âge, dont celles de l’exposition des nourrissons et des enfants, et avons examiné les études de toxicité pour le développement et la reproduction afin d’en dégager les effets nocifs sur la santé, le cas échéant. De plus, l’exposition des personnes vivant à proximité d’installations qui produisent des émissions industrielles a également été prise en compte.
À la lumière des renseignements contenus dans la présente évaluation, il a été conclu que la MEK et la MIBK satisfont au critère énoncé à l’alinéa 64c) de la LCPE, car elles pénètrent ou peuvent pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Toutefois, il a été conclu que la MPK, la MIAK, le DAA, le diacétyle, la 2,3‑PD, l’acétoïne, la 2,4‑PD et l’OM ne satisfont pas au critère énoncé à l’alinéa 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Par conséquent, il a été conclu que la MEK et la MIBK satisfont à un ou plusieurs des critères énoncés à l’article 64 de la LCPE, et que la MPK, la MIAK, le DAA, le diacétyle, la 2,3-PD, l’acétoïne, la 2,4-PD et l’OM ne satisfont à aucun des critères énoncés à l’article 64 de la LCPE.
1. Introduction
En vertu de l’article 68 de la Loi canadienne sur la protection de l’environnement (1999) (LCPE) [Canada, 1999], les ministres de l’Environnement et de la Santé ont réalisé une évaluation des 10 substances formant le groupe des cétones, afin de déterminer si ces substances présentent ou peuvent présenter un risque pour l’environnement ou la santé humaine. Les substances de ce groupe ont été jugées prioritaires pour une évaluation, car elles répondaient aux critères de catégorisation ou ont été jugées comme telles selon d’autres mécanismes (ECCC, SC [modifié en 2017]).
Les risques pour l’environnement associés aux substances du groupe des cétones ont été caractérisés à l’aide de l’approche de classification du risque écologique (CRE) des substances organiques (ECCC, 2016a). La CRE décrit le danger associé à une substance à l’aide de paramètres clés comme le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne établis d’après le réseau trophique, la biodisponibilité et l’activité chimique et biologique, et tient compte de l’exposition possible des organismes dans les milieux aquatiques et terrestres en fonction de facteurs tels que le taux d’émissions potentielles, la persistance globale et le potentiel de transport à grande distance dans l’atmosphère. Les divers éléments de preuve ont été combinés afin de cerner les substances justifiant une évaluation plus poussée de leur potentiel de causer des effets nocifs pour l’environnement ou dont la probabilité de causer des effets nocifs pour l’environnement est faible.
Certaines substances sont évaluées en sous-groupes, en raison des similitudes de leur structure chimique, de leurs propriétés et/ou de leur toxicité. Étant donné que ces substances peuvent être utilisées de la même façon et dans des applications similaires, nous avons évalué le potentiel de risque pour la santé humaine en posant des hypothèses d’exposition s’appliquant à l’ensemble du groupe.
Quelques substances du groupe des cétones, examinées dans la présente évaluation, ont fait l’objet d’études internationales par l’Organisation pour la coopération et le développement économiques (OCDE), dans le cadre de son Programme d’évaluation coopérative des produits chimiques, et l’ensemble des données d’évaluation (Screening Information Data Set, ou SIDS) ainsi que les rapports d’évaluation initiale (Initial Assessment Reports, ou SIAR) sont également accessibles. Ces évaluations ont été soumises à une révision rigoureuse (notamment par des pairs) et à des processus d’approbation par des autorités gouvernementales d’autres pays. Santé Canada et Environnement et Changement climatique Canada participent activement à ce processus et considèrent ces évaluations comme fiables. Certaines des substances ont également été évaluées par le Programme international sur la sécurité des substances chimiques (PISSC), l’Environmental Protection Agency des États-Unis (US EPA), le Centre international de recherche sur le cancer (CIRC), l’Agency for Toxic Substances and Disease Registry (ATSDR) et le National Toxicology Program (NTP) des États‑Unis. Les études effectuées par ces institutions ont servi à la caractérisation des effets sur la santé de la présente évaluation.
Le diacétyle, la 2,3-PD et l’acétoïne ont été détectés dans des produits de vapotage (Farsalinos et coll., 2015; Klager et coll., 2017) qui peuvent représenter une source supplémentaire d’exposition à ces substances. Les produits de vapotage (comme les cigarettes électroniques et les dispositifs de vapotage pour produits contenant du cannabis) sont visés par des cadres législatifs distincts. Santé Canada a pris des mesures pour informer l’industrie que les substances présentant un risque connu associé à l’inhalation (par exemple, le diacétyle et la 2,3-PD) ne devraient jamais être ajoutées aux produits de vapotage (Santé Canada [modifié, 2020a,b]). De plus, d’après les analyses continues qu’effectue Santé Canada (dans le cadre du projet de caractérisation ouverte), les dicétones ne sont que rarement détectées dans les produits de vapotage vendus au Canada (communication personnelle, courriel de la Direction de la sécurité des produits de consommation et des produits dangereux [DSPCPD], Santé Canada [SC], au Bureau de l’évaluation des risques pour les substances existantes [BERSE], SC; daté du 3 décembre 2020; source non mentionnée).
La présente évaluation tient compte des propriétés chimiques, du devenir dans l’environnement, des dangers, des utilisations et des expositions aux substances chimiques, y compris d’autres renseignements présentés par les intervenants. Les données pertinentes ont été recensées jusqu’en avril 2017. D’autres données ont été reçues jusqu’en octobre 2019. Les recherches ciblées dans la littérature scientifique ont pris fin en juin 2021. Les conclusions s’appuient sur des données empiriques tirées d’études clés et sur certains résultats issus de modélisations. Lorsqu’elles étaient pertinentes, les données d’évaluations d’autres instances ont été prises en compte.
Le présent rapport d’évaluation a été préparée par le personnel du Programme d’évaluation des risques de la LCPE, à Santé Canada et à Environnement et Changement climatique Canada, et comprend des renseignements provenant d’autres programmes de ces ministères. Les sections du présent rapport d’évaluation portant sur la santé humaine ont fait l’objet d’une révision ou de consultations externes. Les commentaires reçus sur les sections techniques consacrées à la santé humaine ont été formulés par Theresa Lopez, Jennifer Flippin et Joan Garey (TetraTech Inc.) et de D.L. Morgan (National Toxicology Program et National Institute of Environmental Health Sciences, États-Unis). Le volet environnemental de ce rapport repose sur l’approche de CRE (publiée le 30 juillet 2016) et a fait l’objet d’une révision par des pairs et d’une consultation publique de 60 jours. En outre, l’ébauche de ce rapport (publiée le 19 janvier 2019) a fait l’objet d’une consultation publique de 60 jours. Bien que les commentaires externes aient été pris en considération, le contenu final et les résultats de cette évaluation demeurent la responsabilité de Santé Canada et d’Environnement et Changement climatique Canada.
Pour déterminer si les substances répondent aux critères de l’article 64 de la LCPE, nous avons réalisé l’évaluation en nous appuyant principalement sur des données scientifiques essentielles, notamment sur les sous-groupes de la population pouvant être plus sensibles ou davantage exposés, les milieux vulnérables et les effets cumulatifs Note de bas de page 2 et en employant une approche fondée sur le poids de la preuve et le principe de précautionNote de bas de page 3. Dans le présent document, nous présentons les données essentielles et les considérations sur lesquelles reposent les conclusions.
2. Identité des substances
Les 10 substances étudiées dans la présente évaluation sont des cétones, c’est-à-dire qu’elles ont la structure générale montrée à la figure 2-1. Dans la présente évaluation, les cétones ont été divisées en 3 sous-groupes, selon leur structure chimique, leurs propriétés et/ou leur toxicité, et 2 substances sont restées à part.
Figure 2-1. Structure générale des cétones
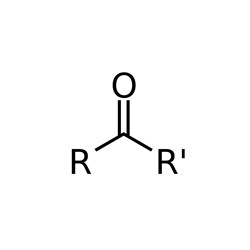
Le tableau 2‑1 présente le numéro au registre du Chemical Abstracts Service (no CASNote de bas de page 1), le nom inscrit sur la Liste intérieure des substances (LIS), ainsi que le nom commun et/ou l’acronyme de chacune des substances du groupe des cétones. Une liste d’autres noms de produits chimiques (par exemple, les noms commerciaux) est offerte par les National Chemical Inventories (NCI, 2015).
| Sous-groupe | No CAS | Nom sur la LIS (nom commun et/ou acronyme) | Structure chimique et formule moléculaire | Masse moléculaire (g/mol) |
|---|---|---|---|---|
| 1 | 78-93-3 | Butanone (méthyl éthyl cétone; MEK) | 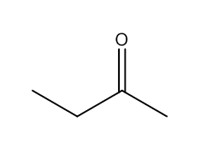 C4H8O |
72,11 |
| 1 | 107-87-9 | Pentan-2-one (méthyl propyl cétone; MPK) | 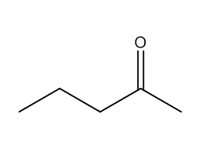 C5H10O |
86,13 |
| 2 | 108-10-1 | 4-Méthylpentan-2-one (méthyl isobutyl cétone; MIBK) | 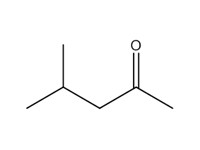 C6H12O |
100,16 |
| 2 | 110-12-3 | 5-Méthylexan-2-one (méthyl isoamyl cétone; MIAK) | 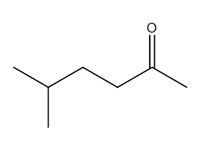 C7H14O |
114,19 |
| 2 | 123-42-2 | 4-Hydroxy-4-méthyl-2-pentanone (alcool de diacétone; DAA) | 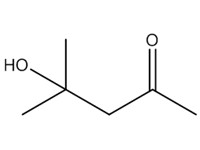 C6H12O2 |
116,16 |
| 3 | 431-03-8 | 2,3-Butanedione (diacétyle) | 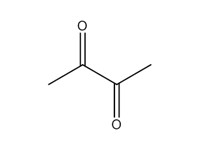 C4H6O2 |
86,09 |
| 3 | 600-14-6 | Pentane-2,3-dione (2,3-PD) | 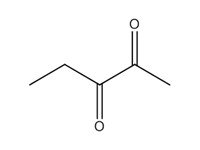 C5H8O2 |
100,12 |
| 3 | 513-86-0 | 3-Hydroxybutan-2-one (acétoïne) | 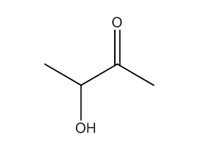 C4H8O2 |
88,11 |
| Distincte | 123-54-6 | Pentane-2,4-dione (2,4-PD) | 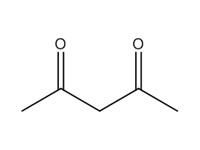 C5H8O2 |
100,12 |
| Distincte | 141-79-7 | 4-Méthylpent-3-én-2-one (oxyde de mésityle; OM) | 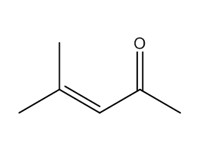 C6H10O |
98,14 |
2.1 Choix des analogues et modèles (Q)SAR utilisés
Une méthode de lecture croisée a été appliquée aux données d’analogues et aux résultats des modèles de relations (quantitatives) structure-activité (QSAR), le cas échéant, pour l’évaluation des substances sur le plan de la santé humaine. Les analogues choisis ont une structure semblable à celle des substances de ce groupe et/ou sont un de leurs métabolites (par exemple, ils sont similaires sur le plan des propriétés physico-chimiques et de la toxicocinétique) et des données empiriques pertinentes pouvant être utilisées dans une lecture croisée en remplacement des substances dont les données empiriques sur les effets sur la santé humaine sont peu nombreuses. L’applicabilité des modèles (Q)SAR a été déterminée au cas par cas. Pour des précisions sur les données obtenues par lecture croisée utilisées afin d’éclairer l’évaluation des effets de chaque sous-groupe et de chaque substance distincte sur la santé humaine, veuillez consulter les sections pertinentes du présent rapport. Le tableau 2‑2 renseigne sur l’identité et la structure chimique des analogues utilisés dans la présente évaluation. Dans certains cas, les substances d’un sous‑groupe ont été utilisées comme analogues pour éclairer l’évaluation de leurs effets sur la santé humaine. Pour de plus amples renseignements sur les propriétés physico‑chimiques et les données sur les effets sur la santé des analogues ainsi que des substances cibles dans cette évaluation de groupe, veuillez consulter l’annexe A.
| Sous-groupe ou substance évalués | No CAS | Nom sur la LIS (nom commun et acronyme) | Structure chimique et formule moléculaire | Masse moléculaire (g/mol) |
|---|---|---|---|---|
| Sous-groupe 1 | 78-92-2 | Butan-2-ol | 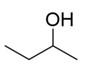 C4H10O |
74,1 |
| OM | 110-93-0 | 5-Heptén-2-one, 6-méthyl- (6-méthyl-5-heptén-2-one; MHE) | 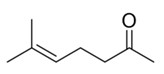 C8H14O |
126,2 |
3. Propriétés physiques et chimiques
Une synthèse des propriétés physiques et chimiques des substances du groupe des cétones est présentée dans les tableaux 3‑1 à 3‑4. Le document d’ECCC de 2016 (2016b) renferme d’autres propriétés physiques et chimiques.
| Propriété | MEK | MPK | Document de référence |
|---|---|---|---|
| État physique | Liquide incolore | Liquide incolore | HSDB, 1983- |
| Point de fusion (°C) | -85,9 | -76,9 | OCDE, 1997a; ChemIDplus, 1993- |
| Pression de vapeur (Pa) | 10 332 | 4 720 | OCDE, 1997a; ChemIDplus, 1993- |
| Constante de la loi d’Henry (Pa·m3/mol) | 5,85 | 8,47 | ATSDR, 2020; ChemIDplus, 1993- |
| Solubilité dans l’eau (mg/L) | 276 000 | 43 000 | OCDE, 1997a; ChemIDplus, 1993- |
| log Koe (sans dimension) | 0,29 | 0,91 | OCDE, 1997a; ChemIDplus, 1993- |
| log Kco (sans dimension) | 0,55 | 1,87 [valeur estimative] | ATSDR, 2020; HSDB, 1983- |
Abréviations : Koe, coefficient de partage octanol-eau; Kco, coefficient de partage carbone organique‑eau
| Propriété | MIBK | MIAK | DAA | Document de référence |
|---|---|---|---|---|
| État physique | Liquide incolore | Liquide incolore, clair | Liquide incolore | OCDE, 1996; HSDB, 1983- |
| Point de fusion (°C) | -84,7 | -74 | -44 | OCDE, 1996; ChemIDplus, 1993- |
| Pression de vapeur (Pa) | 2 653 | 769 | 228 | ChemIDplus, 1993- |
| Constante de la loi d’Henry (Pa·m3/mol) | 14,0 [valeur estimative] | 16,2 [valeur estimative] | 0,026 [valeur estimative] | ChemIDplus, 1993- |
| Solubilité dans l’eau (mg/L) | 19 000 | 5 400 | 1 000 000 | ChemIDplus, 1993- |
| log Koe (sans dimension) | 1,31 | 1,88 | -0,34 [valeur estimative] | ChemIDplus, 1993- |
| log Kco (sans dimension) | 2,08 [valeur estimative] | 2,40 [valeur estimative] | 1,32 [valeur estimative] | HSDB 1983- |
Abréviations : Koe, coefficient de partage octanol-eau; Kco, coefficient de partage carbone organique–eau
| Propriété | Diacétyle | 2,3-PD | Acétoïne | Document de référence |
|---|---|---|---|---|
| État physique | Liquide jaune-verdâtre | Liquide jaune foncé à jaune-verdâtre | Liquide jaunâtre ou cristaux | HSDB, 1983-; CDC, 2016 |
| Point de fusion (°C) | -2,40 | -29,38 [valeur estimative] | 15,0 | ChemIDplus, 1993-; EPI Suite, c2000-2012 |
| Pression de vapeur (Pa) | 7 572 | 4 146 [valeur estimative] | 359 [valeur estimative] | ChemIDplus, 1993- ; EPI Suite, c2000-2012 |
| Constante de la loi d’Henry (Pa·m3/mol) | 1,35 | 0,674 [valeur estimative] | 1,04 [valeur estimative] | ChemIDplus, 1993- ; EPI Suite, c2000-2012 |
| Solubilité dans l’eau (mg/L) | 200 000 | 66 700 (à 15 °C) | 1 000 000 | ChemIDplus, 1993- |
| log Koe (sans dimension) | -1,34 | -0,85 [valeur estimative] | -0,36 [valeur estimative] | ChemIDplus, 1993- |
| log Kco (sans dimension) | -0,28 [valeur estimative] | -0,004 [valeur estimative] | 0,3 [valeur estimative] | EPI Suite, c2000-2012; HSDB, 1983- |
Abréviations : Koe, coefficient de partage octanol-eau; Kco, coefficient de partage carbone organique‑eau
| Propriété | 2,4-PD | OM | Document de référence |
|---|---|---|---|
| État physique | Liquide incolore ou jaunâtre | Liquide huileux, incolore à jaune pâle | HSDB 1983- |
| Point de fusion (°C) | -23,0 | -59,0 | ChemIDplus, 1993- |
| Pression de vapeur (Pa) | 395 | 1 095 | ChemIDplus, 1993- |
| Constante de la loi d’Henry (Pa·m3/mol) | 0,238 [valeur estimative] | 3,72 [valeur estimative] | ChemIDplus, 1993- |
| Solubilité dans l’eau (mg/L) | 166 000 | 28 900 | ChemIDplus, 1993- |
| log Koe (sans dimension) | 0,34-0,4 | 1,2-1,7 | ChemIDplus, 1993-; OCDE, 1997b; OCDE, 2001 |
| log Kco (sans dimension) | 1,54 [valeur estimative] | 1,04 | EPI Suite, c2000-2012; OCDE, 1997b |
Abréviations : Koe, coefficient de partage octanol-eau; Kco, coefficient de partage carbone organique‑eau
4. Sources et utilisations
Les 10 substances du groupe des cétones sont naturellement présentes dans l’environnement, dans différents végétaux ou denrées alimentaires, ou sont produites par des microbes ou d’autres organismes, mais elles peuvent aussi être synthétisées (VCCEP, 2003; Burdock, 2010; O’Donoghue, 2012a,b). La MEK, le diacétyle et l’acétoïne sont également produits de manière endogène chez l’humain (OMS, 1999a; VCCEP, 2003; NTP, 2007a).
Hormis la MEK, toutes les substances du groupe des cétones ont fait l’objet d’une enquête menée en 2011, conformément à l’article 71 de la LCPE (Environnement Canada, 2012). La MEK, elle, a fait l’objet d’une enquête menée en 2001, conformément à l’article 71 de la LCPE. Les quantités fabriquées de MEK déclarées variaient entre 1 et 10 millions de kg en 2000. Toutefois, cette substance a cessé d’être fabriquée au Canada en 2002 (Environnement Canada, 2001). Les quantités importées de MEK au Canada déclarées en 2000 étaient supérieures à 10 millions de kg. Selon la Base de données sur le commerce international de marchandises du Canada (CIMC), entre 2011 et 2016, les importations annuelles moyennes de MEK au Canada étaient d’environ 4,9 millions de kg (CIMC, 2017). Le tableau 4‑1 présente une synthèse des quantités totales fabriquées et importées des substances du groupe des cétones déclarées au Canada.
| Nom commun | Quantité totale fabriquéea (kg) | Quantité totale importéea (kg) |
|---|---|---|
| MEK | n.d. | 6 042 865(données pour 2011; CICM, 2017) |
| MPK | n.d. | 1 097 844 |
| MIBK | n.d. | 1 241 783 |
| MIAK | n.d. | 35 906 |
| Alcool de diacétone | 23 000 | 265 529 |
| Diacétyle | n.d. | 1 430 |
| 2,3-PD | 1 200 | n.d. |
| Acétoïne | n.d. | 100 à 1 000 |
| 2,4-PD | n.d. | 100 000 à 1 000 000 |
| OM | n.d. | n.d. |
Abréviation : n.d. = quantité non déclarée supérieure au seuil de déclaration de 100 kg
a Les valeurs représentent les quantités déclarées en réponse aux enquêtes menées conformément à l’article 71 de la LCPE (Environnement Canada, 2012), à l’exception de celles de la MEK. Voir les enquêtes (annexes 2 et 3) pour connaître les inclusions et les exclusions (Environnement Canada, 2012).
Le tableau 4‑2 présente une synthèse des principales utilisations des substances du groupe des cétones, établie d’après les renseignements recueillis dans le cadre d’enquêtes menées conformément à l’article 71 de la LCPE (Environnement Canada, 2001 et 2013). Le tableau 4‑3 présente d’autres utilisations recensées au Canada.
| Principales utilisations | Sous-groupe 1a | Sous-groupe 2 | Sous-groupe 3 | Distincte |
|---|---|---|---|---|
| Peinture et revêtements | MEK, MPK | MIBK, MIAK, DAA | s.o. | 2,4-PD |
| Aliments et boissons | s.o. | s.o. | 2,3-PD, acétoïne | s.o. |
| Produits, mélanges ou articles manufacturés pour l’agriculture (autres que les pesticides) | MEK | s.o. | Diacétyle | s.o. |
| Adhésifs et produits d’étanchéité | MEK, MPK | MIBK, DAA | s.o. | 2,4-PD |
| Encres, encres en poudre et colorants | MEK, MPK | MIBK, DAA | s.o. | s.o. |
| Automobiles, aéronefs et transports | MEK, MPK | MIBK, DAA | s.o. | s.o. |
| Matériaux en plastique et en caoutchouc non mentionnés ailleurs | s.o. | MIBK | s.o. | 2,4-PD |
| Électricité et électronique | s.o. | MIBK, DAA | s.o. | s.o. |
| Revêtements de sol | MEK | MIBK | s.o. | s.o. |
| Nettoyage et entretien du mobilier | MEK | Alcool de diacétone | s.o. | s.o. |
| Produits de soins personnels | s.o. | Alcool de diacétone | 2,3-PD, acétoïne | s.o. |
| Jouets, terrains de jeux et articles de sport | s.o. | Alcool de diacétone | s.o. | s.o. |
| Autresb | MEK, MPK | MIBK, DAA | Diacétyle | s.o. |
Abréviation : s. o., sans objet
a Utilisations non confidentielles déclarées en réponse à une enquête menée conformément à l’article 71 de la LCPE (Environnement Canada, 2012). Voir l’enquête (annexes 2 et 3) pour connaître les inclusions et les exclusions. Les résultats concernant la MEK proviennent des données d’utilisation déclarées en 2000 et pourraient ne plus être pertinents.
b « Autres » désigne les utilisations mineures ou les utilisations qui ne peuvent pas être divulguées en raison de demandes de confidentialité.
| Utilisation | Sous-groupe 1 | Sous-groupe 2 | Sous-groupe 3 | Distincte |
|---|---|---|---|---|
| Additif alimentairea | MEK | N | N | N |
| Aromatisant alimentairea | MEK, MPK | MIBK | Diacétyle, acétoïne, 2,3-PD | OM |
| Matériau d’emballage alimentairea | MEK, MPK | MIBK, DAA | N | 2,4-PD |
| Additif indirecta | MEK | N | N | N |
| Base de données sur les ingrédients des produits de santé naturelsb | MEK, MPK | MIBK, DAA | Diacétyle, acétoïne, 2,3-PD | OM |
| Base de données des produits de santé naturels homologués en tant qu’ingrédients non médicinaux dans des produits de santé naturels au Canadac | MEK | MIBK | N | N |
| Présence signalée dans les cosmétiques, selon les déclarations faites à Santé Canada en vertu du Règlement sur les cosmétiquesd | MEK, MPK | MIBK, DAA | Diacétyle | N |
| Produit de formulation de produits antiparasitaires homologués au Canadae | MPK | MIBK, MIAK, DAA | Diacétyle, acétoïne, 2,3-PD | N |
Abréviation : N = non, utilisation non déclarée pour cette substance
a Communication personnelle; courriel de la Direction des aliments (DA), SC, adressé au BERSE, SC; daté du 18 août 2016; source non mentionnée
b BDIPSN (modifiée en 2022)
c BDPSNH (modifiée en 2021)
d Communication personnelle; courriels du DSPCPD, SC, adressés au BERSE, SC, et datés d’août 2016 et de novembre 2019; source non mentionnée
e Communication personnelle; courriel de l’Agence de réglementation de la lutte antiparasitaire (ARLA), SC, adressé au BERSE, SC; daté du 28 juillet 2016; source non mentionnée
En général, on utilise surtout les cétones comme solvants dans différents produits, dont des produits de consommation, et dans de nombreuses applications industrielles, notamment comme produits chimiques intermédiaires et solvants (Braithwaite, 2000; O’Donoghue, 2012a,b). La MEK est inscrite dans la Liste des solvants de support ou d’extraction autorisés de Santé Canada comme additif alimentaire autorisé dans les extraits naturels et les extraits d’épices, liste qui est incorporée par renvoi dans l’autorisation de mise en marché accordée conformément à la Loi sur les aliments et drogues. La MEK, la MPK, la MIBK, le DAA et la 2,4-PD peuvent être ajoutés comme composants dans la fabrication de matériaux d’emballage alimentaire qui n’entrent pas en contact direct avec les aliments au Canada. La MEK peut être utilisée comme composant d’additifs indirectsNote de bas de page 4 (nettoyants) dans les établissements de transformation alimentaire où elle est sans contact direct avec les aliments. Aucune donnée de référence n’a été trouvée concernant l’utilisation de MEK, de MPK, de MIBK, de diacétyle, d’acétoïne, de 2,3-PD et d’OM comme aromatisants alimentaires au Canada. Toutefois, comme ces substances sont utilisées comme aromatisants alimentaires aux États‑Unis et en Europe, il est possible qu’elles soient présentes comme aromatisants dans des aliments vendus au Canada (communication personnelle, courriel de la Direction des aliments, SC, adressé au BERSE, SC; daté du 18 août 2016; source non mentionnée).
La MEK est figure dans la ligne directrice sur les solvants résiduels (Q3C[R8]) de l’International Council for Harmonization (ICH) parmi les solvants de catégorie 3, soit comme solvant à faible potentiel toxique dont l’utilisation devrait être limitée grâce à l’application de bonnes pratiques de fabrication ou à d’autres exigences en matière de qualité. Elle est considérée comme acceptable sans justification lorsqu’elle est en quantités ne dépassant pas 50 mg/j (ce qui correspond à 5 000 ppm ou 0,5 %, si l’on suppose une masse de produit de 10 g administrée quotidiennement). La MIBK est inscrite dans une ligne directrice de l’ICH parmi les solvants de catégorie 2, soit comme solvant dont l’emploi devrait être limité, et est également associée à une exposition journalière admissible (EJA) pouvant atteindre 45 mg/j (ce qui correspond à 4 500 ppm ou 0,45 %, si l’on suppose une masse de produit de 10 g administrée quotidiennement) (communication personnelle, courriel de la Direction des produits biologiques et des thérapies génétiques, SC, adressé au BERSE, SC; daté du 15 juillet 2012; source non mentionnée).
La MEK est inscrite dans la Base de données sur les ingrédients de produits de santé naturels (BDIPSN) comme ayant un rôle médicinal et comme substance de produit de santé naturel (PSN), et est visée par l’article 2 (isolat) de l’annexe 1 du Règlement sur les produits de santé naturels. Elle a aussi un rôle non médicinal pour une utilisation topique comme agent dénaturant (jusqu’à 1 %) ou une utilisation par voie orale comme exhausteur de goût (jusqu’à 28,76 ppm). Dans la BDIPSN, on indique également que la MEK est soumise à d’autres exigences réglementaires, conformément au Règlement sur les précurseurs, puisqu’elle figure à l’annexe VI de la Loi réglementant certaines drogues et autres substances. La MPK, la 2,3-PD et l’OM sont énumérés dans la BDIPSN comme substances ayant un rôle non médicinal, pour une utilisation par voie orale, comme exhausteurs de goût. La MIBK y figure comme substance ayant un rôle non médicinal, pour une utilisation par voie orale, comme exhausteur de goût (jusqu’à 25 ppm) ou par voie topique, comme agent dénaturant (jusqu’à 4 %). Le DAA est inscrit comme substance ayant un rôle non médicinal, pour une utilisation topique seulement, comme ingrédient de parfum ou solvant. Finalement, l’acétoïne figure comme substance ayant un rôle non médicinal, pour une utilisation par voie orale, comme exhausteur de goût ou par voie topique, comme ingrédient de parfum. Dans la BDIPSN, la MIBK est également associée à une exposition journalière admissible comme résidu de solvant pouvant atteindre 45 mg/j, ce qui équivaut à une limite de concentration de 4 500 ppm, si l’on suppose une masse de produit de 10 g administrée quotidiennement, et l’on précise en outre que cette limite s’applique quelles que soient les formes posologiques et les voies d’administration. Seules la MEK et la MIBK sont inscrites dans la Base de données des produits de santé naturels homologués (BDPSNH) en tant qu’ingrédients non médicinaux présents dans un nombre limité de PSN à utilisation topique actuellement homologués au Canada (BDIPSN [modifiée en 2022]; BDPSNH [modifiée en 2021]; communication personnelle, courriel de la Direction des produits de santé naturels et sans ordonnance [DPSNSO], SC, au BERSE, SC; daté du 16 août 2016; source non mentionnée).
Selon les déclarations faites à Santé Canada en vertu du Règlement sur les cosmétiques, la MEK, la MPK, la MIBK, le DAA et le diacétyle sont utilisés dans certains produits cosmétiques au Canada, principalement dans les produits de soins pour les ongles (communication personnelle, courriels de la DSPCPD, SC, adressés au BERSE, SC, datés d’août 2016, de novembre 2019 et d’avril 2020; source non mentionnée). D’après des sources accessibles au public (renseignements publiés sur les sites Web de détaillants), le diacétyle serait présent dans d’autres cosmétiques au Canada. La MEK, la MPK, la MIBK, la MIAK et le DAA sont utilisés dans des produits de consommation, dont la peinture et des revêtements liquides et en aérosol, des produits d’entretien automobile, des produits de bricolage comme les décapants pour peinture, les adhésifs et la pâte d’étanchéité pour tuyaux) (Environnement Canada, 2012; CPID [modifié en 2019]; SDS, 2008, 2011, 2012a,b,c, 2013, 2014a,b, 2015a,b,c,d, 2016a,b,c,d, 2017a,b, 2018a,b,c, 2019a,b,c,d,e,f,g). Des scientifiques du Conseil national de recherches du Canada ont décelé de la MEK, de la MPK et de la MIBK, au Canada, dans les émissions de différents matériaux de construction (par exemple, bois, tapis et moquettes, produits isolants) et produits de consommation (par exemple, peinture, nettoyants pour automobile, calfeutrant) (Won et Lusztyk, 2011; Won et Yang, 2012; Won et coll., 2013, 2014, 2015).
Au Danemark, la MEK a été décelée dans plusieurs produits destinés aux enfants, dont des tentes et des tunnels (Hanson et coll., 2004), des jouets à base de glu (slime) (Svendsen et coll., 2005), des figurines en caoutchouc et des marqueurs de vitesse (Glensvig et Ports, 2006). Selon le Children’s Product Safety Act du département de l’Environnement de l’État de Washington (WSDE, 2020), la MEK a été décelée dans plusieurs produits destinés aux enfants de 12 ans et moins, y compris dans le matériel de bricolage, les meubles pour bébés, les bavettes, les sucettes, les anneaux de dentition, les jouets et les jeux pour enfants, la literie et les vêtements pour bébés et enfants, les chaussures et le matériel de camping (WSDE, 2020). La MEK se trouvait principalement dans ces produits par contamination, mais elle était également présente comme adhésif, liant, colorant, pigment, teinture, encre, composant d’un procédé de fabrication de plastiques, de résines ou de polymères, agent de durcissement, additif de fabrication, agent de conservation, enduit protecteur, agent de renforcement et solvant (WSDE, 2020). Au Danemark, la MEK a également été quantifiée dans des produits de soins des animaux (Nylén et coll., 2004) et des jouets pour adultes (Nilsson et coll., 2006).
Les autres sources de ces cétones comprennent les gaz d’échappement des véhicules (MEK, diacétyle) (PISSC, 1993), la poudrette de pneus en caoutchouc ainsi que le gazon synthétique fabriqué avec de la poudrette de pneus en caoutchouc (MIBK) (US EPA et CDC/ATSDR, 2019), la fumée de cigarette (MEK, diacétyle, 2,3-PD) et les liquides aromatisés pour cigarettes électroniques (diacétyle, 2,3-PD, acétoïne). (communication personnelle, courriels de la Direction de la lutte contre le tabagisme, SC, adressés au BERSE, SC, datés du 15 au 18 août 2016 et du 16 novembre 2017; source non mentionnée). Les renseignements reçus dans le cadre de la consultation publique sur l’ébauche du rapport d’évaluation ont révélé d’autres sources de ces cétones, dont des utilisations en laboratoire (MEK, DAA) et leur utilisation dans l’assemblage des fibres optiques (MIBK), ainsi que dans l’encre utilisée pour marquer les composants internes d’appareils électroniques (par exemple, blocs d’alimentation électrique, inducteurs, lecteurs) (MEK).
Deux des 10 cétones, soit la MEK et la MIBK, sont des substances à déclaration obligatoire en vertu de l’Inventaire national des rejets de polluants (INRP). Le tableau 4‑4 présente une synthèse des données sur les quantités rejetées et éliminées, de 2011 à 2019 (INRP, 2011-2017a,b, 2021).
| Substance | Rejet sur place, dans l’atmosphèrea,b | Rejet sur place, dans l’eaua,b | Rejet sur place, dans le sola,b | Élimination sur placea,b | Élimination hors sitea,b | Recyclage hors sitea,b |
|---|---|---|---|---|---|---|
| MEK | 720 à 1 380 | 5,4 à 20 | 0 à 2 | 0,802 à 67 | 90 à 1 563 | 1 441 à 3 074 |
| MIBK | 164 à 242 | 0,02 à 1,9 | 0 à 0,049 | 1,3 à 32 | 23 à 318 | 243 à 323 |
a Les données figurant dans ce tableau étaient à jour le 22 juin 2021. Les installations peuvent en tout temps mettre à jour leurs déclarations à l’INRP. Par conséquent, une analyse similaire effectuée avec différentes versions des données peut produire des résultats différents (INRP, 2021).
b Fourchette des installations qui atteignent les seuils de déclaration de l’INRP. Les valeurs sont arrondies à la tonne près.
5. Devenir et comportement dans l’environnement
5.1 Persistance dans l’environnement
D’après les modèles utilisés dans l’approche de CRE (ECCC, 2016 b), la MEK, le DAA, le diacétyle, la 2,3-PD, la 2-4-PD et l’OM devraient persister dans l’air, mais pas dans l’eau, les sédiments et le sol. Cependant, les renseignements sur la tautomérisation de la 2,4-PD indiquent que sa forme énolique devrait être plus abondante que sa forme cétonique dans l’air (Spencer et coll., 1982; Folkendt et coll., 1985). De plus, les calculs des demi-vies, à l’aide de plusieurs constantes de vitesse empiriques publiées (Holloway et coll., 2005; Zhou et coll., 2008; Messaadia et coll., 2015) et des résultats du modèle AOPWIN (Atmospheric Oxidation Program for Microsoft Windows, 2010), semblent indiquer qu’il est peu probable que la 2,4-PD soit persistante dans l’air.
La MPK, la MIBK, la MIAK et l’acétoïne ne devraient pas être persistantes dans l’air, l’eau, les sédiments et le sol, selon les modèles utilisés dans l’approche de CRE (ECCC, 2016b).
5.2 Potentiel de bioaccumulation
En raison des faibles valeurs de leur log Koe et de leurs facteurs de bioconcentration (ECCC, 2016b), la MEK, la MIAK, le diacétyle, l’acétoïne, la 2,3-PD, la 2,4-PD et l’OM ne devraient pas s’accumuler de façon importante dans les organismes. Bien que les valeurs de log Koe de la MPK et de la MIBK soient élevées, les facteurs de bioconcentration de ces substances sont faibles (1,4 et 2 L/kg, respectivement). Par conséquent, ces substances ne devraient pas s’accumuler de façon considérable dans les organismes (ECCC, 2016b).
6. Potentiel de causer des effets nocifs pour l’environnement
6.1 Caractérisation des risques pour l’environnement
Les risques pour l’environnement associés aux substances du groupe des cétones ont été caractérisés selon l’approche de CRE (ECCC, 2016a). La CRE est une méthode fondée sur les risques qui tient compte de plusieurs paramètres liés au danger et à l’exposition et qui pondère plusieurs éléments de preuve pour classer les risques. Elle associe les divers éléments de preuve de façon à distinguer les substances plus ou moins dangereuses et leurs potentiels d’exposition plus ou moins élevés dans divers milieux. Cela permet de réduire l’incertitude globale liée à la caractérisation des risques, contrairement à une approche reposant sur un seul paramètre mesuré dans un seul milieu (par exemple, la concentration létale médiane). La démarche, qui est décrite en détail par ECCC (2016a), est résumée ci-dessous.
Les propriétés physiques et chimiques ainsi que les données sur le devenir (demi-vies chimiques dans divers milieux et biotes, coefficients de partage et bioconcentration dans les poissons), l’écotoxicité aiguë pour les poissons et les volumes des substances importées et fabriquées au Canada ont été extraites de publications scientifiques, de bases de données empiriques actuellement en usage (par exemple, la boîte à outils [Q]SAR de l’OCDE, 2014) et de réponses aux enquêtes menées conformément à l’article 71 de la LCPE, ou ont été produites à l’aide de certains modèles (Q)SAR ou modèles du devenir du bilan massique et de la bioaccumulation. Ces données ont été utilisées comme intrants dans d’autres modèles de bilan massique ou pour compléter les profils d’exposition et de danger des substances.
Les profils de danger reposent principalement sur des paramètres tels que le mode d’action toxique, la réactivité chimique, les seuils de toxicité interne établis d’après le réseau trophique, la biodisponibilité et l’activité chimique et biologique. Les profils d’exposition étaient également fondés sur plusieurs paramètres, dont les taux d’émission potentielle, la persistance globale et le potentiel de transport à grande distance. Les profils de danger et d’exposition ont été comparés aux critères de décision afin de catégoriser les potentiels de danger et d’exposition de chaque substance comme étant faibles, moyens ou élevés. D’autres règles (par exemple, cohérence du classement et marge d’exposition) ont été appliquées pour préciser les classements préliminaires du danger et de l’exposition.
Une matrice de risques a été utilisée pour attribuer à chaque substance un risque faible, modéré ou élevé, le cas échéant, en fonction du classement de ses profils de danger et d’exposition. Les classements du risque obtenus par l’approche de CRE ont été vérifiés au moyen d’une méthode en 2 étapes. La première étape a consisté à modifier à la baisse le classement des risques (qui sont passés de modérés ou élevés, à faibles) des substances présentant un taux d’émission estimatif faible dans l’eau après le traitement des eaux usées, ce qui représente un potentiel d’exposition faible. La deuxième étape a servi à réévaluer un classement de risque faible dans les scénarios de risques relativement prudents, à échelle locale (soit dans la zone proche du point de rejet), conçus pour protéger l’environnement, afin de déterminer s’il faudrait hausser le classement du risque, le cas échéant.
La CRE est une approche pondérée qui vise à réduire au minimum le potentiel de surclasser ou de sous-classer le danger et l’exposition, ainsi que du risque en découlant. Les approches équilibrées pour compenser les incertitudes sont décrites en plus amples détails dans le document d’ECCC 2016a. 2 des plus importants domaines d’incertitudes sont décrits ci-dessous. Les valeurs empiriques ou modélisées erronées de toxicité aiguë pourraient entraîner un changement dans le classement du danger, plus particulièrement lorsque les paramètres reposent sur les valeurs de résidus dans les tissus (par exemple, le mode d’action toxique), dont un grand nombre sont prédites par modélisation (Q)SAR (OCDE, Boîte à outils QSAR, 2014). Cependant, l’impact de ces erreurs est atténué par le fait qu’une surestimation de la létalité médiane se traduira par une valeur prudente (protectrice) relative aux résidus présents dans les tissus, utilisée dans l’analyse des résidus corporels critiques. L’erreur (sous-estimation) sur la valeur de la toxicité aiguë sera atténuée par le recours à d’autres paramètres de danger comme le profilage structural du mode d’action, la réactivité ou l’affinité de liaison à l’œstrogène. Comme la classification de l’exposition et du risque est très sensible au taux d’émission et à la quantité utilisée, les modifications ou les erreurs relatives à la quantité de la substance chimique pourraient se traduire par des classements différents de l’exposition. Les classements obtenus au moyen de la CRE représentent donc l’exposition et le risque au Canada, établis d’après les quantités estimatives actuellement utilisées, mais ils pourraient ne refléter les tendances futures.
En outre, il convient de noter que, dans la présente évaluation, l’évaluation du potentiel à causer des effets nocifs pour l’environnement a porté sur chaque substance séparément. Si l’exposition à plusieurs substances est concomitante, cela pourrait se solder par des effets cumulatifs sur les organismes et présenter un risque plus élevé. Le potentiel de causer des effets cumulatifs et la manière dont ces effets peuvent se manifester dans l’environnement n’ont pas été examinés plus en profondeur puisque ces substances affichent un faible risque écologique lors de la classification selon l’approche CRE, en considérant l’exposition et les dangers écologiques.
Le document d’ECCC de 2016 en référence (2016b) présente les données essentielles et les facteurs à considérer pour déterminer les profils propres à chaque substance du groupe des cétones, ainsi que les résultats de la classification du danger, de l’exposition et du risque.
Les classements du danger et de l’exposition des substances du groupe des cétones sont présentés en synthèse au tableau 6‑1.
| Substance | Classement du danger selon la CRE | Classement de l’exposition selon la CRE | Classement du risque selon la CRE |
|---|---|---|---|
| MEKa | Faible | Élevé | Faible |
| MPK | Faible | Faible | Faible |
| MIBKa | Faible | Faible | Faible |
| MIAK | Faible | Faible | Faible |
| DAA | Faible | Élevé | Faible |
| Diacétyle | Faible | Faible | Faible |
| Acétoïne | Faible | Faible | Faible |
| 2,3-PD | Faible | Faible | Faible |
| 2,4-PD | Faible | Faible | Faible |
| OM | Faible | Faible | Faible |
a Des données sur la concentration de ces substances dans l’air provenant du programme du Réseau national de surveillance de la pollution atmosphérique (RNSPA) sont accessibles et ont été prises en compte, mais elles n’ont eu aucune incidence sur le classement pour l’environnement (voir les sections 6.1.1 et 6.2.1 pour consulter les données du RNSPA sur la MEK et la MIBK, respectivement).
Comme le classement du danger et de l’exposition de la MPK, de la MIBK, de la MIAK, du diacétyle, de l’acétoïne, de la 2,3-PD, de la 2,4-PD et de l’OM est faible, selon les données prises en compte dans la CRE, leur potentiel de risque pour l’environnement est faible. Il est donc peu probable que ces substances suscitent des préoccupations pour l’environnement au Canada.
D’après les données prises en compte dans la CRE, les potentiels d’exposition de la MEK et du DAA sont élevés, étant donné les quantités utilisées élevées, déclarées en réponse à une enquête menée conformément à l’article 71 de la LCPE (Environnement Canada, 2013), en concomitance avec une longue demi-vie critique dans l’air. Les potentiels de danger et de risque pour l’environnement de la MEK et du DAA ont été classés faibles. Il est donc peu probable que ces substances suscitent des préoccupations pour l’environnement au Canada.
7. Potentiel de causer des effets nocifs pour la santé humaine
7.1 Évaluation des substances du sous-groupe 1 (MEK, MPK)
7.1.1 Évaluation de l’exposition aux substances du sous-groupe 1 (MEK, MPK)
Milieux environnementaux
La MEK a été suivie par le programme du RNSPA (ECCC, 2017a). Les concentrations de cette substance dans l’air ambiant ont été mesurées dans 56 stations de surveillance du RNSPA dans l’ensemble du Canada, de 2006 à 2010. Pendant cette période, ses concentrations moyennes et au 95e centile mesurées sur 24 heures aux diverses stations variaient respectivement de 0,20 à 5,7 µg/m3 et de 0,53 à 19,3 µg/m3 (ECCC, 2017a). Les données obtenues du Hamilton Air Monitoring Network (HAMN), en Ontario, indiquent que les concentrations de MEK mesurées dans l’air ambiant pendant diverses périodes de 12 jours, entre 2015 et 2019, à 3 endroits différents du secteur industriel de Hamilton, variaient d’une valeur inférieure au seuil de détection fiable, soit de 0,295 µg/m3, à un maximum de 31,5 µg/m3. Les concentrations moyennes à ces endroits variaient de 1,19 à 6,11 µg/m3 (HAMN, 2020).
Les concentrations de MEK et de MPK dans l’air extérieur ont aussi été mesurées dans 5 études canadiennes sur la qualité de l’air menées à Windsor, Regina, Edmonton et Ottawa (Zhu et coll., 2005; Santé Canada, 2010a,b, 2012, 2013). Dans ces études, les concentrations des échantillons d’air extérieur mesurées près des habitations (par exemple, dans les arrière-cours) ont été ajoutées dans la composante de l’air intérieur des études décrites plus en détail ci-dessous.
Les concentrations de MEK dans l’air ambiant mesurées dans ces études canadiennes variaient d’une valeur inférieure à 0,03 à 39,06 µg/m3, tandis que les concentrations géométriques moyennes et au 95e centile variaient de 0,41 à 1,77 µg/m3 et de 0,78 à 5,53 µg/m3, respectivement (Zhu et coll., 2005; Santé Canada, 2010a,b, 2012, 2013). Les concentrations de MPK dans l’air ambiant, mesurées dans les 5 études canadiennes, variaient de 0,002 à 14,38 µg/m3, tandis que les concentrations géométriques moyennes et au 95e centile variaient de 0,055 à 0,49 µg/m3 et de 0,22 à 1,25 µg/m3 (Santé Canada, 2010a,b, 2012, 2013). La concentration maximale de 31,5 µg/m3 pour la MEK du HAMN et la concentration au 95e centile de 1,25 µg/m3 pour la MPK de l’étude de Regina ont été utilisées de façon prudente pour estimer les concentrations d’exposition, de la population générale au Canada, à la MEK et à la MPK dans l’air extérieur.
Comme la MEK peut être utilisée par les installations et que ses rejets dans l’atmosphère au Canada sont déclarés à l’INRP (voir la section 4), le modèle SCREEN3 de l’EPA des États-Unis a été employé pour estimer les concentrations d’exposition, le cas échéant, des personnes vivant à proximité d’installations qui rejettent de la MEK dans l’air ambiant. Les concentrations obtenues par modélisation sont présentées dans le tableau 7‑1, et les paramètres d’entrée du modèle, à l’annexe B. La concentration annuelle estimative la plus élevée de MEK dans l’air ambiant (406 µg/m3) a servi à estimer les valeurs maximales des concentrations d’exposition, le cas échéant, des résidants vivant à proximité d’installations rejetant de la MEK dans l’atmosphère.
| Paramètre d’exposition | Concentration de MEK (µg/m3) |
|---|---|
| Concentration maximale sur une heure | 142 à 2 029 |
| Concentration maximale sur 24 heuresa | 57 à 812 |
| Concentration annuelleb | 28 à 406 |
a En supposant que la substance soit rejetée de façon continue sur une période de 24 heures et en tenant compte des variations dans la direction du vent pendant cette période, on estime la concentration maximale moyenne sur 24 heures en multipliant la concentration maximale sur une heure par un facteur de 0,4 (US EPA, 1992).
b Pour ce qui est de l’exposition sur une période d’un an, on peut s’attendre à ce que, avec les variations de direction du vent, les concentrations atmosphériques de la substance dans une source de rejet diffuse ne puissent pas varier autant que celles mesurées dans une source de rejet ponctuelle. Les conditions météorologiques donnant lieu à une exposition maximale sur 1 heure peuvent persister plus longtemps. Ainsi, on détermine la concentration maximale sur 1 an en multipliant la concentration maximale sur 1 heure par un facteur de 0,2 (US EPA, 1992).
Les concentrations de MEK et de MPK ont été mesurées dans l’étude nationale sur la qualité de l’air intérieur du Canada, menée de 2009 à 2011 dans le cadre du cycle 2 de l’Enquête canadienne sur les mesures de la santé (ECMS). La MEK a été détectée dans 99 % des échantillons avec une concentration géométrique moyenne de 1,14 µg/m3 (données pondérées à l’échelle du foyer) et une concentration au 95e centile de 9,76 µg/m3. La MPK a été détectée dans 97 % des échantillons avec une concentration géométrique moyenne (données pondérées à l’échelle du foyer) de 0,36 µg/m3 et une concentration au 95e centile de 1,58 µg/m3 (Zhu et coll., 2013). Dans le cycle 3 de l’ECMS (2012-2013), les concentrations de MEK et de MPK observées dans l’air intérieur étaient similaires (Li et coll., 2019).
Les concentrations de MEK et de MPK dans l’air intérieur ont également été mesurées dans les 5 mêmes études canadiennes mentionnées ci-dessus. Les substances ont été mesurées dans l’air intérieur de la salle familiale ou de la salle de séjour de certains foyers. Entre 45 et 48 foyers de participants non-fumeurs à Windsor ont fait l’objet d’un suivi de janvier 2005 à août 2006, et des échantillons ont été prélevés toutes les 24 heures pendant 5 jours consécutifs (Santé Canada, 2010a). Dans l’étude de Regina, 146 foyers en tout, dont 34 comptaient au moins un participant fumeur, ont été suivis en 2007, en hiver et en été, un échantillon sur 24 heures et un échantillon sur 5 jours ayant été prélevés dans chaque foyer (Santé Canada, 2010b). En 2009, dans l’étude d’Halifax, 50 maisons sans fumée ont été suivies, en hiver et en été, les échantillons ayant été prélevés toutes les 24 heures pendant 7 jours consécutifs (Santé Canada, 2012). En 2010, dans l’étude menée à Edmonton, 50 foyers ont été suivis, en hiver et en été, les échantillons ayant été prélevés toutes les 24 heures pendant 7 jours consécutifs. À l’hiver 2002-2003, dans l’étude d’Ottawa, 75 foyers, dont 10 comptaient des occupants qui fumaient à l’intérieur, ont été suivis, et des échantillons de 10 L d’air, à raison d’un débit de 100 mL/min, ont été prélevés pendant 100 minutes (Zhu et coll., 2005). Les concentrations géométriques moyennes de MEK dans l’air intérieur variaient de 1,14 à 9,81 µg/m3, et les concentrations au 95e centile, de 9,9 à 51,63 µg/m3 (Zhu et coll., 2005; Santé Canada, 2010a,b, 2012, 2013). Les concentrations géométriques moyennes de MPK dans l’air intérieur variaient de 0,089 à 2,77 µg/m3 et les concentrations au 95e centile variaient de 1,34 à 12,77 µg/m3 (Santé Canada, 2010a,b, 2012, 2013).
La concentration de MEK a également été mesurée dans les 36 échantillons d’air intérieur prélevés lors d’une étude sur le terrain à Ottawa, et la concentration maximale obtenue était de 92,6 µg/m3 (Won et coll., 2019). La MEK a également été mesurée dans 81 % des 54 échantillons d’air intérieur provenant d’une étude sur le terrain au Nunavik, et la concentration maximale obtenue était de 14,9 µg/m3 (Won et coll., 2019).
Par prudence, les concentrations au 95e centile les plus élevées de MEK et de MPK obtenues dans l’ensemble des études sur la qualité de l’air intérieur ont été utilisées pour estimer les concentrations d’exposition de la population générale (92,6 µg/m3 pour la MEK dans l’étude sur le terrain d’Ottawa et 12,77 µg/m3 pour la MPK dans l’étude de Regina).
Les concentrations de MEK et la MPK ont également été mesurées dans l’air de la zone respiratoire dans l’étude sur la qualité de l’air menée à Windsor, en Ontario (Santé Canada, 2010a). Dans l’étude de 2005, des échantillons d’air de la zone respiratoire ont été prélevés toutes les 24 heures pendant 5 jours consécutifs. Les mesures de concentration des échantillons d’air de la zone respiratoire tiennent compte des concentrations de l’exposition à la MEK dans l’air intérieur et l’air extérieur à divers endroits, y compris à domicile, au bureau et pendant les déplacements. Les concentrations géométrique moyenne et au 95e centile de MEK dans les échantillons prélevés en été étaient respectivement de 8,79 µg/m3 et de 28,22 µg/m3, ce qui est plus élevé que celles des échantillons prélevés pendant l’hiver (concentration géométrique moyenne de 4,24 µg/m3 et concentration au 95e centile de 11,44 µg/m3). La concentration géométrique moyenne de MPK dans l’air de la zone respiratoire pendant l’été et l’hiver étaient respectivement de 2,91 µg/m3 et de 1,44 µg/m3. Les concentrations de MPK au 95e centile en été et en hiver étaient respectivement de 12,65 µg/m3 et de 6,30 µg/m3 (Santé Canada, 2010a).
La MEK et la MPK sont très solubles dans l’eau. Mais, en raison de leur pression de vapeur élevée et de leur constante de la loi d’Henry modérée, elles devraient se volatiliser rapidement depuis l’eau (HSDB, 1983-). De plus, comme la MEK et la MPK devraient se biodécomposer dans l’eau, il est peu probable que l’eau soit une source importante d’exposition humaine (VCCEP, 2003; HSDB, 1983-). En 2000, la MEK n’a pas été détectée en concentrations supérieures au seuil de détection de 0,99 µg/L dans l’eau potable (taille de l’échantillon inconnue) à Montréal, au Québec (Bernier, 2000). Aucune autre donnée canadienne sur la présence de MEK dans l’eau n’a été trouvée. La MEK a été détectée peu fréquemment (dans 0,5 % à 0,8 % des échantillons) et à des concentrations variant de 0,6 à 340 µg/L, dans un petit nombre d’études américaines sur la qualité de l’eau potable (Grady et Casey, 2001; Delzer et Ivahnenko, 2003; Grady, 2003). Aucune donnée sur la présence de MPK dans l’eau au Canada n’a été trouvée. La MPK a été détectée dans l’eau potable à Ottumwa, en Iowa, à une concentration de 0,1 µg/L (0,1 ppb) et a été décelée, non quantitativement, dans l’eau potable de 5 autres villes américaines, ainsi qu’en Angleterre (HSDB, 1983-). Pour estimer avec prudence les concentrations d’exposition possibles à la MEK et à la MPK par l’eau potable, on a utilisé le seuil de détection de 0,99 µg/L de l’étude de Montréal pour la MEK et la concentration de 0,1 µg/L de l’Iowa pour la MPK.
En ce qui concerne le sol, une étude canadienne menée par Golder Associates (1987), dans laquelle les concentrations de MEK ont été suivies dans 2 forêts-parcs à proximité de raffineries de pétrole dans le sud de l’Ontario, a été trouvée. La MEK a été détectée dans 19 des 30 échantillons de sol, et la concentration moyenne mesurée était de 5,78 µg/g (maximum : 25 µg/g). L’utilisation de la concentration maximale de MEK dans le sol a donné lieu à une exposition de la population générale inférieure à 1 ng/kg p.c./j, quel que soit le groupe d’âge. Cependant, l’exposition au MEK par le sol est considérée comme négligeable. Aucune donnée portant sur la présence de MPK dans le sol ou les sédiments n’a été relevée au Canada ni ailleurs. Pour obtenir les concentrations possibles de MPK dans le sol, on a appliqué les données quantitatives provenant du tableau 4‑1 (c’est-à-dire 1 097 844 kg) à la v6.00 de ChemCAN (2003) et en supposant que la quantité totale importée a été rejetée dans une seule région du Canada (c’est-à-dire la région des plaines à bois mixtes de l’Ontario). La concentration estimative de MPK dans le sol était de 0,0682 µg/kg et a donné lieu à des absorptions inférieures à 1 ng/kg p.c./j dans la population générale du Canada, ce qui est considéré comme négligeable.
Les concentrations estimatives de l’exposition à la MEK et à la MPK dans des milieux environnementaux (air extérieur, air intérieur et eau potable) variaient de 16,9 µg/kg p.c./j chez les personnes âgées de 60 ans et plus, à 51,0 µg/kg p.c./j chez les enfants de 6 mois à 4 ans, et de 2,3 µg/kg p.c./j chez les personnes âgées de 60 ans et plus, à 6,8 µg/kg p.c./j chez les enfants de 6 mois à 4 ans, respectivement (Santé Canada, 2024). Pour de plus amples renseignements, veuillez consulter le document de Santé Canada de 2024 recensé dans la bibliographie.
Aliments
Les concentrations de MEK et de MPK ont été mesurées dans les aliments ou parmi les composés volatils provenant des aliments de la plupart des groupes alimentaires, principalement parce qu’ils sont présents naturellement dans les végétaux ou parce qu’ils sont produits par des microbes (c’est-à-dire par fermentation). De plus, on sait que la MEK et la MPK sont utilisées comme aromatisants dans les aliments, y compris dans les produits de boulangerie, les graisses et les huiles, les produits laitiers surgelés, les gélatines et les poudings, les boissons non alcoolisées et les bonbons mous (Burdock, 2010). Au Canada, la MEK est employée comme additif alimentaire dans les extraits naturels et les extraits d’épices. Cependant, par rapport à la présence naturelle de cette cétone dans les aliments, cette application devrait peu contribuer à la concentration d’exposition de MEK. De la MEK (5 échantillons sur 12) et de la MPK (4 échantillons sur 12) ont été décelées dans le lait maternel, mais n’ont pas été quantifiées (Pellizari et coll., 1982).
Le Comité mixte Organisation des Nations Unies pour l’alimentation et l’agriculture (FAO)-Organisation mondiale de la Santé (OMS) d’experts des additifs alimentaires (JECFA) a évalué un groupe de 39 alcools et cétones aliphatiques acycliques saturés secondaires ainsi qu’esters saturés et non saturés apparentés utilisés comme aromatisants alimentaires, comprenant la MEK et la MPK (OMS, 1999 b). Dans le cadre de cette évaluation, le Comité a estimé que l’absorption de MEK et de MPK par habitant, découlant de l’utilisation de ces substances comme aromatisants alimentaires, était respectivement de 0,6 et de 0,7 µg/kg p.c./j dans la population américaine, et de 2 µg/kg p.c./j pour les 2 substances, dans la population européenne (pour de plus amples renseignements, veuillez consulter l’annexe A). Faute de données sur l’utilisation réelle au Canada, ces absorptions estimatives par habitant sont des valeurs acceptables de l’exposition possible, par les aliments, à la MEK et à la MPK utilisées comme aromatisants alimentaires dans la population générale (chez les 1 an et plus).
Il ne devrait pas y avoir d’exposition à la MEK et à la MPK lorsque ces substances sont utilisées dans la fabrication de matériaux d’emballage alimentaire et lorsque la MEK est employée comme composant d’additifs indirects (nettoyants) dans les établissements de transformation des aliments.
Les concentrations estimatives de l’exposition à la MEK et à la MPK lorsqu’elles sont présentes naturellement dans les alimentsNote de bas de page 5 ont varié de 66 µg/kg p.c./j chez les adolescents de 14 à 18 ans à 185 µg/kg p.c./j chez les enfants d’un an, et de 68 µg/kg p.c./j chez les adolescents de 14 à 18 ans à 216 µg/kg p.c./j chez les enfants d’un an, respectivement (pour de plus amples renseignements, veuillez consulter l’annexe C).
Produits de consommation
MEK
Selon les déclarations faites à Santé Canada en vertu du Règlement sur les cosmétiques, la MEK est utilisée dans certains produits cosmétiques au Canada, comme les hydratants pour le visage, et différents produits de soins pour les ongles, y compris les vernis de base, les vernis de finition, les vernis à ongles, les dissolvants de vernis à ongles, les adhésifs pour ongles, les brosses à ongles, les fortifiants pour ongles, les crèmes à ongles, les produits accélérant le séchage et les produits pour la réparation des ongles (communication personnelle, courriels de la Direction de la sécurité des produits de consommation et des produits dangereux [DSPCPD], SC, adressés au BERSE, SC, datés d’août 2016 et d’avril 2017; source non mentionnée). Dans ces cosmétiques, la MEK sert de solvant ou d’agent parfumant (Commission européenne, 2017).
Les concentrations d’exposition par inhalation ont été estimées pour certains produits sentinelles (vernis de finition, vernis à ongles et dissolvants de vernis à ongles), dont les concentrations d’exposition sont les plus élevées par rapport à celles des produits similaires, à l’aide du logiciel ConsExpo Web (2016). Le tableau 7‑2 présente une synthèse des plages des concentrations de la MEK dans ces divers produits, ainsi que les concentrations estimatives connexes de l’exposition par inhalation. Seules les concentrations estimatives de l’exposition chez les enfants de 6 mois à 4 ans et les personnes âgées de 12 ans et plus sont présentées. Toutefois, ces valeurs représentent la plage de concentrations des expositions possibles de tous les groupes d’âge. Pour des précisions sur la méthode et les paramètres appliqués pour estimer les concentrations de l’exposition par inhalation à la MEK dans les produits cosmétiques, veuillez consulter l’annexe D.
| Scénario d’utilisation du produit | Concentration maximalea | Concentration moyenne dans l’air, par exposition (mg/m3) | MPTb (mg/m3) |
|---|---|---|---|
| Vernis de finition (12 ans et plus) | 55,7 % | 140 | 6,0 |
| Vernis à ongles (12 ans et plus) | 94,7 % | 520 | 43,3 |
| Vernis à ongles (6 mois à 4 ans) | 94,7 % | 180 | 15 |
| Dissolvant de vernis à ongles (12 ans et plus) | 84 %c | 280 | 5,3 |
| Dissolvant de vernis à ongles (6 mois à 4 ans) | 79,6 % | 230 | 4,4 |
Abréviation : MPT, moyenne pondérée dans le temps
a Communication personnelle; courriels de la DSPCPD, SC, adressés au BERSE, SC; datés d’août 2016, d’avril 2017 et de novembre 2019; source non mentionnée.
b Les concentrations moyennes pondérées sur 7 heures ont été obtenues pour tous les scénarios d’utilisation afin de correspondre aux durées d’exposition de l’étude de caractérisation des risques à l’aide des effets critiques. MPT sur 7 heures = concentration moyenne par exposition (mg/m3) × durée d’exposition (min)/(7 × 60 min).
c Le produit n’est pas censé être utilisé par de jeunes enfants (communication personnelle, courriels de la DSPCPD, SC, adressés au BERSE, SC; datés d’avril 2017 et de novembre 2019; source non mentionnée).
L’exposition par voie cutanée devrait contribuer à l’exposition globale découlant de l’utilisation de produits de consommation, mais l’exposition par inhalation est considérée comme la voie principale. Dans une étude in vitro sur peau humaine non recouverte, Wilkinson et Williams (2001) ont obtenu une mesure d’absorption cutanée de moins de 1 % pour la MEK. En raison de la volatilité élevée et de la faible absorption cutanée de la MEK, l’exposition par voie cutanée est considérée comme minime par rapport à l’exposition par inhalation. Par conséquent, seules les valeurs estimatives de l’exposition par l’inhalation sont présentées.
Produits pour enfants
La MEK a été décelée aux États-Unis et au Danemark dans plusieurs produits pour enfants, y compris dans les sucettes et les anneaux de dentition (WSDE, 2020), ainsi que dans les jouets à base de glu (Svendsen et coll., 2005). Ces produits contenant de la MEK pourraient également être présents sur le marché canadien. La voie orale (objets portés à la bouche) et l’inhalation devraient être les principales voies d’exposition lorsque ces produits pour enfants sont utilisés.
Nous avons estimé le potentiel d’exposition par voie orale occasionnée par des jouets de dentition ou des objets pour enfants contenant de la MEK en utilisant une sucette et un jouet de dentition dans un scénario d’exposition sentinelle. Le WSDE (2020) a déterminé que la MEK était un contaminant dans les sucettes et les jouets de dentition, dont les concentrations variaient d’une valeur égale ou supérieure à 100 ppm à une valeur maximale de 500 ppm. Les concentrations d’exposition par voie orale, estimées au moyen de la méthode décrite à l’annexe D, variaient de 110 à 232 µg/kg p.c./j chez les enfants de 6 mois à 4 ans, et de 91 à 300 µg/kg p.c./j chez les bébés de la naissance à 6 mois.
Il y avait peu de données sur le transfert de la MEK depuis les produits de consommation. Selon Svendsen et coll. (2005), la MEK n’aurait pas été transférée dans la sueur et la salive artificielles depuis les jouets à base de glu, dont les concentrations étaient respectivement de 2,3 % et de 9 %. Les concentrations, dans l’air de la zone respiratoire, de la substance provenant des jouets à base de glu étaient, respectivement, de 0,079 µg/m3 et de 0,098 µg/m3 (Svendsen et coll., 2005), valeurs inférieures à celles mesurées dans l’air intérieur et qui ont été présentées dans la section portant sur les milieux environnementaux. Nilsson et coll. (2006) ont analysé la MEK dans les jouets pour adultes à l’aide d’analyses de l’espace de tête et de sueur artificielle (pH de 4,5 et de 6,5). Les concentrations de MEK variaient de 174 à 13 016 ng/180 min dans les analyses de l’espace de tête, et de 12 à 49 µg/dm2 dans la sueur artificielle dont le pH était de 4,5, et était de 17 µg/dm2 dans la sueur artificielle dont le pH était de 6,5.
Autres produits de consommation
La MEK utilisée comme ingrédient non médicinal aurait été décelée dans quelques PSN à usage topique actuellement homologués au Canada, notamment dans un nettoyant antiseptique pour la peau et un traitement contre l’acné (BDPSNH [modifiée en 2021]). Les scénarios d’utilisation sentinelles des produits cosmétiques tiennent compte de toutes les expositions à la MEK découlant de l’utilisation de PSN.
La MEK est également présente dans de nombreux produits de consommation (CPID [modifié en 2019]). Le tableau 7‑3 ne présente que les scénarios d’utilisation de produits qui donnent lieu aux concentrations d’exposition à la MEK les plus élevées par inhalation, le cas échéant. Les concentrations de l’exposition par inhalation possible ont été estimées à l’aide du logiciel ConsExpo Web (ConsExpo, 2016). L’annexe D présente en synthèse les valeurs des paramètres utilisés dans chaque modèle.
| Scénario d’utilisation du produit | Concentration de MEK | Concentration moyenne dans l’air, par exposition (mg/m3) | MPTa sur 7 h (mg/m3) |
|---|---|---|---|
| Décapant pour peinture ou revêtement (par exemple, décapant pour laque) | 20 % à 40 %b | 1 800 à 3 500 | 257 à 500 |
| Dissolvant d’adhésif, dégraissant | 100 %c | 1 800 | 921 |
| Diluants pour peinture ou revêtement) | Entièrement dilué à 3 % dans le revêtementc | 840 | 120 |
| Peinture liquide (peinture à teneur élevée en solvant) pour plate-forme de camion | 10 % à 20 %d | 110 à 210 | 35 à 66 |
| Produits à pulvériser (par exemple, peinture en aérosol) | 1 % à 75 %e,f | 57 à 3 900 | 3,4 à 232 |
| Apprêts pour PVC, seulement | 15 % à 40 %g | 7,7 à 18 | 4,4 à 10 |
| Adhésifs pour PVC, seulement | 5 % à 70 %h | 2,6 à 18 | 1,5 à 10 |
| Apprêts et adhésifs pour PVC i | 10 % à 55 %j | 12 à 48 | 7 à 27 |
| Adhésif tout usage | 3 % à 100 %k,l | 8,8 à 280 | 1,7 à 53 |
| Nettoyant pour le volet de départ et le papillon des gaz des voitures | 1 % à 5 %m | 0,099 à 0,23 | 0,0035 à 0,0082 |
| Agent hydrofuge, traitement hydrophobe (par exemple, liquide lave-glace et traitement hydrophobe, en aérosol, pour pare-brise) | 10 % à 25 %n | 44 à 110 | 6,28 à 15,7 |
Abréviation : MPT, moyenne pondérée dans le temps
a Les concentrations moyennes pondérées sur 7 heures (MPT) ont été déterminées dans tous les scénarios d’utilisation des produits afin qu’elles correspondent à celles des durées d’exposition utilisées dans l’étude sur les effets critiques employée pour caractériser les risques. MPT sur 7 heures = concentration moyenne, par exposition (mg/m3) × durée de l’exposition (min)/(7 × 60 min).
b SDS, 2018a
c SDS, 2019a
d FDS, 2021
e SDS, 2016a
f SDS, 2019b
g SDS, 2019e
h SDS, 2018b
i Ce scénario décrit l’exposition découlant de l’application d’un adhésif ou d’un apprêt pour PVC, suivie de l’application d’un adhésif pour PVC, à la concentration déclarée la plus élevée pour chaque produit de consommation au Canada, ainsi que par l’exposition, postérieure à l’application, aux résidus restants depuis l’application, le cas échéant.
j Moyenne pour l’utilisation de l’apprêt et de l’adhésif.
k SDS, 2019c
l SDS, 2014a
m SDS, 2019d
n SDS, 2016b
MPK
Selon les déclarations faites à Santé Canada en vertu du Règlement sur les cosmétiques, la MPK est utilisée dans certains produits de soins pour les ongles, y compris le vernis à ongles et les adhésifs pour ongles (communication personnelle, courriels de la DSPCPD, SC, adressés au BERSE, SC; datés de novembre 2019 et de décembre 2019; source non mentionnée). La MPK a également été décelée dans plusieurs produits de peinture (ECCC, 2017b; CPID [modifié en 2019]).
Le tableau 7‑4 présente en synthèse les concentrations estimatives de l’exposition par inhalation, obtenues à l’aide du logiciel ConsExpo Web (ConsExpo, 2016), aux produits de consommation contenant de la MPK. Comme pour la MEK, même si l’exposition par voie cutanée pouvait contribuer à l’exposition globale découlant de l’utilisation de produits de consommation, l’inhalation est considérée comme la principale voie d’exposition. Par conséquent, seules les concentrations estimatives de l’exposition par inhalation sont présentées.
| Scénario d’utilisation du produit | Concentration de MPK | Concentration moyenne dans l’air, par exposition (mg/m3) | MPTa sur 6 h (mg/m3) |
|---|---|---|---|
| Peinture liquide pour l’acier (peinture à haute teneur en solides) (20 ans et plus) | 1 % à 10 %b | 87 à 870 | 32 à 319 |
| Adhésif pour ongles et vernis à ongles (12 ans et plus) | 1 % à 3 %c | 4,9 à 15 | 0,48 à 1,46 |
| Vernis à ongles (6 mois à 4 ans) | 0,3 % à 1 %c | 0,61 à 2 | 0,059 à 0,19 |
Abréviation : MPT, moyenne pondérée dans le temps
a Les concentrations moyennes pondérées (MPT) d’exposition sur 6 heures ont été déterminées dans tous les scénarios d’utilisation des produits afin qu’elles correspondent à celles des durées d’exposition utilisées dans l’étude sur les effets critiques employée pour caractériser les risques. MPT sur 6 h = concentration moyenne, par exposition × durée de l’exposition/6 × 60 min
b ECCC, 2017 b
c Communication personnelle, courriels de la DSPCPD, SC, adressés au BERSE, SC; datés d’août 2016, d’avril 2017 et de novembre 2019; source non mentionnée.
7.1.2 Évaluation des effets des substances du sous-groupe 1 (MEK et MPK) sur la santé
La MEK et la MPK sont des monocétones de structures similaires qui se distinguent uniquement par la chaîne carbonée, qui est plus longue d’un atome de carbone dans un cas. Étant donné la similitude des effets de l’exposition à la MEK et au butan-2-ol, et la métabolisation rapide du butan-2-ol en MEK chez le rat, le butan-2-ol est utilisé comme analogue pour éclairer l’évaluation des effets des substances de ce sous-groupe sur la santé. Les données sur la toxicité du butan-2-ol ont été extrapolées pour la MEK ou la MPK, selon le cas (voir l’annexe A).
7.1.2.1 MEK
La MEK a été évaluée par l’OCDE (1997a), l’US EPA (2003a) et l’ATSDR (2020), et les résultats ont servi de base à la caractérisation des effets sur la santé de la présente évaluation. Les recherches dans la littérature scientifique ont commencé un an avant la publication du rapport de l’EPA des États-Unis (2003a) du Système intégré d’information sur les risques (Integrated Risk Information System, ou IRIS) et se sont poursuivies jusqu’en octobre 2019. Des recherches ciblées dans la littérature scientifique ont été menées jusqu’en mars 2021. Aucune étude sur les effets de la substance sur la santé pouvant avoir une incidence sur la caractérisation des risques (c’est-à-dire qui aboutirait à des critères d’effets critiques différents ou à des critères de départ plus faibles par rapport à ceux indiqués dans le document de l’US EPA [2003a]) n’a été trouvée.
Toxicocinétique
La MEK administrée par voie orale à des rongeurs s’est révélée être largement absorbée dans le tube digestif, puis rapidement éliminée (Dietz et coll., 1981; étude revue dans l’US EPA, 2003a). En raison de son rapport de solubilité sang/air élevé, la substance est également bien absorbée chez les humains et les rats en cas d’exposition par inhalation. De plus, il a été constaté que la substance était rapidement absorbée après l’exposition par voie cutanée (Munies et Wurster, 1965; étude revue dans l’US EPA, 2003a). D’après les renseignements recensés, la métabolisation de la MEK chez les humains est semblable chez les animaux de laboratoire, et le butan-2-ol et le 2,3-butanediol seraient les principaux métabolites (Perbellini et coll., 1984; Liira et coll., 1988, 1990a; étude revue dans l’US EPA, 2003a). Chez le rat et le cobaye, une petite fraction de la MEK absorbée est réduite pour donner le butan-2-ol, lequel est rapidement oxydé pour se transformer en MEK (US EPA, 2003a). D’origine endogène chez les humains, la MEK (la substance est, normalement, un constituant mineur de l’urine) est présente dans le sérum et l’urine chez les diabétiques, ainsi que dans l’air expiré (OMS, 1992; étude revue dans l’US EPA, 2003a).
Cancérogénicité et génotoxicité
L’EPA des États-Unis (US EPA, 2003a) a conclu que les « données recensées sont considérées comme inappropriées pour l’évaluation du potentiel cancérogène chez les humains », parce que les études sur l’exposition chronique à la MEK chez les humains ne sont pas concluantes et que la cancérogénicité de la MEK n’a pas été déterminée chez les animaux par voie orale ou par inhalation. L’ATSDR (2020) a également appuyé cette conclusion et indiqué que les études épidémiologiques préliminaires semblent indiquer que l’exposition professionnelle à la MEK n’augmente pas l’incidence des néoplasmes. Bien que les effets génotoxiques de la MEK aient été étudiés à l’aide de plusieurs ensembles de tests, les résultats ont été invariablement négatifs dans les tests de génotoxicité, tant in vitro qu’in vivo (US EPA, 2003a).
Toxicité à doses répétées
Aucune étude sur le caractère chronique des effets chez les animaux après une exposition par inhalation n’a été trouvée. Cependant, plusieurs études sur l’exposition à doses répétées à court terme, par inhalation, à la MEK ont été recensées.
Les effets mentionnés de la MEK sur la santé étaient principalement des effets sur le développement (voir la section suivante) ainsi que des effets neurologiques réversibles. Des augmentations du poids absolu ou relatif des organes, principalement du foie, ont également été observées (US EPA, 2003; ATSDR, 2020).
Toxicité pour la reproduction et le développement
Aucune étude évaluant le potentiel de toxicité pour la reproduction de la MEK, quelle que soit la voie d’exposition, n’a été trouvée. Plusieurs études sur le potentiel de toxicité pour le développement après exposition à la MEK par inhalation ont été recensées.
La MEK a été décrite dans l’ATSDR (2020) comme étant légèrement toxique pour le fœtus, compte tenu d’une diminution du poids du fœtus, des variations au niveau du squelette et d’une ossification retardée ou incomplète.
Dans l’étude de toxicité pour le développement menée par Deacon et coll. (1981), des rates gravides ont été exposées à des concentrations moyennes de MEK de 1 215 mg/m3, de 2 955 mg/m3 et de 8 865 mg/m3 (dans des enceintes d’exposition dynamique du corps entier) à raison de 7 h/j, du jour de gestation (JG) 6 au JG 15. Un ralentissement de la prise de poids corporel et une augmentation de la consommation d’eau ont été observés chez les mères exposées à 8 865 mg/m3, indiquant une toxicité maternelle. À cette dose, des anomalies au squelette, notamment une ossification retardée des corps vertébraux et des côtes surnuméraires, ont également été observées chez les petits.
Dans une étude ultérieure de toxicité pour le développement après exposition par inhalation, concordant avec les résultats antérieurs (anomalies au niveau du squelette), des souris gravides ont été exposées à des concentrations moyennes de 0, 398, 1 010 et 3 020 ppm (0, 1 174, 2 980 et 8 909 mg/m3) de MEK par inhalation, dans des enceintes d’exposition du corps entier, à raison de 7 h/j, du JG 6 au JG 15 (Schwetz et coll., 1991, étude revue dans l’US EPA, 2003a). Une augmentation légère, mais statistiquement significative, du poids absolu du foie, liée à la dose, a été observée chez les mères exposées à 8 909 mg/m3 (augmentation d’environ 7 % par rapport aux mères du groupe témoin). Il y a eu une diminution statistiquement significative du poids fœtal moyen (de 5 %, par portée) chez les mâles et une diminution de 4 % chez tous les fœtus, à la dose d’essai la plus élevée. À mesure que les concentrations d’exposition augmentaient, l’incidence du défaut d’alignement des sternèbres chez les fœtus augmentait également, montrant ainsi une tendance positive. D’autres effets non significatifs sur le développement (fente palatine, côtes fusionnées, vertèbres manquantes et syndactylie) ont été observés dans les groupes d’animaux exposés à la substance, mais non dans les groupes témoins. La CSENO établie d’après les effets négatifs sur les mères et le développement, était de 2 980 mg/m3, tandis que la CMENO établie d’après les effets négatifs sur le développement et les mères était de 8 909 mg/m3), d’après une diminution du poids fœtal chez les mâles, une augmentation de l’incidence du défaut d’alignement des sternèbres et une augmentation du poids relatif du foie chez les mères. D’après les données sur le défaut d’alignement des sternèbres (considéré comme le paramètre le plus protecteur), l’EPA des États-Unis (2003a) a établi la limite inférieure de la concentration efficace d’après la concentration entraînant un effet sur 10 % de la population (CE10)Note de bas de page 6 à 5 202 mg/m3 (limite inférieure de la confiance à 95 % de la concentration associée à un risque supplémentaire de 10 %) pour une exposition intermittente (7 h/j) et une CMECEHNote de bas de page 7 (concentration équivalente chez l’humain ajustée pour une exposition continue) de 1 517 mg/m3.
Une étude de toxicité pour le développement menée chez des rates gravides exposées par inhalation à 0 mg/m3, 2 950 mg/m3, 5 900 mg/m3, 11 800 mg/m3 ou 17 700 mg/m3 (exposition du corps entier) à raison de 6 h/j, du JG 6 au JG 20, a également révélé des effets sur le développement et les mères (Saillenfait et coll., 2006). Une CSENO de 2 949 mg/m3 a été établie d’après une diminution du poids corporel fœtal observée à 5 899 mg/m3, tandis qu’un ralentissement de la prise de poids corporel des mères (52 %), une diminution de la consommation d’aliments (12 %) et une augmentation de l’incidence d’ossification incomplète des sternèbres ont également été observés à 11 797 mg/m3 et plus (Saillenfait et coll., 2006). Une autre étude sur le développement a mentionné des effets sur le développement sans toxicité maternelle à la dose d’essai de 7 723 mg/m3, la CSENO étant de 3 322 mg/m3) (Schwetz et coll., 1974, mentionné dans l’US EPA, 2003a].
Faute d’étude sur les effets de la MEK sur la reproduction ou d’études sur la toxicité de la MEK pour le développement par voie orale, on a extrapolé les données de l’étude sur la toxicité pour la reproduction et le développement par voie orale menée avec le butan‑2‑ol (lequel est rapidement métabolisé en MEK chez le rat). Dans une étude multigénérationnelle sur l’exposition à la substance dans l’eau potable, des rats Wistar mâles et femelles ont été exposés à des concentrations de butan-2-ol de 0 %, 0,3 %, 1,0 % ou 3,0 % (équivalant à des doses de 0, 538, 1 644 et 5 089 mg/kg p.c./j [rats mâles] et de 0, 594, 1 771 et 4 571 mg/kg p.c./j [rats femelles]) pendant les 8 semaines précédant l’accouplement (Cox et coll., 1975, étude revue dans l’US EPA, 2003a). En raison de la hausse du taux de mortalité et de la diminution du poids corporel constatées dans les portées F1A à la dose de 3 %, la dose la plus élevée a été réduite à 2 % (apport quotidien moyen de 3 384 mg/kg p.c./j chez les mâles et de 3 122 mg/kg p.c./j chez les femelles) pour le reste de l’étude. Les femelles F0 ont été accouplées de nouveau, et les petits F1A se sont accouplés pour produire les portées F2. Des concentrations aussi élevées que 3 % n’ont pas eu d’effet sur la performance de reproduction chez les rats, mais elles ont causé une toxicité chez les mères (ralentissement de la prise de poids corporel chez les mères). Comme l’a fait remarquer l’EPA des États-Unis (2003a), cette étude ne comprenait pas certains paramètres couramment évalués dans les études plus récentes. Parmi les lacunes, mentionnons le manque de mesures de la cyclicité œstrale, des paramètres spermatiques ainsi que du poids de l’utérus, des épididymes, des vésicules séminales et du cerveau; sans compter le caractère très parcellaire des analyses en chimie clinique ainsi que des examens hématologiques et histopathologiques. Une dose sans effet nocif observé (DSENO) de 1 771 mg/kg p.c./j a été établie pour le butan-2-ol d’après les effets observés sur la mère et sur le développement. D’après une diminution du poids corporel (effet le plus sensible observé) chez les petits de la génération F1A au 21e jour postnatal (JPN), l’EPA des États-Unis (2003a) a estimé la dose minimale efficace (DME05) (limite inférieure de la confiance à 95 % de la dose efficace [DE]) à 639 mg/kg p.c./j pour la MEK (ajustement reposant sur le poids moléculaire établi par la DME05 de 657 mg/kg p.c./j pour le butan-2-ol).
Aucune étude de toxicité pour le développement par voie cutanée n’a été trouvée pour la MEK ou son analogue, le butan-2-ol.
Toxicité à court terme et toxicité aiguë
Des primates (4 babouins juvéniles), exposés de manière continue pendant 7 jours à environ 300 mg/m3 de MEK, ont présenté des signes hâtifs de narcose, d’incoordination et de réaction différée dans des tests neurocomportementaux (Geller et coll., 1979). Comme il en a été question dans l’ATSDR (2020), les tests ont permis d’évaluer les réponses à une tâche discriminante complexe axée sur le comportement, et de détecter des effets neurocomportementaux subtils. Toutefois, il a également été constaté qu’une seule concentration d’exposition avait été mise à l’essai, que l’effet observé s’était estompé quelque peu vers la fin de l’expérience et qu’aucun test statistique n’avait été appliqué (PISSC, 1993; ATSDR, 2020).
Effets chez les humains
Les effets neurologiques et les effets sur la fonction respiratoire sont les effets les plus couramment constatés de l’exposition à la MEK chez les participants humains et d’autres personnes exposées en milieu de travail (ATSDR, 2020). L’exposition professionnelle chronique à la MEK a fait l’objet de plusieurs études épidémiologiques revues par l’EPA des États-Unis (US EPA, 2003a). Toutefois, les données recensées ont été jugées insuffisantes pour dégager une association entre l’exposition à la MEK et les effets neurologiques, pulmonaires ou autres effets chroniques en raison de plusieurs limites, notamment celles liées à la caractérisation de l’exposition, ou de lacunes dans la méthodologie.
De légers effets sur le système nerveux central (SNC) (par exemple, maux de tête, fatigue et malaises assimilables à une intoxication) ont été observés chez des participants humains exposés à environ 300 mg/m3 pendant 4 heures, les femmes obtenant une note plus élevée que les hommes dans les questionnaires sur les symptômes (Tomicic et coll., 2011). Des effets similaires ont également été observés dans d’autres études à des doses d’essai plus élevées (Muttray et coll., 2002; Dick et coll., 1984, 1988, 1989, 1992, étude revue dans l’US EPA, 2003a; ATSDR, 2020).
7.1.2.2 MPK
La MPK n’a pas été évaluée par d’autres organismes. L’évaluation suivante sur les effets sur la santé repose sur les données recensées dans les dossiers d’homologation de l’ECHA (ECHA, c2007-2019a) et le High Production Volume Information System (HPVIS) de l’EPA des É.-U. (US EPA, 2010).
Toxicocinétique
Aucune donnée quantitative sur l’absorption de la MPK quelle que soit la voie d’exposition n’a été trouvée. Comme la MPK a une structure semblable à celle de la MEK et de son métabolite, le butan-2-ol, son absorption devrait être aussi rapide et importante que celle de la MEK et de son métabolite.
Cancérogénicité et génotoxicité
Aucune étude de cancérogénicité par voie orale, par voie cutanée ou par inhalation concernant la MPK n’a été trouvée. La modélisation de la relation quantitative structure-activité (QSAR) n’a dégagé aucune prédiction positive ni alerte structurale de génotoxicité ou de cancérogénicité. En outre, la MPK ne s’est pas révélée génotoxique dans maints essais in vitro (par exemple, tests d’Ames, test d’aberration chromosomique et test du lymphome de souris; ECHA, c2007-2019a).
Toxicité à doses répétées
Dans une étude sur la toxicité à doses répétées par voie orale, des rats CD mâles ont été exposés à la MPK dans leur eau potable, à des concentrations de 0 %, de 0,25 %, de 0,5 % ou de 1,0 % (équivalant à des doses de 0, 144, 250 et 454 mg/kg p.c./j, respectivement) pendant 13 mois. Le seul effet rapporté était un léger ralentissement de la prise de poids corporel (9 %) à la dose d’essai la plus élevée (454 mg/kg p.c./j). Aucun effet clinique, ni variation du poids des organes, ni modification histologique n’ont été observés. De même, aucun changement pathologique n’a été constaté dans les systèmes nerveux central et périphérique (Bingham et coll., 2001, mentionné dans HSDB, 1983; US EPA, 2010).
Dans le cadre d’une étude de toxicité subchronique par inhalation, des rats ont été exposés à la MPK à raison de 6 h/j et de 5 j/sem., pendant 13 semaines, à des concentrations de 250, 750 ou 1 500 ppm (équivalant à 880, 2 640 ou 5 300 mg/m3, respectivement). Les effets observés liés à la substance d’essai comprenaient une augmentation de l’incidence de la matière rougeâtre autour du nez et dans le visage chez les femelles et des anomalies microscopiques dans la région nasale, le larynx et la glande thyroïde chez les mâles de tous les groupes exposés à la substance. Toutefois, ces effets n’ont pas été jugés nocifs par les auteurs de l’étude. Aucun effet sur la réaction d’éveil n’a été constaté. La CSENO inscrite dans le dossier d’enregistrement du système Enregistrement, évaluation et autorisation des substances chimiques (Registration, Evaluation, Authorization and Restriction of Chemicals, ou REACH) est de 5 300 mg/m3 chez les mâles et les femelles (ECHA, c2007-2019a).
Aucune étude convenable de la toxicité par voie cutanée n’a été trouvée.
Toxicité pour la reproduction et le développement
Dans l’étude combinée de toxicité pour la reproduction et le développement par inhalation, des rats SD ont été exposés à des doses de MPK allant jusqu’à 5 000 mg/m3, à raison de 6 h/j, pendant 35 à 48 j (femelles), jusqu’au JG 19, ou pendant 51 j (mâles) (ECHA, c2007-2019a; AcToR de l’US EPA, 2015). À la dose la plus élevée, on a constaté que les mâles et les femelles étaient moins vigilants et moins actifs, et qu’ils réagissaient plus lentement au bruit du tapotement sur la paroi de l’enceinte. Aucun autre effet significatif n’a été mentionné. La CSENO de la toxicité pour la reproduction et le développement indiquée dans le dossier d’enregistrement REACH est de 5 000 mg/m3 (ECHA, c2007-2019a).
Dans une étude de toxicité pour le développement prénatal par inhalation, des rates SD ont été exposées à des concentrations de 0, 250, 750 et 1 500 ppm (équivalant à 0, 880, 2 650 et 5 300 mg/m3, respectivement) de MPK, du JG 6 au JG 19 (ECHA, c2007-2019a). Aucun effet sur le poids corporel moyen, la prise de poids corporel, le poids corporel net, la prise de poids corporel nette, le poids de l’utérus gravide ou la consommation alimentaire n’a été observé, quel que soit le groupe exposé à la substance d’essai. Aucun effet nocif chez les mères ni effet sur la croissance intra-utérine, le taux de survie et la morphologie chez les fœtus, y compris sur la réaction d’éveil, n’a été constaté, quelle que soit la concentration d’exposition. À la lumière de ces observations, les auteurs de l’étude ont déterminé la CSENO à 1 500 ppm (5 300 mg/m3) (la concentration d’exposition évaluée la plus élevée) pour la toxicité maternelle et la toxicité pour le développement de l’embryon ou du fœtus.
Les résultats de ces études indiquent que la MPK n’est pas une substance toxique pour le développement. En outre, la modélisation in silico à l’aide de la boîte à outils de l’OCDE n’a donné lieu à aucune alerte structurelle indiquant que la MPK pourrait être toxique pour le développement.
Aucune donnée n’a été trouvée sur la toxicité pour la reproduction ou le développement concernant la MPK administrée par voie orale ou cutanée.
7.1.3 Caractérisation des risques associés aux substances du sous-groupe 1 (MEK et MPK)
MEK
En ce qui concerne les effets nocifs observés chez les animaux découlant d’une exposition à doses répétées par inhalation à la MEK, des données probantes cohérentes ont été recensées dans des études chez le rat et la souris, selon lesquelles les effets sur le développement seraient les effets critiques pour la santé, et se produiraient surtout en concomitance avec une légère toxicité chez les mères (ATSDR, 2020). Parmi les études recensées, l’EPA des É.-U. (2003a) a sélectionné l’étude chez la souris de Schwetz et coll. (1991), dont la CE10 pour une exposition intermittente (à raison de 7 h/j) était de 5 202 mg/m3 et la CMECEH pour une exposition continue, de 1 517 mg/m3, valeurs établies d’après l’incidence du défaut d’alignement des sternèbres (IUS EPA, 2003a). Par conséquent, ces valeurs ont été considérées comme les points de départ les plus appropriés aux fins de la caractérisation des risques associés à la MEK.
Faute d’études de toxicité à doses répétées par voie orale pour la MEK, l’étude de toxicité pour la reproduction et le développement du butan-2-ol dans l’eau potable chez le rat (Cox et coll., 1975, mentionné dans l’US EPA, 2003a) a été choisie pour caractériser les risques par voie orale. L’EPA des É.-U. (2003) a estimé la DE05 (limite inférieure de la confiance à 95 % de la dose efficace, DE) à 639 mg/kg p.c./j pour la MEK (ajusté d’après les masses moléculaires établies à partir de la DE05 de 657 mg/kg p.c./j pour le butan-2-ol) d’après une diminution du taux de survie des petits et du poids corporel des nouveau-nés, en concomitance avec une toxicité chez les mères.
La principale source d’exposition de l’ensemble de la population à la MEK dans les milieux environnementaux (air extérieur, air intérieur et eau potable) et les aliments sont le régime alimentaire et, dans une moindre mesure, l’air intérieur. D’après les données recensées, la majeure partie de la concentration d’exposition à la MEK par le régime alimentaire découlerait de l’exposition aux aliments dans lesquels la substance est naturellement présente. L’absorption de MEK dans les aliments dans lesquels ;a substance est présente naturellement n’a pas été jugée préoccupante pour la santé humaine.
La population générale du Canada peut également être exposée à la MEK, principalement par inhalation, lorsqu’elle utilise des produits de consommation qui contiennent la substance, notamment des produits pour les ongles, de la peinture et des produits de bricolage. Le tableau 7‑5 présente les valeurs pertinentes d’exposition et de concentrations causant un effet critique sur la santé, ainsi que les ME résultantes, aux fins de la caractérisation des risques associés à la MEK.
| Scénario d’exposition | Exposition | Dose associée à un effet critique | Effet critique sur la santé | ME |
|---|---|---|---|---|
| Milieu environnementala (tous les groupes d’âge) | 16,9 à 51,0 µg/kg p.c./j | DE05 = 639b μg/kg p.c./j | Étude de toxicité pour le développement pour le butan‑2‑ol; diminution du poids des fœtus et des petits, et ralentissement de la prise de poids corporel chez les mères | > 12 529 |
| Milieu environnemental pour les résidants vivant à proximité d’installations rejetant de la MEKc (tous les groupes d’âge) | 80,6 à 243,6 µg/kg p.c./j | DE05 = 639b μg/kg p.c./j | Étude de toxicité du butan-2-ol pour le développement; diminution du poids des fœtus et des petits, et ralentissement de la prise de poids corporel chez les mères | 2 623 à 7 922 |
| Aromatisant alimentaire (voie orale) (1 an et plus) | 0,6 à 2,0 µg/kg p.c./j | DE05 = 639b μg/kg p.c./j | Étude de toxicité du butan-2-ol pour le développement; diminution du poids des fœtus et des petits, et ralentissement de la prise de poids corporel chez les mères | > 319 500 |
| Produits pour les ongles (inhalation) (6 mois et plus) | 4,4 à 43,3 ng/m3 d | DE10 > 5 202 mg/m3 e (intermittente) | Augmentation de l’incidence du défaut d’alignement des sternèbres chez les fœtus | 120 à 1 182 |
| Sucettes et jouets de dentition (voie orale) (0 à 4 ans) | 0,09 et 0,30 mg/kg p.c./j |
DE05 = 639b μg/kg p.c./j | Étude de toxicité du butan-2-ol pour le développement; diminution du poids des fœtus et des petits, et ralentissement de la prise de poids corporel chez les mères | 2 130 à 7 100 |
| Décapant pour peinture ou revêtement (par exemple, décapant pour laque) (inhalation) (20 ans et plus) | 257 à 500 ng/m3 d | DE10 > 5 202 mg/m3 e (exposition intermittente) | Augmentation de l’incidence du défaut d’alignement des sternèbres chez les fœtus | 10 à 20 |
| Dissolvant d’adhésif, dégraissant (par inhalation) (20 ans et plus) | 921 mg/m3 d | DE10 > 5 202 mg/m3 e (exposition intermittente) | Augmentation de l’incidence du défaut d’alignement des sternèbres chez les fœtus | 6 |
| Diluants pour peinture ou revêtement (inhalation) (20 ans et plus) | 120 mg/m3 d | DE10 > 5 202 mg/m3 e (exposition intermittente) | Augmentation de l’incidence du défaut d’alignement des sternèbres chez les fœtus | 43 |
| Peinture liquide (à teneur élevée en solvant) pour plate-forme de camion (inhalation) (20 ans et plus) | 35 à 66 mg/m3 d | DE10 > 5 202 mg/m3 e (exposition intermittente) | Augmentation de l’incidence du défaut d’alignement des sternèbres chez les fœtus | 79 à 150 |
| Produits de pulvérisation (par exemple, peinture en aérosol) (inhalation) (20 ans et plus) | 3,4 à 232 ng/m3 d | DE10 > 5 202 mg/m3 e (exposition intermittente) | Augmentation de l’incidence du défaut d’alignement des sternèbres chez les fœtus | 22 à 1 530 |
| Exposition aiguë par inhalation d’adhésif pour PVC ou d’adhésif et apprêt pour PVC (5 % à 70 %) (20 ans et plus) | 1,5 à 10,0 mg/m3 d | DE10 > 5 202 mg/m3 e (exposition intermittente) | Augmentation de l’incidence du défaut d’alignement des sternèbres chez les fœtus | 520 à 3 468 |
| Exposition aiguë par inhalation découlant de l’utilisation d’adhésif et d’apprêt pour PVC (10 % à 55 %) (20 ans et plus) | 7 à 27 mg/m3 d | DE10 > 5 202 mg/m3 e (exposition intermittente) | Augmentation de l’incidence du défaut d’alignement des sternèbres chez les fœtus | 193 à 743 |
| Adhésifs tout usage (inhalation) (20 ans et plus) | 1,7 à 53 mg/m3 d | DE10 > 5 202 mg/m3 e (exposition intermittente) | Augmentation de l’incidence du défaut d’alignement des sternèbres chez les fœtus | 98 à 3 060 |
| Nettoyant pour le volet de départ et le papillon des gaz des voitures (inhalation) (20 ans et plus) | 0,0035 - 0,0082 mg/m3 d | DE10 > 5 202 mg/m3 e (exposition intermittente) | Augmentation de l’incidence du défaut d’alignement des sternèbres chez les fœtus | 634 390 à 1 486 286 |
| Agent hydrofuge, traitement hydrophobe (par exemple, liquide lave-glace et traitement hydrophobe, en aérosol, pour pare-brise) (inhalation) (20 ans et plus) | 6,28 à 15,7 mg/m3 d | DE10 > 5 202 mg/m3 e (exposition intermittente) | Augmentation de l’incidence du défaut d’alignement des sternèbres chez les fœtus | 331 à 828 |
Abréviations : CE10, limite inférieure de la concentration efficace entraînant un taux de réponse de 10 %; DE05, dose efficace la plus faible (limite inférieure de la confiance à 95 % de la dose efficace [DE]); ME, marge d’exposition.
a Cela comprend l’exposition à la substance par l’air extérieur, l’air intérieur et l’eau potable (Santé Canada, 2024).
b Ajustement molaire, calculé à l’aide de la valeur obtenue par extrapolation (Cox et coll., 1975, mentionné dans l’US EPA, 2003a). Les masses moléculaires sont de 74,12 g/mol pour le butan-2-ol, de 72,11 g/mol pour la MEK et de 86,13 g/mol pour la MPK. ME cible = 100 (× 10 pour l’extrapolation interspécifique; × 10 pour la variation intraspécifique).
c Les absorptions estimatives tiennent compte de la concentration annuelle estimative la plus élevée de MEK dans l’air (voir tableau 7‑1) des installations qui déclarent leurs rejets de cette substance à l’INRP (2021), ainsi que dans d’autres milieux environnementaux (Santé Canada, 2024).
d Moyenne pondérée dans le temps sur 7 h
e Schwetz et coll., 1991, mentionné dans l’US EPA, 2003a. ME cible = 100 (× 10 pour l’extrapolation interspécifique; × 10 pour la variation intraspécifique).
Les ME pour l’exposition à la MEK dans les milieux environnementaux, y compris pour les sous-groupes de la population vivant à proximité d’installations qui déclarent des rejets de cette substance dans l’atmosphère, les aliments (lorsqu’ils utilisent cette substance dans les aliments comme aromatisant alimentaire), les sucettes et les jouets de dentition, sont considérées comme suffisantes pour compenser les incertitudes dans les données recensées sur les effets sur la santé et l’exposition, utilisées pour caractériser les risques. D’après les concentrations estimatives de l’exposition à la MEK par le régime alimentaire, le JECFA (OMS, 1999b) a conclu qu’il n’y avait « aucun souci de sécurité, compte tenu des quantités estimatives ingérées de la substance lorsque celle-ci est utilisée comme aromatisant dans les aliments ».
Les ME calculées pour l’exposition par inhalation aux produits pour les ongles, aux adhésifs tout usage, aux nettoyants pour le volet de départ et le papillon des gaz des voitures, aux adhésifs et aux apprêts pour PVC, ainsi qu’aux agents hydrofuges et traitements hydrophobes (par exemple, liquide lave-glace et traitement hydrophobe, en aérosol, pour pare-brise) sont considérées comme suffisantes. Toutefois, les ME pour l’exposition par inhalation à la MEK présente dans d’autres produits de consommation (c’est-à-dire décapants pour peinture ou revêtement [par exemple, décapants pour laque], dissolvants d’adhésifs, dégraissants, diluants pour peinture ou revêtement, peinture liquide et produits en aérosol, notamment la peinture en aérosol) sont considérées comme insuffisantes pour compenser les incertitudes dans les données recensées sur les effets sur la santé et l’exposition.
L’évaluation des effets sur la santé humaine a tenu compte des sous-groupes de la population canadienne qui, parce qu’ils sont plus sensibles ou davantage exposés, sont plus sujets à subir des effets nocifs pour la santé. Par exemple, nous avons estimé les valeurs d’exposition en fonction de l’âge, notamment chez les nourrissons et les enfants, et avons examiné les études de toxicité pour le développement et la reproduction afin de dégager les effets nocifs qu’il pourrait y avoir pour la santé. De plus, le potentiel d’exposition élevé pour les personnes vivant à proximité d’installations qui pourraient rejeter de la MEK dans l’atmosphère a été pris en compte dans l’évaluation.
MPK
Aucune étude de cancérogénicité concernant la MPK n’a été recensée. Toutefois, la modélisation QSAR n’a dégagé aucune prédiction positive ni alerte structurale associée à la cancérogénicité. En outre, d’après les résultats de plusieurs essais in vitro, la substance n’est pas génotoxique. Dans la seule étude recensée sur la toxicité par voie orale, des effets minimes (un léger ralentissement de la prise de poids corporel) ont été rapportés chez le rat, à la dose la plus élevée de MPK ajoutée à l’eau potable, à laquelle les animaux ont été exposés pendant 13 mois (Bingham et coll., 2001, mentionné dans HSDB, 1983-). La DSENO a été établie à 454 mg/kg p.c./j. En ce qui concerne l’exposition par inhalation, aucun effet nocif, à l’exception d’une légère neurotoxicité transitoire chez les mères pendant l’exposition, n’a été observé dans les études dans lesquelles les CSENO de 5 000 et de 5 300 mg/m3 ont été trouvées (ECHA, c2007-2019a).
La principale source d’exposition de la population générale à la MPK dans les milieux environnementaux et les aliments est alimentaire. D’après les données recensées, la principale source d’exposition par le régime alimentaire à la MPK serait les aliments dans lesquels la substance est présente naturellement.
Une comparaison des concentrations estimatives de l’exposition à la MPK dans les milieux environnementaux (2,3 à 6,8 µg/kg p.c./j) et comme aromatisant dans les aliments (0,7 à 2,0 µg/kg p.c./j) avec la DSENO de 454 mg/kg p.c./j a donné lieu à des ME supérieures à 66 765, considérées comme suffisantes pour compenser les incertitudes dans les données recensées sur les effets sur la santé et l’exposition, utilisées pour caractériser les risques. L’ingestion alimentaire supplémentaire de MPK, de par sa présence naturelle dans les aliments, n’a pas été jugée préoccupante pour la santé humaine. De plus, d’après les concentrations estimatives de l’exposition à cette substance par le régime alimentaire, le JECFA (OMS, 1999 b) a conclu qu’il n’y avait « aucun souci de sécurité, compte tenu des quantités estimatives ingérées de la substance lorsque celle-ci est utilisée comme aromatisant dans les aliments ».
La population générale du Canada pourrait également être exposée à la MPK, principalement par inhalation, lorsqu’elle utilise des produits de consommation dans lesquels la substance est présente, notamment dans la peinture et les produits pour les ongles. Étant donné le faible potentiel de danger de la MPK par inhalation, les risques pour la santé humaine associés à la présence de la substance dans les produits de consommation sont considérés comme faibles.
L’évaluation des effets sur la santé humaine a tenu compte des sous-groupes de la population canadienne qui, parce qu’ils sont plus sensibles ou davantage exposés, sont plus sujets à subir des effets nocifs pour la santé. Par exemple, les valeurs d’exposition ont été estimées en fonction de l’âge, y compris chez les nourrissons et les enfants, et les études de toxicité pour le développement et la reproduction ont été examinées afin de dégager les effets nocifs qu’il pourrait y avoir pour la santé.
7.1.4 Incertitudes dans l’évaluation des risques associés à la MEK et à la MPK pour la santé humaine
Les principales sources d’incertitudes sont présentées dans le tableau 7‑6 ci-dessous.
| Principales sources d’incertitudes | Effet |
|---|---|
| Il est présumé que l’exposition par voie cutanée est minime par rapport à l’exposition par inhalation, étant donné la forte volatilité de la substance. | – |
| Il est présumé que toute la quantité de MEK présente dans les sucettes et les jouets de dentition peut s’échapper du produit. | + |
| Aucune étude de toxicité chronique par voie orale ou par inhalation n’a été trouvée pour la MEK et la MPK. | +/- |
| L’utilisation des données du butan-2-ol pour l’extrapolation à la MEK dans l’évaluation de la toxicité à doses répétées pour la reproduction et le développement. | +/- |
| Aucune donnée n’a été trouvée sur la toxicité de la MEK après une exposition par voie orale à long terme. Toutefois, le butan-2-ol, le principal métabolite de la MEK, a été considéré comme un analogue approprié pour la caractérisation des risques. | +/- |
+ = incertitude pouvant entraîner une surestimation de l’exposition ou des risques; - =incertitude pouvant entraîner une sous-estimation de l’exposition ou des risques; +/ – = potentiel inconnu de surestimation ou de sous-estimation des risques.
7.2 Évaluation des substances du sous-groupe 2 (MIBK, MIAK et DAA)
7.2.1 Évaluation de l’exposition des substances du sous-groupe 2 (MIBK, MIAK et DAA)
Milieux environnementaux
La MIBK a été suivie dans le cadre du programme du RNSPA (ECCC, 2017a). Les concentrations de MIBK dans l’air ambiant ont été mesurées dans 64 stations de surveillance du RNSPA dans l’ensemble du Canada, de 2006 à 2010. Pendant cette période, les concentrations de MIBK moyennes et au 95e centile mesurées sur 24 heures dans les différentes stations variaient respectivement de 0,014 à 0,29 µg/m3 et de 0,08 à 1,05 µg/m3 (ECCC, 2017a).
Les données provenant du HAMN, en Ontario, indiquent que les concentrations de MIBK mesurées dans l’air ambiant, sur plusieurs périodes de 24 heures entre 2015 et 2019, à 3 endroits du secteur industriel de Hamilton, variaient d’une valeur inférieure au seuil de détection fiable (0,41 µg/m3) à un maximum de 6,55 µg/m3. Les concentrations moyennes à ces endroits variaient d’une valeur inférieure au seuil de détection fiable à 0,42 µg/m3 (HAMN, 2020).
Dans les 5 études canadiennes sur la qualité de l’air mentionnées à la section 6.1.1, les concentrations géométriques moyennes de MIBK mesurées dans l’air ambiant variaient d’une valeur inférieure à 0,016 µg/m3 à 0,185 µg/m3, tandis que les concentrations au 95e centile variaient de 0,086 à 0,470 µg/m3 (Zhu et coll., 2005; Santé Canada, 2010a,b, 2012, 2013). La concentration la plus élevée (6,55 µg/m3, selon HAMN) a été utilisée pour estimer les concentrations d’exposition de la population générale. Aucune information ou donnée sur la MIAK ou le DAA dans l’air ambiant au Canada ou ailleurs n’a été trouvée.
Comme la MIBK peut être employée par des installations et que ses rejets dans l’atmosphère au Canada sont déclarés (voir la section 4), le modèle SCREEN3 de l’EPA des États-Unis (1996) a été utilisé pour estimer les concentrations de MIBK dans l’air ambiant attribuables aux rejets de la substance sur place, dans l’atmosphère, par les installations qui l’utilisent, comme le rapporte l’INRP. Les résultats de ces modélisations, soit les concentrations estimatives, sont présentés au tableau 7‑7, et les paramètres d’entrée du modèle, à l’annexe B. La concentration annuelle estimative de MIBK la plus élevée dans l’air ambiant (30 µg/m3) a été utilisée pour estimer empiriquement les valeurs maximales de l’exposition des résidants vivant à proximité d’installations rejetant de la MIBK dans l’atmosphère.
| Paramètre d’exposition | Concentration de MIBK (µg/m3) |
|---|---|
| Concentration maximale sur 1 heure | 1,62 à 150 |
| Concentration maximale sur 24 heuresa | 0,65 à 60 |
| Concentration annuelleb | 0,325 à 30 |
a En supposant que la substance soit rejetée de façon continue sur une période de 24 h et en tenant compte des variations dans la direction du vent pendant cette période, on estime la concentration maximale moyenne sur 24 h en multipliant la concentration maximale sur une heure par un facteur de 0,4 (US EPA, 1992).
b Pour ce qui est des concentrations d’exposition sur une période d’un an, en raison des changements de direction du vent, les concentrations atmosphériques de la substance provenant d’une source de rejet diffuse ne devraient pas varier autant que les celles provenant d’une source de rejet ponctuelle. Dans les conditions météorologiques donnant lieu à une exposition maximale sur 1 h, la substance peut persister plus longtemps. Ainsi, on détermine la concentration maximale sur 1 an en multipliant la concentration maximale sur 1 heure par un facteur de 0,2 (US EPA, 1992).
On a mesuré la MIBK dans l’étude sur l’air intérieur dans le cadre du cycle 2 de l’ECMS, et elle a été détectée dans environ 96 % des échantillons. Dans cette étude (Zhu et coll., 2013), la concentration moyenne géométrique de MIBK était de 0,235 µg/m3, et la concentration au 95e centile était de 1,62 µg/m3 (données pondérées à l’échelle des foyers) (Zhu et coll., 2013). Dans l’étude sur la qualité de l’air intérieur du cycle 2 de l’ECMS, la concentration de MIAK a également été mesurée, mais n’a été détectée que dans 1,45 % des échantillons (seuil de détection de 0,19 µg/m3). Dans l’air intérieur, des concentrations de MIBK et des taux de détection de MIAK similaires ont été observés au cycle 3 de l’ECMS (2012-2013) (Li et coll., 2019).
Les concentrations géométriques moyennes de MIBK recensées dans les 5 études canadiennes sur la qualité de l’air variaient de 0,14 à 1,33 µg/m3, et les concentrations au 95e centile, de 0,33 à 13,82 µg/m3 (Zhu et coll., 2005; Santé Canada, 2010a,b, 2012, 2013). La concentration de MIBK a également été mesurée dans 94 % des 36 échantillons d’air intérieur prélevés dans une étude sur le terrain à Ottawa (concentration maximale de 5,5 µg/m3) et dans 6 % des 54 échantillons d’air intérieur prélevés dans une étude sur le terrain au Nunavik (concentration maximale de 0,6 µg/m3) (Won et coll., 2019).
La concentration de MIAK a été mesurée dans 24 échantillons d’air intérieur prélevés dans une étude sur le terrain menée au Québec : la concentration géométrique moyenne était de 0,23 µg/m3, et la concentration maximale, de 1,51 µg/m3 (Won et Lusztyk, 2011). Le DAA a été mesuré dans 15 % des échantillons d’air intérieur prélevés dans l’étude sur le terrain au Nunavik : la concentration maximale était de 2,4 µg/m3 (Won et coll., 2019).
Les concentrations dans l’air intérieur suivantes ont été utilisées pour estimer avec prudence l’exposition de la population générale : la concentration au 95e centile était de 13,82 µg/m3 pour la MIBK (étude à Windsor), la concentration maximale de 1,51 µg/m3 pour la MIAK (étude au Québec) et la concentration maximale, de 2,4 µg/m3 pour le DAA (étude au Nunavik).
Les concentrations dans les échantillons d’air de la zone respiratoire ont également été mesurées dans l’étude menée à Windsor (Santé Canada, 2010a). Les concentrations géométriques moyennes de MIBK dans l’air de la zone respiratoire pendant l’été et pendant l’hiver étaient respectivement de 1,04 µg/m3 et de 0,23 µg/m3. Les concentrations au 95e centile de MIBK étaient de 7,96 µg/m3 pendant l’été et de 0,99 µg/m pendant l’hiver (Santé Canada, 2010a).
Aucune étude mesurant la concentration de MIBK, de MIAK et de DAA dans l’eau potable au Canada n’a été trouvée. Aucune autre donnée sur la présence de MIAK dans l’eau ailleurs dans le monde n’a été trouvée. Dans une étude menée aux États‑Unis, la MIBK a été détectée dans 3 des 646 échantillons d’eau potable, à des concentrations variant de 16 à 20 µg/L (Grady et Casey, 2001). La MIBK a également été mesurée dans plusieurs études, dans les eaux de surface (Sheldon et Hites, 1978; Hall et coll., 1987; Benfenati et coll., 1992; Bianchi et Varney, 1998). De plus, des concentrations élevées de MIBK ont été observées dans les eaux souterraines, les effluents et le lixiviat à proximité de sites d’enfouissement, d’installations de retraitement des hydrocarbures et d’usines de traitement des eaux usées (Mutch et coll., 1983; Sabel et Clark, 1984; Sawhney et Kozloski, 1984; US EPA, 1988; Canter et Sabatini, 1994; Paxéus, 1996). La valeur maximale de 20 µg/L de MIBK établie dans l’eau potable aux États-Unis a été utilisée pour estimer l’exposition de la population générale à cette substance. On a employé le modèle ChemCan v6.00 (ChemCAN, 2003) pour déterminer les concentrations de MIAK et de DAA dans les eaux de surface à l’aide de données quantitatives provenant du tableau 4‑1 et en supposant que la quantité totale importée était rejetée dans une seule région du pays (c’est-à-dire dans la région des plaines à bois mixtes de l’Ontario). Les concentrations estimatives de la MIAK et du DAA dans les eaux de surface étaient respectivement de 0,15 ng/L et de 46,6 ng/L, et ont été utilisées pour estimer l’absorption de ces substances dans l’eau potable dans la population générale du Canada.
Aucune information ou donnée sur la MIBK, la MIAK ou le DAA dans le sol au Canada n’a été trouvée. Le DAA a été qualitativement détecté dans les sédiments d’un lac en Saskatchewan, au Canada (HSDB, 1983-). À l’aide d’une approche semblable à celle utilisée pour déterminer les concentrations dans les eaux de surface mentionnée ci‑dessus, on a employé le modèle ChemCan (2003) pour estimer les concentrations de MIBK, de MIAK et de DAA dans le sol. Comme les concentrations de MIBK, de MIAK et de DAA dans le sol étaient respectivement de 0,13 µg/kg, de 0,006 µg/kg et de 3,4 ng/kg, l’exposition à ces substances dans le sol est jugée négligeable (absorptions inférieures à 1 ng/kg p.c./j).
Les concentrations estimatives de l’exposition par les milieux environnementaux variaient de 2,7 µg/kg p.c./j chez les personnes âgées de 60 ans et plus à 8 µg/kg p.c./j chez les enfants âgés de 6 mois à 4 ans pour la MIBK; de 0,3 µg/kg p.c./j chez les personnes âgées de 60 ans et plus à 0,9 µg/kg p.c./j chez les enfants âgés de 6 mois à 4 ans pour le MIAK; et de 0,48 µg/kg p.c./j chez les personnes âgées de 60 ans et plus à 1,44 µg/kg p.c./j chez les enfants âgés de 6 mois à 4 ans pour le DAA (Santé Canada, 2024). Pour de plus amples renseignements, veuillez consulter le document de Santé Canada de 2024 recensé dans la bibliographie.
Aliments
La MIBK a été détectée dans diverses denrées alimentaires qui en contiennent naturellement, dont la bière, le brandy, le poulet, les fruits, l’huile d’olive, les œufs, le café et le lait de vache (Nijssen et coll., 1963-2018; Burdock, 2010). La MIBK serait également employée comme aromatisant alimentaire dans les produits de boulangerie, les produits laitiers glacés, les gélatines, les poudings, les produits carnés, les boissons non alcoolisées et les bonbons mous (Burdock, 2010). La MIBK a été détectée (dans 2 échantillons sur douze) dans le lait maternel, mais n’a pas été quantifiée (Pellizzari et coll., 1982).
Le JECFA a également évalué un groupe de 39 alcools aliphatiques acycliques saturés secondaires, des cétones et les esters saturés et insaturés apparentés, dont la MIBK, utilisés comme aromatisants alimentaires (OMS, 1999b). Dans le cadre de cette évaluation, le JECFA a estimé l’apport de MIBK par habitant découlant de l’utilisation de cette substance comme aromatisant alimentaire était de 0,03 µg/kg p.c./j dans la population des États-Unis et de 0,12 µg/kg p.c./j chez les Européens (pour de plus amples renseignements, veuillez consulter l’annexe A). Faute de données sur l’utilisation réelle de cette substance au Canada, les valeurs estimatives de l’apport par habitant sont des valeurs acceptables de l’exposition par le régime alimentaire, le cas échéant, à la MIBK découlant de son utilisation comme aromatisant alimentaire dans la population générale (chez les 1 an et plus).
La MIAK a été détectée dans quelques denrées alimentaires qui en contiennent naturellement, dont le café (0,5 µg/g) et la papaye (0,001 µg/g) (Nijssen et coll., 1963‑2018), ainsi que dans les avelines rôties et le bacon, le bœuf et le porc cuits (HSDB, 1983-). Le DAA a été détecté comme composant naturel dans diverses denrées alimentaires, notamment dans les fruits, les légumes, les produits laitiers, le miel, les noix, les œufs, le poulet et les boissons alcoolisées (Nijssen et coll.,1963-2018).
Aucune exposition ne devrait découler de l’utilisation de MIAK et de DAA comme composants dans la fabrication de matériaux d’emballage alimentaire.
Les estimations quantitatives de l’exposition à la MIBK, à la MIAK et au DAA dans les alimentsNote de bas de page 5 qui en contiennent naturellement variaient de 0,4 µg/kg p.c./j, chez les enfants âgés de 4 à 8 ans, à 32 µg/kg p.c./j, chez les adultes de 19 ans et plus, pour la MIBK, de 0,001 µg/kg p.c./j chez les enfants d’un an, à 3 µg/kg p.c./j chez les adultes de 19 ans et plus, pour la MIAK, et de 0,04 µg/kg p.c./j chez les bébés de 6 à 12 mois, à 4 µg/kg p.c./j chez les enfants de 2 à 3 ans, pour le DAA (pour de plus amples renseignements, veuillez consulter l’annexe C).
Biosurveillance
Lors du cycle 5 de l’ECMS (2016 à 2017), la MIBK a été mesurée dans 73,4 % des échantillons de sang total de 2 363 personnes représentant la population canadienne âgée de 12 à 79 ans (Santé Canada, 2019). L’ECMS est une enquête continue et représentative à l’échelle nationale dans le cadre de laquelle on recueille des données importantes sur la santé et le bien-être ainsi que des échantillons biologiques auprès de personnes de tout le pays. Les valeurs de la moyenne géométrique et du 95e centile des mesures de la MIBK s’élevaient respectivement à 0,04 μg/L et à 0,12 µg/L. Le seuil de détection était de 0,029 µg/L. Ces données appuient la conclusion que la population générale du Canada peut être exposée de manière chronique à la MIBK.
Produits de consommation
MIBK
On a signalé la présence de MIBK comme ingrédient non médicinal dans l’alcool à friction, homologué comme PSN, à usage topique, avec une concentration de 0,98 % (communication personnelle, courriel de la DPSNSO, SC, au BERSE, SC, daté du 16 août 2016; source non citée). À l’aide du logiciel ConsExpo Web (2016), nous avons estimé les expositions par inhalation de MIBK liées à une utilisation de ce produit par les enfants de 6 mois à 4 ans et les adultes de 20 ans et plus. Les paramètres employés dans le modèle sont présentés à l’annexe D. La concentration moyenne par événement, quel que soit le groupe d’âge de ce scénario d’exposition, a été estimée à 0,19 mg/m3, la concentration moyenne le jour de l’exposition, à 2,7 ×10-4 mg/m3, et la moyenne pondérée de 6 heures, à 0,003 mg/m3. Même si l’exposition par voie cutanée pourrait contribuer à l’exposition globale pendant l’utilisation de produits de consommation, on considère que la voie principale est l’inhalation, compte tenu de la forte volatilité de la MIBK. C’est pourquoi nous présenterons seulement des estimations de l’exposition par inhalation.
D’après les déclarations présentées à Santé Canada en vertu du Règlement sur les cosmétiques, la MIBK est utilisée dans certains produits cosmétiques au Canada, tels que les tatouages temporaires et les produits de soins des ongles, notamment les vernis à ongles, les dissolvants de vernis à ongles et les adhésifs pour les ongles (communication personnelle, courriel de la DSPCPD, SC, au BERSE, SC, daté de novembre 2019; source non citée).
Divers autres produits de consommation contiennent de la MIBK, ce qui peut entraîner une exposition de la population générale du Canada (CPID [modifié, 2019]). Seuls les scénarios d’utilisation des produits qui entraînent les niveaux d’exposition potentielle les plus élevés à la MIBK par inhalation sont présentés au tableau 7‑8. Nous avons aussi estimé l’exposition indirecte par voie orale, due à l’utilisation de marqueurs à essuyage à sec, des personnes de 6 mois à 4 ans et de 5 à 11 ans (qui représentent les groupes d’âge les plus exposés). Les estimations de cette exposition par événement se situaient entre 0,16 mg/kg p.c. et 0,48 mg/kg p.c. pour les personnes de 5 à 11 ans et entre 0,32 mg/kg p.c. et 0,97 mg/kg p.c. pour les personnes de 6 mois à 4 ans. Les expositions potentielles ont été estimées au moyen du logiciel ConsExpo Web (2016) ou d’algorithmes pertinents. L’annexe D présente plus de détails.
| Scénario pour le produit | Concentration de MIBK | Concentration moyenne par événement (mg/m3) | Concentration moyenne pondérée de 6 heuresa (mg/m3) |
|---|---|---|---|
| Adhésifs pour les ongles (12 ans et plus)b | de 1 à 3 %c | de 4,1 à 12 | de 0,4 à 1,2 |
| Vernis à ongles (6 mois à 4 ans) | de 0,3 à 1 %c | de 0,42 à 1,4 | de 0,04 à 0,14 |
| Dissolvant de vernis à ongles (12 ans et plus) | de 10 à 30 %c | de 18 à 56 | de 0,4 à 1,2 |
| Dissolvant de vernis à ongles (6 mois à 4 ans) | de 10 à 30 %c | de 11 à 35 | de 0,2 à 0,8 |
| Tatouages temporaires (6 mois et plus) | de 1 à 3 %c | de 0,035 à 0,1 | de 0,0005 à 0,001 |
| Laque pour bois (20 ans et plus) | de 2,5 à 10 %d | de 670 à 2 600 | de 112 à 433 |
| Peinture liquide (à forte teneur en solvant) pour revêtement de plate-forme de camion, appareils (20 ans et plus) | de 10 à 15 %e | de 100 à 150 | de 37 à 55 |
| Produits en aérosol (par exemple, peinture en aérosol) (20 ans et plus) | de 0,4 à 25 %f, g | de 21 à 1 100 | de 1,5 à 76 |
| Remplissage ou mastic en tube (automobile) (20 ans et plus) | de 1 à 5 %h | de 6,7 à 28 | de 1 à 5 |
| Marqueur à essuyage à sec (inhalation) (tous les groupes d’âge) | de 10 à 30 %i | de 1,2 à 3,6 | de 0,1 à 0,45 |
a Les concentrations moyennes pondérées de 6 heures ont été calculées pour tous les scénarios de produit de manière à correspondre aux durées d’exposition de l’étude des effets critiques ayant servi à caractériser le risque. Concentration moyenne pondérée de 6 h = concentration moyenne par événement × durée d’exposition / 6 × 60 min.
b Le scénario porte sur l’utilisation de vernis à ongles ordinaires.
c Communication personnelle, courriels de la DSPCPD, SC, au BERSE, SC, datés d’août 2016, d’avril 2017 et de novembre 2019; source non citée.
d FDS, 2016c.
e FDS, 2021.
f FDS, 2020.
g FDS, 2017a.
h FDS, 2018c.
i FDS, 2015b.
La MIBK a été mesurée dans la poudrette de pneus en caoutchouc recyclés ainsi que dans l’air au-dessus de terrains à gazon synthétique (EPA des É.-U., 2009a; EPA des É.-U. et CDC/ATSDR, 2019; Schneider et coll., 2020a, b). Au Canada, la poudrette de pneus en caoutchouc recyclés peut être utilisée pour le rembourrage ou le revêtement des surfaces des terrains de sport et des terrains de jeu (Cantin, 2009; AR, 2017). Les études qui comprenaient la mesure de la MIBK dans des échantillons d’air prélevés au-dessus de terrains à gazon synthétique ou de terrains de jeux ont été considérées comme les plus pertinentes en ce qui concerne la population générale du Canada. L’EPA des É.-U. (2009a) a effectué une étude exploratoire durant laquelle elle a prélevé des échantillons près de 3 terrains à gazon synthétique et d’un terrain de jeux. Les concentrations mesurées dans l’air allaient de non détectables à 0,13 ppbv (0,53 µg/m3). Schneider et coll. (2020a, b) ont réalisé plusieurs études sur la poudrette de pneus recyclés, qui comprenaient l’analyse d’échantillons de remplissage et la collecte d’échantillons d’air au-dessus de 17 terrains de sport en Europe, y compris une installation intérieure. Ils ont noté que la concentration de MIBK la plus élevée provenait d’une installation extérieure (Schneider et coll., 2020b). La moyenne arithmétique des concentrations de MIBK obtenues pour l’ensemble des installations sportives était de 3,32 µg/m3 (médiane de 0,15 µg/m3) et le 95e centile de la concentration dans l’air s’établissait à 17,85 µg/m3. Cette dernière valeur est inférieure à la concentration annuelle estimée la plus élevée de MIBK dans l’air ambiant (30 µg/m3), laquelle a servi à estimer les valeurs maximales de l’exposition potentielle des résidents vivant à proximité d’installations rejetant de la MIBK dans l’air. Par conséquent, les estimations de l’exposition à la MIBK des personnes pratiquant des sports sur du gazon synthétique ou jouant sur des terrains de jeu recouverts de gazon synthétique seraient inférieures à celles estimées pour les personnes vivant à proximité d’installations déclarant des rejets de MIBK dans l’air.
MIAK
Il a été déterminé que la MIAK était présente dans un stylo de réparation de revêtement automobile, dans une proportion de 3 % à 7 % (FDS, 2015c; CPID [modifié, 2019]). La concentration moyenne par événement calculée par le logiciel ConsExpo Web (ConsExpo, 2016) à laquelle un adulte utilisant un tel stylo contenant de la MIAK est exposé variait de 1,5 mg/m3 à 3,5 mg/m3, tandis que la concentration moyenne pondérée de 6 heures variait de 0,125 mg/m3 à 0,29 mg/m3 (voir l’annexe D pour plus de détails). Même si l’exposition par voie cutanée pourrait contribuer à l’exposition globale pendant l’utilisation de produits de consommation, on considère que la voie principale est l’inhalation, compte tenu de la forte volatilité de la MIAK. C’est pourquoi nous présenterons seulement des estimations de l’exposition par inhalation.
Alcool de diacétone
Selon les déclarations faites à Santé Canada en vertu du Règlement sur les cosmétiques, l’alcool de diacétone est utilisé comme solvant ou agent masquant d’odeur dans certains produits cosmétiques au Canada tels que les traceurs d’yeux autocollants et divers produits de soins pour les ongles, dont les vernis de base, les vernis de finition, les vernis à ongles, les dissolvants de vernis à ongles et les fortifiants pour ongles (communication personnelle, courriels de la DSPCPD, SC, au BERSE, SC, datés d’août 2016, d’avril 2017 et de novembre 2019; source non citée).
Les estimations de l’exposition par inhalation ont été calculées pour certains produits sentinelles (vernis à ongles et traceurs d’yeux autocollants) dont les niveaux d’exposition sont les plus élevés par rapport à des produits semblables. Le tableau 7‑9 résume la plage de concentrations pour différents scénarios de produits ainsi que les estimations de l’exposition par inhalation associée. Des précisions sur la méthode et les paramètres utilisés pour produire les estimations de l’exposition par inhalation aux cosmétiques sont présentées à l’annexe D.
L’exposition à l’alcool de diacétone par voie cutanée découlant de l’utilisation de ces produits est aussi possible et, contrairement aux autres cétones abordées jusqu’à maintenant, est plus probable étant donné la plus faible pression de vapeur et la plus grande hydrosolubilité de la substance. Nous avons trouvé une étude d’absorption cutanée in vitro sur des tissus humains qui a révélé que les quantités d’alcool de diacétone pénétrant la peau après 10 minutes, 60 minutes et 24 heures se chiffraient respectivement à 0,04 %, à 0,15 % et à 5,71 % pour une dose de 25 mg/cm2 (Fasano et McDougal, 2008; ECHA, c2007-2019b). Le tableau 7‑9 présente les expositions systémiques par voie cutanée estimées en supposant une absorption de 6 % par la peau.
| Scénario pour le produit | Concentration maximalea | Concentration moyenne par événement (mg/m3) | Concentration moyenne pondérée de 6 heuresb (mg/m3) | Exposition systémique par voie cutanéec (mg/kg p.c./évén.) |
|---|---|---|---|---|
| Vernis à ongles (12 ans et plus) | 10 % | 3,5 | 0,34 | de 0,014 à 0,016 |
| Vernis à ongles (6 mois à 4 ans) | 10 % | 3,1 | 0,30 | 0,023 |
| Traceur d’yeux autocollant (12 ans et plus) | 30 % | 0,67 | 1,3 | de 0,007 à 0,008 |
Abréviation : évén. = événement.
a Communication personnelle, courriels de la DSPCPD, SC, au BERSE, SC, datés d’août 2016, d’avril 2017 et de novembre 2019; source non citée.
b Les concentrations moyennes pondérées de 6 heures ont été calculées pour tous les scénarios de produit de manière à correspondre aux durées d’exposition de l’étude des effets critiques ayant servi à caractériser le risque. Concentration moyenne pondérée de 6 h = concentration moyenne par événement × durée d’exposition / 6 × 60 min.
c Un facteur d’absorption cutanée de 6 % a été pris en compte.
On a trouvé de l’alcool de diacétone dans des scellants pour filets de tuyaux, des produits à pulvériser, dont des peintures, des agents de nettoyage et des produits automobiles, ainsi que des diluants pour peinture (utilisés pour diluer les laques et nettoyer les brosses). Le tableau 7‑10 résume les scénarios calculés avec le logiciel ConsExpo Web (ConsExpo, 2016) de l’exposition par inhalation et par la peau à l’alcool de diacétone contenu dans des peintures et des produits de bricolage offerts aux consommateurs (détails à l’annexe D).
| Scénario pour le produit | Concentration d’alcool de diacétone | Concentration moyenne par événement (mg/m3) | Dose interne inhalée le jour de l’exposition (mg/kg p.c./jour) | Exposition systémique par voie cutanéea (mg/kg p.c./évén.) |
|---|---|---|---|---|
| Scellant pour filets de tuyau (20 ans et plus) | de 20 à 30 %b | de 35 à 51 | de 1,3 à 2 | de 0,014 à 0,02 |
| Nettoyant pour le volet de départ des voitures (à pulvériser) (20 ans et plus) | de 1 à 30 %c, d | de 13 à 110 | de 0,032 à 0,26 | de 0,013 à 0,38 |
| Décapant (à pulvériser) à peinture ou à marqueur (20 ans et plus) | 7 %e | 71 | 0,22 | 0,089 |
| Peinture en aérosol (20 ans et plus) | de 1 à 5 %f | de 21 à 72 | de 0,085 à 0,28 | de 0,017 à 0,085 |
| Diluant pour peinture époxy (20 ans et plus) | de 5 à 10 %g | de 55 à 71 | de 0,26 à 0,34 | de 0,09 à 0,18 |
a Un facteur d’absorption cutanée de 6 % a été pris en compte.
b FDS, 2013.
c FDS, 2011.
d FDS, 2012b.
e FDS, 2018d.
f FDS, 2012a.
g FDS, 2017b.
On a également trouvé de l’alcool de diacétone dans des marqueurs permanents (CPID [modifié, 2019]; FDS, 2008, 2012c, 2014b). Ces produits peuvent être utilisés par de jeunes enfants et donc, les expositions indirectes par voie orale et par voie cutanée ont été estimées. En raison du peu de données disponibles, nous avons supposé une concentration de 100 % d’alcool de diacétone dans les marqueurs. Les estimations de l’exposition indirecte par voie orale résultant de chaque utilisation de marqueurs permanents se chiffraient à 1,6 et à 3,2 mg/kg p.c. pour les enfants de 5 à 11 ans et de 6 mois à 4 ans, respectivement. Les estimations de l’exposition systémique par voie cutanée quotidienne, fondées sur une absorption cutanée de 6 %, variaient entre 0,002 mg/kg p.c./jour pour les adultes de 20 ans et plus et 0,005 mg/kg p.c./jour pour les enfants de 5 à 11 ans (il est présumé que les enfants de 6 mois à 4 ans n’utilisent pas de marqueurs permanents de façon quotidienne). Toute exposition à l’alcool de diacétone par inhalation résultant de l’utilisation de marqueurs permanents est considérée comme incluse dans les estimations prudentes des expositions par voie orale et par voie cutanée (détails à l’annexe D).
7.2.2 Évaluation des effets sur la santé du sous-groupe 2 (MIBK, MIAK et alcool de diacétone)
La MIBK et la MIAK sont des composés dont la structure est similaire. Elles se distinguent l’une de l’autre par la présence d’un groupe méthyle supplémentaire sur la chaîne carbonée. Sur le plan biologique, elles interagissent et se métabolisent de manière semblable dans l’organisme. Nous avons inclus l’alcool de diacétone dans ce sous-groupe puisqu’il s’agit d’un métabolite principal de la MIBK. Sa clairance métabolique est probablement semblable, et il pourrait être responsable de certains des effets biologiques observés après une exposition à la MIBK. Les effets communs aux 3 produits chimiques comprennent une diminution du poids corporel, une hausse du poids des reins et du foie et une dépression du SNC. Nous n’avons trouvé aucune donnée sur la métabolisation de la MIAK. Toutefois, les similitudes structurales avec la MIBK laissent à penser que ces 2 substances ont des métabolites et des taux métaboliques analogues. Un résumé des données de toxicité pour ce sous-groupe se trouve dans le tableau A-2 de l’annexe A.
7.2.2.1 MIBK
La MIBK a fait l’objet d’un examen par l’OCDE (1996), le PISC (1997), l’EPA des É.-U. (2003b), le CIRC (2013), le National Industrial Chemicals Notification and Assessment Scheme (NICNAS) (2017) et l’ECHA (2019). Ces examens servent de base à la caractérisation des effets sur la santé dans la présente évaluation. Nous avons réalisé une recherche documentaire s’étendant de l’année précédant le rapport d’évaluation initiale de l’ensemble de données de dépistage de l’OCDE (1996) à janvier 2019. D’après une étude de 2 ans sur la cancérogénicité occasionnée par l’inhalation menée par le NTP (2007b) chez 2 espèces de mammifères (le rat et la souris), le CIRC a classifié la MIBK comme faisant partie du groupe 2B, « possiblement cancérogène pour les humains », compte tenu des données probantes suffisantes montrant la cancérogénicité chez les animaux de laboratoire (CIRC, 2013). Dans l’Union européenne (UE), la MIBK est classée par l’ECHA (2019) comme étant « susceptible de provoquer le cancer » (cancérogène 2B). Nous avons utilisé le rapport du CIRC (2013) pour fonder la caractérisation des effets cancérogènes, et le document de l’EPA des É.-U. (2003b) pour fonder la caractérisation des effets non cancérogènes de la MIBK.
Toxicocinétique et métabolisme
La MIBK est rapidement absorbée après une exposition par voie orale, par inhalation ou par voie cutanée (Hjelm et coll., 1990; Hjelm et coll., 1991; Duguay et Plaa, 1995, cité dans EPA des É.-U., 2003b et NTP, 2007b). Le principal métabolite détecté dans le plasma des rats qui ont reçu de la MIBK par gavage est l’alcool de diacétone, et, dans une moindre mesure, le 4-méthyl-2-pentanol (DiVincenzo et coll., 1976; Duguay et Plaa, 1995, cité dans NTP, 2007b et EPA des É.-U., 2003b). Toutefois, le 4-méthyl-2-pentanol a été le principal métabolite (environ 2 fois la quantité d’alcool de diacétone) détecté dans les poumons des rats après une exposition par inhalation. Chez les humains, l’exposition par inhalation à des concentrations de 10 mg/m3, de 100 mg/m3 ou de 200 mg/m3 de MIBK pendant 2 heures a entraîné une rétention pulmonaire d’environ 60 %, avec une clairance sanguine moyenne de 1,6 L/h/kg, et environ 0,04 % de la dose totale a été excrétée sous forme inchangée dans l’urine dans les 3 heures suivant l’exposition (Hjelm et coll., 1990, cité dans NTP, 2007b). En ce qui concerne l’exposition par voie cutanée, le taux d’absorption percutanée de la MIBK chez les cobayes exposés variait de 0,11 μmol/min/cm à 2,0 μmol/min/cm et s’élevait en moyenne à 1,1 μmol/min/cm (Hjelm et coll., 1991, cité dans EPA des É.-U., 2003b).
Cancérogénicité et génotoxicité
Lors d’une étude de l’inhalation sur 2 ans, durant laquelle des souris et des rats mâles et femelles ont été exposés à 0, 450, 900 ou 1 800 ppm (correspondant à environ 0, 1 840, 3 681 et 7 362 mg/m3) pendant 6 heures par jour, 5 jours par semaine, la MIBK a accru les incidences d’adénome hépatocellulaire ainsi que d’adénome hépatocellulaire et de carcinome combinés chez les souris mâles et femelles. Elle a également augmenté les incidences d’adénome des tubules rénaux ainsi que d’adénome des tubules rénaux et de carcinome combinés chez les rats mâles. De plus, elle a causé 2 tumeurs rénales malignes rares de nature mésenchymateuse chez les rattes exposées à la dose élevée, soit une concentration de 7 362 mg/m3 (NTP, 2007b; CIRC, 2013). 2 tumeurs rénales malignes rares de nature mésenchymateuse et une incidence accrue de leucémie à cellules mononucléées ont également été observées chez les rats ayant reçu la dose la plus élevée. Chez les rats, l’incidence et la gravité des effets rénaux, y compris la néphropathie chronique, ont considérablement augmenté. Bien que les changements pathologiques chez les rats mâles correspondent au spectre de la néphropathie induite par l’α2u-globuline et qu’on ait rapporté la formation de gouttelettes hyalines chez les rats mâles exposés à la MIBK dans des études à plus court terme (par exemple, Phillips et coll., 1987; Nemec et coll., 2004, cité dans NTP, 2007b), comme la néphropathie a également été observée chez les rats femelles, le NTP (2007b) a déclaré que des tumeurs rénales pouvaient se développer indépendamment d’un mécanisme de l’α2u-globuline. De surcroît, le CIRC (2013) a déterminé que la pertinence des tumeurs rénales chez les rats pour les humains ne pouvait être exclue.
À la suite de la publication du rapport du NTP (2007b) et de la monographie du CIRC (2013), de récentes études ont indiqué que les tumeurs rénales et hépatiques induites par la MIBK apparaissaient chez les rongeurs par des mécanismes tels que la néphropathie de l’α2u-globuline et le mode d’action médié par le récepteur constitutif des androstanes (RCA), respectivement, qui ne sont pas transposables chez les humains (Borghoff et coll., 2015; Hughes et coll., 2016). Dans un examen de ces données, le NICNAS (2017) a conclu que, bien que des éléments probants appuient la conclusion selon laquelle les tumeurs hépatiques chez les souris résultent de l’activation du RCA, un mécanisme autre que celui mettant en cause l’α2u-globuline pourrait être responsable des tumeurs rénales chez les rats. Cette conclusion a également été étayée dans l’examen de l’ECHA (2019). Cette information, ainsi que l’observation de la leucémie mononucléée chez les rats mâles et des tumeurs rénales de nature mésenchymateuse chez les rats femelles, étayent la conclusion selon laquelle les tumeurs chez les rats sont transposables chez les humains et suffisantes pour classer la MIBK parmi les cancérogènes de catégorie 2 selon le Système général harmonisé de classification et d’étiquetage des produits chimiques (SGH).
De nombreuses études in vivo et in vitro permettent de conclure que la MIBK n’est pas génotoxique (NTP, 2007b; CIRC, 2013; ECHA, 2019).
Toxicité à doses répétées
L’exposition répétée à la MIBK par inhalation et par voie orale a été associée à des effets sur le poids du foie et des reins, les paramètres biochimiques ou le SNC des rats et des souris, à partir d’une concentration de 410 mg/m3 (MacEwen et coll., 1971; Phillips et coll., 1987; David et coll., 1999, tous cités dans EPA des É.-U., 2003b).
Dans le cadre de l’étude sur 2 ans de l’inhalation par des souris et des rats mâles et femelles décrite plus haut, la CMENO associée à des effets chroniques non cancérogènes de la MIBK a été établie à la plus faible dose mise à l’essai (1 843 mg/m3), d’après une néphropathie minime à légère (NTP, 2007b).
Dans une étude de toxicité subchronique par voie orale, des rats mâles et femelles ont reçu une dose de 0, de 50, de 250 ou de 1 000 mg/kg p.c./jour de MIBK par gavage pendant 13 semaines (MAI, 1986, cité dans EPA des É.-U., 2003b et PISC, 1990). Des modifications dans une série de paramètres de chimie clinique indiquant des effets hépatiques et rénaux ont été observées chez les mâles et les femelles à la plus forte dose; une augmentation du poids absolu et relatif des reins a aussi été observée chez les 2 sexes à 250 mg/kg p.c./jour et plus. Il y a eu une incidence accrue de néphropathie légère chez les mâles à 1 000 mg/kg p.c./jour. On n’a noté aucun effet à 50 mg/kg p.c./jour, valeur que le PISC (1990) et le CIRC (2013) ont déterminée comme étant la dose sans effet observé (DSEO). Cependant, l’EPA des É.-U. (2003b) considère 1 000 mg/kg p.c./jour comme une DSENO, ce qui laisse entendre que les effets observés ont été difficiles à interpréter et pourraient ne pas être néfastes biologiquement compte tenu de l’absence de changements histopathologiques clairs. L’EPA des É.-U. a également établi que la DSENO pour une étude de la toxicité par voie orale dans l’eau potable était d’environ 1 000 mg/kg p.c./jour, d’après l’incertitude entourant la nocivité biologique des effets rénaux observés (Institut de recherche de l’Université Carnegie-Mellon, 1977a, b, cité dans EPA des É.-U., 2003b).
À la lumière des incertitudes entourant la nocivité des effets observés dans les études de toxicité subchronique par voie orale, la CMENO de 1 843 mg/m3, déterminée à partir de l’étude par inhalation plus récente et complète du NTP (2007b), a été extrapolée à une dose orale de 102 mg/kg p.c./jour aux fins de la caractérisation du risque après une exposition par voie orale de longue durée. L’extrapolation d’une voie à l’autre est jugée appropriée pour les effets internes critiques sur les reins des rats mâles et femelles.
Dans une étude d’exposition par voie cutanée sur 4 mois, on a appliqué de la MIBK sur la queue (les 2 tiers inférieurs) d’un nombre indéfini de rats blancs mâles, chaque jour (à raison de 4 h/jour) à des doses de 300 ou 600 mg/kg. Ces doses ont provoqué des changements morphologiques de la peau, du cerveau, du foie, de la glande surrénale, de la rate et des testicules ainsi qu’une réduction du nombre de spermatocytes, de spermatides et de spermatozoïdes (Malysheva, 1988, cité dans NTP, 2007b).
Toxicité pour la reproduction et le développement
Dans une étude sur la toxicité pour la reproduction et le développement occasionnée par l’inhalation, des groupes de 35 rattes F344 et de 30 souris CD 1 gravides ont été exposés pendant les JG 6 à 15 à des concentrations de MIBK respirable de 0, de 300, de 1 000 ou de 3 000 ppm (0, 1 229, 4 106 et 12 292 mg/m3) (Tyl et coll., 1987, cité dans EPA des É.-U., 2003b et PICS, 1990). Chez les rats, on a observé des signes de toxicité maternelle à 12 292 mg/m3, dont une diminution du gain de poids corporel et de la consommation alimentaire (avec retour à la normale dès la cessation de l’exposition) et une augmentation du poids relatif des reins. Le poids corporel des mères est resté inchangé chez les souris, quoiqu’un accroissement de la mortalité et des poids relatif et absolu du foie aient été observés chez les mères exposées à 12 292 mg/m3 de MIBK. D’autres effets chez les mères, dont l’hypoactivité, l’ataxie et le larmoiement, ont été observés à cette dose. Chez les rats, le poids corporel des fœtus a diminué à 1 229 mg/m3 et à 12 292 mg/m3, mais pas à 4 106 mg/m3; les auteurs de l’étude ont attribué cette observation aux différences dans la taille des portées, et non pas à l’exposition. Le poids corporel des fœtus a aussi diminué chez les souris, à la plus forte concentration. À 12 292 mg/m3, on a constaté des retards dans certains paramètres d’ossification du squelette (considérés comme étant réversibles à mesure de la croissance des petits), tant chez les rats que chez les souris. Comme nous l’avons mentionné plus haut relativement à la MEK, la dépression du SNC observée chez les individus gravides pendant l’exposition peut avoir influencé les effets observés chez la progéniture. En se fondant sur cette étude, l’EPA des É.-U. (2003b) a établi une CSENO de 4 106 mg/m3 et une CMENO de 12 292 mg/m3 étant donné les effets chez les mères et l’ossification fœtale du squelette retardée chez les rats et les souris. Une CSENOCEH de 1 026 mg/m3 a également été dérivée pour l’exposition continue (CMENOCEH = 3 073 mg/m3).
Dans une étude portant sur 2 générations, des rats SD ont été exposés à des concentrations de MIBK de 0, 500, 1 000 et 2 000 ppm (0, 2 050, 4 100 et 8 200 mg/m3, respectivement) avant et pendant l’accouplement, tout au long de la gestation et durant le sevrage (Nemec et coll., 2004). Aux doses de 4 100 et de 8 200 mg/m3, il a été observé que la réponse à un stimulus sonore était nulle ou réduite chez les groupes F0. À la dose la plus élevée, les petits ont présenté des signes cliniques de neurotoxicité ou de toxicité neuromusculaire (balancement, chancellement, dandinement, prostration, paupières mi-closes). D’autres effets (principalement observés à la dose de 8 200 mg/m3) comprenaient une augmentation du poids du foie, des vésicules séminales, des reins, des ovaires et des glandes surrénales. À 4 100 et 8 200 mg/m3, une néphropathie a été observée chez les mâles. La DSENO relative à la toxicité systémique chez les parents a été considérée comme étant de 2 050 mg/m3 (effet sédatif aigu). La DSENO associée à la toxicité néonatale (basée sur les signes cliniques de neurotoxicité ou de toxicité neuromusculaire) a également été établie à 4 100 mg/m3. La DSENO pour la toxicité reproductive a été considérée comme étant de 8 200 mg/m3 (Nemec et coll., 2004, cité dans ECHA, 2019).
Toxicité à court terme et aiguë
La MIBK s’est révélée peu toxique après une exposition aiguë par voie orale, par voie cutanée et par inhalation (Smyth et coll., 1951, 1956; Batyrova, 1973; Zakhari et coll., 1977; RTECS, 1987). Des effets neurologiques (surtout des changements comportementaux attribués à la dépression du SNC) ont été observés lors de plusieurs études sur des animaux de laboratoire à des concentrations aussi faibles que 200 mg/m3 (Geller et coll., 1979; De Ceaurriz et coll., 1981; David et coll., 1999; ECHA, 2019). Cependant, certains effets neurologiques ont généralement diminué lorsque l’exposition se prolongeait. De même, dans des études auprès de volontaires humains, des symptômes liés au SNC (maux de tête, nausées, vertiges) et une irritation réversibles ont été signalés à des concentrations aussi faibles que 200 mg/m3 (Hjelm et coll., 1990; Iregren et coll., 1993).
7.2.2.2 MIAK
La MIAK n’a pas été évaluée par d’autres organismes. L’évaluation suivante des dangers est basée sur l’information trouvée dans un dossier d’inscription de l’ECHA (ECHA, c2007-2019c). Un examen documentaire a également été effectué jusqu’en juin 2017, et des recherches ciblées dans la littérature ont été faites jusqu’en janvier 2020. Des renseignements supplémentaires ont été intégrés au présent rapport lorsqu’ils étaient utiles.
Toxicocinétique
On a rapporté que la clairance de la MIAK après une administration par voie orale était plus lente qu’après une exposition par inhalation. Les résultats d’une étude d’absorption cutanée in vitro (LD 428 de l’OCDE) indiquent que l’absorption cutanée est modérée (ECHA, c2007-2019c).
Cancérogénicité et génotoxicité
Aucune étude sur la toxicité chronique de la MIAK n’a été trouvée. Une variété d’études in vitro ont donné comme résultat que la MIAK n’était pas génotoxique (ECHA, c2007-2019c).
Toxicité à doses répétées
Lors d’une étude sur l’exposition par inhalation subchronique, des rats SD ont été exposés à des vapeurs de MIAK à des concentrations de 0, de 200, de 1 000 et de 2 000 ppm (ce qui équivaut à 0, à 934, à 4 670 et à 9 340 mg/m3), pour un total de 69 expositions échelonnées sur 96 jours. On n’a pas observé de changements importants sur les plans du poids corporel, de l’hématologie, de la chimie clinique sérique ou de la pathologie clinique. Des augmentations statistiquement significatives du poids absolu et relatif du foie en fonction de la dose ont été observées chez les mâles et les femelles à des concentrations de 4 670 et de 9 340 mg/m3. On a aussi observé une hausse du poids absolu et relatif des reins chez les mâles à ces concentrations, et, à la dose la plus forte, le poids relatif des reins des femelles était élevé. L’histopathologie a révélé la formation de gouttelettes hyalines dans les reins des rats mâles, ainsi qu’une hypertrophie des hépatocytes dans le foie et une régénération de l’épithélium tubulaire dans les reins des mâles et des femelles exposés à la MIAK aux 2 concentrations les plus élevées. De manière globale, on a déterminé que la concentration sans effet observé (CSEO) était de 200 ppm (934 mg/m3) en fonction des changements de poids des organes et des changements histologiques observés dans le foie et les reins des mâles et des femelles à 4 670 mg/m3 ou plus (Katz et coll., 1986; ECHA, c-2007-2019c).
Au chapitre de l’exposition par voie orale, nous n’avons trouvé qu’une seule étude d’exposition par voie orale à doses répétées dans laquelle seule une très forte dose a été testée (2 000 mg/kg p.c./jour). On y a associé un large éventail d’effets, principalement rénaux et hépatiques (ECHA, c2007-2019c).
À la lumière des limites de la seule étude sur la toxicité à doses répétées par voie orale, nous avons établi une DSEO par voie orale de 52 mg/kg p.c./jourNote de bas de page 8 en effectuant une extrapolation d’une voie à l’autre à partir de l’étude d’inhalation, en nous fondant sur les effets similaires sur le foie et les reins associés aux 2 voies d’exposition.
Nous n’avons trouvé aucune étude sur la toxicité de la MIAK à doses répétées par voie cutanée.
Toxicité à court terme et aiguë
L’exposition de rats SD mâles et femelles à 1 000 ou à 2 000 ppm (4 670 ou 9 340 mg/m3, respectivement) de MIAK par inhalation pour un total de 12 expositions sur 16 jours a provoqué une légère augmentation en fonction de la dose des poids absolu et relatif du foie des rats sans effets correspondants sur les chimies cliniques sériques ou l’histopathologie. À 9 340 mg/m3, la formation de gouttelettes hyalines a été notée dans les reins des mâles, tout comme une minéralisation du cœur des femelles (Anonyme, 1983; Katz et coll., 1986, cité dans ECHA, c-2007-2019c). Sur la base de ces observations, les auteurs ont déterminé une CSENO de 1 000 ppm (4 670 mg/m3).
Une toxicité maternelle a également été observée à de plus faibles doses dans l’étude sur le développement mentionnée ci-dessous. Les mères exposées à 3 503 mg/m3 et plus de MIAK pendant 14 jours ont affiché des fluctuations pondérales et des effets neurologiques importants (c’est-à-dire une moindre réactivité aux stimuli). À la dose la plus élevée (7 005 mg/m3), des diminutions significatives du poids corporel moyen, du gain de poids corporel moyen et de la consommation alimentaire moyenne correspondante ont également été observées. La CSENO relative à la toxicité maternelle a été fixée à 3 505 mg/m3, et la CSENO associée aux effets neurologiques (dépression du SNC) a été considérée par les auteurs de l’étude comme étant de 380 ppm (1 775 mg/m3) (ECHA, c-2007-2019c).
L’exposition de 6 souris Swiss OF1 à des concentrations de 1 942, 3 190, 4 871 ou 7 075 mg/m3 pendant 15 minutes a entraîné une dépression respiratoire liée à la dose (De Ceaurriz et coll., 1984). À la plus faible dose mise à l’essai, une diminution de 27 % de la respiration a été observée, ce qui peut constituer un marqueur de la dépression générale du SNC.
Toxicité pour la reproduction et le développement
Dans une étude de dépistage de la toxicité de l’exposition par inhalation pour la reproduction ou le développement chez le rat, la MIAK n’a eu aucune incidence sur un ensemble de paramètres étudiés chez les parents ou les petits; la substance n’a donc pas été jugée toxique sur le plan de la reproduction jusqu’à concurrence de la plus forte concentration analysée, soit 5 000 mg/m3 (ECHA, c2007-2019c). Dans le cadre d’une étude prolongée de toxicité pour la reproduction sur une génération, des rats mâles et femelles ont été exposés par inhalation (corps entier) à des concentrations de MIAK de 0, 380, 750 ou 1 500 ppm (équivalant à 0, 1 775, 3 503 ou 7 005 mg/m3) pendant 6 h/jour. Aucun effet sur le rendement reproducteur n’a été observé. Le seul effet noté a été une diminution du poids corporel moyen de la progéniture et des gains de poids corporel à la dose de 7 005 mg/m3. En se fondant sur cet effet, les auteurs de l’étude ont déterminé que la CSENO relative à la toxicité néonatale était de 3 503 mg/m3 (ECHA, c2007-2019c).
Dans une étude sur la toxicité de la MIAK pour le développement prénatal, des rattes SD gestantes ont été exposées par inhalation (corps entier) à des concentrations de 0, de 380, de 750 ou de 1 500 ppm (concentrations équivalentes à 0, à 1 775, à 3 503 et à 7 005 mg/m3) pendant les JG 6 à 19. Dans le groupe exposé à 7 005 mg/m3, des diminutions importantes du poids corporel moyen, du gain de poids corporel moyen et de la consommation alimentaire moyenne correspondante ont été observées chez les rattes tout au long de la période d’exposition, tandis qu’une réactivité réduite aux stimuli sonores a été constatée à des concentrations de 3 503 ou de 7 005 mg/m3. La CSENO pour la toxicité maternelle a été fixée à 1 775 mg/m3. Aucune malformation externe, viscérale ou squelettique ni variation du développement associée à l’exposition n’a été observée chez les fœtus jusqu’à concurrence de 7 005 mg/m3. Toutefois, on a noté une réduction considérable du poids des fœtus dans le groupe exposé à la dose la plus élevée comparativement au groupe témoin. Ainsi, la CSENO relative à la toxicité pour le développement a été fixée à 3 503 mg/m3 (ECHA, c2007-2019c). Dans une autre étude sur le développement, des lapines gravides exposées à la MIAK ont présenté des effets de toxicité maternelle similaires, et des malformations cardiaques ont été observées chez 3 petits issus de portées distinctes (ces malformations n’étaient pas considérées par les auteurs comme une conséquence secondaire non spécifique de la toxicité maternelle). La CSENO pour la toxicité maternelle et la toxicité pour le développement a été établie à 5 837 mg/m3 (ECHA, c2007-2019c).
7.2.2.3 Alcool de diacétone
L’alcool de diacétone a fait l’objet d’une étude par l’OCDE (2000). Cette étude a servi de base à la caractérisation des effets sur la santé dans la présente évaluation. Nous avons réalisé une recherche documentaire s’étendant de l’année précédant le rapport d’évaluation initiale de l’ensemble de données de dépistage de l’OCDE (2000) à janvier 2020.
Toxicocinétique et métabolisme
La faible masse moléculaire, la faible valeur du log Koe et l’état physique de l’alcool de diacétone favorisent son absorption par différentes voies d’exposition (orale, cutanée et inhalation). Les données disponibles portent à croire que l’absorption par voie cutanée et par inhalation est importante. Dans une étude d’absorption cutanée in vitro, la pénétration de la peau s’est chiffrée à 0,04 %, à 0,15 % et à 5,71 % de la dose (25 mg/cm2) après 10 minutes, 60 minutes et 24 heures, respectivement (Fasano et McDougal, 2008). Comme mentionné plus haut, l’alcool de diacétone est un métabolite direct de la MIBK.
Cancérogénicité et génotoxicité
Aucune étude sur la cancérogénicité de l’alcool de diacétone n’a été trouvée. L’alcool de diacétone s’est révélé non génotoxique dans divers essais in vitro : d’Ames, essais de mutation génétique sur des mammifères et essais d’aberration chromosomique sur des mammifères (OCDE, 2000; ECHA, c2007-2019b).
Toxicité à doses répétées
Dans une étude combinée de toxicité à doses répétées et de dépistage de la toxicité pour la reproduction et le développement, on a administré par gavage de l’alcool de diacétone quotidiennement pendant 45 jours à des rats SD mâles et femelles à des doses de 0, de 30, de 100, de 300 ou de 1 000 mg/kg p.c./jour (Ministère de la santé et du bien-être, 1997, cité dans OCDE, 2000). Une baisse de l’activité locomotrice et de la réponse aux stimulations a été observée à 300 et à 1 000 mg/kg p.c./jour chez les 2 sexes, alors qu’on a noté des modifications des paramètres de chimie hématologique et sanguine à 1 000 mg/kg p.c./jour chez les mâles. Toujours chez les mâles, on a observé des effets rénaux, dont la formation de gouttelettes hyalines à 100 mg/kg p.c./jour et plus, des tubules basophiles à 300 mg/kg p.c./jour et plus et une dilatation des tubules distaux à 1 000 mg/kg p.c./jour. À 300 et à 1 000 mg/kg p.c./jour, les femelles présentaient une dilatation des tubules distaux et une dégénérescence graisseuse de l’épithélium tubulaire proximal des reins. Selon l’OCDE, les DSENO pour la toxicité à doses répétées sont de 30 mg/kg p.c./jour chez les mâles et de 100 mg/kg p.c./jour chez les femelles. Toutefois, comme la formation de gouttelettes hyalines est considérée comme uniquement propre aux rats mâles (et non biologiquement transposable à l’humain), la DSENO a été fixée à 100 mg/kg p.c./jour.
Dans une étude d’inhalation, des rats Wistar ont été exposés quotidiennement pendant 6 semaines à des concentrations de 0, de 233, de 1 041 et de 4 685 mg/m3 d’alcool de diacétone (Butterworth et coll., 1980, cité dans ECHA, c2007-2019b). Les auteurs ont convenu d’une CSENO de 4 685 mg/m3 et d’une CSEO de 1 041 mg/m3. Seuls des changements dans le poids du foie, non associés à des modifications histologiques, ont été observés à 1 041 mg/m3. À 4 685 mg/m3, on a observé chez les mâles une augmentation du poids du foie et des reins ainsi que des gouttelettes hyalines éosinophiles propres aux rats dans les cellules tubulaires. L’OCDE a jugé que la concentration moyenne était une CSENO (1 035 mg/m3 selon les rapports) (SHELL Research Ltd., 1979, cité dans OCDE, 2000).
Aucune étude de toxicité à doses répétées par voie cutanée n’était disponible pour l’alcool de diacétone. Par conséquent, la DSENO par voie orale de 100 mg/kg p.c./jour servira à cerner le risque posé par l’exposition par voie cutanée.
Toxicité pour la reproduction et le développement
Les auteurs de l’étude de la toxicité à doses répétées combinée à l’étude de dépistage de la toxicité pour la reproduction et le développement décrite ci-dessus ont constaté une diminution des paramètres de reproduction (indice de fertilité, nombre d’implantations et indice d’implantation) et des paramètres du développement (nombre de petits nés, indice de mise bas, indice de naissances vivantes, nombre de petits vivants et indice de viabilité) à la plus forte dose, soit 1 000 mg/kg p.c./jour. Même si aucun de ces changements n’était statistiquement significatif, on a considéré que l’alcool de diacétone pourrait causer des effets sur la reproduction et le développement à 1 000 mg/kg p.c./jour. Sur cette base, les auteurs ont convenu d’une DSENO de 300 mg/kg p.c./jour pour les effets sur la reproduction et le développement, avec une DSENO parentale de 100 mg/kg p.c./jour, conformément à la description ci-dessus (Ministère de la santé et du bien-être, 1997, cité dans OCDE, 2000). Dans une autre étude sur le développement des rats, aucun effet n’a été observé jusqu’à concurrence de 1 000 mg/kg pc/jour (ECHA, c2007-2019b).
En l’absence d’études de la toxicité de l’alcool de diacétone sur la reproduction et le développement par inhalation et par voie cutanée, nous avons utilisé une DSENO par voie orale de 300 mg/kg p.c./jour, relative aux effets sur la reproduction et le développement, pour caractériser le risque.
Effets chez les humains
Des volontaires humains (environ 12, hommes et femmes) exposés à 475 mg/m3 d’alcool de diacétone pendant 15 minutes dans une enceinte ont fait part de maux de tête, de nausées ou de vomissements (Silverman et coll., 1946, cité dans OCDE, 2000).
7.2.3 Caractérisation des risques posés par les substances du sous-groupe 2 (MIBK, MIAK et alcool de diacétone)
MIBK
Selon le CIRC (2013), la MIBK est un cancérogène de catégorie 2B (« possiblement cancérogène pour les humains ») d’après les incidences accrues de tumeurs dans les études de 2 ans sur des rats et des souris. Elle est également classée comme un cancérogène 2 H351 (« susceptible de provoquer le cancer ») par l’ECHA (2019). Bien que des éléments probants aient indiqué que ces tumeurs hépatiques et rénales puissent ne pas être transposables chez les humains, de récentes analyses du NICNAS (2017) ont permis de conclure que, même si des éléments probants étayent la conclusion que les tumeurs hépatiques chez les souris résultent de l’activation du RCA, un mécanisme autre que celui mettant en cause l’α2u-globuline pourrait être à l’origine des tumeurs rénales chez les rats. Cette information ainsi que l’observation de la leucémie mononucléée chez les rats mâles et des tumeurs rénales de nature mésenchymateuse chez les rats femelles étayent la conclusion du NICNAS selon laquelle ces tumeurs chez le rat sont transposables chez l’humain et sont suffisantes pour classer la MIBK comme un cancérogène de catégorie 2 selon le SGH (NICNAS, 2017). Cette conclusion a également été étayée dans un examen récent de l’ECHA (2019). Toutefois, on ne prévoit pas que la MIBK soit génotoxique (NTP, 2007b; CIRC, 2013; ECHA, 2019).
La CMENO pour les effets non cancérogènes de l’inhalation chronique a été établie à 1 843 mg/m3, sur la base d’une néphropathie de minime à légère dans l’essai biologique de 2 ans (NTP, 2007b). Les effets rénaux ont été utilisés comme point de départ pour caractériser le risque pour la santé humaine causé par une exposition chronique, et sont considérés comme adéquats pour prévenir la survenue d’effets cancérogènes potentiels chez l’humain.
Les données disponibles des études d’inhalation de MIBK à court terme chez les animaux indiquent que les effets sur le développement ont été les effets critiques sur la santé. Une CSENO de 4 106 mg/m3 a été déterminée pour les effets sur le développement des souris et des rats (Tyl et coll., 1987, cité dans EPA des É.-U., 2003b). On a calculé une CSENOCEH correspondante pour les effets sur le développement de 1 026 mg/m3 pour l’exposition continue.
En ce qui concerne la voie orale, à la lumière des incertitudes entourant la nocivité des effets observés dans les études de toxicité subchronique par voie orale, nous avons converti la CMENO établie lors de l’étude par inhalation plus récente et complète du NTP (2007b) en une dose de 102 mg/kg p.c./jour (modifiée pour une exposition continue) aux fins de la caractérisation du risque associé à une exposition par voie orale de longue durée. L’extrapolation d’une voie à l’autre est jugée appropriée pour les effets critiques sur les reins des rats mâles et femelles. En outre, cette démarche est considérée comme permettant de prévenir la survenue d’effets cancérogènes potentiels à des doses plus élevées.
Dans la seule étude par voie cutanée disponible, la MIBK a entraîné des changements morphologiques à la peau et à de multiples organes des rats qui ont reçu des doses de 300 mg/kg p.c./jour et plus pendant 4 mois (Malysheva, 1988, cité dans NTP, 2007b). Malgré le peu de détails disponibles pour cette étude, le niveau d’effet critique de 300 mg/kg p.c/jour est appuyé par les effets observés chez les rats ayant reçu 250 mg/kg p.c./jour par voie orale pendant 13 semaines.
Les principales sources d’exposition de l’ensemble de la population à la MIBK par les milieux environnementaux (air extérieur, air intérieur et eau potable) et les aliments sont l’air et l’alimentation. D’après les données disponibles, on s’attend à ce que la plus grande exposition par le régime alimentaire à la MIBK provienne des aliments dans lesquels la substance est naturellement présente. L’absorption de MIBK en raison de sa présence naturelle dans les aliments n’a pas été jugée préoccupante pour la santé humaine.
La MIBK est utilisée dans un certain nombre de produits de consommation, dont l’alcool à friction, les marqueurs à essuyage à sec et divers produits de peinture et de bricolage. Le tableau 7‑11 présente toutes les valeurs d’exposition et les effets critiques sur la santé pertinents, ainsi que les marges d’exposition (ME), obtenues pour la caractérisation des risques de la MIBK.
| Scénario d’exposition | Exposition | Niveau d’effet critique | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Milieux environnementauxa (tous les groupes d’âge) | de 2,7 à 8 µg/kg p.c./ jour | DMENO = 102 mg/kg p.c./jourb | Effets rénaux chez les rats (hyperplasie, néphropathie, minéralisation) dans une étude de 2 ans (extrapolation de voie à voie à partir d’une étude sur l’inhalation, modifiée en fonction d’une exposition continue) | de 12 750 à 37 778 |
| Milieux environnementaux pour les personnes vivant près d’installations rejetant de la MIBKc (tous les groupes d’âge) | de 6,07 à 18,26 µg/ kg p.c./jour |
DMENO = 102 mg/kg p.c./jourb | Effets rénaux chez les rats (hyperplasie, néphropathie, minéralisation) dans une étude de 2 ans (extrapolation de voie à voie à partir d’une étude sur l’inhalation, modifiée en fonction d’une exposition continue) | de 5 586 à 16 804 |
| Aromatisant alimentaire (1 an et plus) | de 0,03 à 0,12 µg/ kg p.c./jour |
DMENO = 102 mg/kg p.c./jourb | Effets rénaux chez les rats (hyperplasie, néphropathie, minéralisation) dans une étude de 2 ans (extrapolation de voie à voie à partir d’une étude sur l’inhalation, modifiée en fonction d’une exposition continue) | ≥ 850 000 |
| Alcool à friction (par inhalation) (6 mois et plus) | 0,003 mg/m3 d | CSENO = 4 106 mg/m3 e | Variations au niveau du squelette des souris et des rats et réduction du poids corporel des fœtus et mortalité fœtale accrue chez les souris | 1 369 000 |
| Produits pour les ongles (par inhalation) (6 mois et plus) | de 0,04 à 1,2 mg/m3 d | CSENO = 4 106 mg/m3 e | Variations au niveau du squelette des souris et des rats et réduction du poids corporel des fœtus et mortalité fœtale accrue chez les souris | de 3 422 à 102 650 |
| Tatouages temporaires (par inhalation) (6 mois et plus) | de 0,0005 à 0,001 mg/m3 d | CSENO = 4 106 mg/m3 e | Variations au niveau du squelette des souris et des rats et réduction du poids corporel des fœtus et mortalité fœtale accrue chez les souris | de 4 106 000 à 8 212 000 |
| Laque pour bois (par inhalation) (20 ans et plus) | de 112 à 433 mg/m3 d | CSENO = 4 106 mg/m3 e | Variations au niveau du squelette des souris et des rats et réduction du poids corporel des fœtus et mortalité fœtale accrue chez les souris | de 9 à 37 |
| Peinture liquide (à forte teneur en solvant) pour camions (par inhalation) (20 ans et plus) | de 37 à 55 mg/m3 d | CSENO = 4 106 mg/m3 e | Variations au niveau du squelette des souris et des rats et réduction du poids corporel des fœtus et mortalité fœtale accrue chez les souris | de 75 à 111 |
| Produits en aérosol (par exemple, peinture en aérosol) (par inhalation) (20 ans et plus) | de 1,5 à 76 mg/m3 d | CSENO = 4 106 mg/m3 e | Variations au niveau du squelette des souris et des rats et réduction du poids corporel des fœtus et mortalité fœtale accrue chez les souris | de 54 à 2 737 |
| Remplissage ou mastic en tube (par inhalation) (20 ans et plus) | de 1 à 5 mg/m3 d | CSENO = 4 106 mg/m3 e | Variations au niveau du squelette des souris et des rats et réduction du poids corporel des fœtus et mortalité fœtale accrue chez les souris | de 821 à 4 106 |
| Marqueurs à essuyage à sec (par événement) [par voie orale] | de 0,16 à 0,48 mg/kg p.c. (5 à 11 ans) | DMEO = 300 mg/kg p.c./jourf | Changements morphologiques dans plusieurs tissus à la plus faible dose analysée dans une étude par voie cutanée de 4 mois | de 625 à 1 875 |
| Marqueurs à essuyage à sec (par événement) [par voie orale] | de 0,32 à 0,97 mg/kg p.c. (6 mois à 4 ans) | DMEO/DSENO = 250 mg/kg p.c./jourg | Effets hépatiques et rénaux à 1 000 mg/ kg p.c./jour dans une étude par voie orale de 13 semaines |
de 258 à 782 |
| Marqueurs à essuyage à sec [par inhalation] (tous les groupes d’âge) | de 0,1 à 0,45 mg/m3 d | CSENO = 4 106 mg/m3 e | Variations au niveau du squelette des souris et des rats et réduction du poids corporel des fœtus et mortalité fœtale accrue chez les souris | de 9 124 à 41 060 |
Abréviations : CSENO = concentration sans effet nocif observé; DMENO = dose minimale avec effet nocif observé; DMEO = dose minimale avec effet observé; DSENO = dose sans effet nocif observé; ME = marge d’exposition.
a Cette catégorie comprend l’exposition à l’air extérieur, à l’air intérieur et à l’eau potable (Santé Canada, 2024).
b NTP, 2007b. ME cible = 1 000 (x 10 pour l’extrapolation interspécifique; x 10 pour les variations intraspécifiques; x 10 pour l’utilisation d’une DMENO, compte tenu de la gravité de l’effet).
c L’absorption estimée tient compte de la plus forte concentration annuelle estimée de MIBK dans l’air (voir le tableau 7‑7) associée aux installations qui déclarent leurs rejets de substances à l’INRP (2021), ainsi que celle provenant d’autres milieux environnementaux (Santé Canada, 2024).
d Les concentrations moyennes pondérées de 6 heures ont été calculées pour tous les scénarios de produit de manière à correspondre aux durées d’exposition de l’étude des effets critiques ayant servi à caractériser le risque.
e Tyl et coll., 1987, cité dans EPA des É.-U., 2003b. ME cible = 100 (x 10 pour l’extrapolation interspécifique; x 10 pour les variations intraspécifiques).
f Malysheva, 1988, cité dans NTP, 2007b.
g MAI, 1986, cité dans EPA des É.-U., 2003b et PICS, 1990. ME cible = 100 (x 10 pour l’extrapolation interspécifique; x 10 pour les variations intraspécifiques).
Les marges d’exposition calculées pour la MIBK dans les milieux environnementaux et les aliments (d’après l’utilisation potentielle comme aromatisant alimentaire) pour la population générale du Canada et les personnes vivant près d’installations déclarant des rejets de MIBK dans l’air sont considérées comme adéquates pour compenser les incertitudes dans les données disponibles sur les effets sur la santé et l’exposition qui ont été utilisées pour caractériser le risque. Le JECFA (OMS, 1999b) a conclu qu’il n’y avait aucun problème de sécurité aux niveaux d’ingestion estimés lorsque la MIBK est utilisée comme agent aromatisant, principalement parce que celle-ci est « métabolisée en produits inoffensifs ».
Les ME pour l’exposition par inhalation à la MIBK découlant de l’utilisation de certains produits de consommation, c’est-à-dire l’alcool à friction, les marqueurs à essuyage à sec, les produits pour les ongles et les tatouages temporaires, sont considérées comme adéquates pour compenser les incertitudes dans les données disponibles sur les effets sur la santé et l’exposition qui ont été utilisées pour caractériser le risque. Les ME pour l’exposition par inhalation à la MIBK associée à l’utilisation de laques pour bois, de peintures liquides et de produits en aérosol, y compris les peintures en aérosol, sont considérées comme inadéquates compte tenu de la gravité des effets observés (c’est-à-dire la toxicité pour le développement) et de l’incertitude entourant la gravité des effets observés à de plus faibles concentrations.
L’évaluation des effets sur la santé humaine a tenu compte des sous-groupes de la population canadienne qui, en raison d’une vulnérabilité accrue ou d’une plus grande exposition, peuvent être plus susceptibles de subir des effets nocifs pour la santé. Par exemple, nous avons estimé les valeurs d’exposition en fonction de l’âge, y compris pour les nourrissons et les enfants, et avons examiné les études de toxicité pour le développement et la reproduction afin de dégager les effets nocifs potentiels sur la santé. En outre, le risque d’exposition élevée chez les personnes résidant près d’installations susceptibles de rejeter de la MIBK dans l’air a été pris en considération dans l’évaluation.
MIAK
Aucune étude sur la toxicité chronique de la MIAK n’a été trouvée. Plusieurs études ont donné comme résultat que la MIAK n’était pas génotoxique.
L’exposition subchronique à la MIAK a produit des effets hépatiques et rénaux (changements dans le poids des organes et sur le plan histologique) chez les rats exposés à des concentrations de 4 670 mg/m3 et plus. On a déterminé que la CSEO était de 934 mg/m3 (Katz et coll., 1986; ECHA, c2007-2019c). Pour ce qui est de l’exposition par voie orale, dans la seule étude sur la toxicité à doses répétées par voie orale relevée, un large éventail d’effets ont été observés à la seule dose testée de 2 000 mg/kg p.c./jour (ECHA, c2007-2019c). Donc, une DSEO par voie orale de 52 mg/kg p.c./jour a été dérivée en extrapolant d’une voie à l’autre à partir d’une étude d’inhalation, en se fondant sur les effets similaires sur le foie et les reins pour les 2 voies d’exposition.
En ce qui a trait à l’exposition par inhalation à court terme à la MIAK, le niveau d’effet critique a été établi comme une CSENO de 3 503 mg/m3 en fonction de la réduction du poids corporel, du gain de poids corporel et de la consommation alimentaire observée chez les rattes gravides exposées à une dose de 7 005 mg/m3 (ECHA, c2007-2019c).
La population générale du Canada pourrait être exposée à la MIAK par l’air intérieur et la présence naturelle de la substance dans certains aliments. La MIAK est également utilisée dans un stylo de réparation de revêtement automobile offert aux consommateurs. Le tableau 7‑12 présente toutes les estimations relatives à l’exposition et les valeurs des effets critiques pertinentes, ainsi que les ME obtenues.
| Scénario d’exposition | Exposition | Niveau d’effet critiquea | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Milieux environnementauxb | de 0,3 à 0,9 µg/kg p.c./ jour |
DSEO = 52 mg/kg p.c./ jour |
Extrapolation d’une voie à l’autre à partir de la CSEO = 934 mg/m3 | ≥ 57 778 |
| Stylo de réparation de revêtement automobile (20 ans et plus) | de 0,125 à 0,29 mg/m3 c | CSENO = 3 503 mg/m3 | Baisses importantes du poids corporel moyen, du gain de poids corporel moyen et de la consommation alimentaire moyenne correspondante chez les mères à 7 005 mg/m3 | de 12 079 à 28 024 |
Abréviations : CSENO = concentration sans effet nocif observé; DSEO = dose sans effet observé; ME = marge d’exposition.
a ECHA, c2007-2019c. ME cible = 100 (x 10 pour l’extrapolation interspécifique; x 10 pour la variation intraspécifique) pour les 2 niveaux d’effet critique.
b Cette catégorie comprend l’exposition à l’air intérieur et extérieur. La concentration utilisée pour calculer l’absorption associée à l’air intérieur a également été utilisée pour calculer l’absorption associée à l’air extérieur (Santé Canada, 2022).
c Pour le scénario de stylo de réparation de revêtement automobile, les concentrations moyennes pondérées de 6 heures ont été calculées de manière à correspondre aux durées d’exposition de l’étude des effets critiques ayant servi à caractériser le risque.
Les marges d’exposition calculées pour la MIAK dans les milieux environnementaux sont jugées adéquates pour compenser les incertitudes dans les données disponibles sur les effets sur la santé et l’exposition utilisées pour caractériser le risque. L’absorption supplémentaire de MIAK en raison de sa présence naturelle dans les aliments n’a pas été jugée préoccupante pour la santé humaine. Les ME pour l’exposition par inhalation à la MIAK contenue dans les stylos de réparation de revêtement automobile offerts aux consommateurs sont considérées comme adéquates pour compenser les incertitudes dans les données disponibles sur les effets sur la santé et l’exposition utilisées pour caractériser le risque.
L’évaluation des effets sur la santé humaine a tenu compte des sous-groupes de la population canadienne qui, en raison d’une vulnérabilité accrue ou d’une plus grande exposition, peuvent être plus susceptibles de subir des effets nocifs pour la santé. Par exemple, nous avons estimé les valeurs d’exposition en fonction de l’âge, y compris pour les nourrissons et les enfants, et avons examiné les études de toxicité pour le développement et la reproduction afin de dégager les effets nocifs potentiels sur la santé.
Alcool de diacétone
Aucune étude sur la toxicité chronique de l’alcool de diacétone n’a été trouvée. Une DSENO par voie orale de 100 mg/kg p.c./jour pour la toxicité systémique (changements rénaux et chimie hématologique et sanguine modifiée chez les rats), déterminée dans le cadre de l’étude sur la reproduction et le développement, est utilisée pour gérer le risque posé par les expositions chroniques à l’alcool de diacétone (Ministère de la santé et du bien-être, 1997, cité dans OCDE, 2000; ECHA, c2007-2019b). En l’absence d’études par voie cutanée, l’extrapolation d’une voie à l’autre à partir de la DSENO par voie orale est utilisée pour caractériser le risque posé par l’exposition à l’alcool de diacétone par voie cutanée.
Dans la seule étude d’inhalation sur des animaux que l’on a trouvée, seuls des changements dans le poids du foie, non associés à des modifications histologiques, ont été observés à 1 041 mg/m3 (1 035 mg/m3 selon l’OCDE [2000]) dans une étude d’inhalation de 6 semaines (Butterworth et coll., 1980, cité dans ECHA, c2007-2019b).
La DSENO pour la reproduction et le développement a été établie à 300 mg/kg p.c./jour sur la base des effets sur de nombreux paramètres de reproduction et de développement observés à 1 000 mg/kg p.c./jour. Afin de protéger les fœtus en développement et les enfants, un niveau d’effet critique de 300 mg/kg p.c./jour est utilisé pour caractériser le risque lié à l’utilisation à court terme de produits de consommation. En l’absence d’études de la toxicité de l’alcool de diacétone pour la reproduction et le développement par inhalation et par voie cutanée, la DSENO par voie orale de 300 mg/kg p.c./jour a été utilisée.
La principale source d’exposition à l’alcool de diacétone par les milieux environnementaux et les aliments est sa présence dans l’air intérieur et sa présence naturelle dans diverses denrées alimentaires.
L’alcool de diacétone est employé dans divers produits de consommation, dont les produits de soins pour les ongles et les marqueurs permanents, les scellants pour filets de tuyau, les revêtements de plancher, le diluant et les produits à pulvériser, dont les décapants à peinture et les produits nettoyants pour automobile.
Le tableau 7‑13 présente toutes les estimations relatives à l’exposition et les valeurs des effets critiques pertinentes, ainsi que les ME obtenues. Bien qu’elles soient limitées, les données disponibles sur l’absorption cutanée indiquent que l’alcool de diacétone n’est pas fortement absorbé par la peau (dans une proportion de moins de 1 % à environ 6 % chez les humains); donc, les estimations ci-dessous comportent une valeur d’absorption cutanée de 6 %. Étant donné que la même étude des effets sur la santé de l’exposition par voie orale sert à caractériser les risques liés aux expositions potentielles par voie cutanée et par inhalation à l’alcool de diacétone découlant de l’utilisation de produits de consommation, on a combiné ces estimations des expositions.
| Scénario d’exposition | Exposition | Niveau d’effet critique | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Milieux environnementauxa | de 0,48 à 1,44 µg/kg p.c./jour | DSENO = 100 mg/ kg p.c./jourb | Changements rénaux et chimie hématologique et sanguine modifiée | > 69 000 |
| Cosmétiques (inhalation)c (tous les groupes d’âge) | Concentration moyenne pondérée de 6 heures = de 0,3 à 1,3 mg/m3 | CSENO = 1 035 mg/m3 d | Changements dans le poids du foie sans modifications histopathologiques à 4 685 mg/m3 | de 796 à 3 450 |
| Cosmétiques (voie cutanée)a (tous les groupes d’âge) | de 0,007 à 0,023 mg/ kg p.c./évén. | DSENO = 100 mg/ kg p.c./jourb | Changements rénaux et chimie hématologique et sanguine modifiée | de 4 348 à 14 286 |
| Produits de peinture et de bricolage (inhalation et voie cutanée) (20 ans et plus) | de 0,013 à 2 mg/kg p.c./ évén. | DSENO = 300 mg/ kg p.c./joure | Effets sur la reproduction et le développement | de 150 à 23 077 |
| Marqueurs permanents (par événement) [voie orale] | de 1,6 mg/ kg p.c./jour (5 à 11 ans) à 3,2 mg/ kg p.c./jour (6 mois à 4 ans) | DSENO = 300 mg/ kg p.c./joure | Effets sur la reproduction et le développement à 1 000 mg/ kg p.c./jour | de 94 à 188 |
| Marqueurs permanents (utilisation quotidienne) [voie cutanée] | de 0,002 (20 ans et plus) à 0,005 (5 à 11 ans) mg/kg p.c./jour | DSENO = 100 mg/ kg p.c./jourb | Changements rénaux et chimie hématologique et sanguine modifiée | de 20 000 à 50 000 |
Abréviations : CSENO = concentration sans effet nocif observé; DSENO = dose sans effet nocif observé; évén. = événement; ME = marge d’exposition.
a Cette catégorie comprend l’exposition à l’air intérieur et extérieur. La concentration utilisée pour calculer l’absorption associée à l’air intérieur a également été utilisée pour calculer l’absorption associée à l’air extérieur (Santé Canada, 2023).
b Ministère de la santé et du bien-être, 1997, cité dans OCDE, 2000; ECHA, c2007-2019b. ME cible = 100 (x 10 pour l’extrapolation interspécifique; x 10 pour les variations intraspécifiques).
c Cette catégorie comprend l’utilisation de vernis à ongles et de traceurs d’yeux autocollants.
d SHELL Research Ltd., 1979, cité dans OCDE, 2000. ME cible = 100 (x 10 pour l’extrapolation interspécifique; x 10 pour les variations intraspécifiques).
e Ministère de la santé et du bien-être, 1997, cité dans OCDE, 2000. ME cible = 100 (x 10 pour l’extrapolation interspécifique; x 10 pour les variations intraspécifiques).
Les ME calculées pour l’exposition à l’alcool de diacétone dans les milieux environnementaux sont considérées comme adéquates pour compenser les incertitudes dans les données disponibles sur les effets sur la santé et l’exposition utilisées pour caractériser le risque. L’absorption supplémentaire d’alcool de diacétone qui découle de sa présence naturelle dans les aliments n’a pas été jugée préoccupante pour la santé humaine. En outre, les ME calculées d’après l’utilisation de produits de consommation (qui s’appuient sur l’hypothèse qu’on trouve de l’alcool de diacétone à une concentration de 100 % dans les marqueurs permanents et sur les changements non statistiquement significatifs des paramètres de reproduction et de développement utilisés pour caractériser le risque associé à l’utilisation de marqueurs et de produits de peinture et de bricolage) sont considérées comme adéquates pour compenser les incertitudes dans les données disponibles sur les effets sur la santé et l’exposition utilisées pour caractériser le risque.
L’évaluation des effets sur la santé humaine a tenu compte des sous-groupes de la population canadienne qui, en raison d’une vulnérabilité accrue ou d’une plus grande exposition, peuvent être plus susceptibles de subir des effets nocifs pour la santé. Par exemple, nous avons estimé les valeurs d’exposition en fonction de l’âge, y compris pour les nourrissons et les enfants, et avons examiné les études de toxicité pour le développement et la reproduction afin de dégager les effets nocifs potentiels sur la santé.
7.2.4 Incertitudes de l’évaluation des risques pour la santé humaine de la MIBK, de la MIAK et de l’alcool de diacétone
Les sources clés d’incertitude sont présentées dans le tableau 7‑14.
| Sources clés d’incertitude | Incidence |
|---|---|
| Nous présumons que les expositions par voie cutanée sont minimales pour la MIBK et la MIAK par rapport aux expositions par inhalation, vu la forte volatilité des substances; toutefois, il est fort probable que l’exposition soit surestimée, compte tenu de la nature prudente des modèles d’exposition. | + |
| Nous présumons que l’alcool de diacétone est présent dans les marqueurs permanents à une concentration de 100 %. | + |
| Manque d’études sur la toxicité chronique de la MIAK et de l’alcool de diacétone. | +/- |
| Nous avons recouru à l’extrapolation d’une voie à l’autre pour l’exposition à long terme à la MIBK. | - |
| Nous avons recouru à l’extrapolation d’une voie à l’autre à partir d’une étude d’inhalation sur 96 jours pour les scénarios d’exposition à la MIAK par voie orale et cutanée. | +/- |
| Aucune étude d’inhalation à court terme n’est disponible pour l’alcool de diacétone. On a appliqué l’extrapolation d’une voie à l’autre à partir d’une étude par voie orale. | +/- |
| En ce qui concerne le risque posé par l’utilisation de produits de consommation contenant de l’alcool de diacétone, la confiance dans le caractère adéquat des marges est élevée, en raison de la prudence associée à la valeur d’absorption cutanée (qui repose sur la quantité d’alcool de diacétone ayant pénétré la peau après une exposition de 24 heures) et des effets non statistiquement significatifs sur les paramètres de reproduction et de développement au niveau d’effet critique. | + |
+ = incertitude ayant le potentiel de causer une surestimation de l’exposition ou du risque; - = incertitude ayant le potentiel de causer une sous-estimation de l’exposition ou du risque; +/- = potentiel inconnu de causer soit une surestimation soit une sous-estimation du risque.
7.3 Évaluation du sous-groupe 3 (diacétyle, 2,3-PD et acétoïne)
7.3.1 Évaluation de l’exposition au sous-groupe 3 (diacétyle, 2,3-PD et acétoïne)
Milieux environnementaux
On n’a recensé aucune donnée empirique, ou seules des données empiriques limitées, relativement au diacétyle, à la 2,3-PD ou à l’acétoïne dans l’air (2,3-PD uniquement), l’eau ou le sol au Canada.
On a déterminé que le diacétyle était un sous-produit de la désinfection à l’ozone (É.-U.), et on l’a détecté dans l’eau potable (É.-U.) et les eaux de surface (France) (HSDB, 1983-). On n’a trouvé aucune donnée sur la présence de diacétyle dans le sol ou les sédiments; toutefois, à en juger par son faible log Kco, le diacétyle ne devrait pas être présent dans ces milieux.
Une unique étude de l’air ambiant ayant révélé la présence de 2,3-PD dans l’air à Roseville, en Californie, a été recensée. Elle mentionnait des concentrations de 11,1 et 8,1 ng/cm3 de 2,3-PD durant l’été et l’hiver, respectivement (HSDB, 1983-). Dans une étude de terrain au Nunavik qui comprenait l’analyse de 54 échantillons d’air intérieur, la 2,3-PD a été détectée dans 4 % des échantillons, avec une concentration maximale de 2,8 µg/m3 (Won et coll., 2019). On n’a trouvé aucune autre donnée sur la concentration dans l’environnement.
D’après ses propriétés physiques et chimiques, l’acétoïne pourrait être présente dans l’air et dans l’eau, mais elle est peu susceptible de se retrouver dans le sol et les sédiments. D’après sa constante de la loi d’Henry modérée, on s’attend à ce qu’elle se volatilise depuis l’eau. Dans l’air, sa demi-vie est d’environ 37 h (HSBD, 1983-).
Nous avons utilisé le modèle ChemCAN, version 6.00 (ChemCAN, 2003) pour calculer des concentrations de diacétyle, de 2,3-PD (eau et sol uniquement) et d’acétoïne dans l’air, l’eau et le sol au Canada, en nous fondant sur la valeur la plus élevée des quantités énumérées au tableau 4‑1 et en supposant que la quantité totale importée était rejetée dans une seule région du pays (c’est-à-dire dans la région des Plaines à forêts mixtes de l’Ontario). Nous avons ensuite utilisé ces concentrations pour estimer l’exposition au diacétyle, à la 2,3-PD (eau et sol) et à l’acétoïne par les milieux environnementaux pour l’ensemble de la population canadienne. Toutes les expositions résultantes étaient inférieures à 2,5 ng/kg p.c./jour. À partir des renseignements présentés ci-dessus, nous estimons que l’exposition à ces substances par les milieux environnementaux est négligeable.
Aliments
Le diacétyle, la 2,3-PD et l’acétoïne sont naturellement présents dans diverses denrées alimentaires et peuvent également servir d’agents aromatisants alimentaires (Nijssen et coll., 1963-2018; Burdock, 2010). Le diacétyle est en voie d’être remplacé dans certains produits par la 2,3-PD, l’acétoïne et d’autres dicétones ayant un arôme et un goût semblables de « beurre » (Doepker et coll., 2012; Gaffney et coll., 2015; CDC, 2016).
Le JECFA a évalué un groupe d’α-dicétones aliphatiques acycliques et alicycliques et de composés connexes d’α-hydroxycétones, dont le diacétyle, la 2,3-PD et l’acétoïne (OMS, 1999a). Dans le cadre de cette évaluation, le Comité a estimé l’absorption par personne de diacétyle, de 2,3-PD et d’acétoïne occasionnée par leur présence comme agents aromatisants alimentaires. Pour la population américaine, les estimations de l’absorption par personne se chiffraient respectivement à 133 µg/kg p.c./jour, à 1 µg/kg p.c./jour et à 30 µg/kg p.c./jour. Pour la population européenne, elles étaient de 55 µg/kg p.c./jour, 4 µg/kg p.c./jour et 47 µg/kg p.c./jour, respectivement (OMS, 1999a). (L’annexe C donne plus de détails.) Faute de données sur l’utilisation réelle de ces substances au Canada, l’estimation de l’absorption par personne constitue une estimation acceptable de l’exposition possible par le régime alimentaire de la population générale (1 an et plus) au diacétyle, à la 2,3-PD et à l’acétoïne en raison de leur utilisation comme aromatisants alimentaires.
Les estimations quantitatives de l’exposition au diacétyle, à la 2,3-PD et à l’acétoïne de par leur présence naturelle dans les alimentsNote de bas de page 5 variaient de 281 µg/kg p.c./jour pour les adolescents âgés de 14 à 18 ans à 1 625 µg/kg p.c./jour pour les bébés d’un an pour le diacétyle, de 6,5 µg/kg p.c./jour pour les nourrissons de 6 à 12 mois à 208 µg/kg p.c./jour pour les adultes de 19 ans et plus pour la 2,3-PD, et de 161 µg/kg p.c./jour pour les adolescents de 14 à 18 ans à 369 µg/kg p.c./jour pour les tout-petits de 2 à 3 ans pour l’acétoïne. (L’annexe C présente plus de détails).
Les estimations de l’absorption quotidienne de diacétyle étant donné sa présence naturelle dans les aliments se fondent principalement sur sa teneur (environ 30 µg/g) dans le lait pasteurisé d’après les publications scientifiques (De Leonardis et coll., 2013). On a signalé des concentrations plus élevées de diacétyle dans le lait cru et le lait pasteurisé à ultra haute température (UHT) (Macciola et coll., 2008; De Leonardis et coll., 2013). Or, d’autres études ont signalé des concentrations de diacétyle dans le lait beaucoup plus faibles (de plusieurs ordres de grandeur), qui variaient de 0,0002 µg/g à 0,024 µg/g (Nijssen et coll., 1963-2018; Imhof et coll., 1995; Shimoda et coll., 2000; Valero et coll., 2001; Toso et coll., 2002). En supposant que les concentrations de diacétyle dans le lait au Canada soient comparables à celles trouvées en Europe, on a sélectionné la valeur la plus élevée dans le lait pasteurisé (partiellement écrémé) de l’étude de De Leonardis et coll. (2013). Les auteurs expliquent que la méthode analytique utilisée dans cette étude consiste à extraire le diacétyle qui est principalement lié aux protéines et au lactose du lait. Les autres études susmentionnées ont employé des techniques d’espace de tête qui ne permettent de capturer que la portion volatile de la substance dans l’aliment (De Leonardis et coll., 2013).
Outre les expositions par voie orale à ces substances, il est possible que les expositions par inhalation soient également importantes pour certains produits alimentaires tels que le maïs à éclater au four à micro-ondes. Le diacétyle, l’acétoïne et la 2,3-PD ont été mesurés dans le maïs à éclater (Buttery et coll., 1997; Rosati et coll., 2007). Selon Rosati et coll., (2007), le diacétyle et l’acétoïne ont été mesurés durant une étude de l’air dans une enceinte, et les concentrations variaient de 0,02 mg/m3 à 5,8 mg/m3 et de 0,01 mg/m3 à 4,2 mg/m3 pour le diacétyle et l’acétoïne, respectivement. La quantité moyenne de diacétyle émise par un sac de maïs éclaté au four à micro-ondes était de 778,9 µg/sac (Rosati et coll., 2007). Selon les renseignements tirés de Rosati et coll. (2007) et une approche décrite dans Zhu et coll. (2001), cela équivaut environ à 0,03 mg/m3 de diacétyle dans une pièce standard une heure après la préparation du maïs éclaté (maximum de 0,04 mg/m3 durant la première heure suivant la cuisson) (voir l’annexe E). Les renseignements disponibles ne permettaient pas de quantifier la concentration dans l’air de 2,3-PD provenant du maïs à éclater. On a également mesuré le diacétyle et la 2,3-PD dans l’air d’usines de torréfaction (McCoy et coll., 2017), et le diacétyle de l’air a été mesuré dans une étude visant à simuler des expositions qui pourraient survenir dans le local d’un petit café (Pierce et coll., 2015).
Produits de consommation
Selon les déclarations présentées à Santé Canada en vertu du Règlement sur les cosmétiques, le diacétyle est utilisé dans des savons pour le corps et des hydratants pour le visage au Canada (communication personnelle, courriels de la DSPCPD, SC, au BERSE, SC, datés de novembre 2019 et d’avril 2020; source non citée). En outre, plusieurs cosmétiques mentionnant le diacétyle parmi leurs ingrédients ont été trouvés sur les sites Web de détaillants, notamment des hydratants pour le corps, des huiles pour le corps, des savons liquides pour le corps, des shampooings, des revitalisants, des crèmes pour les mains et les ongles, ainsi que des savons pour le corps. Les hydratants pour le corps et le visage sont présentés comme des scénarios sentinelles. La fonction du diacétyle dans les cosmétiques est celle d’agent parfumant (Commission européenne, 2017).
On a trouvé de la 2,3-PD dans certains assainisseurs d’air pour l’entretien de la maison et dans des huiles parfumées, qui peuvent servir à assainir l’air (FDS, 2015d, e, 2019f; CPID [modifié, 2019]). Le tableau 7‑15 résume les estimations de l’exposition par inhalation aux produits de consommation contenant du diacétyle ou de la 2,3-PD. Même si l’exposition par voie cutanée pourrait contribuer à l’exposition globale pendant l’utilisation de produits de consommation (Commission européenne, 2014), nous considérons que la voie préoccupante principale étant donné les effets critiques est l’inhalation et, par conséquent, seules les estimations pour l’inhalation sont présentées.
On n’a trouvé d’acétoïne dans aucun produit de consommation au Canada.
| Scénario pour le produit | Concentration | Concentration moyenne par événement (mg/m3) | Concentration moyenne pondérée de 6 heuresa (mg/m3) |
|---|---|---|---|
| Hydratant pour le visageb (20 ans et plus) (diacétyle) | 0,1 % | 0,0099 | 0,0198 |
| Hydratant pour le visageb (5 à 11 ans) (diacétyle) | 0,1 % | 0,0035 | 0,014 |
| Hydratant pour le corps (12 ans et plus) (diacétyle)c | 0,1 % | 0,72 | 0,04 |
| Assainisseur d’aird (2,3-PD) | de 0,1 à 5 % | de 0,0031 à 0,064 | de 0,004 à 0,14 |
a Les concentrations moyennes pondérées de 6 heures ont été calculées pour tous les scénarios de produit de manière à correspondre aux durées d’exposition de l’étude des effets critiques ayant servi à caractériser le risque. Concentration moyenne pondérée de 6 h = concentration moyenne par événement × durée d’exposition / 6 × 60 min.
b Communication personnelle, courriel de la DSPCPD, SC, au BERSE, SC, daté d’avril 2020; source non citée.
c Comme il n’y avait aucune donnée disponible sur la concentration dans les hydratants pour le corps, nous avons présumé que le diacétyle y est présent aux mêmes concentrations que dans les hydratants pour le visage.
d Comprend l’utilisation d’huiles essentielles comme assainisseurs d’air, ainsi que les assainisseurs d’air à brancher ou de type gel.
7.3.2 Évaluation des effets sur la santé du sous-groupe 3 (diacétyle, 2,3-PD et acétoïne)
Le diacétyle et la 2,3-PD sont des alpha-dicétones et leur structure est identique, à l’exception d’un groupe méthyle supplémentaire dans la 2,3-PD. La similitude de leurs structures et de leurs groupes fonctionnels se reflète dans leurs propriétés physicochimiques et organoleptiques comparables.
On s’attend à ce que la 2,3-PD soit facilement biodisponible par voie orale et cutanée et par inhalation, comme le diacétyle, et à ce que l’incidence du groupe méthyle supplémentaire dans la 2,3-PD soit minime. Les 2 produits chimiques présentent des effets de voie d’entrée dans les voies respiratoires après une exposition par inhalation. À la suite d’une exposition par voie orale, le diacétyle se métabolise rapidement dans le foie en acétoïne et en 2,3-butanediol. Pour la 2,3-PD, le simulateur du métabolisme des rats in vivo et in vitro de la boîte à outils QSAR de l’OCDE (2017) a prédit des métabolites 2-hydroxy-3-pentanone, 3-hydroxy-2-pentanone et 2,3-pentanediol (entre autres), dont la structure ressemblait aux métabolites du diacétyle. Étant donné ces informations, nous avons traité le diacétyle, l’acétoïne et la 2,3-PD comme un groupe, et les données sur la toxicité de ces substances ont permis de faire des lectures croisées pour le groupe (voir l’annexe A).
7.3.2.1 Diacétyle
Le diacétyle a fait l’objet d’un examen par le PISC (1999), l’EFSA (2004), le SCOEL (2014) et le CDC (2016). Ces examens servent de base à la caractérisation des effets sur la santé dans la présente évaluation. Une recension des publications scientifiques a été menée à partir d’un an avant le rapport du CDC (2016) jusqu’en janvier 2020, et de nouveaux renseignements pertinents ont été pris en compte à l’appui de la caractérisation des risques.
Toxicocinétique
Le diacétyle peut être généré de manière endogène et il est un métabolite de l’acétaldéhyde chez les mammifères (PISC, 1999; SCOEL, 2014). Il est prévu que les méthylcétones se métabolisent principalement par l’oxydation du groupe méthyle terminal à de faibles concentrations. À des concentrations plus élevées, le diacétyle est réduit en acétoïne et en 2,3-butanediol, puis se conjugue à l’acide glucuronique avant d’être excrété. Les modèles de dosimétrie régionale suivant l’inhalation chez l’humain diffèrent considérablement de ceux des rats, la pénétration de diacétyle étant beaucoup plus importante dans les voies aériennes bronchiolaires de l’humain. De ce fait, la toxicité du diacétyle est observée principalement dans les voies respiratoires supérieures des rongeurs et les voies respiratoires inférieures des humains (Cichocki et Morris, 2017).
Étant donné ces renseignements, un modèle pharmacocinétique physiologique et de dynamique numérique des fluides a été réalisé pour comparer l’absorption et la concentration tissulaire de diacétyle dans les voies respiratoires des rats et des humains (Gloede et coll., 2011). Le modèle a permis d’estimer que les concentrations de diacétyle dans les tissus bronchiolaires chez les humains pendant un exercice physique léger étaient de 20 à 40 fois plus élevées que chez les rats. Une modélisation plus poussée de la dosimétrie a indiqué que les études de toxicité par inhalation sur des rats sous-estimaient le risque de blessure bronchiolaire chez les humains (Cichocki et Morris, 2017).
Cancérogénicité et génotoxicité
Le diacétyle n’a été classé par aucun organisme sur la base de sa cancérogénicité ou d’autres effets sur la santé. Toutefois, de récentes études du NTP (NTP, 2018) ont démontré quelques preuves d’action cancérogène dans des études d’inhalation sur 2 ans. Des groupes de rats Wistar Han et de souris B6C3F1/N ont été exposés à des vapeurs de diacétyle par inhalation (corps entier) à des concentrations de 0, de 12,5, de 25 ou de 50 ppm (0, 45, 90 et 179 mg/m3, respectivement), à raison de 6 heures par jour, 5 jours par semaine, pendant 105 semaines. Chez les rats, on a constaté des augmentations de l’incidence de carcinomes des cellules squameuses dans la cavité nasale chez les mâles comme chez les femelles et de l’incidence combinée de carcinomes des cellules squameuses et des papillomes dans la cavité nasale des mâles à 179 mg/m3. Chez les souris, l’incidence d’adénocarcinomes du nez a augmenté chez les femelles à cette concentration. Le NTP a conclu qu’« il y avait certaines preuves de l’activité cancérogène du diacétyle chez les rats mâles et femelles. Il n’y a eu aucun signe d’activité cancérogène du diacétyle chez les souris B6C3F1/N mâles exposées à 12,5, à 25, ou à 50 ppm. Il y a eu des indications équivoques d’activité cancérogène du diacétyle chez les souris B6C3F1/N femelles sur la base des cas d’adénocarcinome du nez » (NTP, 2018).
Les données disponibles indiquent que le diacétyle s’est révélé mutagène dans une variété d’essais in vitro (Bjeldanes et Chew, 1979; Marnett et coll., 1985; Shane et coll., 1988; Kato et coll., 1989; Dorado et coll., 1992; Aeschbacher et coll., 1989, examiné dans EFSA, 2004 et NTP, 2018; More et coll., 2012).
Au cours d’études in vivo, une augmentation de la synthèse d’ADN non programmée a été observée dans les cellules de l’estomac de rats exposés par gavage au diacétyle à une dose de 500 mg/kg p.c./jour (Furihata et coll., 1985; Furihata et Matsushima, 1987, examiné dans SCOEL, 2014). Cependant, le diacétyle n’a pas entraîné la formation de micronoyaux chez les souris ou les rats exposés, jusqu’à une dose de 500 mg/kg p.c./jour reçue par injection intrapéritonéale pendant 3 jours ou jusqu’à une dose de 100 ppm reçue par exposition par inhalation pendant 3 mois, ce qui laisse à penser que le diacétyle n’a pas eu d’effet sur l’érythropoïèse (NTP, 2018).
Toxicité à doses répétées
Dans les études sur l’inhalation de 2 ans du NTP (2018) dont il est question plus haut, l’exposition au diacétyle a également entraîné des incidences accrues d’effets non cancérogènes dans le nez, le larynx, la trachée et les poumons des souris à toutes les concentrations analysées et chez les rats aux doses de 90 mg/m3 et de 179 mg/m3, des effets plus graves sur le système respiratoire se manifestant à des concentrations plus élevées chez les souris et les rats. Chez les rats, les lésions nasales dont l’occurrence était considérablement accrue comprenaient une inflammation purulente, une hyperplasie de l’épithélium respiratoire et une métaplasie pavimenteuse, une atrophie de l’épithélium olfactif, une métaplasie respiratoire et une nécrose (mâles), une hyperostose des fosses nasales et une fibrose de la lamina propria. Une incidence considérablement accrue de l’inflammation chronique active ou purulente et de l’hyperplasie de l’épithélium a également été observée dans le larynx, la trachée, les poumons et les yeux à 179 mg/m3. À 90 mg/m3, on a observé une incidence considérablement accrue d’hyperplasie de l’épithélium pavimenteux dans le larynx (mâles et femelles), de régénération de l’épithélium dans la trachée (mâles) et d’hyperplasie de l’épithélium dans les poumons (femelles). Des effets similaires ont été observés à 45 mg/m3 chez les souris, comprenant une métaplasie de l’épithélium respiratoire, une atrophie de l’épithélium olfactif et une atrophie des fosses nasales, ainsi qu’une hyperplasie de l’épithélium pavimenteux dans le larynx. Le taux de survie a modérément diminué chez les femelles à 90 mg/m3 et considérablement diminué chez les mâles à 179 mg/m3. À la fin de l’étude, le poids corporel moyen avait diminué chez les mâles et les femelles à 179 mg/m3, comparativement aux témoins. Ainsi, à la lumière de ces observations d’effets non cancérogènes chez les souris, une CMENO de 45 mg/m3 pour l’inhalation chronique est envisagée dans la présente évaluation des effets sur la santé (NTP, 2018).
Un profil d’effets semblable à celui de l’essai biologique de toxicité chronique a aussi été observé dans des études d’inhalation subchronique chez des rats Wistar Han et des souris B6C3F1 (NTP, 2018). Les animaux ont reçu des doses de 0, 6,25, 12,5, 25, 50 ou 100 ppm (correspondant à 0, 22, 45, 90, 179 ou 350 mg/m3) par exposition (corps entier) pendant 6 heures par jour, 5 jours par semaine pendant 14 semaines. On a établi une CSENO de 45 mg/m3 sur la base d’une augmentation considérable de l’incidence de lésions non néoplasiques dans les voies respiratoires (nez, larynx, trachée et poumons) des souris et des rats, principalement dans les groupes exposés à 179 mg/m3 et à 350 mg/m3 après 14 semaines. À 90 mg/m3, des incidences accrues de métaplasie pavimenteuse de l’épithélium respiratoire ont été observées chez les rats mâles et femelles ainsi qu’une dégénérescence accrue de l’épithélium olfactif chez les rats femelles. Chez les souris, on a observé des incidences accrues de nécrose dans l’épithélium respiratoire chez les mâles et les femelles à 90 mg/m3; une hyperplasie et une inflammation active chronique accrues ont aussi été observées dans le larynx des femelles (NTP, 2018). Des effets similaires ont été rapportés dans une étude antérieure chez des souris exposées au diacétyle pendant 6 ou 12 semaines à 90 mg/m3 ou plus; la plus faible concentration analysée (25 ppm ou 90 mg/m3) a été considérée comme la CMENO, à en juger par l’importante lésion à l’épithélium et l’inflammation lymphoïde péribronchique (Morgan et coll., 2008).
Dans une étude sur la toxicité à doses répétées par voie orale, des rats CFE (Crl:OFA(SD)) mâles et femelles ont reçu 0, 10, 30, 90 ou 540 mg/kg p.c./jour de diacétyle dans de l’eau par intubation orale pendant 90 jours. À la dose la plus élevée, soit 540 mg/kg p.c./jour, les rats présentaient une diminution du gain de poids corporel et consommaient plus d’eau. Les effets observés comprenaient l’anémie, une numération accrue des leucocytes et une augmentation du poids relatif du cerveau, du foie, des reins et des glandes surrénales et pituitaires (les augmentations du poids des organes ont été plus importantes que les changements susceptibles d’être associés à un poids corporel moindre). On a observé des ulcères dans les parties squameuses et glandulaires de la muqueuse gastrique. Aucun effet nocif n’a été remarqué chez les groupes exposés à une dose plus faible. Toutefois, une anémie légère, mais non statistiquement significative, ainsi qu’un accroissement du poids relatif de certains organes ont été observés à de plus faibles doses en l’absence de changements histopathologiques dans l’estomac. Les auteurs ont conclu que la DSENO pour le diacétyle dans cette étude était de 90 mg/kg p.c./jour, bien que l’on ne sache pas clairement si les effets observés à 540 mg/kg p.c./jour ont pu être secondaires à la formation d’ulcères (Colley et coll., 1969; examiné dans PISC, 1999; SCOEL, 2014).
Les résultats d’une autre étude sur la toxicité à doses répétées par voie orale indiquent que le diacétyle peut induire des effets neurologiques et sur la reproduction (Bawazir, 2016). L’administration quotidienne de 25 mg/kg p.c./jour de diacétyle à des rats par intubation orale durant une étude sur 4 semaines a entraîné des changements des niveaux de plusieurs neurotransmetteurs dans différentes régions du cerveau ainsi qu’une baisse des niveaux de testostérone sérique. On a observé des changements histologiques dans les testicules, qui étaient associés à une diminution importante du sperme mature et à des déficits tubulaires. Toutefois, le compte rendu publié de cette étude était plutôt mince, puisque les essais se limitaient à une seule dose, et l’étude ne comportait pas de contrôle adéquat.
Toxicité à court terme et aiguë
Les expositions aiguës et à court terme à la vapeur de diacétyle ont causé une vaste gamme de lésions nasales et olfactives chez des rongeurs (Hubbs et coll., 2002; Morgan et coll., 2008; Larsen et coll. 2009; Morris et Hubbs, 2009), atteint les neurones sensoriels (Goravanahally et coll., 2014) et mené à une hyporéactivité des voies respiratoires (Zaccone et coll., 2013).
Hubbs et coll. (2008) ont exposé des rats Hla:(SD)CVF mâles (6/groupe d’exposition) au diacétyle à certaines concentrations : en régime continu pendant 6 heures à des concentrations moyennes pondérées dans le temps de 0, 99,3, 198,4 ou 294,6 ppm (0, 355, 710 ou 1 055 mg/m3, respectivement); à 4 expositions pulsées de 15 minutes au cours d’une période de 6 heures à des concentrations moyennes pondérées dans le temps de 0, 122, 225 ou 365 ppm (0, 437, 806 ou 1 307 mg/m3, respectivement); et à une exposition pulsée unique de 15 minutes à une concentration moyenne pondérée dans le temps de 92,9 ppm (333 mg/m3). Les schémas d’exposition pulsée et continue ont causé des blessures à l’épithélium, y compris une nécrose épithéliale et une inflammation purulente ou fibrinopurulente au nez, au larynx, à la trachée et aux bronches. L’effet le plus grave a été constaté dans le nez. Le larynx et la trachée ont été affectés à des concentrations de diacétyle de 225 ppm ou plus, et les bronches, à des concentrations de 294,6 ppm ou plus. Les auteurs ont constaté des changements histologiques importants (c’est-à-dire une nécrose) dans le nez des rats ayant subi l’exposition pulsée unique de 15 minutes (concentration moyenne pondérée dans le temps de 92,9 ppm). Ils ont conclu que la CSENO pour l’inhalation aiguë de diacétyle était inférieure à 93 ppm (333 mg/m3), ce qui est considéré ici comme la CMENO.
Toxicité pour la reproduction et le développement
On n’a constaté aucun effet sur la survie maternelle, le poids ou les paramètres de reproduction, ni sur la survie des fœtus ou sur l’apparence microscopique des tissus externes, squelettiques ou mous chez des groupes de souris CD-1 et de rats Winstar albinos qui, pendant les jours 6 à 15 de la gestation, avaient reçu du diacétyle par gavage à des doses allant jusqu’à 1 600 mg/kg p.c./jour. De même, aucun effet sur les mères ou le développement n’a été observé chez les hamsters qui avaient reçu des doses allant jusqu’à 1 600 mg/kg p.c./jour pendant les jours de gestation 6 à 10 (FDA des É.-U., 1973, examiné dans OMS, 1999a; EFSA, 2004).
Effets chez les humains
Plusieurs études épidémiologiques ont trouvé que l’inhalation de vapeurs contenant du diacétyle et d’autres substances par les travailleurs d’usines de fabrication de maïs à éclater au four à micro-ondes ou d’aromatisants est toujours associée au développement de divers troubles respiratoires tels que la bronchiolite oblitérante (Kreiss et coll., 2002; Parmet et Von Essen, 2002; van Rooy et coll., 2007; CDC, 2016). La bronchiolite oblitérante (BO) est une maladie pulmonaire rare et irréversible caractérisée par une cicatrisation chronique et un rétrécissement sévère des voies respiratoires bronchiques (Hubbs et coll., 2008). Au cours de la formation et du développement de la BO, un certain nombre d’autres conditions pathologiques ont été observées, notamment des symptômes d’inflammation pulmonaire allergique, d’asthme, de fibrose interstitielle diffuse et de granulome, de maladie pulmonaire obstructive chronique avec ou sans emphysème, d’alvéolite allergique extrinsèque et de pneumonie (Hubbs et coll., 2008; Commission européenne, 2014). L’Union européenne (SCOEL, 2014) et le CDC (2016) ont examiné plusieurs rapports de cas, séries de cas et études transversales. Le terme « poumon pop-corn » est souvent utilisé pour décrire les symptômes respiratoires observés chez ces employés. Des effets similaires ont été indiqués dans des études de cas d’exposition répétée de consommateurs au maïs à éclater au four à micro-ondes (c’est-à-dire, une consommation quotidienne) sur une période de 10 ans (Egilman et Schilling, 2012).
7.3.2.2 2,3-PD
La 2,3-PD a fait l’objet d’un examen par le PISC (1999), l’EFSA (2004) et le CDC (2016). Ces examens servent de base à la caractérisation des effets sur la santé dans la présente évaluation. Une recherche des publications scientifiques a été menée à partir d’un an avant la publication du CDC (2016) jusqu’en janvier 2020, et de nouveaux renseignements pertinents ont été pris en compte pour appuyer la caractérisation des risques.
Toxicocinétique
Zaccone et coll. (2015) ont démontré que l’épithélium respiratoire humain pouvait métaboliser la 2,3-PD en 2,3-hydroxy-3-pentanone.
Cancérogénicité et génotoxicité
Aucune donnée sur la cancérogénicité n’a été recensée pour la 2,3-PD. 2 études ont démontré que la 2,3-PD n’était pas mutagène pour la salmonelle (Kim et coll., 1987; Aeschbacher et coll., 1989, examiné dans OMS, 1999a et EFSA, 2004, 2016). La 2,3PD n’a pas causé la formation de micronoyaux chez les rats ni les souris des 2 sexes (NTP, 2017).
Toxicité à doses répétées
Dans une étude de toxicité par inhalation à doses multiples, des rats Winstar Han et des souris B6C3F1 mâles et femelles ont été exposés à la 2,3-PD par inhalation à des concentrations de 0, 6,25, 12,5, 25, 50 ou 100 ppm (0, 26, 51, 102, 205 ou 409 mg/m3, respectivement) à raison de 6 heures par jour, 5 jours par semaine pendant 14 semaines. Des résultats semblables à ceux de l’étude d’exposition subchronique au diacétyle ont été observés. À 205 et à 409 mg/m3, des observations cliniques ont été notées, dont une respiration anormale, des éternuements et des anomalies oculaires. Des incidences considérablement accrues de lésions non néoplasiques sont survenues dans les voies respiratoires des rats mâles et femelles, dont une hyperplasie de l’épithélium dans le nez et une métaplasie dans le larynx. À 102 mg/m3 et au-delà, les incidences d’hyperplasie de l’épithélium respiratoire dans le nez étaient considérablement accrues chez les mâles, tandis que les incidences de métaplasie de l’épithélium respiratoire dans le larynx étaient considérablement accrues chez les femelles. Chez les souris, on a constaté une diminution significative du gain de poids corporel et des changements dans le poids des organes internes chez les 2 sexes (en l’absence de modifications histopathologiques) à 205 mg/m3 et plus, ainsi que des incidences accrues de lésions non néoplasiques des voies respiratoires. À 102 mg/m3, les incidences de métaplasie et de régénération de l’épithélium respiratoire étaient considérablement accrues chez les souris mâles. Le NTP a jugé que la CSENO pour les effets sur les voies respiratoires chez les rats et les souris était de 51 mg/m3 et que la CSENO pour les effets non liés aux voies respiratoires chez les souris était de 102 mg/m3 (NTP, 2017).
Aucune étude sur la toxicité à doses répétées par voie orale n’a été rapportée pour la 2,3-PD. Ainsi, l’extrapolation d’une voie d’exposition à l’autre de la CSENO pour les effets non liés aux voies respiratoires a été faite à partir de l’étude d’inhalation subchronique sur la 2,3-PD, pour obtenir une DSENO de 24 mg/kg p.c./jour (voir l’annexe F). La DSENO de l’étude sur l’exposition orale subchronique au diacétyle a aussi été utilisée pour la lecture croisée, afin d’estimer une DSENO de 105 mg/kg p.c./jour pour la 2,3-PD, valeur utilisée à l’appui de la caractérisation des risques (voir l’annexe F).
Toxicité aiguë et à doses répétées à court terme
L’exposition aiguë et à court terme à la 2,3-PD pendant une période allant jusqu’à 2 semaines a causé une variété de lésions histopathologiques ressemblant à des lésions associées à la bronchiolite oblitérante semblables à celles observées chez l’humain (dont la rhinite nécrosante, la trachéite, l’inflammation des muqueuses, la métaplasie squameuse et des changements régénératifs, l’atrophie de l’épithélium et des dépôts d’exsudats et de lymphoïdes) dans le nez, le larynx, la trachée ou les poumons des souris et des rats à toutes les concentrations analysées (Morgan et coll., 2012; Hubbs et coll., 2012; Zaccone et coll., 2013; NTP, 2018).
Effets chez les humains
Comme le diacétyle, la 2,3-PD est un aromatisant α-dicarbonyle supplémentaire au goût de beurre qui est utilisé dans l’industrie de fabrication du maïs à éclater au four à micro-ondes et d’autres environnements de fabrication de produits alimentaires, et elle a été décrite comme une cause potentielle de maladies pulmonaires professionnelles (Hubbs et coll., 2019).
7.3.2.3 Acétoïne
L’acétoïne a fait l’objet d’un examen par le PISC (1999) et l’EFSA (2004, 2016). Ces examens servent de base à la caractérisation des effets sur la santé dans la présente évaluation. Une recension des publications scientifiques a été menée à partir d’un an avant l’examen de l’EFSA (2016) jusqu’en janvier 2020, et certains renseignements ont été trouvés dans un rapport technique du NTP sur la cancérogénicité du diacétyle (NTP, 2018).
Toxicocinétique
L’acétoïne se métabolise principalement par oxydation à faible concentration in vivo, et par réduction en diacétyle à forte concentration (EFSA, 2004; NTP, 2007a).
Cancérogénicité et génotoxicité
Dans un essai de dépistage pour la cancérogénicité pulmonaire des additifs alimentaires, dans lequel un nombre limité de tissus ont été évalués, Stoner et coll. (1973) n’ont pas observé d’augmentation du nombre de tumeurs pulmonaires chez les souris de souche A qui avaient reçu de l’acétoïne par injection intrapéritonéale 3 fois par semaine pendant 7 semaines.
Plusieurs études ont indiqué que l’acétoïne n’était pas mutagène pour la salmonelle ou Escherichia coli (OMS, 1999a; EFSA, 2004; NTP, 2017).
Toxicité à doses répétées
Dans une étude de la toxicité par voie orale, des rats CFE mâles et femelles (15/groupe) ont reçu de l’acétoïne dans de l’eau potable à des concentrations de 0, 750, 3 000 ou 12 000 ppm (ce qui équivaut à 0, 85, 330 ou 1 300 mg/kg p.c./jour) pendant 13 semaines (Gaunt et coll., 1972). Aux concentrations de 85 et 330 mg/kg p.c./jour, aucun effet important n’a été observé en ce qui concerne le gain de poids corporel, les résultats des examens hématologiques, la chimie sérique, l’excrétion de cellules rénales, les analyses de concentration dans l’urine, le poids des organes ou l’histopathologie. À la plus forte concentration, le poids corporel a considérablement diminué chez les mâles à partir de la semaine 5, et le poids relatif du foie a considérablement augmenté aux semaines 2, 6 et 13. Ces effets se sont manifestés chez les femelles après 13 semaines. Ils n’étaient accompagnés d’aucun changement histopathologique et étaient probablement dus à la charge métabolique de l’absorption d’acétoïne. Des baisses légères, mais statistiquement significatives, de la concentration d’hémoglobine et des numérations d’érythrocytes ont également été observées à la dose la plus élevée chez les 2 sexes. Les auteurs ont conclu que la DSENO était de 3 000 ppm dans l’eau potable (équivalant à 330 mg/kg p.c./jour), en fonction des effets de diminution du gain de poids corporel et des effets hématologiques (Gaunt et coll., 1972, examiné dans PISC, 1999).
Des rats Winstar Han et des souris B6C3F1/N mâles et femelles ont été exposés à de l’acétoïne par inhalation (corps entier) à des concentrations allant jusqu’à 800 ppm (2 883 mg/m3) à raison de 6 h/jour, 5 jour/semaine pendant 14 semaines. Aucun effet lié à l’exposition sur la survie, le poids corporel, le poids des organes, la pathologie clinique ou l’histopathologie n’a été observé chez l’une ou l’autre espèce après l’exposition à des concentrations d’acétoïne, jusqu’à concurrence de la plus forte concentration analysée (2 883 mg/m3) (NTP, 2017).
7.3.3 Caractérisation des risques posés par les substances du sous-groupe 3 (diacétyle, 2,3-PD et acétoïne)
Diacétyle
Aucun organisme n’a « classé » le diacétyle sur la base de la cancérogénicité ou d’autres effets sur la santé. Toutefois, de récentes études du NTP (2018) sur l’inhalation sur une période de 2 ans ont montré des preuves d’activité cancérogène chez les souris et les rats, ainsi que des augmentations marquées de l’incidence de tumeurs nasales à 179 mg/m3. Des éléments probants indiquent également que le diacétyle pourrait être génotoxique. De l’information plus récente laisse à penser que la toxicité est largement due au fait que le diacétyle existe en tant que composé α-dicarbonyle réactif à chaîne courte, qui provoque une cytotoxicité par la modification de protéines essentielles, des interactions avec l’ADN et des lésions cellulaires causées par des espèces réactives de l’oxygène (Hubbs et coll., 2019).
Une exposition chronique au diacétyle a également haussé l’incidence d’effets non cancérogènes pour le nez, le larynx, la trachée et les poumons des souris à toutes les concentrations analysées (donnant une CMENO de 45 mg/m3), des effets plus graves sur le système respiratoire des souris et des rats se manifestant à des concentrations plus élevées. Un spectre d’effets sur le système respiratoire similaire a également été observé lors d’études sur la toxicité subchronique, à court terme et aiguë chez les rongeurs. L’exposition pulsée et continue au diacétyle pendant à peine 15 minutes a causé des blessures à l’épithélium. Hubbs et coll. (2008) considèrent que la CSENO d’une dose aiguë de diacétyle inhalé est inférieure à 333 mg/m3.
L’ensemble de données disponibles sur la toxicité de l’exposition par voie orale au diacétyle est plus limité. Dans une étude d’exposition subchronique sur des rats, on a noté des effets sur les paramètres hématologiques et le poids de plusieurs organes à 540 mg/kg p.c./jour (DSENO de 90 mg/kg p.c./jour), qui pourraient avoir été secondaires à l’ulcération observée de l’estomac (Colley et coll., 1969, examiné dans PISC, 1999; EFSA, 2004; SCOEL, 2014). À la lumière des limites des autres études recensées sur la toxicité par voie orale (Bawazir, 2016; FDA des É.-U., 1973, examiné dans PISC, 1999; EFSA, 2004), et de la DSENO par voie orale systémique de 330 mg/kg p.c./jour signalée pour l’acétoïne (un métabolite du diacétyle qui s’est avéré moins puissant que le diacétyle dans des études selon des méthodes similaires) dans une étude sur l’eau potable (Gaunt et coll., 1972), il est proposé que la véritable DSENO pour le diacétyle pourrait se situer entre 90 mg/kg p.c./jour et 330 mg/kg p.c./jour.
Plusieurs éléments de preuve démontrent que les effets observés dans des études d’inhalation sur des animaux de laboratoire sont pertinents pour les humains et étayent la conclusion de l’évaluation épidémiologique quantitative des risques posés par le diacétyle (CDC, 2016), d’après des cas signalés de l’apparition de divers troubles respiratoires chez les travailleurs d’usines de fabrication de maïs à éclater au four à micro-ondes ou d’aromatisants (Kreiss et coll., 2002; Parmet et Von Essen, 2002; van Rooy et coll., 2007). Toutefois, les estimations de la modélisation de la dosimétrie laissent entendre que les concentrations de diacétyle dans les tissus des voies respiratoires humaines pourraient être de 20 à 40 fois supérieures à celles des rongeurs exposés (Gloede et coll., 2011) et que les données issues des essais biologiques chez les rongeurs sont à même de sous-estimer le risque de lésions bronchiolaires chez l’humain (Cichocki et Morris, 2017).
L’alimentation constitue la principale source d’exposition de l’ensemble de la population au diacétyle. Pour la population générale âgée de 1 an et plus, l’absorption par voie orale estimée liée à l’utilisation du diacétyle comme possible agent aromatisant dans les aliments (de 55 µg/kg p.c./jour à 133 µg/kg p.c./jour) est moindre que les absorptions estimées de cette substance par sa présence à l’état naturel (de 281 µg/kg p.c./jour à 1 625 µg/kg p.c./jour). Étant donné que la véritable DSENO pour le diacétyle se situe probablement entre 90 mg/kg p.c./jour et 330 mg/kg p.c./jour (étude de toxicité subchronique par voie orale chez le rat) et que les effets chez le rat sont probablement liés à la formation d’ulcères dans l’estomac, l’ingestion de diacétyle due à sa présence naturelle dans les aliments n’a pas été déterminée comme étant préoccupante pour la santé humaine (les ME se situent entre ≥ 55 et ≤ 203). Les ME calculées pour le diacétyle qui découlent de son utilisation comme possible agent aromatisant dans les aliments sont ≥ 677 et sont jugées suffisantes pour compenser les incertitudes dans les données disponibles sur les effets sur la santé et l’exposition utilisées pour caractériser le risque. Qui plus est, le JECFA (OMS, 1999a) a conclu qu’il n’y a « aucun problème de sécurité aux niveaux d’ingestion actuels lorsque [la substance] est utilisée comme agent aromatisant; les composants secondaires ne présentent pas de risque pour la sécurité », d’après les estimations de l’exposition par le régime alimentaire aux substances comprises dans ce groupe d’agents aromatisants.
Le tableau 7‑16 présente toutes les valeurs d’exposition et les effets critiques sur la santé pertinents en ce qui concerne le diacétyle ainsi que les marges d’exposition (ME) obtenues pour la caractérisation des risques.
| Scénario d’exposition | Exposition | Niveau d’effet critique | Paramètre d’effet critique pour la santé | ME |
|---|---|---|---|---|
| Maïs à éclater au four à micro-ondes (inhalation) | Concentration après 15 minutes = 0,04 mg/m3 | CMENO = 333 mg/m3 a | Effets nasaux et laryngés (nécrose/inflammation dans l’épithélium) | 8 325 |
| Hydratant pour le visage (inhalation) | Concentration moyenne pondérée de 6 heures = de 0,0198 (20 ans et plus) à 0,014 (5 à 11 ans) mg/m3 | CMENO = 45 mg/m3 b | Effets nasaux (exsudat et atrophie de l’épithélium olfactif) | de 3 214 à 2 273 |
| Hydratant pour le corps (inhalation) | Concentration moyenne pondérée de 6 heures = 0,04 mg/m3 (12 ans et plus) | CMENO = 45 mg/m3 b | Effets nasaux (exsudat et atrophie de l’épithélium olfactif) | 1 125 |
Abréviations : CMENO = concentration minimale avec effet nocif observé; ME = marge d’exposition.
a Hubbs et coll., 2008. ME cible = 1 000 (x 10 pour l’extrapolation interspécifique; x 10 pour les variations intraspécifiques; x 10 pour l’utilisation d’une CMENO, compte tenu de la gravité de l’effet).
b NTP, 2018. ME cible = 1 000 (x 10 pour l’extrapolation interspécifique; x 10 pour les variations intraspécifiques; x 10 pour l’utilisation d’une CMENO, compte tenu de la gravité de l’effet).
Les ME pour l’exposition par inhalation au diacétyle dans le maïs à éclater au four à micro-ondes ou l’utilisation de cosmétiques sont considérés comme adéquates pour compenser les incertitudes dans les données disponibles sur les effets sur la santé et l’exposition.
L’évaluation des effets sur la santé humaine a tenu compte des sous-groupes de la population canadienne qui, en raison d’une vulnérabilité accrue ou d’une plus grande exposition, peuvent être plus susceptibles de subir des effets nocifs pour la santé. Par exemple, les valeurs d’exposition en fonction de l’âge, y compris pour les nourrissons et les enfants, ont été estimées.
2,3-PD
Aucune donnée sur la cancérogénicité n’a été recensée pour la 2,3-PD.
D’après les résultats préliminaires d’une étude d’inhalation subchronique chez les rats et les souris (NTP, 2017), les voies respiratoires (les voies nasales et le larynx en particulier) sont la cible de la toxicité induite par la 2,3-PD, à l’instar de ce qui fut observé pour le diacétyle. Les incidences des lésions non néoplasiques ont connu une augmentation considérable chez les rats et les souris à des concentrations de 102 mg/m3 et plus (CSENO = 51 mg/m3). Des études à plus court terme ont donné des résultats semblables, avec une CMENO de 205 mg/m3, la plus faible concentration analysée (Morgan et coll., 2012).
Les effets observés chez les souris et les rats exposés à la 2,3-PD sont principalement localisés dans les voies respiratoires, mais des effets systémiques (diminution du gain moyen de poids corporel et du poids des organes) sont également observés à 205 mg/m3 et plus, en l’absence de modifications histopathologiques. En ce qui a trait aux expositions par voie orale, pour caractériser le risque posé par l’ingestion de 2,3PD, nous avons utilisé l’extrapolation d’une voie d’exposition à l’autre en nous fondant sur l’étude d’inhalation subchronique, ce qui donne une DSENO de 24 mg/kg p.c./jour pour les effets non liés aux voies respiratoires, et le résultat de la lecture croisée à partir de l’étude de toxicité subchronique du diacétyle par voie orale, ce qui donne une DSENO de 105 mg/kg p.c./jour.
La principale source d’exposition de l’ensemble de la population à la 2,3-PD est le régime alimentaire, en particulier les aliments dans lesquels la substance est naturellement présente. Pour la population générale âgée de 1 an et plus, l’absorption par voie orale estimée pour l’utilisation de la 2,3-PD comme possible agent aromatisant dans les aliments (de 1 µg/kg p.c./jour à 4 µg/kg p.c./jour) est moindre que les absorptions estimées de cette substance par sa présence à l’état naturel (de 6,5 µg/kg p.c./jour à 208 µg/kg p.c./jour). La marge d’exposition associée à une DSENO par voie orale de 24 mg/kg p.c./jour basée sur l’extrapolation d’une voie à l’autre est faible. Toutefois, en l’absence de changements histopathologiques dans les organes internes des animaux de laboratoire et à la lumière des approches prudentes employées pour estimer l’exposition à la 2,3PD due à sa présence naturelle dans les aliments, il a été jugé que l’absorption de 2,3-PD découlant de sa présence naturelle dans les aliments n’était pas préoccupante pour la santé humaine (les ME sont comprises entre 115 et 16 154; ME cible = 100 [x 10 pour l’extrapolation interspécifique; x 10 pour les variations intraspécifiques]). Les ME calculées pour la 2,3-PD utilisée comme agent aromatisant possible dans les aliments sont supérieures ou égales à 6 000 (ME cible = 100 [x 10 pour l’extrapolation interspécifique; x 10 pour les variations intraspécifiques]) et sont jugées adéquates pour compenser les incertitudes dans les données disponibles sur les effets sur la santé et l’exposition utilisées pour caractériser le risque. Qui plus est, le JECFA (OMS, 1999a) a conclu ce qui suit : « aucun problème de sécurité aux niveaux d’ingestion actuels lorsque [la substance] est utilisée comme agent aromatisant; les composants secondaires ne présentent pas de risque pour la sécurité » d’après les estimations de l’exposition à la 2,3-PD par le régime alimentaire. Une comparaison des concentrations mesurées de 2,3-PD dans l’air intérieur (2,8 µg/m3) et de la CSENO établie à 9,1 mg/m3 (à partir d’une CSENO de 51 mg/m3 modifiée en fonction d’une exposition continueNote de bas de page 9) donne des marges d’exposition (3 250, ME cible = 100 [x 10 pour l’extrapolation interspécifique; x 10 pour les variations intraspécifiques]) qui sont jugées adéquates pour compenser les incertitudes dans les données disponibles sur les effets sur la santé et l’exposition utilisées pour caractériser le risque.
On a également trouvé de la 2,3-PD dans des produits de consommation, y compris certains assainisseurs d’air en continu pour l’entretien de la maison, et dans des huiles parfumées, qui peuvent servir à assainir l’air. Une comparaison des expositions moyennes pondérées de 6 heures qui ont été estimées pour l’utilisation d’assainisseurs d’air contenant de la 2,3-PD (0,004 mg/m3 à 0,14 mg/m3) et de la CSENO de 51 mg/m3 a donné des marges d’exposition variant entre 364 et 12 750 (ME cible = 100 [x 10 pour l’extrapolation interspécifique; x 10 pour les variations intraspécifiques]) qui sont considérées comme adéquates pour compenser les incertitudes dans les données disponibles sur les effets sur la santé et l’exposition.
L’évaluation des effets sur la santé humaine a tenu compte des sous-groupes de la population canadienne qui, en raison d’une vulnérabilité accrue ou d’une plus grande exposition, peuvent être plus susceptibles de subir des effets nocifs pour la santé. Par exemple, les valeurs d’exposition en fonction de l’âge, y compris pour les nourrissons et les enfants, ont été estimées.
Acétoïne
Il existe peu d’études sur la toxicité de l’acétoïne. L’acétoïne n’a pas favorisé l’apparition de tumeurs pulmonaires dans un essai restreint de dépistage pour vérifier la cancérogénicité des additifs alimentaires chez la souris (Stoner et coll., 1973). On ne prévoit pas que l’acétoïne soit génotoxique.
Pour caractériser le risque associé à l’exposition à l’acétoïne par voie orale, nous avons utilisé une DSENO de 330 mg/kg p.c./j, fondée sur des changements dans le poids corporel et les paramètres hématologiques déterminés dans une étude de 13 semaines chez le rat (Gaunt et coll. 1972, examiné dans OMS, 1999a).
Selon un compte rendu préliminaire des résultats d’une étude d’inhalation, l’acétoïne n’a causé aucun effet chez les souris exposées à des concentrations allant jusqu’à 2833 mg/m3 pendant 14 semaines (NTP, 2017), ce que nous considérons être la CSENO.
Les aliments dans lesquels elle est naturellement présente sont la principale source d’exposition à l’acétoïne de l’ensemble de la population. L’absorption orale estimée liée à l’utilisation de l’acétoïne comme possible agent aromatisant dans les aliments consommés par la population générale âgée de 1 an et plus (de 30 µg/kg p.c./j à 47 µg/kg p.c./j) est moindre que les absorptions estimées de cette substance par sa présence à l’état naturel (de 161 µg/kg p.c./j à 369 µg/kg p.c./j). L’absorption supplémentaire d’acétoïne en raison de sa présence naturelle dans les aliments n’a pas été jugée préoccupante pour la santé humaine. Sur la base des approches prudentes employées pour estimer l’exposition à l’acétoïne en raison de sa présence naturelle dans les aliments, l’absorption d’acétoïne à partir de cette source n’a pas été jugée préoccupante pour la santé humaine (ME variant de 894 à 2050, ME cible = 100 [x10 pour l’extrapolation interspécifique; x10 pour la variation intraspécifique]). Les ME pour l’acétoïne à partir de son utilisation comme possible agent aromatisant dans les aliments sont ≥7021 et sont jugées suffisantes pour compenser les incertitudes des données disponibles sur l’exposition et les effets sur la santé utilisées pour caractériser les risques. Qui plus est, le JEFCA (OMS, 1999a) a conclu qu’il n’y a « aucun problème de sécurité aux niveaux d’ingestion actuels lorsque [la substance] est utilisée comme agent aromatisant; les composants secondaires ne présentent pas de risque pour la sécurité » d’après les estimations de l’exposition par le régime alimentaire pour les substances comprises dans ce groupe d’aromatisants. On a également tenu compte des expositions potentielles par inhalation de l’acétoïne dans le maïs à éclater au micro-ondes. Une comparaison des estimations prudentes des concentrations atmosphériques d’acétoïne provenant du maïs à éclater au micro-ondes (de 10 µg/m3 à 4200 µg/m3) avec la CSENO de 2833 mg/m3 a donné des marges d’exposition variant entre 686 et 288 300 (ME cible = 100 [x10 pour l’extrapolation interspécifique; x10 pour la variation intraspécifique]), jugées suffisantes pour compenser les incertitudes des données disponibles sur l’exposition et les effets sur la santé utilisées pour caractériser les risques.
L’évaluation des effets sur la santé humaine a tenu compte des sous-groupes de la population canadienne qui, en raison d’une vulnérabilité accrue ou d’une plus grande exposition, peuvent être plus susceptibles de subir des effets nocifs pour la santé. Par exemple, les valeurs d’exposition en fonction de l’âge, y compris pour les nourrissons et les enfants, ont été estimées.
7.3.4 Incertitudes dans l’évaluation des risques posés par le diacétyle, la 2,3-PD et l’acétoïne sur la santé humaine
Les principales sources d’incertitude sont présentées dans le tableau ci-dessous. Pour le diacétyle et la 2,3-PD, bien que l’on soit certain qu’ils induisent des effets nocifs pour la santé à la suite d’une exposition par inhalation, une plus grande incertitude entoure la toxicité de ces substances à la suite d’une exposition par voie orale à long terme, car l’ingestion dans la nourriture est une source importante d’exposition de la population en raison de la présence naturelle de ces dicétones dans la nourriture et leur utilisation comme agents aromatisants dans les aliments. Pour l’acétoïne, bien que l’ensemble de données sur les dangers soit limité, suffisamment de données probantes indiquent que la substance est moins toxique que le diacétyle.
Une incertitude entoure la présence naturelle de diacétyle dans le lait consommé par la population canadienne et l’absorption orale quotidienne de diacétyle estimée en fonction d’une concentration élevée, étant donné la vaste plage de concentrations de diacétyle dans le lait mentionnées dans les publications scientifiques.
| Principales sources d’incertitudes | Incidence |
|---|---|
| Absence ou faible quantité de données de surveillance canadiennes sur la présence dans les milieux de l’environnement et les aliments. | +/- |
| En ce qui concerne la présence naturelle de diacétyle, de la 2,3-PD et de l’acétoïne dans la nourriture, lorsque la documentation scientifique présente une vaste plage de concentrations, les valeurs maximales ont été choisies, sauf dans le cas des valeurs aberrantes. | + |
| Les expositions potentielles par inhalation au diacétyle, à la 2,3-PD et à l’acétoïne par le fait de cuisiner avec des aliments qui contiennent ces substances, tant sous leur forme naturelle que dans les aromatisants alimentaires. | - |
| Données insuffisantes pour quantifier les expositions par inhalation à la 2,3-PD à partir du maïs à éclater au micro-ondes. | - |
| Possible exposition combinée au diacétyle, à la 2,3-PD et à l’acétoïne à partir du maïs à éclater au micro-ondes. | - |
| L’hypothèse que les expositions cutanées au diacétyle sont minimes par rapport aux expositions par inhalation, étant donné la forte volatilité de la substance. | - |
| Il n’existe pas d’études sur la toxicité chronique de l’acétoïne et de la 2,3-PD, et l’ensemble de données global sur l’acétoïne est restreint. | - |
| L’ensemble de données sur la toxicité par voie orale du diacétyle, de la 2,3-PD et de l’acétoïne est limité. | +/- |
| Les humains sont jugés plus sensibles que les rats et les souris aux effets respiratoires du diacétyle (et possiblement de la 2,3-PD). | - |
| Aucune donnée sur l’absorption cutanée du diacétyle, de la 2,3-PD et de l’acétoïne n’a été recensée. | +/- |
| Lecture croisée à partir du diacétyle pour évaluer la 2,3-PD étant donné l’absence de données. | +/- |
+ = incertitude pouvant entraîner une surestimation de l’exposition ou du risque; - = incertitude pouvant entraîner une sous-estimation de l’exposition ou du risque; +/- = potentiel inconnu de surestimation ou de sous-estimation du risque.
7.4 Évaluation individuelle de la 2,4-PD
7.4.1 Évaluation de l’exposition
Milieux environnementaux
Aucune donnée n’a été retrouvée sur la présence de 2,4-PD dans l’air intérieur et extérieur, dans l’eau potable ou dans le sol, au Canada comme ailleurs. D’après ses propriétés physiques et chimiques, si elle est rejetée dans l’environnement, la 2,4-PD devrait se répartir principalement (environ 90 %) dans l’eau et dans une moindre mesure (environ 10 %) dans l’air (HSDB, 1983-; OCDE, 2001). La 2,4-PD est susceptible d’avoir une forte mobilité dans le sol et risque peu d’adhérer aux sédiments ou aux particules en suspension dans l’eau (HSDB, 1983-).
Nous avons exécuté le modèle de fugacité de niveau III « ChemCAN » (2003) pour calculer les concentrations potentielles de 2,4-PD dans l’environnement pour le Canada à partir de la quantité la plus élevée figurant dans le tableau 4‑1 (c’est-à-dire 1 000 000 kg) et en présumant que la quantité totale importée était rejetée dans une seule région du Canada (soit la région des plaines à forêts mixtes de l’Ontario). Les concentrations estimées dans l’air, l’eau et le sol étaient respectivement de 6,5 ng/m3, 2,7 ng/L et 0,025 ng/g. Nous avons utilisé ces concentrations pour estimer l’exposition à la 2,4-PD par les milieux environnementaux (air, eau et sol) pour la population générale du Canada. Les concentrations de 2,4-PD dérivées de ChemCAN pour le sol étaient toutes de l’ordre du nanogramme, ce qui se traduit par des expositions de moins de 1 ng/kg p.c./j, une valeur jugée négligeable.
Les estimations de l’exposition à la 2,4-PD par les milieux environnementaux variaient entre 0,002 µg/kg p.c./j pour les adultes de 60 ans et plus à 0,004 µg/kg p.c./j pour les enfants âgés de 6 mois à 4 ans (Santé Canada, 2024). Plus de détails sont disponibles dans le document de Santé Canada (2024).
Aliments
La 2,4-PD est un composé volatil naturellement présent dans certains aliments, comme le bœuf, le poulet, le café, les champignons, la papaye et le fruit de la passion (Nijssen et coll., 1963-2018). Seules des données quantitatives sur le poulet rôti (0,004 ppm) et le jus de fruit de la passion (moins de 0,01 ppm) étaient disponibles. Elles ont servi à estimer les expositions potentielles de la population générale du Canada à la 2,4-PD contenue dans la nourriture. Les estimations quantitatives de l’exposition à la 2,4-PD en raison de sa présence naturelle dans les alimentsNote de bas de page 5 variaient de 0,02 µg/kg p.c./j pour les adultes de 19 ans et plus à 0,1 µg/kg p.c./j pour les enfants âgés de 1 à 3 ans (voir l’annexe C pour les détails).
Il ne devrait pas y avoir d’exposition à la 2,4-PD découlant de son utilisation dans la fabrication de matériaux d’emballage alimentaire.
Produits utilisés par les consommateurs
On n’a signalé la présence de 2,4-PD dans aucun produit de consommation au Canada.
7.4.2 Évaluation des effets sur la santé
L’OCDE (2001) et l’EFSA (2004) ont étudié la 2,4-PD. Ces études servent de base à la caractérisation des effets sur la santé dans la présente évaluation. Une recension des publications scientifiques a été menée à partir d’un an avant la publication du rapport d’évaluation initiale de l’ensemble de données préalables par l’OCDE (2001) jusqu’en juin 2017, et des recherches ciblées ont été effectuées jusqu’en janvier 2020. Les nouveaux renseignements importants ont été inclus pour appuyer la caractérisation des risques.
Toxicocinétique
L’EFSA (2004) a noté qu’en raison de sa structure et de ses caractéristiques physicochimiques, la substance devrait être rapidement absorbée par le tractus gastro-intestinal et largement distribuée et métabolisée. Aucun renseignement sur la toxicocinétique n’a été recensé pour l’exposition cutanée à la 2,4-PD.
Cancérogénicité et génotoxicité
Dans le cadre d’une étude sur la cancérogénicité par inhalation, des rats F344 et des souris B6D2F1 ont été exposés à des vapeurs de 2,4-PD à des concentrations cibles de 0, de 100, de 200 ou de 400 ppm (0, 417, 834 ou 1668 mg/m3, respectivement) pendant 6 h/j, 5 j/sem, durant 2 ans (JBRC, 2010a, b). Aucune incidence accrue de lésions néoplasiques n’a été observée dans le grand éventail de tissus des animaux exposés qui ont été examinés.
L’OCDE (2001) et l’EFSA (2004) ont étudié la génotoxicité potentielle de la 2,4-PD. Dans l’ensemble, la 2,4-PD ne s’est pas toujours avérée mutagène in vitro, mais présentait un potentiel clastogène (aberrations chromosomiques et échanges de chromatides sœurs), notamment en l’absence d’activation métabolique (Ballantyne et Cawley, 2001; OCDE, 2001; NTP, 2019). In vivo, un potentiel clastogène (micronoyaux) a été observé chez les souris exposées par administration orale et intrapéritonéale, mais pas chez les rats ou les souris exposés par inhalation, ce qui indique une dépendance par rapport à la voie d’exposition (Ballantyne et Cawley, 2001; OCDE, 2001; NTP, 2019). L’administration de 2,4-PD par voie orale a causé des dommages à l’ADN chez les souris (NTP, 2019), mais pas chez les rats (ECHA, c2007-2019d). Il n’y a pas eu d’aberrations chromosomiques dans les spermatogonies des souris (OCDE, 2001), bien que l’exposition par inhalation ait entraîné un léger effet à dominance létale réversible chez les rats (Tyl et coll., 1989). L’EFSA (2004) a conclu que l’utilisation de la 2,4-PD comme substance aromatisante n’était pas acceptable en raison de son potentiel génotoxique (clastogène).
Toxicité à doses répétées
Dans le cadre d’une étude par voie cutanée, des lapins blancs néo-zélandais ont été exposés quotidiennement pendant 9 jours à des doses de 0, 244, 975 et 1463 mg/kg p.c./j de 2,4-PD par contact obstrué (Ballantyne, 2001, cité dans OCDE, 2001). Environ 50 % des animaux de l’un ou de l’autre sexe du groupe ayant reçu une dose élevée (1463 mg/kg p.c./j) sont morts. Aux doses moyenne et élevée, la 2,4-PD a causé des signes d’hypoactivité, de prostration, de salivation, de tremblements, de halètement, de convulsions, de cyanose (indiquée par le bleuissement du derme de la région nasale), ainsi qu’une diminution du gain de poids corporel et de la consommation alimentaire, de même que des hémorragies et une dégénérescence neuronale dans le cerveau. D’après les effets systémiques, l’auteur a déterminé une DSENO de 244 mg/kg p.c./j et une DMENO de 975 mg/kg p.c./j.
Selon les données limitées sur l’exposition par voie orale, l’administration par gavage de doses de 500 mg/kg p.c./j à des rats pendant 2 semaines a causé un éventail d’effets systémiques sur la vessie, les poumons, les yeux, le thymus, le foie, les reins, le cœur et les ganglions, et tous les animaux ayant reçu 1000 mg/kg p.c./j sont morts. On considère que la DSENO est de 100 mg/kg p.c./j (Eastman Kodak, 1979, cité par OCDE, 2001). D’autres études par gavage menées par ces chercheurs sont citées dans EFSA (2004), dont une étude de 126 jours sur des rats (DSENO inférieure à 200 mg/kg p.c./j) et une étude de 14 jours sur des lapins (DSENO = 250 mg/kg p.c./j). Toutefois, les détails publiés sont insuffisants pour permettre une évaluation.
Dans le cadre de l’étude de 2 ans sur la cancérogénicité par inhalation décrite précédemment, des rats et des souris ont été exposés à des concentrations de 2,4-PD allant jusqu’à 1668 mg/m3 (JBRC, 2010a,b). Chez les rats, les lésions non néoplasiques étaient principalement localisées dans la cavité nasale chez les 2 sexes aux concentrations de 834 mg/m3 et plus, y compris une métaplasie pavimenteuse de l’épithélium respiratoire, une inflammation et une hyperplasie de l’épithélium transitoire et une atrophie de l’épithélium olfactif. De même, les effets sur la cavité nasale observés chez les souris comprenaient une métaplasie pavimenteuse, des changements éosinophiles, des ulcères, une nécrose et une hyperplasie des cellules transitionnelles dans l’épithélium respiratoire, une atrophie, une métaplasie respiratoire, des changements éosinophiles et une nécrose dans l’épithélium olfactif ainsi qu’une métaplasie respiratoire dans la glande sous-muqueuse à 834 mg/m3 et à 1668 mg/m3, tandis que l’exsudat et l’atrophie dans l’épithélium olfactif se sont produits à toutes les concentrations. On a également noté des modifications des paramètres biochimiques chez les mâles et les femelles à 834 mg/m3 et à 1668 mg/m3. D’après les lésions nasales, les auteurs de l’étude ont déterminé que 417 mg/m3 constituait la CSENO chez les rats et la CMENO chez les souris (JBRC, 2010a,b).
L’exposition des rats par inhalation à 0, 100, 300 ou 650 ppm (0, 417, 1217 ou 2711 mg/m3, respectivement) de 2,4-PD pendant 14 semaines a induit une grande variété d’effets systémiques à 1217 mg/m3 et plus, et une mortalité élevée à 2711 mg/m3. D’après les effets sur la chimie hématologique, clinique et urinaire dans le groupe exposé à 1217 mg/m3 et les effets graves observés à 2711 mg/m3, y compris des effets histopathologiques au cerveau et au thymus, les auteurs ont établi une CSENO de 417 mg/m3 pour cette étude (Dodd et coll., 1986, cité dans OCDE 2001). Dans une étude de 2 semaines menée par les mêmes auteurs, la CSENO et la CMENO ont été fixées à 834 mg/m3 et à 1668 mg/m3, respectivement, d’après le poids réduit des organes et la nécrose ou l’inflammation nasale à de plus fortes concentrations (OCDE, 2001).
Puisqu’aucune étude de la toxicité par voie orale n’était disponible, on a procédé à une extrapolation d’une voie à l’autre à partir de la CSENO par inhalation de 417 mg/m3 tirée de l’étude de 14 semaines susmentionnée pour obtenir une DSENO par voie orale de 23 mg/kg p.c./j (voir l’annexe F).
Toxicité pour la reproduction et le développement
Dans l’étude par inhalation subchronique effectuée sur des rats F344 mâles et femelles exposés à la 2,4-PD, à des concentrations allant jusqu’à 2711 mg/m3, on n’a noté aucun résultat pathologique important dans les testicules et les épididymes des mâles ni dans l’utérus, le col et les ovaires des femelles (Dodd et coll.,1986, cité dans OCDE, 2001). On n’a recensé aucune étude se penchant sur les effets potentiels de l’exposition à la 2,4-PD sur la performance reproductive.
Dans une étude sur la toxicité par inhalation pour le développement, des rattes F344 gravides ont été exposées à des concentrations de 0, 53, 202 ou 398 ppm (0, 217, 827 ou 1629 mg/m3, respectivement) de 2,4-PD pendant 6 h/j les JG 6 à 15 (Tyl et coll., 1990). Aucun effet n’a été observé sur le nombre de corps jaunes, d’implants par portée, de pertes avant ou après l’implantation ou sur le rapport de masculinité des fœtus. On a rapporté une réduction importante du poids corporel des fœtus par portée (environ 10 %) chez les mâles, les femelles et tous les fœtus à 1629 mg/m3. À cette concentration, un schéma constant de diminution de l’ossification du fœtus, de variations du squelette et de poids réduit de la mère a aussi été rapporté. À 827 mg/m3, on a observé une réduction légère, mais statistiquement significative (d’environ 3 %), du poids corporel des fœtus par portée, mais seulement chez les mâles. Les auteurs ont conclu que la CSEO était de 217 mg/m3 pour la toxicité maternelle et la toxicité pour le développement (Tyl et coll., 1990). De même, l’OCDE (2001) a conclu que la CSENO pour le développement était de 217 mg/m3. Toutefois, à la lumière de la diminution minime du poids corporel des fœtus mâles seulement, ce qui est peu susceptible d’être jugé nocif, on considère, aux fins de la présente évaluation des effets sur la santé, que la CSENO de toxicité pour le développement et de toxicité maternelle est de 827 mg/m3.
7.4.3 Caractérisation des risques posés par la 2,4-PD
La 2,4-PD ne s’est pas avérée cancérogène pour les rats et les souris exposés par inhalation. Des lésions non cancéreuses étaient principalement localisées dans la cavité nasale (JBRC, 2010a,b). On a toutefois signalé des effets clastogènes pour la 2,4-PD, ce qui a amené l’EFSA (2004) à conclure que l’utilisation de la 2,4-PD comme aromatisant alimentaire n’était pas acceptable.
Les toxicités systémiques et pour le développement sont jugées être des effets critiques sur la santé aux fins de la caractérisation des risques liés à l’exposition par inhalation à court terme à la 2,4-PD. La CSENO pour la toxicité systémique et pour le développement chez les rats a été fixée à 827 mg/m3. Une CSENO de 834 mg/m3 établie dans le cadre d’une étude de 14 jours chez le rat (Dodd et coll., 1986, cité dans OCDE, 2001) appuie la sélection de cette concentration entraînant un effet critique pour la caractérisation des risques. En ce qui touche l’exposition à plus long terme, divers effets systémiques ont été observés durant l’étude de 14 semaines chez le rat, et la CSENO a été fixée à 417 mg/m3 (Dodd et coll., 1986, cité dans OCDE, 2001).
Pour ce qui est de l’exposition chronique, en raison des données limitées, nous avons tenu compte de l’étude par gavage à court terme qui a produit une DSENO de 100 mg/kg p.c./j (Eastman Kodak,1979, cité dans OCDE, 2001) et d’une extrapolation d’une voie à l’autre à partir de l’étude de toxicité par inhalation pour le développement pour une exposition à plus long terme, ce qui a donné une DSENO de 23 mg/kg p.c./j.
L’exposition par voie cutanée à la 2,4-PD a aussi produit différents effets chez les lapins ayant reçu 500 mg/kg p.c./j; ainsi, une DSENO de 244 mg/kg p.c./j (Ballantyne, 2001, cité dans OCDE, 2001) a été utilisée pour caractériser les risques associés à l’exposition par voie cutanée à la 2,4-PD.
La population générale du Canada est exposée à la 2,4-PD en petites quantités par les milieux environnementaux et l’alimentation en raison de la présence naturelle de la substance dans les aliments. La comparaison des estimations de l’exposition à la 2,4-PD dans les milieux environnementaux (0,002 µg/kg p.c./j à 0,004 µg/kg p.c./j) et des CSENO de 100 mg/kg p.c./j (toxicité systémique dans une étude par voie orale de 2 semaines) et de 23 mg/kg p.c./j (extrapolation d’une voie à l’autre à partir d’une étude par inhalation de 14 semaines) a donné lieu à des ME (>3 millions, ME cible = 100 [x10 pour l’extrapolation interspécifique; x10 pour la variation intraspécifique]) jugées suffisantes pour compenser les incertitudes des données disponibles sur l’exposition et les effets sur la santé utilisées pour caractériser les risques. L’absorption supplémentaire de 2,4-PD en raison de sa présence naturelle dans les aliments n’a pas été jugée préoccupante pour la santé humaine.
Les ME calculées pour l’exposition à la 2,4-PD dans les milieux environnementaux sont jugées suffisantes pour compenser les incertitudes des données disponibles sur l’exposition et les effets sur la santé utilisées pour caractériser les risques. L’absorption supplémentaire de 2,4-PD en raison de sa présence naturelle dans les aliments n’a pas été jugée préoccupante pour la santé humaine.
L’évaluation des effets sur la santé humaine a tenu compte des sous-groupes de la population canadienne qui, en raison d’une vulnérabilité accrue ou d’une plus grande exposition, peuvent être plus susceptibles de subir des effets nocifs pour la santé. Par exemple, nous avons estimé les valeurs d’exposition en fonction de l’âge, y compris pour les nourrissons et les enfants, et avons examiné les études de toxicité pour le développement et la reproduction afin de dégager les effets nocifs potentiels sur la santé.
Bien que l’exposition de la population générale à la 2,4‑PD ne soit pas préoccupante aux niveaux actuels, il est possible que les niveaux d’exposition augmentent à l’avenir. Étant donné les possibles effets préoccupants pour la santé associés à cette substance, une augmentation des niveaux d’exposition pourrait entraîner des préoccupations pour la santé humaine.
7.4.4 Incertitudes dans l’évaluation des risques pour la santé humaine
Les principales sources d’incertitude sont présentées dans le tableau ci-dessous. À la lumière des données démontrant la génotoxicité de la 2,4-PD, il serait utile d’avoir d’autres données provenant d’études à plus long terme afin d’accroître la certitude que les éventuels risques liés aux expositions prolongées seraient faibles.
| Principale source d’incertitude | Incidence |
|---|---|
| Absence ou faible quantité de données de surveillance canadiennes sur la présence dans les milieux environnementaux et les aliments. | +/- |
| Il n’existe pas d’étude de toxicité chronique par voie orale ou cutanée ou d’étude de toxicité subchronique par voie orale pour la 2,4-PD. | +/- |
+ = incertitude pouvant entraîner une surestimation de l’exposition ou du risque; - = incertitude pouvant entraîner une sous-estimation de l’exposition ou du risque; +/- = potentiel inconnu de surestimation ou de sous-estimation du risque.
7.5 Évaluation individuelle de l’oxyde de mésityle
7.5.1 Évaluation de l’exposition
Milieux environnementaux
On a mesuré la quantité d’oxyde de mésityle dans l’étude sur l’air intérieur dans le cadre du cycle 2 de l’Enquête canadienne sur les mesures de la santé (ECMS) et lors d’une étude plus succincte sur l’air intérieur au Québec (communication personnelle, courriel du Bureau de la science et de la recherche en santé environnementale [BSRSE], SC, au BERSE, SC, daté de décembre 2012, source non citée; Won et Lusztyk, 2011). On a détecté de l’oxyde de mésityle dans moins de 12 % des échantillons (limite de détection de 0,16 µg/m3) lors de l’étude de l’ECMS, avec une concentration moyenne géométrique inférieure à la limite de détection et une concentration au 95e centile de 0,26 µg/m3 (données pondérées à l’échelle du ménage) (Zhu et coll., 2013). La concentration moyenne géométrique d’oxyde de mésityle mesurée dans 12 échantillons d’air intérieur prélevés dans le cadre de l’étude sur le terrain au Québec était de 0,30 µg/m3 et la concentration maximale, de 4,15 µg/m3 (Won et Lusztyk, 2011).
Aucune donnée canadienne sur la présence d’oxyde de mésityle dans l’eau n’a été recensée. On a détecté qualitativement de l’oxyde de mésityle dans l’eau potable de Cincinnati, en Ohio, ainsi que dans une rivière en Suisse (HSDB, 1983-). En raison de sa constante de la loi d’Henry modérée et de sa pression de vapeur élevée, l’oxyde de mésityle est susceptible de se volatiliser depuis l’eau (HSDB, 1983-). L’eau potable ne devrait donc pas être une source importante d’exposition de la population.
Aucune donnée n’a été recensée sur la présence d’oxyde de mésityle dans le sol au Canada ou ailleurs. En raison de son faible log Kco, l’oxyde de mésityle est susceptible d’avoir une forte mobilité dans le sol et risque peu de se lier aux sédiments ou aux particules en suspension dans l’eau (HSDB, 1983-); le sol ne devrait donc pas être une source importante d’exposition.
Les estimations de l’exposition à l’oxyde de mésityle par l’air (en supposant que les concentrations dans l’air intérieur et l’air ambiant sont identiques) variaient de 0,08 µg/kg p.c./j pour les adultes de 60 ans et plus à 2,5 µg/kg p.c./j pour les enfants âgés de 6 mois à 4 ans (Santé Canada, 2024). Plus de détails sont disponibles dans le document de Santé Canada (2024).
Aliments
L’oxyde de mésityle est naturellement présent dans divers aliments, comme la nectarine, le poivron, la tomate, le pain croustillant, le fromage parmesan, le lait, le café, le thé, les arachides, le basilic et les crevettes pour n’en nommer que quelques-uns (Nijssen et coll., 1963-2018; Burdock, 2010). Il peut également servir d’aromatisant alimentaire dans les produits de boulangerie, les produits laitiers surgelés, les gélatines et les poudings, les produits laitiers et les bonbons mous (Burdock, 2010). Les estimations quantitatives de l’exposition à l’oxyde de mésityle en raison de sa présence naturelle dans les alimentsNote de bas de page 5 variaient de 0,3 µg/kg p.c./j pour les bébés âgés de 6 à 12 mois à 2 µg/kg p.c./j pour les enfants de 2 à 3 ans (voir l’annexe C pour les détails). Faute de données sur l’utilisation réelle de la substance au Canada, l’estimation de l’absorption par personne constitue une estimation acceptable de l’exposition possible par le régime alimentaire de la population générale (1 an et plus) à l’oxyde de mésityle en raison de son utilisation comme aromatisant alimentaire.
Le JECFA a évalué un groupe d’alcools aliphatiques secondaires, de cétones et d’esters apparentés utilisés comme substances aromatisantes, y compris l’oxyde de mésityle (OMS, 2003). Dans le cadre de cette évaluation, le Comité estimait que l’absorption d’oxyde de mésityle par une personne découlant de son utilisation en tant qu’aromatisant alimentaire était de 0,0067 µg/kg p.c./j pour la population européenne (aucune donnée d’absorption n’a été rapportée pour les États-Unis) (voir l’annexe C pour les détails).
Produits de consommation
On n’a signalé la présence d’oxyde de mésityle dans aucun produit de consommation au Canada.
7.5.2 Évaluation des effets de l’oxyde de mésityle sur la santé
L’oxyde de mésityle a été étudié par l’OCDE (1997b) et l’EFSA (2012). Ces études servent de base à la caractérisation des effets sur la santé dans la présente évaluation. Une recension des publications scientifiques a été menée à partir d’un an avant la publication de l’OCDE (1997b) jusqu’en octobre 2019. Nous n’avons recensé aucune nouvelle information sur les effets de l’exposition à l’oxyde de mésityle sur la santé.
Peu de renseignements toxicologiques sont disponibles pour l’oxyde de mésityle. Par conséquent, l’extrapolation d’une voie à l’autre pour l’oxyde de mésityle s’appuie sur une lecture croisée à partir de l’analogue 6-méthyl-5-heptén-2-one ou MHE (NR CAS 110-93-0). Le MHE a été le seul analogue retenu pour la lecture croisée de l’oxyde de mésityle en fonction de sa similitude structurale et de la disponibilité des données (TERA, 2004). L’oxyde de mésityle et le MHE sont tous 2 des cétones insaturées; l’oxyde de mésityle contient un groupe alcène et un groupe cétone sur des atomes de carbone adjacents, tandis que l’on trouve 2 autres carbones dans la chaîne entre le groupe alcène et cétone du MHE. Cette différence structurale laisse à penser que l’oxyde de mésityle pourrait être plus réactif (et donc plus toxique) que le MHE en raison de la présence d’un carbonyle α,β-insaturé. Les données sur la toxicité du MHE ont servi à la lecture croisée pour l’oxyde de mésityle lorsque nécessaire.
Cancérogénicité et génotoxicité
Aucune donnée sur la cancérogénicité n’a été recensée pour l’oxyde de mésityle.
L’oxyde de mésityle ne s’est pas avéré mutagène pour Salmonella, Escherichia coli ou lors du test du lymphome de souris, ni n’a induit de micronoyaux dans les lymphocytes humains cultivés ou chez les souris qui ont reçu de l’oxyde de mésityle par injection intrapéritonéale (ECHA, c2007-2019e).
Toxicité à doses répétées
Il existe 2 études sur la toxicité à doses répétées par inhalation de l’oxyde de mésityle et il n’y a pas de données disponibles sur les voies d’exposition orale et cutanée.
Une étude combinée de toxicité à doses répétées et de toxicité pour la reproduction et le développement a été menée sur des groupes de rats SD exposés par inhalation du corps entier à l’oxyde de mésityle à des concentrations de 0, 31, 103 et 302 ppm (0, 124, 413 et 1211 mg/m3, respectivement) pendant 6 h/j, 7 j/sem pour un total de 49 expositions pour les rats mâles et de 36 à 49 expositions pour les rats femelles. Il n’y a pas eu d’effets sur la mortalité, les paramètres hématologiques ou urinaires, ni de pathologie clinique chez les animaux parents. Toutefois, d’importantes réductions de la consommation alimentaire, du poids corporel et du gain de poids corporel ainsi que des anomalies cliniques et une pathologie des voies nasales ont été observées chez tous les groupes d’essai en fonction de la concentration. Les anomalies cliniques comprenaient une incidence accrue d’écoulement de porphyrine par le nez et de sialorrhée après l’exposition. Les observations histopathologiques comprenaient la présence d’exsudats sérocellulaires, une inflammation focale chronique et une métaplasie focale de l’épithélium respiratoire et olfactif des voies nasales. Ces changements sont considérés comme une réaction commune à une vapeur irritante (Bernard et Faber, 1992, cité dans OCDE, 1997b). Une CMENO par inhalation de 124 mg/m3 a été déterminée en fonction des effets sur la consommation alimentaire, le poids corporel, le gain de poids corporel et l’histopathologie des voies nasales (OCDE, 1997b; US EPA, 2006; ECHA, c2007-2019e). Aucune CSENO par inhalation pour la toxicité systémique n’a été déterminée dans cette étude.
Des groupes de rats Wistar et de cobayes des 2 sexes ont été exposés par inhalation du corps entier à l’oxyde de mésityle à des concentrations de 0, 50, 100, 250 ou 500 ppm (0, 200, 400, 1000 ou 2000 mg/m3, respectivement) à raison de 8 h/j, 5 j/sem pendant 6 semaines. Les résultats publiés n’étaient pas ventilés par espèce. Une incidence accrue de mortalité (65 %) a été relevée à 2000 mg/m3, après quoi les auteurs ont limité à 10 le nombre d’expositions à cette concentration. Des conjonctivites chroniques, une irritation nasale et une albuminurie légère ont été observées à 1000 mg/m3 et à 2000 mg/m3. Des augmentations des effets pathologiques en lien avec les concentrations ont été observées dans les reins, les poumons et/ou le foie à des doses de 400 mg/m3 et plus. Les changements pathologiques comprenaient les retards de croissance, la congestion du foie, la dilatation de la capsule de Bowman, l’enflure et des circonvolutions de l’épithélium tubulaire dans les reins et la congestion des poumons. Aucun effet n’a été observé à une concentration de 200 mg/m3 (Smyth et coll., 1942). Une CSENO de 200 mg/m3 a été incluse dans le dossier d’enregistrement présenté à l’ECHA au titre du règlement REACH d’après les changements pathologiques observés dans les poumons, le foie et/ou les reins (ECHA, c2007-2019e).
Toxicité pour la reproduction et le développement
Dans le cadre de l’étude combinée de toxicité à doses répétées et de toxicité pour la reproduction et le développement décrite précédemment (Bernard et Faber, 1992, cité dans OCDE, 1997b), lors de laquelle des groupes de rats SD ont été exposés à l’oxyde de mésityle pendant 49 jours dans le cas des mâles et de 36 à 49 jours dans le cas des femelles (jusqu’au JG 20), on n’a relevé aucun effet important sur les organes reproducteurs, le rendement de la reproduction ou la durée de la gestation, et ce, pour aucune des concentrations d’essai. Toutefois, une réduction du nombre de portées produites par les couples reproducteurs a été observée à une concentration de 1211 mg/m3. Aucune malformation externe n’a été notée, mais les petits n’ont subi aucun examen histopathologique. La CSENO de toxicité pour la reproduction était de 413 mg/m3 d’après la diminution du nombre de portées (Bernard et Faber, 1992, cité dans OCDE, 1997b; US EPA, 2006; ECHA, c2007-2019e).
On n’a recensé aucune donnée sur une éventuelle toxicité pour la reproduction et le développement attribuable à l’exposition par voie orale ou cutanée à l’oxyde de mésityle.
Extrapolation d’une voie à l’autre et caractérisation des risques par lecture croisée
En raison du manque de données sur la toxicité de l’oxyde de mésityle administré par voie orale, les observations tirées d’études par inhalation ont servi à extrapoler d’une voie à l’autre. Dans l’étude combinée de toxicité à doses répétées et de toxicité pour la reproduction et le développement chez le rat, les effets critiques se sont manifestés principalement dans les voies nasales (c’est-à-dire le point de contact), ce que l’OCDE (1997b) a attribué aux propriétés irritantes de l’oxyde de mésityle. Pour dériver la DSENO par voie orale de l’oxyde de mésityle, nous avons donc jugé qu’il était plus approprié d’utiliser la CSENO de 2200 mg/m3 tirée de l’étude par inhalation de 6 semaines sur des rats, chez qui des effets systémiques dans le foie et les reins ont été observés. La DSENO par voie orale ajustée pour la toxicité à doses répétées est de 15,0 mg/kg p.c./j (voir l’annexe F).
Nous avons déterminé que le MHE (NR CAS 110-93-0) était le seul analogue pouvant servir à la lecture croisée pour l’oxyde de mésityle, en raison de sa similitude structurale et de la disponibilité des données (TERA, 2017). Une DSENO de 39 mg/kg p.c./j pour l’oxyde de mésityle peut être déduite par lecture croisée de la DSENO par voie orale de 50 mg/kg p.c./j du MHE (d’après les modifications des paramètres de chimie hématologique et clinique lors d’une étude de 90 jours chez le rat [OCDE, 2003] en appliquant une correction pour tenir compte de la masse moléculaire [annexe A, tableau A-4]). La DSENO fondée sur la lecture croisée pour l’oxyde de mésityle ressemble à la DSENO obtenue par extrapolation d’une voie à l’autre (elle est seulement 2 fois et demie plus élevée, ce à quoi l’on peut s’attendre, étant donné que la chaîne est plus longue).
7.5.3 Caractérisation des risques posés par l’oxyde de mésityle
Aucune étude sur la cancérogénicité de l’oxyde de mésityle n’a été recensée.
La CMENO de 124 mg/m3 pour la toxicité systémique chez le rat a servi à caractériser le risque associé à l’exposition par inhalation à l’oxyde de mésityle (OCDE, 1997b; ECHA, c2007-2019e). Même si l’on n’a trouvé aucune étude de la toxicité par voie orale de l’oxyde de mésityle, l’extrapolation de la CSENO d’une voie à l’autre à partir d’une étude par inhalation de 6 semaines (Smyth et coll., 1942; ECHA, c2007-2019e) est jugée appropriée pour caractériser les dangers potentiels associés à l’ingestion de la substance. On a déterminé que la DSENO équivalente par voie orale est de 15 mg/kg p.c./j (voir l’annexe F). Cette valeur est appuyée par la lecture croisée des données sur la toxicité d’une substance analogue, le MHE.
La population générale est principalement exposée à l’oxyde de mésityle par l’air et le régime alimentaire en raison de la présence naturelle de la substance dans certains aliments.
On n’a signalé la présence d’oxyde de mésityle dans aucun produit de consommation au Canada.
Une comparaison des estimations de l’exposition à l’oxyde de mésityle par l’air (en supposant que les concentrations dans l’air intérieur et l’air ambiant sont identiques, de 1,2 µg/kg p.c./j à 2,5 µg/kg p.c./j) et par son utilisation possible comme aromatisant alimentaire pour la population générale de 1 an et plus (0,0067 µg/kg p.c./j) avec la DSENO de 15 mg/kg p.c./j a donné des ME supérieures à 6000 (ME cible = 100 [x10 pour l’extrapolation interspécifique; x10 pour la variation intraspécifique]), qui sont jugées suffisantes pour compenser les incertitudes des données disponibles sur l’exposition et les effets sur la santé utilisées pour caractériser les risques. L’absorption supplémentaire d’oxyde de mésityle en raison de sa présence naturelle dans les aliments n’a pas été jugée préoccupante pour la santé humaine. Qui plus est, le JEFCA (OMS, 2003) a conclu qu’il n’y a « aucun problème de sécurité aux niveaux d’ingestion actuels lorsque [la substance] est utilisée comme agent aromatisant » d’après les estimations de l’exposition à l’oxyde de mésityle par le régime alimentaire.
L’évaluation des effets sur la santé humaine a tenu compte des sous-groupes de la population canadienne qui, en raison d’une vulnérabilité accrue ou d’une plus grande exposition, peuvent être plus susceptibles de subir des effets nocifs pour la santé. Par exemple, nous avons estimé les valeurs d’exposition en fonction de l’âge et examiné les études de toxicité pour le développement et la reproduction afin de dégager les effets nocifs qu’il pourrait y avoir sur la santé.
7.5.4 Incertitudes dans l’évaluation des risques pour la santé humaine
Les principales sources d’incertitude sont présentées dans le tableau ci-dessous. Bien que l’ensemble de données sur l’oxyde de mésityle soit limité, à la lumière des ME élevées, il est fort probable que le risque posé par cette substance pour la population canadienne soit faible.
| Principale source d’incertitude | Incidence |
|---|---|
| Les données de surveillance environnementale sont limitées pour l’oxyde de mésityle. | + |
| L’ensemble de données sur les dangers est limité pour l’oxyde de mésityle (en particulier en ce qui concerne les données à long terme). | +/- |
+ = incertitude pouvant entraîner une surestimation de l’exposition ou du risque; - = incertitude pouvant entraîner une sous-estimation de l’exposition ou du risque; +/- = potentiel inconnu de surestimation ou de sous-estimation du risque.
8. Conclusion
Compte tenu de tous les éléments de preuve présentés dans la présente évaluation, la MEK, la MPK, la MIBK, la MIAK, l’alcool de diacétone, le diacétyle, la 2,3-PD, l’acétoïne, la 2,4-PD et l’oxyde de mésityle présentent un faible risque de causer des effets nocifs pour l’environnement. Il est conclu que ces 10 substances ne satisfont pas aux critères énoncés aux alinéas 64a) et b) de la LCPE, car elles ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique, ou à mettre en danger l’environnement essentiel pour la vie.
À la lumière des renseignements contenus dans la présente évaluation, il est conclu que la MEK et la MIBK satisfont aux critères énoncés à l’alinéa 64c) de la LCPE, car elles pénètrent ou peuvent pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
À la lumière des renseignements contenus dans la présente évaluation, il est conclu que la MPK, la MIAK, l’alcool de diacétone, le diacétyle, la 2,3-PD, l’acétoïne, la 2,4-PD et l’oxyde de mésityle ne satisfont pas aux critères énoncés à l’alinéa 64c) de la LCPE, car ils ne pénètrent pas dans l’environnement en une quantité ou concentration ou dans des conditions de nature à constituer un danger au Canada pour la vie ou la santé humaines.
Par conséquent, il est conclu que la MEK et la MIBK satisfont à un ou à plusieurs des critères énoncés à l’article 64 de la LCPE, et que la MPK, la MIAK, l’alcool de diacétone, le diacétyle, la 2,3-PD, l’acétoïne, la 2,4-PD et l’oxyde de mésityle ne satisfont à aucun des critères énoncés à l’article 64 de la LCPE.
Bibliographie
Aeschbacher HU, Wolleb U, Löliger J, Spadone JC, Liardon R. 1989. Contribution of coffee aroma constituents to the mutagenicity of coffee. Food Chem Toxicol. 27(4):227-232. (Disponible en anglais seulement).
Annan NT, Plahar WA, Poll L, Jakobsen M. 2005. Effect of soybean fortification on Ghanaian fermented maize dough aroma. Int J Food Sci Nutr. 56(5):315-26. (Disponible en anglais seulement).
[AOPWIN] Atmospheric Oxidation Program for Microsoft Windows [estimation model]. 2010. Ver. 1.92a. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. (Disponible en anglais seulement).
[AR] Alberta Recycling. 2017. Progress report 2017. Progress report. Edmonton (AB): AR. (Disponible en anglais seulement).
[ATSDR] Agency for Toxic Substances & Disease Registry. 2020. Toxicological profile for 2-butanone [PDF]. Atlanta (GA): US Department of Health and Human Services, Public Health Service. (Disponible en anglais seulement).
Ballantyne B. 2001. Systemic toxicity from repeated cutaneous contact with 2,4-pentanedione. Vet Hum Toxicol. 43(1):14-18. (Disponible en anglais seulement).
Ballantyne B, Cawley TJ. 2001. Toxicology update: 2,4-pentanedione. J Appl Toxicol. 21(2):165-171. (Disponible en anglais seulement).
Batyrova TF. 1973. Substantiation of the maximum permissible concentration of methylisobutyl ketone in air or workrooms. Gig Tr Prof Zabol. 17(11):52-53. (Disponible en anglais seulement).
Bawazir AE. 2016. Evaluation of neurotoxicity and testicular toxicity of artificial Butter flavorings. Int J Pharm Res Allied Sci. 5(1):248-258. (Disponible en anglais seulement).
[BDIPSN] Base de données d’ingrédients de produits de santé naturels [base de données]. [Modifié le 9 avril 2022]. Ottawa (Ont.) : Santé Canada. [Consulté le 22 juin 2022]. (Disponible en anglais seulement).
[BDPSNH] Base de données sur les produits de santé naturels homologués [base de données]. [modifié le 8 septembre 2021]. Ottawa (Ont.) : Santé Canada. [Consulté le 22 juin 2022]. (Disponible en anglais seulement).
Benfenati E, Di Toro N, Fanelli R, Lualdi G, Tridico R, Stella G, Buscaini P, Stimilli L. 1992. Characterization of organic and inorganic pollutants in the Adige river (Italy). Chemosphere. 25(11):1665-1674. (Disponible en anglais seulement).
Bernier AM. 2000. Qualité de l’eau potable produite par la Ville de Montréal. Rapport annuel 2000. (Disponible en anglais seulement).
Bianchi AP, Varney MS. 1998. Volatile organic compounds in the surface waters of a British estuary. Part 1: occurrence, distribution and variation. Water Res. 32(2):352-370. (Disponible en anglais seulement).
Birch AN, Petersen MA, Arneborg N, Hansen ÅS. 2013. Influence of commercial baker's yeasts on bread aroma profiles. Food Res Int. 52(1):160-166. (Disponible en anglais seulement).
Bjeldanes LF, Chew H. 1979. Mutagenicity of 1,2-dicarbonyl compounds: maltol, kojic acid, diacetyl and related substances. Mutat Res. 67(4):367-371. (Disponible en anglais seulement).
Borghoff SJ, Poet TS, Green S, Davis J, Hughes B, Mensing T, Sarang SS, Lynch AM, Hard GC. 2015. Methyl isobutyl ketone exposure-related increases in specific measures of a2u-globulin (a2u) nephropathy in male rats along with in vitro evidence of reversible protein binding. Toxicology. 333:1-13. (Disponible en anglais seulement).
Borkowski L. 2007. Another microwave popcorn problem. The Pump Handle: A water cooler for the public health crowd. [Consulté en septembre 2017]. (Disponible en anglais seulement).
Braithwaite J. 2000. Ketones. In: Kirk-Othmer encyclopedia of chemical technology. Online version. New York (NY): John Wiley & Sons, Inc. [Consulté en juillet 2016]. [Accès limité]. (Disponible en anglais seulement).
Burdock GA. 2010. Fenaroli’s handbook of flavor ingredients. 6th ed. Orlando (FL): Burdock Group. (Disponible en anglais seulement).
Buttery RG, Ling LC, Stern DJ. 1997. Studies on popcorn aroma and flavor volatiles. J Agric Food Chem. 45(3):837-843. (Disponible en anglais seulement).
Canada. 1999. Loi canadienne sur la protection de l’environnement (1999). L.C. 1999, ch. 33. Gazette du Canada, Partie III, vol. 22, no 3.
Canter LW, Sabatini DA. 1994. Contamination of public ground water supplies by Superfund sites. Int J Environ Stud. 46(1):35-57. (Disponible en anglais seulement).
Cantin S. 2009. Les pneus hors d’usage [PDF]. Fiches informatives. Recyc-Quebec. [Consulté le 13 août 2018].
Cardoso DR, Bettin SM, Reche RV, Lima-Neto BS, Franco DW. 2003. HPLC-DAD analysis of ketones as their 2,4-dinitrophenylhydrazones in Brazilian sugar-cane spirits and rum. Journal of Food Composition and Analysis. 16:563-573. (Disponible en anglais seulement).
[CDC] Centers for Disease Control and Prevention (US). 2016. Criteria for a recommended standard: occupational exposure to diacetyl and 2,3-pentanedione. Cincinnati (OH): US Department of Health and Human Services, Centers for Disease Control and Prevention, National Institute for Occupational Safety and Health, DHHS (NIOSH). [Consulté le 13 octobre 2017]. Publication No. 2016-111. (Disponible en anglais seulement).
ChemCAN [level III fugacity model of 24 regions of Canada]. 2003. Version 6.00. Peterborough (ON): Trent University, Canadian Centre for Environmental Modelling and Chemistry. [mentionné le 19 octobre 2016]. (Disponible en anglais seulement).
ChemIDplus [base de données]. 1993- . Bethesda (MD): US National Library of Medicine. [Mis à jour le 26 novembre 2012; consulté en mars 2017]. (Disponible en anglais seulement).
Cichocki JA, Morris JB. 2017. Inhalation dosimetry modeling provides insights into regional respiratory tract toxicity of inhaled diacetyl. Toxicology. 388:30-39. (Disponible en anglais seulement).
[CICM] Commerce international canadien de marchandises [base de données]. 2017. 291412 Butanone (méthyléthylcétone), 2011-2016. Ottawa (Ont.) : Statistique Canada. [Mentionné en mai 2017].
[CIRC] International Agency for Research on Cancer. 2013. IARC Monographs on the Evaluation of Carcinogenic Risks to Humans – Volume 101: Some Chemicals Present in Industrial and Consumer Products, Food and Drinking-water. IARC Monogr Eval Carcinog Risks Hum. 101. Lyon, France. (Disponible en anglais seulement).
Colley J, Gaunt IF, Lansdown AB, Grasso P, Gangolli SD. 1969. Acute and short-term toxicity of diacetyl in rats. Food Cosmet Toxicol. 7(6):571-580. (Disponible en anglais seulement).
[ConsExpo Web] Consumer Exposure Web Model. 2016. Bilthoven (NL): Rijksinstituut voor Volksgezondheid en Milieu [National Institute for Public Health and the Environment]. (Disponible en anglais seulement).
[CPID] Consumer Product Information Database [base de données]. [Modifié en 2019]. DeLima Associates. [Consulté en décembre 2019]. (Disponible en anglais seulement).
Curry P, Kramer G, Newhook R, Sitwell J, Somers D, Tracy B, Oostdam JV. 1993. Reference values for Canadian populations. Prepared by the Environmental Health Directorate Working Group on Reference Values. Santé Canada. Inédit. 1988 [mis à jour en 1993]. (Disponible en anglais seulement).
David RM, Bernard LG, Banton MI, Tyler TR, Topping DC, Gill MW, O’Donoghue JL. 1999. The effect of repeated methyl iso-butyl ketone vapor exposure on schedule-controlled operant behavior in rats. Neurotoxicology. 20(4):583-593. (Disponible en anglais seulement).
De Ceaurriz J, Micillino JC, Bonnet P, Guenier JP. 1981. Sensory irritation caused by various industrial airborne chemicals. Toxicol Lett. 9(2):137-143. (Disponible en anglais seulement).
De Ceaurriz J, Micillino JC, Marignac B, Bonnet P, Muller J, Guenier JP. 1984. Quantitative evaluation of sensory irritating and neurobehavioural properties of aliphatic ketones in mice. Food Chem Toxicol. 22(7):545-549. (Disponible en anglais seulement).
De Leonardis A, Lopez F, Nag A, Macciola V. 2013. Occurrence and persistence of diacetyl in unfermented and fermented milks. Eur Food Res Technol. 236(4):691-697. (Disponible en anglais seulement).
Deacon MM, Pilny MD, John JA, Schwetz BA, Murray FJ, Yakel HO, Kuna RA. 1981. Embryo- and fetotoxicity of inhaled methyl ethyl ketone in rats. Toxicol Appl Pharmacol. 59(3):620-622. (Disponible en anglais seulement).
Delzer GC, Ivahnenko T. 2003. Occurrence and temporal variability of methyl tert-butyl either (MTBE) and other volatile organic compounds in select sources of drinking water: results of the focused survey [PDF]. Water-resources investigations report 02-4084. Rapid City (ND): US Geological Survey. (Disponible en anglais seulement).
Dietz FK, Rodriguez-Giaxola M, Traiger GJ, Stella VJ, Himmelstein KJ. 1981. Pharmacokinetics of 2-butanol and its metabolites in the rat. J Pharmacokinet Biopharm. 9(5):553-576. (Disponible en anglais seulement).
DiVincenzo GD, Kaplan CJ, Dedinas J. 1976. Characterization of the metabolites of methyl n-butyl ketone, methyl iso-butyl ketone, and methyl ethyl ketone in guinea pig serum and their clearance. Toxicol Appl Pharmacol. 36(3):511-522. (Disponible en anglais seulement).
Dodd DE, Garman RH, Pritts IM, Troup CM, Snellings WM, Ballantyne B. 1986. 2,4-Pentanedione: 9-day and 14-week vapor inhalation studies in Fischer-344 rats. Fundam Appl Toxicol. 7(2):329-339. (Disponible en anglais seulement).
Doepker CL, Maier A, Willis A, Hermansky SJ. 2012. Toxicology of flavors in the food industry. In: Bingham E, Cohhrssen B, editors. Patty’s Toxicology. 6th ed., vol. 5. New York (NY): John Wiley & Sons, Inc. p. 133-168. (Disponible en anglais seulement).
Dorado L, Montoya MR, Rodríguez Mellado JM. 1992. A contribution to the study of the structure-mutagenicity relationship for alpha-dicarbonyl compounds using the Ames test. Mutat Res. 269(2):301-306. (Disponible en anglais seulement).
Duguay AB, Plaa GL. 1995. Tissue concentrations of methyl isobutyl ketone, methyl n-butyl ketone and their metabolites after oral or inhalation exposure. Toxicol Lett. 75(1-3):51-58. (Disponible en anglais seulement).
[ECCC] Environnement et Changement climatique Canada. 2016a. Document sur l’approche scientifique : Classification du risque écologique des substances organiques. Gatineau (Qc) : ECCC.
[ECCC] Environnement et Changement climatique Canada. 2016b. Supporting documentation: data used to create substance-specific hazard and exposure profiles and assign risk classifications. Gatineau (QC): ECCC. Information in support of the science approach document: ecological risk classification of organic substances. Accessible sur demande à : substances@ec.gc.ca. (Disponible en anglais seulement)
[ECCC] Environnement et Changement climatique Canada. 2017a. RNSPA : données annuelles brutes pour 2006 à 2010 [Internet]. Gatineau (Qc) : Environnement Canada, Centre de technologie environnementale. [Consulté en février 2017].
[ECCC] Environnement et Changement climatique Canada. 2017b. Données recueillies dans le cadre d’une initiative de collecte de données ciblée pour une évaluation du Plan de gestion des produits chimiques (octobre 2017). Données préparées par ECCC, Santé Canada; Programme des substances existantes. (Disponible en anglais seulement).
[ECCC, SC] Environnement et Changement climatique Canada, Santé Canada. [Modifié le 12 mars 2017]. Catégorisation de substances chimiques. Ottawa (Ont.) : gouvernement du Canada.
[ECHA] European Chemicals Agency. c2007-2019a. Registered substances database; search results for CAS RN 107-87-9. Helsinki (FI): ECHA. [Mis à jour le 25 août 2017; consulté le 13 octobre 2017]. (Disponible en anglais seulement).
[ECHA] European Chemicals Agency. c2007-2019b. Registered substances database; search results for CAS RN 123-42-2. Helsinki (FI): ECHA. [Mis à jour le 21 septembre 2017; consulté le 23 octobre 2017]. (Disponible en anglais seulement).
[ECHA] European Chemicals Agency. c2007-2019c. Registered substances database; search results for CAS RN 110-12-3. Helsinki (FI): ECHA. [Mis à jour le 28 juin 2017; consulté le 13 octobre 2017]. (Disponible en anglais seulement).
[ECHA] European Chemicals Agency. c2007-2019d. Registered substances database; registered dossier for pentane-2,4-dione, CAS RN 123-54-6. Helsinki (FI): ECHA. [Mis à jour le 2 octobre 2017; consulté le 13 octobre 2017]. (Disponible en anglais seulement).
[ECHA] European Chemicals Agency. c2007-2019e. Registered substances database; registered dossier for 4-methylpent-3-en-2-one, CAS RN 141-79-7. Helsinki (FI): ECHA. [Mis à jour le 14 avril 2017; consulté le 13 octobre 2017]. (Disponible en anglais seulement).
[ECHA] European Chemicals Agency. 2019. Committee for Risk Assessment RAC Opinion proposing harmonised classification and labelling at EU level of 4-methylpentan-2-one; isobutyl methyl ketone. CAS RN 108-10-1. Adopted 20 September 2019. CLH-O-0000001412-86-295/F. Helsinki (FI): ECHA. [Consulté le 19 novembre 2020]. (Disponible en anglais seulement).
[EFSA] European Food Safety Authority. 2004. Opinion of the Scientific Panel on Food Additives, Flavourings, Processing Aids and Materials in contact with Food (AFC) on a request from the Commission related to Flavouring Group Evaluation 11 (FGE.11): aliphatic dialcohols, diketones, and hydroxyketones from chemical group 10 [PDF] (Commission Regulation (EC) No 1565/2000 of 18 July 2000). Parma (IT): EFSA. EFSA J. 166:1-44. (Disponible en anglais seulement).
[EFSA] European Food Safety Authority. 2012. Scientific opinion on Flavouring Group Evaluation 204 (FGE.204): consideration of genotoxicity data on representatives for 18 mono-unsaturated, aliphatic, α,β-unsaturated ketones and precursors from chemical subgroup 1.2.1 of FGE.19 by EFSA [PDF]. EFSA J. 10(12):2992. Parma (IT): EFSA. (Disponible en anglais seulement).
[EFSA] European Food Safety Authority. 2015. Scientific opinion on the risks to public health related to the presence of bisphenol A (BPA) in foodstuffs: executive summary [PDF]. EFSA J. 13(1):3978. (Disponible en anglais seulement).
[EFSA] European Food Safety Authority. 2016. Safety and efficacy of secondary aliphatic saturated or unsaturated alcohols, ketones, ketals and esters with a second secondary or tertiary oxygenated functional group belonging to chemical group 10 when used as flavourings for all animal species. EFSA Panel on Additives and Products or Substances used in Animal Feed (FEEDAP), Rychen et coll., 2016. Parma (IT): EFSA. EFSA J. 14(11):4618-4619. (Disponible en anglais seulement).
Egilman DS, Schilling JH. 2012. Bronchiolitis obliterans and consumer exposure to butter-flavored microwave popcorn: a case series. Int J Occup Environ Health. 18(1):29-42. (Disponible en anglais seulement).
Environnement Canada. 2001. Data for selected substances collected under the Canadian Environmental Protection Act, 1999. Section 71: Notice with Respect to Certain Substances on the Domestic Substances List (DSL). Data prepared by: Environment Canada, Existing Substances Program. (Disponible en anglais seulement).
Environnement Canada. 2012. Loi canadienne sur la protection de l’environnement, 1999 : Avis concernant certaines substances de la Liste intérieure [PDF]. Gazette du Canada, Partie I, vol. 146, nº 48, Supplément.
Environnement Canada. 2013. Données de la Mise à jour de l’inventaire de la LIS recueillies en vertu de l’article 71 de laLoi canadienne sur la protection de l’environnement de 1999 : Avis modifiant l’Avis concernant certaines substances de la Liste intérieure. Données préparées par : Environnement Canada, Santé Canada, Programme des substances existantes.
Environnement Canada, Santé Canada. 2002. Canadian Environmental Protection Act: Priority substances list health assessment supporting documentation report: 2-butoxyethanol. Ottawa (ON): Government of Canada. [Consulté en septembre 2017]. Inédit. (Disponible en anglais seulement)
[EPI Suite] Estimation Program Interface Suite for Microsoft Windows [estimation model]. c2000-2012. Ver. 4.11. Washington (DC): US Environmental Protection Agency, Office of Pollution Prevention and Toxics; Syracuse (NY): Syracuse Research Corporation. (Disponible en anglais seulement).
European Commission. 2014. Recommendation from the Scientific Committee on Occupational Exposure Limits for diacetyl. SCOEL/SUM/149. Brussels (BE): European Commission; Employment, Social Affairs and Inclusion. [Consulté en avril 2020]. (Disponible en anglais seulement).
European Commission. 2017. Cosmetic Ingredients and Substances (CosIng) Simple Search Database [base de données]. [Mis à jour le 20 octobre 2017; consulté en septembre 2017]. (Disponible en anglais seulement).
Fasano WJ, McDougal JN. 2008. In vitro dermal absorption rate testing of certain chemicals of interest to the Occupational Safety and Health Administration: summary and evaluation of USEPA's mandated testing. Regul Toxicol Pharmacol. 51(2):181-194. (Disponible en anglais seulement).
Farsalinos KE, Kistler KA, Gillman G, Voudris V. 2015. Evaluation of electronic cigarette liquids and aerosol for the presence of selected inhalation toxins. Nicotine Tob Res. 17(2):168-174. (Disponible en anglais seulement).
Ficheux AS, Chevillotte G, Wesolek N, Morisset T, Dornic N, Bernard A, Bertho A, Romanet A, Leroy L, Mercat AC, et coll. 2016. Consumption of cosmetic products by the French population second part: amount data. Food Chem Toxicol. 90:130-141. (Disponible en anglais seulement).
Ficheux AS, Morisset T, Chevillotte G, Postic C, Roudot AC. 2014. Probabilistic assessment of exposure to nail cosmetics in French consumers. Food Chem Toxicol. 66:36-43. (Disponible en anglais seulement).
Folkendt MM, Weiss-Lopez BE, Chauvel P Jr., True, NS. 1985. Gas-phase proton NMR studies of keto-enol tautomerism of acetylacetone, methyl acetoacetate, and ethyl acetoacetate. J Phys Chem. 89:3347-3352. (Disponible en anglais seulement).
Furihata C, Matsushima T. 1987. Use of in vivo/in vitro unscheduled DNA synthesis for identification of organ-specific carcinogens. Crit Rev Toxicol. 17(3):245-277. (Disponible en anglais seulement).
Furihata C, Yoshida S, Matsushima T. 1985. Potential initiating and promoting activities of diacetyl and glyoxal in rat stomach mucosa. Jpn J Cancer Res. 76(9):809-814. (Disponible en anglais seulement).
Gaffney SH, Abelmann A, Pierce JS, Glynn ME, Henshaw JL, McCarthy LA, Lotter JT, Liong M, Finley BL. 2015. Naturally occurring diacetyl and 2,3-pentanedione concentrations associated with roasting and grinding unflavored coffee beans in a commercial setting. Toxicol Rep. 2:1171-1181. (Disponible en anglais seulement).
García-Martínez T, de Lerma NL, Moreno J, Peinado RA, Millán MC, Mauricio JC. 2013. Sweet wine production by two osmotolerant Saccharomyces cerevisiae strains. J Food Sci. 78(6):M874-M879. (Disponible en anglais seulement).
Gaunt IF, Brantom PG, Kiss IS, Grasso P, Gangolli SD. 1972. Short-term toxicity of acetoin (acetylmethylcarbinol) in rats. Food Cosmet Toxicol. 10(2):131-141. (Disponible en anglais seulement).
Geller I, Gause E, Kaplan H, Hartmann RJ. 1979. Effects of acetone, methyl ethyl ketone and methyl isobutyl ketone on a match-to-sample task in the baboon. Pharmacol Biochem Behav. 11(4):401-406. (Disponible en anglais seulement).
Giri A, Okamoto A, Okazaki E, Ohshima T. 2010. Headspace volatiles along with other instrumental and sensory analyses as indices of maturation of horse mackerel miso. J Food Sci. 75(8):S406-S417. (Disponible en anglais seulement).
Glensvig D, Ports J. 2006. Mapping of perfume in toys and children’s articles [PDF]. Denmark: Danish Ministry of Environment. [Consulté en mai 2017]. (Disponible en anglais seulement).
Gloede E, Cichocki JA, Baldino JB, Morris JB. 2011. A validated hybrid computational fluid dynamics-physiologically based pharmacokinetic model for respiratory tract vapor absorption in the human and rat and its application to inhalation dosimetry of diacetyl. Toxicol Sci. 123(1):231-246. (Disponible en anglais seulement).
Golder Associates. 1987. Testing of specific organic compounds in soils in background in urban areas. Draft working paper to Shell Canada Limited and Texaco Canada Limited. (Disponible en anglais seulement).
Goravanahally MP, Hubbs AF, Fedan JS, Kashon ML, Battelli LA, Mercer RR, Goldsmith WT, Jackson MC, Cumpston A, Frazer DG, et coll. 2014. Diacetyl increases sensory innervation and substance P production in rat trachea. Toxicol Pathol. 42(3):582-590. (Disponible en anglais seulement).
Grady SJ. 2003. A national survey of methyl tert-butyl ether and other volatile organic compounds in drinking-water sources: results of the random survey [PDF]. Water-Resources Investigations Report 02-4079. East Hartford (CT): US Geological Survey. (Disponible en anglais seulement).
Grady SJ, Casey GD. 2001. Occurrence and distribution of methyl tert-butyl ether and other volatile organic compounds in drinking water in the northeast and mid-Atlantic regions of the United States, 1993-98 [PDF]. Water-Resources Investigations Report 00-4228. East Hartford (CT): US Geological Survey. (Disponible en anglais seulement).
Hall LW Jr., Hall WS, Bushong SJ, Herman RL. 1987. In situ striped bass (Morone saxatilis) contaminant and water quality studies in the Potomac River. Aquat Toxicol. 10(2-3):73-99. (Disponible en anglais seulement).
[HAMN] Hamilton Air Monitoring Network. 2020. Air Quality Summary Reporting - Volatile Organic Compounds (VOCs). (Disponible en anglais seulement).
Hansen, J, Hansen OC, Pommer K. 2004. Mapping of chemical substances in consumer products. Release of chemical substances from tents and tunnels for children [PDF, 360 KB]. Denmark: Danish Ministry of Environment. [Consulté en mai 2017]. (Disponible en anglais seulement).
Hansen PL, Tønning K, Malmgren-Hansen B, Jacobsen E. 2008. Survey and health assessment of chemical substances in hobby products for children [PDF, 372 KB]. Survey of Chemical Substances in Consumer Products, No. 93. Denmark: Danish Ministry of the Environment. (Disponible en anglais seulement).
Hjelm EW, Boman A, Fernström P, Hagberg M, Johanson G. 1991. Percutaneous uptake and kinetics of methyl isobutyl ketone (MIBK) in the guinea pig. Toxicol Lett. 56(1-2):79-86. (Disponible en anglais seulement).
Hjelm EW, Hagberg M, Iregren A, Löf A. 1990. Exposure to methyl isobutyl ketone: toxicokinetics and occurrence of irritative and CNS symptoms in man. Int Arch Occup Environ Health. 62(1):19-26. (Disponible en anglais seulement).
Holloway AL, Treacy J, Sidebottom H, Mellouki A, Daële V, Le Bras G, Barnes I. 2005. Rate coefficients for the reactions of OH radicals with the keto/enol tautomers of 2,4-pentanedione and 3-methyl-2,4-pentanedione, allyl alcohol and methyl vinyl ketone using the enols and methyl nitrite as photolytic sources of OH. J Photochem Photobiol A Chem. 176:183-190. (Disponible en anglais seulement).
[HSDB] Hazardous Substances Data Bank [base de données]. 1983-. Bethesda (MD): National Library of Medicine (US). [Consulté le 23 octobre 2017]. (Disponible en anglais seulement).
Hubbs AF, Battelli LA, Goldsmith WT, Porter DW, Frazer D, Friend S, Schwegler-Berry D, Mercer RR, Reynolds JS, Grote A, et coll. 2002. Necrosis of nasal and airway epithelium in rats inhaling vapors of artificial butter flavouring. Toxicol Appl Pharmacol. 185(2):128-135. (Disponible en anglais seulement).
Hubbs AF, Cumpston AM, Goldsmith WT, Battelli LA, Kashon ML, Jackson MC, Frazer DG, Fedan JS, Goravanahally MP, Castranova V, et coll. 2012. Respiratory and olfactory cytotoxicity of inhaled 2,3-pentanedione in Sprague-Dawley rats. Am J Pathol. 181(3):829-844. (Disponible en anglais seulement).
Hubbs AF, Goldsmith WT, Kashon ML, Frazer D, Mercer RR, Battelli LA, Kullman GJ, Schwegler-Berry D, Friend S, Castranova V. 2008. Respiratory toxicologic pathology of inhaled diacetyl in Sprague-Dawley rats. Toxicol Pathol. 36(2):330-344. (Disponible en anglais seulement).
Hubbs AF, Kreiss K, Cummings KJ, Fluharty KL, O’Connell R, Cole A, Dodd TM, Clingerman SM, Flesher JR, Lee R, et coll. 2019. Flavorings-related lung disease: a brief review and new mechanistic data. Toxicol Pathol. 47(8):1012-1026. (Disponible en anglais seulement).
Hughes BJ, Thomas J, Lynch AM, Borghoff SJ, Green S, Mensing T, Sarang SS, LeBaron MJ. 2016. Methyl isobutyl ketone-induced hepatocellular carcinogenesis in B6C3F1 mice: a constitutive androstane receptor (CAR)-mediated mode of action. Regul Toxicol Pharmacol. 81:421-429. (Disponible en anglais seulement).
Imhof R, Glättli H, Bosset JO. 1995. Volatile organic compounds produced by thermophilic and mesophilic single strain dairy starter cultures. LWT - Food Sci Technol. 28(1):78-86. (Disponible en anglais seulement).
[INRP] Inventaire national des rejets de polluants [base de données]. 2011-2017a. Ensembles de données de l’INRP : Méthyléthylcétone (78-93-3). Gatineau (Qc) : Environnement et Changement climatique Canada. Résultats de recherche pour 78-93-3. [Modifié le 20 août 2019; consulté le 22 novembre 2019].
[INRP] Inventaire national des rejets de polluants [base de données]. 2011-2017b. Ensembles de données de l’INRP : Méthylisobutylcétone (108-10-1). Gatineau (Qc): Environnement et Changement climatique Canada. Résultats de recherche pour 8-10-1. [Modifié le 20 août 2019; consulté le 22 novembre 2019].
[INRP] Inventaire national des rejets de polluants. 2021. Tableaux de données pour une année, par installation – Rejets, transferts et éliminations, Inventaire national des rejets de polluants (INRP). Ensembles de données de l’INRP pour 2015, 2016, 2017, 2018, 2019 [Internet]. Gatineau (Qc) : Environnement et Changement climatique Canada. [Consulté en juin 2021].
[IPCS] International Programme on Chemical Safety. 1990. Environmental Health Criteria 117: Methyl isobutyl ketone. Geneva (CH): United Nations Environment Programme, International Labour Organization, World Health Organization. [Consulté le 23 octobre 2017]. (Disponible en anglais seulement).
[IPCS] International Programme on Chemical Safety. 1993. Environmental Health Criteria 143: Methyl ethyl ketone. Geneva (CH): United Nations Environment Programme, International Labour Organization, World Health Organization. [Consulté le 23 octobre 2017]. (Disponible en anglais seulement).
[IPCS] International Programme on Chemical Safety. 1997. Methyl isobutyl ketone. Geneva (CH): International Chemical Safety Cards, International Program on Chemical Safety, World Health Organization. (Disponible en anglais seulement).
[IPCS] International Programme on Chemical Safety. 1999. Safety evaluation of aliphatic acyclic and alicyclic alpha-diketones and related alpha-hydroxy ketones. Prepared by the Fifty-first meeting of the Joint FAO/WHO Expert Committee on Food Additives, World Health Organization, Geneva, International Programme on Chemical Safety. (WHO Food Additive Series 42). [Consulté le 20 janvier 2017]. (Disponible en anglais seulement).
Iregren A, Tesarz M, Wigaeus-Hjelm E. 1993. Human experimental MIBK exposure: effects on heart rate, performance, and symptoms. Environ Res. 63(1):101-108. (Disponible en anglais seulement).
[JBRC] Japan Bioassay Research Center. 2010a. Summary of inhalation carcinogenicity study of 2,4-pentanedione in F344 rats [PDF, 1,24 mb]. Japan Industrial Safety and Health Association. [Consulté le 15 juin 2017]. (Disponible en anglais seulement).
[JBRC] Japan Bioassay Research Center. 2010b. Summary of inhalation carcinogenicity study of 2,4-Pentanedione in B6D2F1 mice [PDF, 1.24 MB]. Japan Industrial Safety and Health Association. [Consulté le 15 juin 2017]. (Disponible en anglais seulement).
Juberg DR, Alfano K, Coughlin RJ, Thomson KM. 2001. An observational study of object mouthing behavior by young children. Pediatrics. 107(1):135-142. (Disponible en anglais seulement).
Kato F, Araki A, Nozaki K, Matsushima T. 1989. Mutagenicity of aldehydes and diketones. Mutat Res. 216:366-367. (Disponible en anglais seulement).
Katz GV, Renner ER Jr., Terhaar CJ. 1986. Sub-chronic inhalation toxicity of methyl isoamyl ketone in rats. Fundam Appl Toxicol. 6(3):498-505. (Disponible en anglais seulement).
Klager S, Vallarino J, MacNaughton P, Christiani DC, Lu Q, Allen JG. 2017. Flavoring chemicals and aldehydes in e-cigarette emissions. Environ Sci Technol. 51(18):10806-10813. (Disponible en anglais seulement).
Kim SB, Hayase F, Kato H. 1987. Desmutagenic effect of alpha-dicarbonyl and alpha-hydroxycarbonyl compounds against mutagenic heterocyclic amines. Mutat Res. 177(1):9-15. (Disponible en anglais seulement).
Kreiss K, Gomaa A, Kullman G, Fedan K, Simoes EJ, Enright PL. 2002. Clinical bronchiolitis obliterans in workers at a microwave-popcorn plant. N Engl J Med. 347(5):330-338. (Disponible en anglais seulement).
Larsen ST, Alarie Y, Hammer M, Nielsen GD. 2009. Acute airway effects of diacetyl in mice. Inhal Toxicol. 21(13):1123-1128. (Disponible en anglais seulement).
Lawson AM, Speers RA, Zhu J. 1995. Chemical and sensory detection of diacetyl in strawberry juice (short communication) [PDF]. Nahrung. 39(4):323-327. (Disponible en anglais seulement).
Li Y, Cakmak S, Zhu J. 2019. Profiles and monthly variations of selected volatile organic compounds in indoor air in Canadian homes: results of Canadian national indoor air survey 2012-2013. Environ Int. 126:134-144. (Disponible en anglais seulement).
Liira J, Riihimäki V, Pfäffli P. 1988. Kinetics of methyl ethyl ketone in man: absorption, distribution and elimination in inhalation exposure. Int Arch Occup Environ Health. 60(3):195-200. (Disponible en anglais seulement).
Loretz LG, Api AM, Barraj LM, Burdick J, Dressler WE, Gettings SD, Han Hsu H, Pan YHL, Re TA, Renskers KJ, et coll. 2005. Exposure data for cosmetic products: lipstick, body lotion, and face cream. Food Chem Toxicol. 43(2):279-291. (Disponible en anglais seulement).
Macciola V, Candela G, De Leonardis A. 2008. Rapid gas-chromatographic method for the determination of diacetyl in milk, fermented milk and butter. Food Control. 19(9):873-878. (Disponible en anglais seulement).
MacEwen JD, Vernot EH, Haun CC. 1971. Effect of 90-day continuous exposure to methylisobutylketone on dogs, monkeys and rats. Aerospace Medical Research Laboratory Document No. AMRL-TR-71-65. NTIS No. AD Rep. 730291. (Disponible en anglais seulement).
[MAI] Microbiological Associates, Inc. 1986. Sub-chronic toxicity of methyl isobutyl ketone in Sprague Dawley rats. Final report. Study No. 5221.04. Performed by Microbiological Associates, Inc. for Research Triangle Institute. Unpublished report dated July 15, 1986. (Disponible en anglais seulement).
Malysheva MV. 1988. The effect of the methods of cutaneous administration of methyl isobutyl ketone on its toxicity. Gig Sanit. 10:79-80. (Disponible en anglais seulement).
Marnett LJ, Hurd HK, Hollstein MC, Levin DE, Esterbauer H, Ames BN. 1985. Naturally occurring carbonyl compounds are mutagens in Salmonella tester strain TA104. Mutat Res. 148(1-2):24-34. (Disponible en anglais seulement).
Messaadia L, El Dib G, Ferhati A, Chakir A. 2015. UV–visible spectra and gas-phase rate coefficients for the reaction of 2,3-pentanedione and 2,4-pentanedione with OH radicals. Chem Phys Lett. 626:73-79. (Disponible en anglais seulement).
McCready D, Fontaine D. 2010. Refining ConsExpo evaporation and human exposure calculations for REACH. Human and Ecological Risk Assessment: An International Journal. 16(4):783-800. (Disponible en anglais seulement).
McCoy MJ, Hoppe Parr KA, Anderson KE, Cornish J, Haapala M, Greivell J. 2017. Diacetyl and 2,3-pentanedione in breathing zone and area air during large-scale commercial coffee roasting, blending and grinding processes. Toxicol Rep. 4:113-122. (Disponible en anglais seulement).
More SS, Raza A, Vince R. 2012. The butter flavorant, diacetyl, forms a covalent adduct with 2-deoxyguanosine, uncoils DNA, and leads to cell death. J Agric Food Chem. 60(12):3311-3317. (Disponible en anglais seulement).
Morgan DL, Flake GP, Kirby PJ, Palmer SM. 2008. Respiratory toxicity of diacetyl in C57BL/6 mice. Toxicol Sci. 103(1):169-180. (Disponible en anglais seulement).
Morgan DL, Jokinen MP, Price HC, Gwinn WM, Palmer SM, Flake GP. 2012. Bronchial and bronchiolar fibrosis in rats exposed to 2,3-pentanedione vapors: implications for bronchiolitis obliterans in humans. Toxicol Pathol. 40(3):448-465. (Disponible en anglais seulement).
Morris JB, Hubbs AF. 2009. Inhalation dosimetry of diacetyl and butyric acid, two components of butter flavoring vapors. Toxicol Sci. 108(1):173-183. (Disponible en anglais seulement).
Mujić I, Bavcon Kralj M, Jokić S, Jug T, Subarić D, Vidović S, Zivković J, Jarni K. 2014. Characterisation of volatiles in dried white varieties figs (Ficus carica L.). J Food Sci Technol. 51(9):1837-1846. (Disponible en anglais seulement).
Munies R, Wurster DE. 1965. Investigation of some factors influencing percutaneous absorption III: absorption of methyl ethyl ketone. J Pharm Sci. 54(9):1281-1284. (Disponible en anglais seulement).
Mutch RD Jr, Daigler J, Clarke JH. 1983. Clean-up of Shope’s landfill, Girard, PA. In: National Conference on Management of Uncontrolled Hazardous Waste Sites. Washington, DC. p. 296-300. (Disponible en anglais seulement).
[NCI] National Chemical Inventories [logiciel]. 2015. Issue 2. Columbus (OH): American Chemical Society, Chemical Abstracts Service. (Disponible en anglais seulement).
Nemec M, Pitt J, Topping D, Gingell R, Pavkov K, Rauckman E, Harris S. 2004. Inhalation two-generation reproductive toxicity study of methyl isobutyl ketone in rats. Int J Toxicol. 23(2):127-143. (Disponible en anglais seulement).
[NICNAS] National Industrial Chemicals Notification and Assessment Scheme. 2017. 2-Pentanone, 4-methyl-. Sydney (AU): Department of Health, National Industrial Chemicals Notification and Assessment Scheme. Human Health Tier III assessment for 2-Pentanone, 4-methyl- , CAS No. 108-10-1. [Consulté le 13 octobre 2017]. (Disponible en anglais seulement).
Nijssen LM, Ingen-Visscher CA van, Donders JJH, editors. 1963-2018. VCF Volatile Compounds in Food online database [base de données]. Version 16.6.1. Zeist (NL): Triskelion B.V. [Mis à jour en 2018; consulté en janvier 2020]. (Disponible en anglais seulement).
Nilsson NH, Malmgren-Hansen B, Bernth N, Pedersen E, Pommer K. 2006. Survey of chemical substances in consumer products: survey and health assessment of chemicals substances in sex toys [PDF, 892 KB]. Report no. 77. Denmark: Danish Ministry of Environment. [Consulté en mai 2017]. (Disponible en anglais seulement).
[NTP] National Toxicology Program. 2007a. Chemical information review document for artificial butter flavoring and constituents. Diacetyl (CAS No. 431-03-8) and acetoin (CAS No. 513-86-0). Supporting nomination for toxicological evaluation by the National Toxicology Program, January 2007. Prepared by Integrated Laboratory Systems, Inc. Research Triangle Park (NC): US Department of Health and Human Services, National Toxicology Program. Contract No.: N01-ES-35515. (Disponible en anglais seulement).
[NTP] National Toxicology Program. 2007b. NTP toxicology and carcinogenesis studies of Methyl Isobutyl Ketone (CAS NO. 108–10–1) in F344/N rats and B6C3F1 mice (inhalation studies). Research Triangle Park (NC): US Department of Health and Human Services, National Toxicology Program. Report No. 538: 1-236. (Disponible en anglais seulement).
[NTP] National Toxicology Program. 2017. Tox-99: Acetoin and 2,3-pentanedione, Toxicity Report Tables & Curves. Research Triangle Park (NC): US Department of Health and Human Services, National Toxicology Program. [Consulté le 13 octobre 2017]. Résultats uniquement. (Disponible en anglais seulement).
[NTP] National Toxicology Program. 2018. NTP Technical Report on the toxicology and carcinogenesis studies of 2,3-butanedione in Wistar Han rats and B6C3F1/N mice (inhalation studies) [PDF]. NTP TR 593. Final. Août 2018. (Disponible en anglais seulement).
[NTP] National Toxicology Program. 2019. Acetylacetone (123-54-6). Chemical Effects in Biological Systems (CEBS). Research Triangle Park (NC): National Toxicology Program. [Consulté le 12 décembre 2019]. (Disponible en anglais seulement).
Nylén D, Borling P, Sørensen H. 2004. Survey of chemical substances in consumer products: Mapping of chemical substances in animal care products [PDF, 976 KB]. Report no. 44. [Consulté en mai 2017]. Denmark: Danish Ministry of Environment. (Disponible en anglais seulement).
[OCDE] Organisation for Economic Co-operation and Development. 1996. SIDS initial assessment report: Methyl isobutyl ketone: CAS No. 108-10-1 [PDF, 71.4 KB]. SIAM [SIDS Initial Assessment Meeting] 5: 1996 Oct. [Consulté en avril 017]. (Disponible en anglais seulement).
[OCDE] Organisation for Economic Co-operation and Development. 1997a. SIDS initial assessment report: Methyl ethyl ketone: CAS No. 78-93-3. SIAM [SIDS Initial Assessment Meeting] 6: 1997 June: Paris, France. [Consulté le 5 mai 2017]. (Disponible en anglais seulement).
[OCDE] Organisation for Economic Co-operation and Development. 1997b. SIDS initial assessment report: Mesityl oxide: CAS No. 141-79-7. SIAM [SIDS Initial Assessment Meeting] 6: 1997 June: Paris, France [Mis à jour en novembre 2010; consulté le 5 mai 2017]. (Disponible en anglais seulement).
[OCDE] Organisation for Economic Co-operation and Development. 2000. SIDS initial assessment report: Diacetone alcohol, CAS No. 123-42-2. SIAM [SIDS Initial Assessment Meeting] 10; 2000 March; Japan [Consulté en avril 2017]. (Disponible en anglais seulement).
[OCDE] Organisation for Economic Co-operation and Development. 2001. SIDS initial assessment report: 2,4-Pentanedione, CAS No. 123-54-6 [PDF, 465 KB]. SIAM [SIDS Initial Assessment Meeting] 13; 2001 Sept; Bern, Switzerland. [Consulté le 13 octobre 2017]. (Disponible en anglais seulement).
[OCDE] Organisation for Economic Co-operation and Development. 2003. SIDS initial assessment report: 6-methylhept-5-en-2-one: CAS No. 110-93-0 [PDF, 531 KB]. SIAM [SIDS Initial Assessment Meeting] 17: 2003 November: Paris, France [Consulté le 17 mai 2017]. (Disponible en anglais seulement).
[OCDE] QSAR Toolbox [Read-across tool]. 2014. Version 3.3. Paris (FR): Organisation for Economic Co-operation and Development, Laboratory of Mathematical Chemistry. (Disponible en anglais seulement).
[OCDE] QSAR Toolbox [Read-across tool]. 2017. Ver. 4.1. Paris (FR): Organisation for Economic Co-operation and Development, Laboratory of Mathematical Chemistry. (Disponible en anglais seulement).
O’Donoghue JL. 2012a. Ketones of four or five carbons. In Patty’s Toxicology Sixth Edition, E. Bingham, and B. Cohrssen (eds.). John Wiley & Sons, Inc. p. 753-806. (Disponible en anglais seulement).
O’Donoghue JL. 2012b. Ketones of 6 to thirteen carbons. In Patty’s Toxicology Sixth Edition, E. Bingham, and B. Cohrssen (eds.). John Wiley & Sons, Inc. p. 807-914. (Disponible en anglais seulement).
[OMS] World Health Organization. 1999a. Safety evaluation of certain food additives: aliphatic acyclic and alicyclic alpha-diketones and related alpha-hydroxyketones. Geneva (CH): World Health Organization, International Programme on Chemical Safety. (WHO Food Additive Series 42). Prepared by the Fifty-first meeting of the Joint FAO/WHO Expert Committee on Food Additives. (Disponible en anglais seulement).
[OMS] World Health Organization. 1999b. Safety evaluation of certain food additives: saturated aliphatic acyclic secondary alcohols, ketones, and related saturated and unsaturated esters. Geneva (CH): World Health Organization, International Programme on Chemical Safety. (WHO Food Additive Series 42). Prepared by the Fifty-first meeting of the Joint FAO/WHO Expert Committee on Food Additives. (Disponible en anglais seulement).
[OMS] World Health Organization. 2003. Safety evaluation of certain food additives: aliphatic secondary alcohols, ketones and related esters. Geneva (CH): World Health Organization, International Programme on Chemical Safety. (WHO Food Additive Series 50). Prepared by the Fifty-ninth meeting of the Joint FAO/WHO Expert Committee on Food Additives. (Disponible en anglais seulement).
Parmet AJ, von Essen S. 2002. Rapidly progressive, fixed airway obstructive disease in popcorn workers: a new occupational pulmonary illness? J Occup Environ Med. 44(3):216-218. (Disponible en anglais seulement).
Paxéus, N. 1996. Organic pollutants in the effluents of large wastewater treatment plants in Sweden. Water Res. 30(5):1115-1122. (Disponible en anglais seulement).
Pellizzari ED, Hartwell TD, Harris III BSH, Waddell RD, Whitaker DA, Erickson MD. 1982. Purgeable organic compounds in mother’s milk. Bull Environ Contam Toxicol. 28(3):322-328. (Disponible en anglais seulement).
Perbellini L, Brugnone F, Mozzo P, Cocheo V, Caretta D. 1984. Methyl ethyl ketone exposure in industrial workers. Uptake and kinetics. Int Arch Occup Environ Health. 54(1):73-81. (Disponible en anglais seulement).
[P&G] Procter & Gamble. c2017a. Febreze® PLUG. [Consulté en octobre 2017]. (Disponible en anglais seulement).
[P&G] Procter & Gamble. c2017b. Febreze Set & Refresh Rain Air Freshener 5.5 ml. [Consulté en octobre 2017]. (Disponible en anglais seulement).
Phillips RD, Moran EJ, Dodd DE, Fowler EH, Kary CD, O’Donoghue J. 1987. A 14-week vapor inhalation toxicity study of methyl isobutyl ketone. Fundam Appl Toxicol. 9(3):380-388. (Disponible en anglais seulement).
Pierce JS, Abelmann A, Lotter JT, Comerford C, Keeton K, Finley BL. 2015. Characterization of naturally occurring airborne diacetyl concentrations associated with the preparation and consumption of unflavoured coffee. Toxicol Rep. 2:1200-1208. (Disponible en anglais seulement).
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [National Institute for Public Health and the Environment]. 2002. Children’s toys fact sheet: to assess the risks for the consumer [PDF, 303 KB]. Bilthoven (NL): RIVM. [Consulté en avril jusqu’en octobre 2017]. Report No.: 612810012/2002. (Disponible en anglais seulement).
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [National Institute for Public Health and the Environment]. 2006. Cosmetics fact sheet: to assess the risks for the consumer: Mis à jour le version for ConsExpo 4 [PDF, 330 KB]. Bilthoven (NL): RIVM. [Consulté en avril jusqu’en octobre 2017]. Report No.: 320104001/2006. (Disponible en anglais seulement).
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [National Institute for Public Health and the Environment]. 2007a. Do-it-yourself products fact sheet: to assess the risks for the consumer [PDF, 417 KB]. Bilthoven (NL): RIVM. [Consulté en avril jusqu’en octobre 2017]. Report No.: 320104007/2007. (Disponible en anglais seulement).
[RIVM] Rijksinstituut voor Volksgezondheid en Milieu [National Institute for Public Health and the Environment]. 2007b. Paint products fact sheet: to assess the risks for the consumer: Mis à jour le version for ConsExpo 4 [PDF, 264 KB]. Bilthoven (NL): RIVM. [Consulté en avril jusqu’en octobre 2017]. Report No.: 320104008/2007. (Disponible en anglais seulement).
Rosati JA, Krebs KA, Liu X. 2007. Emissions from cooking microwave popcorn. Crit Rev in Food Sci Nutr. 47(8):701-709. (Disponible en anglais seulement).
[RTECS] Registry of toxic effects of chemical substances.1987. Registry of toxic effects of chemical substances. 1985-86 ed., vol 1-6. Cincinnati (OH): National Institute for Occupational Safety and Health. DHSS (NIOSH) Publication No. 87-114. (Disponible en anglais seulement).
Rychlik M, Grosch W. 1996. Identification and quantification of potent odorants formed by toasting of wheat bread. LWT - Food Sci Technol. 29(5-6):515-525. (Disponible en anglais seulement).
Sabel GV, Clark TP. 1984. Volatile organic compounds as indicators of municipal solid waste leachate contamination. Waste Manag Res. 2(2):119-130. (Disponible en anglais seulement).
Saillenfait AM, Gallissot F, Sabaté JP, Bourges-Abella N, Cadot R, Morel G, Lambert AM. 2006. Developmental toxicity of combined ethylbenzene and methylethylketone administered by inhalation to rats. Food Chem Toxicol. 44(8):1287-1298. (Disponible en anglais seulement).
Sánchez-Peña CM, Luna G, García-González DL, Aparicio R. 2005. Characterization of French and Spanish dry-cured hams: influence of the volatiles from the muscles and the subcutaneous fat quantified by SPME-GC. Meat Sci. 69(4):635-645. (Disponible en anglais seulement).
Santé Canada. 1994. L’évaluation du risque à la santé humaine des substances d’intérêt prioritaire. Ottawa (Ont.) : Ministre des Approvisionnements et Services Canada. Nº au cat. : En40-215/41F [Consulté le 25 mai 2017]. (Disponible en anglais seulement).
Santé Canada. 1998. Exposure factors for assessing total daily intake of priority substances by the general population of Canada. Unpublished report. Ottawa (ON): Health Canada, Environmental Health Directorate. (Disponible en anglais seulement).
Santé Canada. 2010a. Étude d’évaluation de l’exposition à Windsor (2005-2006) : sommaire des données d’échantillonnage des composés organiques volatiles. Ottawa (Ont.) : Santé Canada. 85 p.
Santé Canada. 2010b. Étude de la qualité de l’air intérieur à Régina (2007) : sommaire des données d’échantillonnage des composés organiques volatiles. Ottawa (Ont.) : Santé Canada. 164 p.
Santé Canada. 2012. Étude de la qualité de l’air intérieur à Halifax (2009) : sommaire des données d’échantillonnage des composés organiques volatils (ébauche). Ottawa (Ont.) : Santé Canada. 37 p.
Santé Canada. 2013. Étude de la qualité de l’air intérieur à Edmonton (2010) : sommaire des données des composés organiques volatils (COV). Ottawa (Ont.) : Santé Canada. 50 p.
Santé Canada. 2015a. Tableau de la consommation des aliments tiré de Statistique Canada, Enquête sur la santé dans les collectivités canadiennes, cycle 2.2, Nutrition (2004), fichier partagé. Ottawa.
Santé Canada. 2015b. Keep calm and use hand sanitizer – how much and how often. Unpublished. Existing Substances Risk Assessment Bureau and New Substances Assessment and Control Bureau, Health Canada. Presented at Health Canada Science Forum 2015. (Disponible en anglais seulement).
Santé Canada. 2019. Cinquième rapport sur la biosurveillance humaine des substances chimiques de l’environnement au Canada : Résultats de l’Enquête canadienne sur les mesures de la santé cycle 5 (2016 à 2017) [PDF]. Ottawa (Ont.) : Santé Canada. [Consulté le 4 février 2020].
Santé Canada. [Modifié le 14 juillet 2020]. 2020a. Règlements sur les produits de vapotage. Ottawa (Ont.) : gouvernement du Canada. [Consulté le 4 décembre 2020].
Santé Canada. [Modifié le 11 novembre 2020] 2020b. Guide à l’intention de l’industrie sur les produits de vapotage visés par la Loi canadienne sur la sécurité des produits de consommation. Ottawa (Ont.) : gouvernement du Canada. [Consulté le 21 décembre 2020].
Santé Canada. 2024. Supporting documentation: intake tables for Ketones Group. Ottawa (ON): Health Canada. Information in support of the assessment for the Ketones Grouping. Accessible sur demande à ccessible sur demande à : eccc.substances.eccc@canada.ca. (Disponible en anglais seulement).
Sawhney BL, Kozloski RP. 1984. Organic pollutants in leachates from landfill sites. J Environ Qual. 13(3):349-352. (Disponible en anglais seulement).
Schneider K, de Hoogd M, Madsen MP, Haxaire P, Bierwishch A, Kaiser E. 2020a. ERASSTRI – European risk assessment study on synthetic turf rubber infill – Part 1: analysis of infill samples. Sci Total Environ. 718:137174. (Disponible en anglais seulement).
Schneider K, de Hoogd M, Haxaire P, Philipps A, Bierwishch A, Kaiser E. 2020b. ERASSTRI – European risk assessment study on synthetic turf rubber infill – Part 2: migration and monitoring studies. Sci Total Environ. 718:137173. (Disponible en anglais seulement).
Schwetz BA, Leong BKJ, Gehring PJ. 1974. Embryo- and fetotoxicity of inhaled carbon tetrachloride, 1,1-dichloroethane and methyl ethyl ketone in rats. Toxicol Appl Pharmacol. 28(3):452-464. (Disponible en anglais seulement).
Schwetz BA, Mast TJ, Weigel RJ, Dill JA, Morrissey RE. 1991. Developmental toxicity of inhaled methyl ethyl ketone in Swiss mice. Fundam Appl Toxicol. 16(4):742-748. (Disponible en anglais seulement).
[SCOEL] European Commission. Scientific Committee on Occupational Exposure Limits. 2014. Recommendation from the Scientific Committee on Occupational Exposure Limits for diacetyl [PDF, 506.16 KB]. SCOEL/SUM/149. [Consulté le 13 octobre 2017]. (Disponible en anglais seulement).
Scott B, Moore L. 2000. Assessment of the risks to human health posed by azo colourants in toys, writing inks and paper products, and analysis of the advantages and drawbacks of restrictions on their marketing and use. Final report. United Kingdom Laboratory of the Government Chemist. (Disponible en anglais seulement).
[SCREEN3] Screening Tool Program for Windows. 1996. Version 4.10. Research Triangle Park (NC): US Environmental Protection Agency, Office of Air Quality Planning and Standards Emissions, Monitoring, and Analysis Division. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2008. Permanent markers. La Mirada (CA): Kittrich Corporation. [Consulté en juillet 2016]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2011. 3M™ Throttle Plate & Carb Cleaner. St. Paul (MN): 3M. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2012a. Homax Wall Texture Pro Grade- Orange Peel [PDF]. Bellingham (WA): Homax Group Inc. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2012b. 03405-0720 MOTOMASTER CARBURETOR CLEANER 312G [PDF]. Vaughan (ON): K-G SPRAY-PAK INC. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2012c. Sharpie Fine Point Marker, Sharpie Ultra Fine Point Marker, etc. Oak Brook (IL): Newell Rubbermaid. [Consulté en juillet 2016]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2013. RectorSeal No.5. Houston (TX): RectorSeal. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2014a. Loctite® Stik 'n Seal Oil & Gas Resistant Adhesive[PDF]. Rocky Hill (CT): Henkel Corporation. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2014b. Berol, Expo Low Odor, Expo Click, etc. Oak Brook (IL): Newell Rubbermaid. [Consulté en juillet 2016]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2015a. Oatey Clear Cleaner [PDF]. Cleveland (OH): Oatey Inc. [Consulté en novembre 2017]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2015b. BIC Great Erase Bold Dry Erase Marker [PDF]. Shelton (CT): BicUSA Inc. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2015c. Turtle Wax Premium Scratch Repair Kit - Clear Coat Pen. Willowbrook (IL): Turtle Wax Inc. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2015d. Febreze Noticeables Air Freshener – Autumn Charm. Cincinnati (OH): Procter & Gamble, Fabric and Home Care Division. [Consulté en juillet 2016]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2015e. Febreze Set & Refresh – Cozy Vanilla Sugar. Cincinnati (OH): Procter & Gamble, Fabric and Home Care Division. [Consulté en juillet 2016]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2016a. Gun Metal Gray PDS Aerosol. Blaine (MN): Plasti Dip International. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2016b. NEVERWET 11 FL OZ 6PK RAIN REPELNT. Vernon Hills (IL): Rust-Oleum Corporation. [Consulté en septembre 2021]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2016c. WATCO 6X946ML LACQUER CLEAR GLOSS WF [PDF]. Concord (ON): Rust-Oleum Corporation. [Consulté en novembre 2017]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2016d. Vanilla Custard Flavor. Scotts Valley (CA): Perfumer’s Apprentice. [Consulté en juillet 2016]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2017a. AUTORF +SSPR 6PK VINYL AND FABRIC SAND [PDF]. Vernon Hills (IL): Rust-Oleum Corporation. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2017b. Epoxy Thinner. Montreal (QC): Swing Paints Ltd. [Consulté en novembre 2017]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2018a. Furniture Refinisher 1801. Montreal (QC): Swing Paints Ltd. [Consulté en novembre 2019]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2018b. Vacubond Solvent Cement (Clear) [PDF]. Markham (ON): Sluyter Company Ltd. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2018c. 3M™ Bondo® Glazing & Spot Putty 907, 907M, 907C, 907ES, 907W, 937, 937C. St. Paul (MN): 3M. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2018d. TRMCLD 6X426g GRAFFITI REMOVER [PDF]. Concord (ON): Rust-Oleum Canada (ROCA). [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2019a. Methyl Ethyl Ketone (MEK). Montreal (QC): Recochem Inc. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2019b. DUPLI-COLOR® Adhesion Promoter. Ciudad de México (MX): Compania Sherwin-Williams. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2019c. 3M™ Bondo® MEKP Liquid Hardener. London (ON): 3M Canada Company. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2019d. Berryman B-12 Chemtool Carburetor, Choke & Throttle Body Cleaner. Arlington (TX): Berryman Products, Inc. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2019e. 3 Primer (Clear) [PDF]. Markham (ON): Sluyter Company Ltd. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2019f. Maple Sugar Fragrance Oil [PDF]. Mississauga (ON): New Directions Aromatics Inc. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2020. KRYLON® FARM AND IMPLEMENT International Harvest Red. Mississauga (ON): Krylon Products Group. [Consulté en avril 2020]. (Disponible en anglais seulement).
[SDS] Safety Data Sheet. 2021. DUPLI-COLOR™ Truck Bed Liner Black [PDF]. Cleveland (OH): Dupli-Color Products Company. [Consulté en août 2021]. (Disponible en anglais seulement).
Shane BS, Troxclair AM, McMillin DJ, Henry CB. 1988. Comparative mutagenicity of nine brands of coffee to Salmonella typhimurium TA100, TA102, and TA104. Environ Mol Mutag. 11(2):195-206. (Disponible en anglais seulement).
Sheldon LS, Hites RA. 1978. Organic compounds in the Delaware River. Environ Sci Technol. 12(10):1188-1194. (Disponible en anglais seulement).
Shimoda M, Yoshimura T, Ishikawa H, Hayakawa I, Osajima Y. 2000. Volatile compounds of human milk. J Fac Agr. 45(1):199-206. (Disponible en anglais seulement).
Silverman L, Schulte HF, First MW. 1946. Further studies on sensory response to certain industrial solvent vapors. J Ind Hyg Toxicol. 28(6):262-266. (Disponible en anglais seulement).
Smyth HF Jr. 1956. Hygienic standards for daily inhalation. Am Ind Hyg Assoc Q. 17(2):129-185. (Disponible en anglais seulement).
Smyth HF Jr, Seaton J, Fischer L. 1942. Response of guinea pigs and rats to repeated inhalation of vapors of mesityl oxide and isophorone. J Ind Hyg Toxicol. 24(3):46-50. (Disponible en anglais seulement).
Smyth HF Jr, Carpenter CP, Weil CS. 1951. Range-finding toxicity data: list IV. AMA Arch Ind Hyg Occup Med. 4(2):119-122. (Disponible en anglais seulement).
Sparks LE, Tichenor BA, Chang J, Guo Z. 1996. Gas-phase mass transfer model for predicting volatile organic compound (VOC) emission rates from indoor pollutant sources. Indoor Air(1). 6:31-40. (Disponible en anglais seulement).
Spencer JN, Holmboe ES, Kirshenbaum MR, Firth DW, Pinto PB. 1982. Solvent effects on the tautomeric equilibrium of 2,4-pentadione. Can J Chem. 60:1178-1182. (Disponible en anglais seulement).
Stoner GD, Shimkin MB, Kniazeff AJ, Weisburger JH, Weisburger EK, Gori GB. 1973. Test for carcinogenicity of food additives and chemotherapeutic agents by the pulmonary tumor response in strain A mice. Cancer Res. 33(12):3069-3085. (Disponible en anglais seulement).
Svendsen N, Pedersen SF, Hansen OC, Pedersen E, Bernth N. 2005. Survey and release of chemical substances in “slimy” toys [PDF, 892 KB]. [Consulté en mai 2017]. Denmark: Danish Ministry of Environment. (Disponible en anglais seulement).
[TDS] Technical Data Sheet. 2015. Klenk’s Epoxy Thinner. Montreal (QC): Swing Paints. [Modifié le 11 août 2015; consulté en novembre 2017]. (Disponible en anglais seulement).
TERA. 2004. Report of the Peer Consultation Meeting on Methyl Ethyl Ketone. Submission by the VCCEP Task Group of the American Chemistry Council Ketones Panel for the Voluntary Children's Chemical Evalua(Disponible en anglais seulement).tion Program (VCCEP). Toxicology Excellence for Risk Assessment (TERA) Center, Cincinatti, Ohio.
TERA. 2017. Read across approach for the Methyl Iso Ketone group of chemicals. Toxicology Excellence for Risk Assessment (TERA) Center, Cincinatti, Ohio. Inédit. (Disponible en anglais seulement).
Tomicic C, Berode M, Oppliger A, Castella V, Leyvraz F, Praz-Christinaz SM, Danuser B. 2011. Sex differences in urinary levels of several biological indicators of exposure: a human volunteer study. Toxicol Lett. 202(3):218-225. (Disponible en anglais seulement).
Toso B, Procida G, Stefanon B. 2002. Determination of volatile compounds in cows’ milk using headspace GC-MS. J Dairy Res. 69(4):569-577. (Disponible en anglais seulement).
Tyl RW, Ballantyne B, Fisher LC, Tarasi DJ, Dodd DE. 1989. Dominant lethal assay of 2,4-pentanedione vapour in Fischer 344 rats. Toxicol Ind Health. 5(3):463-477. (Disponible en anglais seulement).
Tyl RW, Ballantyne B, Pritts IM, Garman RH, Fisher LC, France KA, McNeil DJ. 1990. An evaluation of the developmental toxicity of 2, 4-pentanedione in the Fischer 344 rat by vapor exposure. Toxicol Ind Health. 6(3-4):461-474. (Disponible en anglais seulement).
Tyl RW, France KA, Fisher LC, Pritts IM, Tyler TR, Phillips RD, Moran EJ. 1987. Developmental toxicity evaluation of inhaled methyl isobutyl ketone in Fischer 344 rats and CD-1 mice. Fundam Appl Toxicol. 8(3):310-327. (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 1988. Superfund Record of Decision: Kin-Buc Landfill, NJ (September 1988). EPA/ROD/R02-88/068. (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 1992. Screening procedures for estimating the air quality impact of stationary sources. Revised. Office of Air and Radiation, Office of Air Quality Planning and Standards. EPA-454/R-92-019. (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 1994. Methods for Derivation of Inhalation Reference Concentrations and Application of Inhalation Dosimetry. Research Triangle Park (NC): US EPA, Environmental Criteria and Assessment Office, Office of Health and Environmental Assessment, Office of Research and Development. (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 1999. Estimate of stack heights and exit gas velocities for TRI facilities in OPPT's Risk-Screening Environmental Indicators Model [PDF]. United States Environmental Protection Agency; Office of Pollution Prevention and Toxics; Economics, Exposure, and Technology Division. (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 2003a. Toxicological review of methyl ethyl ketone in support of summary information on the Integrated Risk Information System (IRIS) [PDF, 1.07 MB]. National Center for Environmental Assessment, Washington, DC. EPA 635/R-03/009. Bethesda (MD): US National Library of Medicine. [Consulté le 4 janvier 2017] (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 2003b. Toxicological review of methyl isobutyl ketone CAS NO. 108-10-1 in support of summary information on the Integrated Risk Information System (IRIS) [PDF, 586 KB]. National Center for Environmental Assessment, Washington, DC. EPA EPA/635/R-03/002. [Consulté le 18 août 2016]. (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 2005. PARAMS model. Washington (DC): US Environmental Protection Agency. [Modifié le 18 août 2011; consulté en octobre 2017]. (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 2006. Inert reassessment – mesityl oxide (CAS Reg. No. 141-79-7) [PDF]. Washington (DC): US EPA, Office of Pollution Prevention and Toxics. [Consulté en janvier 2020]. (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 2009a. A scoping-level field monitoring study of synthetic turf fields and playgrounds. Washington (DC): US EPA, Office of Research and Development. EPA/600/R-09/135. (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 2009b. Risk Assessment Guidance for Superfund Volume I: Human Health Evaluation Manual (Part F, Supplemental Guidance for Inhalation Risk Assessment). Washington (DC): US EPA, Office of Superfund Remediation and Technology Innovation. (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 2010. High Production Volume Information System. Washington (DC): US EPA, Office of Pollution Prevention and Toxics. 2-Pentanone. Submission ID 24977107. [Consulté le 17 novembre 2020]. (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 2011. Exposure factors handbook: 2011 edition. Washington (DC): Office of Research and Development. (Disponible en anglais seulement).
[US EPA] United States Environmental Protection Agency. 2019. Consumer Exposure Model v2.1. Washington (DC): US EPA, Office of Pollution Prevention and Toxics. (Disponible en anglais seulement).
[US EPA AcToR]. United States Environmental Protection Agency Aggregated Computational Toxicology Resource System. 2015. 2-Pentanone. CAS RN. 107-87-9. [Consulté le 1er février 2017]. (Disponible en anglais seulement).
[US EPA & CDC/ATSDR] United States Environmental Protectional Agency, Centers for Disease Control and Prevention/Agency for Toxic Substances & Disease Registry. 2019. Synthetic turf field recycled tire crumb rubber research under the Federal Research Action Plan: final report part 1 – tire crumb rubber characterization (volume 1) [PDF]. EPA/600/R-19/051. (Disponible en anglais seulement).
Valero E, Villamiel M, Miralles B, Sanz J, Martinez-Castro I. 2001. Changes in flavour and volatile components during storage of whole and skimmed UHT milk. Food Chem. 72(1):51-58. (Disponible en anglais seulement).
Van Engelen JGM, Park MVDZ, Janssen PJCM, Omen AG, Brandon EFA, Bouma K, Sips AJAM, Van Raaij MTM. 2008. Chemicals in toys. A general methodology for assessment of chemical safety of toys with a focus on elements [PDF]. RIVM report 320003001/2008. (Disponible en anglais seulement).
Van Rooy FGBGJ, Rooyackers JM, Prokop M, Houba R, Smit LAM, Heederik DJJ. 2007. Bronchiolitis obliterans syndrome in chemical workers producing diacetyl for food flavorings. Am J Respir Crit Care Med. 176(5):498-504. (Disponible en anglais seulement).
Versar. 1986. Standard scenarios for estimating exposure to chemical substances during use of consumer products. Vol. II. Consumer use of used motor oil. Springfield (VA): Versar, Inc. Prepared for US Environmental Protection Agency. (Disponible en anglais seulement).
[VCCEP] Voluntary Children’s Chemical Evaluation Program. 2003. Methyl ethyl ketone (CAS No. 78-93-3). VCCEP Submission. Prepared by: American Chemistry Council’s Ketones Panel. [Consulté en novembre 2016]. (Disponible en anglais seulement).
Wilkinson SC, Williams FM. 2001. In vitro dermal absorption of liquids. Contract Research Report 350/2001. Newcastle-upon-Tyne (UK): University of Newcastle, Department of Environmental and Occupational Medicine, Skin Research Group. (Disponible en anglais seulement).
Won D, Lusztyk E. 2011. Data gathering on chemicals released to indoor air of residences from building materials and furnishings. Final report. Ottawa (ON): National Research Council Canada. 158 p. Report No.: B3332.2. (Disponible en anglais seulement).
Won D, Yang, W. 2012. Material emission information from 105 building materials and consumer products. Final report. Ottawa (ON): National Research Council Canada. 164 p. Report No.: B3341.1.
Won D, Nong G, Yang W, Schleibinger H. 2013. Material emissions data: 52 building materials tested for 124 compounds. Ottawa (ON): National Research Council Canada. 300 p. Report No.: A1-000342. (Disponible en anglais seulement).
Won D, Nong G, Yang W, Collins P. 2014. Material emissions testing: VOCs from wood, paint, and insulation materials. Ottawa (ON): National Research Council Canada. Report No.: A1-000342.2. (Disponible en anglais seulement).
Won D, Nong G, Yang W, Lusztyk E. 2015. VOC emissions from evaporative sources in residential garages. Ottawa (ON): National Research Council Canada. 235 p. Contract No.: A1-000342. (Disponible en anglais seulement).
Won D, Yang W, So S, Aubin D. 2019. Investigation of sources and indoor levels of CMP3 chemicals. Phase 1 - analysis of indoor air samples from two field studies. Ottawa (ON): National Research Council. Report A1-014282.1. Inédit. (Disponible en anglais seulement).
[WSDE] Washington State Department of Ecology [base de données]. 2020. Search results for CAS RN [78-93-3]. Lacey (WA): Department of Ecology State of Washington. [Consulté le 14 juillet 2016]. (Disponible en anglais seulement).
Yu H, Chen S. 2010. Identification of characteristic aroma-active compounds in steamed mangrove crab (Scylla serrata). Food Res Int. 43(8):2081-2086. (Disponible en anglais seulement).
Yue J, Zheng Y, Liu Z, Deng Y, Jing Y, Luo Y, Yu W, Zhao Y. 2015. Characterization of volatile compounds in microfiltered pasteurized milk using solid-phase microextraction and GCxGC-TOFMS. Int J Food Prop. 18:2193-2212. (Disponible en anglais seulement).
Zaccone EJ, Goldsmith WT, Shimko MJ, Wells JR, Schwegler-Berry D, Willard PA, Case SL, Thompson JA, Fedan JS. 2015. Diacetyl and 2,3-pentanedione exposure of human cultured airway epithelial cells: ion transport effects and metabolism of butter flavoring agents. Toxicol Appl Pharmacol. 289(3):542-549. (Disponible en anglais seulement).
Zaccone EJ, Thompson JA, Ponnoth DS, Cumpston AM, Goldsmith WT, Jackson MC, Kashon ML, Frazer DG, Hubbs AF, Shimko MJ, et coll. 2013. Popcorn flavoring effects on reactivity of rat airways in vivo and in vitro. J Toxicol Environ Health A. 76(11):669-689. (Disponible en anglais seulement).
Zakhari S, Levy P, Liebowitz M, Aviado DM. 1977. Acute oral, intraperitoneal, and inhalation toxicity of methyl isobutyl ketone in the mouse. In: L. Goldberg, editor. Isopropanol and ketones in the environment. Cleveland (OH): CRC Press. p. 101-104 (Chapter 11). (Disponible en anglais seulement).
Zhou S, Barnes I, Zhu T, Bejan I, Albu M, Benter T. 2008. Atmospheric Chemistry of acetylacetone. Environ Sci Technol. 42:7905-7910. (Disponible en anglais seulement).
Zhu J, Cao X-L, Beauchamp R. 2001. Determination of 2-butoxyethanol emissions from selected consumer products and its application in assessment of inhalation exposure associated with cleaning tasks. Environ Int. 26(7-8):589-597. (Disponible en anglais seulement).
Zhu J, Newhook R, Marro L, Chan CC. 2005. Selected volatile organic compounds in residential air in the city of Ottawa, Canada. Environ Sci Technol. 39(11):3964-3971. (Disponible en anglais seulement).
Zhu J, Wong SL, Cakmak S. 2013. Nationally representative levels of selected volatile organic compounds in Canadian residential indoor air: population-based survey. Environ Sci Technol. 47(23):13276-13283. (Disponible en anglais seulement).
Annexes
Annexe A. Tableaux de lecture croisée
| Nom chimique | 2-Butanol | MEK | MPK |
|---|---|---|---|
| Rôle | Substance analogue | Produit chimique cible | Produit chimique cible |
| NR CAS | 78-92-2 | 78-93-3 | 107-87-9 |
| Structure chimique |  MM : 74,12 g/mol log Koe : 0,61 |
 MM : 72,11 g/mol log Koe : 0,29 |
 MM : 86,13 g/mol log Koe : 0,91 |
| Toxicocinétique et métabolisme | Conversion rapide en MEK | Absorption rapide par inhalation et par voies orale et cutanée. Réduction en 2‑butanol, qui est rapidement oxydé en MEK (US EPA, 2003a). | L’absorption devrait être tout aussi rapide et importante que la MEK et le 2-butanol. |
| Toxicité aiguë | N. D. | DL50 par voie orale = 2737 mg/kg p.c. (rats), 4044 mg/kg p.c. (souris) CL50 par inhalation >23 600 mg/m3 (rats, souris, cochons d’Inde) CMENO, effets neurocomportementaux = 4800 mg/m3 (4 h, souris) |
DL50 par voie orale >1600 à <3200 mg/kg p.c. (rats) CL50 par inhalation >25 mg/L DL50 par voie cutanée = 8000 mg/kg p.c. CMENO, effets neurocomportementaux = 3500 mg/m3 (4 h, souris) |
| Études de toxicité à court terme par inhalation | N. D. | CMENO, effets neurocomportementaux = 300 à 600 mg/m3 (humains, babouins), 4800 mg/m3 (rats) | N. D. |
| Toxicité à doses répétées (voie orale) | DSENO = 1771 mg/kg p.c./j (8 sem, rats femelles) | DSENO de neurotoxicité (effets non aigus) = 173 mg/kg p.c./j (rats) DSENO = 1723 mg/kg p.c./j (lecture croisée à partir du 2-butanola) |
DSENO = 454 mg/kg p.c./j (13 mois, rats mâles) |
| Toxicité à doses répétées (inhalation) | N. D. | CSENO = 14 750 mg/m3 (90 j, rats) | CSENO = 5300 mg/m3 (13 sem, rats) CMENO, effets neurocomportementaux = 5000 mg/m5 (jusqu’à 51 j, rats) |
| Toxicité à doses répétées (voie cutanée) | N. D. | N. D. | DSENO = 454 mg/kg p.c./j (étude sur l’exposition à la MPK par voie orale) |
| Toxicité pour la reproduction ou le développement (voie orale) | DSENO de toxicité pour la reproduction (limitéeb) = 5089 mg/kg p.c./j (rats mâles), 4571 mg/kg p.c./j (rats femelles) DSENO pour les mères et le développement = 1771 mg/kg p.c./j DEM05 pour le développement = 657 mg/kg p.c./j (étude de 8 sem sur plusieurs générations, rats) |
DEM05 de toxicité pour le développement = 639 mg/kg p.c./j (lecture croisée à partir du 2-butanola) | DEM05 = 763 mg/kg p.c./j (déduite à partir du 2‑butanola) |
| Toxicité pour la reproduction ou le développement (inhalation) | N. D. | CEI10 de toxicité pour le développement = 5202 mg/m3 (exposition intermittente, souris) | CSENO de toxicité pour la reproduction = 5000 mg/m3 CSENOdév = 5000 mg/m3 et 5300 mg/m3 |
| Toxicité pour la reproduction ou le développement (voie cutanée) | N. D. | DEM05 = 639 mg/kg p.c./j (lecture croisée à partir de l’étude sur l’exposition par voie orale au 2-butanola) | DEM05 = 763 mg/kg p.c./j (lecture croisée à partir de l’étude sur l’exposition par voie orale au 2-butanola) |
| Génotoxicité | Non génotoxique | Résultats négatifs lors d’essais in vitro et in vivo | Résultats négatifs lors d’essais in vitro, prévisions négatives du modèle QSAR pour les alertes structurales |
| Cancérogénicité | N. D. | Résultats négatifs/non concluants (EPA, 2003) | Prévisions négatives du modèle QSAR pour la cancérogénicité |
Abréviations : N. D., non disponible; log Koe, coefficient de partage octanol-eau; MM, masse moléculaire; CL50, concentration d’une substance qu’on estime létale pour 50 % des organismes d’essai; DL50, dose d’une substance qu’on estime létale pour 50 % des organismes d’essai; CEI10, limite inférieure de la concentration efficace produisant un taux de réponse de 10 %; DEM05, dose efficace minimale (limite inférieure de confiance de 95 % de la dose efficace [DE]); CMENO, concentration minimale avec effet nocif observé; DMENO, dose minimale avec effet nocif observé; DMEO, dose minimale avec effet observé; CSENO, concentration sans effet nocif observé; DSENO, dose sans effet nocif observé.
a Ajustement molaire calculé à partir de la valeur obtenue par lecture croisée. Les masses moléculaires sont 74,12 g/mol pour le 2-butanol, 72,11 g/mol pour la MEK et 86,13 g/mol pour la MPK.
b Comme relevé par l’EPA des États-Unis (2003a), cette étude ne comprenait pas l’évaluation de certains paramètres couramment mesurés dans le cadre d’études de conception plus récente. Parmi les lacunes, mentionnons l’absence de mesures de la cyclicité œstrale, des paramètres du sperme, du poids de l’utérus, des épididymes, des vésicules séminales et du cerveau, ainsi que des données incomplètes sur la chimie et l’hématologie cliniques et l’histopathologie.
| Nom chimique | MIBK | MIAK | Alcool de diacétone |
|---|---|---|---|
| Rôle | Produit chimique cible | Produit chimique cible | Produit chimique cible |
| NR CAS | 108-10-1 | 110-12-3 | 123-42-2 |
| Structure chimique |  MM = 100,16 g/mol |
 MM = 114,18 g/mol |
 MM = 116,16 g/mol |
| Toxicité aiguë par voie orale | DL50 rat = 2080 à 4570 mg/kg p.c. DL50 souris = 1900 à 2850 mg/kg p.c. |
DL50 rat = 5657 mg/kg p.c. | DL50 rat = 3002 mg/kg p.c. |
| Toxicité aiguë par inhalation | CL50 rat = 8200 à 16 400 mg/m3 CMENO babouins juvéniles = 200 mg/m3 (exposition de 1 à 7 j), dépression du SNC CMENO volontaires humains = 200 mg/m3 (exposition de 2 h), dépression du SNC |
CL50 rat (6 h) = 17 806 mg/m3 |
CL50 rat (4 h) = 7600 mg/m3 |
| Toxicité aiguë par voie cutanée | DL50 lapin = >20 000 mg/kg p.c. | N. D. | DL50 rat (24 h) >1875 mg/kg p.c. |
| Toxicité à court terme (14 j) par inhalation | CSENO = 410 mg/m3 (poids relatif des reins accru et néphrose tubulaire liée aux gouttelettes hyalines) | CSENO = 1775 mg/m3 (toxicité maternelle, car dépression du SNC observée lors d’une étude de toxicité pour le développement) | CSENO = 968 mg/m3 (d’après une étude de toxicité pour le développement par voie orale de 15 j) |
| Toxicité à court terme (14 j) par voie cutanée | N. D. | DSEO = 137 mg/kg p.c./j (d’après une étude de toxicité pour le développement par inhalation) | DSEO = 1000 mg/kg p.c./j (d’après une étude de toxicité pour le développement par voie orale de 15 j) |
| Toxicité à doses répétées (voie orale) | DMEO/DSENO = 250 mg/kg p.c./j (13 sem; effets hépatiques et rénaux à 1000 mg/kg p.c./j) DMENO = 101 mg/kg p.c./j (2 ans; néphropathie chronique chez les femelles) |
DSEO = 52 mg/kg p.c./j (d’après la CSENO par inhalation) | DSENO = 100 mg/kg p.c./j (45 j; changements aux reins et chimie hématologique et sanguine modifiée) |
| Toxicité à doses répétées (inhalation) | CMENO = 410 mg/m3 (incidence accrue d’hyperplasie des tubules rénaux et de néphropathie chronique [femelles] et de la minéralisation des papilles rénales [mâles]) CMENO = 1843 mg/m3 (2 ans; néphropathie chronique chez les femelles) |
CSENO = 934 mg/m3 (96 j; hausse du poids du foie et des reins, hypertrophie des hépatocytes dans le foie et régénération de l’épithélium tubulaire dans les reins des mâles et des femelles à 4670 mg/m3) | CSENO = 1035 mg/m3 (6 sem; variations du poids du foie sans modifications histopathologiques à 4685 mg/m3) |
| Toxicité à doses répétées (voie cutanée) | DMENO = 300 mg/kg p.c./j (4 mois; plus faible dose d’essai; changements morphologiques dans plusieurs tissus) DMEO/DSENO = 250 mg/kg p.c./j (d’après l’exposition à la MIBK par voie orale) |
DSEO = 52 mg/kg p.c./j (d’après la CSENO par inhalation) | DSENO = 100 mg/kg p.c./j (d’après la DSENO par voie orale) |
| Toxicité pour la reproduction ou le développement (voie orale) | DSENO = 259 mg/kg p.c./j (lecture croisée à partir de l’alcool de diacétone) | CSENOdév = 271 mg/m3 (d’après la CSENO par inhalation) CSENOmat = 137 mg/m3 (d’après la CSENO par inhalation) |
DSENOdév = 300 mg/kg p.c./j (effets sur la reproduction et le développement à 1000 mg/kg p.c./j) DSENOmat = 100 mg/kg p.c./j (changements aux reins et chimie hématologique et sanguine modifiée) |
| Toxicité pour la reproduction ou le développement (inhalation) | CSENOdév/mat = 4106 mg/m3 (d’après la diminution transitoire du poids corporel et de la consommation alimentaire, les changements dans le poids des organes reproducteurs chez les parents et les effets dépresseurs aigus sur le SNC des petits) |
CSENOdév = 1775 mg/m3 (d’après la dépression du SNC à 3505 mg/m3) CSENOmat = 3505 mg/m3 (d’après la diminution du poids corporel et de la consommation alimentaire à 7005 mg/m3) |
CSENOdév = 968 mg/m3 (d’après la DSENO tirée de l’étude de toxicité par voie orale de 45 j) CSENOdév/mat = 3182 mg/m3 (d’après les JG 6 à 20 de l’étude de toxicité par voie orale) |
| Toxicité pour la reproduction ou le développement (voie cutanée) | DSENO = 259 mg/kg p.c./j (lecture croisée à partir de l’alcool de diacétone) | CSENOdév = 271 mg/m3 (d’après la CSENO par inhalation) CSENOmat = 137 mg/m3 (d’après la CSENO par inhalation) |
DSENOdév = 300 mg/kg p.c./j DSENOmat = 100 mg/kg p.c./j |
| Génotoxicité | Négative | Négative | Négative |
| Cancérogénicité | Positive | Possible | Possible |
Abréviations : MM, masse moléculaire; N. D., non disponible; dév, toxicité pour le développement; CL50, concentration d’une substance qu’on estime létale pour 50 % des organismes d’essai; DL50, dose d’une substance qu’on estime létale pour 50 % des organismes d’essai; CMENO, concentration minimale avec effet nocif observé; DMENO, dose minimale avec effet nocif observé; DMEO, dose minimale avec effet observé; CSENO, concentration sans effet nocif observé; mat, toxicité maternelle; DSENO, dose sans effet nocif observé; DSEO, dose sans effet observé.
| Nom chimique | Diacétyle | Acétoïne | 2,3-PD |
|---|---|---|---|
| Rôle | Produit chimique cible | Produit chimique cible | Produit chimique cible |
| NR CAS | 431-03-8 | 513-86-0 | 600-14-6 |
| Structure chimique |  MM = 86,09 g/mol |
 MM = 88,10 g/mol |
 MM = 100,12 g/mol |
| Toxicité aiguë (létalité) | DL50 par voie orale = 3000 mg/kg chez le rat | DL50 par voie orale >5000 mg/kg | DL50 par voie orale = 3000 mg/kg chez le rat |
| Toxicité à court terme | CMENO = 92,9 ppm (333 mg/m3) sous forme d’une exposition unique pulsée de 15 min | N. D. | CSENO = 112 ppm (459 mg/m3) (cytotoxicité respiratoire et olfactive) |
| Toxicité à doses répétées (inhalation, <2 sem) | CMENO = 100 ppm (358 mg/m3), soit la plus faible concentration d’essai chez le rat CMENO = 50 ppm (176 mg/m3) (lecture croisée à partir de la 2,3‑PD) |
N. D. | CMENO = 50 ppm (205 mg/m3) (changements histopathologiques chez les rats et les souris, 10 à 12 j) |
| Toxicité subchronique (voie orale, 90 j) | DSENO = 90 mg/kg p.c./j | DSENO = 330 mg/kg p.c./j (eau potable) (diminution du poids corporel et anémie) | DSENO = 105 mg/kg p.c./j (lecture croisée à partir du diacétyle) DSENO = 24 mg/kg p.c./j (d’après les effets non liés aux voies respiratoires observés lors de l’étude par inhalation de 90 j) |
| Toxicité subchronique (inhalation, 90 j) | CSENO = 12,5 ppm (45 mg/m3) | CSENO = 800 ppm (2883 mg/m3), soit la plus forte concentration d’essai (NTP, 2017) | CSENO = 12,5 ppm (51 mg/m3) (effets histopathologiques sur l’appareil respiratoire chez les rats et les souris; 14 sem) |
| Toxicité subchronique (voie cutanée) | DSENO = 90 mg/kg p.c./j (d’après l’exposition par voie orale) | DSENO = 330 mg/kg p.c./j (extrapolation à partir de l’exposition par voie orale) | DSENO = 105 mg/kg p.c./j (lecture croisée à partir du diacétyle) |
| Toxicité chronique (inhalation) | CRI10 = 30,23 mg/m3 d’après la présence de papillomes et de carcinomes des cellules squameuses (valeur corrigée pour une exposition continue) | N. D. | N. D. |
| Toxicité pour le développement (voie orale) | DSENO = 1600 mg/kg p.c./j | DSENO = 1640 mg/kg p.c./j (lecture croisée à partir du diacétyle) | N. D. |
| Génotoxicité | Probablement génotoxique | Possiblement génotoxique en raison de sa similitude avec le diacétyle | Probablement génotoxique (lecture croisée à partir du diacétyle) |
| Cancérogénicité | Certaines études de toxicité chronique menées sur des animaux ont révélé des preuves de cancérogénicité. | Possiblement génotoxique en raison de sa similitude avec le diacétyle | Certaines études de toxicité chronique menées sur des animaux ont révélé des preuves de cancérogénicité (lecture croisée à partir du diacétyle). |
Abréviations : N. D., non disponible; MM, masse moléculaire; CRI10, limite inférieure d’un intervalle de confiance unilatéral de 95 % pour la concentration repère (CRI) qui devrait entraîner un taux d’incidence des tumeurs de 10 %; DL50, dose d’une substance qu’on estime létale pour 50 % des organismes d’essai; CMENO, concentration minimale avec effet nocif observé; DMENO, dose minimale avec effet nocif observé; CSENO, concentration sans effet nocif observé; DSENO, dose sans effet nocif observé.
| Nom chimique | Oxyde de mésityle | 6-Méthyl-5-heptén-2-one (MHE) |
|---|---|---|
| Rôle | Produit chimique cible | Substance analogue |
| NR CAS | 141-79-7 | 110-93-0 |
| Structure chimique |  MM = 98,1 g/mol log Koe : 1,2 à 1,7 |
 MM = 126,2 g/mol log Koe : 2,06 |
| Toxicité à doses répétées (inhalation, exposition de 49 j) | CMENO = 124 mg/m3 (réduction du poids corporel et du gain de poids corporel, histopathologie des voies nasales); aucune CSENO recensée. | N. D. |
| Toxicité à doses répétées (inhalation, 6 sem) | CSENO = 200 mg/m3 (effets histopathologiques dans les reins, les poumons et le foie) | N. D. |
| Toxicité à doses répétées (voie orale) | DSENO = 15,0 mg/kg p.c./j (extrapolation d’une voie à l’autre à partir d’une étude par inhalation de 6 sema) DSENO = 39 mg/kg p.c./j (lecture croisée à partir du MHE avec correction de la masse moléculaire) |
DSENO = 50 mg/kg p.c./j (augmentation de la numération plaquettaire chez les rats femelles lors d’une étude de 90 j) DMENO = 200 mg/kg p.c./j (OCDE, 2003) |
| Toxicité pour le développement (inhalation) | Aucune toxicité pour le développement n’a été observée jusqu’à une concentration de 1211 mg/m3 | N. D. |
| Toxicité pour le développement (voie orale) | Aucune toxicité pour le développement n’a été observée jusqu’à une dose de 95,2 mg/kg p.c./j (extrapolation d’une voie à l’autre à partir d’une étude par inhalationa) DSENO = 165 mg/kg p.c./j (lecture croisée à partir du MHE avec correction de la masse moléculaire) |
DSENO = 200 mg/kg p.c./j (toxicité maternelle et pour le développement prénatal observée lors d’une étude de toxicité pour le développement prénatal chez le rat) DMENO = 1000 mg/kg p.c./j. Aucune malformation fœtale observée jusqu’à une dose de 1000 mg/kg p.c./j (OCDE, 2003) |
| Toxicité pour la reproduction (inhalation) | CSENO = 413 mg/m3 (nombre réduit de portées à 1211 mg/m3) | N. D. |
| Toxicité pour la reproduction (voie orale) | DSENO = 32,5 mg/kg p.c./j (extrapolation d’une voie à l’autre à partir d’une étude combinée de toxicité à doses répétées et de toxicité pour la reproduction et le développement) DSENO = 165 mg/kg p.c./j (lecture croisée à partir du MHE avec correction de la masse moléculaire) |
DSENO = 200 mg/kg p.c./j (toxicité testiculaire chez les rats mâles lors d’une étude de 90 j) DMENO = 1000 mg/kg p.c./j Aucun effet chez les rats femelles (OCDE, 2003) |
| Génotoxicité | Négative | Négative |
| Cancérogénicité | N. D. | N. D. |
Abréviations : N. D., non disponible; MM, masse moléculaire; log Koe, coefficient de partage octanol-eau; CMENO, concentration minimale avec effet nocif observé; DMENO, dose minimale avec effet nocif observé; CSENO, concentration sans effet nocif observé; DSENO, dose sans effet nocif observé.
*Cette concentration a été convertie à la dose orale à l’aide de paramètres de Santé Canada (1994), d’un poids corporel moyen pour le rat de 0,35 kg et d’un taux d’inhalation de 0,11 m3/j, c’est-à-dire 200 mg/m3 × 0,11 m3/j × 8 h/24 h × 5 j/7 j / 0,35 kg = 15,0 mg/kg p.c./j pour la toxicité à doses répétées ou 413 mg/m3 × 0,11 m3/j × 6 h/24 h / 0,35 kg = 32,5 mg/kg p.c./j pour la toxicité pour la reproduction.
Annexe B. Paramètres d’estimation de l’exposition à proximité de certaines installations
Le modèle SCREEN3 (1996) a servi à estimer les concentrations dans l’air ambiant près d’installations ayant déclaré des rejets de MEK et de MIBK dans l’air. SCREEN3 est basé sur le modèle Industrial Source Complex (ISC) qui permet d’évaluer les concentrations de polluants provenant de diverses sources dans un complexe industriel. Il est conçu pour estimer les concentrations maximales d’une substance à une hauteur de récepteur donnée et à diverses distances à partir d’une source de rejet pour un événement d’émission continue donné. La concentration d’exposition maximale calculée est sélectionnée au moyen d’une matrice intégrée de données météorologiques contenant différentes combinaisons de conditions météorologiques, dont la vitesse du vent, la turbulence et l’humidité. Le principal paramètre du modèle SCREEN3 pour la dispersion atmosphérique est le vent. Ce modèle permet de prédire directement les concentrations résultant de sources ponctuelles, étendues et volumiques.
Le tableau ci-dessous présente les paramètres d’entrée du modèle SCREEN3 utilisés pour estimer les concentrations de MEK dans l’air ambiant attribuables aux rejets atmosphériques de certaines installations déclarantes en 2016.
| Paramètre | Valeur d’entrée | Valeur d’entrée |
|---|---|---|
| Type de la source de rejeta | Étendue | Ponctuelle |
| Superficie d’émission efficace (m2)b | 95 550 | N. R. |
| Taux d’émission (g/s•m2)c | 1,06 x 10-5 | N. R. |
| Hauteur de la source de rejet (m) | 10 | N. R. |
| Hauteur de la cheminée (m) | N. R. | 9,14 |
| Diamètre interne de la cheminéeb (m) | N. R. | 0,5 |
| Taux d’émission (g/s)c | N. R. | 4,02 |
| Vitesse d’échappement du gaz de la cheminéed (m/s) | N. R. | 10,44 |
| Température d’échappement du gaz de la cheminée (K)e | N. R. | 293 |
| Hauteur du récepteur au-dessus du sol (m)f | 1,74 | 1,74 |
| Facteur d’ajustement du vent variableg | 0,4 (moyenne quotidienne), 0,2 (moyenne annuelle) | 0,4 (moyenne quotidienne), 0,2 (moyenne annuelle) |
| Milieu urbain ou ruralb | Urbain | Urbain |
| Type de météorologie | Complète | Complète |
| Distance minimale et maximale (m) | 0 à 500 | 0 à 200 |
Abréviations : N. R., non requis pour le type de source de rejet sélectionné
a Le type de source de rejet a été sélectionné en fonction des données de l’INRP sur les rejets sur place.
b Jugement professionnel et d’après l’analyse de photos aériennes
c Estimations fondées sur les quantités déclarées à l’INRP par les installations, en présumant d’un rejet continu (INRP, 2021)
d US EPA (1999)
e Valeur réglementaire par défaut dans le modèle SCREEN3
f Curry et coll. (1993
g US EPA (1992) et jugement professionnel
Le tableau ci-dessous présente les paramètres d’entrée du modèle SCREEN3 utilisés pour estimer les concentrations de MIBK dans l’air ambiant attribuables aux rejets atmosphériques de certaines installations déclarantes en 2015.
| Paramètre | Valeur d’entrée | Valeur d’entrée |
|---|---|---|
| Type de la source de rejeta | Étendue | Ponctuelle |
| Superficie d’émission efficace (m2)b | 592 500 | N. R. |
| Taux d’émission (g/s•m2)c | 5,45 x 10-8 | N. R. |
| Hauteur de la source de rejet (m) | 10 | N. R. |
| Hauteur de la cheminée (m) | N. R. | 18,59 |
| Diamètre interne de la cheminéeb (m) | N. R. | 0,5 |
| Taux d’émission (g/s)c | N. R. | 0,03 |
| Vitesse d’échappement du gaz de la cheminéed (m/s) | N. R. | 11,89 |
| Température d’échappement du gaz de la cheminée (K)e | N. R. | 293 |
| Hauteur du récepteur au-dessus du sol (m)f | 1,74 | 1,74 |
| Facteur d’ajustement du vent variableg | 0,4 (moyenne quotidienne), 0,2 (moyenne annuelle) | 0,4 (moyenne quotidienne), 0,2 (moyenne annuelle) |
| Milieu urbain ou ruralb | Urbain | Urbain |
| Type de météorologie | Complète | Complète |
| Distance minimale et maximale (m) | 0 à 700 | 0 à 700 |
Abréviations : N. R., non requis pour le type de source de rejet sélectionné
a Le type de source de rejet a été sélectionné en fonction des données de l’INRP sur les rejets sur place.
b Jugement professionnel et d’après l’analyse de photos aériennes
c Estimations fondées sur les quantités déclarées à l’INRP par les installations, en présumant d’un rejet continu (INRP, 2021)
d US EPA (1999)
e Valeur réglementaire par défaut dans le modèle SCREEN3
f Curry et coll. (1993)
g US EPA (1992) et jugement professionnel.
Annexe C. Cétones dans les aliments
| Nom de la substance | Absorption par personne aux États-Unis (µg/j) | Absorption par personne aux États-Unis (µg/kg p.c./j) | Absorption par personne en Europe (µg/j) | Absorption par personne en Europe (µg/kg p.c./j) |
|---|---|---|---|---|
| MEK | 36 | 0,6 | 110 | 2 |
| MPK | 42 | 0,7 | 140 | 2 |
| MIBK | 2 | 0,03 | 7 | 0,12 |
| Diacétyle | 8 000 | 133 | 3 300 | 55 |
| 2,3-PD | 80 | 1 | 220 | 4 |
| Acétoïne | 1 800 | 30 | 2 800 | 47 |
| Oxyde de mésityle | N. D. | N. D. | 0,40 | 0,0067 |
Abréviations : N. D., non disponible
Ces estimations de l’absorption par personne (µg/j) ont été calculées par le JECFA au moyen de la méthode de calcul de la dose maximale journalière basée sur des données d’enquête (MSDI), en présumant que les quantités des diverses substances produites annuellement déclarées aux États-Unis et en Europe sont consommées par seulement 10 % de la population (« consommateurs uniquement ») et que seulement 60 % des quantités produites annuellement ont été déclarées lors des enquêtes sur les volumes produits. Nous avons postulé un poids corporel de 60 kg pour estimer l’absorption en µg/kg p.c./j (Organization of the Flavor Industry, 1995; US National Academy of Sciences, 1989, tous 2 cités dans OMS, 1999b).
Nous avons calculé les estimations quantitatives de l’exposition pour la présence naturelle des 10 substances au moyen des données sur la consommation pour les catégories d’aliments comparables du tableau de la consommation des aliments du cycle 2.2 de l’Enquête sur la santé dans les collectivités canadiennes (ESCC) (Santé Canada, 2015a). Les données sur les concentrations de chacune des substances dans les aliments recensées dans la documentation scientifique et la base de données des composés volatils contenus dans les aliments (Nijssen et coll., 1963-2018) sont résumées dans les tableaux C-2, C-3, C-4 et C-5. Comme des données quantitatives n’étaient pas disponibles pour tous les aliments, nous avons utilisé les valeurs maximales déclarées pour divers aliments afin d’estimer les expositions maximales potentielles à toutes les substances dans les aliments pour la population générale du Canada. Le tableau C-6 présente les expositions estimées pour les 10 substances en raison de leur présence naturelle dans les aliments.
| Catégorie d’aliments | MEK (µg/g) | MPK (µg/g) |
|---|---|---|
| Bières et panachés | 0,06 | 0,02 |
| Spiritueux et liqueurs | 2,00 | 1,20 |
| Jus de fruits | 0,20 | 0,10 |
| Café (Les produits en poudre sont reconstitués.) | N. D. | 4,70 |
| Thé, dont le thé glacé | 8,00 | N. D. |
| Laits | N. D. | 0,10b |
| Crèmes | 0,07 | 0,05 |
| Fromages | 67,10 | 14,71 |
| Yogourts | 7,00 | 0,01 |
| Bananes | N. D. | 27,00 |
| Cerises | N. D. | 0,01 |
| Poires | 1,00 | 2,40 |
| Ananas | N. D. | 0,01 |
| Prunes et pruneaux | N. D. | 2,00 |
| Fraises | N. D. | 3,10 |
| Autres fruits (bleuets, dattes, kiwis, salades de fruits) | 0,02 | 3,30 |
| Légumes, à l’exclusion des pommes de terre | 6,00 | 20,00 |
| Pommes de terre, frites | 0,13 | 0,07 |
| Poulet, dinde et autres volailles | 0,10 | 0,23 |
| Porc frais et jambon | 0,72c | N. D. |
| Poissons | 0,60 | N. D. |
| Mollusques et crustacés | N. D. | 0,12 |
| Œufs | 0,01 | N. D. |
| Noix, graines et beurre d’arachides | 0,10 | 7,60 |
| Légumineuses | 0,05 | N. D. |
| Beurre | 0,16 | 0,95 |
| Autres graisses et tartinades | 1,51 | 0,03 |
| Sucres, sirops et conserves | 0,08 | 0,03 |
| Collations salées | 0,13 | N. D. |
Abréviations : N. D., non disponible
a Données tirées de la base de données des composés volatils dans les aliments (Nijssen et coll., 1963-2018) sauf indication contraire.
b Yue et coll., 2015
c Sánchez-Peña et coll., 2005
| Catégorie d’aliments | MIBK (µg/g) | MIAK (µg/g) | Alcool de diacétone (µg/g) |
|---|---|---|---|
| Bières et panachés | 0,12 | N. D. | N. D. |
| Café (Les produits en poudre sont reconstitués.) | 6,50 | 0,50 | N. D. |
Laits |
0,016b | N. D. | 0,00015c |
| Prunes et pruneaux | 0,01 | N. D. | N. D. |
| Autres fruits (bleuets, dattes, kiwis, salades de fruits) | 0,02 | 0,001 | 0,408 |
| Poulet, dinde et autres volailles | 0,0004 | N. D. | 0,07 |
| Œufs | 0,003 | N. D. | N. D. |
| Autres graisses et tartinades | 0,38 | N. D. | N. D. |
| Sucres, sirops et conserves | N. D. | N. D. | 2,70 |
| Autres ingrédients figurant dans les recettes (par exemple, épices, ingrédients de cuisson) | N. D. | N. D. | 28,50 |
Abréviations : N. D., non disponible
a Données tirées de la base de données des composés volatils dans les aliments (Nijssen et coll., 1963-2018) sauf indication contraire.
b Yue et coll., 2015
c Toso et coll., 2002
| Catégorie d’aliments | Diacétyle (µg/g) | 2,3-PD (μg/g) | Acétoïne (µg/g) |
|---|---|---|---|
| Bières et panachés | 0,20 | 0,30 | 9,00 |
| Spiritueux et liqueurs | 9,77b | 0,60 | 335,00 |
| Vins | 4,10 | N. D. | 234,00l |
| Jus de fruits | 3,15c | N. D. | 0,35 |
| Café (Les produits en poudre sont reconstitués.) | 58,70 | 39,60 | 4,90 |
| Thé, dont le thé glacé | 1,00 | 2,00 | N. D. |
| Laits | 29,3d | 0,20j | N. D. |
| Crèmes | 30,00 | N. D. | N. D. |
| Fromages | 4,20 | N. D. | 40,00 |
| Yogourts | 43,00e | N. D. | 28,00 |
| Pâtes, riz, grains céréaliers et farines | 0,19 | 0,25 | 0,75 |
| Pains blancs | 0,92 | 0,14 | N. D. |
| Pains complets | 1,52 | 0,14k | 1,22m |
| Autres pains | 0,33 | 0,04 | N. D. |
| Pommes | 0,40 | N. D. | 3,50 |
| Cerises | N. D. | N. D. | 4,70 |
| Poires | N. D. | N. D. | 0,11 |
| Fraises | 0,20 | N. D. | 0,49 |
| Autres fruits (bleuets, dattes, kiwis, salades de fruits) | 0,60f | N. D. | 22,63 |
| Légumes, à l’exclusion des pommes de terre | 0,79g | N. D. | 6,40 |
| Pommes de terre, frites | 0,31 | N. D. | N. D. |
| Bœuf | 23,00 | 6,50 | 8,40 |
| Veau | 23,00 | 6,50 | 8,40 |
| Poulet, dinde et autres volailles | 0,90 | N. D. | 2,40 |
| Foies et pâtés de foie | 27,81 | N. D. | N. D. |
| Viandes à sandwich (viandes froides ou en conserve) | 27,81 | N. D. | N. D. |
| Porc frais et jambon | 0,36 | N. D. | N. D. |
| Poissons | 0,0017 | 0,69 | 0,31 |
| Mollusques et crustacés | 0,10h | N. D. | 0,16 |
| Noix, graines et beurre d’arachides | 0,09 | 0,23 | N. D. |
| Beurre | 21,00e | 0,05e | 2,00 |
| Margarines, en contenant | N. D. | 0,01 | N. D. |
| Margarines, en barquette | N. D. | 0,01 | N. D. |
| Autres graisses et tartinades | 0,60 | 0,01 | 0,04 |
| Confiseries, barres de chocolat | 0,40 | N. D. | 17,00 |
| Sucres, sirops et conserves | 2,60 | N. D. | 26,00 |
| Collations salées | N. D. | 0,20 | N. D. |
| Soupes sans légumes | 0,00056i | 0,42i | N. D. |
| Sauces | 0,09 | N. D. | N. D. |
| Assaisonnements, sel, poivre, vinaigre | 197,00 | N. D. | 1020 |
| Autres ingrédients figurant dans les recettes (par exemple, épices, ingrédients de cuisson) | 238,00 | 109,00 | 951,00 |
Abréviations : N. D., non disponible
a Données tirées de la base de données des composés volatils dans les aliments (Nijssen et coll., 1963-2018) sauf indication contraire.
b Cardoso et coll., 2003
c Lawson et coll., 1995
d De Leonardis et coll., 2013
e Macciola et coll., 2008
f Mujic et coll., 2014
g Annan et coll., 2005
h Yu et Chen, 2010
i Giri et coll., 2010
j Imhof et coll., 1995
k Rychlik et Grosch, 1996
l Garcia-Martinez et coll., 2013
m Birch et coll., 2013
| Catégorie d’aliments | 2,4-PD (μg/g) | Oxyde de mésityle (µg/g) |
|---|---|---|
| Vins | N. D. | 0,00005 |
| Jus de fruits | 0,01 | N. D. |
| Autres fruits (bleuets, dattes, kiwis, salades de fruits) | N. D. | 0,01 |
| Légumes, à l’exclusion des pommes de terre | N. D. | 0,04 |
| Poulet, dinde et autres volailles | 0,004 | N. D. |
| Autres graisses et tartinades | N. D. | 3,00 |
| Autres ingrédients figurant dans les recettes (par exemple, épices, ingrédients de cuisson) | N. D. | 2,40 |
Abréviations : N. D., non disponible
a Données tirées de la base de données des composés volatils dans les aliments (Nijssen et coll., 1963-2018) sauf indication contraire.
| Substance | De 0 à 6 moisa | De 6 à 12 mois | 1 an | De 2 à 3 ans | De 4 à 8 ans | De 9 à 13 ans | De 14 à 18 ans | 19 ans et plus |
|---|---|---|---|---|---|---|---|---|
| MEK | 0 | 112 | 185 | 174 | 130 | 82 | 66 | 67 |
| MPK | 0 | 146 | 216 | 192 | 137 | 86 | 68 | 98 |
| MIBK | 0 | 0,5 | 0,9 | 0,7 | 0,4 | 0,8 | 5 | 32 |
| MIAK | 0 | 0 | 0,001 | 0,001 | 0,0004 | 0,04 | 0,4 | 3 |
| Alcool de diacétone | 0 | 0,04 | 3 | 4 | 4 | 3 | 2 | 2 |
| Diacétyle | 0 | 996 | 1 625 | 1 118 | 671 | 370 | 281 | 445 |
| 2,3-PD | 0 | 6,5 | 22 | 22 | 20 | 16 | 40 | 208 |
| Acétoïne | 0 | 173 | 346 | 369 | 293 | 189 | 161 | 308 |
| 2,4-PD | 0 | 0,04 | 0,1 | 0,1 | 0,08 | 0,04 | 0,03 | 0,02 |
| Oxyde de mésityle | 0 | 0,3 | 1 | 2 | 1 | 0,9 | 0,7 | 0,6 |
a Nous présumons que les nourrissons âgés de 0 à 6 mois sont exclusivement nourris au lait maternel ou aux préparations pour nourrissons.
Annexe D. Paramètres ayant servi à estimer les expositions humaines attribuables à l’utilisation de produits de consommation
Nous avons estimé l’exposition occasionnée par les cosmétiques à l’aide du logiciel ConsExpo Web (2016). Les estimations de l’exposition ont été calculées en fonction des poids corporels suivants : 70,9 kg (20 ans et plus), 59,4 kg (12 à 19 ans), 31 kg (5 à 11 ans), 15,5 kg (6 mois à 4 ans) et 7,5 kg (0 à 6 mois) (Santé Canada, 1998). Les paramètres de l’exposition estimée aux cosmétiques par inhalation et par voie cutanée sont donnés dans le tableau D-1. Seules les absorptions par voie cutanée de l’alcool de diacétone et de la 2,4-PD sont données. Un taux d’inhalation de 16,2 mg/m3 a été utilisé pour calculer la dose interne d’alcool de diacétone dans les produits de bricolage (Santé Canada, 1998). Sauf indication contraire, les valeurs par défaut proviennent de la fiche d’information pertinente de ConsExpo pour le scénario présenté.
| Produit (substance) | Hypothèsesa |
|---|---|
| Couche de finition (que l’on présume appliquée sur les ongles des mains et des pieds) (MEK) | Concentration de MEK : 55,7 % (communication personnelle, courriels de la DSPCPD, SC, au BERSE, SC, datés d’août 2016, d’avril 2017 et de novembre 2019; source non citée) Inhalation – Exposition à la vapeur, modèle d’évaporationDurée de l’exposition : 18 min Quantité de produit : 0,33 g (Ficheux et coll., 2014) Volume de la pièce : 1 m3 (près du visage) Taux de renouvellement d’air : 1 renouvellement/h Coefficient de transfert de masse : 6,401 m/h (méthode de Sparks) Mode de libération dans une superficie : constant Superficie de libération : 26,2 cm2 (d’après les données extraites de Ficheux et coll., 2014 et l’hypothèse selon laquelle les ongles des mains et des pieds sont peints) Matrice de masse moléculaire : 124 g/mol |
| Vernis/adhésif à ongles (deux couches sur les ongles des mains et des pieds) (MEK, MPK, MIBK) | Concentration : MEK = 94,7 %, MPK = 1 % à 3 %, MIBK = 1 % à 3 % (communication personnelle, courriels de la DSPCPD, SC, au BERSE, SC, datés d’août 2016, d’avril 2017 et de novembre 2019; source non citée) Inhalation – Exposition à la vapeur, modèle d’évaporationDurée de l’exposition : 35 min Quantité de produit : 0,8 g pour les adolescents et les adultes de 20 ans et plus, et 0,27 g pour les enfants âgés de 6 mois à 4 ans (Ficheux et coll., 2014) Volume de la pièce : 1 m3 (près du visage) Taux de renouvellement d’air : 1 renouvellement/h Coefficient de transfert de masse : MEK : 6,401 m/h (20 ans et plus), 9,082 m/h (6 mois à 4 ans) (méthode de Sparks); MPK : 10 m/h; MIBK : 10 m/h Mode de libération dans une superficie : constant Superficie de libération : 26,2 cm2 (12 ans et plus), 8,8 cm2 (6 mois à 4 ans) (d’après les données extraites de Ficheux et coll., 2014 et l’hypothèse selon laquelle les ongles des mains et des pieds sont peints) Matrice de masse moléculaire : 124 g/mol |
| Vernis à ongles (deux couches sur les ongles des mains et des pieds) (Alcool de diacétone) | Concentration d’alcool de diacétone : 10 % (communication personnelle, courriels de la DSPCPD, SC, au BERSE, SC, datés d’août 2016, d’avril 2017 et de novembre 2019; source non citée) Inhalation – Exposition à la vapeur, modèle d’évaporation Quantité sur la peau (g/utilisation) : 0,16 (12 ans et plus), 0,06 (6 mois à 4 ans) (Ficheux et coll., 2014) |
| Dissolvant pour vernis à ongles (MEK, MIBK) | Concentration : MEK : 84 % (20 ans et plus), 79,6 % (6 mois à 4 ans); MIBK : 10 % à 30 % (communication personnelle, courriels de la DSPCPD, SC, au BERSE, SC, datés d’août 2016, d’avril 2017 et de novembre 2019; source non citée) Inhalation – Exposition à la vapeur, modèle d’évaporationDurée de l’exposition : 8 min Quantité de produit : 5,36 g (12 ans et plus), 1,82 g (6 mois à 4 ans) Volume de la pièce : 1 m3 (près du visage) Taux de renouvellement d’air : 1 renouvellement/h Coefficient de transfert de masse : MEK : 5,080 m/h (20 ans et plus), 7,209 m/h (6 mois à 4 ans) (méthode de Sparks); MIBK : 10 m/h (valeur par défaut dans ConsExpo) Mode de libération dans une superficie : constant Superficie de libération : 34 cm2 (12 ans et plus), 25 cm2 (6 mois à 4 ans) (d’après les données extraites de Ficheux et coll., 2014 et l’hypothèse selon laquelle les ongles des mains et des pieds sont peints) Matrice de masse moléculaire : 75 g/mol |
| Hydratant pour le visage (diacétyle) | Concentration : diacétyle : 0,1 % (communication personnelle, courriel de la DSPCPD, SC, au BERSE, SC, daté d’avril 2020; source non citée) Inhalation – Exposition à la vapeur, modèle d’évaporation (RIVM)Fréquence : 2/j (20 ans et plus), 1/j (5 à 11 ans) Durée de l’exposition : 12 h (20 ans et plus), 24 h (5 à 11 ans) Quantité de produit : 1,5 g (20 ans et plus), 1,1 g (5 à 11 ans) Matrice de masse moléculaire : 1000 g/mol Volume de la pièce : 20 m3 Taux de renouvellement d’air : 0,6 renouvellement/h Coefficient de transfert de masse : 10 m/h Mode de libération dans une superficie : constant Superficie de libération : 638 cm2 (20 ans et plus), 605 cm2 (5 à 11 ans) Durée de l’émission : 12 h (20 ans et plus), 24 h (5 à 11 ans) |
| Hydratant pour le corps (diacétyle) | Concentration : diacétyle : 0,04 % à 0,1 % (comme il n’y avait aucune donnée disponible sur les hydratants pour le corps, nous avons présumé que le diacétyle est présent aux mêmes concentrations que dans les hydratants pour le visage) Inhalation – Exposition à la vapeur, modèle d’évaporationFréquence : 1 Durée de l’exposition : 20 min (temps dans la salle de bain) Quantité de produit : 10 g (12 ans et plus) (Ficheux et coll., 2016) Matrice de masse moléculaire : 1000 g/mol Volume de la pièce : 10 m3 Taux de renouvellement d’air : 2 renouvellements/h Coefficient de transfert de masse : 10 m/h Mode de libération dans une superficie : constant Superficie de libération : 17 530 cm2 (20 ans et plus) Durée de l’émission : 20 min |
| Alcool à friction (MIBK) | Concentration de MIBK : 0,98 % (communication personnelle, courriel du DPSNSO, SC, au BERSE, SC, daté du 16 août 2016; source non citée) Comme aucun scénario n’a été recensé dans ConsExpo, on s’en est remis au jugement professionnel. Inhalation – Exposition à la vapeur, modèle de libération instantanée Superficie : superficie présumée de 5 cm × 5 cm = couverture de 25 cm2 Quantité sur la peau (g/utilisation) : la quantité de désinfectant pour les mains de 0,7 g (Santé Canada, 2015c) pour une superficie de 910 cm2 est corrigée pour une superficie de 25 cm2 = 0,02 g |
| Tatouages temporaires (MIBK) | Concentration de MIBK : 1 % à 3 % (communication personnelle, courriel de la DSPCPD, SC, au BERSE, SC, daté de novembre 2019; source non citée) Inhalation – Exposition à la vapeur, libération instantanéeDurée de l’exposition : 5 min Quantité de produit : 0,0036 g (jugement professionnel d’après Scott et Moore, 2000, et communication personnelle, courriel de la DSPCPD, SC, au BERSE, SC, daté de décembre 2019; source non citée) Volume de la pièce : 1 m3 Taux de renouvellement d’air : 1 renouvellement/h |
| Traceurs d’yeux autocollants (Alcool de diacétone) | Concentration d’alcool de diacétone : 30 % (communication personnelle, courriels de la DSPCPD, SC, au BERSE, SC, datés d’août 2016, d’avril 2017 et de novembre 2019; source non citée) Voie cutanée : Quantité de produit (g/utilisation) : 27 mg (95e centile d’après Ficheux et coll., 2016) Durée de l’exposition : 12 h Quantité de produit : 27 mg/utilisation (Loretz et coll., 2005) Volume de la pièce : 1 m3 (près du visage) Coefficient de transfert de masse : 6,844 m/h (méthode de Sparks) Mode de libération dans une superficie : constant Superficie de libération : 5 cm2 (jugement professionnel) Taux de renouvellement d’air : 1 renouvellement/h Matrice de masse moléculaire : 124 g/mol |
a Sauf indication contraire, un facteur de rétention de 1 a été utilisé.
| Produit (substance) | Hypothèsesa |
|---|---|
| Suce et/ou jouet de dentition | Concentration résiduelle de MEK : 500 ug/g (WSDE, 2020) Voie orale : Ejouet = qproduit × ftemps × fsurface / p.c. où : Ejouet = exposition venant du jouet de dentition (µg/kg p.c./j) Suce : qproduit = quantité de substance lixiviée du produit en 24 h (µg) = 22 500 µg (500 ug/g × 45 g)b ftemps = fraction de la journée que le produit passe dans la bouche (temps de succion) = 0,2 (nourrissons) et 0,32 (tout-petits) (Juberg et coll., 2001, cité dans EFSA, 2015)fsurface = fraction de la surface du produit qui est portée à la bouche = 0,5 (Lassen et coll., 2011, cité dans EFSA, 2015) Jouet de dentition : qproduit = quantité de substance lixiviée du produit en 24 h (µg) = 68 000 µg (500 ug/g × 136 g)b ftemps = fraction de la journée que le produit passe dans la bouche (temps de succion) = 0,02 (Juberg et coll., 2001, cité dans EFSA, 2015) à 0,05 (Van Engelen et coll., 2008) (nourrissons et tout-petits) fsurface = fraction de la surface du produit qui est portée à la bouche = 0,5 (RIVM, 2002) |
a Approche de l’EFSA (2015), poids corporels de 7,5 kg et de 15,5 kg pour les nourrissons (0 à 6 mois) et les tout-petits (6 mois à 4 ans), respectivement (Santé Canada, 1998).
b On présume que toute la MEK (500 ug/g) pourrait être libérée. On a trouvé le poids de la suce et du jouet de dentition en examinant le poids des produits sur les étiquettes de fabrication des produits.
Autres produits
Des scénarios d’exposition sentinelle ont servi à estimer l’exposition potentielle aux substances du groupe des cétones. Les expositions ont été estimées en fonction du poids hypothétique de 70,9 kg pour un adulte (Santé Canada, 1998) et des comportements d’utilisation d’un adulte (âgé de 20 ans ou plus). Les expositions ont été estimées au moyen du logiciel ConsExpo Web (2016) ou d’algorithmes (voir ci-dessous pour plus de détails). Le tableau D-3 présente les hypothèses sous-tendant les différents scénarios. Le modèle PARAMs (US EPA, 2005) a servi à estimer les coefficients de transfert de masse (méthode de Sparks). Se reporter au tableau D-4 pour connaître les valeurs par défaut utilisées dans le modèle PARAMs.
| Scénario d’exposition | Hypothèses |
|---|---|
| Décapant pour peinture ou revêtement (par exemple, décapant pour laque) (MEK) | Concentration de MEK : 20 % à 40 % (FDS, 2018a) Scénario : décapant pour peinture dans la fiche d’information sur les produits de bricolage (RIVM, 2007a). Nous présumons que le travail sera fait dans un garage. Inhalation – Exposition à la vapeur, modèle d’évaporationDurée d’application : 60 min Durée de l’exposition : 60 min Quantité de produit : 1 000 g Volume de la pièce : 34 m3 (garage) Taux de renouvellement d’air : 1,5 renouvellement/h Coefficient de transfert de masse : 2,758 m/h (méthode de Sparks) Mode de libération dans une superficie : croissant Superficie de libération : 2 m2 Matrice de masse moléculaire : 3000 g/mol |
| Dissolvant d’adhésif, dégraissant (MEK) | Concentration de MEK : 100 % (FDS, 2019a) Scénario : dissolvant d’adhésif utilisé dans la maison, d’après la fiche d’information sur les produits de bricolage (RIVM, 2007a) et les valeurs par défaut de l’EPA des États-Unis (US EPA, 2011) Inhalation – Exposition à la vapeur, modèle d’évaporationDurée de l’exposition : 215 min (durée de l’application + durée d’exposition après la durée d’utilisation d’environ 94 min, d’après US EPA, 2011) Durée d’application : 121 min (valeur moyenne pour les dissolvants d’adhésif, d’après US EPA, 2011) Quantité de produit : 200 g [d’après la quantité moyenne de produit utilisée par année, 34,46 oz/a (env. 1019 ml/a) × masse volumique de la MEK (0,8 g/ml), divisé par le nombre moyen d’utilisations par année (4,22) = 193 g] (US EPA, 2011) Volume de la pièce : 20 m3 Taux de renouvellement d’air : 0,6 renouvellement/h Coefficient de transfert de masse : 3,743 m/h (méthode de Sparks) Mode de libération dans une superficie : croissant Superficie de libération : 5 m2 Matrice de masse moléculaire : 3000 g/mol |
| Diluant à peinture ou à revêtement (pour diluer la laque ou un autre revêtement) (MEK) | Concentration : MEK = 100 % (dilué à 3 % dans le produit) (FDS, 2019a) Scénario : revêtement pour usage général (plancher) dans la fiche d’information sur les produits de bricolage (RIVM, 2007a). On présume que le travail est fait dans un garage. La concentration finale de MEK dans le produit se fonde sur les renseignements du produit, selon lesquels les laques devraient être diluées avec de la MEK pure à 4 oz par gallon tout au plus (3 %). Durée de l’exposition : 60 min Quantité de produit : 3000 g Volume de la pièce : 34 m3 Taux de renouvellement d’air : 1,5 renouvellement/h Coefficient de transfert de masse : MEK = 2,595 m/h (méthode de Sparks) Mode de libération dans une superficie : croissant Superficie de libération : 15 m2 Matrice de masse moléculaire : 3000 g/mol |
| Peinture liquide (peinture riche en solvant pour plate-forme de camion) (MEK, MIBK) | Concentration : MEK = 10 % à 20 % (FDS, 2021), MIBK = 10 % à 15 % (FDS, 2021) Scénario : peinture pour pinceau ou rouleau riche en solvant (peinture pour plate-forme de camion) dans la fiche d’information sur les peintures (RIVM, 2007b). On présume que le travail est fait dans un garage. Inhalation – Exposition à la vapeur, modèle d’évaporationDurée de l’exposition : 132 min Quantité de produit : 420 g (quantité de produit corrigée d’après la superficie couverte, de 1000 g pour 12–15 m2 à 420 g pour 5 m2) Volume de la pièce : 90 m3 (garage; un garage plus grand serait nécessaire si l’on peignait un camion) (US EPA, 2019) Taux de renouvellement d’air : 1,5 renouvellement/h Coefficient de transfert de masse : MEK = 2,595 m/h, MIBK = 2,115 m/h (méthode de Sparks) Mode de libération dans une superficie : croissant Superficie de libération : 5 m2 Durée d’application : 120 min Matrice de masse moléculaire : 300 g/mol |
| Peinture liquide pour l’acier (peinture à haut extrait sec) (MEK) | Concentration de MPK : 1 % à 10 % (ECCC, 2017b) Scénario : peinture pour pinceau ou rouleau à haut extrait sec dans la fiche d’information sur les peintures (RIVM, 2007). On présume que le travail est fait dans un garage. Inhalation – Exposition à la vapeur, modèle d’évaporationDurée de l’exposition : 132 min Quantité de produit : 1 300 g Volume de la pièce : 34 m3 (garage) Taux de renouvellement d’air : 1,5 renouvellement/h Coefficient de transfert de masse : 10 m/h Mode de libération dans une superficie : croissant Superficie de libération : 10 m2 Durée d’application : 120 min Matrice de masse moléculaire : 550 g/mol |
| Produits en aérosol (par exemple, peinture en aérosol) (MEK, MIBK, alcool de diacétone) | Concentration : MEK = 1 % à 75 % (FDS, 2016a, 2019b), MIBK = 0,4 % à 25 % (FDS, 2017a, 2020), alcool de diacétone = 1 % à 5 % (FDS, 2012a) Scénario : bombe aérosol dans la fiche d’information sur les peintures (RIVM, 2007b), mais on a utilisé l’exposition à la vapeur – modèle d’évaporation puisque les substances sont volatiles. On présume que le travail est fait dans un garage. Certaines bombes aérosol pèsent environ 400 grammes : la quantité de produit est donc corrigée à 400 g et les durées d’application et d’exposition, prolongées de 5 minutes chacune. Inhalation – Exposition à la vapeur, modèle d’évaporation Charge : taux constant Taux de contact : 100 mg/min Durée de libération : 20 min Fraction absorbée : 6 % |
| Apprêt/ciment pour PVC (MEK) | Modèle : Exposition à la vapeur – évaporation de ConsExpo, avec les valeurs par défaut du scénario de colle universelle à bois en bouteille, lorsque pertinent (RIVM, 2007a) Concentration de MEK :
Durée totale d’exposition : 240 min (RIVM, 2007a) Volume de la pièce : 20 m3 (RIVM, 2007a) Taux de renouvellement d’air : 0,6 renouvellement/h (RIVM, 2007a) Matrice de masse moléculaire : 3000 g/mol (RIVM, 2007a) Quantité de produit pour :
Durée d’émission pour :
Superficie de libération :
|
| Adhésif multi-usage (MEK) | Concentration de MEK : 3 % à 100 % (FDS, 2019c, 2014a) Scénario : colle en tube (colle de contact) dans la fiche d’information sur les produits de bricolage (RIVM, 2007a) Inhalation – Exposition à la vapeur, modèle d’évaporationDurée de l’exposition : 80 min (d’après la durée d’exposition moyenne en minutes après la durée d’utilisation d’environ 70 min, d’après US EPA, 2011) Quantité de produit : 9 g Volume de la pièce : 20 m3 Taux de renouvellement d’air : 0,6 renouvellement/h Mode de libération dans une superficie : croissant Superficie de libération : 200 cm2 Durée d’application : 10 min Matrice de masse moléculaire : 3000 g/mol Coefficient de transfert de masse : MEK = 8,064 m/h (méthode de Sparks) |
| Produit hydrofuge/hydroprotecteur (par exemple, nettoyant/protecteur pour pare-brise en aérosol) (MEK) | Concentration de MEK = 10 % à 25 % (FDS, 2016b) Scénario : nettoyant pour vitres en aérosol dans la fiche d’information sur les produits nettoyants (RIVM, 2007a) Inhalation – Exposition à la vapeur, modèle de libération instantanéeDurée de l’exposition : 60 min (d’après la fiche technique du produit) Masse libérée : 29 g (on suppose que la masse libérée serait semblable à celle du nettoyant pour vitres en aérosol, étant donné qu’il faut appliquer 2 fois le protecteur pour pare-brise en aérosol) Volume de la pièce : 34 m3 (garage) Taux de renouvellement d’air : 1,5 renouvellement/h Taux d’inhalation : 15,1 m3/j |
| Laque pour bois (MIBK) | Concentration : MIBK = 2,5 % à 10 % (FDS, 2016c) Scénario : revêtement pour usage général sur un plancher (dans un garage) dans la fiche d’information sur les produits de bricolage (RIVM, 2007a) Inhalation – Exposition à la vapeur, modèle d’évaporationDurée de l’exposition : 60 min Quantité de produit : 3000 g Volume de la pièce : 34 m3 Taux de renouvellement d’air : 1,5 renouvellement/h Mode de libération dans une superficie : croissant Superficie de libération : 15 m2 Durée d’application : 60 min Matrice de masse moléculaire : 3000 g/mol Coefficient de transfert de masse : MIBK = 2,115 m/h (méthode de Sparks) |
| Bouche-pores/mastic en tube (automobile) (MIBK) | Concentration de MIBK : 1 % à 5 % (FDS, 2018c) Modèle : bouche-pores/mastic en tube (dans un garage) dans la fiche d’information sur les produits de bricolage (RIVM, 2007a). On présume que le travail est fait dans un garage. Inhalation – Exposition à la vapeur, modèle d’évaporationDurée de l’exposition : 60 min Quantité de produit : 100 g (corrigée à partir de 40 g en fonction de la taille du produit et d’autres renseignements, comme la masse médiane, d’après US EPA, 2019) Volume de la pièce : 34 m3 (garage) Taux de renouvellement d’air : 1,5 renouvellement/h Mode de libération dans une superficie : croissant Superficie de libération : 200 cm2 Durée d’application : 60 min Matrice de masse moléculaire : 3000 g/mol Coefficient de transfert de masse : MIBK = 8,28 m/h (méthode de Sparks) |
| Stylo de réparation de revêtement automobile | Concentration de MIAK : 3 % à 7 % dans un stylo de réparation de revêtement automobile (FDS, 2015c) Inhalation – Exposition à la vapeur, modèle d’évaporationDurée de l’exposition : 30 min Quantité de produit : 8,5 g (10 ml × 0,85; FDS, 2015c) Volume de la pièce : 34 m3 (garage) Taux de renouvellement d’air : 1,5 renouvellement/h Mode de libération dans une superficie : croissant Superficie de libération : 450 cm2 Durée d’application : 30 min (jugement professionnel) Matrice de masse moléculaire : 300 g/mol Coefficient de transfert de masse : 10 m/h (valeur par défaut dans ConsExpo) |
| Nettoyant à volet de départ automobile (MEK, alcool de diacétone) | Concentration : MEK = 1 % à 5 % (FDS, 2019d), alcool de diacétone = 1 % à 30 % (FDS, 2011, 2012b) Scénario : peinture en aérosol (dans un garage) dans la fiche d’information sur les peintures (RIVM, 2007b). On présume que le travail est fait dans un garage. Inhalation – Exposition à la vapeur, modèle d’évaporation Charge : taux constant Taux de contact : 100 mg/min Durée de libération : 15 min Fraction absorbée : 6 % |
| Scellant pour filetage de tuyau (alcool de diacétone) | Concentration : 20 % à 30 % (FDS, 2013) Scénario : colle universelle à bois dans la fiche d’information sur les produits de bricolage (RIVM, 2007a) Inhalation – Exposition à la vapeur, modèle d’évaporation Charge : application instantanée Quantité de produit : 0,08 g Fraction absorbée : 6 % |
| Décapant à peinture ou à marqueur en aérosol (alcool de diacétone) | Concentration d’alcool de diacétone : 7 % (FDS, 2018d) Modèle : peinture en aérosol (dans une pièce indéterminée) dans la fiche d’information sur les peintures (RIVM, 2007b). Inhalation – Exposition à la vapeur, modèle d’évaporation Charge : taux constant Taux de contact : 100 mg/min Durée de libération : 15 min Modèle d’absorption – fraction fixe Fraction absorbée : 6 % |
| Diluant à peinture (pour les peintures époxy) (Alcool de diacétone) | Concentration : alcool de diacétone = 5 % à 10 % (FDS, 2017b) Scénario : diluant pour époxy, afin de nettoyer les brosses ou les surfaces. On présume que le scénario pourrait se produire lorsque de l’époxy est utilisé dans la maison (pièce non précisée). Inhalation – Exposition à la vapeur, modèle d’évaporation Quantité de produit sur la peau : 2,07 g (Versar, 1986) |
| Marqueurs (MIBK, alcool de diacétone) | Concentration : MIBK = 10 % à 30 % dans les marqueurs à essuyage à sec (FDS, 2015b), alcool de diacétone = 60 % à 100 % dans les marqueurs permanents (FDS, 2008, 2012c, 2014b) Scénario : marqueurs (à essuyage à sec ou permanents) Inhalation : scénario dans la fiche d’information sur les produits pour enfants (RIVM, 2002) – pour la MIBK seulement Voie cutanée ou orale (scénario relatif à l’encre tiré de l’approche de l’Arts & Creative Materials Institute [ACMI]; communication personnelle de l’ACMI au BERSE, SC, 2009; source non citée) Scénario d’exposition aiguë ou par événement Absorption (mg/kg p.c./événement = [concentration de la substance dans le marqueur (p/p) × quantité estimée d’encre par exposition (50 mg) × fraction absorbée] / poids corporel (kg) Quantité d’encre par exposition = 50 mg (Hansel et coll., 2008) Scénario d’exposition chronique Absorption (mg/kg p.c./j) : [Concentration de la substance dans le marqueur (p/p) × taux de dépôt d’encre (µg/cm) × ligne d’encre de 25 cm/j)/1000 µg/mg] / poids corporel (kg) Taux de dépôt d’encre = 100 µg/cm (90e centile du dépôt d’encre pour les instruments d’écriture) (communication personnelle, du Duke Medical Centre au BERSE, SC, 2009; source non citée) |
| Huile essentielle comme assainisseur d’air (inhalation) (2,3-PD) | Concentration de 2,3-PD : 0,1 % à 1 % (FDS, 2019f) Scénario : huile essentielle comme assainisseur d’air (dans un salon) dans la fiche d’information sur les cosmétiques (RIVM, 2006) Modèle : Inhalation – Exposition à la vapeur, taux constantDurée de l’exposition : 240 min Quantité de produit : 1,08 g Volume de la pièce : 58 m3 Taux de renouvellement d’air : 0,5 renouvellement/h Durée de l’émission : 180 min |
| Assainisseur d’air à brancher (inhalation) (2,3-PD) | Concentration de 2,3-PD : 0,1 % à 1 % (FDS, 2015d) Scénario : assainisseur d’air à brancher Inhalation – Exposition à la vapeur, scénario de libération instantanée Fréquence : à longueur de journée, tous les joursDurée de l’exposition : 24 h/j Quantité de produit : une unité à brancher contient environ 26 ml de produit et peut durer jusqu’à 30 jours (P&G, c2017a). On présume que la quantité émise est la même chaque jour (26 ml/30 j = environ 0,9 ml ou 0,9 g/j) Volume de la pièce : 20 m3 Taux de renouvellement d’air : 0,6 renouvellement/h |
| Assainisseur d’air en gel (inhalation) (2,3-PD) | Concentration de 2,3-PD : 1 % à 5 % (FDS, 2015e) Scénario : assainisseur d’air en gel Inhalation – Exposition à la vapeur, scénario de libération instantanée Fréquence : à longueur de journée, tous les joursDurée de l’exposition : 24 h/j Quantité de produit : une unité en gel contient environ 5,5 ml de produit et peut durer jusqu’à 30 jours (P&G, c2017b). On présume que la quantité émise est la même chaque jour (5,5 ml/30 j = environ 0,2 ml ou 0,2 g/j) Volume de la pièce : 20 m3 Taux de renouvellement d’air : 0,6 renouvellement/h |
| Paramètre | Valeur | Renseignements supplémentaires |
|---|---|---|
| Masse volumique de l’air (g/cm3) | 0,0011774 | À 25 °C, une pression atmosphérique de 760 mmHg et une humidité relative de 50 % |
| Viscosité de l’air (g/cm/s) | 1,86 × 10-4 | À 25 °C |
| Vitesse de l’air (cm/s) | 10 | (Sparks et coll., 1996; McGready et Fontaine, 2010) |
| Coefficient de diffusion dans l’air (cm2/s) | MEK : 9,19 × 10-2 MPK : 8,22 × 10-2 MIBK : 7,49 × 10-2 MIAK : 6,92 × 10-2 Alcool de diacétone : 7,24 x 10-2 Diacétyle : 8,91 × 10-2 2,3-PD : 8,02 × 10-2 2,4-PD : 8,02 × 10-2 |
À 25 °C |
| Longueur de surface dans divers scénarios | Vernis à ongles : 20 cm (20 ans et plus), 7 cm (6 mois à 4 ans) Dissolvant pour vernis à ongles : 40 cm (20 ans et plus), 14 cm (6 mois à 4 ans) Décapant pour peinture ou revêtement (par exemple, décapant pour laque) : 2,5 m Dissolvant d’adhésif, dégraissant : 1 à 5 m Diluant à peinture ou à revêtement : 3 à 5 m Peinture pour plate-forme de camion : 3 à 5 m Peinture en aérosol : 1 à 2 m Adhésif multi-usage : 10 à 20 cm Produit de finition du bois (plancher) : 3 à 5 m Marqueurs : 25 cm Dissolvant pour graffiti (en aérosol) : 1 à 2 m Traceurs d’yeux autocollants : 8 cm Revêtement pour usage général : 3 à 5 m Bouche-pores/mastic : 2 à 5 cm |
Valeurs estimées en tenant compte de la superficie de libération indiquée dans les fiches d’information de ConsExpo pour chaque scénario particulier (lorsque le scénario ne figurait pas dans ConsExpo, on s’en est remis au jugement professionnel) |
Annexe E. Exposition humaine par inhalation au diacétyle contenu dans le maïs à éclater au micro-ondes
L’approche employée dans Zhu et coll. (2001) et l’évaluation de la Liste des substances d’intérêt prioritaire pour le 2-butoxyéthanol (Environnement Canada, Santé Canada, 2002) a été utilisée pour convertir les données de Rosati et coll. (2007) sur les émissions de diacétyle provenant d’un sac de maïs à éclater au micro-ondes d’après des études en chambre à une certaine concentration dans l’air dans une pièce standard. Des détails sur les hypothèses avancées figurent ci-dessous.
On a supposé que les émissions de diacétyle provenant du maïs à éclater au micro-ondes suivaient une dégradation de premier ordre et qu’il n’y avait pas d’effet de puits dans la chambre. Étant donné ces hypothèses, la concentration de la substance dans une chambre d’émission (ou une pièce) est liée au coefficient d’émission comme suit :
Équation 1 : C = [(CE0 × S) / (V × (N - k))] × [exp(-kt) - exp(-Nt)]
où :
C = concentration de diacétyle dans la chambre à tout moment [mg/m3]
CE0 = coefficient d’émission initial pour le diacétyle contenu dans l’échantillon de produit [mg/m2/h]
S = superficie émettrice de l’échantillon de produit [m2]
N = nombre de renouvellements d’air à l’heure dans la chambre [h-1]
V = volume de la chambre [m3]
t = durée d’émission [h]
k = constante de dégradation des émissions [h-1]
Pour une source d’émissions quasi constante ou qui s’épuise lentement, la valeur k (constante de dégradation) avoisine zéro. Lorsque t (période d’essai) devient infini ou qu’un état d’équilibre est atteint, l’équation 1 peut être reformulée comme suit :
Équation 2 : C = (CE0 × S) / (V × N)
On a présumé qu’un état d’équilibre avait été atteint lors des essais sur les produits. Pour le calcul des coefficients d’émission initiaux, nous avons remanié l’équation 2 comme suit :
Équation 3 : CE0 = (C × N × V) / S [mg/m2/h] = [mg/m3] [h-1][m3] / [m2]
où N est le nombre de renouvellements d’air à l’heure dans la chambre, V est le volume de la cellule et S est la superficie émettrice, et où la concentration moyenne de diacétyle émise par le sac de maïs à éclater au micro-ondes de 778,9 µg/sac (Rosati et coll., 2007).
Étape 1 : Calculer le coefficient d’émission initial à l’aide de l’équation 3 (données extraites de Rosati et coll., 2007).
| Plage de concentrations (mg/m3) | N = renouvellements d’air à l’heure (h-1) | V = volume de la chambre (m3) | S = superficie émettricea (m2) | CE0 (mg/m2/h) |
|---|---|---|---|---|
| 5,8 | 2,3 | 0,515 | 0,1 | 68,70 |
| 0,02 | 2,3 | 0,515 | 0,1 | 0,237 |
a Nous présumons que la superficie émettrice correspond à celle d’un sac de maïs, soit 1000 cm2 (Borkowski, 2007).
Étape 2 : Calculer la constante de dégradation des émissions selon la formule k = CE0 × S/M, où M est la quantité évaporable totale de la substance dans la source (M = quantité moyenne émise par un sac de maïs à éclater au micro-ondes, soit 0,779 mg).
| CE0 (mg/m2/h) | S (m2) | M (mg) | k (h-1) |
|---|---|---|---|
| 68,7 | 0,1 | 0,779 | 8,82 |
| 0,237 | 0,1 | 0,779 | 0,03 |
Étape 3 : Calculer la concentration dans une pièce standard selon l’équation 1.
| CE0 (mg/m2/h) | S (m2) | V (m3) | N (h-1) | k (h-1) | t (h) | Concentration (mg/m3) |
|---|---|---|---|---|---|---|
| 68,7 | 0,1 | 17,4 | 0,5 | 8,82 | 1 | 0,0288 |
| 0,237 | 0,1 | 17,4 | 0,5 | 8,82 | 1 | 0,0001 |
Pour 5,8 mg/m3 de diacétyle :
| Temps (minutes) | Concentration (mg/m3) |
|---|---|
| 0 | 0 |
| 10 | 0,0328 |
| 20 | 0,0377 |
| 30 | 0,0364 |
| 40 | 0,0339 |
| 50 | 0,0313 |
| 60 | 0,0288 |
| 120 | 0,0175 |
| 180 | 0,0106 |
| 240 | 0,0064 |
| 300 | 0,0039 |
| 360 | 0,0024 |
| Moyenne après 6 heures | 0,02 |
Pour 0,02 mg/m3 de diacétyle :
| Temps (minutes) | Concentration (mg/m3) |
|---|---|
| 0 | 0 |
| 10 | 0,00011 |
| 20 | 0,00013 |
| 30 | 0,00013 |
| 40 | 0,00012 |
| 50 | 0,00011 |
| 60 | 0,00010 |
| 120 | 0,00006 |
| 180 | 0,00004 |
| 240 | 0,00002 |
| 300 | 0,00001 |
| 360 | 0,00001 |
| Moyenne après 6 heures | 0,00007 |
Annexe F. Paramètres utilisés pour l’extrapolation d’une voie à l’autre
| Substance | Paramètres de l’étude | Dose originale | Dose convertie | Formule |
|---|---|---|---|---|
| MIBK | 2 ans; 6 h/j; 5 j/sem | 1843 mg/m3 | 101 mg/kg p.c./j | 1843 × 0,31a × (6 h/24 h)b × (5 j/7 j)c |
| MIAK | 69 expositions échelonnées sur 96 jours civils; 6 h/j; | 934 mg/m3 | 52 mg/kg p.c./j | 934 × 0,31a × (6 h/24 h)b × (69 j/96 j)d |
| 2,3-PD | Lecture croisée à partir d’une étude de 90 j sur le diacétyle | 90 mg/kg p.c./j | 105 mg/kg p.c./j | 90 × (100,12 / 86,09)e |
| 2,3-PD | 14 sem; 6 h/j; 5 j/sem | 51 mg/m3 | 12 mg/kg p.c./j | 51 × 1,33f × (6 h/24 h)b × (5 j/7 j)c |
| 2,3-PD | 14 sem; 6 h/j; 5 j/sem | 102 mg/m3 | 24 mg/kg p.c./j | 102 × 1,33f × (6 h/24 h)b × (5 j/7 j)c |
| 2,4-PD | 6 h/j;JG6–15 | 827 mg/m3 | 64 mg/kg p.c./j | 827 × 0,31a × (6 h/24 h)b |
| 2,4-PD | 6 h/j; 5 j/sem; 14 sem | 417 mg/m3 | 23 mg/kg p.c./j | 417 × 0,31a × (6 h/24 h)b × (5 j/7 j)c |
| Oxyde de mésityle | 6 sem; 8 h/j; 5 j/sem | 200 mg/m3 | 15 mg/kg p.c./j | 200 × 0,31a × (8 h/24 h)b × (5 j/7 j)c |
a Compte tenu d’un poids corporel standard pour le rat de 0,35 kg et d’un volume d’inhalation de 0,11 m3/j, ce qui donne une constante de 0,31 m3/j kg (d’après Santé Canada,1994).
b Durée d’exposition dans une journée
c Durée de l’étude
d Nombre d’expositions
e Masse moléculaire (substance/analogue)
f Compte tenu d’un poids corporel standard pour la souris de 0,03 kg et d’un volume d’inhalation de 0,04 m3/j, ce qui donne une constante de 1,33 m3/j kg (d’après Santé Canada,1994).
