Chapitre 15 des Normes canadiennes pour la lutte
antituberculeuse : Le suivi du rendement de programme de lutte antituberculeuse
Sur cette page
- Auteurs et affiliations
- Points clés
- Introduction
- État de la situation
- Conception et limites d'un cadre de suivi du rendement
- Indicateurs clés du rendement du programme
- Stratégies analytiques et d'action
- Résumé
- Énoncé de divulgation
- Financement
- Annexe 1 : Suivi du rendement du programme de lutte antituberculeuse
- Références
Auteurs et affiliation
Courtney Heffernan; Tuberculosis Program Evaluation and Research Unit, Département de médecine, Faculté de médecine et de soins dentaires, Université de l'Alberta, Edmonton, Alberta, Canada
Margaret Haworth-Brockman; Centre de collaboration nationale des maladies infectieuses, Rady Faculty of Health Sciences, Université du Manitoba, Winnipeg, Manitoba, Canada
Pierre Plourde; Max Rady College of Medicine, Rady Faculty of Health Sciences, Université du Manitoba; Winnipeg Regional Health Authority, Winnipeg, Manitoba, Canada
Tom Wong; Bureau de la santé publique et de la population, Services aux Autochtones Canada; Centre de la lutte contre les maladies transmissibles et les infections, Agence de la santé publique du Canada, Ottawa, Ontario, Canada
Giovanni Ferrara; Tuberculosis Program Evaluation and Research Unit, Département de médecine, Faculté de médecine et de soins dentaires, Université de l'Alberta, Edmonton, Alberta, Canada
Richard Long; Tuberculosis Program Evaluation and Research Unit, Département de médecine, Faculté de médecine et de soins dentaires, Université de l'Alberta, Edmonton, Alberta, Canada
Points clés
- Le suivi du rendement de programme fournit des données probantes sur la qualité et la valeur des services offerts par les programmes de lutte antituberculeuse.
- Tous les programmes de lutte antituberculeuse au Canada sont encouragés à surveiller les mêmes indicateurs de base de rendement en utilisant les définitions et les cibles proposées fournies dans ce chapitre.
- Ce cadre devrait être considéré comme une norme minimale pour le suivi des programmes canadiens de lutte antituberculeuse; les provinces et les territoires sont également encouragés à surveiller d'autres indicateurs pertinents pour les populations desservies.
- L'évaluation du programme par rapport aux cibles qu'il contient produit des mesures quantitatives de rendement qui sont utiles pour réaffecter les efforts et les ressources.
- Le suivi du rendement de programme devrait se faire annuellement et des résumés devraient être mis à la disposition des intervenants d'autres programmes de lutte antituberculeuse et des autres intervenants pertinents, ainsi que du public.
- Ce suivi exige des ressources humaines adéquates consacrées aux processus de collecte, de validation et d'analyse des données.
- L'interprétation des résultats du suivi doit être effectuée en étroite collaboration avec le médecin ou les responsables des soins infirmiers pour s'assurer que les jugements pertinents sur le plan clinique sont correctement pris en compte.
- La recherche de solutions pour remédier à la sous-performance programmatique doit être collaborative; elle doit inclure les membres des communautés touchées par la tuberculose (TB), certains groupes de la population et les intervenants concernés.
- Les programmes de lutte antituberculeuse devraient évaluer la capacité du personnel à dispenser des soins centrés sur le patient et à influencer de manière favorable les résultats à long terme, ce qui dépend entre autres du soutien spécifique d'un travailleur social.
1. Introduction
Ce nouveau chapitre des Normes canadiennes de lutte antituberculeuse (les Normes) est axé sur le rôle du suivi du rendement des programmes à l'ère de l'élimination de la tuberculose. Le présent chapitre décrit un cadre pour le suivi du rendement de programme qui s'inscrit dans les Normes et vise à mesurer la valeur, la qualité et l'incidence des services inclus dans les programmes de lutte antituberculeuse au Canada.Référence 1Référence 2 En plus du personnel de première ligne de ces programmes, l'auditoire visé par ce chapitre comprend les gestionnaires des programmes de lutte antituberculeuse, les responsables des politiques en matière de santé, de même que les médecins et les responsables des soins infirmiers.
2. État de la situation
En 2014, l'Organisation mondiale de la Santé (OMS) a commencé à promouvoir la nouvelle stratégie Halte à la tuberculose comme approche globale pour éliminer la tuberculose, après l'approbation entière de ses États membres par une résolution de l'Assemblée mondiale de la Santé.Référence 3 Cette stratégie définit trois piliers principaux : la prestation de soins préventifs et de soins de qualité centrés sur le patient (pilier 1); une volonté politique accrue et des ressources soutenues pour une action audacieuse (pilier 2); et la recherche et l'innovation (pilier 3).Référence 4 La mise en œuvre de ces piliers vise à aider à atteindre trois objectifs d'ici 2035 : 1) réduire de 90 % le nombre de nouveaux cas de TB, 2) réduire de 95 % le nombre de décès attribuables à la TB, ces deux derniers par comparaison à 2015; et 3) que les familles touchées par la TB n'engagent pas de frais catastrophiques en raison de la maladie.Référence 4
Pour évaluer les progrès nationaux vers la réalisation de ces objectifs, un suivi systématique du rendement de programme est recommandé dans le cadre de la stratégie Halte à la tuberculose et a été largement adopté à l'échelle internationale.Référence 5Référence 6Référence 7Référence 8Référence 9 Le Canada est signataire de cette stratégie et a donc l'obligation de mettre en œuvre cette recommandation. Le but de ces évaluations est de distinguer les programmes qui font la promotion de la santé et qui préviennent les maladies de ceux qui ne le font pas.Référence 10 À son tour, le suivi génère des renseignements qui peuvent être utilisés pour juger de la qualité et de la valeur des programmes de santé publique, comme les services de lutte contre la TB.Référence 11 Un cadre de suivi du rendement d'un programme bien conçu devrait documenter les progrès vers les objectifs, identifier les domaines à améliorer et démontrer l'incidence des investissements en ressources.Référence 12
Bien que l'importance du suivi du rendement des programmes de lutte antituberculeuse au Canada ait fait l'objet de discussions depuis plus de 20 ans, notamment par Santé Canada, le Réseau pancanadien de santé publique et l'organisme Inuit Tapiriit Kanatami, un cadre national n'a pas encore vu le jour.Référence 13Référence 14Référence 15Référence 16Référence 17 Au cours de la même période, le Canada n'a pas été en mesure de réduire de façon substantielle le nombre de cas; l'incidence annuelle globale de la TB au pays est demeurée stable pendant 16 ans, comme le montre la Figure 1 (voir le Chapitre 1 : L'épidémiologie de la tuberculose au Canada).
Incidence réelle : cas signalés sur le site Maladies à déclaration obligatoire en direct (Agence de la santé publique du Canada)Référence 20 1924 à 2019 au Canada.
Cible de 1997 : réduction annuelle de 5 % des cas.Référence 21
Cible de 2006 : atteindre une incidence de 3,6 en 2015. Une relation linéaire a été tracée et étendue au-delà de l'objectif de 2015.Référence 22
Cible de 2015 : réduire de 90 % les nouveaux cas d'ici 2035 par rapport à 2015.Référence 4 À noter que ces nombres de cas sont pour l'ensemble du Canada et diffèrent pour certaines populations au Canada.
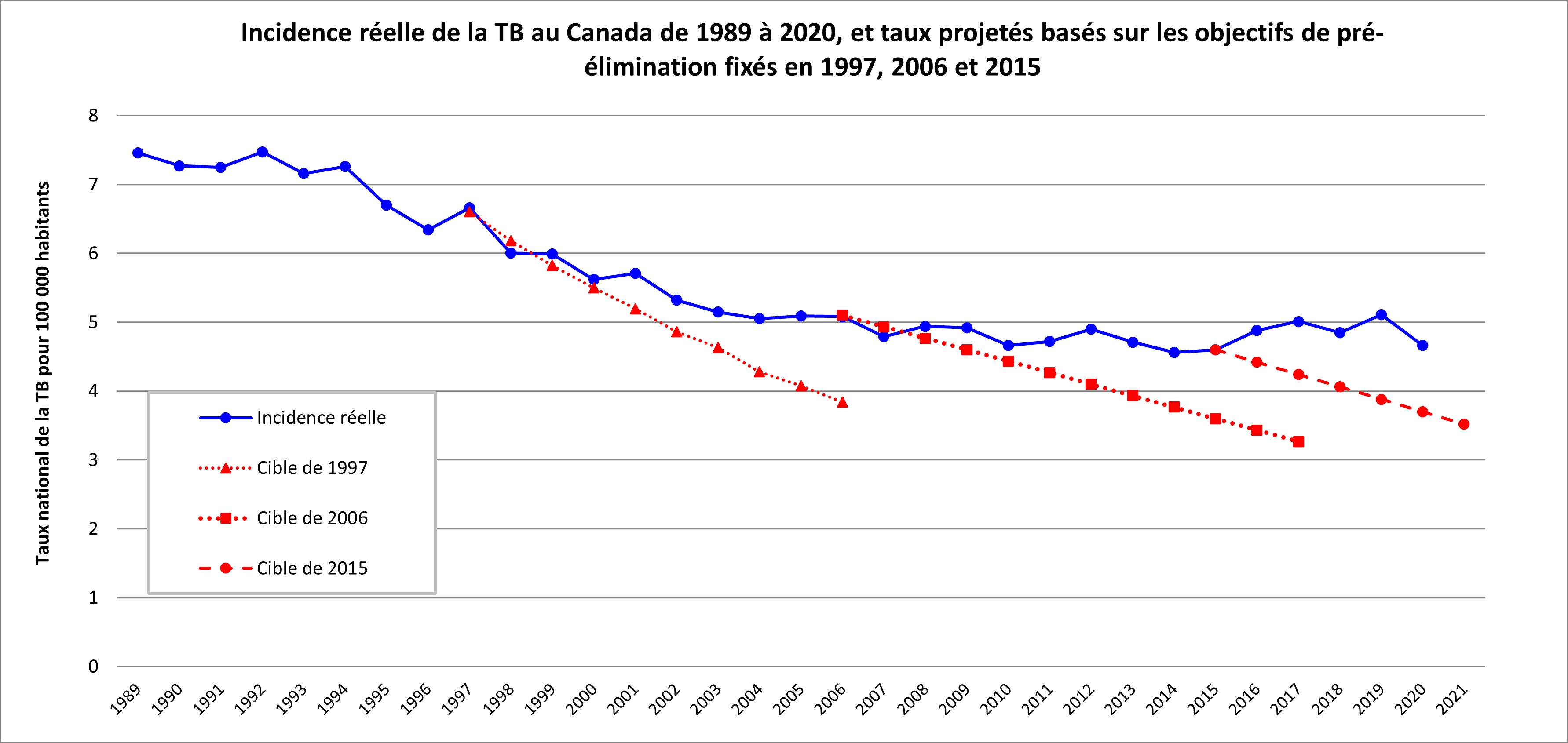
Figure 1 : Texte descriptif
| Ans | Incidence réelle (taux national de la TB pour 100 000 habitants) | Cible de 1997 | Cible de 2006 | Cible de 2015 |
|---|---|---|---|---|
| 1989 | 7,46 | - | - | - |
| 1990 | 7,27 | - | - | - |
| 1991 | 7,25 | - | - | - |
| 1992 | 7,47 | - | - | - |
| 1993 | 7,16 | - | - | - |
| 1994 | 7,26 | - | - | - |
| 1995 | 6,70 | - | - | - |
| 1996 | 6,34 | - | - | - |
| 1997 | 6,66 | 6,60 | - | - |
| 1998 | 6,00 | 6,18 | - | - |
| 1999 | 5,99 | 5,83 | - | - |
| 2000 | 5,62 | 5,50 | - | - |
| 2001 | 5,71 | 5,19 | - | - |
| 2002 | 5,32 | 4,86 | - | - |
| 2003 | 5,15 | 4,63 | - | - |
| 2004 | 5,05 | 4,28 | - | - |
| 2005 | 5,09 | 4,08 | - | - |
| 2006 | 5,08 | 3,84 | 5,10 | - |
| 2007 | 4,79 | - | 4,93 | - |
| 2008 | 4,94 | - | 4,77 | - |
| 2009 | 4,92 | - | 4,60 | - |
| 2010 | 4,66 | - | 4,43 | - |
| 2011 | 4,72 | - | 4,27 | - |
| 2012 | 4,90 | - | 4,10 | - |
| 2013 | 4,71 | - | 3,93 | - |
| 2014 | 4,56 | - | 3,77 | - |
| 2015 | 4,60 | - | 3,60 | 4,60 |
| 2016 | 4,88 | - | 3,43 | 4,42 |
| 2017 | 5,01 | - | 3,27 | 4,24 |
| 2018 | 4,85 | - | - | 4,06 |
| 2019 | 5,11 | - | - | 3,88 |
| 2020 | 4,66 | - | - | 3,70 |
| 2021 | - | - | - | 3,52 |
Entre-temps, des indicateurs de rendement ont été adoptés dans d'autres contextes pour évaluer les services régionaux et nationaux de prévention et de soins contre la TB. Par exemple, une étude menée aux États-Unis a révélé des améliorations marquées des résultats dans les régions sanitaires locales qui faisaient le suivi du rendement en l'évaluant activement par rapport à ceux qui recueillaient passivement des données.Référence 18 En Angleterre, où il existe une norme nationale d'indicateurs de rendement, la recherche a contribué à la formulation de recommandations pour de nouveaux indicateurs en vue d'améliorer la qualité et la valeur globales des services de lutte antituberculeuse dans le contexte de l'élimination de la maladie.Référence 19 En somme, le suivi du rendement des programmes a été fructueux ailleurs, et ce chapitre fournit des recommandations à l'intention des programmes de lutte antituberculeuse au Canada.
3. Conception et limites d'un cadre de suivi du rendement
En 2018, le Centre national de collaboration pour les maladies infectieuses a effectué un examen de la portée en compilant des rapports et des indicateurs de rendement à partir de 25 programmes distincts de lutte antituberculeuse d'autres pays et régions à faible incidence, ainsi que pour trois groupes de population touchés par la TB au Canada : les Premières Nations, les Inuits et les personnes nées à l'étranger. L'analyse de ces documents a permis de dresser une liste de 105 indicateurs de rendement de programme pouvant s'appliquer au Canada. La même année, ces indicateurs ont été abordés lors d'une réunion nationale et classés à l'aide d'une technique Delphi modifiée.Référence 23Référence 24 La réunion s'est conclue par un consensus d'experts sur huit indicateurs clés de rendement de programme de lutte antituberculeuse pertinents pour les populations prioritaires susmentionnées.Référence 17Référence 24
Ces huit indicateurs clés ont été examinés par tous les auteurs de ce chapitre et des ajouts ont été effectués au cours de la discussion pour produire un outil plus généralisable. Le résultat final est un cadre de douze indicateurs (voir le Tableau 1) qui peuvent être consultés pour évaluer les services de lutte antituberculeuse au Canada.
| Numéro d'indicateur | Indicateur clé | Définition | Cible |
|---|---|---|---|
| Objectifs d'élimination | |||
| 1.0 | Taux annuel total (brut) d'incidence de la tuberculose (TB), toutes formes confondue | Le nombre total de personnes déclarées positives à la TB dans la juridiction, exprimé comme taux par 100 000 habitants | Cible de pré-élimination fixée à un taux de cas actifs de 1/100 000 ou, comme ci-dessus, 10/1 000 000 d'habitants d'ici 2035 |
| Cibles pour l'examen des immigrants et des réfugiés | |||
| 2.0 | Des personnes dont l'examen médical aux fins de l'immigration (EMI) a indiqué le besoin d'un suivi, la proportion (%) de celles qui sont évaluées par un clinicien de la TB | Le nombre total de rendez-vous auxquels ont assisté les personnes dont l'EMI a conduit à un aiguillage vers la santé publique pour une surveillance médicale de la TB | ≥90% |
| Cibles pour la gestion et le traitement des cas | |||
| 3.0 | De toutes les personnes ayant une nouvelle infection de TB, vivant une rechute ou recevant un second traitement pour la TB, la proportion (%) de celles dont le statut au virus de l'immunodéficience humaine (VIH) est connu | Le nombre annuel de personnes ayant une TB incidente dont le statut au VIH est connu à la date de début du traitement | ≥95% |
| 3.1 | De toutes les personnes ayant une TB pulmonaire àfrottis positif, la proportion (%) de celles ayant commencé le traitement dans les 72 heures suivant un résultat positif au test d'amplification des acides nucléiques (TAAN) | Le nombre annuel de personnes ayant une TB pulmonaire incidente à frottis positif qui ont commencé un traitement antituberculeux dans les 72 heures suivant un résultat positif au TAAN | ≥95% |
| 3.2 | De toutes les personnes ayant une TB pulmonaire à frottis positif, la proportion (%) de celles ayant commencé un traitement de 4 médicaments antituberculeux ou plus, et auquel elles risquent d'être sensiblesTable 1 note de bas de page a | Le nombre annuel de personnes ayant une TB pulmonaire incidente à frottis positif, sensible à la rifampicine (par TAAN), qui commencent un traitement de 4 médicaments antituberculeux en l'absence de tout facteur de risque de résistance ou d'hépatotoxicité | ≥95% |
| 3.3 | De toutes les personnes ayant une TB pulmonaire confirmée par culture, la proportion (%) de celles dont l'échantillon d'expectorations a été soumis à un frottis/une culture de bacille acido-alcoolo-résistant, et ayant obtenu une radiographie thoracique à la fin de la phase initiale de traitement | Le nombre annuel de personnes ayant une TB pulmonaire confirmée par culture, et dont l'échantillon d'expectorations a été soumis à un frottis et à une culture de bacille acido-alcoolo-résistant, et qui ont obtenu une radiographie thoracique dans les 2 semaines suivant la fin de la phase initiale du traitement | ≥95% |
| 3.4 | De tous les cas actifs ayant commencé le traitement au cours des 12 derniers mois, la proportion (%) de ceux qui ont atteint un succès de traitement (qui ont guéri ou terminé le traitement)b | La proportion de cas déclarés positifs à la TB au cours des 12 mois précédents qui ont été guéris ou ont terminé le traitement | ≥90% |
| 3.5 | Le programme de lutte antituberculeuse est-il soutenu par des travailleurs sociaux pour dispenser des soins centrés sur le patient? | La TB est considérée comme une expression biologique des inégalités sociales, nécessitant donc des solutions qui tiennent compte de facteurs sociaux et structurels* *voir le texte ci-dessous pour plus de détails. |
Yes |
| Cibles pour la gestion des contacts | |||
| 4.0 | De tous les contacts étroits de personnes présentant une TB pulmonaire à frottis positif, la proportion (%) dont le premier contact a eu lieu dans les 3 jours ouvrables après avoir été répertoriés comme contacts | Le nombre de contacts étroits de personnes présentant une TB pulmonaire à frottis positif dont le premier contact a eu lieu dans les 3 jours ouvrables après avoir été répertoriés comme contacts | ≥95% |
| 4.1 | De tous les contacts étroits de personnes présentant une TB pulmonaire à frottis positif, la proportion (%) ayant reçu une évaluation complète | Le nombre de contacts étroits (familiaux et non familiaux) de personnes présentant une TB pulmonaire à frottis positif dont les évaluations sont terminées | ≥95% |
| 4.2 | De tous les contacts étroits de personnes présentant une TB pulmonaire à frottis positif, la proportion (%) de ceux ayant reçu un diagnostic d'infection tuberculeuse latente (ITL) qui ont commencé le traitement | Le nombre de contacts étroits de personnes présentant une TB pulmonaire à frottis positif, ayant reçu un diagnostic d'ITL qui initient un traitement préventif dans les 12 mois suivant le diagnostic du cas source | ≥90% |
| 4.3 | De tous les contacts étroits de personnes présentant une TB pulmonaire à frottis positif, la proportion (%) de ceux ayant reçu un diagnostic d'ITL qui ont terminé le traitement | Le nombre de contacts étroits de personnes présentant une TB pulmonaire à frottis positif qui terminent le traitement préventif antituberculeux après l'avoir commencé |
≥90% |
|
Notes de bas de page :
|
|||
Le cadre qui en résulte comprend des indicateurs (actions) de rendement de programme qui sont largement pragmatiques et jugés conformes aux critères suivants : pertinents, bien définis, fiables, techniquement réalisables, pratiques et ayant un historique d'utilisation ailleurs.Référence 25 Ce cadre connaît toutefois certaines limites. Par exemple, les programmes de lutte antituberculeuse dans les provinces et les territoires qui comptent une forte proportion de personnes nées à l'étranger peuvent, à terme, donner de bons résultats quant à la plupart ou la totalité des indicateurs du rendement de programme, mais connaitre une réduction limitée de l'incidence.Référence 26Référence 27 Cela est dû au fait que le réservoir d'infections tuberculeuses peut être réalimenté de manière continuelle parmi les personnes qui proviennent de pays où l'incidence de la TB est élevée.Référence 28Référence 29Référence 30Référence 31 (voir le Chapitre 13 : La surveillance de la tuberculose et le dépistage et le traitement de la tuberculose chez les migrants). La mise en œuvre de ce cadre nécessitera des ressources humaines dédiées avec les qualifications requises pour bien compiler et communiquer ces données. Cet investissement est justifié, car le suivi du rendement de programme produit des informations précieuses pour l'amélioration des programmes, renforce les activités de gestion de programme, améliore la responsabilisation et génère des données probantes de la valeur des services de lutte antituberculeuse.Référence 11Référence 18Référence 32
4. Indicateurs clés de rendement de programme
Ce cadre de suivi du rendement du programme comprend 12 indicateurs, accompagnés de cibles. En l'absence de données nationales préexistantes, les cibles ont été fixées pour trouver un équilibre entre le fait d'être réalisables et celui d'être une source de motivation et sont fondées sur les conseils d'experts.
Les itérations futures de ce cadre applicable à l'échelle nationale devraient ajuster ces cibles en fonction du rendement réel.
Dans l'ensemble, ce cadre initial de suivi du rendement se concentre sur la prise en charge des cas de TB pulmonaire à frottis positif et de leurs contacts, car ces groupes sont considérés comme hautement prioritaires en ce qui concerne le rendement optimal du programme. Les indicateurs sont regroupés selon les objectifs/les cibles suivants.
4.1. Élimination
Les objectifs en matière de pré-élimination et d'élimination sont fixés dans les engagements internationaux du Canada et les intervenants des programmes devraient surveiller leurs propres progrès d'une année à l'autre en vue de les atteindre. La cible de pré-élimination pour les régions à faible incidence de TB est un taux de cas actifs de 10/1 000 000 d'habitants d'ici 2035, tandis que la cible d'élimination est de 1/1 000 000 d'habitants d'ici 2050 à l'échelle nationale. Les progrès vers l'élimination dépendent de l'atteinte d'un taux de déclin qui correspond à ces cibles, mais ils seront influencés par l'épidémiologie locale de la TB dans les populations desservies par le programme. Par conséquent, le taux de déclin variera selon le programme de déclaration.
4.2. Cibles pour l'examen des immigrants et des réfugiés
Les personnes nées à l'étranger représentent le nombre absolu et la proportion les plus élevés (>70 %) de cas de TB au Canada, ce qui crée une pression sur le rythme du déclin qui peut être atteint au pays. Les programmes devraient donc accorder la priorité à la gestion des aiguillages provenant des examens médicaux aux fins de l'immigration (voir le Chapitre 13 : La surveillance de la tuberculose et le dépistage et le traitement de la tuberculose chez les migrants). Référence 26Référence 33
4.3. Cibles pour la gestion et le traitement des cas
Le diagnostic rapide et l'initiation efficace du traitement chez les personnes atteintes de TB pulmonaire sont primordiaux pour prévenir la transmission de la TB et pour prévenir une morbidité et une mortalité accrues chez ces personnes. Maximiser la réussite du traitement (guérison ou traitement terminé) tout en minimisant les résultats infructueux du traitement (décès lié à la TB, perte en raison d'un traitement non terminé au suivi) sont des objectifs clés. En outre, les besoins psychosociaux et comportementaux des personnes atteintes de TB peuvent influencer l'épidémiologie locale et les résultats individuels. Le traitement de ces problèmes est essentiel à la capacité du programme de dispenser des soins centrés sur le patient (voir le Chapitre 5 : Le traitement de la tuberculose).
4.4. Cibles pour la gestion des contacts
La prévention de la réactivation des infections tuberculeuses latentes est un élément tout aussi crucial dans l'élimination de la TB, en particulier pour les contacts prioritaires, c'est-à-dire les contacts étroits avec des cas de TB pulmonaire à frottis positif (voir le Chapitre 11 : La recherche et la prise en charge des contacts lors d'une éclosion de tuberculose).
Les calculs pour chaque indicateur tabulent le nombre de fois que l'action a été complétée sur le nombre de fois qu'elle a été applicable, et sont affichés en proportions.Référence 34 Ces proportions sont ensuite comparées quantitativement à des cibles définies. Les définitions de ces actions et cibles sont fournies dans le Tableau 1, tandis que les méthodes d'analyse et de déclaration sont fournies dans le Tableau 2.
5. Stratégies analytiques et d'action
Le Tableau 2 décrit comment mesurer et analyser le rendement des programmes de lutte antituberculeuse en fonction des indicateurs de ce cadre. Cette stratégie analytique est distincte des soins cliniques destinés aux patients, qui sont abordés dans d'autres chapitres de ces normes.
5.1. Calendrier des déclarations
Le suivi du rendement sera réalisé en remplissant les rapports sur les indicateurs présentés ici, selon les formules fournies dans le Tableau 2. Les indicateurs de rendement de programme pour l'année civile écoulée doivent être déclarés en février ou en mars de l'année en cours, à l'exception des résultats de traitement de tous les patients diagnostiqués avec la TB au cours de l'année civile précédente, qui ne peuvent être déclarés qu'après une année entière. Les rapports annuels sur le rendement de programme devraient faire l'objet de discussions avec les représentants locaux appropriés de la santé publique et les partenaires communautaires afin d'assurer l'imputabilité, déterminer comment les actions devraient être modifiées pour améliorer les résultats s'il y a lieu et contextualiser l'information de manière qu'elle soit adaptée à la culture.Référence 35 Les gestionnaires de programme (responsables) sont les mieux placés pour mettre en œuvre le changement.
Il est donc essentiel que les gestionnaires de programme supervisent le processus et élaborent un mécanisme pour faire participer de façon adéquate les groupes d'intervenants.Référence 36 Les rapports de synthèse annuels devraient être publiés en ligne afin de promouvoir la transparence et de contribuer aux analyses comparatives à l'échelle du pays.
La mise en œuvre de ce cadre de suivi du rendement de programme comprend la production de rapports annuels (pour évaluer le rendement local au fil du temps) qui sont uniformes d'une administration à l'autre (pour évaluer le rendement relatif). L'achèvement et le partage en temps opportun de ces rapports aideront à minimiser les retards dans l'amélioration du programme. Les programmes de lutte antituberculeuse devraient affecter des ressources humaines adéquates pour la collecte et la validation des données afin de surveiller ces indicateurs. La validation des données doit être effectuée en étroite collaboration avec le médecin ou les responsables des soins infirmiers et les partenaires communautaires concernés.
5.2. Variables démographiques, cliniques et sociales recommandées
Il est recommandé d'analyser les données en fonction de l'âge, du sexe/genre et du groupe de population pour continuer à se concentrer sur les personnes ayant le plus besoin de services et de soins antituberculeux et pour atténuer les inégalités. Ces niveaux de désagrégation concordent avec les normes internationales et canadiennes en matière d'analyse des données sur la santé fondée sur le sexe et le genre.Référence 37Référence 38Référence 39Référence 40Référence 41 Selon les décisions locales concernant les programmes de collecte de données ou de couplage avec d'autres données, les analyses peuvent également inclure d'autres strates sociales de risque importantes, y compris le statut au virus de l'immunodéficience humaine (VIH), les personnes sans abri, les personnes ayant une participation limitée au marché du travail ou celles qui exercent des professions à risque élevé et les personnes actuellement ou récemment incarcérées.
5.3. Rôle du travail social dans la réponse aux besoins des patients et des clients
Dans le cadre du programme de lutte antituberculeuse, les réponses aux facteurs de risque social associés à la TB devraient être traitées par un travailleur social spécialisé; on devrait s'assurer de pouvoir avoir recours à une telle personne pour ce genre de programme. Parmi les maladies infectieuses transmissibles, la TB en particulier illustre comment les obstacles structurels imposés par le racisme, le classisme et le colonialisme au Canada exigent un engagement politique pour rendre les systèmes de santé disponibles et accessibles à tous (voir le Chapitre 12 : Guide d'introduction aux soins antituberculeux pour améliorer les compétences culturelles des travailleurs de la santé et des professionnels de la santé publique au service des peuples autochtones du Canada et le Chapitre 13 : La surveillance de la tuberculose et le dépistage et le traitement de la tuberculose chez les migrants).Référence 42Référence 43 En même temps, des considérations psychosociales, comportementales et biologiques compliquent la TB et sa prise en charge (p. ex. les troubles liés à la consommation d'alcool et d'autres drogues, les structures des réseaux pour repérer les contacts, le VIH/sida [syndrome d'immunodéficience acquise], le diabète, la dénutrition).Référence 44Référence 45Référence 46Référence 47Référence 48Référence 49Référence 50Référence 51Référence 52Référence 53Référence 54Référence 55 Étant donné que les tâches précises du travailleur social du programme de lutte antituberculeuse peuvent varier, les intervenants des programmes peuvent évaluer l'influence de ce soutien de diverses façons, notamment : 1) en signalant la proportion de patients ayant recours à un dispensateur de soins primaires à la fin des soins antituberculeux; 2) en signalant la proportion de patients sans-abri qui sont adéquatement logés à la fin des soins antituberculeux; et 3) en évaluant les conditions de logement chez les patients atteints de TB infectieuse.
| Numéro d'indicateur | Comment calculer le rendement pour les rapports |
|---|---|
| Objectif de l'élimination | |
| 1.0 | Numérateur : nombre de cas de TB déclarés dans la juridiction entre le 1er janvier et le 31 décembre inclusivement. Dénominateur : estimation de la population totale en milieu d'année. Formule: 
En outre, calculez le taux de déclin annuel nécessaire pour parvenir à la pré-élimination dans la juridiction (voir ci-dessous) où « années de différence » est la période entre l'année de déclaration et 2035 et la cible de 1 est le numérateur. 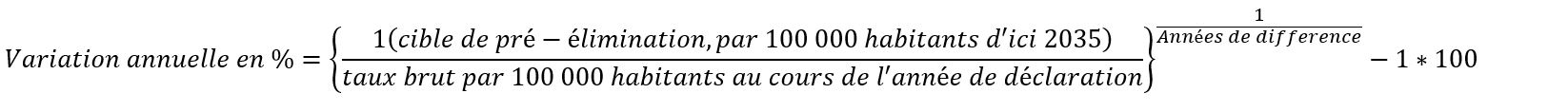
Variation annuelle en % = {1(cible de pré-élimination, par 100 000 habitants d'ici 2035)/ taux brut par 100 000 habitants au cours de l'année de déclaration}^Années de différence – 1*100 |
| Cibles pour l'examen des immigrants et des réfugiés | |
| 2.0 | Numérateur : nombre d'aiguillages d'immigrants et de réfugiés issus d'Immigration, Réfugiés et Citoyenneté Canada (IRCC) datant du 1er juillet de l'année précédente et dont le premier rendez-vous avec un médecin ou un spécialiste désigné en santé publique a été respecté dans les six mois suivant la date de réception de l'aiguillage. Dénominateur : nombre total d'aiguillages d'IRCC à l'autorité de santé publique dans la juridiction entre le 1er juillet et le 30 juin. Formule:  |
| Cibles pour la gestion et le traitement des cas | |
| 3.0 | Numérateur : nombre de cas de TB déclarés entre le 1er janvier et le 31 décembre dont le statut au virus de l'immunodéficience humaine (VIH) est établi au début du traitement. Dénominateur : nombre total de cas de TB traités. Formule: 
Les résultats au test de dépistage du VIH comprennent les possibilités suivantes : · Positif au VIH : documentation médicale d'un test de dépistage positif du VIH effectué à tout moment. · Négatif au VIH : documentation médicale d'un test de dépistage négatif du VIH effectué pas plus de 90 jours avant la date de début du traitement de la TB. |
| 3.1 | Numérateur : nombre de cas de TB pulmonaire à frottis positif déclarés entre le 1er janvier et le 31 décembre qui commencent le traitement dans les 72 heures suivant un test d'amplification des acides nucléiques positif (TAAN). Dénominateur : nombre total de cas de TB pulmonaire à frottis positif. Formule :  |
| 3.2 | Numérateur : nombre de cas admissibles de TB pulmonaire à frottis positif, sensibles à la rifampicine (par test d'amplification des acides nucléiques [TAAN]) déclarés entre le 1er janvier et le 31 décembre, qui commencent un traitement par quatre médicaments antituberculeux. Dénominateur : nombre total de cas de TB admissibles traités. Exclusions : les patients jugés à haut risque d'hépatotoxicité, de goutte ou ayant des antécédents d'exposition manifeste à un cas source connu de TB résistante aux médicaments (tout médicament antituberculeux de première intention), et les patients qui ont été précédemment traités ne seront pas tenus en compte dans le numérateur ou le dénominateur. Formule:  |
| 3.3 | Numérateur : nombre de cas de TB pulmonaire confirmés par culture dont l'échantillon d'expectorations a été soumis à un frottis/une culture de bacille acido-résistant, et ayant obtenu une radiographie thoracique dans les deux semaines suivant la fin de la phase initiale de traitement. Dénominateur : nombre total de cas de TB pulmonaire confirmés par culture qui sont vivants et n'ont pas été transférés à la fin de la phase initiale du traitement. Exclusions : les patients décédés pendant la phase initiale du traitement ou qui ont été transférés hors de la juridiction avant la fin de la phase initiale du traitement ne seront pas tenus en compte dans le numérateur ou le dénominateur. Formule:  |
| 3.4 | Numérateur : incidence annuelle - nombre de cas de TB déclarés au cours des 12 mois précédents qui ont guéri ou ont terminé le traitement. Dénominateur : incidence annuelle - nombre total de cas de TB déclarés au cours des 12 mois précédents qui étaient vivants au moment du diagnostic et qui ont commencé ≥ un médicament antituberculeux. Exclusions : les patients ayant une résistance à la rifampicine, les patients dont le traitement a été initié dans une autre juridiction canadienne (qui ont été transférés) et les patients qui ont été transférés hors du pays pendant le traitement sont exclus du numérateur et du dénominateur. Formule :  |
| 3.5 | Le programme de lutte antituberculeuse est-il soutenu par des travailleurs sociaux? Si oui, leur rendement devrait faire l'objet d'un suivi en fonction des besoins objectifs des patients et des clients dans la juridiction (voir la section 5.3 pour des exemples). Si non, sous la direction du gestionnaire/responsable de programme, les besoins objectifs des patients et des clients mal desservis devraient être définis dans le programme pour plaider en faveur d'un soutien par des travailleurs sociaux. |
| Cibles pour la gestion des contacts | |
| 4.0 | Numérateur : nombre de contacts étroits (familiaux et non familiaux) avec des cas de TB pulmonaire à frottis positif déclarés entre le 1er janvier et le 31 décembre dont le premier contact a eu lieu dans les 3 jours ouvrables suivant la date à laquelle le contact a été répertorié. Dénominateur : incidence annuelle - nombre total de contacts étroits avec des cas de TB pulmonaire à frottis positif. Formule :  |
| 4.1 | Numérateur : nombre de contacts étroits (familiaux et non familiaux) avec des cas de TB pulmonaire à frottis positif déclarés entre le 1er janvier et le 31 décembre qui ont fait l'objet d'une évaluation complèteTable 2 note de bas de page a. Dénominateur : incidence annuelle - nombre total de contacts étroits avec des cas de TB pulmonaire à frottis positif. Formule : 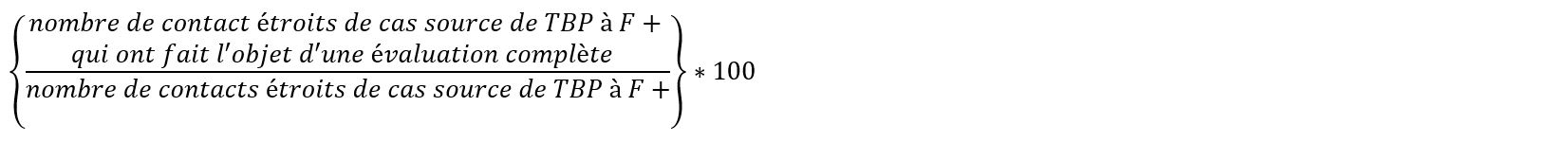 |
| 4.2 | Numérateur : nombre de contacts étroits (familiaux et non familiaux) avec des cas de TB pulmonaire à frottis positif déclarés entre le 1er janvier et le 31 décembre, admissibles au traitement antituberculeux préventif (TAP) et qui le commencent. Dénominateur : incidence annuelle - nombre total de contacts étroits avec des cas de TB pulmonaire à frottis positif qui sont admissibles au TAP. Formule :  |
| 4.3 | Numérateur : nombre de contacts étroits (familiaux et non familiaux) avec des cas de TB pulmonaire à frottis positif déclarés entre le 1er janvier et le 31 décembre, admissibles au traitement antituberculeux préventif qui le commencent et le terminent. Dénominateur : incidence annuelle - nombre total de contacts étroits avec des cas de TB pulmonaire à frottis positif, admissibles au TAP et qui ont commencé un traitement pour une ITL. Formule : 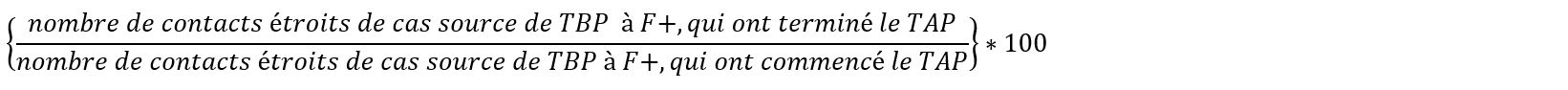 |
|
Notes de bas de page :
|
|
6. Résumé
Dans une fédération, il est plus difficile de relever le défi de l'élimination de la TB en raison de différences inhérentes dans la prestation des services de santé dans l'ensemble du pays. En conséquence, chaque province et territoire contribue en partie à ce qui constitue, en somme, la réponse nationale. Chaque personne atteinte de TB active au Canada est importante, et en nous engageant à atteindre les cibles ambitieuses de la stratégie Halte à la tuberculose, nous reconnaissons que chaque cas évité compte plus que jamais. L'objectif de ce chapitre est d'encourager les responsables et le personnel du programme de lutte antituberculeuse à fournir des données probantes aux communautés, au grand public, aux autorités sanitaires et aux gouvernements des progrès réalisés vers les résultats souhaités. Les indicateurs de rendement de base du programme décrits dans le présent chapitre sont considérés comme la norme minimale pour tous les programmes.
Énoncé de divulgation
Les éditeurs et auteurs des Normes canadiennes pour la lutte antituberculeuse ont déclaré des conflits d'intérêts potentiels au moment de leur nomination et ceux-ci ont été mis à jour tout au long du processus, conformément à la politique de divulgation des conflits d'intérêts de la Société canadienne de thoracologie (SCT).
Les déclarations de conflits d'intérêts des membres individuels sont publiées sur le site Web des Normes canadiennes pour la lutte antituberculeuse.
Financement
Les Normes canadiennes pour la lutte antituberculeuse 8e édition sont financées par la SCT et l'Agence de la santé publique du Canada. Elles sont éditées par la SCT et publiées par la SCT en collaboration avec l'Association pour la microbiologie médicale et l'infectiologie (AMMI) Canada (en anglais seulement). Il importe cependant de souligner que les recommandations cliniques contenues dans les Normes ont été formulées par la SCT. Les éditeurs et auteurs des Normes canadiennes pour la lutte antituberculeuse sont responsables devant le Comité des lignes directrices canadiennes en santé respiratoire de la SCT et le conseil d'administration de la SCT. Les éditeurs et auteurs des Normes canadiennes pour la lutte antituberculeuse de la SCT sont fonctionnellement et éditorialement indépendants de toute source de financement et n'ont reçu aucun financement direct de sources externes.
La SCT reçoit des subventions sans restriction qui sont combinées à un compte d'exploitation central afin de faciliter les activités d'application des connaissances assemblées de la SCT et de ses panels de directives et de normes. Aucun bailleur de fonds du milieu des affaires n'a joué un rôle dans la collecte, l'examen, l'analyse ou l'interprétation des publications scientifiques ou dans toute décision concernant les recommandations présentées dans ce document.
Annexe 1 : Suivi du rendement de programme de lutte antituberculeuse
Le cadre de suivi du rendement de programme de lutte antituberculeuse décrit au Chapitre 15 est composé de 12 indicateurs de rendement du programme; une justification pour chacun d'eux, ainsi que l'historique international et national de leur utilisation ou les précédents de recommandations sont fournis ci-dessous. Comme indiqué dans le texte, en 2018, le Centre de collaboration nationale des maladies infectieuses (CCNMI) a effectué un examen de la portée des indicateurs de rendement de programme de lutte antituberculeuse dans des contextes similaires sur le plan épidémiologique (incidence de la TB dans les pays à revenu élevé et faible incidence de la maladie), conjugué à des recommandations générales à l'échelle mondiale. Les indicateurs ont été sélectionnés à partir de cet examen de la portée. Comme le démontrent les données suivantes, des recommandations et des stratégies plus récentes ont été examinées en vue de préparer ce chapitre pour un historique d'utilisation. Cette liste d'utilisation/de recommandations antérieures est représentative et non exhaustive.
Abréviations : CCNMI, Centre de collaboration nationale des maladies infectieuses; OMS, Organisation mondiale de la Santé; CDC, Centers for Disease Control and Prevention; DGSPNI, Direction générale de la santé des Premières Nations et des Inuits; RSI, retour sur investissement; VIH, virus de l'immunodéficience humaine; P/T, provincial et territorial; TAAN, test d'amplification des acides nucléiques; IC, intervalle de confiance; RCa, rapport de cotes ajusté; TCT, test cutané à la tuberculine; BAAR, Bacille acido-alcoolo-résistant; CXR, radiographie thoracique; ITK, Inuit Tapiriit Kanatami; 4R, rifampicine quotidiennement pendant 4 mois; 9INH, régime quotidien à l'isoniazide pendant 9 mois; TAP, traitement antituberculeux préventif; ITL, infection tuberculeuse latente.
Objectif de l'élimination: L'indicateur, la cible et la justification
1.0 Taux brut d'incidence de la TB : toutes formes confondues cible
Signaler l'incidence et le taux de déclin.
Justification : Il s'agit de la cible renforcée de la pré-élimination et de l'élimination. Cette mesure établit la norme ultime en fonction de laquelle le programme fonctionne. L'incidence devrait faire l'objet d'un suivi et d'un rapport annuel afin d'éclairer les changements efficaces à adopter à mi-parcours sur la voie de l'élimination.Référence 56Référence 57 Le Canada est responsable de la déclaration des données nationales et infranationales à la communauté mondiale; par conséquent, ces données devraient être accessibles et déclarables.Référence 58
Notes : Les responsables de programme devraient établir un taux de déclin suffisant pour atteindre les cibles d'élimination.
Recommandé internationalement par : l'OMS – Compendium of Indicators for Monitoring and Evaluation of National Tuberculosis Control Programs; Référence 56 les CDC – National Tuberculosis Program Objectives and Performance Targets for 2025;Référence 59 l'Australie – The Strategic Plan for Control of Tuberculosis in Australia 2011-2015, et National Tuberculosis Performance Indicators, Australia 2013-2014;Référence 5Référence 60 Public Health England – Public Health England Tuberculosis Strategy Monitoring Indicators 2015-2020 (moyenne sur trois ans)Référence 7 l'Alaska – Alaska Department of Health and Social Services TB Manual;Référence 61 le Minnesota – Tuberculosis (TB) Prevention and Control Program;Référence 62 et la Californie – CID TB Performance Trends for US, California Objectives.Référence 63
Recommandé pour le Canada par : le Réseau pancanadien de santé publique – Orientations pour les programmes de prévention et de contrôle de la tuberculose au Canada;Référence 15 Direction générale de la santé des Premières Nations et des Inuits (DGSPNI) – Stratégie de lutte contre la tuberculose de Santé Canada pour les membres des Premières Nations vivant dans les réserves et Cadre de surveillance et de rendement pour les programmes sur la tuberculose chez les membres des Premières Nations vivant dans les réserves;Référence 13Référence 14 Cadre pour l'élimination de la tuberculose chez les Inuit;Référence 16 Heffernan et Long – Would program performance indicators and a nationally coordinated response accelerate tuberculosis elimination in Canada?;Référence 64 et le CCNMI – Toward TB Elimination: Shared Priorities for TB Program Performance Measurement in Canada, a Proposal for Discussion.Référence 17
Cibles pour l'examen des immigrants et des réfugiés: L'indicateur, la cible et la justification
2.0 Proportion de personnes aiguillées par les services de l'immigration vers une surveillance médicale et qui ont été évaluées par un médecin
Cible : ≥90 %
Justification : Les personnes nées à l'étranger représentent le nombre absolu le plus élevé (aujourd'hui >70 % à l'échelle nationale) de cas de TB recensés au Canada, ce qui crée une pression sur le rythme du déclin qui peut être atteint au pays.Référence 26Référence 33 Un examen systématique et une méta-analyse de l'incidence de la TB chez les migrants jugés « à haut risque » lors du dépistage prémigration a révélé une incidence élevée de la maladie active dans ce groupe. L'incidence cumulée de la TB post-migration dans la population de l'étude répartie dans 22 cohortes était de 2 794 pour 100 000 personnes (95 % IC 2 179-3 409; I2 = 99 %). Dans dix des cohortes, l'incidence cumulée de la TB à la première visite de suivi était de 3 284 pour 100 000 personnes (95 % IC 2 173-4 395; I2 = 99 %). Dans 15 des cohortes, l'incidence cumulée de TB était de 1 249 pour 100 000 années-personnes de suivi (95 % IC 924-1 574; I2 = 98 %).Référence 65 Il y a un débat récent sur la question de savoir si l'expression phénotypique de la maladie chez les nouveaux arrivants pose un risque important pour la santé publique, ce qui suggère que le risque de transmission dans le pays est limité par rapport au risque de transmission par les personnes qui connaissent une réactivation de la TB pulmonaire en raison d'une ITL non détectée à l'arrivée au pays.Référence 28Référence 66 Par conséquent, cet indicateur seul est insuffisant pour une réduction à long terme de la TB chez les personnes nées à l'étranger. Même si l'on considère que l'aiguillage des personnes nées à l'étranger vers la santé publique pour une surveillance médicale contribue de façon minimaleRéférence 67 à l'élimination de la maladie, le dépistage ciblé des ITL chez les immigrants et les réfugiés arrivant au Canada n'a pas encore atteint son plein potentiel.
Notes : Malgré ses limites, cet indicateur de rendement est un aspect mesurable des services de prévention et de soins antituberculeux et contribue à générer des données probantes à l'appui de la valeur (rendement des investissements).
Recommandé internationalement par : les CDC – National Tuberculosis Program Objectives and Performance Targets for 2025;Référence 59 la Californie – CID TB Performance Trends for US, California Objectives;Référence 63 et Public Health England – Public Health England Tuberculosis Strategy Monitoring Indicators 2015-2020.Référence 61
Recommandé pour le Canada par : le Réseau pancanadien de santé publique – Orientations pour les programmes de prévention et de contrôle de la tuberculose au Canada;Référence 15 Heffernan et Long – Would program performance indicators and a nationally coordinated response accelerate tuberculosis elimination in Canada?.Référence 64 Le Chapitre 15 de la sixième édition des Normes canadiennes pour la lutte antituberculeuse, l'immigration et la lutte antituberculeuse au Canada fait état d'une évaluation de la conformité à cet indicateur, effectuée à l'échelle nationale (le rendement moyen était d'environ 50 % à l'époque).Référence 68
Cibles pour la gestion et le traitement des cas: L'indicateur, la cible et la justification
3.0 Proportion de tous les nouveaux cas de TB et de ceux qui vivent une rechute ou reçoivent un second traitement pour la TB, et dont le statut au VIH est établi
Cible : ≥95 %
Justification : Un diagnostic de VIH, indépendamment de la TB, a des implications sur la santé individuelle et publiqueRéférence 69 et, en cas de co-infection, a des implications sur le traitement de la TB. En Alberta, où plus de 90 % des patients atteints de TB subissent un test de dépistage du VIH, près de 50 % des infections au VIH sont décelées au moment d'un diagnostic de TB (cela est attribuable à une stratégie de non-participation).Référence 70 Un examen systématique et une méta-analyse récents de l'adoption de tests de dépistage du VIH en se fondant sur les conditions de l'indicateur dans les pays occidentaux ont montré que peu de patients atteints de TB au Canada ont déclaré avoir subi un test de dépistage du VIH (4/28 articles); il existait une variabilité dans le taux de déclaration du statut au VIH pendant le traitement antituberculeux allant de 53,6 à 90,6 %. Cela indique à la fois un besoin accru de déclaration et la mise en œuvre de stratégies pour améliorer le respect des recommandations à l'échelle du programme.Référence 71
Notes : L'objectif est d'offrir un test de dépistage du VIH à tous les cas de TB si leur statut au VIH est inconnu au moment du diagnostic, et ce, de manière systématique; il est entendu que le taux d'acceptation sera plus faible.
Recommandé internationalement par : l'OMS – Compendium of Indicators for Monitoring and Evaluating National Tuberculosis Programs;Référence 56 Horsburgh et al. – Practice Guidelines for the Treatment of Tuberculosis;Référence 34 l'OMS – Stratégie Halte à la tuberculose;Référence 4 l'OMS/ONUSIDA – Guide to Monitoring and Evaluation for Collaborative TB/HIV Activities;Référence 72 l'Australie – The Strategic Plan for Control of Tuberculosis in Australia 2011-2015, et National Tuberculosis Performance Indicators, Australia 2013-2014;Référence 5Référence 60 Public Health England – Public Health England Tuberculosis Strategy Monitoring Indicators 2015-2020 (moyenne sur trois ans);Référence 7 l'Alaska – Alaska Department of Health and Social Services TB Manual;Référence 61 et la Californie – CID TB Performance Trends for US, California Objectives.Référence 63
Recommandé pour le Canada par : Tuberculosis Directors of Canada et le ministère de la Santé nationale et du Bien-être social en consultation avec des épidémiologistes des niveaux provinciaux et territoriaux – Guidelines for the identification, investigation and treatment of individuals with concomitant tuberculosis and HIV infection;Référence 73 le Comité canadien de lutte antituberculeuse, Santé Canada – Recommendations for screening and prevention of tuberculosis in patients with HIV and for screening for HIV in patients with tuberculosis and their contacts;Référence 74 le Réseau pancanadien de santé publique – Orientations pour les programmes de prévention et de contrôle de la tuberculose au Canada;Référence 15 et Haworth-Brockman et Keynan – Strengthening tuberculosis surveillance in Canada.Référence 75
3.1 Proportion de tous les cas de TB pulmonaire à frottis positif qui commencent le traitement dans les 72 heures suivant un résultat positif au TAAN
Cible : ≥95 %
Justification : L'initiation rapide du traitement procure un avantage individuel en limitant le risque accru de complications associées à un retard dans le début du traitement, ainsi qu'un avantage pour la santé publique, en réduisant rapidement l'infectivité.Référence 76 Une étude de cohorte prospective aux États-Unis a révélé un risque accru de transmission à des contacts étroits (résultat = positivité au TCT) de cas nés aux É.-U. qui ont connu un retard dans l'initiation du traitement ≥90 jours (40 %) par rapport à ceux qui ont initié le traitement plus rapidement (24 %) (RCa 2,34; p = 0,03), et ce risque de transmission augmente à (RCa 3,29; p = 0,01) parmi les contacts étroits de cas nés aux É.-U. qui ont présenté un résultat positif au bacille acido-résistant au frottis d'expectoration et dont l'initiation du traitement a été retardée.Référence 77 En conséquence, l'initiation rapide de médicaments antituberculeux pour les cas de TB pulmonaire est une priorité, et ces patients devraient être en tête de liste quant au rendement du programme.
Notes : Ici, l'indicateur et la cible connexe sont l'initiation rapide du traitement (dans un délai de 3 jours), ≥95 % du temps. Ce choix était fondé sur les attentes en matière de délai d'exécution des laboratoires relatives à l'analyse et au renvoi des résultats du test dans les 24 heures suivant la soumission. Nous proposons l'ajout de deux jours supplémentaires pour tenir compte de la possibilité que la notification d'un résultat positif au TAAN puisse survenir au début d'un long week-end.
Recommandé internationalement par : les CDC – National Tuberculosis Program Objectives and Performance Targets for 2025;Référence 59 l'Alaska – Alaska Department of Health and Social Services TB Manual;Référence 61 et la Californie – CID TB Performance Trends for US, California Objectives.Référence 63
Recommandé pour le Canada par : le Réseau pancanadien de santé publique – Orientations pour les programmes de prévention et de contrôle de la tuberculose au Canada.Référence 15
3.2 Proportion de cas de TB pulmonaire à frottis positif qui commencent un traitement antituberculeux avec quatre médicaments ou plus
Cible : ≥95 %
Justification : L'initiation rapide d'un traitement par médicaments antituberculeux, en particulier pour les cas de TB pulmonaire à frottis positif, est essentielle pour réduire l'infectivité et interrompre la transmission.Référence 76Référence 78 Compte tenu de cette réalité et des délais associés à l'obtention des résultats des tests de sensibilité aux médicaments, les plus grands avantages pour la santé individuelle et publique découlent de l'initiation d'un traitement empirique chez les cas infectieux sans facteurs de risque de résistance, de suspicion d'hépatotoxicité ou de goutte. Il est à noter qu'au Canada, la résistance aux médicaments est un phénomène relativement peu fréquent, mais certains programmes de lutte antituberculeuse peuvent prévoir qu'il existe une variabilité dans l'épidémiologie régionale des formes de TB résistantes aux médicaments qui pourrait contribuer à des exceptions plus fréquentes au numérateur.Référence 79
Recommandé internationalement par : les CDC – National Tuberculosis Program Objectives and Performance Targets for 2025;Référence 59 et Public Health England – Public Health England Tuberculosis Strategy Monitoring Indicators 2015-2020.Référence 7
Recommandé pour le Canada par : le Réseau pancanadien de santé publique – Orientations pour les programmes de prévention et de contrôle de la tuberculose au Canada;Référence 15 DGSPNI/Santé Canada – Stratégie de lutte contre la tuberculose de Santé Canada pour les membres des Premières Nations vivant dans les réserves et Cadre de surveillance et de rendement pour les programmes sur la tuberculose chez les membres des Premières Nations vivant dans les réserves;Référence 13Référence 14 CCNMI – Toward TB Elimination: Shared Priorities for TB Program Performance Measurement in Canada, a Proposal for Discussion;Référence 17 et Heffernan et Long – Would program performance indicators and a nationally coordinated response accelerate tuberculosis elimination in Canada?Référence 64
3.3 Proportion de tous les cas dont la TB pulmonaire a été confirmée par culture et dont l'échantillon d'expectorations a été soumis à un frottis/une culture de bacille acido-résistant, et ayant obtenu une radiographie thoracique à la fin de la phase initiale de traitement
Cible : ≥95 %
Justification : Le virage de la culture d'expectorations à la fin de la phase initiale est considéré comme un bon prédicteur de la guérison future; plus significativement, il y a des implications pour le traitement.Référence 56 La positivité prolongée de la culture ou la présence de cavernes non fermées sur la radiographie thoracique à la fin de la phase initiale du traitement peut suggérer l'échec du traitement/une rechute et induire une résistance médicamenteuse.Référence 80 Un examen systématique et une méta-analyse récents du virage de la culture d'expectorations au cours d'un traitement efficace ont trouvé que 12, et 41 % des cas confirmés par frottis positif sont demeurés positifs par la culture solide et liquide, respectivement, à la fin de la phase initiale du traitement. Les analyses de sous-groupes par des covariables importantes que l'on sait être indépendamment associées au virage des cultures d'expectorations, telles que le statut au VIH et la formation de cavernes, étaient, quant à elles, limitées.Référence 81 La surveillance de l'adhésion aux meilleures pratiques cliniques fournit des renseignements utiles au programme de lutte antituberculeuse concernant les efforts déployés pour apparemment améliorer les résultats du traitement en réduisant le risque de rechute.
Recommandé internationalement par : l'OMS – Compendium of Indicators for Monitoring and Evaluation of National Tuberculosis Control Programs;Référence 56 la Californie – CID TB Performance Trends for US, California Objectives;Référence 63 et les CDC – National Tuberculosis Program Objectives and Performance Targets for 2025.Référence 59
Recommandé pour le Canada par : le Réseau pancanadien de santé publique – Orientations pour les programmes de prévention et de contrôle de la tuberculose au Canada;Référence 15 et la DGSPNI/Santé Canada – Stratégie de lutte contre la tuberculose de Santé Canada pour les membres des Premières Nations vivant dans les réserves, et Cadre de surveillance et de rendement pour les programmes sur la tuberculose chez les membres des Premières Nations vivant dans les réserves.Référence 13Référence 14
3.4 Réussite du traitement (cas guéri ou ayant terminé le traitement) dans les 12 mois suivant le début du traitement
Cible : ≥90 % des cas
Justification : La réussite du traitement (guérison ou traitement terminé) est essentielle pour éliminer la TB en empêchant la transmission, en jugulant la gravité de la maladie et en évitant les décès. Un traitement incomplet ou une perte de suivi peut entraîner une résistance aux médicaments et une transmission à d'autres personnes. Lors d'une résolution de l'Assemblée mondiale de la Santé de 1991, un objectif mondial de réussite du traitement a été fixé à 85 %, mais dans les environnements à faible prévalence du VIH où la protection en matière de santé est universelle, un taux de réussite plus élevé devrait être atteignable.Référence 82
Recommandé internationalement par : l'OMS – Compendium of Indicators for Monitoring and Evaluation of National Tuberculosis Control Programs;Référence 56 les CDC – National Tuberculosis Program Objectives and Performance Targets for 2025;Référence 59 l'Australie – The Strategic Plan for Control of Tuberculosis in Australia 2011-2015, et National Tuberculosis Performance Indicators, Australia 2013-2014;Référence 5Référence 60 l'OMS – Stratégie Halte à la tuberculose;Référence 4 l'Alaska – Alaska Department of Health and Social Services TB Manual;Référence 61 le Minnesota – Tuberculosis (TB) Prevention and Control Program;Référence 62 et la Californie – CID
TB Performance Trends for US, California Objectives.Référence 63
Recommandé pour le Canada par : le Réseau pancanadien de santé publique – Orientations pour les programmes de prévention et de contrôle de la tuberculose au Canada;Référence 15 la DGSPNI/Santé Canada – Stratégie de lutte contre la tuberculose de Santé Canada pour les membres des Premières Nations vivant dans les réserves et Cadre de surveillance et de rendement pour les programmes sur la tuberculose chez les membres des Premières Nations vivant dans les réserves;Référence 13Référence 14 l'organisme Inuit Tapiriit Kanatami – Cadre pour l'élimination de la tuberculose chez les Inuit;Référence 16 et Heffernan et Long – Would program performance indicators and a nationally coordinated response accelerate tuberculosis elimination in Canada?Référence 64
3.5 Le programme de lutte antituberculeuse est-il soutenu par des travailleurs sociaux?
Cible : Oui
Justification : Ce chapitre recommande que les programmes de lutte antituberculeuse soient soutenus par un travailleur social et que leur flux de travail associé soit évalué. Voici quelques exemples de mesures possibles du rendement du travailleur social : la proportion de patients ayant recours à un dispensateur de soins primaires à la fin des soins antituberculeux; la proportion de patients sans abri ou sous-logés qui sont convenablement logés grâce à leurs efforts; la surveillance des cas qui signalent un logement surpeuplé. Les besoins psychosociaux objectifs des clients et des patients peuvent varier selon la juridiction, et doivent être clairement définis par le gestionnaire/responsable de programme.
Recommandé par : En ce qui a trait au soutien d'un travailleur social dans les programmes de lutte antituberculeuse, nous n'avons pas trouvé d'indicateur précis de rendement du programme correspondant. Cependant, les recommandations visant à répondre aux besoins psychosociaux des patients et des clients qui souffrent des effets de l'infection tuberculeuse et de la maladie sont courantes, mais les conseils pratiques sur la façon d'y parvenir demeurent limités.Référence 83 Par conséquent, cet indicateur est inclus comme moyen de générer de l'information sur les mesures pratiques que les programmes de lutte peuvent prendre pour s'attaquer aux répercussions des déterminants de la santé structurels et sociaux dans la vie des clients/patients servis.
Cibles pour la gestion des contacts : L'indicateur, la cible et la justification
4.0 Proportion de contacts étroits avec des cas de TB pulmonaire à frottis positif dont le premier contact a eu lieu dans les 3 jours ouvrables suivant la date à laquelle le contact a été répertorié
Cible : ≥95 %
Justification : Au Canada, les programmes de lutte antituberculeuse font généralement appel à une méthode du type « pierre jetée à l'eau » pour démasquer les données probantes de transmission entre les contacts de personnes atteintes de TB pulmonaire.Référence 84 Cette méthode est considérée comme favorable lorsque le risque relatif de transmission aux contacts est plus élevé que le risque d'infection dans le grand public.Référence 84Référence 85 La recherche de contacts rapide limite la transmission dans des cercles de contacts plus larges, ce qui représente un avantage pour la santé publique.Référence 86 L'identification rapide des contacts et le repérage de la rencontre initiale des contacts étroits avec un cas source infectieux offrent un mécanisme de priorisation. Une modification à la méthode « pierre jetée à l'eau » consiste à rapidement évaluer (la priorisation) des contacts vulnérables (jeunes enfants et personnes immunovulnérables, notamment celles vivant avec le VIH) qui sont connus pour être à risque d'une progression très rapide de la maladie.Référence 87Référence 88
Notes : On considère trois jours comme étant une fenêtre raisonnable et rapide, mais également quelque peu arbitraire.Référence 86 L'objectif ici est d'assurer un suivi avec l'ambition d'atteindre et de dépasser la cible, en réorientant les actions en cas de rendement insuffisant.
Recommandé internationalement par : les CDC – Guidelines for the investigation of contacts of patients with infectious tuberculosis: Recommendations from the National Tuberculosis Controllers Association and the CDC.Référence 86
Recommandé pour le Canada par : le Chapitre 12 de la septième édition des Normes canadiennes de lutte antituberculeuse, Le suivi des contacts et la gestion des éclosions dans le cadre de la lutte antituberculeuse.Référence 89
4.1 Proportion de contacts étroits avec des cas de TB pulmonaire à frottis positif qui ont fait l'objet d'une évaluation complète
Cible : ≥95 %
Justification : La prévention de la réactivation chez les cas de TB est tout aussi importante pour une gestion appropriée des cas, en particulier des cas infectieux, tout en contribuant aux cibles de pré-élimination et d'élimination de la maladie.
Recommandé internationalement par : l'OMS – Stratégie Halte à la tuberculose;Référence 4 les CDC – National Tuberculosis Program Objectives and Performance Targets for 2025;Référence 59 et Public Health England – Public Health England Tuberculosis Strategy Monitoring Indicators 2015-2020 (en cours d'élaboration).Référence 7
Recommandé pour le Canada par : la DGSPNI/Santé Canada – Stratégie de lutte contre la tuberculose de Santé Canada pour les membres des Premières Nations vivant dans les réserves, et Cadre de surveillance et de rendement pour les programmes sur la tuberculose chez les membres des Premières Nations vivant dans les réserves;Référence 12Référence 13 et Heffernan et Long – Would program performance indicators and a nationally coordinated response accelerate tuberculosis elimination in Canada?Référence 64
4.2 Proportion de contacts étroits avec des cas de TB pulmonaire à frottis positif admissibles au traitement antituberculeux préventif (TAP) et qui le commencent
Cible : ≥90 %
Justification : Symboliquement, l'ITL est le lit de semences des cas de TB futurs, mais le traitement de l'ITL, en l'absence de risque de réinfection, est considéré comme une pleine protection contre la réactivation de la TB.Référence 90Référence 91Référence 92Référence 93Référence 94Référence 95 Ainsi, le jumelage de la prévention de la réactivation avec une excellente gestion des cas sources infectieux fonctionne comme deux stratégies hautement complémentaires en vue de réduire l'incidence future de la TB.Référence 49Référence 90
Notes : Les cibles sont ambitieuses, mais le rendement en question et notamment l'observance du traitement devraient bénéficier de la richesse actuelle de la recherche visant à réduire la durée du traitement et le fardeau posologique tout en maintenant l'efficacité et la sécurité, comme l'atteste l'utilisation plus répandue de la rifampicine pendant 4 mois comparativement à l'isoniazide pendant 9 mois, la posologie administrée depuis longtemps.Référence 96Référence 97
Recommandé internationalement par : l'OMS – Stratégie Halte à la tuberculose;Référence 4 les CDC – National Tuberculosis Program Objectives and Performance Targets for 2025;Référence 59 et Public Health England – Public Health England Tuberculosis Strategy Monitoring Indicators 2015-2020 (en cours d'élaboration).Référence 7
Recommandé pour le Canada par : le Réseau pancanadien de santé publique – Orientations pour les programmes de prévention et de contrôle de la tuberculose au Canada;Référence 15 la DGSPNI/Santé Canada – Stratégie de lutte contre la tuberculose de Santé Canada pour les membres des Premières Nations vivant dans les réserves et Cadre de surveillance et de rendement pour les programmes sur la tuberculose chez les membres des Premières Nations vivant dans les réserves;Référence 13Référence 14 et Heffernan et Long – Would program performance indicators and a nationally coordinated response accelerate tuberculosis elimination in Canada?Référence 64
4.3 Proportion de contacts étroits avec des cas de TB pulmonaire à frottis positif qui ont commencé et terminé un TAP pour un diagnostic d'ITL
Cible : ≥90 %
Justification : Comme mentionné, le traitement réussi protège contre la réactivation de la TB (contre l'infection traitée); la réussite est une fonction de l'observance du traitement et les stratégies pour faciliter l'observance sont encouragées, en particulier pour les schémas posologiques plus courts par lesquels chaque dose contribue davantage à l'efficacité du traitement.Référence 96Référence 97Référence 98Référence 99
Notes : Idem 4.2
Recommandé internationalement par : les CDC – National Tuberculosis Program Objectives and Performance Targets for 2025.Référence 59
Recommandé pour le Canada par : le Réseau pancanadien de santé publique – Orientations pour les programmes de prévention et de contrôle de la tuberculose au Canada;Référence 15 la DGSPNI – Stratégie de lutte contre la tuberculose de Santé Canada pour les membres des Premières Nations vivant dans les réserves et Cadre de surveillance et de rendement pour les programmes sur la tuberculose chez les membres des Premières Nations vivant dans les réserves;Référence 13Référence 14 CCNMI – Toward TB Elimination: Shared Priorities for TB Program Performance Measurement in Canada, a Proposal for Discussion;Référence 17 et Heffernan et Long – Would program performance indicators and a nationally coordinated response accelerate tuberculosis elimination in Canada?Référence 64
Références
- Référence 1
-
World Health Organization. Strategy for the control and elimination of tuberculosis. Dans : Implementing the WHO Stop TB Strategy: A Handbook for National Tuberculosis Control Programmes. Geneva: WHO Press; 2008.
- Référence 2
-
Cole B, Nilsen DM, Will L, Etkind SC, Burgos M, Chorba T. Essential Components of a Public Health Tuberculosis Prevention, Control, and Elimination Program: Recommendations of the Advisory Council for the Elimination of Tuberculosis and the National Tuberculosis Controllers Association. MMWR Recomm Rep. 2020;69(7):1–27. doi:10.15585/mmwr.rr6907a1.
- Référence 3
-
Uplekar M, Weil D, Lonnroth K, et al. WHO's new End TB Strategy. The Lancet. 2015;385(9979):1799–1801. doi:10.1016/S0140-6736(15)60570-0.
- Référence 4
-
World Health Organization. The End TB Strategy. https://www.who.int/tb/strategy/End_TB_Strategy.pdf. Publié en 2015. Consulté le 5 juillet 2021.
- Référence 5
-
Australian Government Department of Health and Ageing. The strategic plan for control of tuberculosis in Australia: 2011–2015. Australian Government Department of Health and Ageing. www1.health.gov.au. Consulté le 30 juin 2021.
- Référence 6
-
Degeling C, Carroll J, Denholm J, Marais B, Dawson Ending TB in Australia: Organizational challenges for regional tuberculosis programs. Health Policy. 2020;124(1):106–112. doi:10.1016/j.healthpol.2019.11.009.
- Référence 7
-
Public Health England. Collaborative TB Strategy for England, 2015 to 2020: end of programme report. 2015. GW-1954.
- Référence 8
-
Pan American Health Organization. The End TB Strategy: Main Indicators in the Americas. 2020.
- Référence 9
-
Kritski A, Barreira D, Junqueira-Kipnis AP, et al. Brazilian Response to Global End TB Strategy: The National Tuberculosis Research Agenda. Revista da Sociedade Brasileira de Medicina Tropical. 2016;49:135-145. doi:10.1590/0037-8682-0330-2015.
- Référence 10
-
Davidson EJ. Evaluative Reasoning. Methodological Briefs: Impact Evaluation. 2014;4:1–14.
- Référence 11
-
Coelho AA, Martiniano CS, Brito EWG, et al. Tuberculosis care: an evaluability study. Revista Latino-Americana de Enfermagem. 2014;22(5):792–800. doi:10.1590/0104-1169.3294.2482.
- Référence 12
-
Centers for Disease Framework for Program Evaluation in Public Health. MMWR. 1999;48(RR-11):1–40.
- Référence 13
-
Santé Canada. Stratégie de lutte contre la tuberculose de Santé Canada pour les membres des Premières Nations vivant dans les réserves. Ottawa, Ontario : Santé Canada; 2012.
- Référence 14
-
Santé Canada. Cadre de surveillance et de rendement pour les programmes sur la tuberculose chez les membres des Premières Nations vivant dans les réserves de Santé Canada. 12 février 2016.
- Référence 15
-
Réseau pancanadien de santé publique. Orientations pour les programmes de prévention et de contrôle de la tuberculose au Canada. 2013.
- Référence 16
-
Inuit Tapiriit Kanatami. Cadre pour l'élimination de la tuberculose chez les Inuit. 2018.
- Référence 17
-
Haworth-Brockman M, Balakumar S, Head B, Keynan Y.Towards TB Elimination: Shared Priorities for TB Program Performance Measurement in Canada, a Proposal for Discussion. Winnipeg, Manitoba: National Collaborating Centre for Infectious Diseases; juin 2019. 453.
- Référence 18
-
Cass A, Shaw T, Ehman M, Young J, Flood J, Royce S. Improved Outcomes Found After Implementing a Systematic Evaluation and Program Improvement Process for Tuberculosis. Public Health Reports. 1974-). 2013;128(5):367–376. doi:10.1177/003335491312800507.
- Référence 19
-
Cavany SM, Sumner T, Vynnycky E, et al. An evaluation of tuberculosis contact investigations against national standards. Thorax. 2017;72(8):736–745. doi:10.1136/thoraxjnl-2016-209677.
- Référence 20
-
Gouvernement du Canada, Agence de la santé publique du Canada. Nombre de cas signalés de maladies de 1924 à 2019 au Canada - Maladies à déclaration obligatoire en direct. https://maladies.canada.ca/declaration-obligatoire/graphiques?c=pl. Publié en 2000. Mise à jour consultée le 1er janvier 2000.
- Référence 21
-
Proceedings of the National Consensus Conference on Tuberculosis. 3-5 décembre 1997. 1998; 24(Supplément 2):1-24.
- Référence 22
-
Plan mondial Halte à la tuberculose, 2006-2015 – Agir pour la vie – Vers un monde sans tuberculose. Genève : Partenariat Halte à la tuberculose; 2006.
- Référence 23
-
Stewart TR. The Delphi technique and judgmental forecasting. Clim Change. 1987; 11(1-2):97–113. doi:10.1007/BF00138797.
- Référence 24
-
Niederberger M, Spranger J. Delphi Technique in Health Sciences: A Map. Front Public Health. 2020;8:457. doi:10.3389/ fpubh.2020.00457.
- Référence 25
-
von Schirnding Y.Health in Sustainable Development Planning: The Role of Indicators. Genève : Organisation mondiale de la Santé. 2003. WHO/HDE/HID/02.11.
- Référence 26
-
Langlois-Klassen D, Wooldrage KM, Manfreda J, et al. Piecing the puzzle together: foreign-born tuberculosis in an immigrant-receiving country. European Respiratory Journal. 2011;38(4):895–902. doi:10.1183/09031936.00196610.
- Référence 27
-
World Health Organization. Global Tuberculosis Control: Surveillance, Planning, Financing. Genève : WHO Press; 2005.
- Référence 28
-
Asadi L, Heffernan C, Menzies D, Long R. Effectiveness of Canada's tuberculosis surveillance strategy in identifying immigrants at risk of developing and transmitting tuberculosis: a population-based retrospective cohort study. The Lancet Public Health. 2017;2(10):e450–e457. doi :10.1016/ S2468- 2667(17)30161-5.
- Référence 29
-
Greenaway C, Pareek M, Chakra C-NA, et al. The effectiveness and cost-effectiveness of screening for latent tuberculosis among migrants in the EU/EEA: a systematic review. Eurosurveillance. 2018;23(14):17. doi:10.2807/1560-7917.ES.2018.23.14.17-00543.
- Référence 30
-
Berrocal-Almanza LC, Harris R, Lalor MK, et al. Effectiveness of pre-entry active tuberculosis and post-entry latent tuberculosis screening in new entrants to the UK: a retrospective, population-based cohort study. The Lancet Infectious Diseases. 2019;19(11):1191–1201. doi:10.1016/S1473-3099(19)30260-
- Référence 31
-
Kruijshaar ME, Abubakar I, Stagg HR, Pedrazzoli D, Lipman M. Migration and tuberculosis in the UK: targeting screening for latent infection to those at greatest risk of disease. Thorax. 2013;68(12):1172–1174. doi:10.1136/thoraxjnl-2013-203254.
- Référence 32
-
Ehman M, Shaw T, Cass A, et al. Developing and Using Performance Measures Based on Surveillance Data for Program Improvement in Tuberculosis Control. Journal of Public Health Management and Practice. 2013;19(5):E29–E37. doi:10.1097/0b013e3182751d6f.
- Référence 33
-
Partenariat Halte à la tuberculose, Organisation mondiale de la santé. The Global Plan to Stop TB 2011-2015: Transforming the Fight Towards Elimination of Tuberculosis. Genève, Organisation mondiale de la Santé,
- Référence 34
-
Horsburgh CR, Feldman S, Ridzon R. Practice Guidelines for the Treatment of Tuberculosis. Clinical Infectious Diseases. 2000;31(3):633–639. doi:10.1086/314007.
- Référence 35
-
Curtis E, Jones R, Tipene-Leach D, et al. Why cultural safety rather than cultural competency is required to achieve health equity: a literature review and recommended definition. International Journal for Equity in Health. 2019;18(1):174. doi:10.1186/s12939-019-1082-3.
- Référence 36
-
Fondation canadienne pour l'amélioration des services de santé. Performance Reporting to Help Organizations Promote Quality Improvement. Healthcare Policy | Politiques de Santé. 2008; 4(2):70–74.
- Référence 37
-
Santé Canada. Politique en matière d'analyse comparative fondée sur le sexe et le genre. https://www.canada.ca/fr/sante-canada/organisation/transparence/rapports-gestion/portefeuille-sante-politique-matiere-d-analyse-comparative-fondee-sur-sexe-genre.html. Publié en 2017. Consulté le 27 juillet 2021.
- Référence 38
-
Organisation mondiale de la Santé. Closing data gaps in gender. https://www.who.int/activities/improving-treatment-for-snakebite-patients. Publié en 2019. Consulté le 27 juillet 2021.
- Référence 39
-
Global Health Data Exchange | GHDx. http://ghdx.healthdata.org/. Consulté le 27 juillet 2021.
- Référence 40
-
Gigli KH. Data Disaggregation: A Research Tool to Identify Health Inequities. Journal of Pediatric Health Care. 2021;35(3):332–336. doi:10.1016/j.pedhc.2020.12.002.
- Référence 41
-
Gomes MGM, Barreto ML, Glaziou P, et al. End TB strategy: the need to reduce risk inequalities. BMC Infectious Diseases. 2016;16(1):132. doi:10.1186/s12879-016-1464-8.
- Référence 42
-
Smith A, Herington E, Loshak H. Tuberculosis Stigma and Racism, Colonialism, and Migration: A Rapid Qualitative Review. Ottawa (ON) : Agence canadienne des médicaments et des technologies de la santé; 2021.
- Référence 43
-
Mathema B, Andrews JR, Cohen T, et al. Drivers of Tuberculosis J Infect Dis. 2017;216(suppl_6):S644–S653. doi:10.1093/infdis/jix354.
- Référence 44
-
Kwan CK, Ernst JD. HIV and tuberculosis: a deadly human syndemic. Clinical Microbiology Reviews. 2011;24(2):351–376. doi:10.1128/CMR.00042-10.
- Référence 45
-
Gupta KB, Gupta R, Atreja A, Verma M, Vishvkarma S. Tuberculosis and nutrition. Lung India: Official Organ of Indian Chest Society. 2009;26(1):9–16. doi:10.4103/0970-2113.45198.
- Référence 46
-
Sylla L, Bruce RD, Kamarulzaman A, Altice FL. Integration and co- location of HIV/AIDS, tuberculosis and drug treatment services. International Journal of Drug Policy. 2007;18(4):306–312. doi:10.1016/j.drugpo.2007.03.001.
- Référence 47
-
Zumla A, Malon P, Henderson J, Grange J. Impact of HIV infection on tuberculosis. Postgraduate Medical Journal. 2000;76(895):259–268. doi:10.1136/pmj.76.895.259.
- Référence 48
-
Marais BJ, Lönnroth K, Lawn SD, et al. Tuberculosis comorbidity with communicable and non-communicable diseases: integrating health services and control efforts. The Lancet Infectious Diseases. 2013;13(5):436–448. doi:10.1016/S1473-3099(13)70015-X.
- Référence 49
-
Cormier M, Schwartzman K, N'Diaye DS, et al. Proximate determinants of tuberculosis in Indigenous peoples worldwide: a systematic review. The Lancet Global Health. 2019;7(1):e68–e80. doi:10.1016/S2214-109X(18)30435-2.
- Référence 50
-
Ali M. Treating tuberculosis as a social disease. The Lancet. 2014;383(9936):2195. doi:10.1016/S0140-6736(14)61063-1.
- Référence 51
-
Khan K, Rea E, McDermaid C, et al. Active tuberculosis among homeless persons, Toronto, Ontario, Canada, 1998–2007. Emerging Infectious Diseases. 2011;17(3):357–365. doi:10.3201/eid1703.100833.
- Référence 52
-
Marks SM, Taylor Z, Burrows NR, Qayad MG, Miller B. Hospitalization of homeless persons with tuberculosis in the United States. Am. J. Public Health. 2000;90(3):435–438. doi:10.2105/ajph.90.3.435.
- Référence 53
-
Parriott A, Malekinejad M, Miller AP, Marks SM, Horvath H, Kahn JG. Care Cascade for Targeted Tuberculosis Testing and Linkage to Care in Homeless Populations in the United States: a meta- analysis. BMC Public Health. 2018;18:485. doi:10.1186/s12889-018-5393-x.
- Référence 54
-
Baker MA, Harris AD, Jeon CY, et al. The impact of diabetes on tuberculosis treatment outcomes: a systematic review. BMC Medicine. 2011;9(1):81. doi:10.1186/1741-7015-9-81.
- Référence 55
-
Stevenson CR, Forouhi NG, Roglic G, et al. Diabetes and tuberculosis: the impact of the diabetes epidemic on tuberculosis incidence. BMC Public Health. 2007;7(1):234. doi:10.1186/1471-2458-7-234.
- Référence 56
-
Organisation mondiale de la Santé. Compendium of Indicators for Monitoring and Evaluating National Tuberculosis Programs. Genève, Organisation mondiale de la Santé, 2004.
- Référence 57
-
Henderson DA. The challenge of eradication: lessons from past eradication campaigns. Int J Tuberc Lung Dis 1998;2(12):984-88.
- Référence 58
-
Organisation mondiale de la Santé. Règlement sanitaire international. Genève : WHO Press; 2005.
- Référence 59
-
Centers for Disease TB – National TB Program Objectives and Performance Targets for 2025. Centers for Disease Control and Prevention (CDC). https://www.cdc.gov/tb/programs/evaluation/indicators/default.htm. Publié en 2019. Consulté le 18 septembre 2019.
- Référence 60
-
Bareja C, Waring J, Stapledon R, Toms C, Douglas P. Tuberculosis notifications in Australia. Commun Dis Intell. 2011; 38(4):E356– E368. 2014;
- Référence 61
-
Alaska Department of Health and Social Services. Alaska Tuberculosis Program Manual. 2017.
- Référence 62
-
Minnesota Department of Health. Publié en 2021. https://www.health.state.mn.us/diseases/tb/stats/index.html. Consulté le 6 juillet 2021.
- Référence 63
-
California Department of Public Health. TB Performance Trends for National and California Objectives. 2016.
- Référence 64
-
Heffernan C, Long R. Would program performance indicators and a nationally coordinated response accelerate the elimination of tuberculosis in Canada? Can J Public Health. 2019;110(1):31– doi:10.17269/s41997-018-0106-x.
- Référence 65
-
Chan IHY, Kaushik N, Dobler CC. Post-migration follow-up of migrants identified to be at increased risk of developing tuberculosis at pre-migration screening: a systematic review and meta-analysis. The Lancet Infectious Diseases. 2017;17(7):770–779. doi:10.1016/S1473-3099(17)30194-9.
- Référence 66
-
Long R, Asadi L, Heffernan C, et al. Is there a fundamental flaw in Canada's post-arrival immigrant surveillance system for tuberculosis? PLOS One. 2019;14(3):e0212706. doi:10.1371/journal.pone.0212706.
- Référence 67
-
Ronald LA, Campbell JR, Rose C, et al. Estimated impact of World Health Organization latent tuberculosis screening guidelines in a region with a low tuberculosis incidence: retrospective cohort study. Clin Infect Dis. 2019; 69(12):2101–2108. doi:10.1093/cid/ciz188.
- Référence 68
-
Long R, Ellis E. Agence de santé publique du Canada, Association pulmonaire du Canada, Société canadienne de thoracologie. Normes canadiennes pour la lutte antituberculeuse. 2007.
- Référence 69
-
Rutstein SE, Ananworanich J, Fidler S, et al. Clinical and public health implications of acute and early HIV detection and treatment: a scoping review. J Int AIDS Soc. 2017;20(1):2157 doi:10.7448/IAS.20.1.21579.
- Référence 70
-
Long R, Niruban S, Heffernan C, et al. A 10-year population based study of 'opt-out' HIV testing of tuberculosis patients in Alberta, Canada: national implications. PLoS One. 2014;9(6):e98993. doi:10.1371/journal.pone.0098993.
- Référence 71
-
Bogers SJ, Hulstein SH, Schim van der Loeff MF, et al. Current evidence on the adoption of indicator condition guided testing for HIV in western countries: A systematic review and meta-analysis. EClinicalMedicine. 2021;35:100877. doi:10.1016/j.eclinm.2021.100877.
- Référence 72
-
Organisation mondiale de la santé, ONUSIDA, Fonds mondial, PEPFAR. A Guide to Monitoring and Evaluation for Collaborative TB/HIV Activities-2015 Revisions. Genève : WHO Press; 2015.
- Référence 73
-
Association médicale canadienne. Guidelines for the identification, investigation and treatment of individuals with concomitant tuberculosis and HIV infection. Bureau de l'épidémiologie des maladies transmissibles, ministère de la Santé nationale et du Bien-être social (aujourd'hui Santé Canada). CMAJ. 1993; 148(11):1963–1970.
- Référence 74
-
Long R, Houston S, Hershfield E. Canadian Tuberculosis Committee of the Centre for Infectious Disease Prevention and Control Population and Public Health Branch Health Canada. Recommendations for screening and prevention of tuberculosis in patients with HIV and for screening for HIV in patients with tuberculosis and their contacts. CMAJ. 2003;169(8):789–791.
- Référence 75
-
Haworth-Brockman MJ, Keynan Y. Strengthening tuberculosis surveillance in Canada. CMAJ. 2019;191(26):E743–E744. doi:10.1503/cmaj.72225.
- Référence 76
-
Migliori GB, Nardell E, Yedilbayev A, et al. Reducing tuberculosis transmission: a consensus document from the World Health Organization Regional Office for Europe. Eur Respir J. 2019; 53(6):1900391. doi:10.1183/13993003.00391-2019.
- Référence 77
-
Golub JE, Bur S, Cronin WA, et al. Delayed tuberculosis diagnosis and tuberculosis transmission. The International Journal of Tuberculosis and Lung Disease. 2006;10(1):24–30.
- Référence 78
-
Mitchison DA. Infectivity of patients with pulmonary tuberculosis during chemotherapy. Eur Respir J. 1990; 3(4):385– 386.
- Référence 79
-
LaFreniere M, Dam D, Strudwick L, McDermott S. Tuberculosis drug resistance in Canada: 2018. Can Commun Dis Rep. 2020;46(1):9–15. doi:10.14745/ccdr.v46i01a02.
- Référence 80
-
Benator D, Bhattacharya M, Bozeman L, et al. Rifapentine and isoniazid once a week versus rifampicin and isoniazid twice a week for treatment of drug-susceptible pulmonary tuberculosis in HIV-negative patients: a randomised clinical trial. Lancet (London, England). 2002;360(9332):528–534.
- Référence 81
-
Calderwood CJ, Wilson JP, Fielding KL, et al. Dynamics of sputum conversion during effective tuberculosis treatment: A systematic review and meta-analysis. PLOS Med. 2021;18(4):e1003566. doi:10.1371/journal.pmed.1003566.
- Référence 82
-
Organisation mondiale de la Santé. 8 Tuberculosis Control Programme. 1991.
- Référence 83
-
Hargreaves JR, Boccia D, Evans CA, Adato M, Petticrew M, Porter JDH. The social determinants of tuberculosis: from evidence to action. Am. J. Public Health. 2011;101(4):654–662. doi:10.2105/AJPH.2010.199505.
- Référence 84
-
Veen J. Microepidemics of tuberculosis: the stone-in-the-pond principle. Tuber Lung Dis. 1992;73(2):73–76. doi:10.1016/0962-8479(92)90058-R.
- Référence 85
-
Fox GJ, Dobler CC, Marks GB. Active case finding in contacts of people with tuberculosis. The Cochrane Database of Systematic Reviews. 2011;(9):CD008477. doi:10.1002/14651858.CD008477.pub2.
- Référence 86
-
National Tuberculosis Controllers Association, Centers for Disease Control and Guidelines for the investigation of contacts of persons with infectious tuberculosis. Recommendations from the National Tuberculosis Controllers Association and CDC. MMWR Recomm Rep. 2005;54(RR-15):1–47.
- Référence 87
-
Luzzati R, Migliori GB, Zignol M, et al. Children under 5 years are at risk for tuberculosis after occasional contact with highly contagious patients: outbreak from a smear-positive healthcare worker. Eur Respir J. 2017;50(5):1701414. doi:10.1183/13993003.01414-2017.
- Référence 88
-
Daley CL, Small PM, Schecter GF, et al. An outbreak of tuberculosis with accelerated progression among persons infected with the human immunodeficiency virus. An analysis using restriction-fragment-length polymorphisms. The New England Journal of Medicine. 1992;326(4):231–235. doi:10.1056/NEJM199201233260404.
- Référence 89
-
Agence de la santé publique du Canada. Normes canadiennes pour la lutte antituberculeuse 7e édition : 2014 – Chapitre 12 : Le suivi des contacts et la gestion des éclosions dans le cadre de la lutte antituberculeuse. Publié en https://www.canada.ca/fr/sante-publique/services/maladies-infectieuses/normes-canadiennes-lutte-antituberculeuse-7e-edition/edition-8.html. Consulté le 17 février 2014.
- Référence 90
-
Ai J-W, Ruan Q-L, Liu Q-H, Zhang W-H. Updates on the risk factors for latent tuberculosis reactivation and their managements. Emerging Microbes Infect. 2016;5(2):e10. doi:10.1038/emi.2016.10.
- Référence 91
-
Fox GJ, Dobler CC, Marais BJ, Denholm JT. Preventive therapy for latent tuberculosis infection—the promise and the challenges. International Journal of Infectious Diseases. 2017;56:68–76. doi:10.1016/j.ijid.2016.11.006.
- Référence 92
-
Rangaka MX, Cavalcante SC, Marais BJ, et al. Controlling the seedbeds of tuberculosis: diagnosis and treatment of tuberculosis infection. Lancet. 2015;386(10010):2344–2353. doi:10.1016/S0140-6736(15)00323-2.
- Référence 93
-
Dobler CC, Martin A, Marks GB. Benefit of treatment of latent tuberculosis infection in individual patients. European Respiratory Journal. 2015;46(5):1397–1406. doi:10.1183/13993003.00577-2015.
- Référence 94
-
Kim HW, Kim JS. Treatment of Latent Tuberculosis Infection and Its Clinical Efficacy. Tuberculosis and Respiratory Diseases. 2018;81(1):6–12. doi:10.4046/trd.2017.0052.
- Référence 95
-
Comstock GW, Edwards PQ. The competing risks of tuberculosis and hepatitis for adult tuberculin reactors. Am Rev Respir Dis. 1975;111(5):573–577. doi:10.1164/arrd.1975.111.5.573.
- Référence 96
-
Menzies D, Adjobimey M, Ruslami R, et al. Four months of rifampin or nine months of isoniazid for latent tuberculosis in adults. N Engl J Med. 2018;379(5):440–453. doi:10.1056/NEJMoa1714283.
- Référence 97
-
Macaraig MM, Jalees M, Lam C, Burzynski J. Improved treatment completion with shorter treatment regimens for latent tuberculous infection. Int j Tuberc Lung Dis. 2018;22(11):1344–1349. doi:10.5588/ijtld.18.0035.
- Référence 98
-
Ferebee SH, Mount FW. Tuberculosis Morbidity in a Controlled Trial of the Prophylactic Use of Isoniazid among Household Contacts. American Review of Respiratory Disease. 1962;85(4):490–510.
- Référence 99
-
Molhave M, Wejse C. Historical review of studies on the effect of treating latent tuberculosis. Int J Infect Dis. 2020;92S:S31–S36. doi:10.1016/j.ijid.2020.03.011.