Chapitre 6-10 - Guide canadien sur la biosécurité, Deuxième édition
À partir du 1er avril 2023, la Norme canadienne sur la biosécurité, Deuxième édition (NCB2), auquel ce document fait référence, est désuète. Le Guide canadien sur la biosécurité est en cours de mise à jour afin de refléter la Norme canadienne sur la biosécurité, Troisième édition (NCB3). Nous communiquerons la publication de cette mise à jour dans le bulletin de Nouvelles sur la biosécurité et la biosûreté des agents pathogènes et des toxines.
[Table des matières] [Page suivante]
Chapitre 6 - Biosûreté
Bien que les concepts de la biosécurité et de la biosûreté soient étroitement liés, il est important de bien les différencier, surtout en ce qui concerne les installations où sont manipulées et entreposées des matières infectieuses ou des toxines. Le terme « biosécurité » réfère à l'ensemble des principes, des technologies et des pratiques opérationnelles liés au confinement qui sont mis en application pour prévenir l'exposition non délibérée à des agents pathogènes ou à des toxines, ou leur libération accidentelle; quant au terme « biosûreté », il fait référence aux mesures de sécurité conçues pour prévenir la perte, le vol, l'utilisation malveillante, le détournement et la libération intentionnelle de matières infectieuses ou de toxines. Ces concepts ne sont pas indépendants l'un de l'autre; ils sont plutôt essentiellement complémentaires, car l'utilisation de bonnes pratiques de biosécurité sert à renforcer les programmes de biosûreté, et vice versa.
L'approche à l'égard de la biosécurité et celle à l'égard de la biosûreté sont, dans une même mesure, axées sur les risques et le rendement. Les installations peuvent atteindre les objectifs visés par les exigences réglementaires en appliquant des mesures physiques et des procédures opérationnelles qui leur sont propres. La Norme canadienne sur la biosécurité (NCB), 2e édition, contient les exigences physiques en matière de confinement, les exigences opérationnelles, ainsi que les exigences relatives aux essais de vérification et de performance, minimales en matière de la biosûreté qui sont applicables aux installations canadiennes réglementéesNote de bas de page 1. Le présent chapitre a pour but de présenter les éléments à examiner et les démarches qui permettent la mise en place d'un programme de biosûreté solide.
Il convient de noter que, dans le Guide canadien sur la biosécurité (GCB), le terme « biosûreté » ne réfère pas au concept de « biosûreté agricole », qui est hors de la portée de ce document. La biosûreté agricole désigne les pratiques visant à protéger, à l'échelle canadienne, le bétail et l'approvisionnement alimentaire contre les maladies. Elle se rapporte aux mesures de prévention qui visent à réduire au minimum le risque d'introduction d'une maladie au sein d'une population animale ou végétale et le risque de propagation d'un agent pathogène à l'intérieur d'un lieu déjà infecté.
6.1 Évaluation des risques de biosûreté
La première étape de l'élaboration d'un programme de biosûreté consiste à réaliser une évaluation des risques de biosûreté. Plusieurs ressources sont disponible qui peuvent être utiles pour réaliser de telles évaluations et élaborer des programmes de biosûretéNote de bas de page 2Note de bas de page 3Note de bas de page 4Note de bas de page 5. Le programme de biosûreté varie en complexité et en précision de façon semblable aux autres types d'évaluations des risques décrits dans le GCB (aux chapitres 4 et5), c'est-à-dire en fonction du niveau de risque lié aux agents pathogènes, aux matières infectieuses ou aux toxines présents. On recommande que l'évaluation des risques de biosûreté soit mise à jour au besoin et réexaminée annuellement pour tenir compte des modifications qui influent sur le niveau de risque (c.-à-d. l'introduction d'un nouvel agent pathogène, la construction d'une nouvelle installation). Les mesures énoncées ci-dessous constituent les éléments fondamentaux qui font partie d'une évaluation des risques de biosûreté.
6.1.1 Recenser les ressources et établir les priorités
La première étape de l'évaluation des risques de biosûreté consiste à recenser toutes les « ressources » concernées. Dans le domaine de la biosûreté, le terme « ressource » fait référence à tous les agents pathogènes, à toutes les matières infectieuses et à toutes les toxines qui se trouvent dans l'installation; toutefois, le matériel, l'équipement, les matières non infectieuses, les animaux, les connaissances, l'information, et même les personnes peuvent être reconnus comme des ressources. Au minimum, il est nécessaire de tenir un inventaire des agents pathogènes, des toxines et des autres matières infectieuses réglementées entreposées à long terme (c.-à-d. pendant plus de 30 jours) dans l'installation, en y indiquant le ou les groupes de risque ainsi que l'emplacement. Pour les matières associées à un risque plus élevé (c.-à-d. agents biologiques à cote de sécurité élevée [ABCSE], groupe de risque 3 [GR3] et group de risque 4 [GR4]), il faut mettre en place des mécanismes permettant de détecter rapidement les échantillons manquants ou volés. D'après les pratiques exemplaires, d'autres facteurs (p. ex. la concentration, la quantité et la phase de la matière) peuvent également figurer dans l'inventaire. Avec cette information, il est possible de déterminer le potentiel pour l'utilisation malveillante des agents pathogènes ou des toxines, et la ressource peut être priorisé en fonction des conséquences de cette utilisation malveillante. Il faudrait aussi tenir compte des répercussions de la perte sur les opérations de l'installation.
L'existence d'agents pathogènes et de toxines qui présentent une possibilité de double usage (c.-à-d. dont les propriétés inhérentes lui permettent d'être utilisé de façon légitime dans des applications scientifiques, mais aussi de façon délibérément malveillante pour créer une arme biologique qui cause des maladies chez l'humain ou l'animal) est une préoccupation de premier plan en matière de biosûreté. Dans la Loi sur les agents pathogènes humains et les toxines (LAPHT) et le Règlement sur les agents pathogènes humains et les toxines (RAPHT), les termes « agents pathogènes précisés » et « toxines précisées » désignent les agents pathogènes humains ou les toxines qui présentent un risque de mésusage; dans la NCB et le GCB, on les désigne collectivement par le terme ABCSENote de bas de page 6Note de bas de page 7.
Les ressources sont classées en fonction de leur niveau de risque pour la biosécurité, lequel est établi selon plusieurs facteurs déterminants, notamment les conséquences d'une utilisation à des fins malveillantes, la facilité d'utilisation de la matière ainsi que les répercussions de la perte de la matière pour l'installation.
6.1.2 Définir les menaces
Les personnes, les organisations ou les groupes qui peuvent représenter un risque pour la sécurité des ressources au sein de l'installation (p. ex. vol) doivent être repérés et listés. Ces personnes ou ces groupes sont considérés comme des adversaires ou des menaces. On différencie les menaces externes (c.-à-d. engendrées par une personne non autorisée ou qui n'a pas de droit d'accès aux ressources, à la zone de confinement ou à l'installation; cette personne peut ne pas être liée officiellement à l'installation) des menaces internes (c.-à-d. ;engendrées par le risque de vol ou d'utilisation malveillante des ressources par des personnes autorisées à avoir accès aux ressources dans le cadre de leur travail). Les menaces internes comprennent les employés actuels mécontents, y compris les personnes qui pensent voler, libérer ou détourner des agents pathogènes ou des toxines à des fins malveillantes, et les employés autorisés à accéder aux agents pathogènes et aux toxines qui permettent l'accès aux matières ou fournissent des renseignements à des personnes non autorisées en cédant à la contrainte ou à la manipulation. Les anciens employés, les groupes terroristes, les groupes criminels organisés, les groupes extrémistes de protestation, les personnes souffrant de troubles mentaux et les criminelles opportunistes sont des exemples de menaces externes.
L'évaluation des risques pour la biosûreté comprend l'évaluation des menaces afin de déterminer la possibilité et la manière pour chaque menace d'obtenir, d'endommager ou d'utiliser de manière malveillante les ressources, par exemple les agents pathogènes ou les toxinesNote de bas de page 4. L'analyse des menaces doit tenir compte des motifs, des moyens et des occasions associés à chaque menace. Elle indique également les vulnérabilités, c'est-à-dire les faiblesses existant dans les mesures de sécurité qui peuvent influencer « les moyens et les occasions » pour une menace d'accéder à une ressource et, par conséquent, la probabilité qu'un événement survienne. Les vulnérabilités repérées peuvent faire l'objet de stratégies d'atténuation.
6.1.3 Déterminer les risques et les stratégies d'atténuation
Le niveau de risque en matière de biosûreté est déterminé d'après une analyse du risque associé à chaque ressource (ou à chaque groupe de ressources dotés de caractéristiques semblables) pour chaque menace. Les risques en matière de biosûreté les plus élevés correspondent aux événements ayant les conséquences les plus importantes, même s'il est peu probable qu'ils surviennent, suivis des événements ayant des conséquences modérées qui sont plus susceptibles de survenir.
Les risques peuvent être atténués à l'aide de mesures de sécurité physique, d'une vérification rigoureuse des antécédents du personnel, d'un cadre de responsabilisation clair visant les agents pathogènes et les toxines, de protocoles efficaces d'intervention en cas d'urgence et d'incident ainsi que de mesures de protection de l'information. Les ressources peuvent être gérées en fonction du niveau de risque; ils sont classés ainsi :
- ressources jugés à faible risque d'accès non autorisé nécessitent des mesures de gestion et de contrôle minimes;
- ressources à risque moyen ou élevé d'accès non autorisé et qui nécessitent une gestion et une atténuation des risques modérées;
- ressources à risque très élevé et qui nécessitent des mesures de gestion et de contrôle de grande portée.
La détermination des niveaux de risque acceptables en fonction des scénarios formulés (c.-à-d. la tolérance au risque) et des ressources accessibles pour atténuer les risques incombe à la haute direction de l'organisation. Les stratégies potentielles d'atténuation des risques liés aux vulnérabilités cernées devraient être énoncées, y compris les mesures préventives qui peuvent être instaurées pour réduire les risques relevés. Il est à noter qu'il est possible que les risques cernés soient déjà soumis à des mesures existantes de biosécurité ou de biosûreté. Tout risque non atténué ou jugé acceptable doit être consigné avec une explication de la décision.
Les stratégies d'atténuation qui sont développées afin de protéger contre les risques inacceptables peuvent être utilisées afin de développer un plan de biosûreté qui sera complémentaire au plan de biosécurité.
6.1.4 Énoncés de risque et registres des risques
Un énoncé de risque décrit fidèlement un risque et revêt une importance particulière dans le cadre du processus de gestion des risquesNote de bas de page 8. Les énoncés de risque ont comme objectif de cerner et de consigner les différents risques lors des évaluations des risques de biosûreté. Un énoncé de risque qui traite d'une menace comprend au moins deux éléments : la menace en tant que telle ainsi que ses répercussions négatives potentielles au cas où elle se produirait. Un énoncé de risque (c.-à-d. la menace) peut être formulé de cette façon : « S'il arrive que [la menace], on peut s'attendre à [répercussions négatives] ».
Un registre des risques est un outil de gestion de projet commun pour documenter les résultats de l'évaluation de risque quantitative et qualitative, et la planification de réponse aux risques. Il s'agit essentiellement d'une liste de tous les énoncés de risque décelés et du niveau de risque dans un format facile à examiner, à modifier et à mettre à jour au besoin.Note de bas de page 9
6.2 Plan de biosûreté
Pour toute installation où sont manipulées ou entreposées des matières infectieuses ou des toxines, le plan de biosûreté est un élément clé du programme de biosécurité. Le plan de biosûreté s'appuie sur l'évaluation des risques de biosûreté. Il peut être simple ou complexe en fonction des agents pathogènes, des matières infectieuses ou des toxines dont dispose l'installation, et en fonction de la structure ou de la complexité de l'installation ou de l'organisationNote de bas de page 10. Le plan de biosûreté devrait être axé sur les risques qui sont causés par les menaces internes et externes et jugés inacceptables. Son élaboration devrait suivre un processus collaboratif auquel participent des membres du personnel de l'installation, par exemple des directeurs scientifiques, des chercheurs principaux, des employés de laboratoire, des administrateurs, des responsables des technologies de l'information, des responsables de l'hygiène et de la sécurité au travail, du personnel de sécurité ainsi que du personnel technique. Puisqu'il est possible qu'un programme de sécurité soit déjà en place et prévoie des mesures de biosûreté, il est essentiel que le personnel responsable de la sécurité générale de l'installation participe à la mise en place de ce plan, lequel pourrait aussi bénéficier de la participation des différents corps policiers. Grâce à la révision et à la mise à jour fréquentes du plan de biosûreté, les mesures, les politiques et les procédures liées à la biosûreté demeurent exactes et efficaces pour assurer la biosûreté de façon continue. Les exigences minimales liées aux plans de biosûreté et aux évaluations des risques de biosûreté sont énoncées à la matrice 4.1 de la NCB.
6.2.1 Éléments d'un plan de biosûreté
Après avoir effectué l'évaluation des risques de biosûreté, un plan de biosûreté adapté à l'installation peut être élaboré, exécuté, évalué et sans cesse amélioré au besoin. L'inclusion des éléments du plan de biosûreté au programme général de biosécurité réduira le dédoublement des renseignements et améliorera l'efficacité du système de gestion de la biosécurité. Un plan de biosûreté englobe les éléments ci-dessous. Au minimum, un plan de biosécurité devrait documenter que les risques associés à chaque élément ont été évalué, et décrire les stratégies, s'ils existent ou qui ont été ajouté pour d'atténuer les risques. L'ASPC et l'Agence canadienne d'inspection des aliments (ACIA) ont conçu une ligne directrice supplémentaire qui précise un certain nombre de thèmes de biosécurité présentés dans le GCB et qui sert de ressource pour les intervenants qui veulent obtenir des renseignements additionnels et établir un plan de biosécurité robuste et complet; consultez le site Web de l'ACIA ou de l'ASPC pour de plus amples détails.
6.2.1.1 Sécurité physique
Dans un plan de biosûreté, les éléments de sécurité physiques visent à atténuer le risque qu'une personne non autorisée accède aux ressources recensées ou aux autres matières de nature délicate (c.-à-d. à protéger contre les menaces externes). Les installations devraient adopter des mesures de sécurité physique adéquates afin de réduire au minimum les risques associés à l'entrée non autorisées de personnes aux zones de confinement et à l'accès non autorisée aux matières infectieuses ou aux toxines dans l'installation. L'évaluation des mesures de sécurité physiques devrait comprendre un examen minutieux des lieux, du bâtiment, des zones de confinement et des aires d'entreposage.
Des barrières de sécurité (c.-à-d. des structures matérielles conçues pour prévenir l'entrée de personnel non autorisé), telles que des portes et des fenêtres verrouillées, des systèmes de contrôle d'accès, et des contenants ou de l'équipement d'entreposage sûrs, peuvent être intégrées à l'installation afin de rendre la zone de confinement plus sécuritaire et d'empêcher le personnel non autorisé d'y avoir accès. Il conviendrait d'envisager l'ajout de barrières de sécurité au périmètre de la propriété, au périmètre de l'édifice, au périmètre de l'installation, à la zone de confinement ainsi qu'aux salles et au mobilier qui comportent des agents pathogènes ou des toxines. Les barrières de sécurité aux points d'accès de la zone de confinement (p. ex. portes verrouillables, stations de sécurité ou postes de surveillance dotés de gardiens), les mesures de contrôle de l'accès (c.-à-d. accès limité ou accès restreint), les mécanismes de détection des accès non autorisés ou des tentatives d'accès non autorisé (p. ex. caméras de sécurité, registres tenus grâce à un système électronique de contrôle de l'accès), les barrières de sécurité additionnelles (p. ex. coffrets de sécurité ou congélateurs verrouillables) et l'entretien des barrières de sécurité sont des éléments clés à prendre en considération au moment de déterminer le niveau approprié de sécurité physique. Les exigences de sécurité physique minimales qui s'appliquent aux zones de confinement réglementées sont énoncées aux matrices 3.1, 3.2 et 3.3 de la NCB; quant aux exigences opérationnelles liées à la biosûreté, elles se trouvent aux matrices 4.5 et 4.6 de la NCB.
6.2.1.2 Compétence et fiabilité du personnel
Les directeurs devraient utiliser une procédure d'embauche qui garantit que les candidats qui obtiennent le droit d'accès aux agents pathogènes, aux toxines ou aux autres ressources possèdent la qualification, les aptitudes et les traits de caractère nécessaires à la réalisation des tâches ainsi qu'un profil qui convient parfaitement au poste offertNote de bas de page 11. Les diplômes et les attestations d'études, tout comme l'expérience, peuvent garantir la compétence d'un candidat sur le plan scientifique; cependant, ils ne permettent pas toujours d'évaluer s'il possède les qualités requises pour manipuler des agents pathogènes ou des toxines, ou y avoir accès. Des politiques et des procédures pour prendre compte de la compétence et la fiabilité des employés devraient être établie afin de diminuer le risque de menace interne; les exigences relatives à la formation, à l'expérience, à la compétence et à la fiabilité du personnel qui manipule des matières infectieuses ou des toxines, ou qui y a accès, devraient être clairement définies et consignées. Le processus de présélection des employés est une étape déterminante dans l'évaluation de la compétence du candidat. Des procédures d'approbation et d'attribution des droits d'accès pour les visiteurs pourraient également être requises.
Le recours à un programme d'évaluation continue de la fiabilité permet de vérifier que l'accès aux agents pathogènes et aux toxines accordé à un individu continu à être justifié en fonction des critères établis de compétence du personnel. Ce programme permet aussi de cerner les menaces internes qui proviennent des employés auxquels un droit d'accès avait déjà été accordé. Toute circonstance à risque de compromettre la capacité d'une personne à remplir ses fonctions en toute sécurité peut également exercer une influence sur la validité de l'Habilitation de sécurité en vertu de la Loi sur les agents pathogènes humains et les toxines (LAPHT), notamment : la participation à des activités criminelles; des difficultés financières ou des ennuis avec l'immigration; des changements importants dans le comportement, l'attitude, la conduite ou les agissements (p. ex. l'employé s'isole progressivement, démontre de la colère ou de l'agressivité, s'absente sans justification, semble en état d'ébriété ou sous l'influence de drogues); ou la non-conformité aux politiques et aux lois en vigueur. Des programmes qui permettent de repérer les employés en difficulté et de leur offrir de l'aide peuvent aider à réduire les risques.
6.2.1.3 Responsabilité à l'égard des agents pathogènes, des toxines et de leur inventaire
Des critères de responsabilité à l'égard des agents pathogènes et des toxines sont établis afin de suivre et de consigner les agents pathogènes et les toxines, ce qui comprend tout autre matière infectieuse réglementée présents en entreposage à long terme (c.-à-d. plus de 30 jours) dans la zone de confinement ou dans l'organisation. Ainsi, il est possible de déceler plus rapidement les éléments manquants et de repérer les différentes matières au besoin. Pour prévenir les menaces internes, l'instauration de mesures en matière d'inventaire peut s'avérer une approche fructueuse. Le niveau de précision d'un système d'inventaire est déterminé en fonction des risques associés aux agents pathogènes, aux toxines et aux autres matières infectieuses manipulés ou entreposés. Par exemple, l'inventaire des ABCSE ainsi que des agents pathogènes du GR3 et du GR4 qui sont entreposés à long terme doit être plus détaillé que celui des agents pathogènes du groupe de risque 2 (GR2); les échantillons d'agents pathogènes, de toxines et d'autres matières infectieuses réglementées peuvent ainsi être facilement reconnus et, par conséquent, on peut rapidement les localiser ou en indiquer la perte ou le vol (matrice 4.10 de la NCB). Des dispositions visant à préserver la responsabilité pendant le transport, la réception, la surveillance et l'entreposage des colis qui contiennent des agents pathogènes, des toxines et d'autres matières infectieuses réglementées doivent également être incluses dans le plan de biosûreté. Le chapitre 19 fournit de plus amples renseignements sur la responsabilité à l'égard des agents pathogènes et des toxines ainsi que sur les systèmes d'inventaire qui leur sont liés.
6.2.1.4 Gestion de l'information et sécurité
Des politiques et des procédures en matière de sécurité et de gestion de l'information sont mises en place pour assurer le niveau de confidentialité approprié et prévenir l'accès non autorisé à l'information de nature délicate ou le vol de celle-ci. L'information de nature délicate peut comprendre les plans de sécurité de l'installation, l'information concernant les employés, les codes d'accès, les mots de passe, l'inventaire des matières infectieuses et des toxines ainsi que l'emplacement des aires d'entreposage. Dans certains cas, des renseignements scientifiques peuvent aussi être considérés comme de l'information de nature délicate (p. ex. la procédure de clonage pour reconstituer un virus éteint)Note de bas de page 12. Les politiques sur la gestion de l'information et la sécurité devraient régir la classification et la manipulation de l'information de nature délicate, en plus de dicter la façon dont cette information devrait être recueillie, consignée, transmise, consultée et détruite. La première étape d'atténuation des risques liés à l'usage malveillant de l'information par une menace externe consiste souvent à instaurer des contrôles d'accès adéquats aux renseignements de nature délicate, aux zones de confinement et aux aires associées.
Les mesures de protection de l'information devraient être adaptées au niveau de risque associé aux matières en question. Dans certains environnements de travail, l'accès aux registres et aux documents relatifs aux activités comportant des agents pathogènes ou des toxines est restreint aux seules personnes autorisées (matrice 4.10 de la NCB).
Sur le plan de la sécurité de l'information, des politiques ou des protocoles clairs en ce qui concerne la sécurité de base des technologies de l'information, telles que la création d'un mot de passe fort, la dissuasion ou la restriction de l'utilisation de connexions sans-fil non sécurisées et l'utilisation de réseau privé virtuel (RPV) pour communiquer entre plusieurs bureaux, sont des éléments à prendre en compte. L'utilisation et la surveillance des dispositifs électroniques mobiles comme les tablettes électroniques, les appareils personnels de sauvegarde de données et les appareils photo numériques méritent d'être envisagé comme une vulnérabilité car ils peuvent compromettre la sécurité de l'information. En plus d'être faciles à dissimuler, ils permettent la sauvegarde et le transfert de données sur des supports qui peuvent être amovibles et entreposés de façon indépendante.
6.2.1.5 Intervention en cas d'incident ou d'urgence
Les éléments du plan de biosûreté qui concernent l'intervention en cas d'incident ou d'urgence devraient, pour permettre une plus grande efficacité, être inclus au programme général de biosécurité (c.-à-d. en tant que composante du plan d'intervention d'urgence [PIU]). Par exemple, il est recommandé d'y inclure une procédure d'expulsion des personnes non autorisées. Tous les incidents devraient être déclarés. La déclaration des incidents liés à la biosûreté (p. ex. la perte ou le vol d'agents pathogènes ou de toxines, l'accès non autorisé à de l'information de nature délicate, la perte de clés ou de mots de passe) à l'agent de la sécurité biologique (ASB) devrait être mise de l'avant pour que ces incidents puissent être consignés, visés par une enquête et déclarés de façon appropriée. L'ASB pourrait, en fonction de l'incident, avoir à le déclarer aux organismes locaux d'application de la loi. L'ASB pourrait aussi se voir dans l'obligation de déclarer l'incident à l'Agence de la santé publique du Canada (ASPC) en vertu des conditions liées au permis. Des renseignements supplémentaires au sujet des PIU et des enquêtes sur les incidents se trouvent respectivement aux chapitres 17 et18.
6.3 Habilitations de sécurité en vertu de la Loi sur les agents pathogènes humains et les toxines
L'ASPC a déterminé qu'une habilitation de sécurité délivrée en vertu de la LAPHT constitue une mesure importante de vérification des antécédents des employés. Cette habilitation est en complément aux évaluations de compétence et a le but d'atténuer le risque posé par les menaces internes potentielles dans les installations canadiennes détenant une autorisation visant les activités réglementées comportant la manipulation d'ABCSE. Conformément à la LAPHT, quiconque veut accéder aux locaux de l'installation où sont effectuées des activités réglementées comportant la manipulation d'ABCSE autorisée aux termes d'un permis doit détenir une habilitation de sécurité valide en vertu de la LAPHT délivrée par l'ASPC (LAPHT 33). L'Habilitation de sécurité en vertu de la LAPHT délivrée par l'ASPC exige la vérification approfondie des bases de données des différents corps policiers et des services de renseignements, ainsi qu'une enquête de crédit. Sans habilitation de sécurité valide en vertu de la LAPHT, on peut accéder aux locaux où des activités réglementées comportant la manipulation d'ABCSE ont été autorisées uniquement s'il n'y a pas d'ABCSE dans cette partie de l'installation; si des ABCSE sont présents, mais rangés sous clé et inaccessibles; ou si le non-titulaire est accompagné et supervisé par un titulaire d'une Habilitation de sécurité en vertu de la LAPHT valide visant cette partie de l'installation (LAPHT 33). Le filtrage de sécurité est un élément de biosûreté important du cadre réglementaire découlant de la LAPHT, car il permet d'évaluer la crédibilité et la compétence de tous ceux qui seront autorisés à accéder aux ABCSE. L'Habilitation de sécurité en vertu de la LAPHT ne peut être traitée sans consentement - le filtrage repose sur l'information contenu dans le formulaire de demande de filtrage de sécurité. Les articles pertinents de la LAPHT et du RAPHT sont indiqués aux fins de référence dans la présente section.
6.3.1 Processus d'obtention d'une Habilitation de sécurité en vertu de la LAPHT
Le processus d'obtention d'une Habilitation de sécurité en vertu de la LAPHT comprend une vérification des registres électroniques par la Gendarmerie royale du Canada (GRC) et le Service canadien du renseignement de sécurité (SCRS), ainsi qu'une vérification des antécédents de crédit. La GRC détermine si une personne a un casier judiciaire au Canada et vérifie les registres des organismes d'application de la loi pour savoir si cette personne a participé à des activités criminelles ou si elle est associée à ce type d'activités, ce qui représenterait un risque inacceptable. Le SCRS examine les menaces domestiques et étrangères à la sécurité canadienne que posent les individus et les organismes, et évalue la loyauté du demandeur envers le Canada pour ce qui est des aspects de menaces à la sécurité nationale. En vertu de l'article 12 de la LAPHT, on exige du demandeur d'une habilitation de sécurité qu'il fournisse des renseignements supplémentaires pour appuyer sa demande notamment (mais non exclusivement), une copie de son certificat de naissance, une copie de deux cartes d'identité avec photo émises par un gouvernement, et une déclaration signée par le titulaire qui atteste que le demandeur a besoin d'une Habilitation de sécurité en vertu de la LAPHT pour accéder à un ou des locaux de l'établissement. On demande aussi que ses empreintes digitales soient prises dans un établissement reconnu par la GRC. En ce qui concerne les étrangers, on leur demande également de fournir une copie de leur curriculum vitæ, les résultats d'une vérification du casier judiciaire dans toutes leurs juridictions ainsi qu'une copie de leur visa actuel, le cas échéant.
Au moment de la publication, la norme de service pour la vérification des demandes et la délivrance d'une Habilitation de sécurité en vertu de la LAPHT n'était pas établie. Toutefois, il est estimé que le processus de filtrage de sécurité pourrait prendre jusqu'à 80 jours ouvrables ou plus, mais si une demande est incomplète ou nécessite que la GRC ou le SCRS enquête davantage, le délai peut s'allonger. En vertu du RAPHT, la décision de délivrer, de suspendre, de refuser ou de révoquer une Habilitation de sécurité en vertu de la LAPHT revient au ministre de la Santé ou à ses délégués. Dans le cas où un demandeur est refusé une habilitation de sécurité ou qu'une habilitation de sécurité est révoqué ou suspendu, l'individu peut porter en appel la décision en demandant une révision dans les 30 jours civils suivant la date qu'il a été informé de la décision de suspendre, de refuser ou de révoquer une habilitation de sécurité. Pour obtenir de plus amples renseignements sur le formulaire de demande d'une Habilitation de sécurité en vertu de la LAPHT et le processus d'appel, veuillez visiter le site Web de l'ASPC (www.santepublique.gc.ca/pathogenes).
6.3.2 Exemptions
Il n'est pas nécessaire de détenir une Habilitation de sécurité en vertu de la LAPHT pour accéder aux installations visées par un permis et autorisées à manipuler et à entreposer les toxines précisées à l'annexe 1 de la LAPHT dans des quantités égales ou inférieures à la quantité seuil énoncée à l'article 10(2) du RAPHT. L'Habilitation de sécurité en vertu de la LAPHT n'est pas non plus requise pour accéder à un agent pathogène du GR3 ou du GR4 qui est aussi un ABCSE et qui a été modifié au point où il ne correspond plus à la description du profil de risque dans la définition des groupes de risque respectifs de la LAPHT (p. ex. une souche vaccinale d'un agent pathogène du GR3 atténuée à un point tel que son profil de risque correspond à celui d'un agent pathogène du GR2).
6.3.3 Validité et transférabilité
L'Habilitation de sécurité en vertu de la LAPHT délivrée par l'ASPC est valide pour une durée maximale de cinq ans et autorise son titulaire à accéder aux locaux de l'établissement ou des installations inscrites sur la demande. Elle est délivrée à une personne et est donc transférable entre des installations visées par un permis. Pour qu'un titulaire d'une Habilitation de sécurité en vertu de la LAPHT puisse accéder à une installation qui ne figure pas sur sa demande d'habilitation sans avoir à être accompagné d'une personne autorisée, l'ASPC exigera qu'il lui fournisse une nouvelle déclaration, laquelle sera signée par le titulaire de permis de la nouvelle installation et prouvera qu'une Habilitation de sécurité en vertu de la LAPHT est nécessaire pour accéder à cette installation (RAPHT 18). Dans ce cas, le titulaire d'une Habilitation de sécurité en vertu de la LAPHT ne peut pas accéder à la nouvelle installation visée par un permis tant que l'ASPC n'a pas reçu la déclaration signée par le titulaire de permis. Une déclaration propre à l'installation sera nécessaire chaque fois qu'un titulaire voudra accéder à un nouvel emplacement visé par un permis. Cette mesure s'applique pour toute la période de validité de l'Habilitation de sécurité en vertu de la LAPHT.
6.3.4 Suspension et révocation
Dans le cas où l'ASPC obtient des renseignements qui lui aurait fait refuser la demande d'Habilitation de sécurité en vertu de la LAPHT d'un demandeur, elle suspendra l'Habilitation de sécurité en vertu de la LAPHT visée. La suspension sera en vigueur jusqu'à ce que l'analyse des renseignements en question soit terminée et que la suspension soit levée, ou jusqu'à ce que l'Habilitation de sécurité en vertu de la LAPHT soit révoquée. L'ASPC révoque une Habilitation de sécurité en vertu de la LAPHT lorsqu'elle juge que son titulaire n'est plus approprié.
6.3.5 Déclaration d'infraction criminelle
Un titulaire d'une Habilitation de sécurité en vertu de la LAPHT doit obligatoirement aviser l'ASPC s'il est reconnu coupable d'un acte criminel (RAPHT 19). Une révision de l'Habilitation de sécurité en vertu de la LAPHT d'un individu pourrait être initiée en fonction de la nature de l'infraction. La déclaration peut être transmise électroniquement à l'ASPC par courriel ou à l'aide du formulaire de déclaration des actes criminels qui se trouve sur le site Web de l'ASPC (www.santepublique.gc.ca/pathogenes). La non-déclaration d'une condamnation pour un acte criminel peut se traduire par la suspension ou la révocation de l'habilitation de sécurité délivrée en vertu de la LAPHT.
6.3.6 Accompagnement et supervision
Une personne qui ne détient pas d'Habilitation de sécurité en vertu de la LAPHT peut seulement accéder aux locaux de l'établissement où sont menées des activités autorisées réglementées comportant des ABCSE si elle est accompagnée d'un titulaire d'une Habilitation de sécurité en vertu de la LAPHT pour ces locaux de l'établissement, en plus d'être sous sa supervision (LAPHT 33). Dans ce cas, l'accompagnateur doit détenir une Habilitation de sécurité en vertu de la LAPHT délivrée par l'ASPC; il ne peut accompagner et superviser qu'une personne non-titulaire à la fois (c.-à-d. dans un rapport de un pour un). L'accompagnateur doit se trouver dans la même pièce que le non-titulaire et en surveiller les activités (RAPHT 23); le non-titulaire devrait toujours être dans le champ de vision de l'accompagnateur. Ceux qui ne détiennent pas d'Habilitation de sécurité en vertu de la LAPHT ne sont pas des personnes autorisées et n'ont donc pas accès aux ABCSE sauf s'ils sont sous la supervision directe comme décrit ci-dessus. Celui qui détient une Habilitation de sécurité en vertu de la LAPHT suspendue ou révoquée, ou qui s'est vu refuser la délivrance de celle-ci, ne peut jamais, même s'il est accompagné ou supervisé, accéder aux locaux de l'établissement pour laquelle la tenue d'activités réglementées comportant des ABCSE a été autorisée (RAPHT 24).
6.3.7 Installations partagées
L'accès aux espaces partagés situés dans les locaux de l'installation où sont menées des activités comportant des ABCSE qui sont réglementées et autorisées aux termes d'un permis peut être problématique pour tout le personnel. Les gestionnaires et les directeurs de l'installation ainsi que le titulaire du permis devront déterminer la meilleure façon d'aborder ces enjeux. En somme, deux solutions sont possibles, chacun avec ses avantages et ses défis, selon l'horaire de travail et les aires entreposage sécurisées pour les ABCSE :
- tous les employés qui travaillent dans les espaces partagés sont titulaires d'une Habilitation de sécurité en vertu de la LAPHT valide; ainsi, qu'ils aient besoin de travailler avec les ABCSE ou non, ils peuvent accéder aux locaux de l'installation où ces agents sont présents;
- les non-titulaires d'une Habilitation de sécurité en vertu de la LAPHT (c.-à-d. ceux qui n'ont pas besoin d'avoir accès aux ABCSE) peuvent accéder aux installations partagées seulement dans les cas où :
- il n'y a pas d'ABCSE présent;
- les ABCSE sont mis sous clé et inaccessibles;
- le non-titulaire est accompagné et supervisé par un titulaire d'une Habilitation de sécurité en vertu de la LAPHT valide pour cette partie de l'installation (c.-à-d. ratio de 1 pour 1).
La première solution offre une plus grande souplesse en termes des travaux qui peuvent avoir lieu dans l'espace partagé et quand, mais dépend plus fortement sur des contrôles opérationnels pour gérer le plus grand nombre de personnes ayant accès aux ABCSE. Cette solution a la possibilité d'affaiblir une attitude de sûreté, ce qui pourrait mener à la complaisance (c.-à-d. s'il est supposé que tous ceux qui accède à la salle détiennent une habilitation de sécurité, et que cela implique beaucoup d'individu, le personnel pourrait être moins apte de questionner un inconnu). En revanche, la deuxième solution aborde les défis ci-haut, avec moins de dépendance sur les contrôles opérationnels, et plus sur une planification stricte des activités.
Références
- Note 1
- Gouvernement du Canada. (2015). Norme canadienne sur la biosécurité, 2 e éd., Ottawa, ON, Canada: Gouvernement du Canada.
- Note 2
- CEN Workshop 31 - Laboratory biosafety and biosecurity. CEN Workshop Agreement (CWA) 15793:2011, Laboratory biorisk management. (2011 ). Bruxelles, Belgique: Comité européen de normalisation.
- Note 3
- CEN Workshop 55 - CEN Workshop Agreement (CWA) 16393:2012, Laboratory biorisk management - Guidelines for the implementation of CWA 15793:2008. (2012) . Bruxelles, Belgique: Comité européen de normalisation. (2012).
- Note 4
- Salerno, R. M. et J. Gaudioso. (2007). Laboratory Biosecurity Handbook, Boca Raton, FL, États-Unis : CRC Press.
- Note 5
- Centers for Disease Control and Prevention des États-Unis, Division of Select Agents and Toxins et Animal and Plant Health Inspection Service Agriculture Select Agent Program. (2013). Security Guidance for Select Agent or Toxin Facilities, 2 e révision. Consulté le 3 novembre 2015 à l’adresse http://www.selectagents.gov/resources/Security_Guidance_v3-English.pdf
- Note 6
- Loi sur les agents pathogènes humains et les toxines (L.C. 2009, ch. 24). (2015).
- Note 7
- Règlement sur les agents pathogènes humains et les toxines. (DORS/2015-44). (2015).
- Note 8
- Secrétariat du Conseil du Trésor du Canada. (2014). Guide sur les énoncés de risque. Consulté le 3 novembre 2015 à l’adresse http://www.tbs-sct.gc.ca/tbs-sct/rm-gr/guides/rmg-gertb-fra.asp.
- Note 9
- Travaux publics et Services gouvernementaux Canada. (2014). Modèle de registre des risques - Introduction. Consulté le 3 novembre 2015 à l’adresse http://www.tpsgc-pwgsc.gc.ca/biens-property/sngp-npms/ti-it/rgtenjx-rsklg-fra.html.
- Note 10
- Department of Health and Human Services des États-Unis, Centers for Disease Control and Prevention des États-Unis, Division of Select Agents and Toxins and Department of Agriculture des États-Unis Animal and Plant Health Inspection Service (APHIS) Agriculture Select Agent Program. (2007). Select Agents and Toxins Security Plan Template. Consulté le 3 novembre 2015 à l’adresse http://www.selectagents.gov/resources/Security_Plan_Template_Final_APHIS-CDC-English.pdf
- Note 11
- Centers for Disease Control and Prevention des États-Unis, Division of Select Agents and Toxins and Animal and Plant Health Inspection Service Agriculture Select Agent Program. (2013). Guidance for Suitability Assessments , 2 e révision. Consulté le 3 novembre 2015 à l’adresse http://www.selectagents.gov/resources/Tier_1_Suitability_Guidance_v3-English.pdf
- Note 12
- Tumpey T, Basler C, Aguilar P, Zeng H, Solórzano A, Swayne D, Cox N, Katz J, Taubenberger J, Palese P, García-Sastre A. (2005). Characterization of the Reconstructed 1918 Spanish Influenza Pandemic Virus. Science . 310(5745):77-80.
Chapitre 7 - Programme de surveillance médicale
L’objectif principal d’un programme de surveillance médicale est d’aider à prévenir et à détecter les maladies associées à l’exposition du personnel à des agents pathogènes ou à des toxines. Ce programme est essentiellement axé sur la prévention, mais il prévoit également un mécanisme d’intervention qui permet de détecter une infection potentielle et de la traiter avant qu’une blessure grave, qu’une maladie ou que des transmissions secondaires ne surviennent. La surveillance médicale du personnel qui manipule des agents pathogènes et des toxines peut souvent être intégrée au programme de surveillance médicale déjà en place dans le milieu de travail (p. ex. programmes de santé et de sécurité au travail visant les dangers chimiques ou radiologiques).
Les exigences particulières associées à un programme de surveillance médicale sont énoncées dans la matrice 4.2 de la Norme canadienne sur la biosécurité (NCB), 2e éditionNote de bas de page 1. Le programme de surveillance médicale est mis en œuvre en fonction des résultats d’une évaluation globale des risques et des évaluations locales des risques (ELR), afin de déterminer les agents pathogènes et les toxines manipulés, entreposés ou trouvés dans la zone de confinement ou dans l’organisation, et de déterminer les risques associés. Une description du programme de surveillance médicale est comprise dans le Manuel de biosécurité de la zone de confinement pour que le personnel puisse y avoir accès à des fins de référence. Il est important de mettre à jour le programme de surveillance médicale si des changements sont apportés à un programme de laboratoire (p. ex. lorsque des agents pathogènes ou les toxines différents seront introduits, ou de nouvelles procédures ou activités prendront place). Il pourrait être bon d’associer à l’élaboration du programme de surveillance médicale un professionnel de la santé au travail ou de la santé local (p. ex. médecin, personnel infirmier, hôpital local), ainsi que des intervenants d’urgence (p. ex. professionnels des services locaux d’ambulance, d’incendie et de police), en particulier lorsque les programmes comportent des agents pathogènes présentant un risque élevé.
Le présent chapitre traite d’un certain nombre d’aspects à prendre en considération dans l’élaboration d’un programme de surveillance médicale. Le niveau de détail et la complexité du programme dépendront de la nature de l’organisation (c.-à-d. sa taille, sa structure, sa complexité), des activités associées aux agents pathogènes et aux toxines qui y sont menées et des dispositions des lois applicables associées à la sécurité. Les éléments qui peuvent être pris en considération lors de l’élaboration d’un programme de surveillance médicale comprennent l’examen médical préalable à l’affectation, le dépistage sérologique, les épreuves sérologiques ou l’entreposage de sérum, la vaccination et d’autres examens, selon les résultats d’une ELR.
Le programme de surveillance médicale complète les procédures d’intervention en cas d’urgence médicale, lesquelles font partie du plan d’intervention d’urgence (PIU) d’une installation. Les chapitres 17 et18 fournissent de plus amples renseignements sur les PIU ainsi que sur les rapports d’incidents et les enquêtes sur les incidents, respectivement.
7.1 Expositions en laboratoire et infections (ou intoxications) contractées en laboratoire
Le personnel des secteurs où sont manipulées ou entreposées des matières infectieuses ou des toxines court le risque d’être exposées aux agents pathogènes ou aux toxines, et aux effets néfastes associés à une exposition (c.-à-d. une infection ou une intoxication). Le terme « infection (ou intoxication) contractée en laboratoire », ou « ICL », est communément utilisé pour désigner des maladies associées aux expositions aux matières infectieuses ou aux toxines survenues au travail, à l’intérieur d’un laboratoire. Toutefois, le terme « exposition », traite plus précisément des infections et des intoxications (c.-à-d. le résultat d’une exposition aux toxines), qu’elles soient ou non associées à des symptômes, ainsi que ceux qui pourraient être relié à une zone de confinement mais qui surviennent à l’extérieur d’un laboratoire (p. ex. l’infection d’un employée de bureau dans une installation visée par un permis par un agent pathogène manipulé ou entreposé dans l’installation).
En plus des risques immédiats encourus par les personnes qui manipulent des matières infectieuses, les personnes exposées peuvent présenter un risque pour la santé publique par la transmission des infections à d’autres personnes à l’intérieur ou à l’extérieur du laboratoire. Même s’il peut s’avérer difficile de déterminer les causes fondamentales de l’infection dans tous les cas, les ICL causées par une exposition ne sont pas rares. La plus récente étude épidémiologique exhaustive a recensé 5 527 cas et 204 décès à l’échelle mondiale entre 1930 et 2004 Note de bas de page 2. Même si les ICL surviennent encore et qu’ils sont consignés, l’incidence des ICL semble avoir diminué avec les années, phénomène qui pourrait être attribuable à un renforcement des pratiques de biosécurité, à une meilleure conception de l’équipement et des installations de confinement ou, tout simplement, à une sous-déclaration des incidentsNote de bas de page 3Note de bas de page 4Note de bas de page 5. Malgré cette diminution apparente, on continue d’observer des cas d’exposition et d’ICL, et les professionnels du domaine de la biosécurité peuvent utiliser les données recueillies sur ces incidents pour mieux comprendre et quantifier le risque associé à un agent pathogène donné ou à une activité de laboratoire en particulier. De même, l’information peut ensuite servir à améliorer les normes, les lignes directrices, la formation, l’équipement et les systèmes, et les pratiques exemplaires en matière de biosécurité et de bioconfinement, ainsi que les programmes de surveillance médicale (p. ex. les recommandations en matière d’immunisation, de prophylaxie post-exposition ou de traitement). L’Agence de la santé publique du Canada (ASPC) recueille actuellement des rapports d’incidents sur les ICL et les cas d’exposition à des agents pathogènes ou à des toxines. Les données obtenues seront analysées et mises à profit pour adapter les pratiques actuelles et élaborer les futures pratiques en matière de bioconfinement et de biosécurité au Canada.
L’exposition à une matière infectieuse ou à une toxine n’est pas toujours suivie immédiatement par des symptômes ou une maladie patente. De plus, les ICL peuvent elles-mêmes être associées à des symptômes ou non. Certaines installations peuvent utiliser des pratiques de surveillance médicale qui peuvent déterminer une séroconversion, laquelle peut offrir une source supplémentaire de renseignements pour l’identification ou la confirmation d’infection ou de maladie récente ou antérieure. La séroconversion peut se produire après la première infection et le rejet de l’agent pathogène, et peut indiquer une période de latence après l’infection avant l’apparition de la maladie associée à certains agents pathogènes (p. ex. le virus de l’immunodéficience humaine [VIH], Mycobacterium tuberculosis, virus de l’hépatite C et les prions). Il faut faire preuve d’un bon jugement au moment d’évaluer les données historiques associées aux ICL, car une sous-déclaration des incidents est probable, ce qui compromettrait l’exactitude des calculs statistiques. La sous-déclaration des cas d’exposition et d’ICL peut être attribuée à de nombreux facteurs, notamment :
- l’absence de mécanismes permettant de déclarer les cas d’exposition et d’ICL et de faire les suivis nécessaires;
- l’identification et la déclaration seulement des cas confirmés en laboratoire ou présentant des symptômes;
- le fait que les revues scientifiques ou médicales font peu état des cas d’ICL en raison de contraintes d’espace;
- l’incertitude quant à savoir si une maladie est causée par une exposition survenue dans un laboratoire ou dans la communauté;
- un manque d’intérêt ou de motivation à déclarer les incidents courants ou les incidents qui mettent en cause un agent pathogène fréquemment utilisé;
- la crainte de reproches ou de représailles.
La Loi sur les agents pathogènes humains et les toxines (LAPHT), article 13, exige que toute exposition à des agents pathogènes humains ou à des toxines qui peuvent causer une maladie ou que toute maladie qui pourrait avoir été causée par une exposition à un agent pathogène humain ou à une toxine dans l’installation soit déclarées à l’ASPC sans délaiNote de bas de page 6. Les rapports permettent à l’ASPC d’évaluer la gravité de l’incident d’exposition et, après une demande ou lorsque c’est nécessaire, d’aider l’installation dans ses interventions. L’ASPC peut aussi offrir une expertise et de l’aide au personnel de l’installation dans l’élaboration de mesures correctives pour régler la cause de l’incident et éviter qu’il ne se reproduise. Les renseignements présentés dans un formulaire de notification de l’exposition après un incident d’exposition permettra à l’ASPC de suivre les nouvelles tendances, d’occasionner l’émission d’avis concernant la biosécurité ainsi que de modifier ou de mettre à jour les pratiques exemplaires en matière de biosécurité et de formation, et, par le fait même, d’analyser ces données à l’échelle nationale pour guider les orientations actuelle et future de la biosécurité et du bioconfinement. L’enquête, la consignation et la déclaration locale pour tout type d’incident servent à enregistrer les accidents évités de justesse et les ICL pour lesquelles on ne peut déterminer aucun cas d’exposition évident. Le chapitre 18 fournit de plus amples renseignements sur la déclaration des incidents et les enquêtes sur les incidents.
7.2 Évaluation médicale préalable à l’affectation
Dans certains cas, il pourrait être avantageux que tout employé fait l’objet d’une évaluation médicale préalable à l’affectation. Cette section présente des options à considérer pour la mise en œuvre d’un programme d’évaluation médicale préalable à l’affectation. Une évaluation médicale préalable à l’affectation pourrait être réalisée pour tout nouvel employé, ou tout employé qui reçoit de nouvelles responsabilités, avant d’entreprendre des activités dans le cadre desquelles il pourrait être exposé à des agents pathogènes humains, à des agents pathogènes zoonotiques ou à des toxines. Le but premier d’une évaluation de ce genre est d’évaluer l’état de santé initial de la personne et de déterminer si elle présente des problèmes médicaux sous-jacents qui pourraient accroître le risque associé aux activités prévues dans le cadre de son travail. Cette évaluation peut comprendre un entretien avec le professionnel de la santé au travail de l’établissement ou un questionnaire sur les antécédents médicaux personnels visant à consigner les problèmes médicaux antérieurs et actuels de la personne, les médicaments qu’elle prend actuellement, ses allergies connues à des médicaments, à des animaux ou à des allergènes présents dans l’environnement, ainsi que les vaccins qu’elle a déjà reçus. Les personnes immunodéprimées (p. ex. en raison d’un traitement médical, d’une grossesse, du diabète ou d’autres situations problématiques) peuvent être particulièrement sujettes aux infections ou aux intoxications, être incapables de suivre un traitement après l’exposition, ou être plus gravement atteintes si elles contractent une maladie à la suite d’une exposition à un agent pathogène ou à une toxine. Ce processus nécessite rarement un examen physique complet, mais il pourrait être approprié d’en effectuer un.
Avant toute activité réglementée, on devrait être informé des dangers associés aux agents pathogènes et aux toxines qui seront manipulés, des signes et symptômes des maladies causées par ces agents pathogènes ou ces toxines, ainsi que de toutes les mesures de prévention accessibles, comme des vaccins ou d’autres traitements, ainsi que des risques et des avantages liés à ces mesures. La personne devrait aussi être informée des mesures à prendre en cas d’exposition potentielle, notamment les premiers soins appropriés, la déclaration de l’incident, l’administration rapide de prophylaxie post-exposition et de traitements médicaux. On devrait également décrire aux membres du personnel, dans leur propre intérêt, les premiers signes et symptômes d’une possible infection ou intoxication par les agents pathogènes ou les toxines manipulés, et leur expliquer les mesures immédiates à prendre s’ils présentent ces symptômes. En clinique de diagnostic, il n’est pas toujours possible ou pratique de mentionner aux membres du personnel tous les agents pathogènes qu’ils pourraient rencontrer; en fait, il serait plus raisonnable de les informer des principaux symptômes à prendre en considération dans des situations où les maladies causées par des agents pathogènes inhabituels ont été diagnostiquées en laboratoire.
Avant qu’elles ne commencent à travailler avec les agents pathogènes, les personnes présentant un risque élevé d’exposition pourraient être encouragées à fournir un échantillon de sang, qui servira à la réalisation d’épreuves sérologiques, puis sera entreposé. Cet échantillon pourrait être entreposé à long terme et servir ultérieurement à déterminer si la personne est déjà immunisée parce qu’elle a été vaccinée ou infectée dans le passé, et à établir la séroréactivité de base à des fins de comparaison avec d’autres échantillons sanguins qui seraient recueillis à la suite d’une exposition potentielle.
7.3 Vaccination
Les vaccins sont des produits biologiques complexes fortement réglementés; ils visent à provoquer de manière efficace et sûre une réponse immunitaire protectrice. La disponibilité des vaccins et d’autres agents prophylactiques doit être évaluée et ces traitements devraient être offerts au personnel, au besoin, avant le début du travail comportant la manipulation d’un agent pathogène. Un dosage périodique des anticorps devrait être effectué après la vaccination, afin de déterminer si la protection immunitaire conférée est suffisante et soutenu, et si une dose de rappel est nécessaire. Si une personne refuse de recevoir un vaccin ou ne présente pas de réponse immunitaire à un vaccin qui est jugé nécessaire pour obtenir l’autorisation de travailler dans une zone de confinement, il pourrait s’avérer nécessaire d’envisager la réévaluation de l’affectation de cette personne, l’ajout de contrôles des paramètres environnementaux ou l’utilisation d’équipement de protection individuel (EPI).
D’autres recommandations sur la vaccination peuvent être obtenues auprès des professionnels de la santé spécialistes de ce domaine ou auprès du Comité consultatif national de l’immunisation (CCNI). Le CCNI est un comité consultatif national constitué d’experts en sciences médicale et de la santé qui formule des recommandations à l’ASPC sur l’utilisation des vaccins au Canada, notamment sur l’identification des groupes à risque (p. ex. groupes professionnel, groupes d’âge) en ce qui concerne les maladies évitables par la vaccination. Toutes les recommandations du CCNI sont publiées dans le Guide canadien d’immunisation, et d’autres déclarations et mises à jour sont publiées dans le Relevé des maladies transmissibles au Canada (RMTC)Note de bas de page 7Note de bas de page 8.
7.4 Surveillance médicale continue
La surveillance médicale continue du personnel courant des risques d’exposition aux agents pathogènes ou aux toxines peut donner une indication de l’exposition professionnelle. Le superviseur devrait encourager les membres du personnel à communiquer, sans la crainte de représailles, tout changement de leur état de santé qui pourrait augmenter de manière considérable leur risque d’exposition ou de maladie. Il pourrait notamment s’agir d’un déficit immunitaire ou d’une situation temporaire, comme la nécessité de prendre des antibiotiques, de troubles de la vue ou même de stress. Les évaluations médicales systématiques ou périodiques ne sont généralement pas nécessaires; cependant, ces évaluations pourraient être appropriées dans le cas d’employés qui courent un risque important d’être exposées à des agents pathogènes ou à des toxines, car elles pourraient permettre la détection précoce d’une infection qui pourrait être causée par une exposition en laboratoire. Des essais cliniques (p. ex. épreuves sérologiques) exigés par un conseiller médical ou un médecin devraient être limités à des examens approuvés offerts sur le marché et suffisamment sensibles pour détecter une infection actuelle ou antérieure (c.-à-d. la séroconversion). Les échantillons de sérum prélevés au moment de l’évaluation préalable à l’affectation peuvent être utilisés pour déterminer les valeurs de référence, ou valeurs « préexposition », pour tout examen à effectuer dans le cadre du programme de surveillance médicale. Bien que seuls les patients reçoivent les résultats de leurs examens médicaux, les personnes qui découvrent une infection ou une séroconversion possiblement causées par une exposition qui peut être liée à un laboratoire ont l’obligation d’en informer leur superviseur ou les autorités internes de l’organisation (c.-à-d. l’agent de la sécurité biologique [ASB], le titulaire de permis), qui, à leur tour, ont l’obligation légale d’en informer l’ASPC (LAPHT 13).
7.5 Plan d’intervention post-exposition
Les plans d’intervention post-exposition énoncent les procédures à suivre et les mesures à prendre en cas d’exposition connue, soupçonnée ou potentielle à un agent pathogène ou à une toxine (p. ex. la déclaration, les examens médicaux et le traitement), et ils pourraient faire partie d’un PIU général. Dans les zones de confinement où l’on manipule ou entrepose des agents pathogènes ou des toxines, on peut établir un plan d’intervention post-exposition en consultation avec le professionnel de la santé au travail ou le médecin, le comité institutionnel de biosécurité (CIB), l’ASB ainsi que le conseiller en santé et en sécurité au travail. Le chapitre 18 fournit de plus amples renseignements sur la déclaration des incidents et les enquêtes sur les incidents.
7.6 Points additionnels à prendre en considération au sujet du confinement élevé
Toute exposition professionnelle potentielle qui se produit dans une zone de confinement élevé (c.-à-d. niveau de confinement 3 [NC3]; ce qui comprend les zones de confinement de gros animaux [zone GA] de NC3 [NC3-Ag]; ou niveau de confinement 4 [NC4]) devrait faire l’objet d’une évaluation immédiate, puisqu’une infection par un agent pathogène à risque élevé pourrait causer une maladie grave ou la mort. Les agents pathogènes manipulés dans les zones de NC4 sont souvent exotiques, et une ICL représenterait une grave menace pour la communauté. Dans les zones de confinement élevé, il est particulièrement important de s’assurer que l’ensemble du personnel, y compris le personnel de l’installation et le personnel de soutien, respecte toutes les procédures et tous les protocoles de surveillance médicale. Il est fortement recommandé qu’un spécialiste des maladies infectieuses participe à l’élaboration du programme de surveillance médicale, y compris l’évaluation des risques, les évaluations préalables à l’affectation et l’élaboration du plan d’intervention post-exposition. De plus, il est requis pour les zones de NC4 (matrice 4.2 de la NCB), et fortement recommandé pour les zones de NC3 et les zones de confinement de gros animaux (zones GA) de NC3 (NC3-Ag), que le plan d’intervention post-exposition soit élaboré en consultation avec les établissements de santé locaux, afin de tenir les professionnels de la santé informés des agents pathogènes qui sont manipulés. On recommande également que les procédures et les traitements appropriés soient en place. Des procédures spécifiques concernant la mise en quarantaine du personnel potentiellement infecté pourraient devoir être établies avant qu’une exposition ne se produise. Dans les zones de NC4, il est aussi requis que le superviseur communique avec tout employé de la zone de confinement dont l’absence n’était pas prévue pour déterminer si une maladie qui pourrait être associée aux activités avec les agents pathogènes utilisés en est la cause (matrice 4.2 de la NCB).
7.7 Carte de contact en cas d’urgence médicale
Afin d’offrir un moyen de faciliter la communication entre le personnel de laboratoire, les professionnels de la santé et d’autres personnes, particulièrement lors de situations d’urgence, l’employeur fournit une carte de contact en cas d’urgence médicale aux membres du personnel qui travaillent avec des primates non humains (PNH), ceux qui travaillent avec des agents pathogènes ou des toxines qui sont responsables de maladies peu susceptibles d’être reconnues par un médecin, et tout le personnel des zones de NC4. La carte devrait contenir des renseignements importants sur les agents pathogènes ou les toxines manipulées par la personne, tels que les voies d’infection ou d’intoxication, de transmission, les symptômes et les traitements préventifs et thérapeutiques. Cette mesure est également recommandée pour le personnel des zones de NC3 et les zones GA de NC3 (NC3-Ag). En cas de maladie inexpliquée, cette carte peut être présentée au personnel de l’hôpital ou de l’établissement de soins ou aux intervenants d’urgence. Le superviseur de la zone de confinement devrait préciser dans quelles circonstances le personnel devrait avoir la carte en sa possession (p. ex. lorsqu’il se trouve dans l’installation à l’exception de la zone de confinement, ou tout au long de la période au cours de laquelle on mène une étude comportant un agent pathogène particulier). Il incombe à l’installation de déterminer les circonstances dans lesquelles les employés doivent avoir cette carte en leur possession. Un exemple de carte de contact en cas d’urgence médicale est présenté à la figure 7-1.
Figure 7-1 : Exemple de carte de contact en cas d’urgence médicale
RECTO

VERSO

Équivalent textuel - Figure 7-1
Cette figure illustre le recto et le verso d’une carte de contact en cas d’urgence médicale. Le recto de la carte indique le nom du titulaire de la carte, la date d’émission, ainsi que les matières infectieuses et les toxines manipulées par le titulaire, et elle précise si le titulaire travaille ou non avec des primates non humains. L’énoncé suivant y figure également : « L’employé(e) de laboratoire doit avoir cette carte en sa possession et la remettre à un médecin s’il (ou si elle) présente des symptômes pouvant être associés à un agent pathogène utilisé dans le cadre de ses fonctions. (Voir verso.) » Le verso de la carte indique le nom et l’adresse de l’installation où travaille le titulaire, ainsi que le nom et les numéros de téléphone au travail et à domicile de deux personnes‑ressources à joindre en cas d’urgence. On y trouve aussi l’énoncé suivant : « À l’intention du médecin – L’employé(e) travaille dans un milieu où des microorganismes pathogènes sont présents. Veuillez communiquer avec les personnes ci‑dessous pour obtenir des renseignements sur les agents auxquels l’employé(e) a pu être exposé(e). »
Références
- Note 1
- Gouvernement du Canada. (2015). Guide canadien sur la biosécurité, 2 e éd., Ottawa, ON, Canada : Gouvernement du Canada.
- Note 2
- Harding, A. L. et Brandt Byers, K. (2006). Epidemiology of Laboratory-Associated Infections. Dans Fleming, D. O. et Hunt, D. L. (éds), Biological Safety: Principles and Practices, 4e éd., p. 53-77, Washington, DC, États-Unis: ASM Press.
- Note 3
- Singh K. (2011). It's time for a centralized registry of laboratory acquired infections. Nature Medicine. 17(8):919.
- Note 4
- Singh K. (2009). Laboratory-Acquired Infections. Cinical Infectious Diseases. 49:142-147.
- Note 5
- Willermarck N., Van Vaerenbergh B., Descamps E., Brosius B., Dai Do Thi C., Leunda A., Baldo A. et Herman P. (2015). Laboratory-Acquired Infections in Belgium (2007-2012). Consulté le 3 novembre 2015 à l’adresse http://www.biosafety.be/CU/PDF/2015_Willemarck_LAI%20report%20Belgium_2007_2012_Final.pdf
- Note 6
- Loi sur les agents pathogènes humains et les toxines. (L.C. 2009, ch. 24). (2015).
- Note 7
- Agence de la santé publique du Canada. (2014). Guide canadien d’immunisation, éd. Evergreen. Consulté le 3 novembre 2015 à l’adresse http://www.phac-aspc.gc.ca/publicat/cig-gci/index-fra.php
- Note 8
- Agence de la santé publique du Canada. (2014). Relevé des maladies transmissibles au Canada. Consulté le 3 novembre 2015 à l’adresse http://www.phac-aspc.gc.ca/publicat/ccdr-rmtc/index-fra.php
Chapitre 8 - Programme de formation
Un programme de formation est essentiel à la réussite d'un programme de biosécurité. Il est très important que le personnel soit informé des dangers présents dans le milieu de travail ainsi que des pratiques et des outils qui peuvent les protéger contre ces dangers. Ce type de programme comprend à la fois de l'éducation et de la formation. L'éducation a trait au processus qui consiste à fournir des renseignements généraux ou des connaissances théoriques. On peut former le personnel sur les dangers liés au travail en ayant recours à diverses méthodes, notamment des cours magistraux, des présentations vidéo, l'apprentissage en ligne, la formation en cours d'emploi et la distribution de documents imprimés, tels que des manuels, des Fiches techniques santé-sécurité : agents pathogènes (FTSSP) et des affiches. La formation est de nature pratique et elle est propre à l'emploi; elle comprend la démonstration des pratiques et des procédures. Ces deux concepts complémentaires sont fondamentaux dans la mise sur pied d'un programme de formation solide. La responsabilité de veiller à ce que le personnel de la zone de confinement reçoive une formation adéquate incombe généralement à un superviseur ou le directeur de l'installation. L'agent de la sécurité biologique (ASB) ou le responsable de la biosécurité joue un rôle dans la promotion et la surveillance de la formation portant sur les politiques, les normes et les pratiques en matière de biosécurité et de biosûreté afin qu'elle soit mise en place et consigné dans les installations réglementées où des agents pathogènes humains, des agents zoopathogènes et des toxines sont manipulés et entreposés conformément au Règlement sur les agents pathogènes humains et les toxines (RAPHT) [RAPHT 9(1)(c)(i)] et à la Norme canadienne sur la biosécurité (NCB), 2e éditionNote de bas de page 1Note de bas de page 2. Les éléments devant être inclus dans un programme de formation sur la biosécurité sont exposés dans la matrice 4.3 de la NCB.
8.1 Besoins et objectifs en matière de formation
Le contenu exact du programme de formation varie d'une organisation à l'autre, et même d'une zone de confinement à l'autre, à l'intérieur d'une même installation. Une évaluation des besoins en matière de formation est la première étape de la mise en œuvre d'un programme de formation efficace. Cette évaluation vise à cerner les besoins actuels et futurs du personnel de l'installation en ce qui concerne la formation, ainsi que les lacunes du programme de formation existant. Les résultats de l'évaluation des besoins en matière de formation devraient constituer le point de départ de l'établissement des objectifs d'apprentissage, de la sélection et de la conception des programmes d'apprentissage, de la mise en œuvre des programmes, de la détermination de la fréquence du perfectionnement et de l'évaluation de la formation offerte. L'évaluation des besoins devrait tenir compte des risques cernés dans le cadre des évaluations des agents pathogènes et des risques liés à la biosûreté, ainsi que des problèmes spécifiques pouvant être atténués par la formation.
Le Manuel de biosécurité décrit les principaux éléments du programme de biosécurité, y compris les buts et les objectifs du programme de formation. Les objectifs devraient être mesurables et devraient définir clairement les comportements ou les compétences que les participants devraient avoir appris au cours de la formation.
8.2 Contenu du programme de formation
Tous les programmes de formation ont un certain nombre d'éléments et d'exigences en commun. Le fait d'associer le programme de formation sur la biosécurité et celui sur la biosûreté aux autres exigences du milieu de travail en matière de formation pourrait être avantageux et s'avérer une façon efficace d'utiliser les ressources. Les employés qui suivent la formation sur le Manuel de biosécurité et les procédures opératoires normalisées (PON) doivent bien connaître le contenu de ce manuel, notamment le plan de biosûreté et le plan d'intervention d'urgence (PIU). Les employés qui démontrent qu'ils connaissent et peuvent appliquer correctement les PON sur lesquelles ils ont suivi une formation seront en mesure de manipuler de façon sécuritaire les agents pathogènes et les toxines qu'ils trouveront dans leur milieu de travail et d'intervenir en conséquence lors d'une situation d'urgence.
La formation concernant les dangers qui pourraient être associés au travail effectué est particulièrement importante et peut comprendre les éléments suivants :
- Information sur la nature des matières infectieuses et des toxines qui sont utilisées dans le milieu de travail ainsi que sur la façon de les identifier;
- Signes et symptômes des maladies causées par une exposition aux agents pathogènes que les employés manipuleront. Dans les installations où une vaste gamme d'agents pathogènes pourraient être manipulés (p. ex. installations de diagnostic), une approche plus vaste pourrait être envisagée (c.-à-d. formation sur les signes et les symptômes généraux préoccupants plutôt que sur les symptômes associés à chaque agent pathogène);
- Pratiques de travail sécuritaires et mesures physiques de contrôle, notamment en ce qui concerne la manipulation et l'élimination des matières infectieuses ou des toxines (c.-à-d. décontamination et gestion des déchets), ainsi que le choix, l'utilisation et l'entretien adéquats de l'équipement de protection individuel (EPI);
- Information sur les renseignements pertinents en matière de sécurité (p. ex. FTSSP) et sur la façon de les trouver et de les utiliser;
- Information sur les exigences législatives et réglementaires s'appliquant aux activités comportant les matières infectieuses ou les toxines en question.
Il existe un grand nombre de ressources d'enseignement et de formation pouvant aider à l'élaboration d'un programme de formation. L'Agence de la santé publique du Canada (ASPC) et l'Agence canadienne d'inspection des aliments (ACIA) offre des matières d'apprentissage, y compris des cours de formation sur la biosécurité (p. ex le cours en ligne Principes de la biosécurité en laboratoire), des modèles, des boîtes à outils, des affiches, des vidéos d'instruction, et plus encore, le tout disponible sur le portail de la biosécurité de l'ASPC (www.santepublique.gc.ca/formation).
8.2.1 Formation sur la biosûreté
Pour établir et entretenir le sens de la responsabilité et de la sensibilisation à la sécurité, il est essentiel que tout le personnel suit la formation sur la biosûreté, laquelle peut comprendre les éléments suivants :
- sensibilisation aux menaces internes et aux menaces externes;
- comportements préoccupants;
- repérage et expulsion d'une personne suspecte;
- politiques concernant l'accès aux agents biologiques à cote de sécurité élevée (ABCSE);
- procédures relatives à l'accompagnement;
- procédures d'auto-déclaration et de déclaration par les pairs;
- mesures correctives, procédures et politiques;
- sécurité de l'information;
- politiques sur la sécurité, y compris :
- procédures d'entrée et d'accès, et prévention du talonnage;
- prévention du partage des moyens d'accès individuel;
- déclaration de la perte ou d'un risque d'utilisation abusive d'un mot de passe;
- façon de repérer et de déclarer des personnes ou des activités suspectes;
- gestion de l'inventaire des documents et des registres;
- intervention en cas d'alarme;
- intervention en cas d'infraction à la sécurité.
8.2.2 Formation sur les systèmes et les dispositifs de confinement
Les programmes de formation doivent comprendre des renseignements sur les éléments de la conception physique de la zone de confinement et des systèmes de confinement qui sont pertinents à l'individu en formation (matrice 4.3 de la NCB). Afin d'éviter un bris de confinement, la formation devrait aussi inclure une révision des types de dispositifs de confinement primaire et des systèmes de confinement associés à la zone de confinement, un aperçu de la façon d'identifier lorsqu'ils fonctionnent correctement et quand ils sont défectueux.
Là où des systèmes de confinement secondaires (p. ex. les systèmes de confinement de secours) ont été intégrés dans la zone de confinement, la formation devrait comprendre une révision du fonctionnement de ces systèmes. Le programme de formation doit réviser l'utilisation et l'exploitation adéquates des systèmes de confinement, des dispositifs de confinement primaires et d'autre équipement de laboratoire, pour qu'ils soient utilisés correctement et continuent de protéger le personnel contre la libération d'un agent pathogène ou d'une toxine, ou l'exposition à ceux-ci. Le personnel doit démontrer qu'il connaît et peut appliquer correctement les PON sur lesquelles il a été formé, y compris les PON pour l'utilisation correcte des systèmes, des dispositifs et des autres équipements de confinement. Des exemples de dispositifs de confinement primaires et de systèmes de confinement qui devraient être révisés lors de la formation en biosécurité comprennent notamment :
- enceintes de sécurité biologique (ESB);
- systèmes de chauffage, ventilation et air climatisé (CVAC);
- technologie de décontamination (p. ex. autoclaves, systèmes de décontamination des effluents, cuves d'immersion);
- systèmes de cages de confinement primaire utilisés dans des zones de confinement de petits animaux (zone PA);
- centrifugeuses;
- équipements de laboratoire et appareil utilisé pour des activités avec des agents pathogènes et des toxines.
8.3 Choix des participants
La détermination des destinataires cibles est un élément clé de la conception d'un programme de formation, puisqu'elle permet de déterminer les besoins exacts en matière de formation ainsi que le type de formation convenant le mieux aux styles d'apprentissage des destinataires.
8.3.1 Nouveaux employés
La mise en œuvre d'un programme d'orientation pour les nouveaux employés leur donne l'information nécessaire avant d'être exposés aux dangers liés au travail. La formation offerte aux nouveaux employés devrait comprendre tous les éléments énumérés à la section 8.2 du présent chapitre, ainsi que tous les autres sujets pertinents (p. ex. révision de l'historique de l'organisation, programme de sécurité, politiques, droits et responsabilités du personnel, renseignements généraux sur le Système d'information sur les matières dangereuses utilisées au travail [SIMDUT]). De la formation pratique en cours d'emploi, une supervision et des directives supplémentaires devraient être données pendant la période d'emploi initiale de tout nouvel employé. En plus de la formation officielle, l'expérience pratique de travail compte pour beaucoup. Les stagiaires peuvent exécuter des activités comportant des matières infectieuses et des toxines à l'intérieur de la zone de confinement, à condition qu'ils soient supervisés par des personnes autorisées.
8.3.2 Personnel de laboratoire existant
La formation est un processus continu et, par conséquent, ne se limite pas aux nouveaux employés. Il est possible que le personnel existant ait besoin de recevoir des renseignements ou de la formation sur les nouvelles procédures, le travail dans un nouvel environnement ou encore la manipulation de matières infectieuses ou de toxines nouvelles. La formation d'appoint, offerte à une fréquence fondée sur une évaluation des besoins en formation ou lorsqu'un changement dans le programme de biosécurité le justifie, contribue à tenir à jour les connaissances du personnel au sujet des dangers, des risques, des ressources et des mesures de contrôle dans le milieu de travail. Une formation d'appoint annuelle sur les procédures d'intervention d'urgence doit être offerte (matrice 4.3 de la NCB). La formation d'appoint est aussi une occasion de communiquer au personnel toute nouvelle information sur les matières infectieuses ou les toxines utilisées, ainsi que de le mettre au courant des modifications apportées aux pratiques recommandées ou aux exigences réglementaires.
8.3.3 Autres membres du personnel
Le programme de formation doit s'appliquer à tous les membres du personnel qui ont accès à la zone de confinement, et non pas seulement à ceux qui manipulent des matières infectieuses et des toxines. Les visiteurs, les entrepreneurs, ainsi que les employés des services de nettoyage, de sécurité et d'entretien, doivent recevoir une formation sur les dangers, les risques et les mesures de contrôle, en fonction des activités prévues, et faire l'objet d'une supervision par des membres autorisés du personnel pendant qu'ils mènent des activités dans une zone de confinement (matrice 4.3 de la NCB).
8.3.4 Conditions d'apprentissage
L'intégration des principes d'apprentissage des adultes dans la conception des programmes d'éducation et de formation sur la biosécurité contribuera au succès du programme. Ces principes peuvent comprendre la motivation, le renforcement, la conservation et l'application des compétences et des connaissances déjà acquises. Étant donné que les styles d'apprentissage varient d'une personne à l'autre, une gamme d'outils et de méthodes d'enseignement sont recommandés afin d'atteindre le plus grand nombre de personnes. La formation est plus efficace si des outils d'éducation variés sont utilisés, par exemple un exposé combiné à des aides visuelles, des présentations vidéo, des didacticiels d'autoformation et des activités de résolution de problèmes. Le fait de participer dans des simulations et des exercices d'intervention d'urgence renforcent les connaissances et les compétences acquises au moyen des autres méthodes d'enseignement. Les formateurs devraient aussi prendre en compte les questions liées à l'accessibilité, par exemple les barrières linguistiques ou la déficience auditive de certains participants, et s'adapter en conséquence.
8.4 Évaluation de la formation
Une variété de méthodes peut être utilisée pour évaluer l'assimilation des connaissances et des compétences transmises dans un programme de formation. La méthode d'évaluation qui est choisie (p. ex. examen écrit, évaluation pratique) devrait permettre de mesurer efficacement le perfectionnement et l'acquisition de connaissances chez celui qui reçoit la formation. Les examens ou les questionnaires administrés avant et après la formation sont des outils utiles pour évaluer l'atteinte des objectifs d'apprentissage. L'évaluation des pratiques et des comportements en milieu de travail, au moyen d'audits de l'installation, d'inspections ou d'une surveillance régulière par les superviseurs, peut aussi donner une indication utile de la mesure dans laquelle la formation a été comprise et de la nécessité d'offrir ou non du perfectionnement ou de revoir le programme de formation. Des formulaires d'évaluation de la formation peuvent être remis à la fin d'un cours ou d'une séance de formation pour solliciter les commentaires des participants. Cette méthode permet d'obtenir des commentaires précieux, notamment sur l'efficacité du contenu du cours, le ou les formateurs et les méthodes d'enseignement utilisées, et elle peut contribuer à l'amélioration du programme de formation.
Un examen annuel (ou périodique) de la performance des personnes qui ont accès aux agents pathogènes humains, aux agents zoopathogènes et aux toxines permet d'évaluer leur respect et leur compréhension des procédures de biosécurité et de biosûreté. L'examen annuel offre l'occasion au superviseur d'examiner et de renforcer l'importance de la biosécurité et de la biosûreté, de discuter des exigences de la Loi sur les agents pathogènes humains et les toxines (LAPHT), le RAPHT, la Loi sur la santé des animaux (LSA), le Règlement sur la santé des animaux (RSA) et la NCB, et de se pencher sur tout problème possible qui ont déjà eu, ou pourrait avoir, une incidence sur le rendement au travail,Note de bas de page 3Note de bas de page 4Note de bas de page 5.
8.5 Registres sur la formation
Les registres sur la formation et le perfectionnement font état de la participation à la formation et indiquent si celle-ci a été complétée avec succès. Ils peuvent contenir des feuilles de présence, des aide-mémoire, des examens, des certificats ou d'autres types de registres (p. ex. une description de la formation avec les signatures du participant, du formateur et du superviseur) jugés pertinents par l'organisation. Pour faciliter le suivi du perfectionnement nécessaire, on indique dans ces registres : la date du cours ou de la formation; le nom des participants ou des stagiaires; et le type ou le nom du cours ou de la formation. Les registres sur la formation et le perfectionnement en matière de biosécurité peuvent être combinés à ceux de la formation en santé et en sécurité au travail, le cas échéant. Tous les registres sur la formation et le perfectionnement devraient être tenus à jour, et la version la plus récente devrait être conservée (c.-à-d. si la formation est répétée ou actualisée, ou si un cours d'appoint est donné, on ne conserve que les renseignements les plus récents d'une personne donnée). Les périodes de conservation minimales pour les registres de formation se trouvent dans la matrice 4.10 de la NCB. On utilisera ces registres pour déterminer les besoins en matière de formation d'appoint.
8.6 Examen du programme de formation
L'évaluation régulière du contenu du programme de formation aidera à déterminer les secteurs qui ont besoin d'une mise à jour pour faire en sorte qu'il demeure exact et pertinent. Il est recommandé que le programme soit revu et mis à jour au moins une fois par année ou dès qu'on apporte des changements aux conditions de travail, aux procédures, aux dangers ou à l'information sur les dangers. L'examen des programmes de biosécurité et de biosûreté devrait aussi comprendre un examen des registres sur la formation et le perfectionnement, de manière à mesurer la performance du programme de formation (p. ex. fréquence des séances de formation, nombre de participants, variété des thèmes et des programmes). Cet examen permettra d'adapter les ressources de manière à optimiser le programme de formation.
Références
- Note 1
- Règlement sur les agents pathogènes humains et les toxines. (DORS/2015-44). (2015).
- Note 2
- Gouvernement du Canada. (2015). Norme canadienne sur la biosécurité, 2 e éd., Ottawa, ON, Canada: Gouvernement du Canada.
- Note 3
- Loi sur les agents pathogènes humains et les toxines (L.C. 2009, ch. 24). (2015).
- Note 4
- Loi sur la santé des animaux (L.C. 1990, ch. 21). (2015).
- Note 5
- Règlement sur la santé des animaux (C.R.C., ch. 296). (2015).
Chapitre 9 - Équipement de protection individuel
L'équipement de protection individuel (EPI) fait référence aux dispositifs et aux vêtements conçus pour réduire au maximum le risque d'exposition à divers dangers. L'EPI demeure le dernier moyen de défense pour protéger le personnel et réduire au minimum le risque de transmission d'agents pathogènes et de toxines au public et à la population animale. L'EPI aide à prévenir la dissémination d'agents pathogènes et des toxines sur les individus contaminés (ou leurs vêtements) en créant une barrière entre la personne et les matières infectieuses et les toxines manipulés ou entreposés. L'EPI devrait être le dernier élément de contrôle appliqué, puisqu'il constitue une barrière additionnelle pour se protéger contre l'exposition aux matières dangereuses en cas de défaillance des mesures de contrôle administratives ou des mesures d'ingénierie. Les exigences en matière d'EPI sont énoncées à la matrice 4.4 de la Norme canadienne sur la biosécurité (NCB), 2e éditionNote de bas de page 1.
Au Canada, la santé et la sécurité au travail sont réglementées à l'échelle provinciale, territoriale et fédérale, et les exigences relatives à l'EPI ont été intégrées dans les lois pertinentes sur la santé et la sécurité au travail. L'employeur est chargé de veiller à ce que l'EPI approprié soit disponible et à ce qu'il soit entretenu et utilisé adéquatement; il est également responsable de s'assurer que le personnel soit adéquatement formé pour se servir de l'EPI. Les exigences relatives à l'EPI énoncées dans la NCB portent précisément sur la biosécurité et ne visent pas à remplacer les lois provinciales ou territoriales, ni les exigences de la réglementation locale sur la santé et la sécurité au travail. Le présent chapitre offre des recommandations sur les différents types d'EPI et l'utilisation générale de l'EPI habituellement porté dans les zones de confinement où sont manipulées ou entreposées des matières infectieuses et des toxines.
9.1 Types et choix d'équipement de protection individuel
L'EPI peut comprendre des appareils de protection respiratoire, des dispositifs de protection des mains, des pieds, de la tête et des yeux, et des combinaisons de protection complète du corps. Le choix d'un EPI se fonde sur une évaluation locale des risques (ELR) de la zone de confinement et est propre au travail à réaliser.
9.1.1 Protection des mains
Les gants protègent les mains contre la contamination et réduisent les risques associés à l'ingestion (p. ex. transfert des mains à la bouche) ou à l'absorption par la peau. Les gants constituent une barrière protectrice lorsqu'on manipule des matières infectieuses, des toxines, des animaux infectés ou du matériel potentiellement contaminé par un agent pathogène ou une toxine (p. ex. tissus, cultures, sang et liquides organiques). Les gants peuvent être fabriqués de différents matériaux et devraient être choisis en fonction d'une activité ou d'un danger en particulier; pour la manipulation de matières infectieuses ou de toxines, les gants devraient être propres, jetables et résistant aux liquides.
La résistance des gants aux liquides est influencée par les conditions d'utilisation, notamment la nature et la concentration des substances chimiques employées, la durée d'utilisation, la température, le stress physique et l'épaisseur du matériau du gantNote de bas de page 2. Le tableau 9-1 présente les recommandations générales concernant les matériaux des gants couramment utilisés pour travailler avec des agents pathogènes, des matières infectieuses, des toxines ainsi que des désinfectants chimiques uniquement en fonction des données sur la compatibilité chimique. La compatibilité des matériaux des gants avec une substance chimique peut être évaluée à l'aide de la mesure du temps écoulé entre l'exposition de la surface externe d'un gant à un produit chimique et la détection de la substance à l'intérieur du gant (c.-à-d. le temps de protection); de la mesure de la vitesse à laquelle un produit chimique traverse le matériau du gant (c.-à-d. le taux de perméation) et de l'évaluation de la dégradation des propriétés physiques (p. ex. la fragilisation, l'assouplissement, le gonflement) du matériau du gant à la suite de l'exposition aux substances chimiquesNote de bas de page 3.
| Type de désinfectant | Désinfectant chimique | Latex de caoutchouc naturel | Caoutchouc synthétique | Polymère de plastique | |
|---|---|---|---|---|---|
| Néoprène | Nitrile | Polychlorure de vinyle (PVC) | |||
| Agents oxydants | Hypochlorite de sodium (<15 %) | B | B | P | TB |
| Iode | B | B | B | B | |
| Peroxyde d’hydrogène (30 %) | TB | TB | TB | TB | |
| Hydroxyde de sodium (50 %) | TB | TB | TB | TB | |
| Hydroxyde d’ammonium | B | B | B | TB | |
| Phénoliques | Hexachlorophène | B | B | B | -- |
| Composés ammoniés quaternaires | Chlorure de N,N-didécyl N,N-diméthyle ammonium | B | B | TB | -- |
| Aldéhydes | Glutaraldéhyde (25 %) | TB | TB | TB | TB |
| Formaldéhyde (37 % dans 1/3 méthanol/eau) | P | B | TB | TB | |
| Alcools | Éthanol (92 %) | P | TB | TB | B |
| Alcool isopropylique | B | TB | TB | TB | |
| Bisbiguanides | Digluconate de chlorhexidine (4 %) | P | P | TB | -- |
|
|||||
Outre la compatibilité chimique, on devrait tenir compte du niveau de réduction de la dextérité ou de la susceptibilité aux perforations associées au matériau du gant. Des gants antistatiques peuvent être nécessaires lors de la manipulation de toxines lyophilisées. En général, le port de gants en latex, en nitrile ou en vinyle permet d'empêcher efficacement les mains d'être exposées aux matières infectieuses ou aux toxines. Les gants résistant aux coupures ou à la perforation protègent bien les mains en cas de risque de coupure, de morsure, de piqûre ou d'abrasion accidentelles.
9.1.1.1 Port de gants doubles
Bien que la plupart des matériaux couramment utilisés pour la fabrication des gants forment une barrière convenable contre les matières infectieuses et les toxines, ils ne demeurent pas toujours imperméables. Les gants peuvent s'user, se percer ou se déchirer, et ne plus offrir une protection suffisante avec le temps. Le port de deux paires de gants jetable résistants au liquide réduit considérablement la détérioration du gant interneNote de bas de page 8. Dans certaines situations, il est parfois recommandé de porter deux paires de gants, et dans les zones de confinement élevé, il est indiqué d'en porter deux paires, selon l'ELR.
9.1.1.2 Protection contre les dangers physiques
Il est important de vérifier que le matériau dans lequel les gants sont fabriqués procure une protection efficace contre les dangers, avant de manipuler des matières dangereuses (c.-à-d. compatible avec les désinfectants ou les solvants utilisés). Par exemple, les gants en latex, en nitrile et en vinyle offrent peu ou pas de protection contre les dangers physiques, comme les températures extrêmes (p. ex. chaleur d'un autoclave, froid de l'azote liquide), ou contre les objets pointus ou tranchants (p. ex. aiguilles, scalpels, dents d'animaux). Dans ces situations, des gants faits d'autres matériaux ou une paire additionnelle de gants conviendraient. Les gants résistants à la chaleur composés de tissu éponge ou de laine protègent contre les températures élevées, et les gants de nylon doublés de tricot jersey ou de coton protègent contre les basses températures. Pour se protéger contre les objets pointus ou tranchants, les coupures ou les morsures, les gants en fibre para-aramide ou en maille d'acier inoxydable offrent une protection efficace. Pour certaines activités, il peut être nécessaire de les combiner avec des gants imperméables pour obtenir une protection suffisante.
9.1.2 Protection des pieds
Les chaussures protectrices visent à fournir une barrière efficace contre les agents pathogènes et les toxines potentiels présents dans les zones de confinement. Ils protègent notamment contre les déversements de matières infectieuses ou de toxines, et les blessures résultant d'une chute, d'un trébuchement, d'un écrasement ou d'une perforation, tous susceptible d'entrainer ou d'augmenter le risque d'entrainer une exposition à un agent pathogène ou une toxine, ce qui pourrait conduire à des infections ultérieurs chez la population humaine ou animale. Les chaussures complètement fermées protègeront tout le pied d'une exposition à des liquides dangereux dans l'éventualité d'un déversement. Le risque de trébuchement ou de chute accidentelle peut être réduit par le port de chaussures sans talons ou à talons plats, ou munies d'une semelle antidérapante dans les aires où la surface de marche est souvent humide ou glissante. Le port de chaussures à embout d'acier protège contre les blessures par écrasement lorsqu'on travaille avec des objets lourds ou de gros animaux. Dans le cas des activités dans lesquelles on utilise des objets tranchants ou pointus, les chaussures dotées de semelles résistantes à la perforation offrent une protection contre les blessures par perforation. Les chaussures fabriquées de matériaux non absorbants seront faciles à nettoyer et à désinfecter. Le port de chaussures à usage réservé limite la dispersion des matières infectieuses ou soupçonnées de l'être se trouvant sur les chaussures hors de la zone de confinement.
Les couvre-chaussures jetables et imperméables offrent une couche de protection supplémentaire contre la contamination par des liquides. Les couvre-bottes réutilisables peuvent être portés, à condition que des procédures de décontamination appropriées soient en place. Des bottes en caoutchouc, utilisées conjointement avec des pédiluves, peuvent aussi être portées par le personnel pour se protéger dans les zones où de grands volumes d'eau seront employés (p. ex. décontamination de box, nettoyage de cages). Dans les salles animalières, les box et les salles de nécropsie, on peut porter une protection supplémentaire comme les couvre-bottes dans les zones de confinement où l'on héberge des petits animaux et des bottes de caoutchouc ou d'autres chaussures de sécurité dans les box et les salles de nécropsie des zones où l'on héberge des gros animaux.
Outre les exigences énoncées à la matrice 4.4 de la NCB, les chaussures protectrices devraient être conformes à la norme de l'Association canadienne de normalisation (CSA) CSA-Z195, Chaussures de protection, s'il y a lieuNote de bas de page 9.
9.1.3 Protection de la tête
Certaines activités au cours desquelles on manipule des matières infectieuses ou des toxines sont associées à un risque d'exposition attribuable à des vaporisations ou des éclaboussures, ou à des agents pathogènes ou des toxines en suspension dans l'air. Ce risque peut être réduit par le port d'un bonnet ou d'un dispositif de protection de la tête (p. ex. bonnet bouffant résistant aux liquides) qui protège les cheveux et le cuir chevelu d'une contamination. Le cas échéant, les dispositifs protégeant la tête devraient être conformes à la norme CSA Z94.1, Casques de sécurité pour l'industrie : tenue en service, sélection, entretien et utilisationNote de bas de page 10.
9.1.4 Protection des yeux et du visage
Il existe de nombreux types de dispositifs de protection des yeux et du visage qui protègent les yeux, le nez ou la bouche des objets projetés ou des éclaboussures de liquides infectieux ou de toxines. Le type de protection des yeux et du visage choisi dépendra du degré de protection nécessaire à l'accomplissement de la tâche. Les lunettes de sécurité protègent les yeux des blessures associées aux objets d'une certaine taille, tels que les copeaux, les fragments, le sable, la saleté et les éclaboussures mineures. Les lunettes à coques offrent un degré de protection supérieur en raison de l'ajustement serré au-dessus et autour des yeux, qui forme une barrière contre les liquides dangereux. Les visières protègent le nez, la bouche et la peau en plus des yeux. Selon le type de dispositif de protection des yeux ou du visage choisi, les lunettes à verres correcteurs peuvent être portées sous le dispositif en question; les lunettes de sécurité peuvent aussi avoir des verres correcteurs. Pour ce qui est des personnes portant des lentilles cornéennes, certaines activités peuvent être associées à un risque supplémentaire en cas d'exposition ou de blessure des yeux. En cas d'exposition ou de lésion des yeux, on pourra intervenir rapidement et convenablement si l'on dispose d'un moyen permettant de déceler les porteurs de lentilles cornéennes. Les dispositifs de protection des yeux et du visage peuvent être réutilisés, s'ils ont été bien décontaminés après avoir entrés en contact avec des matières infectieuses ou des toxines. Les dispositifs de protection à usage unique qui ont été utilisés sont considérés comme des déchets contaminés.
Le cas échéant, les dispositifs de protection des yeux et du visage devraient être conformes aux normes CSA Z94.3, Protecteurs oculaires et faciaux, et CSA Z94.3.1, Sélection, utilisation et entretien des lunettes de protectionNote de bas de page 11Note de bas de page 12. Selon la norme CSA Z94.3, on considère que les visières sont des dispositifs de protection secondaire et n'offrent une protection oculaire adéquate que lorsqu'elles sont portées avec des lunettes de sécurité ou des lunettes à coques.
9.1.5 Protection du corps
Le sarrau est le type d'EPI le plus couramment utilisé pour protéger le corps et les vêtements personnels contre la contamination par des matières infectieuses. Les sarraus qui descendent jusqu'au genou et qui couvrent le bras jusqu'aux poignets protègent la peau et les vêtements d'une exposition aux matières dangereuses. Les sarraus ajustés au corps et avec des manches à poignets élastiques risquent moins de traîner et de s'accrocher durant le travail de laboratoire. Les boutons-pression sont préférables aux boutons, car, en cas d'urgence, ils permettent de retirer rapidement le sarrau. Il existe sur le marché des sarraus à usage unique (c.-à-d. jetables) ou réutilisables ainsi que des sarraus ignifuges et imperméables. Ces derniers fournissent une protection accrue contre les flammes ou les liquides dangereux. Portés et gardés les sarraus ou autres vêtements de protection uniquement dans les aires prévues, à l'intérieur de la zone de confinement, évite la contamination des zones « propres ».
Le port de vêtements personnels appropriés contribue également à la protection du corps. Le port de vêtements qui couvrent les jambes jusqu'aux chevilles confère une protection. Les shorts, les jupes et les autres vêtements qui laissent certaines parties des jambes exposées sous le sarrau ne devraient pas être portés dans la zone de confinement.
9.1.5.1 Autres couches de vêtements protecteurs
Pour obtenir une protection accrue lors du travail avec des matières infectieuses, des toxines ou des animaux infectés par des agents pathogènes zoonotiques, on peut porter une couche additionnelle d'EPI à usage réservé. Cette couche additionnelle peut comprendre une deuxième paire de gants, un bonnet, une blouse ne s'ouvrant pas à l'avant avec poignets serrés à porter par-dessus les vêtements de laboratoire à usage réservé, une combinaison recouvrant le corps en entier, des couvre-manches jetables ou un tablier imperméable porté par-dessus un sarrau s'ouvrant ou non à l'avant. Une blouse ne s'ouvrant pas à l'avant et s'attachant à l'arrière habituellement porté par-dessus des vêtements à usage réservé (p. ex. tenue de bloc opératoire) au lieu d'un sarrau de laboratoire, protège le torse et peut être porté lors du travail avec des récipients ouverts contenant des matières infectieuses ou des toxines. Une tenue de bloc opératoire peut être portée sous la couche externe de vêtements protecteurs pour prévenir la contamination des vêtements personnels en cas de déchirure de la couche externe de protection. La tenue de bloc opératoire fait généralement partie de l'EPI à usage réservé utilisé dans les zones de confinement élevé ou les salles animalières et les box, car elle peut être stérilisée et nettoyée en vue d'une nouvelle utilisation. Les blouses chirurgicales destinées aux salles d'opération comportent une couche de tissu imperméable, et les pans à l'arrière se superposent et s'attachent à l'aide de rubans pour offrir une protection accrue. Les tabliers sont fréquemment portés dans les salles de nécropsie par-dessus le sarrau ou la blouse; ils offrent une protection additionnelle contre les déversements ou les éclaboussures de matières infectieuses ou de toxines. Les combinaisons recouvrant le corps entier fournissent une protection additionnelle et peuvent être fabriquées de matériaux jetables ou réutilisables. Les personnes qui travaillent avec de gros animaux portent généralement une combinaison pour se protéger contre les matières organiques. Les matériaux qui entrent dans la composition des combinaisons, tels que les fibres de polyéthylène à haute densité soumises à un filage éclair, le tissu caoutchouté, le PVC et le néoprène forment une bonne barrière, car ils sont difficiles à déchirer ou à perforer et bloquent les contaminants biologiques, chimiques et particulaires.
9.1.5.2 Combinaisons à pression positive
Les combinaisons à pression positive offrent une protection maximale de tout le corps (c.-à-d. de la tête aux orteils) contre l'environnement de la zone de confinement, et elles sont dotées de bottes, de gants et d'un casque. L'approvisionnement en air respirable est assuré par un tuyau d'alimentation raccordé à la combinaison, qui crée une pression positive à l'intérieur de celle-ci. Des essais d'intégrité sont effectuer pour vérifier que les combinaisons sont étanches aux gaz (c.-à-d. pas de déchirure ni fuite) et peuvent maintenir une pression positive stable lorsqu'elles sont ventilées.
9.1.6 Masques et protection respiratoire
Les pratiques opérationnelles sécuritaires et l'utilisation de dispositifs de confinement primaire peuvent limiter la formation d'aérosols infectieux ou de toxines aérosolisées et réduire l'exposition à ceux-ci. Les masques chirurgicaux et de nombreux types de masques antipoussières offrent peu de protection contre les agents pathogènes aéroportés, les aérosols infectieux et les toxines aérosolisées, mais ils protègent les muqueuses du nez et de la bouche contre les déversements et les éclaboussures. Les masques n'ont pas été conçus pour être utilisés plus d'une fois. Les appareils de protection respiratoire sont employés en présence d'un risque d'exposition à des toxines aérosolisées ou à des aérosols infectieux qui peuvent être inhalés. On dispose de deux types d'appareils : les appareils de protection respiratoire à épuration d'air et les appareils de protection respiratoire à approvisionnement en air. Le type d'appareil de protection respiratoire dépend des risques associés à l'activité exercée. La formation du personnel sur les matières dangereuses aéroportées et sur le choix, l'ajustement, l'inspection et l'entretien d'un appareil de protection respiratoire sont des exemples d'éléments pouvant faire partie d'un programme de protection respiratoire mis en œuvre en milieu professionnel, programme obligatoire dans tous environnements de travail dans lequel on utilise des appareils de protection respiratoire. Le cas échéant, les appareils de protection respiratoire devraient être conformes à la norme CSA Z94.4, Choix, utilisation et entretien des appareils de protection respiratoireNote de bas de page 13.
9.1.6.1 Vérifications de l'ajustement de l'appareil de protection respiratoire
Les appareils de protection respiratoire doivent être bien ajustés à la figure pour fonctionner adéquatement. Pour assurer une bonne protection, certains types d'appareils nécessitent un joint d'étanchéité entre l'appareil et le visage. Il est autant dangereux de porter le mauvais appareil ou de mal le porter que de ne pas en porter du tout. L'appareil devrait être choisi et ajusté en fonction du visage de l'utilisateur, et l'étanchéité après ajustement devrait être vérifiée. Les poils faciaux, les imperfections de la peau, le maquillage et les variations de poids peuvent avoir des effets sur l'ajustement. Au Canada, la plupart des provinces et des territoires exigent la réalisation d'essais d'ajustement qualitatifs ou quantitatifs garantissant le bon ajustement du ou des appareils choisis avant que l'utilisateur s'adonne aux activités nécessitant le port de ces appareils. De plus, la norme CSA Z94.4, Choix, utilisation et entretien des appareils de protection respiratoire, précise que l'employeur doit s'assurer que la personne est médicalement autorisée à porter un appareil de protection respiratoire. L'utilisation et l'entretien appropriés des appareils de protection respiratoire sont une composante clé du programme de formation dans les lieux de travail où ces appareils sont portés.
9.1.6.2 Appareils de protection respiratoire à épuration d'air
Les appareils de protection respiratoire à épuration d'air aident à réduire la concentration de microorganismes et de particules dans l'air inhalé par l'utilisateur pour le ramener à un degré d'exposition acceptable en faisant passer l'air à travers un filtre à particules ou une cartouche chimique. Les demi-masques à épuration d'air recouvrent le nez et la bouche, mais non les yeux, tandis que les masques complets recouvrent le visage entier. Les demi-masques à épuration d'air jetables, dont les masques N95 et N100, sont destinés à un usage unique. Les demi-masques et les masques complets de protection respiratoire à ventilation non assistée peuvent être munis de cartouches filtrantes jetables de sorte qu'ils offriront un degré de protection similaire. Les appareils de protection respiratoire à ventilation non assistée créent une pression négative à l'intérieur du masque pendant l'inhalation. Le National Institute of Occupational Safety and Health (NIOSH) des États-Unis a approuvé neuf classes de filtres à particules à utiliser avec les appareils de protection respiratoire à ventilation non assistée, à savoir les filtres de la série N (N95, N99 et N100; non résistants à l'huile), de la série R (R95, R99 et R100; résistants à l'huile) et de la série P (P95, P99, P100; à l'épreuve de l'huile)Note de bas de page 14. Les numéros indiquent l'efficacité de l'élimination des contaminants. Les masques portant la cote N95 ou une cote supérieure protègent suffisamment le personnel au cours de la plupart des activités menées avec des microorganismes.
9.1.6.3 Appareils de protection respiratoire à épuration d'air motorisés
Les appareils de protection respiratoire à épuration d'air motorisés (APRM) créent une pression positive autour de la tête de l'utilisateur. Ces appareils sont destinés à être décontaminés et réutilisés, et les cartouches filtrantes doivent être remplacées régulièrement, selon l'ELR. Les filtres à particules de ces appareils sont tous à haute efficacité (HE), ce qui veut dire qu'ils retiennent au moins 99,97 % des particules les plus pénétrantes (0,3 µm) selon leur certification. Compte tenu des effets de l'impaction, de la diffusion et de l'interception, les filtres à haute efficacité pour les particules de l'air (HEPA) sont encore plus efficaces contre les particules dont la taille est inférieure ou supérieure à 0,3 µmNote de bas de page 15. La plupart des filtres de ces appareils retiennent les aérosols à base d'huile, mais certains ne le font pas; l'utilisateur devrait consulter les directives du fabricant avant d'utiliser un appareil de protection respiratoire dans un environnement où se trouvent des particules contenant de l'huile.
9.1.6.4 Appareil de protection respiratoire à approvisionnement d'air
Les appareils de protection respiratoire à approvisionnement d'air fournissent de l'air propre et respirable provenant d'une source, telle qu'une bouteille d'air comprimé ou un réservoir. Il s'agit généralement d'appareils de protection respiratoire à adduction d'air, mais il peut également s'agir d'appareils respiratoires autonomes (ARA). L'air des appareils à adduction d'air provient d'un petit tuyau raccordé à un compresseur d'air ou à une bouteille d'air comprimé, tandis que les appareils autonomes fournissent de l'air respirable provenant d'une bouteille portée sur le dos.
9.2 Éléments clés à prendre en considération lors du choix de l'équipement de protection individuel
Il n'existe aucun type de gants ou d'appareil de protection respiratoire pouvant offrir une protection contre tous les différents dangers présents dans un milieu de travail. Le port d'un EPI inapproprié peut avoir des répercussions sur le rendement du personnel (p. ex. des gants rigides ou encombrants peuvent réduire la dextérité et la capacité de manipuler des objets), ce qui crée un risque d'accident et peut entraîner l'exposition à des dangers. Dans les lieux de travail où des matières infectieuses ou des toxines sont manipulées, une ELR doit être menée avant toute chose pour établir des pratiques de travail sécuritaires et choisir le bon EPI. Le choix de l'EPI dépend du niveau de confinement, de la quantité et du type de matières infectieuses ou de toxines utilisées ainsi que de la nature des activités. Cette évaluation devrait être effectuée par l'agent de la sécurité biologique (ASB) ou autre personnel compétent (c.-à-d. un spécialiste de la prévention des infections ou d'hygiène du travail) et l'employé concerné, éventuellement en consultation avec l'employeur, le comité de biosécurité de l'établissement ainsi que le comité de santé et de sécurité au travail. Une fois qu'on a établi la nécessité d'un EPI, l'équipement est choisi en fonction du degré de protection nécessaire et de la pertinence de l'équipement dans le contexte (p. ex. gants qui permettent une bonne dextérité, vêtements et chaussures qui offrent une bonne protection). Par exemple, dans les zones de confinement de gros animaux (zones GA), où le box offre le confinement primaire et que l'EPI est la principale protection contre une exposition à des agents pathogènes et à des toxines, il est essentiel que l'employé choisisse son EPI en conséquence. Il importe que l'employé joue un rôle dans le choix de l'EPI, pour garantir un ajustement et un confort satisfaisants et favoriser le port. Une fois l'EPI choisi, l'employé devrait recevoir la formation nécessaire sur la bonne utilisation de l'EPI, notamment les situations dans lesquelles l'EPI doit être porté, la marche à suivre pour l'enfiler et le retirer correctement, ses limites, son entretien, sa décontamination et son élimination.
De nombreux facteurs liés aux risques doivent être pris en considération dans le choix de l'EPI approprié, mais on doit aussi tenir compte des allergies et d'ergonomie. Les allergies à certains matériaux (p. ex. le latex des gants) peuvent parfois poser plus de risques pour la santé que les dangers eux-mêmes. L'ajustement et le confort sont des facteurs importants à considérer pour régler les problèmes d'ergonomie potentiels; le personnel peut être tenté de retirer l'EPI s'il est inconfortable ou mal ajusté. Au moment de choisir l'EPI qui sera utilisé lors de la manipulation de gros animaux, il faudrait songer à opter pour de l'équipement léger, aéré, qui n'entrave pas les déplacements, qui n'a pas tendance à s'accrocher sur le matériel ni à s'emmêler et qui ne sera pas endommagé par les animaux.
9.3 Utilisation de l'équipement de protection individuel
9.3.1 Enfilage de l'EPI
Le protocole d'enfilage de l'EPI décrit l'ordre particulier dans lequel il faut enfiler chacun des articles. Les procédures opératoires normalisées(PON) sur l'enfilage de l'EPI avant de pénétrer dans des espaces de travail en laboratoire, des salles animalières, des box, des salles de nécropsie ou des zones de confinement sont élaborées en fonction de l'ELR et varient en complexité selon le type d'EPI porté. Il est important que ces PON soient comprises et suivies par tous les employés. Le rangement de l'EPI à tous les points d'entrée courants de la zone de confinement facilite l'accès à l'EPI pendant la préparation précédant l'entrée dans la zone. Les employés devraient vérifier soigneusement si les dispositifs ou vêtements présentent une détérioration avant de les enfiler. Voici l'ordre d'enfilage préconisé dans les zones de confinement qui nécessitent seulement le port d'un sarrau et de gants :
- Une seule paire de gants et un sarrau
- Ordre d'enfilage
- Sarrau (bien attaché)
- Gants (portés par-dessus les poignets du sarrau)
- Ordre de retrait
- Gants
- Sarrau
- Ordre d'enfilage
- Deux paires de gants et un sarrau
- Order de retrait
- Première paire de gants
- Sarrau (bien attaché)
- Deuxième paire de gants (portés par-dessus les poignets du sarrau)
- Ordre de retrait
- Deuxième paire de gants
- Sarrau
- Première paire de gants
- Order de retrait
Les zones GA de Niveau de confinement 2 (NC2) (c.-à-d. les zones NC2-Ag) et les zones de confinement élevé sont munies de vestiaires utilisés pour séparer les vêtements personnels des vêtements réservés à la zone de confinement, ou pour séparer des vêtements protecteurs réservés aux différents espaces de confinement (c.-à-d. zone de confinement d'animaux par opposition à un box). Voici un exemple de protocole d'enfilage d'un EPI à plusieurs couches. Les vêtements personnels (y compris les sous-vêtements lorsqu'une douche est exigé à la sortie) et les accessoires, notamment les bijoux et les cartes d'identité, sont retirés et gardés dans un espace réservé à cette fin avant l'enfilage de l'EPI.
- EPI à plusieurs couches
- Ordre d'enfilage
- Vêtements réservés à la zone de confinement, par exemple tenue de bloc opératoire, des chaussures réservées à la zone, des couvre chaussures et un bonnet
- Première paire de gants
- Sarrau se fermant à l'arrière ou couche de vêtement protecteur équivalente
- Masque ou appareil de protection respiratoire
- Dispositif de protection des yeux, notamment les lunettes de sécurité, les lunettes à coques ou une visière
- Deuxième paire de gants, portés par-dessus les poignets du sarrau
- Ordre de retrait
- Deuxième paire de gants
- Dispositif de protection des yeux
- Masque ou appareil de protection respiratoire
- Sarrau se fermant à l'arrière ou couche de vêtement protecteur équivalente
- Première paire de gants
- Vêtements réservés à la zone de confinement
- Ordre d'enfilage
Selon la nature des activités menées dans la zone de confinement, le personnel doit se conformer à des exigences particulières qui pourraient être affichées aux points d'entrée, avant de pénétrer dans la zone de confinement, par exemple sur la nécessité de porter certains dispositifs d'EPI. L'EPI et l'ordre d'enfilage peuvent être différents selon le contexte (p. ex. travail dans une zone GA de niveau de confinement 3 [c.-à-d. NC3-Ag] ou une salle de nécropsie où l'ELR préconise le port d'un APRM).
9.3.2 Retrait de l'EPI
Il est important de retirer ou d'enlever l'EPI soigneusement afin de réduire au minimum le risque de contamination de la peau et des cheveux. Les PON sur le retrait de l'EPI à la sortie des espaces de travail en laboratoire, des salles animalières, des box, des salles de nécropsie ou des zones de confinement décrivent l'ordre de retrait à suivre et toute instruction particulière portant sur les articles d'EPI à enlever. Le retrait se fait généralement dans l'ordre inverse de l'enfilage, comme il est mentionné à la section 9.3.1 du présent chapitre. Il faut se rappeler que le devant et les manches du sarrau peuvent être contaminés.
Voici les éléments dont il faut tenir compte lorsque vous retirez des gants :
- Les gants devraient être retirés avec soin de la façon suivante : pincer l'extérieur du gant près du poignet avec la main gantée opposée et soigneusement retourner le gant pour que l'intérieur soit exposé.
- Une fois le gant retiré, le tenir dans la main gantée opposée; glisser un doigt de la main dégantée et pincer l'autre gant par l'intérieur à l'endroit du poignet et retourner le gant de façon à exposer son intérieur et à former une boule avec les deux gants, puis les jeter avec soin dans un contenant destiné aux déchets biologiques dangereux. Si deux paires de gants sont portées, il faut répéter ces étapes pour la deuxième paire.
- Les mains doivent ensuite être lavées, conformément aux protocoles de sortie, avant de quitter la zone de confinement, la salle animalière, le box ou la salle de nécropsie. Il est recommandé de se laver les mains avec du savon sous l'eau courante; les mains devraient être frottées l'une contre l'autre pour produire de la mousse et il faut bien nettoyer partout, y compris le dos de chaque main, entre les doigts et sous les ongles, pendant au moins 15 à 30 secondes avant de rincerNote de bas de page 16. Les désinfectants pour les mains à base d'alcool sont moins efficaces que le lavage des mains avec de l'eau et du savon et ils n'éliminent pas tous les types d'agents pathogènesNote de bas de page 17. Si l'efficacité d'un désinfectant pour les mains contre les agents pathogènes et les toxines manipulés dans la zone de confinement a été démontrée, il peut s'agir d'une solution de rechange pour éviter la propagation de la contamination en l'absence de lavabos facilement accessibles pour le lavage des mains. Voir l'annexe B pour la technique efficace de lavage des mains.
Les éléments à considérer lors du retrait d'autres articles ainsi que la séquence recommandée pour retirer l'EPI sont présentés dans l'exemple suivant:
- Après avoir manipulé des matières infectieuses ou des toxines, il faut enlever les gants avant de sortir les mains de l'enceinte de sécurité biologique (ESB). Il faut jeter les gants de la même façon que les déchets biologiques dangereux dans l'ESB. Ceci aidera à prévenir la propagation non intentionnelle de la contamination à l'extérieur de l'ESB. Lorsque deux paires de gants sont portées, c'est la deuxième paire (extérieure) qui est enlevée avant la sortie de l'ESB. La première paire (intérieure) protégera les mains de l'utilisateur contre l'exposition aux aérosols infectieux ou aux toxines aérosolisées résiduels avant la sortie de l'ESB. Afin de prévenir la propagation de la contamination hors de l'ESB, les mains gantées doivent être désinfectées ou décontaminées immédiatement après leur sortie de l'ESB. Les mains nues devraient être lavées immédiatement après la sortie de l'ESB.
- Retirer ensuite la blouse en gardant à l'esprit le fait que le devant et les manches pourraient être contaminés. Pour retirer la blouse, les rubans à l'arrière sont défaits, puis la blouse est enlevée à partir du cou et des épaules en prenant soin d'éviter tout contact entre le côté contaminé et le corps. Une fois retiré, la blouse doit être plié ou roulé en boule avant d'être jeté dans le contenant de déchets réservé aux articles à décontaminer.
- Retirer ensuite la visière ou les lunettes de sécurité, en gardant à l'esprit le fait que la face externe des lentilles peut être contaminée. Pour retirer les lunettes de sécurité, prendre la bande élastique ou les montures et tirer les lunettes loin du visage avant de les mettre dans un contenant réservé aux articles à décontaminer.
- Le masque ou l'appareil de protection respiratoire peut ensuite être retiré; il importe de se rappeler que le devant du masque peut être contaminé. Retirer ensuite le masque conformément aux directives du fabricant en prenant les précautions nécessaires pour ne pas propager les contaminants pouvant se trouver à l'extérieur du masque. Le masque doit ensuite être jeté.
- Retirer les bonnets et les autres dispositifs de protection de la tête, puis les jeter ou les décontaminer.
- Retirer ensuite les chaussures protectrices ou les couvre-chaussures et les ranger ou les jeter.
- Finalement, la paire de gants intérieure (lorsque deux paires sont portées) peut être enlevée et jetée. Les mains sont immédiatement lavées en profondeur avec de l'eau et du savon pour les décontaminer et enlever tout agent pathogène potentiel qui aurait pu traverser les couches d'EPI.
Il faudrait toujours se laver les mains dans l'évier réservé à cet usage immédiatement après avoir retiré l'EPI, après quoi l'employé peut enlever la tenue de bloc opératoire et remettre ses vêtements personnels. Les désinfectants pour les mains peuvent remplacer le lavage des mains uniquement lorsque les lavabos ne sont pas facilement accessibles, si l'efficacité du désinfectant pour les mains contre les agents pathogènes ou les toxines manipulées dans la zone de confinement a été démontrée. Cet exemple ne s'applique pas lorsqu'une douche prise dans une installation de douche corporelle est exigée à la sortie, mais il indique l'ordre dans lequel l'EPI devrait être retiré pour réduire au minimum le risque de contamination. Les membres du personnel qui travaillent dans des zones de confinement élevé doivent retirer la couche additionnelle de vêtements protecteurs couvrant le corps en entier lorsqu'ils traversent la barrière de confinement. Les membres du personnel sortant de salles animalières, de box ou de salles de nécropsie situées dans de n'importe quel niveau de confinement doivent retirer les vêtements réservés à la zone (y compris les chaussures) ou la couche additionnelle d'EPI et les chaussures (le cas échéant), sauf si la sortie s'effectue par un corridor « sale ». Si un changement de vêtements n'est pas exigé à la sortie des box et des salles de nécropsie, c'est une bonne pratique que les membres du personnel passe leurs pieds dans un pédiluve contenant un désinfectant adapté à l'agent pathogène utilisé, afin de décontaminer efficacement les chaussuresNote de bas de page 18.
9.3.3 Conseils généraux d'utilisation
Les sections suivantes portent sur des généralités relatives au port de différents articles d'EPI.
9.3.3.1 Gants
- Au lieu de gants en latex, on peut porter des gants en nitrile ou en vinyle pour fournir une résistance aux liquides (p. ex. en cas d'allergie au latex).
- S'assurer que les gants sont intacts; vérifier qu'ils ne présentent pas de déchirures ni de défauts avant de les enfiler.
- Changer de gants souvent s'ils doivent être portés longtemps.
- Ne jamais réutiliser des gants jetables. Jeter les gants utilisés dans un contenant pour déchets contaminés.
- Retirer les gants et se laver les mains avant de sortir de la zone de confinement, de la salle animalière, du box ou de la salle de nécropsie.
9.3.3.2 Chaussures
- Porter des chaussures qui recouvrent entièrement le pied, sans talons ou à talons bas.
- Les chaussures devraient offrir une protection contre les liquides dangereux et pouvoir être facilement nettoyées et désinfectées. S'assurer que les couvre-chaussures jetables sont intacts; vérifier qu'ils ne présentent pas de déchirures avant de les enfiler.
- Ne jamais réutiliser des couvre-chaussures. Jeter les couvre-chaussures utilisés dans un contenant pour déchets contaminés.
- Ne jamais porter de chaussures réservées à la zone de confinement en dehors de cette dernière.
- Porter des bottes imperméables en milieu humide.
9.3.3.3 Protection de la tête
- Retirer le dispositif de protection de la tête avant de sortir de la zone de confinement.
- Décontaminer le dispositif de protection de la tête réutilisable après usage; recueillir les bonnets jetables et les décontaminer avant de les sortir de la zone de confinement pour les éliminer.
9.3.3.4 Protection des yeux et du visage
- Porter des lunettes de sécurité dans les zones présentant un risque d'exposition pour les yeux.
- Porter des lunettes à coques pour protéger les yeux contre les éclaboussures et les déversements.
- Porter une visière pour protéger le nez, la bouche et la peau contre les éclaboussures et les déversements.
- Décontaminer les dispositifs réutilisables de protection des yeux et du visage après chaque usage, même s'ils sont rangés dans la zone de confinement.
- Décontaminer les verres correcteurs à la barrière de confinement avant de sortir des zones de niveau de confinement élevé, sauf s'ils étaient protégés par de l'EPI supplémentaire (p. ex. APRM ou un autre dispositif recouvrant toute la tête, conformément à l'ELR).
- Ne jamais porter de dispositifs de protection des yeux et du visage réservés aux zones de confinement en dehors de ces dernières.
9.3.3.5 Protection du corps
- Porter des vêtements protecteurs bien fermés dont les manches recouvrent entièrement les bras.
- Retirer, décontaminer et faire nettoyer les vêtements protecteurs après qu'ils ont été contaminés. Dans les zones de niveau de confinement élevé, retirer la couche de vêtements protecteurs en sortant avant de traverser la barrière de confinement. Tout l'EPI (réutilisable ou jetable) est décontaminé avant d'être sorti de la zone de confinement. Les vêtements de protection réutilisables sont décontaminés avant d'être envoyés à la buanderie; des installations de buanderie situées à l'intérieur de la zone de confinement peuvent convenir pour la décontamination, si leur efficacité contre les agents pathogènes manipulés a été démontrée (c.-à-d. validée).
- Ne jamais porter de vêtements protecteurs réservés aux zones de confinement en dehors de ces dernières (p. ex. bureaux, cafétéria).
9.3.3.6 Masques et protection respiratoire
- Suivre une formation sur les appareils de protection respiratoire et s'assurer de leur bon ajustement par des essais qualitatifs ou quantitatifs avant d'amorcer toute activité nécessitant le port d'un appareil de protection respiratoire.
- Vérifier l'étanchéité à chaque utilisation de l'appareil de protection respiratoire.
- Après chaque utilisation, nettoyer et désinfecter ou décontaminer l'appareil de protection respiratoire conformément aux instructions du fabricant ou aux PON élaborées en collaboration avec le fabricant, même s'il est entreposé dans la zone de confinement.
- On doit faire preuve de prudence pour éviter que les filtres ou les cartouches soient mouillés pendant la décontamination. Remplacer les cartouches dont la fin de la vie utile approche.
- Ne jamais réutiliser un masque ou un appareil de protection respiratoire jetable; décontaminer les appareils de protection respiratoire et les masques usagés avant de les jeter.
- Inspecter l'appareil de protection respiratoire après chaque utilisation; jeter ou réparer toutes les pièces défectueuses.
- Retirer l'appareil de protection respiratoire en sortant de la zone de confinement, à un endroit où une évaluation des risques permet de conclure qu'il n'y a plus de danger.
- Les appareils de protection respiratoire réutilisables devraient être entreposés de manière à les protéger contre tout danger potentiel qui pourrait avoir un effet néfaste (p. ex. poussière, lumière du soleil, chaleur, froid extrême).
Références
- Note 1
- Gouvernement du Canada. (2015). Norme canadienne sur la biosécurité, 2 e éd., Ottawa, ON, Canada : Gouvernement du Canada.
- Note 2
- Klingner, T. D. et Boeniger, M. F. (2010). A critique of assumptions about selecting chemical-resistant gloves: A case for workplace evaluation of glove efficacy. Applied Occupational and Environmental Hygiene. 17(5): 360-367.
- Note 3
- ASTM F739-12. Standard Test for Permeation of Liquids and Gases through Protective Clothing Materials under Conditions of Continuous Contact. (2012). West Conshohocken, PA, États-Unis: American Society for Testing and Materials.
- Note 4
- Ansell Occupational Healthcare. (2008). Chemical Resistance Guide: Permeation & Degradation Data , 8th ed. Red Bank, NJ, États-Unis. Consulté le 3 novembre 2015 à l’adresse http://www.ansellpro.com/download/Ansell_8thEditionChemicalResistanceGuide.pdf
- Note 5
- Ansell Occupational Healthcare. (2009). A Guide to Safe Handling of Hazardous Materials. Red Bank, NJ, États-Unis. Consulté le 3 novembre 2015 à l’adresse http://www.ansellhealthcare.com/pdf/guide_hazardous_materials.pdf
- Note 6
- All Safety Products. (2015). Glove Selection Chart- Chemical Breakthrough Ratings. Consulté le 3 novembre 2015 à l’adresse http://www.allsafetyproducts.com/glove-selection-chart-chemical-breakthrough-ratings.html
- Note 7
- National Research Council des États-Unis. (1981). Prudent Practices for Handling Hazardous Chemicals in Laboratories, Washington, DC, États-Unis: The National Academies Press, pp. 159-160.
- Note 8
- Albin, M. S., Bunegin, L., Duke, E. S., Ritter, R. R. et Page, C.P. (1992). Anatomy of a defective barrier: sequential glove leak detection in a surgical and dental environment. Critical Care Medicine. 20(2):170-184.
- Note 9
- CSA Z195-F14 - Chaussures de protection. (2014). Mississauga, ON, Canada: Association canadienne de normalisation
- Note 10
- CSA Z94.1-F15, Casques de sécurité pour l’industrie: Tenue en service, sélection, entretien et utilisation. (2015). Mississauga, ON, Canada : Association canadienne de normalisation.
- Note 11
- CSA Z94.3-F07 (C2014), Protecteurs oculaires et faciaux. (2007). Mississauga, ON, Canada : Association canadienne de normalisation.
- Note 12
- CSA Z94.3.1-F09, Sélection, utilisation et entretien des lunettes de protection. (2009). Mississauga, ON, Canada : Association canadienne de normalisation.
- Note 13
- CSA Z94.4-F11, Choix, utilisation et entretien des appareils de protection respiratoires. (2011). Mississauga, ON, Canada : Association canadienne de normalisation.
- Note 14
- National Institute for Occupational Safety and Health des États-Unis (1996). NIOSH Guide to the Selection and Use of Particulate Respirators, DHHS (NIOSH) Publication Number 96-101. Consulté le 30 novembre 2015 à l’adresse http://www.cdc.gov/niosh/docs/96-101/
- Note 15
- Richardson, A. W., Eshbaugh, J. P., Hofacre, K. C. et le Edgewood Chemical Biological Center, U.S. Army Research, Development and Engineering Command. (2006). ECBC-CR-085: Respirator Filter Efficiency Testing Against Particulate and Biological Aerosols Under Moderate to High Flow Rates, Columbus, OH, États-Unis : Battelle Memorial Institute.
- Note 16
- Agence de la santé publique du Canada. (2012). Pratiques en matière d’hygiène des mains dans les milieux de soins, Ottawa, ON, Canada: Agence de la santé publique du Canada.
- Note 17
- Centers for Disease Control and Prevention des États-Unis. (2015). Show Me the Science - When to Use Hand Sanitizers. Consulté le 3 novembre 2015 à l’adresse http://www.cdc.gov/handwashing/show-me-the-science-hand-sanitizer.html
- Note 18
- Morley, P. S., Morris, S. N., Hyatt, D. R. et Van Metre, D. C. (2005). Evaluation of the efficacy of disinfectant footbaths as used in veterinary hospitals. Journal of the American Veterinary Medical Association . 226(12):2053-2058.
Chapitre 10 - Traitement de l'air
Le système de chauffage, ventilation et air climatisé (CVAC) fournit de l'air frais et permet le maintien d'une bonne qualité de l'air intérieur. Ce système nettoie et filtre l'air intérieur, régule la température et l'humidité et contrôle les odeurs provenant des animaux, tout en assurant une ventilation (p. ex. pendant l'utilisation de produits chimiques à des fins de décontamination). Les lignes directrices sur la ventilation des laboratoires s'appuient sur plusieurs normes, notamment les normes American National Standards Institute (ANSI)/American Industrial Hygiene Association (AIHA) Z9.5, ANSI/ American Society of Heating, Refrigerating and Air-Conditioning Engineers (ASHRAE) 62.1 et Norme nationale du Canada (CAN)/Association canadienne de normalisation (CSA)-Z317.2, mais la réglementation locale ainsi que le code du bâtiment ou le code de prévention des incendies devraient également être consultésNote de bas de page 1Note de bas de page 2Note de bas de page 3. Les Lignes directrices du Conseil canadien de protection des animaux (CCPA) sur : les animaleries contiennent d'autres recommandations sur les systèmes de CVAC utilisés dans le cadre d'un travail avec des animauxNote de bas de page 4. Les exigences propres au traitement de l'air des zones de confinement réglementées par l'Agence de la santé publique du Canada (ASPC) et l'Agence canadienne d'inspection des aliments (ACIA) sont énoncées à la matrice 3.5 de la Norme canadienne sur la biosécurité (NCB), 2e édition.Note de bas de page 5
10.1 Courant d'air vers l'intérieur
Les systèmes de CVAC peuvent être conçus pour maintenir une pression d'air différentielle négative dans la zone de confinement, de sorte que l'air traverse la barrière de confinement et s'écoule à l'intérieur de la zone, des aires de confinement inférieur vers les aires de confinement plus élevé. Ce courant d'air vers l'intérieur (CAVI) favorise l'établissement d'une zone tampon d'air à la barrière de confinement, qui sert à réduire le risque de propagation des matières infectieuses ou des toxines aérosolisées hors de l'espace de travail. Aux endroits où un courant d'air vers l'intérieur (CAVI) est maintenu, il existe souvent des sas et des portes munies d'un dispositif d'interverrouillage (ou des procédures opératoires normalisées [PON]) permettant l'entrée du personnel, des animaux et du matériel à travers la barrière de confinement. Les systèmes de CVAC qui maintiennent un courant d'air vers l'intérieur (CAVI) sont essentiels aux systèmes de confinement. Les sas sont décrits en détail au chapitre 3, où l'on retrouve d'autres éléments à prendre en compte. Les exigences propres aux sas sont énoncées dans la matrice 3.3 de la NCB. Les exigences propres au courant d'air vers l'intérieur (CAVI) sont énoncées dans la matrice 3.5 de la NCB.
Les zones de confinement élevé sont conçues de façon que la pression de l'air diminue progressivement à mesure qu'on progresse dans la zone de confinement (p. ex. grâce à une séquence de différences de pression entre le côté « sale » et le côté « propre » des sas et des douches). Dans les zones de confinement élevé, les systèmes de CVAC sont reliés à une alimentation de secours, et, dans les zones de NC4, les systèmes de contrôle automatique du bâtiment sont reliés à une source d'alimentation continue (UPS) garantissant le fonctionnement en cas de panne d'électricité. Des portes munies d'un dispositif d'interverrouillage, des avertisseurs visuels ou sonores, ou encore des protocoles peuvent être utilisés pour empêcher l'ouverture simultanée de la porte critique sur la barrière de confinement et d'une porte de l'extérieur de la zone de confinement donnant sur un sas ainsi que d'une porte du sas donnant sur un espace de travail en laboratoire, une salle animalière, un box ou une salle de nécropsie, car cela pourrait perturber le courant d'air vers l'intérieur (CAVI) et altérer l'intégrité de la barrière de confinement.
Le scellement des ouvertures de la barrière de confinement (p. ex. fenêtres, portes, conduits d'aération, autres conduits) et l'utilisation adéquate de l'équipement bien conçu traversant la barrière de confinement (p. ex. autoclaves installés à même la barrière, passe-plats et cuves d'immersion) favoriseront le maintien du courant d'air vers l'intérieur (CAVI) et l'intégrité de la barrière de confinement (matrices 3.2 et 4.8 de la NCB). Des dispositifs de surveillance comme les dispositifs de bille dans un tube placés en haut de portes, lesquels confirment visuellement la présence du courant d'air vers l'intérieur (CAVI), ou un manomètre différentiel mesurant la différence de pression entre deux pièces, sont prévus pour que le personnel de la zone de confinement puisse vérifier que le courant d'air vers l'intérieur (CAVI) est maintenu, avant de pénétrer dans la pièce (matrices 3.5 et 4.5 de la NCB).
La filtration à haute efficacité pour les particules de l'air (HEPA ) de l'air évacué réduit le risque de dispersion des matières infectieuses ou des toxines à l'extérieur des zones de confinement élevé. De petits filtres HEPA disposés en série servent à protéger les canalisations des dispositifs de surveillance des différences de pression qui traversent la barrière de confinement. L'arrivée d'air peut également passer par des filtres HEPA, selon le niveau de confinement (matrice 3.5 de la NCB).
Les exigences et les recommandations suivantes devraient être prises en considération au moment d'installer des systèmes de CVAC :
- L'air des zones de confinement élevé devrait être évacué afin d'éviter sa réintroduction dans le bâtiment, conformément aux normes applicables, par exemple la norme ANSI/ASHRAE 62.1Note de bas de page 2.
- Des mécanismes de régulation comme des systèmes d'approvisionnement et d'évacuation de l'air interdépendants devraient être mis en place pour qu'une pressurisation soutenue du laboratoire soit évitée durant les pannes de ventilateur, et des avertisseurs visuels ou sonores sont prévus pour aviser le personnel de ces pannes (matrice 3.5 de la NCB).
- Les dispositifs de transfert de l'air utilisés pour limiter les fuites dans les zones de confinement devraient être conçus pour assurer le maintien des courants d'air directionnels et offrir une protection antirefoulement. Il s'agit de dispositifs fixés aux murs ou aux portes permettant un transfert de l'air et limitant les différences de pression entre deux pièces.
- L'utilisation d'humidificateurs auxiliaires à certains endroits pourrait contribuer au bien-être du personnel et des animaux.
- Les services de soutien mécanique des systèmes de CVAC devraient être situés le plus près possible de la barrière de confinement. Afin de réduire la longueur des conduits potentiellement contaminés, les boîtiers de filtres HEPA devraient aussi être le plus près possible de la barrière de confinement. De plus, l'installation de vannes isolant des sections de conduits facilitera la décontamination.
10.1.1 Vérification du courant d'air vers l'intérieur et de l'intégrité de la barrière de confinement
La vérification visuelle du courant d'air vers l'intérieur (CAVI) à toutes les portes critiques de la barrière de confinement permet de s'assurer que l'air s'écoule des zones de niveau de confinement inférieur aux zones de niveau de confinement plus élevé, compte tenu de la conception, et jamais dans le sens opposé. La différence de pression entre des zones adjacentes peut être vérifiée visuellement dans des conditions normales de fonctionnement du système de CVAC en tenant une poire à fumée devant chaque porte placée dans son état normal (c. à d. généralement fermée). Les vérifications à l'aide d'une poire à fumée ou d'un autre moyen visuel devraient être effectuées dans des conditions opérationnelles normales et dans le cadre de pannes simulées.
Les tests de fumée servent également à détecter les fuites au niveau des surfaces qui forment la barrière de confinement dans une zone de confinement. Les joints, les angles, les pénétrations scellées (p. ex. conduits, plomberie, câblage), ainsi que les joints autour des portes, des fenêtres, des autoclaves et des cuves à immersion, devraient tous être vérifiés pour détecter la présence de fuites. Les inspections visuelles des planchers, des murs et des plafonds, ainsi que des joints plancher-mur et mur-plafond, permettent de détecter les fissures, les ébréchures ou l'usure pouvant nécessiter une réparation.
10.1.1.1 Tests de perte de pression
Dans les zones de confinement dotées de portes hermétiques ou de portes scellables, les tests de perte de pression dans la zone de confinement (salle entière) permettent de vérifier l'intégrité du périmètre de la salle (c.-à-d. la capacité des gaz et des liquides de passer à travers la membrane du périmètre et les perforations prévues pour les services). Voici la procédure de base à suivre pour effectuer les tests de perte de pression en cas de pression négativeNote de bas de page 6.
- Isoler la zone en fermant et en verrouillant toutes les portes et valves ainsi que les volets de confinement à la barrière de confinement. Éviter d'installer sur les portes, les fenêtres et les services des dispositifs de scellement temporaires qui couvriraient les scellants permanents et les empêcheraient d'être testé pour des fuites. Capuchonner toutes les conduites des sondes de pression (p. ex. manomètres différentiels).
- Installer un manomètre calibré à travers la barrière de confinement de manière à ce qu'il ne soit pas influencé par la distribution d'air. Le manomètre devrait avoir une précision minimale de 10 Pa (c.-à-d. 0,05 pouce de colonne d'eau [po C.E.]) et pouvoir lire une pression allant jusqu'à 750 Pa (c.-à-d. 3 po C.E.).
- Installer un robinet à bille dans la tuyauterie entre la source de vide (c.-à-d. le ventilateur ou la pompe) et la salle pour que la salle puisse être scellée une fois la pression nécessaire obtenue.
- Brancher la salle à une source de vide pour créer un différentiel de pression négative de 500 Pa (c.-à-d. 2 po C.E.). Laisser stabiliser la pression de la salle, puis fermer le robinet entre la source de vide et la salle pour sceller la salle à 500 Pa (c.-à-d. 2 po C.E.).
- Mesurer la perte progressive de pression négative à partir de 500 Pa (c.-à-d. 2 po C.E.); enregistrer le différentiel de pression toutes les minutes pendant 20 minutes.
- Attendre au moins 20 minutes avant d'effectuer un deuxième test, au besoin, afin de permettre au système CVAC d'atteindre l'équilibre.
- Débrancher la source de vide et ouvrir lentement le robinet à bille pour permettre le retour à une pression normale.
- Si le taux de fuite dépasse la valeur acceptable :
- pressuriser la salle à un niveau adéquat pour localiser les fuites;
- tout en conservant une pression continue dans la salle, appliquer une solution bulleuse aux sections devant être évaluées (p. ex. joints, angles, pénétrations scellées); il est également possible de localiser les fuites à l'oreille si une méthode sonore (c.-à-d. équipement de détection électronique des sons) est utilisée;
- repérer les endroits où se forment des bulles;
- réparer la ou les fuites avant de refaire un test, au besoin.
10.2 Filtres à haute efficacité pour les particules de l'air (HEPA)
Les filtres HEPA permettent de retenir plus de 99,97 % des particules présentes dans l'air dont le diamètre est de 0,3 micron, soit les particules les plus pénétrantes. En raison des effets de l'impaction, de la diffusion et de l'interception, les filtres HEPA sont encore plus efficaces envers les particules dont le diamètre est inférieur ou supérieur à 0,3 micronNote de bas de page 7. Bien qu'il soit établi en usine que ces filtres sont efficaces à 99,97 %, ils atteignent généralement un niveau d'efficacité beaucoup plus élevé. Des filtres HEPA d'une efficacité minimale de 99,99 % devraient être utilisés dans les installations de confinement. Avant l'achat, il faut expliquer clairement au fournisseur les exigences en matière de filtration que les filtres HEPA doivent satisfaire une fois installésNote de bas de page 8.
Les filtres HEPA sont normalement constitués d'une feuille de fibres pliée en accordéon. Des séparateurs (p. ex. en aluminium ondulé) maintiennent l'espace entre les plis et empêchent l'air de les aplanir (voir le médaillon de la figure 10-1). Le milieu filtrant est collé dans un cadre en bois, en métal ou en plastique, qui peut facilement être endommagé ou déformé s'il n'est pas manipulé correctement. C'est la raison pour laquelle il est important que l'intégrité et l'efficacité des filtres soient vérifiées après leur installation ou leur déplacement, et à intervalles réguliers par la suite.
Les filtres HEPA sont habituellement fixés dans leur boîtier (figure 10-1) au moyen d'un joint d'étanchéité (en néoprène) ou d'un scellant (gel). Il arrive fréquemment que ces joints soient comprimés, se déchirent ou soient incompatibles avec les décontaminants gazeux. Par exemple, le peroxyde d'hydrogène (H2O2) peut désagréger certains types de néoprène (joints en néoprène noir à cellules ouvertes). Les joints en matériaux denses peuvent résister plus longtemps aux fréquents cycles de décontamination que les joints fabriqués dans les mêmes matériaux, mais à cellules ouvertes. Les scellants de gel sont posés entre le boîtier de filtres et la rainure ménagée sur le pourtour du filtre pour assurer une étanchéité parfaite. Le rebord aminci du boîtier s'introduit dans cette rainure pour compléter l'étanchéité. Les scellants de gel résistent généralement aux problèmes de compression et de compatibilité associés aux joints d'étanchéité. L'intégrité des filtres HEPA a fait l'objet d'un essai de performance afin de confirmer l'absence de fuites de la matière filtrante, des joints ou des joints d'étanchéité du boîtier du filtre. Pour effectuer le test visant le boîtier du filtre, le boîtier est mis en présence d'une concentration de particules connue et on analyse le pourcentage de pénétration en aval du filtre (c.-à-d. essai par balayage).
Les filtres encrassés devraient être remplacés lorsque le courant d'air ne peut être maintenu à l'intérieur d'un intervalle cible ou conformément aux instructions du fabricant. L'installation de préfiltres devrait être envisagée, surtout dans les zones de confinement d'animaux, afin de protéger les filtres HEPA de la poussière et des débris (p. ex. poils, pelage). La norme AHSRAE 52.2, Gravimetric and Dust-Spot Procedures for Testing Air-Cleaning Devices Used in General Ventilation for Removing Particle Matter fournit de plus amples renseignements sur les préfiltresNote de bas de page 9.
Les filtres HEPA qui peuvent être décontaminés par fumigation in situ avec un gaz (p. ex. du formaldéhyde, du peroxyde d'hydrogène vaporisé [PHV] ou du dioxyde de chlore [ClO2]) subissent ce procédé de décontamination avant leur élimination. Dans les zones de confinement où les procédés de décontamination utilisés sont inefficaces contre les agents pathogènes et les toxines manipulés (les prions, par exemple, ne sont pas complètement inactivés par la plupart des procédés de décontamination les plus courants), il est nécessaire d'éliminer les filtres HEPA de façon sécuritaire par un autre moyen. Citons notamment le recours à des filtres HEPA de type bag-in/bag-out ou à un protocole permettant de confiner le filtre HEPA à retirer, puis de le décontaminer par la suite.
Figure 10-1 : Diagramme représentatif d'un boîtier de filtre à haute efficacité pour les particules de l'air (HEPA) et vue en coupe dévoilant les filtres HEPA situés dans le boîtier
Le médaillon illustre le milieu filtrant, soit une feuille de fibres pliée en accordéon munie d'un séparateur entre chacun des plis.
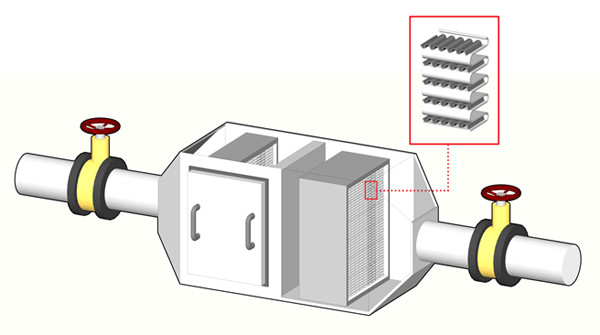
Équivalent textuel - Figure 10-1
Cette figure montre des conduits d’air reliés à un boîtier contenant un filtre HEPA. Des volets se trouvent sur les conduits de part et d’autre du boîtier pour permettre la décontamination du filtre. L’ouverture de la porte du boîtier permet d’accéder aux filtres et de les remplacer. La vue en coupe montre l’emplacement des filtres. Le médaillon illustre le milieu filtrant, soit une feuille de fibres pliée en accordéon munie d’un séparateur entre chacun des plis pour en assurer la rigidité.
Références
- Note 1
- ANSI/AIHA Z9.5-2012, Laboratory Ventilation. (2012). Fairfax, VA, États-Unis: American National Standards Institute / American Industrial Hygiene Association.
- Note 2
- ANSI/ASHRAE 62.1-2013, Ventilation for Acceptable Indoor Air Quality. (2013). Atlanta, GA, États-Unis: American National Standards Institute / American Society of Heating, Refrigerating and Air-Conditioning Engineers.
- Note 3
- CAN/CSA-Z317.2-F10 (C2015), Systèmes de chauffage, de ventilation et de conditionnement d’air (CVCA) dans les établissements de santé: exigences particulières. (2010). Mississauga, ON, Canada: Association canadienne de normalisation.
- Note 4
- Conseil canadien de protection des animaux. (2003). Lignes directrices sur : les animaleries - les caractéristiques, la conception et le développement. Ottawa, ON, Canada : Conseil canadien de protection des animaux.
- Note 5
- Gouvernement du Canada. (2015). Norme canadienne sur la biosécurité, 2 e éd., Ottawa, ON, Canada : Gouvernement du Canada.
- Note 6
- Department of Agriculture des États-Unis, Research, Education, and Economics Division. (2012). Agriculture Research Service (ARS) Facilities Design Standards, ARS-242.1. Washington, DC, États-Unis: Government Printing Office.
- Note 7
- Richardson, A. W., Eshbaugh, J. P., Hofacre, K. C. et le Edgewood Chemical Biological Center, U.S. Army Research, Development and Engineering Command. (2006). ECBC-CR-085: Respirator Filter Efficiency Testing Against Particulate and Biological Aerosols Under Moderate to High Flow Rates, Columbus, OH, États-Unis : Battelle Memorial Institute.
- Note 8
- IEST RP-CC001.5, HEPA and UPLA Filters. (2010). Rolling Meadows, IL, États-Unis: Institute of Environmental Sciences and Technology.
- Note 9
- ASHRAE 52.2-2012, Method of Testing General Ventilation Air-Cleaning Devices for Removal Efficiency by Particle Size. (2012). Atlanta, GA, États-Unis: American National Standards Institute / American Society of Heating, Refrigerating and Air-Conditioning Engineers.