Approche proposée fondée sur le risque pour l'autorisation d'aliments à des fins diététiques spéciales pour bébés
Il s'agit d'un document de consultation sur une proposition d'approche fondée sur le risque pour l'autorisation d'aliments à des fins diététiques spéciales pour bébés. La consultation est maintenant terminée. Elle s'est tenue du 26 novembre 2025 au 25 janvier 2026.
Sur cette page
- Liste des abréviations
- 1.0 Introduction
- 2.0 Contexte
- 3.0 Consultation des parties prenantes
- 4.0 Contexte international
- 5.0 Aperçu de l'approche proposée fondée sur le risque pour l'autorisation d'aliments à des fins diététiques spéciales pour bébés
- 6.0 Questions pour les parties prenantes
- 7.0 Conclusion
- Annexe
- Références
Liste des abréviations
- AFDS
- Aliments à des fins diététiques spéciales
- AFMS
- Aliments à des fins médicales spéciales
- ARE
- Autorités réglementaires étrangères
- AUDS
- Aliments à usage diététique spécial
- CE
- Commission européenne
- FDA
- Food and Drug Administration (autorité américaine de réglementation des aliments et des médicaments)
- FLH
- Fortifiants pour lait humain
- FSANZ
- Food Standards Australia New Zealand (normes alimentaires d'Australie et de Nouvelle-Zélande)
- FSMP
- « Food for special medical purposes » (aliments à des fins médicales spéciales)
- IPR
- Incorporation par renvoi
- LAD
- Loi sur les aliments et drogues
- NIAB
- Nouvel ingrédient alimentaire pour bébés
- ONG
- Organisations non gouvernementales
- RAD
- Règlement sur les aliments et drogues
- SMPPi
- « Special medical purpose product for infants » (produit destiné à des fins médicales spéciales pour nourrissons)
1.0 Introduction
Santé Canada procède à la modernisation des titres 24 et 25 de la partie B du Règlement sur les aliments et drogues (RAD), qui établissent la réglementation des aliments à usage diététique spécial (AUDS)Note de bas de page 1 et des aliments pour bébés.
À ce jour, Santé Canada a mené deux préconsultations sur la modernisation de ces titres. La première consultation, qui s'est déroulée du 28 novembre 2023 au 26 février 2024, proposait une restructuration du cadre réglementaire actuel, notamment la suppression du terme AUDS et la création d'un cadre pour réglementer les aliments à des fins diététiques spéciales (AFDS)Note de bas de page 2. Ce terme a été introduit dans la Loi sur les aliments et drogues (LAD) en 2019 dans le cadre d'une modernisation législative plus large. Son objectif est de permettre une approche réglementaire plus adaptée aux produits à risque élevé relevant de cette définition. Dans le cadre de la présente consultation, il s'agit notamment des préparations pour nourrissons et des aliments médicaux pour bébés tels que les fortifiants pour lait humain (FLH). Le document de préconsultation de 2023 proposait que la plupart des AFDS pour bébés soient soumis à une autorisation préalable à la mise en marché et s'engageait à revoir les délais d'évaluation préalable à la mise en marché. La deuxième consultation, qui s'est déroulée du 23 octobre 2024 au 22 janvier 2025, présentait des exigences de composition proposées pour de nombreux aliments visés par les titres 24 et 25, y compris les préparations pour nourrissons.
La proposition de Santé Canada visant à modifier la réglementation pour exiger une autorisation préalable à la mise en marché pour la plupart des AFDS pour bébés a suscité des réactions mitigées. Bien que ce changement ne ferait que formaliser la pratique actuelle et ait reçu l'appui de certains intervenants, d'autres ont souligné la nécessité de s'aligner davantage sur les juridictions internationales et de mettre en œuvre une surveillance fondée sur le risque.
Pour répondre à ces préoccupations et à l'engagement récent du gouvernement du Canada visant à moderniser la réglementation et à réduire le fardeau administratif, cette proposition présente une approche fondée sur le risque pour la surveillance des AFDS pour bébés, avec des exigences adaptées à la complexité et au niveau d'incertitude face au produit. L'approche proposée vise à faciliter l'accès aux produits et à réduire le fardeau réglementaire inutile, tout en maintenant des normes de sécurité rigoureuses pour les populations vulnérables qui les utilisent.
1.1 Objectif
L'objectif de ce document de préconsultation est de présenter l'approche proposée par Santé Canada, fondée sur le risque, pour l'autorisation des AFDS pour bébés. Les commentaires des parties prenantes sur cette proposition orienteront la rédaction de la réglementation, qui sera prépubliée dans la Gazette du Canada, Partie I pour consultation publique. La section 5.0 présente l'approche proposée d'autorisation fondée sur le risque, tandis que la section 6.0 propose des questions aux parties prenantes.
1.2 Portée et définitions
La portée de cette proposition est limitée uniquement à l'autorisation des préparations pour nourrissons et des aliments médicaux enrichis pour bébés.
Préparation pour nourrissons
Aux fins de cette proposition, une préparation pour nourrissons est définie comme « tout aliment étiqueté ou annoncé comme pouvant remplacer partiellement ou totalement le lait humain et destiné à la consommation par des bébés ». Dans le contexte de ce document, cela inclut :
- Les préparations standards pour nourrissons, destinées aux bébés nés à terme en bonne santé et répondant aux exigences de composition standard;
- Les préparations médicales pour nourrissons, adaptées aux bébés présentant des conditions médicales et pouvant déroger à la composition standard pour répondre à un objectif médical spécifique.
Aliment médical enrichi pour bébés
Aux fins de cette proposition, un aliment médical pour bébés est défini comme « un aliment, autre qu'une préparation pour nourrissons, qui a été spécialement transformé ou formulé et qui est destiné à la prise en charge diététique des bébés, à utiliser sous supervision médicale. Il est destiné à l'alimentation partielle des bébés :
- ayant une capacité limitée ou altérée à prendre, digérer, absorber, métaboliser ou excréter des aliments ordinaires ou certains nutriments, ou leurs métabolites;
- ayant d'autres besoins nutritionnels déterminés médicalement;
dont la prise en charge diététique ne peut raisonnablement être assurée par la modification du régime alimentaire normal seul ».
Le terme « enrichi » fait référence à l'ajout de vitamines, de minéraux et d'acides aminés aux aliments afin de restaurer ou d'améliorer leur qualité nutritionnelle. Un aliment médical enrichi pour bébés contient donc des nutriments ajoutés. Un exemple d'aliment médical enrichi pour bébés est un FLH.
Exclusions
Cette proposition exclut d'autres aspects du projet de modernisation des titres 24 et 25. Plus précisément, d'autres catégories d'aliments (par exemple, aliments médicaux pour les personnes d'un an et plus) ou des éléments tels que la composition des produits et l'étiquetage des préparations pour nourrissons et des aliments médicaux pour bébés ne sont pas inclus. Les aliments médicaux non enrichis pour bébés (par exemple les épaississants alimentaires), qui, bien qu'ils répondent à la définition d'aliments médicaux pour bébés, sont également exclus. En effet, ils ne sont pas visés par cette proposition car aucune exigence d'autorisation n'est proposée pour ceux-ci. Sauf indication contraire, les références aux « aliments médicaux pour bébés » dans ce document concernent uniquement les aliments médicaux enrichis. Tous les volets de la modernisation des titres 24 et 25 seront abordés dans un vaste projet réglementaire qui sera publié dans la Gazette du Canada, Partie I.
1.3 Principes directeurs
L'approche proposée par Santé Canada pour l'autorisation des aliments à des AFDS pour bébés repose sur les principes directeurs suivants :
- Assurer la sécurité, la suffisance nutritionnelle et la qualité
- Tous les AFDS pour bébés vendus au Canada continueront de répondre à des normes réglementaires rigoureuses afin de protéger la population vulnérable qui les utilise.
- Favoriser l'accès, réduire les obstacles à l'importation et soutenir l'innovation
- L'accès rapide à une gamme diversifiée d'AFDS pour bébés, y compris des produits innovants et/ou disponibles à l'échelle mondiale, sera facilité.
- Mettre en œuvre une surveillance réglementaire fondée sur le risque
- La surveillance sera adaptée à la complexité et au niveau d'incertitude face au produit, de sorte que l'examen réglementaire soit proportionnel au risque potentiel.
- Améliorer l'efficacité réglementaire
- Les processus réglementaires modernisés augmenteront l'efficacité, réduiront le fardeau administratif et soutiendront l'engagement du gouvernement du Canada à réduire les formalités administratives.
Pour soutenir ces principes directeurs, l'approche proposée intègre plusieurs mesures, décrites à la section 5.1.
2.0 Contexte
2.1 Approche actuelle du Canada
En vertu du titre 25 du RAD, les requérants doivent aviser Santé Canada au moins 90 jours avant de vendre ou de faire la publicité de toute nouvelle préparation pour nourrissons ou de toute préparation ayant subi un changement majeurNote de bas de page 3. Ce processus exige la soumission de renseignements détaillés sur le produit — y compris la composition, l'étiquetage, l'emballage, la fabrication et la suffisance nutritionnelle — comme indiqué dans les lignes directrices. Le même processus s'applique tant aux préparations standards qu'aux préparations médicales pour nourrissons. Si la soumission de renseignements est jugée satisfaisante, Santé Canada délivre une lettre de non-objection, que les requérants attendent généralement avant de commercialiser leurs produits, bien que cela ne soit pas exigé par la réglementation.
Pour les FLH, qui ont été ajoutés au titre 25 du règlement en 2021, une autorisation préalable à la mise en marché est requise pour tout nouveau produit ou tout changement majeur. Les autres aliments médicaux pour bébés, y compris les produits non enrichis, ne font l'objet d'aucune exigence spécifique dans la réglementation.
Pour les préparations pour nourrissons et les FLH, la norme de rendement est de rendre une décision dans un délai de 410 jours pour 90 % des demandes préalables à la mise en marché.
Une demande préalable à la mise en marché est aussi requise pour tout nouvel ingrédient qui n'a pas été utilisé auparavant dans une préparation pour nourrissons ou un FLH au Canada. Si l'ingrédient est considéré comme un aliment nouveau (tel que défini au titre 28 du RAD), une évaluation préalable à la mise en marché est effectuée afin d'appuyer son utilisation sécuritaire dans la population générale, y compris chez les bébés. Si l'ingrédient n'est pas considéré comme nouveau pour la population générale, l'approche actuelle de Santé Canada, décrite dans les lignes directrices, exige un examen préalable de l'innocuité du nouvel ingrédient alimentaire pour bébés (NIAB) dans la population des bébés. Dans tous les cas, l'ingrédient doit être jugé sécuritaire avant d'être autorisé dans une préparation pour nourrissons.
2.2 Approche proposée du Canada en 2023
En 2023, Santé Canada a consulté sur une proposition visant à élargir l'exigence d'autorisation préalable à la mise en marché, actuellement en vigueur pour les FLH, à toutes les nouvelles préparations pour nourrissons et à tous les aliments médicaux enrichis pour bébés ayant subi un changement majeur. Santé Canada s'est également engagé à revoir les délais d'évaluation préalable à la mise en marché dans le but d'accélérer le processus pour les demandes moins complexes.
Pour répondre aux préoccupations concernant les délais d'examen et la gestion des renseignements exclusifs, le document de préconsultation de 2023 recommandait d'établir une réglementation qui exigerait qu'un NIAB obtienne une autorisation préalable distincte avant qu'une demande pour une préparation pour nourrissons contenant ce NIAB puisse être déposée. Il était également proposé que la responsabilité de soumettre la demande préalable incombe au fabricant du NIAB plutôt qu'au fabricant de la préparation pour nourrissons qui utilise le NIAB.
3.0 Consultation des parties prenantes
La proposition de 2023 visant à modifier la réglementation afin d'exiger une autorisation préalable à la mise en marché pour toutes les préparations pour nourrissons, plutôt que la notification préalable actuellement requise, a suscité des réactions mitigées. Bien que ce changement soit conforme à l'approche actuelle pour les FLH et ait reçu l'appui de certains intervenants (deux organisations non gouvernementales (ONG), une autorité régionale de santé publique, un représentant de l'industrie et un consultant), certains représentants de l'industrie ont exprimé des préoccupations importantes, notamment concernant :
- Un possible manque d'harmonisation avec les partenaires commerciaux internationaux, ce qui pourrait avoir une incidence sur l'accès au marché et la cohérence réglementaire;
- Le fardeau réglementaire et les retards potentiels dans la mise en marché des produits de préparation pour nourrissons. Les préoccupations spécifiques incluaient :
- la norme actuelle de 410 jours pour compléter un examen préalable à la mise en marché;
- le manque de détails sur les délais proposés pour l'examen préalable dans le nouveau cadre et la crainte que la transition de la notification préalable à l'autorisation préalable puisse allonger les délais;
- la difficulté de mener des essais cliniques chez les bébés présentant des conditions médicales, en raison du nombre de patients et du design des études;
- La perception que la proposition n'est pas fondée sur le risque, c'est-à-dire que le niveau d'examen pourrait ne pas être proportionnel au risque potentiel.
À l'inverse, une ONG a souligné que les préparations médicales pour nourrissons devraient faire l'objet d'une surveillance accrue, notamment en ce qui concerne la justification de leur composition.
Les intervenants de l'industrie ayant exprimé des préoccupations ont noté que permettre une entrée plus rapide sur le marché pour les nouvelles préparations pour nourrissons favoriserait le commerce, stimulerait l'innovation et améliorerait la disponibilité et la diversité des produits au Canada. Les recommandations pour accélérer les délais incluaient l'application d'une approche fondée sur le risque, le recours aux décisions d'autres autorités réglementaires compétentes et la prise en compte de l'historique d'utilisation sécuritaire.
En ce qui concerne les aliments médicaux pour bébés, un intervenant de l'industrie a recommandé un processus accéléré de notification préalable à la mise en marché, tenant compte des approbations et de l'historique d'utilisation sécuritaire dans d'autres pays. Un autre intervenant de l'industrie a exprimé son appui à la proposition selon laquelle les aliments médicaux non enrichis pour bébés ne seraient pas soumis à des exigences d'autorisation préalable à la mise en marché.
Plusieurs recommandations ont émergé des commentaires des parties prenantes sur le processus de demande des NIAB. Il a été suggéré que les demandes de NIAB soient permises par le fabricant du NIAB, le producteur de la préparation pour nourrissons, ou conjointement par les deux parties. De plus, les intervenants ont préconisé l'acceptation de demandes simultanées pour le NIAB et la préparation pour nourrissons qui le contiendrait, ou que l'évaluation du NIAB soit intégrée au processus de demande de la préparation pour nourrissons elle-même. Un fort appui a également été exprimé pour la prise en compte des approbations de nouveaux ingrédients accordées par d'autres juridictions afin de simplifier les processus.
4.0 Contexte international
Food and Drug Administration des États-Unis
Selon le cadre réglementaire de la Food and Drug Administration des États-Unis (FDA)Note de bas de page 4, une approche de notification préalable à la mise en marché s'applique à toutes les préparations pour nourrissons, y compris les préparations médicales pour nourrissons et certains aliments médicaux pour bébés qui sont réglementés comme des préparations pour nourrissons exemptées. Toutes les préparations pour nourrissons vendues aux États-Unis doivent respecter les exigences réglementaires, y compris les normes de compositionNote de bas de page 5. Toutefois, les préparations pour nourrissons exemptées, destinées à des conditions médicales particulières, peuvent déroger aux spécifications nutritionnelles standards pour des raisons médicales. Les fabricants doivent s'enregistrer auprès de la FDA et fournir une notification de toute nouvelle préparation pour nourrissons ou modification à une préparation existante 90 jours avant la distribution.
Les nouveaux ingrédients qui sont « Generally Recognized as Safe » (généralement reconnus comme sécuritaires) (GRAS) pour une utilisation dans les préparations pour nourrissons ne sont pas tenus de passer par une approbation préalable à la mise en marché par la FDA. Pour être considérés comme GRAS et acceptables dans les préparations pour nourrissons, les ingrédients doivent répondre aux dispositions GRAS de la Federal Food, Drug and Cosmetic ActNote de bas de page 6. Les fabricants sont fortement encouragés à notifier la FDA de leur détermination GRAS avant de soumettre une notification pour une nouvelle préparation pour nourrissonsNote de bas de page 7. Toutefois, la FDA a récemment annoncé son intention de publier une règle proposée qui rendrait obligatoire la soumission des avis GRAS pour les nouveaux ingrédients alimentaires, éliminant ainsi les déterminations GRAS auto-affirmées et élargissant l'inventaire public des avis GRAS pour accroître la transparenceNote de bas de page 8.
Union européenne - Commission européenne
La Commission européenne (CE) applique un système de notification après la mise en marché pour les préparations pour nourrissons. Les préparations pour nourrissons vendues dans les pays de l'Union européenne (UE) doivent respecter des normes de composition détailléesNote de bas de page 9.
Dans l'UE, les préparations médicales pour nourrissons et les aliments médicaux pour bébés sont réglementés comme des aliments à des fins médicales spéciales (AFMS) et sont également soumis à la notification après la mise en marché. Les AFMS sont destinés à l'alimentation exclusive ou partielle des bébés dont les besoins nutritionnels ne peuvent être satisfaits par des aliments ordinaires. Les produits peuvent déroger aux exigences de composition prescrites pour les AFMS afin de répondre à leur objectif médicalNote de bas de page 10.
Les substances pouvant être ajoutées aux préparations pour nourrissons et aux AFMS sont énumérées dans une liste positive. Un examen préalable à la mise en marché est requis pour permettre l'ajout de nouvelles substances à cette listeNote de bas de page 9,Note de bas de page 10.
Normes alimentaires d'Australie et de Nouvelle Zélande
En Australie, les préparations pour nourrissons, y compris celles destinées à des fins médicales, sont autorisées à être vendues sans notification ou évaluation par Food Standards Australia New Zealand (FSANZ), à condition que le produit soit conforme à la réglementation, y compris aux exigences de compositionNote de bas de page 11. Les préparations médicales pour nourrissons (réglementées comme « special medical purpose product for infants » [SMPPi]) suivent généralement la composition standard des préparations pour nourrissons; toutefois, des dérogations sont permises pour répondre à des besoins médicaux spécifiques. La catégorie SMPPi n'inclut pas les produits médicaux spécialisés pour bébés qui ne sont pas utilisés comme source principale ou exclusive de nutrition (par exemple, les FLH); ces produits sont plutôt réglementés comme « food for special medical purposes » (FSMP)Note de bas de page 12.
Les substances ajoutées aux préparations pour nourrissons et aux SMPPi doivent figurer sur la liste des ingrédients autorisés. Les substances non inscrites sur la liste doivent faire l'objet d'une évaluation préalable à la mise en marché par FSANZ, suivie du processus standard de modification de la réglementationNote de bas de page 11,Note de bas de page 12.
5.0 Aperçu de l'approche proposée fondée sur le risque pour l'autorisation d'aliments à des fins diététiques spéciales pour bébés
Conformément à l'engagement récent du gouvernement du Canada visant à moderniser la réglementation et à réduire le fardeau administratif, une approche fondée sur le risque pour la surveillance des AFDS destinés aux bébés est proposée. Cette approche vise à améliorer l'efficacité réglementaire et à garantir que la surveillance soit proportionnelle au niveau de risque. Elle facilite l'accès aux produits, réduit les obstacles à l'importation et favorise l'innovation et la diversification du marché, tout en maintenant des normes de sécurité rigoureuses pour protéger la population vulnérable qui dépend de ces produits.
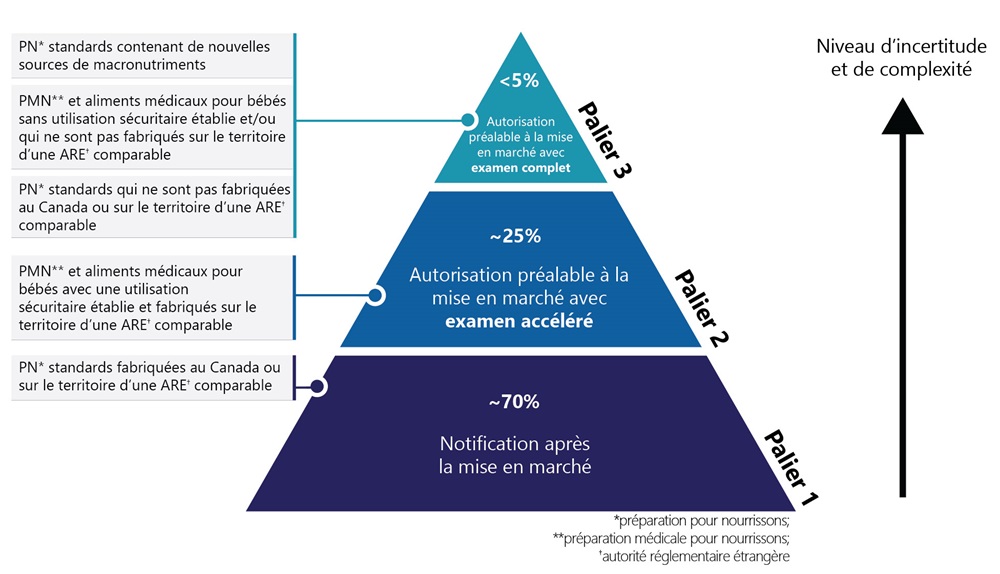
Comme illustré à la figure 1, la proposition introduit une approche à trois paliers, avec une surveillance réglementaire accrue en fonction de la complexité et de l'incertitude des produits :
- Les produits à faible risque, estimés à environ 70 % des AFDS pour bébés, seraient réglementés dans le cadre d'un régime de notification post-commercialisation, s'appuyant sur des mesures de protection intégrées qui imposent aux fabricants/importateurs la responsabilité de garantir la conformité et la sécurité;
- Les produits à risque modéré, estimés à environ 25 % des AFDS pour bébés, seraient soumis à une autorisation préalable à la mise en marché avec un examen accéléré, permettant une évaluation rapide tout en maintenant les contrôles de sécurité essentiels;
- Les produits à risque élevé, estimés à moins de 5 % des AFDS pour bébés, seraient soumis à une autorisation préalable à la mise en marché avec un examen complet, offrant une surveillance accrue lorsque le niveau de complexité et d'incertitude est le plus élevé.
Title : Description textuelle
Un diagramme en forme de pyramide illustre l'approche proposée par Santé Canada, fondée sur le risque et comportant trois paliers pour l'autorisation des AFDS destinés aux bébés. La pyramide est divisée en trois paliers horizontaux, chacun d'une couleur différente et représentant un palier distinct de surveillance réglementaire.
Sous la pyramide, la légende suivante est précisée : *préparation pour nourrissons, **préparation médicale pour nourrissons, †autorité réglementaire étrangère.
- Palier 1 (bas, bleu foncé) :
- Étiquette : « ~70 % Notification après la mise en marché »
- Une boîte de texte à gauche du palier 1, reliée par une ligne, indique les types de produits correspondant à cette catégorie : « PN* standards fabriquées au Canada ou sur le territoire d'une ARE † comparable »
- Palier 2 (milieu, bleu moyen) :
- Étiquette : « ~25 % Autorisation préalable à la mise en marché avec examen accéléré »
- Une boîte de texte à gauche du palier 2, reliée par une ligne, indique les types de produits correspondant à cette catégorie : « PMN** et aliments médicaux pour bébés avec une utilisation sécuritaire établie et fabriqués sur le territoire d'une ARE † comparable »
- Palier 3 (haut, bleu pâle) :
- Étiquette : « <5 % Autorisation préalable à la mise en marché avec examen complet »
- Trois boîtes de texte distinctes à gauche du palier 3, reliées par une seule ligne, indiquent les types de produits correspondant à cette catégorie :
- « PN* standards contenant de nouvelles sources de macronutriments »
- « PMN** et aliments médicaux pour bébés sans utilisation sécuritaire établie et/ou qui ne sont pas fabriqués sur le territoire d'une ARE † comparable »
- « PN* standards qui ne sont pas fabriquées au Canada ou sur le territoire d'une ARE † comparable »
À droite de la pyramide, une flèche pointant vers le haut, étiquetée « Niveau d'incertitude et de complexité », indique que ces deux éléments augmentent du palier 1 au palier 3.
L'approche proposée assure que les ressources réglementaires sont concentrées là où elles sont le plus nécessaires, tout en permettant une voie plus agile pour les produits à faible risque. Cette approche, ainsi que plusieurs mesures d'appui décrites ci-dessous, améliorerait l'efficacité, facilitant ainsi l'entrée sur le marché de nouveaux produits ou de produits modifiés. Un aperçu des principaux éléments de l'approche fondée sur le risque proposée est inclus en annexe.
5.1 Mesures de soutien pour améliorer l'efficacité
5.1.1 Tirer parti des informations et/ou des décisions des autorités réglementaires étrangères
Pour soutenir le régime post-commercialisation applicable au palier 1 et pour simplifier le processus d'évaluation préalable à la mise en marché applicable au palier 2, Santé Canada tirerait parti de certaines informations et décisions provenant d'autorités réglementaires étrangères (ARE) qui disposent de normes comparables et de règlements rigoureux en matière de salubrité des aliments (par exemple, les bonnes pratiques de fabrication), similaires à ceux du Canada. Cela signifie que, plutôt que d'examiner de manière indépendante tous les aspects d'un produit ou d'un procédé de fabrication, Santé Canada pourrait choisir d'accepter ou de se référer aux approbations, évaluations ou autres informations déjà établies par des ARE comparables. Essentiellement, cela permettrait à Santé Canada de s'appuyer sur le travail de partenaires internationaux réputés pour prendre des décisions éclairées concernant l'autorisation et la surveillance des produits au Canada.
5.1.2 Utilisation de l'incorporation par renvoi
Le cadre proposé sera conçu pour garantir que les mises à jour futures puissent être mises en œuvre rapidement en réponse à l'évolution des connaissances scientifiques. À cette fin, Santé Canada propose de recourir à des listes incorporées par renvoi. Les documents incorporés par renvoi peuvent être modifiés de manière administrative à la suite de consultations auprès des parties prenantes. Le règlement inclurait les listes incorporées par renvoi décrites ci-dessous.
- Liste des autorités réglementaires étrangères incorporée par renvoi
Pour appuyer l'approche fondée sur le risque de Santé Canada en matière de surveillance réglementaire, il est proposé que des ARE comparables soient établies dans une liste incorporée par renvoi. Cette liste servirait à identifier les ARE dont certaines informations pourraient être utilisées, telles que les normes de fabrication et l'établissement d'une utilisation sécuritaire. L'inclusion dans la liste incorporée par renvoi serait limitée aux ARE dont les normes de salubrité et de qualité des aliments sont comparables à celles du Canada et qui harmonisent largement leurs exigences réglementaires avec les normes de la Commission du Codex Alimentarius (Codex).
- Liste incorporée par renvoi pour la composition des préparations standards pour nourrissons
Les exigences de composition pour les préparations standards pour nourrissons seraient fondées sur les données scientifiques les plus récentes et harmonisées avec celles des ARE comparables dans la mesure du possible. En conséquence, Santé Canada suivra les travaux des ARE comparables dans le but d'établir des exigences canadiennes en matière de composition des préparations standards pour nourrissons qui permettraient d'accommoder les produits fabriqués dans ces juridictions.
La ou les listes incorporées par renvoi pour la composition des préparations standards pour nourrissons incluraient :
- Les nutriments obligatoires et facultatifs avec les niveaux minimum et maximum associés, le cas échéant;
- Les sources acceptables de macronutriments, vitamines, minéraux et autres substances, le cas échéant;
- Autres ingrédients facultatifs (y compris ceux actuellement désignés comme NIAB) avec les niveaux maximums et les spécifications associées, le cas échéant.
Les préparations pour nourrissons qui s'écartent de la liste incorporée par renvoi, à l'exception des préparations médicales pour nourrissons dont les formulations répondent à un besoin médical, ne seraient pas conformes au règlement et ne pourraient pas être vendues au Canada. Quelques exemples incluent les préparations pour nourrissons qui contiennent un nouvel ingrédient facultatif ne figurant pas sur la liste incorporée par renvoi et celles qui ont un niveau de nutriment dépassant la quantité maximale ou une nouvelle source pour une vitamine ou un minéral. Dans de tels cas, les fabricants peuvent choisir de reformuler leur produit pour se conformer aux exigences. Alternativement, les fabricants pourraient demander à Santé Canada de modifier la liste incorporée par renvoi afin d'ajuster les exigences de composition. Si l'évaluation de Santé Canada appuie la modification proposée, la proposition de modification de la liste incorporée par renvoi ferait l'objet d'une consultation publique. Si aucune nouvelle information scientifique n'est fournie lors de la période de consultation pour justifier des révisions à la proposition, Santé Canada procéderait à la modification officielle de la liste incorporée par renvoi.
À noter : les écarts concernant les sources de macronutriments ne seraient pas traités par le processus de modification de la liste incorporée par renvoi. Les produits contenant des sources non identifiées sur la liste incorporée par renvoi seraient plutôt soumis à une autorisation préalable à la mise en marché dans le cadre du palier 3. Une fois que des données probantes suffisantes permettent l'utilisation d'une nouvelle source de macronutriment dans toutes les préparations pour nourrissons, la liste incorporée par renvoi pourrait être modifiée pour ajouter cette source.
Pour les aliments médicaux destinés aux bébés, aucune exigence de composition n'est proposée, car ces produits sont spécifiquement formulés pour répondre aux besoins du consommateur visé. Toutefois, les produits doivent être fabriqués avec des sources acceptables de vitamines et minéraux identifiées dans la liste incorporée par renvoi pour la composition des préparations standards pour nourrissons. Alternativement, les fabricants pourraient reformuler le produit ou demander à Santé Canada de modifier la liste incorporée par renvoi.
5.1.3 Approche pour les ingrédients optionnels (c'est-à-dire ceux actuellement désignés comme NIAB)
Actuellement, les ingrédients facultatifs ne sont pas inclus dans les exigences de composition du RAD pour les préparations pour nourrissons, mais Santé Canada effectue un examen préalable à la mise en marché, propre au fabricant, avant d'autoriser leur utilisation dans les préparations pour nourrissons. L'approche proposée remplacerait les approbations propres au fabricant par des approbations génériques des ingrédients, en adoptant un modèle similaire à celui de l'UE et de FSANZ. La liste incorporée par renvoi pour la composition des préparations standards pour nourrissons inclurait tous les ingrédients précédemment examinés et approuvés par Santé Canada pour utilisation dans les préparations pour nourrissons, ainsi que les spécifications pertinentes.
Pour répondre aux préoccupations des parties prenantes concernant le processus d'approbation des nouveaux ingrédients facultatifs, il est proposé de ne pas restreindre qui peut demander à Santé Canada de modifier la liste incorporée par renvoi; par exemple, cela inclurait — sans s'y limiter — le fabricant de la préparation pour nourrissons ou le fabricant de l'ingrédient.
5.1.4 Utilisation des exemptions pour les produits alimentaires médicaux à des fins diététiques spéciales destinés aux bébés
- Exemptions permettant des écarts par rapport aux exigences de composition
Comme indiqué lors des consultations précédentes, les préparations médicales pour nourrissons devraient respecter les exigences de composition des préparations standards pour nourrissons. Toutefois, des exemptions seraient permises lorsque des écarts sont nécessaires pour atteindre l'objectif médical prévu du produit.
- Exemptions visant à réduire les obstacles à l'importation
Étant donné que les préparations médicales pour nourrissons et les aliments médicaux destinés aux bébés sont essentiels pour les bébés vulnérables et en grande partie importés au Canada, Santé Canada examine la possibilité d'accorder des exemptions ciblées à certaines exigences réglementaires, telles que les écarts dans la composition des produits qui ne visent pas à répondre à un besoin médical spécifique. L'objectif de ces exemptions serait de réduire les obstacles à l'importation au Canada de produits conformes aux exigences du pays exportateur — à condition que ce pays soit représenté par une ARE figurant sur la liste incorporée par renvoi. L'Australie, qui dépend également des importations, dispose d'un cadre permettant de telles exemptions spécifiques pour les SMPPi afin de garantir l'approvisionnement en ces produits essentiels pour les bébés vulnérables qui en dépendent. Santé Canada prévoit réaliser des analyses supplémentaires pour déterminer si des exemptions similaires pourraient être incluses dans le cadre réglementaire proposé.
5.2 Descriptions des paliers
5.2.1 Palier 1 ─ Notification après la mise en marché
5.2.1.1 Portée
Il est proposé que les produits inclus dans le palier 1 soient :
- Des préparations pour nourrissons destinées aux bébés nés à terme et en bonne santé (0 à 12 mois)
- Fabriquées au Canada ou sous la juridiction d'une ARE comparable
Les produits du palier 1 doivent respecter les exigences de composition pour les préparations standards pour nourrissons.
Exemples de produits inclus dans le palier 1 :
- Préparations à base de lait de vache ou de lait de chèvre, y compris :
- Celles à faible teneur en lactose/sans lactose et/ou à base de protéines partiellement hydrolysées
- Préparations à base de protéines de soja, y compris :
- Celles à base de protéines partiellement hydrolysées
5.2.1.2 Justification
Les produits inclus dans le palier 1 présentent le plus faible niveau d'incertitude et de complexité. Les produits ont été attribués au palier 1 en fonction des considérations suivantes :
- La composition du produit repose sur des exigences rigoureusement examinées et conformes aux normes établies par des ARE comparables, favorisant une croissance et un développement adéquats — sans exemptions permises;
- Les produits sont fabriqués au Canada ou sous la juridiction d'une ARE comparable dont les normes de salubrité et de qualité des aliments sont similaires à celles du Canada.
5.2.1.3 Exigences des notifications
Les produits du palier 1 seraient vendus sans approbation préalable à la mise en marché; toutefois, les fabricants/importateurs devraient soumettre à Santé Canada des informations justificatives par le biais d'une notification post-commercialisation au plus tard le premier jour de vente au Canada. Les exigences de notification sont encore à l'étude, mais il est prévu qu'elles ne soient pas contraignantes (par exemple, elles pourraient inclure une copie de l'étiquette, le nom de l'importateur/fabricant). Ces informations soutiendraient la surveillance des produits sur le marché canadien et aideraient à assurer une réponse appropriée en cas de pénurie ou de risque de pénurie.
Il est important de noter que la responsabilité incomberait aux fabricants/importateurs de veiller à ce qu'ils respectent la réglementation. En plus des règlements spécifiques aux préparations pour nourrissons, y compris les règlements sur l'utilisation des additifs alimentaires dans les aliments pour bébés, les fabricants/importateurs sont responsables de s'assurer que leur produit est conforme à toutes les exigences législatives et réglementaires applicables en vertu de la Loi et du Règlement sur les aliments et drogues et de la Loi et du Règlement sur la salubrité des aliments au Canada, y compris détenir une licence, la traçabilité, l'emballage, l'étiquetage et la salubrité des aliments. Cela signifie qu'une demande de modification réglementaire serait nécessaire pour tout écart par rapport aux règlements et que la demande devrait être approuvée avant la vente du produit.
5.2.2 Palier 2 ─ Autorisation préalable à la mise en marché avec examen accéléré
5.2.2.1 Portée
Deux types de produits, énumérés ci-dessous, sont proposés pour inclusion dans le palier 2. Pour les deux catégories, les produits doivent être fabriqués et avoir une utilisation sécuritaire établie dans la juridiction d'une ARE comparable. Les critères pour démontrer une utilisation sécuritaire établie sont décrits à la section 5.2.2.3.
- Préparations médicales pour nourrissons (formulées comme substitut au lait maternel et convenant comme source unique de nutrition)
- Ces produits devraient respecter les exigences de composition prescrites pour les préparations standards pour nourrissons; toutefois, des écarts seraient permis, y compris pour les sources de macronutriments, afin de répondre à un objectif médical spécifique.
- Aliments médicaux enrichis pour bébés (strictement destinés à une alimentation partielle)
- Ces produits pourraient être enrichis; cependant, la réglementation n'imposerait pas de niveaux minimums et maximums. Néanmoins, à moins qu'un micronutriment soit désigné pour une application médicale particulière, la formulation doit inclure uniquement les sources de vitamines et de minéraux autorisées dans les préparations standards pour nourrissons.
Reconnaissant l'importance de l'harmonisation internationale et la dépendance du Canada à l'égard des AFDS médicaux importés pour répondre aux besoins des bébés vulnérables, Santé Canada examine la possibilité d'exemptions ciblées pour les produits du palier 2, comme décrit à la section 5.1.4(ii).
Des exemples de produits inclus dans le palier 2 sont présentés au tableau 1.
Types de produits |
|
|---|---|
Préparations médicales pour nourrissons |
Aliments médicaux enrichis pour bébés |
|
|
5.2.2.2 Justification
Comparativement aux autres produits classés dans le système à trois paliers, ces produits présentent un niveau modéré d'incertitude et de complexité. À l'instar du cadre actuel pour les FLH, l'autorisation préalable à la mise en marché assure une surveillance pour ces produits médicalement nécessaires. Toutefois, l'examen accéléré proposé s'appuie sur des informations provenant d'ARE comparables afin de gagner en efficacité, permettant ainsi un accès plus rapide tout en maintenant les normes de sécurité et de qualité. Les produits ont été attribués au palier 2 en fonction des considérations suivantes :
- Une surveillance de la composition du produit est nécessaire, car :
- Des écarts par rapport aux exigences de composition standard sont permis pour les préparations médicales pour nourrissons;
- Aucun niveau maximal de nutriments n'est prescrit pour les aliments médicaux destinés aux bébés;
- Les lignes directrices de la pratique clinique et/ou les recommandations nutritionnelles peuvent varier selon les juridictions.
- Cependant, la nécessité d'un examen complet, comme proposé pour les produits du palier 3, est atténuée puisque :
- Les produits sont fabriqués dans la juridiction d'une ARE comparable avec des normes de salubrité et de qualité des aliments similaires à celles du Canada;
- Les produits doivent avoir une utilisation sécuritaire établie dans la juridiction d'une ARE comparable.
5.2.2.3 Exigences des demandes préalables à la mise en marché avec examen accéléré
Comme c'est le cas pour les produits du palier 1, les fabricants/importateurs sont responsables de s'assurer que leur produit est conforme à toutes les exigences législatives et réglementaires applicables en vertu de la Loi sur les aliments et drogues et de son règlement, ainsi que de la Loi sur la salubrité des aliments au Canada et de son règlement, y compris détenir une licence, la traçabilité, l'emballage, l'utilisation des additifs alimentaires, l'étiquetage et la salubrité des aliments. Cela signifie qu'une demande de modification réglementaire serait nécessaire pour tout écart par rapport à la réglementation à des fins non médicales, et que cette demande devrait être approuvée avant l'examen de la demande de la préparation pour nourrissons par Santé Canada. Ceci s'applique indépendamment des exemptions envisagées à la section 5.1.4(ii) visant à réduire les obstacles à l'importation.
Une description complète des exigences des demandes pour les produits du palier 2 est encore à l'étude. Toutefois, à ce stade, les exigences suivantes sont proposées :
- Données démontrant une utilisation sécuritaire établie dans la juridiction d'une ARE comparable :
- Preuve que le produit :
- a été examiné et autorisé pour utilisation par une ARE comparable (par exemple, la dernière étiquette étrangère approuvée et la lettre d'approbation de l'ARE qui l'autorise)
ou
- a été vendu et utilisé en toute sécurité dans la juridiction d'une ARE comparable pendant une période minimale de deux ans (par exemple, rapports d'experts cliniques ayant supervisé l'utilisation sécuritaire du produit ou rapports d'ARE tels que des dossiers de surveillance post-commercialisation).
- Preuve que le produit :
À noter : dans ce dernier cas, une période de deux ans est proposée afin de permettre le signalement de tout problème de sécurité, y compris les réactions indésirables, après douze mois d'utilisation.
- Données à l'appui de la composition du produit :
- Pour les préparations médicales pour nourrissons qui diffèrent des exigences de composition standard en raison d'un objectif médical spécifique, une brève justification et des preuves à l'appui de la variation seraient nécessaires.
- Pour les aliments médicaux destinés aux bébés, même s'il n'existe pas d'exigences de composition prescrites, une justification concise et des preuves à l'appui seraient nécessaires pour soutenir la formulation du produit.
5.2.2.4 Processus accéléré d'autorisation préalable à la mise en marché
Il est proposé que les fabricants/importateurs soient tenus d'envoyer une demande écrite à Santé Canada pour commercialiser leur produit. Dès réception de la demande, un examen initial serait effectué et une lettre d'accusé de réception serait envoyée au requérant.
Il est proposé que l'examen accéléré porte principalement sur la vérification de la sécurité et de la suffisance nutritionnelle. Par exemple :
- Confirmation du statut d'utilisation sécuritaire dans la juridiction d'une ARE comparable
- Examen de la justification médicale des écarts par rapport aux exigences réglementaires
L'autorisation de commercialiser le produit serait accordée lorsque le fabricant/importateur recevra une autorisation écrite de Santé Canada.
5.2.3 Palier 3 ─ Autorisation préalable à la mise en marché avec examen complet
5.2.3.1 Portée
Il est proposé que les produits inclus dans le palier 3 regroupent les mêmes catégories de produits que celles des paliers 1 et 2, à l'exception des cas suivants :
- Pour les préparations pour nourrissons nés à terme et en bonne santé:
- Le produit n'est pas fabriqué au Canada ou dans la juridiction d'une ARE comparable et/ou
- Contient une nouvelle source de macronutriments (par exemple, protéine de riz, protéine de pois)
- Pour les préparations médicales pour nourrissons et les aliments médicaux enrichis pour bébés:
- Le produit n'est pas fabriqué dans la juridiction d'une ARE comparable et/ou n'a pas d'utilisation sécuritaire établie dans une juridiction d'ARE comparable, ou
- Le produit est fabriqué au Canada et n'a pas d'utilisation sécuritaire établie
5.2.3.2 Justification
Comparativement aux autres produits classés dans le système à trois paliers, ces produits présentent le plus haut niveau d'incertitude et de complexité. L'approche proposée d'autorisation préalable à la mise en marché avec examen complet permettrait d'atténuer le risque accru associé à ces produits, en lien avec les trois enjeux suivants :
Premièrement, certains produits du palier 3 ne sont pas fabriqués au Canada ou dans la juridiction d'une ARE comparable. Un examen préalable complet permettra à Santé Canada de vérifier que le produit respecte les exigences réglementaires applicables et d'évaluer le procédé de fabrication ainsi que les procédures de contrôle de la qualité afin de garantir que les produits sont fabriqués selon des normes de salubrité et de qualité reconnues internationalement.
Deuxièmement, les préparations médicales pour nourrissons et les aliments médicaux pour bébés inclus dans le palier 3 n'ont pas d'utilisation sécuritaire établie au Canada ou dans une juridiction d'ARE comparable. Un examen préalable complet permettra à Santé Canada d'évaluer la suffisance nutritionnelle et la sécurité de la formulation sur la base de données cliniques.
Enfin, pour les préparations pour nourrissons utilisant de nouvelles sources de macronutriments, il existe peu de données sur leur rôle dans la croissance et le développement des bébés nés à terme et en bonne santé. Le processus d'autorisation préalable à la mise en marché du palier 3 permettra à Santé Canada d'évaluer l'adéquation nutritionnelle et la sécurité d'un produit contenant une nouvelle source de macronutriments en examinant les données cliniques.
5.2.3.3 Exigences des demandes préalables à la mise en marché avec examen complet
Comme c'est le cas pour les produits des paliers 1 et 2, les fabricants/importateurs de produits du palier 3 sont responsables de s'assurer que leur produit est conforme à toutes les exigences législatives et réglementaires applicables en vertu de la Loi sur les aliments et drogues et de son règlement, ainsi que de la Loi sur la salubrité des aliments au Canada et de son règlement, y compris détenir une licence, la traçabilité, l'emballage, l'utilisation des additifs alimentaires, l'étiquetage et la salubrité des aliments. Cela signifie qu'une demande de modification réglementaire serait nécessaire pour tout écart par rapport à la réglementation à des fins non médicales, et que cette demande devrait être approuvée avant l'examen de la demande de la préparation pour nourrissons par Santé Canada.
Pour les produits qui ne sont pas fabriqués au Canada ou dans la juridiction d'une ARE comparable, il est proposé que les fabricants/importateurs soient tenus de soumettre des preuves démontrant leur conformité aux exigences réglementaires ainsi que des détails complets sur le procédé de fabrication et les procédures de contrôle de la qualité (par exemple, des données démontrant que le produit a été fabriqué selon de bonnes pratiques de fabrication).
Pour les préparations médicales pour nourrissons et les aliments médicaux pour bébés sans utilisation sécuritaire établie, ainsi que pour toute préparation pour nourrissons contenant une nouvelle source de macronutriments, il est proposé que le fabricant/importateur soit tenu de soumettre des données cliniques à l'appui de la suffisance nutritionnelle et de la sécurité de la formulation dans les conditions d'utilisation recommandées. De plus, une justification de la composition du produit serait également requise pour les préparations médicales pour nourrissons et les aliments médicaux pour bébés.
5.2.3.4 Processus d'autorisation préalable à la mise en marché
Il est proposé que les fabricants/importateurs soient tenus d'envoyer une demande écrite à Santé Canada pour commercialiser leur produit. Dès réception de la soumission, un examen initial serait effectué et une lettre d'accusé de réception serait envoyée au requérant. Ensuite, Santé Canada procéderait à l'évaluation des informations requises afin de déterminer si la sécurité, la qualité et/ou la suffisance nutritionnelle du produit ont été démontrées. Les éléments de l'examen de Santé Canada sont présentés dans le tableau récapitulatif de l'annexe.
L'autorisation de commercialiser le produit serait accordée lorsque le fabricant/importateur recevra une autorisation écrite de Santé Canada.
5.3 Gains d'efficacité attendus
En transférant la majorité des produits vers un régime de notification post-commercialisation et en accélérant les examens préalables à la mise en marché grâce à l'utilisation d'informations et/ou de décisions provenant d'ARE comparables, l'approche proposée permettrait de réaliser des gains d'efficacité significatifs sans compromettre la sécurité.
Les délais d'examen préalable à la mise en marché pour les produits des paliers 2 et 3 seront proposés en même temps que le projet de règlement et tiendront compte des commentaires reçus dans le cadre de cette consultation. Toutefois, il est prévu que les délais d'examen pour les produits du palier 2 soient plus courts que ceux pour les produits du palier 3.
5.4 Modifications aux produits commercialisés
Actuellement, tout changement majeur apporté à une préparation pour nourrissons ou à un FLH commercialisé nécessite une demande préalable à la mise en marché. Dans le cadre du nouveau cadre réglementaire modernisé, des mises à jour de cette approche sont proposées.
5.4.1 Changements en conformité avec les exigences du Règlement sur les aliments et drogues
Les changements apportés aux AFDS pour bébés commercialisés — qu'il s'agisse de préparations standards pour nourrissons, de préparations médicales pour nourrissons ou d'aliments médicaux enrichis pour bébés — seraient permis sans notification, à condition que le produit révisé demeure conforme à la réglementation en vigueur. Par exemple, un changement concernant :
- les ingrédients ou les niveaux, tel qu'un changement d'additif alimentaire ou de nutriment, tant que le nouvel ingrédient et/ou niveau est permis selon la réglementation;
- un site de fabrication, à condition que le produit soit toujours fabriqué au Canada ou dans la juridiction d'une ARE comparable.
Pour les aliments médicaux destinés aux bébés, puisque les niveaux de nutriments ne seraient pas définis dans le RAD, tout changement à ces niveaux nécessiterait une demande d'autorisation préalable à la mise en marché, comme décrit ci-dessous.
5.4.2 Changements nécessitant une action réglementaire
Si un changement ne respecte pas la réglementation, deux voies s'appliquent :
- Demande de modification réglementaire
Une demande de modification réglementaire serait nécessaire si le changement implique un écart par rapport au RAD et n'est pas destiné à un objectif médical. Par exemple, le produit révisé contient un ingrédient ou un niveau non permis selon le RAD, tel qu'un additif alimentaire non approuvé ou un niveau de nutriment dépassant la quantité maximale autorisée.
Il est prévu que la plupart des demandes de modification réglementaire concernent des mises à jour des documents incorporés par renvoi, où les changements pourraient être effectués de façon administrative.
- Demande d'autorisation préalable à la mise en marché
Une demande d'autorisation préalable à la mise en marché serait nécessaire dans les circonstances suivantes :
- Le produit n'est plus fabriqué au Canada ou dans la juridiction d'une ARE comparable;
- Un changement de site ou de procédé de fabrication pour un produit non fabriqué au Canada ou dans la juridiction d'une ARE comparable;
- Le changement implique un écart par rapport au RAD pour répondre à un objectif médical spécifique (par exemple, sur la base de nouvelles données cliniques), tel que des modifications à la composition d'une préparation médicale pour nourrissons;
- Le changement affecte les niveaux de nutriments dans les aliments médicaux enrichis pour bébés.
- Puisque les niveaux d'enrichissement ne seraient pas prescrits dans le RAD, un examen préalable à la mise en marché serait nécessaire pour garantir la sécurité.
À noter : les demandes d'autorisation préalable à la mise en marché pourraient être rationalisées pour les produits ayant une utilisation sécuritaire établie et/ou fabriqués au Canada ou dans la juridiction d'une ARE comparable.
6.0 Questions pour les parties prenantes
Santé Canada invite les répondants à formuler leurs commentaires en répondant aux questions suivantes. Veuillez détailler vos réponses lorsque cela est pertinent. Par exemple, si vous n'êtes pas d'accord avec une proposition, veuillez expliquer pourquoi.
- Appuyez-vous l'approche proposée d'autorisation des AFDS pour bébés fondée sur le risque et structurée en trois paliers?
- Appuyez-vous la portée proposée des produits inclus dans chaque palier?
- Appuyez-vous la proposition visant à utiliser certaines informations et décisions provenant d'ARE comparables pour accélérer certains aspects du processus d'examen préalable à la mise en marché ?
- Appuyez-vous l'approche proposée visant à inclure les exigences de composition, y compris les ingrédients facultatifs (c'est-à-dire ceux actuellement désignés comme NIAB), dans un document incorporé par renvoi au règlement?
- Avez-vous des commentaires concernant la possibilité pour Santé Canada d'envisager des exemptions pour les AFDS médicaux pour bébés (c'est-à-dire les produits du palier 2) qui respectent les exigences d'une ARE comparable afin de réduire les obstacles à l'importation de produits conformes aux exigences du pays exportateur ?
- Appuyez-vous l'approche proposée pour traiter les modifications apportées aux produits commercialisés?
- Appuyez-vous la proposition concernant les exigences des demandes préalables à la mise en marché proposées pour les paliers 2 et 3 ?
- Avez-vous d'autres commentaires sur des aspects qui n'auraient pas été abordés ?
7.0 Conclusion
L'approche proposée par Santé Canada pour l'autorisation des AFDS pour bébés, fondée sur le risque, s'aligne sur l'initiative du gouvernement du Canada visant à moderniser la réglementation désuète et à réduire le fardeau administratif, en équilibrant la surveillance réglementaire avec la nécessité de soutenir l'innovation, de faciliter l'accès à une gamme diversifiée de produits et de s'harmoniser avec les ARE. En adaptant les exigences selon la complexité et le niveau d'incertitude face aux produits, cette approche vise à maintenir des normes de sécurité rigoureuses pour les produits destinés aux populations vulnérables tout en réduisant le fardeau réglementaire inutile et en soutenant le commerce. Il est important de souligner que ces objectifs sont atteints en transférant la majorité des produits (c'est-à-dire ceux présentant un faible risque) vers un régime de notification post-commercialisation et en accélérant les examens préalables à la mise en marché pour les produits à risque modéré grâce à l'utilisation d'informations et/ou de décisions provenant d'ARE comparables, ce qui permet de réaliser des gains d'efficacité significatifs sans compromettre la sécurité.
La rétroaction des parties prenantes est essentielle pour garantir que la réglementation soit efficace et réponde aux besoins des consommateurs, des professionnels de la santé et de l'industrie. Les commentaires reçus lors de cette préconsultation orienteront la rédaction du règlement, qui sera prépublié dans la Gazette du Canada, Partie I pour une consultation publique supplémentaire.
Annexe
| Catégories | Origine de la fabrication | Doit respecter les exigences de composition et autres exigences applicables du RAD | Dérogations à la composition standard pour des raisons médicales | Élément de l'examen (i) : Conformité aux exigences du RAD | Élément de l'examen (ii) : Fabrication (sécurité et qualité) | Élément de l'examen (iii) : Justification de la dérogation médicale/de la composition | Élément de l'examen (iv) : Données démontrant une utilisation sécuritaire établie | Élément de l'examen (v) : Données cliniques pour les dérogations médicales/composition | Élément de l'examen (vi) : Données cliniques pour les nouvelle source de macronutriments |
|---|---|---|---|---|---|---|---|---|---|
| Palier 1 - Notification après la mise en marché | |||||||||
| PN destinée aux bébés nés à terme et en bonne santé | Canada ou la juridiction d'une AREc | Oui | S.O. | N.R. | N.R. | S.O. | S.O. | S.O. | S.O. |
| Palier 2 - Autorisation préalable à la mise en marché avec examen accéléré | |||||||||
| PMN et aliments médicaux pour bébésNote de bas de page a du tableau 2 | La juridiction d'une AREc | Oui | OuiNote de bas de page b du tableau 2 | N.R. | N.R. | Oui | Oui | N.R. | N.R. |
| Palier 3 - Autorisation préalable à la mise en marché avec examen complet | |||||||||
| PN destinée aux bébés nés à terme et en bonne santé | Toute juridiction autre que le Canada ou une AREc | Oui | S.O. | Oui | Oui | S.O. | S.O. | S.O. | S.O. |
| PN destinée aux bébés nés à terme et en bonne santé contenant une nouvelle source de macronutriments | Toute juridiction | Oui | S.O. | OuiNote de bas de page c du tableau 2 | OuiNote de bas de page c du tableau 2 | S.O. | S.O. | S.O. | Oui |
| PMN et aliments médicaux pour bébés | Canada ou toute juridiction autre qu'une AREc | Oui | OuiNote de bas de page b du tableau 2 | OuiNote de bas de page d du tableau 2 | OuiNote de bas de page d du tableau 2 | Oui | S.O. | Oui | OuiNote de bas de page e du tableau 2 |
RAD - Règlement sur les aliments et drogues; PMN - Préparation médicale pour nourrissons; PN - Préparation pour nourrissons; AREc - Autorité réglementaire étrangère comparable; N.R. - non requis; S.O. – sans objet |
|||||||||