Document d’orientation pour le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères)
Version 1.0
Le présent Document d’orientation a été rédigé pour aider les déclarants à se conformer au Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [le Règlement] de la Loi canadienne sur la protection de l’environnement (1999) [la Loi]. Il a pour but d’aider les déclarants à établir si une substance doit être déclarée en vertu du Règlement et à déterminer quels renseignements fournir. Il renferme également des instructions détaillées pour compléter une Déclaration de substances nouvelles (DSN). Ce Document d’orientation remplace les Directives pour la déclaration et les essais de substances nouvelles : substances chimiques et polymères publiées en 2005.
Nous avons veillé à ce que le présent Document d’orientation réflète fidèlement les exigences de la Loi et du Règlement. Toutefois, en cas d’incompatibilité entre le Document d’orientation et le Règlement ou la Loi, le Règlement et la Loi ont préséance.
Pour obtenir une version PDF du Document d’orientation, veuillez consulter le site Web des publications du gouvernement du Canada.
Consultation publique sur le Document d’orientation
Les commentaires que nous avons reçus durant la période de consultation publique de 90 jours sur le Document d’orientation et qui ont été soumis au plus tard le 30 juin 2021 ont été pris en considération lors de la finalisation du Document d’orientation. Continuer sur la page Web de notre réponse aux commentaires afin de les consulter.
Résumé
Le présent document (appelé Document d’orientation) a été rédigé pour aider les déclarants à se conformer au Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [le Règlement] de la Loi canadienne sur la protection de l’environnement (1999).
Le Document d’orientation a pour but d’aider les déclarants à établir si une substance doit être déclarée en vertu du Règlement et à déterminer quels renseignements fournir. Il renferme également, mais sans s’y limiter, des instructions détaillées pour compléter une déclaration de substances nouvelles, des diagrammes permettant de décider facilement quelle annexe doit être produite (consulter l’appendice 1), des précisions sur les renseignements techniques exigés, des renseignements détaillés sur la manière de remplir le formulaire de Déclaration de substances nouvelles, l’énumération des pratiques et procédures d’essai appropriées et un aperçu de la méthode de communication des renseignements confidentiels.
Enfin, il précise comment le Programme des substances nouvelles (SN) utilise et évalue les renseignements fournis dans une Déclaration de substances nouvelles et explique les implications possibles des décisions d’évaluation pour les déclarants.
Remarque : Les organismes vivants ne figurant pas sur la Liste intérieure peuvent être assujettis au Règlement sur les renseignements concernant les substances nouvelles (organismes). Ils ne sont pas visés par le Document d’orientation puisque celui-ci concerne les substances chimiques et biochimiques ainsi que les polymères et les biopolymères. Pour déterminer si, en vertu du Règlement sur les renseignements concernant les substances nouvelles (organismes), il faut déclarer un organisme vivant, veuillez consulter les Lignes directrices pour la déclaration et les essais de substances nouvelles : organismes.
Pour un aperçu des processus appliqués par le Programme des SN lors de l’admnistration des présentations de renseignements reçues conformément au Règlement, veuillez consulter l’Administration du Programme des substances nouvelles – Traitement des demandes.
Comment utiliser le Document d’orientation
Le présent Document d’orientation a été rédigé à l’intention des personnes visées par les dispositions du Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) pris en vertu de la Loi canadienne sur la protection de l’environnement (1999). Un survol des parties du Document d’orientation, énumérées plus bas, permettra au lecteur de repérer les exigences qui le concernent.
Pour éviter les retards inutiles pendant la production d’une Déclaration de substances nouvelles, il importe de bien connaître les propriétés de la substance concernée et de savoir quelles dispositions du Règlement s’appliquent, ce que le Document d’orientation vous aidera à faire.
Le Document d’orientation comporte 10 parties :
- Introduction et survol : Porte sur l’objectif, les pouvoirs légaux et les caractéristiques du Programme des substances nouvelles;
- Inventaires : Explique ce que sont la Liste intérieure et la Liste extérieure, le processus de modification de ces listes et les moyens de vérifier si une substance est inscrite à l’une ou l’autre;
- Substances : Aide à déterminer si une substance à fabriquer, importer ou utiliser doit être déclarée et présente les définitions des substances de catégories particulières ainsi que des substances assujetties ou non aux exigences de la déclaration;
- Renseignements requis pour les déclarations : Aide dans le choix de l’annexe qui doit être présentée pour une substance assujettie aux exigences de la déclaration et indique quand il faut présenter une Déclaration de substances nouvelles au ministre de l’Environnement ou par l’entremise du Programme des substances nouvelles;
- Déclaration de substances nouvelles : Indique quels renseignements sont requis dans une Déclaration de substances nouvelles;
- Formulaire de Déclaration de substances nouvelles : Indique comment remplir le formulaire de Déclaration de substances nouvelles ainsi que la signification et le but de chacune des exigences en matière de renseignements et présente les cas pour lesquels ces éléments d’information ne sont pas exigés;
- Renseignements confidentiels : Porte sur des aspects liés aux renseignements commerciaux confidentiels comme les demandes de confidentialité, le maquillage de la dénomination de substances et la recherche de substances confidentielles dans la Liste intérieure et la Liste extérieure;
- Protocoles d’essai recommandés et méthodes de rechange : Contient des recommandations relatives aux méthodes d’essai acceptables et les méthodes de rechange ainsi qu’une explication du paragraphe 81(8) de la Loi qui permet d’obtenir une dérogation relative à l’information requise dans le cas de substances satisfaisant à un ou à des critères. Le Programme des substances nouvelles permet aux déclarants de présenter une demande de Consultation avant déclaration [CAD] (consulter la partie 8.8) afin de résoudre des problèmes relatifs à la déclaration pendant la préparation d’une Déclaration de substances nouvelles;
- Traitement de la Déclaration de substances nouvelles : Explique le cheminement des Déclaration de substances nouvelles après leur réception, notamment leur traitement et leur examen, et les types de lettres que pourrait expédier le Programme des substances nouvelles;
- Responsabilités après la déclaration : Examine les obligations des déclarants et du Programme des substances nouvelles après le dépôt d’une Déclaration de substances nouvelles.
Pour plus de précisions ou pour obtenir les dernières mises au point sur le Document d’orientation, veuillez consulter le site Web du Programme des substances nouvelles, communiquez avec la Ligne d’information de la gestion des substances au 1-800-567-1999 (au Canada) ou au 1-819-938-3232 (à l’extérieur du Canada) ou écrivez à substances@ec.gc.ca.
Partie 1. Introduction et survol
1.1 Objet du Document d’orientation
Le présent Document d’orientation contient des conseils pour assurer la conformité au Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [le Règlement]. Il explique quels sont les renseignements qu’une personneNote de bas de page 1 qui fabrique ou importe des substancesNote de bas de page 2 nouvelles au Canada (le déclarant) doit présenter au ministre de l’Environnement (le ministre) au sens des paragraphes 81(1) et 81(4) de la Loi canadienne sur la protection de l’environnement (1999) [la Loi] avant de fabriquer ou d’importer une substance chimique ou biochimiqueNote de bas de page 3, un nanomatériau, un polymère ou un biopolymèreNote de bas de page 4 qui ne figure pas sur la Liste intérieure.Note de bas de page 5 Ces renseignements sont exigés afin que le ministre ou le ministre de la Santé puisse déterminer si la substance est toxique ou pourrait le devenir au sens de l’article 64 de la Loi. Dans le Document d’orientation, le sens donné à « toxique » est celui précisé à l’article 64 de la Loi (consulter la partie 9.5.2). De plus, le Document d’orientation décrit les obligations du ministre de l’Environnement et du ministre de la Santé (les ministres) relativement aux délais pour les évaluations, ainsi que celles du ministre concernant l’inscription d’une substance chimique ou d’un polymère sur la Liste intérieure, en vertu de l’article 87 de la Loi.
Précisons que le Document d’orientation pour le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) n’aborde pas le Règlement sur les renseignements concernant les substances nouvelles (organismes). Les renseignements relatifs à la réglementation des organismes vivants figurent aux Lignes directrices pour la déclaration et les essais de substances nouvelles : organismes.
Les membres de l’équipe du Programme des substances nouvelles (SN) sont des fonctionnaires d’Environnement et Changement climatique Canada et de Santé Canada. Chacun de ces ministères évalue les renseignements de la Déclaration de substances nouvelles (DSN) présentée au ministre.
1.2 La Loi canadienne sur la protection de l’environnement (1999)
La Loi est une disposition législative sur le développement durable et la prévention de la pollution. Les objectifs de cette loi sont réalisés ou facilités par plusieurs mécanismes comme les dispositions relatives aux substances et activités nouvelles au Canada. En vertu de ces dispositions, les ministres doivent évaluer les substances qui ne figurent pas sur la Liste intérieure afin d’établir si elles satisfont les critères énoncés à l’article 64 de la Loi et si elles devraient faire l’objet de mesures suite à l’évaluation.
1.3 Aperçu des dispositions de la Loi concernant les substances nouvelles
Il est obligatoire de déclarer les substances visées par les articles 80 à 89 de la Loi. Ces substances à déclaration obligatoire sont :
- les substances nouvelles au Canada (celles ne figurant pas sur la Liste intérieure) qui sont fabriquées au Canada ou importées au Canada;
- les substances utilisées pour une nouvelle activité (NAc) (consulter la partie 9.6).
La Loi comporte plusieurs clauses portant notamment sur les critères qui déterminent si une substance doit être déclarée, sur les obligations des fabricants et des importateurs relativement à la déclaration, sur un mécanisme d’évaluation détaillé et sur les autorités habilitantes concernant l’application des mesures de gestion des risques.
La Loi prévoit une gestion à la fois proactive et préventive des substances nouvelles. En effet, elle suit un processus de déclaration et d’évaluation préalable à la fabrication ou à l’importation. Si ce processus déterminait qu’une substance nouvelle était susceptible de poser un risque pour la santé humaine ou l’environnement, la Loi habiliterait le ministre à intervenir avant ou durant les premières étapes de l’introduction de ladite substance au Canada. Grâce à cette capacité d’intervention précoce, le Programme des SN est une composante unique et essentielle de la démarche fédérale de saine gestion des produits chimiques au Canada.
Le Règlement prescrit les renseignements exigés pour la déclaration. Les principales caractéristiques du Programme des SN sont :
- l’établissement de catégories de substances;
- l’énumération des exigences administratives et des autres exigences en matière de renseignements;
- la prescription de conditions, de méthodes d’essai et de pratiques de laboratoire pour la préparation des données d’essai;
- la désignation du moment de la déclaration avant la fabrication, l’importation ou le début d’une nouvelle activité;
- l’obligation pour le Programme des SN d’évaluer les renseignements reçus au cours d’une période déterminée.
Pour tenir compte des besoins d’évaluation des différentes catégories de substances, on a établi les exigences en matière de renseignements en séparant les substances en catégories et en groupes de déclaration. En général, on classe d’abord les substances par type de substance (par exemple, les produits chimiques et les polymères) et on subdivise ensuite chaque type de substance en groupes de déclaration, d’après des facteurs comme la quantité de substance fabriquée ou importée ou l’utilisation prévue (par exemple, la recherche et le développement).
Le processus d’évaluation commence lorsque le Programme des SN reçoit une DSN complète pour une substance nouvelle qui doit être fabriquée ou importée. Les DSN doivent contenir tous les renseignements administratifs et techniques prescrits par le Règlement et le paiement du droit approprié (s’il y a lieu), ainsi que la justification des requêtes de confidentialité. Selon le groupe de déclaration, les DSN doivent être présentées au Programme des SN au minimum de 5 à 75 jours civils avant de dépasser la quantité seuil applicable.
Les déclarations de nouvelle activité (DNAc) doivent contenir tous les renseignements prescrits par l’avis ou l’arrêté de NAc (consulter la partie 9.6.2) et il faut les présenter avant d’entreprendre toute nouvelle activité selon l’échéancier prévu à l’avis ou l’arrêté de NAc (habituellement 90 jours avant le début de la nouvelle activité).Note de bas de page 6
Il arrive qu’une quantité soit précisée dans l’avis ou l’arrêté de NAc (par exemple, toute activité concernant plus de 10 kg par année civile). Dans un tel cas, toute personne qui propose une nouvelle activité pour la substance doit divulguer les renseignements prescrits au moins 90 jours avant de dépasser la quantité précisée au cours d’une année civile.
Lorsque l’avis ou l’arrêté de NAc ne précise pas de quantité pour la substance, toute personne proposant une nouvelle activité (0 kg par année civile) doit fournir les renseignements requis dans l’avis ou l’arrêté de NAc 90 jours avant le début de la nouvelle activité prévue.
Au nom du ministre, le Programme des SN évalue les risques pour l’environnement et la santé humaine en se fondant sur les renseignements fournis et sur toute autre information qui lui est disponible pour établir si la substance est toxique ou susceptible de le devenir (consulter la partie 9.5.2). Ces évaluations doivent être terminées avant l’expiration du délai d'évaluation prescrit (consulter la partie 1.5.1); elles peuvent avoir pour effet de déterminer notamment :
- qu’une substance n’est pas toxique ni potentiellement toxique;
- qu’une substance est toxique ou potentiellement toxique, ce qui peut rendre nécessaire :
- l’application de conditions visant à limiter la manière dont le déclarant peut fabriquer ou importer cette substance;
- l’interdiction de la fabrication ou de l’importation de cette substance;
- l’interdiction de la fabrication ou de l’importation de cette substance à la personne visée jusqu’à la présentation et l’évaluation des renseignements supplémentaires jugés nécessaires;
- qu’une substance est soupçonnée de devenir toxique à la suite d’une nouvelle activité. Dans ce cas, un avis de NAc sera émis pour cette substance.
1.4 Qui est tenu de faire une déclaration?
Au sens du Règlement et de l’article 81 de la Loi, toute personne (individu ou entreprise) qui fabrique ou importe une substance nouvelle au Canada (le déclarant) doit présenter une DSN au Programme des SN (consulter aussi la partie 1.4.2). Ce dossier doit contenir tous les renseignements exigés par le Règlement.
Le déclarant est tenu de se conformer au Règlement et il doit soumettre la DSN requise correspondant aux quantités fabriquées ou importées. Le déclarant doit fournir l’information dans le formulaire de DSN (consulter la partie 6).
En signant l’attestation (case A.1.1) du formulaire de DSN, le déclarant accepte toutes les autres responsabilités découlant de l’observation de la Loi, incluant le dépôt des annexes subséquentes qui pourraient être exigées et le paiement des droits appropriés. Le déclarant devra conserver tous les renseignements et les données à l’appui pour une période de 5 ans, conformément à l’article 13 du Règlement.
1.4.1 Transfert des décisions relatives à une déclaration – Formulaire d’attestation – Interprétation de personne
Le paragraphe 81(5) de la Loi précise les règles de succession dans le cas de transfert de certains droits relatifs aux substances visées par l’article 81 de la Loi.
Avant le transfert de propriété, les successeurs auxquels le paragraphe 81(5) s’applique devront signer un formulaire d’attestation s’ils souhaitent profiter des décisions préalables au changement de propriétaire. Cela inclut les entreprises qui changent de nom. Ce formulaire indique le transfert du déclarant original au successeur, des droits ou des privilèges découlant des renseignements fournis pour une substance.
On peut obtenir le Formulaire d’attestation pour l’interprétation de personne sur le site Web du Programme des SN ou en communiquant avec la Ligne d’information de la gestion des substances.
Les formulaires d’attestation doivent être signés par un mandataire autorisé du successeur et doivent désigner toutes les DSN faisant l’objet d’un transfert de propriété.
Cette disposition permet aux successeurs de continuer à fabriquer ou à importer une substance nouvelle sans devoir soumettre une nouvelle déclaration et attendre l’expiration du délai d'évaluation.
1.4.2 Agent canadien – paragraphe 14(3) du Règlement
Si le déclarant qui présente la DSN n’est pas un résident canadien, il devra, en vertu de l’alinéa 14(1)b) du Règlement, désigner un résident du Canada autorisé à agir en son nom à titre d’ « agent canadien ». Le Programme des SN enverra tous les avis et la correspondance à l’ « agent canadien ». En application de l’article 13 du Règlement, ce dernier doit aussi conserver tous les renseignements et les données à l’appui pendant 5 ans après la fin de l’année de leur communication.
À titre d’exemple, un déclarant qui n’est pas un résident canadien, mais qui possède le « statut d’importateur canadien » pour la substance importée et qui est l’importateur officiel figurant sur la Déclaration en détail commerciale de l’Agence des services frontaliers du Canada, doit nommer un résident du Canada autorisé à agir en son nom à titre d’ « agent canadien ».
L’ « agent canadien » doit s’assurer de l’exactitude et de l’exhaustivité des renseignements présentés dans la DSN.
Veuillez noter que l’ « agent canadien » ne peut être l’importateur de la substance nouvelle. Si l’ « agent canadien » importe directement la substance et la revend, la reconditionne, la distribue, etc., à partir de ses locaux au Canada, il est l’importateur officiel inscrit au dossier. Aussi faut-il remplir une DSN qui désigne cette personne comme déclarant à la case A.2 (consulter la partie 6.2.2) et non comme « agent canadien ». Dans ce cas, la case A.4 doit être laissée vide. Le Tiers fournisseur de renseignements doit être identifié dans la case A.5 si cette personne fournit des renseignements confidentiels exclusifs pour remplir la DSN (consulter la partie 6.2.5).
1.4.3 Fabricant en sous-traitance
On parle de fabrication en sous-traitance lorsqu’une entreprise engage un fabricant pour transformer sa matière première pour créer une substance nouvelle. Tout au long des activités, la propriété de la matière première et de la substance qui en résulte demeure celle de l’entreprise contractante. L’entreprise contractante est désignée comme le déclarant des substances nouvelles fabriquées moyennant une redevance. De plus, si des mesures sont prises suite à l’évaluation, le déclarant devra en informer le fabricant en sous-traitance et le fabricant sera responsable de s’y conformer.
1.5 Quand faut-il déposer une Déclaration de substances nouvelles au Programme des substances nouvelles?
Le moment du dépôt d’une DSN dépend du groupe de déclaration (le délai d'évaluation prescrit selon l’annexe appropriée) et de la date à laquelle la quantité prescrite (quantité seuil) selon l’annexe requise sera probablement dépassée.
1.5.1 Périodes d’évaluation pour les Déclarations de substances nouvelles
Les périodes d’évaluation vont de 5 à 75 jours civils en fonction du type et de la quantité de substance fabriquée ou importée (consulter la partie 4). La DSN devra être présentée au minimum un nombre de jour correspondant au délai d'évaluation prescrit et avant le dépassement de la quantité seuil. Par exemple, une déclaration pour l’annexe 9 devra être présentée au minimum 30 jours avant de dépasser 1 000 kg/année. Les détails pour les périodes d’évaluation figurent dans le tableau 1-1.
| Annexea | Classe | Délai d’évaluation (jour) | Quantités annuelles (kg) |
|---|---|---|---|
| Ann. 1 – Catégorie spécialeb (figurent sur la Liste extérieure ou non) | Substances chimiques | 30 | 1 000 |
| Ann. 1 – Catégorie spéciale (mise à jour des renseignements) | Substances chimiques | 30 | 10 000 |
| Ann. 3 – Catégorie spéciale (figurent sur la Liste extérieure ou non) | Polymères | 30 | 10 000 |
| Ann. 4 – Ne figurent pas sur la Liste extérieure | Substances chimiques | 5 | 100 |
| Ann. 4 – Figurent sur la Liste extérieure | Substances chimiques | 30 | 1 000 |
| Ann. 5 – Ne figurent pas sur la Liste extérieure | Substances chimiques | 60 | 1 000 |
| Ann. 5 – Figurent sur la Liste extérieure | Substances chimiques | 60 | 10 000 |
| Ann. 5 – Figurent sur la Liste extérieure (rejetée en dans l’environnement en grande quantité ou degré d’exposition du public élevéc) | Substances chimiques | 75 | 50 000 |
| Ann. 6 – Ne figurent pas sur la Liste extérieure | Substances chimiques | 75 | 10 000 |
| Ann. 9 – Tous les polymères | Polymères | 30 | 1 000 |
| Ann. 10 – Polymères non-ERRd figurant sur la Liste extérieure ou dont tous les réactifs figurent sur la Liste intérieure ou sur la Liste extérieure | Polymères | 60 | 10 000 |
| Ann. 10 – Polymères non-ERR figurant sur la Liste extérieure ou dont tous les réactifs figurent sur la Liste intérieure ou sur la Liste extérieure – rejeté dans l’environnement en grande quantité ou degré d’exposition du public élevé | Polymères | 60 | 50 000 |
| Ann. 11 – Polymères non-ERR ne figurant pas sur la Liste extérieure et dont les réactifs ne figurent pas tous sur la Liste intérieure ou la Liste extérieure | Polymères | 60 | 10 000 |
a Des renseignements supplémentaires sont exigés au titre de l’annexe 2 si toute substance faisant l’objet d’une demande est une substance biochimique ou un biopolymère (consulter les parties 4.2 à 4.9).
b Les catégories spéciales comprennent les substances destinées à la recherche et au développement, les substances confinées intermédiaires limitées au site et les substances confinées destinées à l’exportation (consulter la partie 4.2).
c Il peut y avoir un délai d'évaluation supplémentaire pour les substances dont la quantité dépasse les 50 000 kg/année si l’un des critères suivants s’applique : rejets prévus dépassant 3 kg/jour dans l’environnement aquatique après le traitement des eaux usées ou le degré d’exposition du public est élevé (consulter la partie 4.4.3 ou 4.9.2). Si aucun de ces critères ne s’applique, les exigences finales sont celles de l’annexe 5 ou de l’annexe 10.
d Polymères non-ERR s’entend de polymères qui ne sont pas des polymères à exigences réglementaires réduites (consulter la partie 3.3.1.6).
1.5.2 Droits pour les déclarations de substances nouvelles
Le Règlement sur les droits concernant les substances nouvelles (RDSN) a été adopté pour incorporer les droits exigés pour la plupart des DSN présentées en application du Règlement. Le montant des droits exigés dépend des ventes annuelles du déclarant au Canada, de l’annexe visée par la déclaration, et des autres services demandés, le cas échéant (par exemple, des recherches confidentielles dans la Liste intérieure ou la Liste extérieure ou encore une demande de dénomination maquillée). La page Web des Droits pour les déclarations de substances nouvelles énumère les tarifs correspondant aux différents degrés de service. Des renseignements supplémentaires sont disponibles dans le RDSN.
Les déclarants dont les entreprises satisfont aux critères établis pour les petites ou moyennes entreprises (consulter la page Web des Droits pour les déclarations de substances nouvelles) ou qui satisfont aux conditions des déclarations concordantes ou consolidées décrites aux parties 5.1 et 5.3 du Document d’orientation, respectivement, peuvent bénéficier de réductions de tarifs.
1.5.3 Substances non visées par des droits de déclaration
Le RDSN ne prescrit pas de droits pour les substances biochimiques, les biopolymères, les substances destinées à la recherche et au développement ou pour les substances qui sont uniquement destinées à une utilisation dans des produits réglementés aux termes de toute autre loi fédérale, notamment la Loi sur les aliments et drogues (LAD), la Loi sur les pêches et la Loi sur la santé des animaux.
Les droits ne s’appliquent pas aux DNAc (consulter les parties 1.3 et 9.6.2), à la présentation de la mise à jour des renseignements requis au seuil de 10 000 kg/année pour la déclaration de substances chimiques de catégorie spéciale de l’annexe 1 (consulter la partie 4.2.2) et à la présentation de renseignements additionnels requis au seuil de 50 000 kg/année pour les substances qui sont rejetées dans l’environnement aquatique en grande quantité ou auxquelles le degré d’exposition du public est élevée (consulter les parties 4.4.3 et 4.9.2).
1.6 Application de la Loi
S’ils veulent obtenir des renseignements sur l’application de la Loi et du Règlement, les déclarants devraient consulter la Politique d'observation et d'application de la Loi canadienne sur la protection de l'environnement (1999). Cette politique vise à garantir l’application équitable, prévisible et uniforme de la Loi partout au Canada.
Partie 2. Inventaires
2.1 Rôle de la Liste intérieure
Dans le présent Document d’orientation, l’expression « Liste intérieure » comprend les substances figurant autant sur les parties publiques que sur les parties confidentielles de cette liste.
L’appendice 12 du Document d’orientation donne une description complète de chacune des parties de la Liste intérieure.
2.1.1 La Liste intérieure – Définition d’une substance nouvelle
La Liste intérieure est une liste de substances fabriquées ou importées au Canada à l’échelle commerciale. Une substance ne figurant pas sur la Liste intérieure est une substance nouvelle au Canada. La présence d’une substance sur la Liste intérieure est le seul critère qui permet de déterminer si cette substance est nouvelle aux termes de la Loi canadienne sur la protection de l’environnement (1999) [la Loi] et du Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [le Règlement]. Les substances inscrites sur la Liste intérieure portent un numéro d’identification unique (c’est-à-dire, un numéro d’enregistrement du Chemical Abstracts Service [CAS]Note de bas de page 7, un numéro d’identification confidentielle [NIC](consulter la partie 2.1.2) ou un numéro de classification des enzymes [consulter la partie 6.4.2.4]).
Les substances figurant sur la Liste intérieure ne sont pas assujetties aux exigences de déclaration du Règlement. Néanmoins, lorsque l’identifiant d’une substance sur la Liste intérieure est suivi par une mention réglementaire (c’est-à-dire, mention S, mention S prime ou mention P), cette substance est assujettie à des exigences de déclaration selon certaines circonstances (consulter la partie 2.1.4.1). La Liste intérieure inclut la liste originale, publiée le 4 mai 1994 dans la Partie II de la Gazette du Canada, à laquelle il faut intégrer tous les ajouts et radiations publiés subséquemment dans la Partie II de la Gazette du Canada.
2.1.2 Substances confidentielles figurant sur la Liste intérieure
Un déclarant peut demander que la substance qu’il déclare soit inscrite de manière confidentielle sur la Liste intérieure grâce à une dénomination maquillée conforme au Règlement sur les dénominations maquillées (consulter la partie 2.1.2.1). La marche à suivre pour créer la dénomination maquillée d’une substance est expliquée dans la partie 7.2.2 et dans l’appendice 5 du Document d’orientation. Un Tiers fournisseur de renseignements qui demande que les renseignements sur la substance qu’il communique ne soient pas divulgués au déclarant peut également demander à ce que la substance soit inscrite sur une partie confidentielle de la Liste intérieure. Les substances admissibles pour l’inscription sur la Liste intérieure sous une dénomination maquillée se voient attribuer un NIC, même si un numéro d’enregistrement CAS est disponible. Le Programme des substances nouvelles (SN) communiquera ce NIC au déclarant ou au Tiers fournisseur de renseignements. Une fois la substance jugée admissible, le NIC et la dénomination maquillée acceptable pour ladite substance sont publiés dans la Partie II de la Gazette du Canada. Les substances qui figurent sur une partie confidentielle de la Liste intérieure sont traitées de la même façon que celles qui figurent sur une partie publique de la Liste intérieure.
2.1.2.1 Justification pour maquiller l’identité d’une substance
S’il est soutenu que l’identité de la substance déclarée soit considérée confidentielle, on demandera alors au déclarant de fournir une justification pour le traitement confidentiel des renseignements, en outre d’une dénomination maquillée conforme au Règlement sur les dénominations maquillées. Cette justification devrait être sélectionnée à partir des critères suivants :
- L’identité de la substance est un secret industriel de l’auteur de la demande;
- L’identité de la substance est aussi d’une nature financière, commerciale, scientifique ou technique qui est toujours traitée de façon confidentielle par l’auteur de la demande;
- On peut raisonnablement s’attendre à ce que la divulgation de l’identité de la substance entraîne des pertes ou des gains financiers importants ou encore à ce qu’elle soit préjudiciable à la position concurrentielle de l’auteur de la demande;
- On peut raisonnablement s’attendre à ce que la divulgation de l’identité de la substance nuise à des négociations d’ordre contractuel ou autre menées par l’auteur de la demande.
La justification à fournir doit aussi inclure les renseignements visés à la partie 7.2.2 du Document d’orientation. Advenant que les pièces justificatives soient jugées insuffisantes selon les critères de justification, le déclarant sera informé que le Programme des SN envisage d’inscrire le numéro d’enregistrement CAS approprié (consulter la partie 6.2.16). Avant la publication de l’information, le déclarant aura la possibilité de faire appel de cette décision.
Le paragraphe 315(1) de la Loi précise que le ministre de l’Environnement (le ministre) peut toutefois divulguer des renseignements si :
- a) d’une part, leur communication est dans l’intérêt de la santé ou de la sécurité publiques ou de la protection de l’environnement;
- b) d’autre part, cet intérêt l’emporte clairement sur les pertes financières importantes pouvant en découler ou le préjudice porté à la position concurrentielle de l’intéressé — la personne qui les a fournis ou au nom de qui ils l’ont été — et sur le préjudice causé à la vie privée, la réputation ou la dignité de toute personne.
2.1.3 Modifications de la Liste intérieure
Suivant les exigences de la Loi, la Liste intérieure est modifiée de temps à autre pour les raisons suivantes :
- La proposition d’inscrire sur la Liste intérieure une substance qui a été fabriquée ou importée au Canada entre le 1er janvier 1984 et le 31 décembre 1986 [paragraphe 66(1) de la Loi];
- Tous les renseignements prescrits et tous les renseignements additionnels ainsi que les résultats d’essais ont été présentés au ministre; le ministre de l’Environnement et le ministre de la Santé sont convaincus que la substance a été fabriquée ou importée au Canada par la personne qui a fourni les renseignements, une évaluation de la substance a été effectuée aux termes de l’article 83 et aucune condition imposée par le ministre selon l’alinéa 84(1)a) concernant la fabrication ou l’importation de la substance n’est en vigueur [paragraphe 87(1) ou 87(5) de la Loi];
- Pour tenir à jour la liste, par exemple en corrigeant une coquille dans l’identifiant d’une substance [paragraphe 66(1) de la Loi].
Les modifications sur la Liste intérieure sont publiées dans la Partie II de la Gazette du Canada toutes les 6 à 8 semaines environ.
Pour obtenir des renseignements supplémentaires concernant les exigences d’admissibilité pour l’inscription de substances sur la Liste intérieure, consulter la partie 10.2.1 du Document d’orientation.
2.1.3.1 Proposition d’inscrire une substance sur la Liste intérieure
Toute substance (substances chimiques et biochimiques, nanomatériaux, polymères et biopolymères) est éligible pour une proposition d’inscription sur la Liste intérieure si elle a été, entre le 1er janvier 1984 et le 31 décembre 1986, soit fabriqué ou importé au Canada en une quantité d'au moins 100 kg au cours d'une année civile, soit commercialisé ou utilisé à des fins de fabrication commerciale au Canada. Pour proposer d’inscrire une substance, il faut fournir le Formulaire de proposition d’inscription – Liste intérieure au Programme des SN avec la documentation applicable qui permet d’établir qu’une substance répond aux exigences mentionnées ci-dessus (c’est-à-dire les dossiers de vente, d’achat, de production/fabrication et d’importation). Les substances éligibles peuvent être inscrites sur la partie publique ou confidentielle de la Liste intérieure.
De plus amples instructions pour la proposition d’inscrire une substance sur la Liste intérieure figurent sur le formulaire de proposition d’inscription. On peut obtenir le Formulaire de proposition d’inscription – Liste intérieure sur le site Web du Programme des SN ou en s’adressant à la Ligne d’information de la gestion des substances. Il n’y a pas d’échéance réglementaire concernant l’inscription de substances sur la Liste intérieure suivant la présentation d’un formulaire de proposition d’inscription.
On n’exige pas de droits pour la proposition d’inscrire une substance sur la Liste intérieure mais des droits sont exigés pour une demande de dénomination maquillée (consulter le tableau des frais à la page Web des Droits pour les déclarations de substances nouvelles) lorsque des substances sont inscrites sur une partie confidentielle de la Liste intérieure.
2.1.4 Mentions présentes sur la Liste intérieure
La Liste intérieure comporte 5 mentions différentes pour les substances et selon la situation, certaines mentions peuvent être associées. Certaines mentions servent à des fins de suivi gouvernemental et d’autres indiquent que des exigences de déclarations pourraient s’appliquer. Il incombe au déclarant d’identifier et de se conformer aux obligations résultant de toutes mentions ou règlements s’appliquant à une substance.
2.1.4.1 Mentions réglementaires
Les 3 mentions réglementaires ci-dessous indiquent aux déclarants qu’il pourrait être nécessaire de s’acquitter d’exigences de déclaration avant de fabriquer, d’importer ou d’utiliser la substance.
Mention « S »
La lettre « S » après un numéro d’identification de substance indique qu’elle est visée par le paragraphe 81(3) de la Loi. Elle désigne une substance nouvelle dont l’évaluation effectuée conformément à l’article 83 de la Loi a déterminé qu’une nouvelle activité liée à la substance pourrait faire en sorte que celle-ci soit considérée toxique au sens de la Loi. La mention « S » s’ajoute au moment de l’inscription de la substance sur la Liste intérieure.
Mention « S′ » (S prime)
La lettre « S′ » après un numéro d’identification de substance indique que le paragraphe 81(3) de la Loi s’applique à cette substance. Elle désigne une substance dont l’évaluation effectuée conformément aux articles de la Loi, tels que les articles 68 ou 74, a déterminé qu’une nouvelle activité liée à la substance pourrait faire en sorte que celle-ci soit considérée toxique au sens de la Loi. La mention « S′ » modifie et met à jour le numéro d’identification de la substance dans la Liste intérieure.
Le but des mentions « S » et « S′ » est d’indiquer que des renseignements concernant la substance désignée doivent être déclarés si une nouvelle activité utilisant la substance est proposée. Toute personne qui considère d’entreprendre une nouvelle activité en lien avec la substance doit fournir les renseignements prescrits au ministre dans le délai prévu avant le début de la nouvelle activité proposée. Ces nouveaux renseignements permettront au Programme des SN d’évaluer les risques pour l’environnement et la santé humaine découlant de la nouvelle activité, de modifier les exigences relatives aux NAc ou, au besoin, de mettre en œuvre d’autres mesures de gestion des risques (consulter la partie 9.6.2).
Pour obtenir la liste complète de toutes les substances faisant l’objet d’exigences relatives aux NAc, veuillez consulter les Publications relatives aux nouvelles activités en vertu de la Loi canadienne sur la protection de l’environnement (1999).
Mention « P »
La lettre « P » après un numéro d’identification de substance indique qu’elle était visée par les paragraphes 81(1) ou 81(2) de la Loi, a fait l’objet d’une évaluation et a été inscrite sur la Liste intérieure parce qu’elle satisfait aux critères établis pour les polymères à exigences réglementaires réduites (ERR) (consulter la partie 3.3.1.5).
Le but de la mention « P » est d’indiquer que toute personne qui prévoit fabriquer le polymère ou l’importer au Canada sous une forme qui n’est plus considérée comme un polymère ERR au-delà des quantités prescrites doit présenter une Déclaration de substances nouvelles (DSN). Celle-ci devra inclure les renseignements de l’annexe applicable du Règlement concernant un polymère qui n’est pas un polymère à exigences réglementaires réduites (non-ERR). Par souci de clarté, cette obligation s’applique aussi au déclarant initial du polymère.
Dans le cas où le Programme des SN évalue une substance faisant l’objet d’une nouvelle déclaration et conclue que rien n’indique que le polymère non-ERR pourrait être toxique et qu’il est à nouveau admissible sur la Liste intérieure, cette dernière sera modifiée en conséquence et la mention « P » supprimée. Si le Programme des SN évalue le polymère non-ERR et conclut qu’il y a lieu de soupçonner qu’il soit toxique, il prendra des mesures appropriées (consulter la partie 9.6) après l’évaluation.
2.1.4.2 Mentions administratives
Le Programme des SN utilise les 2 mentions administratives suivantes pour l’identification de substances inscrites sur la Liste intérieure selon des scénarios spécifiques.
Mention « T »
La lettre « T » suivant un numéro d’identification de substance indique que celle-ci était fabriquée ou importée au Canada pendant la période transitoire (du 1er janvier 1987 au 1er juillet 1994) et qu’en vertu du paragraphe 81(2) de la Loi, le déclarant a fourni les renseignements prescrits au Programme des SN qui a évalué la substance conformément à l’article 83 de ladite Loi.
Mention « N »
La lettre « N » suivant un numéro d’identification de substance indique que la substance a été inscrite sur la Liste intérieure en se basant sur le fait que celle-ci a été fabriquée ou importée après le 1er juillet 1994 et qu’en vertu du paragraphe 81(1) de la Loi, le déclarant a fourni les renseignements prescrits au ministre, qui les a évalués conformément à l’article 83 de ladite Loi.
S’il n’existe aucune mention associée à une substance qui figure sur la Liste intérieure, la substance a été inscrite sur la liste selon une proposition de substance aux termes de l’article 66 de la Loi (consulter la partie 2.1.3).
2.2 Rôle de la Liste extérieure
2.2.1 La Liste extérieure
Dans le Document d’orientation, l’expression « Liste extérieure » comprend les substances figurant autant sur les parties publiques que sur les parties confidentielles de cette liste.
La Liste extérieure est une liste de substances qui ne sont pas utilisées commercialement au Canada au-dessus des quantités seuils énoncées dans le Règlement mais qui sont utilisés commercialement à l’extérieur du Canada. Les substances inscrites sur la Liste extérieure sont assujetties aux exigences de déclarations du Règlement. Toutefois, les exigences en matière de renseignements sont moindres que pour les substances qui ne figurent pas sur la Liste extérieure.
Pour obtenir une description complète de chacune des parties de la Liste extérieure, veuillez consulter l’appendice 12 du Document d’orientation.
2.2.2 Substances confidentielles figurant sur la Liste extérieure
La Liste extérieure comprend des substances dont leur identité est maquillée pour protéger les Renseignements commerciaux confidentiels (RCC). Ces substances sont identifiées par leur dénomination maquillée élaborée selon les exigences du Règlement sur les dénominations maquillées et leur NIC attribué par le Programme des SN. Un NIC peut être attribué par le programme même si un numéro d’enregistrement CAS est disponible pour la substance. Une substance qui figure sur la Liste extérieure sous une dénomination maquillée est traitée de la même façon qu’une substance qui y figure sous une dénomination explicite. Pour cette raison, elle est assujettie à moins d’exigences en matière de renseignements en comparaison aux substances ne figurant pas sur la Liste extérieure. Lors des déclarations subséquentes, le NIC devrait être utilisé pour désigner la substance s’il est connu.
2.2.3 Modifications sur la Liste extérieure
La Liste extérieure est modifiée sur une base régulière pour les raisons suivantes :
- En conséquence des modifications sur la Liste intérieure (les substances inscrites sur la Liste intérieure sont radiées de la Liste extérieure lorsqu’elles y figuraient);
- Pour des mises à jour annuelles selon l’inventaire des substances chimiques de la Toxic Substances Control Act (TSCA) de l’Agence de protection environnementale des États-Unis (United States Environmental Protection Agency - US EPA);
- Suite à une proposition d’inscrire une substance sur la Liste extérieure avec la présentation du formulaire : Formulaire de proposition d’inscription – Liste extérieure;
- Pour tenir à jour la liste, par exemple en corrigeant une coquille dans l’identifiant d’une substance.
Les modifications sur la Liste extérieure sont publiées dans la Partie I de la Gazette du Canada toutes les 6 à 8 semaines environ. Il n’y a pas d’échéance réglementaire pour les modifications sur la Liste extérieure, incluant les mises à jour annuelles ou la présentation d’un formulaire de proposition d’inscription.
2.2.3.1 Mises à jour basées sur l’inventaire des substances chimiques de la TSCA de l’US EPA
La Liste extérieure est modifiée annuellement pour y inscrire des substances qui figurent sur la partie publique de l’inventaire de la TSCA de l’US EPA depuis au moins un an. Les substances figurant sur la partie confidentielle de l’inventaire de la TSCA de l’US EPA ne sont pas inscrites automatiquement sur la Liste extérieure lors des mises à jour annuelles. Toutefois, il est possible de proposer l’inscription de ces substances (consulter la partie 2.2.3.2).
Certaines substances figurant sur l’inventaire de la TSCA ne sont pas inscrites sur la Liste extérieure. Cela inclut les substances visées par des mesures de gestion des risques au Canada ou aux États-Unis ainsi que les substances visées par la Convention de Stockholm sur les polluants organiques persistants ou à la Convention de Rotterdam sur la procédure de consentement préalable en connaissance de cause applicable dans le cas de certains produits chimiques et pesticides dangereux qui font l’objet du commerce international. Lorsqu’il est établi qu’une substance figurant sur la Liste extérieure pourrait devenir préoccupante (par exemple lorsqu’elle est visée par de telles mesures de gestion des risques), cette substance peut être radiée de la Liste extérieure suivant une consultation publique.
2.2.3.2 Proposition d’inscrire une substance sur la Liste extérieure
Toute substance qui a figuré sur l’inventaire de la TSCA de l’US EPA pendant au moins une année est éligible pour une proposition d’inscription sur la Liste extérieure. Cela inclut aussi les substances figurant sur la partie confidentielle de l’inventaire de la TSCA de l’US EPA. Pour proposer d’inscrire une substance, il faut fournir le Formulaire de proposition d’inscription – Liste extérieure au Programme des SN avec la documentation applicable qui démontre que la substance a figuré sur l’inventaire de la TSCA de l’US EPA pendant au moins une année. Les substances éligibles peuvent être inscrites sur la partie publique ou confidentielle de la Liste extérieure et sont inscrites lors des mises à jour annuelles de la Liste extérieure.
Pour proposer d’inscrire une substance sur la partie confidentielle de la Liste extérieure, le formulaire de proposition d’inscription doit inclure une dénomination maquillée proposée et les droits exigés pour une demande de dénomination maquillée (consulter le tableau des frais à la page Web des Droits pour les déclarations de substances nouvelles). La personne qui a fourni la proposition d’inscription sur la partie confidentielle sera aussi tenu de fournir une justification pour la demande confidentialité (consulter la partie 2.1.2.1). Si aucune dénomination maquillée n’est fournie, la substance sera inscrite sur la Liste extérieure sous son numéro d’enregistrement CAS.
De plus amples instructions pour la proposition d’inscrire une substance sur la Liste extérieure figurent sur le formulaire de proposition d’inscription. On peut obtenir le Formulaire de proposition d’inscription – Liste extérieure sur le site Web du Programme des SN ou en s’adressant à la Ligne d’information de la gestion des substances.
2.3 Recherche de substances dans les inventaires
Pour déterminer si une substance figure sur la Liste intérieure ou sur la Liste extérieure, on peut entrer le nom de la substance, son numéro d’enregistrement CAS, son NIC (s’il est connu) ou son numéro de classification des enzymes (Union internationale de biochimie et de biologie moléculaire [UIBBM]) dans le Moteur de recherche de substances.
Si le NIC est inconnu et si le déclarant veut savoir si une substance figure sur la partie confidentielle de la Liste intérieure ou de la Liste extérieure, il doit envoyer une demande de recherche dans la partie confidentielle au Programme des SN (consulter la partie 2.3.1). Il peut également envoyer un numéro d’enregistrement CAS ou un NIC directement au CAS, lequel fera des recherches dans tous les inventaires pour cette substance contre rétribution (pour plus de renseignements au sujet du CAS, consulter l’appendice 4).
Il est important de noter que le moteur de recherche n’indique pas les mentions. Il incombe au déclarant de vérifier dans la Gazette du Canada qu’aucune mention n’est associée à une substance particulière. (Pour plus de renseignements au sujet des mentions, consulter la partie 2.1.4).
2.3.1 Demande de recherche dans la partie confidentielle
Les substances figurant sur une partie confidentielle de la Liste intérieure ou de la Liste extérieure sont désignées par un NIC accompagnée d’une dénomination maquillée créée de la façon prescrite par le Règlement sur les dénominations maquillées. Tout déclarant qui souhaite entreprendre la fabrication, l’importation ou l’utilisation d’une substance qu’il suspecte de figurer sur une partie confidentielle de l’une ou l’autre de ces listes peut demander au Programme des SN de confirmer ce statut en lui fournissant le Formulaire de demande de recherche confidentielle disponible sur le site Web du Programme des SN. De plus amples instructions figurent sur le formulaire ou peuvent être demandées en s’adressant à la Ligne d’information de la gestion des substances.
Si un déclarant qui a l’intention d’importer une substance est incapable de fournir tous les renseignements requis parce qu’un Tiers fournisseur de renseignements estime qu’ils sont confidentiels, le déclarant devra s’assurer que le Tiers fournisseur renseignements soumet directement les renseignements confidentiels au Programme des SN.
Lorsqu’un déclarant fourni une demande de recherche dans la partie confidentielle, le Programme des SN fait une recherche dans la partie confidentielle de la Liste intérieure et de la Liste extérieure et, dans les 15 jours suivant la réception de la documentation complète, indique si la substance figure (ou non) sur l’une de ces listes. Veuillez noter que des droits sont exigés pour une demande de recherche dans la partie confidentielle (consulter le tableau des frais à la page Web des Droits pour les déclarations de substances nouvelles).
2.3.2 Exemplaires de la Liste intérieure et de la Liste extérieure
On peut consulter la Liste intérieure et la Liste extérieure en ligne ou en télécharger le contenu au format (.xlsx) en visitant le Moteur de recherche de substances. Les substances chimiques et biochimiques, tout comme les polymères et les biopolymères, sont désignées par leur numéro d’enregistrement CAS alors que les substances biochimiques qui sont des enzymes sont désignées par leur numéro d’enregistrement CAS ou leur numéro de classification des enzymes de l’UIBBM. Les substances confidentielles sont désignées par leur NIC respectif et sont accompagnée d’une dénomination maquillée créée selon la méthode prescrite par le Règlement sur les dénominations maquillées (consulter la partie 7.2.2). Les déclarants devraient consulter régulièrement ces listes puisqu’elles sont modifiées plusieurs fois par année (consulter les parties 2.1.3 et 2.2.3).
Partie 3. Substances
3.1 Définition de « substance »
Aux fins de la réglementation du régime de Déclaration de substances nouvelles, dans l’article 3 de la Loi canadienne sur la protection de l’environnement (1999) [la Loi], une « substance » est définie comme :
toute matière organique ou inorganique, animée ou inanimée, distinguable. La présente définition vise notamment :
- a) les matières susceptibles soit de se disperser dans l’environnement, soit de s’y transformer en matières dispersables, ainsi que les matières susceptibles de provoquer de telles transformations dans l’environnement;
- b) les radicaux libres ou les éléments;
- c) les combinaisons d’éléments à l’identité moléculaire précise soit naturelles, soit consécutives à une réaction chimique;
- d) des combinaisons complexes de molécules différentes, d’origine naturelle ou résultant de réactions chimiques, mais qui ne pourraient se former dans la pratique par la simple combinaison de leurs composants individuels.
Dans certains cas, les matières dérivées d’une source naturelle ou d’une réaction complexe peuvent être considérées comme des substances simples aux fins de déclaration. Ces matières sont communément appelées des substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques; elles sont souvent désignées par l’acronyme « UVCB » (pour substances of Unknown or Variable composition, Complex reaction products or Biological materials) (consulter la partie 3.3.1.3)
3.2 Substances non assujetties aux exigences de déclaration
Les exigences de déclaration aux terme du Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [le Règlement] ne s’appliquent pas aux substances visées aux parties 3.2.1 à 3.2.11 du Document d’orientation.
3.2.1 Mélanges
Selon le paragraphe 3(1) de la Loi,
les mélanges combinant des substances et ne produisant pas eux-mêmes une substance différente de celles qui ont été combinées
ne sont pas couverts par la définition statutaire d’une substance nouvelle aux fins des dispositions de la Loi relatives aux substances nouvelles et aux Nouvelles activités (NAc) et, par conséquent, il n’est pas obligatoire de les déclarer.
Note : Si un constituant quelconque d’un mélange est une substance nouvelle, il est assujetti à une déclaration.
Note : Certains mélanges qui proviennent de sources naturelles ou de réactions complexes sont considérées être des substances simples qu’il peut être obligatoire de déclarer (par exemple les UVCB, consulter la partie 3.3.1.3).
Les mélanges tels que ceux décrits ci-dessous sont des exemples de mélanges qui ne sont pas assujetties aux exigences de déclaration.
Hydrates
Les hydrates d’une substance ou les ions hydratés formés par l’association d’une substance avec de l’eau sont considérés comme un mélange de cette substance avec de l’eau. Donc, si la forme anhydre d’une substance figure sur la Liste intérieure, aucune de ses formes hydratées ne constitue une substance à déclaration obligatoire. Par exemple, le carbonate de magnésium (ou magnésite, numéro d’enregistrement du Chemical Abstracts Service [CAS] 546-93-0) est une substance anhydre qui figure sur la Liste intérieure et donc sa forme hydratée MgCO3·nH2O ne doit pas être déclarée.
Note : Les hydroxydes métalliques, souvent nommés hydrates de métaux, ne contiennent pas d’eau d’hydratation et, pour cette raison, ils ne sont pas considérés comme des hydrates aux fins de la déclaration. Il faut ainsi déclarer ces substances si elles ne figurent pas sur la Liste intérieure. L’hydroxyde de cuivre, Cu(OH)2 constitue un exemple d’hydroxyde métallique.
Alliages homogènes ou hétérogènes
Les alliages homogènes et hétérogènes sont considérés être des mélanges et, ainsi, ils ne devraient pas être déclarés. Les alliages qui sont des mélanges liquides ou solides de 2 ou plusieurs métaux ou sont des mélanges d’un ou plusieurs métaux avec certains éléments non métalliques (par exemple certains aciers au carbone) sont considérés comme des mélanges et, ainsi, leur déclaration n’est pas obligatoire. C’est le cas, par exemple, de l’alliage homogène du cuivre, composé avec zinc (CuZn), et de l’alliage hétérogène du cuivre, composé avec cobalt (CuCo).
Note : Les composés intermétalliques dont la stœchiométrie est bien définie ne sont pas considérés comme des alliages et doivent être déclarés. C’est le cas, par exemple, du composé intermétallique d’étain In–49Sn.
3.2.2 Articles manufacturés
Selon le paragraphe 3(1) de la Loi,
les articles manufacturés dotés d’une forme ou de caractéristiques matérielles précises pendant leur fabrication et qui ont, pour leur utilisation finale, une ou plusieurs fonctions en dépendant en tout ou en partie
ne sont pas couverts par la définition statutaire d’une substance nouvelle aux fins des dispositions de la Loi relatives aux substances nouvelles et aux NAc et, par conséquent, il n’est pas obligatoire de les déclarer.
Pour ces matières, la forme décrit la macrostructure, c’est-à-dire la structure tridimensionnelle physique de l’article final. Les vêtements, les contenants d’entreposage, les meubles, les carrelages et les fils électriques sont des exemples d’articles dont l’utilisation finale dépend de leur forme finale de fabrication.
Note : Les substances solides auxquelles une forme particulière a été donnée pour satisfaire à des exigences subséquentes de traitement et de fabrication, plutôt que pour leur utilisation finale (par exemple, les lingots de métal et les pastilles de polymère), ne correspondent pas à la définition ci-dessus d’un article manufacturé, et, par conséquent, elles sont assujetties aux exigences de déclaration. Les fluides (par exemple, les gaz, les liquides, les cires, les solutions et les suspensions) et les particules (par exemple, les poussières, les poudres, les dispersions, les granulés, les grumeaux, les flocons et les agrégats de taille non spécifiée) ne sont pas considérés comme des articles manufacturés, même si l’utilité du produit dépend de la forme de la particule.
Les caractéristiques matérielles désignent l’organisation ou la disposition des composants solides au sein de la macrostructure (par exemple, le mode de tissage de tissus et de tapis, la disposition des couches dans une feuille de contreplaqué, le type d’encollage des fibres de papier) qui n’est pas altérée par un traitement subséquent. Par exemple, un tissu conserve ses caractéristiques matérielles finales peu importe s’il s’agit d’un rouleau de tissu ou d’un vêtement, puisque la fabrication du vêtement ne modifie pas les caractéristiques matérielles (ou mode de tissage) de ce tissu.
Les substances dont le rejet depuis un article manufacturé n’est pas prévu pendant son utilisation normale font partie intégrante de celui-ci et, par conséquent, elles ne sont pas assujetties aux exigences de déclaration.
Note : S’il est prévu qu’une substance soit rejetée d’un article manufacturé, elle peut être assujettie aux exigences de déclaration. Le rejet d’une substance depuis un article manufacturé est considéré être prévu lorsqu’il survient pendant l’utilisation de l’article manufacturé et que le rejet contribue à une fonction de l’article manufacturé. Le transfert de substances d’un article manufacturé vers un récipient d’entreposage lors d’un entretien n’est pas considéré comme un rejet qui contribue au fonctionnement de l’article.
| Exemple | Article manufacturé (non assujetti aux exigences de déclaration) | Substance dont le rejet depuis un article manufacturé est prévu (assujetti aux exigences de déclaration) |
|---|---|---|
| 1 | Assainisseur d’air électrique | Substances diffusées à partir d’un assainisseur d’air, comme les fragrances et les solvants |
| 2 | Lingettes d’hygiène personnelle | Substances libérées par les lingettes, comme les surfactants et les parfums |
| 3 | Produit déodorant ou antisudorifique | Substances libérées par le produit déodorant ou antisudorifique, comme les antimicrobiens, les chélateurs, les propulseurs, les parfums |
| 4 | Outils d’écriture (par exemple stylos, marqueurs à essuyage à sec) | Substances libérées par l’outil d’écriture (composants de l’encre) comme les pigments, les colorants, les agents de solubilisation, les parfums |
| 5 | Cartouche d’encre d’imprimante | Substances libérées par la cartouche (composants de l’encre ou du toner) comme les agents antistatiques et les pigments |
| 6 | Assouplissant en feuilles | Substances libérées pendant l’utilisation, comme les parfums et les substances antistatiques |
| 7 | Seringue préremplie | Substances injectées par la seringue comme les ingrédients actifs pharmaceutiques et les ingrédients non actifs |
| 8 | Contenant ou distributeur de Rouge à lèvres | Substances libérées par le contenant ou le distributeur de rouge à lèvres comme les pigments et les émollients |
| 9 | Véhicule à moteur | Substances destinées à être rejetées, comme les substances dans le liquide lave-glace |
| Exemple | Article manufacturé (non assujetti aux exigences de déclaration) | Rejet non intentionnel d’une substance depuis l’article manufacturé (non assujetti aux exigences de déclaration) |
|---|---|---|
| 1 | Appareils électroniques (par exemple ordinateur) | Substances comme les produits ignifuges qui ne sont pas censées être rejetées du boîtier de l’appareil (tout rejet d’une telle substance ne contribuerait pas au fonctionnement de l’article) |
| 2 | Textiles (par exemple tapis, serviettes, vêtements) | Substances comme les antitaches et les teintures qui ne sont pas censées être rejetées du textile (tout rejet d’une telle substance ne contribuerait pas au fonctionnement de l’article) |
| 3 | Véhicule à moteur | Substances comme les lubrifiants et les antioxydants dans l’huile du carter de moteur qui ne sont pas censées être rejetées du véhicule à moteur (tout rejet d’une telle substance ne contribuerait pas au fonctionnement de l’article). Le transfert de substances du véhicule aux récipients d’entreposage lors d’un entretien, par exemple., un changement d’huile, n’est pas considéré comme un rejet qui contribue au fonctionnement de l’article. |
3.2.3 Déchets
Selon le paragraphe 3(1) de la Loi,
les matières animées ou les mélanges complexes de molécules différentes qui sont contenus dans les effluents, les émissions ou les déchets attribuables à des travaux, des entreprises ou des activités
ne sont pas couverts par la définition statutaire d’une substance nouvelle aux fins des dispositions de la Loi relatives aux substances nouvelles et aux NAc et, par conséquent, il n’est pas obligatoire de les déclarer.
Note : Si une matière décrite ci-dessus est isolée et commercialisée, et que la substance résultante ne figure pas sur la Liste intérieure, celle-ci peut être assujettie aux exigences de déclaration en vertu du Règlement.
3.2.4 Autres lois du Parlement
Selon l’alinéa 81(6)a) de la Loi et le paragraphe 3(1) du Règlement, le Règlement et les dispositions de la Loi relatives aux NAc ne s’appliquent pas
à une substance fabriquée ou importée en vue d’une utilisation réglementée aux termes de toute autre loi fédérale qui prévoit un préavis de fabrication, d’importation ou de vente et une évaluation en vue de déterminer si elle est effectivement ou potentiellement toxique.
Par conséquent, il n’est pas obligatoire de déclarer une substance qui est fabriquée ou importée pour une utilisation réglementée par tout autre règlement ou loi du Parlement qui figure sur la liste de l’annexe 2 de la Loi.
Note : Les substances non visés par d’autres règlements ou lois du Parlement énumérés à l’annexe 2 de la Loi peuvent faire l’objet d’une déclaration. Il s’agit notamment de composés intermédiaires isolés, de matières premières et d’autres produits de départ utilisés dans la fabrication de toute substance nouvelle.
Les déclarants de substances nouvelles destinées à des utilisations réglementées par d’autres règlements ou lois du Parlement devraient faire un suivi des sites Web du gouvernement fédéral [Registre de la Loi canadienne sur la protection de l’environnement (1999)] et de la Gazette du Canada afin de déterminer si l’utilisation d’une substance est toujours assujettie à ces autres règlements ou lois du Parlement. Par exemple, la Loi sur les aliments et drogues (LAD) n’est pas énumérée à l’annexe 2 de la Loi canadienne sur la protection de l’environnement (1999) et, par conséquent, les substances nouvelles qui sont destinées à être utilisées dans un produit réglementé par la LAD peuvent être assujetties aux exigences de déclaration du Règlement.
Les substances pour lesquelles certaines utilisations peuvent être assujetties à plus d’un règlement ou d’une loi du Parlement doivent être conformes aux exigences de chacun d’entre eux. Par exemple, une substance utilisée dans un pesticide réglementé en vertu de la Loi sur les produits antiparasitaires peut aussi avoir des applications autres que pesticides qui peuvent être assujetties à la Loi et au Règlement.
3.2.5 Intermédiaires de réaction non isolés
Selon l’alinéa 81(6)b) de la Loi, le Règlement et les dispositions de la Loi relatives aux NAc ne s’appliquent pas
aux intermédiaires de réaction non isolés et non susceptibles d’être rejetés dans l’environnement.
Par conséquent, il n’est pas obligatoire de les déclarer.
Les intermédiaires de réaction sont des substances produites lors d’une séquence de réactions chimiques conduisant des composés de départ au produit final et qui :
- sont contenues dans un réacteur ou un système de production clos (y compris les réservoirs de stockage) situé dans un même bâtiment ou une même zone de traitement;
- sont prévues pour être complètement consommées au cours de la réaction chimique;
- constituent un élément d’un procédé de production ininterrompu (c’est-à-dire qu’à tout moment, les composés de départ ou les intermédiaires de la séquence de réactions sont traités, sauf dans le cas d’un arrêt non prévu);
- ne sont pas susceptibles d’être relâchées dans l’environnement au cours des opérations normales et des mesures sont mises en place afin de réduire au minimum les rejets lors de bris accidentels du système de production clos.
Le Programme des substances nouvelles (SN) conseille aux déclarants de conserver des données techniques (renseignements relatifs au procédé et aux rejets dans l’environnement) afin de justifier qu’une substance est un intermédiaire de réaction non isolé tel que décrit ci-dessus.
3.2.6 Impuretés
Selon l’alinéa 81(6)c) de la Loi, le Règlement et les dispositions de la Loi relatives aux NAc ne s’appliquent pas
aux impuretés, aux contaminants et aux matières ayant subi une réaction partielle et dont la formation est liée à la préparation de la substance.
Par conséquent, il n’est pas obligatoire de les déclarer.
Les impuretés et les contaminants sont des substances que l’on retrouve habituellement en très faibles concentrations dans les produits de départ ou qui sont créées lors des réactions secondaires au cours du procédé de fabrication. Ces substances et produits de départ qui ont réagi partiellement et qui sont présents dans le produit final sont le résultat direct de la préparation; ils ne sont pas nécessaires pour l’utilisation finale du produit, ils n’ont pas été ajoutés volontairement à la substance et n’en augmentent pas la valeur.
3.2.7 Produits de réaction involontaires
Selon l’alinéa 81(6)d) de la Loi, le Règlement et les dispositions de la Loi relatives aux NAc ne s’appliquent pas
aux substances résultant de la réaction chimique subie par une substance dans le cadre de son utilisation ou en raison de leur entreposage ou de facteurs environnementaux.
Par conséquent, il n’est pas obligatoire de les déclarer.
Parmi les exemples de produits de réaction involontaires, on retrouve des substances formées lors de réactions chimiques pendant :
- l’exposition à des agents du milieu ambiant comme l’air, l’humidité, les micro-organismes et la lumière du soleil (les substances produites par des réactions délibérées avec l’eau peuvent être assujetties à une déclaration, par exemple, les hydroxydes métalliques formés par la réaction d’un oxyde métallique et de l’eau);
- l’entreposage (par exemple, la polymérisation partielle des huiles siccatives);
- l’utilisation prévue d’une substance ou d’un mélange (par exemple, des adhésifs, des peintures, des nettoyants, des produits de combustion de carburants, des additifs pour carburants et des adoucisseurs d’eau);
- le mélange d’une formulation, dont le but n’est pas de produire une substance nouvelle et dont les réactions chimiques possibles n’en augmentent pas la valeur (par exemple, si des monomères sont mélangés selon des proportions déterminées pour satisfaire un client, ce mélange ne deviendra pas une substance à déclaration obligatoire, même si cela cause certaines réactions. Toutefois, la fabrication intentionnelle d’un prépolymère pour satisfaire aux spécifications de transformation d’un client peut produire une substance à déclaration obligatoire).
3.2.8 Exemptions pour les substances fabriquées ou importées en faibles quantités
Selon l’alinéa 81(6)e) de la Loi, le Règlement et les dispositions de la Loi relatives aux NAc ne s’appliquent pas
aux substances utilisées, fabriquées ou importées en une quantité n’excédant pas la quantité maximale réglementaire
Par conséquent, il n’est pas obligatoire de les déclarer.
Le Règlement ne s’applique pas aux substances fabriquées ou importées dont la quantité n’excède pas la quantité seuil. Le tableau 1-1 du Document d’orientation énumère les quantités entraînant les exigences de déclaration en vertu du Règlement.
3.2.9 Substances passant par le Canada
Conformément au paragraphe 3(2) du Règlement,
une substance chargée à bord d’un moyen de transport à l’extérieur du Canada et acheminée via le Canada vers un lieu à l’extérieur du Canada, qu’il y ait ou non changement de mode de transport au cours du transit.
Par conséquent, une telle substance n’est pas assujettie aux exigences de déclaration en vertu du Règlement.
Note : Si une substance est importée au Canada et entreposée en vue d’une distribution subséquente, elle peut faire l’objet d’une déclaration.
3.2.10 Polymères figurant sur la Liste intérieure dont les modifications sont égales ou inférieures à 2 % en masse
Dans le cas des polymères figurant sur la Liste intérieure qui sont modifiés par l’ajout de réactifs, mais aucun à plus de 2 % en masse, il n’est pas nécessaire de changer la dénomination explicite de la substance, et celle-ci ne doit donc pas faire l’objet d’une déclaration. Le terme « modification » désigne la quantité de réactif supplémentaire incorporée dans la structure du polymère ou la quantité versée dans la cuve.
Note : Puisque l’on utilise la dénomination explicite de la substance et le numéro d’enregistrement CAS pour identifier une substance donnée, un changement de nom ou de numéro d’enregistrement CAS pourra entraîner l’obligation de déclaration d’une substance.
Dans le cas des biopolymères, le Programme des SN considère que les unités monomères et les réactifs sont des unités répétées au sein de la substance polymérique, lesquelles sont soit produites in situ par un micro-organisme, soit ajoutées dans la cuve de réaction.
3.2.11 Substances existant à l’état naturel
Le Programme des SN considère que les substances existant à l’état naturel ne sont pas assujetties aux exigences de déclaration. Ces substances qui, par définition, existent naturellement sont:
- non traitées;
- traitées uniquement par des procédés manuels, mécaniques ou gravitationnels, par dissolution dans l’eau, par flottation ou par chauffage à la seule fin d’éliminer l’eau;
- extraites de l’air par tout procédé.
Les critères pour les substances existant à l’état naturel limitent l’inclusion aux seules substances dérivées de sources naturelles (incluant la terre, l’eau, l’atmosphère et les formes de vie qui habitent naturellement la Terre) par les moyens spécifiés. L’interprétation de ces critères est littérale et stricte. À titre d’exemple, la distillation n’est pas considérée comme un procédé mécanique et la dissolution dans des solvants autres que l’eau ne correspond pas à cette définition.
3.3 Substances devant faire l’objet d’une déclaration
En vertu de l’article 81 de la Loi, il est obligatoire de déclarer :
- les substances nouvelles au Canada (celles ne figurant pas inscrites sur la Liste intérieure) qui sont fabriquées au Canada ou importées au Canada;
- les substances utilisées pour une nouvelle activité (consulter la partie 9.6).
3.3.1 Classification des substances
Aux fins du Règlement, les substances nouvelles sont regroupées en 2 catégories principales dont chacune comporte des exigences particulières quant à la déclaration de renseignements. Ces catégories sont les substances autres que les polymères (appelées dans le Document d’orientation « substances chimiques et biochimiques ») et les substances polymériques (appelées dans le Document d’orientation « polymères et biopolymères »). Le Document d’orientation précise les exigences de déclaration et les procédés visant les substances chimiques et biochimiques ainsi que les polymères et biopolymères (dont les substances UVCB et les nanomatériaux).
3.3.1.1 Substances chimiques et biochimiques
Les exigences en matière de renseignements pour les substances chimiques et biochimiques sont prescrites par le Règlement et s’appliquent à toutes les substances assujetties aux exigences de déclaration, qui ne sont ni des polymères ni des organismes vivants. Le terme « biochimique » qualifie une substance chimique qui provient d’un micro-organisme, ou qui est une protéine ou un acide nucléique provenant de végétaux ou d’animaux [définition du paragraphe 1(1) du Règlement]. Veuillez noter que les substances chimiques dérivées de végétaux ou d’animaux entiers, ou de parties de ceux-ci, ne sont pas des substances biochimiques aux fins du Règlement. Un exemple de substance biochimique est la subtilisine, une enzyme produite par Bacillus subtilis.
Note : L’organisme servant à la production d’une substance biochimique peut être assujetti au Règlement sur les renseignements concernant les substances nouvelles (organismes) s’il satisfait à la définition d’un organisme vivant énoncé à l’article 104 de la Loi et s’il ne figure pas sur la Liste intérieure.
3.3.1.2 Polymères et biopolymères
Selon la définition du paragraphe 1(1) du Règlement, les polymères sont des substances constituées de :
- a) molécules caractérisées par l’enchaînement d’au moins un type d’unité monomère;
- b) plus de 50 %, en masse, de molécules contenant au moins trois unités monomères liées par covalence à au moins une autre unité monomère ou à un autre réactif;
- c) moins de 50 %, en masse, de molécules de même masse moléculaire;
- d) molécules distribuées à l’intérieur d’un intervalle de masses moléculaires et dont la différence de masse moléculaire est attribuée essentiellement à des différences dans le nombre d’unités monomères.
Le terme « biopolymère » désigne un polymère produit par un micro-organisme, ou désigne une protéine ou un acide nucléique dérivés d’une plante ou d’un animal [définition du paragraphe 1(1) du Règlement]. Veuillez noter que les polymères dérivés de végétaux ou d’animaux entiers, ou de parties de ceux-ci, ne sont pas des biopolymères aux fins du Règlement, et doivent faire l’objet d’une déclaration comme polymères. Dans le cas des biopolymères, les composés monomères et les réactifs sont considérés comme les unités répétées de la substance polymère, lesquels sont produits in situ par le micro-organisme ou ajoutés dans la cuve de réaction. Comme exemple de biopolymère, on peut citer le polysaccharide de type xanthane produit par Xanthomonas camprestris.
Note : L’organisme servant à la production d’un biopolymère peut être assujetti au Règlement sur les renseignements concernant les substances nouvelles (organismes) s’il satisfait à la définition d’un organisme vivant énoncé à l’article 104 de la Loi et s’il ne figure pas sur la Liste intérieure.
3.3.1.3 Substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques
Généralement, les UVCB ont les caractéristiques suivantesNote de bas de page 8 :
- Ils contiennent de nombreuses substances chimiques et ne peuvent pas être représentés par une structure chimique simple ou définis par une formule moléculaire spécifique;
- Ils ne sont pas des mélanges intentionnels de substances chimiques;
- Nombre d’entre eux sont d’origine naturelle (par exemple, le pétrole brut, le charbon, les extraits de plantes, les produits de réaction) et ne peuvent pas être séparés en leurs constituants chimiques;
- Le concept d’« impuretés » ne s’applique habituellement pas aux substances complexes;
- Ils sont souvent produits selon des spécifications des exigences en matière de performance reliées à leurs propriétés physico-chimiques.
Les UVCB sont considérés comme des substances simples aux fins de la déclaration (consulter la partie A3.2 pour des exemples). Les exigences de renseignements prévus pour les substances chimiques s’appliquent aux UVCB, sauf si la substance satisfait aux critères de la définition de polymère.
Note : Par souci de clarté, lorsqu’une substance satisfait aux critères de la définition de polymère, les exigences de renseignements prévus pour les polymères s’appliquent.
3.3.1.4 Substances chimiques à l’échelle nanométrique (ou nanomatériaux)
Le Programme des SN utilise actuellement la Définition ad hoc de nanomatériaux de Santé Canada comme base pour les identifier. Selon cette définition, une substance est considérée être parmi les nanomatériaux s'il s'agit d’une substance fabriquée et :
- si elle est à l'échelle nanométrique, ou dans les limites de celle-ci, dans au moins une dimension externe ou présente une structure interne ou en surface à l'échelle nanométrique; ou,
- si elle est plus petite ou plus grande que l'échelle nanométrique dans toutes les dimensions et affiche un ou plusieurs phénomènes ou propriétés à l'échelle nanométrique.
Aux fins de la présente définition :
- le terme « à l'échelle nanométrique » signifie 1 à 100 nanomètres (nm) inclusivement;
- le terme « propriétés ou phénomènes à l'échelle nanométrique » signifie des propriétés qui sont attribuables à la taille et à aux effets; ces propriétés sont faciles à distinguer des propriétés chimiques ou physiques des atomes, molécules et matériaux particuliers et les matériaux en vrac;
- le terme « fabriqué » comprend les processus d'ingénierie et le contrôle de la matière qui permet la synthèse, la production, la fabrication ou l'isolement de nanomatériaux. Santé Canada pourrait demander des renseignements au sujet d'un nanomatériau fabriqué de façon délibérée ou incidemment à des fins d'évaluation des risques. Ce terme comprend également les composantes naturelles qui ont été utilisées ou mises au point de façon délibérée pour obtenir des propriétés ou des phénomènes à l'échelle nanométrique qui servent à l'encapsulage à l'échelle nanométrique de composantes bioactives ou utilisées pour l'ingénierie tissulaire.
Plus de détails sur ces termes se trouvent dans la définition ad hoc de Santé Canada.
Afin de clarifier la réglementation, le Programme des SN évalue comme nanomatériau toute substance répondant aux critères de la définition ad hoc de nanomatériaux et contenant 10 % ou plus de sa distribution de particules primaires en nombre dans le domaine nanométrique (1 à 100 nm, limite comprise). Le seuil de 10 % (en nombre) est conforme avec les exigences de déclaration utilisées lors du recueil de renseignements sur les nanomatériaux en 2015Note de bas de page 9. Autrement, si la distribution granulométrique en nombre n’est pas disponible, le Programme des SN évalue comme nanomatériau toute substance répondant aux critères de la définition ad hoc de nanomatériaux et dont au moins 1 % (en masse) des particules se situe dans le domaine nanométrique. L’utilisation du seuil de distribution granulométrique de 1 % (en masse) est en accord avec la règle finale de l’Agence de protection environnementale des États-Unis (United States Environmental Protection Agency - US EPA) pour les exigences en matière de rapports et de tenues de registre de la Toxic Substances Control Act (TSCA) pour les nanomatériauxNote de bas de page 10.
Afin que les particules nanométriques de plus petite taille soient mieux représentées, il est aussi recommandé que la distribution granulométrique soit déterminé par comptage plutôt qu’avec la masse ou le volume. L’utilisation d’une seule méthode peut ne pas mener à une représentation complète de la distribution granulométrique. Ainsi, il est recommandé d’utiliser une combinaison de différentes méthodes afin de déterminer la distribution granulométrique générale (consulter l’appendice 10).
La Liste intérieure est la seule base qui peut être utilisée pour déterminer si, aux fins de la Loi, une substance est nouvelle ou non. De ce fait, toutes les substances qui sont fabriquées à l’échelle nanométrique et qui ne figurent pas sur la Liste intérieure sont assujetties aux exigences de déclaration en vertu du Règlement, comme les autres substances qui ne sont pas à l’échelle nanométrique et qui ne figurent pas sur la Liste intérieure.
Les substances figurant sur la Liste intérieure qui peuvent être fabriquées à l’échelle nanométrique ne sont pas assujetties aux exigences de déclaration en vertu du Règlement. Cependant, ces substances sont traitées dans l’Approche à l'égard des formes nanométriques des substances figurant sur la Liste intérieure.
Veuillez consulter l’appendice 10 pour obtenir des renseignements supplémentaires sur les nanomatériaux.
3.3.1.5 Polymères à exigences réglementaires réduites
Les polymères à exigences réglementaires réduites (ERR) sont des polymères qui satisfont à des critères spécifiques sur la masse moléculaire, la teneur en oligomère, la composition élémentaire, la stabilité et les quantités relatives des groupes fonctionnels réactifs et cationiques. Ces critères sont stipulés aux alinéas 9a) à 9 c), ainsi qu’aux articles 1 à 5 de l’annexe 7 du Règlement (consulter l’appendice 2). Les polymères ERR sont assujetties aux exigences de déclaration du Règlement, mais ceux-ci le sont avec moins d’exigences en matière de renseignements que les polymères qui ne sont pas des polymères à exigences réglementaires réduites (non-ERR) [consulter la partie 4.8]. La mention « P » inscrite après l’identifiant d’une substance sur la Liste intérieure (consulter la partie 2.1.4.1) indique que la substance a été évaluée, puis inscrite sur la Liste intérieure, selon le renseignement qu’elle satisfait aux critères des polymères ERR. Cette lettre indique aussi qu’une forme non-ERR du polymère portant la mention « P » est assujettie à une DSN de l’annexe appropriée pour les polymères non-ERR s’il est fabriqué ou importé au Canada (consulter la partie 2.1.4.1).
L’article 9 du Règlement décrit les polymères ERR comme l’une des substances suivantes :
- a) un polymère qui n’appartient pas aux types de polymères visés par les articles 1 à 4 de l’annexe 7 du Règlement (consulter la partie 3.3.1.7), qui possède une masse moléculaire moyenne en nombre dépassant les 10 000 daltons, dont moins de 2 % des composantes ont des masses moléculaires inférieures à 500 daltons et moins de 5 % ont des masses moléculaires inférieures à 1 000 daltons;
- b) un polymère qui n’appartient pas aux types des polymères visés par l’annexe 7 du Règlement (consulter la partie 3.3.1.7), qui possède une masse moléculaire moyenne en nombre supérieur à 1 000 daltons, mais égale ou inférieure à 10 000 daltons, dont moins de 10 % des composantes ont des masses moléculaires inférieures à 500 daltons et moins de 25 % ont des masses moléculaires inférieures à 1 000 daltons;
- c) un polymère qui est un polyester entièrement produit à partir de réactifs énumérés à l’annexe 8 du Règlement (consulter l’appendice 2) ou à partir d’une forme anhydre de ces réactifs, autres que les réactifs ou les formes anhydres de ces réactifs qui incluent le butan-1-ol et l’acide fumarique ou maléique.
Note : L’alinéa 9c) du Règlement ne fait pas référence à l’annexe 7 et n’inclut pas de restrictions sur la masse moléculaire. Un polymère satisfaisant aux critères de ce paragraphe est considéré comme un polymère ERR, peu importe sa stabilité ou sa masse moléculaire.
3.3.1.6 Polymères qui ne sont pas des polymères à exigences réglementaires réduites
Les polymères non conformes aux critères de l’article 9 du Règlement sont appelés polymères non-ERR. Des exigences supplémentaires de déclaration s’appliquent aux polymères non-ERR lorsque les quantités produites ou importées atteignent de grandes quantités (consulter le tableau 1-1). Les polymères non-ERR sont inscrits sur la Liste intérieure lorsque tous les critères pour leur inscription sont satisfaits (consulter la partie 4.9).
3.3.1.7 Polymères décrits à l’annexe 7 du Règlement
L’annexe 7 du Règlement présente certains des critères utilisés pour déterminer si un polymère est considéré comme un polymère ERR en vertu des alinéas 9a) et 9b) du Règlement, en fonction des quantités de groupes cationiques, de la stabilité, de la composition élémentaire et des quantités de groupes fonctionnels réactifs. L’annexe 7 comprend 5 articles. Les articles 1 à 4 s’appliquent en vertu de l’alinéa 9a) et les articles 1 à 5 s’appliquent en vertu de l’alinéa 9b). Aux fin des alinéas 9a) et 9b) du Règlement, un polymère décrit à l’annexe 7 est considéré comme un polymère non-ERRNote de bas de page 11.
Selon l’article 1, un polymère qui devrait raisonnablement devenir cationique dans un environnement aquatique naturel est considéré comme un polymère non-ERR. Toutefois, un polymère qui est potentiellement cationique pourrait être considéré comme un polymère ERR s’il satisfaisait au critère de l’alinéa 1a) ou 1b). Pour déterminer l’applicabilité de l’alinéa 1a), la masse équivalente du groupe fonctionnel (MEGF) des groupes cationiques doit être calculée (consulter la partie 3.3.1.8). Pour déterminer l’applicabilité de l’alinéa 1b), aucun calcul de la MEGF n’est requis.
L’article 2 décrit un polymère qui est considéré comme un polymère non-ERR en se basant sur sa stabilité (consulter la partie 3.3.1.9).
Les articles 3 et 4 décrivent un polymère qui est considéré comme un polymère non-ERR en se basant sur sa composition élémentaire.
L’article 5 ne s’applique seulement qu’en vertu de l’alinéa 9b). Il décrit un polymère qui est considéré comme un polymère non-ERR en se basant sur la combinaison de MEGF de groupes fonctionnels réactifs spécifiques :
- Un polymère qui a une MEGF combinée inférieure à 5 000 daltons pour les groupes fonctionnels réactifs autres que ceux mentionnés à l’alinéa 5a) est considéré comme un polymère non-ERR;
- Un polymère qui a une MEGF combinée inférieure à 1 000 daltons pour les groupes fonctionnels mentionnés à l’alinéa 5b) est aussi considéré comme un polymère non‑ERR.
Le seuil plus élevé de MEGF de l’alinéa 5a) indique des préoccupations plus importantes associées aux groupes fonctionnels mentionnés dans cet alinéa.
Les méthodes pour calculer la MEGF de groupes fonctionnels cationiques ou réactifs pour différentes distributions de groupes fonctionnels sont présentées à la partie 3.3.1.8.
La figure 3-1 ci-après représente un arbre décisionnel pour déterminer si un polymère est considéré comme un polymère ERR ou non.

Description longue
Les polymères sont considérés soit comme des polymères ERR ou des polymères non-ERR selon les critères établis de l’article 9 et de l’annexe 7 du Règlement. La figure 3-1 illustre ces critères dans un arbre décisionnel qui contient des questions à réponse Oui/Non selon une approche séquentielle regroupées en 3 catégories (Critères de monomères/réactifs, Critères de masse moléculaire et Critères de l’annexe 7) afin de déterminer si un polymère est considéré comme un polymère ERR ou un polymère non-ERR :
- Critères de monomères/réactifs :
- Le polymère est-il un polyester entièrement fabriqué à partir de monomères et de réactifs (incluant les formes anhydres) énumérés à l’annexe 8 et qui ne contient pas de butanol-1 ou d’acide fumarique/maléique?
- Si Oui, le polymère est considéré comme un polymère ERR.
- Si Non, poursuivre aux questions de la catégorie 2.
- Le polymère est-il un polyester entièrement fabriqué à partir de monomères et de réactifs (incluant les formes anhydres) énumérés à l’annexe 8 et qui ne contient pas de butanol-1 ou d’acide fumarique/maléique?
- Critères de masse moléculaire :
- Le polymère possède-t-il une masse moléculaire moyenne en nombre (Mn) < 1 000 daltons?
- Si Oui, le polymère est considéré comme un polymère non-ERR.
- Si Non, poursuivre à la question 2 b.
- Le polymère possède-t-il une 1 000 < Mn ≤ 10 000 daltons, dont moins de 10 % des composantes ont des masses moléculaires < 500 daltons et dont moins de 25 % des composantes ont des masses moléculaires < 1 000 daltons?
- Si Oui, poursuivre à la question a de la catégorie 3.
- Si Non, poursuivre à la question 2 c.
- Le polymère possède-t-il une Mn > 10 000 daltons, dont moins de 2 % des composantes ont des masses moléculaires < 500 daltons et dont moins de 5 % des composantes ont des masses moléculaires < 1 000 daltons?
- Si Oui, poursuivre à la question b de la catégorie 3.
- Si Non, le polymère est considéré comme un polymère non-ERR.
- Le polymère possède-t-il une masse moléculaire moyenne en nombre (Mn) < 1 000 daltons?
- Critères de l’annexe 7 :
- Le polymère fait-il partie des types de polymères visés à l’article 5 de l’annexe 7?
- Si Oui, le polymère est considéré comme un polymère non-ERR.
- Si Non, poursuivre à la question 3 b.
- Le polymère fait-il partie des types de polymères visés aux articles 1 à 4 de l’annexe 7?
- Si Oui, le polymère est considéré comme un polymère non-ERR.
- Si Non, le polymère est considéré comme un polymère ERR.
- Le polymère fait-il partie des types de polymères visés à l’article 5 de l’annexe 7?
3.3.1.8 La masse équivalente du groupe fonctionnel
La MEGF est la masse moléculaire théorique de polymère qui contient un poids équivalent (une mole) d’un groupe fonctionnel donné. Il y a une relation inverse entre la MEGF d’un groupe fonctionnel particulier et le nombre attendue de ce groupe dans le polymère. Par exemple, une MEGF de 700 daltons signifie qu’il y a en moyenne un groupe fonctionnel dans chaque 700 daltons de polymère, alors qu’une MEGF de 4 500 daltons signifie qu’il y a en moyenne un groupe fonctionnel dans chaque 4 500 daltons de polymère. En conséquence, une valeur élevée de la MEGF est associée à un niveau potentiel de préoccupation inférieur.
Les groupes fonctionnels peuvent être distribués à travers le polymère ou situés en position terminale. Pour calculer la MEGF d’un groupe fonctionnel réactif préoccupant ou d’un groupe cationique, il est essentiel de connaître la distribution de ces groupes dans le polymère et, dans le cas de groupes en position terminale, de savoir si le polymère est linéaire ou ramifié.
| N° éq. | Description du calcul | Équation |
|---|---|---|
| 1 | MEGF d’un groupe fonctionnel réparti dans l’ensemble du polymère | |
| 2 | MEGF d’un groupe fonctionnel réparti aux extrémités (groupe terminal) d’un polymère linéaire | |
| 3 | MEGF d’un groupe fonctionnel réparti aux extrémités (groupe terminal) d’un polymère ramifié | |
| 4 | Équation de la MEGF combinée | |
| 5 | MEGF dérivée du nombre de groupes amines | |
| 6 |
Nombre de moles pour un groupe fonctionnel (nombre de moles du groupe fonctionnel / 100 g polymère) |
Liste des abréviations des équations pour calculer la MEGF :
- MEGF : masse équivalente du groupe fonctionnel (dalton);
- %m : pourcentage massique;
- nGF : nombre de groupes fonctionnels disponibles, où « disponibles » signifie groupes fonctionnels qui doivent être pris en compte pour le calcul de la MEGF;
- Mn : masse moléculaire moyenne en nombre (dalton);
- mm : masse moléculaire (dalton);
- nGT : nombre de groupes terminaux;
- nSR : nombre de sites réactifs;
- xamine : nombre de groupes amines, mg KOH/g de polymère;
- mm KOH : masse moléculaire de KOH = 56,1 g/mol.
Liste des indices des équations pour calculer la MEGF :
- mon : monomère;
- AR : agent de ramification;
- GFT : groupe fonctionnel terminal;
- GFT_PL : GFT polymère linéaire;
- GFT_PR : GFT polymère ramifié;
- comb. : combinée;
- MEGFn n=1,2,3… : calcul individuel de la MEGF;
- Amine : amine cationique.
L’équation 1 tient compte des quantités de réactifs chargées dans le réacteur et suppose que les réactifs sont incorporés dans le polymère en totalité lors de la réaction. Cette équation devrait être utilisée à chaque fois que les groupes fonctionnels réactifs restent disponibles après l’incorporation du réactif : c’est-à-dire que la disponibilité des groupes fonctionnels réactifs n’est pas affectée par la position du réactif. Cette équation peut aussi être utilisée pour vérifier les résultats d’autres équations (consulter les exemples 1, 2 et 3).
Les groupes fonctionnels qui sont consommés et incorporés dans le squelette du polymère ne sont pas pris en compte pour le calcul de la MEGF. Lorsqu’un groupe fonctionnel est incorporé dans le squelette, mais qu’il apparaît encore en position terminale d’un polymère, la MEGF devrait être calculée au moyen de l’équation 2 ou 3. Si l’équation 1 était utilisée quand les groupes fonctionnels ne sont disponibles que dans les positions terminales, la MEGF obtenue serait artificiellement faible et surestimerait la préoccupation puisque cette équation ne tient pas compte des groupes fonctionnels qui deviennent indisponibles après avoir été incorporés dans le squelette du polymère. Les équations 2 et 3 tiennent compte respectivement des réactifs du polymère dont les groupes fonctionnels sont consommés lors de la polymérisation et dont les seuls groupes fonctionnels restant disponibles sont en position terminale des polymères linéaires ou ramifiés. Veuillez noter que pour ce calcul il est supposé que toutes les positions terminales sont occupées par le réactif portant le groupe fonctionnel préoccupant. Des équations supplémentaires qui tiennent compte des rapports molaires des autres groupes fonctionnels du polymère et de l’ordre de leur ajout peuvent aussi améliorer la précision du calcul de la MEGF. Toutefois, ceci est en dehors de la portée de la matière présentée dans le Document d’orientation.
Exemple 1
Un polymère acrylique a une Mn de 2 745 daltons, dont 21 % en poids des composantes ont une masse inférieure à 1 000 daltons et 7 % ont une masse inférieure à 500 daltons.
Le squelette acrylique comporte des groupes latéraux amines aliphatiques distribués de manière aléatoire et dérivés uniquement de sa teneur de 2 % en poids de prop-2-ènoate de 2-aminoéthyle (numéro d’enregistrement CAS 7659-38-3, C5H9NO2, mm = 115 daltons).
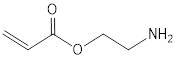
C5H9NO2, mm = 115 daltons
Note : le groupe fonctionnel acrylique de ce réactif réagira avec le squelette du polymère; seule l’amine primaire cationique doit être prise en compte.
La MEGFamine est calculée au moyen de l’équation 1 : MEGF d’un groupe fonctionnel réparti dans l’ensemble du polymère.
Le polymère satisfait au critère d’exception de l’alinéa 1a) de l’annexe 7 (la MEGF combinée des groupes cationiques doit être supérieure à 5 000 daltons) et, en conséquence, ce polymère n’est pas l’un des types mentionnés à l’article 1 de l’annexe 7. Ce polymère est donc considéré comme un polymère ERR.
Exemple 2
Un produit de la réaction de l’acide prop-2-ènoïque (numéro d’enregistrement CAS 79-10-7) avec du poly(alcool vinylique), homopolymère (numéro d’enregistrement CAS 9002-89-5), a une Mn de 8 500 daltons dont 17 % en poids des composantes ont une masse inférieure à 1 000 daltons et 4,7 % ont une masse inférieure à 500 daltons.
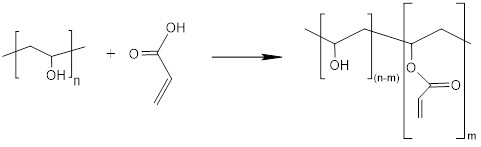
Le groupe acide carboxylique de l’acide prop-2-ènoïque (mm = 72 daltons) réagit avec les groupes latéraux alcools du prépolymère. Le polymère résultant contient donc des groupes latéraux prop-2-ènoates distribués aléatoirement.
En se basant sur la description susmentionnée (Mn et réactifs), ce polymère ne satisfait pas à la définition de l’alinéa 9a) ni à celle de l’alinéa 9c) du Règlement. Conformément à l’alinéa 9b), il faut déterminer si le polymère est décrit à l’annexe 7, y compris à l’article 5.
Les groupes latéraux prop-2-ènoates sont des groupes fonctionnels réactifs qui ne sont pas mentionnés à l’alinéa 5a) de l’annexe 7. Le seuil correspondant de 5 000 daltons pour la MEGF s’applique donc à ce groupe fonctionnel.
Le polymère contient 5,5 % en poids d’acide prop-2-ènoïque, qui a une masse moléculaire de 72 daltons.
La MEGF du groupe fonctionnel latéral prop-2-ènoate est aussi calculée au moyen de l’équation 1 :
La MEGF du groupe fonctionnel latéral prop-2-ènoate est inférieure à 5 000 daltons. Le polymère est donc décrit à l’alinéa 5a) de l’annexe 7. Ce polymère est donc considéré comme un polymère non-ERR.
Note : un polymère ayant la même composition et satisfaisant aux exigences de l’alinéa 9a) sur la Mn et la teneur en oligomère serait considéré comme un polymère ERR. Un calcul de la MEGF ne serait pas requis.
Exemple 3
Note : l’exemple suivant illustre que, même lorsque le groupe fonctionnel préoccupant est situé uniquement en position terminale, le calcul de la MEGF au moyen d’une analyse par groupe terminal pourrait être inapproprié.
Le polymère de cet example a une Mn de 6 800 daltons, dont 7 % en poids des composantes ont une masse moléculaire inférieure à 1 000 daltons et 3 % ont une masse inférieure à 500 daltons.
Le polymère est constitué de 91,6 % en poids d’un prépolymère d’acide hexanedioïque, polymérisé avec de l’hexane-1,6-diol (numéro d’enregistrement CAS 25212-06-0) ayant réagi avec 8,4 % en poids de triester d’acide prop-2-ènoïque et de 2,2‑bis(hydroxyméthyl)propane-1,3-diol (numéro d’enregistrement CAS 3524-68-3).
Le numéro d’enregistrement CAS 25212-06-0 est constitué des numéro d’enregistrement CAS 629-11-8 et 124-04-9.
Hexanediol, mm = 118 daltons
numéro d’enregistrement CAS 629-11-8
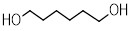
Acide hexanedioïque, mm = 146 daltons
numéro d’enregistrement CAS 124-04-9
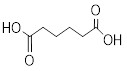
Triester d’acide prop-2-ènoïque et de 2,2‑bis(hydroxyméthyl)propane-1,3-diol, mm = 298 daltons, numéro d’enregistrement CAS 3524-68-3
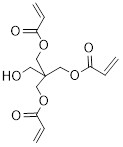
Le triester d’acide prop-2-ènoïque et de 2,2‑bis(hydroxyméthyl)propane-1,3-diol ne peut réagir avec le prépolymère que par son groupe alcool. Les 3 groupes fonctionnels prop-2-ènoates resteront latéraux.
En se basant sur la description susmentionnée (Mn et réactifs), ce polymère ne satisfait pas à la définition de l’alinéa 9a) ni à celle de l’alinéa 9c) du Règlement. En vertu de l’alinéa 9b), il faut déterminer si le polymère est décrit à l’annexe 7, y compris à l’article 5.
Les groupes latéraux prop-2-ènoates sont des groupes fonctionnels réactifs qui ne sont pas mentionnés à l’alinéa 5a) de l’annexe 7. Le seuil correspondant de 5 000 daltons pour la MEGF s’applique donc à ce groupe fonctionnel.
Le prépolymère est linéaire et ses seuls groupes fonctionnels disponibles sont en position terminale. Le groupe alcool du triester d’acide prop-2-ènoïque et de 2,2‑bis(hydroxyméthyl)propane-1,3-diol ne peut réagir qu’avec l’acide hexanedioïque, c’est-à-dire avec les positions terminales qui sont occupées par l’acide hexanedioïque.
Si des quantités molaires égales d’acide hexanedioïque et d’hexane-1,6-diol réagissent, les positions terminales du polymère résultant seront idéalement occupées par des groupes acides et alcools.
![Polymère OC(CCCCC(OCCCCCCO[H])=O)=O](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-IMG6.jpg)
Ce serait le cas si le polymère était constitué de 55,3 % en poids d’acide hexanedioïque et de 44,7 % en poids d’hexane-1,6-diol. L’équation 6 est utilisée pour la comparaison des quantités molaires/100 g :
En cas d’un excès suffisantNote de bas de page 12 d’acide hexanedioïque, le polymère résultant ne contiendrait que des groupes terminaux acides.
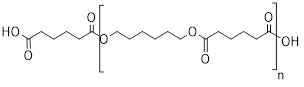
La présence d’acide hexanedioïque dans une ou les deux positions terminales déterminera si le triester d’acide prop-2-ènoïque et de 2,2‑bis(hydroxyméthyl)propane-1,3-diol peut réagir avec une position terminale (A) ou les deux (B).
(A) ![O=C(OCC(CO)(COC(=O)C=C)COC(=O)C=C)C=C qui réagit avec une position terminal du polymère OC(CCCCC(OCCCCCCO[H])=O)=O](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-IMG8.jpg)
(B) ![O=C(OCC(CO)(COC(=O)C=C)COC(=O)C=C)C=C qui réagit avec les deux positions terminal du polymère OC(CCCCC(OCCCCCCO[H])=O)=O](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-IMG9.jpg)
La MEGFprop-2-ènoate pourrait donc être calculée au moyen de l’équation 2 : MEGF d’un groupe fonctionnel réparti aux extrémités (groupe terminal) d’un polymère linéaire.
Pour (A), le calcul serait
Pour (B), le calcul serait
Aucun des 2 polymères (A) ou (B) ne serait donc considéré comme un polymère ERR, le polymère étant considéré comme d’un type des polymères décrits à l’alinéa 5a).
Important
Ce calcul suppose qu’il est prévu que le polymère final ait autant de groupes terminaux prop-2-ènoates que la composition du prépolymère le permette, c’est-à-dire que suffisamment de triester d’acide prop-2-ènoïque et de 2,2‑bis(hydroxyméthyl)propane-1,3-diol est ajouté pour couvrir toutes les positions terminales disponibles.
Pour vérifier que c’est effectivement le cas, l’équation 1 doit être utilisée, cette équation prenant en compte la quantité de réactif.
Le calcul de la MEGF au moyen de cette équation aurait fourni immédiatement la réponse à si le polymère est considérée comme un polymère ERR ou non.
En tenant compte du calcul élaboré susmentionné, la MEGFprop-2-ènoate calculée avec cette équation indique que suffisamment de prop-2-ènoate est chargé pour avoir tous les groupes terminaux disponibles du cas (B) couverts par ce réactif. Si le polymère était en fait la version (A), le chargement de cette quantité de prop-2-ènoate constituerait un excès (souvent observable en tant que pic de faible masse moléculaire en chromatographie sur gel [Gel permeation chromatography – GPC]).
Exemple 4
Un polyuréthane linéaire a une Mn de 100 000 daltons et ne comporte aucune composante de masse moléculaire inférieure à 1 000 daltons. Son réactif contenant de l’isocyanate est aliphatique et, par conséquent, est considéré cationique après hydrolyse. Puisque le groupe fonctionnel réagit avec des liaisons uréthanes de la chaîne polymère et s’hydrolyse en une amine cationique en position terminale uniquement, la MEGF doit être évaluée au moyen d’une analyse des groupes terminaux disponibles. En supposant que toutes les positions terminales du polymère sont occupées par des groupes isocyanates aliphatiques, la MEGFGFT est donc calculée au moyen de l’équation 2 :
La MEGF pour le groupe amine cationique (c’est-à-dire après hydrolyse de l’isocyanate aliphatique) est supérieure au seuil de MEGF de 5 000 daltons pour les groupes cationiques. Ce polymère satisfait donc au critère d’exception de l’alinéa 1a) de l’annexe 7. Ce polymère ne fait pas partie des types mentionnés à l’article 1 de l’annexe 7. Ce polymère est donc considéré comme un polymère ERR.
Note : un isocyanate aromatique n’aurait pas nécessité de calcul puisque les isocyanates aromatiques ne deviennent pas cationiques et le polymère aurait satisfait aux exigences de l’alinéa 9a) [l’article 5 de l’annexe 7 ne s’applique seulement qu’en vertu de l’alinéa 9b)].
Exemple 5

Un polyuréthane ramifié de 9 600 daltons contient en position terminale des groupes isocyanates provenant d’un diisocyanate aromatique. L’agent de ramification, le 2‑éthyl‑2-(hydroxyméthyl)propane-1,3-diol (numéro d’enregistrement CAS 77-99-6) a une masse moléculaire de 134 daltons et représente 1 % en poids du polymère. Il comporte 3 sites réactifs.
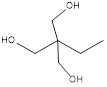
La MEGF pour le groupe fonctionnel en position terminale d’un polymère ramifié doit être calculée au moyen de l’équation 3 :
Avec une MEGF de 3 534 pour les groupes isocyanates, le polymère est décrit à l’alinéa 5a) de l’annexe 7 et, par conséquent, n’est pas considéré comme un polymère ERR.
Exemple 6
![Polymère NCOC(C(C[R])CC(C[R])C(OCN(C)C)=O)=O](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-IMG12.jpg)
Un polymère acrylique contient des groupes amines aliphatiques provenant de 1 % en poids de prop-2-ènoate de 2-aminoéthyle (numéro d’enregistrement CAS 7659-38-3, masse moléculaire = 115 daltons) et de 2 % en poids de 2-méthylprop-2-ènoate de (diméthylamino)éthyle (numéro d’enregistrement CAS 2867-47-2, masse moléculaire = 157 daltons). La MEGF pour chacun des groupes cationiques est calculée au moyen de l’équation 1 :
La MEGF combinée est ensuite calculée au moyen de l’équation 4 :
Avec une MEGF combinée inférieure à 5 000 daltons pour les groupes cationiques, le polymère est décrit à l’article 1 de l’annexe 7 et n’est donc pas considéré comme un polymère ERR.
Exemple 7
Pour de nombreux polymères complexes (par exemple des polymères contenant des prépolymères), il est impossible de calculer la MEGF pour un groupe fonctionnel spécifique préoccupant sans obtenir des renseignements supplémentaires, par exemple la composition du prépolymère, la Mn ou les deux.
Dans le cas de groupes fonctionnels cationiques, un nombre de groupes amines déterminé empiriquement fournit le renseignement la plus précis sur la charge cationique réellement présente. Par exemple, pour un nombre de groupes amines de 7,5 mg KOH/g polymère, le calcul au moyen de l’équation 5 serait :
En faisant le calcul inverse, tout nombre de groupes amines supérieur à 11,22 indique que le polymère est mentionné à l’article 1 de l’annexe 7 et est considéré comme un polymère non-ERR :
3.3.1.9 Polymères qui se dégradent, se décomposent ou se dépolymérisent considérablement
Pour déterminer si un polymère peut être classé comme un polymère ERR, il faut en outre déterminer s’il est conçu pour se dégrader, se décomposer ou se dépolymériser considérablement, ou s’il est susceptible de le faire. Ce critère est présenté à l’article 2 de l’annexe 7 du Règlement. Si la substance satisfait à ce critère, ou à tout autre critère énoncé dans l’annexe 7, elle ne serait pas classée comme un polymère ERR.
Le Programme des SN tiendra compte de l’ampleur de la dégradation, de la décomposition ou de la dépolymérisation ainsi que du danger lié aux produits de transformation pour l’interprétation de ce critère. Si les produits de transformation d’un polymère sont peu dangereux, on pourrait considérer qu’il s’agit d’un polymère ERR même s’il se dégrade, se décompose ou se dépolymérise, selon si d’autres critères sont satisfaits ou non.
Lorsqu’un déclarant indique qu’un polymère doit être considéré comme un polymère ERR, il devrait fournir l’information pour appuyer l’évaluation selon laquelle le polymère se dégrade considérablement. En l’absence de cette information, le Programme des SN fera preuve de discernement pour prendre une décision à cet égard. Pour étayer leur allégation, les déclarants devraient fournir de l’information quant à la dégradation du polymère, notamment si le polymère fait partie d’une classe de polymères qui est reconnue comme se transformant facilement (par exemple des polysaccharides ou certains biopolymères). Dans les cas où il est prévu que le polymère se dégradera, ou s’il y a des données empiriques qui démontrent qu’il se dégradera, le déclarant devrait indiquer les produits de transformation connus ou prévus et fournir de l’information quant à leurs dangers, pour que les responsables du Programme des SN puissent évaluer l’affirmation selon laquelle il s’agit d’un polymère ERR.
Il est possible qu’aucune information expérimentale ne soit disponible. Des programmes de modélisation prédictive peuvent alors être utilisés pour aborder la stabilité du polymère, la formation de produits de transformation stables et la caractérisation de leurs dangers. Il peut également être acceptable d’utiliser d’autres méthodes, comme l’accès aux données des publications scientifiques ou l’utilisation de données de substitution.
À l’instar de toute information ou affirmation donnée dans une déclaration, le Programme des SN évaluera les mérites pour déterminer si la substance répond à ce critère.
3.4 Substances de catégorie spéciale
Par définition, les substances de catégorie spéciale sont celles qui sont fabriquées ou importées dans les conditions suivantes :
- a) les substances pour la recherche et le développement;
- b) les substances confinées intermédiaires limitées au site;
- c) les substances confinées destinées à l’exportation.
3.4.1 Substances destinées à la recherche et au développement
Selon la définition du paragraphe 1(1) du Règlement, les substances destinées à la recherche et au développement sont celles qui font l’objet d’une investigation ou de recherches systématiques, par voie d’expérimentation ou d’analyse, à l’exclusion des tests de marché; le principal objectif des investigations et des recherches étant l’un ou l’autre des objectifs suivants :
- a) la création ou l’amélioration d’un produit ou d’un procédé;
- b) la détermination de la viabilité technique ou des caractéristiques de rendement d’un produit ou d’un procédé;
- c) l’évaluation de la substance avant sa commercialisation au moyen d’essais pilotes en usine, d’essais de production, y compris la production à grande échelle, ou d’essais individualisés en usine de sorte que les spécifications techniques puissent être adaptées aux exigences de rendement de clients éventuels.
Cette catégorie comprend les substances chimiques et les polymères fabriqués en sous-traitance pour des clients du Canada ou de l’étranger qui effectuent des recherches (consulter la partie 1.4.3).
De plus, selon la définition du Règlement, en ce qui a trait aux produits ci-dessus, un test de marché est « l’étude des possibilités de mise en marché d’un produit en situation de concurrence lorsque la création ou l’amélioration du produit n’est pas le principal objectif ».
3.4.2 Substances confinées intermédiaires limitées au site
Selon la définition du paragraphe 1(1) du Règlement, une substance confinée intermédiaire limitée au site est une substance consommée dans une réaction chimique servant à la fabrication d’une autre substance et qui est :
- a) soit fabriquée et consommée dans le site de fabrication;
- b) soit fabriquée dans un site et transportée à un second site où elle sera consommée;
- c) soit importée et transportée directement au site où elle sera consommée.
De plus, selon leur définition dans le Règlement :
- « confinée » s’entend d’« une limite absolue de rejet dans le milieu aquatique de 1 kg par jour par site, après le traitement des eaux usées »;
- « consommée » s’entend d’une substance « détruite ou complètement convertie en une autre substance ».
Si une substance est classée comme substance intermédiaire limitée au site, elle doit être, pendant toute son existence (fabrication, importation, entreposage, transport, manutention, utilisation et élimination), confinée conformément à la définition ci-dessus de manière à prévenir tout rejet important dans l’environnement.
Une substance qui est un précurseur direct au cours de la fabrication d’un article conformément à la définition de la partie 3.2.2, n’est pas considérée comme une substance intermédiaire limitée au site, et elle est assujettie à l’obligation de déclaration. Toutefois, si un précurseur direct de l’article fabriqué correspond aux critères définissant les « substances intermédiaires de réaction non isolées » (consulter la partie 3.2.5), sa déclaration n’est pas obligatoire.
3.4.3 Substances confinées destinées à l’exportation
La désignation de substance confinée destinée à l’exportation est limitée aux substances nouvelles fabriquées ou importées au Canada qui sont destinées uniquement aux marchés étrangers, et qui sont confinées.
Selon la définition du paragraphe 1(1) du Règlement, « confinée » se dit d’une limite absolue de rejet de la substance dans le milieu aquatique de 1 kg par jour par site, après le traitement des eaux usées.
Partie 4. Exigences en matière de renseignements pour les déclarations
4.1 Détermination des renseignements exigés pour les déclarations
Le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [le Règlement] prescrit des exigences en matière de renseignements en fonction de l’utilisation et de la quantité de la substance chimique ou du polymère fabriqué ou importé. Énoncées dans les annexes au Règlement, elles sont présentées dans l’appendice 2 du présent Document d’orientation. La partie 4 et l’appendice 1 contiennent des diagrammes de décision qui faciliteront la sélection de l’annexe appropriée.
Bien que le Règlement donne une approche par étapes pour la déclaration liant les exigences en matière de renseignements à des facteurs comme la quantité, l’utilisation, les propriétés intrinsèques et la catégorie, il faut savoir que cette approche n’est pas obligatoire. Un déclarant peut, s’il le souhaite, choisir de présenter d’emblée l’annexe prévue pour la déclaration qui a le numéro le plus élevé, à condition que les quantités prescrites les plus faibles pour l’annexe de numéro le plus bas soient respectées et que la Déclaration de substances nouvelles (DSN) soit présentée dans les délais prévus pour l’annexe de numéro le plus élevé.
Comme l’indique les diagrammes de décision présentés ci-dessous et à l’appendice 1, un certain nombre de facteurs doivent être pris en compte pour déterminer la nature des renseignements à présenter et le moment de le faire. Ces facteurs sont notamment :
- si la substance nouvelle est une substance chimique ou un polymère (consulter la partie 3.3);
- si la substance nouvelle est une substance de catégorie spéciale (par exemple, destinée à la recherche et au développement ou confinée qui est intermédiaire limitée au site ou destinée à l’exportation; consulter la partie 3.4);
- si la substance nouvelle figure sur la Liste extérieure (consulter la partie 2.2);
- les quantités annuelles de la substance nouvelle qui seront fabriquées ou importées au Canada (consulter le tableau 1-1 et les parties 4.2, 4.4, 4.5, 4.8 et 4.9);
- lorsque la substance nouvelle est un polymère, si elle satisfait à la définition pour les polymères à exigences réglementaires réduites (ERR) (consulter la partie 3.3.1.5);
- lorsque la substance nouvelle est un polymère, si elle est constituée uniquement de monomères et d’agents réactifs qui figurent sur la Liste intérieure ou la Liste extérieure (consulter la partie 4.7.1);
- si la substance nouvelle sera rejetée dans l’environnement aquatique en grande quantité ou le degré d’exposition du public sera élevée (consulter les parties 4.4.3 et 4.9.2).
4.1.1 Quantités annuelles
Le Règlement prévoit un mode de déclaration avant fabrication et avant importation. Dans ce contexte, le déclarant doit produire une estimation exacte des quantités annuelles (par année civile) de la substance nouvelle destinée à être fabriquée ou importée au Canada et il doit présenter une DSN avant d’excéder chacune des quantités prescrites.
Ces quantités prescrites dépendent de la quantité réelle de la substance fabriquée et importée, et non de la quantité de la formulation qui contient cette substance. Ainsi, s’il est prévu d’importer au cours d’une année civile 10 000 kg de la formulation A qui contient 13 % de la substance nouvelle X, alors la quantité annuelle importée sera de 1 300 kg.
Les parties suivantes aideront à déterminer les annexes qui s’appliquent ainsi que la date limite de présentation des DSN au Programme des substances nouvelles (SN).
4.2 Déclaration de substances de catégorie spéciale
La présente partie décrit comment déclarer les diverses substances fabriquées ou importées aux fins des activités regroupées sous le terme « catégorie spéciale » (consulter la partie 3.4). Si une quantité de la substance est utilisée pour une activité autre que celles qui la classeraient dans la catégorie spéciale, elle doit être déclarée au titre des annexes appropriées en fonction de la quantité qui sera utilisée par ces activités (consulter les parties 4.3 et 4.7). Ces exigences sont énoncées dans les annexes au Règlement présentées dans l’appendice 2 du Document d’orientation.
4.2.1 Déclaration des substances chimiques de catégorie spéciale fabriquées ou importées en faibles quantités (consulter la figure 4-1)
Tous les déclarants qui fabriquent ou importent une substance chimique pour la recherche et le développement ou une substance confinée qui est intermédiaire limitée au site ou destinée à l’exportation, doivent présenter au ministre de l’Environnement (le ministre) les renseignements prévus à l’annexe 1 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile.
4.2.1.1 Substances biochimiques destinées à la recherche et au développement en faibles quantités
Dans le cas d’une substance biochimique destinée à la recherche et au développement, le déclarant doit fournir, en plus des renseignements prévus par l’annexe 1 susmentionnés, ceux qui sont prescrits aux articles 1 et 2 de l’annexe 2 du Règlement.
4.2.1.2 Substances biochimiques confinées intermédiaires limitées au site en faibles quantités
S’il s’agit d’une substance biochimique confinée intermédiaire limitée au site qui n’est ni fabriquée ni consommée au site de fabrication, le déclarant doit fournir, en plus des renseignements prévus à l’annexe 1 susmentionnés, ceux qui sont prescrits par les articles 1 à 4 de l’annexe 2 du Règlement et :
- a) si la substance biochimique est un acide nucléique, ceux qui sont prescrits par les articles 5 et 6 de l’annexe 2 du Règlement;
- b) si la substance biochimique a des propriétés enzymatiques, ceux qui sont prescrits par les articles 7 à 13 de l’annexe 2 du Règlement.
Dans le cas d’une substance biochimique confinée intermédiaire limitée au site qui est fabriquée et consommée au site de fabrication, le déclarant doit fournir, en plus des renseignements prévus à l’annexe 1, ceux qui sont prescrits par les articles 1, 2 et 4 de l’annexe 2 du Règlement.
4.2.1.3 Substances biochimiques confinées destinées à l’exportation en faibles quantités
Dans le cas des substances biochimiques confinées, destinées à l’exportation, le déclarant doit fournir, en plus des renseignements prévus à l’annexe 1 susmentionnés, ceux qui sont prescrits par les articles 1 à 4 de l’annexe 2 du Règlement et :
- a) si la substance biochimique est un acide nucléique, ceux qui sont prescrits par les articles 5 et 6 de l’annexe 2 du Règlement;
- b) si la substance biochimique a des propriétés enzymatiques, ceux qui sont prescrits par les articles 7 à 13 de l’annexe 2 du Règlement.
4.2.2 Déclaration des substances chimiques de catégorie spéciale fabriquées ou importées en grandes quantités (consulter la figure 4-1)
De plus, en outre des renseignements de l’annexe 1 (et de l’annexe 2, le cas échéant) mentionnés ci-dessus, le déclarant doit actualiser tous les renseignements déjà fournis au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile. S’il n’y a aucun changement dans ces renseignements, il faut l’indiquer à ce moment.

Description longue
Les déclarants qui fabriquent ou importent une nouvelle substance chimique comme indiqué à l’article 5 du Règlement ou un nouveau polymère comme indiqué à l’article 6 du Règlement, c'est-à-dire une substance pour la recherche et le développement, une substance confinée qui est intermédiaire limitée au site ou une substance destinée à l’exportation, doivent présenter au ministre les renseignements de l’annexe appropriée avant de dépasser la quantité seuil qui s’applique et dans les délais prescrits pour cette annexe. La figure 4-1 illustre les délais prescrits et les renseignements à fournir pour ces substances :
- Pour une substance chimique/biochimique (article 5 du Règlement) :
- Présenter au ministre les renseignements prévus à l’annexe 11 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile.
- Actualiser tous les renseignements déjà fournis au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
- Pour un polymère/biopolymère (article 6 du Règlement) :
- Présenter au ministre les renseignements prévus à l’annexe 32 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
1Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’une substance biochimique [consulter les paragraphes 5(2), (3) et (4) du Règlement].
2Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’un biopolymère [consulter les paragraphes 6(2), (3) et (4) du Règlement].
4.2.3 Déclaration de polymères de catégorie spéciale fabriqués ou importés en grandes quantités (consulter la figure 4-1)
Les déclarants qui fabriquent ou importent un polymère destiné à la recherche et au développement ou un polymère confiné qui est intermédiaire limité au site ou destiné à l’exportation doivent présenter au ministre les renseignements prévus à l’annexe 3 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
4.2.3.1 Biopolymères destinés à la recherche et au développement en grande quantité
Dans le cas d’un biopolymère destiné à la recherche et au développement, le déclarant doit fournir, en plus des renseignements prévus par l’annexe 3 susmentionnés, ceux qui sont prescrits aux articles 1 et 2 de l’annexe 2 du Règlement.
4.2.3.2 Biopolymères confinés intermédiaires limités au site en grande quantité
S’il s’agit d’un biopolymère confiné intermédiaire limité au site qui n’est pas fabriqué et consommé au site de fabrication, le déclarant doit fournir, en plus des renseignements prévus à l’annexe 3 susmentionnés, ceux qui sont prescrits par les articles 1 à 4 de l’annexe 2 du Règlement et si le biopolymère est un acide nucléique, ceux qui sont prescrits par les articles 5 et 6 de l’annexe 2.
Dans le cas d’un biopolymère confiné intermédiaire limité au site qui est fabriqué et consommé au site de fabrication, le déclarant doit fournir, en plus des renseignements prévus à l’annexe 3, ceux qui sont prescrits par les articles 1, 2 et 4 de l’annexe 2 du Règlement.
4.2.3.3 Biopolymères confinés destinés à l’exportation en grande quantité
Si la substance est un biopolymère confiné destiné à l’exportation, le déclarant doit fournir, en plus des renseignements prévus à l’annexe 3 susmentionnés, ceux qui sont prescrits par les articles 1 à 4 de l’annexe 2 du et si le biopolymère est un acide nucléique, ceux qui sont prescrits par les articles 5 et 6 de l’annexe 2 du Règlement.
4.3 Déclaration des substances chimiques
Comme l’indique la partie 4.1, le Règlement prescrit des exigences en matière de renseignements en fonction de l’utilisation et de la quantité des substances chimiques. Ces exigences sont énoncées dans les annexes au Règlement présentées dans l’appendice 2 du Document d’orientation. Pour faciliter la sélection de l’annexe appropriée pour la déclaration, un diagramme de décision est inclus ci-dessous (consulter la figure 4-2) et dans l’appendice 1 du Document d’orientation.
Avant d’utiliser ces diagrammes, le tableau 1-1, ainsi que les parties 2.2, 3.3, 3.4, 4.2.1, 4.2.2, 4.4 et 4.5 du Document d’orientation devraient être examinés afin de déterminer :
- si la substance nouvelle correspond à la définition d’une substance chimique au sens du Règlement (consulter la partie 3.3.1.1);
- si la substance chimique nouvelle est une substance de catégorie spéciale (par exemple, destinée à la recherche et au développement ou confinée qui est intermédiaire limitée au site ou destinée à l’exportation; consulter la partie 3.4);
- si la substance chimique nouvelle figure sur la Liste extérieure (consulter la partie 2.2);
- les quantités annuelles de la substance nouvelle qui seront fabriquées ou importées au Canada (consulter le tableau 1-1 et les parties 4.2 à 4.5);
- si la substance chimique nouvelle figurant sur la Liste extérieure sera rejetée dans l’environnement aquatique en grande quantité ou le degré d’exposition du public sera élevée (consulter la partie 4.4.3).
Les parties suivantes ne s’appliquent qu’aux produits chimiques fabriqués ou importés à une fin autre que celles de la catégorie spéciale conformément à la partie 3.4 du Document d’orientation.
4.4 Exigences en matière de renseignements pour les substances chimiques figurant sur la Liste extérieure (consulter la figure 4-2)
4.4.1 Substances chimiques fabriquées ou importées en faibles quantités
Les déclarants qui fabriquent ou importent une substance chimique qui figure sur la Liste extérieure doivent présenter au ministre les renseignements prévus à l’annexe 4 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile.
S’il s’agit d’une substance biochimique, le déclarant doit présenter, outre les renseignements prévus à l’annexe 4, ceux prescrits par les articles 1 à 3 de l’annexe 2 du Règlement.
4.4.2 Substances chimiques fabriquées ou importées en grandes quantités
Les déclarants qui fabriquent ou importent une substance chimique qui figure sur la Liste extérieure doivent présenter au ministre les renseignements prévus à l’annexe 5 du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
S’il s’agit d’une substance biochimique, le déclarant doit présenter, outre les renseignements prévus à l’annexe 5, ceux prescrits par les articles 1 à 4 de l’annexe 2 du Règlement et :
- a) si la substance biochimique est un acide nucléique, ceux qui sont prescrits par les articles 5 et 6 de l’annexe 2 du Règlement;
- b) si la substance biochimique a des propriétés enzymatiques, ceux qui sont prescrits par les articles 7 à 13 de l’annexe 2 du Règlement.
4.4.3 Substances chimiques figurant sur la Liste extérieure, rejetées dans l’environnement aquatique en grande quantité et/ou le degré d'exposition du public est élevé
Les déclarants qui fabriquent ou importent une substance chimique qui figure sur la Liste extérieure et :
- qui est rejetée dans l’environnement aquatique en une quantité supérieure à 3 kg par jour par site (la moyenne devant être calculée sur une base mensuelle et après traitement des eaux usées);
- le degré d’exposition du public à cette substance chimique contenue dans un produit pourrait être élevé.
doivent présenter au ministre les renseignements supplémentaires sur les essais prescrits par les paragraphes 7(2) ou 7(3) du Règlement au moins 75 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 50 000 kg au cours d’une année civile. Les renseignements supplémentaires requis sont indiqués dans les parties qui suivent.
4.4.3.1 Substances chimiques rejetées dans l’environnement aquatique
Il incombe au déclarant de présenter, dans la DSN, les éléments probants prescrits par l’alinéa 10c) de l’annexe 5 afin d’étayer son allégation selon laquelle cette substance n’est pas rejetée dans l’environnement aquatique en quantités supérieures à la limite indiquée plus haut. Ces renseignements devraient aussi inclure toutes les utilisations et quantités futures envisagées par les autres utilisateurs et une description des applications envisagées. Veuillez consulter la partie 6.6.5 du Document d’orientation pour calculer les rejets quotidiens dans le milieu aquatique.
Les représentants du Programme des SN évalueront ces renseignements et s’il est déterminé que cette substance est rejetée dans l’environnement aquatique en quantités supérieures à celles indiquées ci-dessus, le déclarant doit présenter les renseignements supplémentaires prescrits par le paragraphe 7(2) du Règlement. Le Programme des SN indiquera au déclarant si la substance est assujettie à des exigences supplémentaires relatives aux renseignements mentionnées ci-dessous. Le déclarant peut présenter des renseignements supplémentaires pour étayer ses allégations et demander une réévaluation de la décision prise par le Programme des SN en communiquant avec la Ligne d’information de la gestion des substances. Le Programme des SN examinera et prendra en compte ces renseignements.
Conformément au paragraphe 7(2) du Règlement, les renseignements supplémentaires requis comprennent :
- a) pour les substances ayant une solubilité dans l’eau supérieure ou égale à 200 µg/L :
- (i) les données provenant d’un essai de présélection sur l’adsorption et la désorption,
- (ii) le taux d’hydrolyse en fonction du pH et, s’ils sont connus, les produits de l’hydrolyse;
- b) les données provenant d’un essai de toxicité d’au moins 28 jours de doses répétées de la substance chez les mammifères administré par voie orale, cutanée ou par inhalation, selon le mode d’exposition le plus probable du public, et les renseignements suivants :
- (i) l’âge, le sexe, le nombre, l’espèce, la souche et la source des animaux testés,
- (ii) la voie d’administration de la substance et les conditions dans lesquelles l’essai est effectué,
- (iii) la posologie de la substance, le vecteur par lequel elle est administrée et sa concentration dans le vecteur.
4.4.3.2 Degré d'exposition du public à une substance chimique contenue dans un produit
Il incombe au déclarant de présenter dans la DSN, les renseignements prescrits par l’alinéa 10d) de l’annexe 5 afin d’étayer son allégation selon laquelle le public est peu exposé à une substance contenue dans un produit. Le Programme des SN indiquera au déclarant si la substance est assujettie à des exigences supplémentaires relatives aux renseignements mentionnées ci-dessous. Le déclarant peut présenter des renseignements supplémentaires pour étayer ses allégations et demander une réévaluation de la décision prise par le Programme des SN en communiquant avec la Ligne d’information de la gestion des substances. Le Programme des SN examinera et prendra en compte ces renseignements.
Puisque l’exposition du public dépend d’un grand nombre de facteurs, un calcul permettant de déterminer ce qui constitue un « degré d’exposition élevé » ne peut être applicable à toutes circonstances, sans tomber dans une prudence extrême. Pour cette raison, le Programme des SN évalue au cas par cas le « degré d’exposition élevé ». À cette fin, il faut prendre en compte des facteurs comme le type d’utilisation, la durée et la fréquence de l’utilisation, la concentration de la substance chimique dans un produit et les circonstances de l’exposition qui peuvent limiter l’exposition directe du public (par exemple, si la substance est chimiquement consommée pendant son utilisation ou si elle peut migrer depuis un produit).
Les produits de consommation contenant une substance à laquelle le degré d'exposition du public pourrait être élevé comprennent notamment le détergent à vaisselle, les produits de lessive, les savons, le papier hygiénique, les solutions de nettoyage, les encaustiques, les agents de polissage, les assainisseurs d’air, les peintures, les huiles, les graisses, les lotions corporelles et les encres.
S’il est déterminé que le degré d'exposition du public pourrait être élevé à une substance chimique contenue dans un produit, le déclarant doit fournir les renseignements supplémentaires prescrits par le paragraphe 7(3) du Règlement et doivent comprendre :
- a) les données provenant d’un essai de toxicité d’au moins 28 jours de doses répétées de la substance chez les mammifères administré par voie orale, cutanée ou par inhalation, selon le mode d’exposition le plus probable du public, et les renseignements suivants :
- (i) l’âge, le sexe, le nombre, l’espèce, la souche et la source des animaux testés,
- (ii) la voie d’administration de la substance et les conditions dans lesquelles l’essai est effectué,
- (iii) la posologie de la substance, le vecteur par lequel elle est administrée et sa concentration dans le vecteur;
- b) les données provenant d’un essai in vitro, avec et sans activation métabolique, pour déterminer la présence d’aberrations chromosomiques dans des cellules de mammifères ou, si elles existent déjà, les données d’une étude in vivo chez les mammifères pour déterminer la présence d’aberrations chromosomiques qui, jumelées à des données établissant que le tissu en question a été exposé à la substance ou à ses métabolites, permettent l’évaluation du pouvoir clastogène in vivo.
4.5 Exigences en matière de renseignements pour les substances chimiques ne figurant pas sur la Liste extérieure (consulter la figure 4-2)
4.5.1 Substances chimiques fabriquées ou importées en faibles quantités
Avant d’excéder 100 kg par année
Les déclarants qui fabriquent ou importent une substance chimique qui ne figure pas sur la Liste extérieure doivent présenter au ministre les renseignements prévus à l’annexe 4 du Règlement au moins 5 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 100 kg au cours d’une année civile.
S’il s’agit d’une substance biochimique, le déclarant doit présenter, outre les renseignements prévus à l’annexe 4, ceux prescrits par les articles 1 à 3 de l’annexe 2 du Règlement.
Avant d’excéder 1 000 kg par année
Les déclarants qui fabriquent ou importent une substance chimique qui ne figure pas sur la Liste extérieure doivent présenter au ministre les renseignements prévus à l’annexe 5 du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile.
S’il s’agit d’une substance biochimique, le déclarant doit présenter, outre les renseignements prévus à l’annexe 5, ceux prescrits par les articles 1 à 4 de l’annexe 2 du Règlement et :
- a) si la substance biochimique est un acide nucléique, ceux qui sont prescrits par les articles 5 et 6 de l’annexe 2 du Règlement;
- b) si la substance biochimique a des propriétés enzymatiques, ceux qui sont prescrits par les articles 7 à 13 de l’annexe 2 du Règlement.
4.5.2 Substances chimiques fabriquées ou importées en grandes quantités
Les déclarants qui fabriquent ou importent une substance chimique qui ne figure pas sur la Liste extérieure doivent présenter au ministre les renseignements prévus à l’annexe 6 du Règlement au moins 75 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
S’il s’agit d’une substance biochimique, le déclarant doit présenter, outre les renseignements prévus à l’annexe 6, ceux prescrits par les articles 1 à 4 de l’annexe 2 du Règlement et :
- a) si la substance biochimique est un acide nucléique, ceux qui sont prescrits par les articles 5 et 6 de l’annexe 2 du Règlement;
- b) si la substance biochimique a des propriétés enzymatiques, ceux qui sont prescrits par les articles 7 à 13 de l’annexe 2 du Règlement.
4.6 Exigences en matière de renseignements pour les substances chimiques inscrites subséquemment sur la Liste extérieure
Il est important de noter que si une substance chimique est inscrite sur la Liste extérieure après la présentation d’une DSN à l’annexe 5, le déclarant peut, conformément au paragraphe 8(2) du Règlement, aviser par écrit le Programme des SN que ces mêmes renseignements doivent être traités comme s’ils avaient été fournis en application de l’alinéa 7(1)b) du Règlement. Pour qu’une évaluation dans le cadre d’une DSN finale commence, l’avis doit aussi inclure les renseignements de l’article 10 de l’annexe 5 du Règlement si ceux-ci n’ont pas déjà été fournis. Dès que le Programme des SN reçoit les droits exigés (consulter le tableau des frais à la page Web des Droits pour les déclarations de substances nouvelles), il dispose d’un délai de 60 jours pour l’évaluation pour réexaminer la substance dans le cadre d’une DSN finale.
De plus, l’inscription d’une substance chimique sur la Liste intérieure peut nécessiter la présentation de données supplémentaires prescrites par les paragraphes 7(2) ou 7(3), si la substance est rejetée dans l’environnement aquatique en grande quantité ou le degré d’exposition du public est élevée (consulter la partie 4.4.3).

Description longue
Les déclarants qui fabriquent ou importent une nouvelle substance chimique autre que celles indiquées à l’article 5 du Règlement (c'est-à-dire une nouvelle substance chimique autre que celles décrites dans la figure 4-1) doivent fournir au ministre les renseignements de l’annexe appropriée avant de dépasser la quantité seuil qui s’applique et dans les délais prescrits pour cette annexe. La figure 4-2 illustre les délais prescrits et les renseignements à fournir pour ces substances chimiques :
- Pour une substance chimique/biochimique qui figure sur la Liste extérieure (article 7 du Règlement) :
- Présenter au ministre les renseignements prévus à l’annexe 41 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile.
- Présenter au ministre les renseignements prévus à l’annexe 52 du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
- Si la substance chimique est rejetée dans l’environnement aquatique en une quantité supérieure à 3 kg par jour par site (la moyenne devant être calculée sur une base mensuelle et après traitement des eaux usées) ou si le degré d’exposition du public à cette substance contenue dans un produit pourrait être élevé, présenter au ministre les renseignements supplémentaires sur les essais prescrits par les paragraphes 7(2) ou 7(3) du Règlement au moins 75 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 50 000 kg au cours d’une année civile.
- Pour une substance chimique/biochimique qui ne figure pas sur la Liste extérieure (article 8 du Règlement)3:
- Présenter au ministre les renseignements prévus à l’annexe 44 du Règlement au moins 5 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 100 kg au cours d’une année civile.
- Présenter au ministre les renseignements prévus à l’annexe 54 du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile.
- Présenter au ministre les renseignements prévus à l’annexe 64 du Règlement au moins 75 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
1 Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’une substance biochimique [consulter le sous-alinéa 7(1)a)(ii) du Règlement].
2 Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’une substance biochimique [consulter le sous-alinéa 7(1)b)(ii) du Règlement]. Aucun autre renseignement additionnel ne sera exigé, sauf si, selon le cas : a) la substance chimique est rejetée dans l’environnement aquatique en une quantité supérieure à 3 kg par jour par site – la moyenne devant être calculée sur une base mensuelle et après traitement des eaux usées [consulter le paragraphe 7(2) du Règlement]; b) le degré d’exposition du public à la substance contenue dans un produit pourrait être élévé [consulter le paragraphe 7(3) du Règlement].
3 Le ministre doit être avisé de l’inscription de la substance chimique ou biochimique sur la Liste extérieure si les renseignements visés au sous-alinéa 8(1)b)(i) du Règlement et à l’article 10 de l’annexe 5 ont été fournis avant son inscription [consulter le paragraphe 8(2) du Règlement].
4 Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’une substance biochimique [consulter les sous-alinéas 8(1)a)(ii), b)(ii) et c)(ii) du Règlement].
4.7 Déclaration des polymères
Comme pour la déclaration de substances chimiques et biochimiques, le Règlement prescrit des exigences en matière de renseignements spécialement adaptées à l’utilisation et à la quantité de polymères. Ces exigences sont énoncées dans les annexes au Règlement présentées dans l’appendice 2 du Document d’orientation. Pour faciliter la sélection de l’annexe appropriée pour la déclaration, un diagramme de décision est inclus ci-dessous (consulter la figure 4-3) et dans l’appendice 1 du Document d’orientation.
Avant d’utiliser les diagrammes, le tableau 1-1 et les parties 2.2, 3.3 et 3.4, 4.2.3, 4.7, 4.8 et 4.9 du Document d’orientation devraient être examinés afin de déterminer :
- si la substance nouvelle correspond à la définition d’un polymère au sens du Règlement (consulter la partie 3.3.1.2);
- si le nouveau polymère est une substance de catégorie spéciale (par exemple, destinée à la recherche et au développement ou confinée qui est intermédiaire limitée au site ou destinée à l’exportation; consulter la partie 3.4);
- si le nouveau polymère figure sur la Liste extérieure (consulter la partie 2.2);
- les quantités annuelles du nouveau polymère qui seront fabriqués ou importés au Canada (consulter le tableau 1-1 et les parties 4.2.3, 4.8 et 4.9);
- si le nouveau polymère satisfait à la définition des polymères ERR (consulter la partie 3.3.1.5);
- si le nouveau polymère est fabriqué uniquement à partir de monomères et de réactifs qui figurent sur la Liste intérieure ou sur la Liste extérieure (consulter la partie 4.7.1);
- si le polymère figurant sur la Liste extérieure ou le polymère fabriqué uniquement à partir de monomères et de réactifs qui figurent sur la Liste intérieure ou sur la Liste extérieure sera rejetée dans l’environnement aquatique en grande quantité ou le degré d’exposition du public sera élevée (consulter la partie 4.9.2).
Les parties suivantes ne s’appliquent qu’aux polymères fabriqués ou importés à une fin autre que celles de la catégorie spéciale décrite à la partie 3.4 du Document d’orientation.
4.7.1 Monomères et réactifs figurant sur la Liste extérieure et sur la Liste intérieure
Afin de déterminer si un polymère n’est pas un polymère à exigences réglementaires réduites (non-ERR) peut être considéré sous une annexe avec moins d’exigences en matière de renseignements, c’est-à-dire, sous l’annexe 10 au lieu de l’annexe 11 pour une quantité seuil de 10 000 kg, il faut vérifier si les monomères et les réactifs de cette substance figurent sur la Liste intérieure ou sur la Liste extérieure.
Pour déterminer la présence de monomères et de réactifs sur les parties publiques ou confidentielles de la Liste intérieure ou de la Liste extérieure, on peut interroger le Moteur de recherche de substances.
Les déclarants peuvent également envoyer au Programme des SN une demande de recherche dans la partie confidentielle (consulter la partie 2.3.1).
4.8 Exigences en matière de renseignements pour les polymères (consulter la figure 4-3)
4.8.1 Polymères à exigences réglementaires réduites et Polymères qui ne satisfont pas aux critères établis pour les polymères à exigences réglementaires réduites et qui sont fabriqués ou importés en faibles quantités
Les déclarants qui fabriquent ou importent un polymère doivent présenter au ministre les renseignements prévus à l’annexe 9 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile. Si cette substance est considérée comme un polymères ERR (consulter la partie 3.3.1.5), la DSN de l’annexe 9 est la dernière déclaration requise.
Si la substance est un biopolymère, le déclarant doit présenter, outre les renseignements prévus à l’annexe 9, ceux prescrits par les articles 1 à 3 de l’annexe 2 du Règlement.
4.9 Exigences en matière de renseignements pour les Polymères qui ne satisfont pas aux critères établis pour les polymères à exigences réglementaires réduites (consulter la figure 4-3)
Les parties 4.9.1 à 4.9.3 ne s’appliquent pas aux polymères qui satisfont aux critères des polymères ERR.
4.9.1 Polymères non-ERR figurant sur la Liste extérieure ou fabriqués à partir de réactifs figurant sur la Liste intérieure ou sur la Liste extérieure et qui sont fabriqués ou importés en grandes quantités
Les déclarants qui fabriquent ou importent un polymère non-ERR (consulter la partie 3.3.1.6) qui figure sur la Liste extérieure ou qui est fabriqué uniquement à partir de monomères ou de réactifs qui figurent sur la Liste intérieure ou sur la Liste extérieure doivent présenter au ministre les renseignements prévus à l’annexe 10 du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
Si la substance est un biopolymère, le déclarant doit présenter, outre les renseignements prévus à l’annexe 10, ceux prescrits par les articles 1 à 4 de l’annexe 2 du Règlement. Si le biopolymère est un acide nucléique, le déclarant doit aussi présenter les renseignements prescrits par les articles 5 et 6 de l’annexe 2 du Règlement.
Les paramètres de toxicité pour la santé humaine prévus à l’article 4 de l’annexe 10 du Règlement ne sont pas requis pour les polymères non-ERR en raison uniquement de la présence de l’un ou l’autre des groupes fonctionnels suivants :
- a) les aldéhydes dont la masse équivalente du groupe fonctionnel (MEGF, consulter la partie 3.3.1.8) est inférieure ou égale à 1 000 daltons;
- b) les éthers vinyliques à MEGF inférieure ou égale à 5 000 daltons;
- c) les acides sulfoniques à MEGF inférieure ou égale à 5 000 daltons.
4.9.2 Polymères rejetés dans l’environnement aquatique en grande quantité et/ou le degré d'exposition du public est élevé
Les déclarants qui fabriquent ou importent un polymère qui figure sur la Liste extérieure ou qui est fabriqué uniquement à partir de monomères ou de réactifs qui figurent sur la Liste intérieure ou sur la Liste extérieure et :
- qui est rejeté dans l’environnement aquatique en une quantité supérieure à 3 kg par jour par site (la moyenne devant être calculée sur une base mensuelle et après traitement des eaux usées);
- le degré d’exposition du public du polymère contenue dans un produit pourrait être élevé
doivent présenter au ministre les renseignements supplémentaires sur les essais prescrits par les paragraphes 11(2) ou 11(3) du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 50 000 kg au cours d’une année civile. Les renseignements supplémentaires requis sont indiqués dans les parties qui suivent.
Ces renseignements supplémentaires ne sont pas requis pour les polymères non-ERR en raison uniquement de la présence de l’un ou l’autre des groupes fonctionnels suivants :
- a) les aldéhydes à MEGF inférieure ou égale à 1 000 daltons;
- b) les éthers vinyliques à MEGF inférieure ou égale à 5 000 daltons;
- c) les acides sulfoniques à MEGF inférieure ou égale à 5 000 daltons.
4.9.2.1 Polymères rejetés dans l’environnement aquatique
Il incombe au déclarant de présenter, dans la DSN, les renseignements prescrits par l’alinéa 5g) de l’annexe 10 afin d’étayer son allégation selon laquelle cette substance n’est pas rejetée dans l’environnement aquatique en quantités supérieures à la limite indiquée plus haut. Ces renseignements devraient aussi inclure toutes les utilisations et quantités futures envisagées par les autres utilisateurs et une description des applications envisagées. La partie 6.6.5 du Document d’orientation présente davantage de renseignements concernant le calcul des rejets quotidiens dans le milieu aquatique.
Les représentants du Programme des SN évalueront cette information et s’il est déterminé que cette substance est rejetée dans l’environnement aquatique en quantités supérieures à celles indiquées plus haut, le déclarant devra présenter les renseignements supplémentaires prescrits par le paragraphe 11(2) du Règlement. Le Programme des SN indiquera au déclarant si la substance est assujettie à des exigences supplémentaires relatives aux renseignements mentionnées ci-dessous. Le déclarant peut présenter des renseignements supplémentaires pour étayer ses allégations et demander une réévaluation de la décision prise par le Programme des SN en communiquant avec la Ligne d’information de la gestion des substances. Le Programme des SN examinera et prendra en compte ces renseignements.
Conformément au paragraphe 11(2) du Règlement, les renseignements supplémentaires requis comprennent :
- a) les données provenant d’un essai de toxicité d’au moins 28 jours de doses répétées du polymère chez les mammifères par voie orale, cutanée ou par inhalation, selon le mode d’exposition le plus probable du public, et les renseignements suivants :
- (i) l’âge, le sexe, le nombre, l’espèce, la souche et la source des animaux testés,
- (ii) la voie d’administration du polymère et les conditions dans lesquelles l’essai est effectué,
- (iii) la posologie du polymère, le vecteur par lequel il est administré et sa concentration dans le vecteur;
- b) les données sur le pouvoir mutagène provenant d’un essai in vitro, avec et sans activation métabolique, pour déterminer la présence de mutations génétiques ou d’aberrations chromosomiques dans des cellules de mammifères.
4.9.2.2 Degré d'exposition du public d’un polymère contenu dans un produit
Il incombe au déclarant de présenter dans la DSN les renseignements prescrits par l’alinéa 5h) de l’annexe 10 afin d’étayer son allégation selon laquelle le public est peu exposé à la substance dans un produit. Le Programme des SN indiquera au déclarant si la substance est assujettie à des exigences supplémentaires relatives aux renseignements mentionnées ci-dessous. Le déclarant peut présenter des renseignements supplémentaires pour étayer ses allégations et demander une réévaluation de la décision prise par le Programme des SN en communiquant avec la Ligne d’information de la gestion des substances. Le Programme des SN examinera et prendra en compte ces renseignements.
Puisque l’exposition du public dépend d’un grand nombre de facteurs, un calcul permettant de déterminer ce qui constitue un « degré d’exposition élevé » ne peut être applicable à toutes circonstances, sans tomber dans une prudence extrême. Pour cette raison, le Programme des SN évalue au cas par cas le « degré d’exposition élevé ». À cette fin, il faut prendre en compte des facteurs comme le type d’utilisation, la durée et la fréquence de l’utilisation, la concentration de la substance dans un produit et les circonstances de l’exposition qui peuvent limiter l’exposition directe du public (par exemple, si la substance est chimiquement consommée pendant son utilisation ou si elle peut migrer depuis un produit).
Les produits de consommation contenant une substance à laquelle le degré d'exposition du public pourrait être élevé comprennent notamment le détergent à vaisselle, les produits de lessive, les savons, le papier hygiénique, les solutions de nettoyage, les encaustiques, les agents de polissage, les assainisseurs d’air, les peintures, les huiles, les graisses, les lotions corporelles et les encres.
S’il est déterminé que le degré d'exposition du public pourrait être élevé au polymère contenu dans un produit, le déclarant doit fournir les renseignements supplémentaires prescrits par le paragraphe 11(3) du Règlement. Conformément au paragraphe 11(3) du Règlement, les renseignements supplémentaires requis comprennent :
- a) les données provenant d’un essai de toxicité d’au moins 28 jours de doses répétées de polymère chez les mammifères administré par voie orale, cutanée ou par inhalation, selon le mode d’exposition le plus probable du public, et les renseignements suivants :
- (i) l’âge, le sexe, le nombre, l’espèce, la souche et la source des animaux testés,
- (ii) la voie d’administration de la substance et les conditions dans lesquelles l’essai est effectué,
- (iii) la posologie du polymère, le vecteur par lequel il est administré et sa concentration dans le vecteur;
- b) les données sur le pouvoir mutagène provenant d’un essai in vitro, avec et sans activation métabolique, pour déterminer la présence de mutations génétiques;
- c) les données provenant d’un essai in vitro, avec et sans activation métabolique, pour déterminer la présence d’aberrations chromosomiques dans des cellules de mammifères ou, si elles existent déjà, les données d’une étude in vivo chez les mammifères pour déterminer la présence d’aberrations chromosomiques qui, jumelées à des données établissant que le tissu en question a été exposé au polymère ou à ses métabolites, permettent l’évaluation du pouvoir clastogène in vivo.
4.9.3 Polymères non-ERR ne figurant pas sur la Liste extérieure et qui ne sont pas fabriqués uniquement à partir de réactifs figurant sur la Liste intérieure ou sur la Liste extérieure et qui sont fabriqués ou importés en grandes quantités
Les déclarants qui fabriquent ou importent un polymère non-ERR (consulter la partie 3.3.1.6) qui ne figure pas sur la Liste extérieure et qui contient un ou plusieurs réactifs qui ne figurent pas sur la Liste intérieure ni sur la Liste extérieure doivent présenter au ministre les renseignements prévus à l’annexe 11 du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
Si la substance est un biopolymère, le déclarant doit présenter, outre les renseignements prévus à l’annexe 11, ceux prescrits par les articles 1 à 4 de l’annexe 2 du Règlement. Si le biopolymère est un acide nucléique, le déclarant doit aussi présenter les renseignements prescrits par les articles 5 et 6 de l’annexe 2 du Règlement.
Les paramètres de toxicité pour la santé humaine prévus aux articles 5 à 10 de l’annexe 11 du Règlement ne sont pas requis pour les polymères non-ERR en raison uniquement de la présence de l’un ou l’autre des groupes fonctionnels suivants :
- a) les aldéhydes à MEGF inférieure ou égale à 1 000 daltons;
- b) les éthers vinyliques à MEGF inférieure ou égale à 5 000 daltons;
- c) les acides sulfoniques à MEGF inférieure ou égale à 5 000 daltons.

Description longue
Les déclarants qui fabriquent ou importent un nouveau polymère autre que ceux indiqués à l’article 6 du Règlement (c'est-à-dire un nouveau polymère autre que ceux décrits dans la figure 4-1) doivent fournir au ministre les renseignements de l’annexe appropriée avant de dépasser la quantité seuil qui s’applique et dans les délais prescrits pour cette annexe. La figure 4-3 illustre les délais prescrits et les renseignements à fournir pour ces polymères :
- Pour un polymère/biopolymère qui est considéré comme un polymère ERR (article 9 du Règlement) :
- Présenter au ministre les renseignements prévus à l’annexe 92 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile1.
- Pour un polymère/biopolymère qui n’est pas considéré comme un polymère ERR et qui figure sur la Liste extérieure ou dont tous les réactifs figurent sur cette liste ou sur la Liste intérieure (article 11 du Règlement) :
- Présenter au ministre les renseignements prévus à l’annexe 92 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile1.
- Présenter au ministre les renseignements prévus à l’annexe 103 du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
- Si le polymère est rejeté dans l’environnement aquatique en une quantité supérieure à 3 kg par jour par site (la moyenne devant être calculée sur une base mensuelle et après traitement des eaux usées) ou si le degré d’exposition du public à ce polymère contenue dans un produit pourrait être élevé, présenter au ministre les renseignements supplémentaires sur les essais prescrits par les paragraphes 11(2) ou 11(3) du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 50 000 kg au cours d’une année civile.
- Pour un polymère/biopolymère qui n’est pas considéré comme un polymère ERR et qui ne figure pas sur la Liste extérieure ou dont un ou plusieurs réactifs ne figurent pas sur cette liste ou sur la Liste intérieure (article 12 du Règlement) :
- Présenter au ministre les renseignements prévus à l’annexe 92 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile1.
- Présenter au ministre les renseignements prévus à l’annexe 114 du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
1Article 10 du Règlement.
2Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’un biopolymère [consulter l'alinéa 10b) du Règlement].
3Ces renseignements n’ont pas à être fournis à l’égard des polymères à exigences réglementaires réduites. Des exceptions sont prévues au paragraphe 11(5) du Règlement. Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’un biopolymère [consulter l'alinéa 11(1)b) du Règlement]. Aucun autre renseignement additionnel ne sera exigé, sauf si, selon le cas : a) le polymère est rejeté dans l’environnement aquatique en une quantité supérieure à 3 kg par jour par site – la moyenne devant être calculée sur une base mensuelle et après traitement des eaux usées [consulter le paragraphe 11(2) du Règlement]; b) le degré d’exposition du public au polymère contenu dans un produit pourrait être élevé [consulter le paragraphe 11(3) du Règlement].
4Ces renseignements ne sont pas exigés pour les polymères à exigences réglementaires réduites. Des exceptions sont prévues au paragraphe 12(3) du Règlement. Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’un biopolymère [consulter l'alinéa 12(1)b) du Règlement].
Partie 5. Déclaration de substances nouvelles (DSN)
Le paragraphe 81(1) de la Loi canadienne sur la protection de l’environnement (1999) [la Loi] interdit la fabrication ou l’importation de toute substance qui ne figure pas sur la Liste intérieure, sauf si le déclarant qui fabrique ou importe la substance a fourni les renseignements prescrits dans les délais prévus et a payé les droits prescrits (consulter le tableau des frais à la page Web des Droits pour les déclarations de substances nouvelles), et si le délai d'évaluation des renseignements est expirée ou si le programme y a mis fin plus tôt que prévu (partie 9.3.6). Les renseignements prescrits par le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [le Règlement] (consulter l’appendice 2) sont constitués de renseignements administratifs et techniques (consulter les parties 6.2 à 6.6).
Note : Afin que les déclarants évitent de produire des nouvelles données d’essai en utilisant des animaux, une personne autre que le déclarant peut fournir les renseignements prescrits à l’appui de la Déclaration de substances nouvelles (DSN) du déclarant, si cette autre personne dispose déjà des données d’essais prescrits, tels que décrits dans les scénarios suivant.
5.1 Déclarations concordantes
On parle de déclaration concordante lorsqu’un déclarant demande au Programme des substances nouvelles (SN) d’utiliser des renseignements déjà fournis par un autre déclarant pour la même substance. Ces renseignements sont notamment des exigences relatives aux essais ou des renseignements supplémentaires. Le déclarant qui fournit ces renseignements doit présenter une lettre d’autorisation au Programme des SN indiquant son numéro de référence de DSN ainsi que le nom du déclarant pour lequel il soumet ces renseignements, avec le numéro de référence de DSN de ce dernier, s’il est connu. S’il est déterminé que des dossiers sont concordants, les droits exigés peuvent être réduits (consulter la page Web des Droits pour les déclarations de substances nouvelles). Ce cas est différent de celui des soumissions par un Tiers fournisseur de renseignements (consulter la partie 5.2).
5.2 Soumissions par un Tiers fournisseur de renseignements (information confidentielle présentée par un tiers)
Il est possible de demander que tous les renseignements présentés au Programme des SN soient traités de manière confidentielle (consulter la partie 7). Si le déclarant n’a pas accès à des renseignements jugés confidentiels par le Tiers fournisseur de renseignements, ce dernier doit fournir directement au Programme des SN les renseignements confidentiels présentés à l’appui de la DSN, lesquels seront désignés comme une « soumission par un Tiers fournisseur de renseignements ».
Pour soumettre des renseignements dans le cadre d’une soumission par un Tiers fournisseur de renseignements, le déclarant doit entamer le processus de DSN en présentant :
- tous les renseignements administratifs (cases A.1 à A.15 du formulaire de DSN; consulter la partie 6.2);
- tous les renseignements sur l’exposition, incluant les exigences en matière de renseignements pour la fabrication, l’importation, l’utilisation, le transport, l’exposition, le rejet et l’élimination (partie E du formulaire de DSN; consulter la partie 6.6);
- toute autre information que le déclarant a en sa possession relativement à la substance.
La DSN doit aussi faire référence aux renseignements qui seront présentés par un Tiers fournisseur de renseignements. Lorsqu’un déclarant a entrepris un processus de DSN et a reçu un numéro de référence pour cette DSN, les renseignements confidentiels requis pour compléter la DSN doivent être présentés directement au Programme des SN par le Tiers fournisseur de renseignements en indiquant le numéro de référence de la DSN pour laquelle il présente les renseignements.
Si plusieurs entreprises fabriquent ou importent la même substance du même Tier fournisseur de renseignements, chaque déclarant doit présenter une DSN au Programme des SN et il est responsable du suivi des quantités de substances qu’il fabrique ou importe. Chaque DSN se verra attribuer un numéro de référence différent.
Si un Tiers fournisseur de renseignements a déjà présenté les renseignements confidentiels au sujet d’une substance à la demande d’un déclarant, il n’est pas nécessaire que ceux-ci soient présentés de nouveau par d’autres déclarants. Toutefois, le Tiers fournisseur de renseignements doit envoyer au Programme des SN une lettre d’autorisation qui permet de vérifier la concordance et l’utilisation de ces renseignements lors de sa présentation initiale de renseignements en tant que Tiers fournisseur de renseignements afin que puissent être complétés chacune des DSN subséquentes présentées par d’autres déclarants pour la même substance. Des réductions de tarif sont possibles dans ce cas (consulter la page Web des Droits pour les déclarations de substances nouvelles).
5.3 Déclarations consolidées
On parle de déclarations consolidées lorsqu’un déclarant présente simultanément de 2 à 6 DSN pour des substances de la même catégorie et qu’on utilise des renseignements techniques fournis pour une substance afin de satisfaire aux exigences en matière de renseignements techniques pour les autres substances. Dans ces cas, le Programme des SN attribue un numéro de référence de DSN distinct à chacune des substances visées par la déclaration consolidée, même si les DSN sont consolidées pour une évaluation commune des risques. Des réductions de tarif sont possibles pour ces cas (consulter la page Web des Droits pour les déclarations de substances nouvelles). Il est recommandé (mais non obligatoire) que les déclarants consultent le Programme des SN s’ils souhaitent simultanément déclarer un certain nombre de substances très semblables à l’occasion d’une déclaration consolidée en faisant une demande de Consultation avant déclaration CAD (consulter la partie 8.8) afin de s’assurer que les renseignements techniques fournis permettent de satisfaire aux exigences relatives au DSN pour toutes les substances concernées.
5.4 Production des données d’essai
Le Règlement prescrit des exigences en matière de renseignements techniques qui doivent être satisfaites en fournissant des données d’essai ou des demandes de dérogation. Le Programme des SN accepte l’utilisation de méthodes de rechange appropriées (aussi appelées Nouvelles approches méthodologiques [NAM]) afin de satisfaire à ces exigences en matière de renseignements techniques.
Lors de la production des données d’essai, il faut tenir compte des conditions à respecter et des procédures à suivre et de leur conformité aux Lignes directrices (LD) de l’Organisation de coopération et de développement économiques (OCDE) pour les essais dans leurs versions à jour au moment de la production desdites données (consulter la partie 8.1).
De plus, certaines données d’essai doivent être conformes aux Bonnes pratiques de laboratoire en vigueur au moment de leur production (consulter la partie 8.3.1).
La partie 8 du Document d’orientation décrit les protocoles et pratiques de laboratoire recommandés par le Programme des SN pour la production de données expérimentales. Les méthodes de rechange qui peuvent être utilisées pour satisfaire à une exigences en matière de renseignements techniques sont décrites dans la partie 8.4.
Lorsque les déclarants fournissent des données d’essai afin de satisfaire à une exigence en matière de renseignements techniques, ils doivent présenter des rapports d’essai complets, et non des sommaires. Il faut s’assurer que le nom de la substance ou le nom commercial indiqué dans le rapport d’essai présenté correspondent à celui ou à ceux de la DSN. Il faut également indiquer les valeurs des données d’essai et leurs conditions dans les parties B.1, B.2 et B.3 du formulaire de DSN (consulter la partie 6.3) même si lesdites données apparaissent dans les rapports d’essai.
Une copie de chaque publication scientifique citée en référence doit être fournie (le cas échéant). Si des estimations ou des modèles informatiques sont utilisés, il faut fournir des renseignements sur le modèle utilisé (par exemple, la version du logiciel), ainsi que les données d’entrée et les résultats du modèle afin de permettre au Programme des SN d’évaluer ces données (consulter la partie 8.4.4).
Il n’est pas nécessaire de présenter les données d’essai antérieurement jointes à une DSN, une demande de CAD ou un avis en vertu de l’article 70 de la Loi déjà présentés. Il faut toutefois présenter le numéro de référence exact (consulter le code « P » dans la partie 6.1.2).
La partie 8.7 du Document d’orientation décrit les conditions dans lesquelles des dérogations pour des renseignements prescrits peuvent être autorisées. L’appendice 6 en présente des exemples.
5.4.1 Nanomatériaux
Les directives et LD spécifiques de l’OCDE visant les nanomatériaux ont été publiées en ligneNote de bas de page 13, incluant, par exemple, les directives sur la préparation des échantillons et de la dosimétrie pour les nanomatériaux fabriqués ainsi que les LD adoptées. En outre, on s’attend à ce que de nouvelles directives et LD associées aux nanomatériaux continueront d’être publiées dans les prochaines années. Si, pour un paramètre donné, l’OCDE n’avait publié aucune LD, une CAD devrait être envisagée pour s’assurer de la pertinence des méthodes proposées.
5.5 Exigences relatives à la tenue des dossiers
Selon l’article 13 du Règlement, un déclarant qui doit fournir des renseignements exigés par le Règlement au ministre de l’Environnement ou au Programme des SN doit aussi conserver un exemplaire de ces renseignements et de toutes les données probantes à son siège social au Canada ou au bureau principal de son représentant au Canada. Il doit conserver ces renseignements et les données probantes pendant les 5 années qui suivent la présentation de ces renseignements.
Partie 6. Formulaire de Déclaration de substances nouvelles
Le formulaire de Déclaration de substances nouvelles (DSN) est conçu pour faciliter le respect des exigences du Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [le Règlement]. Il comporte 5 parties :
- Partie A : Exigences relatives aux renseignements administratifs et liés à la dénomination de la substance;
- Partie B : Exigences relatives aux renseignements techniques;
- Partie C : Exigences supplémentaires en matière de renseignements sur les substances biochimiques et les biopolymères;
- Partie D : Exigences relatives aux renseignements supplémentaires;
- Partie E : Renseignements sur l’exposition humaine et environnementale (connus et prévus).
De plus, le formulaire de DSN comprend 4 appendices (I à IV) :
- Appendice I : Formulaire de paiement de droits pour les substances nouvelles;
- Appendice II : Codes d’utilisation fonctionnelle des substances;
- Appendice III : Codes d’application;
- Appendice IV : Codes de données, pièces jointes et renseignements confidentiels.
Une DSN complète doit présenter les renseignements précis exigés aux parties A, B, C et E, notamment toutes les données d’essai, les rapports de laboratoire, les justifications des demandes de dérogation et les autres pièces jointes exigées par le Règlement. Les autres renseignements doivent être présentés à la partie D. L’appendice I aide à déterminer le calcul du droit à payer pour chaque DSN.
Si un formulaire de DSN est incomplet ou s’il n’a pas été rempli correctement, la demande peut être retournée au déclarant. Le délai d’évaluation ne débutera que lorsque le formulaire est complet et rempli correctement (consulter la partie 9.2.1).
Le déclarant doit présenter dans une pièce jointe tout renseignement qu’il ne peut inscrire dans la case appropriée du formulaire de DSN.
Selon le paragraphe 14(2) du Règlement, tous les renseignements doivent être présentés en français ou en anglais. Il est possible de transmettre ces renseignements électroniquement par courriel, sur un support de stockage (par exemple, une clé USB) ou en se connectant au système de Gestion de l'information du guichet unique (GIGU) d’Environnement et Changement climatique Canada, en faisant la déclaration au moyen du Formulaire de DSN en ligne. Le Programme des substances nouvelles (SN) n’accepte pas les fichiers ZIP, RAR ou tout autre type de programme de compression à l’intérieur d’un courriel ou sur un dispositif de stockage (par exemple, une clé USB). Deux exemplaires sur papier de tous les renseignements présentés en application du Règlement peuvent également être soumis à l’une des adresses de la Ligne d’information de la gestion des substances.
Le Programme des SN confirmera la réception d’une DSN et attribuera un numéro de référence de DSN (consulter la partie 9.3.2) qui sera utilisé pour toute correspondance ultérieure relative à cette déclaration.
Les formulaires de DSN peuvent être reproduits aussi souvent que nécessaire. Une copie électronique du Formulaire de Déclaration de substances nouvelles peut être obtenue à partir du site Web du Programme des SN ou en s’adressant à la Ligne d’information de la gestion des substances.
6.1 Codes de données, pièces jointes et renseignements confidentiels
En plus de la liste des renseignements obligatoires, les parties B et C du formulaire de DSN contiennent les colonnes supplémentaires suivantes : Exigences de l’annexe, Code de données, Valeur et conditions, Numéro de la pièce jointe, et Renseignements confidentiels. L’utilité de chacune de ces colonnes est expliquée ci-dessous. Cette explication se trouve également à l’appendice IV du formulaire de DSN.
6.1.1 Exigences de l’annexe
Cette colonne permet au déclarant de déterminer rapidement pour laquelle des annexes les renseignements doivent être fournis. Les notes en bas de page donnent des recommandations supplémentaires sur les exceptions et conditions associées à certains éléments de données. Il est important de noter que si une substance fait l’objet d’une déclaration pour la première fois sous une annexe de numéro élevé, tous les renseignements prescrits par les annexes de numéro inférieur sont aussi exigés.
6.1.2 Code de données
Un code de données est un indice qui indique si des données sont fournies, le type de données fournies ou si une demande de dérogation à l’obligation de fournir des renseignements est présentée. Les codes de données (et leur remarque explicative) sont :
- D = données d’essai de la substance déclarée, protocole d’essai recommandé : ce code est utilisé lorsque les données fournies sur la substance déclarée ont été obtenues en suivant les protocoles compatibles avec ceux des tableaux 8-1 à 8-4. Il faut employer ce code même si les renseignements sont fournis pour satisfaire aux exigences relatives aux renseignements supplémentaires des annexes (consulter la partie 6.5);
- A = autres procédés : ce code est utilisé lorsque les données fournies ont été obtenues en utilisant un autre protocole d’essai, des données de substitution ou des modèles de relations quantitatives structure-activité [RQSA] (consulter la partie 8.4). Il faut employer ce code même si les renseignements sont fournis pour satisfaire aux exigences relatives aux renseignements supplémentaires des annexes (consulter la partie 6.5);
- W = demande de dérogation : ce code est utilisé lorsqu’une dérogation à l’obligation de fournir des renseignements est demandée en application du paragraphe 81(8) de la Loi canadienne sur la protection de l’environnement (1999) [la Loi]. Les demandes de dérogation doivent être accompagnées des justifications nécessaires pour satisfaire à l’un des critères indiqués dans le paragraphe susmentionné de la Loi (consulter la partie 8.7);
- N/A = sans objet : ce code est utilisé lorsque le Règlement précise qu’il n’est pas obligatoire de fournir des renseignements dans certaines conditions. Par exemple, il n’est pas nécessaire de fournir des données d’un essai de présélection sur l’adsorption et la désorption, si la solubilité dans l’eau est inférieure à 200 μg/L. Ce code ne doit pas être utilisé comme abréviation de : « non disponible »;
- NR = non requis : ce code est utilisé lorsque les renseignements n’ont pas été fournis et qu’ils ne sont pas exigés pour une annexe spécifique du Règlement;
- P = numéro de DSN précédent, numéro de Consultation avant déclaration (CAD) ou avis en vertu de l’article 70 de la Loi : ce code est utilisé pour indiquer que le déclarant a déjà fourni les renseignements dans une DSN précédente, une CAD précédente ou un avis en vertu de l’article 70 de la Loi. Le numéro de référence approprié de la DSN, de la CAD ou d’avis selon l’article 70 doit être indiqué dans la colonne des pièce jointes.
6.1.3 Valeur et conditions
Même si le déclarant doit présenter des données physico-chimiques complètes dans les rapports d’essai (sauf pour l’état physique ou si la substance déclarée est conçue pour se disperser dans l’eau), il doit inscrire la valeur et les conditions dans l’espace approprié du formulaire. Ces renseignements aideront le déclarant à organiser ses données afin de les utiliser dans une demande de dérogation à l’obligation de fournir des renseignements, à justifier les cas pour lesquels des données ne sont pas exigibles et à discuter des déclarations avec les représentants du Programme des SN.
6.1.4 Numéro de pièce jointe
Le déclarant doit indiquer un numéro de référence distinct à chacune des pièces jointes (par exemple, pièce jointe 6) de manière à les repérer facilement dans la DSN. Les pièces jointes comprennent notamment les justifications des demandes de dérogation, les rapports de procédés expérimentaux, les rapports de résultats d’essais, les justifications de l’utilisation de données de substitution, les résultats et la validation des modélisations, les raisons pour lesquelles les renseignements sont considérés comme étant « sans objet » ou les renseignements supplémentaires relatifs à une demande de confidentialité.
6.1.5 Renseignements confidentiels
Le déclarant doit cocher la case appropriée pour indiquer que les renseignements fournis sont jugés confidentiels (cocher la case « Oui » si les renseignements sont jugés confidentiels et la case « Non » si ils ne le sont pas). Le Programme des SN considère que les renseignements fournis ne sont pas jugés confidentiels si aucune des cases n’est cochée. Si les renseignements fournis sont confidentiels, le déclarant doit fournir dans la DSN les renseignements additionnels présentés à la partie 7.2 du Document d’orientation.
6.2 Exigences relatives aux renseignements administratifs et liés à la dénomination de la substance
Les différentes exigences relatives aux renseignements administratifs et liés à la dénomination de la substance sont expliquées ci-dessous afin d’aider le déclarant à remplir le formulaire de DSN. Le paragraphe 14(1) du Règlement indique les renseignements nécessaires pour s’acquitter des exigences administratives propres à une DSN.
Les cases A.1 à A.15 du formulaire de DSN doivent être remplies pour toutes les substances assujetties à une annexe du Règlement.
6.2.1 Page de signature, demandes de confidentialité et ententes (case A.1)
6.2.1.1 Représentant du fabricant ou de l’importateur résident de la substance identifiée dans les cases A.2 ou A.3 (déclarant)[case A.1.1]
La personne nommée dans la case A.1.1 est le déclarant résident qui fabrique ou importe la substance déclarée au Canada (identifié à la case A.2) ou le déclarant non résident (identifié à la case A.3). Le déclarant doit signer et dater l’attestation à la case A.1.1. La signature sert à certifier que les renseignements fournis dans la DSN sont précis et complets, à la connaissance du déclarant.
6.2.1.2 Agent de l’importateur non-résident de la substance identifiée dans la case A.4 (agent canadien) [case A.1.2]
La case A.4 doit être remplie si l’importateur n’est pas un résident canadien et qu’il faut désigner un « agent canadien » pour l’« importateur non-résident ». L’agent doit signer à la case A.1.2 (consulter la partie 6.2.4).
6.2.1.3 Énoncé des responsabilités du fabricant en sous-traitance identifiée dans la case A.7 [case A.1.3]
Dans le cas d’une substance déclarée qui serait fabriquée en sous-traitance au Canada (le fabricant produit la substance au profit du déclarant), le fabricant en sous-traitance doit signer à la case A.1.3 (consulter la partie 6.2.7). Une attestation signée par le fabricant en sous-traitance indique qu’il accepte les responsabilités en matière d’observations de la loi liées à la fabrication de la substance déclarée et à tout rejet accidentel de celle-ci.
6.2.1.4 Droits versés (s’il y a lieu) [case A.1.4]
Le déclarant doit indiquer le montant des droits versés en application du Règlement sur les droits concernant les substances nouvelles [RDSN] (consulter le tableau des frais à la page Web des Droits pour les déclarations de substances nouvelles). Il doit également remplir l’appendice I du formulaire de DSN et le joindre à la DSN.
En général, des droits s’appliquent aux substances assujetties à une déclaration. Néanmoins, veuillez noter que le RDSN ne s’applique pas aux substances biochimiques, aux biopolymères, aux substances destinées à la recherche ou pour les substances qui sont uniquement destinées à une utilisation dans des produits réglementées aux termes de toute autre loi fédérale, notamment la Loi sur les aliments et drogues (LAD), la Loi sur les pêches et la Loi sur la santé des animaux.
6.2.1.5 Demande de confidentialité et justification (case A.1.5)
Le déclarant doit également cocher la case appropriée pour indiquer si les renseignements sont confidentiels ou non. S’ils sont jugés en tant que Renseignements commerciaux confidentiels (RCC), le déclarant doit présenter, dans la DSN, les renseignements supplémentaires décrits en détail dans la partie 7.2 du Document d’orientation. Une justification distincte est demandée pour l’identité de la substance.
Le fait de cocher la case entraîne ce qui suit :
- Nom du fabricant ou de l’importateur : le lien entre l’identité de la substance et l’entreprise ou les personnes indiquées dans l’une ou dans l’ensemble des cases A.1.1, A.1.2, A.1.3, A.2, A.3, A.4, A.5 et A.6 est confidentiel;
- Activité avec la substance (située dans la case A.12) : le fait que l’entreprise identifiée dans la case A.2 fabrique ou importe la substance à l’endroit indiqué dans la case A.7, A.8 ou à n’importe quel endroit indiqué dans n’importe quelle pièce jointe du formulaire de DSN est confidentiel;
- Utilisations envisagées de la substance (situées dans la case A.15.1) : les utilisations de la substance que le déclarant envisage entreprendre, ainsi que les renseignements de l’une ou l’ensemble des cases A15.2, A15.3, A15.4, A15.5, A15.6, sont confidentielles;
- Quantité de la substance (située dans la case A.10) : la quantité de substance que le déclarant prévoit dépasser, tel qu’indiqué à la case A.10, ainsi que la date prévue du dépassement, telle qu’indiquée à la case A.11, sont confidentielles;
- Identité de la substance (si elle est cochée, remplir la case A.18) : l’identité de la substance indiquée dans les cases A.16 et A.17 est confidentielle, ainsi que les renseignements de l’une ou l’ensemble des cases A.19, A.20, A.21, A.22, A.23, A.24, A.25, A.26, A.27 et A.28. Toute demande relative à la confidentialité doit être accompagnée des renseignements supplémentaires indiqués à la partie 7.2.2 et dans la partie A5.4 du Document d’orientation.
De plus, une entreprise qui demande que les renseignements déposés ci-dessus soient considérés comme des renseignements confidentiels doit décrire pourquoi elle fait une telle demande en sélectionnant le ou les critères suivants qui s’appliquent à la case A.1.5 :
- Il s’agit d’un secret industriel de l’auteur de la demande;
- Il s’agit de renseignements de nature financière, commerciale, scientifique ou technique qui sont toujours traités de façon confidentielle par l’auteur de la demande;
- On peut raisonnablement s’attendre à ce que leur divulgation entraîne des pertes ou des gains financiers importants ou encore à ce qu’elle soit préjudiciable à la position concurrentielle de l’auteur de la demande;
- On peut raisonnablement s’attendre à ce que leur divulgation nuise à des négociations d’ordre contractuel ou autre menées par l’auteur de la demande.
6.2.1.6 Entente de divulgation limitée (case A.1.6)
Cette case n’est pas obligatoire. Elle permet à Environnement et Changement climatique Canada à divulguer les renseignements concernant la substance, y compris les renseignements pour lesquels une demande de confidentialité est présentée, aux divisions de gestion des produits chimiques de l’Agence de protection environnementale des États-Unis (United States Environmental Protection Agency - US EPA), de l’Agence européenne des produits chimiques (European Chemicals Agency - ECHA) ou du Système australien d’introduction des produits chimiques industriels (Australian Industrial Chemicals Introduction Scheme - AICIS). La case appropriée doit être cochée afin d’autoriser la divulgation des renseignements avec l’un des organismes susmentionnés.
6.2.1.7 Entente de partage de renseignements (case A.1.7)
Il peut survenir qu’une substance particulière déclarée ne soit pas inscrite sur la Liste intérieure pour l’une ou plusieurs des raisons suivantes :
- La substance ne répond pas à tous les critères énoncés par l’article 87 de la Loi;
- La substance fait l’objet de mesures de gestion des risques;
- L’évaluation de la substance ou le traitement de la DSN n’est pas terminé.
Dans de tels cas, toute autre personne souhaitant fabriquer ou importer la substance en question doit présenter une DSN complète. Afin de réduire la répétition des essais et les dépenses que nécessite la production des renseignements pour l’élaboration d’une DSN, les responsables du Programme des SN donnent aux déclarants d’une substance commune l’occasion d’échanger des données dans le cadre d’une Entente de partage de renseignements (EPR). Aucun droit n’est associé à l’utilisation d’une EPR.
Une EPR est enclenchée lorsqu’un déclarant fournit au Programme des SN :
- la documentation attestant avoir l’intention de fabriquer ou d’importer une substance particulière;
- l’autorisation de divulguer le nom, l’adresse et le numéro de téléphone de la personne-ressource technique de l’entreprise à toute autre entreprise qui satisfait également à ces 2 critères.
La documentation indiquant l’intention de fabriquer ou d’importer une substance peut être soit une DSN, soit une demande de recherche dans la partie confidentielle (consulter la partie 2.3.1). Après avoir reçu et accepté cette documentation, les responsables du Programme des SN cherchent d’éventuels candidats à une EPR et, s’ils en trouvent, fournissent simultanément à chaque déclarant le nom, l’adresse et le numéro de téléphone de la personne-ressource technique de l’autre ou des autres entreprises. La participation des responsables du Programme des SN s’arrêtera à ce point, et les déclarants pourront alors négocier une EPR.
Si un déclarant accepte de contracter une EPR, la case d’autorisation (case A.1.7) doit être cochée.
6.2.2 Siège social du fabricant résident ou de l’importateur résident (principale adresse d’affaires au Canada) [case A.2]
Un déclarant qui réside au Canada et qui fabrique ou importe une substance au Canada doit inscrire les renseignements demandés dans la case A.2 :
- Le nom et le titre de la personne-ressource;
- Numéro d’entreprise fédéral du Canada;Note de bas de page 14
- Le nom et l’adresse du fabricant ou de l’importateur;
- Le numéro de téléphone (y compris l’indicatif régional) ainsi que l’adresse courriel du fabricant ou de l’importateur de la substance déclarée;
- La langue de correspondance préférée.
Si l’importateur ou le fabricant ne se trouve pas au Canada, passer à la case A.3.
6.2.3 Siège social de l’importateur non-résident (case A.3)
Lorsqu’une entreprise étrangère ou un « importateur non-résident » est l’« importateur officiel » figurant sur la Déclaration en détail commerciale utilisée par l’Agence des services frontaliers du Canada et que cette entreprise ou cet importateur :
- possède le statut d’« importateur canadien »;
- possède le statut d’« importateur officiel »;
- importe la substance déclarée au Canada,
cette entreprise étrangère ou cet « importateur non-résident » doit laisser la case A.2 vide et inscrire les renseignements demandés dans la case A.3 :
- Le nom et le titre de la personne-ressource de l’« importateur non-résident »;
- Les adresses municipale et postale, les numéros de téléphone (y compris l’indicatif régional) ainsi que l’adresse courriel de l’« importateur non-résident » pour la substance déclarée;
- La langue de correspondance préférée.
Lorsque le déclarant est un « importateur non-résident », il doit désigner une personne, en vertu de l’alinéa 14(1)b) du Règlement, une personne résidant au Canada qui est autorisée à agir au nom du déclarant en tant que « agent canadien » (consulter les parties 1.4.2 et 6.2.4).
6.2.4 Agent canadien de l’importateur non-résident (nécessaire si la case A.3 est remplie) [case A.4]
Comme susmentionné, aux termes du paragraphe 14(3) du Règlement, si la personne qui fournit les renseignements au titre du Règlement ne réside pas au Canada, elle doit désigner, en application de l’alinéa 14(1)b) du Règlement, une personne autorisée à agir en son nom à titre d’ « agent canadien » qui réside au Canada.
Par conséquent, des renseignements doivent être fournis sur l’ « agent canadien » lorsqu’un « importateur non-résident » (consulter la partie 6.2.3) est l’« importateur officiel » selon la documentation de Douanes Canada pour la substance déclarée importée.
Lorsqu’il faut un « agent canadien », les renseignements suivants doivent être fournies :
- La signature de l’ « agent canadien » à la case A.1.2;
- Tous les renseignements de l’« importateur non-résident » dans la case A.3 (consulter la partie 6.2.3);
- Le nom, le titre, le numéro d’entreprise fédéral du Canada, le nom de l’entreprise, l’adresse, le numéro de téléphone (y compris l’indicatif régional), l’adresse courriel et la langue de correspondance préférée de l’ « agent canadien » dans la case A.4.
Si un « importateur non-résident » fournit les renseignements en application du Règlement, mais ne fournit pas les renseignements exigés sur l’ « agent canadien », la DSN sera jugée incomplète et retournée.
Si, pour la même substance déclarée, l’« importateur non-résident » a plus d’un client canadien, il n’est pas nécessaire de fournir une DSN pour chaque client, pourvu que l’« importateur non-résident » soit considéré comme l’« importateur officiel » pour toutes les marchandises expédiées à ses clients. L’ « agent canadien » et l’« importateur non-résident » devraient assurer le suivi des quantités d’importation annuelles afin de veiller à ce que les obligations subséquentes concernant la déclaration de quantités supérieures soient remplies.
Le déclarant peut demander de recevoir une copie de toute la correspondance. Cependant l’ « agent canadien » est tenu légalement de recevoir tous les avis et la correspondance envoyés relativement à la DSN et de conserver un exemplaire de celle-ci, incluant les renseignements confidentiels (sauf dans le cas où un Tiers fournisseur de renseignements est impliqué), ainsi que l’ensemble de la correspondance et des données à l’appui se rapportant à la DSN pendant une période de 5 ans suivant la fin de l’année durant laquelle les renseignements sont communiqués (consulter l’article 13 du Règlement).
6.2.5 Tiers fournisseur de renseignements (nécessaire seulement si les renseignements sont soumis par un tiers) [case A.5]
Si une personne qui n’est pas le déclarant (un tiers) fournit une partie ou la totalité des renseignements techniques confidentiels contenus dans le formulaire de DSN, il faut inscrire dans la case A.5 le nom et le titre, l’adresse, le numéro d’entreprise fédéral du Canada (le cas échéant), le nom de l’entreprise, le numéro de téléphone (y compris l’indicatif régional), l’adresse courriel et la langue de correspondance préférée du Tiers fournisseur de renseignements.
6.2.6 Personne-ressource technique (case A.6)
Il faut fournir le nom d’une personne-ressource technique qui connaît bien le contenu de la DSN et qui peut aider à résoudre les problèmes causés par le fait que certains renseignements sont ambigus, incomplets ou absents. Cette personne doit être identifiée en donnant son nom, son titre, le nom de son entreprise ainsi que le numéro d’entreprise fédéral du Canada (le cas échéant), son adresse, son numéro de téléphone (y compris l’indicatif régional), son adresse courriel et sa langue de correspondance préférée. Il n’est pas nécessaire que la personne-ressource technique réside au Canada, mais la nature et le contenu de la DSN doivent lui être familiers.
6.2.7 Site de fabrication au Canada proposé, y compris les renseignements sur le fabricant en sous-traitance (case A.7)
Dans le cas d’une substance déclarée qui est fabriquée au Canada, le déclarant doit indiquer le nom de la personne-ressource et son titre, le numéro d’entreprise fédéral du Canada, le nom de l’entreprise et l’adresse municipale du site de fabrication au Canada pour la substance déclarée. S’il y a plus d’un site de fabrication, tous les emplacements doivent être précisés dans une pièce jointe.
Dans le cas d’une substance déclarée qui serait fabriquée en sous-traitance au Canada (le fabricant produit la substance au profit du déclarant), le déclarant doit fournir les renseignements suivants :
- Le nom et le titre de la personne-ressource, le nom de l’entreprise et le numéro d’entreprise fédéral du Canada du fabricant en sous-traitance;
- L’adresse et le numéro de téléphone (y compris l’indicatif régional) ainsi que l’adresse courriel du fabricant en sous-traitance;
- L’énoncé des responsabilités signé par le fabricant en sous-traitance (consulter la partie 6.2.1.3);
- Tous les renseignements requis concernant l’installation de fabrication, tels que spécifiés à la partie 6.6.
6.2.8 Le port d’entrée au Canada proposé (cases A.8)
Dans le cas d’une substance importée au Canada, le déclarant doit indiquer le port d’entrée de la substance au Canada, au minimum la ville et la province d’entrée. S’il y a plus d’un port d’entrée, tous doivent être indiqués sur une pièce jointe.
Veuillez consulter la Liste des services de l’Agence des services frontaliers du Canada pour le répertoire des ports d’entrée.
6.2.9 Numéro de Déclaration de substances nouvelles antérieur / numéro de Consultation avant déclaration ou autres mécanismes de consultation établis (case A.9)
Toutes les annexes prescrivent au déclarant de fournir les numéros de référence de DSN, les numéros de CAD ou les numéros des autres mécanismes de consultation établis antérieurs, si de tels numéros ont été attribués, et la date (AAAA-MM-JJ) à laquelle ces renseignements ont été fournis.
6.2.10 Quantité (case A.10)
Le déclarant doit indiquer la quantité seuil annuelle qui a entraîné l’obligation de déclarer.
Un déclarant peut, s’il le souhaite, choisir de présenter d’emblée l’annexe prévue pour la déclaration qui a le numéro le plus élevé, à condition que les quantités prescrites les plus faibles pour l’annexe de numéro le plus bas soient respectées et que la DSN soit présentée dans les délais prévus pour l’annexe de numéro le plus élevé. Par exemple, advenant qu’un déclarant souhaite présenter une déclaration finale pour une substance chimique ne figurant pas sur la Liste extérieure (annexe 6), et qu’il n’a présenté aucune des annexes de numéro plus bas précédemment, celui-ci doit respecter la quantité prescrite de l’annexe 4 (100 kg/an) jusqu’à ce que la période d’évaluation pour la déclaration au titre de l’annexe 6 soit complétée.
6.2.11 Date à laquelle la quantité inscrite à la case A.10 devrait être dépassée (case A.11)
Le déclarant doit indiquer à la case A.10, dans le format AAAA-MM-JJ, la date à laquelle la quantité seuil indiquée à la case A.10 devrait être dépassée.
6.2.12 Activité (case A.12)
Le déclarant doit indiquer si la substance déclarée sera fabriquée ou importée au Canada.
6.2.13 Type de substance (case A.13)
Le déclarant doit cocher les cases appropriées pour indiquer le type de substance (substance chimique, substance biochimique, polymère, biopolymère, substance de catégorie spéciale, nanomatériau, UVCBNote de bas de page 15, substance figurant sur la Liste extérieure). S’il s’agit d’un polymère, il faut cocher d’autres cases sur les critères relatifs aux réactifs et aux polymères à exigences réglementaires réduites (ERR) (consulter la partie 3.3.1.5). Si la substance déclarée figure sur la partie confidentielle de la Liste extérieure, le déclarant doit également fournir le numéro d’identification confidentielle (si connue).
6.2.14 Numéro de l’annexe (case A.14)
Il faut cocher la case appropriée pour indiquer le numéro de l’annexe fournie qui correspond au type de substance déclarée. Les DSN pour les substances déclarées qui sont des substances biochimiques ou des biopolymères doivent aussi contenir des renseignements spécifiés à l’annexe 2 du Règlement. Dans ces cas, les cases pour les numéros de l’annexe déclarée et de l’annexe 2 devraient être cochées.
6.2.15 Description des utilisations envisagées de la substance (cases A.15.1 à A.15.6)
Toute utilisation envisagée de la substance déclarée doit être inscrite dans la case A.15.1. Des renseignements supplémentaires sont également requis au titre de certaines annexes; ils devraient être fournis dans la partie E.2 du formulaire de DSN (consulter la partie 6.6). S’il est connu, le code d’utilisation fonctionnelle et le code d’application précisé aux appendices II et III du formulaire de DSN doit être inscrit aux cases A.15.2 et A.15.3.
Dans la case A.15.4 s’il est connu, le code du Système de classification des industries de l'Amérique du Nord (SCIAN) de cette substance doit être inscrit.
Dans la case A.15.5, le déclarant doit indiquer s’il prévoit que la substance sera fabriquée ou importée :
- uniquement aux fins d’utilisation dans des produits réglementés en vertu de la LAD;
- aux fins d’utilisation industrielle, commerciale ou par les consommateurs autres qu’aux fins d’utilisation dans des produits réglementés en vertu de la LAD;
- aux fins d’utilisation dans des produits réglementés en vertu de la LAD et dans des produits industriels, commerciaux ou de consommation (double usage).
S’il est prévu que la substance sera fabriquée ou importée conformément aux deux derniers scénarios ci-dessus, le déclarant doit présenter sa DSN avec les droits appropriés (consulter le tableau des frais à la page Web des Droits pour les déclarations de substances nouvelles).
Pour plus de renseignements concernant la déclaration des substances utilisées dans les produits réglementés par la LAD, veuillez communiquer avec l’Unité des évaluations environnementales de Santé Canada par téléphone au 1-866-996-9913 ou au 1-613-948-3591 ou par courriel à eau-uee@hc-sc.gc.ca.
Dans la case A.15.6, le déclarant doit aussi indiquer si la substance nouvelle vise à remplacer une autre substance actuellement sur le marché. Il doit également indiquer la dénomination et le numéro d’enregistrement du Chemical Abstracts Service (CAS) de la substance remplacée ainsi que le(s) avantage(s) ou le(s) motif(s) du remplacement (par exemple, remplace une substance toxique, atténue les changements climatiques ou se substitue à une substance appauvrissant la couche d’ozone).
6.2.16 Numéro d’enregistrement du Chemical Abstracts Service (case A.16)
Il est obligatoire pour identifier la substance déclarée de mentionner dans toutes les annexes au Règlement le numéro d’enregistrement CAS si un tel numéro peut être attribué. Il est aussi requis par l’annexe 2 du Règlement que le numéro de classification des enzymes, s’il existe, soit mentionné pour les substances biochimiques qui ont une capacité d’action enzymatique (consulter la partie 6.4.2.4).
« Peut être attribué » renvoie à la capacité du CAS à attribuer un numéro de registre à la substance en question. Dans le cas où un numéro d’enregistrement CAS n’a pas été attribué, le déclarant doit fournir une justification écrite décrivant la raison pour laquelle un numéro d’enregistrement CAS n’a pas été attribué à la substance. Si un numéro d’enregistrement CAS n’est pas attribué, une demande de confidentialité doit être présentée (consulter la partie 6.2.1.5).
Si la DSN ne comporte pas de numéro d’enregistrement CAS (ou le motif de son absence), celle-ci sera jugée incomplète et un avis indiquant qu’il manque des renseignements sera communiqué. Le délai d'évaluation ne commencera que lorsque l’ensemble des renseignements prescrits a été reçu et accepté.
Le numéro d’enregistrement CAS le plus précis disponible doit être fourni pour la substance déclarée.
Par exemple, pour les substances biochimiques, on peut distinguer les numéros d’enregistrement CAS pour α-amylase selon l’organisme source : 9001-19-8 (α-amylase, Aspergillus oryzae) par rapport à 75496-59-2 (α-Amylase [glande salivaire de souris avec réduction de l’isoenzyme]).
Par exemple, pour les substances chimiques, le numéro d’enregistrement CAS 68527-02-6 (oléfines chlorées [C12–C24]) ne serait pas acceptable pour désigner le (5Z)-1-chloro-5-dodécène; dans ce cas, le numéro d’enregistrement CAS approprié serait 71673-24-0.
Les sources pour obtenir les numéros d’enregistrement CAS sont données dans l’appendice 4 du Document d’orientation. Pour de plus amples renseignements sur les numéros d’enregistrement CAS, veuillez communiquer avec le :
Chemical Abstracts Service (en anglais seulement)
2540 Olentangy River Road
P.O. Box 3012
Columbus, OH 43210
États-Unis
Téléphone :
- 800-7534227 (Canada et États-Unis)
- 614-4473713
6.2.17 Dénomination chimique explicite de la substance (case A.17)
Toutes les annexes prescrivent, pour l’identification des substances, l’emploi des dénominations exactes suivant strictement la nomenclature de l’Union internationale de chimie pure et appliquée (UICPA) ou du CAS. La dénomination devrait permettre de dessiner la structure chimique, sauf si la substance déclarée est considérée être une UVCB
Pour les UVCB, les termes « produits de la réaction » et « composés » ou une autre nomenclature acceptable peuvent être utilisés. En voici quelques exemples :
- Carbonate de sodium produits de réaction avec l’aniline, la p-phénylènediamine, le sulfure de sodium (Na2(Sx)), le soufre et le p-toluidine;
- Amines, colophane, composées avec l’acide 6'-(diéthylamino) 3'-hydroxy-3-oxo-spiro[isobenzofuranne-1(3H),9'-[9H]xanthène]-2'-carboxylique et le bis[2-hydroxy-benzoato(2-)-O1,O2]chromate(1-) de sodium;
- Huiles, essences de menthe, Mentha arvensis var. piperascens, sans terpène.
La dénomination d’une UVCB devrait inclure, s’il y a lieu, une description de la synthèse (comme l’acétylation ou l’hydrolyse alcaline) et, s’il y a lieu, l’éventail des compositions possibles (par exemple, les alcanes [pétrole] normales C5–20). Les renseignements sur la composition des UVCB doivent être données dans la case A.20. L’appendice 3 du Document d’orientation présente des renseignements supplémentaires sur la dénomination des substances chimiques bien définies et des UVCB.
Lorsque la nomenclature des polymères et des biopolymères, incluant celle des prépolymères, incorpore l’identité des monomères et des réactifs utilisés dans la fabrication du polymère ou du biopolymère, le déclarant peut choisir d’inclure ou non dans la dénomination du polymère les monomères ou réactifs incorporés dans le polymère ou chargés dans la cuve de réaction et dont la masse est de 2 % ou moins de la masse du polymère. Cependant, ces substances doivent être incluses dans la description de la composition du polymère (consulter la partie 6.2.24).
Voici des exemples de nomenclature de polymères :
- Styrène polymérisé avec l’éthylène glycol, l’acrylate de butyle, le (chlorométhyl)oxirane, la 2,5-furanedione et le méthacrylate de méthyle;
- Formaldéhyde polymérisé avec le (chlorométhyl)oxirane, le 4-isobutylphénol, le 4,4’‑(isopropylidène)bis[phénol], le méthyloxirane polymérisé avec l’oxyde d’oxirane et de glycérol (propane-1,2,3-triol) [(3/1)] et l’oxirane.
6.2.18 Dénomination maquillée proposée (case A.18)
S’il est soutenu que la dénomination chimique de la substance déclarée soit considérée confidentielle, une dénomination maquillée devrait être fournie conformément au Règlement sur les dénominations maquillées. Dans le cas d’une substance faisant l’objet d’une demande de confidentialité, la case « Identité de la substance » dans la case A.1.5 doit être cochée. La marche à suivre pour créer la dénomination maquillée d’une substance est expliquée dans la partie 7.2.2 et dans l’appendice 5 du Document d’orientation. Cette marche à suivre existe en vue d’assurer la protection des RCC tout en assurant un certain niveau de transparence.
6.2.19 Noms commerciaux connus ou synonymes de la dénomination chimique explicite de la substance, y compris les codes internes et la dénomination des substances d’essai (case A.19)
Les noms commerciaux connus de la substance déclarée et les synonymes de la dénomination chimique doivent être fournis pour l’ensemble des substances assujetties à une annexe du Règlement (quelle qu’elle soit). La concentration de la substance déclarée (le pourcentage massique) doit également être fournie pour chacun des noms commerciaux connus, y compris les codes internes et la dénomination des substances d’essai, cela surtout lorsque la substance est utilisée à titre de substance d’essai afin de répondre aux exigences relatives aux renseignements techniques (consulter la partie B du formulaire de DSN). Il faut également inscrire des renseignements supplémentaires à la case A.25 pour chaque nom ou identifiant de la substance d’essai.
6.2.20 Composition des UVCB (précurseurs immédiats et composants majeurs ou clés prévus) (case A.20)
S’il s’agit d’une substance de la catégorie des UVCB, le déclarant doit fournir la dénomination et le numéro d’enregistrement CAS des précurseurs immédiats et des composants majeurs ou clés prévus, ainsi que la gamme des compositions possibles exprimé en pourcentage (%).
6.2.21 Formule développée de la substance, si possible, ou formule semi‑développée (case A.21)
Le diagramme de la formule développée doit être fourni pour les substances chimiques assujetties aux annexes 1, 5 ou 6 du Règlement.
Il faut présenter le diagramme de la formule développée de la substance, si possible, ou une formule semi-développée pour les polymères assujettis aux annexes 3, 9, 10 ou 11 du Règlement.
Dans les deux cas, le diagramme doit être assez grand pour indiquer clairement l’identité de tous les atomes, les types de liens, les charges ioniques et la stéréochimie. Si la structure est trop grande pour la case, le diagramme devrait être fournie en pièce-jointe.
Pour les polymères, le nombre ou l’étendue du nombre d’unités répétées doit être bien indiqué en fonction de la masse moléculaire moyenne en nombre (Mn) (par exemple, x = 7-15, y = 10-50). S’il y a lieu, il faut indiquer les proportions d’isomères ou de formes tautomériques.
L’appendice 3 du Document d’orientation fournit des renseignements supplémentaires et des exemples de formules développées.
Pour les substances biochimiques et les biopolymères qui sont des protéines, une structure primaire (séquence d’acides aminés) peut être fournie s’il n’est pas possible de fournir la formule développée.
S’il n’est pas possible de fournir la formule développée pour les UVCB, il faut fournir une formule semi-développée qui comprend les précurseurs immédiats.
Plan de réaction
De plus, il est nécessaire de présenter un plan de réaction fournissant une description détaillée du procédé par lequel la substance déclarée est fabriquée dans le cas des polymères qui sont considérés comme des polymères ERR (consulter la partie 3.3.1.5).
Comme les monomères sont multifonctionnels, il peut être difficile d’établir la structure du polymère final sans comprendre la séquence réactionnelle. Les renseignements détaillés fournis dans le plan de réaction aideront à confirmer plus facilement si le polymère en question est un polymère ERR et à mieux informer l’évaluation. Le plan de réaction devrait comporter les renseignements suivants :
- L’identité chimique des monomères, des prépolymères et des réactifs dans le polymère;
- Les détails de la synthèse du polymère, y compris la séquence d’addition des monomères et des réactifs, leur pourcentage massique et le nombre relatif de moles;
- La nature des réactions (par exemple hydrolyse, époxydation ou estérification);
- La structure du polymère et de tout sous-produit connu.
Le plan de réaction ne devrait pas être une description du procédé. En d’autres mots, il n’est pas nécessaire qu’il renferme un schéma technique comportant des détails tels que les cuves à réaction et les contenants servant à l’entreposage et au transport. Le plan de réaction doit renfermer des renseignements sur les monomères et sur les réactifs ainsi qu’une description de la séquence. L’appendice 8 comporte des renseignements supplémentaires sur les exigences en matière de plan de réaction.
Il convient de noter qu’un plan de réaction est seulement exigé pour les polymères ERR qui satisfont aux critères des alinéas 9 a) ou b) du Règlement. Un plan de réaction n’est pas exigé pour les polymères ERR qui satisfont aux critères de l’alinéa 9 c) du Règlement ou pour les polymères qui ne sont pas des polymères à exigences réglementaires réduites (non-ERR). Toutefois, la présentation d’un plan de réaction pour les polymères non-ERR aidera à mieux informer l’évaluation du polymère déclaré en illustrant son procédé de fabrication.
6.2.22 Formule moléculaire (case A.22)
La formule moléculaire est exigée pour les substances chimiques assujetties aux annexes 1, 5 ou 6 du Règlement ainsi que pour les polymères assujettis aux annexes 3, 9, 10 ou 11 du Règlement. Une formule moléculaire non définie peut également être acceptable (par exemple consulter la partie A3.2.2 pour les UVCB). La formule empirique doit être fournie et indiquer chacune des unités monomères. Voici des exemples :
- Méthacrylate de méthyle polymérisé avec de l’acrylate d’éthyle (C5H8O2×C5H8O2)x;
- Tétraoléate de polyoxyéthylène sorbitol (C2H4O)n(C2H4O)n(C2H4O)n(C2H4O)n(C2H4O)n(C2H4O)nC78H142O10.
6.2.23 Masse moléculaire en grammes (case A.23)
Ces renseignements sont requis pour les substances chimiques assujetties aux annexes 1, 5 ou 6 du Règlement. La masse moléculaire en grammes doit être indiquée pour les substances chimiques qui ont une formule développée définie. Dans le cas des UVCB, une estimation ou un intervalle des masses moléculaires est exigé, s’il est connu.
Il est question de la masse moléculaire moyenne en nombre des polymères dans la partie 6.3.1.14 du Document d’orientation. Cette masse doit être inscrite dans la case B.1 et non dans la case A.23 du formulaire de DSN.
6.2.24 Monomères et réactifs (case A.24)
Il faut fournir des renseignements sur les monomères et les réactifs dans le cas des polymères assujettis aux annexes 3, 9, 10 ou 11 du Règlement. Les réactifs comprennent des composés comme les initiateurs de radicaux libres, les agents de réticulation, les agents de terminaison en chaîne, les agents neutralisants et les agents de transfert d’enchaînements, incluant les monomères qui sont destinés à faire partie du polymère. Il faut fournir la dénomination, le numéro d’enregistrement CAS et le pourcentage massique de chaque réactif. Il faut également déclarer les réactifs, qu’ils soient incorporés dans le polymère ou chargés dans la cuve de réaction, représentant 2 % ou moins de la masse du polymère lors de sa fabrication, même s’ils n’ont pas été inclus dans la dénomination du polymère. Le total des pourcentages massiques des réactifs doit équivaloir à 100 %.
Prépolymères ne figurant pas sur la Liste intérieure ni sur la Liste extérieure, mais dont tous leurs réactifs y figurent.
Si un polymère non-ERR contient un prépolymère qui ne figure pas sur la Liste intérieure ni sur la Liste extérieure, mais que tous les réactifs du prépolymère figurent sur la Liste intérieure ou la Liste extérieure, il peut être considéré sous une annexe avec moins d’exigences en matière de renseignements, c’est-à-dire, sous l’annexe 10 au lieu de l’annexe 11 pour une quantité seuil de 10 000 kg.
Le terme « réactif » est défini de la façon suivante au paragraphe 1(1) du Règlement :
Dans la fabrication d’un polymère, substance utilisée pour faire partie intégrante de la composition chimique du polymère. La présente définition comprend les monomères.
Pour déterminer si un polymère non-ERR est admissible ou non à l’allégement des exigences prévu à l’article 11 du Règlement (consulter la partie 4.7.1), on définit le terme « réactif » pour inclure les précurseurs des prépolymères.
Par exemple, le polymère ABCDE contient les réactifs A et E qui figurent sur la Liste intérieure et le prépolymère BCD qui ne figure ni sur la Liste intérieure ni sur la Liste extérieure. Le prépolymère BCD est composé des réactifs B, C et D; dont B et D figurent sur la Liste intérieure et C figure sur la Liste extérieure. Par conséquent, dans ce cas, la substance déclarée, soit le polymère ABCDE, pourrait être considérée sous une annexe avec moins d’exigences en matière de renseignements.
Si un prépolymère entre dans la fabrication de la substance déclarée et que ce prépolymère ne figure pas sur la Liste intérieure ni sur la Liste extérieure, mais que tous les réactifs du prépolymère y figurent, des données sur la composition du prépolymère doivent être fournies, y compris la dénomination et le numéro d’enregistrement CAS de chaque réactif. Cela est nécessaire pour déterminer si moins d’exigences en matière de renseignements s’appliquent à la substance déclarée.
Il faut également indiquer le pourcentage massique de la composition du prépolymère si celui-ci comprend des groupes réactifs ou cationiques (consulter la partie 3.3.1.5). Cela est nécessaire pour déterminer si la substance déclarée est considérée comme un polymère ERR.
6.2.25 Additifs, stabilisateurs et solvants présents lors des essais pour chaque nom ou dénomination figurant dans la case A.19 (case A.25)
Ces renseignements sont requis dans le cas des substances chimiques assujetties aux annexes 1, 5 ou 6 du Règlement et le cas des polymères assujettis aux annexes 3, 9, 10 ou 11 du Règlement. Les additifs sont des substances délibérément introduites dans un produit final qui contient la substance déclarée (par exemple des stabilisateurs, des émulsifiants, des solvants et des antioxydants) et qui sont présentes lors des essais sur la substance déclarée.
Pour satisfaire aux exigences relatives aux renseignements techniques (consulter la partie B du formulaire de DSN), il faut indiquer les renseignements relatifs à la composition pour chaque nom ou identifiant de la substance d’essai indiquée à la case A.19. Cela comprend la dénomination de la substance, le numéro d’enregistrement CAS et la concentration de chaque composant (le pourcentage massique). Pour chaque nom ou identifiant de la substance d’essai indiquée à la case A.19, le total des pourcentages massiques des composants doit être égal à 100 % (c’est-à-dire le total des pourcentages massiques des additifs, stabilisateurs et solvants et de la substance déclarée précisé à la case A.19 doit être égal à 100 %). Il est possible de fournir des intervalles de pourcentage dans certains cas. Si les renseignements relatifs à la composition sont inadéquats, la déclaration sera jugée incomplète et un avis indiquant qu’il manque des renseignements sera communiqué.
6.2.26 Degré de pureté de la composition de qualité technique (case A.26)
Ces renseignements sont requis pour les substances chimiques assujetties aux annexes 1, 5 ou 6 du Règlement.
6.2.27 Impuretés et leur concentration massique (case A.27)
Il faut fournir ces renseignements pour les substances assujetties aux annexes 1, 3, 5, 6, 9, 10 et 11 du Règlement.
Les impuretés sont des substances qui sont présentes habituellement en faibles concentrations dans le produit final qui contient la substance déclarée mais qui ne sont pas nécessaires à son utilisation prévue. Elles comprennent, entre autres, des produits de départ qui n’ont pas réagi et des sous-produits de réaction. Il faut fournir la dénomination, le numéro d’enregistrement CAS et la concentration massique de chaque impureté, si ces renseignements sont connues.
6.2.28 Fiche de données de sécurité (case A.28)
Toutes les annexes exigent qu’une fiche de données de sécurité soit fournie, si un tel document est disponible. Définie à l’article 2 de la Loi sur les produits dangereux, cette fiche doit être fournie si elle a été rédigée.
6.3 Exigences relatives aux renseignements techniques (partie B)
Toutes les exigences de renseignements techniques doivent être satisfaites en présentant des données d’essai, des données provenant de méthodes de rechange ou des demandes de dérogation. Les méthodes de rechange comprennent l’emploi de données de substitution, de protocoles d’essai de rechange et de méthodes de calcul ou d'estimation. Consulter la partie 8.4 pour de plus amples renseignements sur les méthodes de rechange et les critères permettant de déterminer si une méthode de rechange proposée est acceptable à des fins d'évaluation des risques. Consulter aussi la partie 8.7 sur les demandes de dérogation à l’obligation de fournir des renseignements et les circonstances dans lesquelles elles peuvent être accordées en vertu de la Loi.
Afin de satisfaire aux exigences sur les renseignements techniques, les renseignements sur la composition de chaque substance d’essai doivent aussi être fournis (consulter la partie 6.2.25). Il incombe au déclarant de fournir des renseignements acceptables. Des explications sur les exigences en matière de renseignements, provenant des différentes annexes du Règlement, sont données et aideront à produire et réunir les données techniques prescrites par ledit Règlement. Ces notes explicatives donnent des détails, notamment les annexes pour lesquelles des renseignements sont requis, les conditions nécessaires aux différents essais et ce qui constitue des renseignements complets et adéquats pour les responsables du Programme des SN.
La partie B du formulaire de DSN comporte 3 parties :
- B.1 Propriétés physico-chimiques;
- B.2 Renseignements sur l’écotoxicité;
- B.3 Renseignements sur la toxicité pour la santé humaine.
Des notes explicatives sur les renseignements techniques exigés sont fournies dans les parties suivantes du Document d’orientation.
6.3.1 Propriétés physico-chimiques (case B.1)
Des directives propres aux nanomatériaux et des mises à jour des Lignes directrices (LD) de l’Organisation de coopération et de développement économiques (OCDE) pour les essais ont été publiées au cours des dernières années et devraient être intégrées à toute stratégie d’essai.
6.3.1.1 Point de fusion
Cet essai est exigé pour les substances chimiques qui sont assujetties aux annexes 5 ou 6 du Règlement. Si le point de fusion se situe entre 25 et 300 °C, il faut fournir une valeur unique ou un intervalle de valeurs. Par contre, s’il tombe hors de cette plage de températures, « < -25 °C » ou « > 300 °C » peut être inscrit. Dans les cas où la substance déclarée subit une transformation chimique autre que la fusion (par exemple, dégradation, décomposition ou réarrangement), il faut indiquer la température à laquelle elle survient. Si cela est approprié, le point de liquéfaction, de ramollissement ou de sublimation peut être indiqué comme donnée de substitution au lieu du point de fusion. Dans le cas des substances biochimiques et des biopolymères, le point isoélectrique peut être substitué au point de fusion.
6.3.1.2 Point d’ébullition
Cet essai est exigé pour les substances chimiques qui sont assujetties aux annexes 5 ou 6 du Règlement. Si le point d’ébullition se situe entre 50 °C et 300 °C, il faut fournir une valeur unique ou un intervalle de valeurs. Par contre, s’il tombe hors de cette plage, « < -50 °C » ou « > 300 °C » peut être inscrit. Dans les cas où la substance déclarée subit une transformation chimique autre que la fusion (par exemple, dégradation, décomposition ou réarrangement), il faut indiquer la température à laquelle elle survient.
6.3.1.3 Solubilité dans l’eau
Il faut indiquer la solubilité dans l’eau des substances chimiques assujetties aux annexes 5 ou 6 du Règlement.
La solubilité dans l’eau est une propriété pertinente des nanomatériaux. Il est toutefois nécessaire de différencier la solubilité de la dispersibilité dans l’eau. Il faut fournir des renseignements sur la dispersion des nanomatériaux (par exemple, la dispersion colloïdale). Dans le cas de certains nanomatériaux, dont les oxydes métalliques, on recommande de réaliser l’essai de dissolution approprié. Les renseignements pertinents se trouvent dans le Document d’orientation sur la transformation/dissolution des métaux et des composés métalliques en milieu aqueux [PDF] de l’OCDE.
6.3.1.4 Extractibilité dans l’eau
Des renseignements sur l’extractibilité de la substance dans l’eau sont requis pour les polymères assujettis aux annexes 10 ou 11 du Règlement.
L’essai devrait être réalisé conformément à la LD 120 de l’OCDE, qui est une version modifiée de la méthode par agitation en flacon de la LD 105 de l’OCDE. La LD 105 de l’OCDE sur la méthode par élution sur colonne ne permet pas d’obtenir le paramètre requis, ce qui la rend inacceptable. Le Programme des SN recommande également la LD 120 de l’OCDE pour l’essai sur les polymères qui contiennent des groupes fonctionnels hydroréactifs. L’appendice 9 donne des renseignements supplémentaires.
Selon la nature du nouveau polymère, les essais doivent être réalisés au pH indiqué par le Règlement (dans le cas des polymères anioniques et neutres, au pH 7, dans celui des polymères cationiques, aux pH 2 et 7, finalement dans celui des polymères amphotères, aux pH 2, 7 et 9). Les résultats doivent être exprimés en pourcentage de substances extractibles.
6.3.1.5 Pression de vapeur
Cet essai est exigé pour les substances chimiques qui sont assujetties à l’annexe 5 ou 6 du Règlement. Toutefois, l’essai n’est pas exigé si le point d’ébullition normal de la substance chimique est inférieur à 0 °C.
6.3.1.6 Densité
Cette valeur est exigée pour les substances chimiques assujetties aux annexes 5 ou 6 du Règlement.
6.3.1.7 Coefficient de partage entre l’octanol et l’eau
Ce renseignement est exigé pour les substances chimiques assujetties aux annexes 5 ou 6 du Règlement lorsque leur solubilité dans l’eau est égale ou inférieure à 5 g/L. Toutefois, comme il n’y a pas de limite relative à l’extractibilité dans l’eau pour les polymères, la divulgation de ce coefficient est obligatoire pour toutes les substances assujetties aux annexes 10 ou 11 du Règlement.
6.3.1.8 Hydrolyse en fonction du pH
Le taux d’hydrolyse en fonction du pH est exigé pour les substances chimiques assujetties à l’annexe 6 du Règlement lorsque leur solubilité dans l’eau est égale ou supérieure à 200 µg/L.
Le taux d’hydrolyse en fonction du pH est également exigé pour les substances chimiques assujetties à l’annexe 5 du Règlement qui figurent sur la Liste extérieure et qui répondent aux critères de rejets dans l’environnement aquatique en grande quantité [paragraphe 7(2) du Règlement] (consulter la partie 4.4.3.1) lorsque leur solubilité dans l’eau est égale ou supérieure à 200 µg/L. Il faut également identifier les produits de l’hydrolyse, s’ils sont connus.
Cet essai est également exigé pour les polymères assujettis aux annexes 10 ou 11 du Règlement et dont l’extractibilité dans l’eau est supérieure à 2 %. Il faut également identifier les produits de l’hydrolyse, s’ils sont connus.
6.3.1.9 Biodégradabilité immédiate
Un essai de biodégradabilité immédiate est exigé pour les substances chimiques assujetties aux annexes 5 ou 6 du Règlement. Il faut également identifier tous les produits connus de la biodégradation.
Cet essai est également exigé pour les polymères qui sont assujettis à l’annexe 11 du Règlement. L’essai de biodégradabilité immédiate est requis pour la portion hydrosoluble du polymère, sauf si l’extractibilité dans l’eau, au pH 7, est égale ou inférieure à 2 %. Sont aussi exemptés les polymères ramifiés de silicone et de siloxane.
L’essai doit être conforme aux Bonnes pratiques de laboratoire (BPL) [consulter la partie 8.3.1].
6.3.1.10 Adsorption et désorption
Cet essai est exigé pour les substances chimiques assujetties à l’annexe 6 du Règlement lorsque leur solubilité dans l’eau est égale ou supérieure à 200 µg/L.
L’essai est également exigé pour les substances chimiques assujetties à l’annexe 5 du Règlement qui figurent sur la Liste extérieure et qui répondent aux critères de rejets dans l’environnement aquatique en grande quantité [paragraphe 7(2) du Règlement] (consulter la partie 4.4.3.1) lorsque leur solubilité dans l’eau est égale ou supérieure à 200 µg/L.
6.3.1.11 Spectroscopie
Cette mesure est exigée pour les substances chimiques qui sont assujetties à l’annexe 6 du Règlement. Il faut fournir au moins un spectre approprié pour la caractérisation de la substance (par exemple, Infrarouge [IR], Ultraviolet [UV], Résonance magnétique nucléaire [RMN]). Il faut également fournir les détails de la méthodologie employée (par exemple, solvant, technique d’ionisation, force du champ, largeur de la bande, instrumentation). L’intervalle des spectres UV doit descendre à 290 nm.
6.3.1.12 Conçu pour se disperser dans l’eau
Il faut fournir des renseignements sur la dispersibilité dans l’eau lorsqu’il s’agit de polymères assujettis aux annexes 3, 10 ou 11 du Règlement. Il n’est pas nécessaire de déterminer le degré de dispersibilité, mais, le cas échéant, il faut indiquer si le polymère est conçu pour se disperser dans l’eau. Il suffit d’indiquer « oui » ou « non » dans la colonne de la case B.1 du formulaire de DSN. Il n’est donc pas nécessaire de donner des déterminations quantitatives pour cette exigence en matière de renseignement.
6.3.1.13 État physique
Il faut indiquer l’état physique des polymères qui sont assujettis aux annexes 3, 10 ou 11 du Règlement. Pour ce faire, il suffit d’inscrire la mention appropriée (par exemple « solide », « matière cireuse » ou « liquide ») dans la colonne de la case B.1 du formulaire de DSN. Il n’est donc pas nécessaire de donner des déterminations quantitatives pour cette exigence en matière de renseignement.
6.3.1.14 Masse moléculaire moyenne en nombre
Cet essai est exigé pour les polymères qui sont assujettis aux annexes 3, 9, 10 ou 11 du Règlement. En règle générale, s’il est possible de se procurer le polymère dans une collection de formulations de masses moléculaires différentes, les renseignements sur la formulation ayant la Mn la plus petite doivent être obtenus. Toutefois, les renseignements préexistants relatifs aux compositions ayant des masses moléculaires plus élevées devraient également être communiqués. Les renseignements sur la Mn doivent comprendre les méthodes d’essai employées ainsi que le chromatogramme, la courbe d’étalonnage et les tables des coupes produites durant l’essai. Diverses méthodes permettent de déterminer la valeur Mn, mais la méthode la plus utilisée reste la chromatographie sur gel perméable (Gel Permeation Chromatography - GPC). L’appendice 7 du Document d’orientation comporte des renseignements supplémentaires sur les exigences et sur les problèmes les plus fréquents affectant les données obtenues à l’aide de cette technique.
Si la solubilité de la substance déclarée est égale ou supérieure à 2 % dans un solvant approprié, la Mn doit être déterminée à partir de la portion extractible de la substance déclarée (par exemple, dans le cas d’un polymère qui affiche une solubilité de 5 %, la Mn doit être déterminée à partir de cette portion de 5 %).
Lorsqu’un polymère est insoluble (solubilité inférieure à 2 %) dans un système de solvants généralement utilisé aux fins de la GPC, les données relatives à la solubilité doivent être indiquées pour un éventail de solvants. Par exemple, l’insolubilité dans les solvants classiques pourrait être le signe de la forte réticulation du polymère. Des méthodes alternatives doivent alors être employées pour déterminer la Mn ou, encore, une demande de dérogation doit accompagner les résultats d’insolubilité. Dans cet exemple, la Mn d’un prépolymère pourrait aussi être fournie comme donnée de substitution.
Dans le cas des polymères fabriqués ou importés à des fins de recherche et de développement et qui sont assujettis à l’annexe 3 du Règlement, seule une valeur cible de Mn est exigée.
6.3.1.15 Composante résiduelle dont la masse moléculaire est inférieure à 500 daltons et inférieure à 1 000 daltons
Ces renseignements sont exigés pour les polymères assujettis aux annexes 3, 9, 10 ou 11 du Règlement, à l’exception des substances assujetties à l’annexe 3 qui sont destinées à la recherche et au développement.
Le pourcentage des composantes résiduelles doit être déterminé à partir de la formulation ayant la plus petite Mn de n’importe quelle formulation destinée à la fabrication ou à l’importation.
6.3.2 Renseignements sur l’écotoxicité (case B.2)
Le nombre et le type des essais d’écotoxicité dont une substance doit faire l’objet dépendent de l’annexe du Règlement qui s’y applique ou de l’espèce la plus sensible à ses effets. Les rapports d’essai complets doivent être fournis. Les résumés ne sont pas acceptés. Les renseignements relatifs à la composition doivent être fournis pour chaque substance d’essai afin de satisfaire aux exigences relatives aux renseignements techniques (consulter la partie 6.2.25).
Le document Guidance on Sample Preparation and Dosimetry for the Safety Testing of Manufactured Nanomaterials [PDF] de l’OCDE (en anglais seulement) devrait être consulté pour avoir un aperçu de toutes les exigences en matière de renseignements sur l’écotoxicité des nanomatériaux. Des directives propres aux nanomatériaux et des mises à jour des LD de l’OCDE ont été publiées au cours des dernières années et devraient être intégrées à toutes les stratégies d’essai.
Il est recommandé de déterminer la distribution granulométrique en nombre afin de mieux prendre compte de la présence de nanoparticules de plus petites tailles. Si les renseignements sur la taille des particules primaires et la distribution granulométrique ne sont pas indiqués et que le Programme des SN croit que la substance pourrait être un nanomatériau, la substance sera traitée comme un nanomatériau potentiel aux fins de l’évaluation et de la gestion des risques.
6.3.2.1 Toxicité aiguë en milieu aquatique
Au moins un de ces essais est exigé pour les substances chimiques assujetties aux annexes 5 ou 6 du Règlement et pour les polymères assujettis aux annexes 10 ou 11 du Règlement.
En ce qui concerne les substances chimiques assujetties à l’annexe 5 du Règlement, les données d’un essai de toxicité aiguë chez le poisson, la daphnie ou les algues sont exigées.
En ce qui concerne les substances chimiques assujetties à l’annexe 6 du Règlement, les données des 2 essais d’écotoxicité restants (qui n’ont pas été réalisés pour le dépôt de l’annexe 5 du Règlement) sont exigées.
Pour ce qui est des polymères assujettis à l’annexe 10 du Règlement, excepté les polymères caractérisés par une extractibilité dans l’eau au pH 7 égale ou inférieure à 2 %, il faut fournir les données d’un essai de toxicité aiguë pour l’espèce la plus sensible (poisson, daphnie ou algues) ou, si la sensibilité de ces espèces est inconnue, les données d’un essai de toxicité aiguë chez les algues.
En ce qui concerne les polymères assujettis à l’annexe 11 du Règlement et caractérisés par une extractibilité dans l’eau au pH 7 supérieure à 2 %, les données des essais suivants sont exigées :
- a) si la sensibilité des trois espèces est connue, un essai de toxicité aiguë du polymère pour chacune des deux espèces les plus sensibles : le poisson, la daphnie ou les algues;
- b) si la sensibilité d’une seule espèce est connue et qu’il ne s’agit pas des algues, un essai de toxicité aiguë pour les algues et, au choix selon la plus sensible des espèces, un essai de toxicité aiguë pour le poisson ou la daphnie;
- c) si la sensibilité des trois espèces n’est pas connue ou que la sensibilité d’une seule espèce est connue et qu’il s’agit des algues, un essai de toxicité aiguë pour les algues et, au choix, un essai de toxicité aiguë pour le poisson ou la daphnie.
Ces essais doivent être conformes aux BPL (consulter la partie 8.3.1).
6.3.3 Renseignements sur la toxicité pour la santé humaine (case B.3)
Il faut également fournir les renseignements suivants pour satisfaire à toutes les exigences en matière de renseignements sur la toxicité pour la santé humaine :
- a) l’âge, le sexe, le nombre, l’espèce, la souche et la source des animaux testés;
- b) la voie d’administration de la substance et les conditions dans lesquelles l’essai est effectué;
- c) la posologie de la substance, le vecteur par lequel elle est administrée et sa concentration dans le vecteur.
Les renseignements relatifs à la composition doivent être fournis pour chaque substance d’essai afin de satisfaire aux exigences relatives aux renseignements techniques (consulter la partie 6.2.25).
Le document Guidance on Sample Preparation and Dosimetry for the Safety Testing of Manufactured Nanomaterials [PDF]de l’OCDE (en anglais seulement) devrait être consulté pour avoir un aperçu de toutes les exigences en matière de renseignements sur la toxicité des nanomatériaux sur la santé humaine. Des directives propres aux nanomatériaux et des mises à jour des LD de l’OCDE ont été publiées au cours des dernières années et devraient être intégrées à toutes les stratégies d’essai.
Il est recommandé de déterminer la distribution granulométrique en nombre afin de mieux prendre compte de la présence de nanoparticules de plus petites tailles. Si les renseignements sur la taille des particules primaires et la distribution granulométrique ne sont pas indiqués et que le Programme des SN croit que la substance pourrait être un nanomatériau, la substance sera traitée comme un nanomatériau potentiel aux fins de l’évaluation et de la gestion des risques.
6.3.3.1 Toxicité aiguë chez les mammifères
Ces renseignements sont exigés pour les substances chimiques assujetties aux annexes 5 ou 6 du Règlement et les polymères assujettis aux annexes 10 ou 11 du Règlement. Les animaux d’essai devraient recevoir leurs doses par le ou les modes d’exposition correspondant au mode ou aux modes d’exposition les plus probables du public (orale, cutanée ou par inhalation ou une combinaison de celles-ci). Dans le Règlement, le mode d’exposition le plus probable du public signifie l’exposition de la population canadienne en général. Pour choisir le ou les modes d’exposition convenant le mieux à l’essai, il faut prendre en considération la concentration prévue de la substance déclarée dans les divers milieux naturels et produits de consommation et la biodisponibilité de la substance par ingestion, inhalation et absorption par voie cutanée. Le mode d’exposition le plus probable à une substance pour la population en général peut différer des modes d’exposition des travailleurs en milieu de travail. Par conséquent, il se peut que les données produites pour les lieux de travail ne satisfassent pas aux exigences relatives au mode d’exposition le plus probable du public mentionné dans le Règlement. Si le choix du ou des mode d’exposition pour les essais au sens de la Loi est complexe, veuillez consulter le Programme des SN (consulter la partie 8.8).
Dans le cas des nanomatériaux, un essai de toxicité aiguë par inhalation est généralement recommandé. Une révision du document Guidance Document on Inhalation Toxicity Studies [PDF] de l’OCDE (en anglais seulement) qui règle des problèmes spécifiques aux nanomatériaux a été publié en 2018.
On ne considère pas que les données des essais de toxicité aiguë produites après le 16 décembre 2002 en suivant la LD 401 de l’OCDE satisfont aux exigences réglementaires de ce paramètre toxicologique.
Ces essais doivent être conformes aux BPL (consulter la partie 8.3.1).
6.3.3.2 Irritation cutanée
Il faut donner les renseignements nécessaires à l’évaluation du degré d’irritation cutanée causée par les substances chimiques assujetties à l’annexe 6 du Règlement et aux polymères assujettis à l’annexe 11 du Règlement. Ces renseignements peuvent être obtenus grâce aux méthodes d’essais validés pour les différents paramètres toxicologiques suivants :
- Irritation de la peau (par exemple, LD 404 de l’OCDE);
- Sensibilisation cutanée (par exemple, LD 406 de l’OCDE), y compris les résultats d’une évaluation appropriée des réactions de la peau;
- Toxicité par voie cutanée (par exemple, LD 402, 410 et 411 de l’OCDE), y compris les résultats d’une évaluation appropriée des réactions de la peau;
- Corrosion cutanée in vitro (réponse positive seulement) [par exemple, LD 430 et 431 de l’OCDE];
- Irritation cutanée in vitro avec de l’épiderme humain reconstitué (par exemple, LD 439 de l’OCDE).
La liste ci-dessus n’est pas exhaustive. À mesure que de nouvelles méthodes seront mises au point et validées, les responsables du Programme des SN détermineront si celles-ci fournissent assez de renseignements pour permettre l’évaluation du degré d’irritation cutanée. Pour consulter les méthodes d’essais, consulter la partie 8.6.
Des essais épicutanés par applications répétées (réponse positive ou négative) sur l’humain peuvent être un remplacement acceptable aux essais réalisés chez des animaux. La concentration de la substance déclarée à laquelle des personnes ont été exposées sera un facteur critique pour décider de l’acceptabilité des essais épicutanés sur l’humain. Il se peut aussi qu’une expérience d’utilisation par les humains puisse être une option de rechange acceptable (réponse positive seulement), dans la mesure où cette expérience d’utilisation est bien décrite, avec la quantification la plus exacte possible de l’exposition et de la réaction de la peau. Les renseignements anecdotiques provenant de personnes qui ont manipulé la substance ou qui y ont été exposées ne constituent pas une option de rechange acceptable à l’essai prévu.
En outre, des renseignements pour l’évaluation de l’irritation cutanée peuvent être tirées des RQSA si le déclarant donne une justification scientifique adéquate pour la validation et le domaine d’application du modèle.
Ces essais doivent être conformes aux BPL (consulter la partie 8.3.1).
6.3.3.3 Sensibilisation cutanée
Ces renseignements sont exigés pour les substances chimiques assujetties à l’annexe 6 du Règlement et les polymères assujettis à l’annexe 11 du Règlement. Ces renseignements pourraient être obtenus à partir de données des méthodes d’essai validées suivantes :
- Les approches définies pour la sensibilisation cutanée qui utilisent les LD 442C, 442D et 442E de l’OCDE en une combinaison de méthodes in vivo et in chemico afin de réduire la dépendance aux données d’essai impliquant des animaux (consulter la ligne directrice n° 497 de l’OCDE pour de plus amples renseignements sur comment utiliser ce genre d’approche);
- Sensibilisation cutanée (par exemple, LD 406 de l’OCDE), y compris les résultats d’une évaluation appropriée des réactions de la peau;
- Sensibilisation cutanée avec l’Essai de stimulation locale des ganglions lymphatiques [ELGL] (LD 429, 442A et 442B de l’OCDE).
La liste ci-dessus n’est pas exhaustive. À mesure que de nouvelles méthodes seront mises au point et validées, les responsables du Programme des SN détermineront si celles-ci fournissent assez de renseignements pour permettre l’évaluation du degré de sensibilisation cutanée. Pour consulter les méthodes d’essais, consulter la partie 8.6.
Des essais épicutanés par applications répétées (réponse positive ou négative) sur l’humain peuvent être un remplacement acceptable aux essais réalisés chez des animaux. La concentration de la substance déclarée à laquelle des personnes ont été exposées sera un facteur critique pour décider de l’acceptabilité des essais épicutanés sur l’humain. Il se peut aussi qu’une expérience d’utilisation par les humains puisse être une option de rechange acceptable (réponse positive seulement), dans la mesure où cette expérience d’utilisation est bien décrite, avec la quantification la plus exacte possible de l’exposition et de la réaction de la peau. Les renseignements anecdotiques provenant de personnes qui ont manipulé la substance ou qui y ont été exposées ne constituent pas une option de rechange acceptable à l’essai prévu.
Ces essais doivent être conformes aux BPL (consulter la partie 8.3.1).
6.3.3.4 Toxicité à doses répétées chez les mammifères
Ces renseignements sont exigés pour les substances chimiques assujetties à l’annexe 6 du Règlement et les polymères assujettis à l’annexe 11 dudit Règlement. Le déclarant doit présenter un rapport d’une étude s’étendant sur une durée d’au moins 28 jours. Conformément aux exigences énoncées dans la partie 6.3.3.1 du Document d’orientation (« Toxicité aiguë chez les mammifères »), l’exposition des animaux lors des essais doit correspondre au mode d’exposition le plus probable de la population générale au Canada.
L’essai susmentionné est également exigé pour une substance chimique ou un polymère qui figure sur la Liste extérieure, ou encore dont tous les réactifs figurent sur la Liste intérieure ou la Liste extérieure et qui répond aux critères de rejets dans l’environnement aquatique en grande quantité, ou lorsque le degré d'exposition du public pourrait être élevé à la substance contenue dans un produit [paragraphes 7(2), 7(3), 11(2) ou 11(3) du Règlement]. Les parties 4.4.3 et 4.9.2 du Document d’orientation donnent plus de détails sur ces données.
L’essai doit être conforme aux BPL (consulter la partie 8.3.1).
6.3.3.5 Essai in vitro pour déterminer la présence de mutations génétiques
Un essai in vitro, avec et sans activation métabolique, pour déterminer la présence de mutations génétiques est exigé pour les substances chimiques assujetties à l’annexe 5 ou 6 du Règlement et les polymères assujettis à l’annexe 11 du Règlement.
L’essai susmentionné est également exigé pour un polymère qui figure sur la Liste extérieure, ou dont tous les réactifs figurent sur la Liste intérieure ou la Liste extérieure et qui répond aux critères de rejets dans l’environnement aquatique en grande quantité, ou lorsque le degré d'exposition du public pourrait être élevé au polymère dans un produit [paragraphes 11(2) et 11(3) du Règlement]. Pour en savoir davantage sur ces paramètres, consulter la partie 4.9.2 du Document d’orientation.
Lorsque ces renseignements sont exigés en vertu du paragraphe 11(2) du Règlement, le déclarant peut substituer aux renseignements résultant de l’essai susmentionné, les résultats d’un essai in vitro, avec et sans activation métabolique, mené pour déterminer la présence d’aberrations chromosomiques (consulter la partie suivante).
L’essai doit être conforme aux BPL (consulter la partie 8.3.1).
Les travaux du Colloque sur la génotoxicité des nanomatériaux manufacturés du Groupe de travail sur les nanomatériaux manufacturés de l’OCDENote de bas de page 16 à Ottawa en novembre 2013, ont conclu que l’Essai de mutation réverse sur des bactéries (LD 471 de l’OCDE) n’est pas une méthode d’essai recommandée pour l’étude de la génotoxicité des nanomatériaux. Il a donc été recommandé que le programme de l’OCDE sur les LD pour les essais de produits chimiques modifie le champ d’application de la LD 471 afin de tenir compte de cette conclusion. Les données produites par un Essai de mutation réverse sur des bactéries conviennent uniquement dans les cas où les nanomatériaux sont de très petites tailles (par exemple, ceux qui peuvent traverser directement la membrane cellulaire), solubles ou capables de produire des dérivés réactifs de l’oxygène. Par conséquent, la réalisation d’essais de génotoxicité in vitro sur des cellules de mammifères (par exemple, essais de mutation génique in vitro sur des cellules de mammifères et essais in vitro du micronoyau) est encouragée pour la plupart des cas. L’Essaie in vitro de mutation génique sur des cellules de mammifères (LD 476 de l’OCDE) est celui que l’on recommande pour satisfaire aux exigences en matière de renseignements dans le cadre d’un essai de mutagénicité in vitro (article 7 de l’annexe 5 du Règlement) mené sur un nanomatériau.
6.3.3.6 Essai in vitro pour déterminer la présence d’aberrations chromosomiques
Un essai in vitro, avec et sans activation métabolique, pour déterminer la présence d’aberrations chromosomiques dans des cellules de mammifères est exigé pour les substances chimiques assujetties à l’annexe 6 du Règlement et les polymères assujettis à l’annexe 11 du Règlement.
Cet essai est également exigé pour une substance chimique qui figure sur la Liste extérieure ou un polymère qui figure sur la Liste extérieure ou encore dont tous les réactifs figurent sur la Liste intérieure ou la Liste extérieure, et lorsque le degré d'exposition du public pourrait être élevé à la substance contenue dans un produit [paragraphes 7(3) et 11(3) du Règlement]. Pour en savoir davantage sur ces paramètres, consulter les parties 4.4.3.2 et 4.9.2.2 du Document d’orientation.
Lorsque ces renseignements sont exigés en vertu du paragraphe 7(3) ou 11(3) du Règlement, le déclarant peut substituer aux données résultant d’un essai in vitro, celles produites par un essai in vivo mené antérieurement pour déterminer la présence d’aberrations chromosomiques dans des cellules de mammifères avec des données établissant que le tissu étudié a été exposé à la substance déclarée ou à ses métabolites.
L’essai doit être conforme aux BPL (consulter la partie 8.3.1).
6.3.3.7 Essai de mutagénicité in vivo chez les mammifères pour déterminer la présence d’aberrations chromosomiques ou de mutations génétiques
Dans le cas des substances chimiques assujetties à l’annexe 6 du Règlement ou des polymères assujettis à l’annexe 11 du Règlement, il faut présenter un essai de mutagénicité in vivo chez les mammifères pour déterminer la présence d’aberrations chromosomiques ou de mutations génétiques ou un autre indicateur du pouvoir mutagène qui, jumelé à des données établissant que le tissu en question a été exposé à la substance ou à ses métabolites, permet d’obtenir une évaluation du pouvoir mutagène in vivo acceptable dans le cadre du Programme des SN.
Les critères établis pour déterminer ce que sont des « données établissant que le tissu en question a été exposé à la substance ou à ses métabolites » et ce qui constitue un « indicateur de mutagénicité » et une évaluation « acceptable dans le cadre du Programme des SN » sont décrits dans l’appendice 13 du Document d’orientation.
Le Programme des SN accorde une certaine flexibilité dans le choix de l’essai in vivo pour permettre au déclarant d’effectuer l’essai qui convient le mieux à la substance en question. Le choix de l’essai in vivo devrait être basé sur les résultats d’essais de génotoxicité in vitro, sur la structure et le mécanisme d’action de la substance ainsi que sur les derniers progrès réalisés dans le domaine de la génotoxicité.
L’essai doit être conforme aux BPL (consulter la partie 8.3.1).
6.3.4 Exceptions réglementaires : essais de toxicité pour la santé humaine non exigés dans le cas de certains polymères
Les renseignements prescrits aux paragraphes 11(2) et 11(3) du Règlement pour les polymères rejetées dans l’environnement aquatique en grande quantité et auquel le degré d’exposition du public est élevée (consulter la partie 4.9.2) ainsi que les essais de toxicité pour la santé humaine décrits dans la partie 6.3.3 du Document d’orientation ne sont pas exigés dans le cas des polymères appartenant à l’une des classes indiquées dans le tableau 6-1.
| Classe de polymères | Définition |
|---|---|
| Polymères ERRa | Définis à la partie 3.3.1.5 du présent Document d'orientation. |
| Aldéhydes | Polymères non-ERRb en raison uniquement de la présence d’aldéhydes dont la MEGFc est égale ou inférieure à 1 000 daltons. |
| Éthers vinyliques | Polymères non-ERR en raison uniquement de la présence d’éthers vinyliques dont la MEGF est égale ou inférieure à 5 000 daltons. |
| Acides sulfoniques | Polymères non-ERR en raison uniquement de la présence d’acides sulfoniques dont la MEGF est égale ou inférieure à 5 000 daltons. |
a Polymères ERR – Polymères à exigences réglementaires réduites.
b Polymères non-ERR – Polymères qui ne sont pas des polymères à exigences réglementaires réduites.
c MEFG – Masse équivalente du groupe fonctionnel.
6.3.5 Dérogations relatives aux données sur la toxicité de polymères pour la santé humaine
Le tableau 6-2 donne des exemples de polymères pour lesquels il serait possible d’obtenir une dérogation et d’autres qui ne feraient vraisemblablement pas l’objet de dérogations à l’obligation des essais de toxicité pour la santé humaine. Les renseignements dans ce tableau pourraient changer si d’autres renseignements plus précis devenaient disponibles. Les évaluations en vue d’accorder des dérogations sont effectuées au cas par cas. Bien qu’ils ne soient pas tenus de le faire, les responsables du Programme des SN donnent l’occasion aux déclarants de présenter une demande de CAD (consulter la partie 8.8) pendant l’élaboration de la DSN pour déterminer s’il est acceptable d’accorder une dérogation.
| Exemple | Description de polymère | Vraisemblance que des dérogations à l’obligation des essais de toxicité pour la santé humaine soient accordées |
|---|---|---|
| 1 | Polymères non-ERRa en raison uniquement de la présence des groupes cationiques ou potentiellement cationiques suivants : groupes d’amines primaires, secondaires ou tertiaires, cyanamides ou sulfoniums. | Feront vraisemblablement l’objet de dérogations. |
| 2 | Polymères contenant d’autres groupes cationiques, tels des amines quaternaires, des amines stabilisées par encombrement, des azotures, des isocyanates (libres et bloqués) et des phosphoniums (consulter la partie 8.7.2). | Ne feront vraisemblablement pas l’objet de dérogations. |
| 3 | Polymères pour lesquels l’inhalation sera le principal mode d’exposition (aérosol) ou destinés à être utilisés dans des produits de soins personnels ou des jouets pour enfants. | Ne feront vraisemblablement pas l’objet de dérogations. |
| 4 | Polymères cationiques comprenant des espèces qui ont une Mn supérieure à 10 000 daltons s’il est prévu que l’inhalation sera, selon l’utilisation prévue, le mode d’exposition le plus probable de la population en général, ou si la substance est utilisée dans des produits régis par la LADb. | Aucune dérogation à l’obligation de fournir les résultats d’essais de toxicité aiguë et de toxicité à doses répétées ne sera accordée |
a Polymères non-ERR – Polymères qui ne sont pas des polymères à exigences réglementaires réduites.
b LAD – Loi sur les aliments et drogues.
6.4 Exigences supplémentaires en matière de renseignements sur les substances biochimiques et les biopolymères (partie C)
Des renseignements supplémentaires sont exigés dans le cas des substances biochimiques et des biopolymères fabriqués ou importés, y compris les substances fabriquées ou importées qui appartiennent à l’une des catégories spéciales indiquées dans la partie 3.4 du Document d’orientation. Il faut fournir les renseignements suivant pour prendre en compte la nature du procédé de production (par exemple, utilisation d’un organisme vivant) et l’activité biologique potentiellement unique d’enzymes et d’acides nucléiques.
6.4.1 Renseignements exigés sur l’organisme de production (case C.1)
6.4.1.1 Identification, source et historique de l’organisme de production
Pour toute substance biochimique et tout biopolymère assujettis à n’importe quelle annexe du Règlement, l’organisme de production et, s’il y a lieu, l’organe duquel la substance est isolée doivent être précisés. Les désignations taxonomiques devraient être fondées sur le Code international de nomenclature et les sources taxonomiques standards. L’organisme utilisé pour produire la substance biochimique ou le biopolymère doit être indiqué en donnant sa désignation taxonomique au moins jusqu’au niveau de l’espèce et à un degré qui permet de distinguer l’organisme des espèces pathogènes voisines. Il faut corroborer l’identité de l’organisme à l’aide de méthodes qui sont conformes à celles utilisées actuellement en taxonomie microbienne. Lorsqu’il s’agit d’un organisme génétiquement modifié, il faut préciser l’organisme hôte et tous les organismes sources du matériel génétique exogène (organismes donneurs).
Ces renseignements doivent également comprendre :
- tous les synonymes, tous les noms communs et tous les noms périmés de l’organisme, s’ils sont connus, y compris les synonymes et les noms périmés de l’espèce. Il faut également indiquer tous les codes connus, employés à l’interne par les entreprises et les désignations de la collection de culture;
- la source originale et l’historique – le déclarant doit fournir des renseignements relatifs à l’historique de la souche du micro-organisme déclaré, depuis sa source originale d’isolation (souche environnementale ou clinique) jusqu’au développement du produit final. Ces renseignements comprennent toute banque de souche et tout numéro d’accès (par exemple, l’American Type Culture Collection) ainsi que l’historique des conditions d’entreposage et de culture. Il faut fournir un exemplaire de tout rapport publié sur l’isolement de souches, la caractérisation et toute modification génétique précédente.
S’il est soutenu que la dénomination de la substance déclarée soit considérée confidentielle, une dénomination maquillée devrait être fournie conformément au Règlement sur les dénominations maquillées. Les Lignes directrices pour la déclaration et les essais de substances nouvelles : organismes donne la marche à suivre pour maquiller une dénomination d’un micro-organisme.
6.4.1.2 Effets nocifs de l’organisme de production sur l’environnement ou la santé humaine
Ces renseignements sont exigés pour toute substance biochimique ou tout biopolymère assujetti à une quelconque annexe du Règlement. Il faut décrire les effets nocifs connus sur l’environnement ou la santé humaine qu’entraîne l’exposition à l’organisme de production. Les renseignements requis doivent être étayés par une revue de littérature approfondie.
La documentation présentée devrait inclure un exemplaire des résultats de la revue de littérature indiquant :
- la période visée par la recherche;
- la date à laquelle la recherche a été réalisée;
- les sources de renseignement (bases de données utilisées);
- les titres et les résumés des résultats de recherche en anglais ou en français;
- la stratégie de recherche et les termes utilisés.
Pour ces exigences de renseignements, un résumé des résultats de la revue de littérature qui montre clairement leur pertinence devrait être fourni. Si la plupart de ces renseignements se trouvent dans des publications récentes, il n’est pas nécessaire d’explorer les écrits scientifiques remontant à plusieurs années. Toutefois, s’il n’existe pas de publications récentes ou si elles sont non concluantes, non exhaustives ou contradictoires, une recherche bibliographique plus poussée sur une plus longue période devrait être menée. Des copies intégrales en anglais ou en français de tous les documents cités, y compris les brevets, doivent être fournies dans la réponse.
Lorsque les renseignements fournis sont fondés sur une revue de littérature, celle-ci doit avoir été réalisée dans les 6 mois qui précèdent la présentation de la déclaration et doit avoir exploré les principales sources de renseignements scientifiques.
Si une revue de littérature est effectuée en réponse à une exigence précise relative aux renseignements et que cette recherche est vaine, il faudra clairement l’indiquer dans la réponse pour cette exigence relative aux renseignements et inclure tous les renseignements concernant la revue de littérature effectuée. Il est à noter que dans ce cas, la recherche devrait être élargie et s’entendre aux trente dernières années.
6.4.1.3 Concentration de l’organisme de production viable (y compris dans les produits finis)
Ces renseignements sont exigés pour les substances biochimiques et les biopolymères assujettis à une quelconque annexe du Règlement. Il faut indiquer la concentration de l’organisme de production viable dans la substance biochimique ou le biopolymère, ainsi que, si elle est connue, sa concentration dans les produits finis. Ces concentrations doivent être exprimées en utilisant des unités de mesure précises (par exemple, CFU/mL).
Les organismes de production présents dans la substance déclarée peuvent être assujettis au Règlement sur les renseignements concernant les substances nouvelles (organismes); par conséquent, leur concentration doit être mesuré et signalé et la méthode de dosage employée doit être décrite. De plus, la présence d’organismes viables dans une substance peut entraîner une exposition à un organisme ou aux produits de son métabolisme et pourrait constituer un danger potentiel.
Au stade de la recherche et du développement menant à la fabrication, le nombre de personnes exposées à une substance est normalement faible et le procédé de fabrication à l’échelle pilote n’est pas nécessairement représentatif des conditions qui existeraient pendant une production à échelle réelle. Pour ces raisons, il n’est pas nécessaire de déterminer la concentration de l’organisme ou des organismes de production dans la substance déclarée s’il s’agit de substances destinées à la recherche et au développement ou de substances confinées intermédiaires limitées au site, qui sont fabriquées et consommées au site de fabrication et qui sont assujetties aux annexes 1 ou 3 du Règlement.
6.4.1.4 Méthode utilisée pour séparer l’organisme de production de la substance biochimique ou du biopolymère
Ces renseignements sont exigés pour les substances biochimiques assujetties aux annexes 1, 5 ou 6 du Règlement et les biopolymères assujettis aux annexes 3, 10 ou 11 du Règlement. Ils doivent comprendre une description de la méthode ou des méthodes employées pour séparer l’organisme de production de la substance biochimique ou du biopolymère.
Ces renseignements ne sont pas exigés pour les substances destinées à la recherche et au développement, assujetties aux annexes 1 ou 3 du Règlement.
6.4.2 Renseignements exigés sur les substances biochimiques et les biopolymères (case C.2)
6.4.2.1 Produits encodés
Ces renseignements sont exigés pour les substances biochimiques qui sont des acides nucléiques (unités répétitives de désoxyribonucléotides ou de ribonucléotides) et qui sont assujetties aux annexes 1, 5 ou 6 du Règlement et des biopolymères qui sont des acides nucléiques assujettis aux annexes 3, 10 ou 11 du Règlement. Cela comprend l’identification des produits encodés, s’ils sont connus.
Ces renseignements ne sont pas exigés pour les substances destinées à la recherche et au développement ou les substances confinées intermédiaires limitées au site qui sont fabriquées et consommées au site de fabrication et qui sont assujetties aux annexes 1 ou 3 du Règlement.
6.4.2.2 Activités biologiques
Ces renseignements sont exigés pour les substances biochimiques qui sont des acides nucléiques (unités répétitives de désoxyribonucléotides ou de ribonucléotides) et qui sont assujetties aux annexes 1, 5 ou 6 du Règlement et des biopolymères qui sont des acides nucléiques assujettis aux annexes 3, 10 ou 11 du Règlement. Ces renseignements doivent comprendre une description des activités biologiques connues (par exemple, résistance aux antibiotiques) ou des effets nocifs connus sur l’environnement ou la santé humaine associés à l’acide nucléique ou aux produits encodés visés à l’article 5 de l’annexe 2.
Ces renseignements ne sont pas exigés pour les substances destinées à la recherche et au développement ou les substances confinées intermédiaires limitées au site, qui sont fabriquées et consommées au site de fabrication et qui sont assujetties aux annexes 1 ou 3 du Règlement.
6.4.2.3 Fonctions catalytiques
Il faut décrire toutes les fonctions catalytiques connues des substances biochimiques qui ont une capacité d’action enzymatique et qui sont assujetties aux annexes 1, 5 ou 6 du Règlement.
Ces renseignements ne sont pas exigés pour les substances destinées à la recherche et au développement ou pour les substances confinées intermédiaires limitées au site qui sont fabriquées et consommées au site de fabrication et qui sont assujetties aux annexes 1 du Règlement.
6.4.2.4 Numéro de classification des enzymes et dénomination
Le numéro de classification des enzymes à quatre chiffres, s’il est disponible, et la dénomination doivent être indiqués dans le cas des substances biochimiques ayant une capacité d’action enzymatique et et qui sont assujetties aux annexes 1, 5 ou 6 du Règlement.
Ces renseignements ne sont pas exigés pour les substances destinées à la recherche et au développement ou pour les substances confinées intermédiaires limitées au site, qui sont fabriquées et consommées au site de fabrication et qui sont assujetties aux annexes 1 du Règlement.
Les composés biochimiques qui sont des enzymes doivent être nommés en suivant strictement les règles de nomenclature de l’Union internationale de biochimie et biologie moléculaire (UIBBM) ou du CAS. Les termes pour un groupe, comme protéase, ne sont pas acceptables. Le nom doit identifier de manière unique un seul enzyme (par exemple, subtilisine produite par Bacillus subtilis).
Les numéros de classification des enzymes, qui sont attribués par le comité de la nomenclature de l’UIBBM, sont couramment désignés sous l’appellation « numéro UIBBM ». Ils constituent la source de systèmes de nomenclature et de classification des enzymes acceptés à l’échelle internationale.
Le numéro de classification des enzymes comprend 4 chiffres, dont le premier indique l’une des 6 principales classes de substances catalytiques basées sur la réaction catalysée, le deuxième et le troisième indiquent des sous-classes et le quatrième correspond au numéro de série de la substance catalytique dans sa sous-classe. Il s’agit d’un numéro unique attribué à une substance ayant une activité catalytique. Lorsqu’une enzyme est déclarée, il faut obtenir et mentionner le numéro de classification des enzymes jusqu’au quatrième niveau le plus précis. Par exemple, pour désigner le mannitol déshydrogénase (cytochrome), le numéro de classification des enzymes 1.1.2 ne serait pas acceptable. Le numéro approprié dans cet exemple serait 1.1.2.2.
Les numéros de classification des enzymes sont répertoriés sur la page Web de la Nomenclature des enzymes de l’UIBBM (en anglais seulement).
6.4.2.5 Caractéristiques spécifiques des substrats
Ces renseignements sont exigés pour les substances biochimiques ayant une capacité d’action enzymatique et assujetties aux annexes 1, 5 ou 6 du Règlement. Les renseignements fournis doivent comprendre les caractéristiques spécifiques connues des substrats pour chacune des fonctions catalytiques visées par l’article 7 de l’annexe 2 du Règlement.
Ces renseignements ne sont pas exigés pour les substances destinées à la recherche et au développement ou pour les substances confinées intermédiaires limitées au site, qui sont fabriquées et consommées au site de fabrication et qui sont assujetties aux annexes 1 du Règlement.
6.4.2.6 Le pH et la température optimaux
Ces renseignements sont exigés pour les substances biochimiques ayant une capacité d’action enzymatique et assujetties aux annexes 1, 5 ou 6 du Règlement. Les renseignements fournis doivent comprendre le pH et la température optimaux pour les substrats visés par l’article 9 de l’annexe 2 du Règlement.
Ces renseignements ne sont pas exigés pour les substances destinées à la recherche et au développement ou pour les substances confinées intermédiaires limitées au site qui sont fabriquées et consommées au site de fabrication et qui sont assujetties aux annexes 1 du Règlement.
6.4.2.7 Constantes catalytiques KM et Kcat
Ces renseignements sont exigés pour les substances biochimiques ayant une capacité d’action enzymatique et assujetties aux annexes 1, 5 ou 6 du Règlement. Les renseignements fournis doivent comprendre les constantes catalytiques KM et Kcat et les conditions dans lesquelles celles-ci ont été mesurées.
Ces renseignements ne sont pas exigés pour les substances destinées à la recherche et au développement ou pour les substances confinées intermédiaires limitées au site, qui sont fabriquées et consommées au site de fabrication et qui sont assujetties aux annexes 1 du Règlement.
6.4.2.8 Cofacteurs
Ces renseignements sont exigés pour les substances biochimiques ayant une capacité d’action enzymatique et assujetties aux annexes 1, 5 ou 6 du Règlement. Les renseignements fournis doivent comprendre les cofacteurs connus nécessaires à l’activité enzymatique (par exemple, la NADPH et la coenzyme Q).
Ces renseignements ne sont pas exigés pour les substances destinées à la recherche et au développement ou pour les substances confinées intermédiaires limitées au site, qui sont fabriquées et consommées au site de fabrication et qui sont assujetties aux annexes 1 du Règlement.
6.4.2.9 Activité enzymatique
Ces renseignements sont exigés pour les substances biochimiques ayant une capacité d’action enzymatique et assujetties aux annexes 1, 5 ou 6 du Règlement. Les renseignements fournis doivent comprendre l’activité par unité de poids des produits et, si elle est connue, celle des produits finis.
Ces renseignements ne sont pas exigés pour les substances destinées à la recherche et au développement ou pour les substances confinées intermédiaires limitées au site, qui sont fabriquées et consommées au site de fabrication et qui sont assujetties à l'annex 1 du Règlement.
6.5 Exigences relatives aux renseignements supplémentaires (partie D)
Lorsque le déclarant utilise la partie D pour dresser la liste de toutes les pièces jointes, il doit cocher la case appropriée pour indiquer que le document fourni est confidentiel (c’est-à-dire, cocher la case « Oui » pour indiquer que les renseignements fournis sont confidentiels ou la case « Non » pour indiquer que les renseignements ne le sont pas). Le Programme des SN considère que les renseignements fournis ne sont pas jugés confidentiels si aucune des cases n’est cochée. Si les renseignements fournis sont jugés confidentiels, le déclarant doit présenter, dans la DSN, les renseignements supplémentaires décrits en détail dans la partie 7.2 du Document d’orientation.
6.5.1 Autres organismes (case D.1)
Ces renseignements sont exigés pour toutes les substances assujetties à une quelconque annexe du Règlement. Ces renseignements doivent comprendre :
- tous les cas où la fabrication ou l’importation de la substance ont été signalées à d’autres organismes gouvernementaux, au Canada ou à l’étranger, et l’objectif de l’avis donné;
- l’identité de l’organisme en question, si elle est connue, dont son nom au complet, ainsi que la ville et le pays où il se trouve;
- le numéro de dossier attribué par l’organisme en question, le résultat de l’évaluation et les mesures de gestion des risques imposées par l’organisme, s’ils sont connus.
Par exemple, il se peut que qu’un fournisseur américain ait avisé l’US EPA en vertu des dispositions portant sur les avis relatifs à la préfabrication de la Toxic Substances Control Act.
6.5.2 Autres exigences (case D.2)
Ces renseignements sont exigés pour toutes les substances assujetties à une quelconque annexe du Règlement. Ils doivent inclure un résumé de tous les autres renseignements et de toutes les autres données d’essais sur la substance en question dont dispose la personne qui fabrique ou importe la substance, ou auxquels elle peut normalement avoir accès, et qui permettent de déterminer les dangers que présente la substance pour l’environnement et la santé humaine de même que le degré d’exposition de l’environnement et du public à la substance. Les responsables du Programme des SN utilisent tous les renseignements disponibles pour éclairer leur évaluation des risques, notamment les données provenant d’essais in vitro, les mécanismes d’action, les données toxicogénomiques ainsi que les données provenant d’autres nouvelles technologies. Les résumés devraient donner suffisamment de détails concernant la méthodologie et les résultats afin de permettre aux responsables du Programme des SN d’évaluer la pertinence et la qualité de ces renseignements. Les responsables du Programme des SN peuvent demander de consulter le rapport complet après avoir pris connaissance des résumés présentés.
Par « dont dispose la personne qui fabrique ou importe », on entend les renseignements qui se trouvent dans les bureaux de l’entreprise au Canada si la DSN a été présentée par une entreprise canadienne ou les renseignements qui se trouvent dans les bureaux du pays d’où provient la déclaration si la DSN a été présentée par une entreprise étrangère par l’intermédiaire d’un « agent canadien ». La formule « auxquels elle peut normalement avoir accès » s’applique aux renseignements se trouvant dans n’importe quel bureau de l’entreprise partout dans le monde ou dans un autre endroit où le déclarant peut y avoir accès.
6.5.3 Autres exigences concernant les nanomatériaux (case D.3)
Dans le cas des nanomatériaux, les responsables du Programme des SN peuvent exiger que le déclarant fournisse des renseignements additionnels, en plus des renseignements techniques exigés. Il faut également soumettre des renseignements tels que sur la taille des particules primaires et leur distribution granulométrique, l’état d’agglomération ou d’agrégation, la forme, la surface active, la fonctionnalisation de surface, le revêtement de surface et la charge superficielle de la substance. Ces renseignements sont recommandés pour toutes les substances assujetties à une annexe du Règlement quelle qu’elle soit.
En ce qui concerne la solubilité dans l’eau et l’essai in vitro pour déterminer la présence de mutations génétiques dans les cellules de mammifères, d’autres protocoles d’essai sont recommandés pour les nanomatériaux. Veuillez consulter les parties 6.3.1.3 et 6.3.3.5 du Document d’orientation.
6.5.4 Renseignements additionnels et pièces jointes (case D.4)
Dans certains cas, les responsables du Programme des SN peuvent exiger que le déclarant fournisse des renseignements additionnels, en plus des renseignements techniques exigés. Les exigences en matière de renseignements additionnels ne font pas partie du Règlement, car elles ne s’appliquent qu’à un petit sous-ensemble de substances déclarées. Par exemple, s’il est connu qu’une substance se répartit dans le sol ou les sédiments, les résultats d’un essai de toxicité sur un organisme vivant dans le sol ou benthique pourraient être nécessaires afin de réaliser une évaluation. L’essai de toxicité sur un organisme vivant dans le sol ou benthique peut également servir d’option de rechange pour satisfaire aux exigences en matière de renseignements, dont les données provenant d’essais de toxicité aiguë sur les poissons, la daphnie ou les algues.
Le tableau 6-3 décrit les données additionnelles qui pourraient être exigées dans certaines circonstances. Ces descriptions ont pour objet d’aviser les déclarants qu’ils pourraient devoir produire des données additionnelles. Il est recommandé à l’éventuel déclarant d’une substance correspondante à l’une des circonstances présentées au tableau 6-3 de présenter une demande de CAD (consulter la partie 8.8) avant de produire des renseignements techniques additionnels afin d’aborder au cas par cas la validité et la pertinence de chaque élément de données.
| Item | Substance | Autres renseignements techniquesa pouvant être exigés |
|---|---|---|
| 1 | Utilisée comme un additif dans un polymère (> 10 % en poids) et pour une utilisation à l’extérieur ou exposée aux intempéries (asphalte, revêtements époxydiques des pipelines, etc.) | Potentiel de lixiviabilité, toxicité du sol, potentiel d’efflorescence, potentiel de dégazage, produits de dégradation, potentiel de pénétrer dans la nappe phréatique |
| 2 | Utilisée dans les milieux d’eau salée | Toxicité marine, solubilité relative dans les eaux douces ou salées |
| 3 | Insoluble ou peu soluble dans l’eau ou pour laquelle il est prévu que le coefficient de partage entre l’octanol et l’eau soit élevé | Solubilité dans l’eau par agitation douce, facteur de bioconcentration, facteur de bioaccumulation, toxicité chronique en milieu aquatique, toxicité subchronique chez les mammifères (toxicocinétique) |
| 4 | Pour laquelle on prévoit un résultat négatif aux critères de l’essai de biodégradabilité immédiate | Biodégradation intrinsèque, toxicité subchronique chez les mammifères (toxicocinétique) |
| 5 | Tensioactive | Tension superficielle, concentration micellaire critique, irritation et sensibilisation cutanées, toxicité cutanée |
| 6 | Ionisable | Coefficient de partage (log D), constante de dissociation (pKa), tension superficielle |
| 7 | Pouvant se répartir dans le sol ou les sédiments | Toxicité en milieu benthique, toxicité du sol, toxicité pour les organismes terrestres |
| 8 | Biologiquement active (par exemple, produits pharmaceutiques) | Toxicité chronique en milieu aquatique, toxicité ou cancérogénicité subchronique chez les mammifères (toxicocinétique), produits issus de la dégradation métabolique, biodisponibilité relative (par voie cutanée ou orale) |
| 9 | Substance appauvrissant la couche d’ozone (par exemple les halons, définis dans le Protocole de Montréal) | Potentiel d’appauvrissement de la couche d’ozone, potentiel de réchauffement de la planète, essai de toxicité par inhalation chez les mammifères (toxicocinétique) |
| 10 | Cationique | Atténuation du potentiel de toxicité chez le poisson par les acides humiques |
| 11 | Disrupteur endocrinien potentiel | Essai de dépistage des mécanismes d’action in vitro, essai de métamorphose des amphibiens, essai de toxicité pour la reproduction sur 2 générations avec dépistage de troubles endocriniens |
| 12 | Nanomatériau confirmé ou potentiel (consulter l’appendice 10) | Taille des particules primaires, distribution granulométrique, état d’agglomération ou d’agrégation, forme, surface active, fonctionnalisation de surface, revêtement de surface, charge superficielle, etc; Potentiel de libération de la substance à partir d’un produit final, toxicité du sol, essai de toxicité par inhalation chez les mammifères (incluant la toxicocinétique), essai de génotoxicité (autre que l’essai d’Ames) |
| 13 | Phtalate ou produits ignifuge ou substance perfluorée | Toxicité chronique en milieu aquatique, toxicité pour la reproduction et le développement, toxicité subchronique chez les mammifères (toxicocinétique), essai de dépistage des mécanismes d’action in vitro |
| 14 | Métal et composé métallique | Transformation et dissolution en milieu aqueux, toxicité subchronique chez les mammifères (toxicocinétique) par mode d’exposition approprié, sensibilisation cutanée, cancérogénicité |
| 15 | Enzyme | Séquences en acides aminés de l’enzyme d’origine et de l’enzyme mutée |
a Veuillez consulter les Lignes directrices de l’OCDE pour les essais de produits chimiques pour connaître les méthodes d’essai normalisées reconnues à l’échelle internationale.
Le déclarant doit fournir tous les renseignements et données relatives à l’identification des risques pour l’environnement et la santé, notamment :
- les données expérimentales (incluant les résultats négatifs);
- les résumés des revues de littérature;
- les résultats des recherches dans des bases de données effectuées par le déclarant;
- les analyses des relations structure–activité effectuées sur la substance ou sur des substances de structure semblable;
- les rapports indiquant des effets nocifs résultant de l’utilisation de la substance déclarée dans un lieu de travail;
- les résultats d’études du risque pour les employés, les clients, le public ou l’environnement (par exemple, des données de modélisation du devenir de la substance dans l’environnement) que peut présenter l’utilisation de la substance;
- les données toxicogénomiques.
Le déclarant peut aussi fournir des renseignements sur les éventuels bénéfices pour l’environnement de la fabrication ou de l’utilisation de la substance déclarée. Si ces bénéfices découlent du remplacement pour une autre substance, il faut fournir les renseignements dans la case A.15.6 du formulaire de DSN. Voici quelques exemples de ces avantages :
- La substance constitue une solution de rechange « moins toxique » d’une substance ou d’une technologie existante;
- La substance est récupérée d’un flux de déchets;
- La fabrication ou l’utilisation de la substance générera moins de déchets que celle d’une substance existante;
- La substance peut être recyclée.
Les renseignements additionnels peuvent être fournis dans la langue dans laquelle les renseignements originaux ont été préparés. Les responsables du Programme des SN demandent qu’au moins un résumé des renseignements additionnels soit présenté en français ou en anglais.
6.6 Renseignements sur l’exposition humaine et environnementale (connus et prévus) [partie E]
La partie E du formulaire de DSN indique tous les renseignements relatifs à la fabrication, l’importation, l’utilisation et le rejet prescrits par le Règlement. Cette partie demande également certains renseignements qui ne sont pas exigés par le Règlement mais qui sont particulièrement pertinents pour la prévision des rejets dans l’environnement et une potentielle exposition des humains à la substance nouvelle.
Les renseignements fournis dans cette partie sont directement utilisés dans l’évaluation des risques pour évaluer l’exposition potentielle et le rejet de la substance nouvelle pendant toutes les étapes principales de son cycle de vie. Cela comprend entre autres le transport, l’entreposage, la fabrication, la formulation et la transformation, le nettoyage de l’équipement, l’utilisation et la manipulation des déchets et leur élimination.
Cette évaluation des risques tient compte de l’exposition résultant des activités prévues par le déclarant ainsi que des activités potentielles des entreprises de transformation en aval et des utilisateurs de la substance. Si certains renseignements ne sont pas connus par le déclarant, notamment lorsque les renseignements portent sur des activités menées à un site géré par d’autres parties (par exemple, fabrication ou formulation), le déclarant doit fournir les réponses dont il a connaissance ou qui sont facilement vérifiables en communiquant avec des fournisseurs ou des clients. Les renseignements sur l’exposition fournis dans l’avis relatif à la préfabrication de l’US EPA peut également être fournis pour aider à l’évaluation.
Il faut remplir toutes les sections de cette partie de manière la plus complète possible si les renseignements sont connus. En l’absence de renseignements détaillés, les responsables du Programme des SN retiennent généralement les estimations prudentes et les renseignements de modélisation pour évaluer l’ampleur de l’exposition potentielle.
6.6.1 Quantités annuelles prévues pour la fabrication, l’importation et l’exportation de la substance déclarée (case E.1)
Déclarer la quantité de la substance pure, sans les solvants ou les autres composants si la substance se trouve dans un mélange. Pour les déclarations consolidées, indiquer les quantités pour chaque substance.
6.6.1.1 Quantité de la substance fabriquée, importée et exportée (case E.1.1)
Ces renseignements sont exigés pour les substances assujetties à n’importe quelle annexe prescrite par le Règlement.
Remplir le tableau en suivant les instructions suivantes :
- Quantité fabriquée au Canada : indiquer la quantité annuelle anticipée de substance qui sera fabriquée au Canada, le cas échéant. Ces renseignements doivent comprendre les quantités prévues pour les douze premiers mois et, si elle est connue, la quantité maximale qui est envisagée de fabriquer pendant toute période future de douze mois, en kg/an. Si aucune fabrication n’est prévue, il faut l’indiquer;
- Quantité importée au Canada : indiquer la quantité annuelle anticipée de substance qui sera importée au Canada, le cas échéant. Ces renseignements doivent comprendre les quantités prévues pour les douze premiers mois et, si elle est connue, la quantité maximale qui est envisagée d’importer pendant toute période future de douze mois, en kg/an. Si aucune importation n’est prévue, il faut l’indiquer;
- Quantité à exporter : indiquer les quantités annuelles prévues qui seront fabriquées au Canada ou importées au Canada aux fins d’exportation, le cas échéant. Ces renseignements doivent inclure les quantités prévues pour les douze premiers mois et, si elle est connue, la quantité maximale qui est envisagée d’exporter pendant toute période future de douze mois, en kg/an. Si aucune exportation n’est prévue, il faut l’indiquer.
6.6.1.2 Sites canadiens où se trouveront les plus grandes quantités de la substance (case E.1.2)
Ces renseignements sont exigés pour les substances chimiques assujetties aux annexes 5 ou 6 du Règlement et pour les polymères non-ERR assujettis aux annexes 9, 10 ou 11 du Règlement. Pour les substances confinées qui sont intermédiaires limitées au site et assujetties aux annexes 1 ou 3 du Règlement, l’emplacement unique d’utilisation est requis.
Remplir le tableau selon les instructions suivantes :
- Sites : s’ils sont connus, nommer les 3 sites (noms d’entreprise et adresses) au Canada où il est prévu que les plus grandes quantités de la substance, fabriquée ou importée par le déclarant, soient utilisées ou transformées;
- Quantité : indiquer la quantité utilisée ou transformée estimée au site (en kg/an).
6.6.2 Utilisations mettant en cause la substance (case E.2)
6.6.2.1 Description des activités au Canada (case E.2.1)
Ces renseignements sont exigés pour les substances assujetties à n’importe quelle annexe prescrite par le Règlement. Toute activité industrielle, commerciale et par les consommateurs mettant en cause la substance au Canada (par exemple fabrication, importation et distribution, formulation industrielle, reformulation d’un concentré, activité commerciale) doit être décrite, dans la mesure où les renseignements sont connues ou raisonnablement vérifiables. Cela doit inclure les activités entreprises par le déclarant ainsi que par les entreprises de transformation en aval et les utilisateurs de la substance au Canada.
Si la substance est importée au Canada, une description du produit importé contenant la substance déclarée (par exemple substance déclarée pure, produit intermédiaire, produit fini) doit être fournie.
Les activités industrielles, commerciales et par les consommateurs peuvent être définies comme suit :
- Activités industrielles : la substance ou des produits contenant la substance seront utilisés aux sites des fabricants, des entreprises/utilisateurs de transformation à grande échelle (par exemple teinture de textile, formulation de peinture, utilisation d’une résine durcissable pour fabriquer un produit);
- Activités commerciales : la substance ou des produits contenant la substance seront utilisés par une entreprise commerciale qui offre un service à la consommation (par exemple établissement commercial de nettoyage à sec, entrepreneurs de peinture, couvreurs de toits pour la construction de bâtiments commerciaux);
- Activités par les consommateurs : la substance ou des produits contenant la substance seront utilisés par des particuliers (par exemple produits de soins personnels, huile pour automobiles, détergent à vaisselle).
6.6.2.2 Utilisations finales, fonctions et concentrations prévues de la substance (case E.2.2)
Le but de cette partie est de décrire comment la substance est importée et d’indiquer si elle est mélangée dans des produits intermédiaires avant d’être intégrée aux produits finis. Elle vise également à obtenir des renseignements sur la fonction et les utilisations finales de la substance dans les produits existants ou prévisibles qui la contiennent.
Donner la concentration ou la gamme de concentrations de la substance déclarée, dans le produit sous la forme dans laquelle il sera importé ou fabriqué au Canada. Ces renseignements sont exigés pour les substances chimiques assujetties aux annexes 1, 4, 5 ou 6 du Règlement et les polymères non-ERR assujettis aux annexes 3, 9, 10 ou 11 du Règlement.
Indiquer et décrire chaque produit fini prévu contenant la substance nouvelle (par exemple, peinture pour bâtiment, shampoing, lubrifiant pour automobile). Indiquer la fonction de la substance. La fonction est liée aux propriétés physiques et chimiques inhérentes de la substance (par exemple dégraisseur, catalyseur, plastifiant, absorbeur UV ou parfum). Indiquer si l’utilisation finale vise une activité industrielle, commerciale ou par les consommateurs. Indiquer la concentration de la substance, si elle est connue, ainsi que le pourcentage de la quantité annuelle. Le pourcentage de la quantité annuelle correspond au pourcentage de la quantité annuelle totale importée ou fabriquée pour chaque utilisation finale (la somme des pourcentages pour chaque utilisation finale devrait équivaloir à 100 %). Certaines substances peuvent avoir différentes utilisations qui doivent chacune être déclarées. Par exemple, un émollient dans du savon à mains peut servir de surfactant dans une cire pulvérisable pour voiture. Ces renseignements sont exigés pour toute substance assujettie à une quelconque annexe du Règlement.
Voici quelques exemples de fonctions et d’utilisations :
- Émollient dans du savon à mains;
- Excipient de colorants dispersés pour la finition de fibres de polyester;
- Agent de réticulation pour les revêtements de type époxy pour des surfaces métalliques;
- Ignifugeant pour l’application de surface sur des vêtements en coton, des meubles ménagers en tissu et des articles extérieurs en toile;
- Surfactant dans de la cire pulvérisable pour voiture;
- Colorant pour des produits papier et d’autres produits cellulosiques;
- Colorant réactif pour les moquettes en nylon et le rembourrage;
- Antioxydant dans le mazout et les lubrifiants.
6.6.2.3 Utilisations finales, fonctions et concentrations passées ou probables de la substance (case E.2.3)
Ces renseignements sont exigés pour les substances chimiques figurant sur la Liste extérieure et assujetties à l’annexe 5, les substances chimiques assujetties à l’annexe 6 et les polymères assujettis aux annexes 10 ou 11 du Règlement.
Le but de cette partie est d’obtenir des renseignements au sujet des utilisations finales et des fonctions passées ou probables de la substance nouvelle. Remplir le tableau en suivant les directives données à la partie 6.6.2.2. Ces utilisations et fonctions ne sont pas envisagées par le déclarant, mais il est connu qu’elles ont déjà existé dans d’autres territoires ou dans la documentation de brevet ou qu’elles sont comprises étant données les connaissances des propriétés de la substance.
Les responsables du Programme des SN recommandent que le déclarant indique tous les renseignements dont il a connaissance, cela même s’il n’envisage pas de poursuivre certaines utilisations. Par exemple, les surfactants destinés aux fins industrielles peuvent également servir dans des produits de soins personnels. Les renseignements détaillés à cet égard permettront au Programme des SN d’établir les caractéristiques de la substance relativement à l’exposition. Si peu de renseignements sont donnés, les évaluations d’exposition reposeront sur des estimations prudentes.
6.6.3 Exposition humaine (case E.3)
Le but de cette partie est d’obtenir des renseignements au sujet du potentiel de l’exposition directe des humains à la substance, y compris celles découlant de l’utilisation de produits de consommation. Si le déclarant ne dispose pas de renseignements précis sur le potentiel d’exposition humaine, les descriptions peuvent être basées sur des renseignements communiqués par des entreprises de transformation en aval et des utilisateurs de la substance ou sur les expériences découlant de l’utilisation de substances analogues. Le déclarant doit fournir tous les renseignements demandés dans la mesure où ils sont connus ou raisonnablement vérifiables. Si peu de renseignements sont donnés, les évaluations d’exposition reposeront sur des estimations prudentes.
6.6.3.1 Exposition humaine directe (case E.3.1)
Ces renseignements sont exigés pour les substances chimiques assujetties aux annexes 5 ou 6 du Règlement ou les polymères non-ERR assujettis aux annexes 9, 10 ou 11 du Règlement.
Décrire les circonstances prévues et l’ampleur prévisible de l’exposition directe des humains à la substance, y compris la concentration de la substance, la durée et la fréquence de l’exposition et la voie d’exposition (cutanée, orale ou respiratoire).
Indiquer s’il est prévu que la substance soit utilisée dans des produits destinés aux enfants. Le cas échéant, décrire les types de produits (par exemple shampoing, marqueurs).
Décrire toute condition d’utilisation ou facteurs pouvant limiter l’exposition directe des humains à la substance.
6.6.3.2 Degré d’exposition du public élevé (case E.3.2)
Ces renseignements sont exigés pour les substances assujetties aux annexes 1, 3 ou 10 du Règlement ou des substances chimiques figurant sur la Liste extérieure assujetties à l’annexe 5 du Règlement. Des données d’essais supplémentaires peuvent être exigées avant que les quantités de fabrication ou d’importation atteignent 50 000 kg/an, selon les résultats de l’évaluation de ces renseignements (consulter les parties 4.4.3.2 et 4.9.2.2).
Indiquer s’il est prévu que le degré d'exposition du public soit élevé à la substance dans un produit, compte tenu, notamment, de la concentration de la substance, de la durée et de la fréquence d’exposition, des circonstances menant à l’exposition (par exemple la voie d’exposition) et des facteurs qui pourraient réduire l’exposition directe des humains. Dans le cas contraire, fournir des renseignements démontrant que le degré d’exposition du public ne devrait pas être élevé.
6.6.4 Exposition environnementale (case E.4)
6.6.4.1 Description des activités (industrielles, commerciales et par les consommateurs) [case E.4.1]
Cette partie porte sur les étapes principales du cycle de vie où le rejet dans l’environnement pourrait survenir, y compris pendant la fabrication, la transformation, l’utilisation commerciale et les utilisations par les consommateurs de la substance ou des produits qui la contiennent. Dans de nombreux cas, ces étapes du cycle de vie peuvent concerner plusieurs utilisateurs de la substance, y compris des fabricants, des mélangeurs et des utilisateurs finaux distincts. Par exemple, dans le cas d’un surfactant utilisé dans des fluides pour le travail des métaux, il peut y avoir la fabrication du surfactant, la transformation en fluide pour le travail des métaux, et l’utilisation pendant des activités industrielles de découpage des métaux.
Dans la plupart des cas, le déclarant aura accès à des renseignements précis sur les activités qu’il gère. Si certains renseignements ne sont pas disponibles, par exemple lorsque les activités sont contrôlées par des entreprises de transformation en aval ou des utilisateurs de la substance, les descriptions peuvent être basées sur les renseignements disponibles et l’expérience avec des substances analogues. Le déclarant doit fournir tous les renseignements demandés dans la mesure où ils sont connus ou raisonnablement vérifiables. Si peu de renseignements sont donnés, les évaluations d’exposition reposeront sur des estimations prudentes.
Remplir les parties E.4.1A, E.4.1B et E.4.1C pour la substance, s’il y a lieu.
Fabrication ou transformation de la substance déclarée au Canada (case E.4.1A)
Ces renseignements sont exigés pour les substances fabriquées au Canada assujetties à n’importe quelle annexe prescrite par le Règlement.
Le terme transformation de la substance déclarée peut couvrir la formulation ou le mélange de la substance.
Pour la description des activités ou le diagramme de leur déroulement, indiquer les étapes principales en mettant l’accent sur les flux de déchets et les points de rejet potentiels de la substance pendant les activités et le nettoyage de l’équipement.
Si les mêmes activités se déroulent à différents sites avec des procédés très différents, ou s’il y a plusieurs activités, le tableau peut être reporduit pour déclarer les renseignements.
Remplir le tableau en suivant les instructions ci-dessous :
- Nombre de sites : inscrire le nombre de sites où la substance est fabriquée ou traitée;
- Activités d’exploitation par lot : tous les composants sont chargés ensemble dans un récipient ou dans une séquence prédéfinie jusqu’à ce que le produit voulu soit formé et ensuite déchargé en un seul lot. La transformation des lots subséquents doit attendre jusqu’à ce que le lot actuel soit terminé. Dans le tableau, fournir la quantité maximale produite par lot, le nombre maximal de lots quotidiens et le nombre maximal de lots qui devraient être produits par mois;
- Activités en continu : les composants sont continuellement chargés dans le récipient et le produit voulu est continuellement formé et déchargé. Dans le tableau, fournir la quantité maximale produite par jour et le nombre maximal prévu de jours d’activité par mois;
- Description des activités ou du diagramme : relever les étapes opérationnelles principales dans la fabrication de la substance en mettant l’accent sur les flux de déchets et les points de rejet potentiels de la substance. Il faut inclure une brève description ou un diagramme des étapes principales du procédé de fabrication qui indique :
- les éléments comme les réservoirs de transformation, les réservoirs de stockage et les tours de distillation;
- les points d’entrée de toutes les composantes;
- les points de rejet de la substance;
- Procédures de nettoyage : fournir une brève description des méthodes utilisées pour nettoyer l’équipement de production, les voies de transport et les récipients (par exemple aspiration, lavage à l’eau, lavage avec des solvants organiques) et la fréquence de nettoyage maximale (par exemple, chaque mois, après chaque lot).
Utilisations industrielles et commerciales (case E.4.1B)
Ces renseignements sont exigés pour les substances à utilisations industrielles et commerciales assujetties à n’importe quelle annexe prescrite par le Règlement.
Décrire les utilisations industrielles ou commerciales de la substance. Les utilisations industrielles comprennent, par exemple, la peinture des pièces automobiles, l’application de revêtements intérieurs de tuyaux et la lubrification d’équipement. Les utilisations commerciales comprennent, par exemple, le nettoyage à sec, les lave-autos et l’entretien des véhicules.
Pour remplir le reste du tableau, se reporter aux directives de la case E.4.1A.
Utilisations par les consommateurs (case E.4.1C)
Ces renseignements sont exigés pour les substances destinées aux utilisations par les consommateurs assujetties à n’importe quelle annexe prescrite par le Règlement.
Décrire les utilisations par les consommateurs de la substance. Ces utilisations comprennent, par exemple, le lavage de la vaisselle ou le changement d’huile à faire soi-même.
6.6.4.2 Description des activités de transport et d’entreposage (case E.4.2)
Ces renseignements sont exigés pour les substances chimiques assujetties aux annexes 1, 5 ou 6, du Règlement ou les polymères assujettis aux annexes 3, 10 ou 11 du Règlement.
Dans le passé, le nettoyage des récipients de transport et d’entreposage a causé des rejets dans l’environnement. Pour cette raison, l’évaluation de l’exposition effectuée pour chaque substance nouvelle accorde une attention particulière aux récipients utilisés pour le transport et l’entreposage de la substance.
Dans la plupart des cas, le déclarant aura accès à des renseignements précis sur les activités qu’il gère. Si certains renseignements ne sont pas disponibles, par exemple lorsque les activités sont contrôlées par des entreprises de transformation en aval ou des utilisateurs de la substance, les descriptions peuvent être basées sur les renseignements disponibles et l’expérience avec des substances analogues. Le déclarant doit fournir tous les renseignements demandés dans la mesure où ils sont connus ou raisonnablement vérifiables. Si peu de renseignements sont donnés, les évaluations d’exposition reposeront sur des estimations prudentes.
6.6.4.3 Limitation de l’exposition environnementale (case E.4.3)
Décrire tous les facteurs qui pourraient limiter l’exposition environnementale à la substance (par exemple incinération, traitement chimique, pratiques de prévention de la pollution, recyclage, exigences réglementaires existantes), y compris le traitement sur place. Ces renseignements sont exigés pour les substances chimiques figurant sur la Liste extérieure et assujetties à l’annexe 5, les substances chimiques assujetties à l’annexe 6 et les polymères assujettis aux annexes 10 ou 11 du Règlement.
Décrire les méthodes recommandées pour la destruction ou l’élimination de la substance. Ces renseignements sont exigés pour les substances chimiques assujetties aux annexes 1, 5 ou 6 du Règlement ou les polymères assujettis aux annexes 3, 10 ou 11 du Règlement.
Les activités de recyclage comprennent la récupération des composants chimiques utiles des déchets qui seraient autrement rejetées sous forme d’émissions atmosphériques, de déversement dans l’eau ou de dépôt sur le sol pendant la fabrication, la transformation ou l’utilisation. Toutes les descriptions peuvent être quantitatives ou qualitatives.
Pour les substances biochimiques et les biopolymères qui sont des protéines, une description des procédés de dénaturation ou de dégradation qui précèdent l’élimination ainsi qu’une description de l’activité résiduelle devraient être fournies si ces renseignements sont disponibles.
6.6.4.4 Manipulation des déchets contenant la substance (case E.4.4)
Les renseignements demandés dans cette partie sont fournis pour décrire et quantifier les rejets potentiels de la substance et des déchets dans l’environnement. Ils doivent inclure les renseignements sur toutes les activités industrielles et commerciales et sur les utilisations par les consommateurs au Canada.
Dans de nombreux cas, les rejets peuvent survenir à différentes étapes du cycle de vie où interviennent différents utilisateurs de la substance, dont les fabricants, les mélangeurs et les utilisateurs finaux distincts. Par exemple, dans le cas d’un surfactant utilisé dans un fluide pour le travail des métaux, cela peut couvrir la fabrication du surfactant, la transformation en fluide pour le travail des métaux, et l’utilisation pendant le découpage industriel de métaux.
Dans la plupart des cas, le déclarant aura accès à des renseignements précis sur les activités qu’il gère. Si certains renseignements ne sont pas disponibles, par exemple lorsque les activités sont effectuées par des entreprises de transformation en aval ou des utilisateurs de la substance, les descriptions peuvent être basées sur les renseignements disponibles et l’expérience avec des substances analogues. Le déclarant doit fournir tous les renseignements demandés dans la mesure où ils sont connus ou raisonnablement vérifiables. Si peu de renseignements sont donnés, les évaluations d’exposition reposeront sur des estimations prudentes.
Les renseignements au sujet des rejets de la substance découlant de toute activité industrielle et commerciale et de toute utilisation par les consommateurs au Canada doivent être fournis. Les rejets provenant des procédés opérationnels et du nettoyage de l’équipement et des récipients de transport et d’entreposage doivent être inclus. Ces renseignements sont exigés pour les substances chimiques assujetties aux annexes 1, 5 ou 6 du Règlement ou les polymères assujettis aux annexes 3, 10 ou 11 du Règlement.
Les renseignements à fournir comprennent les composantes de l’environnement dans lesquelles il est prévu que la substance sera rejetée (par exemple plan d’eau récepteur, terres agricoles, air). Ces renseignements sont exigés pour les substances chimiques assujetties aux annexes 1, 5 ou 6 du Règlement ou les polymères assujettis aux annexes 3 ou 11 du Règlement.
S’il y a différentes sources de rejets, le tableau peut être reproduit pour déclarer les renseignements.
Si des déchets contenant la substance ne sont produits par aucune des activités industrielles et commerciales et aucune des utilisations par les consommateurs au Canada, une explication devrait être fournit dans la case appropriée à cet effet pour justifier pourquoi il n’y a aucune production de déchet contenant la susbtance.
6.6.4.5 Rejets dans l’environnement aquatique en grande quantité (case E.4.5)
Ces renseignements sont exigés pour les substances chimiques figurant sur la Liste extérieure et assujetties à l’annexe 5 du Règlement ou les polymères assujettis à l’annexe 10 du Règlement. D’autres données d’essais pourraient être nécessaires avant que les quantités fabriquées ou importées atteignent 50 000 kg/an, selon les résultats de l’évaluation de ces renseignements (consulter les parties 4.4.3.1 et 4.9.2.1).
Il faut indiquer s'il est prévu que la substance soit rejetée dans l’environnement aquatique en une quantité supérieure à 3 kg par jour par site, la moyenne devant être calculée sur une base mensuelle et après traitement des eaux usées (c’est-à-dire si la substance devrait mener à des rejets dans l’environnement en grande quantité). Si le rejet est égal ou inférieur à 3 kg par jour par site, fournir les données qui permettent d’estimer la quantité rejetée. La partie suivante fournit des directives détaillées sur les exigences ainsi que sur la manière de calculer les estimations de rejets dans l’environnement en grande quantité.
6.6.5 Calculs des rejets dans l’environnement aquatique en grande quantité
En général, pour calculer les rejets quotidiens dans l’environnement aquatique basés sur une moyenne mensuelle, RQmoy mens, il est possible d’utiliser pour chaque site la formule suivante :
Où :
- JRM = nombre de jours de rejet par mois
- QR = quantité rejetée pendant les jours de rejets
- EE = efficacité d’élimination après le traitement des eaux usées
- 30,417 = nombre moyen de jours dans un mois
On présume généralement qu’un jour de rejet signifie un événement de rejet, mais il peut y en avoir plus. Par exemple, si le déclarant ou un utilisateur en aval rejette 5 kilos de la substance déclarée à une usine municipale de traitement des eaux le matin et 3 autres kilos l’après-midi, le jour de rejet inclut alors la somme de ces quantités par jour ou, dans ce cas-ci, la quantité rejetée (QR) au cours du jour de rejet sera de 8 kg/jour.
Un mois moyen comporte 30,417 jours, soit le résultat de 365 ÷ 12. Cette valeur sert à comptabiliser les rejets dont la moyenne est calculée sur une base mensuelle.
6.6.5.1 Estimation du nombre de jours de rejets par mois
Le nombre de jours de rejet par mois (JRM) dépend des activités et peut varier tout au long de l’année, quel que soit le site. Voici quelques scénarios en exemple :
- Rejets survenant 7 jours par semaine tout au long de l’année : s’il y a eu des rejets chaque jour de l’année, le JRM équivaut alors au nombre type de jours dans un mois, c’est-à-dire 30,417 jours/mois;
- Rejets survenant 5 jours par semaine : s’il y a généralement eu des rejets 5 jours par semaine, mais que les activités faisant intervenir la substance n’ont eu lieu que 200 jours dans l’année, il faut sélectionner le mois de l’année affichant le pire scénario (c’est-à-dire chaque semaine) et multiplier cette valeur par le nombre moyen de semaines par mois, soit (4,345 semaines/mois) × (5 rejets/semaine) pour obtenir un JRM de 22 jours/mois;
- remarque : 30,417 jours/mois ÷ 7 jours/semaine = 4,345 semaines/mois
- Rejets survenant pendant une semaine seulement dans l’année : par exemple, si les activités de l’installation rejettent la substance pendant 5 jours consécutifs dans l’année, cette valeur est utilisée pour représenter le mois affichant le pire scénario et le JRM est de 5 jours/mois;
- Rejets survenant une ou deux fois par mois tout au long de l’année : si l’installation rejette la substance déclarée une ou deux fois chaque mois tout au long de l’année, le JRM reflète alors le mois affichant le pire scénario et est établi à 2 jours/mois.
6.6.5.2 Détermination de la quantité rejetée les jours de rejet
La QR peut être déterminée pour des rejets continus ou des rejets périodiques. S’il est connu qu’une certaine quantité de la substance est perdue chaque jour de rejet, ce facteur peut être appliqué directement en tant que QR. Si aucun des scénarios ci-dessous ne s’applique, des preuves doivent être fournies à l’appui de la QR.
Rejets quotidiens continus
Si les rejets vers une usine de traitement des eaux usées sont continus et ont lieu quotidiennement toute l’année, la QR pourra alors être déterminée sur la base de la quantité annuelle ainsi que d’une fraction perdue estimée ou mesurée durant les activités, par exemple découlant du nettoyage de l’équipement ou des pertes de fonctionnement. Par exemple, si la quantité annuelle de la substance est de 20 000 kg/an à un site pendant plus de 250 jours et qu’il est connu ou il est estimé que 3 % de la substance est perdue durant des opérations, la quantité moyenne rejetée les jours de rejet est alors calculée comme suit :
Exemple 1
QR = 20 000 kg/an × 0,03 ÷ 250 = 2,4 kg/jour
Par conséquent, la QR sera de 2,4 kg/jour.
Rejets périodiques
Si le rejet est occasionné par le nettoyage périodique de la tuyauterie de transport et les récipients à mélange après la production de plusieurs lots, il faut alors tenir compte de la quantité de rejet spécifique au cours de ce processus particulier. Par exemple, si la quantité totale de la substance dans un lot quelconque est de 2 000 kg, le niveau résiduel de la substance dans l’équipement avant le nettoyage est de 2,5 % et les opérations de nettoyage ont lieu pendant une journée, la quantité rejetée de la substance pendant le jour de rejet est estimée comme suit :
Exemple 2
QR = 2 000 kg/lot × 0,025 ÷ 1 jour = 50 kg/jour
Par conséquent, la QR est de 50 kg/jour.
6.6.5.3 Détermination de l’efficacité d’élimination du traitement des eaux usées
L’efficacité d’élimination (EE) de la substance par le traitement des eaux usées constitue un facteur important de l’équation appuyant l’estimation de rejets dans l’environnement en grande quantité. Il existe diverses manières de calculer l’EE. Par exemple, l’EE peut être déterminée en surveillant les influents et effluents réels d’une usine de traitement des eaux usées. Dans ce cas, une description des activités de surveillance doit être fournie. Dans la plupart des cas, on prévoit plutôt une estimation de l’EE. Les estimations peuvent être basées sur des propriétés physiques et chimiques et le jugement professionnel ou sur une modélisation simulée par ordinateur. Dans les deux cas, le processus ou les éléments probants doivent être décrits.
Par exemple, pour une structure et des propriétés physiques chimiques particulières, on estime à l’aide du programme d’estimation informatique EPI Suite™ de l’US EPA que l’efficacité d’élimination par le traitement des eaux usées est de 82 %. Cette valeur peut être considérée comme l'EE.
6.6.5.4 Exemples de calculs
Sur la base des scénarios ci-dessus, nous calculons les RQmoy mens suivants.
Exemple 1
JRM = 22 jours/mois
QR = 2,4 kg/jour
EE = 82 %
RQmoy mens = (22 jours/mois) x (2,4 kg/jour) x (1-0,82)/30,417 jours/mois
Par conséquent, le RQmoy mens est de 0,34 kg/jour par site, calculé sur une base mensuelle et, après le traitement des eaux usées, et il ne devrait pas se traduire par des rejets dans l’environnement aquatique en grande quantité.
Exemple 2
JRM = 2 jours/mois
QR = 50 kg/jour
EE = 82 %
RQmoy mens = (2 jours/mois) x (50 kg/jour) x (1-0,82)/30,417 jours/mois
Par conséquent, le RQmoy mens est de 0,59 kg/jour par site, calculé sur une base mensuelle et, après le traitement des eaux usées, et il ne devrait pas se traduire par des rejets dans l’environnement aquatique en grande quantité.
Partie 7. Renseignements confidentiels
En vertu de l’article 313 de la Loi canadienne sur la protection de l’environnement (1999) [la Loi], quiconque fournit des renseignements au gouvernement peut en même temps réclamer par écrit qu’ils soient considérés comme confidentiels. Cela empêche la divulgation publique des Renseignements commerciaux confidentiels (RCC). Le degré de protection des renseignements pour lesquels on demande la confidentialité est fonction des articles 314 à 321 de la Loi et des dispositions de la Loi sur l’accès à l’information.
7.1 Demande de confidentialité
La requête pour une demande de confidentialité doit obligatoirement être jumelée avec la Déclaration de substances nouvelles (DSN) afin que les renseignements soient traitées de manière confidentielle et elle doit:
- indiquer quels renseignements sont confidentiels dans la colonne du formulaire de DSN prévue à cette fin (les renseignements spécifiques fournis dans les pièces jointes au formulaire de DSN peuvent également être entre crochets [ ]);
- fournir tous les renseignements supplémentaires (décrits en détail dans la partie 7.2).
7.2 Renseignements à l’appui d’une demande de confidentialité
Le Programme des substances nouvelles (SN) a pour objectif d’assurer la protection des RCC tout en maintenant un certain niveau de transparence. Les demandes de confidentialité générales et les demandes liées à la confidentialité de l’identité d’une substance dans une DSN doivent être accompagnées des renseignements supplémentaires stipulés dans les parties 7.2.1 et 7.2.2. Les déclarants seront avisés si leur demande de confidentialité est inacceptable et ils auront la possibilité de l’examiner et de l’étayer avec des preuves supplémentaires. Si aucune preuve supplémentaire n’est fournie, la demande de confidentialité peut être rejetée, ce qui entraîne la publication non souhaitée des renseignements déclarés. Par ailleurs, le déclarant peut choisir de retirer sa demande de confidentialité.
7.2.1 Demandes de confidentialité générales
Les demandes de confidentialité doivent être présentées seulement lorsque les renseignements visés sont réellement de nature confidentielle, par exemple, lorsqu’il s’agit d’un secret industriel ou lorsque la divulgation des renseignements serait préjudiciable à la position concurrentielle de l’auteur de la demande. Afin de réduire le champ d’application des demandes de confidentialité et viser les renseignements qui sont réellement de nature confidentielle, une demande de confidentialité doit indiquer quels renseignements doivent être traités comme tels. Toute demande de confidentialité doit être appuyée par une justification décrivant la nature de la confidentialité. Cette justification devrait être sélectionnée à partir des critères suivants :
- Il s’agit d’un secret industriel de l’auteur de la demande;
- Il s’agit de renseignements de nature financière, commerciale, scientifique ou technique et sont toujours traités de façon confidentielle par l’auteur de la demande;
- On peut raisonnablement s’attendre à ce que leur divulgation entraîne des pertes ou des gains financiers importants ou encore à ce qu’elle soit préjudiciable à la position concurrentielle de l’auteur de la demande;
- On peut raisonnablement s’attendre à ce que leur divulgation nuise à des négociations d’ordre contractuel ou autre menées par l’auteur de la demande.
7.2.1.1 Renseignements qui, en règle générale, ne sont pas jugés confidentiels
Bien que le déclarant puisse faire une demande de confidentialité pour n’importe quel renseignement, il est attendu que certains types de renseignements utiles aux fins de l’évaluation des risques des substances et à d’autres fins liées à la protection de la santé humaine et de l’environnement ne soient pas confidentiels. La divulgation de ces renseignements est souhaitable pour promouvoir la transparence.
Les pays membres de l’ Organisation de coopération et de développement économiques (OCDE) s’entendent qu’aucune interdiction ne soit requise en ce qui a trait au partage des renseignements ci-dessous entre les gouvernements ou à la divulgation publique de ces renseignements.
La liste suivante indique les types de renseignements qui ne sont généralement pas confidentiels, bien qu’il soit entendu qu’il y aura des exceptions. Cette liste n’est pas restrictive et est fondée sur la Recommandation du Conseil relative à la liste de l’OCDE de données non confidentielles sur les produits chimiques de l’OCDE :
- Les noms commerciaux ou noms usuels;
- Les renseignements généraux sur les usages (les usages ne doivent être décrits qu’en terme généraux, par exemple, système ouvert ou fermé, agriculture, usage domestique, etc.);
- Les précautions à observer pour la sécurité de manipulation au cours de la fabrication, du stockage, du transport et de l’utilisation de la substance;
- Les méthodes recommandées pour l’évacuation et l’élimination;
- Les mesures de sécurité en cas d’accident;
- Les propriétés physicochimiques, à l'exception de celles qui révèlent l’identité de la substance (par exemple, les spectres). Si les propriétés physicochimiques permettent de déduire l’identité de la substance, seules des fourchettes de valeurs non-confidentielles doivent être fournies;
- Les résumés des données de santé, de sécurité et d’environnement comprenant des chiffres précis et des interprétations. Dans le cas d’une étude faisant l’objet d’une demande de confidentialité, l’auteur de l’étude sur la santé, la sécurité et l’environnement peut opter pour rédiger un résumé non confidentiel. En l’absence d’un résumé, Environnement et Changement climatique Canada et Santé Canada rédigent un résumé conforme au Modèle harmonisé de l’OCDE (en anglais seulement).
7.2.2 Demandes de confidentialité de l’identité d’une substance
Dans le cas d’une substance faisant l’objet d’une demande de confidentialité, les procédures pour la création d’une dénomination maquillée sont énoncées dans le Règlement sur les dénominations maquillées. Ces procédures sont détaillées davantage dans l’appendice 5 du Document d’orientation. Cette marche à suivre existe en vue d’assurer la protection des RCC tout en maintenant un certain niveau de transparence.
Le maquillage peut se faire en masquant certains aspects structuraux de la dénomination chimique de la substance tout en conservant son identité et sa structure moléculaire générique. Dans la plupart des cas, il est suffisant de maquiller une seule caractéristique de la structure, mais il est acceptable de maquiller plusieurs caractéristiques si cela peut être justifié.
La dénomination chimique de la substance est la dénomination établie conformément aux règles de nomenclature de l’Union internationale de chimie pure et appliquée (UICPA) ou du Chemical Abstracts Service (CAS). La dénomination explicite est exigé lorsqu’un formulaire de DSN, un formulaire de proposition d’inscription sur la Liste intérieure ou un formulaire de proposition d’inscription sur la Liste extérieure est présenté. Il convient de noter qu’une substance ne sera pas inscrite sur la Liste intérieure avant qu’une dénomination maquillée acceptable ait été reçue (consulter la partie 10.2 pour les critères d’admissibilité).
Les dénominations maquillées seront évaluées lors de la demande. Si la demande de confidentialité de la dénomination chimique est acceptable, la dénomination maquillée sera évaluée pour déterminer si elle est conforme au Règlement sur les dénominations maquillées. Si une dénomination maquillée est considérée comme inacceptable, le Programme des SN communiquera sa décision au déclarant qui devra fournir un autre nom. Si un consensus n’est pas atteint, le Programme publiera une dénomination maquillée qui, à son avis, respectera la demande de confidentialité présentée par l’entreprise tout en conservant la structure moléculaire générique de la substance. L’examen de la dénomination maquillée se fait séparément de l’examen de la DSN et n’a aucune incidence sur le délai d'évaluation de la substance. Le Programme des SN indiquera si la dénomination maquillée est acceptable dans les 60 jours suivant la réception d’une demande de dénomination maquillée complète. Veuillez noter que des droits sont exigés pour une demande de dénomination maquillée (consulter le tableau des frais à la page Web des Droits pour les déclarations de substances nouvelles).
L’article 88 de la Loi prévoit la publication d’une dénomination maquillée acceptable si la publication de l’identité réelle de la substance conduisait à la divulgation de RCC. Lorsque le déclarant demande la confidentialité de l’identité de la substance, il doit fournir, outre la justification décrite à la partie 7.2.1 du présent document, les renseignements précisés ci-dessous:
- Une proposition de dénomination maquillée élaborée par la méthode de maquillage prescrite (consulter l’appendice 5);
- La justification du maquillage de plus d’un segment descriptif (consulter la section A5.4);
- Les renseignements suivants :
- Les effets nuisibles que l’inclusion de l’identité de la substance dans la Liste intérieure ou dans toute autre publication aurait sur la position concurrentielle de l’entreprise du déclarant;
- La manière dont un concurrent pourrait utiliser l’identité de la substance;
- Une indication à savoir si l’identité de la substance est restée confidentielle dans la mesure où les concurrents ne savent pas qu’elle est fabriquée, importée ou utilisée;
- Une indication à savoir si la substance a été brevetée et qu’elle a donc été divulguée dans le brevet;
- Une indication à savoir s’il est de notoriété publique (par exemple, publications dans des journaux techniques ou des publications commerciales) que la substance soit fabriquée, importée ou utilisée;
- Les mesures qui ont été prises pour prévenir la divulgation involontaire de l’identité de la substance et l’ampleur de toute divulgation à ce jour;
- Une indication à savoir si la substance se retrouve, ou se retrouvera, dans des effluents, des émissions ou des déchets rejetés dans l’environnement;
- Une indication à savoir si la substance est ou sera contenue dans un produit accessible au public et si l’analyse du produit permet d’identifier la substance;
- La raison pour laquelle la substance est ou sera fabriquée, importée ou utilisée;
- Une indication à savoir si, dans la mesure des connaissances du déclarant, les responsables du Programme des SN, une autre entité fédérale, une entité provinciale ou territoriale ou une entité d’un gouvernement étranger a déjà déterminé si cette substance : 1) a un effet immédiat ou à long terme sur l’environnement, 2) constitue ou peut constituer un danger pour l’environnement ou 3) constitue ou peut constituer un danger pour la vie ou la santé humaines (si cela a déjà été déterminé, il faut fournir des détails).
Une dénomination maquillée acceptable dissimule le nom chimique tel que décrit ci-dessus. Ainsi, il n’est pas autorisé de remplacer un composant de la dénomination chimique par un synonyme pour ensuite le maquiller.
Durée de la demande de confidentialité concernant l’identité de la substance
Toute demande de confidentialité liée à l’identité de la substance sera révisée après une période de 10 ans pour aider à accroître la sensibilisation aux substances présentes sur le marché canadien. Le Programme des SN fera des efforts raisonnables pour contacter le déclarant avant la fin de cette période. Un avis sera communiqué au déclarant un minimum de 30 jours avant la date d’expiration afin qu’il puisse renouveler la demande s’il désire que l’identité de la substance demeure confidentielle pour une période additionnelle de 10 ans. Le déclarant doit suivre les instructions décrites dans la partie ci-dessus pour renouveler la demande de confidentialité.
7.2.3 Certains critères desquels les renseignements peuvent être divulgués
Il peut y avoir des cas où le gouvernement du Canada souhaite rendre publiques certains renseignements confidentiels. Ceux-ci incluent, mais sans s’y limiter, les cas dont la divulgation des renseignements est dans l’intérêt de la santé et la sécurité publiques ou de la protection de l’environnement ou lorsque la divulgation est nécessaire aux fins de l'administration ou de l'application de la Loi.
Le cas échéant, un examen sera effectué pour déterminer si certains renseignements déclarés confidentiels pourraient être divulgués afin de promouvoir la transparence ou parce que c’est dans l’intérêt supérieur des canadiens. Des efforts raisonnables seront faits pour contacter la personne qui a présenté les renseignements afin qu’elle puisse fournir des renseignements additionnels qui étayent la demande initiale.
L’article 316 de la Loi prévoit que les renseignements peuvent être communiqués dans toutes les circonstances suivantes :
- a) avec le consentement écrit de l’intéressé;
- b) en tant que de besoin pour l’exécution ou le contrôle d’application de la présente Loi;
- c) dans le cadre d’un accord ou arrangement conclu entre le gouvernement fédéral ou une de ses institutions et tout autre gouvernement au Canada ou à l’étranger, une organisation internationale ou une de leurs institutions, ou entre le ministre et un autre ministre fédéral, à la fois :
- (i) visant l’exécution ou le contrôle d’application d’une loi,
- (ii) aux termes duquel l’autre gouvernement, l’organisation internationale, l’institution ou l’autre ministre s’engagent à en protéger la confidentialité;
- d) dans le cadre d’un accord ou arrangement conclu entre le gouvernement fédéral et le gouvernement d’un État étranger ou une organisation internationale aux termes duquel ce dernier gouvernement ou l’organisation s’engage à en protéger la confidentialité;
- e) au médecin ou au professionnel de la santé désigné par règlement qui les demande en vue du diagnostic ou du traitement médical d’un patient nécessitant des soins urgents.
7.3 Détermination de la présence de substances confidentielles sur les listes
Les noms des substances figurant sur la partie confidentielle de la Liste intérieure ou la Liste extérieure sont publiés avec leur numéro d’identification confidentielle par le truchement de dénominations maquillées créées de la façon prescrite par le Règlement sur les dénominations maquillées, comme indiqué ci-dessus. Tout déclarant qui souhaite entreprendre la fabrication ou l’importation d’une substance qui, à son avis, figure sur la partie confidentielle de l’une ou l’autre de ces listes peut demander aux responsables du Programme des SN de confirmer sa présence. Les responsables du Programme des SN ne répondent à la demande que si le déclarant fournit une demande de recherche dans la partie confidentielle. Pour plus de renseignements, consulter la partie 2.3.1.
Partie 8. Protocoles d’essai recommandés et méthodes de rechange
Le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [le Règlement] prescrit des exigences en matière de renseignements techniques que le déclarant doit satisfaire en fournissant des données d’essai ou des demandes de dérogation. Dans le but de reconnaître les méthodes visant à remplacer, réduire ou raffiner l’utilisation des animaux dans les essais de toxicité traditionnels, le Programme des substances nouvelles (SN) accepte l’utilisation de méthodes de rechange appropriées (aussi appelées Nouvelles approches méthodologiques [NAM]) pour satisfaire à ces exigences en matière de renseignements techniques (consulter la partie 8.4).
8.1 Lignes directrices de l’Organisation de coopération et de développement économiques
Le paragraphe 15(1) du Règlement stipule que les conditions et les procédures d’essai à respecter dans l’obtention de données d’essai sur une substance doivent être compatibles à celles énoncées dans les Lignes directrices (LD) de l’Organisation de coopération et de développement économiques (OCDE) pour les essais de produits chimiques qui sont à jour au moment de l’obtention des données d’essai. Les LD de l’OCDE sont énoncées dans l’annexe 1 de la Décision du Conseil relative à l’acceptation mutuelle des données pour l’évaluation des produits chimiques de l’OCDE, adoptée par l’OCDE le 12 mai 1981.
Il faut déterminer si la méthode énoncée dans les LD de l’OCDE convient à la substance en question. Si des modifications à cette méthode sont apportées, il faut les signaler et les expliquer. Les LD de l’OCDE ne sont pas destinées à servir de méthodes d’essai rigides convenant pour toutes les substances; elles comportent assez de souplesse pour permettre aux experts d’exercer leur jugement et de s’adapter à l’évolution.
8.2 Méthodes d’essai recommandées
Les tableaux 8-1 à 8-4 ci-dessous donnent des exemples de méthodes d’essai basées sur les LD de l’OCDE et recommandées par les responsables du Programme des SN pour la production de données sur les propriétés physico-chimiques, la toxicité et l’écotoxicité des substances. L’acceptabilité de ces méthodes est fonction de l’applicabilité des méthodes à la substance à l’étude. La partie 8.6 du Document d’orientation présente les références pour les documents dans lesquels sont exposées les méthodes indiquées dans les tableaux 8-1 à 8-4.
| Exigence relative aux données | Annexes | Méthode d’essai |
|---|---|---|
| Point de fusion | 5, 6 | LD 102 de l’OCDEa |
| Point d’ébullition | 5, 6 | LD 103 de l’OCDE |
| Densité | 5, 6 | LD 109 de l’OCDE |
| Pression de vapeur | 5, 6 | LD 104 de l’OCDE |
| Solubilité dans l’eau | 5, 6 | LD 105 de l’OCDE |
| Coefficient de partage entre l’octanol et l’eau | 5, 6 | LD 107 ou 117 de l’OCDE |
| Spectre IR,b UV,c de masse ou RMNd | 6 | Selon les besoins |
| Adsorption et désorption | 6 et dans le cas de rejets dans l’environnement aquatique en grande quantité [paragraphe 7(2) du Règlement] | LD 106 ou 121 de l’OCDE, selon les besoins |
| Hydrolyse en fonction du pH | 6 et dans le cas de rejets dans l’environnement aquatique en grande quantité [paragraphe 7(2) du Règlement] | LD 111 de l’OCDE |
a LD de l’OCDE – Ligne directrice de l’Organisation de coopération et de développement économiques.
b IR – Infrarouge.
c UV – Ultraviolet.
d RMN – Résonance magnétique nucléaire.
| Exigence relative aux données | Annexes | Méthode d’essai |
|---|---|---|
| Masse moléculaire moyenne en nombre | 3, 9, 10, 11 | Selon les besoins (par exemple, LD 118 de l’OCDE)a |
| Composantes résiduelles dont la masse moléculaire est < 500 daltons et < 1 000 daltons | 3, 9, 10, 11 | Selon les besoins (par exemple, LD 119 de l’OCDE) |
| Extractibilité dans l’eau | 10, 11 | LD 120 de l’OCDE |
| Hydrolyse en fonction du pH | 10, 11 | LD 111 de l’OCDE |
| Coefficient de partage entre l’octanol et l’eau | 10, 11 | LD 117 de l’OCDE |
a LD de l’OCDE – Ligne directrice de l’Organisation de coopération et de développement économiques.
| Exigence relative aux données | Annexes | Méthode d’essai |
|---|---|---|
| Toxicité aiguë chez les mammifères | 5, 6, 10, 11 | LD 402, 403, 420, 423, 425, 436 de l’OCDEa |
| Irritation cutanée | 6, 11 | LD 404, 430, 431, 439 de l’OCDE; consulter aussi la partie 6.3.3.2 |
| Sensibilisation cutanée | 6, 11 | LD 406, 429, 442 (A-E)b de l’OCDE |
| Toxicité à doses répétées | 6, 11 et dans le cas de rejets dans l’environnement aquatique en grande quantité ou si le degré d’exposition du public est élevée [paragraphes 7(2), 7(3), 11(2) et 11(3) du Règlement] | LD 407, 408, 409, 410, 412, 413, 422 de l’OCDE |
| Génotoxicité | 5, 6, 11 et dans le cas de rejets dans l’environnement aquatique en grande quantité ou si le degré d’exposition du public est élevée [paragraphes 7(3), 11(2) et 11(3) du Règlement] | LD 471, 473, 474, 475, 476,c 487,c 488, 489, 490c de l’OCDE |
a LD de l’OCDE – Ligne directrice de l’Organisation de coopération et de développement économiques.
b Fournir la méthode d’essai 442A, 442B ou 442 (C-E) pour satisfaire aux exigences en matière de renseignements de la sensibilisation cutanée.
c Essai recommandé pour les essais in vitro de la génotoxicité des nanomatériaux.
| Exigence relative aux données | Annexes | Méthode d’essai |
|---|---|---|
| Toxicité aiguë chez les poissons | 5, 6, 10, 11 | LD 203 de l’OCDEa, méthodes d’essai biologique SPE 1/RM/9 et SPE 1/RM/13 d’Environnement Canada |
| Toxicité aiguë chez la daphnie | 5, 6, 10, 11 | LD 202 de l’OCDE, méthode d’essai SPE 1/RM/11 d’Environnement Canada |
| Toxicité pour les algues | 5, 6, 10, 11 | LD 201 de l’OCDE, méthode d’essai SPE 1/RM/25 d’Environnement Canada |
| Biodégradabilité immédiate | 5, 6, 11 | LD 301 de l’OCDE |
a LD de l’OCDE – Ligne directrice de l’Organisation de coopération et de développement économiques.
8.3 Rapport d’essai
Le déclarant est tenu de présenter un rapport d’essai fournissant suffisamment de renseignements pour permettre aux responsables du Programme des SN d’évaluer la qualité de ces analyses et leurs résultats. Au moment de fournir des données d’essai, ou des données provenant d’une méthode de rechange (consulter la partie 8.4), pour satisfaire à une exigence en matière de renseignements, l’ensemble de l’étude doit être fourni, y compris les renseignements suivants :
- Le numéro de la LD et la méthode employée;
- Le nom de la substance analysée (le nom de la substance inscrit dans le rapport d’essai doit correspondre au nom indiqué à la case A.19 du formulaire de Déclaration de substances nouvelles[DSN]), son degré de pureté et sa composition (consulter la partie 6.2.25);
- Les méthodes de référence, les normes et les contrôles utilisés;
- Le nom et l’adresse des installations d’essai et le nom de la personne responsable de l’étude;
- Les dates de début et de fin de l’étude;
- Les données brutes;
- Les écarts par rapport au protocole d’essai;
- Les détails sur l’analyse, y compris la préparation de l’échantillon ou des échantillons et le réglage de l’instrument ou des instruments;
- La présentation des résultats, des calculs et des méthodes statistiques employées.
8.3.1 Bonnes pratiques de laboratoire
Le paragraphe 15(2) du Règlement stipule que les pratiques de laboratoire pour l’obtention des données des essais énumérés ci-dessous doivent être conformes à celles énoncées dans les Principes de l’OCDE relatifs aux Bonnes pratiques de laboratoire (BPL) qui sont à jour au moment de l’obtention des données d’essai. Ces principes sont présentées à l’annexe 2 de la Décision du Conseil relative à l’acceptation mutuelle des données pour l’évaluation des produits chimiques de l’OCDE, adoptée par l’OCDE le 12 mai 1981 :
- a) essai de toxicité aiguë chez les mammifères;
- b) essai de toxicité de doses répétées chez les mammifères;
- c) essais de génotoxicité;
- d) essais de l’évaluation du degré d’irritation cutanée;
- e) essais de sensibilisation cutanée;
- f) essais de toxicité aiguë chez les poissons, la daphnie ou les algues;
- g) essais de biodégradabilité.
Si l’un ou l’autre des essais susmentionnés a commencé ou s’est terminé avant le jour de l’entrée en vigueur du Règlement (c’est-à-dire le 31 octobre 2005), les pratiques de laboratoire utilisées doivent être compatibles à celles énoncées dans les Principes de l’OCDE relatifs aux BPL.
Les Principes de l’OCDE relatifs aux BPL visent à promouvoir la qualité et la validité des données d’essai et à établir une base pour l’acceptation mutuelle des données parmi les diverses parties prenantes à l’échelle internationale. Ils recouvrent le processus organisationnel et les conditions dans lesquelles les études sont planifiées, réalisées, vérifiées, enregistrées et déclarées.
Veuillez consulter les documents de la Série de l’OCDE sur les Bonnes pratiques de laboratoire et vérification du respect de ces pratiques.
Pour être conforme aux BPL, le rapport final de l’essai doit indiquer le numéro d’enregistrement du Chemical Abstracts Service (CAS), la dénomination chimique ou le nom commercial ainsi que le degré de pureté de la substance mise à l’essai. Les renseignements suivants doivent également être inclus :
- Le nom, le titre et la signature, avec la date de signature, du directeur de l’étude;
- Une attestation du directeur de l’étude concernant la conformité aux BPL;
- Le nom, le titre et la signature, avec la date de signature, du chercheur principal;
- Le nom, le titre et la signature, avec la date de signature, du responsable du programme d’assurance de la qualité;
- Des attestations du responsable du programme d’assurance de la qualité concernant l’assurance de la qualité;
- Les dates des vérifications d’assurance de la qualité, y compris les vérifications effectuées pendant l’essai, et les explications afférentes.
Un rapport présenté au sujet d’un essai qui n’est pas conforme aux BPL ou qui n’est pas accompagné de tous les renseignements indiqués ci-dessus ne sera pas accepté et le délai d’évaluation ne commencera que lorsque les renseignements appropriés et acceptables auront été fournis.
Il convient de noter qu’il n’est pas obligatoire que les analyses des propriétés physico-chimiques soient conformes aux BPL.
8.3.2 Laboratoires accrédités
Si les données d’essai fournies proviennent d’une installation accréditée, il faut le signaler et en préciser le nom.
8.4 Méthodes de rechange
Le Programme des SN accepte l’utilisation de méthodes de rechange appropriées (aussi appelées NAM) pour satisfaire aux exigences en matière de renseignements techniques. Par exemple, les renseignements à l’appui d’une DSN peuvent aussi être tirés de l’utilisation de protocoles d’essai de rechange, de données de substitution, ou encore de méthodes de calcul ou d’estimation, plutôt que de produire des nouvelles données d’essais sur la substance déclarée. Ces méthodes de rechange sont acceptables lorsque, selon les responsables du Programme des SN, elles conviennent autant ou mieux que les méthodes de base pour la mesure du paramètre analysé aux fins de l’évaluation des risques.
Il n’est pas nécessaire de demander de dérogation à l’obligation de fournir des renseignements lorsqu’on présente des renseignements tirés de l’emploi d’une méthode de rechange acceptable.
Bien que cela ne soit pas obligatoire, les déclarants sont encouragés à présenter une demande de Consultation avant déclaration [CAD] (consulter la partie 8.8) lors de la préparation de leur DSN afin d’obtenir des conseils sur l’acceptabilité et l’utilisation de méthodes de rechange pour satisfaire à une exigence en matière de renseignement.
8.4.1 Protocoles d’essai de rechange
Les protocoles d’essai de rechange incluent, entre autres, les protocoles reconnus à l’échelle nationale ou internationale, par exemple les méthodes d’essai mises au point ou reconnues par le Programme des SN, l’Organisation internationale de normalisation (ISO) ou la Société américaine pour les essais et les matériaux (American Society for Testing and Materials - ASTM), ainsi que celles mises au point conformément à la Federal Insecticide, Fungicide, and Rodenticide Act (FIFRA) et à la Toxic Substances Control Act (TSCA) des États-Unis. En outre, des protocoles élaborés par des entreprises ou des associations peuvent aussi être acceptables. Ces protocoles comprennent notamment les protocoles d’essai de dépistage in vitro, les protocoles d’essai des mécanismes d’action, les protocoles d’essai toxicogénomique et les protocoles d’essai axés sur de nouvelles technologies. Le déclarant doit fournir les références exactes sur la méthode qu’il a employée et décrire celle-ci avec suffisamment de détails pour qu’elle puisse être évaluée.
Les protocoles de rechange doivent être clairement indiqués et doivent produire des données ayant un degré d’exactitude acceptable pour le Programme des SN. Le déclarant doit les décrire avec assez de détails pour que la méthode et les résultats puissent être évalués. Le Programme des SN évalue si le protocole de rechange fournit suffisamment de renseignements relativement à la LD pertinente de l’OCDE (consulter la partie 8.1) et veille à ce que la production des données requises soit selon un degré d’exactitude acceptable pour le programme afin de réaliser des évaluations correctes.
La description du protocole de rechange doit comprendre, mais sans s’y limiter :
- une description détaillée des principes et de la conception de l’essai;
- une description détaillée de la méthodologie et des contrôles utilisés;
- des études de validation de l’exactitude et de la variabilité de la méthode d’essai par rapport à la méthode prescrite;
- toute référence au protocole dans les publications scientifiques ou techniques.
Le déclarant doit présenter un rapport d’essai fournissant suffisamment de renseignements pour permettre au Programme des SN d’évaluer la qualité de ces analyses et leurs résultats (consulter la partie 8.3).
Par exemple, des essais épicutanés par applications répétées (réponse positive ou négative) sur l’humain peuvent constituer une option de rechange acceptable aux essais réalisés chez des animaux pour évaluer le degré d’irritation ou de sensibilisation cutanée. La concentration de la substance utilisée pour l’essai est un facteur critique pour déterminer le caractère acceptable des renseignements fournis. Il se peut qu’une expérience d’utilisation par les humains bien documentée puisse être une option de rechange acceptable aux protocoles prévus pour les paramètres toxicologiques, surtout en ce qui concerne l’irritation et la sensibilisation cutanée (réponse positive seulement). Il faut décrire correctement l’expérience d’utilisation en mettant tout spécialement l’accent sur la quantification la plus exacte possible de l’exposition (concentration de la substance, durée et fréquence de l’exposition). Les renseignements anecdotiques provenant de personnes qui ont manipulé la substance ou qui y ont été exposées ne constituent pas une option de rechange acceptable à un essai prévu.
Bien que cela ne soit pas obligatoire, les déclarants sont encouragés à présenter une demande de CAD (consulter la partie 8.8) lors de la préparation de leur DSN afin d’obtenir des conseils sur l’acceptabilité et l’utilisation du protocole d’essai de rechange.
8.4.2 Remplacement, réduction ou raffinement
Le Programme des SN appuie les principes de l’approche par remplacement, réduction ou raffinement visant l’emploi d’autres protocoles d’essai afin de réduire le plus possible l’utilisation et les souffrances des mammifères, pourvu que cela ne nuise pas à la qualité des renseignements produits pour l’évaluation des risques. La rigueur scientifique, la reproductibilité et la fidélité des mesures de la méthode de rechange employée doivent avoir été validées.
Les méthodes de remplacement sont celles qui ne font pas appel à un mammifère. Elles comprennent notamment l’utilisation de modèles numériques validés, de renseignements sur les propriétés physico-chimiques (par exemple, des renseignements sur le pH pour évaluer le risque d’irritation), d’organismes autres que des mammifères (par exemple, les poissons zèbre, les amphibiens) et d’essais in vitro sur des tissus, des embryons et des cultures cellulaires de mammifères.
Une méthode nécessitant moins d’animaux pour l’évaluation d’un paramètre particulier sans nuire à la valeur scientifique de l’essai serait une méthode de rechange respectant le principe de la réduction. Il existe de telles méthodes acceptées par des organismes de réglementation internationaux, par exemple les LD de l’OCDE de toxicité aiguë (LD 420, 423 et 425 de l’OCDE) et de sensibilisation cutanée (LD 429 de l’OCDE). Un autre exemple du principe de réduction est l’utilisation d’animaux autres que des mammifères (par exemple, les embryons de poisson zèbre) pour l’évaluation d’un paramètre particulier.
Les méthodes reposant sur le principe du raffinement visent à améliorer la conception ou l’efficacité d’un essai afin de mieux prédire la toxicité (par exemple, l’intégration de biomarqueurs additionnels comme des marqueurs d’immunochimie pour l’analyse d’un échantillon de sang). L’augmentation du nombre de paramètres de toxicité évalués lors d’un seul essai diminue le besoin pour des essais additionnels impliquant des organismes entiers. Le principe du raffinement peut aussi inclure plus de mesures pour réduire les souffrances ou l’inconfort imposés aux animaux de laboratoire pendant et après les essais. Par exemple, il est possible de regrouper les animaux ensemble pour réduire l’anxiété liée à l’isolement et d’éviter de les manipuler ou de les stresser inutilement.
8.4.3 Utilisation de données de substitution
Les données de substitution, ou données croisées, résultent une démarche par laquelle un paramètre mesuré expérimentalement d’une substance (appelée substance de substitution ou analogue) est utilisé pour prédire la production du même paramètre par une autre substance jugée semblable. Le principe général des données croisées est que les substances analogues par un ou plusieurs aspects devraient être analogues sous d’autres aspects, notamment leurs propriétés physiques et chimiques, et leur toxicité pour les mammifères ou l’environnement.
Les données croisées sont acceptables lorsque, selon les responsables du Programme des SN, elles conviennent autant ou mieux que les données sur la substance déclarée pour la mesure du paramètre analysé. Cette approche peut être utilisée pour répondre aux exigences relatives aux données prévues par le Règlement et pour lesquelles des données expérimentales ou d’étude ne sont pas disponibles. Toutefois, il est important de noter qu’une seule substance de substitution pourrait ne pas convenir pour tous les paramètres étudiés.
Les données croisées à l’appui peuvent être qualitatives (par exemple, la substance est mutagène) ou quantitatives (par exemple, concentration efficace médiane [CE50]).
8.4.3.1 Justification pour l’utilisation de données de substitution
Toute présentation de données de substitution à la place de données expérimentales sur la substance déclarée doit s’appuyer sur une justification scientifique expliquant le choix de la substance de substitution et l’utilisation de données croisées. Une justification séparée est exigée pour chaque exigence en matière de renseignement où des données de substitions sont fournis. De plus, il est recommandé d’inclure un tableau comparant la substance déclarée avec la ou les substances de substitution (consulter la partie 8.4.3.3). Dans la justification, les renseignements suivants devraient être fournis tant pour la substance déclarée que pour la ou les substances de substitution :
- Des renseignements d’identification, y compris, mais sans s’y limiter, la formule développée, la masse moléculaire et les groupes fonctionnels;
- Des données sur les propriétés physico-chimiques et le devenir environnemental.
Pour les paramètres écotoxicologiques et toxicologiques chez les mammifères, il faut notamment mentionner, outre la solubilité dans l’eau et les comparaisons des coefficients de partage entre l’octanol et l’eau, les renseignements suivants lorsqu’ils sont disponibles :
- Mode d’action;
- Mécanisme d’action;
- Biodisponibilité;
- Réactivité;
- Toxicocinétique;
- Voies et les produits métaboliques;
- Voies et les produits de dégradation.
La formule développée doit être présentée sous forme graphique. Elle doit être détaillée et les principaux éléments structuraux ou groupes fonctionnels susceptibles d’influencer un paramètre particulier doivent être montrés. Les similitudes et les différences entre les substances doivent être prises en compte et analysées.
Pour les paramètres écotoxicologiques et toxicologiques chez les mammifères, le niveau de confiance à l’égard des données de substitution peut être renforcé en démontrant que la substance déclarée et la substance de substitution s’inscrivent dans un certain groupe chimique qui présente une tendance de toxicité ou une toxicité similaire dans l’ensemble du groupe.
Si des données de substitution sont utilisées pour satisfaire à des exigences réglementaires, des rapports d’essai complets pour les études ainsi que leurs résultats doivent être fournis, y compris les éléments décrits dans la partie 8.3 du Document d’orientation. Les responsables du Programme des SN recommandent de fournir les rapports d’essai complets pour toute étude utilisée à titre de comparaison. Si elle est disponible, une évaluation de la fiabilité des résultats de l’étude devra également être fournie.
Si des publications scientifiques sont citées en référence, il faut fournir une copie de chacune d’elles. Les examens menés par d’autres organismes de réglementation doivent aussi être fournis, si possible.
Des estimations des relations quantitatives structure-activité (RQSA) peuvent être utilisées pour étayer la comparaison de la substance déclarée et de la substance de substitution dans le cadre d’une approche fondée sur des données croisées, notamment si la validité des estimations peut être démontrée (consulter la partie 8.4.4).
8.4.3.2 Exigences de justification supplémentaires pour certaines catégories de substances
La justification pour les catégories de substances décrites ci-dessous doit inclure, sans toutefois s’y limiter, une comparaison des éléments supplémentaires suivants pour la substance déclarée et la substance de substitution.
- Polymères :
- Des renseignements sur la masse moléculaire (c’est-à-dire chromatogrammes produits par chromatographie sur gel perméable (Gel Permeation Chromatography - GPC) ou d’exclusion stérique (Size-exclusion Chromatography - SEC), polydispersité, masse moléculaire moyenne en nombre (Mn), masse moléculaire moyenne en poids (Mw), pourcentage massique inférieur à 500 daltons et à 1 000 daltons);
- La composition en monomères et les concentrations initiales de monomères utilisées pour synthétiser les polymères;
- Les concentrations ou quantités de monomères résiduels ou excessifs;
- La présence de tout groupe fonctionnel réactif et tout calcul de la masse équivalente du groupe fonctionnel (MEGF) connexe (consulter la partie 3.3.1.8);
- Le plan de réaction des polymères.
- Substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques (substances of Unknown or Variable composition, Complex reaction products or Biological materials – UVCB) :
- La composition (structures et rapports représentatifs);
- La toxicité des composants majeurs ou clés;
- Les réactifs de départ et les conditions de réaction.
- Produits chimiques inorganiques :
- Des données sur la structure cristalline ou des données tridimensionnelles;
- La fraction métallique et le taux de dissolution;
- L’état ionique;
- La stabilité.
- Substances biochimiques et biopolymères (par exemple, enzymes) :
- La structure primaire (séquence d’acides aminés) alignée avec la substance déclarée afin de mettre en évidence les différences;
- Les propriétés propres aux enzymes (par exemple, constantes catalytiques KM et Kcat, pH et la température optimaux; consulter la partie 6.4.2).
Les facteurs pris en compte pour l’acceptation de toute substance de substitution potentielle pour les catégories de substances décrites ci-dessus peuvent être complexes. Ainsi, les déclarants sont encouragés à soumettre une demande de CAD (consulter la partie 8.8).
8.4.3.3 Tableau de comparaison
Afin de faciliter la comparaison de la substance déclarée et de la substance de substitution, il est recommandé que les données soient incluses dans un tableau. Des exemples de tableaux de comparaison sont présentés ci-dessous et peuvent être utilisés au besoin des déclarants pour organiser les comparisons. Si plusieurs substances de substitution sont utilisées, elles peuvent être disposées en colonnes dans un ordre adéquat (par exemple, selon leur masse moléculaire) afin de montrer une tendance ou une progression relativement à un paramètre cible dans le groupe. Les cellules du tableau doivent également indiquer si les données ne sont pas disponibles. Lorsque que cela s’applique, une description qualitative peut aussi être fournie. Si possible, le niveau de fiabilité des résultats d’étude devrait aussi être indiqué.
Voici des tableaux généraux montrant un échantillon de paramètres; ils ne constituent pas une liste exhaustive de tous les paramètres possibles. Étant donné que l’utilisation d’une approche fondée sur des données croisées est propre aux paramètres, tous les paramètres pour lesquels une substance de substitution potentielle est soumise aux fins d’étude doivent être clairement indiqués.
| Paramètre | Type | Substance déclarée | Substance de substitution 1 |
|---|---|---|---|
| numéro d’enregistrement CASa | Identification | * | * |
| Dénomination chimique | Identification | * | * |
| Formule développée (image) | Identification | * | * |
| Masse moléculaire (g/mol) | Identification | * | * |
| Indices de similarité (par exemple, Tanimoto, Dice) | Identification | * | * |
| Groupes fonctionnels et caractéristiques structurales pertinents | Identification | * | * |
| Pression de vapeur (Pa ou mm Hg) | Physico-chimiqueb | * | * |
| Solubilité dans l’eau (mg/L) | Physico-chimiqueb | * | * |
| Concentration micellaire critique | Physico-chimiqueb | * | * |
| Coefficient de partage octanol-eau | Physico-chimiqueb | * | * |
| Hydrolyse en fonction du pH | Physico-chimiqueb | * | * |
| Autres données (au besoin) | Physico-chimiqueb | ** | ** |
| Biodégradabilitéc | Devenir dans l’environnement | * | * |
| Toxicité chronique chez les poissons | Écotoxicologiqued | ** | ** |
| Toxicité aiguë chez la daphnie | Écotoxicologiqued | ** | ** |
| Autres données (au besoin) | Écotoxicologiqued | ** | ** |
| Toxicité aiguë chez les mammifères | Toxicologiquese | ** | ** |
| Toxicité chronique et sous-chronique | Toxicologiquese | ** | ** |
| Sensibilisation | Toxicologiquese | ** | ** |
| Autres données (au besoin) | Toxicologiquese | ** | ** |
a CAS – Chemical Abstracts Service.
b Les unités SI sont privilégiées pour tous les paramètres.
c Quantité et identité de tout produit de dégradation stable.
d Paramètres tels que la CL50 – concentration médiane létale, la CMEO – concentration minimale avec effet observé, la CSEO – concentration sans effet observé, incluant l’espèce et la durée.
e Paramètres tels que la DL50 – dose médiane létale, la CMEO, la CSEO, incluant l’espèce et la durée.
* Indique les paramètres qui devraient être inclus dans le tableau de comparaison. Lorsque qu’applicable, une description qualitative peut être fournie. Si les données ne sont pas disponibles, il faut l’indiquer.
** Indique les paramètres qui sont fournis à titre d’exemple. Lorsque qu’applicable, une description qualitative peut être fournie.
| Paramètre | Type | Polymère déclaré | Polymère de substitution 1 |
|---|---|---|---|
| numéro d’enregistrement CASa | Identification | * | * |
| Dénomination chimique du polymère | Identification | * | * |
| Formule développée représentative (image) | Identification | * | * |
| Monomère 1 concentration (%)b | Identification | * | * |
| Monomère 2 concentration (%)b | Identification | * | * |
| Monomère 3 concentration (%)b | Identification | * | * |
| Répartition de la masse moléculaire et polydispersité des polymères (par exemple, Mnc / Mw,d Mw/Mn) | Physico-chimique | * | * |
| Pourcentage massique moléculaire < 1 000 daltons | Physico-chimique | * | * |
| Pourcentage massique moléculaire < 500 daltons | Physico-chimique | * | * |
| Groupes fonctionnels réactifs et MEFGe | Physico-chimique | * | * |
| Autres données (au besoin) | Physico-chimique | ** | ** |
a CAS – Chemical Abstracts Service.
b Inclure le nom et le numéro d’enregistrement CAS pour tous les monomères.
c Mn – masse moléculaire moyenne en nombre.
d Mw – masse moléculaire moyenne en poids.
e MEFG – masse équivalente du groupe fonctionnel.
* Indique les paramètres qui devraient être inclus dans le tableau de comparaison.
** Indique les paramètres qui sont fournis à titre d’exemple. Lorsque qu’applicable, une description qualitative peut être fournie.
8.4.4 Estimations des relations quantitatives structure-activité
Les RQSA permettent de faire des estimations quantitatives de propriétés particulières; elles sont généralement obtenues par des logiciels exécutant des analyses de régression ou utilisant des descripteurs moléculaires qui représentent mathématiquement les composants de la structure d’une molécule. La régression linéaire ou multiple d’une propriété particulière par rapport à une autre propriété (par exemple, le coefficient de partage entre l’octanol et l’eau par rapport à la solubilité dans l’eau ou encore la pression de vapeur par rapport au point d’ébullition) peut servir à dériver une relation empirique pour une ou plusieurs classes de substances chimiques.
La validité d’une estimation de RQSA doit être expliquée dans la DSN en fonction de la question suivante : est-ce que cette estimation est raisonnable en comparaison avec les données mesurées compte tenu des caractéristiques structurelles de la substance déclarée et des caractéristiques structurelles ou des classes de substances chimiques utilisées pour produire les estimations? Il faut déterminer la validité des RQSA en déterminant si le modèle peut prévoir correctement le paramètre cible de la substance déclarée.
Les renseignements à l’appui de l’acceptation des données basées sur les RQSA devraient inclure :
- des renseignements sur le modèle utilisé (par exemple, la version du logiciel), ainsi que les données d’entrée et les résultats du modèle;
- une validation de l’estimation (incluant l’indication des substances chimiques ou des structures utilisées pour produire l’estimation et les données expérimentales sur ces substances chimiques);
- le niveau de fiabilité de l’estimation.
Une méthode recommandée pour appuyer l’acceptation de données basées sur des RQSA est présentée dans le document Report from the Expert Group on (Quantitative) Structure–Activity Relationships [(Q)SARs] on the Principles for the Validation of (Q)SARs [PDF] de l’OCDE (en anglais seulement).
Selon les 5 principes de validation de l’OCDE, le modèle RQSA doit :
- être associé à un paramètre défini;
- devrait être basé sur un algorithme sans ambiguïté;
- avoir un domaine d’application défini;
- être associé à des mesures appropriées d’ajustement, de fiabilité et de fidélité;
- être associé à une interprétation du mécanisme, si possible.
Les estimations des modèles RQSA produites en suivant ces principes de validation de l’OCDE devraient être documentées de manière adéquate en utilisant 2 formats de rapports accessibles au public : le Modèle de rapport de modèle RQSA (QSAR Model Reporting Format - QMRF) et le Modèle de rapport de prédiction de RQSA (QSAR Prediction Reporting Format - QPRF). Le QMRF fournit une validation du modèle RQSA lui-même alors que le QPRF fournit des renseignements sur l’applicabilité du modèle à la substance chimique en question. Ces 2 documents doivent être fournis s’ils sont disponibles. Le Programme des SN examinera, au cas par cas, l’adéquation de toute prédiction RQSA en tenant compte de la validité et de l’applicabilité du modèle fourni dans la documentation.
Le Programme des SN évalue une vaste gamme de substances, dont bon nombre posent des difficultés de modélisation, car elles se situent hors du domaine d’application des modèles, les caractéristiques de la molécule n’étant pas représentées dans l’ensemble d’apprentissage du programme. Par conséquent, le Programme des SN recommande d’exercer son jugement lorsque des données modélisées sont utilisées. Elles devraient se limiter à des prédictions sur les propriétés de classes bien connues de substances chimiques à l’aide de modèles robustes faisant appel à des ensembles d’apprentissage solides.
Actuellement, le Programme des SN considère que les RQSA pour les nanomatériaux sont aux premiers stades de leur développement et devront ainsi démontrer qu’elles sont assez fiables pour effectuer des prédictions sur des paramètres cibles en utilisant des propriétés physico-chimiques.
Bien que cela ne soit pas obligatoire, les déclarants sont encouragés à présenter une demande de CAD (consulter la partie 8.8) lors de la préparation de leur DSN afin d’obtenir des conseils sur l’acceptabilité, l’utilisation et la documentation des estimations obtenues à partir de modèles RQSA.
8.4.5 Principe du poids de la preuve
Lorsque des données obtenues au moyen de plusieurs approches énumérées dans la partie 8.4 sont disponibles, le Programme des SN encourage fortement l’utilisation de ces différents éléments de preuves dans le cadre d'une approche basée sur le poids de la preuve pour satisfaire à une exigence en matière de renseignements techniques d’une DSN. Le déclarant peut utiliser toute combinaison de ces approches pour satisfaire à une exigence en matière de renseignements techniques. Une approche seule pourrait être insuffisante pour satisfaire à l’exigence en matière de renseignements; cependant, la combinaison d’une approche avec d’autres renseignements pourrait former un ensemble de preuves suffisant pour indiquer l’effet d’une substance. Par exemple, des renseignements peuvent être recueillis à partir des publications scientifiques concernant une substance de substitution et à partir de modèles RQSA pour la substance déclarée. Une approche basée sur le poids de la preuve doit s’appuyer sur une justification scientifique expliquant l’utilisation des différents éléments de preuve et expliquant leur pertinence pour caractériser les risques de la substance déclarée (c’est-à-dire, le potentiel que la substance soit nocive pour la santé humaine ou l’environnement aux termes des critères énoncés à l’article 64 de la Loi canadienne sur la protection de l’environnement (1999) [la Loi].
Bien que cela ne soit pas obligatoire, les déclarants sont encouragés à présenter une demande de CAD (consulter la partie 8.8) lors de la préparation de leur DSN afin d’obtenir des conseils sur l’acceptabilité de l’utilisation de plusieurs méthodes de rechange dans le cadre d'une approche basée sur le poids de la preuve.
8.5 Données d’essai sur les UVCB et les substances impures
Le sigle UVCB désigne des substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques. Ces matières sont dérivées de sources naturelles ou de réactions complexes et sont considérés comme des substances simples aux fins de la déclaration et en vertu des dispositions de la Loi relatives aux substances nouvelles; par conséquent, tous les essais devraient être réalisés sur l’UVCB dans son ensemble. Si un essai prévu ne convient pas (par exemple, la mesure du point de fusion), il faut envisager la possibilité d’employer d’autres méthodes (par exemple, la mesure du point de ramollissement). En outre, tous renseignements sur les composants connus de l’UVCB aidera à interpréter les données obtenues sur l’UVCB en question.
En raison de la nature complexe de ce groupe de substances, les responsables du Programme des SN encouragent les déclarants à présenter tous renseignements supplémentaires sur les matières premières, les étapes et les mécanismes de réaction des UVCB qui aideront dans l’évaluation des risques.
Des difficultés peuvent se produire lorsqu’on effectue des essais sur des substances renfermant beaucoup d’impuretés (comme des réactifs résiduels, des solvants ou des sous-produits), car celles-ci peuvent nuire à l’interprétation des données des essais. Il faut donc mener les essais sur un échantillon de pureté élevée de la substance. Toutefois, s’il est techniquement impossible ou peu pratique de purifier la substance, des essais sur la substance brute pourraient être acceptés. Dans tous les cas, il faut indiquer le degré de pureté de la matière à l’étude et documenter les mesures prises pour isoler la substance. Les renseignements sur les propriétés physico-chimiques ou toxicologiques de n’importe laquelle des impuretés aideront à interpréter les données sur la substance impure. Dans les cas où les renseignements sur le mélange ne seraient pas utiles pour l’évaluation de la substance déclarée (par exemple, dans le cas où la substance déclarée ne comprend qu’une infime partie du mélange et où toute purification additionnelle est impossible), une demande de dérogation à l’obligation de fournir les renseignements parce que cela est techniquement impossible sera considérée (consulter la partie 8.7.1).
8.6 Sources des méthodes d’essai
Les méthodes d’essai peuvent être accédées aux sites Web de l’OCDE, d’Environnement et Changement climatique Canada ou de l’Agence de protection environnementale des États-Unis (United States Environmental Protection Agency – US EPA) :
- Méthodes d’essais des produits chimiques de l’OCDE;
- Publications sur les méthodes d’essai biologique d’Environnement et Changement climatique Canada;
- Publications environnementales du centre de service national de l’Agence de protection environnementale des États-Unis (en anglais seulement).
8.7 Demandes de dérogation à l’obligation de fournir des renseignements
8.7.1 Introduction
Il est prévu au paragraphe 81(8) de la Loi qu’une dérogation relativement à la communication d’un renseignement quelconque peut être demandée au Programme des SN. La décision d’accorder ou non une telle dérogation est prise au cas par cas selon que le demandeur satisfait à au moins l’un des 3 critères énoncés. Les critères légaux pour les dérogations à l’obligation de fournir des renseignements se trouvent aux paragraphes 81(8) de la Loi et se lisent comme suit :
- a) les ministresNote de bas de page 17 jugent que les renseignements ne sont pas nécessaires pour déterminer si la substance est effectivement ou potentiellement toxique;
- b) la substance est destinée à une utilisation réglementaire ou doit être fabriquée en un lieu où, selon les ministres, la personne qui demande l’exemption est en mesure de la contenir de façon à assurer une protection satisfaisante de l’environnement et de la santé humaine;
- c) il est impossible, selon les ministres, d’obtenir les résultats des essais nécessaires à l’établissement des renseignements.
Les demandes de dérogation doivent être présentées par écrit dans la DSN et elles devraient inclure des explications bien documentées pour chaque demande ainsi qu’une identification du critère légal selon lequel la demande est présentée. En l’absence de justifications appropriées et de documentation à l’appui, le début du délai d’évaluation sera retardé (consulter les parties 9.3.3 et 9.3.4). Pour déterminer si une dérogation est acceptable et éviter de retarder inutilement l’évaluation, les responsables du Programme des SN fournissent l’occasion aux déclarants de présenter une demande de CAD (consulter la partie 8.8) pendant la préparation de la DSN.
Des exemples de conditions dans lesquelles des dérogations peuvent être accordées sont présentés à l’appendice 6 du Document d’orientation. Cette liste n’est pas exhaustive; elle décrit certaines conditions indépendantes qui justifieraient dans la plupart des cas l’octroi d’une dérogation. Les demandes de dérogation peuvent également être basées sur une combinaison de facteurs, comme les propriétés physiques de la substance déclarée, sa toxicité intrinsèque et le risque d’exposition à la substance.
Une fois que la dérogation à l’obligation de fournir des renseignements est accordée, l’information détaillée sur la dérogation est publiée dans la Partie I de la Gazette du Canada, conformément au paragraphe 81(9) de la Loi. L’avis de dérogation ne comprend que : a) le nom du déclarant (ou de l’entreprise) à qui la dérogation est accordée et b) le type d’information dont il s’agit (par exemple, entreprise X, données provenant d’un essai de biodégradabilité immédiate). L’avis n’indique pas à quelle substance s’appliquent la dérogation ni le numéro de référence de la DSN.
Généralement, l’admissibilité d’une substance pour l’inscription sur la Liste intérieure ne sera pas affecté lorsque des dérogations ont été accordées en vertu de l’alinéa 81(8)a), 81(8)b) ou 81(8)c) de la Loi.
Quand une dérogation a été accordée, le déclarant doit indiquer toutes les corrections apportées ensuite aux renseignements fournis pour justifier et évaluer la dérogation conformément au paragraphe 81(11) de la Loi (consulter la partie 10.1.1). Le ministre de l’Environnement peut alors, si nécessaire, demander au déclarant de fournir les renseignements qui avaient fait l’objet de la demande de dérogation ou prendre des mesures de gestion qui conviennent.
Les déclarants ne doivent pas demander de dérogation lorsque les renseignements relatifs à l’élément de donnée en question ont été soumis pour une substance de substitution ou par l’emploi de méthodes de rechange.
8.7.1.1 Dérogations demandées aux termes de l’alinéa 81(8)a) de la Loi
Une dérogation peut être accordée s’il peut être établi que l’essai n’est pas nécessaire pour déterminer si la substance est effectivement ou potentiellement toxique. Dans les cas où l’obligation d’effectuer une partie de l’essai prescrit dépend des résultats d’une partie précédente de l’essai (par exemple, les données de l’essai de mutagénicité), il est suggéré aux déclarants d’effectuer l’essai en fonction de leur propre évaluation des résultats précédents ou de consulter les responsables du Programme des SN en présentant une demande de CAD (consulter la partie 8.8). Après avoir reçu cette demande ou la DSN, le Programme des SN évaluera les renseignements présentés pour déterminer si ils sont acceptables.
8.7.1.2 Dérogations demandées aux termes de l’alinéa 81(8)b) de la Loi
Une dérogation peut être accordée si la substance doit être utilisée à des fins prescrites par un règlement. Aucun règlement portant sur ces dérogations n’a été élaboré.
Une dérogation peut aussi être accordée si la substance est fabriquée en un lieu où, selon les ministres, la personne qui demande la dérogation est en mesure de la contenir de façon à assurer une protection satisfaisante de l’environnement et de la santé humaine.
8.7.1.3 Dérogations demandées aux termes de l’alinéa 81(8)c) de la Loi
De nombreuses demandes de dérogation pouvant être présentées en vertu de l’alinéa 81(8)c) de la Loi ont trait à des situations où il est techniquement difficile ou impossible d’effectuer les essais exigés à l’aide de la technologie classique à cause des propriétés physiques ou chimiques de la substance en question.
Le déclarant devrait envisager d’utiliser des protocoles de rechange ou des données de substitution pour satisfaire aux exigences concernant la communication de renseignements avant de conclure qu’il est impossible ou peu pratique de communiquer certains renseignements. Il est indiqué de ne pas demander une dérogation dans ce cas. Le déclarant ne peut pas invoquer le coût d’obtention de données comme unique justification qu’il est impossible ou peu pratique de fournir les renseignements exigés.
8.7.2 Dérogations de classes
L’expérience de l’évaluation de substances nouvelles acquise par les responsables du Programme des SN a permis de constituer de vastes ensembles de connaissances sur des classes de substances qui peuvent s’appliquer aux substances nouvelles déclarées qui en font partie. L’examen systématique des propriétés d’une classe de substances par rapport aux exigences réglementaires peut révéler des tendances établies pour ces propriétés. Dans de tels cas, il n’est vraisemblablement pas nécessaire de fournir des renseignements sur des paramètres particuliers propres aux substances déclarées de la classe en cause pour déterminer si la substance est effectivement ou potentiellement toxique.
Les déclarants qui préparent des DSN concernant des substances dont les caractéristiques justifient leur appartenance à une de ces classes sont encouragés à demander une dérogation à l’obligation de fournir des renseignements relatifs aux paramètres visés en vertu de l’alinéa 81(8)a) de la Loi.
Les déclarants peuvent communiquer avec le Programme des SN en utilisant la Ligne d’information de la gestion des substances afin de savoir quels renseignements ils doivent fournir pour appuyer une proposition visant la création d’une nouvelle classe de substances.
8.7.2.1 Dérogations pour la classe des polymères cationiques
Les renseignements disponibles sont jugés suffisants pour indiquer qu’une classe comprenant certains polymères cationiques devrait être peu toxique selon les essais de toxicité pour la santé prescrite par le Règlement. Les déclarants sont donc encouragés à demander des dérogations relativement à tous les essais de toxicité des polymères qui répondent à la définition des substances faisant partie de cette classe.
Actuellement, cette classe englobe les polymères qui ne satisfont pas aux critères établis pour les polymères à exigences réglementaires réduites en raison uniquement de la présence des groupes cationiques ou potentiellement cationiques suivants :
- Groupes d’amines primaires, secondaires ou tertiaires;
- Cyanamides;
- Sulfoniums.
Les polymères contenant d’autres groupes cationiques (tels que des amines quaternaires, des amines stabilisées par encombrement, des azides, des isocyanates [libres et bloqués] et des phosphoniums) ne font pas partie de la classe susmentionnée, parce que l’on ne dispose pas actuellement assez de renseignements sur leur toxicité pour justifier leur inclusion dans cette classe ou parce que d’après les renseignements disponibles, ces polymères produisent des effets nocifs. Dans le cas des polymères qui ne peuvent pas entrer dans la classe susmentionnée et qui ne peuvent donc pas justifier l’octroi d’une dérogation relative à cette classe, les déclarants peuvent néanmoins demander une dérogation en présentant une justification suffisante relative à des essais particuliers ou présenter des données de substitution que les responsables du Programme des SN examineront au cas par cas. De même, aucune dérogation à l’obligation de fournir les résultats d’essais de toxicité aiguë et de toxicité à doses répétées ne sera accordée dans le cas des polymères cationiques ayant une Mn supérieure à 10 000 daltons s’il est prévu que l’inhalation sera le mode d’exposition le plus probable de la population en général selon l’utilisation prévue.
8.8 Consultation avant déclaration
Une demande de CAD est une option pour les déclarants qui souhaitent consulter le Programme des SN pendant la planification ou la préparation de leur DSN afin de discuter de toute question ou préoccupation concernant les exigences en matière de renseignements. Une demande de CAD est recommandée lorsqu’une assistance est nécessaire pour déterminer l’acceptabilité des demandes de dérogation, des protocoles d’essai, des déclarations consolidées, des données de substitution ou d’autres paramètres (consulter la partie 6.5.4), ou lorsqu’une clarification est nécessaire concernant la classification des substances.
Les demandes de CAD peuvent être traitées par écrit (par la poste ou par courriel) ou encore au cours d’une réunion ou d’une conférence téléphonique.
Dans le cas des demandes de CAD traitées au cours d’une réunion ou d’une conférence téléphonique, les responsables du Programme des SN mettront tout en œuvre pour répondre aux demandes durant la réunion ou la conférence téléphonique. Ils demandent un délai d’au moins 2 semaines entre la date de réception de la demande préliminaire de CAD, laquelle doit contenir suffisamment de renseignements, et la date de la réunion ou de la conférence téléphonique. Cela leur accordera assez de temps pour donner une réponse éclairée aux questions posées.
Dans le cas des demandes de CAD visant les substances chimiques et polymères, le Programme des SN mettra tout en œuvre pour répondre aux questions par écrit dans un délai équivalant à 30 jours. Ce délai commencera dès que les renseignements fournis seront jugés suffisants pour que la CAD s’amorce.
L’information nécessaire pour amorcer une CAD comprend :
- les renseignements sur l’identité de la substance (par exemple, le nom de la substance, son nom commercial, son numéro d’enregistrement CAS, sa structure moléculaire, une liste de ses réactifs);
- les renseignements sur la personne-ressource (le nom de la personne-ressource, le titre, l’entreprise, l’adresse courriel et l’adresse postale);
- l’annexe visé du Règlement;
- l’utilisation(s) visée(s) de la substance;
- les questions ou préoccupations spécifiques auxquelles le programme des SN doit répondre;
- les données et les rapports d’essai pertinents en possession du déclarant, le cas échéant;
- les demandes de confidentialité liées à l’entreprise, la fabrication, l’importation, la quantité, l’identité de la substance ou l’utilisation envisagée, le cas échéant;
- un bref ordre du jour dans le cas des réunions.
Les responsables du Programme des SN formuleront des avis fondés sur la documentation fournie avec la demande de CAD. Les avis professionnels qu’ils formulent au cours de la consultation ne constituent pas un engagement officiel puisque les conclusions d’ordre technique peuvent varier à la suite d’une étude plus approfondie de la DSN complète.
En plus des demandes de CAD, les responsables du Programme des SN encouragent les déclarants à communiquer avec eux pour clarifier toutes les autres questions concernant le programme.
Il est recommandé de présenter une demande de CAD avec le Formulaire de demande de Consultation avant déclaration disponible sur le site Web du Programme des SN. Le formulaire complété peut être présenté sécuritairement en utilisant le système de Gestion de l'information du guichet unique (GIGU) d’Environnement et Changement climatique Canada ou envoyé par courriel à la Ligne d’information de la gestion des substances.
Partie 9. Traitement de la Déclaration de substances nouvelles
Cette partie décrit les procédures administratives et les responsabilités du Programme des substances nouvelles (SN) à la réception d’une Déclaration de substances nouvelles (DSN).
9.1 Aperçu du processus d’évaluation d’une Déclaration de substances nouvelles
La figure 9-1 donne un aperçu du processus d’évaluation d’une DSN entre le moment où les responsables du Programme des SN la reçoivent et le moment où la substance déclarée est inscrite sur la Liste intérieure ou indiquent les mesures qui seront prises pour gérer les risques que présente cette substance.

Description longue
Le processus d’évaluation d’une déclaration de substance nouvelle s’amorce lorsque le programme des SN reçoit une DSN complète. Ensuite, la DSN est assujettie à un examen préliminaire du contenu avant de poursuivre à une évaluation conjointe par Environnement et Changement climatique Canada et Santé Canada en vue de déterminer les risques potentiels sur l’environnement et les risques liés à la santé humaine. Le ministre de l’Environnement et le ministre de la Santé évalue les renseignements et détermine si la substance est soupçonnée d’être toxique en vertu des critères de l’article 64 de la Loi.
- Si la substance est soupçonnée d’être toxique :
- Des mesures de gestion des risques sont développées en consultation avec le déclarant, incluant les conditions ministérielles, l’obligation de fournir des renseignements complémentaires ou l’interdiction de fabrication ou d’importation.
- Si la substance n’est pas soupçonnée d’être toxique:
- On fournit au déclarant un avis de décision de l’évaluation confirmant que la fabrication ou l’importation peut avoir lieu.
- Lorsqu’une nouvelle activité (NAc) associée à la substance pourrait faire en sorte que celle-ci soit toxique pour la santé humaine ou l’environnement, un avis de NAc est publié.
- La substance est inscrite sur la Liste intérieure lorsque les critères pour son inscription sont satisfaits.
9.2 Réception d’une Déclaration de substances nouvelles
9.2.1 Délai d'évaluation
Le délai d'évaluation correspond au délai accordé, en jours civils, au personnel du Programme des SN pour évaluer une DSN complète. Le nombre de jours du délai d'évaluation apparaît au tableau 1-1.
Le jour 1 de le délai d'évaluation est le jour qui suit la date à laquelle les responsables du Programme des SN reçoivent la DSN complète. Présenter une DSN avec des renseignements manquants ou incomplets pourra affecter le délai pour l’évaluation, par exemple :
- si une DSN est présentée sans que les droits exigés aient été payés (consulter le tableau des frais à la page des Droits pour les déclarations de substances nouvelles), le délai d'évaluation ne commencera qu’à la réception du paiement des droits;
- si une DSN est manifestement inadéquate ou des renseignements exigés par le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [le Règlement] sont absents, le délai d'évaluation ne commencera qu’après la réception d’une DSN complète;
- si un Tiers fournisseur de renseignements doit envoyer des renseignements confidentiels directement aux responsables du Programme des SN, le délai d'évaluation ne commencera pas avant que tous les renseignements requis aient été reçus;
- si des renseignements d’importance mineure sont manquantes ou jugés erronés au moment de l’évaluation, le délai d'évaluation devrait se poursuivre, pourvu que les renseignements corrects soient présentés avant la date déterminée par les responsables du programme (généralement quelques jours ouvrables);
- si, pendant le délai d'évaluation, les renseignements contenus dans la DSN sont jugés incomplets ou erronés, la DSN sera considérée comme étant incomplète et l’évaluation reprendra au jour 1 lors de la réception d’une DSN complète.
9.3 Correspondance
Une correspondance officielle est entretenue entre les responsables du Programme des SN et le déclarant ou l’« agent canadien » tout au long du processus d’évaluation. Les responsables du Programme des SN communiqueront avec le déclarant par courrier électronique. Les déclarants qui veulent encore recevoir de la correspondance par courrier postal doivent en faire la demande dans la lettre de présentation de leur DSN, à défaut de quoi les originaux ne sont pas envoyés par la poste. Les parties 9.3.1 à 9.3.6 décrivent les types de correspondance qu’un déclarant peut recevoir pour les DSN et les déclarations de nouvelle activité (DNAc).
9.3.1 Avis d’ouverture de dossier
Lorsqu’un Tiers fournisseur de renseignements (consulter la partie 5.2) participe à une DSN, le déclarant doit soumettre une DSN partielle pour amorcer le processus. Les responsables du Programme des SN envoient un avis d’ouverture de dossier au déclarant pour accuser réception de ces renseignements partiels requis pour l’établissement de la DSN. Le délai d'évaluation ne commence pas avant que le Tiers fournisseur de renseignements n’ait fourni tous les renseignements prescrits. Une fois que tous les renseignements auront été reçus, un accusé de réception de la DSN complète sera envoyé (consulter la partie 9.3.2) et le délai d'évaluation commencera.
9.3.2 Accusé de réception de la Déclaration substances nouvelles complète
Après réception et acceptation des renseignements fournis dans la DSN, un accusé de réception précisant la date de début du délai d'évaluation et le numéro de référence de DSN est envoyée. Cet accusé indique que les renseignements de nature administrative sont satisfaisants et que tous les renseignements exigés, y compris les droits exigibles, ont été reçus, mais que la DSN n’a pas encore fait l’objet d’une évaluation. L’accusé de réception fournit également le délai prévu de l’évaluation.
Un déclarant peut, au moment du dépôt de la DSN ou après, demander que l’évaluation soit terminée plus tôt que le délai prévu (paragraphe 83(6) de la Loi canadienne sur la protection de l’environnement (1999) [la Loi]) dans l’annexe du Règlement à laquelle la substance déclarée est assujettie. Un déclarant peut inclure une date cible pour que l’évaluation soit terminée plus tôt et une raison pour laquelle l’évaluation devrait être terminée plus tôt. Si une telle demande est reçue, l’accusé de réception indiquera que les responsables du Programme des SN prendront la demande en considération au cours du délai d'évaluation. Bien que les responsables Programme des SN feront tout leur possible pour terminer l’évaluation avant la date cible, il n’est pas garanti qu’ils pourront satisfaire à une telle demande.
9.3.3 Avis de renseignements manquants
Un avis de renseignements manquants est envoyé au déclarant en cas d’omissions ou d’erreurs dans les renseignements devant obligatoirement être fournis dans la DSN. Cet avis décrira tous les manquements relevés dans la DSN. Veuillez consulter la partie 9.2.1 du Document d’orientation pour des exemples de raisons entraînant l’envoi de ce type d’avis. Le délai d'évaluation ne commencera pas avant que tous les renseignements exigés aient été reçus et acceptés. Si les omissions ou les erreurs sont identifiées après l’envoi d’un accusé de réception de la DSN complète, l’évaluation pourra reprendre au jour 1 à la réception des renseignements complémentaires ou corrigés.
9.3.4 Avis de rejet
Un avis de rejet est envoyée en cas d’omissions ou d’erreurs importantes dans les renseignements obligatoires pour la DSN. Cet avis décrira tous les manquements relevés dans la DSN. Les documents originaux peuvent être retournés. Veuillez consulter la partie 9.2.1 du Document d’orientation pour des exemples de raisons entraînant l’envoi de ce type d’avis.
9.3.5 Avis de prolongation du délai d'évaluation
Le délai d'évaluation de toute DSN et DNAc peut être prolongé lorsque plus de temps est nécessaire pour terminer une évaluation. Le ministre de l’Environnement (le ministre) ne peut prolonger le délai d'évaluation qu’une seule fois et pour une durée ne dépassant pas le délai prescrit pour le délai d'évaluation initial. De façon générale, le délai d’évaluation sera prolongé lorsque l’application de mesures de gestion est considérée. Le déclarant recevra un avis de prolongation du délai d'évaluation à la fin ou avant la fin du délai d'évaluation initial avisant que le délai d’évaluation a été prolongé.
9.3.6 Avis de décision de l’évaluation
La décision de l’évaluation est communiquée au déclarant à la fin ou avant la fin du délai d’évaluation applicable.
Note : En vertu du paragraphe 83(6) de la Loi, le délai d’évaluation d’une DSN ou d’une DNAc peut être terminé plus tôt que son expiration. Ces dispositions peuvent être mise en œuvre lorsque l’évaluation est complétée avant la fin du délai d’évaluation prescrit. Dans un tel cas, l’avis indiquerait le jour que le délai d'évaluation prend fin.
Selon les conclusions de l’évaluation (consulter la partie 9.6), l’avis indiquera :
- qu’il n’existe aucun soupçon que la substance soit toxique ni potentiellement toxique;
- qu’il n’existe aucun soupçon de toxicité relativement aux activités courantes liées à la substance, mais il est soupçonné que d’autres activités mettant la substance en cause pourraient rendre celle-ci toxique;
- qu’il existe un soupçon quant à la toxicité et des mesures de gestion des risques sont imposées.
Si applicable, l’avis indiquera aussi que la fabrication ou l’importation peut commencer en des quantités supérieures à celles qui ont exigé la présentation d’une DSN, ou conformément aux termes des mesures de gestion des risques imposées.
L’avis peut aussi inclure tout renseignement additionnel exigé pour que la substance soit inscrite sur la Liste intérieure.
9.4 Retrait d’une Déclaration de substances nouvelles
Un déclarant peut demander le retrait d’une DSN dans l’un ou l’autre des cas suivants :
- La même entreprise a déjà déclaré la même substance au même seuil;
- La substance figure déjà sur la Liste intérieure;
- Le déclarant n’a plus l’intention de poursuivre la fabrication ou l’importation de la substance en cause en des quantités égales ou supérieures au seuil de déclenchement et les quantités déjà fabriquées ou importées n’ont pas dépassé ce seuil.
Les demandes de retrait de DSN peuvent être envoyées au Programme des SN par courriel ou par la poste. La demande de retrait ne sera pas acceptée si le déclarant a été informé d’une proposition de décision de prendre des mesures de gestion des risques ou de publier un avis nouvelle activité (NAc) visant la substance déclarée. Le déclarant sera avisé par écrit de l’acceptation ou du rejet de sa demande de retrait de DSN.
9.5 Évaluation de la Déclaration de substances nouvelles
Le processus d’évaluation et de gestion des risques a pour objet de veiller à ce que l’utilisation de la substance ne pose pas de risque pour la santé humaine ou l’environnement soit en raison de ses propriétés intrinsèques ou grâce aux mesures prises pour atténuer l’exposition à la substance.
9.5.1 Examen des renseignements
Les évaluateurs du Programme des SN examinent la DSN afin de déterminer la validité des renseignements suivants :
- L’identification de la substance et ses dénominations maquillées;
- Les demandes de Renseignements commerciaux confidentiels;
- Les protocoles et les méthodes d’essai;
- Les données d’essai;
- Les raisons pour lesquelles le déclarant demande une dérogation à l’obligation de fournir certains renseignements;
- Les raisons pour lesquelles d’autres protocoles d’essai ou des données de substitution ont été utilisés;
- Les renseignements relatifs à l’exposition à la substance.
Les problèmes relatifs aux renseignements de la déclaration qui ne peuvent pas être facilement résolus peuvent entraîner le rejet de la DSN et la fin du délai d'évaluation (consulter la partie 9.3.4).
9.5.2 Détermination de la toxicité
Le processus d’évaluation des DSN a pour objet de déterminer si une substance est effectivement ou potentiellement toxique en fonction de l’un ou l’autre des critères spécifiés à l’article 64 de la Loi :
64. […] est toxique toute substance qui pénètre ou peut pénétrer dans l’environnement en une quantité ou concentration ou dans des conditions de nature à :
- a) avoir, immédiatement ou à long terme, un effet nocif sur l’environnement ou sur la diversité biologique;
- b) mettre en danger l’environnement essentiel pour la vie;
- c) constituer un danger au Canada pour la vie ou la santé humaines.
Par conséquent, la détermination du fait qu’une substance est effectivement ou potentiellement toxique comporte une évaluation des risques d’exposition à la substance des humains ou des composantes de l’environnement et de ses effets nocifs pour les humains ou l’environnement (y compris d’autres organismes vivants, des systèmes naturels interdépendants et les éléments abiotiques de l’environnement).
Le risque d’exposition à une substance dépend de la quantité, du taux, de la fréquence et des conditions de rejet de la substance dans l’environnement à tous les moments de son cycle de vie, ainsi que de sa mobilité, sa répartition dans les divers milieux de l’environnement et sa persistance. L’évaluation de l’exposition tient compte de l’utilisation de la substance identifiée par le déclarant, ainsi que des autres utilisations possibles de la substance au cas où elle figurerait sur la Liste intérieure sans restrictions.
L’évaluation des effets nocifs sur les humains et les autres organismes vivants tient compte de paramètres comme la létalité, les effets mutagènes, les effets sur le plan de la reproduction et du développement et la toxicité pour les organes cibles alors que les effets nocifs sur les composantes abiotiques de l’environnement comprennent des conséquences comme l’appauvrissement de la couche d’ozone, le réchauffement climatique et la production de pluies acides.
Le Programme des SN peut « soupçonner » qu’une substance puisse être toxique s’il craint que ses effets soient nocifs ou s’il appréhende une éventuelle exposition à cette substance. Par exemple, les substances qui présentent des risques d’exposition élevés en raison du rejet continu de quantités élevées ou de leur persistance dans l’environnement peuvent être soupçonnées d’être toxiques, même si les renseignements provenant de l’évaluation initiale laissent planer un doute quant au risque biologique ou environnemental de la substance. Quand une évaluation indique qu’une substance est « potentiellement toxique », il existe une disposition de la Loi – le paragraphe 84(1) – qui permet au ministre de prendre une des mesures de gestion des risques énoncées (consulter la partie 9.6).
9.6 Conclusions de l’évaluation
L’évaluation peut se conclure par l’un des 3 résultats suivants :
- Il n’existe aucun soupçon de toxicité et aucune mesure n’est prise;
- Il n’existe aucun soupçon de toxicité relativement aux activités courantes liées à la substance, mais un avis de NAc est publié, car les résultats de l’évaluation permettent de soupçonner que d’autres activités mettant la substance en cause pourrait rendre celle-ci toxique (consulter la partie 9.6.2);
- Il existe un soupçon quant à la toxicité et des mesures de gestion des risques sont imposées (consulter la partie 9.6.3).
Le déclarant sera informé par écrit, avant la fin du délai d'évaluation, si les responsables du Programme des SN soupçonnent que la substance déclarée est ou pourrait être toxique; le cas échéant, le déclarant est informé des mesures qui seront prises. Le déclarant sera également informé par écrit, avant la fin du délai d'évaluation, si les responsables du Programme des SN ont l’intention de produire un avis de NAc relatif à la substance en question (consulter la partie 9.6.2).
9.6.1 Aucun soupçon de toxicité, aucune mesure n’est prise
Si les rapports complets d’évaluation des effets de la substance déclarée sur l’environnement et la santé humaine indiquent qu’il n’y a pas lieu de soupçonner que la substance soit effectivement ou potentiellement toxique, aucune mesure n’est prise. Dans le cas où aucune mesure n’est prise avant la fin du délai d'évaluation, le déclarant peut, une fois que le délai d'évaluation est terminée, commencer à fabriquer ou à importer la substance en des quantités supérieures à celles qui ont exigé la présentation de la DSN.
9.6.2 Avis de nouvelle activité
Si l’évaluation de la substance déclarée révèle qu’il n’y a pas lieu de soupçonner que la substance est ou pourrait être toxique en raison des activités déclarées, mais qu’elle permet de soupçonner qu’une nouvelle activité liée à la substance puisse la rendre toxique, les dispositions relatives aux NAc de la Loi peuvent s’appliquer (consulter l’article 85 de la Loi). Un avis de NAc définit ce qui est considéré comme une nouvelle activité pour la substance et décrit les critères en fonction desquels une déclaration est exigée ou non. De façon générale, le déclarant sera informé, avant la fin du délai d'évaluation, si un avis de NAc visant la substance est en préparation.
L’évaluation d’une substance nouvelle examine les risques potentiels que peuvent présenter les activités déclarées et les autres activités éventuelles mettant en cause la substance. Si l’on soupçonne qu’une nouvelle activité puisse rendre la substance toxique, la Loi habilite le ministre à publier un avis de NAc dans les 90 jours suivant la fin du délai d'évaluation.
L’avis de NAc décrit les activités qui peuvent faire en sorte :
- qu’une quantité ou une concentration beaucoup plus grande de la substance pénètre dans l’environnement;
- que l’exposition à la substance ait lieu d’une manière ou dans des circonstances très différentes.
L’avis de NAc comprend :
- l’identification de la substance (par sa dénomination explicite ou par sa dénomination maquillée si la dénomination explicite est jugée confidentielle);
- une description des nouvelles activités;
- une description des renseignements qui doivent être présentés au ministre avant le début des nouvelles activités;
- les délais impartis au déclarant pour la communication des renseignements;
- le délai d'évaluation des renseignements par le ministre de l’Environnement et le ministre de la Santé (les ministres).
L’avis de NAc s’applique à tous les utilisateurs de la substance. Quiconque se propose d’utiliser la substance pour une nouvelle activité définie à l’avis doit soumette une DNAc au ministre comportant tous les renseignements prescrits à l’avis, avant que la nouvelle activité ne soit entreprise. Lorsqu’une déclaration complète est reçue, les ministres évaluent les renseignements fournis par le déclarant et les autres renseignements à leur disposition dans le délai d'évaluation mentionné à l’avis.
Les obligations de déclarations concernant une substance nouvelle visées au Règlement et à la Loi s’appliquent qu’un avis de NAc ait été émis ou non. Le cas échéant, le déclarant doit fournir :
- les annexes de renseignements ultérieures en vertu du Règlement, s’il y a lieu;
- les renseignements supplémentaires prescrits au paragraphe 7(2), 7(3), 11(2) ou 11(3) du Règlement dans le cas d’un rejet dans l’environnement aquatique en grande quantité ou d’un degré d’exposition du public élevé;
- l’avis approprié pour répondre aux critères d’inscription sur la Liste intérieure (consulter la partie 10).
La substance déclarée pourra être inscrite sur la Liste intérieure lorsque tous les renseignements susmentionnés auront été reçus, acceptés et évalués. Jusqu’à ce que la substance soit inscrite sur la Liste intérieure, tout autre déclarant se doit de continuer à respecter les exigences de déclaration en vertu du Règlement pour la fabrication ou l’importation de la substance nouvelle.
Les dispositions de la Loi relatives aux NAc peuvent aussi être appliquées à une substance qui figure sur la Liste intérieure suivant la publication d’un arrêté de NAc dans la Partie II de la Gazette du Canada. Lorsqu’une substance faisant l’objet d’un avis de NAc est inscrite sur la Liste intérieure, cet avis de NAc ne s’applique plus. Pour maintenir les obligations de déclarations concernant la substance, les exigences relatives aux NAc sont inscrites sur la Liste intérieure par l’entremise d’un arrêté de NAc.
Suite à la réception d’une DNAc complète, les responsables du Programme des SN évalueront les renseignements dans le délai prescrit par l’avis ou l’arrêté de NAc. En fonction des résultats de l’évaluation de ces renseignements supplémentaires, les exigences relatives aux NAc peuvent être modifiées ou annulées ou, encore, d’autres mesures de gestion des risques peuvent être imposées au besoin (consulter la partie 9.6.3).
9.6.3 Mesures de gestion du risque
Lorsque le Programme des SN soupçonne qu’une substance puisse être effectivement ou potentiellement toxique, des mesures de gestion des risques peuvent être prises pour atténuer le risque éventuel pour la santé humaine ou l’environnement. Les déclarants seront alors informés, avant la fin du délai d'évaluation, que la substance suscite des préoccupations. Normalement, le délai pour évaluation est prolongé (consulter la partie 9.3.5), ce qui donne le temps de développer les mesures de gestion des risques et d’obtenir l’approbation du ministre. Le déclarant est également informé avant la fin du délai d'évaluation de sa prolongation et des mesures de gestion des risques proposées.
Aux termes de l’article 84 de la Loi, lorsque les ministres soupçonnent la substance d’être effectivement ou potentiellement toxique, les mesures suivantes peuvent être prises :
- a) autoriser toute personne à fabriquer ou importer la substance à certaines conditions;
- b) interdire à toute personne de fabriquer ou d’importer la substance pendant une période ne dépassant pas deux ans (l’interdiction prend fin au terme de cette période de deux ans, sauf si avant la fin de cette période, un avis relatif à la prise d’un règlement proposé en vertu de l’article 93 de la Loi est publié dans la Gazette du Canada);
- c) interdire la fabrication ou l’importation de la substance jusqu’à ce que des renseignements complémentaires ou des résultats d’essais aient été présentés au ministre [paragraphe 84(2) de la Loi] et évalués (le délai d'évaluation de ces renseignements complémentaires prend fin 90 jours après leur réception).
Le ministre doit prendre ces mesures avant l’expiration du délai d'évaluation. Des exemplaires de la correspondance ministérielle et de l’avis seront expédiés par courriel au déclarant. Lorsqu’une condition ou une interdiction est imposée ou modifiée, l’avis décrivant la mesure de gestion et indiquant à quelle substance elle s’applique doit être publié dans Gazette du Canada. Une substance visée par des conditions imposées en vertu de l’article 84(1)a) ne peut pas être inscrite sur la Liste intérieure.
9.6.3.1 Imposition de conditions en vertu de l’alinéa 84(1)a) de la Loi
Lorsqu’on soupçonne qu’une substance puisse être effectivement ou potentiellement toxique, des conditions peuvent être imposées pour atténuer le risque éventuel pour la santé humaine ou l’environnement. Les conditions imposées en vertu de l’alinéa 84(1)a) de la Loi permettent la fabrication ou l’importation d’une substance moyennant des restrictions. Les types de restrictions imposées visent entre autres :
- la quantité autorisée;
- la forme physique de la substance (par exemple, doit être importée sous forme de billes de plastique);
- l’utilisation de la substance;
- l’élimination de la substance ou des contenants dans lesquels elle se trouvait.
Le déclarant et, si cela est prescrit, les clients du déclarant sont tenus de respecter les conditions imposées relativement à la substance par le ministre et de tenir des dossiers comme indiqué. Les conditions ministérielles sont publiées dans la Partie I de la Gazette du Canada après avoir été signifiées au déclarant. Les substances faisant l’objet de conditions ministérielles ne peuvent pas être inscrites sur la Liste intérieure. Par conséquent, un nouveau déclarant qui souhaite fabriquer ou importer la même substance doit présenter une DSN conformément au Règlement. Il peut s’ensuivre que les mêmes conditions ou des conditions similaires soient imposées.
Un déclarant peut présenter des renseignements supplémentaires et demander la réévaluation de la décision prise par les responsables du Programme des SN. Ceux-ci examineront ces renseignements supplémentaires, les prendront en considération et pourront modifier ou annuler les conditions imposées. Les conditions continuent de s’appliquer à moins qu’un avis pour leur modification ou annulation, sur la base des renseignements supplémentaires fournis, ne soit publié dans la Gazette du Canada.
9.6.3.2 Interdictions en vertu de l’alinéa 84(1)b) de la Loi
Lorsqu’une substance est soupçonnée d’être toxique ou potentiellement toxique, une interdiction peut être édictée pour atténuer tout risque pour la santé humaine ou l’environnement. Les interdictions édictées en vertu de l’alinéa 84(1)b) de la Loi interdisent à toute personne de fabriquer ou d’importer quelque quantité que ce soit de la substance. L’interdiction prescrite par le ministre est publiée dans la Partie I de la Gazette du Canada après qu’elle ait été émise au déclarant. D’après le paragraphe 84(4) de la Loi, l’interdiction prend fin soit 2 ans après son édiction, soit, si le gouverneur en conseil publie dans la Gazette du Canada, avant l’expiration de ces 2 ans, un avis de projet de règlement d’application de l’article 93 de la Loi concernant la substance, à l’entrée en vigueur de ce règlement.
Le déclarant peut présenter des renseignements supplémentaires et demander la réévaluation de la décision prise par les responsables du Programme des SN. Ceux-ci examineront ces renseignements supplémentaires, les prendront en considération et pourront modifier ou annuler les conditions imposées ou, encore, prendre d’autres mesures de gestion des risques. Cette interdiction continue de s’appliquer à moins qu’un avis pour sa modification ou son annulation ne soit publié dans la Gazette du Canada, ou encore qu’elle ne prenne fin tel que mentionné plus haut.
9.6.3.3 Demande de renseignements complémentaires en vertu de l’alinéa 84(1)c) de la Loi
Lorsque les responsables du Programme des SN exigent des renseignements complémentaires pour déterminer si la substance évaluée est effectivement ou potentiellement toxique, ils peuvent demander ces renseignements tout en interdisant la fabrication ou l’importation de la substance dans l’attente de l’obtention des résultats des essais, afin d’atténuer les risques éventuels pour la santé humaine ou l’environnement. La demande de fournir des renseignements supplémentaires est autorisée en vertu de l’alinéa 84(1)c) de la Loi et l’interdiction de fabriquer ou d’importer la substance est édictée en vertu du paragraphe 84(2) de la Loi. Le paragraphe 84(2) de la Loi stipule que la fabrication ou l’importation de la substance par la personne ayant reçu la demande de renseignements complémentaires est interdite à moins que les renseignements complémentaires n’aient été fournis et qu’un délai de 90 jours se soit écoulé depuis leur réception par les responsables du Programme des SN. Une fois que les renseignements complémentaires demandés auront été fournis, les responsables du Programme des SN les évalueront pour déterminer si la substance est effectivement ou potentiellement toxique et si d’autres mesures de gestion des risques sont nécessaires.
Partie 10. Responsabilités après la déclaration
10.1 Responsabilités du déclarant
Il incombe au déclarant de veiller à ce que tous les renseignements communiqués aux responsables du Programme des substances nouvelles (SN) soient exacts et complets.
10.1.1 Correction des renseignements
En vertu du paragraphe 81(11) de la Loi canadienne sur la protection de l’environnement (1999) [la Loi], le déclarant qui a communiqué des renseignements à l’appui d’une Déclaration de substances nouvelles (DSN) et qui, par la suite, constaterait que ces renseignements étaient erronés doit immédiatement en informer par correspondance le Programme des SN et présenter les corrections nécessaires à apporter à sa DSN.
Cette exigence ne s’applique qu’aux corrections des renseignements qui existaient au moment de la présentation de la DSN.
10.1.2 Article 70 de la Loi
Les renseignements obtenus après la présentation d’une DSN et qui permettent de conclure que la substance est ou pourrait être toxique doivent être communiqués aux responsables du Programme des SN en vertu des dispositions de l’article 70 de la Loi. Ces renseignements doivent être fournis, à moins que le déclarant ne sache de façon sûre que les responsables du Programme des SN disposent déjà des renseignements.
Pour obtenir les procédures relatives à la présentation de renseignements en vertu de l’article 70 de la Loi, veuillez communiquer avec la Ligne d’information de la gestion des substances.
10.1.3 Avis de quantité excédentaire
En vertu du paragraphe 81(14) de la Loi, un déclarant qui a satisfait aux exigences relatives à la fabrication ou l’importation d’une substance à d’autres fins qu’une substance destinée à la recherche et au développement ou une substance confinée qui est intermédiaire limitée au site ou destinée à l’exportation est tenu de présenter un avis de quantité excédentaire dans les 30 jours suivant la fabrication ou l’importation en quantités dépassant les quantités seuils (consulter la partie 10.1.3.1). Les renseignements qui doivent être fournis dans l’avis de quantité excédentaire sont indiqués dans la partie 10.1.5 du Document d’orientation.
10.1.3.1 Quantités seuils
Tel que prescrit aux articles 17 et 18 du Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [Règlement] et au paragraphe 81(14) de la Loi, tout déclarant qui n’a pas fourni un avis de fabrication ou d’importation (consulter la partie 10.1.4) doit fournir un avis de quantité excédentaire dans les 30 jours qui suivent l’atteinte de l’un des seuils de déclenchement suivants:
17(1) […]
- a) dans le cas d’une substance chimique ou biochimique qui ne figure pas sur la Liste extérieure, une quantité dépassant 10 000 kg au cours d’une année civile;
- b) dans le cas d’une substance chimique ou biochimique qui figure sur la Liste extérieure :
- (i) une quantité dépassant 50 000 kg au cours d’une année civile si :
- (A) la substance chimique ou biochimique est rejetée dans l’environnement aquatique en une quantité dépassant 3 kg par jour par site, la moyenne étant calculée sur une base mensuelle et après traitement des eaux usées,
- (B) le degré d’exposition du public à la substance chimique ou biochimique contenue dans un produit pourrait être élevé, ou
- (ii) une quantité dépassant 10 000 kg au cours d’une année civile, dans les autres cas.
18(1) […]
- a) dans le cas d’un polymère à exigences réglementaires réduites (ERR), une quantité supérieure à 1 000 kg au cours d’une année civile;
- b) pour tout autre polymère ou biopolymère :
- (i) une quantité dépassant 50 000 kg au cours d’une année civile si le polymère ou le biopolymère figure sur la Liste extérieure ou si le polymère ou le biopolymère ne figure pas sur la Liste extérieure, mais dont tous les réactifs figurent sur la Liste intérieure ou la Liste extérieure, et
- (A) le polymère ou le biopolymère est rejeté dans l’environnement aquatique en une quantité dépassant 3 kg par jour par site, la moyenne étant calculée sur une base mensuelle et après traitement des eaux usées,
- (B) le degré d’exposition du public au polymère ou au biopolymère contenu dans un produit pourrait être élevé, ou
- (ii) une quantité dépassant 10 000 kg au cours d’une année civile, dans les autres cas.
10.1.4 Avis de fabrication ou d’importation
Comme alternative, les alinéas 17(2)a) et 18(2)a) du Règlement prescrivent l’envoi d’un avis de fabrication ou d’importation pour les substances chimiques et les polymères. Ce type d’avis est une option alternative à la présentation d’un avis de quantité excédentaire rendant une substance admissible à l’inscription sur la Liste intérieure en vertu de l’alinéa 87(5)a) de la Loi sans qu’il soit nécessaire d’assurer le suivi des quantités fabriquées ou importées. Une fois qu’un avis de fabrication ou d’importation a été soumis, la soumission d’un avis de quantité excédentaire n’est plus exigée. Les renseignements qui doivent être fournis dans l’avis de fabrication ou d’importation sont indiqués ci-dessous.
10.1.5 Contenu et présentation des avis
Le déclarant qui a communiqué tous les renseignements sur une substance et qui a commencé à la fabriquer ou à l’importer peut présenter un avis de fabrication ou d’importation à tout moment avant l’atteinte des seuils de déclenchement indiqués à l’article 17 ou 18 du Règlement (consulter la partie 10.1.3.1). Toute personne qui a déjà déclaré une substance pour laquelle tous les renseignements n’ont pas été divulgués et qui a commencé à fabriquer ou importer la substance en quantités limitées peut présenter l’avis de fabrication ou d’importation au moment où il présente tout le reste des renseignements sur la substance en question.
Le déclarant qui a fourni tous les renseignements sur une substance et qui décide de ne pas présenter d’avis de fabrication ou d’importation est tenu de présenter un avis de quantité excédentaire dans les 30 jours qui suivent l’atteinte du seuil de déclenchement, tel qu’indiqué dans la partie 10.1.3.1 ci-dessus.
L’avis de quantité excédentaire ou l’avis de fabrication ou d’importation doivent être signés par le représentant du fabricant ou de l’importateur résident de la substance, le « déclarant », ou par l'agent de l’« importateur non-résident » de la substance, l’ « agent canadien ». L’avis doit indiquer ce qui suit :
- Le nom de la personne et le nom de l’entreprise;
- Le nom de la substance et, s’il y a lieu, sa dénomination maquillée approuvée;
- Le numéro de référence de DSN au sujet duquel les renseignements complets ont été fournis pour la substance; et
- Une indication que le seuil de déclenchement (consulter la partie 10.1.3.1) a été dépassé et la date à laquelle ce seuil a été dépassé (cette information n’est exigée que dans le cas d’un avis de quantité excédentaire); ou
- Une déclaration indiquant que la substance a été fabriquée ou importée (cette information n’est requise que pour un avis de fabrication ou d’importation; consulter la partie 10.1.4).
Les renseignements ci-dessus doivent être transmis à la Ligne d’information de la gestion des substances.
Une fois que les responsables du Programme des SN ont reçu un de ces avis, la substance déclarée peut être admissible pour son inscription sur la Liste intérieure si toutes les exigences décrites au paragraphe 87 de la Loi sont respectées (consulter la partie 10.2.1).
10.2 Les responsabilités du Programme des substances nouvelles
10.2.1 Inscription sur la Liste intérieure
En vertu de l’article 87 de la Loi, une substance doit être inscrite sur la Liste intérieure, et radiée de la Liste extérieure si cette substance y est inscrite, dans les 120 jours suivant le moment où les critères suivants sont satisfaits :
- Les renseignements prescrits à l’article 81 ou 82 de la Loi de même que les renseignements complémentaires ou les résultats d’essais requis en vertu du paragraphe 84(1) de la Loi ont été fournis;
- Le délai d'évaluation des renseignements prévu à l’article 83 de la Loi a pris fin;
- Aucune condition n’a été imposée à l’égard de la substance en vertu de l’alinéa 84(1)a) de la Loi;
- Une justification a été fournie pour justifier les demandes de confidentialité, s’il y a lieu (consulter la partie 2.1.2); et
- Un avis de fabrication ou d’importation prouvant que la substance a été fabriquée ou importée comme spécifié à la partie 10.1.4; ou
- Un avis de quantité excédentaire a été reçu dans les 30 jours suivants le dépassement des seuils de déclenchement de fabrication ou d’importation comme spécifié dans la partie 10.1.3.1.
Les substances pour lesquelles on ne prévoit pas de risque pour l’environnement et la santé humaine, quelle que soit leur utilisation courante, leur quantité ou toute autre activité prévue, seront inscrites sur la Liste intérieure sans restrictions. Les substances pour lesquelles une nouvelle activité qui pourrait changer le résultat de l’évaluation est envisagée seront inscrites sur la Liste intérieure avec une mention indiquant des exigences supplémentaires en matière de déclaration (consulter les parties 2.1.4 et 9.6.2). Les polymères pour lesquels on ne prévoit pas de risque pour l’environnement ni la vie et la santé humaine lorsqu’ils sont fabriqués ou importés en tant que polymères ERR seront inscrits sur la Liste intérieure avec une mention indiquant qu’une nouvelle déclaration sera exigée s’ils sont ensuite fabriqués ou importés au Canada sous une forme qui n’est plus considérée comme un polymère ERR.
Lorsque l’identité d’une substance admissible sur la Liste intérieure est demandée à être confidentielle par le déclarant et qu’une dénomination maquillée acceptable a été fournie, un numéro d’identification confidentielle (NIC) est attribué à celle-ci et est communiqué au déclarant. Le NIC et la dénomination maquillée acceptable sont ensuite inscrits sur la partie confidentielle de la Liste intérieure.
Appendice 1. Diagrammes de décision
Les diagrammes de décision figurant dans la présente appendice peuvent être consultés pour déterminer quelle annexe utiliser pour déclarer une substance en vertu du Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères). Les exigences en matière de renseignements sont cumulatives d’une sous-division à l’autre. Lors de la consultation des diagrammes de décision, les utilisateurs devraient d’abord choisir le diagramme approprié en fonction du type de substance qu’ils souhaitent déclarer. Ces diagrammes permettront aux utilisateurs de déterminer quels renseignements sont nécessaires et quand ils doivent être communiqués, en se basant sur les quantités seuils qui déclenchent l’obligation de fournir des renseignements.

Description longue
Les déclarants qui fabriquent ou importent une nouvelle substance chimique comme indiqué à l’article 5 du Règlement ou un nouveau polymère comme indiqué à l’article 6 du Règlement, c'est-à-dire une substance pour la recherche et le développement, une substance confinée qui est intermédiaire limitée au site ou une substance destinée à l’exportation, doivent présenter au ministre les renseignements de l’annexe appropriée avant de dépasser la quantité seuil qui s’applique et dans les délais prescrits pour cette annexe. La figure A1-1 illustre les délais prescrits et les renseignements à fournir pour ces substances :
- Pour une substance chimique/biochimique (article 5 du Règlement) :
- Présenter au ministre les renseignements prévus à l’annexe 11 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile.
- Actualiser tous les renseignements déjà fournis au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
- Pour un polymère/biopolymère (article 6 du Règlement) :
- Présenter au ministre les renseignements prévus à l’annexe 32 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
1Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’une substance biochimique [consulter les paragraphes 5(2), (3) et (4) du Règlement].
2Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’un biopolymère [consulter les paragraphes 6(2), (3) et (4) du Règlement].

Description longue
Les déclarants qui fabriquent ou importent une nouvelle substance chimique autre que celles indiquées à l’article 5 du Règlement (c'est-à-dire une nouvelle substance chimique autre que celles décrites dans la figure A1-1) doivent fournir au ministre les renseignements de l’annexe appropriée avant de dépasser la quantité seuil qui s’applique et dans les délais prescrits pour cette annexe. La figure A1-2 illustre les délais prescrits et les renseignements à fournir pour ces substances chimiques :
- Pour une substance chimique/biochimique qui figure sur la Liste extérieure (article 7 du Règlement) :
- Présenter au ministre les renseignements prévus à l’annexe 41 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile.
- Présenter au ministre les renseignements prévus à l’annexe 52 du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile
- Si la substance chimique est rejetée dans l’environnement aquatique en une quantité supérieure à 3 kg par jour par site (la moyenne devant être calculée sur une base mensuelle et après traitement des eaux usées) ou si le degré d’exposition du public à cette substance contenue dans un produit pourrait être élevé, présenter au ministre les renseignements supplémentaires sur les essais prescrits par les paragraphes 7(2) ou 7(3) du Règlement au moins 75 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 50 000 kg au cours d’une année civile.
- Pour une substance chimique/biochimique qui ne figure pas sur la Liste extérieure (article 8 du Règlement)3 :
- Présenter au ministre les renseignements prévus à l’annexe 44 du Règlement au moins 5 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 100 kg au cours d’une année civile.
- Présenter au ministre les renseignements prévus à l’annexe 54 du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile.
- Présenter au ministre les renseignements prévus à l’annexe 64 du Règlement au moins 75 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
1Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’une substance biochimique [consulter le sous-alinéa 7(1)a)(ii) du Règlement].
2Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’une substance biochimique [consulter le sous-alinéa 7(1)b)(ii) du Règlement]. Aucun autre renseignement additionnel ne sera exigé, sauf si, selon le cas : a) la substance chimique est rejetée dans l’environnement aquatique en une quantité supérieure à 3 kg par jour par site – la moyenne devant être calculée sur une base mensuelle et après traitement des eaux usées [consulter le paragraphe 7(2) du Règlement]; b) le degré d’exposition du public à la substance contenue dans un produit pourrait être élévé [consulter le paragraphe 7(3) du Règlement].
3Le ministre doit être avisé de l’inscription de la substance chimique ou biochimique sur la Liste extérieure si les renseignements visés au sous-alinéa 8(1)b)(i) du Règlement et à l’article 10 de l’annexe 5 ont été fournis avant son inscription [consulter le paragraphe 8(2) du Règlement].
4Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’une substance biochimique [consulter les sous-alinéas 8(1)a)(ii), b)(ii) et c)(ii) du Règlement].

Description longue
Les déclarants qui fabriquent ou importent un nouveau polymère autre que ceux indiqués à l’article 6 du Règlement (c'est-à-dire un nouveau polymère autre que ceux décrits dans la figure A1-1) doivent fournir au ministre les renseignements de l’annexe appropriée avant de dépasser la quantité seuil qui s’applique et dans les délais prescrits pour cette annexe. La figure A1-3 illustre les délais prescrits et les renseignements à fournir pour ces polymères :
- Pour un polymère/biopolymère qui est considéré comme un polymère ERR (article 9 du Règlement) :
- Présenter au ministre les renseignements prévus à l’annexe 92 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile1.
- Pour un polymère/biopolymère qui n’est pas considéré comme un polymère ERR et qui figure sur la Liste extérieure ou dont tous les réactifs figurent sur cette liste ou sur la Liste intérieure (article 11 du Règlement) :
- Présenter au ministre les renseignements prévus à l’annexe 92 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile1.
- Présenter au ministre les renseignements prévus à l’annexe 103 du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
- Si le polymère est rejeté dans l’environnement aquatique en une quantité supérieure à 3 kg par jour par site (la moyenne devant être calculée sur une base mensuelle et après traitement des eaux usées) ou si le degré d’exposition du public à ce polymère contenue dans un produit pourrait être élevé, présenter au ministre les renseignements supplémentaires sur les essais prescrits par les paragraphes 11(2) ou 11(3) du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 50 000 kg au cours d’une année civile.
- Pour un polymère/biopolymère qui n’est pas considéré comme un polymère ERR et qui ne figure pas sur la Liste extérieure ou dont un ou plusieurs réactifs ne figurent pas sur cette liste ou sur la Liste intérieure (article 12 du Règlement) :
- Présenter au ministre les renseignements prévus à l’annexe 92 du Règlement au moins 30 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 1 000 kg au cours d’une année civile1.
- Présenter au ministre les renseignements prévus à l’annexe 114 du Règlement au moins 60 jours avant que la quantité de la substance fabriquée ou importée ne dépasse 10 000 kg au cours d’une année civile.
1Article 10 du Règlement.
2Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’un biopolymère [consulter l'alinéa 10b) du Règlement].
3Ces renseignements n’ont pas à être fournis à l’égard des polymères à exigences réglementaires réduites. Des exceptions sont prévues au paragraphe 11(5) du Règlement. Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’un biopolymère [consulter l'alinéa 11(1)b) du Règlement]. Aucun autre renseignement additionnel ne sera exigé, sauf si, selon le cas : a) le polymère est rejeté dans l’environnement aquatique en une quantité supérieure à 3 kg par jour par site – la moyenne devant être calculée sur une base mensuelle et après traitement des eaux usées [consulter le paragraphe 11(2) du Règlement]; b) le degré d’exposition du public au polymère contenu dans un produit pourrait être élevé [consulter le paragraphe 11(3) du Règlement].
4Ces renseignements ne sont pas exigés pour les polymères à exigences réglementaires réduites. Des exceptions sont prévues au paragraphe 12(3) du Règlement. Des renseignements supplémentaires énumérés à l’annexe 2 sont également exigés s’il s’agit d’un biopolymère [consulter l'alinéa 12(1)b) du Règlement].
Appendice 2. Annexes de renseignements en vertu du Règlement
Annexe 1
[paragraphes 2(2) et 5(1) à (4)]
Renseignements sur les substances chimiques et biochimiques destinées à la recherche et au développement et celles, confinées, qui sont intermédiaires limitées au site ou destinées à l’exportation
Annexe 2
[paragraphes 2(2), 5(2) à (4) et 6(2) à (4), sous-alinéas 7(1)a)(ii) et b)(ii) et 8(1)a)(ii), b)(ii) et c)(ii) et alinéas 10b), 11(1)b), 12(1)b), 17(2)b) et 18(2)b) et c)]
Renseignements sur les substances biochimiques et les biopolymères
Annexe 3
[paragraphe 2(2) et article 6]
Renseignements sur les polymères et les biopolymères destinés à la recherche et au développement et ceux, confinés, qui sont intermédiaires limités au site ou destinés à l’exportation
Annexe 4
[paragraphe 2(2), sous-alinéas 7(1)a)(i), 8(1)a)(i) et 17(2)c)(i) et alinéa 17(2)d)]
Renseignements sur les autres substances chimiques et biochimiques non inscrites sur la Liste extérieure (100 kg) ou inscrites sur la liste extérieure (1 000 kg)
Annexe 5
[paragraphe 2(2), sous-alinéas 7(1)b)(i) et 8(1)b)(i), paragraphes 8(2) et 16(3), sous-alinéa 17(2)c)(i) et alinéa 17(2)d)]
Renseignements sur les autres substances chimiques et biochimiques non inscrites sur la Liste extérieure (1 000 kg) ou inscrites sur la liste extérieure (10 000 kg)
Annexe 6
[paragraphe 2(2), sous-alinéa 8(1)c)(i) et alinéa 17(2)d)]
Renseignements sur les autres substances chimiques et biochimiques non inscrites sur la Liste extérieure (10 000 kg)
Annexe 7
[paragraphe 2(2) et alinéas 9a) et b)]
Types de polymères
Annexe 8
[paragraphe 2(2) et alinéa 9c)]
Liste des réactifs et de leur numéro d’enregistrement CAS
Annexe 9
[paragraphe 2(2), alinéas 10a) et 18(2)b), sous-alinéa 18(2)d)(i) et alinéa 18(2)e)]
Renseignements sur les polymères à exigences réglementaires réduites et les autres polymères et biopolymères (1 000 kg)
Annexe 10
[paragraphe 2(2), alinéa 11(1)a), paragraphe 11(5) et sous alinéa 18(2)d)(i)]
Renseignements sur les autres polymères et biopolymères inscrits sur la Liste extérieure ou dont tous les réactifs sont inscrits sur la Liste intérieure ou la Liste extérieure (10 000 kg)
Annexe 11
[paragraphe 2(2), alinéa 12(1)a), paragraphe 12(3) et alinéa 18(2)e)]
Renseignements sur les autres polymères et biopolymères non inscrits sur la Liste extérieure (10 000 kg)
Annexe 12
[paragraphe 2(2)]
Présentation schématique des exigences sur les renseignements à fournir
Appendice 3. Dénomination des substances
A3.1 Représentation des substances par des structures bien définies
A3.1.1 Dénomination chimique de la substance
Il faut donner un nom qui décrit la substance en utilisant la nomenclature du Chemical Abstracts Service (CAS) ou de l’Union internationale de chimie pure et appliquée (UICPA). Tout nom ambigu ou incomplet ne convient pas pour l’identification de la substance ou pour une inscription ultérieure sur la Liste intérieure. Les abréviations, acronymes, noms de laboratoire, noms commerciaux, marques commerciales ou noms triviaux qui ne sont pas chimiquement descriptifs ne devraient pas être donnés. Des éclaircissements sur le niveau de précision requis sont donnés dans le tableau A3-1 du présent document.
Il ne faut jamais supposer qu’un nom ambigu convient du simple fait qu’un seul isomère est utilisé par une industrie particulière ou que le schéma structurel accompagne la déclaration.
Les noms commerciaux des colorants ne devraient pas être utilisés, à moins qu’ils ne correspondent à un nom du volume 5 du Colour Index. Le Colour Index est un ouvrage de référence pour les producteurs et les utilisateurs de colorants. Il est publié par la Society of Dyers and Colourists en collaboration avec l’American Association of Textile Chemists and Colourists.
Les noms des substances inorganiques devraient permettre d’identifier tous les éléments et spécifier leurs rapports. L’utilisation de formules empiriques ou des états d’oxydation est encouragée (les états d’oxydation sont les chiffres romains ajoutés entre parenthèses après l’élément).
A3.1.2 Formule moléculaire
La formule moléculaire est une somme des nombres totaux de chaque atome présent dans une substance. Dans le cas des sels ou des composés d’addition, la formule moléculaire peut être présentée sous la forme d’une formule brute unique ou sous la forme séparée par un point utilisée par le CAS.
Exemple : Acide succinique, sel de dilithium
LiO2C(CH2)2CO2Li
C4H4Li2O4
(sommation)
ou
HO2C(CH2)2CO2H · 2Li
C4H6O4 · 2Li
(séparation par un point)
| Exemple | Représentation structurale | Dénomination non acceptable | Dénomination acceptable |
|---|---|---|---|
| 1 | 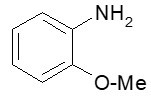 |
Anisidine |
o-Anisidine ou 2-Méthoxyaniline |
| 2 | 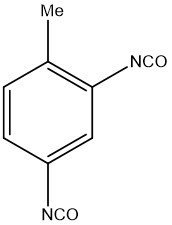 |
Diisocyanate de toluène ou TDI | Toluène-2,4-diisocyanate |
| 3 | ![C(=C\C(O)=O)/C(O)=O.[Na]](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-1-3.jpg) |
Fumarate de sodium ou Butènedioate monosodique |
Fumarate de monosodium ou trans-butènedioate monosodique ou E-butènedioate monosodique |
| 4 | 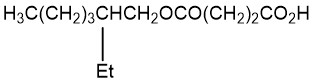 |
Succinate d’octyle ou Succinate d’éthylhexyle |
Succinate de mono(2-éthylhexyle) |
| 5 | 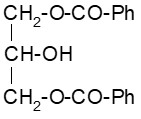 |
Benzoate de glycérol ou Dibenzoate de glycérol |
1,3-Dibenzoate de glycérol |
| 6 | 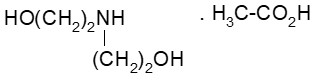 |
Acétate de diéthanolamine | Sel acétique de diéthanolamine |
| 7 | 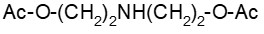 |
Acétate de diéthanolamine ou Ester acétique de diéthanolamine |
Ester diacétique de diéthanolamine |
| 8 | 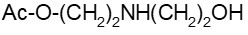 |
Acétate de diéthanolamine ou Ester acétique de diéthanolamine |
Ester monoacétique de diéthanolamine |
| 9 | 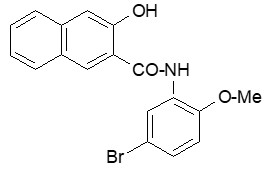
|
Bleu APM ou EMS 17 |
Brenthol BA ou C.I. 37532 ou C.I. Azoic Coupling Component 6 ou Bromo-5'; hydroxy-3 napht-2 o-anisidine ou N-(bromo-5 méthoxy-2 phényl) hydroxy-3 naphtalène |
| 10 | ![O=[Ti]O[Ti]=O](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-1-10.jpg)
|
Titanium oxide | Trioxyde de dititane (Ti2O3) |
A3.1.3 Information sur la structure
Le schéma structurel devrait clairement indiquer l’identité des atomes et la nature des liaisons. Cet appendice renseigne sur la façon de tracer ce schéma.
Les abréviations courantes sont acceptables dans la mesure où elles ne sont pas ambiguës. Le tableau A3-2 contient des exemples d’abréviations qui peuvent être utilisées.
| Exemple | Représentation structurale | Abréviation |
|---|---|---|
| 1 | ![[CH3]](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-1.jpg) |
-Me |
| 2 | ![[CH2]C](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-2.jpg) |
-Et |
| 3 | ![[CH2]CC](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-3.jpg) |
-Pr |
| 4 | C](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-4.jpg) |
-Pr-i or -Pr-iso |
| 5 | ![[CH2]CCC](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-5.jpg) |
-Bu |
| 6 | ![[CH2]C(C)C](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-6.jpg) |
-Bu-i or -Bu-iso |
| 7 | CC](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-7.jpg) |
-Bu-s or -Bu-sec |
| 8 | (C)C](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-8.jpg) |
-Bu-t or -Bu-tert |
| 9 | O](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-9.jpg) |
-CO2H |
| 10 | ](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-10.jpg) |
-CO- |
| 11 | ![[CH]=O](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-11.jpg) |
-CHO |
| 12 | C](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-12.jpg) |
-Ac |
| 13 | (=O)O](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-13.jpg) |
-SO3H |
| 14 | (=O)](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-14.jpg) |
-SO2- |
| 15 | ![[N]=O](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-15.jpg) |
-NO |
| 16 | ![[C]=1C=CC=CC1](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-2-16.jpg) |
-Ph |
Sauf indication contraire, il est supposé que les groupes alkyles sont normaux (linéaires). Si une substance possède des groupes alkyles non linéaires, la nature de la ramification devrait être décrite d’une manière aussi précise que possible. Le tableau A3-3 contient plusieurs représentations différentes du nonylphénol.
| Exemple | Dénomination déclarée | Représentation structurale | Numéro d’enregistrement CAS | Dénomination selon le CA index |
|---|---|---|---|---|
| 1 | p-Nonylphénol | 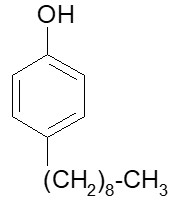 |
104-40-5 | Phénol, 4-nonyl- |
| 2 | p-Isononylphénol | ![OC1=CC=C([C9H19-iso])C=C1](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-3-2.jpg) |
26543-97-5 | Phénol, 4-isononyl- |
| 3 | 4-Nonylphénol, ramifié | ![OC1=CC=C([C9H19-ramifié])C=C1](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-TableA3-3-3-FR.jpg) |
84852-15-3* | Phénol, 4-nonyl-, ramifié |
| 4 | p-Tripropylène phénol | ![OC1=CC=C([C9H19])C=C1](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-TableA3-3-4.jpg) |
87247-00-5 | Phénol, 4-tripropylène- |
Il n’est pas nécessaire d’indiquer explicitement les atomes de carbone et les atomes d’hydrogène des systèmes cycliques.
Par exemple :
Toutes les caractéristiques stéréochimiques connues devraient être indiquées en précisant si elles sont absolues ou relatives. Par exemple :
CCC1](/content/dam/eccc/images/pded/final-guidance-document-cp/20220927-IMG17-FR.jpg)
Le rapport entre les composants d’un composé d’addition ou d’un sel devrait être clairement indiqué si plus d’une forme est théoriquement possible. Il faut aussi indiquer si ce rapport est inconnu.
Par exemple :
![N(CC(O)=O)(CC(O)=O)CCN(CC(O)=O)(CC(O)=O).[Na].[Na]](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-IMG18.jpg)
![N(CC(O)=O)(CC(O)=O)CCN(CC(O)=O)(CC(O)=O).[Na].[Na].[Na].[Na]](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-IMG19.jpg)
![N(CC(O)=O)(CC(O)=O)CCN(CC(O)=O)(CC(O)=O).[Na] where the number of [Na] salts is x](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-IMG20.jpg)
A3.1.3.1 Exemples de substances bien définies
Les exemples suivants (1-17) illustrent les renseignements nécessaires pour identifier et représenter de façon unique des substances ayant une structure bien définie.
Exemple 1
- Dénomination chimique de la substance : N-(s-butoxyméthyl)acrylamide
- Formule moléculaire : C8H15NO2
- Information sur la structure :
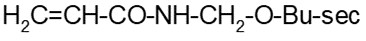
- Remarque : La ramification des groupes alkyles doit être indiquée pour ne pas que l’on suppose qu’ils sont linéaires. Par exemple, le groupe Bu de la représentation suivante serait représenté de manière linéaire sous la forme -CH2CH2CH2CH3.
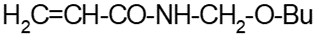
Exemple 2
- Dénomination chimique de la substance : 1,1-di-3,4-xylyléthane; 1,1-bis(3,4-diméthylphényl)éthane
- Formule moléculaire : C18H22
- Information sur la structure :
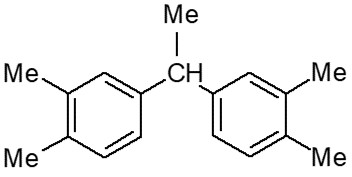
- Remarque : Le point-virgule sert à séparer les 2 noms. Dans les deux noms, des symboles indicateurs de position s’y trouvent. La dénomination dixylyléthane ne convient pas pour cette substance.
Exemple 3
- Dénomination chimique de la substance : sébacate de sodium; décanedioate de sodium
- Formule moléculaire : C10H18O4 · x Na
- Information sur la structure :
![O=C(O)CCCCCCCCC(=O)O.[Na] où il y a x nombre de sels [Na]](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-Example3.jpg)
- Remarque : Le signe « x » dans la formule moléculaire et dans le schéma structurel indique clairement que la proportion est inconnue.
Exemple 4
- Dénomination chimique de la substance : sébacate de disodium; décanedioate de disodium
- Formule moléculaire : C10H18O4 · 2 Na
- Information sur la structure :
![O=C(O)CCCCCCCCC(=O)O.[Na] où il y a x nombre de sels [Na]](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-Example4-1.jpg)
- Remarque : Il faut préciser les proportions dans la dénomination, la formule et le schéma de structure lorsqu’elles sont connues. La formule C10H16Na2O4 pourrait également être donnée. Le schéma de structure pourrait aussi être donné sous la forme :
![O=C(O[Na])CCCCCCCCC(=O)O[Na]](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-Example4-2.jpg)
Exemple 5
- Dénomination chimique de la substance : 1,3-pentadiène; pipérylène
- Formule moléculaire : C5H8
- Information sur la structure :
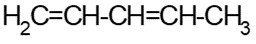
- Remarque : La stéréochimie n’est pas mentionnée dans la dénomination ni dans la structure. Consulter l’exemple 6 qui représente un stéréoisomère spécifique.
Exemple 6
- Dénomination chimique de la substance : cis-1,3-pentadiène; Z-1,3-pentadiène;cis-pipérylène
- Formule moléculaire : C5H8
- Information sur la structure :
- Remarque : La stéréochimie est indiquée dans la dénomination et dans la structure. Consulter l’exemple 5 qui représente une substance non stéréospécifique.
Exemple 7
- Dénomination chimique de la substance : chromate (IV) de manganèse (II); chromate de manganèse (MnCrO4); oxyde de chrome et de manganèse (MnCrO4)
- Formule moléculaire : H2CrO4 · Mn
- Information sur la structure :
(O)O.[Mn]](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-Example7-1.jpg)
- Remarque : Les notations de Stock (degré d’oxydation) et les formules empiriques devraient être mentionnées lorsqu’elles sont connues. La représentation suivante est également acceptable :
([O-])[O-].[Mn++]](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-Example7-2.jpg)
Exemple 8
- Dénomination chimique de la substance : PVC; poly(chlorure de vinyle)
- Formule moléculaire : (C2H3Cl)x
- Information sur la structure :

- Remarque : Les substances polymériques doivent être décrites en tenant compte de leurs réactifs de départ. Les réactifs de départ sont définis comme ceux qui font partie de la composition du polymère. Si le rôle du réactif ABIN est l’amorçage de la réaction, ce réactif ne devrait pas figurer dans la description du polymère sur la Liste intérieure. Si l’ABIN est commercialisé, il doit être déclaré séparément.
Exemple 9
- Dénomination chimique de la substance : copolymère d’acide maléique, phtalate de diméthyle, éthylèneglycol; polymère d’acide cis-but-2-ènodioïque, phtalate de diméthyle, éthylèneglycol
- Formule moléculaire : (C2H6O2-C4H4O4-C10H10O4)x
- Information sur la structure :
Exemple 10
- Dénomination chimique de la substance : éther mono-allylique de styrènepolyéthylèneglycol
- Formule moléculaire : ((C2H4O)nC3H6O · C8H8)x
- Information sur la structure :
- Remarque : Pour décrire les réactifs, les noms et les numéros d’enregistrement CAS peuvent être utilisés plutôt qu’une structure chimique. Les dérivés du polyglycol devraient être représentés en fonction de leur structure polymérique.
Exemple 11
- Dénomination chimique de la substance : 2,4,4-triméthyl-2-pentène
- Formule moléculaire : C8H16
- Information sur la structure :
- Remarque : La dénomination dimère d’isobutylène ne constitue pas une dénomination chimique appropriée pour cette structure. Les désignations comme dimère ou trimère ne sont appropriées que si le degré de polymérisation est une valeur spécifique comprise entre 2 et 10 et que la structure spécifique est inconnue.
Exemple 12
- Dénomination chimique de la substance : ar-nitro-6-hexyl-1-naphtol; ar-nitro-6-hexyl-1-hydroxynaphtalène
- Formule moléculaire : C16H19NO3
- Information sur la structure :
=O) où la spécificité de ([N+]([O-])=O) sur le premier anneau aromatique est inconnue](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-Example12.jpg)
- Remarque : Comparer avec les exemples 13 et 14. La représentation de la structure devrait donner tous les renseignements spécifiques connus.
Exemple 13
- Dénomination chimique de la substance : 6-(nitrohexyl)-1-naphthol; 6-(nitrohexyl)-1-hydroxynaphtalène
- Formule moléculaire : C16H19NO3
- Information sur la structure :
CCCCCCC1=CC=C2C(O)=CC=CC2=C1 où la spécificité de O=[N+]([O-]) sur le groupe hexyl est inconnue](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-Example13.jpg)
- Remarque : Comparer avec les exemples 12 et 14. La représentation de la structure devrait donner tous les renseignements spécifiques connus.
Exemple 14
- Dénomination chimique de la substance : 2 ou 3-nitro-6-hexyl-1-naphtol; 2 ou 3-nitro-6-hexyl-1-hydroxynaphtalène
- Formule moléculaire : C16H19NO3
- Information sur la structure :
=O)C=CC2=C1 ou CCCCCCC1=CC=C2C(O)=CC([N+]([O-])=O)=CC2=C1](/content/dam/eccc/images/pded/final-guidance-document-cp/20220317-Example14.jpg)
- Remarque : Comparer avec les exemples 12 et 13. La représentation de la structure devrait donner tous les renseignements spécifiques connus.
Exemple 15
- Dénomination chimique de la substance : nickel d’aluminium
- Formule moléculaire : Ni3Al
- Information sur la structure : Ni3Al
- Remarque : La stœchiométrie connue devrait être indiquée. La dénomination NiAl ne serait pas acceptable.
Exemple 16
- Dénomination chimique de la substance : geikielite synthétique
- Formule moléculaire : Mg-O3Ti
- Information sur la structure : Mg(TiO3)
- Remarque : Les minéraux synthétiques devraient être indiqués comme tels dans la dénomination chimique de la substance.
Exemple 17
- Dénomination chimique de la substance : hexahydrate de pipérazine; arpézine
- Formule moléculaire : C4H10N2 · 6 H2O
- Information sur la structure :
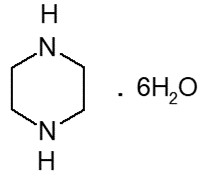
- Remarque : Les substances décrites comme des hydrates devraient être représentées sous leur forme anhydre.
A3.2 Représentation des substances complexes et variables
Les substances qui ne peuvent être représentées par une structure chimique et une formule moléculaire complètes sont reconnues comme des substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques (substances of Unknown or Variable composition, Complex reaction products or Biological materials – UVCB).
A3.2.1 Dénomination chimique de la substance
Les directives pour la dénomination des substances UVCB sont semblables à celles données à la partie A3.1 pour les substances bien définies et elles devraient être consultées pour obtenir plus de renseignements. Le tableau A3-4 donne plus de précisions sur le degré de spécificité requis.
| Exemple | Représentation structurale | Dénomination non acceptable | Dénomination acceptable |
|---|---|---|---|
| 1 | =O)=CC([N+]([O-])=O)=C1C)(O[Na])=O avec le polysulfure de sodium](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-TableA3-4-1-FR.jpg) |
RGP Brown ou polysulfure sodique d’acide dinitrotoluène sulfonique |
C.I. sulphur Brown 42 ou C.I. 53030 ou thionone Brown R0 ou produit de réaction du 3,5‑dinitro-o-toluènesulfonate de monosodium avec le polysulfure de sodium |
| 2 | ![Bromination chlorination de C=C[R] où R = Alkyle en C10-28](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-TableA3-4-2-FR.jpg) |
Alcènes en C12-30 halogénés en α ou bromo et chloroalcènes |
Dérivés bromés ou chlorés de α d’-alcènes en C12-30 ou α-alcènes C12-30 bromés et chlorés ou alcènes en C12-30 bromés et chlorés en α |
| 3 | 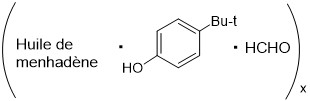 |
Huile de poisson, butylphénol, résine de formaldéhyde ou huile marine, p-tert-butylphénol, résine de formaldéhyde ou huile de menhadène, 4-butylphénol, résine de formaldéhyde |
Huile de menhadène, p-tert-butylphénol, résine de formaldéhyde |
| 4 | Acides gras d’huile de lin · x Na |
Sels sodiques d’acides gras d’origine végétale ou sels sodiques de graines de lin ou sels sodiques d’huile de lin |
Sels de sodium d’acides gras d’huile de lin ou acides gras, huile de lin, sels sodiques |
| 5 | ![O=C(OR)C=1C=CC=CC1C(=O)O où R = [alkyle ramifié en C8-10]](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-TableA3-4-5-FR.jpg) |
Phtalate de nonyle ou phtalate d’isononyle ou monophthalate d’alkyle en C8-10 |
Monophtalate d’alkyle ramifié en C8-10 ou esters monoalkyliques ramifiés en C8-10 de l’acide 1,2-benzènedicarboxylique |
| 6 | ![O=C(OR)C=1C=CC=CC1C(=O)OR où R = [alkyle ramifié en C8-10]](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-TableA3-4-6-FR.jpg) |
Phtalate de dinonyle ou phtalate de diisononyle ou phtalate de di-C8-10-alkyle |
Phtalate de di-C8-10-alkyle ramifié ou esters dialkyliques ramifiés en C8-10 de l’acide 1,2-benzènedicarboxylique |
| 7 | 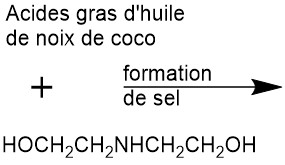 |
Produit de réaction d’acides gras d’huile de noix de coco avec la diéthanolamine |
Acides gras d’huile de noix de coco – sel de la diéthanolamine ou acides gras d’huile de coco, composés avec la diéthanolamine ou acides gras, coco, composés avec la diéthanolamine |
| 8 |  |
Acides gras d’huile de coco, produit de réaction avec la diéthanolamine |
Monoester d’acides gras d’huile de coco et de diéthanolamine ou acides gras, coco, ester 2-(2-hydroxyéthyl)amino éthylique |
| 9 | ![N=1CCN(CCO)C1([nor coco alkyle])](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-TableA3-4-9-FR.jpg) |
Produit de réaction de l’huile de noix de coco avec l’amino-éthyléthanolamine ou alkylimidazolineéthanol de coco |
Produit de la cyclisation de l’huile de noix de coco et de la N-(2-aminoéthyl)éthanolamine ou dérivés 4,5-dihydro-2-norcoco alkyliques du 1H-imidazoléthanol |
A3.2.2 Formule moléculaire
La plupart des substances UVCB ne peuvent être représentées par une formule moléculaire spécifique. Toutefois, dans certains cas, il est possible de fournir une formule moléculaire représentant l’intervalle du nombre et des types précis d’atomes présents dans une molécule. Les formules moléculaires hypothétiques ou idéalisées ne doivent pas être données.
Les formules moléculaires de sels et de composés d’addition, si elles sont fournies, peuvent être présentées sous la forme d’une formule brute unique ou sous la forme séparée par un point utilisée par le CAS.
Exemple : Acide alkyl(C6-12)dicarboxylique, sel disodique
NaO2C-C6-12alkyl-CO2Na
C8-14H12-24Na2O4
ou
HO2C-C6-12alkyl-CO2H · 2Na
C8-14H14-26O4 · 2Na
A3.2.3 Lignes directrices générales
Comme il est impossible, dans la plupart des cas, d’établir un schéma structurel unique, des renseignements descriptifs sur la substance, ses composants ou ses précurseurs devraient être donnés.
S’il est possible de fournir une structure chimique partielle, elle devrait clairement indiquer l’identité des atomes et la nature des liaisons. Des abréviations courantes pour les substituants et les groupes fonctionnels sont acceptables à condition qu’elles ne soient pas ambiguës. Sauf indication contraire, il est supposé que les groupes alkyles sont normaux (linéaires).
Les représentations des substances devraient décrire toutes les caractéristiques connues, comme la proportion des sels et les caractéristiques stéréochimiques.
Les exemples suivants (18-23) illustrent le niveau de spécificité qui devrait être donné. Il est fortement recommandé que le déclarant se conforme au style de ces exemples.
Exemple 18
- Dénomination chimique de la substance : amides N,N-diisopropyliques d’acides gras de tallöl
- Formule moléculaire : aucune possible
- Information sur la structure :
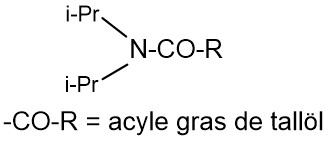
- Remarque : Une substance peut être décrite au moyen d’une structure chimique partielle.
Exemple 19
- Dénomination chimique de la substance : dioxyde-S,S de 4-(C5-11-alkyl)-1,2-oxathiolane
- Formule moléculaire : aucune possible
- Information sur la structure :
![[alkyles en C5-11]C1COS(C1)(=O)=O](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-Example19-FR.jpg)
- Remarque : L’intervalle de carbone des groupes alkyles doit être indiqué.
Exemple 20
- Dénomination chimique de la substance : éthoxylate d’alkylphénol en C8 ramifié
- Formule moléculaire : (C2H4O)nC14H23O
- Information sur la structure :
![C=1C(OCC)=CC=C([C8H17-ramifiés])C1 où (OCC) est une unité polymérique répétée n nombre de fois et où la spécificité de (OCC) et de ([C8H17-ramifiés]) est inconnue](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-Example20-FR.jpg)
- Remarque : Les représentations devraient indiquer toutes les caractéristiques spécifiques connues, y compris les renseignements sur la structure des groupes alkyles.
Exemple 21
- Dénomination chimique de la substance : acide 5-norbornène-2,3-dicarboxylique chloré; dérivés chlorés de l’acide 5-bicyclo (2.2.1) heptène-2,3-dicarboxylique
- Formule moléculaire : C9H(10-x)ClxO4
- Information sur la structure :
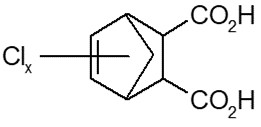
Exemple 22
- Dénomination chimique de la substance : huile de carthame, polymérisée avec de l’acide adipique, le glycérol et l’anhydride phtalique
- Formule moléculaire : aucune possible
- Information sur la structure :
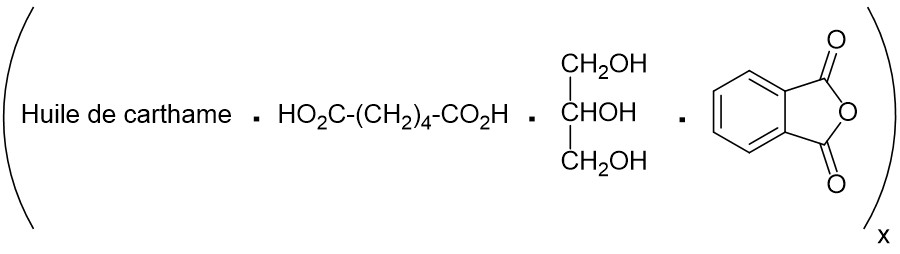
Exemple 23
- Dénomination chimique de la substance : sel disodique du monononyl (ramifié) phénylester phosphorique
- Formule moléculaire : C15H25O4P · 2 Na
- Information sur la structure :
![C=1C(OP(=O)(O)O)=CC=C([C9H19-branched])C1.[Na].[Na] où la spécificité de (OP(=O)(O)O) et de ([C9H19-branched]) est inconnue](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-Example23-FR.jpg)
A3.2.4 Produits animaux et végétaux
Les substances complexes et variables qui sont produites par modification chimique de produits d’origine naturelle ou qui sont séparées de ceux-ci par un procédé physiqueNote de bas de page 18 doivent être identifiées par leur genre et leur espèce, ainsi que d’autres noms non ambigus indiquant leur origine.
Il ne faut jamais supposer qu’un nom commun est adéquat du simple fait qu’une seule source est utilisée par une industrie particulière. Par exemple, le terme « huile de menthe » ne devrait pas être utilisé pour désigner l’huile de menthe japonaise, l’essence de bergamote, l’essence de menthe verte ou l’essence de menthe poivrée. De même, le terme « huile végétale » ne devrait pas être utilisé pour désigner l’huile de maïs, l’huile de soja ou l’huile de lin.
Les exemples suivants (24-30) illustrent le niveau de spécificité qui devrait être donné.
Exemple 24
- Dénomination chimique de la substance : sels diéthylènetriamine des acides gras de soja
- Formule moléculaire : aucune possible
- Information sur la structure :
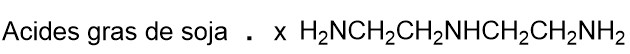
Exemple 25
- Dénomination chimique de la substance : esters de méthyle d’acides gras de mélange d’huiles végétales
- Formule moléculaire : aucune possible
- Information sur la structure : Esters de méthyle d’acides gras provenant d’huiles végétales mélangées
- Remarque : L’expression « mélange de végétaux » devrait être utilisée dans le nom d’une substance lorsque celle-ci est obtenue à partir d’un procédé de fabrication où entrent divers types de végétaux.
Exemple 26
- Dénomination chimique de la substance : huile de menthe japonaise; huile de menthe poivrée japonaise
- Formule moléculaire : aucune possible
- Information sur la structure : Huile extraite de Mentha arvensis, variété piperascens
- Remarque : Le genre et l’espèce de la plante dont l’essence a été extraite doit être indiqué.
Exemple 27
- Dénomination chimique de la substance : huile de Mentha citrata; huile de menthe bergamote
- Formule moléculaire : aucune possible
- Information sur la structure : Huile extraite de Mentha citrata
- Remarque : L’appellation « huile de bergamote » ne serait pas un nom chimique approprié pour cette substance, car l’huile de bergamote est aussi extraite du Citrus bergamia
Exemple 28
- Dénomination chimique de la substance : huile de lemongrass acétylée
- Formule moléculaire : aucune possible
- Information sur la structure :

- Remarque : Le genre et l’espèce, Cymbopogon citratus, sont associés au numéro d’enregistrement CAS 8007-02-1* dans la partie des définitions chimiques de la Toxic Substances Control Act (TSCA).
Exemple 29
- Dénomination chimique de la substance : fraction d’huile de bergamote sans terpènes
- Formule moléculaire : aucune possible
- Information sur la structure : Fraction exempte de terpènes distillée à partir d’huile extraite de Citrus bergamia
Exemple 30
- Dénomination chimique de la substance : distillat désodorisant d’huile de maïs
- Formule moléculaire : aucune possible
- Information sur la structure : Mélange complexe d’acides gras, de stérols, d’aldéhydes, de cétones et d’autres composés produits par distillation à la vapeur d’huile de maïs suivie d’une condensation de la vapeur contenant ces matières
A3.2.5 Produits de réaction
Le schéma de réaction devrait inclure l’identité chimique des précurseurs immédiats, la nature de la réaction ainsi que les réactifs, peu importe si ces derniers sont implicitement indiqués par le type de réaction. La réaction devrait être décrite aussi précisément que possible (par exemple acétylation, hydrolyse alcaline, chloration, diazotation, époxydation). Pour décrire une réaction, les termes généraux tels qu’addition, condensation ou réaction ne devraient pas être utilisés.
Bien que la substance elle-même puisse être un UVCB, ses précurseurs ou composants peuvent être des substances bien définies. Toute description fournie pour des précurseurs ou des composants bien définis devrait satisfaire aux critères cités plus haut.
Les exemples suivants (31-36) illustrent le niveau de spécificité qui devrait être donné.
Exemple 31
- Dénomination chimique de la substance : polymère de méthacrylate, d’acide méthacrylique et de bromotrichlorométhane
- Formule moléculaire : (C4H6O2 · C5H8O2)x · x CBrCl3
- Information sur la structure :
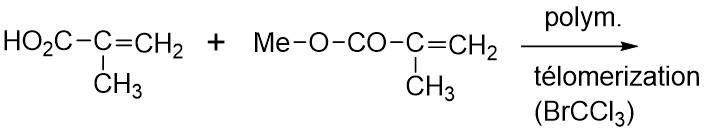
Exemple 32
- Dénomination chimique de la substance : acide 5-norbornène-2,3-dicarboxylique chloré; dérivés chlorés de l’acide 5-bicyclo (2.2.1)heptène-2,3-dicarboxylique
- Formule moléculaire : C9H(10-x)ClxO4
- Information sur la structure :

- Remarque : Comparer avec l’exemple 21. Les deux méthodes sont acceptables. Les deux méthodes ont le même degré de spécificité.
Exemple 33
- Dénomination chimique de la substance : sel disodique du monononyl (ramifié) phénylester phosphorique
- Formule moléculaire : C15H25O4P · 2Na
- Information sur la structure :
![Estérification de OP(=O)(O)O et de C=1C(OH)=CC=C([C9H19-ramifié])C1 où la spécificité de OH et de ([C9H19-ramifié]) est inconnue, et neutralisé part du [Na]O](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-Example33-FR.jpg)
- Remarque : Comparer avec l’exemple 23. Les deux méthodes sont acceptables. Les deux méthodes ont le même degré de spécificité.
Exemple 34
- Dénomination chimique de la substance : copolymère de l’anhydride phtalique et du triméthylolpropane, pélargonate
- Formule moléculaire : (C8H4O3 · C6H14O3)x · x C9H17O2
- Information sur la structure :
![Estérification avec du O=C([O-])CCCCCCCC du copolymère O=C1OC(=O)C2=CC=CC=C12.OCC(CO)(CO)CC](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-Example34-FR.jpg)
Exemple 35
- Dénomination chimique de la substance : C.I. acid black 47; C.I. 56055; sulfonine grey G
- Formule moléculaire : C16H12N2O2 · x H2SO4
- Information sur la structure :
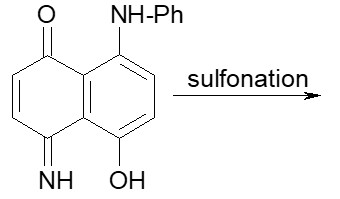
Exemple 36
- Dénomination chimique de la substance : amides d’éthanolamine d’acides gras de suif
- Formule moléculaire : aucune possible
- Information sur la structure :
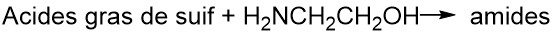
- Remarque : Comme les acides gras de suif et l’éthanolamine peuvent réagir pour former une variété de produits différents (par exemple sels, esters, produits de cyclisation), la description du produit devrait être aussi spécifique que possible et inclure la composition typique.
A3.2.6 Produits obtenus par des procédés industriels
Certaines substances complexes et variables sont plus facilement décrites au moyen d’un texte plutôt que de schémas structurels ou de réaction.
La description devrait inclure les précurseurs, la méthode de préparation, le procédé d’obtention (ébullition à basse température, reformage catalytique), les propriétés physiques (si elles sont connues) et la composition chimique typique. En particulier, les renseignements sur la substance devraient la décrire d’une manière aussi unique que possible et comprendre les renseignements suivants (s’ils sont connus) :
- la description du procédé (par exemple craquage catalytique, déparaffinage, distillation destructrice);
- le nombre minimal et maximal de carbones (alkyles) (par exemple C4 à C12);
- les propriétés physiques (par exemple intervalle d’ébullition, viscosité, solide, scorie, point de ramollissement);
- la composition chimique principale (par exemple hydrocarbures, sulfures, terpènes);
- l’origine (par exemple pétrole, charbon).
Si possible, il est recommandé de fournir des schémas représentant le procédé industriel et l’étape durant laquelle la substance déclarée est isolée.
La description ne devrait pas inclure de termes vagues ou non descriptifs, ou encore de jargon commercial non défini.
Les exemples suivants (37-45) illustrent le niveau de spécificité qui devrait être communiqué. Des exemples supplémentaires sur les renseignements descriptifs requis peuvent être consultés dans le champs présentant les définitions des substances chimiques (Chemical Substance Definitions) de l’inventaire de la TSCA (consulter l’appendice 4).
Exemple 37
- Dénomination chimique de la substance : résidus de la distillation des benzènes alkyliques en C9-13
- Formule moléculaire : aucune possible
- Information sur la structure : Résidus complexes de la distillation des benzènes alkyliques en C9-13 ayant un point d’ébullition > 600°F. Se composent principalement de diphénylalcanes, de dialkylbenzènes et de diphényldialcanes. Les groupes alkyles sont des groupes linéaires en C9-13.
Exemple 38
- Dénomination chimique de la substance : laitier de haut-fourneau provenant de la production de métaux ferreux
- Formule moléculaire : aucune possible
- Information sur la structure : Substance fondue forée par l’action d’un fondant sur la gangue des matériaux ferreux chargés dans le haute-fourneau et sur les impuretés oxydées dans la production du fer. Se compose principalement de soufre et d’oxydes de Al, Ca, Mg et Si.
Exemple 39
- Dénomination chimique de la substance : lessive noire oxydée; lessive résiduaire, oxydée
- Formule moléculaire : aucune possible
- Information sur la structure : Substance résultant de l’oxydation de la lessive noire par différentes substances chimiques utilisées dans les procédés kraft, au bisulfite, semi chimique ou autres de fabrication de pâte. Se compose principalement de lignosulfonates partiellement oxydés, de sucres et d’hémicelluloses.
Exemple 40
- Dénomination chimique de la substance : résidus de la fraction quinoléine d’extraits alcalins du goudron de charbon
- Formule moléculaire : aucune possible
- Information sur la structure :

Exemple 41
- Dénomination chimique de la substance : coke de charbon
- Formule moléculaire : aucune possible
- Information sur la structure : Résidu carboné de distillation destructive à haute température (> 700°C) du charbon. Se compose principalement de carbone, mais peut contenir du soufre et des cendres.
Exemple 42
- Dénomination chimique de la substance : coke de pétrole
- Formule moléculaire : aucune possible
- Information sur la structure : Résidu carboné de la distillation destructive à haute température de fractions du pétrole. Se compose principalement de carbone, mais peut contenir certains hydrocarbures à haute proportion carbone/hydrogène.
Exemple 43
- Dénomination chimique de la substance : huile de naphte à large intervalle d’ébullition (pétrole), hydrodésulfuration
- Formule moléculaire : aucune possible
- Information sur la structure : Une combinaison complexe d’hydrocarbures obtenue à partir d’un procédé catalytique d’hydrodésulfuration. Il s’agit d’hydrocarbures ayant un nombre de carbones allant principalement de C4 à C12 et un point d’ébullition situé approximativement entre 30 et 250°C.
Exemple 44
- Dénomination chimique de la substance : laitier de fusion du cuivre
- Formule moléculaire : aucune possible
- Information sur la structure : Substance résultant de la fusion du cuivre et de métaux précieux obtenus de sources primaires et secondaires et d’installations de recyclage. Se compose principalement d’oxydes de fer et SiO2. Peut aussi contenir du Cu, Pb, Ni et autres métaux et oxydes non ferreux.
Exemple 45
- Dénomination chimique de la substance : bleu d’olivine vanadium
- Formule moléculaire : aucune possible
- Information sur la structure : Pigment inorganique formé par la calcination à haute température de l’oxyde de vanadium (IV) et de l’oxyde de silicium en quantités variables. Une matrice cristalline se forme par diffusion ionique. Des halogénures alcalins-ou alcalino-terreux peuvent être inclus comme modificateurs.
A3.2.7 Combinaisons de substances UVCB
En raison de la complexité de certaines substances UVCB, il est nécessaire de décrire les précurseurs, les réactifs, le schéma de réaction et la substance déclarée aussi précisément que possible lorsque des substances produites par la combinaison d’UVCB sont déclarées. Il est fortement recommandé d’étudier avec attention toutes les parties du présent appendice avant de déclarer ce type de substances.
Les exemples suivants (46-48) illustrent le niveau de spécificité qui devrait être donné.
Exemple 46
- Dénomination chimique de la substance : composé du produit de cyclisation de l’huile de palme et de la diéthylènetriamine avec des résidus de distillation
- Formule moléculaire : aucune possible
- Information sur la structure :
![N=1CCN(CCN)C1([alkyles d'huile de palme])](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-Example46-FR.jpg) Résidus de la distillation des acides monobasiques en C6-18 saturés et insaturés et des acides dibasiques en C8-15. Se composent de sels d’acides dibasiques en C9-18 saturés. Peuvent aussi contenir des polymères, des anhydrides et des polyesters.
Résidus de la distillation des acides monobasiques en C6-18 saturés et insaturés et des acides dibasiques en C8-15. Se composent de sels d’acides dibasiques en C9-18 saturés. Peuvent aussi contenir des polymères, des anhydrides et des polyesters.
Exemple 47
- Dénomination chimique de la substance : composé du produit de cyclisation de l’huile de palme et de la diéthylènetriamine avec des résidus de distillation
- Formule moléculaire : aucune possible
- Information sur la structure :
![N=1CCN(CCN)C1([alkyles d'huile de palme]) et distillats légers de pétrole oxydés (64742-98-9*) qui réagissent ensemble pour donner des sels](/content/dam/eccc/images/pded/final-guidance-document-cp/20220322-Example47-FR.jpg)
- Remarque : L’utilisation du numéro d’enregistrement CAS 64742-98-9* élimine l’obligation d’inclure une longue description des produits de départ.
Exemple 48
- Dénomination chimique de la substance : fraction sesquiterpénique oxydée d’huile de bois de cèdre
- Formule moléculaire : aucune possible
- Information sur la structure :

Appendice 4. Recherche des numéros d’enregistrement du Chemical Abstracts Service
Le présent appendice décrit les différentes sources pouvant être utilisées pour identifier les numéros d’enregistrement du Chemical Abstracts Service (CAS).
A4.1 Services du registre du Chemical Abstracts Services
En utilisant les services du registre du CAS, les déclarants peuvent obtenir les numéros d’enregistrement CAS ou les noms selon l’index Chemical Abstracts pour les substances confidentielles. Ce service fournit les numéros d’enregistrement CAS aux clients soit en leur communiquant les numéros d’enregistrement CAS existants, soit en assignant un numéro d’enregistrement CAS nouveau aux substances qui satisfont aux critères établis pour l’inscription à ce registre.
Il est possible de rechercher les numéros d’enregistrement CAS existants dans la collecte de contenu CAS en utilisant l’outil de recherche en ligne CAS SciFindern (en anglais seulement). Pour de plus amples renseignements, veuillez consulter la foire aux questions du registre CAS et des numéros d’enregistrement CAS (en anglais seulement).
A4.2 Autres inventaires et bases de données
Pour aider dans l’identification de substances, les inventaires et bases de données suivants peuvent être consultés pour identifier les numéros d’enregistrement CAS et autres renseignements techniques :
- L’inventaire de la TSCA (en anglais seulement) : l’inventaire des substances chimiques de la Toxic Substances Control Act (TSCA) inclut plus de 85 000 substances chimiques fabriquées, importées ou transformées aux ÉtatsUnis;
- L’inventaire CE (en anglais seulement) : l’inventaire CE de l’Agence européenne des produits chimiques (European Chemicals Agency - ECHA) inclut plus de 100 000 substances provenant de l’Inventaire européen des substances chimiques commerciales existantes (European Inventory of Existing Commercial Substances - EINECS), de la Liste européenne des substances chimiques déclarées (European List of Notified Chemical Substances - ELINCS) et de la Liste des polymères qui ne sont plus considérés comme des polymères (No-Longer Polymers - NLP);
- L’infobase PCPC en ligne (en anglais seulement) : le Conseil des produits de soins personnels (Personal Care Products Council - PCPC) inclut plus de 27 000 ingrédients cosmétiques identifiés par leur nom conformément à la Nomenclature internationale des ingrédients cosmétiques (International Nomenclature Cosmetic Ingredient - INCI);
- Programme des DCI et classification des produits médicaux (en anglais seulement) : les Dénominations communes internationales (DCI) facilitent l’identification des substances pharmaceutiques ou des principes actifs pharmaceutiques. Chaque DCI est une appellation unique d’une substance active qui est commercialisée en tant que substance pharmaceutique et qui est reconnue au niveau mondial;
- Base de données RTECS : la base de données du Registre des effets toxiques des substances chimiques (Registry of Toxic Effects of Chemical Substances – RTECS) améliorée par le Centre canadien d’hygiène et de sécurité au travail (CCHST) renferme des données toxicologiques concernant plus de 194 000 substances chimiques;
- Base de données en ligne du Merck Index (en anglais seulement) : le Merck Index en ligne de la Royal Society of Chemistry est une base de données qui inclut des substances chimiques, des médicaments et des produits biologiques et qui renferme plus de 11 500 monographies;
- Dictionnaire USP (en anglais seulement) : cette publication de la Pharmacopée des États-Unis (United States Pharmacopeia - USP) est un dictionnaire de dénominations communes pour les médicaments et les structures chimiques.
Appendice 5. Maquillage des dénominations de substances
Les procédures présentées ci-après visent à aider les déclarants à déposer une Déclaration de substances nouvelles (DSN) qui leur permettra de garder confidentielle l’identité d’une substance. Le déclarant devrait également soumettre une dénomination maquillée pour l’inscription confidentielle d’une substance sur la Liste intérieure et la Liste extérieure. L’objectif du maquillage est de maquiller, dans la mesure uniquement où cela est nécessaire, la dénomination chimique d’une substance. Bien que le présent appendice n’illustre le maquillage que d’un seul élément distinctif, le maquillage d’éléments supplémentaires est autorisé si le déclarant peut le justifier (consulter la partie A5.4).
Il existe des différences inhérentes entre la dénomination chimique des substances possédant une structure chimique et une formule moléculaire définies et celle de substances qui ne peuvent être représentées par une structure chimique définie et qui peuvent avoir ou ne pas avoir de formule moléculaire définie. Ces deux cas sont examinés séparément plus bas.
Une dénomination maquillée acceptable dissimule la dénomination chimique explicite de la substance. Ainsi, il n’est pas autorisé de remplacer un composant de la dénomination chimique par un synonyme pour ensuite le maquiller.
A5.1 Substances possédant une structure chimique et une formule moléculaire définies
Les substances qui ont une structure chimique et une formule moléculaire définies peuvent être représentées par une structure chimique et une formule moléculaire uniques. La dénomination chimique de la substance fournit habituellement les renseignements suivants sur la structure :
- L’identité de la structure parentale (par exemple chaîne d’atomes de carbone, système cyclique ou métal coordonné);
- L’identité, le nombre et la position du ou des groupes chimiques liés à la structure parentale ou à d’autres groupes chimiques;
- L’identité des cations et des contre-ions (pour les sels) et leur nombre;
- Les relations stéréochimiques.
Une dénomination peut être maquillée en masquant certains segments descriptifs de la structure dans la dénomination chimique de la substance. Pour ce faire, des éléments distincts de la dénomination chimique peuvent être remplacés par des termes non descriptifs ou éliminer des indicateurs de position. Le nombre d’éléments distinctifs qui peuvent être remplacés ou éliminés dans la dénomination chimique doit se limiter au nombre minimum nécessaire pour assurer la confidentialité (excluant la suppression d’un indicateur stéréochimique d’une dénomination chimique).
Les éléments distinctifs uniques d’une dénomination chimique qui peuvent être masqués pour créer une proposition de dénomination maquillée sont les suivants :
- Un indicateur de position qui précise la position d’un groupe chimique;
- L’indicateur de position et les préfixes multiplicatifs (par exemple di-, tri-, tétra-) qui, ensemble, donnent le nombre et la position d’un groupe chimique donné;
- L’identité d’un groupe chimique donné;
- L’identité d’une structure parentale donnée et les indicateurs de position des groupes chimiques qui y sont fixés;
- L’identité et les préfixes multiplicatifs (précisant le nombre) d’un cation ou d’un anion simple d’un sel.
Le tableau A5-1 décrit, par nom et formule moléculaire, les types de groupes chimiques qui peuvent être maquillés. Les groupes d’atomes indiqués dans ce tableau sont des unités structurales courantes; un groupe donné peut figurer sous plus d’une dénomination. Chaque groupe comprend au moins un atome autre qu’un atome de carbone ou d’hydrogène.
Si le groupe chimique comporte un atome de carbone ayant plus d’une valence libre (par exemple le carbonyle -CO-), son nom ne peut être maquillé si l’atome de carbone est directement lié à un atome de carbone acyclique ou fait partie d’un cycle. Dans un tel cas, seul l’atome ou le groupe d’atomes qui est lié à l’atome de carbone possédant la valence peut être maquillé.
Certains groupes chimiques au tableau A5-1 renferment des atomes d’hydrogène qui sont souvent remplacés par un autre groupe, par exemple le groupe éthyle peut remplacer un atome d’hydrogène dans le groupe sulfamyle (H2NSO2-) pour donner C2H5NHSO2-. S’il y a d’autres substitutions, seul le groupe chimique figurant au tableau A5-1 devrait être maquillé; il ne faut pas maquiller le substituant.
Le tableau A5-1 présente la plupart des groupes fonctionnels courants qui renferment de l’oxygène, par exemple H2NCO-. Bien qu’ils ne figurent pas toujours dans la liste, les analogues soufrés, sélénilés et tellurés (éléments du groupe VIa) de ces groupes fonctionnels (par exemple H2NCSe-) sont considérés comme faisant partie du tableau A5-1 et peuvent donc être utilisés pour créer une dénomination maquillée.
| Article | Groupe chimique | Formule |
|---|---|---|
| 1 | aldo | H(C=O)- |
| 2 | amidino | NH2(C=NH)CH2- |
| 3 | amino | H2N- |
| 4 | (aminoamidino) | H2NC(=NNH2)- or H2NNHC(=NH)- |
| 5 | (aminocarbonyl) | H2NCO- |
| 6 | [(aminocarbonyl)amino] | H2NCONH- |
| 7 | [2-(aminocarbonyl)hydrazino] | H2NCONHNH- |
| 8 | [(aminocarbonyl)hydrazono] | H2NCONHN= |
| 9 | (aminohydrazonométhyle) | H2NC(=NNH2)- |
| 10 | [(aminohydroxyméthyléne)hydrazino] | H2NC(OH)=NNH- |
| 11 | (aminoiminométhyle) | H2NC(=NH)- |
| 12 | (aminoiminophosphoranyle) | H2NPH(=NH)- |
| 13 | (p-aminophosphinimyle) | H2NPH(=NH)- |
| 14 | (aminosulfinyle) | H2NSO- |
| 15 | (aminosulfonyle) | H2NSO2- |
| 16 | (aminothio) | H2NS- |
| 17 | (aminothioxométhyle) | H2NCS- |
| 18 | ammonio | H3N- |
| 19 | antimono | -Sb=Sb- |
| 20 | arséno | -As=As- |
| 21 | arsénoso | OAs- |
| 22 | arsinico | HOAs(O)≡ |
| 23 | arsinidène | HAs= |
| 24 | arsinidyne | As≡ |
| 25 | arsinimyle | AsH2(=NH)- |
| 26 | arsino | AsH2- |
| 27 | arsinothioyle | AsH2(S)- |
| 28 | arsinyle | AsH2(O)- |
| 29 | arsinylidène | AsH(O)≡ |
| 30 | arso | O2As- |
| 31 | arsono | (HO)2As(O)- |
| 32 | (arsonoxy) | (HO)2As(O)O- |
| 33 | arsononitridyle | AsH(=N)- |
| 34 | arsoranyle | AsH4- |
| 35 | arsoranylidyne | AsH2≡ |
| 36 | arsylène | AsH= |
| 37 | arsylidyne | As≡ |
| 38 | astato | At- |
| 39 | astatoxy | O2At- |
| 40 | astatyl | O2At- |
| 41 | azi | -N=N- |
| 42 | azido | N3- |
| 43 | (azidocarbonyle) | N3CO- |
| 44 | (azidofurmyle) | N3CO- |
| 45 | (azidosulfonyle) | N3SO2- |
| 46 | azino | =NN= |
| 47 | azo | -N=N- |
| 48 | azoxy | -N(O)=N- |
| 49 | bismuthino | BiH2- |
| 50 | bismuthylène | BiH= |
| 51 | bismuthylidyne | Bi≡ |
| 52 | borono | (HO)2B- |
| 53 | (boronooxy) | (HO)2BO- |
| 54 | boryle | BH2- |
| 55 | borylène | BH= |
| 56 | borylidyne | B≡ |
| 57 | bromo | Br- |
| 58 | (bromocarbonyle) | BrCO- |
| 59 | (bromoiminométhyle) | BrC(=NH)- |
| 60 | (bromosulfonyle) | BrSO2- |
| 61 | carbamido | H2NCONH- |
| 62 | carbamoyle | H2NCO- |
| 63 | carbamyle | H2NCO- |
| 64 | carbonimidoyle | -C(=NH)= |
| 65 | (carbonimidoylamino) | H2N=C=N- |
| 66 | carbonothioyle | -CS- |
| 67 | carbonyle | -CO- |
| 68 | (carbonylidiimino) | -NHCONH- |
| 69 | (carbonyldioxy) | -OC(O)O- |
| 70 | carboxy | HO2C- |
| 71 | chloro | Cl- |
| 72 | (chlorocarbonyle) | ClCO- |
| 73 | (chloroformyle) | ClCO- |
| 74 | (chloroiminométhyle) | ClC(=NH)- |
| 75 | (chlorosulfinyle) | ClSO- |
| 76 | (chlorosulfonyle) | ClSO2- |
| 77 | chlorosyle | OCl- |
| 78 | (chlorothio) | ClS- |
| 79 | chloryle | O2Cl- |
| 80 | cyanato | NCO- |
| 81 | cyano | NC- |
| 82 | diarsène-1,2-diyle | -As=As |
| 83 | diarsényle | HAs=As- |
| 84 | diarsinetétrayle | =AsAs= |
| 85 | diarsinyle | H2AsAsH- |
| 86 | diazène-1,2-diyle | -N=N |
| 87 | diazéno | HN=N- |
| 88 | diazo | N2= |
| 89 | diazoamino | -NHN=N- |
| 90 | diazonio | N2+- |
| 91 | 1,2-diborane(4)diylidène | =BB= |
| 92 | diborane(4)tétrayle | =BB= |
| 93 | digermanylène | -GeH2GeH2- |
| 94 | digermathianyle | H3GeSGeH2- |
| 95 | dioxy | -OO- |
| 96 | diphosphène-1,2-diyle | -P=P |
| 97 | diphosphine-1,2-diyle | -PHPH- |
| 98 | diphosphine-1,2-diylidène | =PP= |
| 99 | diphosphinetétrayle | =PP= |
| 100 | diphosphinyle | H2PPH- |
| 101 | diséléno | -SeSe- |
| 102 | disilane-1,2-diyle | -SiH2OSiH2- |
| 103 | disilanoxy | H3SiSiH2O- |
| 104 | disilanyle | H3SiSiH2- |
| 105 | disilanylène | -SiH2SiH2- |
| 106 | (disilanyloxy) | H3SiSiH2O- |
| 107 | (disilathianyloxy) | H3SiSSiH2O- |
| 108 | disilazanoxy | H3SiNHSiH2O- |
| 109 | disilazanyle | H3SiNHSiH2- |
| 110 | 2-Disilazanyle | (H3Si)2N- |
| 111 | (disilazanyloxy) | H3SiNHSiH2O- |
| 112 | disiloxane-1,3-diyle | -SiH2OSiH2- |
| 113 | disiloxane-1,3-diylidène | =SiHOSiH= |
| 114 | disilanoxy | H3SiOSiH2O- |
| 115 | disiloxanylène | -SiH2OSiH2- |
| 116 | (disilanyloxy) | H3SiOSiH2O- |
| 117 | disilthianoxy | H3SiSSiH2O- |
| 118 | distannane-1,2-diyle | SnH2SnH2- |
| 119 | distannanylène | -SnH2SnH2- |
| 120 | distannathiane-1,3-diylidène | =SnHSSnH= |
| 121 | distibène-1,2-diyle | -Sb=Sb- |
| 122 | disulfinyle | -S(O)S(O)- |
| 123 | dithio | -SS- |
| 124 | dithiocarboxy | HSSC- |
| 125 | (dithiohydroperoxy) | HSS- |
| 126 | épidioxy | -OO- |
| 127 | épidiséléno | -SeSe- |
| 128 | épidithio | -SS- |
| 129 | épioxy | -O- |
| 130 | épiséléno | -Se- |
| 131 | épithio | -S- |
| 132 | époxy | -O- |
| 133 | fluoro | F- |
| 134 | (fluorocarbonyle) | FCO- |
| 135 | fluoryle | O2F- |
| 136 | formamido | HCONH- |
| 137 | 1,5-formazanidyle | -N=NCH=NNH- |
| 138 | 1-formazano | H2NN=CHN=N- |
| 139 | 5-formazano | HN=NCH=NNH- |
| 140 | formazanyle | HN=NC(=NNH2)- |
| 141 | formimidoyle | HC(=NH)- |
| 142 | formyle | HCO- |
| 143 | (formylamino) | HCONH- |
| 144 | germanetétrayle | =Ge= |
| 145 | germyle | H3Ge- |
| 146 | germylène | H2Ge= |
| 147 | germylidyne | HGe≡ |
| 148 | guanyle | H2NC(=NH)- |
| 149 | hydrazi | -NHNH- |
| 150 | hydrazine-1,2-diylidène | =NN= |
| 151 | hydrazino | H2NNH- |
| 152 | (hydrazinocarbonyle) | H2NNHCO- |
| 153 | (hydrazinoiminométhyle) | H2NNHC(=NH)- |
| 154 | (hydrazinosulfinyle) | H2NNHSO- |
| 155 | (hydrazinosulfonyle) | H2NNHSO2- |
| 156 | (hydrazinothioxométhyle) | H2NNHCS- |
| 157 | 1-hydrazinyl-2-ylidène | -NHN= |
| 158 | hydrazo | -NHNH- |
| 159 | hydrazono | H2NN= |
| 160 | hydroperoxy | HOO- |
| 161 | (hydroperoxycarbonyle) | HOOCO- |
| 162 | (hydroperoxyiminométhyle) | HOOC(=NH)- |
| 163 | (hydroperoxysulfinyle) | HOOS(=O)- |
| 164 | (hydroperoxysulfonyle) | HOOS(=O)2- |
| 165 | (hydroperoxythioxométhyle) | HOOCS- |
| 166 | hydroxy | HO- |
| 167 | (hydroxyamino) | HONH- |
| 168 | (hydroxyimino) | HON= |
| 169 | (hydroxyiminométhyle) | HOC(=NH)- |
| 170 | hydroxyle | HO- |
| 171 | (hydroxyphosphinyle) | HOPH(O)- |
| 172 | imidocarbonyle | -C(=NH)- |
| 173 | (imidocarbonylamino) | HN=C=N- |
| 174 | imino | HN= |
| 175 | (iminomercaptométhyle) | HSC(=NH)- |
| 176 | [imino(mercaptooxy)méthyle] | HSOC(=NH)- |
| 177 | (iminométhyle) | HN=CH- |
| 178 | (iminonitrilo) | -NHN= |
| 179 | (iminophosphoranyle) | H2P(=NH)- |
| 180 | (iminosulfénométhyle) | HOSC(=NH)- |
| 181 | iodo | I- |
| 182 | (iodocarbonyle) | ICO- |
| 183 | iodosyle | OI- |
| 184 | iodyle | O2I- |
| 185 | isocyanato | OCN- |
| 186 | (isocyanatocarbonyle) | OCNCO- |
| 187 | (isocyanatosulfonyle) | OCNSO2- |
| 188 | isocyano | CN- |
| 189 | (isocyanocarbonyle) | CNCO- |
| 190 | isonitro | HON(O)= |
| 191 | isonitroso | HON= |
| 192 | isosemicarbazido | H2NC(OH)=NNH- |
| 193 | isothiocyanato | SCN- |
| 194 | (isothiocyanatocarbonyle) | SCNCO- |
| 195 | (isothiocyanatosulfonyle) | SCNSO2- |
| 196 | isothiocyano | SCN- |
| 197 | keto | O= |
| 198 | mercapto | HS- |
| 199 | (mercaptoamino) | HSNH- |
| 200 | (mercaptooxy) | HSO- |
| 201 | [(mercaptooxy)carbonyle] | HSOCO- |
| 202 | [(mercaptooxy)sulfinyle] | HSOS(=O)- |
| 203 | [(mercaptooxy)sulfonyle] | HSOS(=O)2- |
| 204 | (mercaptooxy)thioxométhyle | HSOCS- |
| 205 | (mercaptotelluro) | HSTe- |
| 206 | nitramino | O2NNH- |
| 207 | aci-nitramino | HON(O)=N- |
| 208 | nitrilio | HN+≡ |
| 209 | nitrilo | N≡ |
| 210 | (nitrilophosphoranyle) | HP(=N)- |
| 211 | nitro | O2N- |
| 212 | acinitro | HON(O)= |
| 213 | (nitroamino) | O2NNH- |
| 214 | (aci-nitroamino) | HON(O)=N- |
| 215 | (nitrooxy) | O2NO- |
| 216 | nitroso | ON- |
| 217 | (nitrosoamino) | ONNH- |
| 218 | (nitrosoimino) | ONN= |
| 219 | (nitrosooxy) | ONO- |
| 220 | (nitrothio) | O2NS- |
| 221 | oximido | HON= |
| 222 | oxo | O= |
| 223 | (oxoboryle) | OB- |
| 224 | oxy | -O- |
| 225 | pentaza-1,3-diényle | H2NN=NN=N- |
| 226 | perchloryle | O3Cl- |
| 227 | perséléno | Se=Se= |
| 228 | perthio | S=S= |
| 229 | phosphinico | HOP(O)= |
| 230 | phosphinidène | HP= |
| 231 | phosphinidyne | P≡ |
| 232 | phosphinimyle | H2P(=NH)- |
| 233 | phosphino | H2P- |
| 234 | phosphinothioyle | H2P(S)- |
| 235 | phosphinothioylidène | HP(S)= |
| 236 | phosphinyle | H2P(O)- |
| 237 | phosphinylidène | HP(O)= |
| 238 | phosphinylidyne | P(O)= |
| 239 | phospho | O2P- |
| 240 | phosphono | (HO)2P(O)- |
| 241 | (phosphonocarbonyle) | (HO)2P(CO)- |
| 242 | phosphononitridyle | HP(=N)- |
| 243 | (phosphonooxy) | (HO)2P(O)O- |
| 244 | phosphoranyle | H4P- |
| 245 | phosphoranylidène | H3P= |
| 246 | phosphoranylidyne | H2P≡ |
| 247 | phosphoro | -P=P- |
| 248 | phosphoroso | OP- |
| 249 | plumbanetétrayle | =Pb= |
| 250 | plumbyle | H3Pb- |
| 251 | plumbylène | H2Pb= |
| 252 | plumbylidyne | HPb= |
| 253 | séléneno | HOSe- |
| 254 | sélénino | HOSe(O)- |
| 255 | séléninosélénoyle | Se=Se= |
| 256 | séléninyle | OSe= |
| 257 | séléno | -Se- |
| 258 | sélénocyanato | NCSe- |
| 259 | sélénono | (HO)SeO2- |
| 260 | sélénonyle | O2Se= |
| 261 | sélénoxo | Se= |
| 262 | sélényle | HSe- |
| 263 | semicarbazido | H2NCONHNH- |
| 264 | semicarbazono | H2NCONHN= |
| 265 | silanetétrayle | =Si= |
| 266 | silyle | H3Si- |
| 267 | silylène | H2Si= |
| 268 | silylidyne | HSi≡ |
| 269 | (silyloxy) | H3SiO- |
| 270 | stannanetétrayle | =Sn= |
| 271 | stannono | HOSn(O)- |
| 272 | stannyle | H3Sn- |
| 273 | stannylène | H2Sn= |
| 274 | stannylidyne | HSn≡ |
| 275 | stibinico | HOSb(O)= |
| 276 | stibino | H2Sb- |
| 277 | stibo | O2Sb- |
| 278 | stibono | (HO)2Sb(O)- |
| 279 | (stibonooxy) | (HO)2Sb(O)O- |
| 280 | stiboso | OSb- |
| 281 | stibyle | H2Sb- |
| 282 | stibylène | HSb= |
| 283 | stibylidyne | Sb≡ |
| 284 | sulfamino | HOSO2NH- |
| 285 | sulfamoyle | H2NSO2- |
| 286 | sulfamyle | H2NSO2- |
| 287 | sulféno | HOS- |
| 288 | (sulfénocarbonyle) | HOSCO- |
| 289 | sulfénosulfinyle | HOSS(=O)- |
| 290 | (sulfénosulfonyle) | HOSS(=O)2- |
| 291 | (sulfénothioxométhyle) | HOSCS- |
| 292 | sulfhydryle | HS- |
| 293 | sulfinimidoyle | HN=S= |
| 294 | sulfino | HOS(O)- |
| 295 | (sulfinooxy) | HOS(O)O- |
| 296 | sulfinothioyle | S=S= |
| 297 | sulfinyle | OS= |
| 298 | sulfo | HO3S- |
| 299 | (sulfoamino) | HOSO2NH- |
| 300 | sulfonimidoyle | HN=S(O)= |
| 301 | sulfonodiimidoyle | (HN=)2S= |
| 302 | sulfonyle | -SO2- |
| 303 | (sulfooxy) | HO3SO- |
| 304 | sulfuryle | -SO2- |
| 305 | telluro | -Te- |
| 306 | telluroxo | Te= |
| 307 | telluryle | HTe- |
| 308 | tétraphosphine-1,4-diyle | -(PH)4- |
| 309 | tétrasiloxane-1,7-diyle | -SiH2(OSiH2)2OSiH2- |
| 310 | tétrathio | -SSSS- |
| 311 | tétrazane-1,4-diyle | -(NH)4- |
| 312 | tétrazane-1,4-diylidène | =N(NH)2N= |
| 313 | tétrazén-1-yle | H2NNHN=N- |
| 314 | thio | -S- |
| 315 | (thioarsénoso) | S=As- |
| 316 | (thiocarbamoyle) | H2NCS- |
| 317 | thiocarbamyle | H2NCS- |
| 318 | (thiocarbonyle) | -CS- |
| 319 | (thiocarboxy) | HOSC- |
| 320 | thiocyanato | NCS- |
| 321 | thiocyano | NCS- |
| 322 | (thioformyle) | HCS- |
| 323 | thiohydroperoxy | HOS- ou HSO- |
| 324 | (thiohydroxy) | HS- |
| 325 | (thionitroso) | SN- |
| 326 | thionyle | -SO- |
| 327 | (thioséléneno) | HSSe- |
| 328 | (thiosulféno) | HSS- |
| 329 | (thiosulfo) | (HO2S2)- |
| 330 | thioxo | S= |
| 331 | (thioxoarsino) | S=As- |
| 332 | (thioxométhyle) | HCS- |
| 333 | thiurame | H2NCS- |
| 334 | triazanyle | H2NNHNH- |
| 335 | 1-triazène-1,3-diyle | -NHN=N- |
| 336 | 1-triazényle | H2NN=N- |
| 337 | triséléno | -SeSeSe- |
| 338 | trisilane-1,3-diyle | -(SiH2)3- |
| 339 | trisiloxane-1,3,5-triyle | -SiH(OSiH2-)2 |
| 340 | trithio | -SSS- |
| 341 | uramino | H2NCONH- |
| 342 | uréido | H2NCONH- |
| 343 | uréylène | -NHCONH- |
A5.1.1 Maquillage de la structure parentale
La dénomination chimique de la structure parentale d’une substance qui peut être décrite par une structure chimique et une formule moléculaire définies ne peut être maquillée qu’en utilisant les termes non descriptifs suivants :
- Alkyle ou alcane;
- Alcényle ou alcène;
- Alcynyle ou alcyne;
- Carbomonocyclique ou carbomonocycle (par exemple benzène, cyclopentane);
- Carbopolycyclique ou carbopolycycle (par exemple naphtalène, spiro-undécane);
- Hétéromonocyclique ou hétéromonocycle (par exemple pyrrole, p-dioxane);
- Hétéropolycyclique ou hétéropolycycle (par exemple indole, benzothiazole).
Dans le cas d’un composé métallique coordonné, l’identité de l’atome de métal peut être maquillée en utilisant le terme « métal » dans la dénomination chimique.
Seulement une structures parentale ou des multiples de la même structure parentale devrait être maquillé.
Les exemples suivants montrent comment maquiller des dénominations chimiques courantes en ne masquant qu’un seul élément distinctif.
Exemple 1
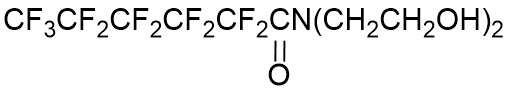
Dénomination complètement définie :
- 2,2,3,3,4,4,5,5,6,6,6-Undécafluoro-N,N-bis(2-hydroxyéthyl) hexanamide
Dénominations maquillées acceptables :
- Atomes de fluor maquillés :
- 2,2,3,3,4,4,5,5,6,6,6-Undécahalo-N,N-bis(2-hydroxyéthyl)hexanamide.
- Indicateurs de position et préfixe multiplicatif d’atomes de fluor maquillés :
- Polyfluoro-N,N-bis(2-hydroxyéthyl)hexanamide.
- Groupes hydroxyles maquillés :
- 2,2,3,3,4,4,5,5,6,6,6-Undécafluoro-N,N-bis(2-éthyle substitué)hexanamide.
- Hexane (plus indicateurs de position des groupes chimiques) maquillé :
- Undécafluoro-N,N-bis(2-hydroxyéthyl)alcanamide.
- Groupe amide (plus indicateurs de position de l’azote) maquillé :
- Dérivé de 2,2,3,3,4,4,5,5,6,6,6-undécafluorobis(2-hydroxyéthyl)hexane.
Exemple 2
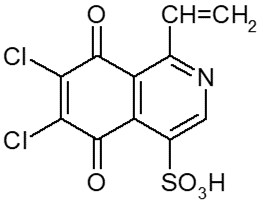
Dénomination complètement définie :
- Acide 6,7-dichloroéthén-1-yl-5,8-dihydro-5,8-dioxo-4-isoquinoléinesulfonique.
Dénominations maquillées acceptables :
- Atomes de chlore maquillés :
- Acide éthén-1-yl-6,7-dihalo-5,8-dihydro-5,8-dioxo-4-isoquinoléinesulfonique.
- Groupe vinyle maquillé :
- Acide alcén-1-yl-6,7-dichloro-5,8-dihydro-5,8-dioxo-4-isoquinoléinesulfonique.
- Groupe oxo maquillé :
- Acide 6,7-dichloroéthén-1-yl-5,8-dihydro-5,8-disubstitué-4-isoquinoléinesulfonique.
- Groupe sulfo maquillé :
- Acide 6,7-dichloroéthén-1-yl-5,8-dihydro-5,8-dioxo-4-isoquinoléine substitué.
- Cycle isoquinoléine (plus indices de position des groupes chimiques fixés à l’isoquinoléine) maquillé :
- Acide dichloroéthényldihydrodioxo hétéropolycyclique sulfonique; ou
- Dichloroéthényldihydrodioxosulfo hétéropolycycle.
A5.2 Substances ne possédant pas une structure chimique ou une formule moléculaire définies
Certaines substances, comme les polymères, ne peuvent être représentées par des schémas de structure définis et peuvent avoir ou ne pas avoir de formules moléculaires définies. Dans d’autres cas, la composition ne peut être décrite qu’au moyen d’une combinaison complexe de plusieurs composants différents, connus ou inconnus, comme les substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques (substances of Unknown or Variable composition, Complex reaction products or Biological materials – UVCB).
La méthode de fabrication peut aussi servir à identifier une substance. Pour une substance obtenue par une réaction chimique, l’identification peut être faite en tenant compte des précurseurs immédiats et d’autres réactifs qui interviennent dans la réaction finale de synthèse ainsi que de la nature de la réaction (par exemple éthoxylation ou bromation). Pour une substance dont la fabrication ne comporte pas de réaction chimique, les renseignements sur le traitement permettent de désigner la source et le procédé de production (par exemple distillation ou extraction avec du chlorure de méthylène).
Bien que la dénomination chimique des substances sans structure chimique définie ou sans schéma de structure unique puisse être basée sur divers types de termes descriptifs, des procédures de maquillage semblables à celles utilisées pour les substances ayant une structure chimique et une formule moléculaire définies peuvent être employées (consulter la partie A5.1).
La composition d’une substance pouvant être représentée par un schéma structurel partiel ou incomplet peut généralement être décrite par une dénomination chimique commune qui tient compte de la variabilité de la structure ou de son caractère incomplet. Une dénomination maquillée pour une telle substance sera habituellement acceptable si les directives relatives au maquillage partiel de la structure chimique des substances possédant une structure chimique et une formule moléculaire définies ont été respectées.
Dans d’autres cas, la dénomination chimique peut indiquer un ou plusieurs composants prédominants de sa composition, un ou plusieurs précurseurs immédiats ou d’autres réactifs par leur dénomination chimique. Une dénomination maquillée proposée sera habituellement acceptable pour une telle substance si elle est établie en maquillant la dénomination chimique de l’un de ces composants, précurseurs ou réactifs.
Il est clair que les méthodes de maquillage de cet appendice sont surtout utiles pour maquiller l’identité de substances ayant un seul élément distinctif et qu’elles ne seront utiles que pour certains types de substances qui ne peuvent pas être décrites par une structure chimique unique. Dans certains de ces derniers cas, il se peut que l’application des présentes méthodes de maquillage soit limitée. Pour des raisons d’uniformité, les déclarants doivent choisir la dénomination maquillée en se basant sur la dénomination chimique de la substance établie conformément aux règles de nomenclature actuelles de l’Union internationale de chimie pure et appliquée (UICPA) ou du Chemical Abstracts Service (CAS) et telle qu’elle figure sur le formulaire de déclaration (formulaire de DSN, formulaire de proposition d’inscription sur la Liste intérieure, formulaire de proposition d’inscription sur la Liste extérieure, etc.). Le Programme des substances nouvelles (SN) étudiera chaque dénomination maquillée proposée au cas par cas.
Changement de l’ordre des éléments d’une dénomination chimique d’un polymère
Même s’il est généralement acceptable de changer l’ordre des monomères et des réactifs dans la dénomination chimique d’un polymère avant de les maquiller, le premier élément du nom ne peut être déplacé. De plus, il faut présenter une déclaration écrite justifiant la nécessité de déplacer le nom des monomères et des réactifs ainsi qu’une liste indiquant la position de chacun des monomères et des réactifs qui ont été déplacés avec les noms et schémas structurels connexes.
Maquillage d’un prépolymère
Un prépolymère qui est conservé dans la dénomination chimique est considéré comme un seul réactif aux fins de la dénomination et ne peut être divisé en ses éléments. Par conséquent, si le nom d’un prépolymère est conservé dans la dénomination chimique d’un polymère, le nom chimique du prépolymère doit également être conservé dans la dénomination maquillée. Toutefois, il est toujours possible de maquiller les éléments structurels de la dénomination d’un prépolymère conformément aux dispositions du Règlement sur les dénominations maquillées de la même façon que l’ensemble des éléments structuraux du nom du polymère.
Exemple 3
Description de la substance :
- Polymère d’acides gras d’huile de lin, de l’acide fumarique, du glycérol et de l’anhydride maléique.
Dénomination chimique spécifique :
- Acides gras, huile de lin polymérisée avec l’acide fumarique, le glycérol et l’anhydride maléique.
Dénominations maquillées acceptables :
- Maquillage de l’huile de lin :
- Acides gras, huile végétale, polymères avec l’acide fumarique, le glycérol et l’anhydride maléique.
- Maquillage de l’acide fumarique :
- Acides gras, huile de lin, polymères avec un acide alcènedioïque, le glycérol et l’anhydride maléique.
Exemple 4
Description de la substance :
- Polyéthylèneglycol, éthers monoalkyliques en C12-15, phosphates, sels de potassium.
Dénomination chimique spécifique :
- Éthers monoalkyliques en C12-15 de l’α-hydro-ω-hydroxypoly (oxyéthane-1,2-diyle), phosphates, sels de potassium.
Noms maquillés acceptables :
- Maquillage des sels potassiques :
- Éthers monoalkyliques en C12-15 de l’α-hydro-ω-hydroxypoly (oxyéthane-1,2-diyl), phosphates, sels métalliques.
- Groupe alkylique en C12-15 maquillé :
- Éthers monoalkyliques de l’α-hydro-ω-hydroxypoly (oxyéthane-1,2-diyle), phosphates, sels de potassium.
- Éthane maquillé :
- Éthers monoalkyliques en C12-15 de l’α-hydro-ω-hydroxypoly (oxyalkylènediyle), phosphates, sels de potassium.
A5.3 Maquillage de l’identité de substances biochimiques et de biopolymères
Les substances biochimiques et les biopolymères qui n’ont pas d’activité catalytique peuvent être maquillés en déguisant les segments descriptifs de leur dénomination chimique. Le maquillage de plus d’un segment de la dénomination chimique est considéré comme du maquillage supplémentaire, ce qui n’est pas autorisé sans justification. Un maquillage peut être effectué en substituant des éléments distinctifs uniques de la dénomination chimique ou biologique par des termes non descriptifs ou en supprimant les indicateurs de position (consulter les parties A5.1 et A5.2).
A5.3.1 Substances enzymatiques
Les dénominations maquillées pour les enzymes devraient être créées en masquant la description correspondant au quatrième niveau du numéro de classification des enzymes et en utilisant la description correspondante du niveau de la classification des enzymes choisi comme terme distinctif. La suppression de chaque élément du numéro de classification des enzymes (a.b.c.d.) constitue un maquillage unique. Par exemple, le retrait de « d » est un maquillage unique; le retrait de « c,d » est un double maquillage et le retrait de « b,c,d » est un triple maquillage. Veuillez noter que le premier élément « a » ne peut être maquillé. Dans les cas où le numéro de classification des enzymes de quatrième niveau ne comporte qu’une seule entrée, le Programme des substances nouvelles accepte un numéro de classification des enzymes de deuxième niveau comme maquillage simple.
Exemple 5
Description de la substance :
- 6-Hydroxynicotinate réductase (numéro de classification des enzymes 1.3.7.1).
Maquillage double proposé :
- Réductase avec hétéromonocycle substitué (numéro de classification des enzymes 1.3).
Exemple 6
Description de la substance :
Le numéro d’enregistrement CAS 9042-64-2 :
- Décarboxylase des acides L-aminés aromatiques.
- Numéro de classification des enzymes associé : 4.1.1.28.
Maquillage simple proposé :
- Décarboxylyase.
- Numéro de classification des enzymes associé : 4.1.1.
Exemple 7
Description de la substance :
numéro d’enregistrement CAS 341585-05-5 :
- Xylose-isomérase (numéro de classification des enzymes 5.3.1.5) [Lactococcus lactis lactis, souche IL1403, gène xylA] (9CI).
Maquillage simple proposé :
- Xylose-isomérase (numéro de classification des enzymes 5.3.1.5) [Lactococcus lactis lactis, gène xylA].
Maquillage double proposé :
- Xylose-isomérase (numéro de classification des enzymes 5.3.1.5) [Lactococcus lactis lactis].
Maquillage triple proposé :
- Oxydoréductase intramoléculaire (numéro de classification des enzymes 5.3) [Lactococcus lactis lactis, souche IL1403].
A5.4 Justification d’un maquillage supplémentaire
Si l’application stricte des procédures de maquillage (par exemple, le maquillage d’un unique élément distinctif) ne permet pas de maquiller adéquatement l’identité d’une substance, le déclarant peut proposer une dénomination plus maquillée. Cette dénomination maquillée proposée doit être générée conformément aux procédures décrites dans le Règlement sur les dénominations maquillées et chaque maquillage supplémentaire doit être accompagné d’une justification distincte qui appui la nécessité de maquiller davantage la dénomination explicite de la substance.
Afin d’orienter les déclarants davantage sur comment utiliser le maquillage supplémentaire :
- En règle générale, les déclarants peuvent proposer le maquillage d’un maximum de 5 termes descriptifs;
- Le maquillage du premier élément distinctif n’a pas besoin de justification supplémentaire en outre des justifications déjà fournies de la partie 6.2.1.5 et de la partie 7.2.2-3 du Document d’orientation;
- Une justification supplémentaire est exigée pour chaque maquillage supplémentaire, les déclarants doivent expliquer clairement les raisons justifiant chaque maquillage supplémentaire en utilisant une approche séquentielle.
Par exemple, le maquillage d’un deuxième élément est justifié si le maquillage d’un seul élément révèle des renseignements sur la structure chimique qui pourraient avoir une incidence négative sur la propriété intellectuelle ou sur la valeur marchande de la substance.
Appendice 6. Exemples de demandes de dérogation
Le déclarant peut être exempté de l’obligation de fournir des données d’essais sur une substance chimique ou un polymère si, selon le ministre de l’Environnement (le ministre), l’un des 3 critères en vertu desquels des dérogations peuvent être accordées s’applique au renseignement visé (consulter la partie 8.7).
Les conditions permettant d’accepter une demande de dérogation sont examinées au cas par cas. Chaque demande de dérogation doit être accompagnée d’une justification scientifique bien documentée ainsi qu’une identification du critère légal selon lequel la demande est présentée. Le défaut de fournir une justification adéquate et la documentation à l’appui entraînera le rejet de la demande.
Des exemples de situations où une dérogation peut être accordée par le ministre sont présentés plus bas. Sauf indication contraire, les exemples sont conformes à l’alinéa 81(8)c) de la Loi canadienne sur la protection de l’environnement (1999) [la Loi].
A6.1 Substances chimiques
Les exemples qui suivent décrivent des situations dans lesquelles le ministre peut accorder une dérogation et ils peuvent s’appliquer à n’importe quel essai :
- La substance est créée in situ lors du procédé de fabrication et elle se décompose lors des tentatives d’isolement;
- La substance coexiste avec un ou plusieurs autres composants qui ne peuvent être isolés et qui altèrent les résultats de l’essai;
- La substance réagit de manière dangereuse au cours de l’essai.
A6.1.1 Paramètres physico-chimiques
A6.1.1.1 Point de fusion et point d’ébullition
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- La substance est un sel qui n’est stable qu’en solution aqueuse.
Aucune dérogation n’est nécessaire lorsque :
- le point de fusion de la substance est inférieur à -25 °C ou supérieur à 300 °C; une déclaration à cet effet avec les renseignements à l’appui suffit pour satisfaire à cette exigence;
- le point d’ébullition de la substance est inférieur à -50 °C ou supérieur à 300 °C; une déclaration à cet effet avec les renseignements à l’appui suffit pour satisfaire à cette exigence;
- la substance subit une réaction chimique autre que la fusion ou l’ébullition (par exemple dégradation, réarrangement). La déclaration doit toutefois préciser la température de la réaction chimique.
Des données de substitution comme le point de décomposition, le point d’écoulement, le point de ramollissement ou le point de sublimation peuvent être fournies, pourvu que ces données soient applicables et disponibles. Dans le cas des substances biochimiques et des biopolymères, le point isoélectrique peut être substitué au point de fusion. Le cas échéant, une demande de dérogation n’est pas nécessaire.
A6.1.1.2 Densité
Aucune dérogation n’est nécessaire lorsque :
- la substance n’est stable qu’en solution dans un solvant particulier et la densité de la solution est semblable à celle du solvant. Le cas échéant, il suffit d’indiquer si la densité de la solution est supérieure ou inférieure à celle du solvant.
Une demande de dérogation type peut être formulée comme suit, accompagnée d’une justification scientifique valable :
- Une demande de dérogation est présentée en vertu de l’alinéa 81(8)c) de la Loi relativement à la détermination de la densité, au motif que la substance à déclarer ne peut être isolée et qu’il est techniquement impossible d’en déterminer la densité.
A6.1.1.3 Pression de vapeur
Les exemples qui suivent illustrent des situations dans lesquelles le ministre peut accorder une dérogation :
- La substance a une forte masse moléculaire (supérieure à 1 000 daltons);
- La substance est un solide ionique;
- La substance est un solide dont le point de fusion est élevé (supérieur à 300 °C).
Une demande de dérogation type peut être formulée comme suit, accompagnée d’une justification scientifique valable :
- Une demande de dérogation est présentée en vertu de l’alinéa 81(8)a) de la Loi relativement à la détermination de la pression de vapeur au motif que la substance est un solide ionique et que sa pression de vapeur est de ce fait négligeable.
Aucune dérogation n’est nécessaire lorsque :
- le point d’ébullition normal de la substance est inférieur à 0 °C; une déclaration à cet effet avec les renseignements à l’appui suffit pour satisfaire à cette exigence.
A6.1.1.4 Solubilité dans l’eau
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- La substance forme une émulsion stable dans l’eau, laquelle ne peut pas être séparée par filtration ou centrifugation (par exemple substances tensioactives).
Une demande de dérogation type peut être formulée comme suit, accompagnée d’une justification scientifique valable :
- Une demande de dérogation est présentée en vertu de l’alinéa 81(8)c) de la Loi, car la substance à déclarer réagit dangereusement durant l’essai.
Aucune dérogation n’est nécessaire lorsque :
- la substance est entièrement (100 %) miscible dans l’eau (supérieur à 1 000 g/L, selon la Ligne directrice [LD] 105 de l’Organisation de coopération et de développement économiques [OCDE]);
- la substance est produite dans une solution aqueuse et n’est pas disponible sous forme isolée. Une déclaration à cet effet avec les renseignements à l’appui suffit pour satisfaire à cette exigence.
A6.1.1.5 Coefficient de partage entre l’octanol et l’eau
Les exemples qui suivent illustrent des situations dans lesquelles le ministre peut accorder une dérogation :
- La substance est inorganique, c’est-à-dire qu’elle ne contient pas d’atomes de carbone;
- La solubilité de la substance dans l’eau ou l’octanol ne peut être mesurée quantitativement;
- La substance est tensioactive (tension superficielle inférieure à 60 mN/m), selon la LD 115 de l’OCDE).
Une demande de dérogation type peut être formulée comme suit, accompagnée d’une justification scientifique valable :
- Une demande de dérogation est présentée en vertu de l’alinéa 81(8)c) de la Loi relativement à la détermination du coefficient de partage entre l’octanol et l’eau, car il est techniquement impossible de déterminer ce paramètre selon les LD 107 et 117 de l’OCDE en raison de la nature tensioactive (tension superficielle inférieure à 60 mN/m) de la substance à déclarer.
Aucune dérogation n’est nécessaire lorsque :
- la substance est une substance chimique et sa solubilité dans l’eau est supérieure à 5 g/L. Une déclaration à cet effet avec les renseignements à l’appui suffit pour satisfaire à cette exigence.
A6.1.1.6 Biodégradabilité immédiate
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- La substance est inorganique, c’est-à-dire qu’elle ne contient pas d’atomes de carbone.
Une demande de dérogation type peut être formulée comme suit, accompagnée d’une justification scientifique valable :
- Une demande de dérogation est présentée en vertu de l’alinéa 81(8)c) de la Loi relativement à la biodégradation, car la substance à déclarer ne contient aucun atome de carbone et qu’elle n’est donc pas sujette à la biodégradation.
A6.1.1.7 Adsorption et désorption
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- La solubilité de la substance dans l’eau ne peut être mesurée quantitativement.
Une demande de dérogation type peut être formulée comme suit, accompagnée d’une justification scientifique valable :
- Une demande de dérogation est présentée en vertu de l’alinéa 81(8)c) de la Loi relativement à la détermination de l’adsorption et la désorption, parce qu’il est impossible de déterminer la solubilité dans l’eau de la substance à déclarer, ce paramètre ne pouvant être mesuré quantitativement.
Aucune dérogation n’est nécessaire lorsque :
- la solubilité de la substance dans l’eau est inférieure à 200 µg/L. Une déclaration à cet effet avec les renseignements à l’appui suffit pour satisfaire à cette exigence.
A6.1.1.8 Hydrolyse en fonction du pH
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- La substance ne comporte aucun groupement facilement hydrolysable; elle n’est donc pas susceptible de s’hydrolyser. La liste qui suit présente des exemples de groupes non hydrolysables :
- Acides carboxyliques;
- Acides sulfoniques;
- Alcanes;
- Alcènes;
- Alcools;
- Alcynes;
- Aldéhydes;
- Amines aromatiques;
- Benzènes/biphényles;
- Cétones;
- Composés aromatiques halogénés;
- Composés nitrés aromatiques;
- Éthers;
- Glycols;
- Hydrocarbures;
- Hydrocarbures aromatiques polycycliques;
- Hydrocarbures aromatiques polycycliques hétérocycliques;
- Phénols.
Une demande de dérogation type peut être formulée comme suit, accompagnée d’une justification scientifique valable :
- Une demande de dérogation est présentée en vertu l’alinéa 81(8)a) de la Loi relativement à la détermination du taux d’hydrolyse en fonction du pH parce que la substance ne contient pas de groupes facilement hydrolysables et parce qu’il est attendu qu’elle soit stable.
Aucune dérogation n’est nécessaire lorsque :
- la solubilité de la substance dans l’eau est inférieure à 200 µg/L. Une déclaration à cet effet avec les renseignements à l’appui suffit pour satisfaire à cette exigence.
A6.1.2 Paramètres toxicologiques
A6.1.2.1 Toxicité aiguë chez les mammifères
Les exemples qui suivent illustrent des situations dans lesquelles le ministre peut accorder une dérogation :
- La substance est corrosive et il est attendu qu’elle provoque une douleur intense et persistante chez les animaux de laboratoire. Cette dérogation doit être demandée en vertu de l’alinéa 81(8)a) de la Loi;
- Il est techniquement impossible d’administrer des doses connues de la substance en raison de ses propriétés chimiques ou physiques. Cette dérogation doit être demandée en vertu de l’alinéa 81(8)c) de la Loi.
Une demande de dérogation type peut être formulée comme suit, accompagnée d’une justification scientifique valable :
- Une demande de dérogation est présentée relativement à la détermination de la toxicité cutanée aiguë en vertu de l’alinéa 81(8)a) de la Loi au motif que la substance à déclarer est corrosive ou très irritante pour la peau des animaux de laboratoire, comme l’indique au moins un essai réalisé sur des animaux, ou parce que son pH est inférieur à 2 ou supérieur à 11,5.
Si la pression de vapeur de la substance à déclarer est très élevée et que, de ce fait, l’exposition par voie orale ou cutanée ne devrait pas constituer une voie d’exposition importante, un essai par inhalation devrait être soumis à la place. À elle seule, une pression de vapeur élevée ne constitue pas un facteur permettant d’appuyer nécessairement une demande de dérogation.
A6.1.2.2 Irritation cutanée
Les exemples qui suivent illustrent des situations dans lesquelles le ministre peut accorder une dérogation :
- Il est techniquement impossible d’administrer la substance de manière topique. Cette dérogation doit être demandée en vertu de l’alinéa 81(8)c) de la Loi;
- Il est attendu que la substance soit corrosive pour la peau des animaux de laboratoire ou alors elle a démontré une toxicité élevée aiguë par voie cutanée. Cette dérogation doit être demandée en vertu de l’alinéa 81(8)a) de la Loi.
A6.1.2.3 Sensibilisation cutanée
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- Il est techniquement impossible d’administrer la substance de manière topique. Une dérogation peut être demandée en vertu de l’alinéa 81(8)c) de la Loi.
A6.1.2.4 Toxicité à doses répétées chez les mammifères
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- Il est techniquement impossible d’administrer des doses connues de la substance en raison de ses propriétés chimiques ou physiques. Une dérogation peut être demandée en vertu de l’alinéa 81(8)c) de la Loi.
Si la pression de vapeur de la substance à déclarer est très élevée et que, de ce fait, l’exposition par voie orale ou cutanée ne devrait pas constituer une voie d’exposition importante, un essai d’exposition par inhalation devrait être soumis à la place. À elle seule, une pression de vapeur élevée ne constitue pas un facteur permettant d’appuyer nécessairement une demande de dérogation.
A6.1.2.5 Essai in vitro pour déterminer la présence de mutations génétiques
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- Un essai de génotoxicité in vivo chez des mammifères indique que la substance a un pouvoir mutagène. Une dérogation peut être demandée en vertu de l’alinéa 81(8)a) de la Loi.
A6.1.2.6 Essai in vitro pour déterminer la présence d’aberrations chromosomiques chez les mammifères
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- Un essai de génotoxicité in vivo chez des mammifères indique que la substance possède un pouvoir clastogène. Une dérogation peut être demandée en vertu de l’alinéa 81(8)a) de la Loi.
A6.1.2.7 Essai in vivo de génotoxicité chez les mammifères
Une dérogation peut être demandée en vertu de l’alinéa 81(8)a) de la Loi relativement à la détermination de la génotoxicité in vivo parce que la substance satisfait à toutes les conditions suivantes :
- L’utilisation prévue de la substance n’entraînera pas d’exposition directe, répétée ou prolongée chez l’humain;
- Selon les résultats des essais in vitro visant à déterminer la présence de mutations génétiques et d’aberrations chromosomiques chez les mammifères, la substance n’a montré aucun effet génotoxique;
- La structure chimique de la substance, ou de l’un de ses composants, n’est liée à aucun mutagène ou cancérigène connu.
Une dérogation peut être demandée en vertu de l’alinéa 81(8)a) de la Loi relativement à la détermination de la génotoxicité in vivo parce que les 2 essais de génotoxicité in vitro (étude sur les mutations génétiques chez des bactéries et étude sur les aberrations chromosomiques chez des mammifères) ont donné des résultats positifs. Par cette dérogation, la conclusion pour la substance sera qu’elle est génotoxique.
A6.2 Polymères
Les exemples qui suivent décrivent des situations dans lesquelles le ministre peut accorder une dérogation et ils peuvent s’appliquer à n’importe quel essai :
- La substance est créée in situ lors du procédé de fabrication et elle se décompose lors des tentatives d’isolement;
- La substance réagit de manière dangereuse au cours de l’essai.
A6.2.1 Paramètres physico-chimiques
A6.2.1.1 Masse moléculaire moyenne en nombre et concentration ou quantité de constituants résiduels ou de faible poids moléculaire
Les exemples qui suivent illustrent des situations dans lesquelles le ministre peut accorder une dérogation :
- Il est techniquement impossible de réaliser l’essai, car la substance est un polymère fortement réticulé (joindre une justification scientifique valable);
- La substance est insoluble dans les solvants devant être utilisés pour l’analyse par chromatographie sur gel perméable (Gel Permeation Chromatography - GPC) et aucune autre technique ne peut être utilisée.
A6.2.1.2 Coefficient de partage entre l’octanol et l’eau
Dans le cas de polymères réactifs dans l’eau, le Programme des substances nouvelles (SN) reconnaît que l’autocondensation et la formation de précipités peuvent causer des problèmes. Consulter l’appendice 9 du Document d’orientation pour en savoir plus sur les procédures à suivre dans le cas de polymères hydroréactifs selon le Programme des SN.
Les exemples qui suivent illustrent des situations dans lesquelles le ministre peut accorder une dérogation :
- La solubilité de la substance dans l’eau ou l’octanol ne peut être mesurée par des analyses;
- La substance est tensioactive (tension superficielle inférieure à 60 mN/m), selon la LD 115 de l’OCDE).
Une demande de dérogation type peut être formulée comme suit, accompagnée d’une justification scientifique valable :
- Une demande de dérogation est présentée en vertu de l’alinéa 81(8)c) de la Loi relativement à la détermination du coefficient de partage entre l’octanol et l’eau, car il est techniquement impossible de déterminer ce paramètre selon les LD 107 et 117 de l’OCDE en raison de la nature tensioactive (tension superficielle inférieure à 60 mN/m) de la substance à déclarer.
A6.2.1.3 Hydrolyse en fonction du pH
Dans le cas de polymères réactifs dans l’eau, le Programme des SN reconnaît que l’autocondensation et la formation de précipités peuvent causer des problèmes. Consulter l’appendice 9 du Document d’orientation pour en savoir plus sur les procédures à suivre dans le cas de polymères hydroréactifs selon le Programme des SN.
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- Le polymère ne comporte aucun groupement facilement hydrolysable; il n’est donc pas susceptible de s’hydrolyser. La liste qui suit présente des exemples de groupes non hydrolysables :
- Acides carboxyliques;
- Acides sulfoniques;
- Alcanes;
- Alcènes;
- Alcools;
- Alcynes;
- Aldéhydes;
- Amines aromatiques;
- Benzènes/biphényles;
- Cétones;
- Composés aromatiques halogénés;
- Composés nitrés aromatiques;
- Éthers;
- Glycols;
- Hydrocarbures;
- Hydrocarbures aromatiques polycycliques;
- Hydrocarbures aromatiques polycycliques hétérocycliques;
- Phénols.
Une demande de dérogation type peut être formulée comme suit, accompagnée d’une justification scientifique valable :
- Une demande de dérogation est présentée en vertu l’alinéa 81(8)a) de la Loi relativement à la détermination du taux d’hydrolyse en fonction du pH parce que la substance ne contient pas de groupes hydrolysables et parce qu’il est attendu qu’elle soit stable.
Aucune dérogation n’est nécessaire lorsque :
- l’extractibilité de la substance dans l’eau est inférieure ou égale à 2 %. Une déclaration à cet effet avec les renseignements à l’appui suffit pour satisfaire à cette exigence.
A6.2.1.4 Biodégradabilité immédiate
Dans le cas de polymères réactifs dans l’eau, le Programme des SN reconnaît que l’autocondensation et la formation de précipités peuvent causer des problèmes. Consulter l’appendice 9 du Document d’orientation pour en savoir plus sur les procédures à suivre dans le cas de polymères hydroréactifs selon le Programme des SN.
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- Le polymère est inorganique, c’est-à-dire qu’il ne contient pas d’atomes de carbone.
Une demande de dérogation type peut être formulée comme suit, accompagnée d’une justification scientifique valable :
- Une demande de dérogation est présentée en vertu de l’alinéa 81(8)c) de la Loi relativement à la biodégradation, car la substance à déclarer ne renferme aucun atome de carbone et qu’elle n’est donc pas sujette à la biodégradation.
Aucune dérogation n’est nécessaire lorsque :
- l’extractibilité de la substance dans l’eau est inférieure ou égale à 2 % à un pH de 7 ou la substance est une silicone ramifiée ou un polymère de siloxane. Une déclaration à cet effet avec les renseignements à l’appui suffit pour satisfaire à cette exigence.
A6.2.2 Paramètres toxicologiques
Dans le cas de polymères qui ne sont pas des polymères à exigences réglementaires réduites (non-ERR), les données relatives à la toxicité chez les mammifères peuvent faire l’objet d’une dérogation uniquement du fait que le polymère renferme les groupes cationiques ou potentiellement cationiques suivants : groupes amines primaires, secondaires et tertiaires, cyanamides ou composés sulfonés. Cela dépendra notamment du profil d’utilisation du polymère et du faible risque d’exposition prévu dans la population en général. Cette dérogation doit être demandée en vertu de l’alinéa 81(8)a) de la Loi.
Les polymères destinés à être utilisés dans des produits de soins personnels, des jouets pour enfants ou des matières venant directement en contact avec les aliments ne sont généralement pas admissibles à une dérogation relative aux essais de toxicité aiguë et de toxicité à doses répétées s’il est attendu que le contact cutané prolongé ou l’ingestion par voie orale constituent d’importantes voies d’exposition.
Les polymères ne sont généralement pas admissibles à une dérogation relative aux essais de toxicité aiguë et de toxicité à doses répétées s’il est attendu que l’inhalation soit le mode d’exposition le plus probable de la population générale d’après le type d’utilisation prévu.
Une demande de dérogation type peut être formulée comme suit, accompagnée d’une justification scientifique valable :
- Une demande de dérogation est présentée en vertu de l’alinéa 81(8)a) de la Loi relativement aux essais de toxicité à doses répétées sur 28 jours chez les mammifères, car la substance à déclarer satisfait à la définition de la classe des polymères cationiques et que son profil d’utilisation ne causera pas d’exposition directe, répétée ou prolongée d’un humain.
Les paramètres de toxicité pour la santé humaine prévus à l’article 4 de l’annexe 10 du Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [le Règlement] et aux articles 5 à 10 de l’annexe 11 du Règlement ne sont pas requis si le polymère est un polymère non-ERR du seul fait de la présence de l’un ou l’autre des groupes fonctionnels suivants :
- a) les aldéhydes dont la masse équivalente du groupe fonctionnel (MEGF, consulter la partie 3.3.1.8) est inférieure ou égale à 1 000 daltons;
- b) les éthers vinyliques à MEGF inférieure ou égale à 5 000 daltons;
- c) les acides sulfoniques à MEGF inférieure ou égale à 5 000 daltons.
A6.2.2.1 Toxicité aiguë chez les mammifères
Les exemples qui suivent illustrent des situations dans lesquelles le ministre peut accorder une dérogation :
- Le polymère est corrosif pour la peau des animaux de laboratoire et il est attendu qu’il provoque une douleur intense et persistante chez les animaux de laboratoire. Une dérogation peut être demandée en vertu de l’alinéa 81(8)a) de la Loi;
- Il est techniquement impossible d’administrer des doses connues du polymère à cause de ses propriétés chimiques ou physiques. Une dérogation peut être demandée en vertu de l’alinéa 81(8)c) de la Loi.
A6.2.2.2 Irritation cutanée
Les exemples qui suivent illustrent des situations dans lesquelles le ministre peut accorder une dérogation :
- Il est techniquement impossible d’administrer le polymère de manière topique. Une dérogation peut être demandée en vertu de l’alinéa 81(8)c) de la Loi;
- Il est attendu que le polymère soit corrosif pour la peau des animaux de laboratoire ou alors le polymère a démontré une toxicité aiguë élevée par voie cutanée. Une dérogation peut être demandée en vertu de l’alinéa 81(8)a) de la Loi.
A6.2.2.3 Sensibilisation cutanée
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- Il est techniquement impossible d’administrer le polymère de manière topique. Une dérogation peut être demandée en vertu de l’alinéa 81(8)c) de la Loi.
A6.2.2.4 Toxicité à doses répétées chez les mammifères
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- Il est techniquement impossible d’administrer des doses connues du polymère en raison de ses propriétés chimiques ou physiques. Une dérogation peut être demandée en vertu de l’alinéa 81(8)c) de la Loi.
A6.2.2.5 Essai in vitro pour déterminer la présence de mutations génétiques
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- Un essai de génotoxicité in vivo chez des mammifères indique que le polymère a un pouvoir mutagène. Une dérogation peut être demandée en vertu de l’alinéa 81(8)a) de la Loi.
A6.2.2.6 Essai in vitro pour déterminer la présence d’aberrations chromosomiques chez les mammifères
L’exemple qui suit illustre une situation dans laquelle le ministre peut accorder une dérogation :
- Un essai de génotoxicité in vivo chez des mammifères indique que le polymère a un pouvoir clastogène. Une dérogation peut être demandée en vertu de l’alinéa 81(8)a) de la Loi.
A6.2.2.7 Essai in vivo de génotoxicité chez les mammifères
Une dérogation peut être demandée en vertu de l’alinéa 81(8)a) de la Loi relativement à la détermination de la génotoxicité in vivo parce que le polymère satisfait à toutes les conditions suivantes :
- L’utilisation prévue du polymère n’entraînera pas d’exposition directe, répétée ou prolongée chez l’humain;
- Selon les résultats des essais in vitro visant à déterminer la présence de mutations génétiques et d’aberrations chromosomiques chez les mammifères, le polymère n’a montré aucun effet génotoxique;
- La structure chimique du polymère, ou de l’un de ses composants, n’est liée à aucun mutagène ou cancérigène connu.
Une dérogation peut également être demandée en vertu de l’alinéa 81(8)a) de la Loi relativement à la détermination de la génotoxicité in vivo parce que les 2 essais de génotoxicité in vitro (étude sur les mutations génétiques chez des bactéries et étude sur les aberrations chromosomiques chez des mammifères) ont donné des résultats positifs. Par cette dérogation, la conclusion pour la substance sera qu’elle est génotoxique.
Appendice 7. Satisfaire aux exigences relatives de la masse moléculaire moyenne en nombre via les données de l’analyse par chromatographie sur gel perméable
A7.1 Procédures d’essai
Les procédures d’essai utilisées pour obtenir les données relatives à la masse moléculaire moyenne en nombre (Mn) doivent être spécifiées. Le Programme des substances nouvelles (SN) recommande de suivre les protocoles d’essai de la Ligne directrice (LD) 118 de l’ Organisation de coopération et de développement économiques (OCDE) pour déterminer la Mn par chromatographie sur gel perméable (Gel Permeation Chromatography - GPC) et la LD 119 de l’OCDE pour déterminer les composantes résiduelles dont la masse moléculaire est inférieure à 500 daltons et inférieure à 1 000 daltons.
A7.2 Chromatogramme sur gel perméable
Un chromatogramme présentant la valeur calculée de Mn doit être fourni.
Le nom de la substance déclarée doit être clairement identifié sur les données d’essai de la GPC. La courbe originale et complète de la GPC doit être fournie en précisant clairement l’intervalle d’intégration.
Un essai sur un blanc doit également être fourni.
Dans le cas où les courbes de la GPC sont incomplètes (c’est-à-dire, quand l’intégration des pics n’est pas réalisée sur toute leur largeur), il faut fournir une justification expliquant pourquoi certains pics n’ont pas été inclus dans le calcul de la Mn et fournir le pourcentage de composantes de faible masse moléculaire. Il pourrait alors être nécessaire d’identifier les pics tronqués en indiquant, par exemple, s’ils signifient la présence de monomères résiduels, d’additifs ou d’autres solvants dans l’échantillon.
Le nom de l’essai et la courbe d’étalonnage qui sont référés doivent être clairement indiqués sur la sortie imprimée du tracé chromatographique. Pour identifier la substance, la case A.19 de la Déclaration de substances nouvelles (DSN) doit contenir le numéro d’identification que le laboratoire a attribué à l’échantillon. La figure A7-1 présente un exemple d’un tracé de GPC incluant la description recommandée.

Liste de la description recommendée à inclure avec le tracé de GPC :
- Nom du projet : GPC de nom commercial;
- Nom de l’échantillon : Nom commercial1, la référence devrait correspondre au nom commercial ou au nom de la substance indiqué à la case A.19 de la DSN;
- Volume d’injection : 100.00;
- Instrument : référer à la procédure et à l’instrument utilisé;
- Phase mobile : référer à la procédure et aux renseignements sur la phase mobile;
- Paramètres (colonne) : référer à la procédure et aux paramètres de la colonne du logiciel;
- Date de traitement : 02/02/2019 11:00:00 AM HAE.
| Nom de l’échantillon | MPa | Mnb | Mzc | Mwd | % massique < 500 daltons | % massique < 1 000 daltons | Mw/Mn (polydispersité) |
|---|---|---|---|---|---|---|---|
| Nom commercial1 | 985 | 1 584 | 4 994 | 3 068 | 3.8 | 17.4 | 1.9 |
a MP – masse moléculaire du plus haut pic.
b Mn – masse moléculaire moyenne en nombre.
c Mz – masse moléculaire moyenne z.
d Mw – masse moléculaire moyenne en poids.
A7.3 Étalonnage
L’étalonnage doit mentionner toutes les conditions d’exécution et l’identité chimique des étalons utilisés. La date d’étalonnage devrait se situer dans le mois qui précède la prise de données GPC pour la substance déclarée. Les données d’échantillon qui sont prises à plus d’un mois de la date d’étalonnage devraient être accompagnées de témoins qui démontrent que le système est adéquat pour la mesure (consulter la partie A7.6.4).
Toutes les mesures qui ont servi à produire la courbe d’étalonnage doivent être consignées, de préférence dans un tableau (consulter le tableau A7-2). La figure A7-2 donne un exemple d’une courbe d’étalonnage incluant la description recommandée.
La méthode de diffusion de la lumière multi-angles (Multi Angle Light Scattering – MALS) ou diffusion d’une lumière laser multi-angles (Multi Angle Laser Light Scattering – MALLS) peut mesurer directement la masse moléculaire absolue sans étalonnage avec des étalons.
| Coupe | Temps de rétention (minutes) | Masse moléculaire (daltons) | Masse calculée (daltons) | Pourcentage résiduel |
|---|---|---|---|---|
| 1 | 15.923 | 1 090 000 | 1 054 689 | 3.348 |
| 2 | 16.456 | 579 000 | 590 573 | -1.960 |
| 3 | 17.259 | 246 000 | 262 182 | -6.172 |
| 4 | 18.035 | 130 000 | 127 883 | 1.656 |
| 5 | 18.866 | 67 000 | 63 238 | 5.949 |
| 6 | 19.630 | 34 800 | 34 981 | -0.516 |
| 7 | 20.595 | 17 800 | 17 732 | 0.381 |
| 8 | 21.751 | 8 400 | 8 577 | -2.062 |
| 9 | 23.382 | 3 420 | 3 519 | -2.825 |
| 10 | 25.073 | 1 620 | 1 578 | 2.632 |
| 11 | 27.094 | 682 | 665 | 2.628 |
| 12 | 27.455 | 578 | 572 | 1.053 |
| 13 | 27.893 | 474 | 477 | -0.623 |
| 14 | 28.445 | 370 | 379 | -2.346 |
| 15 | 29.229 | 266 | 272 | -2.180 |
| 16 | 30.441 | 162 | 159 | 1.700 |

Liste de la description recommendée à inclure avec la courbe d’étalonnage de GPC :
- Date de traitement : 02/01/2019 10:00:00 AM HAE;
- Instrument : renseignements de l’instrument;
- Phase mobile : référer à la procédure et aux renseignements sur la phase mobile;
- Paramètres (colonne) : référer à la procédure et aux paramètres de la colonne du logiciel;
- Échantillon : référer à la procédure et aux renseignements de l’échantillon;
- Ordinateur : renseignements de l’ordinateur;
- Étalons : l’étalonnage a été établie avec des étalons de polystyrène.
A7.4 Tables des coupes
Les tables des coupes ne figurent pas expressément parmi les exigences réglementaires du Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères). Elles pourraient toutefois être exigées pour prouver la situation réglementaire du polymère ou son statut de déclaration (polymère à exigences réglementaires réduites ou polymère qui ne satisfait pas aux critères établis pour les polymères à exigences réglementaires réduites; consulter la partie 3.3.1.5 et la partie 3.3.1.6).
Des renseignements sur les coupes devraient être obtenus en utilisant des intervalles raisonnables. Selon la dispersité du polymère, 1 à 3 pages de renseignement suffisent. Le paramètre définitoire des coupes devrait être soit le temps de rétention soit le volume de rétention.
Si des tables des coupes sont fournies, les données doivent correspondre à la courbe de la GPC. La masse moléculaire à un moment particulier (ou à un volume particulier) doit correspondre à la courbe.
Les tables des coupes doivent comprendre au moins 3 colonnes : le temps (ou volume) de rétention, la masse moléculaire et le pourcentage cumulatif (ou autre facteur semblable). Le tableau A7-3 présente un exemple d’une table des coupes incluant la description recommandée.
| Slice | Temps de rétention (minutes) | Masse moléculaire (daltons) | Pourcentage cumulatif |
|---|---|---|---|
| 1 | 21.24 | 11 729 | 1 |
| 2 | 21.91 | 7 802 | 5 |
| 3 | 22.31 | 6 197 | 10 |
| 4 | 22.61 | 5 268 | 15 |
| 5 | 22.87 | 4 590 | 20 |
| 6 | 23.09 | 4 096 | 25 |
| 7 | 23.32 | 3 630 | 30 |
| 8 | 23.53 | 3 270 | 35 |
| 9 | 23.70 | 3 008 | 40 |
| 10 | 23.92 | 2 698 | 45 |
| 11 | 24.23 | 2 327 | 50 |
| 12 | 24.42 | 2 129 | 55 |
| 13 | 24.55 | 2 003 | 60 |
| 14 | 24.70 | 1 863 | 65 |
| 15 | 25.13 | 1 541 | 70 |
| 16 | 25.81 | 1 143 | 75 |
| 17 | 26.06 | 1 026 | 80 |
| 18 | 26.09 | 1 015 | 81 |
| 19 | 26.11 | 1 005 | 82 |
| 20 | 26.13 | 996 | 83 |
| 21 | 26.17 | 978 | 85 |
| 22 | 26.30 | 926 | 90 |
| 23 | 26.92 | 714 | 95 |
| 24 | 27.17 | 513 | 96 |
| 25 | 28.13 | 432 | 97 |
| 26 | 28.77 | 330 | 98 |
| 27 | 29.41 | 252 | 99 |
| 28 | 31.59 | 92 | 100 |
Liste de la description recommendée à inclure avec la table des coupes :
- Nom de l’échantillon : Nom commercial1;
- Date de l’acquisition: 01/31/2019 11:00:00 AM HAE;
- Date de traitement : 02/02/2019 11:00:00 AM HAE.
A7.5 Production de rapports
Les renseignements précisés dans les LD 118 et 119 de l’OCDE pour la production de rapports devraient être transmis pour évaluation, incluant :
- les renseignements disponibles sur la composition de la substance à analyser et sa pureté (identité, additifs, impuretés);
- les procédures de préparation et de prétraitement de l’échantillon avant son envoi au laboratoire;
- une description de la préparation de l’échantillon, ainsi que des observations formulées ou problèmes observés durant l’analyse par GPC;
- le type de colonne utilisée et toute autre renseignement technique pertinent sur l’instrumentation;
- le solvant utilisé et sa pureté;
- des renseignements sur toutes les extrapolations, hypothèses et approximations faites durant l’étalonnage et les essais;
- toute autre renseignement et observation pertinents pour l’interprétation des résultats.
Note : les déclarants omettent souvent d’inclure les résultats réels des essais (par exemple le traitement de l’échantillon, les observations ou les problèmes observés) et devraient inclure ces renseignements pour mieux informer l’évaluation.
Lorsque les LD 118 ou 119 de l’OCDE ne sont pas suivis, il faut aussi inclure la nature et la description de la ligne directrice et de la méthodologie employés pour l’essai. Toute modification apportée à la procédure d’essai doit être décrite en détail.
A7.6 Difficultés les plus fréquemment observées
A7.6.1 Faible solubilité de l’échantillon
Lorsqu’un polymère est insoluble (solubilité inférieure à 2 %) dans un système de solvants généralement utilisé aux fins de la GPC, les données relatives à la solubilité doivent être indiquées pour un éventail de différents solvants. Il faut tenter de dissoudre la substance dans au moins 3 solvants différents. Si la dissolution se fait relativement bien, déclarer la quantité non dissoute dans l’essai pour lequel la solubilité a été la plus grande. Si toutes les tentatives visant à dissoudre la substance dans des solvants convenant à la GPC échouent, une autre méthode pourrait être nécessaire.
L’insolubilité dans les solvants classiques pourrait être le signe de la forte réticulation du polymère. Des méthodes alternatives doivent alors être employées pour déterminer la Mn ou, encore, une demande de dérogation doit accompagner les résultats d’insolubilité. Dans cet exemple, la Mn d’un prépolymère pourrait aussi être fournie comme donnée de substitution.
A7.6.2 Artefacts expérimentaux pouvant survenir lors de la chromatographie
Si les mêmes artefacts apparaissent dans l’essai à blanc ou l’essai témoin de référence, ils peuvent être exclus de l’intégration.
A7.6.3 Renseignements de substitution
Les renseignements de substitution seront acceptés au cas par cas. Dans le cas d’un polymère qui subit un traitement au sel, il est acceptable de fournir la GPC du polymère qui n’a pas subit de traitement au sel. Cela vaut également pour les polymères qui sont bloqués par un groupe terminal.
A7.6.4 Différence notable entre la date d’étalonnage et celle du passage de l’échantillon
Si des procédures générales sont mises en place pour confirmer avant chaque essai l’exactitude de la colonne de GPC et de l’instrumentation au moyen de quelques étalons, ces procédures devraient être mentionnées dans la description de la méthode d’essai. Les témoins positifs devraient être des polymères dont la Mn est connue. Les témoins positifs devraient aussi démontrer que le système est adéquat pour un éventail d’applicabilité suffisamment large, de sorte que la Mn de l’échantillon y est incluse. Un système est considéré adéquat lorsque la Mn du témoin positif est mesurée avec précision dans les limites de l’erreur du système.
Appendice 8. Exigences relatives au plan de réaction
Il est nécessaire de présenter un plan de réaction décrivant en détail le procédé de fabrication de la substance à déclarer dans le cas des polymères à exigences réglementaires réduites (ERR) (consulter la partie 3.3.1.5).
Les exemples suivants illustrent le niveau de détail qui devrait accompagner les plans de réaction.
A8.1 Exemples de plans de réaction
Les 2 exemples suivants illustrent comment la modification de la séquence des monomères et de leurs rapports molaires peut influer sur la situation réglementaire du polymère. Les 3 mêmes monomères servent à la synthèse des 2 polymères :
Monomère A : diisocyanate d’isophorone;
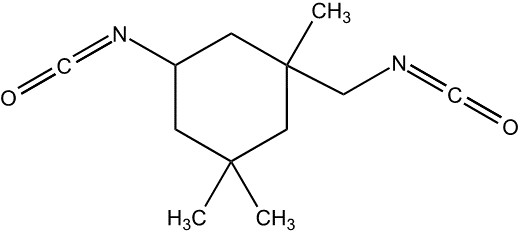 /
/Monomère B: éthylène glycol;
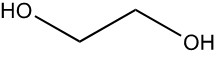
Monomère C: acide butane-1, 4-dioïque.
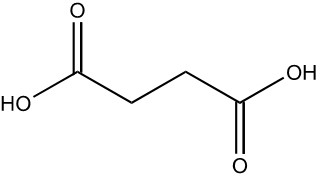
Exemple 1 : Plan de réaction pour synthétiser le Polymère 1.
Étape 1 : Formation du polyuréthane
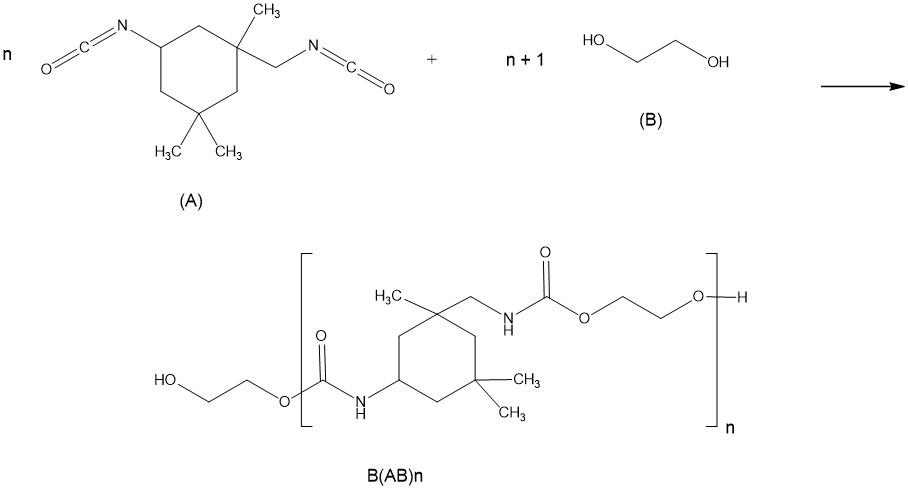
Étape 2 : Estérification
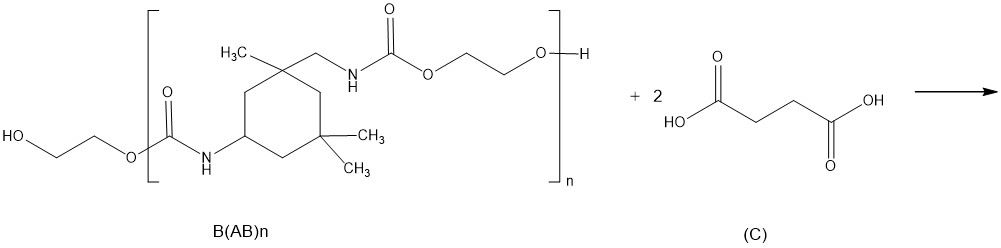
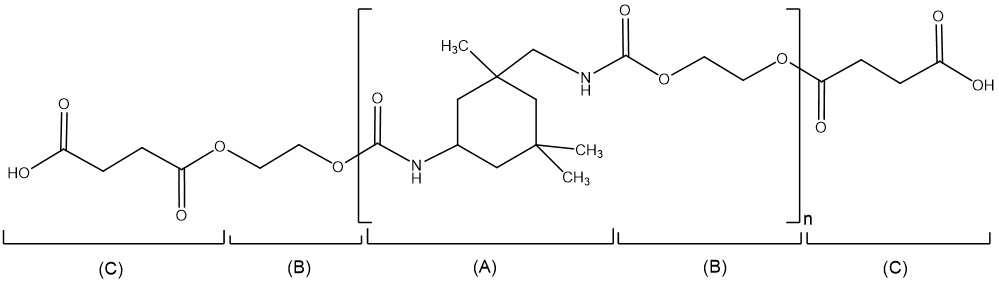
Polymère 1
Le produit final, le Polymère 1, possède la structure CB(AB)nC, dans laquelle l’élément C est dérivé d’un monomère diacide. Comme ce produit ne renferme aucun groupe réactif préoccupant, il peut être considéré comme un polymère ERR.
Exemple 2 : Plan de réaction pour synthétiser le Polymère 2 à partir des 3 mêmes monomères.
Étape 1 : Estérification
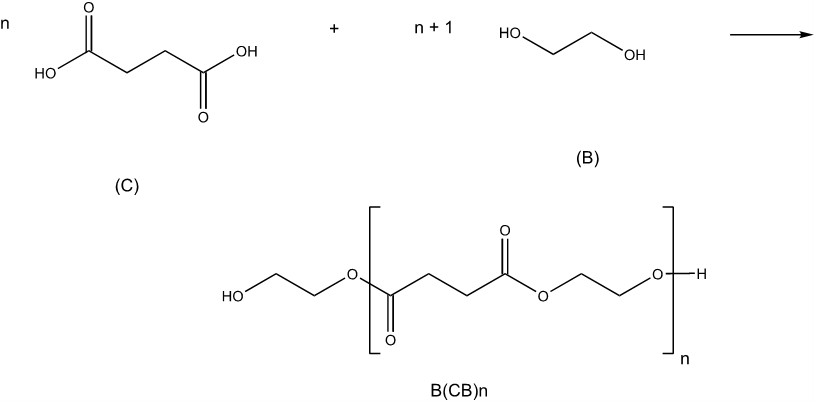
Étape 2 : Formation de l’uréthane
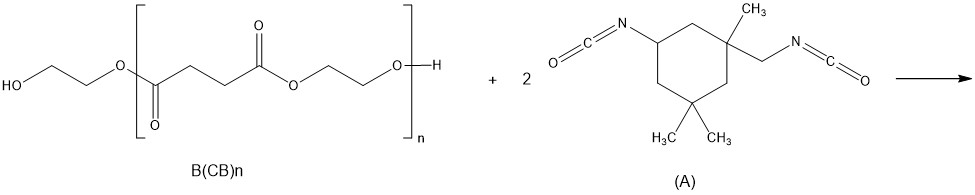
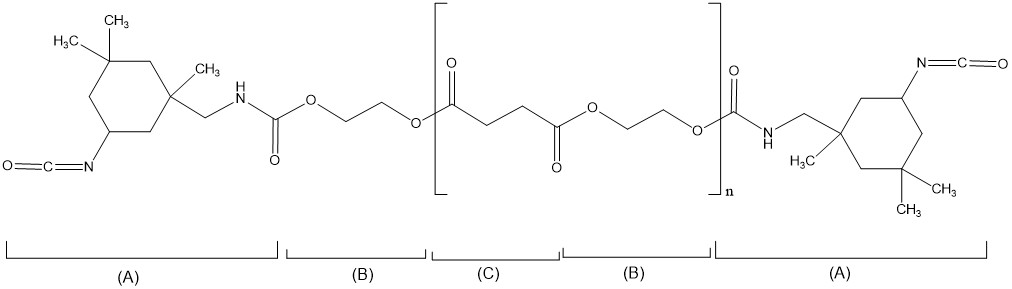
Polymère 2
Le Polymère 2 possède la structure AB(CB)nA et renferme des isocyanates n’ayant pas réagi qui sont des groupes réactifs préoccupants. Ce polymère ne pourrait donc être considéré comme un polymère ERR.
A8.2 Format du plan de réaction
Le plan de réaction renferme des renseignements sur les monomères et sur les réactifs ainsi qu’une description de la séquence.
A8.2.1 Renseignements sur les monomères et les réactifs
Le déclarant doit fournir un tableau précisant la dénomination chimique de tous les monomères, prépolymères et réactifs ainsi que leur numéro d’enregistrement du Chemical Abstracts Service (CAS) et leur pourcentage massique (case A.24 du formulaire de Déclaration de substance nouvelles). Ce tableau devrait aussi présenter les valeurs pour la masse moléculaire et le nombre relatif de moles, et peut être fournit en pièce jointe. Il faut attribuer à chaque monomère, prépolymère et réactif un idenfiant qui sera utilisé pour décrire la séquence.
| ID | Monomères et réactifs | Numéro d’enregistrement CAS | mma | % massique | Nombre relatif de moles |
|---|---|---|---|---|---|
| A | 5-Isocyanato-1-(isocyanatométhyl)-1,3,3-triméthylcyclohexane | 4098-71-9 | 222 | 2,52 | 11 |
| B | α-Hydro-ω-hydroxypoly(oxy-1,2-éthanediyl) | 25322-68-3 | 7 850 | 97,22 | 12 |
| C | Isocyanate d’hexyle normal | 2525-62-4 | 127 | 0,26 | 2 |
a mm – Masse moléculaire
A8.2.2 Description de la séquence
Il faut soit décrire chaque étape et préciser la séquence dans laquelle elle s’inscrit, en indiquant la nature des réactions et en fournissant les identifiants de tous les monomères, réactifs et intermédiaires, par exemple :
- 1re étape : A + B → intermédiaire AB (formation du polyuréthane);
- 2e étape : intermédiaire AB + C → produit final (formation du groupe terminal – uréthane).
ou il faut décrire la séquence en utilisant des formules développées et en incluant la nature des réactions et la séquence dans laquelle elles s’inscrivent ainsi que les identifiants de tous les monomères, réactifs et intermédiaires, par exemple :
Étape 1 : Formation du polyuréthane
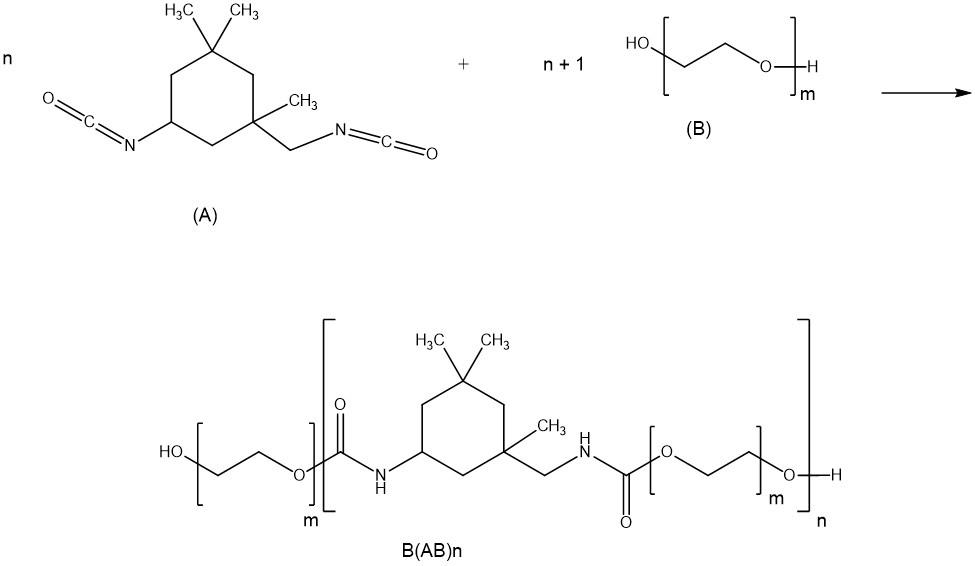
Étape 2 : Formation du groupe terminal sur l’uréthane
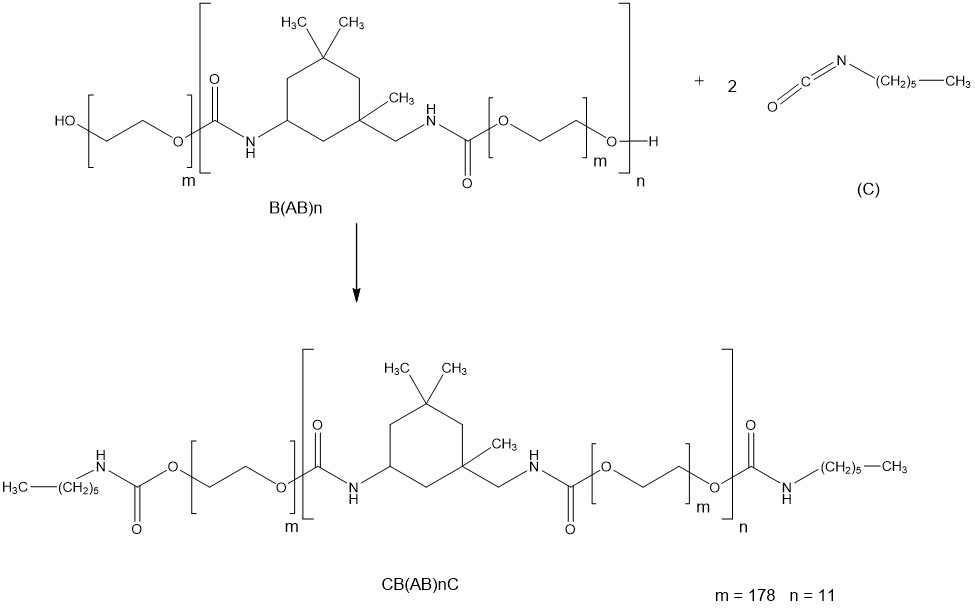
Appendice 9. Directives sur l’essai d’extractabilité dans l’eau selon la Ligne directrice 120 de l’Organisation de coopération et de développement économiques
La disponibilité dans l’eau des polymères devant être déclarés en vertu des annexes 10 et 11 du Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) [le Règlement] est déterminée à partir des renseignements sur l’extractibilité dans l’eau. Pour satisfaire à ces exigences en matière de renseignements, le Programme des substances nouvelles (SN) recommande de suivre le protocole expérimental pour déterminer l’extractibilité dans l’eau, défini dans la Ligne directrice (LD) 120 de l’Organisation de coopération et de développement économiques (OCDE) : Comportement de dissolution – extraction des polymères dans l’eau.
Les polymères sont composés d’une variété de molécules de masses moléculaires variables. En raison de la répartition de leur masse moléculaire, les polymères forment souvent des mélanges hétérogènes dans l’eau (contrairement aux substances chimiques discrètes qui peuvent former de véritables solutions thermodynamiques). Les composantes moléculaires plus petites d’un polymère peuvent se dissoudre complètement alors que les composantes plus grosses peuvent former des émulsions, des dispersions ou des gels. La fraction disponible dans l’eau du polymère représente les composantes qui présentent le plus grand intérêt aux fins de l’évaluation des risques pour la santé humaine et l’environnement en raison de leur biodisponibilité.
A9.1 Ligne directrice 120 de l’Organisation de coopération et de développement économiques
La LD 120 de l’OCDE est une méthode internationalement acceptée pour déterminer l’extractibilité dans l’eau de la plupart des polymères. Cette méthode tient compte du fait que les polymères sont constitués de composantes de masses moléculaires différentes et que la solubilité (c’est-à-dire la fraction pouvant être extraite en milieu aqueux) de chacune de ces composantes varie. Les conseils qui suivent visent à répondre aux problèmes techniques liés à l’application de la LD 120 de l’OCDE pour évaluer l’extractibilité dans l’eau des polymères.
A9.2 Guide technique pour l’application de la Ligne directrice 120 de l’Organisation de coopération et de développement économiques
A9.2.1 Facteurs influençant l’extractibilité dans l’eau
Les méthodes d’analyse et de préparation des échantillons peuvent influer grandement sur l’extractibilité dans l’eau des polymères. Aussi faut-il éviter, dans la mesure du possible, d’utiliser des méthodes d’analyse inadéquates. Les études peuvent être jugées non acceptables par le Programme des SN si les procédures ou les conditions causent des interférences susceptibles d’altérer les résultats. Voici quelques-uns des principaux facteurs qui influent sur l’extractibilité dans l’eau :
- Préparation de l’échantillon : les méthodes utilisées pour extraire le polymère d’un mélange ou l’isoler d’un solvant doivent préserver l’intégrité de la substance polymérique relativement à la distribution de sa masse moléculaire et à son extractibilité dans l’eau;
- Surface de contact de l’échantillon : comme la dissolution se produit essentiellement à la surface de la masse polymérique, les échantillons possédant une grande surface de contact (c’est-à-dire ceux composés de petites particules) se dissolvent plus rapidement;
- Rapport du volume d’eau à la masse de l’échantillon : l’utilisation d’une quantité insuffisante d’eau peut mener à une sous-estimation de l’extractibilité;
- Vitesse de mélange : l’agitation permet de renouveler le solvant près de la surface du soluté;
- Température : le chauffage confère à la solution une énergie cinétique plus grande qui favorise la dissolution des molécules. Il peut également y avoir production de chaleur durant les interactions entre l’eau et le soluté (par exemple liaison hydrogène) ce qui, en retour, peut faciliter la dissolution;
- Qualité de l’eau : certains polymères qui ne sont pas normalement disponibles dans l’eau peuvent se dissoudre dans des solutions aqueuses salées (effet de « dissolution par les sels »). Dans d’autres cas, les sels peuvent réduire l’hydratation des molécules des polymères (effet de « relargage »);
- pH : il est possible d’accroître la disponibilité en solutions aqueuses de polymères renfermant des groupements ionisables, comme des acides carboxyliques ou des amines, en y ajoutant une base ou un acide, respectivement;
- Traitement final : le recours à la centrifugation à grande vitesse ou à des filtres très fins peut permettre de séparer les matières extraites d’une dispersion dans l’eau par ailleurs stable.
A9.2.2 Guide technique
Il est recommandé d’utiliser la LD 120 de l’OCDE pour étudier l’extractibilité dans l’eau de tous les types de polymères, même s’il est indiqué que la méthode ne s’applique pas aux polymères liquides, aux polymères qui semblent liquides à cause de la présence d’impuretés telles que des solvants ou aux substances qui réagissent avec l’eau dans les conditions expérimentales. Le Programme des SN recommande donc que l’extractibilité dans l’eau des polymères soit déterminée selon la LD 120 de l’OCDE en respectant les directives suivantes :
- L’eau utilisée devrait être distillée ou désionisée;
- Comme prescrit par le Règlement, le pH de la phase aqueuse devrait être égal à 2, 7 ou 9, respectivement, avant l’ajout du polymère à déclarer. Le pH devrait être ajusté avec de l’acide chlorhydrique ou de l’hydroxyde de sodium ou de potassium, pour éviter l’utilisation ou la création d’un système tampon;
- S’il s’agit de polymères visqueux, il est recommandé de :
- ne pas utiliser des solvants pour les dissoudre;
- ne pas durcir les polymères ou de les faire réagir avant de réaliser l’essai;
- préparer les récipients expérimentaux en étalant d’abord la substance sur les parois du récipient. La surface du polymère exposée à l’eau sera ainsi maximisée et celui-ci pourrait devenir extractible;
- L’échantillon devrait être agité pendant 24 heures à 20 °C. Les agitateurs normalement employés en laboratoire sont jugés suffisants pour reproduire l’action de l’eau en conditions naturelles;
- Bien que certains polymères liquides puissent ne pas se prêter aux essais, la formation de dispersions liquides stables (émulsions) devrait être étudiée. Le Programme des SN considère que les polymères en émulsion stable sont disponibles dans l’eau;
- Les polymères dans un solvant devraient être séchés de manière appropriée, c’est-à-dire sans compromettre l’intégrité du polymère. Par exemple, le chauffage du polymère au four pour en retirer les résidus de solvant peut entraîner la perte des oligomères et favoriser l’accroissement de la polymérisation de la substance. Selon le Programme des SN, un tel prétraitement invaliderait les résultats de l’essai sur l’extractibilité dans l’eau. Plutôt que d’essayer de retirer tous les résidus de solvant, il est préférable d’analyser l’échantillon de polymère avec ces résidus, puis de soustraire la quantité en question des résultats concernant l’extractibilité dans l’eau;
- Selon la LD 120 de l’OCDE, la filtration ou la centrifugation devraient être utilisées pour obtenir une phase aqueuse limpide; l’objectif du Programme des SN est toutefois de quantifier l’ensemble de la fraction biodisponible du polymère, ce qui, dans certains cas, peut inclure une dispersion ou une émulsion stable dans l’eau. Par conséquent, l’utilisation d’une des techniques suivantes pour retirer les matières en suspension peut être envisagée (consulter la partie A9.2.4) :
- Centrifugation à basse vitesse : méthode jugée idéale si effectuée sur un laps de temps raisonnable (habituellement 2 heures ou moins), à une vitesse inférieure à celles employées en ultracentrifugation;
- Filtration : employer un filtre qui ne s’obstrue pas ou qui ne nécessite pas l’application d’une pression démesurée (les filtres dont les pores sont trop petits peuvent entraîner la séparation des fractions à masse moléculaire élevée ou la dégradation des polymères sous l’action des forces de cisaillement dans le filtre). Si le filtre s’obstrue, le filtrat obtenu ne sera pas représentatif de la disponibilité du polymère dans l’eau. L’encrassement du filtre réduit considérablement la taille des pores de celui-ci, ce qui invalide les résultats sur l’extractibilité dans l’eau. Si le filtre s’obstrue, la centrifugation devrait être utilisée.
A9.2.3 Analyse
La LD 120 de l’OCDE décrit uniquement une méthode d’analyse acceptable pour déterminer les composantes extractibles et propose différentes méthodes pour réaliser cette analyse. Le Programme des SN recommande l’utilisation de la chromatographie sur gel perméable (Gel Permeation Chromatography - GPC) en phase aqueuse, cette méthode d’analyse permettant d’établir une corrélation entre la masse moléculaire et la disponibilité dans l’eau et, ainsi, d’établir une distinction entre l’extractibilité des monomères n’ayant pas réagi et des additifs ou impuretés.
A9.2.4 Production de rapports
Le rapport d’analyse devrait inclure tous les renseignements nécessaires pour pouvoir théoriquement reproduire l’essai, notamment les suivants :
- Tous les renseignements disponibles sur l’échantillon d’essai (identité, additifs, impuretés, masse moléculaire);
- Des descriptions détaillées de la préparation des échantillons, des conditions expérimentales de l’essai et de l’analyse, y compris la vérification de l’applicabilité de la méthode d’analyse utilisée (si nécessaire);
- Le résultat de l’essai doit être rapporté en pourcentage de la concentration nominale (taux de charge) de la substance. Tous les calculs nécessaires pour parvenir à ce résultat doivent être consignés en détail;
- Tous les autres calculs et toute autre information ou observation importante pour l’interprétation du résultat doivent être fournies.
A9.3 Autres facteurs à considérer
A9.3.1 Polymères entièrement disponibles dans l’eau
Les polymères commercialisés sous la forme d’émulsions ou de dispersions et ceux pouvant former des émulsions ou des dispersions stables sont considérés comme 100 % disponibles dans l’eau. Il n’est donc pas nécessaire de présenter des renseignements sur l’extractibilité dans l’eau pour ces polymères. Il faut toutefois clairement indiquer à la case B.1 du formulaire de Déclaration de substances nouvelles que le polymère est à 100 % disponible dans l’eau en cochant la case à cet effet. De plus, les exigences du Règlement relativement à la présentation des résultats des essais sur l’écotoxicité, la biodégradation et l’hydrolyse continuent de s’appliquer.
A9.3.2 Polymères tensioactifs ou dispersés dans l’eau
Dans certains cas, les polymères tensioactifs peuvent former des dispersions (polymères solides) ou des émulsions (polymères liquides) colloïdales.
Aucune donnée sur l’extractibilité dans l’eau n’est exigée dans le cas des polymères tensioactifs et des polymères formulés dans l’eau et commercialisés comme tels, parce qu’on s'attend à ce qu'ils soient totalement disponibles dans l’eau. Les exigences de déclaration applicables à ce type de polymères sont examinées à la partie A9.3.1.
A9.3.3 Dérogation aux exigences relatives à l’extractibilité dans l’eau
Si un polymère est considéré comme entièrement disponible dans l’eau (consulter la partie A9.3.1), il suffit de produire une déclaration à cet effet pour satisfaire à l’exigence relative à l’extractibilité dans l’eau. Aucune demande de dérogation n’est requise.
Une telle demande n’est pas non plus nécessaire si des données sont présentées sur une substance de remplacement ou de substitution.
Si la demande de dérogation aux exigences relatives aux essais sur l’extractibilité dans l’eau est acceptée et que le pourcentage d’extractibilité du polymère à déclarer demeure inconnu, les exigences du Règlement relativement à la présentation des données des essais sur l’écotoxicité, la biodégradation et l’hydrolyse continuent de s’appliquer.
A9.3.4 Analyse de polymères hydroréactifs
Les polymères qui renferment des groupes fonctionnels hydroréactifs, comme les isocyanates et les alkoxysilanes, peuvent être préoccupants. Par conséquent, si ces groupes fonctionnels réactifs sont présents dans des proportions qui dépassent les seuils définis à l’annexe 7 du Règlement, le polymère ne serait pas considéré comme un polymère à exigences réglementaires réduites (consulter la partie 3.3.1.5). Des renseignements sur le comportement du polymère dans l’eau sont nécessaires pour mener une évaluation et les déclarants doivent fournir des données sur l’extractibilité dans l’eau conformément aux annexes 10 ou 11 du Règlement.
Il est généralement admis que les polymères qui renferment des groupes fonctionnels hydroréactifs, comme les isocyanates et les alkoxysilanes, subissent une hydrolyse. L’hydrolyse peut être suivie d’une réaction d’autocondensation qui peut entraîner une augmentation de la masse moléculaire et une réduction de la solubilité du polymère. Le taux d’hydrolyse, le risque d’autocondensation et la solubilité de la substance en résultant dépendent toutefois des caractéristiques structurales de chaque polymère.
Il est également reconnu que l’hydrolyse et le risque de réaction d’autocondensation peuvent réduire la capacité de réaliser des essais en milieu aqueux (par exemple les essais sur l’écotoxicité). Pour ces raisons, le Règlement a été libellé de manière à prévoir une exemption de certaines exigences en matière d’essais (par exemple hydrolyse, biodégradation, écotoxicité) pour les polymères peu extractibles dans l’eau.
Pour qu’une telle exemption soit accordée, le Règlement exige la présentation de données sur l’extractibilité dans l’eau. Le Programme des SN recommande que l’essai sur l’extractibilité dans l’eau soit mené conformément à la LD 120 de l’OCDE. Même si la conduite d’essais sur l’extractibilité dans l’eau peut poser certaines difficultés dans le cas de polymères hydroréactifs, la LD 120 de l’OCDE propose une méthode jugée la plus utile pour obtenir des renseignements significatifs aux fins de l’évaluation de ces polymères.
Les données sur l’extractibilité dans l’eau fournissent des preuves directes sur la solubilité d’un polymère et permettront de déterminer si d’autres essais sont nécessaires :
- Si l’extractibilité dans l’eau est supérieure à 2 %, le polymère doit faire l’objet d’essais d’écotoxicité, de biodégradation et d’hydrolyse requis par le Règlement;
- Si l’extractibilité dans l’eau est inférieure ou égale à 2 %, le polymère à déclarer n’a pas à faire l’objet d’essais d’écotoxicité, de biodégradation et d’hydrolyse requis par le Règlement.
De façon générale, l’essai d’extractibilité dans l’eau du polymère à déclarer est celui qui permet le mieux de satisfaire aux exigences relatives à l’analyse des polymères hydroréactifs. L’extractibilité dans l’eau peut aussi être déterminée par d’autres méthodes (consulter la partie 8.4) ou faire l’objet d’une dérogation (consulter la partie 8.7). Si une demande de dérogation est présentée, il ne suffit pas d’alléguer que le polymère réagit fortement avec l’eau et qu’il est transformé en un polymère réticulé à très haute masse moléculaire pusique les taux d’hydrolyse et d’autocondensation dépendent des caractéristiques structurales de chaque polymère. La demande de dérogation doit être accompagnée d’une justification scientifique bien documentée qui inclut des renseignements à l’appui (par exemple des données empiriques ou de substitution) démontrant la réactivité dans l’eau et le comportement de condensation.
En cas de doute, les déclarants devraient communiquer avec le Programme des SN par la présentation d’une demande de Consultation avant déclaration (consulter la partie 8.8), pour connaître la stratégie d’analyse convenant le mieux pour des polymères hydroréactifs.
Appendice 10. Évaluation des nanomatériaux dans le cadre du Programme des substances nouvelles
Les nanomatériaux ont habituellement un rapport surface/volume plus élevé que les formes non nanométriques de ces substances, ce qui peut leur conférer une plus forte réactivité. Ils peuvent aussi présenter des changements dans leurs propriétés chimiques et physiques qui sont impossibles à prévoir par extrapolation à partir de leurs formes non nanométriques. Ces différences peuvent avoir des répercussions sur les risques pour la santé humaine ou l’environnement que peuvent présenter une substance.
Conformément à la Recommandation de 2013 du Conseil de l’Organisation de coopération et de développement économiques (OCDE),Note de bas de page 19 le Canada utilise son cadre actuel de réglementation des substances chimiques pour gérer les nanomatériaux en l’adaptant au besoin pour tenir compte des propriétés particulières des nanomatériaux.
Comme il n’existe pas de définition réglementaire alignée à l’échelle internationale, le Programme des substances nouvelles (SN) se fonde sur la Définition ad hoc de nanomatériaux de Santé Canada : « 1) avoir une ou plusieurs dimensions (structure interne ou en surface) à l’échelle nanométrique (de 1 à 100 nanomètres inclusivement); ou 2) présenter des phénomènes ou des propriétés à l’échelle nanométrique situés au-dessus ou en-dessous de cette échelle immédiatement ».
Le Programme des SN peut demander la présentation de renseignements sur la taille des particules primaires et la distribution granulométrique afin de déterminer si une substance déclarée est à l’échelle nanométrique. Diverses méthodes, fondées sur différents principes physiques, sont disponibles pour mesurer la taille des particules primaires et la distribution granulométrique.Note de bas de page 20
Si les renseignements sur la taille des particules primaires et la distribution granulométrique ne sont pas indiqués et que le Programme des SN croit que la substance pourrait être un nanomatériau, la substance sera traitée comme un nanomatériau potentiel. L’information obtenue permettra de mieux reconnaître les nouveaux nanomatériaux, ce qui favorisera une évaluation des risques mieux éclairée et, s’il y a lieu, l’adoption de mesures de gestion plus appropriées. Bien que le Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) précise les renseignements qui doivent être communiqués au Programme des SN, il exige aussi généralement la présentation de tous les autres renseignements et données d’essai dont dispose le fabricant ou l’importateur ou auxquels le fabricant ou l’importateur peut normalement avoir accès.
Le Programme des SN pourrait recommander la présentation de renseignements supplémentaires pour tenir compte des propriétés spécifiques aux nanomatériaux. Ces renseignements pourraient inclure les suivants, mais sans s’y limiter :
- Les propriétés physico-chimiques propres à chaque nanomatériau, incluant l’état d’agglomération ou d’agrégation, la forme, la surface active, la fonctionnalisation de surface, le revêtement de surface et la charge superficielle, etc. de la substance;
- Potentiel de libération de la substance à partir d’un produit final;
- Les données et les rapports d’analyse sur l’écotoxicité (par exemple toxicité dans le sol);
- Les essais de toxicité pour les mammifères par inhalation (essai de toxicité aiguë et essai de toxicité de doses répétées) menés conformément aux Lignes directrices (LD) révisés de l’OCDE. Une révision du document Guidance Document on Inhalation Toxicity Studies [PDF] de l’OCDE (en anglais seulement) et des mises-à-jour sur les méthodes d’essai de toxicité par inhalation (LD 412Note de bas de page 21 et 413Note de bas de page 22) adressent les problèmes spécifiques aux nanomatériaux et sont disponibles en ligne.
Bien que cela ne soit pas obligatoire, les déclarants sont encouragés à présenter une demande de Consultation avant déclaration (consulter la partie 8.8) lors de la préparation de leur Déclaration de substances nouvelles pour obtenir des conseils sur les considérations propres aux nanomatériaux (par exemple sur la présentation de données supplémentaires à l’appui de l’évaluation des risques) et sur les méthodes d’essai.
Appendice 11. Accords internationaux
Les accords internationaux en vigueur évoluent constamment. Les renseignements les plus à jour se trouvent sur notre site Web Substances nouvelles : coopération internationale, substances chimiques et polymères.
Appendice 12. Parties de la Liste intérieure et de la Liste extérieure
La Liste intérieure
La Liste intérieure (DORS/94-311) est une liste de substances commercialisées au Canada, initialement publiée dans la Partie II de la Gazette du Canada en mai 1994. La structure courante de la Liste intérieure a été établie en 2001 [Arrêté 2001-87-04-01 modifiant la Liste intérieure (DORS/2001-214) [PDF]], et modifiée en 2012 [Arrêté 2012-87-09-01 modifiant la Liste intérieure (SOR/2012-229)]. La Liste intérieure est modifiée en moyenne 12 fois par année afin d’y inscrire, mettre à jour ou radier des substances.
La Liste intérieure est composée des 8 parties suivantes :
- Partie 1 : Substances chimiques et polymères non visés aux parties 2, 3 ou 4 et désignés par leur numéro d’enregistrement du Chemical Abstracts Service (CAS) ou par leur numéro d’identification de substance attribué par le ministère de l’Environnement et leur dénomination spécifique.
- Partie 2 : Substances chimiques et polymères visés par des exigences relatives aux nouvelles activités (NAc) qui sont désignés par leur numéro d’enregistrement CAS.
- Partie 3 : Substances chimiques et polymères non visés à la partie 4 et désignés par leur dénomination maquillée et leur numéro d’identification confidentielle (NIC) attribué par le ministère de l’Environnement.
- Partie 4 : Substances chimiques et polymères visés par des exigences relatives aux NAc qui sont désignés par leur dénomination maquillée et leur NIC.
- Partie 5 : Produits biotechnologiques inanimés ou organismes vivants non visés aux parties 6, 7 ou 8 et désignés par leur numéro de l’American Type Culture Collection (ATCC), leur numéro de l’Union internationale de biochimie et de biologie moléculaire (UIBBM) ou par leur dénomination spécifique.
- Partie 6 : Produits biotechnologiques inanimés ou organismes vivants visés par des exigences relatives aux NAc qui sont désignés par leur numéro de l'ATCC, leur numéro de l'UIBBM ou par leur dénomination spécifique.
- Partie 7 : Produits biotechnologiques inanimés ou organismes vivants non visés à la partie 8 et désignés par leur dénomination maquillée et leur NIC.
- Partie 8 : Produits biotechnologiques inanimés ou organismes vivants visés par des exigences relatives aux NAc qui sont désignés par leur dénomination maquillée et leur NIC.
Pour une description complète des mentions spéciales pouvant apparaître sur la liste après l’identifiant d’une substance, consulter la partie 2.1.4.
La Liste extérieure
La Liste extérieure est une liste de substances trouvées dans le commerce international, initialement publiée dans la Partie I de la Gazette du Canada en janvier 1998 (volume 132, nº 5) [PDF]. La Liste extérieure est modifiée en moyenne 12 fois par année afin d’y inscrire, mettre à jour ou radier des substances.
La Liste extérieure est composée des 4 parties suivantes :
- Partie 1 : Substances chimiques et polymères non visés à la partie 2 et désignés par leur numéro d’enregistrement CAS.
- Partie 2 : Substances chimiques et polymères désignés par leur dénomination maquillée en conformité avec le Règlement sur les dénominations maquillées et par leur NIC attribué par le ministère de l’Environnement.
- Partie 3 : Enzymes non visées à la partie 4 et désignées par leur numéro d’identification de l’UIBBM.
- Partie 4 : Enzymes désignées par leur dénomination maquillée en conformité avec le Règlement sur les dénominations maquillées et par leur NIC attribué par le ministère de l’Environnement.
Pour déterminer si une substance figure sur la Liste intérieure ou sur la Liste extérieure, on peut entrer le nom de la substance, son numéro d’enregistrement CAS, son NIC (s’il est connu) ou son numéro d’identification de l’UIBBM dans le Moteur de recherche de substances.
Appendice 13. Glossaire, abréviations et acronymes
A13.1 Glossaire
Acceptable dans le cadre du Programme des substances nouvelles (SN), en ce qui concerne les méthodes, s’entend d’une méthode qui permet d’obtenir des données d’une quantité et d’une qualité suffisantes pour que le Programme des SN puisse faire une évaluation significative du paramètre à l’étude. Parmi les aspects importants de la méthode dont il faut tenir compte, mentionnons l’emploi d’étalons et de témoins, les limites de détection, les espèces choisies, les tissus étudiés, les doses, le respect des Bonnes pratiques de laboratoire ainsi que la validation et la puissance statistique de la méthode (consulter aussi Indicateur de mutagénicité).
Adéquatement confinée s'entend d’une substance pour laquelle toutes les précautions et mesures nécessaires ont été mises en place pour en prévenir le rejet dans l’environnement. En ce qui a trait au transport d’une substance, s’entend du respect intégral de la Loi sur le transport des marchandises dangereuses (consulter aussi Confinée).
Agent canadien s'entend d'un agent désigné lorsque le déclarant qui fournit les renseignements exigés en vertu du Règlement n’est pas un résident du Canada. Conformément à l’alinéa 14(1)b) du Règlement, le déclarant doit désigner une personne résidant au Canada autorisée à agir en son nom à titre d’ « agent canadien ». L’ « agent canadien » reçoit les avis et la correspondance concernant la Déclaration de substances nouvelles (DSN) et conserve une copie de la DSN, ainsi que de toute la correspondance et de toutes les données à l’appui s’y rapportant, durant une période de 5 ans suivant la fin de l’année de leur communication (consulter l’article 13 du Règlement). L’ « agent canadien » doit s’assurer de l’exactitude et de l’exhaustivité des renseignements présentés dans la DSN.
Animal s'entend de toute partie d’un animal. La présente définition exclut ce qui existe essentiellement sous forme de cellule unique sans l’organisation type des tissus et des organes.
Auxquels elle peut normalement avoir accès s'entend de renseignements se trouvant dans n’importe quel bureau de l’entreprise partout dans le monde ou dans un autre endroit où la personne peut y avoir accès (consulter aussi Dont dispose la personne qui fabrique ou importe).
Biopolymère s'entend d'un polymère qui provient d’un micro-organisme vivant ou qui est une protéine ou un acide nucléique provenant de végétaux ou d’animaux (consulter aussi organisme vivant et micro-organisme).
Biotechnologie s'entend de l'application de la science et de l’ingénierie à l’utilisation directe ou indirecte d’organismes vivants, ou de parties ou de produits de ces organismes, dans leur forme naturelle ou sous une forme modifiée.
Confinée s'entend d'une substance intermédiaire limitée au site ou une substance destinée à l’exportation ayant une limite absolue de rejet dans le milieu aquatique de 1 kg par jour par site, après le traitement des eaux usées.
Consommée s'entend d'une substance détruite ou complètement transformée en une autre substance.
Délai d'évaluation s'entend du nombre de jours civils dont dispose le gouvernement pour évaluer les renseignements fournis par un déclarant en vertu du Règlement.
Dénomination maquillée s’entend d’un nom basé sur la nomenclature du Chemical Abstracts Service (CAS), de l’Union internationale de chimie pure et appliquée (UICPA) ou de l’Union internationale de biochimie et de biologie moléculaire (UIBBM) dont un ou plusieurs composants sont identifiés d’une manière qui empêche l’identification de la structure chimique précise de la substance. Le maquillage de la dénomination d’une substance n’est acceptable que dans la mesure nécessaire pour maquiller l’identité complète de la substance, tout en conservant sa structure moléculaire générique. Les substances publiées sous une dénomination maquillée sont désignées par leur numéro d’identification confidentielle.
Destinée à la recherche et au développement s'entend d’une substance faisant l’objet d’investigations ou de recherches systématiques, par voie d’expérimentation ou d’analyse, à l’exclusion des tests de marché, le principal objectif des investigations et des recherches étant l’un ou l’autre des objectifs suivants :
- a) la création ou l’amélioration d’un produit ou d’un procédé;
- b) la détermination de la viabilité technique ou des caractéristiques de rendement d’un produit ou d’un procédé;
- c) l’évaluation de la substance avant sa commercialisation au moyen d’essais pilotes en usine, d’essais de production, y compris la production à grande échelle, ou d’essais individualisés en usine de sorte que les spécifications techniques puissent être adaptées aux exigences de rendement de clients éventuels. (consulter aussi Test de marché).
Données établissant que le tissu en question a été exposé à la substance ou à ses métabolites s'entend de données nécessaires, en ce qui concerne l'essai de mutagénicité in vivo prescrit aux annexes 6 et 11 du Règlement, pour déterminer s'il est approprié d'utiliser le ou les tissus analysés pour l’évaluation de la mutagénicité in vivo d’une substance et, par conséquent, la pertinence de l’essai. Cette disposition indique que des renseignements suffisants sont nécessaires pour appuyer une conclusion selon laquelle le tissu analysé a été exposé à la substance à l’étude ou à ses métabolites. La solidité des données exigées sera déterminée en fonction du pouvoir mutagène de la substance, notamment des résultats des essais de mutagénicité in vitro, de la structure de la substance, du risque d’exposition, des tissus analysés et de la méthode d’essai. Voici quelques exemples de données pouvant établir l’exposition des tissus :
- Un résultat positif à l’évaluation d’un paramètre dans le tissu étudié;
- Une cytotoxicité observée dans le tissu étudié, par exemple une réduction statistiquement significative de l’indice mitotique, un délai du cycle cellulaire, une diminution de la proportion érythrocytes polychromatiques par rapport aux érythrocytes normochromatiques;
- Une toxicité organique générale dans le tissu étudié, par exemple une modification importante du poids de l’organe ou une hyperplasie;
- Des données provenant d’une étude de distribution du tissu, indiquant la présence de la substance ou de ses métabolites dans le tissu étudié.
Dont dispose la personne qui fabrique ou importe s'entend des renseignements qui se trouvent dans les bureaux de l’entreprise au Canada si la Déclaration de substances nouvelles (DSN) a été présentée par une entreprise canadienne ou les renseignements qui se trouvent dans les bureaux du pays d’où provient la déclaration si la DSN a été présentée par une entreprise étrangère par l’intermédiaire d’un « agent canadien » (consulter aussi Auxquels elle peut normalement avoir accès).
Estimation croisée s'entend de l'estimation qualitative d’une propriété d’une substance basée sur des données expérimentales portant sur un ou plusieurs autres composés dont la structure chimique est étroitement apparentée.
Exposition directe du public s’entend du fait d’être exposé, sciemment ou non, à une substance à la suite d’un contact cutané, par inhalation ou par voie orale avec la substance durant l’utilisation finale du produit (par exemple dans un produit de consommation). Cette exposition diffère de l’exposition indirecte, qui se produit par contact fortuit avec la substance dans un milieu environnemental suite à son rejet au cours d’une ou plusieurs étapes de son cycle de vie (fabrication, transformation, manutention, entreposage, transport, élimination), excluant les utilisations finales des produits de consommation. Dans le cadre du Règlement, l’exposition directe et indirecte s’entendent d’une exposition de la population générale du Canada.
Fabricant en sous-traitance s'entend de la personne qui fabrique réellement la substance, que cette activité soit faite moyennant une redevance ou au bénéfice du déclarant.
Intermédiaire de réaction non isolé s'entend d'une substance formée et consommée au cours d’une réaction chimique.
Fiche de données de sécurité s’entend d’une fiche signalétique, au sens de l’article 2 de la Loi sur les produits dangereux, à l’égard d’une substance.
Groupe fonctionnel réactif s'entend d'atomes ou groupe d’atomes associés d’une substance qui sont destinés à entrer facilement en réaction ou qui pourraient vraisemblablement entrer facilement en réaction.
Importateur ou importateur officiel s'entend de la personne important la substance et identifiée comme telle sur la Déclaration en détail commerciale délivrée par l’Agence des services frontaliers du Canada.
Impureté s'entend d'un substance dont la présence dans une autre substance n’est pas intentionnelle, n’est pas nécessaire à l’utilisation finale du produit et n’améliore pas la valeur commerciale de ce dernier.
Indicateur de mutagénicité s'entend d'essais, aux fins de l’évaluation du pouvoir mutagène in vitro ou in vivo, qui sont « acceptables dans le cadre du Programme des substances nouvelles » pour déterminer le pouvoir mutagène in vitro ou in vivo de la substance. Cette formulation vise à permettre le choix du ou des essais les mieux appropriés pour une substance et à ce que les progrès dans le domaine de la génotoxicité puissent rapidement être intégrés à la stratégie d’analyse. Il est recommandé que le chercheur consulte les représentants de Santé Canada avant de déterminer l’acceptabilité d’un essai pour une substance donnée (consulter aussi Acceptable dans le cadre du Programme des substances nouvelles).
Intermédiaire limitée au site s'entend d'une substance consommée dans une réaction chimique servant à la fabrication d’une autre substance et qui est :
- a) soit fabriquée et consommée dans le site de fabrication;
- b) soit fabriquée dans un site et transportée à un second site où elle sera consommée;
- c) soit importée et transportée directement au site où elle sera consommée.
Liste extérieure s'entend de la liste établie par le ministre de l’Environnement en application du paragraphe 66(2) de la Loi, avec ses modifications successives apportées par le ministre afin d’y inscrire, mettre à jour ou radier des substances (consulter aussi Liste intérieure).
Liste intérieure s'entend de la liste établie par le ministre de l’Environnement en application du paragraphe 66(1) de la Loi, avec ses modifications successives apportées par le ministre afin d’y inscrire, mettre à jour ou radier des substances (consulter aussi Liste extérieure).
Loi s'entend de la Loi canadienne sur la protection de l’environnement (1999).
Micro-organisme s'entend d'un organisme microscopique qui, selon le cas :
- a) appartient à la famille des bactéries, des archéobactéries, des protistes, y compris les protozoaires et les algues, ou des champignons dont les levures;
- b) est un virus, une particule de type virus ou une particule sous-virale;
- c) est une cellule cultivée d’un organisme non mentionné aux alinéas a) et b), à l’exclusion d’une cellule utilisée pour la multiplication de cet organisme;
- d) est une culture autre qu’une culture pure.
Ministre s'entend du ministre de l’Environnement, alors que les ministres désignent le ministre de l’Environnement et le ministre de la Santé.
Mode d’exposition le plus probable du public s’entend de l’exposition de la population générale du Canada. Pour choisir le ou les modes d’exposition convenant le mieux à l’essai, il faut prendre en considération la concentration prévue de la substance déclarée dans les divers milieux naturels et produits de consommation et la biodisponibilité de la substance par ingestion, inhalation et absorption par voie cutanée. Le mode d’exposition le plus probable à une substance pour la population en général peut différer des modes d’exposition des travailleurs en milieu de travail. Par conséquent, les données sur l’exposition professionnelle pourraient ne pas satisfaire aux exigences relatives au mode potentiel d’exposition le plus probable du public selon le Règlement.
Numéro d’enregistrement du Chemical Abstracts Service s'entend du numéro d’identification qui est attribué à une substance par la Chemical Abstracts Service Division de l’American Chemical Society.
Organisme vivant s’entend d’une substance biotechnologique animée et fait référence à des micro-organismes ou à des organismes autres que les micro-organismes.
Organisme de production s’entend d’un organisme vivant servant à la production d’une substance biochimique ou d’un biopolymère. Un organisme de production peut être assujetti au Règlement sur les renseignements concernant les substances nouvelles (organismes) s’il satisfait à la définition d’un organisme vivant énoncé à l’article 104 de la Loi et s’il ne figure pas sur la Liste intérieure. Voici des exemples d’organismes de production :
- Bacillus subtilis produisant une subtilisine;
- Saccharomyces fragilis produisant une lactase;
- Aspergillus flavus produisant une glucosidase.
Personne s'entend des personnes physiques ou morales, comme les résidents ou les entreprises du Canada.
Polymère s'entend d'une substance constituée de :
- a) molécules caractérisées par l’enchaînement d’au moins un type d’unité monomère;
- b) plus de 50 %, en masse, de molécules contenant au moins trois unités monomères liées par covalence à au moins une autre unité monomère ou à un autre réactif;
- c) moins de 50 %, en masse, de molécules de même masse moléculaire;
- d) molécules distribuées à l’intérieur d’un intervalle de masses moléculaires et dont la différence de masse moléculaire est attribuée essentiellement à des différences dans le nombre d’unités monomères. (consulter aussi Unité monomère, Réactif).
Polymère à exigences réglementaires réduites s'entend de l’un ou l’autre des polymères visés à l’article 9 du Règlement.
Polymère et biopolymère anionique s'entend d’un polymère renfermant une ou plusieurs unités monomères liées par covalence qui portent une charge négative nette (consulter aussi Unité monomère, Polymère).
Polymère/biopolymère amphotère s'entend d'un polymère renfermant des unités monomères liées par covalence et portant à la fois une charge négative et positive (consulter aussi Unité monomère, Polymère).
Polymère/biopolymère cationique s'entend d’un polymère renfermant une ou plusieurs unités monomères liées par covalence qui portent une charge positive nette (consulter aussi Unité monomère, Polymère).
Quantité seuil s’entend de la quantité d’une substance fabriquée ou importée qui, si elle est dépassée, exige la production d’une Déclaration de substances nouvelles par le déclarant. À titre d’exemple, dans le cas d’une substance chimique ou biochimique figurant sur la Liste extérieure, la quantité seuil exigeant la production d’une déclaration au titre de l’annexe 4 est de 1 000 kg/an.
Réactif s'entend d'une substance utilisée dans la fabrication d’un polymère pour faire partie intégrante de la composition chimique du polymère. La présente définition comprend les monomères.
Règlement s’entend du Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères) de la Loi canadienne sur la protection de l’environnement (1999).
Sous-produit s'entend d'une substance produite sans intention commerciale distincte durant la fabrication d’une autre substance.
Substance est définie au paragraphe 3(1) et à l’article 80 de la Loi comme suit :
- Toute matière organique ou inorganique, animée ou inanimée, distinguable. La présente définition vise notamment :
- a) les matières susceptibles soit de se disperser dans l’environnement, soit de s’y transformer en matières dispersables, ainsi que les matières susceptibles de provoquer de telles transformations dans l’environnement;
- b) les radicaux libres ou les éléments;
- c) les combinaisons d’éléments à l’identité moléculaire précise soit naturelles, soit consécutives à une réaction chimique, mais qui ne pourraient se former dans la pratique par la simple combinaison de leurs composants individuels;
- d) des combinaisons complexes de molécules différentes, d’origine naturelle ou résultant de réactions chimiques, mais qui ne pourraient se former dans la pratique par la simple combinaison de leurs composants individuels.
- aux fins des dispositions de la Loi qui portent sur les substances nouvelles (par exemple, articles 66 et 80 à 89 visant les substances chimiques et polymères), cette définition exclut :
- e) les mélanges combinant des substances et ne produisant pas eux-mêmes une substance différente de celles qui ont été combinées;
- f) les articles manufacturés dotés d’une forme ou de caractéristiques matérielles spécifiques pendant leur fabrication et qui ont, pour leur utilisation finale, une ou plusieurs fonctions en dépendant en tout ou en partie;
- g) les matières animées ou les mélanges complexes de molécules différentes qui sont contenus dans les effluents, les émissions ou les déchets attribuables à des travaux, des entreprises ou des activités.
Substance biochimique s'entend d'une substance chimique qui provient d’un micro-organisme vivant ou qui est une protéine ou un acide nucléique provenant de végétaux ou d’animaux (consulter aussi organisme vivant et micro-organisme). Remarque : Les micro-organismes morts sont considérés comme des substances biochimiques.
Substance chimique s'entend d'une substance autre qu’un organisme vivant ou un polymère (consulter aussi substance)
Substance destinée au développement de produits s'entend d'une substance destinée à la recherche et au développement qui est évaluée dans le cadre d’un programme d’au plus 2 ans avant sa commercialisation complète, au moyen d’essais pilotes en usine, d’essais de production ou d’essais de consommation, excluant les tests de marché, en vue d’en modifier les spécifications techniques en réponse aux exigences de rendement de clients potentiels (consulter aussi Destinée à la recherche et au développement, test de marché).
Substance existant à l’état naturel s’entend d’une substance qui existe naturellement et qui n’est pas traitée ou qui est uniquement traitée par des procédés manuels, gravitationnels ou mécaniques, par dissolution dans l’eau, par flottation ou par chauffage à la seule fin d’éliminer l’eau ou qui est extraite de l’air par tout procédé.
Substances nouvelles s'entend de substances qui ne figurent pas actuellement sur la Liste intérieure et qui sont considérées comme nouvelles au Canada. Une réglementation a été créée pour s’assurer qu’aucune substance nouvelle (substances chimiques, polymères ou substance biotechnologique animée) n’est introduite sur le marché canadien avant que son risque de toxicité n’ait été évalué et que les mesures de gestion requises ou appropriées, le cas échéant, n’aient été prises (consulter aussi substance).
Test de marché s'entend de l’étude des possibilités de mise en marché d’un produit en situation de concurrence lorsque la création ou l’amélioration du produit n’est pas le principal objectif (consulter aussi Destinée à la recherche et au développement).
Tiers fournisseur de renseignements est un terme utilisé lorsque le déclarant n’a pas accès à des renseignements jugés confidentiels par le tiers. Le tiers doit fournir directement au Programme des substances nouvelles les renseignements exigés à l’appui de la Déclaration de substances nouvelles; ces renseignements formeront la « déclaration du Tiers fournisseur de renseignements». Les Tiers fournisseur de renseignements incluent les fournisseurs étrangers; un Tiers fournisseur de renseignements peut être basé au Canada ou ailleurs.
Unité monomère s'entend de la forme dérivant de la réaction d’un monomère dans un polymère (consulter aussi Polymère).
UVCB est l'acronyme décrivant les substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques (substances of Unknown or Variable composition, Complex reaction products or Biological materials). Ces matières sont dérivées de sources naturelles ou de réactions complexes et sont considérés comme des substances simples aux fins de la déclaration.
Végétaux s'entend de toute partie d'un végétal. La présente définition exclut ce qui existe essentiellement sous forme de cellule unique sans l’organisation typique des tissus et des organes.
A13.2 Liste des abréviations et acronymes
- %m
pourcentage massique
- AICIS
Système australien d’introduction des produits chimiques industriels (Australian Industrial Chemicals Introduction Scheme)
- amine
amine cationique
- AR
agent de ramification
- ASTM
Société américaine pour les essais et les matériaux (American Society for Testing and Materials)
- BPL
Bonnes pratiques de laboratoire
- CAD
Consultation avant déclaration
- CAS
Chemical Abstracts Service
- CCHST
Centre canadien d’hygiène et de sécurité au travail
- CE50
concentration médiane effective
- CL50
concentration médiane létale
- CMEO
concentration minimale avec effet observé
- comb
combiné
- CSEO
concentration sans effet observé
- DCI
Dénominations communes internationales
- DL50
dose médiane létale
- DNAc
Déclaration de nouvelle activité
- DSN
Déclaration de substances nouvelles
- ECHA
Agence européenne des produits chimiques (European Chemicals Agency)
- EE
efficacité d’élimination
- EINECS
Inventaire européen des substances chimiques commerciales existantes (European Inventory of Existing Commercial Substances)
- ELINCS
Liste européenne des substances chimiques déclarées (European List of Notified Chemical Substances)
- EPR
Entente de partage de renseignements
- ERR
polymères à exigences réglementaires réduites
- ELGL
Essai de stimulation locale des ganglions lymphatiques
- FIFRA
Federal Insecticide, Fungicide, and Rodenticide Act
- GFT
groupe fonctionnel terminal
- GIGU
Gestion de l'information du guichet unique
- GPC
chromatographie sur gel perméable (Gel Permeation Chromatography)
- INCI
Nomenclature internationale des ingrédients cosmétiques (International Nomenclature Cosmetic Ingredient)
- IR
Infrarouge
- ISO
Organisation internationale de normalisation
- JRM
nombre de jours de rejets par mois
- la Loi
Loi canadienne sur la protection de l’environnement (1999)
- LAD
Loi sur les aliments et drogues
- LD
Ligne directrice
- le ministre
le ministre de l’Environnement
- le Règlement
Règlement sur les renseignements concernant les substances nouvelles (substances chimiques et polymères)
- les ministres
le ministre de l’Environnement et le ministre de la Santé
- MALLS
diffusion d’une lumière laser multi-angles (Multi Angle Laser Light Scattering)
- MALS
diffusion de la lumière multi-angles (Multi Angle Light Scattering)
- MEGF
masse équivalente du groupe fonctionnel
- MEGFn
calcul individuel de la masse équivalente du groupe fonctionnel (n = 1, 2, 3,…)
- mm
masse moléculaire
- mm KOH
masse moléculaire de KOH = 56,1 g/mol
- Mn
masse moléculaire moyenne en nombre
- mon
monomère
- MP
masse moléculaire du plus haut pic
- Mw
masse moléculaire moyenne en poids
- Mz
masse moléculaire moyenne z
- NAc
nouvelle activité
- NAM
Nouvelles approches méthodologiques
- nGF
nombre de groupes fonctionnels disponibles
- nGT
nombre de groupes terminaux
- NIC
numéro d’identification confidentielle
- NLP
Polymères qui ne sont plus considérés comme des polymères (No-Longer Polymers)
- non-ERR
polymères qui ne sont pas des polymères à exigences réglementaires réduites
- nSR
nombre de sites réactifs
- OCDE
Organisation de coopération et de développement économiques
- PCPC
Conseil des produits de soins personnels (Personal Care Products Council)
- PL
polymère linéaire
- PR
polymère ramifié
- Programme des SN
Programme des substances nouvelles
- QMRF
Modèle de rapport de modèle RQSA (QSAR Model Reporting Format)
- QPRF
Modèle de rapport de prédiction de RQSA (QSAR Prediction Reporting Format)
- QR
quantité rejetée
- RCC
Renseignements commerciaux confidentiels
- RDSN
Règlement sur les droits concernant les substances nouvelles
- RMN
Résonance magnétique nucléaire
- RQmoy mens
rejets quotidiens dans l’environnement aquatique basés sur une moyenne mensuelle
- RQSA
relation quantitatives structure-activité
- RTECS
Registre des effets toxiques des substances chimiques (Registry of Toxic Effects of Chemical Substances)
- SCIAN
Système de classification des industries de l'Amérique du Nord
- SEC
chromatographie d’exclusion stérique (Size-exclusion Chromatography)
- TSCA
Toxic Substances Control Act
- UIBBM
Union internationale de biochimie et de biologie moléculaire
- UICPA
Union internationale de chimie pure et appliquée
- US EPA
Agence de protection environnementale des États-Unis (United States Environmental Protection Agency)
- USP
Pharmacopée des États-Unis (United States Pharmacopeia)
- UV
Ultraviolet
- UVCB
Substances de composition inconnue ou variable, produits de réaction complexes ou matières biologiques (substances of Unknown or Variable composition, Complex reaction products or Biological materials)
- Xamine
nombre de groupes amines, mg KOH/g de polymère