Traitement des plaintes relatives aux instruments médicaux (GUI-0065) : À propos des plaintes
Sur cette page
- Introduction
- Qu'est-ce qu'une plainte?
- Éléments clés pour traiter efficacement des plaintes
- Aperçu du processus
- Vos responsabilités
- Procédures écrites
Introduction
Le Règlement sur les instruments médicaux (le Règlement) exige que vous teniez des registres à l'égard des problèmes signalés sur le rendement ou la sûreté de votre instrument médical. Il vous invite également à :
- consigner la façon dont vous traitez ces problèmes;
- élaborer des procédures écrites relativement aux enquêtes sur les plaintes;
- vous assurez que vos procédures vous permettent de mener une enquête efficacement et rapidement.
Qu'est-ce qu'une plainte?
Une plainte allègue ou laisse entendre qu'un instrument médical comporte des lacunes sur le plan de son identification, de sa qualité, de sa durabilité, de sa fiabilité, de sa sûreté, de son efficacité ou de son rendement. Elle est portée après la mise en circulation d'un instrument pour la distribution ou la vente.
Une plainte peut être formulée par écrit ou verbalement et peut être soumise par télécopieur, courrier, courriel, téléphone, en personne ou sur un site Web. Elle peut provenir de différentes sources, notamment :
- des utilisateurs finaux;
- comme les patients, les consommateurs et les professionnels de la santé;
- des rapports provenant de représentants commerciaux ou de préposés au service, de la documentation scientifique, des documents juridiques ou d'analyses internes;
- des importateurs, des distributeurs et des détaillants;
- des associations médicales;
- des organismes de réglementation;
- comme Santé Canada;
- des demandes de réparation et des réclamations au titre de la garantie.
Les plaintes peuvent mener à des réparations, des entretiens ou des modifications au mode d'emploi du fabricant ou à un rappel. Elles comprennent les rapports d'incident ou les problèmes rapportés à l'égard d'un instrument médical incluant son étiquette ou son emballage.
Remarque : Les plaintes peuvent découler d'un retour de produit ou d'une demande de réparation sous garantie, et elles ne sont pas toujours identifiées comme telles au départ. Par conséquent, il est important de définir clairement ce qui constitue une plainte et ce qui n'en est pas une.
Éléments clés pour traiter efficacement des plaintes
Pour traiter efficacement les plaintes, vous devriez :
- disposer de procédures écrites quant à la documentation du processus de traitement des plaintes;
- avoir du personnel formé qui applique ces procédures et dispose des connaissances, de la formation et de l'expérience nécessaires pour remplir leurs fonctions;
- recueillir et filtrer les plaintes;
- évaluer les plaintes afin de déterminer si une enquête plus approfondie ou un rapport d'incident est nécessaire;
- établir les critères liés au risque pour la santé ainsi qu'un échéancier, fondé sur le niveau de risque, pour enquêter sur le problème;
- collaborer et diffuser rapidement, au sein de votre entreprise et avec les parties externes concernées, les renseignements liés à la sûreté et au rendement de l'instrument;
- les parties concernées peuvent comprendre le fabricant, l'importateur, le distributeur, les utilisateurs et l'autorité de réglementation;
- tenir des registres pour consigner la plainte ainsi que toutes les mesures prises en réponse à celle-ci ou les raisons pour lesquelles aucune mesure n'a été prise;
- rapporter à toutes les parties concernées à l'extérieur de l'entreprise, au besoin;
- analyser les tendances dans des rapports périodiques afin d'en faire un examen régulier.
Aperçu du processus
Les éléments clés d'un système efficace de traitement des plaintes sont intégrés dans un processus en cinq phases. Chaque phase comprend une série de démarches et de décisions à suivre, qui peuvent se chevaucher selon la situation.
La figure 1 illustre ces cinq phases.
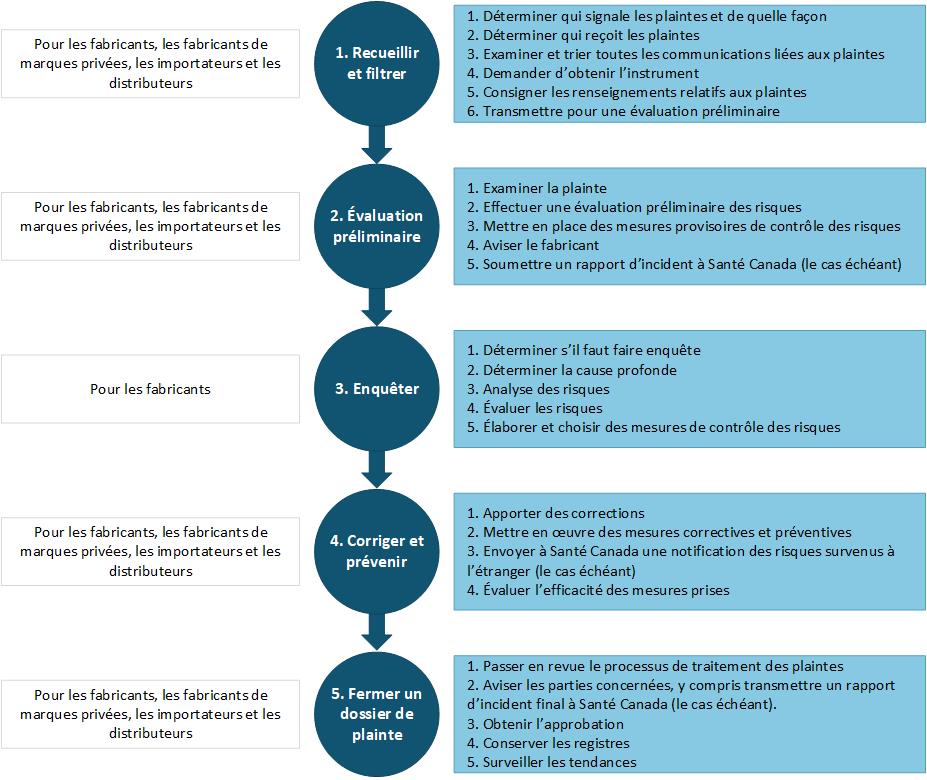
Figure 1: Description textuelle
Voici les étapes d'un processus en 5 phases pour la gestion des plaintes.
La phase 1 est intitulée « Recueillir et filtrer ». Elle s'adresse aux fabricants, fabricants de marques privées, importateurs et distributeurs. Cette phase comporte 6 étapes. La première étape vise à identifier qui signale les plaintes et de quelle façon elles sont signalées. La deuxième étape a pour objectif de déterminer qui reçoit les plaintes dans l'entreprise. La troisième étape consiste à examiner et trier toutes les communications liées aux plaintes. La quatrième étape concerne la demande de l'instrument impliqué dans la plainte. La cinquième étape porte sur la documentation relatifs aux plaintes. La sixième étape prévoit le transfert de la plainte pour une évaluation préliminaire.
La phase 2 est intitulée « Évaluation préliminaire ». Elle s'adresse aux fabricants, fabricants de marques privées, importateurs et distributeurs. Cette phase est organisée en 5 étapes. Elle débute par l'examen de la plainte. La deuxième étape concerne l'évaluation préliminaire des risques. La troisième étape prévoit la mise en place des mesures provisoires de contrôle des risques afin de réduire le(s) risque(s). La quatrième étape implique d'aviser le fabricant de la plainte. La cinquième étape correspond à l'envoi d'un rapport d'incident à Santé Canada, le cas échéant.
La phase 3 est intitulée « Enquêter ». Elle s'adresse aux fabricants. Cette phase implique 4 étapes. La première étape a pour objectif de décider s'il faut enquêter sur la plainte. La deuxième étape vise à déterminer la cause profonde. La troisième étape vise l'analyse du risque posé par le problème, suivie de la quatrième étape qui prévoit l'évaluation du risque. La cinquième étape consiste à élaborer et à choisir des mesures de contrôle des risques.
La phase 4 est intitulée « Corriger et prévenir ». Elle s'adresse aux fabricants, aux fabricants de marques privées, aux importateurs et aux distributeurs. Cette phase comprend 4 étapes. La première étape consiste à apporter rapidement des corrections. La deuxième étape prévoit la mise en œuvre des mesures correctives et préventives. La troisième étape consiste à envoyer à Santé Canada une notification des risques survenus à étranger, le cas échéant. La quatrième étape demande d'évaluer l'efficacité des mesures prises.
La phase 5 est intitulée « Fermer un dossier de plainte ». Elle s'adresse aux fabricants, aux fabricants de marques privées, aux importateurs et aux distributeurs. Cette phase se divise en 5 étapes. Elle débute par la vérification du processus de traitement des plaintes afin de s'assurer que toutes les étapes et les actions ont été complétées. La deuxième étape implique d'aviser les parties concernées, y compris l'envoi d'un rapport d'incident final à Santé Canada, le cas échéant. La troisième étape correspond à l'obtention de l'approbation pour la fermeture du dossier de plainte. La quatrième étape porte sur la conservation de dossiers complets. La cinquième étape prévoit un examen régulier des plaintes afin de détecter les tendances en matière de défaillance.
Vos responsabilités
Que vous soyez un fabricant, un fabricant de marques privées, un importateur ou un distributeur, vous avez un rôle à jouer dans le traitement des plaintes. Vous devez :
- comprendre votre rôle et vos responsabilités;
- définir votre relation avec les autres entreprises de la chaîne de distribution de l'instrument médical;
- consigner dans vos procédures votre rôle, vos responsabilités et vos relations avec d'autres entreprises.
Le tableau 1 énumère les responsabilités liées au traitement des plaintes.
| Responsabilités | |||
|---|---|---|---|
| Fabricant | Fabricant de marques privées et importateur | Distributeur | |
| Recueillir les détails de la plainte et les consigner, et vérifier le bien-fondé de la plainte | Oui | Oui | Oui |
| Effectuer une évaluation préliminaire des risques et mettre en place des mesures provisoires de contrôle des risques | Oui | Oui (au minimum pour les activités dont vous êtes responsable) | Oui (au minimum pour les activités dont vous êtes responsable) |
| Aviser le fabricant | Ne s'applique pas, à moins qu'une autre entreprise soit déléguée pour enquêter sur les plaintes | Oui (aviser le fournisseur si différent du fabricant) | Oui (aviser le fournisseur si différent du fabricant) |
| Soumettre un rapport d'incident préliminaire à Santé Canada | Oui (au besoin) | Oui (au besoin) | Sans objet |
| Mener une enquête sur les causes profondes et évaluer les risques | Oui | Sans objet (sauf si la cause provient de votre entreprise) | Sans objet (sauf si la cause provient de votre entreprise) |
| Élaborer et choisir des mesures de contrôle des risques (p. ex. corrections et mesures correctives et préventives) | Oui | Sans objet (sauf si la cause provient de votre entreprise) | Sans objet (sauf si la cause provient de votre entreprise) |
| Mettre en œuvre des mesures de contrôle des risques | Oui | Oui | Oui |
| Envoyer à Santé Canada une notification des risques survenus à l'étranger | Oui – classes II à IV (au besoin) | Oui – classes II à IV (au besoin) | Sans objet |
| Évaluer l'efficacité des mesures de contrôle des risques | Oui | Sans objet (sauf si la cause provient de votre entreprise) | Sans objet (sauf si la cause provient de votre entreprise) |
| Fournir une rétroaction au fabricant quant aux mesures de contrôle des risques | Sans objet | Oui | Oui |
| Transmettre à Santé Canada un rapport d'incident final | Oui (au besoin) | Oui (au besoin) | Sans objet |
| Communiquer avec le plaignant et, au besoin, avec le déclarant de la plainte (utilisateur final, fabricant de marques privées, importateur ou distributeur) | Oui | Oui | Oui |
| Effectuer la revue finale et fermer le dossier | Oui | Oui | Oui |
| Tenir à jour les registres de traitement des plaintes | Oui | Oui | Oui |
| Effectuer une analyse périodique des tendances liées aux plaintes | Oui | Oui | Oui |
Toutes les parties impliquées dans la chaîne de distribution doivent collaborer et partager rapidement les renseignements relatifs à une plainte (du premier signalement jusqu'à la fermeture du dossier). |
|||
Si vous êtes le fabricant
Vous êtes responsable de votre instrument médical sur le marché canadien. Cela signifie que vous êtes responsable de :
- la sûreté et de l'efficacité de l'instrument médical;
- tout autre risque lié à la manutention, l'entreposage et l'utilisation de l'instrument lorsque le mode d'emploi est respecté;
- l'identification des mauvaises utilisations possibles et les mesures à prendre pour protéger les utilisateurs contre les risques liés à ces mauvaises utilisations.
Remarque : Vous êtes considéré comme un fabricant si le nom de votre entreprise ou votre marque de commerce figure sur l'étiquette de l'instrument médical. Si plus d'un nom d'entreprise apparaît sur l'étiquette, le lien entre chaque nom d'entreprise et l'instrument doit être clairement établie. Pour un instrument médical de classe II, III ou IV, le nom du fabricant figure également sur l’homologation de l'instrument.
Vous devez être prêt à traiter les plaintes qui vous sont transmises par :
- des utilisateurs finaux;
- comme des patients, des consommateurs, des professionnels de la santé et des établissements de soins de santé);
- d'autres sources;
- comme les importateurs, les distributeurs, les fabricants de marques privées et les organismes de réglementation.
Pour ce faire, vous devriez centraliser la collecte des plaintes auprès d'un seul interlocuteur, comme un employé occupant un poste ou une fonction particulière ou un groupe au sein de chaque établissement ou emplacement.
Dès que vous prenez connaissance d'un risque potentiel, vous devez prendre l'initiative d'enquêter sur le problème et de trouver une solution. Les étapes peuvent comprendre une analyse des causes profondes, une évaluation des risques et la mise en place d'actions correctives et préventives.
Votre processus, s'il y a lieu, doit également comprendre des étapes pour évaluer la plainte reçue en fonction des critères de déclaration d'incidents; les mesures prises pour gérer le risque et une évaluation en fonction des critères de notification des risques survenus à l'étranger et de rappel afin de s'assurer que vous répondez aux exigences relatives à d'autres mesures devant être signalées à Santé Canada.
Pour obtenir de plus amples renseignements, veuillez consulter :
- Rapports d'incidents liés aux matériels médicaux : Lignes directrices
- Lignes directrices sur la notification des risques survenus à l'étranger liés aux instruments médicaux
- Guide sur les rappels d'instruments médicaux (GUI-0054)
Vous voudrez peut-être aussi informer la personne qui a déposé la plainte des mesures de contrôle du risque que vous prévoyez mettre en œuvre. Cette communication constitue un élément clé du processus de rétroaction qui vous permet de gérer les risques associés à un instrument.
Si vous êtes le fabricant de marques privées, l'importateur ou le distributeur
Vous constituez un lien essentiel entre les personnes qui utilisent l'instrument médical et le fabricant de ce dernier. Le fabricant et l'utilisateur final comptent sur vous pour recueillir, évaluer et transmettre immédiatement au fabricant les plaintes sur la sûreté et le rendement d'un instrument. Pour ce faire, vous devriez disposer :
- d'une méthode pour consigner les plaintes qui vous sont adressées, par exemple un registre ou dossier de plaintes;
- d'un processus pour transmettre les plaintes au fabricant aux fins d'enquête.
Remarque : Si vous n'avez pas de lien direct avec le fabricant, vous pouvez transmettre la plainte à votre fournisseur direct. Votre fournisseur devra ensuite les transmettre au fabricant ou à leur fournisseur.
En tant que fabricant de marque privée ou importateur, vous devriez également évaluer les critères de déclaration d'incidents afin de déterminer si l'incident doit être déclaré à Santé Canada.
Pour obtenir de plus amples renseignements, veuillez consulter :
Dès que le fabricant vous informe qu'un instrument présente un risque grave, vous devez prendre les mesures qui relèvent de votre ressort. Il s'agit alors de mettre en oeuvre les mesures de contrôle des risques du fabricant. Ces mesures peuvent comprendre, par exemple :
- modifier l'étiquette;
- retourner l'instrument;
- cesser la vente de l'instrument;
- fournir un mode d'emploi plus détaillé;
- aviser les utilisateurs finaux qu'ils doivent cesser d'utiliser l'instrument;
- améliorer les mesures de contrôle d'entreposage ou du transport;
- réparer l'instrument dans les installations de l'utilisateur final.
Vous devriez également évaluer l'efficacité des mesures de contrôle des risques du fabricant et lui faire part des résultats.
Si quelqu'un (p. ex. le distributeur ou l'utilisateur final) vous a rapporté la plainte, vous devriez lui communiquer les efforts déployés pour résoudre le problème.
Remarque : Les mesures de contrôle des risques peuvent correspondre à la définition d'un rappel. Si vous êtes un fabricant de marques privées ou un importateur, vous devez aviser Santé Canada si vous retirez du marché un instrument qui causera probablement un préjudice à la santé d'un patient, d'un utilisateur ou d'une autre personne, ou pouvant causer un préjudice grave à leur santé. Veuillez consulter le document d'orientation suivant pour connaître les renseignements que vous devez transmettre à Santé Canada :
Procédures écrites
Vous devez consigner par écrit le processus de traitement des plaintes dans des procédures écrites. Les procédures peuvent être sous forme électronique ou papier ou une combinaison des deux. Vous pouvez décrire le processus dans une seule procédure ou dans plusieurs procédures. Vous devez être en mesure de démontrer à Santé Canada que :
- vous avez documenté l'ensemble du processus;
- vous suivez la ou les procédures.
Les procédures devraient :
- utiliser une structure uniforme pour organiser et présenter les renseignements;
- définir ce qu'est une plainte et les principales étapes liées au processus de traitement de celle-ci;
- attribuer la responsabilité des principales étapes décrites dans la ou les procédures aux personnes possédant les connaissances et l'autorité nécessaires pour veiller à ce qu'elles soient réalisées efficacement et en temps opportun;
- décrire en détail les étapes du traitement d'une plainte, de sa réception jusqu'à la fermeture du dossier;
- préciser des échéanciers mesurables pour l'exécution de chacune des étapes en fonction du niveau de risque (plus le risque est élevé, plus l'échéancier est court);
- inclure un mécanisme pour veiller au respect des délais, de la réception de la plainte jusqu'à la fermeture du dossier;
- exiger que les mesures prises pour traiter la plainte soient consignées;
- dresser la liste des registres ou des formulaires associés au processus de traitement des plaintes ainsi que l'endroit et la manière dont ces documents sont conservés.
Veuillez consulter le document d'orientation suivant pour vous aider à élaborer vos procédures :
Vous devez suivre vos procédures dès que vous recevez une plainte. À cette fin, vous devez :
- effectuer les tâches ou activités requises;
- consigner ou mettre à jour les renseignements dans les registres, au besoin
- vous assurer que chaque employé responsable d'une tâche ou d'une activité de la procédure :
- a accès à la procédure;
- a reçu la formation appropriée;
- comprend sa responsabilité
- assurer une supervision par la direction afin de veiller à l'application des procédures.
Si vous faites appel à un tiers pour gérer les plaintes, une entente écrite sur la qualité ou un contrat entre vous et ce tiers devrait être signé. Cette entente devrait préciser les rôles et responsabilités de chaque partie et garantir le respect du Règlement sur les instruments médicaux (p. ex. les délais pour la déclaration des incidents graves). L'entente sur la qualité est signée et datée par toutes les parties concernées.