Ligne directrice : Étiquetage des produits de santé naturels
Cette ligne directrice est un document d'orientation qui devrait être lu conjointement avec le Règlement sur les produits de santé naturels ainsi que les modifications réglementaires proposées au Règlement sur les produits de santé naturels afin d'améliorer l'étiquetage des produits de santé naturels.
Table des matières
- 1.0 Introduction
- 2.0 Contenu
- 3.0 Format
- 4.0 Assouplissements
- 5.0 Exemptions
- 6.0 Entrée en vigueur
- 7.0 Coordonnées
- Annexe A : Étiquetage des produits homéopathiques
- Annexe B : Suppléments minéraux à entité unique
- Annexe C : Liste de vérification des renseignements exigés sur l'étiquette
- Appendice 1 : Allergènes et aspartame
1.0 Introduction
1.1 Objectif
L'objectif de la présente ligne directrice est de vous aider à vous conformer aux exigences en matière d'étiquetage des produits de santé naturels (PSN), tel que stipulé dans la partie 5 du Règlement sur les produits de santé naturels (le Règlement). Il remplace le précédent Document de référence concernant l'étiquetage publié en 2006. Vous devriez également vous reporter aux lignes directrices Cheminement des demandes de licence de mise en marché des produits de santé naturels qui font l'objet d'allégations santé fondées sur des preuves modernes, Cheminement des demandes de licences de mise en marché des produits de santé naturels utilisés comme remèdes traditionnels et Preuves relatives aux médicaments homéopathiques, le cas échéant, particulièrement en ce qui concerne les allégations santé des produits.
Parallèlement à cette ligne directrice, les promoteurs peuvent consulter le Guide des bonnes pratiques d'étiquetage et d'emballage pour les médicaments sans ordonnance et les produits de santé naturels, qui comporte certaines pratiques exemplaires pour la conception de l'étiquetage. Veuillez noter que dans les cas où les deux documents se contredisent, vous devriez suivre les directives du présent document et vous devez toujours vous en remettre au Règlement s'il y a lieu.
La présente ligne directrice fournit des renseignements sur les spécifications de conception des étiquettes, les sections requises du tableau Info-produit (TIP) et le contenu de l'étiquetage pour répondre aux exigences du Règlement. Les titulaires de licence de PSN qui cherchent à conformer leur étiquetage à la partie 5 du Règlement devraient respecter ces principes, les spécifications relatives au format, et les exigences relatives au contenu définies dans le Règlement, tel qu'interprété dans la présente ligne directrice. La présente ligne directrice est appuyée par des recommandations sur la façon dont une allégation santé peut être présentée, tel que décrit dans d'autres lignes directrices sur les PSN. Veuillez noter que dans les cas où des documents sont en contradiction avec les nouvelles règles d'étiquetage établies dans le Règlement, vous devriez suivre les directives de la présente ligne directrice et devez toujours vous en remettre aux dispositions du Règlement, s'il y a lieu.
La présente ligne directrice est un outil administratif. Bon nombre des sections du présent document décrivent les exigences du Règlement, qui ont force de loi. La ligne directrice elle-même n'a pas force de loi, mais présente des recommandations de pratiques exemplaires pour aider les titulaires de licences à respecter leurs obligations législatives et réglementaires. Lorsque la ligne directrice fait référence aux exigences du Règlement ou à son interprétation, il est soit indiqué que la référence est « obligatoire » ou que vous « devez » vous y conformer, et renvoie à l'article précis du Règlement. Lorsque la ligne directrice fait référence à une pratique exemplaire qui n'a pas force de loi, il est soit indiqué que l'étape « peut » ou « devrait » être effectuée, soit qu'elle est « recommandée » ou « encouragée ». Nous vous encourageons à utiliser toutes les pratiques décrites dans la ligne directrice, même si elles ne sont pas requises, afin que les consommateurs puissent facilement comprendre les détails du PSN et le comparer à d'autres produits, ce qui leur permettra de faire des choix éclairés. D'autres approches pourraient être acceptables. Avant la mise en œuvre d'une telle approche, il peut être préférable de communiquer avec la Direction des produits de santé naturels et sans ordonnance de Santé Canada pour discuter de ces approches de rechange avant la mise en œuvre de ces dérogations afin d'éviter une non-conformité à la Loi sur les aliments et drogues et au Règlement.
Santé Canada se réserve le droit de définir des exigences qui ne sont pas spécifiquement décrites dans le présent document dans le cadre de l'autorisation du produit (soit l'autorisation de mise en marché). De plus, l'autorisation de mise en marché pourrait imposer des exigences supplémentaires en matière d'étiquetage. Santé Canada s'engage à s'assurer que les conditions sont justifiables et que les décisions sont clairement documentées.
1.2 Portée
La présente ligne directrice s'applique aux PSN au sens du paragraphe 1 (1) du Règlement. Elle comprend :
- les exigences générales relatives à la lisibilité (par exemple, le contraste et la police);
- les exigences en matière de format, notamment un TIP normalisé pour aider les utilisateurs à identifier des informations importantes et à comparer des produits similaires;
- des informations sur l'application des assouplissements disponibles (le cas échéant);
- des instructions d'étiquetage spécifiques pour certaines classes de produits (par exemple, les produits homéopathiques).
Cette ligne directrice ne contient pas de renseignements sur les exigences relatives aux demandes de licence de mise en marché concernant l'étiquetage des PSN ni sur le processus d'examen des étiquettes par Santé Canada. Pour de plus amples renseignements à ce sujet, veuillez consulter la Politique de gestion des demandes d'homologation de produits de santé naturels.
1.3 Définitions
Allergène alimentaire : toute protéine provenant d'un des aliments ci-après, ou toute protéine modifiée — y compris toute fraction protéique — qui est dérivée d'un tel aliment : amandes, noix du Brésil, noix de cajou, noisettes, noix de macadamia, pacanes, pignons , pistaches ou noix; arachides; graines de sésame; blé ou triticale; œufs; lait; soja; crustacés; mollusques; poisson; graines de moutarde. Il s'agit de la définition d'« allergène alimentaire » au paragraphe 1 (1) du Règlement sur les produits de santé naturels. D'autres protéines d'autres aliments peuvent provoquer des réactions allergiques; toutefois, seules les protéines susmentionnées sont considérées comme des « allergènes alimentaires » dans le présent document de référence.
Contenant : un récipient, emballage ou autre conditionnement contenant un produit mis en vente. La présente définition exclut les garnitures d'emballage, les conteneurs et tous les conditionnements extérieurs — notamment les boîtes — qui ne servent pas normalement à la présentation au consommateur. Il s'agit de la définition du terme « contenant » dans la Loi sur l'emballage et l'étiquetage des produits de consommation. Pour plus de clarté, cette définition de contenant inclut les coques, les boîtes, les bouteilles, les couvertures, les sachets, les emballages en bande, les tubes, les récipients, les flacons et autres articles similaires.
Contenant immédiat : le contenant qui est en contact direct avec le PSN. Il s'agit de la définition de « contenant immédiat » au paragraphe 1 (1) du Règlement.
Emballage : notamment récipient, empaquetage ou autre conditionnement contenant, en tout ou en partie tout PSN. Il s'agit de la définition d'« emballage » à l'article 2 de la Loi sur les aliments et drogues, adaptée au contexte des PSN. Les emballages sont interprétés dans ce document de référence comme étant limités aux emballages qui sont habituellement présentés au consommateur. Un présentoir en magasin n'est pas considéré comme un emballage.
Espace principal (ou aire d'affichage principale) : la partie de l'étiquette qui est affichée ou visible dans les conditions normales ou habituelles de vente. Cette définition est adaptée du Règlement sur l'emballage et l'étiquetage des produits de consommation. Les produits qui n'utilisent qu'un seul panel par emballage comme aire d'affichage principale sont admissibles à des assouplissements supplémentaires.
Étiquettes et solutions de rechange :
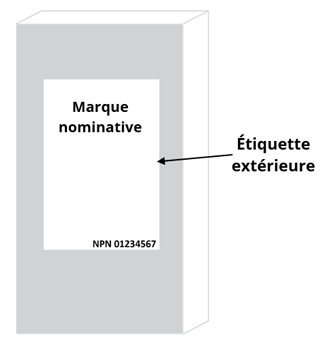
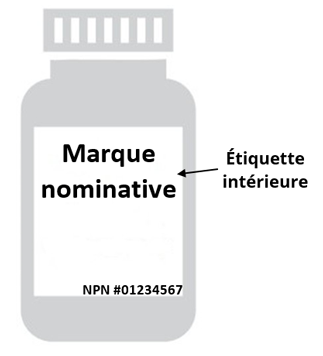
Équivalent textuel
Cette figure fournit une aide visuelle pour différencier l'étiquette intérieure de l'étiquette extérieure.
Il y a deux images, la première image montre un contenant immédiat (par exemple, une bouteille) sur lequel est apposé l'étiquette intérieure. La deuxième image montre l'emballage extérieur (par exemple, la boîte) sur lequel est apposée l'étiquette extérieure. Les deux images montrent la « marque nominative » et le numéro d'identification pour référence.
- Étiquette : sont assimilés aux étiquettes les inscriptions, mots ou marques accompagnant un PSN ou s'y rapportant . Il s'agit de la définition d'« étiquette », à l'article 2 de la Loi sur les aliments et drogues, telle qu'elle est interprétée dans son application aux PSN.
- Étiquette numérique : étiquette affichée électroniquement (par exemple, une étiquette sur un site Web), conforme aux exigences du tableau Info-produit électronique établies par Santé Canada, qui affiche tous les renseignements requis dans un TIP, ce qui permet le retrait de certains renseignements de l'étiquette physique. Le retrait de toute information de l'étiquette physique doit être indiqué, y compris ce qui a été retiré et son emplacement dans l'espace numérique.
- Tableau Info-produit électronique (eTIP) : un TIP, tel que défini dans la présente ligne directrice, affiché numériquement (par exemple, page Web du site Web d'une entreprise). Aucun renseignement sur l'image de marque ne peut être inclus avec le eTIP.
- Étiquette intérieure : l'étiquette apposée sur le contenant immédiat d'un PSN. Il s'agit de la définition d'« étiquette intérieure » au paragraphe 1 (1) du Règlement. Si le produit n'a qu'une seule étiquette, il est considéré comme une « étiquette intérieure ».
- Étiquette innovante : étiquette qui sert d'extension à l'étiquette d'un produit. Certains renseignements, notamment les utilisations et les ingrédients médicinaux, doivent être accessibles au consommateur au point de vente sans détruire ou compromettre l'intégrité de l'étiquette ou de l'emballage. L'étiquette innovante doit être physiquement attachée à l'étiquette d'une manière qui n'encourage pas sa séparation de l'étiquette. Parmi les exemples d'étiquettes innovantes, mentionnons les étiquettes dépliantes, les livrets ou les étiquettes pliables. À titre d'extension de l'étiquette, le contenu et le format de l'étiquette innovante doivent être conformes aux exigences relatives à la police, au contraste et au formatage, telles qu'elles sont décrites à l'article 88 du Règlement, ainsi qu'au présent document de référence, le cas échéant.
- Dépliant (en attache) : étiquette apposée ou attachée au contenant le plus à l'extérieur d'un PSN que le consommateur peut facilement retirer et qui contient des renseignements qui n'entrent pas sur l'étiquette, comme le prévoit le Règlement.
- Étiquette extérieure : l'étiquette sur l'extérieur de l'emballage, autre que le contenant immédiat, d'un PSN, ou y apposée. Il s'agit de la définition d'« étiquette extérieure » au paragraphe 1 (1) du Règlement. Si le produit n'a qu'une seule étiquette (c.-à-d. qu'il n'a pas de boîte extérieure), il est considéré comme une étiquette intérieure.
- Notice d'accompagnement : étiquette insérée dans un manchon (par exemple, emballage en plastique transparent) sur l'emballage extérieur ou le contenant immédiat d'un produit, ou contenu dans l'emballage extérieur d'un produit qui permet de retirer des renseignements de l'étiquette extérieure ou intérieure qui n'entrent pas sur l'étiquette, comme le prévoit le Règlement.
Petit emballage : emballage dont le contenant immédiat n'est pas assez grand pour inclure une étiquette intérieure qui comprend les renseignements et le format requis par l'article 93.1 du Règlement, et qui peut plutôt utiliser un dépliant, dans le format prescrit, qui est apposé ou attaché au contenant immédiat. Différent de « très petit emballage »
Point : unité de mesure de la force de corps des caractères connue comme point PostScript et équivalent à 0,3527777778 mm. Il s'agit de la définition du terme « point » dans le Règlement.
Point de vente en ligne : toute plateforme numérique qui vend des PSN (par exemple, site Web, application) qui devrait fournir les mêmes renseignements dont un Canadien a besoin pour faire un choix éclairé comme si le produit était physiquement disponible pour la sélection au point de vente en question.
Produit homéopathique : un PSN basé sur l'homéopathie, indiqué par la présence d'un DIN-HM plutôt que d'un numéro de produit naturel (NPN) comme numéro d'identification. Les produits homéopathiques doivent être fabriqués à partir de, ou contenir comme ingrédients médicinaux, uniquement les substances référencées dans une monographie homéopathique d'une pharmacopée homéopathique approuvée. Ils doivent être préparés conformément aux méthodes décrites dans une pharmacopée homéopathique approuvée. Ceci est basé sur la définition de « médicament homéopathique » dans le document de référence Preuves relatives aux médicaments homéopathiques.
Produit à faible risque : un PSN qui a un effet localisé ou cosmétique et dont l'utilisation dans la cavité buccale ou sur la peau est recommandée. Les produits à faible risque sont approuvés pour des bienfaits mineurs pour la santé pour des problèmes qui, autrement, se régleraient d'eux-mêmes ou seraient limités (par exemple, pas d'aggravation), et comprennent les rince-bouche, les gouttes contre la toux, les pastilles pour la gorge, les dentifrices au fluorure, les produits dont l'utilisation est recommandée dans le cadre d'un traitement d'aromathérapie ou d'organothérapie (topique et cavité buccale), et les essences de fleur (topique et cavité buccale). Sont cependant exclus les nosodes. Pour plus de clarté, ces produits ne dépendent pas d'une absorption systémique ou d'une ingestion pour obtenir leurs effets bénéfiques sur la santé.
Produit de santé naturel : substance mentionnée à l'annexe 1 du Règlement ou combinaison de substances dont tous les ingrédients médicinaux sont des substances mentionnées à cette annexe, remède homéopathique ou remède traditionnel, qui est fabriqué, vendu ou présenté comme pouvant servir :
- au diagnostic, au traitement, à l'atténuation ou à la prévention d'une maladie, d'un désordre, d'un état physique anormal ou de leurs symptômes chez l'être humain;
- à la restauration ou à la correction des fonctions organiques chez l'être humain;
- à la modification des fonctions organiques chez l'être humain.
La présente définition exclut toutefois les substances mentionnées à l'annexe 2 du Règlement, toute combinaison de substances qui contient une substance mentionnée à cette annexe et tout remède homéopathique ou remède traditionnel qui est une substance mentionnée à cette annexe ou qui contient l'une de ces substances.
Il s'agit de la définition de « produit de santé naturel » au paragraphe 1 (1) du Règlement.
Produit traditionnel : un PSN fondé sur la médecine traditionnelle. La médecine traditionnelle est définie comme une médecine basée sur la somme totale des connaissances, des compétences et des pratiques fondées sur les théories, les croyances et les expériences indigènes de différentes cultures, utilisées dans le maintien de la santé, ainsi que dans la prévention, le diagnostic, l'amélioration ou le traitement des maladies physiques et mentales. Cette définition est basée sur la définition de « médecine traditionnelle » dans le Cheminement des demandes de licences de mise en marché des produits de santé naturels utilisés comme remèdes traditionnels.
Mises en garde relatives à la sélection du produit : renseignements nécessaires pour prendre une décision d'achat en connaissance de cause. Veuillez consulter le tableau 11 pour de plus amples renseignements.
Mises en garde relatives à l'utilisation du produit : renseignements nécessaires pour utiliser le produit de façon sécuritaire. Veuillez consulter le tableau 11 pour de plus amples renseignements.
Nom propre : le nom d'une vitamine; le nom latin du genre pour les plantes, les algues, les bactéries, les champignons, les matières animales ou les probiotiques; ou le nom chimique. Pour une définition plus détaillée, voir le paragraphe 1 (1) du Règlement.
Surface disponible pour l'étiquette : la surface totale d'un contenant sur laquelle une étiquette peut être apposée (voir le Tableau 1).
| Inclus | Exclu |
|---|---|
|
|
Très petit emballage : emballage dont la surface disponible pour l'étiquette est de 90 cm² ou moins. Pour plus de clarté, les étiquettes intérieures et les étiquettes extérieures peuvent être considérées comme de très petits emballages. Cette définition est fondée sur les alinéas 88 (2)(b) et 93.5 (a) du Règlement. Différent de « petit emballage ».
Trousses et produits emballés ensemble (co-emballés) :
- Produit co-emballé : produit avec deux PSN emballés ensemble, mais qui n'ont pas à être utilisés ensemble comme unité. Un produit constituerait un produit co-emballé lorsque chaque article du produit co-emballé a été approuvé individuellement.
- Trousse : un produit constituerait une trousse lorsque :
- la trousse et le PSN sont destinés à être utilisés ensemble comme une unité;
- la trousse constitue un seul traitement, une seule série de traitements ou doit être utilisée dans un ordre particulier; ou
- une marque nominative a été identifiée pour la combinaison de produits.
2.0 Contenu
Vous devez étiqueter et emballer tous les PSN conformément à la Loi sur les aliments et drogues, au Règlement et à toute autre loi, réglementation et directive applicable. Conformément à l'article 87 du Règlement, certains renseignements sur l'étiquette doivent être en français et en anglais.
La publicité du produit dans tout média (par exemple, imprimé, électronique, social, télédiffusé, etc.) doit également être conforme aux dispositions sur la publicité selon les articles 3 et 9 de la Loi sur les aliments et drogues, sous réserve de l'article 103.2 du Règlement, et doit être conforme aux lignes directrices et aux politiques applicables de Santé Canada. Il s'agit notamment des lignes directrices sur la publicité destinée aux consommateurs de produits de santé pour les médicaments en vente libre, les produits de santé naturels, les vaccins et les instruments médicaux (en anglais).
Remarque : Tous les aspects de l'étiquette du produit doivent être conformes à la Loi sur les aliments et drogues, y compris l' article 9 qui stipule : « Il est interdit d'étiqueter, d'emballer, de traiter, de préparer ou de vendre une drogue – ou d'en faire la publicité – d'une manière fausse, trompeuse ou mensongère ou susceptible de créer une fausse impression quant à sa nature, sa valeur, sa quantité, sa composition, ses avantages ou sa sûreté. »
Selon la partie 5 du Règlement, les étiquettes des produits (notamment les étiquettes intérieures et extérieures) doivent comporter des informations spécifiques, telles que le numéro d'identification et le numéro de lot. Le Règlement précise l'emplacement où certains renseignements doivent se trouver, par exemple sur l'espace principal de l'étiquette, conformément à l'article 93 du Règlement, ou dans un TIP, conformément à l'alinéa 93.1(f) du Règlement. L'article 88 du Règlement précise également quels éléments de formatage sont requis, et de nombreux éléments sont détaillés dans les lignes directrices, notamment les styles de police, la taille et le contraste spécifique. Par ailleurs, conformément aux alinéas 88(a) et (b) du Règlement, les étiquettes doivent être clairement lisibles par les consommateurs dans les conditions ordinaires d'achat et d'utilisation. Il existe des assouplissements pour les produits qui ne peuvent pas répondre à tous les renseignements requis tout en respectant les exigences de formatage, prévues dans le Règlement, conformément aux paragraphes 93.3, 93.6 (3) et à l'article 94 du Règlement, que la présente ligne directrice aide à interpréter. Il existe également des exemptions fondées sur le risque pour certains types de produits à l'égard d'exigences en matière d'étiquetage, comme établies au paragraphe 88 (2) et à l'article 93.5 du Règlement.
Conformément aux paragraphes 93.1 (4), (5) et (6) du Règlement, les énoncés promotionnels qui peuvent figurer sur les étiquettes des PSN doivent se trouver à l'extérieur du TIP. Ces énoncés doivent également être conformes aux dispositions législatives et réglementaires sur la publicité des PSN, y compris celles de l'article 9 de la Loi sur les aliments et drogues. Elles doivent aussi être harmonisées avec les documents pertinents de Santé Canada ou les lignes directrices supplémentaires pertinentes, comme les directives fournies par les organismes Canadiens de pré-approbation de la publicité.
2.1 Informations requises sur l'espace principal des étiquettes intérieures et extérieures
Vous devez inclure les renseignements suivants sur l'espace principal des étiquettes intérieure et extérieure, s'il y a une étiquette extérieure, comme il est indiqué à l'article 93 du Règlement. S'il n'y a qu'une seule étiquette, vous devez inscrire les renseignements sur l'espace principal de cette étiquette. Voir la section 4.0 (Assouplissements) pour de plus amples informations sur les autres options de formatage si l'emballage ne peut pas contenir une étiquette avec toutes les informations requises.
- Marque nominative
Il s'agit du nom utilisé pour distinguer ou identifier le produit. Vous ne devez utiliser qu'une seule marque nominative par produit conformément à l'alinéa 5(e) du Règlement, tel qu'elle apparaît dans l'autorisation de mise en marché de votre produit. Remarque : Vous ne devez pas utiliser une marque nominative qui implique une utilisation recommandée différente des conditions approuvées qui apparaissent dans l'autorisation de mise en marché pour ce produit. Cela serait considéré comme une violation de l'article 9 de la Loi sur les aliments et drogues. - Numéro d'identification
Vous obtiendrez un numéro d'identification de Santé Canada après que Santé Canada aura délivré votre licence de mise en marché. Il doit être clairement identifié sur l'étiquette par le préfixe NPN ou le préfixe DIN-HM. Votre numéro d'identification devrait être affiché horizontalement sur l'étiquette. - Forme posologique
La forme posologique correspond à la façon dont le produit est appliqué, ingéré ou inhalé et comprend, par exemple, « comprimés », « gels », etc. Lorsque la forme posologique figure dans la marque nominative du produit, elle n'a pas à être répétée (par exemple, « comprimés de vitamine C »). - « Stérile » (si applicable)
Les produits stériles doivent être désignés par les mots « stérile » et « sterile ». - Quantité nette dans le contenant immédiat exprimée en poids, en volume ou en nombre
La quantité nette est le nombre total d'unités posologiques dans le contenant immédiat, en poids, en volume ou en nombre. Lorsque plusieurs quantités nettes sont utilisées, chacune devrait être indiquée sur l'étiquette. La quantité nette doit être indiquée dans les unités normalisées ou appropriées.
| Montant net | Définition |
|---|---|
| Masse | Pour les produits qui sont solides ou semi-solides, mais qui ne sont pas présentés sous des formes posologiques distinctes (par exemple, 500 g de poudre ou 30 g de crème) |
| Compte | Lorsqu'une forme posologique discrète est présente (par exemple : 100 capsules) |
| Volume | Pour les produits sous forme liquide, mais pas sous forme de dosage discret (par exemple, 500 ml de sirop) |
Un symbole métrique utilisé pour l'unité de mesure abrégée est considéré comme bilingue. Les symboles abrégés ne devraient pas être suivis d'un point. Si le mot complet est utilisé, il doit apparaître à la fois en anglais et en français. Le tableau 3 fournit de plus amples détails sur la façon d'afficher les différentes unités de mesure. D'autres unités de mesure peuvent être incluses, mais l'équivalent métrique doit être affiché en premier. L'abréviation « U » pour « unité » n'est pas recommandée.
| Mot complet – Anglais |
Mot complet – Français |
Abréviations bilingues correctes |
|---|---|---|
| Colony forming units | nombre d'unités formant colonies | CFU/UFC |
| gram(s) | gramme(s) | g |
| kilogram(s) | kilogramme(s) | kg |
| litre(s) | litre(s) | L ou l |
| microgram(s) | microgramme(s) | mcg |
| milligram(s) | milligramme(s) | mg |
| millilitre(s) | millilitre(s) | mL |
2.2 Informations requises sur l'étiquette extérieure
Vous devez inclure les renseignements suivants sur l'étiquette extérieure ou, s'il n'y a pas d'étiquette extérieure, sur l'étiquette intérieure, comme il est indiqué au paragraphe 93.1 du Règlement :
- Un tableau Info-produit (voir les renseignements ci-dessous à la section 2.4) (au besoin);
- Le nom du titulaire de la licence de mise en marché ou de l'importateur (le cas échéant). Un seul des deux est maintenant requis;
- La voie d'administration recommandée (il n'est pas nécessaire de préciser une voie d'administration orale si elle est implicite dans la forme posologique);
- Le numéro de lot.
On recommande l'une des références suivantes avant le numéro de lot, conformément à l'article 90 du Règlement :- « Numéro de lot »;
- « N° lot »;
- « Lot »;
- « LOT »; ou
- « (L) ».
- Date limite d'utilisation :
La date limite d'utilisation, tel que prévu au paragraphe 1 (1) du Règlement, est la première des dates suivantes à survenir :- la date après laquelle :
- le PSN ne conserve plus sa pureté et ses caractéristiques physiques; et
- les ingrédients médicinaux du PSN ne conservent plus leur activité et la quantité par unité posologique; ou
- la date après laquelle le fabricant recommande de ne plus employer le PSN.
- la date après laquelle :
La date limite d'utilisation devrait être suivie d'un terme que le grand public soit en mesure de comprendre clairement, par exemple « Expiration », « Date limite d'utilisation » ou « EXP ».
La date limite d'utilisation devrait être exprimée en année et en mois. Vous pouvez utiliser des tirets (–), des barres obliques (/) ou des espaces pour séparer l'année et le mois. Si vous choisissez d'indiquer un jour, vous devriez utiliser le dernier jour du mois et utiliser des lettres pour le mois afin d'éviter toute confusion. Si vous utilisez le mot complet pour le mois, il doit apparaître en anglais et en français. Vous devriez utiliser les quatre chiffres de l'année pour éviter toute confusion avec le mois ou le jour. Le tableau 4 présente les formats de date limite d'utilisation recommandés. Le tableau 5 présente les abréviations bilingues des mois.
| Formats recommandés | Exemples | Formats non recommandés |
|---|---|---|
| EXP AAAA-MM | EXP 2025 January/janvier EXP 2025-JA EXP 2025-01 |
- |
| EXP MM-AAAA | EXP. Janvier 2025/janvier 2025 EXP JA-2025 EXP 01-2025 |
- |
| EXP AAAA-MM-JJ | EXP 2025-JA-31 EXP 2025-01-31 (lorsque seul le dernier jour du mois correspondant est utilisé) |
EXP JA-25 EXP 2025-01-12 (lorsque le dernier jour du mois correspondant n'est pas utilisé) |
| EXP JJ-MM-AAAA | EXP 31-JA-2025 EXP 31/JA/2025 EXP 31 JA 2025 EXP 01-31-2025 (lorsque seul le dernier jour du mois correspondant est utilisé) |
EXP 25-JA EXP 21-01-2025 (lorsque le dernier jour du mois correspondant n'est pas utilisé) |
| EXP MM-JJ-AAAA | EXP JA-31-2025 EXP 31-01-2025 (lorsque seul le dernier jour du mois correspondant est utilisé) |
EXP 01-12-2025 (lorsque le dernier jour du mois correspondant n'est pas utilisé) |
| Abréviation | Anglais | Français |
|---|---|---|
| JA | January | janvier |
| FE | February | février |
| MR | March | mars |
| AL | April | avril |
| MA | May | mai |
| JN | June | juin |
| JL | July | juillet |
| AU | August | août |
| SE | September | septembre |
| OC | October | octobre |
| NO | November | novembre |
| DE | December | décembre |
2.3 Informations requises sur l'étiquette intérieure
Si le PSN porte à la fois une étiquette intérieure et une étiquette extérieure, les renseignements suivants doivent figurer sur l'étiquette intérieure conformément à l'article 93.4 du Règlement :
- Le nom du titulaire de la licence de mise en marché ou de l'importateur (le cas échéant);
- Les coordonnées de la personne-ressource qui représente le titulaire de la licence de mise en marché ou l'importateur (adresse, numéro de téléphone, adresse électronique ou adresse de site Web);
- Les ingrédients médicinaux, la quantité de chaque ingrédient par unité posologique, et l'activité de chaque ingrédient (le cas échéant). Voir l'annexe B pour des recommandations d'étiquetage spécifiques pour les suppléments de calcium, de fer, de magnésium et de zinc;
- Au moins une fin ou un usage recommandé;
- La voie d'administration recommandée (la politique n'exige pas de voie d'administration orale si elle est implicite par la forme posologique);
- La dose;
- La durée d'utilisation, le cas échéant;
- Les sources d'allergènes alimentaires, la mention « gluten » et les sources de gluten, et les sulfites ajoutés, le cas échéant;
- Une divulgation sur la présente d'aspartame, le cas échéant;
- Mises en garde (y compris celles énumérées dans les sections 6.d à 6.d.10 du tableau 6 et selon les conditions d'autorisation de mise en marché votre produit);
- Les autres renseignements(par exemple, les conditions d'emmagasinage recommandées);
- Le numéro de lot;
- La date limite d'utilisation.
Toutes les exigences relatives au contenu devraient correspondre aux descriptions présentées dans le tableau 6 (Contenu du tableau d'information sur le produit) lorsqu'un TIP est requis.
2.4 Informations requises dans le tableau d'information sur le produit
Conformément à l'alinéa 93.1 (1) (f) du Règlement, pour les produits applicables, l'étiquette la plus éloignée d'un produit doit comprendre un tableau d'information sur le produit, sous l'une des formes suivantes :
- Un TIP bilingue;
- Un TIP anglais (Product Facts table) ET un TIP français.
Le TIP doit figurer sur l'étiquette extérieure ou, s'il n'y a pas d'étiquette extérieure, sur l'étiquette intérieure, et peut être aligné horizontalement ou verticalement. L'information affichée dans le TIP n'a pas à être répétée ailleurs sur l'étiquette, à moins que le titulaire de la licence de mise en marché ne le souhaite.
Les renseignements requis, conformément à l'article 93.1 du Règlement, sont résumés dans le tableau 6 ci-dessous. Le titre, les en-têtes et les sous-titres doivent apparaître dans l'ordre indiqué dans le tableau 6. Si une en-tête ou un sous-titre ne s'applique pas, il devrait être exclu du TIP. Il est possible d'inclure des sous-titres supplémentaires, mais ils ne doivent pas remplacer les sous-titres du tableau 6. Les renseignements contenus dans le TIP doivent refléter l'autorisation de mise en marché du produit et ne doivent pas comprendre de termes de publicité ou de termes promotionnels (par exemple « formulation améliorée » ou « recommandé par 4 experts sur 5 ») conformément à l'article 93.1 du Règlement.
Les assouplissements permettent de transférer des renseignements précis, dans certains cas, hors du TIP et ailleurs sur l'étiquette, vers un dépliant en attache, vers un eTIP hébergé sur un site Web, ou vers une notice d'accompagnement. Un énoncé, y compris une URL si vous utilisez un eTIP, doit ensuite être inclus sous le titre Info-produit pour diriger les consommateurs vers les renseignements déplacés, conformément au paragraphe 93.3 (4) du Règlement. Cette mention devrait être dans une police et un style conformes à l'en-tête et devrait être suffisamment claire pour indiquer que l'information a été déplacée, en plus d'indiquer clairement où elle peut être trouvée. Il n'est pas nécessaire de reproduire cet énoncé pour chaque cas où l'information est retirée.
Les énoncés acceptables comprennent :
“For full Product Facts table, including removed information, visit www.websitename.ca" / « Pour le tableau Info-produit complet, incluant les informations déplacées, visitez www.nomdusiteweb.ca. » ou “Read package insert [or leaflet] for complete warnings before use. " / « Lire la notice [ou le dépliant d'information] pour l'ensemble des mises en garde avant l'utilisation. » ou “For a full list of non-medicinal ingredients, please see leaflet. " / « Pour une liste complète des ingrédients non-médicinaux, consultez le dépliant d'information. »
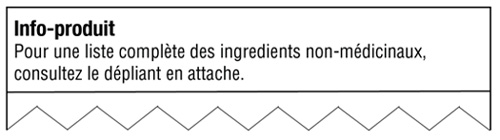

Équivalent textuel
La figure 1 : Exemples d'énoncés acceptables pour les cas où des renseignements sont retirés du TIP. Le texte sous l'en-tête donne des instructions sur l'endroit où les consommateurs peuvent trouver les informations retirées du tableau de la fiche signalétique.
Voir la section 4.1 (Assouplissements) pour plus de détails sur les contenants qui sont trop petits pour contenir une étiquette pouvant afficher un TIP.
Conformément au paragraphe 93.5 du Règlement, l'exigence relative au TIP ne s'applique pas pour :
- les produits avec de très petits emballages (définis comme ayant une surface d'affichage disponible de 90 cm² ou moins);
- les produits qui, lorsqu'utilisés selon le mode d'emploi qui figure sur l'étiquette, contiennent au maximum suffisamment d'unités posologiques pour une utilisation d'un jour ou moins. Il s'agit notamment des échantillons, des sachets ou des produits en format de transport;
- les produits dont le contenant immédiat contient au plus trois unités posologiques recommandées;
- les produits à faible risque (voir la section 1.3 Définitions).
Voir la section 5.0 (Exemptions) pour plus d'informations.
Le tableau suivant résume les renseignements qui doivent être inclus dans le TIP. Pour obtenir des directives détaillées, veuillez consulter la section 2.4 ou d'autres sections du présent document de référence, s'il y a lieu.
| - | Titre/En-tête/ Sous-titre |
Description et commentaires concernant le contenu |
|---|---|---|
| 6.a | Info-produit (suite) / Product Facts (continued) ou Info-médicament (suite) / Drug Facts (continued) |
Si le TIP est divisé entre différents panneaux de l'étiquette, chaque partie supplémentaire du tableau doit être intitulée :
|
| 6.a.1 | Si les renseignements applicables sont transférés à un dépliant en attache, à une notice d'accompagnement ou à un eTIP, conformément au paragraphe 93.3 (4) du Règlement, vous devez indiquer où les trouver directement sous le titre Info-produit en utilisant un énoncé tel que ceux suggérés ci-après, selon le cas :
Si un eTIP est mentionné en référence, l'adresse du site Web mentionnée doit être accessible au consommateur moyen, par exemple en affichant une adresse qui utilise des mots plutôt qu'une série de chiffres ou des caractères alphanumériques aléatoires. L'adresse du site Web devrait aussi être facile à saisir dans un navigateur pour le consommateur, par exemple en affichant une adresse URL personnalisée. Il n'est pas nécessaire de répéter la mention sous des en-têtes individuels lorsque le contenu a été déplacé, pourvu qu'elle ait déjà été indiquée dans le haut du TIP. |
|
| 6.b | Medicinal ingredient(s) (in each dosage unit) / Ingrédient(s) médicinal (médicinaux) (dans chaque unité posologique) |
Énumérez les ingrédients médicinaux en utilisant le nom propre (paragraphe 93.1 (7) du Règlement). Vous pouvez utiliser le nom usuel uniquement si le nom propre est le nom chimique. Pour obtenir des conseils supplémentaires concernant les noms propres et les noms communs, consultez la Base de données d'ingrédients de produits de santé naturels (BDIPSN), laquelle est mise à jour aux deux semaines. Remarque : Pour les minéraux, le nom propre est l'ingrédient médicinal par unité posologique. La forme saline est considérée comme sa matière d'origine. La confusion autour de l'étiquetage des minéraux est un problème de sécurité notable. Voir l'annexe B pour plus d'informations à ce sujet. Les ingrédients médicinaux doivent être énumérés de la plus grande quantité à la plus faible quantité par unité posologique. Pour chaque ingrédient médicinal, vous devez également inclure :
|
| 6.b.1 | Pour les produits homéopathiques : Les exemples suivants de produits homéopathiques sont donnés à titre indicatif et indiquent le nom propre, le nom usuel et la matière d'origine :
Ces exemples sont donnés en vue d'accroître la clarté de la dénomination des ingrédients médicinaux homéopathiques. Toutes les autres exigences d'étiquetage des médicaments homéopathiques sont applicables. Voir la section 5.2 Exigences d'étiquetage spécifiques aux médicaments homéopathiques du document de référence Preuves relatives aux médicaments homéopathiques ainsi que l'annexe A du présent document. Pour les produits homéopathiques, l'unité posologique n'est pas applicable. Vous devez toutefois inclure l'activité autorisée ici conformément au sous-alinéa 93.1 (7) (a) (iii) du Règlement). Vous pouvez également indiquer la concentration du produit (mg/ml). |
|
| 6.c | Utilisations / Use(s) |
Vous ne pouvez afficher que les « Utilisations » ou les « Fins » recommandées en utilisant la formulation exacte (aussi appelée « indications »), comme indiquée dans votre autorisation de mise en marché. Il s'agit du bénéfice attendu du produit lorsqu'il est utilisé selon les conditions d'utilisation recommandées. Vous devez énumérer au moins une des utilisations ou des fins recommandées du PSN conformément au paragraphe 93.1 (8) du Règlement. Toutefois, vous ne devez pas retirer les mises en garde qui sont exigées conformément à l‘autorisation de mise en marché de PSN, peu importe l'utilisation indiquée sur l'étiquette, à moins qu'une modification de l'autorisation de mise en marché ne l'autorise autrement. Les utilisations ou les fins recommandées sont différentes des allégations publicitaires ou commerciales. Les allégations de publicité et commerciales, qui sont de nature non thérapeutique, ne sont permises qu'à l'extérieur du TIP (par exemple, « formulation nouvelle et améliorée »). Votre fin ou votre utilisation ne peut pas renvoyer au traitement, à l'atténuation, au diagnostic ou à la guérison de maladies ou de problèmes de santé énumérés à l'annexe A.1, conformément à l'article 3 de la Loi sur les aliments et drogues; toutefois, dans certains cas, vous pouvez faire des allégations de prévention pour des maladies ou des problèmes de santé mentionnés à l'annexe A.1, mais elles doivent avoir été approuvées dans l'autorisation de mise en marché de votre produit. Veuillez consulter les paragraphes 103.2 et 103.3 du Règlement ainsi que la Ligne directrice : Annexe A et article 3 de la Loi sur les aliments et drogues pour obtenir de plus amples renseignements. |
| 6.c.1 | Pour les produits traditionnels… La fin ou l'usage pour les produits traditionnels doit venir après un qualificatif approuvé, tel que « Utilisé traditionnellement… » et refléter la culture spécifique du produit ou le paradigme de guérison tel qu'il est écrit dans les termes de l'autorisation de mise en marché (par exemple, « Utilisé traditionnellement en médecine ayurvédique pour stimuler le feu digestif ou augmenter l'agni »). Pour obtenir une confirmation ou des précisions supplémentaires sur les qualificatifs recommandés ou requis, veuillez consulter votre autorisation de mise en marché. Si la fin ou l'usage est fondé à la fois sur des preuves traditionnelles et scientifiques, l'exigence ou la recommandation relative aux qualificatifs sera dictée par le processus d'approbation utilisé au moment de demander l'autorisation, tel que décrit dans votre autorisation de mise en marché. Pour les produits comportant à la fois des allégations d'usage traditionnel et non traditionnel, le ou les ingrédients médicinaux soutenant l'allégation traditionnelle devraient être inclus dans l'usage recommandé. Par exemple, « la passiflore est traditionnellement utilisée en phytothérapie comme aide au sommeil » ou « l'ashwagandha est traditionnellement utilisée en Ayurveda comme Rasayana (tonique rajeunissant) ». |
|
| 6.c.2 | Pour les produits homéopathiques : Pour les produits homéopathiques, le qualificatif « produit homéopathique », « médicament homéopathique », « remède homéopathique » ou « préparation homéopathique » doit précéder l'usage ou la fin. Si une utilisation ou une finalité n'est étayée que par des preuves scientifiques, elle ne doit pas inclure de qualificatif homéopathique. Le qualificatif devrait répondre aux exigences de taille et de contraste décrites dans la section 5.2 de la ligne directrice Preuves relatives aux médicaments homéopathiques. |
|
| 6.d | Mise(s) en garde / Warning(s) |
Vous devez inclure les mentions, mises en garde, contre-indications et effets indésirables connus, tels qu'ils sont décrits dans l'autorisation de mise en marché de votre produit, et devriez les énumérer dans l'ordre indiqué ci-dessous. Le libellé des mises en garde doit correspondre aux exigences de votre autorisation de mise en marché et devrait être conforme à toute monographie de produit applicable. Les modifications de ce libellé nécessiteraient une modification de l'autorisation, à moins qu'il ne soit permis de procéder par avis, conformément aux dispositions transitoires prévues dans le Règlement. Dans de tels cas, un avis suffirait. Vous ne devez pas retirer les mises en garde exigées par l'autorisation de mise en marché du PSN, peu importe l'utilisation que vous choisissez d'afficher sur l'étiquette. Tout changement apporté aux mises en garde nécessiterait une modification de votre autorisation. |
| 6.d.1 | (Selon le cas, exemples seulement) Pour usage rectal seulement / Pour usage vaginal seulement / |
Veuillez inclure des mises en garde concernant la voie d'administration recommandée selon votre autorisation de mise en marché. Aucun texte supplémentaire n'est requis. Si cette information est déjà saisie dans la section Mode d'emploi, il n'est pas nécessaire de la répéter dans la section Mises en garde. |
| 6.d.2 | (Selon le cas) Asthma alert / Alerte à l'asthme Contient de l'aspartame / |
Lorsque des allergènes alimentaires ou du gluten sont inclus dans une quantité quelconque du produit, ou lorsque le produit contient 10 p.p.m. de sulfites ajoutés ou plus, la source d'allergènes alimentaires, la source de gluten et les sulfites ajoutés doivent être indiqués, conformément au paragraphe 93.1 (11) du Règlement. Conformément au paragraphe 1 (1), à l'alinéa 91.3 b) et au paragraphe 91.4 du Règlement, la mention des sources d'allergènes alimentaires ou de gluten et des sulfites ajoutés doit indiquer la source de l'allergène alimentaire (le cas échéant), le mot « gluten » et la ou les sources du gluten (le cas échéant), et, si le produit contient 10 p.p.m. de sulfites ajoutés ou plus, les mots « sulfites » ou « agents de sulfitage ». Pour plus de clarté, la source d'un allergène alimentaire doit être indiquée par le nom comme mentionné au paragraphe 91.2 du Règlement. Par exemple, si la caséine est l'ingrédient utilisé, le nom lait doit apparaître après l'en-tête Allergène, et les deux doivent être en gras. Si la protéine germinale de blé dégraissé est l'ingrédient utilisé, le nom gluten, en gras, doit apparaître après l'en-tête Allergène, suivi du mot (blé) entre parenthèses, également en gras. Conformément au paragraphe 93.1 (11) du Règlement, la mention « Allergène » doit être en gras, suivie de la mention des sources d'allergènes alimentaires ou de gluten et des sulfites ajoutés », également en gras. Par exemple, si le produit contient du lait, du blé et des sulfites, la mention apparaîtrait comme suit : Allergène : gluten (blé), lait, sulfites Pour de plus amples renseignements, veuillez consulter l'annexe 1 de la présente ligne directrice. L'étiquetage préventif des allergènes n'est pas requis, à moins qu'on ne s'inquiète de la probabilité que le produit contienne des oligoéléments d'un allergène (par exemple, vous devriez inclure « peut contenir des arachides » s'il y a un risque de contamination croisée). Pour obtenir des renseignements sur les allergènes de contact ou de parfum, consultez les sous-sections sur les Ingrédients médicinaux ou Ingrédients non médicinaux. L'« Alerte à l'asthme » est requise si elle est décrite dans votre autorisation de mise en marché. L'en-tête « Contient de l'aspartame » est requis si le produit contient de l'aspartame. Aucun autre texte relatif à l'aspartame n'est requis. Vous ne pouvez pas utiliser d'autres mentions « contient » ou « sans substance » (par exemple, sans colorant, sans gluten) dans le TIP conformément au paragraphe 93.1 (1) du Règlement. Si elle est vraie et vérifiable, cette information peut figurer ailleurs sur l'étiquette. |
| 6.d.3 | (Selon le cas) Mises en garde – inflammabilité / Flammability warning |
Conformément au Règlement sur les produits chimiques et contenants de consommation (qui est incorporé à la partie 5 du Règlement) :
|
| 6.d.4 | (S'il y a lieu) Mises en garde – Étouffement / Choking Warning |
Incluez toutes les mises en garde contre le danger de suffocation applicables, tel que décrit dans votre autorisation de mise en marché (paragraphe 93.1 (10) du Règlement). |
| 6.d.5 | Ne pas utiliser / Do not use |
Énumérez toutes les contre-indications applicables au produit, telles qu'elles sont décrites dans votre autorisation de mise en marché, y compris « ne pas utiliser le produit à moins qu'un praticien de soins de santé ait donné un diagnostic préalable », le cas échéant (paragraphe 93.1 (10) du Règlement). |
| 6.d.6 | Consultez un praticien de soins de santé avant l'utilisation (si) / Ask a health care practitioner before use (if) |
Énumérez toutes les mises en garde pour les personnes qui ont des problèmes de santé préexistants ou pour les personnes qui présentent des symptômes particuliers, conformément à votre autorisation de mise en marché (paragraphe 93.1 (10) du Règlement). Énumérez toutes les mises en garde relatives aux interactions, y compris avec d'autres PSN, des drogues ou des aliments, telles qu'elles sont décrites dans votre autorisation de mise en marché (paragraphe 93.1 (10) du Règlement). Les énoncés sur l'utilisation ou l'évitement pendant la grossesse et l'allaitement devraient être inclus ici, comme il est indiqué dans votre autorisation de mise en marché (paragraphe 93.1 (10) du Règlement). Les solutions de rechange acceptables pour « praticien de soins de santé » sont : « fournisseur de soins de santé », « professionnel de la santé », « docteur », « médecin » ou « dentiste » (le cas échéant). Les solutions de rechange acceptables pour « health care practitioner » en anglais sont : « health care provider », « health care professional », « doctor », « physician » ou « dentist » (le cas échéant). |
| 6.d.7 | Lorsque vous utilisez ce produit / When using this product |
Énumérez les effets secondaires notables que le consommateur peut subir, tels qu'ils sont décrits dans votre autorisation de mise en marché (paragraphe 93.1 (10) du Règlement). Énumérez les substances (par exemple, l'alcool, les sédatifs) ou les activités (par exemple, faire fonctionner de la machinerie, conduire une voiture) que les consommateurs devraient éviter lorsqu'ils utilisent le produit, comme il est indiqué dans votre autorisation de mise en marché (paragraphe 93.1 (10) du Règlement). |
| 6.d.8 | Cessez d'utiliser et consultez un praticien de soins de santé (si) / Stop use and ask a health care practitioner (if) |
Énumérez tous les signes de toxicité ou autres effets indésirables qui obligeraient une personne à cesser immédiatement d'utiliser le produit, s'il y a lieu et conformément à votre autorisation de mise en marché (paragraphe 93.1 (10) du Règlement).
Les solutions de rechange acceptables pour « praticien de soins de santé » comprennent : « fournisseur de soins de santé », « professionnel de la santé », « docteur », « médecin » ou « dentiste » (le cas échéant). En anglais, les solutions de rechange acceptables pour « health care practitioner » sont : « health care provider », « health care professional », « doctor », « physician » ou « dentist » (le cas échéant). |
| 6.d.9 | Gardez hors de la portée des enfants / Keep out of reach of children |
Cette sous-section doit comprendre une mise en garde au sujet d'une surdose accidentelle ou d'une ingestion accidentelle, s'il y a lieu (par exemple, s'il est inclus dans votre autorisation de mise en marché). Par exemple : « En cas de surdosage ou d'ingestion, appelez un centre antipoison ou obtenez immédiatement une aide médicale »/« In case of overdose/ingestion, call a poison control centre or get medical help right away. » |
| 6.d.10 | Mises en garde (suite) / Warnings (continued) |
Veuillez inclure d'autres mises en garde obligatoires, décrites dans votre autorisation de mise en marché, qui n'ont pas été incluses dans les en-têtes des mises en garde (paragraphe 93.1 (10) du Règlement). Indiquez que des renseignements supplémentaires sont disponibles sur d'autres parties de l'étiquette et du dépliant de l'emballage, si applicable. |
| 6.e | Mode d'emploi / Directions |
Vous devez inclure le mode d'emploi, y compris les instructions pour la posologie (nombre et fréquence d'unités posologiques) et la durée, le cas échéant (paragraphe 93.1 (14) du Règlement). Vous devriez également inclure la voie d'administration. Tous les renseignements doivent correspondre à ceux qui figurent dans votre autorisation de mise en marché. Les instructions posologiques pour des sous-populations spécifiques doivent refléter les informations décrites dans l'autorisation de mise en marché de votre produit. Par exemple, « Adultes (18 ans et plus) et adolescents (12 à 17 ans) : Prendre un comprimé trois fois par jour. Enfants (de 6 à 11 ans) : Prendre un comprimé une fois par jour. » Si l'autorisation de mise en marché prévoit des posologies propres à plusieurs sous-populations, vous pouvez choisir de commercialiser le produit à une seule sous-population. Dans ce cas, les informations sur la posologie ne s'appliqueront qu'à cette sous-population. Par exemple : « Enfants (de 6 à 11 ans) : Prendre un comprimé une fois par jour. » |
| 6.f | Autres renseignements / Other information |
Cette section devrait se limiter aux renseignements d'entreposage et d'emmagasinage ou à d'autres instructions particulières (par exemple, pour l'élimination). Si les conditions d'emmagasinage recommandées sont indiquées ailleurs sur la même étiquette, l'en-tête « Autres renseignements” / Other information » n'est pas obligatoire dans le TIP (paragraphe 93.1 (16) du Règlement). Tout renseignement d'entreposage exigé par l'autorisation de mise en marché de votre produit doit être indiqué sur l'étiquette conformément au paragraphe 93.1 (15) du Règlement. Le cas échéant, les conditions d'emmagasinage recommandées devraient être indiquées en utilisant l'une des formulations suivantes :
Vous devez inclure des renseignements sur la période de stabilité du produit et sur la façon dont il devrait être entreposé après son ouverture, son activité ou sa reconstitution (par exemple, « Réfrigérer après l'ouverture » ou « Le produit devrait être utilisé dans les 24 heures suivant la dilution »), le cas échéant. Des mises en garde générales, le cas échéant, devraient également être incluses dans cette section (par exemple « Éviter la lumière directe » ou « Entreposer dans un endroit sec »). |
| 6.g | Ingrédient(s) non médicinal (médicinaux) / Non-medicinal ingredient(s) |
Veuillez inclure une liste qualitative des ingrédients non médicinaux par nom usuel (paragraphe 93.1 (17) du Règlement). Conformément au paragraphe 87 (3), les ingrédients non médicinaux peuvent être inscrits selon la Nomenclature internationale des ingrédients cosmétiques (INCI), peu importe l'autorisation de mise en marché. Les abréviations des noms latins binomiaux peuvent également être utilisées, le cas échéant. Les ingrédients non médicinaux peuvent être énumérés par ordre alphabétique ou par ordre de quantité. Les ingrédients non médicinaux qui sont des allergènes alimentaires, des sources de gluten ou des sulfites ajoutés doivent être indiqués dans cette section, comme pour tout autre ingrédient non médicinal ajouté, même s'ils sont énumérés dans la section des mises en garde (voir 7.d.2 ci-dessus). Si l'ingrédient non médicinal est un allergène alimentaire, il est recommandé d'indiquer la source de l'allergène alimentaire entre parenthèses en caractères gras (par exemple, caséine [lait]) après l'ingrédient allergène, s'il y a lieu. Si l'ingrédient non médicinal est une source de gluten, il est recommandé d'afficher le mot « gluten » entre parenthèses en caractères gras (par exemple, blé [gluten]), s'il y a lieu. Si l'ingrédient non médicinal est un sulfite ajouté, tel que défini dans le Règlement, vous devez utiliser les noms « sulfites » ou « agents de sulfitage » ou l'indiquer individuellement par le nom applicable prévu dans la définition de sulfites ajoutésau paragraphe 1 (1) du Règlement. Toutefois, les noms « dithionite de sodium », « dioxyde de soufre » ou « acide sulfurique » doivent être suivis, entre parenthèses, des noms « sulfites » ou « agents de sulfitage » (alinéa 91.4 (a) du Règlement). Pour tous les produits, si vous transférez la liste des ingrédients non médicinaux, notamment des ingrédients allergènes, de l'étiquette physique à un dépliant, une notice d'accompagnement ou un site Web, vous devez indiquer clairement sur l'étiquette physique où trouver les renseignements déplacés au moyen d'une mention sous le titre Info-produit (paragraphe 93.3 (4) du Règlement). Si votre produit contient des allergènes de parfums, comme ceux qui sont mentionnés à l'annexe III du Règlement relatif aux produits cosmétiques de la Commission européenne, ils doivent, comme pour tout autre ingrédient non médicinal, être énumérés dans la section « Ingrédient non médicinal » par le nom usuel de chaque fragrance, ou l'INCI, le cas échéant, et non simplement par le terme « parfum » ou « fragrance ». Vous pouvez toutefois regrouper ces ingrédients sous le terme « parfum », mais vous devez ensuite énumérer les fragrances utilisées. Par exemple, vous pouvez les inscrire comme Ingrédients non médicinaux […] parfum (alcool Cinnamyl, Citral, hydroxycitronellal). Conformément au paragraphe 93.1 (17) du Règlement, vous devez énumérer les ingrédients de tout mélange breveté utilisé, c'est-à-dire que vous ne devez pas vous limiter à la mention « mélange exclusif/breveté ». Les renseignements sur les agents de conservation exigés par la réglementation devraient figurer ici (par exemple, le mercuriel). Cela comprend la quantité de mercure contenue dans le produit s'il contient du mercure ou ses sels ou dérivés comme ingrédient non médicinal. Les ingrédients à base de sucre devraient être regroupés entre parenthèses après le nom « sucre(s) », par ordre décroissant de poids. Cette mesure aidera les consommateurs à identifier toutes les sources de sucre ajouté à un PSN et constitue une approche semblable à ce qui est exigé sur les étiquettes des aliments. |
| 6.h | Questions? | Vous devez fournir les coordonnées du titulaire de la licence de mise en marché ou d'un représentant à qui ces activités ont été désignées par contrat, auprès de qui les consommateurs peuvent obtenir des réponses à leurs questions, signaler des problèmes ou signaler des effets indésirables associés au produit (paragraphe 93.1 (18) du Règlement). Les coordonnées fournies doivent comprendre la représentation numérique complète du numéro de téléphone, de l'adresse de courriel ou de l'adresse du site Web (c.-à-d. l'adresse URL) de la personne-ressource conformément au paragraphe 93.1 (18) du Règlement. Vous pouvez également inclure une adresse postale en plus de ces coordonnées, ou toute autre information qui permet de communiquer avec une personne-ressource au Canada, mais cette mesure est optionnelle. Cette section peut également comprendre le symbole d'un récepteur téléphonique (( ou )), mais le symbole ne peut pas remplacer le titre « Questions? ». |
3.0 Format
Conformément à l'article 88 du Règlement, les renseignements exigés sur l'étiquette d'un PSN doivent être clairement affichés, bien en vue et accessibles au consommateur lorsqu'il achète et utilise le produit. Pour un contraste optimal, tout le texte requis doit être imprimé avec une seule couleur qui est l'équivalent visuel d'un caractère noir uni à 100 % (le noir d'écran, le bleu foncé, le brun foncé, le vert foncé et le violet foncé à 100 % sont acceptables) sur un fond blanc ou neutre avec une teinte de couleur de 5 % maximum.
Le texte doit être rédigé dans une police standard sans empattement d'au moins 6 points, sauf pour les ingrédients non médicinaux, qui doivent avoir au moins 5,5 points. Si vous utilisez une police de caractères condensée, la police de 6 points serait de 5,5 points, sauf pour les ingrédients non médicinaux, où la police de 5,5 points serait de 5 points. Les renseignements secondaires qui ne sont pas requis par le Règlement, comme la protection du droit d'auteur et le brevet du produit, peuvent être de n'importe quelle taille de police. Les caractères ne doivent pas entrer en contact les uns avec les autres ni avec les éléments du TIP. Il est recommandé que les en-têtes et les sous-titres soient justifiés à gauche et en gras.
3.1 Spécifications concernant le tableau Info-produit
| - | Élément de conception |
Format | |
|---|---|---|---|
| 7.a | Panneau | On peut utiliser deux panneaux ou plus de l'étiquette (un panneau en anglais et un panneau en français) pour afficher le TIP.
|
|
| 7.b | Style et taille de la police |
Conformément à l'alinéa 93.2f) du Règlement, les renseignements indiqués sous chaque en-tête doivent être de type régulier. Par conséquent, vous ne pouvez pas utiliser :
Les caractères ne doivent pas se toucher ni toucher les lignes du TIP (alinéa 88e) du Règlement). L'espacement des caractères ne devrait pas être supérieur à +/– 5 % de la norme pour ce style de police afin que le texte soit facile à lire. Au besoin, la largeur de caractère du type peut être réduite horizontalement de 10 % (autrement dit, jusqu'à une échelle horizontale de 90 %). |
|
| 7.c | Couleur (fond et impression) |
Conformément à l'alinéa 88 c) du Règlement, la couleur de fond du TIP doit être blanche ou un fond neutre uniforme avec un maximum de 5 % de teinte. Ce niveau de teinte ne donne qu'une légère couleur au fond. Pour un contraste optimal, tous les mots et toutes les lignes devraient être imprimés d'une seule couleur qui est l'équivalent visuel de noir 100 %, comme le noir, le bleu foncé, le brun foncé, le vert foncé et le violet foncé 100 %. |
|
| 7.d | Titre : Info-produit | Police recommandée : |
|
| Taille de police recommandée : |
|
||
| Justification recommandée : |
|
||
| Majuscule : |
|
||
| 7.e | Titre : Info- produit (suite) Info-médicament (suite) |
Police recommandée : |
|
| Taille de police recommandée : |
|
||
| Justification recommandée : |
|
||
| Majuscule : |
|
||
| 7.f | En-têtes Vous devez utiliser 7 points |
Police recommandée : |
|
| Taille de police recommandée : |
|
||
| Justification recommandée : |
|
||
| Majuscule : |
|
||
| 7.g | Sous-titres (par exemple, Ne pas utiliser, Garder hors de portée des enfants) |
Police recommandée : |
|
| Taille de police recommandée : |
|
||
| Justification recommandée : |
|
||
| Majuscule : |
|
||
| 7.h | Texte | Police recommandée : |
|
| Taille de police recommandée : |
|
||
| Justification recommandée : |
|
||
| Majuscule : |
|
||
| 7.i | Puces | Il est possible d'utiliser des puces carrés ou rondes pleines. Il est recommandé d'utiliser des puces avec une police de caractères de 3 points ou plus. | |
| 7.j | Listes à puces | Vous pouvez utiliser des puces sur la même ligne qu'un titre ou un sous-titre, sauf pour le titre « Mises en garde». Le contenu des puces peut passer à la ligne suivante. Pour les sections comportant plusieurs puces, la fin d'une puce devrait être séparée du début de la suivante par au moins un espace carré de la taille de la lettre « m ». |
|
| 7.k | Bordure extérieure, lignes horizontales et lignes fines | Recommandations relatives aux bordures des encadrés :
Lignes horizontales (pour séparer les en-têtes, y compris celle du TIP) :
Lignes fines (pour séparer les sous-titres de la section « Avertissements ») :
La distance entre les lignes horizontales ou les lignes fines et les caractères devrait être cohérente. |
|
| *Si la police Helvetica Neue n'est pas disponible, on peut lui substituer une police acceptable selon le « Style de police » (8 b) ci-dessus. | |||


Équivalent textuel
Cette image montre deux exemples du même TIP. Les rubriques du tableau sont, dans l'ordre : Info-produit, Ingrédients médicinaux, Utilisations, Mises en garde, Mode d'emploi, Autres informations, Ingrédients non médicinaux et Questions avec un point d'interrogation. Le premier exemple illustre une situation où le tableau Info-produit se poursuit sur un panneau additionnel. Après l'en-tête « Mises en garde », il y a une séparation et un tableau Info-produit additionnel débute avec le titre Info-produit (suite), suivi de l'en-tête « Mode d'emploi ».
Chaque rubrique ou sous-rubrique commence sur une nouvelle ligne. Les titres sont séparés les uns des autres par un trait horizontal épais, et chaque sous-titre de la section des mises en garde est séparé du suivant par un trait horizontal.
Sous le titre Mises en garde, on trouve les sous-titres suivants : Allergènes, Ne pas utiliser, Consulter un praticien de soins de santé avant l'utilisation si, Lors de l'utilisation de ce produit, consultez un praticien de soins de santé si, Cessez d'utiliser ce produit et consultez un praticien de soins de santé si, et Garder hors de la portée des enfants. Tous les titres sont en gras et commencent par une majuscule.
Il y a du texte fictif après chaque titre et sous-titre, sous forme de phrases courtes ou de puces.
3.2 Utilisation des graphiques
Vous ne devez pas utiliser de graphiques dans le TIP à moins qu'il ne s'agisse de symboles de marque de commerce (c.-à-d.® ou™), de symboles recommandés par Santé Canada, ou exigés par le Règlement ou le Règlement sur les produits chimiques et contenants de consommation, comme décrit à l'article 93 du Règlement. Des exemples de symboles acceptables incluent :
- un octogone rouge avant les avertissements spécifiques;
- un téléphone, une icône de récepteur téléphonique, des icônes de médias sociaux ou d'autres symboles largement acceptés indiquant des coordonnées modernes sous « Questions? »;
- des graphiques liés à une évaluation des effets indésirables ou des signaux de sécurité;
- un symbole de marque de commerce ou de marque déposée pour les noms d'ingrédients portant une marque de commerce.
Vous ne pouvez pas utiliser de graphiques tels que des formats de comprimés, des aliments ou des représentations d'ingrédients dans le TIP conformément à l'article 93.1 du Règlement. Vous pouvez utiliser ces graphiques à l'extérieur du TIP sur le même panneau d'étiquette si l'espace le permet.
3.3 Emballage
Les trousses ou les produits co-emballés doivent porter un TIP sur l'étiquette extérieure de la trousse ou des produits co-emballés, conformément au paragraphe 93.1 (1), le cas échéant. Conformément à l'article 8 du Règlement, il doit y avoir un TIP distinct pour chaque PSN dans la trousse (autrement dit, pour chaque produit qui a un NPN ou un DIN-HM). Conformément à l'alinéa 88 (b) et au paragraphe 93.1 (1) du Règlement, les tableaux des PSN dans la trousse ou le co-emballage doivent être accessibles au point de vente sans devoir briser l'emballage extérieur. Dans la mesure du possible, vous devriez aussi imprimer le TIP sur l'emballage de chaque PSN, en plus de l'emballage extérieur de la trousse ou des produits co-emballés. L'étiquette extérieure de la trousse ou du co-emballage doit également être conforme aux exigences pour tout autre type de produits inclus dans la trousse ou le co-emballage (par exemple, un cosmétique). Veuillez consulter les règlements respectifs des autres types de produits, comme le Règlement sur les instruments médicaux, le Règlement sur les aliments et drogues ou le Règlement sur les cosmétiques pour connaître les exigences relatives aux étiquettes propres à ces produits.
Les exigences en matière d'emballage de sécurité, telles que décrites à l'article 95 du Règlement sur les produits de santé naturels, doivent être respectées afin que les clients sachent que le produit n'a pas été ouvert au moment de l'achat. Un emballage de sécurité peut comprendre, par exemple, des sceaux, des emballages transparents, des insertions en coton et des couvercles qui sont scellés jusqu'à leur ouverture.
L'emballage de sécurité est seulement requis pour les PSN destinés à un usage humain qui sont :
- un rince-bouche;
- à inhaler, ingérer ou insérer dans le corps;
- pour usage ophtalmique.
Pour plus de clarté, l'emballage de sécurité n'est pas requis pour les produits topiques, l'aromathérapie ou d'autres produits qui sont diffusés dans l'air, ou pour les pastilles, conformément au paragraphe 95 (2) du Règlement.
Pour les produits emballés dans un emballage de sécurité, conformément au paragraphe 95 (3) du Règlement, vous devez mentionner la caractéristique de sécurité sur l'étiquette, à moins qu'elle ne soit évidente dans l'emballage du produit (paragraphe 95 (4) du Règlement). Si la caractéristique de sécurité fait partie de l'emballage extérieur, la référence doit figurer sur l'étiquette extérieure conformément à l'alinéa 95 (3) (b) du Règlement.
Les contenants sous pression doivent comporter des pictogrammes de danger et des mises en garde sur l'espace principal de l'étiquette pour s'assurer que les consommateurs sont informés des préoccupations potentielles en matière de sécurité, conformément à l'article 96 du Règlement, aux articles A01.061 à A.01.063 du Règlement sur les aliments et drogues et au Règlement sur les produits chimiques et contenants de consommation. Pour de plus amples renseignements, veuillez consulter le Manuel de référence pour le Règlement sur les produits chimiques et contenants de consommation (2001) de la Loi sur les produits dangereux.
Les mentions concernant les mises en garde, l'emballage de sécurité pour enfants et l'entreposage sécuritaire (par exemple, « Garder hors de la portée des enfants ») décrits à l'article 97 du Règlement doivent figurer sur l'étiquette des PSN lorsqu'il s'agit d'une exigence de l'autorisation de mise en marché du produit. Si ces renseignements sont inclus dans le TIP, il n'est pas nécessaire de les reproduire ailleurs sur l'emballage.
3.4 Étiquettes innovantes
Aux fins du présent document de référence, une étiquette innovante est considérée comme une extension physique de l'étiquette d'un produit. Parmi les exemples d'étiquettes innovantes, mentionnons les étiquettes-dépliants (auto-adhésives), les étiquettes en accordéon, les panneaux à charnières ou les étiquettes pliables.
Vous pouvez utiliser des étiquettes innovantes pour afficher le contenu requis sur l'étiquette lorsque l'espace est insuffisant sur l'étiquette standard. Un exemple de contenu obligatoire est l'information contenue dans le TIP. Les formats d'étiquettes innovantes doivent être conformes aux règlements applicables et aux lignes directrices, notamment les exigences relatives à la police, au contraste et au format, comme il est indiqué à l'article 88 du Règlement.
Aux fins du présent document, les eTIP, les dépliants (apposés ou attachés au contenant) et les notices d'accompagnement ne sont pas considérés comme des étiquettes innovantes. Ils peuvent appuyer les renseignements sur l'étiquette, mais ils ne peuvent pas être utilisés comme solution de rechange à l'information qui doit être présentée sur l'étiquette, à moins qu'il ne soit expressément prévu dans les assouplissements.
Principes généraux :
- Les étiquettes innovantes sont considérées comme des extensions de l'étiquette. Vous pouvez utiliser une étiquette innovante si votre produit n'utilise qu'un seul panneau comme aire d'affichage principale (par exemple en utilisant un panneau bilingue comme espace principal de l'étiquette).
- Les consommateurs doivent pouvoir accéder au contenu de l'étiquette innovante au moment de la sélection du produit, avant l'achat, et sans détruire ou compromettre l'intégrité de l'étiquette ou de l'emballage, conformément à l'article 88 du Règlement.
- Si vous utilisez une étiquette innovante, vous devriez vous assurer que les informations suivantes sont visibles pour le consommateur au point de sélection sans que celui-ci ait à manipuler l'étiquette innovante :
- Pour les produits avec un TIP :
- le titre « Info-produit » ou « Info-médicament »;
- la section « Ingrédients médicinaux »;
- la section « Utilisations » (si la section « Utilisations » n'a pas déjà été déplacée sur l'espace principal);
- une mention dirigeant le consommateur vers la suite du tableau sur l'étiquette innovante.
- Pour les produits sans TIP, vous devez vous assurer que les informations suivantes sont visibles pour le consommateur au point de sélection sans que celui-ci ait à manipuler l'étiquette :
- la liste des « Ingrédients médicinaux » et des « Utilisations ».
- Pour les produits avec un TIP :
4.0 Assouplissements
Il se peut que certains produits et formats d'emballage n'aient pas suffisamment d'espace pour inclure un TIP selon le format standard sur l'étiquette. Les fabricants peuvent utiliser les assouplissements décrits dans le Règlement (voir le tableau 8 ci-dessous) si un TIP ne peut pas être affiché sur l'étiquette selon le format requis.
L'utilisation des assouplissements ne modifie pas l'ordre des informations figurant dans le TIP. Cela signifie que certains produits afficheraient un tableau complet sur une étiquette, tandis que d'autres pourraient avoir un tableau partiel sur une étiquette et un tableau complet sur un dépliant ou un eTIP, selon les renseignements en question retirés. Tel qu'il est indiqué au paragraphe 93.3 (5) du Règlement, les dépliants ne sont pas tenus de reproduire un TIP complet, à moins que cela ne soit indiqué dans les conditions établies dans la section sur les petits emballages du présent document de référence et à l'article 94 du Règlement. Dans tous les cas, les renseignements nécessaires à la sélection sécuritaire du produit doivent figurer sur l'étiquette extérieure, conformément à l'alinéa 88 (b) du Règlement.
Dans les situations où des renseignements sont transférés à l'extérieur du TIP, une mention indiquant au consommateur où trouver les renseignements déplacés doit figurer immédiatement sous le titre « Info-produit », tel qu'il est indiqué aux paragraphes 93.3 (4) et 93.6 (5) du Règlement, dans une police et un style conformes aux en-têtes de l'étiquette. Par exemple, « Pour le tableau Info-produit complet, incluant les informations déplacées, visitez www.nomdusiteweb.ca / For full Product Facts table, including removed information, visit www.websitename.ca » ou « Lire la notice [ou le dépliant] pour l'ensemble des avertissements avant l'utilisation/Read package insert [or leaflet] for complete warnings before use » ou « Pour une liste complète des ingrédients non-médicinaux, consultez le dépliant en attache/For a full list of non-medicinal ingredients, please see leaflet ».
Si vous utilisez un eTIP, vous devriez suivre les normes techniques du Tableau canadien d'information sur le médicament décrites dans le document Lignes directrices : Normes techniques sur le Tableau électronique canadien d'information sur le médicament (eTCIM). Si vous utilisez un eTIP, l'URL doit être incluse dans la mention indiquant aux consommateurs les renseignements déplacés sous le titre « Info-produit », comme il est indiqué aux paragraphes 93.3 (4) et 93.6 (5) du Règlement.
Remarque : L'utilisation d'un eTIP ne remplace pas l'utilisation d'un TIP sur l'étiquette physique du produit.
Les assouplissements suivants (voir le tableau 8) peuvent être appliqués au besoin, comme il est indiqué aux articles 93.3 et 93.6 du Règlement :
| - | En-tête/ Élément de conception |
Assouplissement |
|---|---|---|
| 8.a | Info-produit / Product Facts |
Si votre TIP couvre plus d'un panneau, vous pouvez supprimer les titres « Info-produit (suite) » et « Product Facts (continued) » et orienter le consommateur vers la suite de l'information (par exemple, en utilisant une flèche). |
| 8.b | Ingrédient(s) médicinal (médicinaux) (dans chaque unité posologique) / Medicinal ingredient(s) (in each dosage unit) |
Vous pouvez déplacer les renseignements sur la matière d'origine des « Ingrédients médicinaux » de l'étiquette à un dépliant apposé ou attaché au contenant extérieur du produit, à une notice d'accompagnement ou à un eTIP (paragraphe 93.3 (3) du Règlement). Conformément au paragraphe 93.3 (5) du Règlement, les renseignements qui doivent figurer dans une notice d'accompagnement ou un eTIP doivent satisfaire aux exigences de formatage du TIP (voir la section 3.0). Si les renseignements sont transférés à un eTIP, l'URL doit être affichée sous le titre du TIP. Remarque : Il n'est pas recommandé de retirer les désignations de souches pour les micro-organismes vivants. |
| 8.c | Utilisations / Use(s) |
Vous pouvez déplacer le contenu de la section « Utilisations » sur l'espace principal de l'étiquette (paragraphe 93.1 (9) du Règlement). Les « Utilisations » doivent correspondre aux renseignements indiqués dans votre autorisation de mise en marché et ne peuvent être combinées à des énoncés promotionnels. Au moins une « Utilisation » recommandée doit figurer sur l'étiquette en tout temps (à l'exception des produits homéopathiques. Pour de plus amples renseignements sur l'étiquetage des produits homéopathiques, voir l'annexe sur l'étiquetage des produits homéopathique.) |
| 8.d | Autres renseignements / Other information |
Vous pouvez déplacer le contenu des « Renseignements d'entreposage/d'emmagasinage » (par exemple, les renseignements sur les conditions d'emmagasinage) ailleurs sur l'étiquette et retirer l'en-tête du TIP (paragraphe 93.1 (16) du Règlement). |
| 8.e | Ingrédient(s) non médicinal (médicinaux) / Non-medicinal ingredient(s) |
Vous pouvez supprimer la section « Ingrédients non médicinaux » et placer les renseignements ailleurs sur l'étiquette, sur un dépliant, une notice d'accompagnement ou un site Web (paragraphes 93.3 (1) et (2) du Règlement). |
| 8.f | Tableau Info-produit bilingue | Vous pouvez utiliser un TIP bilingue au lieu d'un TIP en français et un autre en anglais (alinéa 93.1 (1) f) (i) du Règlement). |
| 8.g | Police de caractères condensée | Vous pouvez également réduire la largeur du caractère à l'horizontale de 10 % (autrement dit, 90 % de l'échelle horizontale). Vous pouvez utiliser une police de caractères condensée pour la section « Ingrédients non médicinaux » conformément à l'alinéa 93.3 (1) c) du Règlement (c.-à-d. une police de 5,5 points condensée, qui apparaîtrait comme une police de 5 points). Vous pouvez également utiliser une police de caractères condensée de 6 points (qui apparaîtrait comme 5,5 points) pour tous les autres renseignements requis conformément à l'alinéa 93.3 (1) c) du Règlement. |
| 8.h | En-têtes | Pour toutes les sections, vous pouvez commencer le texte immédiatement après l'en-tête. |
| 8.i | Bordure extérieure, lignes fines et lignes horizontales (lignes noires pleines séparant les en-têtes) |
Lorsque plusieurs panneaux se suivent, utilisez un cadre unique et continu plutôt qu'un cadre autour de chaque panneau individuel. Lorsque vous appliquez un cadre continu, tous les panneaux du TIP devraient conserver une orientation cohérente. Le texte ne doit pas se trouver à moins de 3,175 mm d'une ligne de pliage. Vous pouvez réduire la taille des règles à 1,0 point pour l'encadré et les lignes horizontales. Les lignes fines peuvent être retirées de la section « Avertissements » et le contenu peut commencer immédiatement après le titre de la section. Chaque section devrait commencer sur une nouvelle ligne avec les titres en gras. |

Équivalent textuel
La figure 3 montre un exemple de TIP utilisant toutes les flexibilités disponibles Ces flexibilités s'appliquent à tous les produits. Les rubriques sont présentées ensemble avec le titre en anglais, suivi d'une barre oblique, puis du titre français. Chaque rubrique comporte un texte fictif en anglais, puis en français, séparés par une barre oblique.
Les en-têtes du tableau sont, dans l'ordre : Product Facts / Info Produit, Medicinal ingredient / Ingrédients médicinaux, Warnings / Mises en garde, Directions / Mode d'emploi et Questions avec un point d'interrogation. Toutes les rubriques sont en gras et commencent par une majuscule. Sous le titre Warnings / Mises en garde, on trouve des sous-titres et du texte factice. Sous l'en-tête Mises en garde, il y a des sous-titres, par exemple, allergènes / allergens et consulter un praticien de soins de santé avant l'utilisation si / ask a health care practitioner before use if. Toutes les en-têtes sont en caractère gras et débutent avec une lettre majuscule.
Les assouplissements suivants (voir le tableau 9) ne sont accessibles que si votre produit n'utilise qu'un seul panneau comme aire d'affichage principale (par exemple en utilisant un panneau bilingue comme espace principal de l'étiquette).
| - | En-tête/ Élément de conception |
Assouplissement |
|---|---|---|
| 9.a | Style et taille de la police | L'espacement des caractères n'a pas besoin de respecter la limite de taille de +/– 5 % indiquée dans le tableau 7, à condition qu'il soit clair et lisible. |
| 9.b | Bordure extérieure, lignes fines et lignes horizontales (lignes noires pleines séparant les en-têtes) |
Les lignes fines et les lignes horizontales peuvent être retirées et le contenu peut commencer immédiatement après le titre de la section. Chaque section doit commencer sur une nouvelle ligne avec les titres de section en gras. Il n'est pas nécessaire d'avoir un espace de deux caractères de la largeur de six points entre la fin de chaque ligne fine et le cadre de l'encadré. La bordure extérieure peut être retiré si l'étiquette environnante est d'une couleur différente de l'arrière-plan du TIP et qu'elle crée une bordure naturelle. |
| 9.c | Ingrédients médicinaux / Medicinal ingredients |
La section des ingrédients médicinaux peut se poursuivre sur la partie intérieure de l'étiquette innovante si le contenu de la section « Utilisations » a été déplacé sur l'espace principal (voir 9.a.5 ci-dessus). Si c'est le cas, il faut alors indiquer clairement que la section des ingrédients médicinaux se poursuit sur la partie intérieure de l'étiquette innovante. On peut utiliser les abréviations des noms latins binomiaux, au besoin. |
| 9.d | Ingrédient(s) non médicinal (médicinaux) / Non-medicinal ingredient(s) |
On peut utiliser les abréviations des noms latins binomiaux, au besoin. |
| 9.e | Mises en garde / Warnings |
Les mises en garde relatives à la sélection du produit (voir le tableau 11) doivent figurer sur l'étiquette, sans exception. Cela comprend les mises en garde liées à la voie d'administration, à la somnolence ou à l'excitabilité. Elles peuvent être en caractère gras.
Les mises en garde relatives à l'utilisation du produit (voir le tableau 11) peuvent être retirées du TIP et placées sur une notice d'accompagnement ou un dépliant apposé ou attaché au contenant extérieur du produit. Ces mises en garde ne doivent pas être déplacées vers un eTIP, sauf pour les produits à faible risque, pour lesquels on peut déplacer les mises en garde relatives à l'utilisation du produit vers un tel espace, pourvu qu'il y ait une mention de l'endroit où l'information complète est disponible. Voici quelques exemples de mises en garde relatives à l'utilisation du produit : « Lorsque vous utilisez ce produit/When using this product » ou « Cessez l'utilisation et consultez un praticien de soins de santé si/Stop use and ask a health care practitioner if ». |
Conformément au paragraphe 93.3 (5) du Règlement, les produits qui utilisent une notice d'accompagnement ou qui affichent une adresse URL pour diriger les consommateurs vers un eTIP doivent afficher un TIP complet sur la notice d'accompagnement ou la page Web, selon le cas.
Vous n'êtes pas tenus de reproduire un TIP complet sur les dépliants, à moins d'indications contraires dans les conditions établies dans la section sur les petits emballages de la présente ligne directrice et telles qu'elles sont décrites à l'article 94 du Règlement. Dans tous les cas, les renseignements nécessaires à une sélection sûre du produit doivent figurer sur l'étiquette extérieure du produit physique. La taille et le type de police, tels qu'ils sont décrits à l'article 88 du Règlement, doivent être respectés, et il doit y avoir une mention sous le titre Info-produit indiquant au consommateur le nouvel emplacement des renseignements déplacés, comme indiqué aux paragraphes 93.3 (4) et 93.6 (5) du Règlement.
Pour plus de clarté, le tableau 10 indique les éléments à inclure sur chaque type d'étiquette.

Équivalent textuel
La figure 4 montre un exemple de TIP utilisant les flexibilités disponibles pour le tableau si un seul panneau est utilisé comme panneau d'affichage principal. Ceci s'applique également à tous les produits. Les en-têtes sont présentées de façon combinée, avec l'en-tête en anglais qui est suivie d'une barre oblique et de la version français de la même en-tête. Chaque rubrique comporte un texte fictif en anglais, puis en français, séparés par une barre oblique.
Les en-têtes dans le tableau sont, dans l'ordre, Product Facts / Info-produit, Medicinal ingredient / Ingrédients médicinaux, Warnings / Mises en garde, Directions / Mode d'emploi et Questions avec un point d'interrogation. Toutes les rubriques sont en gras et commencent par une majuscule. Sous le titre Warnings / Mises en garde, on trouve des sous-titres et du texte factice, par exemple allergènes / allergens, et consulter un praticien de soins de santé avant l'utilisation si / ask a health care practitioner before use if.
Ce tableau doit être lu conjointement avec les tableaux 8, 9 et 10, ainsi qu'avec la section sur les petites étiquettes et les emballages et produits exemptés.
| Élément | Espace principal | Visible sans manipulation de l'étiquette | TIP, le cas échéant | Étiquette innovante | Dépliant | Notice d'accompagnement | eTIP |
|---|---|---|---|---|---|---|---|
| Marque nominative | X | - | - | - | - | - | - |
| Numéro d'identification (NPN/DIN-HM) | X | - | - | - | - | - | - |
| Forme posologique | X | - | - | - | - | - | - |
| Stérile, le cas échéant | X | - | - | - | - | - | - |
| Contenu net | X | - | - | - | - | - | - |
| Le nom du titulaire de la licence ou de l'importateur | O | - | - | * | - | - | - |
| Voie d'administration | O | - | - | * | - | - | - |
| Le numéro de lot. | O | - | - | * | - | - | - |
| La date limite d'utilisation. | O | - | - | * | - | - | - |
| Titre « Info-produit »/ « Product Facts » | - | X | X | * | - | - | - |
| Titre « Ingrédients médicinaux » | - | X | X | * | - | - | - |
| Nom des ingrédients médicinaux et quantité par unité posologique, le cas échéant | - | - | O | * | - | - | - |
| Description de la matière d'origine | O | O | O | * | O | O | O |
| Activité | - | - | O | * | O | O | O |
| Utilisations | O | O | O | - | - | - | - |
| Mises en garde | - | - | X | * | - | - | - |
| Mises en garde relatives à la sélection du produit | - | - | X | * | - | - | - |
| Mises en garde relatives à l'utilisation du produit | - | - | O | * | * | * | - |
| Déclaration sur les allergènes, s'il y a lieu | - | - | X | * | - | - | - |
| Mode d'emploi | - | - | X | * | - | - | - |
| Autres renseignements | O | - | O | * | - | - | - |
| Titre « Ingrédients non médicinaux » et Ingrédients non médicinaux | O | - | O | * | O | O | O |
| Questions? (Coordonnées) | - | - | X | * | - | - | - |
| Exigence relative à la police et au contraste, le cas échéant | X | - | X | X | X | X | X |
| Mention des renseignements déplacés, le cas échéant | - | X | X | - | - | - | - |
Légende X = L'élément doit apparaître à cet endroit précis |
|||||||
| Point de sélection Mises en garde relatives à la sélection sont nécessaires pour prendre une décision d'achat en connaissance de cause. |
Point d'utilisation Mises en garde relatives à l'utilisation sont nécessaires pour utiliser le produit en toute sécurité. |
|---|---|
| Pour utilisation externe/rectale/vaginale uniquement | - |
| Pour utilisation dans le nez, les yeux et les oreilles uniquement | - |
| Déclaration sur les allergènes/alerte à l'asthme | - |
| Avertissement d'inflammabilité | - |
| Mises en garde contre le danger de suffocation | - |
| Ne pas utiliser (si) | - |
| Ne pas prendre d'autres produits | - |
| Demandez à un praticien de soins de santé avant d'utiliser ce produit si | Cessez d'utiliser et consultez un praticien de soins de santé si |
| Consultez un praticien de soins de santé si | - |
| Syndrome de Reye | - |
| Tenir hors de la portée des enfants | - |
| Lors de l'utilisation de ce produit (lié à la somnolence, à l'excitabilité ou à la vision floue) | Lors de l'utilisation de ce produit (non lié à la somnolence, à l'excitabilité ou à la vision floue) |
| D'autres mises en garde peuvent être nécessaires à la sélection ou à l'utilisation du produit selon la nature de la mise en garde, y compris celles identifiées dans le tableau 7 (7.d à 7.d.10). Veuillez communiquer avec Santé Canada à l'adresse indiquée à la section 7.0 du présent document si vous avez besoin de précisions supplémentaires. | |
4.1 Étiquetage des produits contenant six ingrédients médicinaux ou plus
Si le produit contient quatre ingrédients médicinaux ou plus, vous pouvez afficher la section « Ingrédients médicinaux » dans le TIP avec les ingrédients médicinaux, la quantité par unité posologique et l'activité(le cas échéant) de l'une des façons suivantes :
- présentés sur la même ligne, séparés par des puces;
- mis en colonnes pour faire apparaître le texte dans les deux langues officielles sur la même ligne;
- texte justifié à gauche utilisé pour une langue officielle et justifié à droite pour la deuxième.
Vous pouvez également utiliser les sous-titres suivants dans la section « Ingrédients médicinaux » :
- vitamines
- probiotiques
- minéraux
- herbes
- autres ingrédients médicinaux


Équivalent textuel
La figure 5 montre deux exemples du TIP pour les produits contenant quatre ingrédients médicinaux ou plus. Les titres sont, dans l'ordre, Product Facts / Info-roduit, Medicinal ingredients / Ingrédients médicinaux, Warnings / Mises en garde, Directions / Mode d'emploi et Questions avec un point d'interrogation.
Sous la rubrique Medicinal ingredients / Ingrédients médicinaux, le premier tableau énumère les ingrédients sous forme de puces en deux colonnes, et sur le deuxième tableau, les ingrédients sont énumérés sous forme de puces en continu. Toutes les rubriques sont en gras et commencent par une majuscule. Sous l'en-tête Mises en garde / Warnings, il y a des sous-titres et du texte factice.
5.0 Exemptions
5.1 Exemptions du tableau Info-produit et autres exigences en matière d'étiquetage
Conformément à l'article 93.5 du Règlement, les produits répondant à un ou plusieurs des critères suivants sont exemptés des exigences de contenu décrites dans les sections 2.2 (Informations requises sur l'étiquette extérieure), 2.3 (Informations requises sur l'étiquette intérieure), 2.4 (Informations requises dans le TIP), 3.1 (Spécifications concernant le TIP) et 4.1 (Assouplissements) :
- les produits en très petits emballages (tels que définis à la section 1.3 du présent document);
- les produits qui, lorsqu'utilisés selon le mode d'emploi qui figure sur l'étiquette, contiennent au maximum suffisamment d'unités posologiques pour une utilisation d'un jour ou moins, y compris les échantillons, les sachets ou les formats de voyage;
- les produits pour lesquels le contenant immédiat ne contient pas plus de trois unités posologiques recommandées, comme des emballages à doses multiples ou uniques, y compris des coques, des bandelettes, des cartes à enfoncer, des ampoules ou des flacons fixés par une bande de plastique, etc. ;
- les produits à faible risque (tels que définis à la section 1.3 du présent document).
Pour les produits en très petits emballages (au sens de la section 1.3 du présent document), les mentions, les renseignements et les déclarations devant figurer sur l'étiquette de ce très petit emballage sont exemptés des exigences de police et de contraste décrites à la section 3.0 (Format), conformément à l'alinéa 88 (2) (b) du Règlement.
Les produits qui, lorsqu'utilisés selon le mode d'emploi qui figure sur l'étiquette, contiennent au maximum suffisamment d'unités posologiques pour une utilisation d'un jour ou moins, y compris les échantillons, les sachets ou les formats de voyage, et les paquets multiples ou à dose unique contenant trois doses ou moins de produit, comme des coques, des bandelettes, des cartes à enfoncer, les ampoules ou les flacons fixés par une bande de plastique sont exemptés des exigences de police et de contraste décrites à la section 3.0 (Format), conformément au paragraphe 88 (3).
Pour les produits à faible risque (comme définis à la section 1.3 du présent document), le contenu de l'étiquette doit être conforme aux exigences de police et de contraste décrites à la section 3.0 (Format) et à l'article 88 du Règlement, le cas échéant.
Pour obtenir des renseignements sur les exigences en matière d'étiquetage de ces produits, consultez la section 5.2 ci-dessous.
5.2 Étiquetage des produits exemptés
Cette section décrit les exigences en matière d'étiquetage pour :
- les produits en très petits emballages (tels que définis à la section 1.3 du présent document);
- les produits qui, lorsqu'utilisés selon le mode d'emploi qui figure sur l'étiquette, contiennent au maximum suffisamment d'unités posologiques pour une utilisation d'un jour ou moins, notamment les échantillons, les sachets ou les formats de voyage;
- les produits pour lesquels le contenant immédiat ne contient pas plus de trois unités posologiques recommandées, comme des emballages à doses multiples ou uniques, y compris des coques, des bandelettes, des cartes à enfoncer, des ampoules ou des flacons fixés par une bande de plastique, etc. ;
- les produits à faible risque (tels que définis à la section 1.3 du présent document).
Tout le contenu doit être conforme aux descriptions présentées dans le tableau 6. Tel qu'indiqué au paragraphe 93.6 (1) du Règlement, les étiquettes intérieure et extérieure, le cas échéant, doivent afficher :
- le nom du titulaire de la licence de mise en marché ou de l'importateur;
- les coordonnées d'une personne-ressource représentant le titulaire de la licence 'de mise en marché ou l'importateur (adresse, numéro de téléphone, adresse électronique ou adresse de site Web);
- les ingrédients médicinaux, la quantité de chaque ingrédient par unité posologique, et l'activité autorisée de chaque ingrédient (le cas échéant);
- au moins une fin ou un usage recommandé;
- la voie d'administration recommandée;
- la dose;
- la durée de l'utilisation (le cas échéant);
- les mentions “Allergens” / « Allergènes » ou ”Allergens” et « Allergènes » en caractères gras, suivi de la mention des sources d'allergènes alimentaires, de gluten et de la source de gluten et des sulfites ajoutés également en caractères gras, le cas échéant;
- Toute autre mention de risque (y compris celles énumérées aux sections 6.d à 6.d.10 du tableau 6);
- les autres renseignements (par exemple, les conditions d'emmagasinage recommandées);
- le numéro de lot;
- la date limite d'utilisation.
Comme l'indique le paragraphe 93.6 (2) du Règlement, l'étiquette affichée sur le contenant extérieur doit afficher :
- les ingrédients non médicinaux;
- la quantité de mercure contenue dans le produit s'il contient du mercure ou ses sels ou dérivés comme ingrédient non médicinal;
- une description de la matière d'origine des ingrédients médicinaux.
Par ailleurs, ces produits ne sont pas exemptés des conditions établies par l'article 93 du Règlement concernant les renseignements qui doivent être affichés sur l'espace principal de l'étiquette. Ainsi, comme pour tout autre PSN, un produit exempté doit afficher sur l'espace principal de l'étiquette intérieure du produit et sur l'espace principal de l'étiquette extérieure, s'il y en a une :
- sa marque nominative;
- son numéro d'identification;
- sa forme posologique;
- les mentions stériles et sterile s'il s'agit d'un produit sérile;
- la quantité nette du produit se trouvant dans le contenant immédiat, exprimée en poids, en volume ou en nombre.
De plus, à l'exception des produits à faible risque, si la surface disponible pour l'étiquette ne suffit pas à contenir les renseignements exigés dans cette section, les ingrédients non médicinaux ainsi que la mention indiquant la quantité de mercure contenue dans le produit, le cas échéant, peuvent être déplacés, conformément au paragraphe 93.6 (3). du Règlement, de l'étiquette à :
- un dépliant apposé ou attaché au contenant extérieur du produit;
- une notice d'accompagnement;
- un site Web.
De plus, sauf pour les produits à faible risque, s'il n'y a toujours pas suffisamment d'espace sur l'étiquette pour tous les renseignements requis, conformément au paragraphe 93.6 (4) du Règlement, la description de la matière d'origine de chaque ingrédient médicinal, peut être déplacée vers :
- un dépliant attaché au contenant extérieur du produit;
- une notice d'accompagnement;
- un site Web.
Bien que ces produits soient exemptés de devoir afficher un TIP et des exigences en matière de police et de contraste (sauf pour les produits à faible risque), Santé Canada vous encourage à inclure un TIP et à utiliser des polices de caractères et des contrastes appropriés dans la mesure du possible.
Pour les produits à faible risque (tels que définis à la section 1.3 du présent document), le contenu décrit à la section 5.2 est requis en plus des exigences en matière de police et de contraste décrites à la section 3.0 (Format).
En ce qui concerne les assouplissements pour les produits à faible risque, les ingrédients non médicinaux et la mention indiquant la quantité de mercure contenue dans le produit, s'il y a lieu, peuvent également être déplacés vers un dépliant apposé ou attaché au contenant extérieur du produit, une notice d'accompagnement, ou un eTIP, si les renseignements requis ne cadrent pas sur l'étiquette après avoir utilisé une police condensée de 5,5 points (qui apparaîtrait comme 5 points) pour les ingrédients non médicinaux et une police condensée de 6 points (qui apparaîtrait comme 5,5 points) pour tous les autres renseignements requis (paragraphes 93.6 (3) et (4) du Règlement).
Pour les produits à faible risque seulement, les avertissements au point d'utilisation peuvent également être déplacés vers un dépliant attaché au contenant extérieur du produit, une notice d'accompagnement, ou un eTIP. Conformément au paragraphe 93.6 (5) du Règlement, une mention indiquant au consommateur le nouvel emplacement des renseignements déplacés doit apparaître à proximité du titre Info-produit, comme indiqué aux paragraphes 93.3 (4) et 93.6 (5) du Règlement.
S'il n'y a toujours pas suffisamment d'espace sur l'étiquette pour tous les renseignements requis, conformément au paragraphe 93.6 (4) du Règlement, la description de la matière d'origine de chaque ingrédient médicinal peut également être déplacée vers ce même dépliant, notice, ou page Web.
Dans tous les cas, si vous déplacez des informations réglementaires de l'étiquette physique à un dépliant, une notice ou un site Web, vous devez indiquer par le biais d'une mention quelles informations ont été déplacées et où les retrouver, incluant l'URL pour un eTIP, conformément au paragraphe 93.6 (5) du Règlement. Pour davantage d'information sur cette mention, référez-vous à la section 2.4 ou au Tableau 8 du présent document.
Pour les emballages à doses multiples ou uniques, les informations requises sur l'étiquette ne devraient pas être affectées par la séparation des unités posologiques. Vous pouvez le faire en imprimant de façon répétitive ces informations (par exemple, les emballages de coques devraient être imprimés de façon à ce que l'information puisse être lue pour chaque unité après la destruction d'une partie de l'emballage; cependant, les emballages de coques ne sont pas considérés comme des étiquettes intérieures et n'ont pas à respecter les exigences de l'étiquette intérieure).
Les emballages à doses multiples doivent contenir au minimum les renseignements décrits ci-dessous :
- la marque nominative (s'il n'y a pas de nom de marque, alors le nom propre ou usuel et le nom du fabricant);
- l'activité de l'ingrédient médicinal sauf si, dans le cas de plusieurs ingrédients médicinaux, le nom utilisé est unique pour une activité particulière de l'ingrédient médicinal;
- le numéro de lot et la date limite d'utilisation.
5.3 Étiquetage des produits en petits emballages
Si le contenant immédiat et l'espace disponible ne sont pas assez grands pour répondre aux exigences d'étiquetage décrites dans le présent document, l'étiquette intérieure doit plutôt afficher les renseignements suivants conformément au paragraphe 94 (1) du Règlement (et conformément au tableau 6) :
- Marque nominative;
- Ingrédients médicinaux;
- Dose recommandée;
- Durée d'utilisation recommandée (le cas échéant);
- Numéro de lot;
- Date limite d'utilisation;
- Numéro d'identification (de produit);
- « Stérile » et « Sterile » s'il s'agit d'un PSN stérile;
- Quantité nette dans le contenant immédiat, exprimée en poids, en volume ou en nombre;
- Au moins une utilisation ou une fin recommandée.
Cet assouplissement ne s'applique pas aux étiquettes extérieures des petits emballages. L'étiquette extérieure doit être conforme aux exigences relatives au TIP et afficher un TIP complet conformément à l'alinéa 94 (1) b) du Règlement.
Si le petit emballage n'a pas d'étiquette extérieure, les mentions, les renseignements et la déclaration décrits dans le présent document, notamment le TIP, à l'exception des exigences relatives à l'étiquette intérieure décrites dans la présente section, peuvent être indiquées dans un dépliant attaché ou apposé au contenant immédiat. Le dépliant doit alors être conforme aux exigences de police et de contraste énoncées à l'article 88 du Règlement en vertu du paragraphe 94(1)b) du Règlement. Toutefois, si l'étiquette devrait autrement afficher un TIP, un TIP complet doit être indiquée dans le dépliant qui est apposé au contenant immédiat, comme indiqué au paragraphe 94 (2) du Règlement. Le TIP doit également respecter les exigences de format applicables aux tableaux d'information sur le produit. Pour connaître ces exigences, reportez-vous à la section sur les tableaux d'information sur le produit et aux spécifications de format du présent guide.
6.0 Entrée en vigueur
Le Règlement modifiant le Règlement sur les produits de santé naturels est entré en vigueur à la date d'enregistrement de ce règlement, c'est-à-dire le 21 juin 2022. Toutefois, pour les dispositions relatives aux exigences en matière d'étiquetage (articles 17 à 22), la date d'entrée en vigueur est reportée de trois ans, soit le 21 juin 2025. Tout produit de santé naturel pour lequel une licence de mise en marché est délivrée, à compter du 21 juin 2025, devra respecter les nouvelles exigences en matière d'étiquetage. Tout produit de santé naturel pour lequel une licence de mise en marché est délivrée avant le 21 juin 2025 bénéficiera d'une période de transition supplémentaire de trois ans pendant laquelle il pourra être étiqueté conformément à l'ancien règlement (c'est-à-dire jusqu'au 22 juin 2028). Cela signifie que les produits pour lesquels une licence de produit est délivrée avant le 21 juin 2025 auront jusqu'au 22 juin 2028 pour se conformer aux nouvelles exigences d'étiquetage. Toutefois, pour que l'information soit claire, cohérente et lisible pour les consommateurs, Santé Canada encourage la mise en œuvre des exigences d'étiquetage améliorées le plus tôt possible.
6.1 Dispositions transitoires
En vertu de l'alinéa 11(1) c) du Règlement sur les produits de santé naturels, la suppression ou la modification des renseignements sur les risques figurant sur l'une des étiquettes d'un produit, sur toute étiquette du produit, notamment les précautions, mises en garde, contre-indications ou réactions indésirables connues liées à l'utilisation du produit, nécessite une demande de modification des conditions de l'autorisation de mise en marché en vertu du paragraphe 11(2) du Règlement.
Toutefois, en vertu d'une disposition transitoire du paragraphe 24(3) du Règlement modifiant le Règlement sur les produits de santé naturels:
- si vous détenez une licence de mise en marché en vertu du Règlement qui a été délivrée avant le 21 juin 2025 et que vous demandez de supprimer ou de modifier des renseignements sur les risques, notamment les précautions, mises en garde, contre-indications ou réactions indésirables connues liées à l'utilisation du produit pendant la période de transition afin de vous conformer au Règlement modifiant le Règlement sur les produits de santé naturels ou de vous aligner sur les changements apportés aux monographies de produits de Santé Canada, vous n'aurez qu'à soumettre une notification au ministre, tel que décrit à l'article 12 du Règlement, au lieu d'une demande de modification, tel que décrit à l'article 11 du Règlement, qui serait autrement requise. L'avis doit inclure le texte de l'étiquette et être présenté dans les 60 jours suivant le jour où la modification est apportée. Par conséquent, vous pourrez aviser le Ministre d'une telle modification et fournir le texte de l'étiquette modifiée à partir du jour où les modifications d'étiquetage du Règlement modifiant le Règlement sur les produits de santé naturels entreront en vigueur (c'est-à-dire le 21 juin 2025) et jusqu'au 60e jour après la période de transition de trois ans, ou le 21 août 2028, selon le moment où la modification est apportée.
Pour plus de clarté, l'ajout ou la modification d'une mention de risque pour inclure une source d'allergène alimentaire, une source de gluten et une déclaration de sulfites ajoutés, si l'ingrédient était déjà inscrit sur l'étiquette de votre produit, n'est pas considéré comme un changement conformément à l'alinéa 11 (1) (c) ni comme un changement conformément à l'alinéa 12 (2) (f) du Règlement.
7.0 Coordonnées
Pour toute question sur l'étiquetage des PSN, veuillez contacter la Direction des produits de santé naturels et sans ordonnance de Santé Canada à l'adresse suivante : nnhpd.consultation-dpsnso@hc-sc.gc.ca.
Annexe A : Étiquetage des produits homéopathiques
1.0 Portée
La présente annexe s'applique aux produits homéopathiques autorisés par Santé Canada. Ces produits ont des numéros de produit portant le préfixe « DIN-HM ». Ces exigences en matière d'étiquetage doivent être appliquées en plus de celles énoncées dans le présent document (Document de référence : Étiquetage des produits de santé naturels), de celles décrites dans le document de référence Preuves relatives aux médicaments homéopathiques, et dans les monographies pertinentes. Conformément à l'article 2 et au paragraphe 86 (1) du Règlement, les produits homéopathiques doivent satisfaire à toutes les exigences applicables du Règlement.
2.0 Exigences d'étiquetage pour les produits homéopathiques
2.1 Exigences générales en matière d'étiquetage
Cette section remplace l'information sur l'étiquetage des produits homéopathiques décrite dans le document de référence sur l'étiquetage des PSN de 2006. Elle remplace également les changements qui ont été apportés aux produits homéopathiques contre la toux, le rhume et la grippe destinés aux enfants de 12 ans et moins en 2015.
Le tableau A. 1 présente les exigences d'étiquetage des produits homéopathiques avec des allégations spécifiques ainsi que des allégations non spécifiques.
| - | Produits homéopathiques avec une allégation nonSpécifique |
Produits homéopathiques avec une allégation spécifique |
|---|---|---|
| Identification du type de produit | L'un des énoncés suivants doit figurer sur l'étiquette : « Produit homéopathique », « Remède homéopathique », « Médicament homéopathique » ou « Préparation homéopathique » dans une police de caractères d'au moins 6 points sur l'espace principal dans les caractères d'une seule couleur de type qui est un équivalent visuel de 100 % noir sur fond blanc ou d'un fond neutre uniforme avec un maximum de 5 % de teinte de couleur. | |
| Mention Utilisation recommandée ou Fin |
N'inscrivez pas l'utilisation ou la fin recommandée sur l'étiquette.
S'il faut utiliser un tableau d'information sur le produit, la section « Utilisations » devrait indiquer « Remède homéopathique », « Médicament homéopathique » ou « Préparation homéopathique ». |
Vous devez indiquer sur l'étiquette au moins une des utilisations ou des fins recommandées en termes précis, actuels et non ambigus, ou, le cas échéant, conformément à la monographie. |
Mention Voir la section 2.3 du document de référence sur les Preuves relatives aux médicaments homéopathiques pour obtenir de plus amples renseignements sur les exigences relatives à la mention des risques. |
L'étiquette doit indiquer :
« Consulter un praticien de soins de santé/un fournisseur de soins de santé/un médecin si les symptômes persistent ou s'aggravent ». |
L'information sur les risques doit être conforme à la licence de mise en marché. En l'absence d'autres mentions de risque, l'étiquette doit comprendre les mentions suivantes :
« Consulter un praticien de soins de santé, un fournisseur de soins de santé ou un médecin si les symptômes persistent ou s'aggravent » |
2.2 Mention sur le devant de l'emballage
Tous les produits homéopathiques disponibles sur le marché qui ne présentent pas de preuves scientifiques modernes à l'appui de leurs allégations santé dans le cadre de leur demande de licence de mise en marché doivent inclure l'un des énoncés suivants sur le devant de l'emballage (espace principal) :
- Pour tout produit homéopathique : « Cette allégation est fondée sur des références homéopathiques traditionnelles et non sur des preuves scientifiques modernes / This/These claim(s) is/are based on traditional homeopathic references and not modern scientific evidence. »
- Pour les produits homéopathiques sans allégations particulières : « Ce produit est fondé sur des références homéopathiques traditionnelles et non sur des preuves scientifiques modernes/This product is based on traditional homeopathic references and not modern scientific evidence. »
Le format requis pour la déclaration est indiqué ci-dessous :
- Utilisez du texte en gras dans une police sans empattement d'une taille minimale de 12 points.
- Pour un contraste optimal, utilisez une seule couleur qui soit l'équivalent visuel d'un caractère noir uni à 100 % pour le texte de la déclaration. Le noir d'écran à 100 %, le bleu foncé, le brun foncé, le vert foncé et le violet foncé sont acceptables.
- Utilisez du blanc ou un fond neutre uniforme avec une teinte de couleur de 5 % maximum pour l'arrière-plan de la déclaration. Ce niveau de teinte ne donne qu'une légère couleur au fond.
- Si l'étiquette entourant la déclaration est de la même couleur que le fond derrière la déclaration, incluez une bordure rectangulaire autour de la déclaration pour augmenter sa visibilité. La bordure peut être de n'importe quelle couleur suffisamment contrastée pour être visible. Le texte de la mention ne doit pas toucher la bordure. (Remarque : si le contraste entre la couleur de l'étiquette et le fond de la déclaration crée une bordure naturelle, il n'est pas nécessaire d'ajouter une bordure supplémentaire à la déclaration).
Assouplissements progressifs pour les produits en petits emballages :
Certains produits et certaines tailles d'emballage peuvent ne pas avoir suffisamment d'espace pour inclure la déclaration sur le devant de l'emballage avec les spécifications de format décrit ci-dessus. Les fabricants peuvent avoir recours aux assouplissements progressifs suivants pour ces produits si la mention n'est pas adaptée. Utilisez la première méthode d'assouplissement avant d'utiliser la deuxième, et la deuxième avant d'utiliser la troisième :
- Utilisez une police condensée et réduisez la largeur des caractères horizontalement jusqu'à 10 % (en d'autres termes, 90 % d'échelle horizontale).
- Pour les petits emballages, vous pouvez supprimer la bordure de mention.
- Pour les produits dans des emballages dont la surface disponible pour l'étiquette extérieure est de 90 cm² ou moins dont la mention ne correspond pas, la police peut être réduite de façon à ce que la mention soit égale à 50 % de la taille de la police de la marque principale ou de la plus grande marque sur l'emballage à au moins 5,5 points.
Par exemple, si la police de caractères de la marque principale sur l'emballage est de 12 points, l'énoncé doit être d'au moins 6 points. Les exigences en matière de contraste s'appliquent toujours.
3.0 Conseils supplémentaires pour des types de produits particuliers
3.1 Étiquetage des produits homéopathiques nasaux, ophtalmiques et otiques
L'étiquetage des produits homéopathiques à usage nasal ou ophtalmique doit suivre les spécifications de la dernière édition de la Homeopathic Pharmacopeia of the United States ou de la Pharmacopée européenne.
Les spécifications des solutions ophtalmiques de la Homeopathic Pharmacopeia of the United States comprennent :
- une étiquette indiquant les agents de conservation utilisés, le cas échéant;
- pour les récipients à doses multiples, un avertissement indiquant que la préparation ne doit pas être utilisée plus de 30 jours après la rupture du sceau (les récipients à doses multiples ne doivent pas dépasser 15 ml).
Les spécifications des solutions nasales de la Homeopathic Pharmacopeia of the United States comprennent une étiquette indiquant tous les agents de conservation, l'isotonicité, la viscosité et les agents stabilisateurs.
Les gouttes otiques homéopathiques doivent être étiquetées avec la mention « Consultez un médecin si vous avez de la fièvre, une douleur à l'oreille, une modification de l'audition et/ou des écoulements des oreilles ».
3.2 Étiquetage spécifique aux nosodes
En plus des exigences d'étiquetage décrites dans le reste du présent document de référence, les nosodes liées à une maladie infectieuse doivent contenir les mentions d'étiquetage suivantes sur l'espace principal, en caractères sans empattement d'une taille minimale de 12 points :
- « Ce produit n'est ni un vaccin ni une solution de rechange à la vaccination .
- « Il n'a pas été prouvé que ce produit prévient les infections. Santé Canada ne recommande pas son utilisation chez les enfants et conseille à votre enfant de recevoir tous les vaccins habituels. »
Les nosodes liées à des maladies infectieuses doivent contenir les mentions d'étiquetage suivantes sur l'espace principal, en caractères sans empattement d'une taille minimale de 12 points :
- "Il n'a pas été prouvé que ce produit prévient les infections."
Il n'y a pas d'assoupissement ou d'exemption pour l'étiquetage spécifique aux produits nasaux.
Annexe B : Suppléments minéraux à entité unique
En ce qui concerne les suppléments minéraux à entité unique, l‘activité et la teneur du composant actif peuvent différer considérablement entre les différentes formes de sel. La forme saline peut affecter non seulement la quantité de l'élément, mais aussi les caractéristiques d'absorption (par exemple, pour le fer et les produits calciques). Lorsqu'ils examinent un produit, les consommateurs et les praticiens de soins de santé peuvent avoir de la difficulté à distinguer la quantité de la forme saline d'un ingrédient actif de la quantité de la fraction active elle-même.
La confusion entre la fraction active ou la teneur en éléments et la teneur en sel du minéral telle qu'elle est indiquée sur l'étiquette a entraîné des erreurs de médication, notamment des erreurs de posologie.
Pour les suppléments minéraux à entité unique, on recommande d'utiliser les bonnes pratiques d'étiquetage suivantes pour favoriser une utilisation sécuritaire, en portant une attention particulière aux produits qui contiennent du calcium, du fer, du magnésium ou du zinc :
- L'espace principal doit indiquer l'élément et le sel avec leurs quantités correspondantes afin d'assurer l'harmonisation avec les instructions fournies aux consommateurs par les praticiens de soins de santé;
- Les quantités indiquées sur l'espace principal doivent être situées à proximité du nom correspondant (c'est-à-dire, la quantité de sel à proximité du nom du sel, la quantité d'éléments à proximité du nom de l'élément). Il faut éviter de placer la quantité de l'élément près du nom du sel, sans l'identifier clairement comme étant la quantité de l'élément, car cela pourrait entraîner une mauvaise interprétation et des erreurs de posologie;
- Si l'espace pose problème et que l'espace principal ne peut pas contenir à la fois le nom et la quantité du sel et le nom et la quantité de l'élément, la quantité qui figure sur l'espace principal doit correspondre à la description de l'ingrédient et être placée à proximité de ce nom (la matière d'origine ou l'ingrédient médicinal). Autrement dit, si la marque nominative indiquée sur l'espace principal est le nom du sel, la quantité doit correspondre à celle du sel.
- Si le panneau latéral indique à la fois l'élément et le sel, la quantité des deux devrait être précisée et clairement associée au nom correspondant (p. ex., calcium élément 500 mg [carbonate de calcium 1250 mg]). Pour plus de détails sur l'étiquetage de certains suppléments minéraux (calcium, fer, magnésium et zinc) pour le panneau latéral, veuillez vous reporter à l'annexe VIII de la monographie multivitamines/suppléments minéraux ou au générateur de texte de l'étiquette dans la demande de licence de mise en marché électronique.
- Ces bonnes pratiques d'étiquetage s'appliquent particulièrement aux suppléments minéraux à entité unique qui peuvent être recommandés aux consommateurs par les praticiens de soins de santé dans les milieux de pratique conventionnels (c'est-à-dire le fer, le zinc, le magnésium et le calcium avec ou sans vitamine D).
- Si la matière d'origine est composée de sels mélangés ou de complexes du même élément, il n'est pas nécessaire d'identifier la quantité de sel.
-
Exemples de formats d'étiquette recommandés pour l'espace principal des suppléments minéraux : 

Équivalent textuel
Cette figure fournit une aide visuelle pour l'étiquetage des compléments minéraux à entité unique.
Il y a deux images. La première image montre un contenant immédiat (par exemple, une bouteille) sur lequel est apposée l'étiquette intérieure. Sur l'étiquette intérieure, l'élément et sa quantité, "Calcium 500 mg", sont indiqués, suivis du sel et de sa quantité, « carbonate de calcium 1250 mg ».
La deuxième image montre un contenant immédiat (par exemple, une bouteille) sur lequel est apposée l'étiquette intérieure. Sur l'étiquette intérieure, le sel et sa quantité, « carbonate de calcium 1,250 mg », sont suivis de l'élément et de sa quantité, "Calcium 500 mg".
Annexe C : Liste de contrôle pour l'étiquetage
| Exigences en matière d'étiquetage | Étiquette extérieure (PSN avec intérieur/extérieur) | Étiquette intérieure (PSN avec intérieur/extérieur) | Une seule étiquette | Produit exempté |
|---|---|---|---|---|
| 1.0 Espace principal : | ||||
| 1.1 Marque nominative | X | X | X | X |
| 1.2 Numéro d'identification (préfixe NPN ou DIN-HM) | X | X | X | X |
| 1.3 Forme posologique | X | X | X | X |
| 1.4 Si le produit est stérile, les mots « Stérile » et « Sterile » | X | X | X | X |
| 1.5 Quantité nette dans le contenant immédiat exprimée en poids, en volume ou en nombre | X | X | X | X |
| 2.0 Pour n'importe quel espace : | ||||
| 2.1 Nom et coordonnées du titulaire de la licence de mise en marché ou de l'importateur | X | X | X | X |
| 2.2 Nom propre de chaque ingrédient médicinal, ou nom usuel si le nom propre est un nom chimique | X | X | X | X |
| 2.3 Quantité de chaque ingrédient médicinal par unité posologique (y compris l'activité, le rapport d'extraction et la quantité équivalente de brut, le cas échéant) associée au nom propre | X | X | X | X |
| 2.4 Description de la matière d'origine de chaque ingrédient médicinal | X | - | X | Étiquette la plus à l'extérieur |
| 2.5 Utilisation recommandée | X | X | X | X |
| 2.6 Voie d'administration recommandée | X | X | X | X |
| 2.7 Dose recommandée (y compris la sous-population, la quantité, la fréquence et le mode d'emploi, le cas échéant) | X | X | X | X |
| 2.8 Durée d'utilisation recommandée, le cas échéant | X | X | X | X |
| 2.9 Renseignements et mises en garde | X | X | X | X |
| 2.9.1 Mention des sources d‘allergènes alimentaires ou de gluten et des sulfites ajoutés, le cas échéant | X | X | X | X |
| 2.10 Titre « ingrédients non médicinaux », suivi de la liste des ingrédients non médicinaux | X | X | X | Étiquette la plus à l'extérieur |
| 2.11 Conditions d'entreposage | X | X | X | X |
| 2.12 Numéro de lot | X | X | X | X |
| 2.13 Date limite d'utilisation | X | X | X | X |
| 2.14 Dispositif de sécurité, s'il y a lieu. | X | X | X | X |
| 2.15 Si le produit contient du mercure ou ses sels ou dérivés en tant qu'ingrédient non médicinal, la quantité de mercure dans le produit | X | - | X | Étiquette la plus à l'extérieur |
| 3.0 Mises en garde et emballages protège-enfant : | ||||
| 3.1 Mises en garde et emballages à l'épreuve des enfants (article 97) | X | X | X | X |
Appendice 1 : Allergènes et aspartame
Cette liste d'allergènes alimentaires et de sources d'allergènes provient du Règlement sur les produits de santé naturels. Elle est incluse dans la présente ligne directrice pour en faciliter la consultation, suite aux exigences relatives à l'étiquetage des allergènes dans la section 2.4. S'il y a des écarts entre cette liste et le Règlement sur les produits de santé naturels, vous devez vous reporter au Règlement.
Allergène alimentaire s'entend de toute protéine provenant d'un des aliments ci-après, ou toute protéine modifiée — y compris toute fraction protéique — qui est dérivée d'un tel aliment:
- (a) amandes, noix du Brésil, noix de cajou, noisettes, noix de macadamia, pacanes, pignons, pistaches ou noix;
- (b) arachides;
- (c) graines de sésame;
- (d) blé ou triticale;
- (e) œufs;
- (f) lait;
- (g) soja;
- (h) crustacés;
- (i) mollusques;
- (j) poisson;
- (k) graines de moutarde.
Gluten signifie :
- toute protéine de gluten provenant des grains d'une des céréales ci-après ou des grains d'une lignée hybride issue d'au moins une de ces céréales :
- (i) orge;
- (ii) avoine;
- (iii) seigle;
- (iv) triticale;
- (v) blé;
- toute protéine de gluten modifiée – y compris toute fraction protéique de gluten – qui est dérivée des grains d'une des céréales mentionnées à l'alinéa a) ou des grains d'une lignée hybride qui est visée à cet alinéa.
Les sulfites ajoutés désignent un ou plusieurs des additifs alimentaires mentionnés à l'article 21, colonne 1, du tableau 2 du document Noms usuels des ingrédients et constituants et qui sont présents dans un PSN après avoir été ajoutés au produit.
De plus, la définition de l'aspartame, tirée du site Web de Santé Canada, est incluse pour en faciliter la consultation.
Aspartame désigne un édulcorant artificiel qui est un dérivé de l'acide aspartique et de la phénylalanine.
Détails de la page
- Date de modification :