InfoVigilance sur les produits de santé : novembre 2022
Contenu
- Produits de santé mentionnés dans ce numéro
- Maladie à coronavirus (COVID-19)
- Autorisations et communications : médicaments et vaccins contre la COVID-19
- Nuvaxovid vaccin contre la COVID-19
- Spikevax Bivalent (Original / Omicron BA.4/5) (elasomeran/davesomeran)
- Mise à jour de monographie de produit pour les médicaments contre la COVID-19 :
- Récapitulatif mensuel des renseignements sur l'innocuité des produits de santé
- Nouveaux renseignements sur l'innocuité des produits de santé
- Mise à jour de monographie de produit :
- Effets indésirables des produits de santé – rapport annuel 2021
- Résumé de l'innocuité des vaccins :
- Portée
- Pour signaler des effets indésirables
- Liens utiles
- Des suggestions?
- Droit d'auteur
Produits de santé mentionnés dans ce numéro
Produits pharmaceutiques et biologiques
Chlorure de Potassium dans du Lactate de Ringer USP, Injectable
Evusheld (tixagévimab et cilgavimab)
Metronidazole injectable, USP (métronidazole)
Nuvaxovid vaccin contre la COVID-19
Spikevax Bivalent (Original / Omicron BA.4/5) (elasomeran/davesomeran)
Produits de santé naturels et sans ordonnance
Produits pour enfants à base d’ibuprofène et d’acétaminophène
Télécharger en format PDF
(1.43 MB, 12 pages)
Direction générale des produits de santé et des aliments
Direction des produits de santé commercialisés
Équipe de rédaction de l'InfoVigilance sur les produits de santé
ISSN : 2368-8033
Cat. : H167-1F-PDF
Pub. : 210716
Maladie à coronavirus (COVID-19)
Pour obtenir les renseignements les plus à jour au sujet de la COVID-19, consultez le site Web Maladie à coronavirus (COVID-19) du gouvernement du Canada, Canada.ca/le-coronavirus. Le site Web comporte des sections dédiées aux professionnels de la santé et à l’industrie au sujet des produits de santé.
Le portail des vaccins et traitements pour la COVID-19 fournit des renseignements pour les consommateurs, pour les professionnels de la santé et pour les chercheurs sur les vaccins et traitements autorisés pour la COVID-19.
Pour l’information sur les effets secondaires suivant l'immunisation que certaines personnes ont signalés après avoir reçu un vaccin contre la COVID-19 au Canada, sur de nouveaux signaux concernant l'innocuité ou sur d'autres mises à jour concernant l'innocuité, consultez la page Web Sécurité des vaccins contre la COVID-19.
Autorisations et communications : médicaments et vaccins contre la COVID-19
Les nouveaux renseignements ainsi que les communications récentes au sujet des vaccins et des traitements autorisés contre la COVID-19 sont inclus dans cette section.
Nuvaxovid vaccin contre la COVID-19
Le 17 novembre 2022, Santé Canada a autorisé Nuvaxovid vaccin contre la COVID-19 comme dose de rappel chez les personnes âgées de 18 ans et plus. Une dose de rappel de Nuvaxovid (0,5 mL) peut être administrée par voie intramusculaire environ 6 mois après l’administration de la deuxième dose de la série de primovaccination.
Autorisation avec conditions : Nuvaxovid vaccin contre la COVID-19
Spikevax Bivalent (Original / Omicron BA.4/5) (elasomeran/davesomeran)
Le 3 novembre 2022, Santé Canada a autorisé Spikevax Bivalent (Original / Omicron BA.4/5) (elasomeran/davesomeran) à titre de dose de rappel pour l’immunisation active contre la COVID-19 chez les personnes âgées de 18 ans et plus. Afin de permettre un accès rapide au vaccin, Moderna distribuera le produit dans des boîtes et des flacons avec des étiquettes en anglais uniquement avec le nom de marque « Spikevax Bivalent Original / Omicron BA.4/BA.5 » pendant un certain temps. Il manque des renseignements importants propres au Canada sur ces étiquettes.
Les deux présentations des vaccins bivalents Moderna contre la COVID-19, Spikevax Bivalent Original / Omicron BA.4/5 et Spikevax Bivalent (ciblant Original / Omicron BA.1), ont la même couleur de capuchon de flacon, soit bleu roi, que Spikevax monovalent à 0,10 mg/mL en flacon de 2,5 mL. Le capuchon bleu roi représente la concentration de 0,10 mg/mL du produit, mais il ne doit PAS être utilisé comme seul moyen d’identifier le produit. Pour éviter les erreurs d’administration, portez une attention particulière au nom du vaccin et aux étiquettes des flacons et des boîtes.
L’étiquette des flacons et des boîtes de Spikevax Bivalent Original / Omicron BA.4/5 a une bordure grise et la concentration (0,1 mg/mL) est indiquée sur une bande grise. La dose de rappel (50 mcg) et le volume de la dose de rappel (0,5 mL) ne figurent pas sur les étiquettes unilingues anglaises des flacons ou des boîtes.
Communication des risques liés aux produits de santé : Spikevax Bivalent (Original / Omicron BA.4/5) (elasomeran/davesomeran)
Autorisation avec conditions : Spikevax Bivalent (Original / Omicron BA.4/5) (elasomeran/davesomeran)
Mise à jour de monographie de produit pour les médicaments contre la COVID-19
La mise à jour suivante concernant l'innocuité, qui a récemment été apportée à la monographie de produit canadienne, a été sélectionnée afin d'en accroître la sensibilisation. Les monographies de produit canadiennes pour les vaccins et les traitements autorisés contre la COVID-19 sont disponibles par le biais du portail des vaccins et traitements pour la COVID-19 ainsi que dans la Base de données sur les produits pharmaceutiques de Santé Canada.
Evusheld (tixagévimab et cilgavimab)
Les sections Posologie et administration, Effets indésirables et Renseignements destinés aux patients de la monographie de produit canadienne pour Evusheld ont été mises à jour avec des renseignements reflétant l’augmentation de la dose initiale et des directives sur l’administration répétée quand Evusheld est utilisé pour la prophylaxie préexposition de la COVID-19.
Messages clés à l'intention des professionnels de la santéNote de bas de page 1:
- La dose initiale d’Evusheld pour la prophylaxie préexposition de la COVID-19 a été augmentée de 300 mg à 600 mg (300 mg de tixagévimab et 300 mg de cilgavimab), administrée en deux injections distinctes et séquentielles de 3 mL, injections intramusculaires.
- Dans les situations où la prévention continue de la COVID-19 exige l’administration répétée d’Evusheld, les doses subséquentes de 600 mg (300 mg de tixagévimab et 300 mg de cilgavimab) devraient être administrées une fois tous les 6 mois.
- Les recommandations posologiques en vue de la prophylaxie reposent sur les données existantes, dont les données sur la pharmacologie clinique, le comportement pharmacocinétique et l’activité antivirale, et les données issues d’essais cliniques. Les renseignements détaillés peuvent être trouvés dans la monographie de produit canadienne pour Evusheld.
Référence
- Note de bas de page 1
-
Evusheld (tixagévimab et cilgavimab) [monographie de produit]. Mississauga (Ont.) : AstraZeneca Canada Inc., 2022.
Récapitulatif mensuel des renseignements sur l'innocuité des produits de santé
Voici une liste des avis concernant les produits de santé, des rappels de type I, ainsi que des résumés de l'examen de l'innocuité ou de la sûreté publiés en octobre 2022 par Santé Canada.
Pour des avis concernant les produits de santé en lien avec les vaccins et les traitements contre la COVID-19, veuillez consulter la section Autorisations et communications : médicaments et vaccins contre la COVID-19.
Chlorure de Potassium dans du Lactate de Ringer USP, Injectable
Un lot de Chlorure de Potassium dans du Lactate de Ringer USP, Injectable a été rappelé, car le lot affecté est étiqueté avec la concentration et l'ingrédient incorrects.
Rappel type 1 : Chlorure de Potassium dans du Lactate de Ringer USP, Injectable
Produits de santé non autorisés
Santé Canda a avisé les Canadiens que divers produits de santé non autorisés qui pourraient poser un risque grave pour la santé ont été vendus dans des points de vente au détail au Canada ou en ligne.
Avis : Des produits non homologués peuvent présenter de graves risques pour la santé
Produits pour enfants à base d’ibuprofène et d’acétaminophène
Il y a présentement une pénurie de produits à base d’acétaminophène et d’ibuprofène pour nourrissons et enfants en vente libre au Canada. La demande pour ces produits est plus élevée que la normale et, bien que l’approvisionnement augmente, les pénuries se poursuivent. Pour tenir les Canadiens au courant de la situation et des mesures prises par Santé Canada, le Ministère a créé une page Web consacrée à la pénurie d’acétaminophène et d’ibuprofène chez les nourrissons et les enfants.
Avis : Produits pour enfants à base d’ibuprofène et d’acétaminophène
Nouveaux renseignements sur l'innocuité des produits de santé
Les sujets suivants ont été sélectionnés dans le but d'accroître la sensibilisation et d’encourager la déclaration d'effets indésirables.
Mise à jour de monographie de produit
La mise à jour suivante concernant l'innocuité, qui a récemment été apportée à la monographie de produit canadienne, a été sélectionnée afin d'en accroître la sensibilisation. Une liste complète des mises à jour de l'étiquetage pour les produits pharmaceutiques se trouve sur la page L'innocuité des monographies de produits pour les médicaments innovateurs de Santé Canada. Les monographies de produit canadiennes sont disponibles dans la Base de données sur les produits pharmaceutiques de Santé Canada.
Metronidazole injectable, USP (métronidazole)
Les sections Contre-indications, Effets indésirables (Effets indésirables observés après la mise en marché) et Renseignements sur le médicament pour le patient de la monographie de produit canadienne pour Metronidazole injectable, USP ont été mises à jour avec le risque d’hépatotoxicité grave irréversible/d’insuffisance hépatique aiguë parfois mortelles chez des patients atteints du syndrome de Cockayne.
Messages clés à l'intention des professionnels de la santéNote de bas de page 1:
- Metronidazole injectable, USP est contre-indiqué chez les patients atteints du syndrome de Cockayne.
- Des cas d’hépatotoxicité grave et irréversible/d’insuffisance hépatique aiguë parfois mortels, apparaissant très rapidement après l’instauration du métronidazole à action générale, ont été signalés chez des patients atteints du syndrome de Cockayne (délai entre le début du traitement et les signes d’insuffisance hépatique, parfois aussi peu que 2 jours).
Référence
- Note de bas de page 1
-
Metronidazole injectable, USP (métronidazole) [monographie de produit]. Mississauga (Ont.) : Baxter Corporation, 2022.
Effets indésirables des produits de santé – rapport annuel 2021
Introduction
Les systèmes de déclaration spontanée et proactive après la mise en marché aident à cerner et à analyser les nouveaux renseignements sur l'innocuité des produits de santé, de sorte que les mesures appropriées soient prises pour réduire au minimum les risques pour la santé humaine. Au Canada, les effets indésirables (EI) et les incidents liés aux instruments médicaux (IIM) soupçonnés d'être associés à l'utilisation de produits de santé peuvent être signalés au Programme Canada Vigilance (PCV). Le présent rapport résume les renseignements reçus par le PCV en 2021 sur les cas d'EI survenus au pays qui ont été déclarés en lien avec des produits pharmaceutiques, des produits de santé naturels, des médicaments biologiques, des produits radiopharmaceutiques, des désinfectants, et des agents d'assainissement aux propriétés désinfectantes. Bien que les cas d'EI survenus à l'étranger soient inclus dans la base de données interne du PCV, ils ne sont pas discutés dans le présent rapport.
Cas et déclarations d'effets indésirables survenus au pays
En 2021, Santé Canada a reçu 194 560 déclarations d'EI après la mise en marché survenus au pays. Ces déclarations représentaient 81 211 cas d'EI (tableau 1). Un cas regroupe l'ensemble des renseignements décrivant le ou les EI subis par un patient à un moment donné qui sont soupçonnés d'être associés à l'utilisation d'un ou de plusieurs produits de santé. Un cas peut englober une déclaration d'EI initiale et plusieurs déclarations de suivi qui fournissent plus d'information. Des cas peuvent être dupliqués si des déclarations d'EI concernant un même évènement sont reçues de différentes sources (p. ex., professionnels de la santé, consommateurs, hôpitaux, fabricants).
| Type de produit | Nbre (%) de déclarations |
| Produits pharmaceutiques | 42 520 (52,4) |
| Produits biologiquesNote de bas de page * | 36 821 (45,3) |
| Produits radiopharmaceutiques | 502 (0,6) |
| Produits de santé naturels | 468 (0,6) |
| AutresNote de bas de page † | 900 (1,1) |
| Total | 81 211 (100) |
| |
Au Canada, les détenteurs d'une autorisation de mise sur le marché (DAMM) et les hôpitaux doivent transmettre au PCV des déclarations d'EI conformément aux exigences de la Loi sur les aliments et drogues et de ses règlements d'application. Dans le cas d'EI graves survenus au Canada, les DAMM doivent faire parvenir une déclaration dans les 15 jours suivant la date à laquelle ils ont été informés de l'incident. Conformément à la Loi visant à protéger les Canadiens contre les drogues dangereuses (Loi de Vanessa), les hôpitaux doivent soumettre, dans les 30 jours suivant la consignation, toutes les déclarations d'EI graves liés à un produit thérapeutique qui ont été documentés dans leur établissement. Les membres de la collectivité (consommateurs, patients et professionnels de la santé ne pratiquant pas dans les hôpitaux) peuvent soumettre de façon volontaire des déclarations d'EI en tout temps.
En 2021, 87,2 % de tous les cas d'EI survenus au pays ont été déclarés au PCV par des DAMM. Les autres cas ont été en grande partie déclarés directement par des membres de la collectivité (6,3 %) et par les hôpitaux (6,2 %). Pour la plupart des cas d’EI déclarés à Santé Canada directement ou par l’entremise d’un DAMM, le déclarant initial était un professionnel de la santé (figure 1).
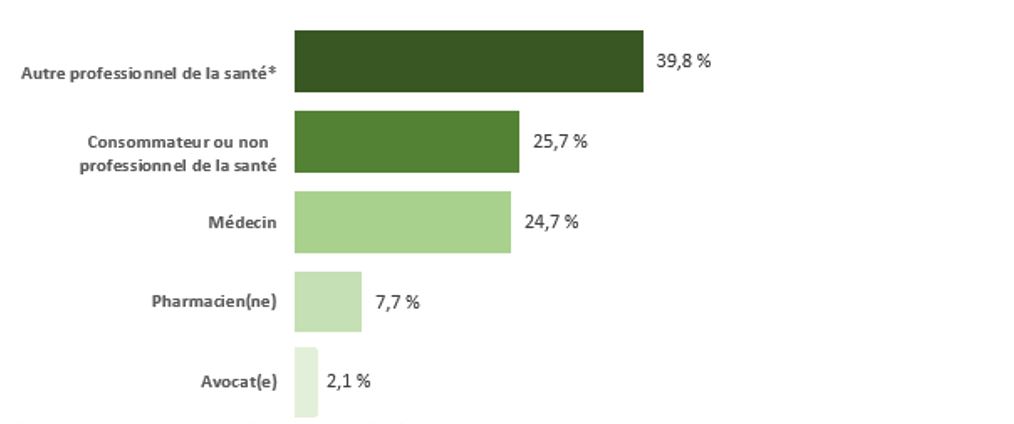
Figure 1 - Équivalent textuel
| Type de déclarant | Pourcentage de nombre de cas |
|---|---|
| Autre professionnel de la santéNote de bas de page * | 39.8% |
| Consommateur ou non-professionnel de la santé | 25.7% |
| Médecin | 24.7% |
| Pharmacien(ne) | 7.7% |
| Avocat(e) | 2.1% |
|
|
Répartition selon le sexe et l'âge
La répartition des 81 211 cas par sexe allait comme suit : 56,9 % de sexe féminin, 38,9 % de sexe masculin et 4,2 % de sexe inconnu ou non déclaré, ce qui correspond à la répartition selon le sexe des cas d’EI observés à l'échelle mondiale1. La répartition par tranche d'âge était de 3,4 % chez les enfants (< 19 ans), 52,3 % chez les adultes (19 à 64 ans), 26,6 % chez les aînés (≥ 65 ans) et l'âge était inconnu ou n'avait pas été déclaré dans 17,6 % des cas.
Produits soupçonnés et effets indésirables
Le tableau 2 présente les 10 groupes de produits soupçonnés les plus fréquemment mis en cause dans les cas d'EI survenus au pays. Ces groupes correspondent aux critères du Système de classification anatomique, thérapeutique et chimique (ATC) de l'Organisation mondiale de la santé.
| Produit de santé (groupe ATC) | Nbre (%) de déclarationsNote de bas de page ‡ |
|---|---|
| Immunosuppresseurs (L04) | 33 586 (41,4) |
| Antinéoplasiques (L01) | 12 148 (15,0) |
| Vaccins (J07) | 6 384 (7,9) |
| Analgésiques (N02) | 5 948 (7,3) |
| PsycholeptiquesNote de bas de page § (N05) | 3 551 (4,4) |
| Médicaments pour les maladies obstructives des voies respiratoires (R03) | 2 942 (3,6) |
| Corticoïdes à usage systémique (H02) | 2 515 (3,1) |
| Antiépileptiques (N03) | 2 408 (3,0) |
| Antibactériens à usage systémique (J01) | 2 126 (2,6) |
| Antidiarrhéiques, anti-inflammatoires intestinaux/agents anti-infectieux (A07) | 1 831 (2,3) |
|
|
Le tableau 3 présente les 10 EI survenus au pays les plus fréquemment signalés au PCV d'après les codes de classe par système et par organe (SOC). Les EI sont codés selon la terminologie du Dictionnaire médical des affaires réglementaires (MedDRA). Les EI les plus couramment déclarés ont été les troubles généraux et les anomalies au point d'administration, qui comprennent les troubles touchant plusieurs systèmes ou sites de l'organisme (p. ex., médicament inefficace, fatigue, fièvre, œdème, douleur, réactions au point d'administration), suivis par les lésions, intoxications et complications d'interventions.
| Classe par système et par organe | Nbre (%) de déclarationsNote de bas de page ‡ |
|---|---|
| Troubles généraux et anomalies au site d'administration | 44 767 (55,2) |
| Lésions, intoxications et complications d'interventions | 21 666 (26,7) |
| Affections gastro-intestinales | 18 116 (22,4) |
| Affections du système nerveux | 15 196 (18,8) |
| Investigations | 14 626 (18,0) |
| Infections et infestations | 14 620 (18,0) |
| Affections musculosquelettiques et du tissu conjonctif | 13 381 (16,5) |
| Affections de la peau et du tissu sous-cutané | 10 270 (12,7) |
| Affections respiratoires, thoraciques et médiastinales | 9 992 (12,3) |
| Affections psychiatriques | 9 552 (11,8) |
|
|
Raison de la gravitéNote de bas de page *
Des 81 211 cas d'EI, 74,3 % ont été jugés graves. Plusieurs raisons de la gravité peuvent être déclarées pour un même cas. En 2021, 22,6 % des cas d'EI indiquaient qu'une hospitalisation avait été exigée, 2,7 % décrivaient un état présentant un danger de mort, et 7,6 % indiquaient que le patient était décédé.
Investigations sur les effets indésirables déclarés
Dans le cadre des activités de surveillance de routine, une déclaration d’EI soumise au PCV est évaluée pour déceler les problèmes d’innocuité potentiels et la détection des signaux grâce à des niveaux d’escalade progressifs. Les résultats préoccupants sont présentés au bureau d’évaluation responsable du produit pour la confirmation, la priorisation et l’évaluation des signaux.
Lorsqu'un EI déclaré est connu et inclus dans la monographie du produit, il n'est pas considéré comme un nouveau signal, à moins d'un changement sur le plan de la fréquence ou de gravité. Les EI signalés après la mise en marché peuvent être attribués à un large éventail de facteurs, notamment des effets pharmacologiques du produit qui étaient jusque-là inconnus, des effets idiosyncrasiques, des interactions médicamenteuses (p. ex., médicament-médicament, médicament-maladie, médicament-produit de santé naturel), des facteurs propres au patient (p. ex., facteurs pharmacogénomiques), des incidents médicamenteux et d'autres facteurs qui pourraient avoir été trop rares pour être reconnus dans les essais cliniques.
Il est difficile de comparer les risques associés aux produits de santé uniquement en fonction du volume de déclarations soumises. Plusieurs facteurs peuvent influer sur les tendances de déclarations d'EI, tels que les risques connus d'un produit, le temps écoulé depuis sa mise en marché, le nombre d'utilisations, la publicité concernant un EI, les mesures réglementaires prises pour réduire les risques, et/ou les méthodes de collecte de données Note de bas de page †. Par exemple, les EI rares et graves peuvent être déclarés plus souvent dans les systèmes organisés de collecte de données que dans les systèmes de déclaration volontaire, ce qui peut avoir une incidence sur la tendance des déclarations. En général, les évènements indésirables sont sous-déclarés dans les systèmes de déclaration spontanée comme le PCV.
Les déclarations d'EI sont un élément important dans le cadre de la surveillance des produits de santé par Santé Canada. Les déclarations d'EI, ainsi que d'autres sources de renseignements provenant de sources nationales et internationales, aident à l'identification et l'analyse de nouveaux renseignements sur l'innocuité, et orientent les décisions prises par Santé Canada concernant les mesures à prendre. Par exemple, une association causale entre le produit et l'EI peut inciter une action de Santé Canada. La même chose s'applique si de nouveaux risques sont déterminés à partir d'un groupe d'EI semblable, ou à partir de déclarations d'EI ayant révélé des lacunes en matière d'étiquetage ou des problèmes sur le plan de la qualité du produit. Les renseignements reliés aux médicaments reçus et évalués par Santé Canada peuvent aboutir à des actions qui incluent la communication de nouveaux renseignements sur l'innocuité aux Canadiens et aux professionnels de la santé, la recommandation de modifications à apporter à l'étiquetage, ou le retrait de médicaments du marché.
En 2021, les renseignements reliés aux médicaments reçus et évalués par Santé Canada ont abouti à plus de 1 180 mesures : 26 signaux d’innocuité, 22 mesures réglementaires, 33 communications des risques liés aux produits de santé et à adresser plus de 1 100 publicités fausses ou trompeuses. Les nouveaux renseignements importants sur l'innocuité sont communiqués aux professionnels de la santé et au public canadiens par l'entremise de la base de données des rappels et des avis de sécurité sur le site Web Canadiens en santé. Les nouveaux renseignements sur l'innocuité sont aussi diffusés par le système de notification par courriel Avis électronique MedEffetMC. De plus, Santé Canada a publié 24 résumés de ses examens de l'innocuité, lesquels décrivent les observations de Santé Canada et les mesures de gestion des risques visant les problèmes d'innocuité potentiels.
Conclusion
Chaque année, le PCV reçoit des milliers de déclarations qui aident à mieux comprendre l'innocuité des produits de santé commercialisés. Santé Canada souhaite remercier tous ceux qui ont contribué à fournir des renseignements et encourage le soutien continu à la surveillance post-commercialisation par la déclaration des EI et des IIM. Tous les EI et les IIM soupçonnés d'être associés à l'utilisation de produits de santé devraient être déclarés au PCV. Chaque déclaration compte, et ensemble elles racontent une histoire.
Référence
- Note de bas de page 1
-
Watson, S., Caster, O., Rochon, P.A. & den Ruijter, H. (2019). Reported adverse drug reactions in women and men: Aggregated evidence from globally collected individual case reports during half a century. EClinicalMedicine, 17, 100188, ISSN 2589-5370. https://doi.org/10.1016/j.eclinm.2019.10.001
Résumé de l'innocuité des vaccins
Santé Canada et l'Agence de la santé publique du Canada (ASPC) partagent la responsabilité de la surveillance de l'innocuité des vaccins au Canada.
Les détenteurs d'une autorisation de mise en marché sont tenus de déclarer les effets secondaires suivant l'immunisation (ESSI) considérés graves au Programme Canada Vigilance de Santé Canada. Le Programme Canada Vigilance reçoit également des déclarations volontaires des professionnels de la santé et des consommateurs.
Les autorités de santé publique provinciales et territoriales déclarent les ESSI provenant des programmes d'immunisation financés par l'État au Système canadien de surveillance des effets secondaires suivant l'immunisation (SCSESSI) de l'ASPC.
Résumé pour la période du 1er juillet au 31 décembre 2020
Messages clés :
- Du 1er juillet 2020 au 31 décembre 2020, le Programme Canada Vigilance a reçu 533 déclarationsNote de bas de page † d'effets secondaires suivant l'immunisation soupçonnés d'avoir été causés par des vaccins.
- Aucun nouveau signal d'innocuité (problème d'innocuité potentiel) n'a été identifié pendant cette période.
Le présent résumé de l'innocuité des vaccins fait un compte rendu des déclarations d'effets secondaires suivant l'immunisation (ESSI) reçues par le Programme Canada Vigilance entre le 1er juillet et le 31 décembre 2020 pour les vaccins n’incluant pas les vaccins contre la COVID-19. Pour accéder aux résumés publiées par le SCSESSI, veuillez consulter le site Web du SCSESSI. Pour des renseignements sur les ESSI que les individus ont déclarés suivant un vaccin COVID-19 au Canada, veuillez visiter la page web Effets secondaires signalés après la vaccination contre la COVID-19 au Canada.
- Du 1er juillet 2020 au 31 décembre 2020, le Programme Canada Vigilance a reçu 533 déclarations d'effets secondaires suivant l'immunisation soupçonnés d'avoir été causés par des vaccins.
- La majorité des déclarations provenait des professionnels de la santé (figure 1) par le biais de la déclaration spontanée.
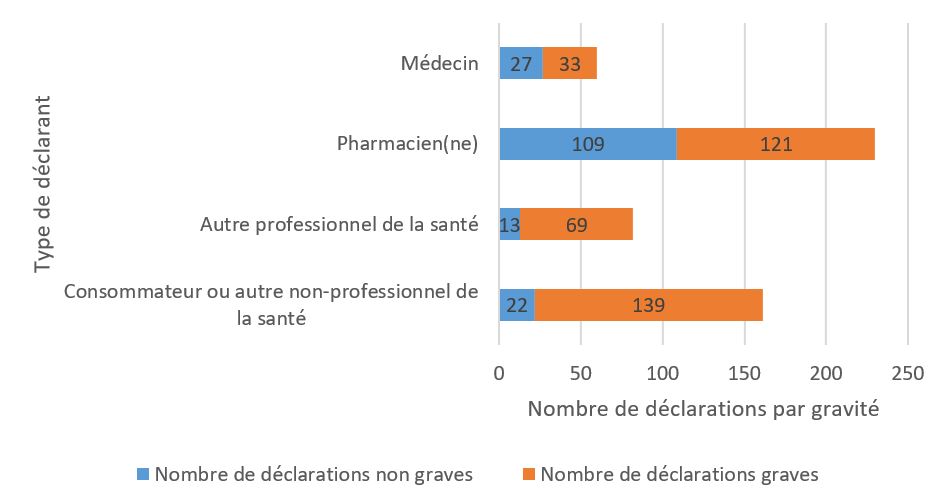
Figure 1 - Équivalent textuel
| Type de déclarant | Nombre de déclarations non graves | Nombre de déclarations graves |
|---|---|---|
| Médecin | 27 | 33 |
| Pharmacien(ne) | 109 | 121 |
| Autre professionnel de la santé | 13 | 69 |
| Consommateur ou autre non-professionnel de la santé | 22 | 139 |
- La majorité des déclarations impliquait des adultes âgés de 19 à 64 ans (183 sur 533 : 34 %) (figure 2).
- La répartition par le sexe pour les 533 déclarations était 56 % de sexe féminin, 34 % de sexe masculin et 10 % de sexe inconnu.
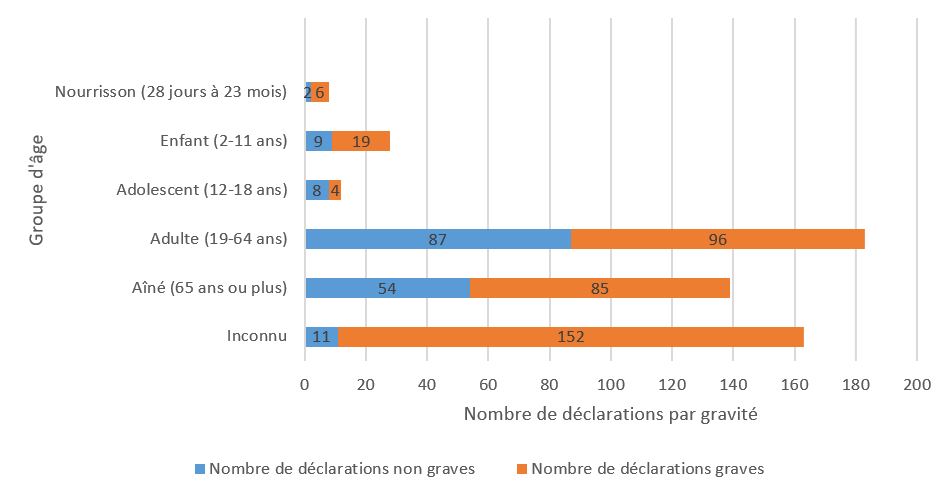
Figure 1 - Équivalent textuel
| Groupe d'âge | Nombre de déclarations non graves | Nombre de déclarations graves |
|---|---|---|
| Nourrisson (28 jours à 23 mois) | 2 | 6 |
| Enfant (2-11 ans) | 9 | 19 |
| Adolescent (12-18 ans) | 8 | 4 |
| Adulte (19-64 ans) | 87 | 96 |
| Aîné (65 ans ou plus) | 54 | 85 |
| Inconnu | 11 | 152 |
- Le plus grand nombre de déclarations (graves et non graves) reçues impliquait les vaccins contre l'influenza (240 déclarations) suivi par les vaccins contre le zona (217 déclarations), et les vaccins contre le pneumocoque (31 déclarations) (figure 3).
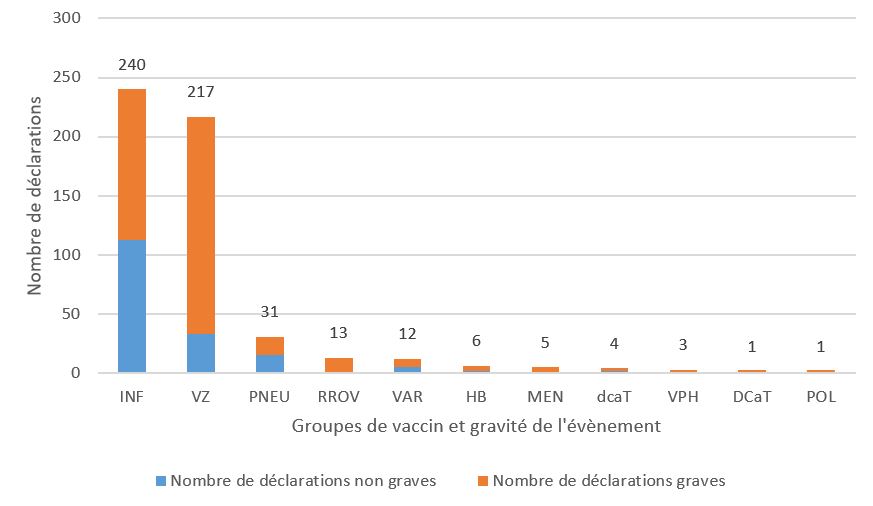
Figure 3 - Équivalent textuel
| Type de vaccin | Nombre de déclarations non graves | Nombre de déclarations graves | |
|---|---|---|---|
| Influenza | INF | 113 | 127 |
| Zona | VZ | 33 | 184 |
| Pneumocoque | PNEU | 15 | 16 |
| Rougeole, Rubéole, Oreillons et Varicelle | RROV | 1 | 12 |
| Varicelle | VAR | 5 | 7 |
| Hépatite B | HB | 2 | 4 |
| Méningocoque | MEN | 0 | 5 |
| Diphtérie (réduite), Coqueluche acellulaire et Tétanos | dcaT | 2 | 2 |
| Virus du papillome humain | VPH | 0 | 3 |
| Diphtérie, Coqueluche acellulaire et Tétanos | DCaT | 0 | 1 |
| Poliomyélite | POL | 0 | 1 |
- Parmi les 533 déclarations, 362 (68 %) étaient des déclarations graves. Les effets secondaires graves signalés le plus fréquemment incluaient le zona, l'échec de la vaccination, la douleur, rash, l’œdème, l’érythème, la dyspnée, la fièvre, le prurit, l’arthralgie et la céphalée. La plupart impliquaient des patients avec des problèmes de santé sous-jacents et/ou des médicaments concomitants et les effets secondaires graves n'étaient probablement pas liés à la vaccination.
- Le décès a été signalé dans 6 déclarations; 2 déclarations étaient de sexe masculin et 4 étaient de sexe féminin. Cinq cas sont survenus chez des individus de 65 ans et plus. Une déclaration n’a pas rapporté l’âge. Les vaccins impliqués dans les déclarations étaient : vaccin contre l’influenza (4), vaccin contre le zona (1), et vaccin contre le pneumocoque (1). L'information fournie dans ces déclarations n'était pas suffisante pour évaluer le lien de causalité avec le vaccin.
- Aucun nouveau signal d'innocuité (problème d'innocuité potentiel) n'a été identifié pendant cette période.
- Les avantages des vaccins autorisés au Canada continuent de l'emporter sur les risques.
- Santé Canada, en collaboration avec l'ASPC, continuera de surveiller étroitement l'innocuité des vaccins autorisés au Canada.
Pour obtenir de plus amples renseignements, veuillez communiquer avec la Direction des produits de santé commercialisés.
Notez qu'en raison d'une mise à jour de l'information reçue par le Programme Canada Vigilance, il peut y avoir des différences dans le nombre de déclarations et les effets secondaires extraits à des dates différentes.
Portée
Cette publication mensuelle s’adresse principalement aux professionnels de la santé et contient des informations sur les produits pharmaceutiques, biologiques, les matériels médicaux et les produits de santé naturels. Elle fournit un résumé des informations clés concernant l’innocuité des produits de santé qui ont été publiés au cours du mois précédent par Santé Canada, ainsi qu’une sélection de nouveaux renseignements en matière d’innocuité sur les produits de santé, pour en accroître la sensibilisation. Les nouvelles informations contenues dans ce numéro ne sont pas exhaustives, mais représentent plutôt une sélection de problèmes d’innocuité cliniquement pertinents, justifiant une dissémination améliorée.
Pour signaler des effets indésirables
Programme Canada Vigilance
Téléphone : 1-866-234-2345
Télécopieur ou courrier : formulaire disponible sur MedEffet Canada
Des renseignements sur la marche à suivre pour déclarer un effet indésirable à Santé Canada sont publiés à la page Déclaration des effets indésirables ou des incidents liés aux matériels médicaux.
Liens utiles
- MedEffetMC Canada
- Base de données sur les rappels et les avis de sécurité
- Nouveaux examens de l'innocuité ou de la sûreté et de l’efficacité
- Base de données en ligne des effets indésirables de Canada Vigilance
- Base de données sur les produits pharmaceutiques
- Liste des instruments médicaux homologués
- Base de données des produits de santé naturels homologués
- Registre des médicaments et des produits de santé
- Pénuries de médicaments Canada
- Pénuries d'instruments médicaux : Liste des pénuries et des interruptions de la vente
- Mettons fin au marketing illégal des médicaments et des instruments médicaux
- Liste des drogues destinées aux importations et aux ventes exceptionnelles
- Autorisation de médicament et de vaccin contre la COVID-19 : Liste des drogues et vaccins autorisés et des drogues à indication supplémentaire
- Effets secondaires signalés après la vaccination contre la COVID-19 au Canada
Des suggestions?
Vos commentaires sont importants pour nous. Dites-nous ce que vous pensez en nous contactant à : infowatch-infovigilance@hc-sc.gc.ca
Équipe de rédaction de l’InfoVigilance sur les produits de santé
Direction des produits de santé commercialisés
Santé Canada
Indice de l’adresse 1906C
Ottawa (ON) K1A 0K9
Téléphone : 613-954-6522
Téléimprimeur : 1-800-465-7735 (Service Canada)
Droit d’auteur
© 2022 Sa Majesté le Roi du Chef du Canada. Cette publication peut être reproduite sans autorisation à condition d'en indiquer la source en entier. Il est interdit de l'utiliser à des fins publicitaires. Santé Canada n'accepte pas la responsabilité de l'exactitude ou de l'authenticité des renseignements fournis dans les notifications.
On ne peut que soupçonner la plupart des effets indésirables (EI) des produits de santé à l'égard desquels on ne peut établir de lien prouvé de cause à effet. Les notifications spontanées d'EI ne peuvent servir pour déterminer l'incidence des EI, étant donné que les EI ne sont pas suffisamment signalés et l'étendue d'exposition des patients est inconnue.
En raison des contraintes de temps concernant la production de cette publication, les informations publiées peuvent ne pas refléter les informations les plus récentes.
Notes de bas de page
- Note de bas de page *
-
La Loi sur les aliments et drogues et ses règlements d'application définissent une « réaction indésirable grave » comme suit : « Réaction nocive et non intentionnelle à une drogue qui est provoquée par l'administration de toute dose de celle-ci, qui nécessite ou prolonge l'hospitalisation, entraîne une malformation congénitale ou une invalidité ou incapacité persistante ou importante, met la vie en danger ou entraîne la mort. » D'autres situations peuvent aussi être désignées comme graves, « par exemple lorsque surviennent d'importants évènements médicaux qui peuvent ne pas présenter un danger de mort immédiat, provoquer la mort ou nécessiter l'hospitalisation, mais qui peuvent compromettre la santé du patient ou nécessiter une intervention en vue de prévenir l'une des conséquences énumérées dans la définition des Règlements. »
- Note de bas de page †
-
Les systèmes organisés de collecte de données englobent les registres de patients, les enquêtes, et les programmes de soutien des patients et de prises en charge des maladies.
- Note de bas de page ‡
-
Glossaire des champs de la base de données en ligne des effets indésirables de Canada Vigilance
