Système canadien de surveillance des effets secondaires suivant l'immunisation (SCSESSI)
Pour des informations sur les effets secondaires possibles après la vaccination, consultez :
Sur cette page
- Effets secondaires suivant l'immunisation au Canada
- À propos du système
- Déclaration des effets secondaires suivant l'immunisation
- Effets secondaires de la COVID-19 suivant l'immunisation
- Publications et rapports sur les données
- Rapports sur l'innocuité des vaccins publiés précédemment
- Liens connexes
Effets secondaires suivant l'immunisation au Canada
Santé Canada (SC) et l'Agence de la santé publique du Canada (ASPC) se partagent la surveillance de la sécurité des vaccins au pays. Les titulaires d'autorisations de mise sur le marché sont tenus de signaler les effets secondaires graves suivant l'immunisation (ESSI) au Programme Canada Vigilance (CVP) à SC.
Le système canadien de surveillance des effets secondaires suivant l'immunisation (SCSESSI) est un système fédéral, provincial et territorial (FPT) de surveillance de la sécurité des vaccins après leur commercialisation par la santé publique. Le SCSESSI est géré par l'ASPC et présente la particularité d'inclure à la fois une surveillance passive (rapports spontanés provenant des FPT), et une surveillance active.
À propos du système
SCSESSI a pour objectifs de :
- surveiller continuellement l'innocuité des vaccins commercialisés au Canada
- détecter les hausses de fréquence ou de gravité des réactions liées aux vaccins déjà décelées
- cerner les effets secondaires précédemment inconnus de l'immunisation qui pourraient être liés aux vaccins (effets secondaires [PDF, en anglais seulement]) imprévus suivant l'immunisation)
- déterminer les secteurs où des études ou des enquêtes plus approfondies s'avèrent nécessaires
- fournir de l'information opportune sur les profils de déclaration des effets secondaires suivant l'immunisation concernant les vaccins commercialisés au Canada afin d'éclairer les décisions relatives à l'immunisation
Déclaration des effets secondaires suivant l'immunisation
Le diagramme ci-dessous illustre de quelle façon les déclarations des effets secondaires suivant l'immunisation passent du point d'origine (sujet vacciné) à ASPC. Le SCSESSI comporte des processus de déclaration des effets secondaires suivant l'immunisation spontanés, améliorés et actifs, qui sont définis plus en détail ci-dessous.
Figure 1 : Chaîne de déclaration en santé publique pour les effets secondaires suivant l'immunisation au SCSESSI
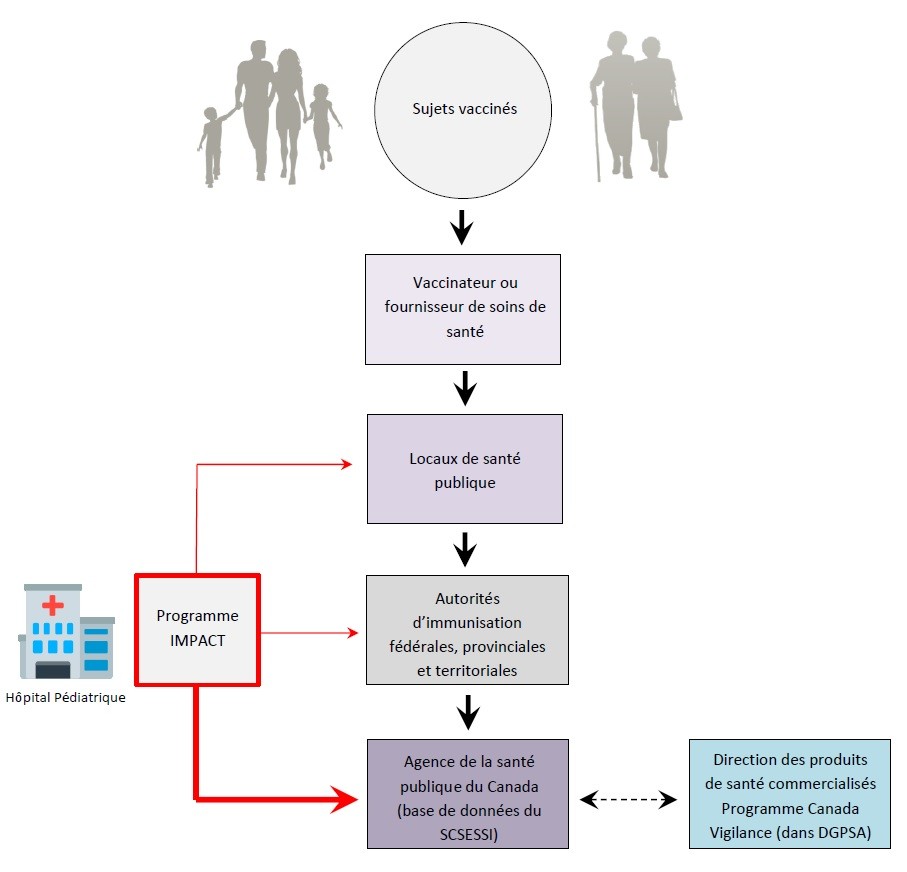
Abréviations: IMPACT, Programme canadien de surveillance active de l'immunisation; DGPSA, La Direction générale des produits de santé et des aliments.
Équivalent textuel - Figure 1
Ce diagramme illustre le parcours des déclarations des effets indésirables suivant l'immunisation depuis l'origine (sujet vacciné) jusqu'à l'Agence de la santé publique du Canada. Dans la partie supérieure de ce diagramme se trouve un cercle représentant le sujet vacciné. À partir du cercle, une flèche pointe vers le bas, en direction d'une case comprenant le vaccinateur ou fournisseur de soins de santé, avec une autre flèche allant de cette case à une autre case contenant les centres locaux de santé publique. À partir de cette case, une flèche pointe vers le bas en direction d'une case contenant les autorités d'immunisation fédérales, provinciales et territoriales, et une flèche pointe vers une case contenant le nom de l'Agence de la santé publique du Canada (base de données du SCSESSI).
À gauche de l'organigramme, on trouve une case rouge illustrant le programme IMPACT, un réseau national de surveillance active en milieu hospitalier pédiatrique, avec une flèche épaisse et continue partant de cette case en direction de la case de la base de données du SCSESSI. Deux flèches minces vont de la case du programme IMPACT à la case des autorités d'immunisation fédérales, provinciales et territoriales, et à la case des bureaux de santé publique locaux. À droite de l'organigramme, on trouve une case intitulée Direction des produits de santé commercialises Programme Canada Vigilance (dans La Direction générale des produits de santé et des aliments (DGPSA)) avec une ligne en pointillé, double flèche pointant entre la case base de données SCSESSI et la case Programme Canada Vigilance.
Rapports soumis
Les déclarations au SCSESSI sont soumises par les autorités provinciales et territoriales de santé publique, qui, pour leur part, les reçoivent des bureaux locaux de santé publique ainsi que des autorités fédérales offrant les vaccins au sein de leur territoire de compétence, dont :
- la GRC
- le Service correctionnel du Canada
- le Services aux Autochtones Canada
La plupart de ces rapports sont générés par les infirmières, les médecins et les pharmaciens qui administrent les vaccins recommandés ou qui soignent les personnes souffrant d'effets secondaires suivant l'immunisation. Le ministère de la Défense nationale et les Forces armées canadiennes signalent directement les effets secondaires suivant l'immunisation à l'Agence de la santé publique du Canada.
Les fabricants de tous les médicaments, y compris les vaccins, sont tenus de signaler les effets secondaires graves ainsi que des effets secondaires inattendus au Programme Canada Vigilance de la Direction des produits de santé commercialisés (DPSC) de la DGPSA de SC.
La surveillance active existe depuis 1991. Elle est menée par l'IMPACT. IMPACT est financé par l'ASPC dans le cadre d'un contrat avec la Société canadienne de pédiatrie. Ce contrat comprend actuellement 12 centres de pédiatrie au Canada, représentant plus de 90% de tous les lits de soins tertiaires pédiatriques du pays.
IMPACT analyse les hospitalisations pour des événements neurologiques, tels que :
- les convulsions
- l'encéphalite
- la thrombocytopénie
- l'abcès au site de vaccination / cellulite
- la paralysie flasque aiguë (incluant le syndrome de Guillain-Barré et la méningite aseptique)
- d'autres complications pouvant survenir après la vaccination
Tout ce qui est provisoirement lié à la vaccination, sans explication claire, est rapporté comme un ESSI. Les rapports IMPACT sont envoyés à l'ASPC, pour être entré au SCSESSI, ainsi qu'aux responsables de la santé locaux, provinciaux et territoriaux afin d'assurer un suivi approprié au niveau individuel.
Découvrez comment signaler un événement indésirable après la vaccination.
Actions de santé publique
Le flux des rapports d'ESSI présenté dans le diagramme permet de prendre des mesures spécifiques à chaque étape du processus.
La gestion des ESSI, y compris une investigation appropriée pour déterminer la cause possible, est généralement entreprise par le prestataire de services de vaccination ou le fournisseur de soins de santé déclarant.
Les actions individuelles de santé publique, notamment les conseils relatifs aux futures immunisations, sont prises au niveau du bureau de santé publique ou du prestataire de services de vaccination.
Les autorités sanitaires FPT collectent les déclarations d'ESSI dans le cadre de l'évaluation continue de leurs programmes de vaccination. À l'échelle de la population, les actions de santé publique liées aux déclarations d'ESSI pourraient inclure des modifications à la politique du programme de vaccination.
L'ASPC rassemble les déclarations d'ESSI dans la base de données canadienne sur les effets secondaires suivant l'immunisation (ESSI) aux fins d'analyse et de compte-rendu de la détection du signal. Si un signal potentiel est identifié, l'ASPC travaillera en étroite collaboration avec la DPSC de SC et discutera des extraits de données du SCSESSI et de CVP afin de permettre aux mesures réglementaires liées aux vaccins commercialisés au Canada.
Évaluations de la causalité
Le Comité consultatif sur l'évaluation de la causalité (CCEC) fait partie du système canadien de surveillance de la sécurité des vaccins. L'évaluation de la causalité constitue un des éléments essentiels de la surveillance de la sécurité des vaccins. Le CCEC examine les rapports d'événements indésirables suivant l'immunisation reçus par le biais de la surveillance nationale. Il détermine si un événement est susceptible d'avoir un lien de causalité avec un vaccin donné. Le CCEC effectue ses évaluations de causalité en utilisant un processus basé sur une procédure normalisée, développée par l'Organisation mondiale de la santé.
Résultats de l'évaluation de la causalité
Effets secondaires de la COVID-19 suivant l'immunisation
Nous mettons cette page à jour régulièrement.
Publications et rapports sur les données
Rapports annuels
- Surveillance de l'innocuité des vaccins au Canada : déclarations au SCSESSI, 2017
- Surveillance de l'innocuité des vaccins au Canada : déclarations au SCSESSI, 2013 à 2016
Rapports semestriels
- Effets secondaires suivant l'immunisation (ESSI) Rapport semestriel du 1er janvier au 30 juin 2019
- Effets secondaires suivant l'immunisation (ESSI) - Rapport semestriel du 1er juillet au 31 décembre 2018
- Effets secondaires suivant l'immunisation (ESSI) - Rapport semestriel du 1er janvier au 30 juin 2018
Rapports trimestriels
2016
2015
Rapports sur l'innocuité des vaccins publiés précédemment
Pour obtenir une copie d'un rapport qui n'est pas affiché en ligne, contactez l'Agence de la santé publique du Canada.
Résumés des effets secondaires suivant l'immunisation pour les vaccins administrés au cours de périodes précises
- Surveillance nationale de l'innocuité des vaccins par le Système canadien de surveillance des effets secondaires suivant l'immunisation, 2018–2019. RMTC. Volume 50-1/2, janvier/février 2024
- Rapport annuel du Système canadien de surveillance des effets secondaires suivant l'immunisation pour les vaccins administrés en 2012. RMTC. Volume 40S-3, 4 décembre 2014
- Rapport national sur l'immunisation au Canada : Chapitre 5-Innocuité des vaccins : surveillance des effets secondaires suivant l'immunisation avec tendances de 1992 à 2004 (archivé)
- 1998 National Report (interim) on Immunization Vaccine Safety Issues and Surveillance (déclarations de 1998 ainsi que les tendances de 1993 à 1997). Publié dans le Canadian Paediatric Society. juillet-août 1999, vol. 4, supplément C
- Canadian Report on Immunization: Update on Vaccine Safety Issues and Surveillance. Publié dans le Canadian Paediatric Society. mars-avril 1998, vol. 3, supplément B
- Rapport sur l'immunisation au Canada, 1996 : Surveillance des incidents indésirables associés au moment de l'administration du vaccin (PDF). RMTC. 1997 vol. 23S4 (archivé)
- Effets secondaires reliés dans le temps à des vaccins - rapport de 1992 (PDF). RMTC. 1995 vol. 21-13:117-128 (archivé)
- Effets secondaires reliés dans le temps à des vaccins - rapport de 1991. RMTC. 1993; 19:168-78 (non disponible en ligne)
- Effets secondaires reliés dans le temps à des vaccins - rapport de 1990. Canadian Family Physician. 1993; 39:1907-13
Rapports sur des vaccins précis
- Rapports de surveillance de l'innocuité des vaccins au Canada suite à l'immunisation avec des vaccins antigrippaux saisonniers, 2021–2022. RMTC. Volume 50-1/2, janvier/février 2024
- Serious adverse events associated with Bacille Calmette-Guérin vaccine in Canada. Pediatric Infectious Disease Journal. 2005; 24:538-541 (en anglais seulement)
- Effets secondaires associés au vaccin antigrippal : résultats de la surveillance passive, Canada 2001-2002 (PDF). RMTC. déc. 2002; vol. 28-23:189-196 (archivé)
- Analyse des réactions indésirables déclarées à la suite de la vaccination contre la fièvre jaune - Canada, 1987-2000 (PDF). RMTC. janv. 2002; vol. 28-2:9-15 (archivé)
Rapports sur des effets secondaires précis
- Myocarditis and/or pericarditis risk after mRNA COVID-19 vaccination: A Canadian head to head comparison of BNT162b2 and mRNA-1273 vaccines (en anglais seulement). Vaccine. 2022 Jul 30;40(32):4663-4671
- Thrombosis with thrombocytopenia syndrome following adenovirus vector COVID-19 vaccination in Canada (en anglais seulement). Vaccine. 2023 Oct 6:S0264-410X(23)01159-3
- Syndrome oculo-respiratoire après la vaccination antigrippale : examen des données de surveillance post-commercialisation pendant quatre saisons grippales au Canada (PDF). RMTC. 2005; vol. 31-21:217-225 (archivé)
- Syndrome oculo-respiratoire associé au vaccin antigrippal : Canada, octobre-novembre 2000 (rapport préliminaire) [PDF]. RMTC. 2000; vol. 26-23:201 (archivé)
Liens connexes
- COVID-19 : Sécurité des vaccins et effets secondaires liés à la vaccination
- Réglementation sur les vaccins
- MedEffet Canada : Déclaration des effets indésirables des médicaments, des produits de santé naturels et des médicaments vétérinaires
- Programme canadien de surveillance active de l'immunisation
- Organisation mondiale de la Santé : Global Advisory Committee on Vaccine Safety (en anglais seulement)