Faits saillants sur les médicaments et les instruments médicaux 2020 : Médicaments à usage vétérinaire
Sur cette page
- Médicaments à usage vétérinaire : 2020 en bref
- Médicaments à usage vétérinaire : quoi de neuf en 2020
- Médicaments à usage vétérinaire : réalisations de 2020
- Clics santé : Aperçu des médicaments à usage vétérinaire
- Médicaments à usage vétérinaire : Cycle de vie
Médicaments à usage vétérinaire : 2020 en bref
L'un des rôles de Santé Canada est de réglementer les médicaments à usage vétérinaire qui jouent un rôle important dans la protection de la santé humaine et animale. Nous évaluons et surveillons l'innocuité, la qualité et l'efficacité des médicaments à usage vétérinaire. Ce faisant, nous nous efforçons de protéger les animaux et l'approvisionnement alimentaire du Canada.
La pandémie de COVID-19 a créé un besoin urgent d'accès à des produits de santé sûrs, efficaces et de haute qualité, y compris des médicaments à usage vétérinaire en cas de besoin spécifique pour traiter des animaux. La COVID-19 est considérée comme une nouvelle maladie humaine, mais son incidence sur la santé animale n'est pas encore totalement connue.
Réponse à la pandémie de COVID-19
Nous avons introduit des mesures réglementaires innovantes et agiles dans le cadre de la réponse du gouvernement à la pandémie, y compris pour les médicaments à usage vétérinaire. Ces mesures ont permis d'accélérer l'examen réglementaire des produits de santé liés à la COVID-19 sans compromettre l'innocuité, l'efficacité et les normes de qualité.
En 2020, nous avons modernisé le règlement du programme de distribution de médicaments d'urgence afin de faciliter l'accès d'urgence à des médicaments non approuvés à usage vétérinaire.
Pour en savoir plus sur notre réponse à la pandémie de COVID-19, consultez la rubrique « Médicaments à usage vétérinaire : réalisations de 2020 ».
Nouveaux produits de santé approuvés
En 2020, nous avons approuvé neuf nouveaux médicaments pour les animaux domestiques ou élevés à des fins alimentaires. Cela a permis l'accès à de nouveaux produits et thérapies innovants pour aider à maintenir et à améliorer la santé des animaux.
Nous avons également approuvé 11 nouveaux médicaments génériques pour offrir des options supplémentaires de prévention et de traitement plus rentables.
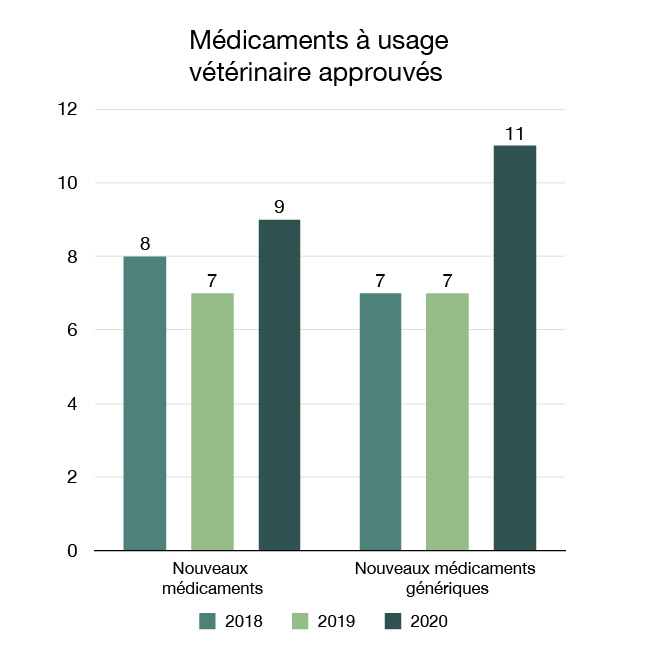
Figure 12 : Médicaments à usage vétérinaire approuvés : Équivalent textuel
| Année | Nouveaux médicaments approuvés | Nouveaux médicaments génériques approuvés |
|---|---|---|
| 2018 | 8 | 7 |
| 2019 | 7 | 7 |
| 2020 | 9 | 11 |
Pour la liste et la description des nouveaux médicaments approuvés en 2020, consultez la rubrique « Approuvés en 2020 : Médicaments à usage vétérinaire ».
Cette année, 761 produits de santé vétérinaires ont fait l'objet d'un avis dans le cadre de notre programme de produits de santé vétérinaires. Ceux-ci offrent plus d'options à faible risque pour maintenir ou promouvoir la santé et le bien-être des animaux.
Essais cliniques et programme de distribution des médicaments d'urgence
Nous examinons les demandes pour permettre aux entreprises et aux chercheurs de mener des études sur les médicaments vétérinaires au Canada. Les nouveaux essais de médicaments vétérinaires (appelés études et nouveaux médicaments expérimentaux) font en sorte que les Canadiens pourraient avoir accès à de nouveaux produits dans l'avenir. En 2020, 94 certificats d'études expérimentales autorisant des essais cliniques ou des activités de recherche ont été autorisés.
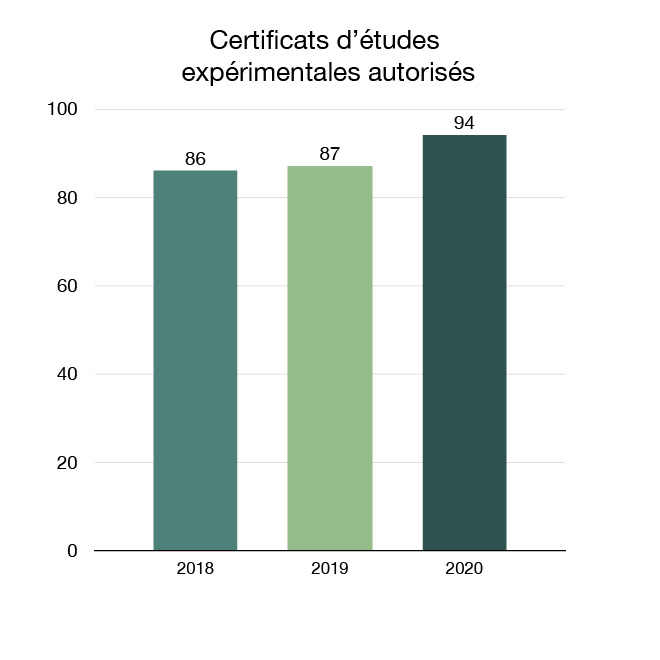
Figure 13 : Certificats d'études expérimentales autorisés : Équivalent textuel
| Année | Certificats d'études expérimentales autorisés |
|---|---|
| 2018 | 86 |
| 2019 | 87 |
| 2020 | 94 |
Les vétérinaires peuvent, par l'entremise de notre Programme de distribution des médicaments d'urgence, demander l'accès à des médicaments à usage vétérinaire qui ne sont pas disponibles au Canada pour répondre à des situations d'urgence. En 2020, 310 demandes ont été autorisées dans le cadre du Programme de distribution des médicaments d'urgence.
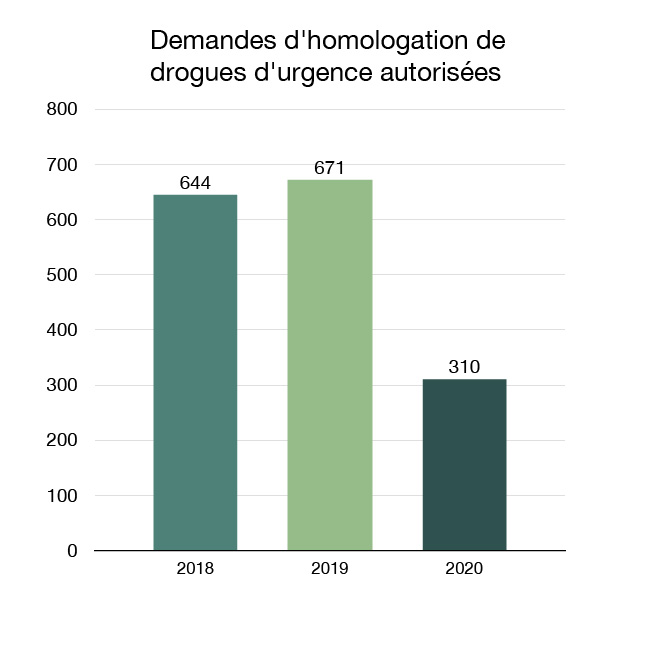
Figure 14 : Demandes d'homologation de drogues d'urgence autorisées : Équivalent textuel
| Année | Demandes d'homologation de drogues d'urgence autorisées |
|---|---|
| 2018 | 644 |
| 2019 | 671 |
| 2020 | 310 |
Surveillance

Directrice générale,
Médicaments vétérinaires
Après avoir approuvé la vente d'un médicament à usage vétérinaire au Canada, nous continuons de surveiller et d'évaluer les rapports d'effets indésirables soupçonnés.
Ce chapitre sur les « médicaments à usage vétérinaire » contient plus de renseignements sur le travail que nous avons accompli en 2020. Pour obtenir des renseignements à jour sur nos activités, veuillez consulter la section intitulée « Clics santé : Aperçu des médicaments à usage vétérinaire » et nous suivre sur les médias sociaux.
Médicaments à usage vétérinaire : quoi de neuf en 2020
En 2020, Santé Canada a approuvé neuf nouveaux médicaments à usage vétérinaire. Vous trouverez d'autres renseignements dans la section intitulée « Approuvés en 2020 : Médicaments à usage vétérinaire ».
Nouveaux médicaments à usage vétérinaire
- Aservo Equihaler
- Bravecto One
- Comfortan
- Comprimés aromatisés Amodip
- Cosacthen
- Eradia
- Gonabreed
- Mirataz
- Zeleris
Médicaments à usage vétérinaire : réalisations de 2020
Réponse à la pandémie de COVID-19
La COVID-19 est considérée comme une maladie essentiellement humaine et on pense que le virus se propage principalement de personne à personne. Cependant, la COVID-19 est une nouvelle maladie et nous ne connaissons peut-être pas entièrement ses répercussions sur la santé animale.
Programme de distribution de médicaments d'urgence
Les médicaments qui ne sont pas approuvés au Canada peuvent être disponibles par l'entremise de notre Programme de distribution de médicaments d'urgence (PDMU). Les vétérinaires peuvent demander l'accès à des médicaments à usage vétérinaire non approuvés pour traiter des patients (un animal ou un groupe d'animaux) souffrant de conditions graves ou mettant leur vie en danger. L'accès à ces médicaments n'est envisagé que lorsque les thérapies conventionnelles ont échoué, sont inadaptées ou indisponibles.
En 2020, nous avons modernisé le règlement du Programme de distribution de médicaments d'urgence afin de faciliter l'accès d'urgence à des médicaments non approuvés à usage vétérinaire.
Pour plus d'informations, consultez les Programmes d'accès spécial de Santé Canada : Demander un médicament vétérinaire par l'intermédiaire de la distribution de médicaments d'urgence (DMU).
Pleins feux sur…
Le programme de distribution de médicaments d'urgence
« L'examen des demandes reçues dans le cadre du Programme de distribution de médicaments d'urgence nous met en relation directe avec les vétérinaires en pratique clinique. Nous avons la chance de disposer d'une réglementation actualisée qui contribue à garantir que des médicaments permettant de sauver des vies et d'améliorer le bien-être des animaux soient mis à leur disposition, notamment lorsque les vétérinaires doivent traiter des maladies émergentes chez leurs patients. C'est une expérience enrichissante que de faire partie de l'effort de collaboration multiforme visant à soutenir la santé et le bien-être des animaux. »
Shaunna Lucas
Agente de l'information,
Médicaments vétérinaires
Annie Tourangeau
Analyste de l'information vétérinaire,
Médicaments vétérinaires
Julie Burke
Analyste de l'information vétérinaire,
Médicaments vétérinaires
Médicaments à usage vétérinaire
Santé Canada a introduit des mesures réglementaires innovantes et agiles dans le cadre de la réponse du gouvernement à la pandémie. Ces mesures nous permettront d'accélérer l'examen réglementaire des médicaments à usage vétérinaire dans le contexte de la COVID-19, sans compromettre nos normes élevées d'innocuité, d'efficacité et de qualité si un fabricant dépose une demande à l'avenir.
Pour plus d'informations sur les arrêtés d'urgence qui ont été publiés pour répondre à la pandémie de COVID-19, consultez la rubrique « Message du chef principal de la réglementation ».
Pénuries de médicaments
Au début de la pandémie, il était évident que la COVID-19 avait une incidence sur l'approvisionnement en produits de santé essentiels au Canada. Nous avons travaillé avec les entreprises et les fabricants, ainsi qu'avec d'autres autorités de réglementation dans le monde, pour cerner les pénuries éventuelles et y répondre. Ces collaborations nous ont permis de cerner, de prévenir et d'atténuer les pénuries pour les Canadiens.
Pour plus d'informations, consultez la section consacrée à la lutte contre les pénuries de produits essentiels.
Communications et collaborations
Tout au long de la pandémie, Santé Canada a publié un certain nombre de pages web pour fournir des informations aux Canadiens, aux partenaires réglementaires et à l'industrie des produits de santé sur notre réponse à la pandémie de COVID-19. Nos sites web fournissent des informations sur les différents produits de santé que nous réglementons, y compris les demandes de médicaments qui ont été soumises et approuvées.
Nous avons travaillé en étroite collaboration avec nos partenaires nationaux, notamment les fabricants, les praticiens et les producteurs d'aliments. Nous avons cherché à connaître leur point de vue sur les priorités et les défis auxquels ils étaient confrontés en raison de la pandémie.
Lutter contre la résistance aux antimicrobiens chez les animaux
La résistance aux antimicrobiens est une menace croissante pour la santé publique au Canada et dans le monde. La surconsommation et le mauvais usage des médicaments antimicrobiens permettent aux germes pathogènes comme les bactéries et les champignons d'évoluer et de devenir résistants aux antimicrobiens.
Chez les animaux, l'utilisation d'antimicrobiens peut contribuer au développement et à la propagation de bactéries résistantes chez les humains. L'approche « Un monde, une santé » reconnaît l'interconnexion entre la santé des humains, des animaux et de leur environnement commun, ainsi que la nécessité d'une collaboration entre les secteurs pour améliorer la santé de tous.
En 2020, Santé Canada a continué d'axer sa prochaine série d'initiatives sur la résistance aux antimicrobiens des médicaments à usage vétérinaires sur le maintien de la santé des animaux afin de réduire l'utilisation des antimicrobiens et de promouvoir leur utilisation responsable lorsqu'ils sont nécessaires. Ceci comprenait les suivants :
- Publier le cadre de réévaluation après la mise en marché des antimicrobiens importants pour la médecine humaine afin de renforcer leur utilisation responsable chez les animaux.
- Finaliser l'analyse de la première année (2018) des données sur les ventes d'antimicrobiens vétérinaires recueillies dans le cadre du programme de déclaration des ventes de médicaments vétérinaires antimicrobiens afin de soutenir les efforts de surveillance. L'analyse est en cours pour les données recueillies au cours de la deuxième année (2019) du programme.
- Lancement d'un projet pilote qui élargit l'accès aux produits de santé vétérinaire qui pourraient être utilisés dans les aliments pour le bétail, en partenariat avec l'Agence canadienne d'inspection des aliments. Ce projet vise à faciliter un accès accru aux produits de santé et de bien-être général afin d'améliorer la santé animale et de réduire la dépendance aux médicaments conventionnels, y compris aux antimicrobiens.
Ces initiatives s'inscrivent dans la foulée du Plan d'action fédéral sur la résistance et le recours aux antimicrobiens au Canada et du Cadre pancanadien de lutte contre la résistance aux antimicrobiens et d'optimisation de leur utilisation.
Pour en savoir plus sur la résistance aux antimicrobiens chez les humains, consultez la section « Médicaments à usage humain : réalisations de 2020 ».
Pleins feux sur…
La semaine mondiale pour un bon usage des antibiotiques du 18 au 24 Novembre 2020
Chaque année, Santé Canada se joint à l'Organisation mondiale de la santé, aux agences sanitaires internationales et à d'autres autorités nationales pour soutenir la Semaine mondiale pour un bon usage des antibiotiques. Cette initiative mondiale vise à sensibiliser à la résistance aux antimicrobiens chez les animaux et les humains et à encourager les pratiques exemplaires pour éviter la propagation d'infections résistantes aux médicaments. En 2020, nous avons accueilli un groupe de conférenciers internationaux pour discuter des difficultés liées à la recherche sur les antimicrobiens, le développement de thérapies et l'accès à celles-ci.
Innovation réglementaire
Le rythme actuel de l'innovation est sans précédent. Cela a donné naissance à de nouveaux produits de santé de plus en plus complexes. Nous avons besoin de nouvelles approches réglementaires pour mieux soutenir l'accès à ces technologies de la santé, tout en continuant à protéger la sécurité des patients.
Santé Canada a continué de privilégier l'innovation réglementaire en 2020. La pandémie de COVID-19 a affecté le calendrier de ce travail. Cependant, elle a également été l'occasion de tester certaines mesures agiles temporaires (pour plus d'informations, voir le « Message du chef principal de la réglementation »). Nous utiliserons les leçons retenues de notre réponse réglementaire à la COVID-19 pour étayer notre travail d'innovation réglementaire, y compris en ce qui a trait à ces médicaments à usage vétérinaire, notamment :
- moderniser la réglementation relative aux études expérimentales, y compris les certificats d'études expérimentales,
- permettre l'accès à des produits thérapeutiques avancés qui ne correspondent pas à notre système actuel,
- octroyer des licences agiles pour les médicaments, en utilisant des outils flexibles pour superviser les produits tout au long de leur cycle de vie,
Pour plus d'informations, consultez la rubrique « Innovation réglementaire pour les produits de santé ».
Collaboration internationale
Depuis de nombreuses années, Santé Canada travaille en étroite collaboration avec les organismes de réglementation du monde entier sur les questions liées aux médicaments à usage vétérinaire. Cette coopération a progressé de manière significative en 2020.
Nous avons poursuivi nos examens simultanés des médicaments vétérinaires en partenariat avec le Center for Veterinary Drugs de la Food and Drug Administration des États-Unis. Ce partenariat offre aux fabricants un accès à deux marchés importants, élargit l'accès aux options de traitement pour les animaux au Canada et aide les producteurs alimentaires canadiens à rester compétitifs au niveau mondial.
En 2020, nous avons publié les Lignes directrices sur les examens conjoints de médicaments vétérinaires avec l'Australie et la Nouvelle-Zélande, qui décrivent le processus d'examen conjoint des médicaments vétérinaires. Toujours en 2020, nous avons lancé un processus d'examen simultané avec le Royaume-Uni. Au 31 décembre 2020, nous avions un examen conjoint en cours avec l'Australie et la Nouvelle-Zélande, et 10 examens simultanés en cours avec les États-Unis.
Offrir plus de choix pour améliorer la santé et le bien-être des animaux
En gardant les animaux en santé, nous pouvons réduire la nécessité de recourir aux médicaments, y compris les antimicrobiens. Les produits de santé vétérinaire sont des produits à faible risque qui peuvent aider à maintenir ou à promouvoir la santé et le bien-être des animaux. Ils contiennent des ingrédients comme des vitamines, des minéraux et des médicaments traditionnels.
À l'heure actuelle, les produits qui contiennent un phytocannabinoïde produit par la plante de cannabis ou présent dans celle-ci ne peuvent être prescrits que par un professionnel de la santé à des fins médicinales. Santé Canada reconnaît que certains Canadiens s'intéressent aux utilisations thérapeutiques potentielles du cannabis, notamment pour soulager la douleur chez les animaux, sans qu'il soit nécessaire de faire appel à la surveillance d'un praticien. En 2019, Santé Canada a mené une consultation sur le marché potentiel de ces produits de santé. Nous avons publié un rapport sommaire en 2020, lequel comprend un aperçu des commentaires reçus des Canadiens.
Dans le cadre de cette consultation, nous avons également établi un Comité consultatif scientifique sur les produits de santé contenant du cannabis, qui comprend un sous-comité chargé d'examiner les questions liées aux produits de santé contenant du cannabis destinés à être utilisés chez les animaux. Ce comité nous fournira des conseils scientifiques et cliniques indépendants sur les considérations appropriées en matière d'innocuité, d'efficacité et de qualité des produits de santé contenant du cannabis, y compris à des fins vétérinaires. Santé Canada utilisera ces informations pour étayer sa démarche réglementaire concernant ces produits.
Pleins feux sur…
Les produits de santé vétérinaire
Santé Canada a mis en place un cadre flexible et adapté aux risques pour les produits de santé à faible risque à usage vétérinaire chez les animaux destinés à l'alimentation et les animaux de compagnie. Ce cadre facilite l'accès à ces produits de santé vétérinaires. Il y a maintenant plus de 2 300 produits de ce type qui ont été notifiés pour la vente au Canada. À mesure que le programme de notification des produits de santé vétérinaires gagne en popularité auprès des Canadiens et des intervenants, nous continuons d'élargir le type d'ingrédients et de produits inclus dans le programme. Nous le faisons sans compromettre la sécurité des animaux ou des humains, y compris la salubrité alimentaire. Notre programme fournit également des informations complètes et consultables aux Canadiens.
« Notre programme fournit des informations aux Canadiens sur les produits de santé vétérinaires – l'application en ligne est conviviale et les informations sont faciles à trouver et à rechercher. »
Femma Van As
Évaluatrice de médicaments,
Médicaments vétérinaires
Consultation sur les changements à notre approche réglementaire
De nombreux médicaments vétérinaires sont conçus pour être utilisés sur des animaux destinés à la production d'aliments tels que les bovins, les volailles et les porcs. Nous travaillons à assurer la salubrité des aliments qui proviennent d'animaux traités avec des médicaments vétérinaires. Pour ce faire, nous fixons des normes telles que les limites maximales de résidus pour la présence de médicaments vétérinaires dans les aliments ainsi que des délais d'attente. En 2020, nous avons mené une consultation sur une proposition de modification de la Liste des limites maximales de résidus de drogues pour usage vétérinaire dans les aliments.
Nous avons également mené une consultation en 2020 sur une proposition de classification réglementaire des produits à base d'acide et destinés à des animaux de ferme. Historiquement, ces produits ont pu être classés soit comme médicament vétérinaire, soit comme produit de santé vétérinaire, soit comme aliment pour bétail. Cette proposition apportera des éclaircissements sur la manière dont ces produits importants doivent être classés et ensuite réglementés.
Clics santé : Aperçu des médicaments à usage vétérinaire
Pour demeurer au courant de nos activités :
- Suivez-nous sur Facebook
- Suivez-nous sur Twitter
- Suivez-nous sur YouTube
- Consultez les dernières nouvelles de Santé Canada sur notre site web
- Trouvez d'autres renseignements liés à la santé sur le site web du gouvernement du Canada
Vous pouvez également trouver des informations particulières sur les médicaments à usage vétérinaire en suivant les liens ci-dessous.
Nouveaux médicaments approuvés
La Base de données sur les produits pharmaceutiques est une liste de tous les médicaments dont la vente est approuvée au Canada. Dans la base de données, de nombreux médicaments sont accompagnés de leur étiquetage vétérinaire qui décrit les conditions d'utilisation du produit.
Base de données des produits pharmaceutiques
La Base de données des avis de conformité répertorie les homologations (avis de conformité ou AC) délivrées pour les nouveaux médicaments.
Surveillance des médicaments vétérinaires
Déclarer un effet indésirable d'un médicament vétérinaire.
Médicaments à usage vétérinaire : Cycle de vie
Chaque année, nous approuvons de nouveaux médicaments vétérinaires au Canada et nous élargissons ainsi l'éventail des options disponibles pour contribuer à maintenir et à améliorer la santé et le bien-être des animaux. Nous travaillons à protéger la santé humaine et animale ainsi que la sécurité de l'approvisionnement alimentaire du Canada.
Dans le cadre de ce travail, nous évaluons les médicaments vétérinaires tout au long de leur cycle de vie, de la recherche et des études à la vente du médicament au Canada.
Essais cliniques
Les certificats d'études expérimentales et les demandes de médicaments nouveaux à des fins expérimentales contribuent à la mise au point de nouveaux médicaments vétérinaires potentiels ou de nouvelles utilisations de produits déjà approuvés. Les promoteurs de ces recherches et études (y compris les fabricants et les chercheurs) soumettent leurs demandes à l'examen de Santé Canada avant que l'essai ne soit mené au Canada.
Programme de distribution de médicaments d'urgence
Les médicaments qui ne sont pas approuvés au Canada peuvent être disponibles par l'entremise de notre Programme de distribution de médicaments d'urgence. Les vétérinaires peuvent demander l'accès à des médicaments à usage vétérinaire pour traiter des patients (un animal ou un groupe d'animaux) souffrant de conditions graves ou mettant leur vie en danger. L'accès à ces médicaments n'est envisagé que lorsque les thérapies conventionnelles ont échoué, sont inadaptées ou indisponibles.
Présentation et examen des médicaments
Lorsqu'une entreprise décide de commercialiser un médicament vétérinaire au Canada, elle dépose une présentation auprès de Santé Canada. Une présentation de drogue nouvelle contient des renseignements scientifiques détaillés sur l'innocuité, l'efficacité et la qualité du médicament.
Les présentations visant des médicaments sont examinées par nos scientifiques afin d'évaluer les avantages et les risques pour la santé humaine et animale. Nos scientifiques contribuent également à faire en sorte que les étiquettes des médicaments vétérinaires comportent un mode d'emploi et des mises en garde clairs.
De nombreux médicaments vétérinaires sont conçus pour être utilisés sur des animaux destinés à la production d'aliments tels que les bovins, les volailles et les porcs. Nous travaillons à assurer la salubrité des aliments qui proviennent d'animaux traités avec des médicaments vétérinaires. Pour ce faire, nous fixons des normes telles que les limites maximales de résidus pour la présence de médicaments vétérinaires dans les aliments ainsi que des délais de rétractation.
Examens innovateurs (coopération internationale des autorités de réglementation)
Grâce à la coopération internationale en matière de réglementation, nous examinons des présentations visant de nouveaux médicaments vétérinaires avec certains partenaires. Nos partenaires sont notamment le Center for Veterinary Medicines de la Food and Drug Administration des États-Unis, l'Australian Pesticides and Veterinary Medicines Authority et le New Zealand Ministry of Primary Industries.
Ces examens concertés permettent d'introduire des médicaments vétérinaires sur le marché au Canada en même temps que dans d'autres pays, ce qui serait autrement impossible. Par conséquent, les propriétaires d'animaux de compagnie, les vétérinaires et les producteurs ont accès plus rapidement à des médicaments vétérinaires sûrs, efficaces et de grande qualité.
Approbation des médicaments
Après avoir examiné une présentation visant un médicament, Santé Canada peut conclure que les avantages l'emportent sur les risques associés à l'utilisation du produit et approuver la vente du médicament vétérinaire au Canada. Lorsqu'un nouveau médicament vétérinaire est approuvé, un avis de conformité et un numéro d'identification du médicament (DIN) sont émis. Cela ne signifie pas que le médicament sera immédiatement disponible au Canada, car de nombreux autres facteurs peuvent influencer ce calendrier.
Surveillance
Une fois que Santé Canada a approuvé un médicament vétérinaire, nous continuons de surveiller son utilisation dans le monde réel. Nous évaluons les problèmes potentiels d'innocuité et d'efficacité et prenons des mesures au besoin.
Collecte de renseignements
Santé Canada recueille des renseignements sur un produit après son approbation auprès de diverses sources.
Les effets indésirables présumés déclarés après l'approbation de la vente des produits constituent une source d'information. Les effets indésirables sont des effets non souhaités ou nuisibles qui se manifestent après l'administration d'un médicament vétérinaire. Sont inclus :
- les réactions ou effets indésirables chez les animaux,
- les réactions ou effets indésirables chez les humains qui ont administré un médicament vétérinaire à un animal,
- les suites d'une absence d'effet présumé.
Réaction à un médicament vétérinaire
Vous pouvez déclarer une réaction à un médicament vétérinaire à Santé Canada.
Évaluation des signaux d'innocuité
Santé Canada évalue les rapports sur les effets indésirables présentés par les fabricants et la population (y compris les propriétaires d'animaux et les vétérinaires), afin de déterminer s'ils sont liés au ou aux médicaments administrés. Nous travaillons avec les fabricants et les vétérinaires pour nous assurer que tout renseignement sur l'innocuité est communiqué.